Содержание
-
Структурная формула
-
Русское название
-
Английское название
-
Латинское название
-
Химическое название
-
Брутто формула
-
Фармакологическая группа вещества Флуцитозин
-
Нозологическая классификация
-
Код CAS
-
Фармакологическое действие
-
Характеристика
-
Фармакология
-
Применение вещества Флуцитозин
-
Противопоказания
-
Ограничения к применению
-
Применение при беременности и кормлении грудью
-
Побочные действия вещества Флуцитозин
-
Взаимодействие
-
Передозировка
-
Способ применения и дозы
-
Меры предосторожности
Структурная формула
Русское название
Флуцитозин
Английское название
Flucytosine
Латинское название
Flucytosinum (род. Flucytosini)
Химическое название
4-Амино-5-фторпиримидин-2(1Н)-он
Брутто формула
C4H4FN3O
Фармакологическая группа вещества Флуцитозин
Нозологическая классификация
Код CAS
2022-85-7
Фармакологическое действие
—
противогрибковое, фунгистатическое, фунгицидное.
Характеристика
Фторированный пиримидин. Белый или почти белый кристаллический порошок без запаха. Растворимость в воде 1,5 г/100 мл при 25 °C. pKa1 3,26. Молекулярная масса 129,09.
Фармакология
Флуцитозин для чувствительных к его воздействию микроорганизмов играет роль конкурентного ингибитора в метаболизме урацила. После проникновения в клетку гриба флуцитозин дезаминируется посредством специфической цитозиндезаминазы до 5-фторурацила. Затем 5-фторурацил при участии урацилфосфорибозилтрансферазы превращается в 5-фтор-уридинмонофосфат. Последний фосфорилируется до 5-фтор-уридинтрифосфата и встраивается в РНК возбудителя вместо урацила, нарушая тем самым синтез белка, что обусловливает фунгистатическую активность препарата. Кроме того, 5-фтор-уридинмонофосфат превращается в 5-фтордезоксиуридинмонофосфат, который подавляет активность тимидилатсинтетазы, что приводит к нарушению синтеза ДНК гриба. По отношению к ряду возбудителей проявляет фунгицидное действие при продолжительном контакте.
Обладает фунгистатическим и фунгицидным действием in vitro и in vivo в отношении Candida spp., а также возбудителей криптококкоза (Cryptococcus neoformans) и хромобластомикоза. При аспергиллезе проявляет фунгистатическую активность. МПК обычно находится на уровне между 0,03 и 12,5 мг/л. При лечении флуцитозином у первоначально чувствительных к нему штаммов постепенно может выработаться устойчивость (определение чувствительности рекомендуется проводить до и во время лечения).
Избирательность действия флуцитозина на клетки грибов объясняется тем, что клетки млекопитающих не способны превращать флуцитозин во фторурацил, поэтому флуцитозин низкотоксичен для человека.
Канцерогенность, мутагенность, влияние на фертильность
Потенциальная канцерогенность флуцитозина в стандартных экспериментах на животных не оценивалась. Флуцитозин не проявлял мутагенных свойств в тесте Эймса с пятью различными штаммами Salmonella typhimurium в присутствии и отсутствии активирующих ферментов. Не выявлено мутагенности в трех различных репаративных тестах. Адекватных исследований у животных с целью оценки влияния флуцитозина на фертильность и общую репродуктивную способность не проведено. При введении мышам флуцитозина in utero с 7-го по 13-й день беременности в дозах 100 мг/кг/сут (345 мг/м2/сут; 0,059 МРДЧ), 200 мг/кг/сут (690 мг/м2/сут; 0,118 МРДЧ) или 400 мг/кг/сут (1380 мг/м2/сут; 0,236 МРДЧ) неблагоприятного влияния на фертильность и репродукцию потомства (F1 поколение) не обнаружено.
Хорошо распределяется в тканях и жидких средах организма, в т.ч. диффундирует в спинно-мозговую жидкость. Объем распределения после в/в введения — 0,8 л/кг. Связывание с белками плазмы — 2,9–4%. Концентрация в ликворе и перитонеальной жидкости составляет примерно 75% от концентрации в сыворотке. Концентрация в сыворотке должна составлять не менее 20–25 мг/л (за исключением лечения кандидоза мочевыводящих путей). Выводится почками в неизмененном виде путем клубочковой фильтрации (90% дозы). Небольшое количество флуцитозина дезаминируется в 5-фторурацил. У взрослых и детей с нормальной функцией почек T1/2 составляет 3–6 ч, у недоношенных детей — 6–7 ч, у пациентов с почечной недостаточностью T1/2 увеличивается (может увеличиваться до 200 ч). При нормальной функции почек концентрация флуцитозина в моче гораздо выше, чем в сыворотке. Эффективно удаляется из организма путем гемодиализа, перитонеального диализа и гемофильтрации.
На основании экспериментальных данных сочетание флуцитозина с амфотерицином В во многих случаях оказывает синергическое (по крайней мере аддитивное) действие. Клинические исследования показали, что комбинация этих двух ЛС дает лучший терапевтический эффект, чем каждый из них в качестве монотерапии. Кроме того, применение комбинированной терапии позволяет уменьшить терапевтическую дозу амфотерицина В и, тем самым, его токсические побочные эффекты. Одновременно сокращается продолжительность курса лечения. Применение комбинированной терапии позволяет предотвратить или отсрочить развитие вторичной устойчивости возбудителей, наблюдаемой при монотерапии флуцитозином. Применение этой комбинации особенно эффективно при лечении криптококкоза, а также при подострых и хронических грибковых инфекциях (менингоэнцефалит, эндокардит, кандидозный увеит и т.д.).
Применение вещества Флуцитозин
Системные инфекции, вызванные дрожжевыми и иными грибковыми возбудителями, чувствительными к воздействию флуцитозина: генерализованный кандидоз; криптококкоз; хромобластомикоз; аспергиллез (только в сочетании с амфотерицином В); инфекции, вызываемые микроорганизмами Torulopsis glabrata и Hansenula.
Противопоказания
Гиперчувствительность, хроническая почечная недостаточность при невозможности определения концентрации флуцитозина в сыворотке крови.
Ограничения к применению
Угнетение функции костного мозга, заболевания крови.
Применение при беременности и кормлении грудью
Тератогенные эффекты. Флуцитозин проявлял тератогенность (сращение позвонков) у крыс при введении в дозах 40 мг/кг/сут (298 мг/м2/сут; 0,051 МРДЧ) с 7-го по 13-й день беременности. При введении флуцитозина в более высоких дозах (700 мг/кг/сут; 5208 мг/м2/сут; 0,89 МРДЧ) с 9-го по 12-й день беременности были зафиксированы такие аномалии развития, как врожденная расщелина верхней губы, расщелина неба и малые размеры верхней челюсти. Флуцитозин не проявлял тератогенности у кроликов при дозах до 100 мг/кг/сут (1423 мг/м2/сут; 0,243 МРДЧ) при введении с 6-го по 18-й день беременности. У мышей дозы флуцитозина 400 мг/кг/сут (1380 мг/м2/сут; 0,236 МРДЧ), введенные с 7-го по 13-й день беременности, ассоциировались с низкой частотой (статистически не значимо) возникновения расщелины неба.
Адекватных и строго контролируемых исследований с участием беременных женщин не проводилось. При беременности можно назначать только в тех случаях, когда ожидаемый терапевтический эффект превышает потенциальный риск для развития плода (проходит через плаценту).
Категория действия на плод по FDA — C.
Не установлено, проникает ли флуцитозин в материнское молоко. В период кормления грудью необходимо принять решение о прекращении грудного вскармливания, либо о прекращении терапии флуцитозином, учитывая важность ее для матери.
Побочные действия вещества Флуцитозин
Со стороны сердечно-сосудистой системы и крови (кроветворение, гемостаз): остановка сердца, нарушение вентрикулярной функции, анемия, агранулоцитоз, апластическая анемия, эозинофилия, лейкопения, тромбоцитопения, гемолитическая анемия; в единичных случаях у ослабленных больных (на фоне имеющейся иммуносупрессии) — признаки угнетения кроветворения в костном мозге (панцитопения), у данной категории больных эти симптомы могут носить необратимый характер.
Со стороны респираторной системы: остановка дыхания, боль в грудной клетке, одышка.
Со стороны кожных покровов: сыпь, зуд, крапивница, светочувствительность, токсический эпидермальный некролиз.
Со стороны органов ЖКТ: тошнота, рвота, боль в области живота, диарея, анорексия, сухость во рту, язва двенадцатиперстной кишки, желудочно-кишечные кровотечения, язвенный колит, повышение уровня билирубина, нарушение функции печени, желтуха, повышенная активность ферментов печени в сыворотке крови; в единичных случаях у ослабленных больных — острая печеночная недостаточность, иногда приводившая к летальному исходу.
Со стороны мочеполовой системы: азотемия, повышение уровней креатинина/мочевины/азота, кристаллурия, острая почечная недостаточность.
Со стороны нервной системы и органов чувств: атаксия, необычная усталость, слабость, головная боль, парестезия, паркинсонизм, периферическая нейропатия, головокружение, седативный эффект, судороги, потеря сознания, галлюцинации, психоз, потеря слуха.
Прочие: аллергические реакции, повышение температуры тела, гипогликемия, гипокалиемия.
Взаимодействие
В исследованиях in vitro и in vivo было показано, что при комбинированном применении флуцитозина и амфотерицина В их активность взаимно усиливается в отношении многих штаммов возбудителей (этот эффект особенно выражен в случае возбудителей, мало чувствительных к флуцитозину).
Поскольку при лечении флуцитозином существует риск развития лейкопении (особенно нейтропении, часто сопровождаемой тромбоцитопенией), при одновременном лечении цитостатиками необходим ежедневный контроль периферической крови. Поскольку выведение флуцитозина осуществляется почти исключительно через почки, то ЛС, снижающие клубочковую фильтрацию, увеличивают T1/2 флуцитозина (требуется регулярный контроль за клиренсом креатинина, а также соответствующая корректировка дозы).
Инфузионные растворы флуцитозина и амфотерицина В следует вводить раздельно. Флуцитозин можно применять одновременно с парентеральными растворами 0,9 или 0,18% натрия хлорида и 5 и 4% глюкозы. Никакие иные ЛС не должны добавляться к инфузионному раствору флуцитозина.
Передозировка
Случаи передозировки неизвестны.
Симптомы (возможные): возрастание риска развития побочных реакций и тяжести их проявления. Превышение сывороточной концентрации в течение длительного времени свыше 100 мг/л сопровождается возрастанием числа побочных эффектов, особенно со стороны ЖКТ (диарея, тошнота, рвота), гематологических (лейкопения, тромбоцитопения), со стороны печени (гепатит).
Лечение: следует обеспечить поступление в организм достаточного объема жидкости (при необходимости в/в введение), поскольку флуцитозин выводится через почки в неизмененном виде. Необходим частый контроль параметров периферической крови, а также тщательный мониторинг функции почек и печени. В случае отклонений от нормы следует применить надлежащие терапевтические меры. Поскольку гемодиализ существенно снижает сывороточную концентрацию флуцитозина у больных, страдающих анурией, можно рассматривать возможность использования гемодиализа в качестве метода терапии в случае передозировки флуцитозина.
Способ применения и дозы
В/в при помощи капельницы; допустимо прямое в/в введение через центральный венозный катетер или введение посредством перитонеальной инфузии.
Рекомендуемая доза для взрослых и детей — 100–200 мг/кг/сут (в зависимости от показаний и чувствительности микроорганизмов), разделенная на 4 дозы, вводимые на протяжении 24 ч. Разовая доза — 37,5–50 мг/кг вводится посредством коротких вливаний (20–40 мин) при условии обеспечения достаточной гидратации больного. При нормальной функции почек интервалы между процедурами — 6 ч. Продолжительность терапии определяется индивидуально. Как правило, продолжительность лечения — 1 нед, при острых инфекциях (например кандидамикотический сепсис) — 2–4 нед; при подострых и хронических инфекциях требуется, как правило, более продолжительное лечение, рекомендуется комбинированное применение с амфотерицином В; при лечении криптококкового менингита — не менее 4 мес.
При нарушении функции почек следует назначать меньшие дозы и увеличивать интервал между процедурами в зависимости от клиренса креатинина; при клиренсе креатинина <10 мл/мин определяют сывороточную концентрацию флуцитозина через 12 ч после введения первой дозы. При введении последующих доз концентрация препарата в сыворотке должна поддерживаться в диапазоне 25–50 мкг/мл и не должна превышать 80 мкг/мл.
Доза для новорожденных рассчитывается так же, как для взрослых и детей. При этом следует учитывать бóльшую вероятность нарушений функции почек, присущую этому возрасту, либо являющуюся следствием проведения токсической для почек терапии. При этом рекомендуется мониторинг уровня флуцитозина в сыворотке и, в случае необходимости, соответствующая корректировка режима дозирования. При нарушении функции почек следует увеличить интервалы между введением разовых доз препарата. Если нарушения функции почек не обнаружено, но отмечается превышение рекомендуемого уровня концентрации флуцитозина в сыворотке, рекомендуется уменьшить дозу, оставив на том же уровне режим интервалов между процедурами.
Режим дозирования и профиль развития побочных эффектов у людей пожилого возраста аналогичны тем, которые установлены для других возрастных групп (особое внимание в этой возрастной группе следует уделить контролю функции почек).
Меры предосторожности
С особой осторожностью следует использовать у пациентов с нарушением функции почек. У всех пациентов необходимо оценить до начала терапии, а затем во время лечения тщательно мониторировать функцию почек (предпочтительно путем определения клиренса креатинина), печени и картину периферической крови. У больных с почечной недостаточностью следует контролировать функцию почек не реже 1 раза в неделю. Не следует назначать больным, страдающим почечной недостаточностью, при отсутствии аппаратуры, позволяющей проводить мониторинг концентрации флуцитозина в сыворотке крови. Следует соблюдать осторожность при применении у больных с подавленной функцией костного мозга или с заболеваниями крови. Необходимо контролировать картину периферической крови и функцию печени — ежедневно в начале лечения, затем — 2 раза в неделю.
Следует избегать длительного поддержания концентраций свыше 100 мг/л из-за увеличения риска развития побочных реакций.
При измерении уровня флуцитозина в сыворотке крови следует учитывать, что концентрация в образцах крови, взятых во время или непосредственно после введения препарата, непоказательна для последующего подъема концентрации флуцитозина в сыворотке. В целях мониторинга сывороточной концентрации рекомендуется проводить анализ крови незадолго до проведения следующей процедуры.
При определении уровня креатинина с помощью двухэтапного ферментного анализа не исключается искажение результатов анализа (ложноположительная азотемия) вследствие влияния флуцитозина. Необходимо использовать другие методы определения креатинина.
При расчетах объема введения растворов электролитов для больных, страдающих почечной и/или сердечной недостаточностью, а также с нарушением электролитного баланса, необходимо учитывать объем вводимого инфузионного раствора флуцитозина и содержание натрия (138 ммоль/л).
Фармакологическое действие
Противогрибковое средство, фторированный пиримидин. В клетках чувствительных возбудителей флуцитозин посредством специфической цитозиндезаминазы дезаминируется до 5-фторурацила, который встраивается в РНК возбудителя вместо урацила, нарушая тем самым синтез белка. Кроме того, подавляется активность тимидилатсинтетазы, что приводит к нарушению синтеза ДНК гриба.
In vivo и in vitro препарат оказывает фунгистатическое и фунгицидное действие в отношении дрожжевых грибов, возбудителей криптококкоза и хромобластомикоза. При аспергиллезе проявляет фунгистатическую активность.
Минимальная подавляющая концентрация — 0.03-12.5 мг/л.
В процессе лечения возможно развитие устойчивости первоначально чувствительных штаммов, поэтому определение чувствительности следует проводить до и во время лечения.
Фармакокинетика
После приема внутрь хорошо распределяется в тканях и жидких средах организма, диффундирует в спинномозговую жидкость. Vd после в/в введения составляет 0.8 л/кг. Связывание с белками плазмы низкое и составляет 2-4%. Концентрация в спинномозговой и перитонеальной жидкостях составляет примерно 75% от концентрации в сыворотке.
Небольшое количество флуцитозина дезаминируется в 5-фторурацил.
90% дозы флуцитозина выводится почками в неизмененном виде (клубочковая фильтрация). У взрослых и детей с нормальной функцией почек T1/2 составляет 3-6 ч. При нормальной функции почек концентрация вещества в моче всегда гораздо выше, чем в сыворотке. Поскольку флуцитозин выводится почками практически в неизмененном виде, при нарушениях функции почек T1/2 увеличивается. T1/2 у недоношенных детей составляет 6-7 ч.
Показания активного вещества
ФЛУЦИТОЗИН
Лечение системных микозов, вызванных чувствительными штаммами грибов: генерализованный кандидоз, криптококкоз, хромобластомикоз, аспергиллез (только в сочетании с амфотерицином В), инфекции, вызываемые грибами Torulopsis glabrata и Hansenula.
Режим дозирования
Вводят в/в капельно; допустимо прямое в/в введение через центральный венозный катетер или введение посредством перитонеальной инфузии.
Рекомендуемая суточная доза для взрослых и детей составляет 100-200 мг/кг массы тела.
Кратность введения и длительность лечения определяются индивидуально и зависят от показаний, схемы лечения, функции почек.
Побочное действие
Со стороны сердечно-сосудистой системы: остановка сердца, нарушение функции желудочков, боли за грудиной.
Со стороны дыхательной системы: остановка дыхания, одышка.
Со стороны пищеварительной системы: тошнота, рвота, боли в области живота, диарея, анорексия, сухость во рту, язва двенадцатиперстной кишки, желудочно-кишечные кровотечения, язвенный колит, нарушение функции печени, желтуха, повышение активности ферментов печени, гипербилирубинемия; в единичных случаях у ослабленных больных отмечалась острая печеночная недостаточность, иногда приводившая к летальному исходу.
Со стороны ЦНС и периферической нервной системы: атаксия, потеря слуха, головные боли, парестезии, паркинсонизм, периферическая невропатия, головокружение, седативный эффект, судороги, утрата четкого восприятия действительности, галлюцинации, психозы.
Со стороны мочевыделительной системы: азотемия, повышение уровня креатинина, мочевины, азота, кристаллурия, острая почечная недостаточность.
Со стороны системы кроветворения: анемия, агранулоцитоз, апластическая анемия, эозинофилия, лейкоцитопения, панцитопения, тромбоцитопения, гемолитическая анемия. В единичных случаях у ослабленных больных (на фоне имеющейся иммуносупрессии) отмечались признаки угнетения кроветворения в костном мозге (панцитопения). У данной категории больных эти симптомы могут носить необратимый характер.
Аллергические реакции: сыпь, зуд, крапивница, фоточувствительность, токсический эпидермальный некролиз.
Прочие: усталость, слабость, чрезмерная чувствительность, пирексия, гипогликемия, гипокалиемия.
Противопоказания к применению
Повышенная чувствительность к флуцитозину.
Применение при беременности и кормлении грудью
Адекватных и строго контролируемых клинических исследований безопасности применения препарата при беременности не проводилось. Поэтому применение возможно только в тех случаях, когда ожидаемая польза терапии для матери превышает потенциальный риск для развития плода.
Не установлено, выделяется ли флуцитозин с грудным молоком. При необходимости применения в период лактации следует решить вопрос о прекращении грудного вскармливания.
Применение при нарушениях функции почек
Не следует применять у больных с почечной недостаточностью при отсутствии оборудования позволяющего проводить мониторинг концентрации флуцитозина в сыворотке крови.
До и во время лечения следует контролировать функцию почек (предпочтительно путем определения клиренса креатинина). У пациентов с почечной недостаточностью следует контролировать функцию почек не реже 1 раза в неделю. При необходимости проводится соответствующая коррекция режима дозирования.
Особые указания
Не следует применять у больных с почечной недостаточностью при отсутствии оборудования позволяющего проводить мониторинг концентрации флуцитозина в сыворотке крови.
До и во время лечения рекомендуется проводить определение чувствительности возбудителей к флуцитозину. Для этой цели используются тесты, а также соответствующие питательные среды, свободные от антагонистов. Рекомендуется использование дисковых тестов с флуцитозином.
Следует соблюдать осторожность при применении у пациентов с миелодепрессией или с заболеваниями крови. Следует контролировать картину периферической крови и показатели функции печени ежедневно в начале лечения, затем — 2 раза в неделю.
При измерении концентрации флуцитозина в сыворотке следует учитывать, что концентрация флуцитозина в образцах крови, взятых во время или непосредственно после введения, не отражает последующий подъем концентрации флуцитозина в сыворотке. В целях мониторинга сывороточной концентрации флуцитозина рекомендуется проводить анализ крови незадолго до проведения следующей процедуры.
До и во время лечения следует контролировать функцию почек (предпочтительно путем определения клиренса креатинина). У пациентов с почечной недостаточностью следует контролировать функцию почек не реже 1 раза в неделю. При необходимости проводится соответствующая коррекция режима дозирования.
При определении уровня креатинина с помощью двухэтапного ферментного анализа возможно искажение результатов анализа (ложноположительная азотемия) вследствие влияния флуцитозина. Необходимо использовать другие методы определения креатинина.
При расчетах объема введения растворов электролитов для больных с почечной и/или сердечной недостаточностью, а также с нарушением электролитного баланса, необходимо учитывать объем вводимого инфузионного раствора флуцитозина и содержание натрия (138 ммоль/л).
Лекарственное взаимодействие
В исследованиях in vitro и in vivo было показано, что при комбинированном применении флуцитозина и амфотерицина В их активность взаимно усиливается в отношении многих штаммов возбудителей. Этот эффект был особенно выражен в отношении возбудителей, малочувствительных к флуцитозину.
При одновременном применении с цитостатиками повышается риск развития лейкопении (особенно нейтропении, часто сопровождаемой тромбоцитопенией). Поэтому при необходимости назначения данной комбинации следует контролировать состав периферической крови.
Поскольку флуцитозин выводится почти исключительно почками, все лекарственные препараты, снижающие клубочковую фильтрацию, увеличивают его T1/2 (в случае комбинированной терапии требуется регулярный контроль КК, а также соответствующая коррекция дозы).
Инфузионный раствор флуцитозина несовместим с другими лекарственными средствами, в т.ч. с амфотерицином В.
Антимикотики (АМ) для системного применения по праву могут быть отнесены к категории жизнеспасающих препаратов. Возрастание числа ИМ требует от клинициста не только грамотных диагностических действий, но и своевременного назначения адекватной по клинико-фармакологическим характеристикам противогрибковой терапии. Несмотря на небольшое число доступных АМ для системного применения, они имеют ряд кардинальных различий, что следует учитывать при выборе препарата. В настоящее время доступны АМ из пяти основных групп: полиены, азолы, эхинокандины, флюоропиримидины и аллиламины. Каждая из групп имеет свои особенности по спектру активности, фармакокинетике, безопасности и показаниям к применению, включая различия и внутри самого класса, что наиболее характерно для азолов. Знание эпидемиологии чувствительности грибковых патогенов служит еще одной важной составляющей адекватного выбора терапии.
Введение
Инвазивные микозы (ИМ) остаются актуальной медицинской проблемой. Ежегодно примерно у 300 млн людей по всему миру регистрируются серьезные микотические инфекции, которые приводят как минимум к 1,5 млн смертей (www.gaffi.org). Грибковые патогены могут вызывать как легкие поверхностные формы инфекций (орофарингеальный или вульвовагинальный кандидоз), так и тяжелые клинические варианты, такие как инвазивный кандидоз, инвазивный аспергиллез, мукормикозы и др. ИМ, как правило, развиваются на фоне тяжелых фоновых заболеваний, включая ВИЧ-инфекцию, злокачественные новообразования, трансплантацию органов, терапию кортикостероидами, а к основным их возбудителям относятся грибы рода Candida, Aspergillus и Cryptococcus. Безусловно, для успешного лечения ИМ необходимо применение адекватной противогрибковой терапии. К сожалению, выбор антимикотиков (АМ) для системного применения очень ограничен, а основными мишенями действия существующих препаратов являются клеточная мембрана, клеточная стенка и биосинтез нуклеиновых кислот. Доступные классы АМ включают полиены, азолы, эхинокандины, флюоропиримидины и аллиламины. Несмотря на то что большинство из применяемых АМ зарегистрировано уже достаточно давно и всесторонне изучено, осведомленность врачей касательно ключевых аспектов клинической фармакологии АМ для системного применения, как показывает практика, зачастую оставляет желать лучшего. Цель данного обзора – изложение в сжатой форме ключевых клинико-фармакологических характеристик имеющихся системных противогрибковых препаратов, использующихся в различных клинических ситуациях среди гетерогенной популяции пациентов с ИМ [1–3].
Полиены
АМ класса полиенов являются одними из первых синтезированных противогрибковых препаратов. Несмотря на то что с середины прошлого века было получено более 200 различных молекул полиенов, проблемы, связанные с растворимостью, стабильностью, биодоступностью и переносимостью, обусловили внедрение в практику очень небольшого числа препаратов для системного применения, которые включают амфотерицин В (АмВ) и его липидные формы: липидный комплекс АмВ, коллоидную дисперсию АмВ и липосомальный АмВ [4].
Амфотерицин В
АмВ был синтезирован в 1955 г. при ферментации гриба Streptomyces nodosum и с 1957 г. применяется в клинической практике, оставаясь АМ с самым широким спектром действия и большим опытом клинического применения. АмВ обладает выраженной фунгицидной активностью с длительным постантифунгальным эффектом (ПАФЭ), достигающим 20 часов. Создает высокие концентрации в печени, селезенке, костном мозге, легких, почках; проходит через плацентарный барьер. У новорожденных и детей младшего возраста имеет место вариабельность фармакокинетики (ФК) АмВ с более продолжительным периодом полувыведения.
У недоношенных новорожденных проникновение АмВ в спинно-мозговую жидкость (СМЖ) достигает 40% от сывороточной концентрации, в то время как у взрослых этот показатель не превышает 2–4% [4, 5].
Ключевой причиной, ограничивающей применение АмВ, служат проблемы, связанные с его переносимостью и безопасностью. Нефротоксическое действие, тяжелые инфузионные реакции, электролитные нарушения, проявления со стороны центральной нервной системы (ЦНС) часто делают невозможным применение АмВ, хотя у детей раннего возраста переносимость препарата лучше таковой у взрослых. В тех ситуациях, когда по тем или иным причинам у нас нет возможности применять другие АМ (непереносимость, отсутствие активности, недоступность препарата), АмВ может стать единственным вариантом терапии. Помимо этого АмВ является, пожалуй, самым доступным с финансовой точки зрения АМ для системного применения, если не учитывать огромное число генериков сомнительного качества среди препаратов других групп. Для АмВ характерна очень низкая частота развития вторичной резистентности, однако проблемными патогенами могут быть Trichosporon beigelii, Aspergillus terreus, Pseudallescheria boydii, Fusarium spp., Candida lusitaniae и др. [4, 5].
АмВ сохраняет свое значение в качестве препарата глубокого резерва при терапии инфекций, вызванных чувствительными возбудителями, при невозможности применения других АМ. При комбинированной терапии криптококковой инфекции, в частности менингита, АмВ является препаратом выбора.
Липидные формы амфотерицина В
Липидные формы АмВ были получены в 1990-х гг., основная цель при их синтезе – улучшение переносимости АмВ при сохранении широты спектра его действия. Действительно, спектр активности липидных форм АмВ идентичен обычному АмВ, однако ФК и нежелательные лекарственные реакции (НЛР) данных препаратов определяют их основные различия, на которых необходимо остановиться подробнее.
Размер молекул и структура липидного компонента – определяющие для их ФК и как следствие – для особенностей применения. Липосомальный АмВ имеет наименьший размер молекул, что позволяет ему создавать высокие концентрации в крови, ЦНС, печени, селезенке; меньшие – в почках и легких. Липидный комплекс АмВ имеет самый крупный размер молекул, что приводит к их быстрому захвату макрофагами с последующим высвобождением в тканях. Это обусловливает относительно низкие концентрации в плазме, но при этом высокие концентрации, например, в легких. Липидный комплекс АмВ и коллоидная дисперсия АмВ создают высокие концентрации в межклеточном пространстве и органах ретикулоэндотелиальной системы. Максимальный концентрационно-зависимый эффект полиенов достигается, как правило, на фоне применения дозы 5 мг/кг, при этом увеличение концентрации в 2–3 раза не сопровождается увеличением эффективности, однако может приводить к увеличению токсичности, что, в частности, было показано в исследовании AmBiLoad при сравнении липосомального АмВ в дозах 3 и 10 мг/кг/сут [5–7].
Среди трех представителей липидных форм АмВ коллоидная дисперсия обладает наиболее неблагоприятным профилем переносимости. Это связано, в частности, с необходимостью применения относительно высоких доз препарата для достижения оптимальных терапевтических концентраций – от 4 мг/кг и выше. Однако при повышении этих значений отмечено возрастание риска нефротоксических и инфузионных реакций, частота которых приближается к таковой обычного АмВ [5].
На сегодняшний день показанием к применению липидных форм АмВ служат тяжелые рефрактерные формы ИМ, вызванные прежде всего мицелиальными грибами, а также эмпирическая терапия нейтропенической лихорадки и комбинированная терапия криптококковой инфекции [4, 6].
Азолы
Азолы в зависимости от времени своего появления, а также клинико-фармакологических особенностей подразделяются на азолы первого поколения (или «ранние» азолы) – кетоконазол, флуконазол и итраконазол, и азолы второго поколения – вориконазол и позаконазол. Механизм действия всех азолов связан с нарушением синтеза эргостерола за счет блокады активности фермента ланостерол-14α-деметилазы. Азолы обладают концентрационно-независимым действием с максимальным эффектом при концентрации, находящейся примерно на уровне МПК, превышение которой не увеличивает степень ингибирования роста грибов [8].
Клиническое значение азолов на сегодняшний день исключительно велико, при этом каждый из системных азолов как первого, так и второго поколения с учетом особенностей ФК, фармакодинамики и результатов проведенных клинических исследований имеет свою нишу в терапии ИМ.
Реально существующей проблемой служат вариабельные, но имеющие тенденцию к постоянному росту показатели вторичной резистентности среди грибов рода Candida. В России в настоящее время процент устойчивых к флуконазолу штаммов C. albicans варьируется в пределах 5–20%, однако для C. glabrata данный показатель может превышать 25%. Эта цифры в целом коррелируют с таковыми в Европе и США, но в некоторых случаях могут быть ощутимо ниже [9–11].
Флуконазол
Флуконазол является, пожалуй, самым широко изученным и наиболее применяемым среди производных азолов, однако его спектр активности ограничен дрожжевыми патогенами (Candida spp., Cryptococcus spp.), некоторыми дерматомицетами и диморфными грибами. Флуконазол не активен в отношении практически всех мицелиальных грибов, включая Aspergillus spp. [5, 12].
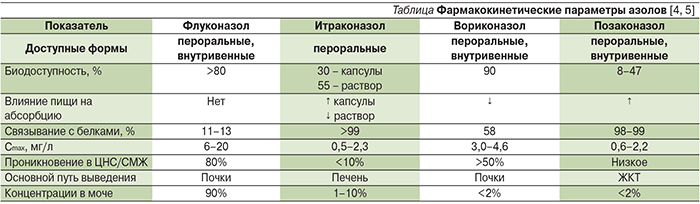
Обладает высокой биодоступностью (до 100%), не зависимой от приема пищи и внутрижелудочного рН, характеризуется длительным периодом полувыведения и низким связыванием с белками, что позволяет создавать высокие концентрации в биологических жидкостях (в моче до 80% от сывороточной). ФК флуконазола наименее вариабельна по сравнению с другими азолами (см. таблицу). У детей отмечается больший объем распределения, а у новорожденных флуконазол имеет особенности дозирования: препарат в первые 2 недели жизни вводится 1 раз в 72 часа, в течение 3-й недели – 1 раз в 48 часов, начиная с 4-й недели дозируется, как и у взрослых, ежедневно 1 раз в сутки [5, 12].
Флуконазол является своего рода «золотым» стандартом безопасности противогрибковой терапии, включая меньший риск развития лекарственных взаимодействий по сравнению с итраконазолом или вориконазолом. Основные НЛР флуконазола связаны с симптомами со стороны желудочно-кишечного тракта (ЖКТ; тошнота, рвота, диарея). Возможны НРЛ со стороны печени, кожи, ЦНС, но их частота редко превышает 1% [5, 12–14].
Основной сферой применения флуконазола являются поверхностные или инвазивные формы кандидозной инфекции, обусловленные чувствительными к флуконазолу штаммами, включая профилактику кандидоза. Он может использоваться для терапии криптококкоза, кокцидиоидомикоза и отдельных форм дерматомикозов. Говоря об инвазивном кандидозе, необходимо выделить те ситуации, когда от применения флуконазола следует воздериважаться: тяжелое состояние пациента, невозможность провести скрининг чувствительности к этому препарату, отсутствие видовой идентификации Candida spp., выделение C. krusei или C. glabrata, терапия азолами в анамнезе и высокий локальный уровень резистентности грибов рода Candida к азолам [15].
Итраконазол
Итраконазол был первым азолом, продемонстрировавшим активность в отношении грибов рода Aspergillus и ряда представителей Dematiaceous. Он обладает примерно одинаковой с флуконазолом активностью в отношении Сandida spp., однако более активен в отношении дерматомицетов и диморфных грибов. Поскольку итраконазол служит слабым основанием, для его оптимального всасывания при приеме внутрь необходима кислая среда. В этом причина вариабельной биодоступности, что наиболее характерно для капсул (≈30%) и в меньшей степени – для перорального раствора (≥55%) итраконазола, который наилучшим образом всасывается натощак и которому в настоящее время отдается предпочтение при терапии per os [13, 16].
Итраконазол является ингибитором и субстратом для Р-гликопротеина и CYP3А4, что приводит к снижению концентраций мидазолама, атазанавира, ритонавира, такролимуса, циклоспорина и некоторых других препаратов. Следует иметь в виду возможность возникновения НЛР со стороны ЖКТ, что характерно для перорального раствора, а также отрицательный инотропный эффект итраконазола, что требует осторожного его применения пациентами с сердечной недостаточностью. Форма для внутривенного введения итраконазола долгое время была зарегистрирована во многих странах, но в настоящее время уходит с рынка, в частности, в связи с нефротоксическим эффектом входящего в ее состав циклодекстрина [13, 17].
С учетом особенностей ФК и профиля безопасности итраконазол сохраняет свою роль при дерматомикозах, в т.ч. онихомикозах, эндемичных микозах (бластомикоз, гистоплазмоз), споротрихозе, а также при некоторых формах аспергиллеза, например аллергическом бронхо-легочном аспергиллезе. Пероральный раствор итраконазола может использоваться для терапии орофарингеального кандидоза, кандидоза пищевода и профилактики ИМ у пациентов групп высокого риска. Терапевтический лекарственный мониторинг (ТЛМ) сывороточных концентраций итраконазола считается рекомендованной процедурой в течение первой недели терапии в случае отсутствия ответа, появления прорывных грибковых инфекций, при нарушенной функции ЖКТ, а также при риске развития лекарственных взаимодействий [13, 18].
Вориконазол
Вориконазол – препарат выбора при терапии большинства форм инфекций, вызванных грибами рода Aspergillus. Обладая приблизительно одинаковой активностью с флуконазолом в отношении Candida spp. (кроме C. krusei, против которой вориконазол демонстрирует стабильно высокую активность), вориконазол действует на грибы рода Fusarium и Scedosporium, что кардинально отличает его от ранних азолов. В настоящее время есть данные о появлении перекрестной резистентности среди флуконазол-резистентных штаммов Candida spp. [5, 19].
Биодоступность пероральной формы вориконазола может превышать 90% при приеме натощак. Вариабельные сывороточные концентрации в связи с нелинейной ФК вориконазола, обусловленные пресистемным метаболизмом в печени, а также генетический полиморфизм CYP2C19 являются причиной появления НЛР, а также обусловливают необходимость проведения ТЛМ. Было показано, что менее 50% пациентов достигают целевых базальных концентраций вориконазола без проведения индивидуального ТЛМ [20]. Среди НЛР помимо характерных для других азолов (симптомы со стороны ЖКТ, гепатотоксичность) следует отметить нарушения со стороны органа зрения (блокада TRPM1 каналов биполярных ON-клеток сетчатки), кожные реакции, ментальные нарушения, случаи периостита, аллопеции, изменения ногтевых пластинок и др. [5, 21].
Для вориконазола характерна высокая внутри- и межиндивидуальная вариабельность ФК, при этом на клиренс препарата значимое влияние оказывает генотип CYP2C19. Осторожность следует соблюдать пациентам с почечной недостаточностью при применении вориконазола внутривенно в связи с входящим в состав внутривенной формы циклодекстрина. При клиренсе креатинина <50 мл/мин необходимо оценивать соотношение польза/риск для внутривенного применения вориконазола. Отдельное внимание следует уделить лекарственным взаимодействиям (CYP2С19, 2С9 и CYP3A4) с учетом метаболизма препарата в печени. Противопоказанные комбинации включают рифампин, длительно действующие барбитураты, карбамазепин, сиролимус, терфенадин и др. [5, 19].
Помимо аспергиллеза, о чем было сказано выше, вориконазол применяется при терапии инвазивного кандидоза, в т.ч. вызванного C. krusei. Может применяться при кандидозе пищевода. При фузариозе и сцедоспориозе вориконазол является пока единственным АМ с официальными показаниями. Разрешен к применению детьми старше 2 лет [13]. Появляется все больше данных о возможностях профилактической терапии вориконазолом пациентов групп высокого риска [22], однако официального показания касательно профилактики препарат в настоящий момент не имеет.
Позаконазол
Позаконазол первым среди всех АМ проявил значимую активность в отношении возбудителей мукормикозов (Mucorales). Активность в отношении грибов рода Candida, Aspergillus, Fusarium, Scedosporium сравнима с таковой вориконазола [23].
Долгое время позаконазол был доступен только в виде суспензии для приема внутрь, для которой характерна вариабельность ФК, что связано с изменяющейся абсорбцией препарата (8–50%) в зависимости от наличия пищи и рН в желудке. Причиной снижения абсорбции и как следствие – плазменной концентрации служат мукозит, прием препаратов подавляющих желудочную секрецию (ингибиторы протоновой помпы, Н2-блокаторы), а также тошнота, диарея и рвота.
В свою очередь повышение плазменной концентрации отмечается на фоне приема высококалорийной пищи. Регистрация Управлением по контролю за качеством пищевых продуктов и лекарственных препаратов (FDA) новых лекарственных форм позаконазола – таблеток и формы для внутривенного введения – открывают новые возможности терапии. Это связано со значимо лучшей ФК таблетированной формы (прием 1 раз в сутки, лучшая системная биодоступность, отсутствие зависимости абсорбции от приема пищи и рН в желудке), а парентеральная форма препарата позволит использовать позаконазол для ступенчатой терапии, однако необходимо отметить, что, как и у внутривенной формы вориконазола, в ее состав входит циклодекстрин, что может стать потенциальной причиной его аккумуляции при клиренсе креатинина < 50 мл/мин [5, 23, 24].
В целом ФК позаконазола одинакова для взрослых и детей старше 8 лет, в то время как для детей младше 8 лет ФК на настоящий момент изучена недостаточно полно. В отличие от итраконазола и вориконазола для позаконазола характерен меньший риск развития лекарственных взаимодействий, т.к. он метаболизируется при незначительном участии ферментов CYP450, однако возможны взаимодействия, обусловленные его ингибированием CYP3A4. В связи с высоким процентом связывания с белками (99%) препарат создает низкие концентрации в моче и СМЖ. Профиль переносимости позаконазола приближается к таковому флуконазола, и основные НЛР представлены симптомами со стороны ЖКТ. При терапии позаконазолом также рекомендовано проведение ТЛМ (отсутствие ответа, прорывные инфекции, нарушения функции ЖКТ, сопутствующая терапия) [5, 23, 24].
Учитывая его спектр активности и тот факт, что пока в РФ позаконазол доступен только в форме раствора для перорального применения, данный АМ используется для терапии тяжелых ИМ при неэффективности препаратов первой линии. Он может применяться как препарат выбора в качестве терапии орофарингеального кандидоза. Однако основной нишей позаконазола является профилактика ИМ у пациентов с высоким риском их развития, что было подтверждено результатами ряда клинических исследований, и в настоящее время в отношении данного показания он имеет наивысший уровень доказательности данных – АI. В отношении детей разрешен к применению с 13 лет [13, 25].
Эхинокандины
Эхинокандины – анидулафунгин, каспофунгин, микафунгин – представляют собой исключительно важный с клинической точки зрения класс АМ. Во-первых, эхинокандины обладают уникальным механизмом действия, связанным с ингибированием ферментов 1,3- и 1,6-β-D-глюкансинтетазы, ответственных за синтез β-D-глюкана, представляющего собой полимер глюкозы, обеспечивающий структуру и целостность клеточной стенки грибковых патогенов [26]. Поскольку данный фермент отсутствует в клетках человека, у эхинокандинов хороший профиль переносимости, включая низкую нефро- и гепатотоксичность. Во-вторых, эхинокандины обладают высокой фунгицидной активностью в отношении грибов рода Candida, включая штаммы, резистентные к азоловым АМ, а также демонстрируют активность в отношении биопленок Candida spp. Они также действуют на грибы рода Aspergillus, Pneumocystis jiroveci и некоторые мицелиальные грибы (Acremonium, Curvularia, Bipolaris и др.). В отношении грибов рода Aspergillus эхинокандины оказывают фунгистатическое действие за счет лизиса апикальных отделов гиф мицелия, изменяя их морфологию и структуру. В-третьих, эхинокандины обладают достаточно предсказуемым и маловариабельным профилем ФК, что безусловно облегчает достижение клинического эффекта. Эхинокандины имеют выраженный концентрационно-зависимый эффект с длительным ПАФЭ, при этом однократные высокие дозы обеспечивают быстрое достижение целевых показателей, в связи с чем все эхинокандины вводятся один раз в сутки. Обладая высокой молекулярной массой, все эхинокандины имеют низкую абсорбцию при приеме внутрь, а в связи с высоким (до 99%) связыванием с белками плохо проникают и, соответственно, создают низкие концентрации в ЦНС и глазном яблоке [5, 27–29].
С 2007 г. при определении чувствительности Сandida spp. к эхинокандинам использовался один критерий, предложенный Институтом клинических и лабораторных стандартов (CLSI), для всех препаратов этой группы применительно ко всем видам Candida – ≤2 мкг/мл. Однако появление за последние несколько лет случаев неэффективности терапии при выделении штаммов с относительно низкими значениями минимальной подавляющей концентрации (МПК), но при наличии у штаммов приобретенных мутаций генов FKS1 и FKS2, сделало необходимым пересмотр данного критерия, представленного CLSI в 2013 г., примерно в одно время с критериями интерпретации Европейского комитета по определению чувствительности к антимикробным препаратам (EUCAST). После внедрения в практику указанных критериев стали появляться данные о недостаточно четком их соответствии эффективности препаратов in vivo, когда при выделении штаммов со сниженной чувствительностью у пациентов, тем не менее, отмечалась клиническая эффективность терапии эхинокандинами. Наиболее часто это имело место при инфекциях C. glabrata-вида, который на сегодня является самым проблемным в плане чувствительности (рост числа устойчивых штаммов c 2–3% в 2001–2006 гг. до >13% в 2009–2010 гг.). Кроме того, было показано, что независимым предиктором клинической неэффективности терапии эхинокандинами инфекции C. glabrata является не МПК, а наличие у штамма мутаций генов FKS1 и FKS2. Вполне возможно, что в будущем это может потребовать определенного пересмотра критериев и стать основой разработки молекулярных методик определения чувствительности. Тем не менее в настоящее время проблем с устойчивостью грибов рода Candida к эхинокандинам в России нет, что, в частности, было показано в недавно проведенном исследовании КРИТ, где каспофунгин показал активность в отношении 100% штаммов с использованием критериев CLSI. В целом это говорит о том, что нам необходимы дальнейшие масштабные исследования оценки корреляции показателей активности эхинокандинов in vitro с имеющимися мутационными изменениями отдельных генов и, что наиболее важно, с клинической эффективностью препаратов, включая оценку режимов дозирования, продолжительности терапии, критериев ее отмены. Отдельным вопросом остаются высокие исходные показатели МПК эхинокандинов в отношении C. parapsilosis complex и C. guilliermondii. Указанная природная сниженная чувствительность не продемонстрировала связи с клинической эффективностью, т.к. случаи ИМ, обусловленных данными возбудителями, с успехом отвечают на терапию эхинокандинами [10, 30–33].
Показатели ФК, профиль лекарственных взаимодействий и показания к применению определяют основные различия между эхинокандинами, которые следует учитывать при их назначении.
Каспофунгин
Каспофунгин был первым зарегистрированным в 2003 г. АМ группы эхинокандинов и в настоящее время является наиболее изученным препаратом с большим опытом применения различными категориями пациентов. Каспофунгин разрешен к терапии инвазивного кандидоза и инфекций, вызванных грибами рода Candida (интраабдоминальные абсцессы, перитонит и инфекции плевры), кандидоза пищевода, и является единственным эхинокандином, показанным к эмпирической терапии нейтропенической лихорадки у пациентов группы высокого риска, а также для терапии инвазивного аспергиллеза при неэффективности препаратов первой линии [5, 13].
Каспофунгин обладает рядом клинически значимых лекарственных взаимодействий, включая рифампицин, эфавиренз, невирапин, фенитоин, дексаметазон и карбамазепин. Каспофунгин, как и другие эхинокандины, не требует коррекции доз при почечной недостаточности, однако в отличие от других представителей этой группы требует снижения дозы на 50% для пациентов с умеренной степенью печеночной недостаточностью. В отличие от микафунгина и анидулафунгина обладает нелинейной ФК. В отношении детей каспофунгин разрешен к применению с 3-месячного возраста [5].
Микафунгин
Микафунгин был зарегистрирован в 2005 г. и стал одним из немногих АМ, разрешенных к применению у детей с рождения. Имея аналогичные с каспофунгином показания касательно инвазивного кандидоза и кандидоза пищевода, микафунгин является единственным эхинокандином, показанным к профилактике ИМ, вызванных грибами рода Candida, пациентам с трансплантацией кроветворных стволовых клеток или у которых предполагается нейтропения (нейтрофилов <500 в мкл) в течение 10 и более дней [5, 13].
Микафунгин не требует коррекции доз при печеночной или почечной недостаточности. Из клинически значимых лекарственных взаимодействий следует отметить сиролимус и нифедипин. С учетом особенностей ФК микафунгина он не требует введения нагрузочной дозы в отличие от других эхинокандинов, однако для достижения равновесной концентрации ему требуется больший период времени (до 72 часов) [5, 13].
Микафунгин в инструкции по применению препарата в Европе имеет т.н. предупреждение в черной рамке (Black Box Warning). Это связано с результатами доклинических исследований длительного применении препарата у крыс в дозах, приводящих к созданию концентраций, близких к терапевтическим концентрациям у человека, которые показали возможность формирования локальных очагов измененных гепатоцитов и печеночно-клеточных опухолей у подопытных животных. Однако с момента получения этих данных и до настоящего времени ни одного случая подобных изменений у человека, в т.ч. и при использовании высоких доз микафунгина, отмечено не было. Кроме того, микафунгин не имеет различий с другими эхинокандинами по частоте появления изменений функциональных показателей печени на фоне терапии, а также не обнаружил изменений ФК у пациентов с фоновыми нарушениями функции печени [13, 34].
Анидулафунгин
Анидулафунгин был зарегистрирован последним из трех эхинокандинов и обладает рядом уникальных свойств. Прежде всего анидулафунгин характеризуется самым большим периодом полувыведения препарата, что потенциально может свидетельствовать о более продолжительном ПАФЭ, и объемом распределения, который говорит об активном накоплении препарата в органах с созданием высоких тканевых концентраций. Анидулафунгин подвергается спонтанной химической деградации, и в связи с отсутствием метаболизма препарата в печени у анидулафунгина нет известных лекарственных взаимодействий; в исследованиях совместное применение с циклоспорином приводило к некоторому увеличению концентраций анидулафунгина, но оно не было расценено как клинически значимое [5, 13, 35].
Анидулафунгин показан к терапии инвазивного кандидоза и кандидемии, а также кандидоза пищевода. Разрешен к применению с 18-летнего возраста [13].
Флюоропиримидины
Флуцитозин (5-фторцитозин)
К флюоропиримидинам относится один препарат – флуцитозин (5-фторцитозин, 5-ФЦ), синтезированный в 1957 г. в качестве, возможно, средства терапии злокачественных новообразований. В последующем на животных моделях была показана его активность при инфекциях, вызванных C. albicans и C. neoformans. Клиническое применение 5-ФЦ началось в 1968 г., в связи с чем это один из старейших из применяемых по сей день АМ. Механизм действия 5-ФЦ связан с подавлением синтеза рибонуклеиновых кислот за счет нарушения белкового синтеза и ингибирования тимидилатсинтетазы, участвующей в синтезе тимидина [4, 36].
5-ФЦ обладает высокой (80–90%) биодоступностью и создает высокие концентрации в СМЖ, костном мозге, синовиальной и в перитонеальной жидкостях, т.к. связывается с белками только на 2–4%. До 90% препарата выводится в неизменном виде через почки с периодом полувыведения от 2,5 до 6,0 часов. Обладает концентрационно-независимым эффектом в отношении Candida spp. с максимальной выраженностью при концентрации, близкой к МПК, с быстрым возобновлением роста при падении концентрации, в связи с чем рекомендовано частое введение небольших доз препарата. С максимальной концентрацией напрямую связана и токсичность, что требует дробного введения 5-ФЦ [4, 36].
Важными ограничивающими факторами применения являются плохая переносимость 5-ФЦ (НЛР со стороны ЖКТ, нефро-, гематотоксичность, неврологические нарушения) и высокий риск быстрого развития вторичной резистентности, в связи с чем препарат применяется только в комбинации с другими АМ [4, 36].
В настоящее время 5-ФЦ является препаратом выбора для комбинированной терапии криптококковой инфекции, в частности криптококкового менингита в сочетании с АмВ (или его липидными формами) или флуконазолом [13].
Аллиламины
Тербинафин
Тербинафин относится к классу аллиламинов и представляет собой препарат как для местного, так и для системного применения с преимущественно фунгицидным действием, связанным с нарушением синтеза эргостерола за счет подавления активности фермента скваленэпоксидазы. Спектр активности тербинафина включает грибы рода Trichophyton, Epidermophyton, Microsporum, что определяет основные показания к его применению. Активен в отношении Malassezia spp., Trichosporon spp., Candida spp., Aspergillus spp., Fusarium spp., возбудителей феогифомикозов (Hortae spp., Exophiala spp.), а также возбудителей эндемичных микозов, хотя это имеет ограниченное клиническое значение [4].
Кислотность и прием пищи не влияют на абсорбцию тербинафина. Он связывается с белками более чем на 90%, в связи с чем создает низкие концентрации в биологических жидкостях, но благодаря высокой липофильности активно накапливается в роговом слое кожи, волосяных фолликулах, волосах. Тербинафин метаболизируется в печени с периодом полувыведения примерно 17 часов [4, 13].
Основные НЛР связаны с симптомами со стороны ЖКТ: диарея, тошнота, абдоминальный дискомфорт, реже – нарушения вкуса, еще реже – нарушения функции печени. На фоне применения тербинафина имели место случаи тяжелых поражений кожных покровов, в частности токсический эпидермальный некролиз [4].
Тербинафин применяется прежде всего для терапии микозов кожи и ее придатков, вызванных дерматомицетами. Помимо этого используется для терапии хромомикоза – инфекций кожи и подкожной клетчатки, вызванных грибами рода Fonsecaea, Phialophora и др., а также при тяжелых рефрактерных инфекциях, вызванных Fusarium spp. и Scedosporium spp., в т.ч. S. prolificans, в комбинации с вориконазолом [13, 37].
Заключение
В данном обзоре мы постарались кратко остановиться на ключевых клинико-фармакологических характеристиках АМ для системного применения. Была дана характеристика показателей активности препаратов in vitro, рассмотрены особенности всасывания метаболизма, выведения и лекарственных взаимодействий, а также профиля безопасности. Определено место в клинической практике каждого из обсуждаемых АМ. Безусловно, данный обзор ни в коей мере не может претендовать на определение «полный», т.к. каждый из препаратов имеет огромное число нюансов, а обсуждение клинического опыта применения любого из АМ потребует колоссальных объемов изложения. Тем не менее мы надеемся, что этот обзор сможет оказать помощь практикующим врачам в непростом выборе системных противогрибковых препаратов при лечении ИМ.
А.В. Веселов – к.м.н.,зам. директора по общим вопросам НИИАХ ГБОУ ВПО СГМУ Минздрава РФ, Смоленск;e-mail: alex.veselov@antibiotic.ru
5-Фторурацил
МНН: Фторурацил
Производитель: EBEWE Pharma Ges.m.b.H. Nfg.KG.
Номер регистрации в РК:
№ РК-ЛС-5№005148
Информация о регистрации в РК:
04.06.2012 — 04.06.2017
-
Скачать инструкцию медикамента
Торговое название
5-Фторурацил
“Эбеве”
Международное непатентованное название
Фторурацил
Лекарственная форма
Концентрат
для приготовления раствора для инфузий, 250 мг/5мл,
500
мг/10мл
Состав
1
мл раствора содержит
активное
вещество – 5-
фторурацил
50мг,
вспомогательные
вещества:
натрия
гидроксид, вода для
инъекций.
Описание
Прозрачный
бесцветный или почти бесцветный раствор.
Фармакотерапевтическая группа
Противоопухолевые
препараты. Пиримидиновые аналоги.
Код
АТС L01BC02
Фармакологические свойства
Фармакокинетика
После
внутривенного введения препарат быстро биотрансформируется и
распределяется в опухолевых тканях, слизистой оболочке кишечника,
костном мозге, печени и других тканях. Легко проникает через
гематоэнцефалический барьер, попадая в спинномозговую жидкость и
ткани головного мозга. Метаболизируется в основном в печени с
образованием неактивных метаболитов. Период полувыведения фторурацила
зависит от вводимой дозы, и составляет 8-22 минуты. Около 20%
препарата выводится почками в неизмененном виде в течение 6 часов
(90% из этого количества выводится в течение 1-го часа) и 60-80% —
через дыхательные пути в форме СО2,
незначительное количество выделяется с желчью.
Фармакодинамика
Фторурацил
— антиметаболит урацила. Механизм действия обусловлен
превращением препарата в тканях в активный метаболит
фторуридинмонофосфат, который является конкурентным ингибитором
фермента тимидилатсинтетазы, принимающего участие в синтезе
нуклеиновых кислот. Фторурацил нарушает синтез ДНК и вызывает
образование структурно несовершенной РНК, угнетая деление опухолевых
клеток. Активные метаболиты локализуются внутри клетки.
Показания к применению
5-
Фторурацил «Эбеве» применяется в качестве
моно-
или комбинированной с другими цитостатиками терапии при таких
злокачественных опухолях, как
—
рак молочной железы
—
колоректальный
рак (рак
толстой и прямой кишки)
Также
терапевтическая активность наблюдалась у пациентов с раком желудка,
раком головы и шеи и карциномой поджелудочной железы
Способ применения и дозы
Выбор
надлежащей дозировки и схемы лечения будет определяться
состоянием
больного, типом рака, подлежащего лечению, и видом терапии, т.е.
назначается ли 5-фторурацил в форме монотерапии или в комбинации с
другим
лекарственным средством.
Лечение
следует начинать в условиях стационара, и суммарная суточная доза
не
должна превышать 1 грамм.
Рекомендуется
ежедневно контролировать уровень тромбоцитов и лейкоцитов.
При
снижении содержания тромбоцитов ниже 100 000/мм3
или содержания
лейкоцитов
ниже 3000/м3,
лечение следует отменить.
Принято
рассчитывать дозу в соответствии с фактическим весом больного, за
исключением
тех случаев, когда имеет место ожирение, отеки или другие
формы
патологической задержки жидкости в организме, например, асцит.
В
вышеперечисленных случаях при расчетах используют величину
идеального
веса пациента.
5-
Фторурацил «Эбеве» назначают
посредством внутривенной инъекции,
внутривенной
или внутриартериальной инфузии.
Ниже
представлены ориентировочные дозировки:
Колоректальный
рак
(рак толстой и прямой кишки):
Лечение
начинают в форме инфузии или инъекции, причем первый способ
назначения предпочтительнее в связи с меньшей токсичностью.
Внутривенная
инфузия:
Суточную
дозу 5-
Фторурацил «Эбеве»,
составляющую 15 мг/кг массы тела (600 мг/м2),
но не более 1 г для каждой инфузии, разводят в 300-500 мл 5%
раствора глюкозы или в 300-500 мл 0,9%-го раствора хлорида натрия и
вводят посредством 4-часовой инфузии.
Такую
дозу назначают в течение нескольких дней подряд до возникновения
признаков токсичности, или пока суммарная доза не достигнет 12-15 г.
Некоторым пациентам назначали дозы до 30 г при максимальной суточной
дозе не выше 1 г.
Лечение
следует продолжать только после устранения гематологической или
желудочно-кишечной токсичности.
Другим
возможным вариантом является назначение 5-
Фторурацил «Эбеве» посредством
непрерывной 24-часовой инфузии.
Внутривенная
инъекция:
Возможно
назначение 5-
Фторурацил «Эбеве» посредством
внутривенной инъекции в дозе 12 мг/кг массы тела (480 мг/м2),
которую выполняют ежедневно в течение 3 дней. При отсутствии
признаков токсичности в дни 5, 7 и 9 пациенту может быть назначена
доза 6 мг/кг массы тела (240 мг/м2).
В
качестве поддерживающего лечения 1 раз в неделю назначают дозу 5-10
мг/кг (200-400 мг/м2)
посредством внутривенной инъекции. В любом случае поддерживающее
лечение можно начинать только после исчезновения проявлений
токсичности.
Рак
молочной железы:
Для
лечения рака молочной железы 5-
Фторурацил «Эбеве» может
быть назначен в
составе
комбинированной терапии, например, совместно с метотрексатом и
циклофосфамидом,
либо совместно с доксорубицином и циклофосфамидом. При
лечении по данной схеме в 1-й и 8-й дни 28-дневного курса назначают
внутривенную инъекцию 5-фторурацил в дозе 10-15 мг/кг (400-600
мг/м2).
Другим
возможным вариантом является назначение 5-
Фторурацил «Эбеве» посредством
непрерывной 24-часовой инфузии в дозе 8,25 мг/кг (350 мг/м2).
Другие
способы назначения.
Внутриартериальная
инфузия 5-
Фторурацил «Эбеве» может
быть назначена в форме непрерывной 24-часовой внутриартериальной
инфузии; суточная доза при этом составляет 5-7,5 мг/кг (200-300
мг/м2).
В отдельных случаях для лечения первичной опухоли или метастазов
может быть назначена региональная инфузия.
Пациентам
с одним из перечисленных ниже состояний рекомендуется снизить
дозировку:
—
кахексия
—
тяжелая операция, проведенная в течение 30 предшествующих дней
—
угнетение костного мозга
—
нарушений функции печени или почек
Рекомендации
по дозировке 5-
Фторурацил «Эбеве» для
детей отсутствуют. Пожилым пациентам коррекция дозы не требуется.
Побочные действия
Очень
часто
—
лейкопения, нейтропения, тромбоцитопения. Наиболее значительное
падение количества лейкоцитов обычно наблюдается с 9 по 14 день
(вплоть до 25 дня), тромбоцитов — с 7 по 17 день лечения
—
тошнота, рвота, диарея, воспаление слизистой оболочки
желудочно-кишечного тракта (стоматит, эзофагит, проктит, фарингит)
Часто
—
агранулоцитоз, анемия, панцитопения
—
преходящий обратимый церебральный синдром, при котором наблюдаются
атаксия, нистагм, спутанность сознания и экстрапирамидные
двигательные и кортикальные расстройства, которые обычно исчезают
после отмены 5- Фторурацила (нарушение речи, афазия, головная боль,
дезориентация, эйфория, судороги, периферическая нейропатия)
—
алопеция, которая является обратимой
Редко
—
лихорадка
—
аллергические реакции: крапивница, бронхоспазм, анафилактический шок
—
фотосенсибилизация
—
сепсис
—
сонливость
—
раздражение слизистой оболочки глаз, избыточное слезотечение,
конъюнктивит, дакриостеноз (стеноз носо — слезного протока),
светобоязнь, катаракта, нарушение зрения, диплопия, блефарит,
эктропион (выворот века) неврит зрительного нерва, корковая слепота
(при высоких дозах)
—
боли в области сердца, аритмии, ишемия, инфаркт миокарда,
стенокардия, мозговая ишемия, тромбоэмболия, сердечная
недостаточность, внезапная сердечная смерть
—
васкулит, синдром Рейно
—
носовое кровотечение, пневмопатия (кашель, одышка) артериальная
гипотензия, тромбофлебит
—
язвы желудочно-кишечного тракта и желудочно-кишечные кровотечения
—
нарушения сперматогенеза (азооспермия) и овуляции, аменорея
—
некроз носовых костей
—
нарушения функции печени
—
почечная недостаточность, гиперурикемия
—
слабость (обычно возникает сразу после введения и сохраняется в
течение 12- 36 часов)
—
иммуносупрессия, развитие вторичных инфекций
—
дерматит, сухость и трещины кожи, эрозии, эритема, сыпь, зуд,
телеангиэктазия, изменение ногтей (в т.ч. разрушение), синдром
ладонно-подошвенной эритродизестезии (ощущение покалывания в кистях и
стопах с последующим появлением боли, гиперемии и опухания),
гиперпигментация кожи, экзантема
—
повышенная утомляемость
Очень
редко
—
увеличение протромбинового времени
—
лейкоэнцефалопатия, инфаркт головного мозга
—
кардиогенный шок
Противопоказания
—
повышенная чувствительность к 5-фторурацилу
—
угнетение костного мозга, в особенности после лучевой терапии или
лечения
другими противоопухолевыми лекарственными средствами
—
глубокие изменения в содержании клеток крови (число
лейкоцитов менее 5 тыс./мкл, тромбоцитов менее 100 тыс./мкл),
инфильтрация костного мозга опухолевыми клетками
—
кровоизлияния
—
стоматиты, язвы в ротовой полости и язвы желудочно-кишечного тракта
—
тяжелая диарея
—
тяжелые нарушения функции печени или почек
—
острые инфекционные заболевания вирусной, грибковой или
бактериальной природы (в том числе туберкулез, ветряная оспа,
опоясывающий лишай)
—
выраженное истощение
—
повышение содержания билирубина в плазме выше 85 мкмоль/л
—
беременность, период лактации
Лекарственные взаимодействия
Кальция
фолинат усиливает терапевтический и токсический эффекты фторурацила.
При
применении в комбинации с другими цитостатиками и альфа-интерфероном
также может наблюдаться усиление, как противоопухолевого эффекта, так
и токсичности фторурацила.
При
длительном совместном применении с митомицином наблюдалось появление
гемолитического уремического синдрома.
Фторурацил
не следует применять после и совместно с терапией аминофеназоном,
фенилбутазоном и сульфаниламидами.
Хлордиазепоксид,
дисульфирам, гризеофульвин и изониазид могут усиливать активность
5-фторурацила.
В
связи с тем, что при лечении фторурацилом возможно подавление
естественных защитных механизмов, вакцинацию живыми или
инактивированными вакцинами рекомендуется проводить спустя некоторое
время после окончания лечения фторурацилом, интервал варьирует от 3
мес. до 1 года.
При
одновременном приеме с соривудином отмечалось выраженная лейкопения,
в некоторых случаях, приводящая к летальному исходу.
Особые указания
5-
Фторурацил «Эбеве»
является цитотоксическим препаратом, поэтому в обращении с ним
необходимо соблюдать осторожность.
При
появлении стоматита или диареи лечение препаратом необходимо
прекратить до исчезновения этих симптомов.
Следует
соблюдать осторожность при назначении больным, ранее подвергавшимся
воздействию высоких доз радиации на область малого таза или
получавших алкилирующие препараты.
В
период лечения необходимо контролировать общее число лейкоцитов,
абсолютное число нейтрофилов, тромбоцитов, гемоглобин, активность
«печеночных» проб и уровень билирубина, осматривать
полость рта больного для выявления признаков стоматита (перед каждым
введением препарата).
При
развитии синдрома ладонно- подошвенной эритродизестезии возможно
назначение внутрь пиридоксина в дозе 100- 150 мг/сут. Больных с
развивающейся лейкопенией следует тщательно наблюдать для выявления
признаков инфекции.
Мужчинам
и женщинам детородного возраста во время лечения фторурацилом и как
минимум в течение 3 месяцев после следует применять надежные методы
контрацепции.
Особенности
влияния лекарственного средства на способность управлять
автотранспортом и потенциально опасными механизмами.
Побочные
эффекты, обусловленные приемом фторурацила, могут отрицательно
повлиять на управление автотранспортным средством.
Передозировка
Симптомы:
Острые:
психотические реакции, сонливость, повышение эффективности
назначаемых седативных препаратов, повышение токсичности алкоголя.
При
необходимости седации могут быть назначены низкие дозы диазепама
внутривенно (например, начальная доза может составлять 5 мг);
одновременно следует контролировать функцию сердечно-сосудистой
системы и легких.
Хронические:
угнетение костного мозга до уровня агранулоцитоза и критической
тромбоцитопении, склонность к кровоизлияниям, язвенные поражения
желудочно-кишечного тракта, диарея, алопеция.
Лечение:
специфический
антидот неизвестен. В профилактических целях могут/должны быть
назначены инфузии концентратов лейкоцитов или тромбоцитов. Следует
уделить внимание достаточной гидратации и диурезу; необходимо
устранять нарушение баланса электролитов. Как правило, гемодиализ не
требуется. Необходимо пристальное наблюдение за пациентом с целью как
можно более раннего выявления поздних осложнений со стороны системы
кроветворения и желудочно-кишечной системы. Дальнейшее лечение должно
быть симптоматическим.
Форма выпуска и упаковка
По
5 мл препарата помещают в ампулы бесцветного стекла или по 5 или 10
мл препарата помещают во флаконы коричневого стекла, укупоренные
резиновыми пробками, обкатанные алюминиевыми колпачками и
закрытые защитной тефлоновой крышкой.
По
5 ампул или по 1 флакону вместе с инструкцией по медицинскому
применению на государственном и русском языках помещают в пачку из
картона.
Условия хранения
Хранить
в оригинальной упаковке при температуре не выше 25°С.
Не
замораживать!
Примечание:
В случае образования осадка под воздействием низких температур
раствор перед использованием следует нагреть до 60°С, энергично
встряхивая, и затем охладить до комнатной температуры.
Хранить
в недоступном для детей месте!
Срок хранения
2
года
Не
применять лекарственное средство по истечении срока годности,
указанного на упаковке.
Условия отпуска из аптек
По
рецепту
Производитель
EBEWE
Pharma
Ges.m.b.H.
Nfg.KG
А
-4866 Унтерах, Австрия, Европа
Наименование
и страна владельца регистрационного удостоверения
EBEWE
Pharma
Ges.m.b.H.
Nfg.KG,
Австрия
Адрес
организации, принимающий на территории Республики Казахстан претензии
от потребителей по качеству продукции (товара)
Филиал
Новартис Фарма Сервисез АГ, в Республике Казахстан
Алматы
, ул. Жамакаева, 155 А,
Тел.:
(727) 258-12-91
Факс:
(727) 250- 64- 63
e-mal:
http://leknet.lek.si
| 023724871477977101_ru.doc | 78.5 кб |
| 181709511477978261_kz.doc | 96 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники
Прозрачный раствор, бесцветный или желтоватого цвета, свободный от посторонних частиц.
1 мл концентрата для приготовления раствора для инфузий содержит:
активное вещество: фторурацил 50 мг;
вспомогательные вещества: натрия гидроксид, вода для инъекций.
Противоопухолевые средства, антиметаболиты, аналоги пиримидинов.
Код ATX: L01BC02.
Фармакодинамика
Фторурацил является антиметаболитом и, будучи антагонистом пиримидина, ингибирует деление клеток, препятствуя синтезу ДНК. В исходном виде фторурацил не обладает противоопухолевой активностью; свою активность он приобретает в организме после ферментативного превращения в фосфорилированные формы: 5-фторуридин и 5-фтордезоксиуридин.
Фармакокинетика
После внутривенного введения фторурацил распределяется по всему организму и обнаруживается преимущественно в костном мозге, слизистой оболочке кишечника и опухолевой ткани. Проходит через гематоэнцефалический барьер.
Фторурацил катаболизируется ферментом дигидропиримидиндегидрогеназой (ДПД). Активность ДПД является фактором, ограничивающим скорость катаболической реакции. Дефицит ДПД может привести к повышенной токсичности фторурацила.
Объем распределения – 0,12 л/кг массы тела (после внутривенного введения дозы 15 мг/кг массы тела). Фторурацил претерпевает метаболические превращения в печени, сходные с метаболизмом урацила. Под действием ферментов фторурацил быстро превращается в активный метаболит – дигидро-5-фторурацил, период полувыведения которого значительно превышает таковой фторурацила. Кроме того, образуются нетоксичные продукты расщепления – двуокись углерода и мочевина. Период полувыведения фторурацила в альфа-фазе составляет 8-22 минуты, а в бета-фазе зависит от дозы и достигает примерно 20 часов. Выведение происходит главным образом через легкие в виде двуокиси углерода. В меньшей степени фторурацил выводится почками в неизмененном виде. Почечный клиренс составляет около 170-180 мл/мин. У лиц со сниженной функцией почек вещество выводится медленнее.
Максимальная концентрация в спинномозговой жидкости достигается примерно через 1,5-2 часа и составляет около 50 % концентрации в плазме.
Кинетика в особых клинических ситуациях: несмотря на то, что почками выводится небольшая часть препарата (около 15%), по причине поражения костного мозга при азотемии (вследствие почечной недостаточности) и потенциального воздействия на тромбоциты показана надлежащая коррекция дозы в зависимости от степени почечной недостаточности и реакции конкретного пациента. Следует также предусмотреть коррекцию дозы при печеночной недостаточности.
Адъювантная или паллиативная терапия:
— распространенного колоректального рака;
— распространенного рака желудка;
— распространенного рака поджелудочной железы;
— распространенного и (или) метастатического рака молочной железы;
— распространенных злокачественных опухолей головы и шеи;
— распространенного рака шейки матки.
Данный препарат применяется у взрослых.
— Гиперчувствительность к фторурацилу или любому из вспомогательных веществ препарата;
— миелосупрессия;
— серьезные отклонения от нормы показателей крови;
— кровотечение;
— тяжелая почечная и (или) печеночная дисфункция;
— острые, тяжелые инфекции (такие как опоясывающий лишай, ветряная оспа);
— стоматит;
— изъязвления полости рта и желудочно-кишечного тракта;
— псевдомембранозный энтероколит;
— общее тяжелое состояние;
— беременность, лактация;
— известное полное отсутствие активности дигидропиримидиндегидрогеназы (ДПД). Фторурацил нельзя применять в сочетании с бривудином, соривудином и их аналогами, поскольку они являются мощными ингибиторами ДПД, расщепляющей фторурацил.
У пациентов с недостаточностью ДПД обычные дозы фторурацила провоцируют усиление выраженности нежелательных реакций. В случае развития серьезных нежелательных реакций может быть показан мониторинг активности ДПД. У пациентов с недостаточностью ДПД фторурацил применять нельзя.
На фоне лечения фторурацилом нельзя прививать живыми вакцинами. Следует избегать любого контакта с полиомиелитными вакцинами.
Лечение следует проводить только под контролем врача, имеющего опыт проведения химиотерапии. На начальном этапе следует рассмотреть вопрос о госпитализации пациента. 5-Фторурацил Эбеве применяют в моно- или комбинированной терапии. Поскольку режим дозирования и способ применения могут значительно отличаться, следующие рекомендации носят исключительно ознакомительный характер. При выборе точной дозы необходимо руководствоваться протоколами лечения, доказавшими свою эффективность в лечении конкретной болезни.
Начальная терапия при ежедневном применении
Внутривенная инфузия: суточную дозу 15 мг/кг массы тела (600 мг/м2) вводят в течение 4 ч – до появления нежелательных реакций.
Внутривенная инъекция: дозу 12 мг/кг массы тела (480 мг/м2) вводят путем медленной внутривенной инъекции (2-3 мин) ежедневно в течение 3 дней; при отсутствии признаков токсичности возможно введение 6 мг/кг массы тела (240 мг/м2) на 5, 7 и 9-й дни.
Начальная терапия при еженедельном применении: 15 мг/кг (600 мг/м2) вводят медленно внутривенно один раз в неделю.
Поддерживающая терапия: вводят 5-10 мг/кг (200-400 мг/м2) внутривенно один раз в неделю после достижения ремиссии или устранения нежелательных реакций и повторного повышения лейкоцитов от 3 000 до 4 000/мкл, а тромбоцитов – от 80 000 до 100 000/мкл.
Максимальная суточная доза не должна превышать 1,0 г.
Приведенные дозы рассчитаны для нормальной массы тела пациента. При наличии ожирения, отека или асцита доза должна быть соответствующим образом скорректирована.
Длительность лечения зависит от типа и течения заболевания; она определяется опытным специалистом или рассчитывается в соответствии с протоколом лечения.
При комбинированном применении фторурацила с другими цитостатиками, имеющими подобный профиль нежелательных реакций, или с лучевой терапией дозу следует соответственно уменьшить. Фторурацил может также вводиться путем 24-часовой непрерывной капельной инфузии.
Специальные рекомендации по дозированию
Рекомендуется снизить дозу на 1/3 или 1/2 при наличии любого из перечисленных состояний: кахексия, обширная операция, миелосупрессия (лейкоциты < 4 000/мкл, тромбоциты < 100 000/мкл), тяжелое нарушение функции печени или почек.
Пациенты с нарушением функции почек и печени. Применять с осторожностью и при необходимости уменьшить дозу.
Пожилые пациенты (старше 65 лет). Коррекция дозы не требуется, однако рекомендован тщательный контроль состояния таких пациентов.
Способ применения
Для внутривенного введения.
Препарат используется только для внутривенного введения путем инъекции или инфузии после разбавления физиологическим раствором хлорида натрия или 5%-ным раствором глюкозы.
Следует избегать внесосудистого попадания препарата.
Наиболее частыми и серьезными нежелательными реакциями являются токсическое действие на костный мозг и желудочно-кишечные нарушения.
Частота развития нежелательных реакций классифицирована следующим образом: очень часто (≥ 1/10), часто (от ≥ 1/100 до < 1/10), нечасто (от ≥ 1/1000 до < 1/100), редко (от ≥ 1/10 000 до < 1/1000), очень редко (< 1/10 000), частота неизвестна (невозможно оценить на основе имеющихся данных).
Нарушения со стороны крови и лимфатической системы
Очень часто: миелосупрессия (лейкопения, нейтропения, тромбоцитопения), анемия, носовое кровотечение.
Часто: фебрильная нейтропения.
Очень редко: агранулоцитоз, панцитопения.
Инфекционные и паразитарные заболевания
Очень часто: инфекции.
Нарушения со стороны иммунной системы
Очень часто: иммуносупрессия с повышением риска развития инфекции.
Редко: генерализованные аллергические реакции, анафилаксия, анафилактический шок.
Нарушения со стороны эндокринной системы
Частота неизвестна: увеличение содержания общего тироксина (Т4) и общего трийодтиронина (Т3) в сыворотке без увеличения свободного Т4 и ТТГ и без клинических признаков гипертиреоза (клинически – эутиреоз).
Нарушения со стороны метаболизма и питания
Очень часто: гиперурикемия.
Психические нарушения
Редко: спутанность сознания.
Нарушения со стороны нервной системы
Нечасто: нистагм, головная боль, головокружение, симптомы паркинсонизма, пирамидные симптомы, эйфория, сонливость.
Редко: периферическая нейропатия (при комбинации с лучевой терапией).
Очень редко: дисгевзия, (лейко-)энцефалопатия с такими симптомами, как атаксия, острый мозжечковый синдром, нарушение речи, дизартрия, спутанность сознания, нарушение ориентации, миастения, афазия, судороги или кома.
Частота неизвестна: гипераммониемическая энцефалопатия.
Нарушения со стороны органа зрения
Нечасто: чрезмерное слезотечение и стеноз слезного протока, нечеткость зрения, нарушения глазной моторики, воспаление зрительного нерва, диплопия, снижение остроты зрения, светобоязнь, конъюнктивит, блефарит, эктропион в результате образования рубцовой ткани, фиброз слезных желез.
Нарушения со стороны сердца
Очень часто: изменения ЭКГ, характерные для ишемии.
Часто: боль в грудной клетке по типу стенокардии.
Нечасто: аритмия, инфаркт миокарда, ишемия миокарда, миокардит, сердечная недостаточность, дилатационная кардиомиопатия и кардиогенный шок.
Очень редко: остановка сердца и внезапная смерть.
Частота неизвестна: перикардит.
Нарушения со стороны сосудов
Нечасто: артериальная гипотензия.
Редко: тромбофлебит.
Частота неизвестна: церебральная, кишечная и периферическая ишемия, синдром Рейно, тромбоэмболия.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения
Очень часто: бронхоспазм.
Нарушения со стороны желудочно-кишечного тракта
Очень часто: желудочно-кишечные заболевания (потенциально угрожающие жизни), такие как воспаление слизистой оболочки (стоматит, фарингит, эзофагит, проктит), анорексия, (водянистая) диарея, тошнота и рвота.
Нечасто: обезвоживание, сепсис, а также изъязвления и кровотечения в желудочно- кишечном тракте, отторжение некротических масс.
Нарушения со стороны печени и желчевыводящих путей
Нечасто: повреждение клеток печени, некалькулезный холецистит.
Очень редко: некроз печени (иногда со смертельным исходом).
Нарушения со стороны кожи и подкожных тканей
Очень часто: выпадение волос, замедленное заживание ран, синдром ладонно-подошвенной эритродизестезии (так называемый синдром «кисть-стопа») с дизестезией, покраснением, отечностью, болью и шелушением кожи на ладонях и стопах.
Нечасто: дерматит, изменения кожи (сухость кожи, эрозии/трещины, эритема, зудящая макулопапулезная сыпь), экзантема, крапивница, светочувствительность, гиперпигментация кожи и поперечно-полосатая гиперпигментация или депигментация в участках прохождения вен, изменения ногтей (например, диффузная поверхностная синяя пигментация, гиперпигментация, ониходистрофия, боль и утолщение ногтевого ложа, паронихия) и онихолизис.
Нарушения со стороны репродуктивной системы и молочных желез
Нечасто: нарушения сперматогенеза и овуляции.
Общие расстройства и нарушения в месте введения
Очень часто: истощение, общая астения, повышенная утомляемость и снижение мотивации, лихорадка.
Описание отдельных нежелательных реакций
Нарушения со стороны крови и лимфатической системы
Миелосупрессия является дозоограничивающей нежелательной реакцией.
Степень тяжести миелосупрессии (от I до IV по Оценочной шкале общих критериев токсичности, разработанной Национальным онкологическим институтом США) зависит от способа введения (в/в струйная инъекция или в/в непрерывная инфузия) и режима дозирования. Нейтропения возникает после каждого курса лечения с введением внутривенной струйной инъекции в обычной дозе (максимальное снижение содержания нейтрофилов: с 9-го по 14-20-й день лечения; нормализация, как правило, начинается после 30-го дня).
Нарушения со стороны сердца
Кардиотоксические эффекты развиваются главным образом во время первого курса лечения или через несколько часов после него. У пациентов с уже имеющейся ишемической болезнью сердца или кардиомиопатией риск развития кардиотоксичности повышен.
Нарушения со стороны желудочно-кишечного тракта
Степень (I-IV по Оценочной шкале общих критериев токсичности Национального онкологического института США) желудочно-кишечных нежелательных реакций зависит от режима дозирования и способа введения. При введении путем непрерывной внутривенной инфузии дозоограничивающим эффектом с большей вероятностью будет стоматит, чем миелосупрессия.
Нарушения со стороны кожи и подкожных тканей
Так называемый синдром «кисть-стопа» начинается с расстройств чувствительности на ладонях и подошвах с присоединением покраснения, отека, боли и шелушения кожи. Данный синдром после непрерывной внутривенной инфузии развивается очень часто, а после внутривенной струйной инъекции – часто.
Симптомы передозировки
Признаки и симптомы передозировки: тошнота, рвота, диарея, тяжелый мукозит, изъязвления и кровоизлияния в желудочно-кишечном тракте, миелосупрессия (тромбоцитопения, лейкопения, агранулоцитоз).
Острая интоксикация включает психотические реакции, сонливость, усиление действия седативных лекарственных средств, усиление токсичности алкоголя. При необходимости приема седативного препарата можно назначать диазепам в малых дозах (например, начиная с 5 мг) в/в под контролем систем кровообращения и дыхания. Для хронической интоксикации характерны миелосупрессия вплоть до агранулоцитоза и критической тромбоцитопении, склонность к кровотечениям, язвы в желудочно-кишечном тракте, диарея, выпадение волос.
Лечение интоксикации
При развитии симптомов интоксикации введение фторурацила немедленно прекращают и начинают симптоматическую терапию.
Проводятся инфузии лейкоконцентрата или тромбоконцентрата, профилактика инфекций. Для восстановления объема циркулирующей крови и минерального баланса может быть полезным форсированный диурез. В большинстве случаев в гемодиализе необходимости нет. Требуется тщательный контроль для своевременного выявления поздних гематологических и желудочно-кишечных осложнений.
Выраженная миелосупрессия подлежит лечению в стационаре, которое включает (при необходимости) восполнение недостающих компонентов крови и антибактериальную терапию. Может потребоваться перевод пациента в асептическую палату.
Функцию кроветворения следует контролировать в течение не менее 4 недель после передозировки. Если несмотря на возникновение нежелательных реакций со стороны сердца терапию фторурацилом необходимо продолжать, для предотвращения развития спазма коронарных артерий показано назначение вазодилататоров.
Возможны тошнота и рвота, нежелательные реакции со стороны нервной системы и нарушения зрения. По этой причине во время лечения фторурацилом рекомендуется воздерживаться от управления транспортными средствами и работы с механизмами.
Приведенные ниже данные также относятся к недавно применявшимся лекарственным средствам.
Все лечебные мероприятия, отрицательно влияющие на физическое состояние пациента или на функции костного мозга (например, применение других цитостатиков), могут усиливать токсичность фторурацила.
Фторурацил может усиливать кожную токсичность лучевой терапии.
Фермент ДПД играет важную роль в расщеплении фторурацила. Аналоги нуклеозидов, такие как бривудин и соривудин, могут приводить к резкому увеличению концентрации фторурацила или других фторпиримидинов в плазме и вследствие этого увеличивать его токсичность. Поэтому промежуток между применением фторурацила и бривудина, соривудина и их аналогов должен составлять не менее 4 недель. При необходимости показано определение активности фермента ДПД до начала терапии фторурацилом.
При случайном введении бривудина пациентам, получающим фторурацил, должны быть приняты эффективные меры для снижения токсичности фторурацила, предотвращения системных инфекций и дегидратации. Рекомендуется немедленная госпитализация.
Кальция фолинат может усиливать действие фторурацила. Вследствие данного взаимодействия может развиваться тяжелая, а в ряде случаев и смертельная диарея, особенно при внутривенном струйном введении фторурацила в дозе 600 мг/м2 площади поверхности тела один раз в неделю в сочетании с кальция фолинатом.
В случае сопутствующего применения фенитоина и фторурацила возможно повышение уровня фенитоина в плазме, что приводит к симптомам интоксикации фенитоином. Необходимо регулярное определение уровня фенитоина в плазме.
Циметидин, метронидазол, аллопуринол и интерфероны могут повышать уровень фторурацила в плазме и его токсичность.
У женщин, получающих тиазидные диуретики в сочетании с циклофосфамидом, метотрексатом или фторурацилом, возможно более выраженное снижение количества гранулоцитов, чем при проведении подобных циклов применения цитостатика без тиазидов.
Сопутствующее применение фторурацила и варфарина может привести к удлинению протромбинового времени; данный параметр следует тщательно контролировать. В единичных случаях у пациентов, получавших варфарин в сочетании с фторулацилом (отдельно или в комбинации с левамизолом), наблюдалось снижение протромбинового индекса.
Во время сопутствующего лечения фторурацилом и левамизолом часто наблюдаются гепатотоксические эффекты (повышение уровней щелочной фосфатазы, трансаминаз или билирубина).
У пациентов с карциномой молочной железы, получающих комбинированную терапию циклофосфамидом, метотрексатом, фторурацилом и тамоксифеном, повышается риск возникновения тромбоэмболических осложнений.
В случае сопутствующего применения винорельбина и фторурацила/фолиниевой кислоты может развиться тяжелый мукозит с летальным исходом.
Методы количественного определения билирубина и 5-гидроксииндолуксусной кислоты могут давать повышенные или ложноположительные результаты.
Фторурацил не следует применять после и совместно с аминофеназоном, фенилбутазоном и сульфонамидом.
Хлордиазепоксид, дисульфирам, гризеофульвин и изониазид могут усиливать активность фторурацила.
При длительном применении фторурацила в комбинации с митомицином наблюдалось развитие гемолитико-уремического синдрома.
При применении фторурацила в комбинации с другими препаратами для проведения химиотерапии (митомицином С или цисплатином) очень редко сообщали о случаях ишемического инсульта.
Общие замечания
Цитостатики могут снижать формирование антител после противогриппозной вакцинации.
Применение цитостатиков сопряжено с повышенным риском развития тяжелой инфекции после введения живой вакцины.
Несовместимость
Концентрат для приготовления раствора для инфузий может быть разбавлен только физиологическим раствором хлорида натрия или 5%-ным раствором глюкозы. Не допускается смешивать фторурацил с другими веществами в растворе для инфузии. Нельзя разбавлять сильно забуференными растворами с pH < 8, поскольку фторурацил в такой среде выпадает в осадок. Не смешивать с другими химиотерапевтическими растворами.
Сообщалось о несовместимости фторурацила со следующими препаратами: фолиниевая кислота, карбоплатин, цисплатин, цитарабин, диазепам, доксорубицин, дроперидол, филграстим, нитрат галлия, лейковорин, метотрексат, метоклопрамид, морфин, ондансетрон, растворы для парентерального введения питательных веществ, винорельбин, другие антрациклины.
Кальция фолинат
Фторурацил нельзя смешивать в одной инфузии с кальция фолинатом, поскольку может образоваться осадок. Показано, что фторурацил 50 мг/мл и кальция фолинат 20 мг/мл в 5%-ном водном растворе декстрозы или без него несовместимы при смешивании в различных пропорциях и хранении при температуре 4 °C, 23 °C или 32 °C в контейнерах из поливинилхлорида.
Препарат нельзя смешивать с другими лекарственными средствами, включая оксалиплатин и иринотекан.
Беременность. Фторурацил может быть мутагенным и тератогенным, в связи с чем его нельзя использовать во время беременности. Женщинам детородного возраста следует применять надежные методы контрацепции во время лечения и в течение 6 месяцев после его окончания. Если во время лечения наступает беременность, необходимо проведение генетической консультации.
Кормление грудью. Поскольку неизвестно, проникает ли фторурацил в грудное молоко, препарат нельзя использовать в период кормления грудью. Если введение препарата является совершенно необходимым, грудное вскармливание должно быть прекращено.
Фертильность. Фторурацил может проявлять генотоксичность. Мужчинам во время лечения фторурацилом и как минимум в течение 6 месяцев после его окончания следует применять надежные методы контрацепции. В связи с возможными серьезными расстройствами сперматогенеза вследствие терапии фторурацилом рекомендуется до начала лечения проконсультироваться по вопросу консервации спермы.
Терапия фторпиримидинами сопровождается кардиотоксичностью, включая инфаркт миокарда, стенокардию, аритмии, миокардит, кардиогенный шок, внезапную смерть и электрокардиографические изменения (включая очень редкие случаи удлинения интервала QT). Эти нежелательные реакции чаще встречаются у пациентов, получающих непрерывную инфузию фторурацила, а не болюсную инъекцию. Наличие ишемической болезни сердца в анамнезе может послужить фактором риска развития нежелательных реакций со стороны сердца. Поэтому следует проявлять осторожность при лечении пациентов, которые испытывали боль в грудной клетке во время курсов лечения, или пациентов с заболеваниями сердца в анамнезе. Во время лечения фторурацилом регулярно контролируют функцию сердца. В случае тяжелой кардиотоксичности лечение прекращают.
Постмаркетинговые источники сообщали о случаях энцефалопатий (включая гипераммониемическую энцефалопатию, лейкоэнцефалопатию), связанных с лечением фторурацилом. Признаками или симптомами энцефалопатии являются нарушенный психический статус, спутанность сознания, дезориентация, кома или атаксия. Если развивается какой-либо из этих симптомов, лечение прекращают и немедленно проверяют уровень аммиака в сыворотке. В случае повышенного уровня аммиака в сыворотке крови начинают терапию, снижающую его уровень.
Следует соблюдать осторожность при назначении фторурацила пациентам с почечной и (или) печеночной недостаточностью. У пациентов с нарушениями функции почек и (или) печени может отмечаться повышенный риск развития гипераммониемии и гипераммониемической энцефалопатии.
Пациенты с отсутствующей или низкой активностью ДПД (также после применения ингибиторов ДПД) подвергаются повышенному риску развития тяжелых, угрожающих жизни или смертельных нежелательных реакций, вызванных фторурацилом.
Хотя дефицит ДПД точно определить невозможно, известно, что пациенты с определенными гомозиготными или определенными сочетанными гетерозиготными мутациями в локусе гена DPYD (например, варианты DPYD*2A, с.1679T>G, с.2846А>Т и c.l236G>A/HapB3), которые могут вызывать полное или почти полное отсутствие активности фермента ДПД (определенное лабораторно), имеют самый высокий риск опасной для жизни или смертельной токсичности и не должны получать терапию фторурацилом. При полном отсутствии у пациентов активности ДПД ни одна доза препарата не может считаться безопасной.
Для выявления пациентов с повышенным риском развития тяжелой токсичности рекомендуется генотипирование этих аллелей. Не исключено, что другие редкие варианты также могут быть связаны с повышенным риском развития тяжелой токсичности.
Лечение пациентов с частичным дефицитом ДПД (например, с гетерозиготными мутациями в гене DPYD) и при преимуществах фторурацила, перевешивающих риски (принимая во внимание целесообразность другого химиотерапевтического режима без фторпиримидина), должно проводиться с особой осторожностью и частым контролем с коррекцией дозы в соответствии с токсичностью. Во избежание развития серьезной токсичности у этих пациентов можно предусмотреть снижение начальной дозы. Для рекомендации конкретной дозы у пациентов с частичной активностью ДПД, измеренной с помощью специального теста, данных недостаточно.
Сообщалось, что варианты DPYD*2A, с.1679T>G приводят к большему снижению активности фермента, чем другие варианты, ассоциированные с более высоким риском нежелательных реакций. Влияние снижения дозы на эффективность в настоящее время не определено. Следовательно, при отсутствии серьезной токсичности доза может быть увеличена при тщательном наблюдении за пациентом. Пациенты с отрицательным тестом на вышеупомянутые аллели все еще могут иметь риск развития серьезных нежелательных реакций.
У пациентов с не выявленным дефицитом ДПД, получающих фторурацил, а также у пациентов с отрицательным тестом на специфические варианты DPYD, может возникнуть опасная для жизни токсичность, проявляющаяся в виде острой передозировки. В случае острой токсичности 2-4-й степени лечение должно быть немедленно прекращено. Полную отмену препарата следует рассматривать на основе клинической оценки возникновения, продолжительности и тяжести наблюдаемой токсичности.
О применении соривудина, бривудина или их аналогов, а также о сопутствующем применении фенитоина см. раздел «Взаимодействие с другими лекарственными средствами и другие виды взаимодействия».
Из-за возможного развития анафилактической реакции соблюдают осторожность и прибегают к профилактическим мерам перед введением фторурацила.
При повреждении стенок кишечника требуется симптоматическое лечение в зависимости от степени тяжести, например, восполнение жидкости в организме. Легкую диарею купируют противодиарейными средствами, однако при умеренной или тяжелой диарее потребуется применение других лекарственных препаратов.
До и во время терапии фторурацилом рекомендуются следующие обследования и анализы:
— ежедневный осмотр полости рта и глотки на предмет выявления повреждений слизистых;
— развернутый анализ крови с лейкоцитарной формулой и определением количества тромбоцитов перед каждым введением фторурацила и каждые 2-3 дня в начале лечения;
— регулярное определение лабораторных показателей функции почек; регулярное определение показателей печеночных проб;
— определение мочевой кислоты;
— анализ кала на наличие скрытой крови.
Пациентов следует предупреждать о возможном развитии стоматита/мукозита, диареи и кровотечения (в частности, из желудочно-кишечного тракта). При появлении первых признаков они должны проконсультироваться с врачом.
Лечение немедленно прекращают при наличии следующих симптомов: реакции со стороны желудочно-кишечного тракта (стоматит, мукозит, тяжелая диарея, тяжелая рвота, язвы, кровотечение), лейкоциты < 3000/мкл, тромбоциты < 80 000/мкл, нежелательные реакции со стороны центральной нервной системы (в том числе атаксия и тремор) и любые нежелательные реакции со стороны сердца. Лечение может быть возобновлено после исчезновения нежелательных реакций и при общем удовлетворительном состоянии пациента. При тяжелых токсических проявлениях со стороны желудочно-кишечного тракта, сердца или нервной системы лечения возобновлять не рекомендуется.
При сопутствующем применении фторурацила с пероральными антикоагулянтами необходим тщательный контроль протромбинового индекса.
Следует соблюдать осторожность при назначении пациентам из группы риска, подвергавшимся воздействию высоких доз облучения на область малого таза, получавшим алкилирующие препараты, с обширными метастазами в костях и печени (сниженное выведение!) и (или) кахектичным пациентам.
В комбинации с метотрексатом для достижения оптимального эффекта метотрексат применяют не позднее чем за 24 часа до фторурацила (не наоборот!).
Фторурацил может проявлять мутагенность. Рекомендации для мужчин и женщин приведены в разделе «Фертильность, беременность и кормление грудью». При планировании беременности после лечения рекомендуется генетическое консультирование.
Дети и подростки
Данных о безопасности и эффективности лечения данной категории пациентов недостаточно.
Данный препарат содержит натрий в количестве не более 9,31 мг на мл; а в максимальной суточной дозе – в количестве 186,20 мг, что соответствует 9,31 % максимального рекомендуемого Всемирной организацией здравоохранения суточного потребления натрия взрослым человеком, равного 2 г.
Флаконы из коричневого стекла (класса I), укупоренные резиновыми пробками под алюминиевой обкаткой, закрытые защитными крышками.
Размер упаковки: по 1 флакону по 250 мг/5 мл, 500 мг/10 мл, 1000 мг/20 мл или 5000 мг/100 мл в упаковке.
Хранить в защищенном от света месте при температуре не выше 25 °C.
Хранить в недоступном для детей месте.
Не хранить в холодильнике и не замораживать!
Примечание: в случае образования осадка под воздействием низких температур раствор перед использованием следует нагреть до 60 °C при энергичном встряхивании, а затем охладить до температуры тела. Применять только прозрачный раствор без осадка.
Особые меры предосторожности при обращении и утилизации
При работе с фторурацилом следует соблюдать общие руководящие принципы для цитостатиков. Должны быть приняты все меры для обеспечения работы в полностью асептических условиях. Работать следует в защитных перчатках, маске для лица и защитной одежде и по возможности в комнате с ламинарным потоком воздуха, специально предназначенной для этой цели. Необходимо избегать контакта препарата с кожей и слизистыми оболочками. Если такой контакт все же произошел, кожу (слизистые) необходимо тщательно промыть водой с мылом. В случае попадания в глаза их необходимо промыть большим количеством воды и немедленно обратиться к врачу. Беременным сотрудницам работать с фторурацилом запрещено.
Неиспользованный препарат или отходы должны утилизироваться в соответствии с местными требованиями.
Только для однократного применения.
2 года. Не применять по истечении срока годности, указанного на упаковке.
Отпускается только по рецепту врача.
Производитель
Эбеве Фарма Гес.м.б.Х. Нфг. КГ, Мондзеештрассе 11, А-4866 Унтерах, Австрия.