Болезнь Гиршпрунга у детей
Версия: Клинические рекомендации РФ 2018-2020 (Россия)
Категории МКБ:
Болезнь Гиршпрунга (Q43.1)
Разделы медицины:
Врожденные заболевания, Педиатрия, Хирургия детская
Общая информация
Краткое описание
Общероссийская общественная организация «Российская Ассоциация детских хирургов»
Клинические рекомендации
БОЛЕЗНЬ ГИРШПРУНГА У ДЕТЕЙ
Год утверждения (частота пересмотра): 2019 (пересмотр каждые 3 года)
Определение.
Болезнь Гиршпрунга (БГ) — врождённый порок развития энтеральной нервной системы, характеризующийся отсутствием ганглионарных клеток дистальных отделов кишечника, что приводит к нарушению перистальтики аганглионарного сегмента и функциональной кишечной непроходимости. (Holschneider, A. M., & Puri, P. (Eds.). (2007). Hirschsprung’s disease and allied disorders. Springer Science & Business Media, Peña, A., & Bischoff, A. (2015). Surgical treatment of colorectal problems in children. Springer. БГ — один из многочисленных вариантов нейрокристопатий (аномалий развития тканей вследствие нарушения миграции клеток от нервного гребня).
Кодирование по МКБ-10
Q43.1 — болезнь Гиршпрунга
Аганглионоз
Врожденный (аганглиозный) мегаколон
Облачная МИС «МедЭлемент»
Облачная МИС «МедЭлемент»

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
Классификация
Классификация
В современных условиях развития детской хирургии Российской Федерации в целях интеграции в международное медицинское сообщество к практическому применению рекомендована зарубежная классификация БГ:
— болезнь Гиршпрунга с коротким сегментом (типичная форма) (S- HSCR, 1 тип) — аганглиоз распространяется ниже первой петли сигмовидной кишки
— болезнь Гиршпрунга с длинным сегментом (L- HSCR, 2 тип) — аганглиоз распространяется выше первой петли сигмовидной кишки
— болезнь Гиршпрунга, тотальная форма (аганглиоз распространяется на всю толстую кишку, часто с захватом разного по протяженности участка тонкой кишки [8, 9].
— тотальный аганглиоз кишечника — поражение всей толстой и тонкой кишки, при котором пациенты в большинстве случаев нежизнеспособны.
При любой форме БГ в описательной части целесообразно указывать уровень распространения аганглиоза. Существование ультракороткой формы БГ является сомнительным и выделение ее как самостоятельной нозологической единицы в настоящее время нецелесообразно.
В отечественных учебниках по проктологии представлены классификации, сыгравшие важную роль на этапах изучения течения заболевания и освоения хирургических методов его лечения. Предложенные авторами различные формы проявления и стадии течения БГ были связаны, прежде всего, с поздней диагностикой заболевания и другими подходами к срокам и этапности хирургического лечения. Тем не менее, знание этих классификаций необходимо для понимания возможных изменений в состоянии ребенка при поздней диагностике БГ.
В нашей стране исторически использовалась классификация профессора А.И. Ленюшкина (1972) [10].
- Ректальная форма. Аганглиоз на протяжении прямой кишки.
- Ректосигмоидальная (ректосигмоидная) форма. Аганглиоз прямой и части сигмовидной кишок (наиболее часто встречающаяся локализация)
- Субтотальная форма. Включает две разновидности, когда зона поражения распространяется на поперечноободочную кишку или на более проксимальные отделы ободочной кишки.
- Тотальная форма. Аганглиоз захватывает всю толстую кишку.
Течение заболевания возможно отразить в классификации стадийности, предложенной Ю.Ф. Исаковым [11]:
|
Компенсированная стадия |
Субкомпенсированная стадия | Декомпенсированная стадия |
|
При рождении — задержка отхождения мекония, небольшое вздутие живота, иногда — рвота. После клизмы симптомы купируются. Общее состояние удовлетворительное. В дальнейшем – задержка стула, вздутие живота, необходимость регулярного выполнения очистительных клизм. |
Общее состояние ребенка постепенно ухудшается. Запоры становятся упорными; для опорожнения кишечника прибегают к сифонным клизмам. Данная стадия чаще всего является переходной от компенсации к декомпенсации | С рождения признаки полной низкой кишечной непроходимости. Мекониевый стул отсутствует или очень скудный, газы не отходят. Прогрессивно усиливается вздутие живота, становится видимой перистальтика кишок, появляется обильная рвота; ребенок беспокоен. Состояние ребенка быстро ухудшается — явления кишечной интоксикации, обезвоживание. |
Течение заболевания по Г.А. Баирову также подразумевает три варианта [12]:
| Острое течение | Подострое течение | Хроническое течение |
| После рождения развивается непроходимость кишечника: задержка мекония и газов, срыгивание, рвота, вздутие живота. Клизмы малоэффективны, газы не отходят. Состояние ребенка быстро ухудшается | После рождения задержка стула разрешается очистительными клизмами, но к 3-6 месяцам запор становится упорным, газы не отходят, может развиться кишечная непроходимость |
Проявляется обычно после 5-6 месяцев. На фоне выполнения клизм отмечается самостоятельный стул («светлые» промежутки) Слабительные средства не эффективны. В толстой кишки формируются каловые камни. Общее состояние детей страдает мало. |
Этиология и патогенез
Этиология и патогенез.
До 13 недели гестации клетки нервного гребня мигрируют от проксимальных отделов кишечной трубки к дистальным с последующей дифференцировкой в зрелые ганглионарные клетки. У детей с БГ вследствие нарушения этого процесса в дистальных отделах кишечника ганглионарные клетки отсутствуют. Предполагаются две основные причины:
— клетки нервного гребня не мигрируют в дистальные сегменты кишки
-клетки нервного гребня мигрируют в дистальные сегменты кишки, однако по различным причинам погибают или не проходят процесс дифференцировки
(Pediatric Surgery, 7th Edition — edited by Arnold G. Coran, Anthony Caldamone, N. Scott Adzick, Thomas M. Krummel, Jean-Martin Laberge, and Robert Shambergerб 2012, 848 р.).
Аганглионарный участок, в силу отсутствия перистальтики, меньше в диаметре по сравнению с расширенными вышележащими отделами, где со временем развивается рабочая гипертрофия мышечной ткани (Болезнь Гиршпрунга. Руководство для врачей под ред. А.Ю.Разумовского, А.Ф.Дронова, А.Н. Смирнова, В.В. Холостовой. «ГЭОТАР-Медиа». 1028 — 368 с.)
В настоящее время установлено более восьми генов, ответственных за развитие БГ. Наиболее изучены мутации генов RET и EDNRB. У 70 % пациентов с тотальными формами БГ выявлена мутация гена RET [1]. БГ может сопровождать генетические синдромы — Ваанденбурга-Шаха, Мовата-Вилсона, Шпритцена-Голдберга, Хаддада, Смита — Лемли — Опица, Дауна, врожденного гиповентиляционного синдрома [2].
Эпидемиология
Эпидемиология
Частота заболевания в России до настоящего времени не уточнена. По данным Росстата частота впервые выявленных всех врожденных пороков развития (ВПР) у детей до 14 лет в 2015 году составила 277,9 тысяч (1154,8 на 100 тысяч детей) [3]. БГ не входит в перечень 21 нозологии (ВПР) обязательного учета в Российской Федерации, поэтому уточнить истинную частоту заболевания в настоящее время не представляется возможным. Отечественными коллегами представлены цифры по отдельным регионам. В Москве ежегодно оперируют 150 детей с болезнью Гиршпрунга [4]. По данным зарубежной литературы частота порока составляет 1 : 4,417; 1 : 5000 живорожденных, у мальчиков в четыре раза чаще, чем у девочек [5, 6]. По данным Европейской ассоциации регистров врожденных пороков развития (2011-2015 гг.) частота БГ составляет 404 на 10000 живорожденных [7].
Диагностика
Диагностика
Жалобы и анамнез
Основные жалобы при БГ — задержка отхождения стула и газов, вздутие живота. У подавляющего большинства детей с БГ после рождения отмечается задержка отхождения мекония в первые сутки. Описаны случаи перфорации слепой кишки и аппендикса как проявления БГ в периоде новорожденности [8]. Следует обратить внимание при сборе анамнеза на наличие БГ у родителей пациента и сибсов.
Клинические признаки БГ представлены в таблице
|
Острое течение (декомпенсация) |
Подострое течение (субкомпенсация) |
Хроническое течение (компенсация) |
|
·развивается у новорожденных детей ·меконий не отходит в первые 24 часа у доношенных детей ·меконий не отходит в первые 48 часов – 8 суток у недоношенных детей ·резкое вздутие живота, газы не отходят ·рвота с желчью |
·развивается в детей 3-6 месяцев ·в анамнезе — меконий не отходил в первые 24 часа у доношенных детей ·меконий не отходил в первые 48 часов – 8 суток у недоношенных детей ·периодическое вздутие живота, газы отходят плохо ·периодически отходит скудный стул ·необходимо выполнять очистительные клизмы |
·развивается в детей от 6 месяцев ·в анамнезе — меконий не отходил в первые 24 часа у доношенных детей ·меконий не отходил в первые 48 часов – 8 суток у недоношенных детей ·периодическое вздутие живота ·необходимо регулярно выполнения клизм ·отсутствие вторичного недержания кала на фоне длительного запора ·отставание в развитии ·формирование каловых камней выше зоны аганглиоза |
Гиршпрунг-ассоциированный энтероколит (ГАЭК).
Осложнение БГ, является жизнеугрожающим состоянием, может развиться как до, так и после оперативного лечения. ГАЭК до настоящего времени является одной из основных причин летальности при БГ (Prato, A. P., Rossi, V., Avanzini, S., Mattioli, G., Disma, N., & Jasonni, V. (2011). Hirschsprung’s disease: what about mortality?. Pediatric surgery international, 27(5), 473-478)
ГАЭК — обобщающий термин, который включает рецидивирующий неспецифический энтероколит, а также псевдомембранозный (клостридиальный) колит (вариант проявления антибиотик-ассоциированной диареи).
Чаще ГАЭК проявляется:
— тяжелой диареей
— нарушением периферического кровообращения
— летаргией
— дилатацией кишечных петель (Frykman, P. K., Kim, S., Wester, T., Nordenskjöld, A., Kawaguchi, A., Hui, T. T. & HAEC Collaborative Research Group. (2018). Critical evaluation of the Hirschsprung-associated enterocolitis (HAEC) score: A multicenter study of 116 children with Hirschsprung disease. Journal of pediatric surgery, 53(4), 708-717)
Частота дооперационного ГАЭК по данным литературы составляет от 5,7 до 50%, послеоперационного — от 2 до 35% (Austin, K. M. (2012, November). The pathogenesis of Hirschsprung’s disease-associated enterocolitis. In Seminars in pediatric surgery (Vol. 21, No. 4, pp. 319-327). WB Saunders, Sellers, M., Udaondo, C., Moreno, B., Martínez-Alés, G., Díez, J., Martínez, L., & de Ceano-Vivas, M. (2018). Hirschsprung-associated enterocolitis: Observational study in a paediatric emergency care unit. Anales de Pediatría (English Edition).)
Причина возникновения до конца не изучена, состояние зачастую требует интенсивной терапии, перевода ребенка на полное или частичное парентеральное питание, декомпрессии кишечника [4].
Препарат выбора при лечении ГАЭК — метронидазол, при неэффективности — ванкомицин. В качестве профилактики развития ГАЭК после хирургического лечения, в предоперационное обследование должны быть включены анализы кала на Clostridium difficile (токсин А и В). В случае их обнаружения перед операцией необходимо провести курс деконтаминационной терапии метронидазолом (в случае неэффективности – ванкомицином), отдавая предпочтение пероральному приему препаратов.
Физикальное обследование
- Рекомендовано оценить общее состояние пациента
Комментарий: Тяжесть состояния ребенка с БГ обусловлена задержкой стула, метеоризмом. При наличии осложнений БГ состояние ребенка может быть тяжелым, что обусловлено клиническими признаками кишечной непроходимости или энтероколита. БГ всегда проявляется с рождения. Самым ранним симптомом является задержка отхождения мекония более 24 часов после рождения, что сопровождается вздутием живота и срыгиваниями или рвотой с примесью желчи. После получения стула с помощью газоотводной трубки или клизмы может наступить «светлый» промежуток, когда у ребенка самостоятельно отходит стул (чаще жидкий, частый, в небольшом количестве) и газы. Этот период является главной причиной диагностических ошибок – исключения хирургической патологии без проведения обследования. Возможные варианты проявления болезни Гиршпрунга в периоде новорожденности:
— низкая кишечная непроходимость (часто сочетается с энтероколитом)
— энтероколит (вздутие живота, частый, жидкий, но скудный стул, повышение температуры тела)
— диарея (разрешение кишечной непроходимости связано с появлением жидкого стула без гипертермии и симптомов интоксикации)
— запор
У детей грудного и старшего возраста необходимо провести пальцевое ректальное исследование (характерно для БГ — пустая ампула прямой кишки на фоне длительного запора. Гипертонус внутреннего анального сфинктера (ВАС) не является однозначным признаком БГ, так как может сопровождать другую проктологическую патологию)
Лабораторная диагностика
- Рекомендовано проведение общего анализа крови, биохимического анализа крови, общего анализа мочи при наличии осложнений (кишечной непроходимости или энтероколита)
Инструментальная диагностика
- Рекомендовано проведение обзорной вертикальной рентгенографии брюшной полости с захватом грудной клетки у новорожденных с подозрением на БГ
Комментарий. При типичной форме БГ характерно повышенное газонаполнение кишечных петель, нет признаков, характерных для атрезии кишечника, мальротации.
- Рекомендовано проведение ирригоскопии
Уровень убедительности рекомендаций I (уровень достоверности доказательств – А) (Chen, X., Xiaojuan, W., Zhang, H., Jiao, C., Yu, K., Zhu, T., & Feng, J. (2017). Diagnostic value of the preoperatively detected radiological transition zone in Hirschsprung’s disease. Pediatric surgery international, 33(5), 581-586)
Комментарий. В случае клинических проявлений энтероколита проведение исследования возможно только после адекватной декомпрессии кишечника и стабилизации состояния.
Диагноз БГ устанавливается на основании выявления трех признаков: зоны сужения кишки, зоны расширения кишки и переходной в виде воронкообразного расширения, которая расценивается как самый важный признак заболевания. Одним из достоверных рентгенологических признаков является разница в диаметре восходящего отдела ободочной кишки и сигмовидной кишки 1:2. При тотальной форме выявить данные признаки не всегда возможно.
Новорожденным детям исследование проводится с водорастворимым контрастом в разведении 1:3, объемом 20 мл на 1 кг веса. Примерно у 10 % новорожденных переходная зона не визуализируется. При сомнительном результате ирригоскопии необходимо выполнить отсроченные снимки толстой кишки с интервалом в 6, 12, 24 часа.
Детям грудного и старшего возраста исследование проводится с сульфатом бария объемом 20 мл на 1 кг веса и поворотом ребенка под рентгенологическим экраном для визуализации суженой аганглионарной зоны.
Обязательным является:
— нетугое заполнение кишки контрастом
— выполнение четырех рентгенограмм в день исследования: в прямой и боковой проекциях (две — при заполнении кишки и две отсроченных — после опорожнения кишки, полного или частичного (рис.1)
Рисунок 1
Ирригограмма с сульфатом бария (боковая проекция, заполнение) ребенка 8 месяцев с короткой формой БГ
1. зона относительного сужения кишки (аганглиоз)
2. «Переходная» зона
3. Расширенные вышележащие отделы кишки
Ошибки в методике, приводящие к ложноотрицательным результатам:
— тугое заполнении прямой кишки контрастом, что приводит к механическому перерастяжению аганглионарной зоны
-ирригография только в прямой проекции — наложение расширенной части кишки на короткий участок аганглиоза.
Задержка контраста в толстой кишки более, чем на 24 часа на отсроченной рентегнографии брюшной полости свидетельствует в пользу БГ.
Оценка метода исследования [13]:
— чувствительность 70%
— специфичность 83 %
- Рекомендовано проведение аноректальной манометрии
Уровень убедительности рекомендаций I (уровень достоверности доказательств – А) (de Lorijn, F., Kremer, L. C., Reitsma, J. B., & Benninga, M. A. (2006). Diagnostic tests in Hirschsprung disease: a systematic review. Journal of pediatric gastroenterology and nutrition, 42(5), 496-505)
Комментарий. Метод основан на регистрации ректоанального ингибиторного рефлекса (РАИР). РАИР характеризует способность внутреннего анального сфинктера к расслаблению (при раздувании баллона, находящегося в прямой кишке, в норме отмечается снижение анального давления — расслабление внутреннего сфинктера) с последующим постепенным восстановлением. Характерно для БГ — отсутствие нормального РАИР (рис. 2, 3).
Рисунок 2
Аноректальная манометрия
с баллоном (исследование РАИР). Стрелками указан момент раздувания ректального баллона, овалами — реакция внутреннего анального сфинктера (ВАС)
а — нормальный РАИР (расслабление ВАС, снижение базального давления более, чем на 20%) у девочки
6 лет с запором
b — отсутствие РАИР (отсутствие расслабления ВАС, снижения базального давления) у девочки 4,5 лет с БГ
Рисунок 3
Аноректальная манометрия (исследование РАИР).
Закрашенными стрелками указана реакция ВАС на раздувание баллона
а — нормальный РАИР (снижение базального давления и постепенное его восстановление)
b — патологический РАИР (резкое повышение базального давления в ответ на раздувание баллона — характерно для БГ)
Оценка метода исследования [13]:
-чувствительность 91 %
-специфичность 94 %
- Рекомендовано проведение биопсии толстой кишки
Уровень убедительности рекомендаций I (уровень достоверности доказательств – А) (de Lorijn, F., Kremer, L. C., Reitsma, J. B., & Benninga, M. A. (2006). Diagnostic tests in Hirschsprung disease: a systematic review. Journal of pediatric gastroenterology and nutrition, 42(5), 496-505.).
Комментарий. Характерно для БГ — отсутствие ганглиев в нервных сплетениях межмышечного и подслизистого слоев кишки, АХЭ-позитивные гипертрофированные нервные волокна, повышение активности тканевой АХЭ, отрицательный иммуногистохимический тест на кальретинин.
Варианты биопсии:
— полнослойная биопсия по О. Свенсону
— полнослойная биопсия при лапаротомии или лапароскопии
— серозно-мышечная биопсия при лапаротомии или лапароскопии
— щипковая и аспирационная биопсия слизистой оболочки кишки с захватом подслизистой оболочки.
Оценка метода исследования [13]:
— чувствительность 93%
— специфичность 98 %
Забор материала необходимо осуществлять не ниже 1,5 — 2,5 см от зубчатой линии ввиду физиологического отсутствия ганглиев в сегменте кишки на расстоянии 1 см от зубчатой линии у детей грудного возраста и порядка 2,5 см у детей старше одного года. [14]. В случаях забора образцов для исследования из физиологической зоны аганглиоза, необходимо дифференцировать эпителий, который отличается от такового в толстой кишке (плоские эпителиальные клетки или столбчатые эпителиальные клетки).
Различия в вариантах забора материала представлены на рис. 3.
Рисунок 3
а – биопсия слизистой оболочки кишки
b – биопсия с захватом подслизистого слоя
c – полнослойная биопсия
1-продольный мышечный слой; 2–межмышечные сплетения; 3–циркулярный мышечный слой; 4–подслизистые сплетения (терминальные); 5-подслизистые сплетения (наружные); 6-подслизистые сплетения (внутренние); 7–мышечные сплетения слизистой; 8–поджелезистые сплетения слизистой; 9–наджелезистые сплетения слизистой (из [5])
Морфологическое исследование биоптатов толстой кишки является «золотым стандартом» диагностики БГ.
Варианты гистологического исследования при подозрении на БГ включают:
классическое морфологическое исследование с окраской биоптатов гематоксилин-эозином (парафиновые блоки)
— чувствительность и специфичность 99% (при правильно выполненном заборе материала)
иммуногистохимическое исследование уровня активности ацетилхолинэстеразы (замороженные блоки)
— чувствительность 88 — 95%
— специфичность 95 — 99 %
иммуногистохимическое исследование биоптата на нейрональные маркеры
— чувствительность и специфичность изучается (наиболее перспективный маркер — кальретинин (100% и 85%, соответственно). Кальретинин (кальцийсвязывающий белок), вырабатывается клетками интрамуральных нервных сплетений и отсутствует в нервных клетках кишки у детей с БГ. Помимо высокой диагностической точности метод исследования на кальретинин проводится с классической фиксацией в парафине и не требует криообработки биоптатов.
Остальные маркеры, такие как S100, нейрон-специфическая енолаза, синптофизин и др. не показывают высокой точности диагностики и возможность их применения исследуется в настоящее время. Интраоперационная биопсия для уточнения зоны резекции и состояния нервного аппарата низводимой кишки предпочтительна, однако требует соответствующей координации работы операционного и патологоанатомического блоков лечебной организации.
В диагностике БГ возможно исследование слизистой оболочки на предмет гипертрофии АХЭ-положительных нервных волокон и повышение активности АХЭ в мышечной и собственной пластинках слизистой оболочки [15]. Однако полученные данные являются косвенными, в связи с чем биопсия только слизистой оболочки кишки (например, при эндоскопии) не рекомендована. Рекомендуемая толщина подслизистого слоя должна быть не менее 1/3 биоптата. В случае отсутствия подслизистого слоя в материале требуется повторение биопсии [5].
Биопсия с захватом подслизистого слоя (щипковая, аспирационная биопсия) является альтернативой полнослойной биопсии, но предназначена в основном для имуногистохимических исследований и мало применима при классической окраске гематоксилин-эозином. [16].
Межмышечное ганглионарное сплетение может быть визуализировано только при полнослойной биопсии. При щипковой биопсии с захватом подслизистого слоя при наличии хотя бы одного ганглия в подслизистом сплетении диагноз аганглиоз не может быть поставлен [17].
Исследования биоптатов с захватом подслизистого слоя включает оценку сплетений Мейсснера на предмет количества ганглиев и АХЭ-позитивные нервные волокна. БГ может быть установлена при обнаружении гипертрофии нервных волокон в мышечной пластинке слизистой оболочки кишки у новорожденного и в собственной пластинке слизистой у детей старше 3 месяцев.
Тест на активность тканевой АХЭ применим только при биопсии прямой и сигмовидной кишок, так как активность парасиматичеких волокон S2-S4 уменьшается в проксимальных отделах и отсутствует выше левого угла colon.
Иная диагностика
- Рекомендовано проведение ультразвукового исследования (УЗИ) прямой кишки и мышц тазового дна как дополнительного метода диагностики
Уровень убедительности рекомендаций II B (уровень достоверности доказательств – C )
(Колисниченко, М. М., Пыков, М. И., & Поддубный, И. В. (2015). Ультразвуковая диагностика болезни Гиршпрунга у детей. Экспериментальная и клиническая гастроэнтерология, (4 (116)).
Комментарий. Предложены методы определения РАИР при УЗИ, а также оценки строения, толщины, просвета прямой кишки. Представлен метод гидросоноколографии, однако необходимы дальнейшие исследования для широкого внедрения методик в клиническую практику [18].
Дифференциальную диагностику БГ у новорожденных проводят в первую очередь с низкой кишечной непроходимостью, вызванной другими причинами (атрезиями и стенозами кишечника), сидромом мекониевой пробки, мекониальным илеусом, мальротацией кишечника, аноректальными пороками, синдромом сужения левой половины толстой кишки. При отсутствии анатомической причины кишечной непроходимости во время оперативного вмешательства, необходимо выполнение поэтажной биопсии кишечника
Лечение
Лечение
Хирургическое лечение
- Рекомендовано хирургическое лечение детей с БГ
Уровень убедительности рекомендаций I (уровень достоверности доказательств – А)
Комментарий. Хирургическое лечение детей с БГ с первой операции экстраректальной ректосигмоидэктомии с первичным анастомозом O. Swenson претерпело изменения [19-23]. Основными радикальными оперативными вмешательствами являются классические операции Свенсона, Соаве и Дюамеля, суть которых состоит в резекции аганглионарного участка кишки с лапаротомией и восстановлении непрерывности кишки. Возможно формирование колоректального анастомоза отсрочено (методика А.И. Ленюшкина). В настоящее время используют миниинвазивные варианты хирургического лечения – трансанальную методику Де ла Торре-Мандрагон-Ортега, трансанальную методику Свенсона и лапароскопическую методику Джорджсона. Рекомендовано владеть несколькими методиками операций, выбирая метод индивидуально для каждого ребенка. Если детские хирурги не обладают достаточным опытом или обеспечением для проведения хирургического лечения БГ, ребенок должен быть направлен в медицинскую организацию третьего уровня. При невозможности своевременной транспортировки пациента и риске развития осложнений БГ рекомендовано наложение кишечной стомы.
Показания для наложения превентивной кишечной стомы:
— тяжелое состояние ребенка, декомпенсация функции ЖКТ
— невозможность точно определить «переходную» зону
— невозможность адекватно подготовить кишечник для радикальной операции
— отсутствие достаточного опыта радикальных операций в медицинской организации.
Наложение колостомы (энтеростомы) осуществляется на участок здоровой кишки выше переходной зоны, возможно использование предварительной лапароскопии для ревизии брюшной полости.
Используют технику петлевой или раздельной колостомии (энтеростомии) с обязательным выведением дистального сегмента кишки. Полнослойная биопсия приводящего и отводящего отдела должна быть выполнена в обязательном порядке для морфологического подтверждения диагноза и оценки состояния интактной кишки. При трудно различимой «переходной» зоне (например, у новорождённых детей) хорошая функция стомы после операции может косвенно демонстрировать правильность выбора уровня будущей резекции. В случае слишком «низкого» наложения стомы и выведения аганглионарного участка после операции отмечается обструктивный синдром, стома нередко стенозируется, требуется повторная операция и стомирование проксимального участка кишки.
Радикальное вмешательство выполняется по стабилизации состоянии ребенка. При тотальных формах БГ и формировании илеоректального анастомоза в большинстве случаев выполняют «защитную» илеостомию.
Нередко классическая БГ сочетается с нейрональной дисплазией кишки выше зоны аганглиоза (патология подслизистых мейсснеровских сплетений). Данный диагноз подтверждается при гистологическом исследовании приводящего сегмента стомы. Тактика при нейрональной дисплазии не разработана и должна быть ориентирована на функцию кишки [24].
Принципы основных видов операций при БГ:
- операция Свенсона – Хиатта – Исакова
Первый этап, абдоминальный. Лапаротомия, мобилизация аганглионарного сегмента и части здоровой кишки, экстраректальная диссекция прямой кишки дистально до расстояния 1,5-2 см от ануса сзади и сбоку и 3-5 см спереди.
Второй этап, промежностный. После дивульсии ануса трансанально эвагинируют кишку до уровня предполагаемой резекции. Ректосигмоидэктомию завершают прямым межкишечным анастомозом чаще двумя рядами узловых швов.
Операция Свенсона может быть выполнена трансанально.
- операция Соаве – Ленюшкина [25]
Два этапа первой операции:
Первый этап, абдоминальный. Лапаротомия, мобилизация аганглионарного сегмента до расстояния 4-5 см от переходной складки брюшины, демукозация ректосигмоида дистально — до расстояния 2,5 — 3 см от ануса.
Второй этап, промежностный. После дивульсии ануса трансанально низводят. мобилизованную кишку, формируя культю, состоящую из двух цилиндров (наружный — слизистая прямой кишки, внутренний — низводимая кишка). На культю накладывают раздавливающие зажимы или швы.
Второй прием — на 12-14 день отмечается формирование межкишечного анастомоза, избыточную культю отсекают.
- операция Дюамеля- Баирова
Первый этап, абдоминальный. Лапаротомия, мобилизация аганглионарного сегмента и части здоровой кишки, резекция аганглионарного сегмента. Тупым путем проделывают тоннель пресакрально по задней поверхности прямой кишки.
Второй этап, промежностный. После дивульсии ануса по задней полуокружности ануса на 1,5-2 см выше производят демукозацию, а затем выходят экстраректально и выводят в отверстие низводимую кишку через пресакральный тоннель. На образованную «шпору» между прямой кишкой и низведенной ободочной накладывают раздавливающий зажим или сшивающие аппараты. Полное устранение «шпоры» описано как операция Дюамеля-Мартина.
- операция Джорджсона — лапароскопическое эндоректальное низведение
Первый этап, абдоминальный. Лапароскопия, мобилизация аганглионарного сегмента до «мышечного комплекса» леваторов и сфинктера прямой кишки.
Второй этап, промежностный. Выполняется субмукозная диссекция прямой кишки до соединения с брюшной полостью. Мышечная манжета рассекается (иссекается частично) в продольном направлении. Аганглионарный сегмент удаляется, накладывается колоректальный анастомоз.
- операция де ла Торре-Мандрагон и Ортега — трансанальное эндоректальное низведение
Операция может быть выполнена при расположении аганглионарной зоны на уровне ректосигмоидного отдела. Со стороны промежности выполняется субмукозная диссекция на расстоянии 5-6 см, затем экстраректально последовательно мобилизуют всю аганглионарную зону до расширенной здоровой кишки. Кишку низводят. После резекции аганглионарной зоны накладывают прямой анастомоз.
В настоящее время с учетом данных мультицентровых исследований, систематических обзоров и метаанализа
- Рекомендовано трансанальное эндоректальное низведение (с экстраректальным или субмукозным выделением кишки) без абдоминального этапа у детей с типичной формой БГ, при невозможности полного выделения кишки трансанально — с лапароскопической ассистенцией или лапаротомией
Уровень убедительности рекомендаций I (уровень достоверности доказательств – А)
(Neuvonen, M. I., Kyrklund, K., Rintala, R. J., & Pakarinen, M. P. (2017). Bowel Function and Quality of Life After Transanal Endorectal Pull-through for Hirschsprung Disease. Annals of surgery, 265(3), 622-629), Kim, A. C., Langer, J. C., Pastor, A. C., Zhang, L., Sloots, C. E., Hamilton, N. A., … & Bax, N. M. (2010). Endorectal pull-through for Hirschsprung’s disease—a multicenter, long-term comparison of results: transanal vs transabdominal approach. Journal of pediatric surgery, 45(6), 1213-1220.
Комментарий
При операциях по поводу субтотальных (высоких форм) болезни Гиршпрунга могут возникнуть трудности при низведении правых отделов ободочной кишки. В таких случаях можно использовать метод ее поворота (разворота) на 180 градусов и низведения справа (слева) с последующим формированием анастомоза одним из методов.
- Анастомоз при радикальной операции накладывают на расстоянии 1 — 1,5 см выше зубчатой линии во избежание послеоперационной анальной недостаточности. После анастомозирования возможно заведение «ректальной» трубки на 5-7 дней для декомпрессии кишки и профилактики обструкции. Рекомендовано пальцевое ректальное исследование через 10-14 дней после операции, у новорожденных детей — калибровочное бужирование.
Лечение тотальных форм проводится только коллективами с многолетним опытом, в медицинских учреждениях третьего уровня.
Медицинская реабилитация
Реабилитация
Реабилитация детей с БГ после операции составляет важную часть комплексного лечения и зачастую требует индивидуального подхода, так как неудовлетворительные функциональные результаты и снижение качества жизни пациентов до сих пор нередки как в России, так и за рубежом [4]
Можно выделить принципиально две группы осложнений:
- осложнения хирургической операции, которые могут быть ранними и поздними. Это — несостоятельность колоректального анастомоза, гнойные осложнения и тазовые абсцессы, параректальные и ректо-везикальные свищи, стенозы и стриктуры зоны анастомоза, «остаточная» зона аганглиоза, вследствие некорректного уровня резекции кишки.
- неудовлетворительные функциональные результаты после успешно выполненной операции, к последним относят – запор, диарею, недержание кала, рецидивирующие колиты.
Для ориентирования в частоте и характере функциональных проблем приведены данные мета-анализа неудовлетворительных результатов после различных лапароскопически- ассистированных операций при БГ (табл.)
Таблица Данные метаанализа 16 валидных исследований, 820 пациентов, оценка отдаленных результатов от 6 месяцев до 6 лет после операции) (Пури 2016)
| Осложнение | ЛА операция Свенсона | ЛА операция Соаве | ЛА операция Дюамеля |
| Недержание кала | 3,8% | 81,1% | 15,1% |
| Запор | 7,2% | 25,7% | 67% |
В разграничении причин сохраняющегося запора следует выделять: возможное наличие стеноза или стриктуры колоректального анастомоза, остаточную зону аганглиоза, гипертонус внутреннего анального сфинктера и/или ахалазию, нарушение моторики низведенных отделов кишки (в том числе на фоне дисганглиоза), функциональные нарушения дефекации [26].
При наличии осложнений хирургического лечения
- Рекомендовано обследование ребенка в стационаре и оперативное вмешательство
Уровень убедительности рекомендаций I (уровень достоверности доказательств – А)
Friedmacher, F., & Puri, P. (2011). Residual aganglionosis after pull-through operation for Hirschsprung’s disease: a systematic review and meta-analysis. Pediatric surgery international, 27(10), 1053.
Комментарий. В зависимости от вида выявленного осложнения решение о сроке и варианте операции принимается индивидуально. При наличии остаточной зоны аганглиоза рекомендована повторная операция низведения, при гнойном воспалении в малом тазу первым этапом необходимо выполнить наложение кишечной стомы и заняться санированием гнойного очага. При стенозе ректального анастомоза после осмотра анального канала под наркозом принимается решение о возможности бужирования стеноза или необходимости повторной операции низведения. При повторных операциях низведения используют методики экстраректальной и подслизистой диссекции в зависимости от индивидуальных особенностей ситуации.
При наличии неудовлетворительных функциональных результатов
- Рекомендовано обследование ребенка амбулаторно или в стационаре
Комментарий. Обследование пациента с БГ после операции направлено на решение следующих задач:
— уточнение характера моторики кишки
— уточнение анатомических особенностей кишки
— уточнение функциональных особенностей кишки и мышц таза
Объем обследования определяется индивидуально и включает различные методы:
— пальцевое ректальное исследование для оценки проходимости зоны анастомоза, содержимого прямой кишки
— осмотр ребенка под наркозом (оценивается состояние анального канала и зубчатой линии, уровень наложения анастомоза).
— рентеноконтрастные методы исследования желудочно-кишечного тракта для оценки анатомических особенностей низведенной кишки, скорости пассажа по ЖКТ, динамики дефекации, (ирригография (скопия), пассаж контраста по кишечнику, дефекография)
— аноректальную манометрию
— УЗИ прямой кишки и сфинктерного аппарата
— ангиографию брыжеечных сосудов по показаниям (подозрение на нарушение мезентериального кровотока в низведенной кишке)
-магнитно-резонансную томографию малого таза по показаниям
В случае недоступности данных методик в клинике, невозможности назначения адекватной консервативной терапии, пациент должен быть направлен в медицинскую организацию второго или третьего уровней.
При наличии неудовлетворительных функциональных результатов
- Рекомендована диета при запоре со вторичным недержанием кала или без него
Комментарий. В случае замедленного пассажа по ЖКТ назначается диета в повышенным содержанием клетчатки. При нормальном пассаже по ЖКТ ребенку назначается обычная диета, соответствующая возрасту.
- Рекомендованы очистительные клизмы при запоре со вторичным недержанием кала или без него
Комментарий. При выполнении клизмы используется вода или солевой раствор (0,9% NaCL) в объеме 20-30 мл/год жизни. Клизму необходимо выполнять 1-2 раза в сутки в одно и то же время в течение 5 — 10 дней, после чего необходимо начать пероральный прием слабительных препаратов
- Рекомендован пероральный прием полиэтиленгликоля (макрогола) при запоре со вторичным недержанием кала или без него у детей старше 6 месяцев
Уровень убедительности рекомендаций I (уровень достоверности доказательств – А)
Tabbers, M. M., DiLorenzo, C., Berger, M. Y., Faure, C., Langendam, M. W., Nurko, S., … & Benninga, M. A. (2014). Evaluation and treatment of functional constipation in infants and children: evidence-based recommendations from ESPGHAN and NASPGHAN. Journal of pediatric gastroenterology and nutrition, 58(2), 258-274.
Комментарий. Полиэтиленгликоль (ПЭГ) является препаратом выбора в лечении функционального запора у детей. Показано постепенное увеличение дозы препарата до 1,5 г/кг/сутки к 5-6 дню, с постепенным снижением до поддерживающей дозы 0,6 г/кг/сутки в течение 1-2 месяцев. Не рекомендуется одновременно применять слабительные препараты и очистительные клизмы. При отсутствии эффекта от препарата или появлении побочных эффектов — вздутия, боли в животе, рекомендовано прекратить прием препарата и продолжить очистительные клизмы
- Рекомендован пероральный прием лактулозы при запоре со вторичным недержанием кала или без него у детей с периода новорожденности
Комментарий. Лактулоза является препаратом второго ряда в лечении функционального запора у детей.
- Рекомендовано введение ботулотоксина в область внутреннего анального сфинктера при запоре со вторичным недержанием кала или без него
Уровень убедительности рекомендаций IIА (уровень достоверности доказательств – В)
Han-Geurts, I. J., Hendrix, V. C., de Blaauw, I., Wijnen, M. H., & van Heurn, E. L. (2014). Outcome after anal intrasphincteric Botox injection in children with surgically treated Hirschsprung disease. Journal of pediatric gastroenterology and nutrition, 59(5), 604-607, Wester, T., & Granström, A. L. (2015). Botulinum toxin is efficient to treat obstructive symptoms in children with Hirschsprung disease. Pediatric surgery international, 31(3), 255-259, Church, J. T., Gadepalli, S. K., Talishinsky, T., Teitelbaum, D. H., & Jarboe, M. D. (2017). Ultrasound-guided intrasphincteric botulinum toxin injection relieves obstructive defecation due to Hirschsprung’s disease and internal anal sphincter achalasia. Journal of pediatric surgery, 52(1), 74-78, Han-Geurts, I. J., Hendrix, V. C., de Blaauw, I., Wijnen, M. H., & van Heurn, E. L. (2014). Outcome after anal intrasphincteric Botox injection in children with surgically treated Hirschsprung disease. Journal of pediatric gastroenterology and nutrition, 59(5), 604-607, .)
Комментарий. Показано в случае выявления повышенного тонуса анальных сфинктеров при пальцевом ректальном исследовании или при аноректальной манометрии, отсутствия РАИР при аноректальной манометрии
- Рекомендована задняя миотомия внутреннего анального сфинктера при его повышенном тонусе или ахалазии
Уровень убедительности рекомендаций I (уровень достоверности доказательств – А)
(Friedmacher, F., & Puri, P. (2012). Comparison of posterior internal anal sphincter myectomy and intrasphincteric botulinum toxin injection for treatment of internal anal sphincter achalasia: a meta-analysis. Pediatric surgery international, 28(8), 765-771.)
- Рекомендована терапия по типу биологической обратной связи (БОС) у детей с недержанием кала
Уровень убедительности рекомендаций IIА (уровень достоверности доказательств – В)
Van Kuyk, E. M., Brugman‐Boezeman, A. T. M., Wissink‐Essink, M., Oerlemans, H. M., Severijnen, R. S. V. M., & Bleijenberg, G. (2001). Defecation problems in children with Hirschsprung’s disease: a prospective controlled study of a multidisciplinary behavioural treatment. Acta Paediatrica, 90(10), 1153-1159.
Комментарий. Метод лечения назначается курсом 7-10 процедур 1-2 раза в год при выявлении недостаточности анальных сфинктеров при пальцевом ректальном исследовании или аноректальной манометрии
- Рекомендовано отмена энтерального кормления при появлении признаков энтероколита
Уровень убедительности рекомендаций I (уровень достоверности доказательств – А)
Gosain, A., Frykman, P. K., Cowles, R. A., Horton, J., Levitt, M., Rothstein, D. H., … & Goldstein, A. M. (2017). Guidelines for the diagnosis and management of Hirschsprung-associated enterocolitis. Pediatric surgery international, 33(5), 517-521.
Комментарий. Необходимо информировать родителей ребенка о возможном развитии энтероколита. До приезда скорой помощи и госпитализации ребенка показана отмена энтерального питания. При удовлетворительном состоянии ребенка и домашнем лечении показано дробное кормление в объеме, не превышающем половину суточной дозы в течение 1-2 дней с постепенным увеличением объема
- Рекомендовано выполнение сифонной клизмы (кишечной ирригации с помощью газоотводной трубки) при появлении признаков энтероколита Уровень убедительности рекомендаций I (уровень достоверности доказательств – А)
Gosain, A., Frykman, P. K., Cowles, R. A., Horton, J., Levitt, M., Rothstein, D. H., … & Goldstein, A. M. (2017). Guidelines for the diagnosis and management of Hirschsprung-associated enterocolitis. Pediatric surgery international, 33(5), 517-521.
- Рекомендована антимикробная терапия при появлении признаков энтероколита
Комментарий. Препарат выбора при ГАЭК — метронидазол перорально и парентерально в возрастной дозировке в течение 3-5 дней
Уровень убедительности рекомендаций I (уровень достоверности доказательств – А)
Gosain, A., Frykman, P. K., Cowles, R. A., Horton, J., Levitt, M., Rothstein, D. H., … & Goldstein, A. M. (2017). Guidelines for the diagnosis and management of Hirschsprung-associated enterocolitis. Pediatric surgery international, 33(5), 517-521.
- Рекомендована инфузионная терапия и парентеральное питание, декомпрессия желудка и кишечника при тяжелом течении энтероколита
Уровень убедительности рекомендаций I (уровень достоверности доказательств – А)
Gosain, A., Frykman, P. K., Cowles, R. A., Horton, J., Levitt, M., Rothstein, D. H., … & Goldstein, A. M. (2017). Guidelines for the diagnosis and management of Hirschsprung-associated enterocolitis. Pediatric surgery international, 33(5), 517-521.
Информация
Источники и литература
-
Клинические рекомендации Российской ассоциации детских хирургов
- 1. Hirschsprung Disease and Related Disorders John R. Goldblum in Rosai and Ackerman’s Surgical Pathology. Elsevier Inc. 2018. 648-87
2. Kapur R. P. Practical pathology and genetics of Hirschsprung’s disease //Seminars in pediatric surgery. – Elsevier, 2009. – Т. 18. – №. 4. – С. 212-223
3. Здравоохранение в России, 2015: статистический сборник. М: Статистика России, 2015. 174 с
4. Холостова В. В. Болезнь Гиршпрунга у детей (диагностика, лечение, реабилитация) //Автореф. дисс… докт. мед. наук. Москва. – 2016
5. Schäppi M. G. et al. A practical guide for the diagnosis of primary enteric nervous system disorders //Journal of pediatric gastroenterology and nutrition. – 2013. – Т. 57. – №. 5. – С. 677-686
6. Peña A., Bischoff A. Surgical treatment of colorectal problems in children. – Springer, 2015
7. Еurocat Association: [Электронный ресурс] – Режим доступа: http://www. www.eurocat-network.eu
8. Holschneider A. M., Puri P. (ed.). Hirschsprung’s disease and allied disorders. – Springer Science & Business Media, 2007
9. Passarge E. Gastrointestinal tract and hepatobiliary duct system //Emery and Rimoin’s Principles and Practice of Medical Genetics. – 2013. – С. 1-17.
10. Исаков Ю. Ф., Ленюшкин А. И., Долецкий С. Я. Хирургия пороков развития толстой кишки у детей //М.: Медицина. – 1972
11. Исаков, Ю.Ф. Болезнь Гиршпрунга у детей : дис. … докт.мед.наук : 14.00.35 / Юрий Федорович Исаков ; 2-й Моск.гос.мед.ин-т ; -М.,1963. -273 л).
12. Баиров Г. А. Хирургия пороков развития у детей //Л.: Медицина. – 1968. – С. 116-132.
13. W. Peranteau, P. Mattei Hirschsprung’s Disease in Pediatric Gastrointestinal and Liver Disease, Ch 54, 622-630.e4
14. Langer J. C. Hirschsprung disease //Fundamentals of pediatric surgery. – Springer, New York, NY, 2011. – С. 475-484
15. Никифоров А.Н. Болезнь Гиршпрунга у детей: Автореф. дис. .д-ра мед. наук-Минск, 1995.-38 с.
16. Kobayashi H. et al. Rectal biopsy: what is the optimal procedure? //Pediatric surgery international. – 2002. – Т. 18. – №. 8. – С. 753-756.
17. Knowles CH, De Giorgio R, Kapur RP, et al. The London Classification of gastrointestinal neuromuscular pathology: report on behalf of the Gastro 2009 International Working Group. Gut 2010; 59:882–887
18. Гераськин А. В., Дронов А. Ф., Смирнов А. Н. Детская колопроктология: Руководство для врачей //Москва: Контэнт. – 2012.
19. Морозов, Д. А., Пименова, Е. С., Филиппов, Ю. В., Гончарь, В. Ф., Айрапетян, М. И., Аршинова, М. А., Чудинов, Д. С. (2016). Операция O. Swenson-базовая технология хирургии болезни Гиршпрунга. Детская хирургия, 20(4).
20. Сварич, В. Г., Киргизов, И. В. (2016). Наш опыт лечения болезни Гиршпрунга у детей. Детская хирургия, 20(5).
21. Дронов, А. Ф., Смирнов, А. Н., Холостова, В. В., Залихин, Д. В., Маннанов, А. Г. (2016). Операция Соаве при болезни Гиршпрунга у детей-50-летний опыт применения. Детская хирургия,20(6).
22. Джорджсон, К., Мюнстерер, О., Козлов, Ю. А. (2016). Болезнь Гиршпрунга-лапароскопическое эндоректальное низведение. Детская хирургия, 20(6).
23. Ионов, А. Л., Гогина, А. А., Сулавко, Я. П. (2017). Повторные операции после хирургического лечения болезни Гиршпрунга у детей. Детская хирургия, 21(1), 42-46.
24. Knowles CH, De Giorgio R, Kapur RP, et al. The London Classification of gastrointestinal neuromuscular pathology: report on behalf of the Gastro 2009 International Working Group. Gut 2010; 59:882–887
25. Ленюшкин А.И. Детская колопроктология. М, — 1990. 352 с.
26. Langer J. C. et al. Guidelines for the management of postoperative obstructive symptoms in children with Hirschsprung disease //Pediatric surgery international. – 2017. – Т. 33. – №. 5. – С. 523-526.
27. Wyllie R., Hyams J. S., Kay M. Pediatric gastrointestinal and liver disease. – Elsevier Inc., 2006.
- 1. Hirschsprung Disease and Related Disorders John R. Goldblum in Rosai and Ackerman’s Surgical Pathology. Elsevier Inc. 2018. 648-87
Информация
Ключевые слова
болезнь Гиршпрунга
дети
аганглиоз кишечника
Список сокращений
БГ — болезнь Гиршпурнга
ВПР — врожденный порок развития
ГАЭК — гиршпрунг-ассоциированный энетроколит
РАИР — ректоанальный ингибиторный рефлекс
ВАС — внутренний анальный сфинктер
Приложение А1. Состав Рабочей группы
Члены Рабочей группы не имеют конфликта интересов
- Аверин Василий Иванович — д.м.н., главный внештатный детский хирург Министерства здравоохранения Республики Беларусь, заведующий кафедрой детской хирургии Белорусского медицинского университета, Минск
- Дегтярев Юрий Григорьевич — д.м.н. ,доцент кафедры детской хирургии Белорусского медицинского университета, Минск
- Ионов Андрей Львович — д.м.н., профессор кафедры детской хирургии РНИМУ им. Н.И. Пирогова, заведующий отделением колопроктологии ФГБУ РДКБ, Москва
- Караваева Светлана Александровна — д.м.н., профессор кафедры детской хирургии с курсом анестезиологии и реанимации ПСПбГМУ им. И.П. Павлова, Санкт-Петербург
- Котин Алексей Николаевич — к.м.н., доцент кафедры детской хирургии с курсом анестезиологии и реанимации ПСПбГМУ им. И.П. Павлова, Санкт-Петербург
- Комиссаров Игорь Алексеевич — д.м.н., профессор кафедры хирургических болезней детского возраста СПбПГМУ, Санкт-Петербург
- Мокрушина Ольга Геннадьевна — д.м.н., профессор кафедры детской хирургии, руководитель отдела пороков развития и неотложных состояний новорожденных НИИ хирургической патологии и критических состояний детского возраста РНИМУ им. Н.И. Пирогова
- Морозов Дмитрий Анатольевич — Председатель Комитета по охране здоровья ГД РФ, заведующий кафедрой детской хирургии и урологии-андрологии ПМГМУ им. И.М. Сеченова, Москва
- Немилова Татьяна Константиновна — д.м.н., профессор кафедры детской хирургии с курсом анестезиологии и реанимации ПСПбГМУ им. И.П. Павлова, Санкт-Петербург
- Новожилов Владимир Александрович — д.м.н., профессор, главный врач Городской Ивано-Матренинской ДКБ, профессор кафедры детской хирургии Иркутской ГМАПО
- Паршиков Вячеслав Владимирович — д.м.н., заведующий кафедрой детской хирургии НижГМА, Нижний Новгород
- Пименова Евгения Сергеевна — к.м.н., доцент кафедры детской хирургии и урологии-андрологии ПМГМУ им. И.М. Сеченова, Москва
- Поддубный Игорь Витальевич — д.м.н., заведующий кафедрой детской хирургии МГСМУ, Москва
- Сварич Вячеслав Гаврилович — д.м.н., заведующий отделением детской хирургии Республиканской детской больницы, Сыктывкар
- Смирнов Алексей Николаевич — д.м.н., профессор кафедры детской хирургии РНИМУ им. Н.И. Пирогова, заведующий отделением неотложной и гнойной хирургии ДГКБ №13 им. Н.Ф.Филатова, Москва
- Хворостов Игорь Николаевич — д.м.н., заведующий кафедрой детской хирургии ВолгГМУ, Волгоград
- Холостова Виктория Валерьевна — д.м.н., доцент кафедры детской хирургии РНИМУ им. Н.И. Пирогова
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций
1. врачи-детские хирурги
2. врачи-педиатры
Класс рекомендаций
Таблица П1 Уровни убедительности рекомендаций
| I | Доказательства и/или общее согласие, что данные методы диагностики/лечения – благоприятные, полезные и эффективные |
| II | Доказательства противоречивы и/или противоположные мнения относительно полезности/эффективности лечения |
| IIа | Большинство доказательств/мнений в пользу полезности/ эффективности. |
| IIб | Полезность/эффективность не имеют достаточных доказательств/ определенного мнения. |
| III | Доказательства и/или общее согласие свидетельствует о том, что лечение не является полезным/эффективным и, в некоторых случаях, может быть вредным. |
Таблица П2
Уровни достоверности доказательств
|
А |
Доказательства основаны на данных многих рандомизированных клинических исследований или мета-анализов. |
| В | Доказательства основаны на данных одного рандомизированного клинического исследования или многих нерандомизированных исследований. |
| С | Согласованные мнения экспертов и/или немногочисленные исследования, ретроспективные исследования, регистры |
Приложение Б. Алгоритмы ведения пациента
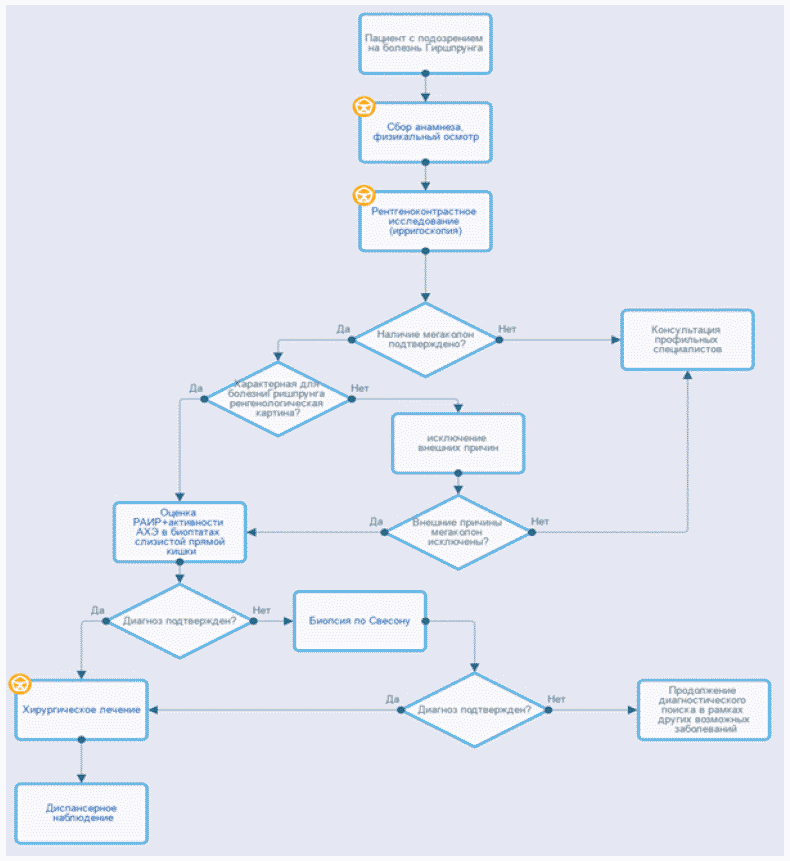
Алгоритм ведения 1 (дети)
Алгоритм ведения 2 (дети)
Прикреплённые файлы
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
Оглавление
Список сокращений
АХЭ – ацетилхолинэстераза
д.м.н. – доктор медицинских наук
ЖКТ – желудочно-кишечный тракт
к.м.н. – кандидат медицинских наук
МКБ – международная классификация болезней
РАИР – ректоанальный ингибиторный рефлекс
РКИ – рандомизированное клиническое исследование
РФП – радиофармпрепарат
ТТГ – тиреотропный гормон
1. Краткая информация
1.1 Определение
Болезнь Гиршпрунга – это аномалия развития толстой кишки, характеризующаяся отсутствием ганглиев подслизистого и межмышечного нервных сплетений всей толстой кишки или ее части.
Синонимы: аганглиоз толстой кишки.
1.2 Этиология и патогенез
В настоящее время болезнь Гиршпрунга считается полиэтиологичным заболеванием.
На 7-12 неделе беременности происходит нарушение формирования нервных структур на определенном участке прямой кишки. Происходят значительные изменения в нервных сплетениях Ауэрбаха (мышечный слой) и Мейснера (подслизистый слой). Эти изменения состоят, главным образом, в отсутствии ганглиев мышечно-кишечного и подслизистого сплетений [1, 2].
На месте ганглиев определяются лишь нервные волокна и мелкие клетки с ядрами, богатыми хроматином – элементы глии [13, 14].
В некоторых случаях не определяются и глиальные клетки, а вместо узлов имеются лишь нервные стволики, ориентированные в одном направлении. Они распадаются на несколько ветвей и не образуют типичных сплетений. В отдельных случаях отсутствуют не только ганглии, но и нервы.
В настоящее время основная теория, объясняющая отсутствие ганглиев в толстой кишке, — нарушение миграции нейробластов из вагусного нервного гребешка в процессе эмбриогенеза, и чем раньше прекращается миграция, тем длиннее аганглионарный сегмент [6, 7, 8].
Исследования в области молекулярной генетики указывают на значительную роль в патогенезе болезни Гиршпрунгамутаций 4 генов: RET (рецептор тирозинкиназы), GDNF (нейтрофический фактор глиальных клеток), ENDRB (ген рецептора эндотелина-В), EDN3 (эндотелин-3) и их определяющее влияние на процесс миграции нейробластов [3, 4, 5].
Кроме этого существует гипотеза, согласно которой аганглиоз развивается вследствие нарушения дифференцировки нервных клеток, уже достигших кишечной стенки. Влиять на созревание клеток могут различные факторы, такие, как гипоксия, воздействие химических агентов, повышенная радиация, вирусная инфекция [9, 10].
Сочетание генетических нарушений с патологическим влиянием внешней и внутренней среды определяет характер поражения не только интрамурального нервного аппарата. По данным разных авторов, сочетание болезни Гиршпрунга с другими пороками развития происходит в 29–32,7% случаев [10, 11, 12].
Накопление ацетилхолинэстеразы в слизистой оболочке наряду с отсутствием медиаторов, обеспечивающих тормозящий эффект в кишечной стенке, вызывает стойкий спазм, который служит патогенетическим признаком болезни Гиршпрунга [15, 16].
Вероятно, аганглионарный участок кишки не участвует в перистальтической активности и является таким образом зоной функционального препятствия для пассажа кишечного содержимого. В результате происходит хроническая задержка каловых масс в вышележащем отделе кишки, последний с течением времени расширяется и формируется мегаколон – основной клинический признак болезни Гиршпрунга.
1.3 Эпидемиология
Болезнь Гиршпрунга является достаточно распространенной аномалией развития. Частота возникновения болезни Гиршпрунга на протяжении нескольких десятилетий колеблется от 1:30 тыс. до 1:2000 к общему числу новорожденных [11, 17, 18].
У мальчиков заболевание встречается в 5 раз чаще, чем у девочек [9, 10, 19].
Распространенность аганглиоза толстой кишки варьирует среди этнических групп. Данное заболевание встречается в Европе у 1 из 4500 новорожденных, а в Японии — у 1 из 4697 родившихся детей. Болезнь Гиршпрунга регистрируется у 1,5 из 10 тыс. человек, родившихся в кавказском регионе, у 2,1 из 10 тыс. новорожденных афроамериканцев и у 2,8 из 10 тыс. детей азиатского происхождения [20, 21].
Существует разница в частоте различных форм заболевания в зависимости от протяженности зоны аганглиоза. Случаи с коротким сегментом встречаются гораздо чаще и составляют до 80% общего числа. Остальные 20% наблюдений приходятся на пациентов, у которых аганглионарный сегмент распространяется проксимальнее прямой кишки [2, 22, 23].
Болезнь Гиршпрунга часто является семейным заболеванием. Риск возникновения этого заболевания у родственников значительно выше по сравнению с остальным населением. Из всех регистрируемых семейные случаи аганглиоза составляют 20% [20, 24].
1.4 Коды по МКБ-10
Другие врожденные аномалии (пороки развития) органов пищеварения (Q 43):
Q43.1 – Болезнь Гиршпрунга
1.5 Классификация
1.5.1 Анатомические формы заболевания.
Выделяют следующие анатомические формы:
- наданальная форма — зона аганглиоза локализуется в нижнеампулярном отделе прямой кишки;
- Ректальная форма — недоразвитие интрамурального нервного аппарата распространяется на всю прямую кишку;
- Ректосигмоидная форма — аганглиоз занимает всю прямую кишку и часть или всю сигмовидную кишку;
- Субтотальная форма — в аганглионарный сегмент включена поперечная ободочная кишка;
- Тотальная форма — поражение всей толстой кишки, выявляется расширение подвздошной кишки.
1.5.2 По локализации расширения кишечника.
- Мегаректум;
- Мегасигма;
- Левосторонний мегаколон;
- Субтотальный мегаколон;
- Тотальный мегаколон;
- Мегаилеум.
1.5.3 По степени компенсации.
- Компенсированное состояние кишки — на протяжении многих лет у больного отмечается редкий, но самостоятельный стул или имеются запоры от 3 до 7 дней, которые легко разрешаются с помощью слабительных препаратов и клизм;
- Субкомпенсированное состояние, в отличие от предыдущего, требует интенсивных мероприятий по опорожнению кишки. В таких случаях без применения слабительных препаратов и клизм самостоятельный стул может отсутствовать свыше 7 дней;
- Декомпенсированное состояние характеризуется отсутствием позыва на дефекацию и самостоятельного стула. У многих пациентов толстая кишка бывает заполнена плотным кишечным содержимым или каловыми камнями. Зачастую даже интенсивные мероприятия не позволяют адекватно опорожнить толстую кишку. В подобных случаях показано срочное хирургическое лечение.
1.5.4 По клиническому течению заболевания.
- Типичный («детский») вариант — интенсивный запор развиваетсядостаточно быстро, практически отсутствует самостоятельный стул, быстро нарастают явления кишечной непроходимости;
- Пролонгированный вариант — медленное течение заболевания, когда с запором удается длительное время справляться с помощью консервативных мероприятий;
- Латентный вариант — впервые запор появляется после 14 лет, и как правило, быстро развивается хроническая толстокишечная непроходимость. Появившийся запор нарастает, слабительные средства совершенно неэффективны, и для опорожнения кишки приходится прибегать к ежедневным клизмам.
2. Диагностика
2.1 Жалобы и анамнез
- Рекомендовано при опросе пациента обратить внимание на жалобы, длительность заболевания, характер стула и т.д. […]
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
Комментарий. Симптомы болезни Гиршпрунга обычно возникают в раннем детстве. Однако ее клинические проявления могут иметь стертую картину у детей и развиться в зрелом возрасте. Главной причиной обращения в клинику является запор, который отмечают все пациенты. При этом у большинства больных наблюдается отсутствие самостоятельного стула. Этот симптом всегда сочетается с отсутствием позыва на дефекацию. У ряда пациентов может быть позыв на дефекацию и самостоятельный стул, однако остается ощущение неполного опорожнения толстой кишки. Наличие самостоятельного стула у этих пациентов обусловлено сохранившейся пропульсивной способностью тех отделов толстой кишки, которые располагаются проксимальнее аганглионарной зоны [23, 25].
Вздутие живота регистрируется у половины пациентов. Этот симптом отмечается на фоне длительного отсутствия самостоятельного стулаи исчезает после опорожнения толстой кишки. Боли в животе носят,как правило, приступообразный характер и возникают на высоте запора, который купируется применением очистительных клизм [1, 26, 27].
Тошнота и рвота появляются, как правило, при декомпенсированном состоянии, сопровождаются болями в животе, длительным отсутствием самостоятельного стула. У ряда пациентов могут отмечаться слабость и недомогание как проявление общей интоксикации [28].
У взрослых пациентов практически не развиваются явления энтероколита, столь характерного для детей, страдающих болезнью Гиршпрунга[20].
2.2 Физикальное обследование
- Рекомендован осмотр и пальпация живота […]
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
Комментарий. При объективном осмотре у многих пациентов отмечается развернутый реберный угол. На фоне вздутия, увеличения в размерах толстой кишки заметны асимметрия живота, увеличение его в размерах, с растянутой передней брюшной стенкой и видимой на глаз перистальтикой. В то же время при адекватно проводимых консервативных мероприятиях мегаколон развивается медленно, что позволяет сохранить нормальную форму живота [1, 22].
При компенсированном состоянии пальпация живота у пациентов с болезнью Гиршпрунга может быть малоинформативной. При субкомпенсированном и декомпенсированном мегаколон пальпаторно определяется раздутая газами или заполненная каловыми массами ободочная кишка, наиболее часто сигмовидная кишка. Она имеет форму баллонообразного цилиндра, располагающегося, как правило, в левой половине живота. В случае переполнения кишки содержимым на ней остаются пальцевые вдавления. У ряда пациентов могут пальпироваться каловые камни, которые в некоторых наблюдениях смещаются в просвете кишки [25, 23].
- Рекомендовано ректальное исследование у больных наданальной формой заболевания позволяет выявить наличие каловых масс или копролитов в ампуле прямой кишки [26, 22].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
Комментарий. Осмотр промежности, перианальной области неинформативен.
2.3 Лабораторная диагностика
Специфичных лабораторных проявлений болезни Гиршпрунга нет.
- Рекомендуется исследование уровня тиреотропный гормон (ТТГ), кальция и калия плазмы для исключения вторичного мегаколон при эндокринологических расстройствах и электролитных нарушениях.
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
2.4 Инструментальная диагностика
Рентгенологические методы исследования.
Эти методы дают возможность оценить функциональное и морфологическое состояние толстой кишки, что существенно влияет на выбор дальнейшей диагностической и лечебной тактики [33, 1, 26].
- Рекомендована обзорная рентгенография брюшной полости без предварительной подготовки позволяет определить наличие признаков кишечной непроходимости, выявить каловые камни.
- Рекомендована ирригоскопия для установления наличия или отсутствия зоны сужения, ее протяженность, а также распространенность мегаколон и состояние нерасширенных отделов ободочной кишки. [25, 9, 22].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
Комментарий. При этом оценивается сократительная способность кишечной стенки, выраженность гаустрации ободочной кишки, полноценность ее опорожнения и наличие продольной складчатости слизистой оболочки в расширенных отделах. При ирригоскопии контролируются уровень и степень заполнения толстой кишки, выбирается проекция для наилучшего выявления зоны сужения, которая обычно соответствует аганглионарному сегменту. Рельеф слизистой оболочки изучается после опорожнения толстой кишки от контрастных сред.
Поскольку при болезни Гиршпрунга имеется очевидная причина нарушения пассажа кишечного содержимого – аганглионарный сегмент, у большинства пациентов нет необходимости в изучении моторно-эвакуаторной функции толстой кишки. [25, 34]
Эндоскопические методы исследования.
- Рекомендована ректороманоскопия, которая дает возможность осмотреть прямую и дистальную часть сигмовидной кишки. […]
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
Комментарий. При подозрении на болезнь Гиршпрунга это исследование проводится без специальной подготовки. При наличии аганглиоза выраженный спазм стенки дистального отдела толстой кишки не позволяет каловым массам проникать в суженный участок, что является патогномоничным признаком заболевания. Проксимальнее суженного участка обнаруживается расширенная часть кишки, содержащая каловые массы. В этом отделе определяются сглаженность и продольная направленность складок слизистой оболочки, иногда ее атрофия или гиперемия [9, 22].
- Колоноскопия рекомендована как вспомогательный методом исследования при болезни Гиршпрунга, так как полноценная подготовка толстой кишки затруднена и большие размеры кишки создают значительные трудности проведения аппарата в связи с отсутствием достаточной площади фиксации колоноскопа [20].
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 4)
Физиологические методы исследования.
- Рекомендована аноректальная манометрия для дианостики болезни Гиршпрунгас. […]
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
Комментарий. У больных с подозрением на болезнь Гиршпрунга важным диагностическим тестом является аноректальная манометрия, в частности, исследование ректоанального ингибиторного рефлекса (рефлекторного расслабления внутреннего сфинктера в ответ на повышение давления в прямой кишке). Отсутствие ректоанального ингибиторного рефлекса является надежным диагностическим критерием болезни Гиршпрунгас чувствительностью 70–95% [35, 36]
2.5 Иная диагностика
Гистохимическая и морфологическая диагностика основана на выявлении ацетилхолинэстеразы в собственной пластинке слизистой оболочки аганглионарногосегмента толстой кишки. Установлено, что накопление ацетилхолинэстеразы в аганглионарной зоне значительно больше, чем в нормально иннервированном участке толстой кишки. Это обстоятельство послужило для разработки гистохимического метода диагностики аганглиоза [15, 16]. Материал для определения уровня ацетилхолинэстеразы берется с уровня 5, 10 и 15 см от края анального канала.
- Рекомендована иммуногистохимическая диагностика.[…]
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
Комментарий. В последние годы активно используется иммуногистохимическая диагностика, направленная на выявление нервных волокон, содержащих оксид азота (NO). Он является нейротрансмиттером, осуществляющим передачу импульсов, расслабляющих внутренний сфинктер. Специфическая качественная реакция демонстрирует отсутствие оксида азота в аганглионарной зоне. Это исследование наиболее ценно для определения диагноза болезни Гиршпрунга с ультракоротким аганглионарным сегментом, когда нет характерной рентгенологической картины, и при отсутствии ректоанального рефлекса обнаруживаются ганглии в биоптате стенки прямой кишки [29, 30, 31].
- Рекомендована биопсия стенки прямой кишки. […]
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
Комментарий. Решающее значение в диагностике болезни Гиршпрунга имеет биопсия стенки прямой кишки. Методика предложена O. Swenson (1955) и заключается в иссечении полнослойного фрагмента стенки прямой кишки на расстоянии 3 см от зубчатой линии с последующим исследованием этого участка на наличие интрамуральных ганглиев. Необходимость в этой инвазивной процедуре возникает при дифференциальной диагностике идиопатического мегаколон и болезни Гиршпрунга, когда имеются противоречия между данными аноректальной манометрии, результатами пробы на ацетилхолинэстеразу и рентгенологической картиной. Выявление аганглиоза межмышечного и подслизистого нервных сплетений является надежным подтверждением болезни Гиршпрунга. Следует помнить, что зона физиологического гипо- и аганглиоза может распространяться до 5 см проксимальнее зубчатой линии [25]. Во избежание ложноположительного результата исследования рекомендуется выполнение биопсии путем иссечения полнослойного лоскута шириной 1 см по задней стенке прямой кишки от зубчатой линии протяженностью не менее 6 см [15, 32].
Дополнительные методы диагностики проводятся с целью дифференциации с другими патологиями, в том числе с психосоматическими состояниями, которые характеризуются развитием обстипационного синдрома. Как правило, требуется участие сторонних специалистов в виде гастроэнтеролога, психотерапевта.
2.6 Диагностические критерии болезни Гиршпрунга у взрослых
- запор в анамнезе с детского возраста;
- наличие зоны относительного сужения в дистальных отделах толстой кишки с супрастенотическим расширением на ирригограммах;
- отсутствиеректоанального ингибиторного рефлекса при аноректальной манометрии;
- положительная реакция слизистой оболочки прямой кишки на ацетилхолинэстеразу.
При совокупности указанных признаков устанавливается диагноз болезнь Гиршпрунга.
В сомнительных случаях, при отсутствии характерного анамнеза, наличии нечеткой рентгенологической картины, ослабленной реакции внутреннего сфинктера на растяжение прямой кишки, слабоположительной реакции на ацетилхолинэстеразу или противоречиях в результатах указанных тестов, необходимо проводить трансанальную биопсию стенки прямой кишки по Свенсону в предложенной модификации для оценки состояния интрамурального нервного сплетения [25, 26, 23].
3. Лечение
3.1 Консервативное лечение
Консервативное лечение носит симптоматический характер (коррекция запоров, метаболических нарушений и т.д.), затягивание консервативной терапиинеизбежно приводит к прогрессированию мегаколон, ухудшению состояния и увеличению риска осложнений. Распространение мегаколон в проксимальном направлении может привести к необходимости более обширной резекции толстой кишки и ухудшению функциональных результатов лечения, а развитие осложнений может быть причиной многоэтапного хирургического вмешательства.
3.2 Хирургическое лечение
Задача лечения — нормализация пассажа кишечного содержимого по толстой кишке и беспрепятственная его эвакуация через анальный канал. Этой цели можно добиться с помощью исключения аганглионарной зоны из кишечного транзита и восстановления эвакуаторной способности лежащих выше отделов толстой кишки [1, 37, 18].
Успех хирургического лечения болезни Гиршпрунга у взрослых зависит от следующих обстоятельств:
- радикальность удаления аганглионарной зоны;
- объем резекции декомпенсированных отделов ободочной кишки;
- адекватная подготовка к операции.
3.2.1 Плановое хирургическое лечение.
- Для хирургического лечения болезни Гиршпрунга рекомендованы различные оперативные вмешательства:
- операция Соаве;
- операция Ребейна;
- операция Свенсона;
- операция Дюамеля.
Однако они применяются главным образом у детей, и их выполнение у взрослых пациентов значительно ухудшает функциональные результаты лечения [38, 39, 40].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
- В качестве метода хирургического лечения болезни Гиршпрунга у взрослых рекомендуется операция Дюамеля в модификации Государственного научного центра колопроктологии им. А.Н.Рыжих (ГНЦК) [25, 41, 9].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4).
Комментарий. Данное оперативное вмешательство преследует следующие цели:
- максимальное удаление аганглионарной зоны без излишней травматизации тазовых органов;
- исключение возможности повреждения внутреннего сфинктера;
- безопасность и асептичность формирования колоректального анастомоза;
- профилактика несостоятельности колоректального анастомоза;
- предотвращение формирования слепого мешка в культе прямой кишки;
- создание условий для хорошей функции анастомоза;
- уменьшение количества послеоперационных осложнений.
3.2.1.1 Операция Дюамеля в модификации Государственного научного центра колопроктологии им. А.Н. Рыжих.
Операцию Дюамеля в модификации ГНЦК проводят в два этапа.
- Первый этап. Резекция ободочной и прямой кишки с резекцией аганглионарной зоны и формирование колоректального конце-бокового ретроректального анастомоза с избытком по Дюамелю.
Задача интраоперационной ревизии состоит в определении проксимальной границы аганглионарной зоны, степени изменений лежащих выше отделов на уровне функционирующей части толстой кишки. Аганглионарная зона у взрослых по внешнему виду мало чем отличается от здоровой кишки. В ряде случаев удается визуализировать участок явного сужения, однако его можно принять и за участок спазма кишечной стенки.
Расширенная декомпенсированная часть толстой кишки при болезни Гиршпрунга имеет очень характерный внешний вид. Степень расширения может быть различной и по величине, и по протяженности, но всегда отмечается выраженная гипертрофия стенки с перестройкой наружного мышечного слоя. Этот отдел кишки обычно имеет серовато-белый цвет, наружный мышечный слой сплошным плотным футляром окружает кишечную стенку, которая в виде грубого полуспавшегося баллона занимает значительную часть брюшной полости. Гаустры в этом отделе кишки отсутствуют, кровеносные сосуды крупные, с множественными разветвлениями. Переходная зона от расширенной части к аганглионарной зоне определяется довольно четко — появляются хорошо выраженные тении и гаустры, а диаметр кишки приближается к нормальному.
Мобилизация начинается с расширенного участка, при этом обязательно пересекается краевой сосуд в самой дистальной части отдела, предполагаемого для низведения. Затем выполняется мобилизация аганглионарной зоны. Ее производят как можно ближе к стенке кишки для уменьшения травматизации тазовых нервных сплетений.
Мобилизацию низводимых отделов производят путем перевязки основных сосудов: сигмовидных — при низведении сигмовидной кишки, нижнебрыжеечной — при низведении левых отделов, нижнебрыжеечных и средних ободочных сосудов — при низведении правой половины ободочной кишки. Мобилизация прямой кишки производится циркулярно до уровня 7–8 см, а по задней стенке — до тазового дна. На высоте 7-8 см от края анального канала кишка пересекается. Низводимая кишка фиксируется к специальному проводнику, с его помощью выпячивают заднюю стенку прямой кишки сразу над верхним краем анального канала.
Промежностной бригадой после дивульсии ануса рассекают заднюю стенку прямой кишки на 1–2 см выше аноректальной линии над проводником. Через эту рану в подготовленный тоннель проводится низведенная кишка на проводнике. Перед этим накладывают провизорные швы, которыми затем сшивают низведенную кишку и прямую кишку по ранее намеченной линии анастомоза. Затем проводник снимают, а избыток низведенной кишки фиксируют к перианальной коже. Производится дренирование культи прямой кишки.
- Второй этап. Отсечение избытка низведенной кишки.
Операция проводится под эпидуральной анестезией. Производят циркулярное отсечение избытка низведенной кишки на уровне ранее наложенных узловых швов. Затем формируется анастомоз с помощью сшивания задней стенки прямой кишки с передней стенкой низведенной узловыми швами. Операция отсечения избытка низведенной кишки и формирование отсроченного колоректального анастомоза выполняются через 12–15 дней после проведения первого этапа операции.
3.2.1.2 Варианты выполнения операции Дюамеля в модификации Государственного Научного Центра Колопроктологии им. А.Н. Рыжих.
У ряда пациентов предпринимается многоэтапное плановое хирургическое лечение. Оно проводится в двух вариантах — с первичным или отсроченным удалением аганглионарной зоны.
1. Вариант
1.1.Резекция прямой и ободочной кишки по типу операции Гартмана;
1.2.Реконструктивно-восстановительное низведение ободочной кишки с формированием колоректальногоконцебоковогоретроректального анастомоза по Дюамелю;
1.3.Отсечение избытка низведенной кишки и формирование отсроченного колоректального анастомоза через 12–15 дней после операции.
2. Вариант.
2.1.Резекция ободочной кишки по типу операции Гартмана;
2.2.Ререзекция толстой кишки с зоной аганглиоза и формирование колоректальногоконцебоковогоретроректального анастомоза по Дюамелю;
2.3.Отсечение избытка низведенной кишки и формирование отсроченного колоректального анастомоза через 12–15 дней после операции.
- Вариант 2 рекомендован при тяжелом состоянии пациентов, когда нецелесообразно расширять объем резекции и удалять прямую кишку. […]
Уровень убедительности рекомендации С (уровень достоверности рекомендации — 4).
3.3Лечение осложнений.
К тяжелым осложнениям болезни Гиршпрунга, требующим выполнения ургентного хирургического вмешательства, относятся:
-
- Острая кишечная непроходимость;
- Перфорация кишки;
- Пролежень толстой кишки каловым камнем.
Экстренные и срочные операции, в зависимости от тяжести состояния пациентов, выраженности осложнений, могут быть произведены в нескольких вариантах:
-
- Резекция ободочной кишки по типу операции Гартмана (в зависимости от выраженности мегаколон выполняются резекция сигмовидной кишки, резекция левых отделов, левосторонняя гемиколэктомия);
- Резекция ободочной и прямой кишки с аганглионарной зоной по типу операции Гартмана;
- Колостомия, илеостомия.
В дальнейшем всем пациентам, перенесшим экстренные и срочные оперативные вмешательства по поводу осложнений болезни Гиршпрунга, проводится плановое хирургическое лечение по указанным выше принципам.
4. Реабилитация
- Специфических методов реабилитации пациентов с болезнью Гиршпрунга нет.
- Послеоперационных больных рекомендуется вести как общехирургических пациентов. […]
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 4)
- Если в процессе хирургического лечения была сформирована кишечная стома, то меры медицинской реабилитации рекомендованы направить на восстановление естественного пассажа кишечного содержимого по ЖКТ. При этом характер оперативного вмешательства и объем резекции толстой кишки определяются по изложенным выше принципам (см. п.п. 3.2.1.1 – 3.2.1.2). […]
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 4)
- Всем пациентам, которым в процессе хирургического лечения была сформирована кишечная стома рекомендуется консультация и наблюдение специалистом по реабилитации стомированных пациентов. […]
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 4)
5. Профилактика и диспансерное наблюдение
5.1 Диспансерное ведение
Цель мониторинга — оценка функциональных результатов лечения, а также выявление и коррекция поздних послеоперационных осложнений.
- Учитывая вероятность формирования стриктуры колоректального анастомоза в ранние сроки после операции, рекомендовано проводить осмотр пациентов еженедельно после выписки из стационара в течение 1 мес.
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 4)
- В дальнейшем рекомендовано больным обращаются для контрольного осмотра 1 раз в 3 мес. в течение 1 года.
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 4)
- Через 1 год после операции кроме клинического осмотра для определения функционального состояния толстой кишки и исключения рецидива мегаколон рекомендовано проведение рентгенологического исследования желудочно-кишечного тракта. Оно должно включать в себя:
- Ирригоскопия
- Проведение пассажа бария по ЖКТ
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 4)
- Кроме этого, при наличии признаков нарушения функции держания кишечного содержимого рекомендовано проводить физиологическое исследование ЗАПК.
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 4)
- При отсутствии поздних послеоперационных осложнений, требующих оперативной или консервативной коррекции, диспансерное наблюдение за пациентами рекомендовано осуществлять 1 раз в год в течение 3-х лет. В дальнейшем пациенты снимаются с диспансерного наблюдения, обращение к специалистам рекомендовано при появлении кишечной симптоматики.
Уровень убедительности рекомендации С (уровень достоверности рекомендации – 4)
6. Дополнительная информация, влияющая на течение и исход заболевания
Прогноз у взрослых пациентов, перенесших операцию Дюамеля в модификации ГНЦК по поводу болезни Гиршпрунга, является благоприятным при двух условиях:
- отсутствии поздних осложнений со стороны колоректального анастомоза;
- нормальной функции запирательного аппарата прямой кишки
Поздние стриктуры колоректального анастомоза могут привести к развитию мегаколон, поэтому необходимо проведение строгого мониторинга у оперированных больных.
6.1. Область применения рекомендаций
Клинические рекомендации предназначены, врачам-терапевтам, врачам общей практики (семейным врачам), гастроэнтерологам, колопроктологам, хирургам, эндоскопистам, организаторам здравоохранения, медицинским работникам со средним медицинским образованием, врачам-экспертам медицинских страховых организаций, в том числе при проведении медико-экономической экспертизы. Хирургическое лечение целесообразно проводить в условиях круглосуточного стационара, прежде всего, в колопроктологических отделениях, в исключительных случаях в отделениях общей хирургии (при наличии специализированных колопроктологических коек и специалиста, имеющего профессиональную переподготовку по специальности «колопроктология»). Для круглосуточного стационара необходимо применение КСГ 75 – операции на кишечнике и анальной области (уровень 3).
6.2. Ограничение применения рекомендаций.
Клинические рекомендации отражают мнение экспертов по наиболее спорным вопросам. В клинической практике могут возникать ситуации, выходящие за рамки представленных рекомендаций, поэтому окончательное решение о тактике ведения каждого пациента должен принимать лечащий врач, на котором лежит ответственность за его лечение.
Критерии оценки качества медицинской помощи
|
№ |
Критерии качества |
Уровень достоверности доказательств |
Уровень убедительности рекомендаций |
|
Событийные (смысловые, содержательные, процессные) критерии качества |
|||
|
1. |
Проведено ли рентгенологическое подтверждение наличия мегаколон? |
4 |
C |
|
2. |
Проводилось ли пальцевое исследование прямой кишки? |
4 |
C |
|
3. |
Проводилась ли дифференциальная диагностика с идиопатическим мегаколон в случае планового обследования? |
4 |
C |
|
Временные критерии качества |
|||
|
4. |
Сформулирован ли клинический диагноз в течение 3 суток с момента поступления? |
4 |
C |
|
5. |
Выполнялась ли обзорная рентгенография органов брюшной полости в случае кишечной непроходимости, обусловленной заворотом кишки или каловым камнем, в течение 2 часов с момента поступления? |
4 |
C |
|
Результативные критерии качества |
|||
|
6. |
На фоне лечения достигнуто клиническое улучшение на момент выписки из стационара? |
4 |
C |
|
Дополнительные критерии качества |
|||
|
7. |
Удовлетворен ли пациент результатами лечения? |
4 |
C |
Список литературы
- Воробьев Г.И. Мегаколон у взрослых (клиника, диагностика и хирургическое лечение): Дис. … д-ра мед наук. — М., 1982. — 402 с.
- Butler Tjaden N.E., Trainor P.A. The developmental etiology and pathogenesis of Hirschsprung disease // Transl. Res. — 2013, Mar 22. — doi: pii: S1931–5244. —Vol. 13. — Р. 71–76.
- Borrego S., Ruiz-Ferrer M., Fern?ndez R.M., Antinolo G. Hirschsprung’s disease as a model of complex genetic etiology // Histol. Histopathol. — 2013. —Vol. 28. — P. 1117–1136.
- Sarsu S.B., Karakus S.C., Erdem A.U. Colon perforation caused by a foreign body in Hirschsprung disease // J. Pediatr. Surg. — 2012. — Vol. 47, N 10. — P. 15–17.
- Swenson O. Hirschsprung’s disease: a review // Pediatrics. — 2002. — Vol. 109, N 5. — P. 914 — 918.
- Aminoso C., Garc?a-Mina?r S., Mart?nez L. et al. Recurrence of Hirschsprung disease due to maternal mosaicism of a novel RET gene mutation // Clin. Genet. —2013, May. — Vol. 13. — doi: 10.1111/cge.12163.
- Lake J.I., Heuckeroth R.O. Enteric Nervous System Development: Migration, Diff erentiation, and Disease // Am. J. Physiol. Gastrointest, Liver Physiol. —2013. — Vol. 305. — P. G1–G24.
- Langer J.C. Hirschsprung disease // Curr. Opin. Pediatr. — 2013. — Vol. 25, N 3. — P. 368–374.
- Воробьев Г.И., Жученко А.П., Ачкасов С.И., Бирюков О.М. Болезнь Гиршпрунга у взрослых: 25-летний опыт клиники. Актуальные вопросы колопроктологии. — Самара, 2003. — 414 с.
- Baranyay F., Bogar G., Sebestyen M. Adult Hirschsprung’s disease with mental retardation and microcephaly // Orv. Hetil. — 2000. — Vol. 141, N 30. — P. 1673–1676.
- Amiel J., Lyonnet S. Hirschsprung’s disease, associated syndromes, and genetics: a review // J. Med. Gen. — 2001. — Vol. 38. — Р. 729–739.
- Fouquet V., De Lagausie P., Faure C. et al. Do prognostic factors exist for total colonic aganglionosis with ileal involvement? // J. Pediatr. Surg. — 2002. — Vol. 37,N 1. — P. 71–75.
- Аруин Л.И., Капуллер Л.Л., Исаков В.А. Морфологическая диагностикаболезней желудка и кишечника. — М., 1998. — 483 с.
- Furness J.В., Costa M. Cytoarchitectonics of the enteric nervous system // The Enteric Nervous system. —N.Y.: Churchill Livingstone, 1987. — Р. 26, 54.
- Вавилова Т.И., Воробьев Г.И., Жученко А.П. Гистохимическая диагностика болезни Гиршпрунга // Хирургия. — 1986. — № 3. — 15–22 С.
- deArrudaLourencao P.L., Takegawa B.K., Ortolan E.V. et al. A useful panel for the diagnosis of Hirschsprung disease in rectal biopsies: calretininimmunostaining and acetylcholinesterasehistochesmistry // Ann. Diagn. Pathol. —2013, May 14. — Vol. 13. — Р. 26–29.
- Hanneman M.J., Sprangers M.A., Mik E.L., van Heurn L.W. Quality of life in patients with anorectal malformation or Hirschsprung’s disease // Dis. ColonRectum. — 2001, Nov. — P. 1650–1660.
- Yee L.M., Mulvihill S.J. Neuroendocrine disorders of the gut // West. J. Med. — 1995. — Vol. 163, N 5. — P. 454–462.
- Crocker N.L., Messmer J.M. Adult Hirschsprung’s disease // Clin. Radiol. —1991. — Vol. 44, N 4. — P. 257–259.
- Воробьев Г.И., Ачкасов С.И. Болезнь Гиршпрунга у взрослых. — М.:Литтерра, 2009. — С. 10–11.
- Gosemann J.H., Friedmacher F., Ure B., Lacher M. Open versus transanal pull-through for Hirschsprung disease: a systematic review of long-term outcome // Eur. J. Pediatr. Surg. — 2013. — Vol. 23, N 2. — P. 94–102.
- Jones O.M., Brading A.F., Mortensen N.J. Role of nitric oxide in anorectal function of normal and neuronal nitric oxide synthase knockout mice // Dis. Colon Rectum. — 2003. — Vol. 46, N 7. — P. 963–970.
- Weber T.R., Fortuna R.S., Silen M.L., Dillon P.A. Reoperation for Hirschsprung’s disease // Pediatr. Surg. — 1999. — Vol. 34, N 1. — P. 153, 156–157.
- WesterТ.,Hoehner J., Olsen L. Rehbein’s anterior resection in Hirschsprung’s disease, using a circular stapler // Eur. J. Pediatr. Surg. — 1995. — Vol. 5, N 6. —P. 358–362.
- Бирюков О.М. Клинико-морфологическая характеристика болезниГиршпрунга у взрослых: Дис. … канд. мед. наук. — М., 2006. — 191 с.
- Красовская Т.В., Вавилова Т.И., Кобзева Т.Н., Муратов И.Д. Диагностическая и лечебная тактика при острых формах болезни Гиршпрунга // Пробл. проктологии. — 1990. — Вып. 11. — С. 55–60.
- Wilkinson D., Kenny S. Anorectal function is not always normal after surgery in Hirschsprung’s disease // BMJ. — 2012. — Vol. 345. — Р. 81–92.
- Sharp N.E., Pettiford-Cunningham J., Shah S.R. et al. The prevalence of Hirschsprung disease in premature infants after suction rectal biopsy // J. Surg. Res. — 2013, Apr 19. — Р. 480–484.
- Chan G.L., Rand J.R. Nitric oxide and vasoactive intestinal polypeptide mediated non-adrenergic, non-cholinergic inhibitory transmission to smooth muscle of the rat gastric fundus // Eur. J. Pharmacol. — 1990. — Vol. 191. —P. 303–309.
- Moore B.G., Singaram C., Eckhoff D.E. et al. Immunohistochemical evaluations of ultrashort-segment Hirschsprung’s disease // Dis. Colon Rectum. —1996, July. — Vol. 39. — P. 817–822.
- Puff enberger E.G., Hosoda K., Washington S.S. et al. A missense mutation of the endothelin-B receptor gene in multigenicHirschsprung’s disease // Cell. — 1994. — Vol. 79. — Р. 1257–1266.
- Solomon R., AttieТ.,Pelet A. et. al. Germline mutations of the RET ligand GDNF are not sufficient to cause Hirschsprung’s disease // Nat. Genet. — 1996. —Vol. 14. — Р. 345–347.
- Ачкасов С.И. Аномалии развития и положения толстой кишки. Клиника, диагностика, лечение: Дис. д-ра мед. наук. — М., 2003. — 294 с.
- Bjornland K., Diseth Т.Н., Emblem R. Long-term functional, manometric, and endosonographic evaluation of patients operated upon with Duhamel technique // Pediatr. Surg. Int. — 1998. — Vol. 13, N 1. — P. 24–28.
- Загороднюк В.П. Исследование неадренергического торможения в гладких мышцах кишечника человека: Автореф. дис. … канд. мед наук. — Киев,1989. — 28 с.
- Emir H., Akman M., Sarimurat N. et al. Anorectalmanometry during the ineonatal period: its specifi city in the diagnosis of Hirschsprung‘s disease // Eur. J. Pediatr. Surg. — 1999. — Vol. 9. — Р. 101–103.
- Чепурной Г.И., Кивва А.Н. Сравнительная оценка различных способовоперативной коррекции болезни Гиршпрунга // Вестн. хир. — 2001. — № 4. —С. 62–65.
- Baillie C.T., Kenny S.E., Rintala R.J. et al. Long-term outcome and colonic motility after the Duhamel procedure for Hirschsprung’s disease // J. Pediatr. Surg. — 1999. — Vol. 34, N 2. — P. 325–329.
- Catto-Smitt A.G., Coffey C.M., Nolan T.M., Hutson J.M. Fecal incontinence after the surgical treatment of Hirschsprung’s disease // J. Pediatr. — 1995. — Vol. 127, N 6. — P. 954–957.
- WesterТ.,O’Briain D.S., Puri P. Notable postnatal alterations in the myenteric plexus of normal human bowel. — 1999. — Vol. 44. — Р. 666–674.
- Воробьев Г.И., Жученко А.П., Ефремов А.В. Поздние осложнения послеоперации Дюамеля по поводу болезни Гиршпрунга у взрослых // Пробл. проктологии. — 1991. — Вып. 12. — С. 58–62.
Приложение А1. Состав рабочей группы
-
Ачкасов Сергей Иванович – д.м.н., профессор. Ассоциация колопроктологов России.
-
Алешин Денис Викторович – к.м.н. Ассоциация колопроктологов России.
-
Бирюков Олег Михайлович к.м.н. Ассоциация колопроктологов России.
-
Васильев Сергей Васильевич – д.м.н., профессор. Ассоциация колопроктологов России.
-
Григорьев Евгений Георгиевич – д.м.н., профессор, член-корреспондент РАН. Ассоциация колопроктологов России.
-
Зароднюк Ирина Владимировна – д.м.н. Ассоциация колопроктологов России.
-
Капуллер Леонард Леонидович – д.м.н., профессор. Ассоциация колопроктологов России.
-
Кашников Владимир Николаевич – к.м.н. Ассоциация колопроктологов России.
-
Лахин Александр Владимирович — Ассоциация колопроктологов России.
-
Майновская Ольга Александровна – к.м.н. Ассоциация колопроктологов России.
-
Муравьев Александр Васильев – д.м.н., профессор. Ассоциация колопроктологов России.
-
Пак Владислав Евгеньевич – к.м.н., доцент. Ассоциация колопроктологов России.
-
Половинкин Вадим Владимирович – д.м.н. Ассоциация колопроктологов России.
-
Тибербулатов Виль Мамилович – д.м.н., профессор, член-корр. РАН. Ассоциация колопроктологов России.
-
Титов Александр Юрьевич – д.м.н. Ассоциация колопроктологов России.
-
Тотиков Валерий Зелимханович – д.м.н., профессор. Ассоциация колопроктологов России.
-
Фоменко Оксана Юрьевна – к.м.н. Ассоциация колопроктологов России.
-
Фролов Сергей Алексеевич – д.м.н. Ассоциация колопроктологов России.
-
Черкасов Михаил Федорович – д.м.н., профессор, Ассоциация колопроктологов России.
-
Шелыгин Юрий Анатольевич – д.м.н., профессор. Ассоциация колопроктологов России.
Конфликт интересов: отсутствует.
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория клинических рекомендаций:
- Врачи-колопроктологи.
- Врачи-гастроэнтерологи.
- Врачи-хирурги.
- Студенты медицинских ВУЗов, ординаторы, аспиранты.
В данных клинических рекомендациях все сведения ранжированы по уровню достоверности (доказательности) в зависимости от количества и качества исследований по данной проблеме.
Таблица 1.Уровни достоверности доказательности.
|
Уровень достоверности |
Тип данных |
|
1а |
Мета анализрандомизированных контролируемых исследований (РКИ) |
|
1b |
Хотя бы одно РКИ |
|
2а |
Хотя бы одно хорошо выполненное контролируемое исследование без рандомизации |
|
2b |
Хотя бы одно хорошо выполненное квазиэкспериментальное исследование |
|
3 |
Хорошо выполненные не экспериментальные исследования: сравнительные, корреляционные или «случай-контроль» |
|
4 |
Экспертное консенсусное мнение либо клинический опыт признанного авторитета |
Таблица 2.Уровни убедительности рекомендаций.
|
Уровень убедительности |
Основание рекомендации |
|
А |
Основана на клинических исследованиях хорошего качества, по своей тематике непосредственно применимых к данной специфической рекомендации, включающих по меньшей мере одно РКИ |
|
В |
Основана на результатах клинических исследований хорошего дизайна, но без рандомизации |
|
С |
Составлена при отсутствии клинических исследований хорошего качества, непосредственно применимых к данной рекомендации |
Порядок обновления клинических рекомендаций
Клинические рекомендации обновляются каждые 3 года.
Приложение А3. Связанные документы
Данные клинические рекомендации разработаны с учётом следующих нормативно-правовых документов:
- Статья 76 Федерального Закона Российской Федерации от 21.11.2011 N 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации», в части разработки и утверждении медицинскими профессиональными некоммерческими организациями клинических рекомендаций (протоколов лечения) по вопросам оказания медицинской помощи;
- Приказ от 2 апреля 2010 г. N 206н «Об утверждении порядка оказания медицинской помощи населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля» Министерства здравоохранения и социального развития Российской Федерации;
- Федеральный Закон Российской Федерации от 29.11.2010 N 326-ФЗ (ред. от 03.07.2016) «Об обязательном медицинском страховании в Российской Федерации»;
- Приказ Минздрава России от 7 июля 2015 г. N 422ан «Об утверждении критериев оценки качества медицинской помощи»;
- ПриказМинистерства Здравоохранения и Социального развития Российской Федерации от 17 декабря 2015 г. № 1024н «О классификации и критериях, используемых при осуществлении медико-социальной экспертизы граждан федеральными государственными учреждениями медико-социальной экспертизы»;
- Федеральный Закон от 17.07.1990 178-ФЗ (в ред. Федеральных законов от 08.12.2010 №345 ФЗ, от 345-ФЗ, от 01.07.2011 № 169ФЗ, от 28.07.2012 № 133- ФЗ, от 25.12.2012 №258-ФЗ, от 07.05.2013 №99-ФЗ, от 07.05.2013 №104-ФЗ, от 02.07.2013 №185-ФЗ, от 25.11.2013 №317-ФЗ) «О государственной социальной помощи».
Приложение Б. Алгоритмы ведения пациента
Приложение В. Информация для пациентов
Болезнь Гиршпрунга (врожденный аганглиоз) – это аномалия развития толстой кишки, характеризующаяся отсутствием ганглиев подслизистого и межмышечного нервных сплетений на определенном участке кишечной стенки. Ганглий – форма организации собственного нервного аппарата всех внутренних органов. Он представляет собой скопление тел нервных клеток – нейронов, окруженных вспомогательными клетками – глией. Ганглии относятся к периферической нервной системе и участвуют в регуляции деятельности внутренних органов. Патогенез аганглиоза связан с нарушением миграции нейробластов из вагусного нервного гребешка в процессе эмбриогенеза. Поскольку прямая кишка заселяется нейробластами в последнюю очередь, зона аганглиоза практически всегда начинается в самом дистальном отделе прямой кишки. Чем раньше прекращается миграция, тем длиннее аганглионарный сегмент.
Вероятно, аганглионарный участок кишки не участвует в перистальтической активности и является таким образом зоной функционального препятствия для пассажа кишечного содержимого. В результате происходит хроническая задержка каловых масс в вышележащем отделе кишки, последний с течением времени расширяется и формируется мегаколон – основной клинический признак болезни Гиршпрунга.
Болезнь Гиршпрунга относительно редкое заболевание, частота его составляет от 1:30000 до 1:2000 к общему числу новорожденных. Мальчики болеют в 4-5 раз чаще девочек. В большинстве случаев яркая клиническая картина в виде отсутствия стула, резкого вздутия живота проявляется буквально с рождения. В силу этого большая часть больных подвергается хирургическому лечению уже в раннем детстве. Однако, у небольшого числа пациентов симптомы болезни могут быть значительно менее выраженными, и только декомпенсация функции кишки или развитие осложнений заставляет их обращаться к врачу уже во взрослом состоянии.
Основными клиническими проявлениями болезни Гиршпрунга являются упорные запоры, как правило, с раннего детства и постоянное вздутие живота, не зависящее от опорожнения кишечника. Постепенно запоры прогрессируют, в расширенных отделах ободочной кишки формируются каловые камни, которые могут привести к развитию кишечной непроходимости или даже перфорации кишки вследствие пролежня камнем, и, соответственно, необходимости экстренной операции.
Лечение болезни Гиршпрунга только хирургическое. Причем чем раньше выполнена операция, тем лучше ее функциональный результат. Отсрочка хирургического вмешательства приводит к прогрессированию мегаколон и увеличению риска осложнений. Операции все равно не избежать, но распространение мегаколон в проксимальном направлении приведет к необходимости более обширной резекции толстой кишки. А развитие осложнений будет причиной многоэтапного лечения с куда более высоким риском для здоровья и вероятностью формирования стомы, чаще временной, но иногда и постоянной. Своевременно же выполненная операция позволяет пациентам вести полноценную жизнь без каких-либо ограничений. Женщины после операции имеют большие шансы зачатия естественным путем и полноценного вынашивания беременности.
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ
БОЛЕЗНЬ ГИРШПРУНГА
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем: Q43.1
Год утверждения (частота пересмотра): 2022
Возрастная категория: Взрослые
Пересмотр не позднее: 2024
ID: 175
Разработчик клинической рекомендации
— Общероссийская общественная организация «Ассоциация колопроктологов России»
Одобрено Научно-практическим Советом Минздрава РФ
Список сокращений
АХЭ — ацетилхолинэстераза
БГ — болезнь Гиршпрунга
ЖКТ — желудочно-кишечный тракт
МКБ — международная классификация болезней
РАИР — ректоанальный ингибиторный рефлекс
РКИ — рандомизированное клиническое испытание
РФП — радиофармацевтический препарат
ТТГ — тиреотропный гормон
Термины и определения
Мегаколон — это расширение ободочной или всей толстой кишки.
Мегаректум — это расширение прямой кишки
1. Краткая информация по заболеванию или состоянию
(группы заболевании или состоянии)
1.1 Определение заболевания или состояния
(группы заболеваний или состояний)
БГ — это аномалия развития толстой кишки, характеризующаяся отсутствием ганглиев подслизистого и межмышечного нервных сплетений всей толстой кишки или ее части и приводящая к нарушению иннервации фрагмента кишки, что проявляется упорными запорами [1].
Синонимы: врожденный аганглиоз толстой кишки.
1.2 Этиология и патогенез заболевания или состояния
(группы заболеваний или состояний)
В основе развития БГ лежат различные эпигенетические механизмы, приводящие к нарушению колонизации кишечника энтеральными стволовыми клетками, происходящими из клеток нервного гребешка. Подобная неполноценная колонизация связана, в первую очередь, с нарушением пролиферации, выживания, миграции и дифференцировки энтеральных стволовых клеток в процессе развития энтеральной нервной системы [2, 3, 4, 5].
Основными генами, контролирующими указанные выше процессы, являются: RET (рецептор тирозинкиназы), GDNF (нейтрофический фактор глиальных клеток), ENDRB (ген рецептора эндотелина-B), EDN3 (эндотелин-3) [6, 7, 8].
Кроме этого, существует гипотеза, согласно которой аганглиоз развивается вследствие нарушения дифференцировки нервных клеток, уже достигших кишечной стенки. Влиять на созревание клеток могут различные факторы, такие, как гипоксия, воздействие химических агентов, повышенная радиация, вирусная инфекция [9, 10].
Накопление ацетилхолинэстеразы в слизистой оболочке наряду с отсутствием медиаторов, обеспечивающих тормозящий эффект в кишечной стенке, вызывает стойкий спазм, который служит патогенетическим признаком БГ [11, 12].
Аганглионарный участок кишки не участвует в перистальтической активности и является, таким образом, зоной функционального препятствия для пассажа кишечного содержимого. В результате происходит хроническая задержка каловых масс в вышележащем отделе кишки, последний с течением времени расширяется и формируется мегаколон — основной клинический признак БГ.
1.3 Эпидемиология заболевания или состояния
(группы заболеваний или состояний)
По данным разных авторов уровень заболеваемости БГ колеблется от 1:30 тыс. до 1:5000 к общему числу новорожденных [13, 14, 15].
Распространенность аганглиоза толстой кишки варьирует и среди различных этнических групп. Так, согласно данным Калифорнийской программы мониторинга врожденных дефектов за период с 1983 по 1997 год, частота БГ среди новорожденных азиатского происхождения составила 2,8:10000, среди новорожденных афроамериканцев — 2,1:10000, европеоидов — 1,5:10000 и 1:10000 у латиноамериканцев [16]. В Японии за последние 4 десятилетия БГ диагностируется примерно у 1 из 5000 новорожденных [17].
Существует разница в частоте различных форм заболевания в зависимости от протяженности зоны аганглиоза. Случаи с коротким сегментом встречаются гораздо чаще и составляют до 80% общего числа. Остальные 20% наблюдений приходятся на пациентов, у которых аганглионарный сегмент распространяется проксимальнее сигмовидной кишки [16].
БГ часто является семейным заболеванием. Риск возникновения этого заболевания у родственников значительно выше по сравнению с остальным населением. Из всех регистрируемых семейные случаи аганглиоза составляют 20% [18].
1.4 Особенности кодирования заболевания или состояния
(группы заболеваний или состояний) по Международной
статической классификации болезней и проблем,
связанных со здоровьем
Класс — Другие врожденные аномалии (пороки развития) органов пищеварения (Q43) [19]:
Q43.1 — Болезнь Гиршпрунга
1.5 Классификация заболевания или состояния
(группы заболеваний или состояний)
Классификация [18, 20, 21, 22].
Анатомические формы заболевания.
Выделяют следующие анатомические формы:
— Наданальная форма — зона аганглиоза локализуется в нижнеампулярном отделе прямой кишки;
— Ректальная форма — недоразвитие интрамурального нервного аппарата распространяется на всю прямую кишку;
— Ректосигмоидная форма — аганглиоз занимает всю прямую кишку и часть или всю сигмовидную кишку;
— Субтотальная форма — в аганглионарный сегмент включена поперечная ободочная кишка;
— Тотальная форма — поражение всей толстой кишки, выявляется расширение подвздошной кишки.
По локализации расширения кишечника.
— Мегаректум;
— Мегасигма;
— Левосторонний мегаколон;
— Субтотальный мегаколон;
— Тотальный мегаколон;
— Мегаилеум.
По степени компенсации.
— Компенсированное состояние кишки — на протяжении многих лет у больного отмечается редкий, но самостоятельный стул или имеются запоры от 3 до 7 дней, которые легко разрешаются с помощью слабительных средств и клизм;
— Субкомпенсированное состояние в отличие от предыдущего требует интенсивных мероприятий по опорожнению кишки. В таких случаях без применения слабительных средств и клизм самостоятельный стул может отсутствовать свыше 7 дней;
— Декомпенсированное состояние характеризуется отсутствием позыва на дефекацию и самостоятельного стула. У многих пациентов толстая кишка бывает заполнена плотным кишечным содержимым или каловыми камнями. Зачастую даже интенсивные мероприятия не позволяют адекватно опорожнить толстую кишку. В подобных случаях показано срочное хирургическое лечение.
По клиническому течению заболевания.
— Типичный («детский») вариант — интенсивный запор развивается достаточно быстро, практически отсутствует самостоятельный стул, быстро нарастают явления кишечной непроходимости;
— Пролонгированный вариант — медленное течение заболевания, когда с запором удается длительное время справляться с помощью консервативных мероприятий;
— Латентный вариант — впервые запор появляется после 14 лет, и, как правило, быстро развивается хроническая толстокишечная непроходимость. Появившийся запор нарастает, слабительные средства совершенно неэффективны, и для опорожнения кишки приходится прибегать к ежедневным клизмам.
1.6 Клиническая картина заболевания или состояния
(группы заболеваний или состояний)
При БГ у взрослых имеет место нарушение проходимости по аганглионарной зоне кишки, вследствие этого вышележащие отделы кишки постепенно расширяются и формируется мегаколон. Постепенно мегаколон прогрессирует в проксимальном направлении. При отсутствии лечения развиваются осложнения: острая кишечная непроходимость, перфорация кишки, пролежень стенки кишки каловым камнем, заворот мегаколона.
2. Диагностика заболевания или состояния
(группы заболеваний или состояний) медицинские показания
и противопоказания к применению методов диагностики
Критерии установки диагноза:
— запор в анамнезе с детского возраста;
— наличие зоны относительного сужения в дистальных отделах толстой кишки с супрастенотическим расширением (мегаколон) на ирригограммах;
— отсутствие ректоанального ингибиторного рефлекса при аноректальной манометрии;
В сомнительных случаях, при отсутствии характерного анамнеза, наличии нечеткой рентгенологической картины, ослабленной реакции внутреннего сфинктера на растяжение прямой кишки или противоречиях в результатах указанных тестов, необходимо проводить трансанальную биопсию стенки прямой кишки по Свенсону для оценки состояния интрамурального нервного сплетения.
2.1 Жалобы и анамнез
К основным клиническим симптомам БГ относят запор и вздутие живота, которые обычно возникают в раннем детстве. Однако клинические проявления могут иметь стертую картину у детей и развиться в зрелом возрасте. Главной причиной обращения в клинику является запор, который отмечают все пациенты. При этом у большинства больных наблюдается отсутствие самостоятельного стула. Этот симптом всегда сочетается с отсутствием позыва на дефекацию. У ряда пациентов может иметь место и позыв на дефекацию и самостоятельный стул, однако остается ощущение неполного опорожнения толстой кишки. Наличие самостоятельного стула у этих пациентов обусловлено сохранившейся пропульсивной способностью тех отделов толстой кишки, которые располагаются проксимальнее аганглионарной зоны [23, 24].
Вздутие живота регистрируется у половины пациентов. Этот симптом отмечается на фоне длительного отсутствия самостоятельного стула и исчезает после опорожнения толстой кишки. Боли в животе носят, как правило, приступообразный характер и возникают на высоте запора, который купируется применением очистительных клизм [25, 26].
Тошнота и рвота появляются, как правило, при декомпенсированном состоянии, сопровождаются болями в животе, длительным отсутствием самостоятельного стула. У ряда пациентов могут отмечаться слабость и недомогание как проявление общей интоксикации [27].
У взрослых пациентов практически не развиваются явления энтероколита, столь характерного для детей, страдающих БГ [18].
К более редким симптомам относятся тошнота и рвота. Как правило, они появляются при декомпенсированном состоянии, сопровождаются болями в животе, длительным отсутствием самостоятельного стула. У ряда пациентов могут отмечаться слабость и недомогание как проявление астенизации и интоксикации.
2.2 Физикальное обследование
— Рекомендуется общеклинический осмотр, включая наружный осмотр перианальной области, оценку анального рефлекса, вагинальное исследование у женщин, всем пациентам с подозрением на БГ [28].
Уровень убедительности рекомендаций C (уровень достоверности доказательств — 5).
Комментарий. Общеклинический осмотр необходимо выполнять у всех пациентов с подозрением на БГ, как с целью выявления характерных для БГ симптомов, так и для дифференциальной диагностики, оценки соматического статуса и сопутствующих заболеваний.
При объективном осмотре у многих пациентов отмечается развернутый реберный угол. На фоне вздутия, увеличения в размерах толстой кишки заметны асимметрия живота, увеличение его в размерах, с растянутой передней брюшной стенкой и видимой на глаз перистальтикой. В то же время при адекватно проводимых консервативных мероприятиях мегаколон развивается медленно, что позволяет сохранить нормальную форму живота [9, 29].
При компенсированном состоянии пальпация живота у пациентов с БГ может быть малоинформативной. При субкомпенсированном и декомпенсированном состояниях пальпаторно определяется раздутая газами или заполненная каловыми массами ободочная кишка, наиболее часто сигмовидная кишка. Она имеет форму баллонообразного цилиндра, располагающегося, как правило, в левой половине живота. В случае переполнения кишки содержимым на ней остаются пальцевые вдавления. У ряда пациентов могут пальпироваться каловые камни, которые в некоторых наблюдениях смещаются в просвете кишки [23, 24].
— Рекомендуется пальцевое исследование прямой кишки всем пациентам с подозрением на БГ [18, 25].
Уровень убедительности рекомендаций C (уровень достоверности доказательств — 5).
Комментарий. пальцевое исследование анального канала и прямой кишки проводится с целью оценки функционального состояния запирательного аппарата прямой кишки, наличия сопутствующих заболеваний анального канала и прямой кишки. У пациентов с наданальной формой заболевания пальцевое исследование позволяет выявить наличие каловых масс или копролитов в ампуле прямой кишки. В случае ректальной и более протяженной формы аганглиоза ампула прямой кишки, как правило, не содержит каловых масс.
2.3 Лабораторные диагностические исследования
Специфическая лабораторная диагностика БГ отсутствует [28]. Лабораторные диагностические исследования следует выполнять пациентам в ходе подготовки и планирования хирургического вмешательства для исключения сопутствующих заболеваний и состояний, а также при необходимости проведения дифференциальной диагностики.
Пациентам с мегаколоном и подозрением на вторичный характер мегаколона, обусловленный эндокринологическими расстройствами, рекомендуется исследование уровня ТТГ, общего кальция и калия в крови для уточнения этиологии заболевания [30].
Уровень убедительности рекомендаций — C (уровень достоверности доказательств — 5)
2.4 Инструментальные диагностические исследования
Рентгенологические методы исследования дают возможность оценить функциональное и морфологическое состояние толстой кишки, что существенно влияет на выбор дальнейшей диагностической и лечебной тактики [29, 32].
— Всем пациентам с БГ рекомендуется ирригоскопия для подтверждения наличия мегаколона, оценки его распространенности, выявления характерной для БГ рентгенологической картины [18, 36].
Уровень убедительности рекомендаций B (уровень достоверности доказательств — 3).
Комментарий. Основным методом диагностики мегаколона является рентгенологический — измерение ширины просвета кишки при тугом ее наполнении, обычно взвесью бария сульфата**, в условиях двойного контрастирования. Нормальные значения были получены в двух основных рентген-морфометрических исследованиях и оказались сопоставимы за исключением ширины прямой кишки [31, 33].
Таблица 1. Ширина просвета различных отделов толстой кишки в норме.
|
Отдел кишки (n = 160) |
Ширина просвета (см) |
|
|
Ачкасов С.И., 2003 (n = 160) |
Preston DM, Lennard-Jones JE, et al, 1985 (n = 50) |
|
|
Слепая |
4,0 — 9,0 |
— |
|
Восходящая |
2,5 — 9,0 |
5,0 — 9,3 |
|
Поперечная |
2,5 — 8,5 |
4,5 — 8,3 |
|
Нисходящая |
1,5 — 6,0 |
3,7 — 7,1 |
|
Сигмовидная |
1,5 — 6,0 |
3,3 — 6,3 |
|
Прямая |
4,5 — 8,5 |
2,2 — 6,5 |
Несоответствие в нормальных показателях диаметра прямой кишки между двумя исследованиями, вероятно, объясняется различиями в методике проведения теста. Косвенным подтверждением этого является тот факт, что верхний предел ширины прямой кишки у здоровых добровольцев по данным эвакуаторной проктографии составил 8,3 см [34].
Для БГ характерна резкая граница между расширенной ободочной кишкой и относительно суженным дистальным аганглионарным сегментом различной протяженности (чаще прямая кишка, возможно с частью сигмовидной) [18].
Эндоскопические методы исследования.
— Рекомендуется всем пациентам с подозрением на БГ ректороманоскопия для выявления характерного резкого перехода относительно суженного аганглионарного участка кишки в вышележащий расширенный [9, 18].
Уровень убедительности рекомендаций C (уровень достоверности доказательств — 5).
Комментарий. При подозрении на БГ это исследование проводится без специальной подготовки. При наличии аганглиоза выраженный спазм стенки дистального отдела толстой кишки не позволяет каловым массам проникать в суженный участок, что является патогномоничным признаком заболевания. Проксимальнее суженного участка обнаруживается расширенная часть кишки, содержащая каловые массы. В этом отделе определяются сглаженность и продольная направленность складок слизистой оболочки, иногда ее атрофия или гиперемия [9].
Физиологические методы исследования.
— Рекомендуется всем пациентам с подозрением на БГ аноректальная манометрия для определения ректоанального ингибиторного рефлекса [9, 22, 28, 36].
Уровень убедительности рекомендаций B (уровень достоверности доказательств — 3).
Комментарий. У пациентов с подозрением на БГ важным диагностическим тестом является аноректальная манометрия, в частности, исследование ректоанального ингибиторного рефлекса (рефлекторного расслабления внутреннего сфинктера в ответ на повышение давления в прямой кишке). Отсутствие ректоанального ингибиторного рефлекса является надежным диагностическим критерием БГ с чувствительностью 91,6% [35].
2.5 Иные диагностические исследования
— Рекомендуется биопсия стенки прямой кишки по Свенсону пациентам с подозрением на БГ с целью дифференциальной диагностики с идиопатическим мегаколоном, когда имеются противоречия между данными аноректальной манометрии и рентгенологической картиной [22, 36].
Уровень убедительности рекомендаций B (уровень достоверности доказательств — 3).
Комментарий. Решающее значение в диагностике БГ имеет полнослойная биопсия стенки прямой кишки. Методика предложена O. Swenson (1955) и заключается в иссечении полнослойного фрагмента стенки прямой кишки на расстоянии 3 см от зубчатой линии с последующим исследованием этого участка на наличие интрамуральных ганглиев. Выявление аганглиоза межмышечного и подслизистого нервных сплетений является надежным подтверждением БГ. Следует помнить, что зона физиологического гипо- и аганглиоза может распространяться до 5 см проксимальнее зубчатой линии. Во избежание ложноположительного результата исследования рекомендуется выполнение биопсии путем иссечения полнослойного лоскута шириной 1 см по задней стенке прямой кишки от зубчатой линии протяженностью не менее 6 см [24].
3. Лечение, включая медикаментозную и немедикаментозную
терапии, диетотерапию, обезболивание, медицинские показания
и противопоказания к применению методов лечения
Радикальное лечение БГ как у взрослых, так и у детей в настоящее время рекомендовано только хирургическим путем. Отсрочка хирургического вмешательства неизбежно приводит к прогрессированию мегаколона, ухудшению состояния и увеличению риска осложнений. Распространение мегаколона в проксимальном направлении может привести к необходимости более обширной резекции толстой кишки и ухудшению функциональных результатов лечения. Развитие осложнений может быть причиной многоэтапного хирургического вмешательства [18].
3.1 Хирургическое лечение
Задача лечения — нормализация пассажа кишечного содержимого по толстой кишке и беспрепятственная его эвакуация через анальный канал. Этой цели можно добиться с помощью исключения аганглионарной зоны из кишечного транзита и восстановления эвакуаторной способности вышележащих отделов толстой кишки [29, 37].
— Рекомендуется резекция прямой и расширенных отделов ободочной кишок с формированием конце-бокового наданального анастомоза по Дюамелю в модификации Г.И. Воробьева при плановом хирургическом лечении взрослых пациентов с неосложненным течением БГ [18, 24, 36, 38].
Уровень убедительности рекомендаций B (уровень достоверности доказательств — 3).
Комментарий. Данное оперативное вмешательство преследует следующие цели:
— исключения аганглионарной зоны из кишечного транзита без излишней травматизации тазовых органов;
— исключение возможности повреждения внутреннего сфинктера;
— безопасность и асептичность формирования колоректального анастомоза;
— профилактика несостоятельности колоректального анастомоза;
— предотвращение формирования слепого мешка в культе прямой кишки;
— создание условий для хорошей функции анастомоза;
— уменьшение количества послеоперационных осложнений.
Операция производят в два этапа.
Первый этап. Резекция расширенной ободочной и прямой кишки с резекцией аганглионарной зоны и формированием колоректального конце-бокового ретроректального анастомоза с избытком по Дюамелю в модификации Г.И. Воробьева.
Вначале производят мобилизацию расширенных отделов ободочной кишки с пересечением магистральных сосудов (нижнебрыжеечных — при низведении левых отделов ободочной кишки, нижнебрыжеечных и средних ободочных сосудов — при низведении правой половины ободочной кишки). Расширенная декомпенсированная часть толстой кишки при БГ имеет очень характерный внешний вид. Степень расширения может быть различной и по величине, и по протяженности, но всегда отмечается выраженная гипертрофия стенки с перестройкой наружного мышечного слоя. Этот отдел кишки обычно имеет серовато-белый цвет, наружный мышечный слой сплошным плотным футляром окружает кишечную стенку, которая в виде грубого полуспавшегося баллона занимает значительную часть брюшной полости. Гаустры в этом отделе кишки отсутствуют, кровеносные сосуды крупные, с множественными разветвлениями. Проксимальную границу резекции определяют на уровне, где диаметр расширенной кишки приближается к нормальному. Затем выполняют мобилизацию аганглионарной зоны. Ее производят как можно ближе к стенке кишки для уменьшения травматизации тазовых нервных сплетений. При этом мобилизацию прямой кишки производят циркулярно до уровня 7 — 8 см от наружного края ануса, а по задней стенке в межфасциальном пространстве — до тазового дна. На высоте 7 — 8 см от края анального канала кишку пересекают. Низводимую кишку фиксируют к специальному проводнику, который проводят в ретроректальном тоннеле и с его помощью выпячивают заднюю стенку прямой кишки сразу над верхним краем анального канала.
Со стороны промежности после дивульсии ануса рассекают заднюю стенку прямой кишки на 1 — 2 см выше аноректальной линии над проводником. На верхнюю губу разреза накладывают 2 — 3 шва, которыми впоследствии заднюю стенку прямой кишки сшивают с передней стенкой низводимой кишки. Через разрез по ретроректальному тоннелю проводят низводимую кишку на проводнике. Затем проводник снимают, а избыток низведенной кишки фиксируют к перианальной коже. В просвет культи прямой кишки вводят газоотводную трубку.
Возможно выполнение операции лапароскопическим доступом. В таком случае проводник не используется, а низведение кишки осуществляют с помощью корнцанга, введенного со стороны промежности через наданальный разрез задней стенки прямой кишки.
Второй этап. Отсечение избытка низведенной кишки и окончательное формирование колоректального анастомоза.
Операцию проводят под эпидуральной анестезией. Производят циркулярное отсечение избытка низведенной кишки на уровне ранее наложенных узловых швов. Затем формируют анастомоз путем сшивания задней стенки прямой кишки с передней стенкой низведенной кишки узловыми швами. Операцию отсечения избытка низведенной кишки и формирования отсроченного колоректального анастомоза выполняются через 12 — 15 дней после первого этапа [18, 24].
— Рекомендуется многоэтапное хирургическое лечение в случае осложненного течения болезни Гиршпрунга [18, 24].
Уровень убедительности рекомендаций C (уровень достоверности доказательств — 5).
Комментарий: Показанием к многоэтапному хирургическому лечению служат ослабленное состояние пациента с выраженными метаболическими нарушениями, а также осложнения БГ, требующие выполнения ургентного вмешательства:
— острая кишечная непроходимость;
— перфорация кишки;
— пролежень толстой кишки каловым камнем;
— заворот мегаколона.
В таком случае первым этапом выполняют резекция расширенных отделов ободочной кишки по типу операции Гартмана. В зависимости от выраженности мегаколона выполняют резекция сигмовидной кишки, резекция левых отделов, левосторонняя гемиколэктомия). В последующем после нормализации состояния пациента (обычно через 6 — 12 месяцев) выполняется реконструктивно-восстановительное низведение ободочной кишки с формированием колоректального концебокового ретроректального анастомоза по Дюамелю в модификации Г.И. Воробьева по описанной выше методике [18, 24].
4. Медицинская реабилитация, медицинские показания
и противопоказания к применению методов реабилитации
Специфических методов реабилитации пациентов с БГ не существует.
Если в процессе хирургического лечения была сформирована кишечная стома, то меры медицинской реабилитации целесообразно направить на восстановление естественного пассажа кишечного содержимого по ЖКТ. При этом характер оперативного вмешательства и объем резекции толстой кишки определяются по изложенным выше принципам (см. п.п. 3.1) [18, 24].
Общие принципы реабилитации после хирургического лечения:
1) Комплексная оценка исходного состояния пациента и формулировка программы реабилитации;
2) Мультидисциплинарный принцип организации реабилитационной помощи. Всем пациентам, которым в процессе хирургического лечения была сформирована кишечная стома, рекомендуется консультация и наблюдение специалистом по реабилитации стомированных пациентов.
5. Профилактика и диспансерное наблюдение,
медицинские показания и противопоказания к применению
методов профилактики
5.1 Профилактика
Специфичных профилактических мероприятий при БГ нет
5.2 Диспансерное ведение
— Учитывая вероятность формирования стриктуры колоректального анастомоза в ранние сроки после операции, рекомендуется проводить осмотр пациентов еженедельно после выписки из стационара в течение 1 месяца. В дальнейшем больным рекомендуется обращаться для контрольного осмотра 1 раз в 3 месяца в течение 1 года [18, 24, 39].
Уровень убедительности рекомендации C (уровень достоверности рекомендации — 5)
Комментарий: Цель мониторинга — оценка функциональных результатов лечения, а также выявление и коррекция поздних послеоперационных осложнений. Через 1 год после операции, кроме клинического осмотра для определения функционального состояния толстой кишки и исключения рецидива мегаколона, необходимо проведение рентгенологического исследования желудочно-кишечного тракта. Оно должно включать в себя ирригоскопию и проведение пассажа бария сульфата** по ЖКТ. Кроме этого, при наличии признаков нарушения функции держания кишечного содержимого может быть выполнено физиологическое исследование ЗАПК.
— При отсутствии поздних послеоперационных осложнений, требующих оперативной или консервативной коррекции, диспансерное наблюдение за пациентами рекомендуется осуществлять 1 раз в год в течение 3-х лет [18, 24, 40].
Уровень убедительности рекомендации C (уровень достоверности рекомендации — 5)
Комментарий: В дальнейшем пациенты снимаются с диспансерного наблюдения, обращение к специалистам рекомендовано при появлении кишечной симптоматики.
6. Организация оказания медицинской помощи
Плановое хирургическое лечение должно осуществляется в колопроктологических отделениях, где есть возможность проведения всего спектра необходимых диагностических исследований. Госпитализация пациентов может осуществляется как в плановом, так и в экстренном порядке. Показанием для плановой госпитализации служат невозможность проведения диагностических или лечебных манипуляций в амбулаторно-поликлинических условиях и необходимость проведения хирургического вмешательства.
Экстренная госпитализация может осуществляться как в колопроктологическое, так и хирургическое отделение. Показанием к экстренной госпитализации являются осложнения БГ:
— острая кишечная непроходимость,
— перфорация кишки,
— пролежень толстой кишки каловым камнем,
— заворот мегаколона.
Показания к выписке пациента:
— неосложненное течение раннего послеоперационного периода;
— контролируемый болевой синдром с возможностью его купирования пероральными препаратами в амбулаторных условиях;
— возможность пациента (для пациентов с ограниченными возможностями) самостоятельно продолжить курс консервативной терапии в амбулаторных условиях под наблюдением регионарного врача-колопроктолога.
7. Дополнительная информация (в том числе факторы, влияющие
на исход заболевания или состояния)
Прогноз у взрослых пациентов, перенесших операцию Дюамеля в модификации Г.И. Воробьева по поводу БГ, является благоприятным при двух условиях:
— отсутствии поздних осложнений со стороны колоректального анастомоза;
— нормальной функции запирательного аппарата прямой кишки.
Поздние стриктуры колоректального анастомоза могут привести к развитию мегаколона, поэтому необходимо проведение строгого мониторинга у оперированных больных [9, 24].
Критерии оценки качества медицинской помощи
|
N |
Критерии качества |
Уровень достоверности доказательств |
Уровень убедительности рекомендаций |
|
1 |
Выполнено рентгенологическое подтверждение наличия мегаколона |
4 |
C |
|
2 |
Выполнено пальцевое исследование прямой кишки |
4 |
C |
|
3 |
Проведена дифференциальная диагностика с идиопатическим мегаколоном в случае планового обследования |
4 |
C |
|
4 |
Выполнена аноректальнакя манометрия |
3 |
C |
Список литературы
1. Kaiser G. Disorders and congenital malformations associated with Hirschsprung»s disease. Hirschsprung»s disease. 1982: 49 — 53.
2. Torroglosa A., Villalba-Benito L., Luzon-Toro B. et al. Epigenetic mechanisms in hirschsprung disease. International Journal of Molecular Sciences. 2019; 20(13): 3123.
3. Aminoso C., Garda-Minaur S., Martmez L. et al. Recurrence of Hirschsprung disease due to maternal mosaicism of a novel RET gene mutation. Clinical genetics. 2014; 85(4): 401.
4. Lake J.I., Heuckeroth R.O. Enteric Nervous System Development: Migration, Differentiation, and Disease. American Journal of Physiology-Gastrointestinal and Liver Physiology. 2013; 305: 1 — 24.
5. Langer J.C. Hirschsprung disease. Curr. Opin. Pediatr. 2013; 25(3): 368 — 374.
6. Borrego S., Ruiz-Ferrer M., Fernandez R.M. et al. Hirschsprung»s disease as a model of complex genetic etiology. Histol. Histopathol. 2013; 28: 1117 — 1136.
7. Sarsu S.B., Karakus S.C., Erdem A.U. Colon perforation caused by a foreign body in Hirschsprung disease. J. Pediatr. Surg. 2012; 47(10): 15 — 17.
8. Swenson O. Hirschsprung»s disease: a review. Pediatrics. 2002; 109(5): 914 — 918.
9. Воробьев Г.И., Жученко А.П., Ачкасов С.И. и соав. Болезнь Гиршпрунга у взрослых: 25-летний опыт клиники. Актуальные вопросы колопроктологии. 2003: 414.
10. Baranyay F., Bogar G., Sebestyen M. Adult Hirschsprung»s disease with mental retardation and microcephaly. Orv. Hetil. 2000; 141(30): 1673 — 1676.
11. Вавилова Т.И., Воробьев Г.И., Жученко А.П. Гистохимическая диагностика болезни Гиршпрунга. Хирургия. 1986; 3: 15 — 22.
12. De Arruda Lourencao P.L., Takegawa B.K., Ortolan E.V. et al. A useful panel for the diagnosis of Hirschsprung disease in rectal biopsies: calretininimmunostaining and acetylcholinesterasehistochesmistry. Annals of diagnostic pathology. 2013; 17(4): 352 — 356.
13. Hanneman M.J., Sprangers M.A., Mik E.L. et al. Quality of life in patients with anorectal malformation or Hirschsprung»s disease. Diseases of the colon & rectum. 2001; 44(11): 1650 — 1660.
14. Bodian M., Carter C. A family study of Hirschsprung.disease. Annals of Human Genetics. 1963; 26(3): 261 — 277.
15. Crocker N.L., Messmer J.M. Adult Hirschsprung»s disease. Clin. Radiol. 1991; 44(4): 257 — 259.
16. Haricharan R.N., Georgeson K.E. Hirschsprung disease. Semin. Pediatr. Surg. 2008; 17(4): 266 — 275.
17. Taguchi T., Obata S., leiri S. Current status of Hirschsprung»s disease: based on a nationwide survey of Japan. Pediatr. Surg. Int. 2017; 33(4): 497 — 504.
18. Воробьев Г.И., Ачкасов С.И. Болезнь Гиршпрунга у взрослых. Литтерра, 2009.
19. Международная классификация болезней 10-го пересмотра. МКБ-10. Доступен с: www.10mkb.ru.
20. Szylberg L., Marszalek A. Diagnosis of Hirschsprung»s disease with particular emphasis on histopathology. A systematic review of current literature. Przeglad gastroenterologiczny. 2014; 9(5): 264 — 269.
21. Ленюшкин А.И. Детская колопроктология. Медицина, 1990.
22. Friedmacher F., Puri P. Classification and diagnostic criteria of variants of Hirschsprung»s disease. Pediatric surgery international. 2013; 29(9): 855 — 872.
23. Weber T.R., Fortuna R.S., Silen M.L. et al. Reoperation for Hirschsprung»s disease. Pediatr. Surg. 1999; 34(1): 156 — 157.
24. Бирюков О.М. Клинико-морфологическая характеристика болезни Гиршпрунга у взрослых. дис. — Государственный научный центр колопроктологии им. А.Н. Рыжих. М.: 2006.
25. Красовская Т.В., Вавилова Т.И., Кобзева Т.Н. и соав. Диагностическая и лечебная тактика при острых формах болезни Гиршпрунга. Пробл. проктологии. 1990; 11: 55 — 60.
26. Wilkinson D., Kenny S. Anorectal function is not always normal after surgery in Hirschsprung»s disease. BMJ. 2012; 345: 81 — 92.
27. Sharp N.E., Pettiford-Cunningham J., Shah S.R. et al. The prevalence of Hirschsprung disease in premature infants after suction rectal biopsy. J. Surg. Res. 2013; 184(1): 374 — 377.
28. Шелыгин Ю.А., Благодарный Л.А. Справочник колопроктолога. Литтера, 2012.
29. Воробьев Г.И. Мегаколон у взрослых (клиника, диагностика и хирургическое лечение). дис. — Государственный научный центр колопроктологии им. А.Н. Рыжих. М.: 1982.
30. Bharucha AE, Philips SF. Slow-transit Constipation. Curr Treat Options Gastroenterol. 2001 Aug; 4(4): 309 — 315. doi: 10.1007/s11938-001-0056-9. PMID: 11469989
31. Ачкасов С.И. Аномалии развития и положения толстой кишки. Клиника, диагностика, лечение. дис. — Государственный научный центр колопроктологии им. А.Н. Рыжих. М.: 2003.
32. Bjornland K., Diseth T.H., Emblem R. Long-term functional, manometric, and endosonographic evaluation of patients operated upon with Duhamel technique. Pediatr. Surg. Int. 1998; 13(1): 24 — 28.
33. Preston D.M., Lennard-Jones J.E., Thomas B.M. Towards a radiologic definition of idiopathic megacolon. Gastrointest Radiol, 1985; 10: 167 — 9.
34. Gladman M.A., Dvorkin L.S., Scott S.M. et al. A novel technique to identify patients with megarectum. Dis Colon Rectum. 2007; 50: 621 — 9.
35. Emir H., Akman M., Sarimurat N. et al. Anorectal manometry during the neonatal period: its specificity in the diagnosis of Hirschsprung’s disease. European journal of pediatric surgery. 1999; 9(2): 101 — 103.
36. Doodnath R., Puri P. A systematic review and meta-analysis of Hirschsprung»s disease presenting after childhood. Pediatr Surg Int. 2010; 26(11): 1107 — 1110.
37. Чепурной Г.И., Кивва А.Н. Сравнительная оценка различных способов оперативной коррекции болезни Гиршпрунга. Вестн. хир. 2001; 4: 62 — 65.
38. Воробьев Г.И., Жученко А.П., Ефремов А.В. Поздние осложнения после операции Дюамеля по поводу болезни Гиршпрунга у взрослых. Пробл. проктологии. 1991; 12: 58 — 62.
39. Catto-Smitt A.G., Coffey C.M., Nolan T.M. et al. Fecal incontinence after the surgical treatment of Hirschsprung»s disease. J. Pediatr. 1995; 127(6): 954 — 957.
40. Baillie C.T., Kenny S.E., Rintala R.J. et al. Long-term outcome and colonic motility after the Duhamel procedure for Hirschsprung»s disease. J. Pediatr. Surg. 1999; 34(2): 325 — 329.
Приложение А1
СОСТАВ
РАБОЧЕЙ ГРУППЫ ПО РАЗРАБОТКЕ И ПЕРЕСМОТРУ
КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
|
N |
Ф.И.О. |
Ученая степень |
Ученое звание |
Профессиональная ассоциация |
|
1. |
Ачкасов Сергей Иванович |
Д.м.н. |
Профессор |
Ассоциация колопроктологов России |
|
2. |
Алешин Денис Викторович |
К.м.н. |
— |
Ассоциация колопроктологов России |
|
3. |
Зароднюк Ирина Владимировна |
Д.м.н. |
— |
Российское общество хирургов |
|
4. |
Кашников Владимир Николаевич |
Д.м.н. |
— |
Ассоциация колопроктологов России |
|
5. |
Москалев Алексей Игоревич |
К.м.н. |
— |
Ассоциация колопроктологов России |
|
6. |
Сушков Олег Иванович |
Д.м.н. |
— |
Ассоциация колопроктологов России |
|
7. |
Фоменко Оксана Юрьевна |
Д.м.н. |
— |
Ассоциация колопроктологов России |
|
8. |
Фролов Сергей Алексеевич |
Д.м.н. |
— |
Ассоциация колопроктологов России |
|
9. |
Шелыгин Юрий Анатольевич |
Д.м.н. |
Профессор, акад. РАН |
Ассоциация колопроктологов России |
Конфликт интересов: отсутствует.
Приложение А2
МЕТОДОЛОГИЯ РАЗРАБОТКИ КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙ
Целевая аудитория клинических рекомендаций:
1. Врачи-колопроктологи
2. Врачи-хирурги
3. Врачи-гастроэнтерологи
4. Врачи-терапевты
5. Врачи общей практики (семейные врачи)
6. Врачи-эндоскописты
7. Средний медицинский персонал
8. Студенты медицинских вузов, ординаторы, аспиранты.
Таблица 1. Шкала оценки УДД (уровней достоверности доказательств) для методов диагностики (диагностических вмешательств)
|
УДД |
Расшифровка |
|
1 |
Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением метаанализа |
|
2 |
Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением метаанализа |
|
3 |
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования |
|
4 |
Несравнительные исследования, описание клинического случая |
|
5 |
Имеется лишь обоснование механизма действия или мнение экспертов |
Таблица 2. Шкала оценки УДД для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
|
УДД |
Расшифровка |
|
1 |
Систематический обзор РКИ (рандомизированные клинические испытания) с применением метаанализа |
|
2 |
Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением метаанализа |
|
3 |
Нерандомизированные сравнительные исследования, в т.ч. когортные исследования |
|
4 |
Несравнительные исследования, описание клинического случая или серии случаев, исследования «случай-контроль» |
|
5 |
Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов |
Таблица 3. Шкала оценки УУР (уровней убедительности рекомендаций) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
|
УУР |
Расшифровка |
|
A |
Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными) |
|
B |
Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными) |
|
C |
Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными) |
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию — не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утвержденным КР (клинические рекомендации), но не чаще 1 раза в 6 месяцев.
Приложение А3
СПРАВОЧНЫЕ МАТЕРИАЛЫ,
ВКЛЮЧАЯ СООТВЕТСТВИЕ ПОКАЗАНИЙ К ПРИМЕНЕНИЮ
И ПРОТИВОПОКАЗАНИЙ, СПОСОБОВ ПРИМЕНЕНИЯ И ДОЗ ЛЕКАРСТВЕННЫХ
ПРЕПАРАТОВ, ИНСТРУКЦИИ ПО ПРИМЕНЕНИЮ
ЛЕКАРСТВЕННОГО ПРЕПАРАТА
Данные клинические рекомендации разработаны с учетом следующих нормативно-правовых документов:
1. Статья 76 Федерального Закона Российской Федерации от 21.11.2011 N 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации», в части разработки и утверждении медицинскими профессиональными некоммерческими организациями клинических рекомендаций (протоколов лечения) по вопросам оказания медицинской помощи;
2. Приказ от 2 апреля 2010 г. N 206н «Об утверждении порядка оказания медицинской помощи населению с заболеваниями толстой кишки, анального канала и промежности колопроктологического профиля» Министерства здравоохранения и социального развития Российской Федерации;
3. Федеральный Закон Российской Федерации от 29.11.2010 N 326-ФЗ (ред. от 03.07.2016) «Об обязательном медицинском страховании в Российской Федерации»;
4. Приказ Минздрава России от 10 мая 2017 г. N 203н «Об утверждении критериев оценки качества медицинской помощи»;
Приложение Б
АЛГОРИТМЫ ДЕЙСТВИЙ ВРАЧА
Алгоритм ведения пациента с болезнью Гиршпрунга
Приложение В
ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТА
Информация о заболевании. Болезнь Гиршпрунга (врожденный аганглиоз) — это аномалия развития толстой кишки, характеризующаяся отсутствием ганглиев подслизистого и межмышечного нервных сплетений на определенном участке кишечной стенки [18]. Ганглий — форма организации собственного нервного аппарата всех внутренних органов. Он представляет собой скопление тел нервных клеток — нейронов, окруженных вспомогательными клетками — глией. Ганглии относятся к периферической нервной системе и участвуют в регуляции деятельности внутренних органов. Патогенез аганглиоза связан с нарушением миграции нейробластов из вагусного нервного гребешка в процессе эмбриогенеза. Поскольку прямая кишка заселяется нейробластами в последнюю очередь, то зона аганглиоза практически всегда начинается в самом дистальном отделе прямой кишки. Чем раньше прекращается миграция, тем длиннее аганглионарный сегмент [4, 5].
Вероятно, аганглионарный участок кишки не участвует в перистальтической активности и является, таким образом, зоной функционального препятствия для пассажа кишечного содержимого [16]. В результате происходит хроническая задержка каловых масс в вышележащем отделе кишки, последний с течением времени расширяется и формируется мегаколон — основной клинический признак болезни Гиршпрунга [18].
Болезнь Гиршпрунга относительно редкое заболевание, частота его составляет от 1:30000 до 1:5000 к общему числу новорожденных [13, 14]. Мальчики болеют в 4 — 5 раз чаще девочек [15]. В большинстве случаев яркая клиническая картина в виде отсутствия стула, резкого вздутия живота проявляется буквально с рождения. В силу этого большая часть больных подвергается хирургическому лечению уже в раннем детстве. Однако у небольшого числа пациентов симптомы болезни могут быть значительно менее выраженными, и только декомпенсация функции кишки или развитие осложнений заставляет их обращаться к врачу уже во взрослом состоянии.
Основными клиническими проявлениями болезни Гиршпрунга являются упорные запоры, как правило, с раннего детства и постоянное вздутие живота, не зависящее от опорожнения кишечника. Постепенно запоры прогрессируют, в расширенных отделах ободочной кишки формируются каловые камни, которые могут привести к развитию кишечной непроходимости или даже перфорации кишки вследствие пролежня камнем, и, соответственно, необходимости экстренной операции [18].
Лечение болезни Гиршпрунга только хирургическое. Причем чем раньше выполнена операция, тем лучше ее функциональный результат. Отсрочка хирургического вмешательства приводит к прогрессированию мегаколона и увеличению риска осложнений [24]. Операции все равно не избежать, но распространение мегаколона в проксимальном направлении приведет к необходимости более обширной резекции толстой кишки. А развитие осложнений будет причиной многоэтапного лечения с куда более высоким риском для здоровья и вероятностью формирования стомы, чаще временной, но иногда и постоянной. Своевременно же выполненная операция позволяет пациентам вести полноценную жизнь без каких-либо ограничений.
Женщины после операции имеют большие шансы зачатия естественным путем и полноценного вынашивания беременности.
Приложение Г1 — ГN
ШКАЛЫ ОЦЕНКИ,
ВОПРОСНИКИ И ДРУГИЕ ОЦЕНОЧНЫЕ ИНСТРУМЕНТЫ СОСТОЯНИЯ
ПАЦИЕНТА, ПРИВЕДЕННЫЕ В КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЯХ
Отсутствуют.
Болезнь Гиршпрунга: причины появления, симптомы, диагностика и способы лечения.
Определение
Болезнь Гиршпрунга (аганглиоз толстой кишки, врожденный мегаколон) – это врожденное отсутствие или значительное уменьшение нервных сплетений кишечной стенки всей толстой кишки или ее части, что проявляется упорными запорами.
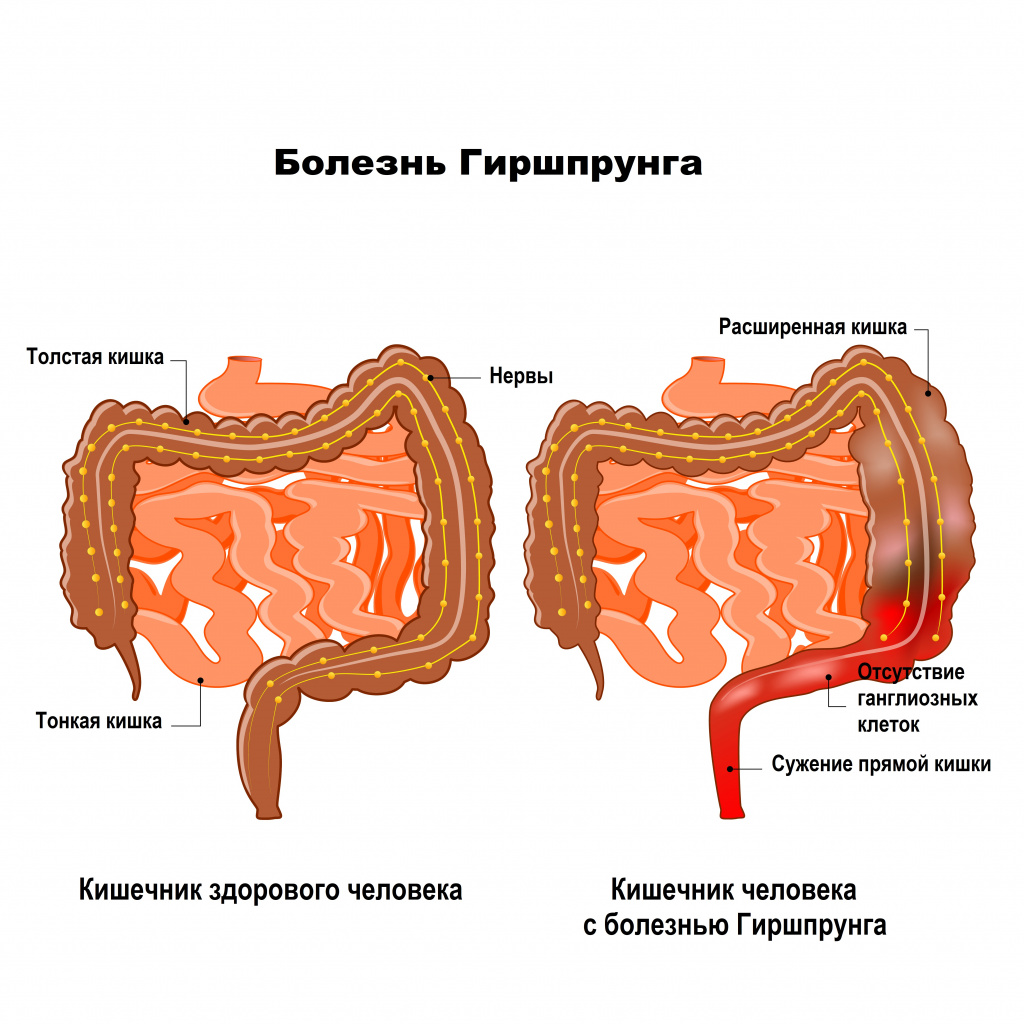
Частота болезни Гиршпрунга составляет примерно 1 на 5000 рождений.
Причины появления болезни Гиршпрунга
В настоящее время болезнь Гиршпрунга считается полиэтиологичной патологией.
Болезнь Гиршпрунга часто является семейным заболеванием. Риск его возникновения у родственников значительно выше по сравнению с остальным населением – семейные случаи болезни Гиршпрунга составляют порядка 20%.
Доказан генетический гетерогенный характер аномалии – исследователи выявили мутацию в 10 различных генах, способствующих развитию болезни Гиршпрунга.
Существует основная теория, объясняющая отсутствие нервных сплетений в кишечной стенке. Заболевание является следствием нарушения миграции в процессе эмбриогенеза (физиологического процесса, в ходе которого происходит образование и развитие эмбриона) нервных клеток. Чем раньше прекращается миграция, тем длиннее участок кишки, лишенный нервных сплетений.
Еще одна гипотеза, согласно которой аганглиоз толстой кишки развивается вследствие нарушения дифференцировки нервных клеток, уже достигших кишечной стенки. Влиять на созревание клеток могут различные факторы, такие как гипоксия, воздействие химических агентов, повышенная радиация, вирусная инфекция и пр.
Из-за отсутствия иннервации сегмент толстой кишки не способен к перистальтике, волнообразному сокращению стенок, что становится функциональным препятствием для продвижения каловых масс по кишечнику. Эта постоянная задержка приводит к запорам и расширению вышележащего отдела кишечника.
Классификация заболевания
Классификация болезни Гиршпрунга основывается на анатомической локализации аганглиоза, распространенности патологии и выраженности клинических проявлений заболевания.
- Наданальная форма – зона поражения локализуется в нижнеампулярном отделе прямой кишки.
- Ректальная форма – недоразвитие нервного аппарата распространяется на всю прямую кишку.
- Ректосигмоидная форма – аганглиоз занимает всю прямую и часть или всю сигмовидную кишку.
- Субтотальная форма – в аганглионарный сегмент включена поперечная ободочная кишка.
- Тотальная форма – поражение всего толстого кишечника.
При тотальной форме аганглиоза выявляется расширение подвздошной кишки. Определяется следующая локализация расширения кишечника:
- мегаректум;
- мегасигма;
- левосторонний мегаколон (левостороннее расширение толстой кишки);
- субтотальный мегаколон;
- тотальный мегаколон;
- мегаилеум.
Функциональное состояние расширенной толстой кишки может быть компенсированным, субкомпенсированным и декомпенсированным.
По клиническому течению у взрослых различают три варианта развития заболевания:
- Типичный детский вариант болезни – самый частый, выявляется почти у 90% больных. Характеризуется быстрым развитием сильных запоров, поэтому самостоятельное опорожнение кишечника практически отсутствует.
Наступает кишечная непроходимость – состояние, при котором нарушается прохождение пищевых масс по кишечнику и требуется неотложное хирургическое вмешательство.
- Пролонгированный вариант – заболевание протекает медленно, что связано с небольшим участком денервации кишки. С запорами длительное время справляются консервативными методами.
- Запоры впервые появляются в подростковом возрасте (при этом развивается хроническая толстокишечная непроходимость) и постоянно нарастают. Слабительные средства не оказывают нужного эффекта, больному требуются ежедневные клизмы.
Симптомы болезни Гиршпрунга
Как правило, симптомы болезни Гиршпрунга проявляются вскоре после рождения, однако у некоторых больных детей могут иметь стертую картину и стать выраженными лишь спустя несколько лет или в зрелом возрасте.
Главным симптомом являются запоры, которые сочетаются с отсутствием позыва к дефекации (дефекация – это физиологический процесс выделения каловых масс из прямой кишки, являющейся конечным отделом толстого кишечника).
У некоторых пациентов позыв к дефекации и самостоятельный стул могут сохраняться, но присутствует ощущение неполного опорожнения толстой кишки.
Вздутие живота беспокоит около половины пациентов. Этот симптом регистрируется на фоне длительного отсутствия самостоятельного стула и исчезает после опорожнения кишечника.
Боль в животе носит, как правило, приступообразный характер и возникает на фоне запоров. Они купируются применением очистительных клизм. Тошнота и рвота появляются уже в запущенных стадиях, сопровождаются болями в животе, длительным отсутствием самостоятельного стула. У ряда пациентов могут отмечаться слабость и недомогание как проявление общей интоксикации.
На фоне вздутия, увеличения в размерах толстой кишки отмечается асимметрия живота, растянутость передней брюшной стенкой.
Диагностика болезни Гиршпрунга
Врач может заподозрить болезнь Гиршпрунга у новорожденных с поздним отхождением стула, увеличением объема живота, рвотой с примесью желчи и нарушением энтерального питания. Наличие у новорожденного ребенка признаков энтероколита должно также вызывать подозрение на болезнь Гиршпрунга.
В диагностических целях проводят следующие исследования:
- ирригоскопия – один из методов рентгеноконтрастного исследования кишечника с введением через задний проход бариевой смеси – позволяет определить наличие зоны сужения кишки, протяженность, степень расширения кишки, локализацию здоровых отделов толстой кишки.
- обзорная рентгенография брюшной полости позволяет определить наличие признаков кишечной непроходимости, выявить каловые камни. На обзорной рентгенограмме у ребенка с болезнью Гиршпрунга можно обнаружить расширение толстой кишки над узким дистальным участком прямой и сигмовидной кишок и переходной зоной между ними. При выраженном энтероколите присутствуют признаки токсической дилатации (расширения) толстой кишки;
Ректосигмоскопия
Эндоскопическое исследование участка толстого кишечника, позволяющее получить информацию о его состоянии и обнаружить различные патологии.
Гистохимическое исследование биоптатов слизистой прямой кишки показывает присутствие ацетилхолин-позитивных гипертрофических нервных волокон, подтверждающих болезнь Гиршпрунга. Основные иммуногистохимические методы — прямая и непрямая иммунофлюоресценция или прямая и непрямая ферментная иммуногистохимическая реакция.
Рекомендуется общий анализ крови для оценки состояния организма. В случае осложненное течения заболевания определяется анемия, лейкоцитоз, повышение СОЭ и количества нейтрофилов.
В биохимическом анализе может наблюдаться гипоальбуминемия, дислипопротеинемия.
Альбумин (в крови) (Albumin)
Синонимы: Человеческий сывороточный альбумин; ЧСА; Альбумин плазмы;
Human Serum Albumin; ALB.
Краткая характеристика исследуемого вещества Альбумин
Альбумин – эт…
Дифференциальный диагноз нужно проводить с кишечной атрезией, мальротацией, заворотом, мекониальной непроходимостью при муковисцидозе, синдромом закупорки меконием, аноректальными мальформациями, синдромом Пайра, электролитными нарушениями.
К каким врачам обращаться
Диагностикой и лечением болезни Гиршпрунга занимаются
хирурги
. Однако первым заподозрить патологию может
врач-педиатр
.
Лечение болезни Гиршпрунга
Лечение болезнь Гиршпрунга у детей и взрослых только хирургическое.
Отсрочка операции приводит к прогрессированию заболевания, ухудшению самочувствия и развитию осложнений.
При проведении хирургического лечения учитывается возраст больного, протяженность пораженного сегмента кишечника, степень возникших нарушений.
Задача лечения — нормализовать пассаж (прохождение) кишечного содержимого по толстой кишке и беспрепятственная его эвакуация через прямую кишку. Этой цели можно добиться с помощью исключения пораженной зоны из кишечного транзита и восстановления эвакуаторной способности лежащих выше отделов толстой кишки.
Возможны два варианта хирургического вмешательства:
Одноэтапная операция показана при незначительной длине пораженного сегмента и компенсированной форме заболевания: удаляется пораженный сегмент и сразу же формируется анастомоз (соединение частей кишки).
Двухэтапная операция проводится в более сложных и запущенных случаях: на первом этапе иссекается участок пораженной кишки с формированием колостомы (из ободочной кишки искусственно формируют отверстие для выхода каловых масс). Второй этап – реконструктивная операция, в ходе которой колостома ушивается с формированием кишечного анастомоза.
При наличии энтероколита сначала проводят интенсивное лечение, включающее коррекцию водно-электролитного баланса и очистительные клизмы.
Экстренная операция проводится в случае развития острой кишечной непроходимости (неотложного состояния, вызванного нарушением пассажа (прохождения) каловых масс по кишечнику), развития перфорации кишечника каловыми камнями.
Диспансерное наблюдение прооперированных пациентов проводится еженедельно в течение месяца после операции, ежеквартально в течение года и ежегодно на протяжении трех лет.
Прогноз при заболевании относительно благоприятный при условии раннего выявления и проведение хирургической коррекции.
Осложнения
Истощение вплоть до кахексии (крайняя степень) связано с нарушением переваривания и всасывания пищи.
Отставание в росте и развитии у детей.
Анемия.
Нарушение кишечной микрофлоры и развитие дисбактериоза кишечника.
Кишечная непроходимость.
Перфорация (прободение) кишки.
Пролежни стенки кишки каловыми массами.
Развитие токсического мегаколона – острой формы растяжения толстой кишки, характеризующейся крайним расширением толстой кишкой и сопровождающейся вздутием живота, а иногда лихорадкой, болью в животе или шоком.
Постоперационные осложнения:
- перитонит, перианальная флегмона или формирование параректального свища;
- энтероколит — главная причина увеличения заболеваемости и смертности у детей после радикального лечения болезни Гиршпрунга.
- рубцовый стеноз;
- частый стул (5-10 раз в день) сразу после операции.
Профилактика болезни Гиршпрунга
Специфические меры профилактики не разработаны. При появлении первых признаков заболевания рекомендовано незамедлительно обратиться к врачу для диагностики и лечения.
Источники:
- Клинические рекомендации «Болезнь Гиршпрунга». Разраб.: Ассоциация колопроктологов России. – 2022.
- Морозов Д. А., Пименова Е. С. Диагностика и лечение болезни Гиршпрунга у детей в Российской Федерации (подготовка проекта Федеральных клинических рекомендаций) // Российский вестник детской хирургии, анестезиологии и реаниматологии. – 2018;8 (1): 6-12.
- Разумовский А.Ю. Болезнь Гиршпрунга у детей: руководство для врачей / под ред. А.Ю. Разумовского, А.Ф. Дронова, А.Н. Смирнова, В.В. Холостовой. – М.: ГЭОТАР-Медиа, 2019. – 368 с.
- Говорухина О.А. Диагностика и лечение болезни гиршпрунга у детей на современном этапе // Новости хирургии. – 2017. –Т. 25. – № 5. С. 510-517. doi: 10.18484/2305-0047.2017.5.510
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Для корректной оценки результатов ваших анализов в динамике предпочтительно делать исследования в одной и той же лаборатории, так как в разных лабораториях для выполнения одноименных анализов могут применяться разные методы исследования и единицы измерения.
Информация проверена экспертом

Лишова Екатерина Александровна
Высшее медицинское образование, опыт работы — 19 лет