Желатиновые капсулы темно-коричневого цвета размера 0, на корпусе и колпачке напечатано «BONJIGAR»
Каждая капсула содержит: активные вещества:
Смесь высушенных густых водных экстрактов: Вербезины белой листьев (3,57:1) – 70,0 мг; Солодки голой корней (3,33:1) – 60,0 мг; Расторопши пятнистой надземных частей (3,33:1) – 60,0 мг; Цикория обыкновенного семян (3,5:1) – 50,0 мг; Барбариса остистого плодов (3,75:1) – 40,0 мг; Пикрорризы курроа корней и корневищ (3,7:1) – 27,0 мг; Берхавии раскидистой надземных частей (3,7:1) – 27,0 мг; Тамарикса гребенщика плодов (3,7:1) – 27,0 мг; Редьки посевной семян (3,85:1) – 13,0 мг, Паслена черного плодов (3,85:1) – 13,0 мг; Сферантуса индийского цветков (3,85: 1) – 13,0 мг;
вспомогательные вещества: кукурузный крахмал, кальция гидрофосфат, целлюлоза микрокристаллическая (Е-460).
Состав желатиновой капсулы: натрия лаурилсульфат (Е-487), метилпарабен (Е-218), пропилпарабен (Е-216), желатин, вода очищенная, титана диоксид (Е-171), краситель хинолиновый желтый (Е-104), краситель красный очаровательный (Е-129), краситель бриллиантовый голубой (Е-133).
Состав чернил: шеллак, безводный спирт, изопропиловый спирт, бутанол, пропиленгликоль, натрия гидроксид, повидон, титана диоксид (Е-171).
Традиционное растительное лекарственное средство.
Код АТС: V03AX.
Комбинированный традиционный растительный препарат, использование основано исключительно на основе длительного опыта применения.
Традиционный растительный препарат. БОНДЖИГАР применяются как средство фитотерапии при заболеваниях печени. БОНДЖИГАР используется для улучшения субъективных жалоб, таких как потеря аппетита, чувство давления в правой верхней части живота, при токсико-нутритивных повреждениях печени и гепатите.
Внутрь взрослым по 1 капсуле 3 раза в день после еды. Капсулы следует проглатывать, не разжевывая, запивая небольшим количеством воды. Курс лечения – 6 недель. Увеличение продолжительности и проведение повторных курсов лечения возможно по рекомендации врача.
Возможны аллергические реакции.
— Повышенная чувствительность к компонентам препарата
— Беременность
— Период грудного вскармливания
— Детский возраст (до 18 лет)
— Желчнокаменная болезнь
— Язвенная болезнь желудка и двенадцатиперстной кишки, синдром Золлингера-Эллисона
— Острый панкреатит или обострение хронического панкреатита
— Кишечная непроходимость
Нет сообщений относительно передозировки препаратом. При передозировке необходимо промыть желудок и назначить симптоматическую терапию.
Применение лекарственного средства во время беременности и в период грудного вскармливания противопоказано в связи с отсутствием данных о безопасности.
Исследования по оценке влияния применения лекарственного средства на способность к вождению автотранспорта и работу с движущимися механизмами не проводились.
• При вирусном гепатите эффективность применения препарата не изучена.
• Не назначать препарат натощак!
Применение у детей
В связи с отсутствием достаточных данных лекарственное средство противопоказано для приема детям и подросткам до 18 лет
Возможно применение лекарственного средства со спазмолитиками и метоклопрамидом.
Беречь от детей
Хранить при температуре не выше 25 °C
3 года
Не применять по истечении срока годности, указанного на упаковке
По 20 и по 60 капсул с пакетиком силикагеля в пластмассовом флаконе почти белого цвета. Флакон закрывается рифленым колпачком с защитой от доступа детей (контроль первого вскрытия) и тисненым текстом на поверхности. Флакон с инструкцией по применению в картонной упаковке.
Без рецепта врача
Производитель
Herbion Pakistan Private Limited
Пакистан, Карачи, 74900, промышленная зона Коранги, участок 30.
Представительство компании «Herbion Pakistan Private Limited» в Республике Беларусь,
220030 г. Минск, пр. Независимости, д. 25, к. 131, тел.: 200-84-01
Описание лекарственного препарата
Бонджигар
(Bonjigar)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для электронного издания справочника Видаль 2011
года, дата обновления: 2020.11.23
Код ATX:
A05BA
(Препараты для лечения заболеваний печени)
Лекарственные формы
| Бонджигар® |
Капс.: 20 шт. рег. №: ЛС-002218 |
|
| Бонджигар |
Сироп: фл. 90 мл 1 шт. рег. №: ЛСР-006277/09 |
Форма выпуска, упаковка и состав
препарата Бонджигар
Капсулы твердые желатиновые, размер №0, коричневого цвета, с надписью белыми чернилами «BONJIGAR» на корпусе и колпачке; содержимое капсул — порошок от светло-коричневого до темно-коричневого цвета, с характерным запахом.
Вспомогательные вещества: тальк.
20 шт. — флаконы пластиковые (1) — пачки картонные.
Сироп от светло-коричневого до темно-коричневого цвета, с характерным запахом.
Вспомогательные вещества: сахароза, лимонная кислота безводная, глицерол, метилпарагидроксибензоат, пропилпарагидроксибензоат, пропиленгликоль, ароматизатор Тутти-фрутти CG-2879, ароматизатор Шоколадная ваниль PDF-144, вода очищенная.
90 мл — флаконы темного стекла (1) — пачки картонные.
Фармакологическое действие
Комбинированный фитопрепарат с гепатопротекторным действием. Способствует нормализации нарушенной клеточной структуры печени, снижает повышенный уровень содержания сывороточных ферментов (АЛТ, АСТ, ЩФ, ГГТ), продуктов перекисного окисления липидов, общего и прямого билирубина.
Фармакокинетика
В соответствии с Международной конвенцией (EMEAHMPWG11/99) при проведении клинических испытаний препаратов растительного происхождения не требуется изолированное исследование фармакокинетических параметров.
Показания препарата
Бонджигар
- алкогольный стеатогепатит умеренной степени, медленно прогрессирующий (монотерапия и в составе комплексной терапии в сочетании со спазмолитиками и метоклопрамидом (церукалом)).
Режим дозирования
Препарат принимать внутрь по 1 капсуле или по 10 мл (2 чайные ложки) 3 раза/сут после еды. Курс лечения — 6 недель.
Увеличение продолжительности и проведение повторных курсов лечения возможно по назначению врача.
Капсулы следует проглатывать не разжевывая, запивая небольшим количеством воды.
Побочное действие
Возможно: аллергические реакции.
Противопоказания к применению
- беременность;
- период лактации (грудного вскармливания);
- детский и подростковый возраст до 18 лет;
- повышенная чувствительность к компонентам препарата.
Сироп следует назначать с осторожностью пациентам с сахарным диабетом.
Применение при беременности и кормлении грудью
Препарат противопоказан к применению при беременности и в период лактации (грудного вскармливания).
Применение у детей
Противопоказание: детский и подростковый возраст до 18 лет.
Особые указания
При вирусном гепатите эффективность применения препарата не изучена.
Сироп содержит сахарозу, что необходимо учитывать при назначении пациентам с сахарным диабетом и пациентам, находящимся на гипокалорийной диете. 1 разовая доза (10 мл) содержит 8 г сахарозы, что соответствует 0.67 ХЕ.
Передозировка
В настоящее время о случаях передозировки препарата Бонджигар® не сообщалось.
Лекарственное взаимодействие
Возможно применение препарата в сочетании со спазмолитиками и метоклопрамидом (церукалом).
Условия хранения препарата Бонджигар
Препарат следует хранить в недоступном для детей месте при температуре не выше 25°C.
Срок годности препарата Бонджигар
Срок годности капсул — 2 года, сиропа — 3 года.
Условия реализации
Препарат отпускается по рецепту.
Брингарадж называют «Король волос», так как он оказывает сильнейшее восстанавливающее действие на волосы, стимулирует их рост, повышает упругость и густоту, придаёт здоровый блеск и силу, оздоравливает кожу головы, избавляя от перхоти и шелушения. Также, препарат укрепляет ногти, кости, зубы и улучшает зрение.
В системе Аюрведы данное средство успешно используется как тоник для печени и селезёнки и эффективный гепатопротектор, он восстанавливает ткани печени и стимулирует функции органа, помогает при циррозе и гепатите. Кроме того, Брингарадж полезен при диабете и его профилактике. Является антивирусным средством.
Бринградж гармонизирует и восстанавливает нервную систему, помогает при психических расстройствах, останавливает кровотечения, снимает лихорадку, действует как лёгкое слабительное, способствует заживлению ран. Источник полезных витаминов и микроэлементов.
Полезные свойства
- Омолаживает организм;
- Тонизирует печень, гепатопротектор;
- Укрепляет внутренние органы;
- Укрепляет волосы, ногти, кости и зубы;
- Источник витаминов и микроэлементов;
- Улучшает зрение, слух и память;
- Антивирусное средство;
- Ранозаживляющее;
- Останавливает кровотечения;
- Слабительное;
- Стимулирует обмен веществ;
- Антидиабетическое;
- Укрепляет нервную систему;
- Снимает стресс;
- Устраняет бессонницу;
- Иммуномодулятор.
Показания к применению
- Анемия,
- Кожные болезни,
- Увеличение печени и селезенки,
- Цирроз,
- Гепатит,
- Заболевания внутренних органов,
- Диабет,
- Нервные расстройства,
- Сухие ломкие волосы, алопеция,
- Бессонница.
Способ применения
По 1-2 таблетки два-три раза в день через полчаса-час после еды, запивая теплой водой. Детям 6-12 лет по 1/2 таблетки два раза в день, запивая теплой водой с добавлением меда.
Состав
Бринградж (эклипта белая, Eclipta alba) – 750 мг.
Противопоказания
Индивидуальная непереносимость; острые лихорадочные состояния.
Все товары, представленные на сайте Himalay.ru в разделе «Средства аюрведы», не являются лекарствами, а относятся к фитосборам или добавкам к питанию. Перед применением рекомендуется проконсультироваться со специалистом по Аюрведе для индивидуального назначения.
Одна капсула содержит
активные вещества:
Вербезины белой травы экстракт густой 130.0 мг
Пикроризы курроа корневищ и корней экстракт густой 43.0 мг
Паслена черного плодов экстракт густой 25.0 мг
Цикория обыкновенного семян экстракт густой 93.5 мг
Тамарикса гребенщика плодов экстракт густой 48.0 мг
Редьки посевной семян экстракт густой 32.0 мг
Барбариса остистого плодов экстракт густой 76.0 мг
Берхавии раскидистой травы экстракт густой 52.5 мг
cостав оболочки капсулы: натрия лаурилсульфат, метилпарабен (Е218), пропилпарабен (Е216), желатин, вода очищенная, титана диоксид (Е171), FD&C Хинолиновый желтый №10 (Е104), FD&C Аллура красный №40 (Е129), FD&C Бриллиантовый синий №1 (Е133).
Твердые желатиновые капсулы размером № 0 с корпусом и крышкой коричневого цвета. На корпусе и на крышке надпись “BONJIGAR”.
Содержимое капсул – порошок коричневого цвета, со специфическим ароматным запахом и горьковатым вкусом.
Пищеварительный тракт и обмен веществ. Препараты для лечения заболеваний печени и желчевыводящих путей. Препараты для лечения желчевыводящих путей и липотропные препараты в комбинации
Код АТХ А05 C
Фармакокинетика
Всасывание происходит из желудочно-кишечного тракта. Действие препарата Бонджигар является совокупным действием его компонентов, поэтому проведение кинетических наблюдений не представляется возможным; компоненты не могут быть прослежены с помощью маркеров или биоисследований. По этой же причине невозможно обнаружить и метаболиты препарата.
Фармакодинамика
Бонджигар – комплексный растительный препарат, фармакологический эффект которого, обусловлен комплексом входящими в его состав активных компонентов, оказывающий гепатопротекторное, противовоспалительное, антитоксическое и желчегонное действие.
Вербезина белая содержит видилолактон и диметил видилолактон, обладающие антигепатоксическими свойствами, аскорбиновую кислоту, алкалоид эклиптин, а также производные тиофена.
Пикрориза курроа содержит гликозиды – пикрозид, куткозид, андросин, апоцинин. Оказывает антигистаминное действие, противовоспалительное (путем ингибирования активизации тромбоцитов), желчегонное и антиоксидантное действие, кроме этого обладает иммуномодулирующим действием.
Паслен черный содержит гликоалкалоиды – соласодин, соламарин, соласонин. Оказывает успокаивающее, болеутоляющее, слабительное действие.
Цикорий обыкновенный – содержит танины, полифенолы, масла. Оказывает желчегонное, гепатопротекторное действие.
Тамариск гребенщик содержит тамарексин, аглюкон. Активизирует действие других гепатозащитных препаратов, обладает кровоостанавливающими свойствами.
Редька посевная содержит гликозиды, эфирные масла, аскорбиновую кислоту, лизоцим, аминокислоты (орнитин, цитрулин, аргинин). Действует как антиоксидант, оказывает гепатотропный и желчегонный эффект, усиливает детоксикационную способность печени, способствует регулированию метаболизма.
Барбарис остистый содержит алкалоиды берберин, бербамин, аромолин, карахин, пальматин, оксиакантин, органические кислоты и сахара, кофейная и ферулевая кислоты. Обладает желчегонным, противомикробным, антидиарейным действием.
Берхавия раскидистая содержит алкалоиды триаконтанол, гентриаконтан, флавоноиды, гликозиды. Оказывает гепатопротекторное, болеутоляющее, мочегонное действие.
Противовоспалительное действие Бонджигара заключается в предотвращении выработки фосфолипида 2-А арахидоновой кислоты, необходимой для биосинтеза простагландинов. За счет гепатопротекторного действия, стабилизируется мембрана лизосом, сокращаются размеры увеличенной печени и показатели АЛТ, АСТ и билирубина быстро приходят в норму. Дезинтоксикационная функция Бонджигара основана на усилении цикла трикарбоновых кислот, что приводит к ускоренному выведению продуктов распада белкового обмена до аммиака и образованию первичной мочи. Липотропное действие Бонджигара заключается в предотвращении жировых отложений в клетках печени за счет выработки липотропных агентов: холина, метионина и лецитина. Они расщепляют жиры до жирных кислот, препятствуют их всасыванию и ускоряют процесс удаления ранее образованных жировых включений из клеток печени. Желчегонный эффект основан на усилении выработки желчи и снижении ее вязкости. Бонджигар регулирует иммунологическую и антибактериальную функцию лейкоцитов, увеличивая их подвижность и стимулируя фагоцитоз. Кроме того, препарат способствует выработке собственного интерферона. Обладает антиоксидантным действием (стимулирует продуцирование энергии внутри клеток и защищает печень от действия свободных радикалов путем их связывания и выведения из организма).
В составе комплексной терапии:
— дискинезия желчевыводящих путей
— хронический некалькулезный холецистит
— острые и хронические гепатиты различной этиологии, токсический гепатит, вызванный побочным действием химических веществ, лекарственных препаратов, алкоголем
— жировой гепатоз (в том числе при сахарном диабете)
— цирроз печени
Взрослые – 1-2 капсулы 2 раза в день.
Препарат принимают после еды.
При лечении острых форм заболеваний продолжительность приема препарата – 2 недели.
При лечении хронических форм заболеваний – 4-6 недель.
— аллергические реакции на компоненты препарата
— учащение стула
— повышенная индивидуальная чувствительность к компонентам препарата
— детский и подростковый возраст до 18 лет
— беременность и период лактации
Клинические данные о применении препарата в период беременности и лактации отсутствуют.
По 20 и 60 капсул во флаконы из пластмассы с закручивающейся пластмассовой крышкой. Во флаконы вместе с капсулами помещают мешочек с поглотителем влаги, свободное пространство заполняют ватой гигроскопической медицинской. Горлышко флакона оклеивают фольгой алюминиевой.
По 1 флакону вместе с инструкцией по медицинскому применению на государственном и русском языках помещают в картонную пачку.
Хранить при температуре не выше 25ºС.
Хранить в недоступном для детей месте!
3 года
Не применять по истечении срока годности.
Без рецепта
Производитель
«Хербион Пакистан Пвт Лтд»,
Промышленная зона Коранги, 30/28
г. Карачи, Пакистан.
Владелец регистрационного удостоверения
«Хербион Пакистан Пвт Лтд», Пакистан.
Наименование, адрес и контактные данные (телефон, факс, электронная почта) организации на территории Республики Казахстан, принимающей претензии (предложения) по качеству лекарственных средств от потребителей и ответственной за пострегистрационное наблюдение за безопасностью лекарственного средства
ТОО «Фармация Юниверсал»
г. Алматы ул. Чаплина/ Халиуллина 71/66
Тел: 234-48-53, 234-44-88
Факс: 234-41-77
Е-mail: info.kz@herbion.com
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-001059
Торговое название:
Брилинта®
Международное непатентованное название:
тикагрелор
Лекарственная форма:
таблетки, покрытые плёночной оболочкой
Состав на 1 таблетку:
Активное вещество: тикагрелор 90 мг
Вспомогательныевещества: маннитол 126 мг, кальция гидрофосфат 63 мг, карбоксиметилкрахмал натрия 9 мг, гипролоза 9 мг, магния стеарат 3 мг;
всоставеплёночнойоболочкитаблетки: гипромеллоза 2910 5,6 мг, титана диоксид E 171 1,7 мг, тальк 1,0 мг, макрогол 400 0,6 мг, краситель железа оксид жёлтый E 172 0,1 мг.
Описание
Круглые, двояковыпуклые таблетки, покрытые плёночной оболочкой жёлтого цвета, с гравировкой 90 на одной стороне.
ФАРМАКОТЕРАПЕВТИЧЕСКАЯ ГРУППА:
антиагрегантное средство
Код АТХ: В01АС24
ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА
Механизм действия
Препарат Брилинта® содержит в своем составе тикагрелор, представитель химического класс циклопентилтриазолопиримидинов, который является пероральным, селективным и обратимым антагонистом P2Y12 рецепторов прямого действия и предотвращает аденозиндифосфат-опосредованную P2Y12-зависимую активацию и агрегацию тромбоцитов. Тикагрелор не предотвращает связывание аденозиндифосфата (АДФ), но его взаимодействие с Р2Y12 рецептором тромбоцитов предотвращает АДФ-индуцированную трансдукцию сигналов. Так как тромбоциты участвуют в инициировании и/или развитии тромботических осложнений атеросклероза, было показано, что ингибирование функции тромбоцитов уменьшает риск развития сердечно-сосудистых явлений, таких как летальный исход, инфаркт миокарда или инсульт.
Тикагрелор имеет дополнительный механизм действия, повышая локальные концентрации эндогенного аденозина путем ингибирования эндогенного равновесного нуклеозидного транспортера (ENT-1).
Аденозин образуется локально в местах гипоксии и повреждения тканей путем высвобождения из аденозинтрифосфата и АДФ. Тикагрелор ингибирует ENT-1 и продлевает период полувыведения аденозина, тем самым увеличивая его локальную внеклеточную концентрацию, усиливая локальный аденозиновый
ответ. Тикагрелор не имеет клинически значимого прямого влияния на аденозиновые рецепторы (A1, A2a, A2b, A3) и не метаболизируется до аденозина.
Аденозин обладает следующими эффектами, которые включают в себя: вазодилатацию, кардиопротекцию, ингибирование агрегации тромбоцитов, модуляцию воспаления и возникновение одышки, которые могут влиять на клинический профиль тикагрелора. Было показано, что у здоровых добровольцев и у пациентов с острым коронарным синдромом (ОКС) тикагрелор усиливал следующие эффекты аденозина: вазодилатацию (оцениваемую как увеличение коронарного кровотока у здоровых добровольцев; головную боль), ингибирование функции тромбоцитов ( in vitro в цельной человеческой крови) и одышку. Тем не менее, связь повышенных локальных концентраций аденозина с клиническими исходами (показатели заболеваемости и смертности) не доказана.
Фармакодинамика
Начало действия
У пациентов со стабильным течением ишемической болезни сердца (ИБС) на фоне применения ацетилсалициловой кислоты тикагрелор начинает быстро действовать, что подтверждается результатами определения среднего значения ингибирования агрегации тромбоцитов (ИАТ): через 0,5 часа после приема нагрузочной дозы 180 мг тикагрелора среднее значение ИАТ составляет примерно 41%, максимальное значение ИАТ 89% достигается через 2-4 часа после приема препарата и поддерживается в течение 2-8 часов. У 90% пациентов окончательное значение ИАТ более 70% достигается через 2 часа после приема препарата.
Конец действия
При планировании АКШ, риск кровотечений возрастает, если тикагрелор прекращают менее, чем за 96 часов до процедуры.
Данные о переходе с одного препарата на другой
Переход с клопидогрела на тикагрелор приводит к увеличению абсолютного значения ИАТ на 26,4%, а изменение терапии с тикагрелора на клопидогрел приводит к снижению абсолютного значения ИАТ на 24,5%. Можно менять терапию с клопидогрела на тикагрелор без прерывания антитромботического эффекта.
Клиническая эффективность
В исследовании PLATO (PLATelet Inhibition and Patient Outcomes – Ингибирование тромбоцитов и исходы у пациентов) участвовало 18 624 пациента, у которых за последние 24 часа развились симптомы нестабильной стенокардии, инфаркта миокарда без подъема сегмента ST или инфаркта миокарда с подъемом сегмента ST и которые лечились консервативно, или посредством чрескожного коронарного вмешательства (ЧКВ), или аортокоронарного шунтирования (АКШ) (см. раздел «Показания к применению»). В этом исследовании на фоне ежедневной терапии ацетилсалициловой кислотой тикагрелор 90 мг дважды в сутки сравнивался с клопидогрелом 75 мг в сутки в отношении эффективности в предупреждении развития комбинированной конечной точки сердечно-сосудистой смерти, инфаркта миокарда или инсульта за счет влияния на частоту сердечнососудистых смертей и инфарктов миокарда. Нагрузочная доза составляла 300 мг клопидогрела (доза 600 мг также допускалась при проведении ЧКВ) или 180 мг тикагрелора.
Эффект тикагрелора проявлялся рано (на 30 день снижение абсолютного риска (САР) на 0,6% и снижение относительного риска (СОР) на 12%), с поддержанием постоянного эффекта терапии в течение 12 месяцев, что приводило к снижению абсолютного риска (САР) на 1,9% и снижению относительного риска (СОР) на 16% в течение года.
Брилинта® снижает относительный риск комбинированной конечной точки (совокупность сердечно-сосудистых смертей, инфаркта и инсульта) у пациентов с нестабильной стенокардией, инфарктом миокарда без подъема сегмента ST и инфарктом миокарда с подъемом сегмента ST на 16% (отношение рисков (ОР) 0,84; 95% доверительный интервал (ДИ) 0,77-0,92; p = 0,0003), сердечно-сосудистой смерти на 21% (ОР 0,79; 95% ДИ 0,69-0,91; р=0,0013), инфаркта миокарда на 16% (ОР 0,84; 95% ДИ 0,75-0,95; р=0,0045).
Эффективность препарата Брилинта® показана у различных подгрупп пациентов, независимо от массы тела, пола, наличия в анамнезе сахарного диабета, транзиторной ишемической атаки или негеморрагического инсульта, реваскуляризации, сопутствующей терапии (включая гепарин, ингибиторы гликопротеиновых llb/llla рецепторов (см. раздел «Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия»), окончательного диагноза (инфаркт миокарда без подъема сегмента ST, инфаркт миокарда с подъемом сегмента ST и нестабильная стенокардия) и лечения, запланированного при рандомизации (инвазивное или консервативное). Дополнительный анализ позволил предположить наличие возможной связи с дозой ацетилсалициловой кислоты, которая выражалась в том, что пониженная эффективность наблюдалась при приеме препарата Брилинта® в комбинации с повышенными дозами ацетилсалициловой кислоты. Рекомендуемая доза ацетилсалициловой кислоты для постоянного приема в сочетании с препаратом Брилинта® — 75-150 мг (см. разделы «Способ применения и дозы» и «Особые указания»).
Брилинта® продемонстрировала статистически значимое СОР по совокупному критерию: смерть от сердечно-сосудистых причин, инфаркт миокарда и инсульт — у пациентов с острым коронарным синдромом, которым запланировано инвазивное вмешательство (СОР 16%, САР 1,7%, р=0,0025). В поисковом анализе Брилинта® также продемонстрировала СОР по первичной конечной точке у пациентов с острым коронарным синдромом, которым назначалась консервативная терапия (СОР 15%, САР 2,3%, номинальное р=0,0444). У пациентов после стентирования при применении тикагрелора отмечалось снижение частоты тромбоза стентов (СОР 32%, САР 0,6%, номинальное р=0,0123).
Брилинта® вызывала статистически значимое СОР на 16% (САР 2,1%) по такому совокупному критерию как смерть от всех причин, инфаркт миокарда и инсульт. СОР смерти от всех причин на приеме препарата Брилинта® составляло 22% при номинальном уровне значимости р=0,0003 и САР — 1,4%.
Совокупный критерий объединенной эффективности и безопасности
Совокупный критерий объединенной эффективности и безопасности (смерть от сердечно-сосудистых причин, инфаркт миокарда, инсульт или большое кровотечение по определению исследования PLATO) подтверждает, что в течение 12 месяцев после острого коронарного синдрома положительный эффект тикагрелора не нейтрализуется случаями больших кровотечений (СОР 8%, САР 1,4%, OP 0,92; p=0,0257).
Фармакокинетика
Тикагрелор демонстрирует линейную фармакокинетику, и экспозиция тикагрелора и активного метаболита (AR-C124910XX) примерно пропорциональна дозе вплоть до 1260 мг.
Абсорбция
Тикагрелор быстро абсорбируется со средней tmax примерно 1,5 часа. Формирование основного циркулирующего в крови метаболита AR-C124910XX (также активного) из тикагрелора происходит быстро со средней tmax примерно 2,5 часа. После приема натощак тикагрелора в дозе 90 мг Cmax составляет 529 нг/мл и AUC – 3451 нг*ч/мл.
Средняя абсолютная биодоступность тикагрелора составляет 36%. Прием жирной пищи не влияет на Cmax тикагрелора или AUC активного метаболита, но приводит к повышению на 21% AUC тикагрелора и снижению на 22% Cmax активного метаболита. Эти небольшие изменения имеют минимальную клиническую значимость; поэтому тикагрелор можно назначать вне зависимости от приема пищи.
Тикагрелор в виде суспензии измельченных таблеток в питьевой воде, принятой внутрь или введенной в желудок через назогастральный зонд, биоэквивалентен тикагрелору, принятому внутрь в виде таблеток препарата Брилинта ® (AUC и Cmax тикагрелора и активного метаболита в диапазоне 80-125%).
В случае приема суспензии первоначальная экспозиция (через 0,5 ч и 1 ч после приема) была выше, чем при приеме тикагрелора в виде таблеток препарата Брилинта ®, но в дальнейшем (от 2 до 48 часов) профиль концентраций был практически одинаковым.
Распределение
Объем распределения тикагрелора в равновесном состоянии составляет 87,5 л. Тикагрелор и активный метаболит активно связываются с белками плазмы крови (> 99%).
Метаболизм
CYP3A4 является основным изоферментом, отвечающим за метаболизм тикагрелора и формирование активного метаболита, и их взаимодействия с другими субстратами CYP3A варьируют от активации до ингибирования.
Тикагрелор и активный метаболит являются слабыми ингибиторами гликопротеина Р (P-gp).
Основным метаболитом тикагрелора является AR-C124910XX, который также активен, что подтверждается результатами оценки связывания с P2Y12 рецептором АДФ тромбоцитов in vitro. Системная экспозиция активного метаболита составляет примерно 30-40% от экспозиции тикагрелора.
Экскреция
Основной путь выведения тикагрелора – через печеночный метаболизм. При введении меченного изотопом тикагрелора в среднем примерно 57,8% радиоактивности выделяется с фекалиями, 26,5% с мочой. Выведение тикагрелора и активного метаболита с мочой составляет менее 1% дозы. В основном активный метаболит выводится с желчью. Средний период полувыведения тикагрелора и активного метаболита составлял 7 и 8,5 часов, соответственно.
Особые популяции больных
Пожилые пациенты
У пожилых пациентов (в возрасте от 75 лет и старше) отмечена более высокая экспозиция тикагрелора (Cmax и AUC примерно на 25% выше) и активного метаболита по сравнению с молодыми пациентами. Эти различия не считаются клинически значимыми (см. раздел «Способ применения и дозы»).
Дети
Нет данных по применению тикагрелора у детей.
Пол
У женщин отмечена более высокая экспозиция тикагрелора и активного метаболита по сравнению с мужчинами. Эти различия не считаются клинически значимыми.
Этнические группы
Средняя биодоступность препарата у пациентов-азиатов на 39% выше, чем у европеоидов. Биодоступность препарата Брилинта ® на 18% ниже у пациентов негроидной расы по сравнению с больными европеоидной расы.
Почечная недостаточность
Экспозиция тикагрелора примерно на 20% ниже, а его активного метаболита примерно на 17% выше у пациентов с тяжелой почечной недостаточностью (клиренс креатинина < 30 мл/мин) по сравнению с пациентами с нормальной функцией почек (см. раздел «Способ применения и дозы»).
Печеночная недостаточность
Сmах и AUC тикагрелора были на 12% и 23% выше у пациентов с печеночной недостаточностью легкой степени по сравнению со здоровыми добровольцами. Не проводились исследования тикагрелора у пациентов с умеренной или тяжелой печеночной недостаточностью, и его использование у этих пациентов противопоказано (см. разделы «Способ применения и дозы» и «Противопоказания»).
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ
Брилинта®, применяемая одновременно с ацетилсалициловой кислотой, показана для профилактики атеротромботических событий у пациентов с острым коронарным синдромом (нестабильной стенокардией, инфарктом миокарда без подъема сегмента ST или инфарктом миокарда с подъемом сегмента ST [STEMI]), включая больных, получавших лекарственную терапию, и пациентов, подвергнутых чрескожному коронарному вмешательству (ЧКВ) или аортокоронарному шунтированию (АКШ)).
ПРОТИВОПОКАЗАНИЯ
- Повышенная чувствительность к тикагрелору или любому из компонентов препарата
- Активное патологическое кровотечение
- Внутричерепное кровоизлияние в анамнезе
- Умеренная или тяжелая печеночная недостаточность
- Совместное применение тикагрелора с мощными ингибиторами CYP3A4 (например, кетоконазолом, кларитромицином, нефазодоном, ритонавиром и атазанавиром)
- Детский возраст до 18 лет (в связи с отсутствием данных об эффективности и безопасности применения у данной группы пациентов)
С ОСТОРОЖНОСТЬЮ
Предрасположенность пациентов к развитию кровотечения (например, в связи с недавно полученной травмой, недавно проведенной операцией, нарушениями свертываемости крови, активным или недавним желудочно-кишечным кровотечением) (см. раздел «Особые указания»).
Пациенты с сопутствующей терапией препаратами, повышающими риск кровотечений (т.е. нестероидные противовоспалительные препараты, пероральные антикоагулянты и/или фибринолитики) в течение 24 часов до приема препарата Брилинта ®.
Пациенты с повышенным риском развития брадикардии (например, больные с синдромом слабости синусового узла без кардиостимулятора, с атриовентрикулярной блокадой 2-ой или 3-ей степени; обмороком, связанным с брадикардией) в связи с недостаточным опытом клинического применения препарата Брилинта ® (см. раздел «Особые указания»). При совместном применении с препаратами, вызывающими брадикардию.
Тикагрелор должен использоваться с осторожностью у пациентов с бронхиальной астмой и хронической обструктивной болезнью легких (ХОБЛ). Если пациент сообщает о возникновении нового эпизода одышки, о длительной одышке или ухудшении одышки, необходимо провести обследование, и в случаенепереносимости, лечение тикагрелором должно быть прекращено.
На фоне приема препарата Брилинта® уровень креатинина может повыситься (см. разделы «Побочное действие», «Особые указания»), в связи с чем необходимо производить оценку почечной функции в соответствии с рутинной клинической практикой, обращая особое внимание на пациентов от 75 лет и старше, пациентов с умеренной или тяжелой почечной недостаточностью, пациентов, получающих терапию антагонистами рецепторов к ангиотензину.
Необходимо соблюдать осторожность у пациентов с гиперурикемией или подагрическим артритом в анамнезе. В качестве превентивной меры следует избегать применения тикагрелора у пациентов с гиперурикемической нефропатией.
Не рекомендуется совместное применение тикагрелора и высокой поддерживающей дозы ацетилсалициловой кислоты (более 300 мг).
При совместном применении дигоксина и препарата Брилинта® рекомендован тщательный клинический и лабораторный мониторинг (частоты сердечных сокращений, и при наличии клинических показаний также ЭКГ и концентрации дигоксина в крови).
Нет данных о совместном применении тикагрелора с мощными ингибиторами гликопротеина P (например, верапамил и хинидин), в связи с чем их совместное применение должно осуществляться с осторожностью (см. раздел «Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия»).
БЕРЕМЕННОСТЬ И ПЕРИОД ЛАКТАЦИИ
Данные о применении препарата Брилинта ® у беременных женщин отсутствуют или ограничены.
В исследованиях на животных тикагрелор вызывал незначительное снижение прибавки массы тела у матери, снижение жизнеспособности новорожденного и его массы тела, замедление роста. Брилинта ® не рекомендована во время беременности.
Доступные фармакодинамические, токсикологические данные у животных показали, что тикагрелор и его активные метаболиты выделяются с молоком. Не может быть исключен риск для новорожденного/младенца. Не рекомендуется применять препарат Брилинта ® в период кормления ребенка грудью.
СПОСОБ ПРИМЕНЕНИЯ И ДОЗЫ
Для приёма внутрь. Препарат Брилинта ® можно принимать вне зависимости от приёма пищи.
Применение препарата Брилинта® следует начинать с однократной нагрузочной дозы 180 мг (две таблетки по 90 мг) и затем продолжать прием по 90 мг два раза в сутки.
Для пациентов с затруднением глотания таблетку (или 2 таблетки – в случае приема нагрузочной дозы) следует измельчить до состояния мелкого порошка, размешать в половине стакана питьевой воды и сразу же выпить полученную суспензию. Остатки смешать с дополнительной половиной стакана питьевой воды и выпить полученную суспензию. Суспензию можно также вводить через назогастральный зонд (CH8 или большего размера). После введения суспензии необходимо промыть назогастральный зонд водой для того, чтобы доза препарата полностью попала в желудок пациента.
Пациенты, принимающие препарат Брилинта®, должны ежедневно принимать ацетилсалициловую кислоту (от 75 мг до 150 мг при постоянном приеме) (см.раздел «Фармакологические свойства»), если отсутствуют специфические противопоказания.
Следует избегать перерывов в терапии. Пациент, пропустивший прием препарата Брилинта®, должен принять только одну таблетку 90 мг (следующая доза) в намеченное время.
При необходимости пациенты, принимающие клопидогрел, могут быть переведены на прием препарата Брилинта ® (см. раздел «Фармакологические свойства»).
Рекомендуется проводить терапию препаратом Брилинта ® в течение 12 месяцев, кроме случаев клинической необходимости в досрочной отмене препарата (см. раздел «Фармакологические свойства»). Данные о применении тикагрелора более 12 месяцев ограничены. У пациентов с острым коронарным синдромом досрочная отмена любой антиагрегантной терапии, включая препарат Брилинта ®, может повысить риск сердечно-сосудистой смерти или инфаркта миокарда в результате основного заболевания (см. раздел «Особые указания»). Необходимо избегать преждевременного прекращения приема препарата.
Пожилые пациенты
Не требуется коррекции дозы (см. раздел «Фармакологические свойства»).
Пациенты с почечной недостаточностью
Не требуется корректировать дозу препарата у пациентов с почечной недостаточностью (см. раздел «Фармакологические свойства»). Отсутствует информация о применении препарата Брилинта ® у пациентов на гемодиализе, поэтому его применение у этих пациентов не показано.
Пациенты с печеночной недостаточностью
Не требуется корректировать дозу препарата у пациентов с легкой печеночной недостаточностью. Не проводились исследования препарата Брилинта ® у пациентов с умеренной или тяжелой печеночной недостаточностью, поэтому его у этих пациентов противопоказано (см. разделы «Фармакологические свойства» и «Противопоказания»).
Дети
Безопасность и эффективность препарата Брилинта ® у детей младше 18 лет по одобренному у взрослых показанию не установлена.
ПОБОЧНОЕ ДЕЙСТВИЕ
По данным исследования PLATO самыми частыми отмечавшимися нежелательными явлениями у пациентов, принимавших тикагрелор, были одышка, ушибы и носовые кровотечения.
Нежелательные реакции классифицированы по частоте развития и классу системы органов. Частота развития нежелательных реакций определяется с использованием следующих условных обозначений: очень часто (≥1/10), часто (≥1/100, <1/10), нечасто (≥1/1000, <1/100), редко (≥1/10000, <1/1000).
Нежелательные лекарственные реакции по частоте развития и классу системы органов
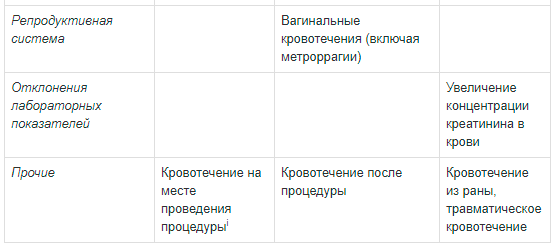
a гиперурикемия, повышение концентрации мочевой кислоты в крови; смотрите раздел «Отклонения в значениях лабораторных показателей» ниже.
b кровоизлияние в мозг, внутричерепное кровоизлияние, геморрагический инсульт.
c одышка, одышка при нагрузке, одышка в покое, ночная одышка
d желудочно-кишечное кровотечение, ректальное кровотечение, кишечное
кровотечение, мелена, положительный анализ на скрытую кровь
е кровотечение из язвы ЖКТ, кровотечение из язвы желудка, кровотечение из язвы двенадцатиперстной кишки, кровотечение из пептической язвы
f подкожная гематома, кожные и подкожные геморрагии, петехии
g ушиб, гематома, экхимоз, повышенная тенденция к синякам, травматическая гематома
h гематурия, кровотечение из мочевыводящих путей
i кровотечение из места пункции сосуда, гематома в месте пункции сосуда, кровотечение из места инъекции, кровотечение из места пункции, кровотечение из места катетеризации
# у пациентов, принимавших тикагрелор в исследовании PLATO (п=9235), случаев гемартроза отмечено не было. Частота гемартроза была рассчитана с использованием верхнего предела 95% ДИ для ожидаемой частоты (по формуле 3/Х, где Х — количество пациентов, получавших тикагрелор, т.е. 9235).
Предполагаемая частота гемартроза составляет 3/9235, что соответствует частоте «редко».
Описание некоторых нежелательных реакций
Кровотечение
В исследовании PLATO использовались следующие определения кровотечения:
• Большое летальное/угрожающее жизни кровотечение: летальное, или внутричерепное кровоизлияние, или кровотечение в полость перикарда с тампонадой сердца; или гиповолемический шок или тяжелая гипотония, вызванные кровотечением и требующие применения вазоконстрикторов или проведения оперативного вмешательства, или клинически явное кровотечение, сопровождающееся снижением уровня гемоглобина более, чем на 50 г/л, или требующее трансфузии 4 или более единиц цельной крови или эритроцитов.
• Большое иное кровотечение: вызывающее существенную недееспособность больного (например, внутриглазное кровоизлияние с необратимой потерей зрения), или клинически явное кровотечение, сопровождающееся снижением уровня гемоглобина на 30-50 г/л, или требующее трансфузии 2-3 единиц цельной крови или эритроцитов.
• Малое кровотечение: требует медицинского вмешательства для остановки или лечения кровотечения (например, носовое кровотечение, требующее посещения больницы для тампонады носа).
Брилинта® и клопидогрел не различались по частоте больших кровотечений в целом по критериям PLATO (11,6%/год и 11,2%/год, соответственно), летальных/угрожающих жизни кровотечений по критериям PLATO (5,8%/год в обеих группах). Однако частота совокупности больших и малых кровотечений по критериям PLATO была выше в группе тикагрелора (16,1%) по сравнению с клопидогрелом (14,6%, р=0,0084).
Возраст, пол, масса тела, раса, географический регион, сопутствующие заболевания, сопутствующая терапия, анамнез, включая предшествующий инсульт и транзиторную ишемическую атаку, не влияли на частоту больших кровотечений в целом и несвязанных с процедурами по критериям PLATO. Не было выявлено групп с повышенным риском кровотечений.
Кровотечение, связанное с АКШ: В исследовании PLATO у 42% больных из 1584 (12% из когорты), подвергнутых АКШ, развивались большие летальные/ угрожающие жизни больного кровотечения без значимых различий в обеих группах лечения. Летальное кровотечение, связанное с АКШ, отмечалось у 6 пациентов в каждой группе лечения.
Кровотечение, не связанное с АКШ, и кровотечение, не связанное с процедурами:
Брилинта® и клопидогрел не отличались по частоте случаев большого летального/ угрожающего жизни кровотечения, не связанного с АКШ по критериям PLATO, но при применении препарата Брилинта® чаще развивались большие кровотечения в целом по определению исследования PLATO (4,5%/год по сравнению с 3,8%/год; р=0,0264). Если удалить случаи развития кровотечений, связанных с АКШ, в группе тикагрелора отмечалось больше кровотечений (3,1%/год), чем в группе клопидогрела (2,3%/год; р=0,0058). Прекращение лечения вследствие кровотечений, не связанных с процедурой, было более частым на фоне тикагрелора (2,9%) по сравнению с клопидогрелом (1,2%, p<0,001).
Внутричерепное кровоизлияние: В группе тикагрелора развивалось больше внутричерепных кровотечений, не связанных с процедурами (n=27 кровотечений у 26 пациентов, 0,3%), чем в группе клопидогрела (n=14 кровотечений, 0,2%), из которых 11 кровотечений на тикагрелоре и 1 на клопидогреле были фатальными. Однако не было значимых различий по общему числу фатальных кровотечений.
Одышка
Нежелательные явления в виде одышки (одышка, одышка в покое, одышка при физической нагрузке, пароксизмальная ночная одышка и ночная одышка) в комбинации развивались у 13,8% больных, получавших препарат Брилинта ®, и у 7,8% пациентов, принимавших клопидогрел. Исследователи посчитали, что у 2,2% пациентов из группы тикагрелора одышка была связана с терапией. Большинство случаев одышки были слабыми или умеренными по своей интенсивности и представляли собой однократные эпизоды сразу после начала терапии. Примерно 30% от всех случаев одышки разрешились в течение 7 дней. Чаще одышка развивалась у пожилых больных, у пациентов с застойной сердечной недостаточностью, ХОБЛ или бронхиальной астмой в начале исследования. 0,9% пациентов прекращали прием препарата Брилинта ® из-за одышки. Одышка не была связана с развитием нового или ухудшением имеющегося заболевания сердца или легких (см. раздел «Особые указания»). Препарат Брилинта® не влияет на показатели функции внешнего дыхания.
Отклонения в значениях лабораторных показателей
Сывороточная концентрация креатинина повышалась более, чем на 30% у 25,5% пациентов и больше, чем на 50% у 8,3% пациентов, получающих препарат Брилинта®. Повышение креатинина более, чем на 50%, чаще встречалось у пациентов старше 75 лет, у пациентов с тяжелой почечной недостаточностью при включении в исследование и у пациентов, получающих терапию антагонистами рецепторов к ангиотензину. Общее число почечных нежелательных явлений составляло 4,9% у пациентов на тикагрелоре, однако исследователи связывали их с приемом препарата в 0,6% случаев.
Сывороточная концентрация мочевой кислоты увеличивалась выше верхней границы нормы у 22% пациентов, получающих препарат Брилинта®.
Нежелательные явления, связанные с гиперурикемией, отмечались в 0,5% случаев на тикагрелоре, из них исследователи связывали с приемом тикагрелора 0,05% случаев. Подагрический артрит наблюдался у 0,2% пациентов на тикагрелоре, ни один из этих случаев не был расценен исследователем, как связанный с приемом препарата.
Постмаркетинговое применение
Ниже представлены нежелательные реакции, которые были отмечены при постмаркетинговом применении препарата Брилинта ®. Поскольку сообщения получены спонтанно от популяции неустановленного размера, не всегда возможно достоверно оценить частоту развития.
Нарушениясостороныиммуннойсистемы:реакции повышенной чувствительности, включая ангионевротический отек (см. раздел «Противопоказания»).
ПЕРЕДОЗИРОВКА
Тикагрелор хорошо переносится в однократной дозе препарата до 900 мг. В единственном исследовании с увеличением дозы неблагоприятное воздействие на желудочно-кишечный тракт было дозолимитирующим. Другими клинически значимыми нежелательными явлениями, которые могли наблюдаться при передозировке, были одышка и желудочковые паузы. В случае передозировки рекомендуется осуществлять наблюдение на предмет этих нежелательных явлений и проводить мониторирование ЭКГ.
Брилинта® не выводится при гемодиализе (см. раздел «Особые указания»), антидот не известен. При передозировке следует проводить симптоматическую терапию в соответствии с локальными стандартами. В связи с ингибированием тромбоцитов увеличение продолжительности кровотечения является предполагаемым фармакологическим действием передозировки препаратом Брилинта®, поэтому при развитии кровотечения необходимо проводить соответствующие поддерживающие мероприятия.
ВЗАИМОДЕЙСТВИЕ С ДРУГИМИ ЛЕКАРСТВЕННЫМИ СРЕДСТВАМИ И ДРУГИЕ ВИДЫ ЛЕКАРСТВЕННОГО ВЗАИМОДЕЙСТВИЯ
Воздействие других лекарственных препаратов на препарат Брилинта®
Лекарственные препараты, метаболизируемые изоферментом CYP3A4 Ингибиторы CYP3A4
• Мощные ингибиторы CYP3A4: совместное применение кетоконазола с тикагрелором увеличивает Cmax и AUC тикагрелора в 2,4 и 7,3 раза, соответственно. Cmax и AUC активного метаболита понижается на 89% и 56%, соответственно. Другие мощные ингибиторы CYP3A4 (кларитромицин, нефазодон, ритонавир и атазанавир) будут оказывать такие же эффекты, поэтому их совместное применение с препаратом Брилинта® противопоказано (см. разделы «Противопоказания», «Особые указания»).
• Умеренные ингибиторы CYP3A4: совместное применение дилтиазема с тикагрелором увеличивает Сmax тикагрелора на 69%, а AUC в 2,7 раз, и снижает Сmax активного метаболита на 38%, а AUC не меняется. Тикагрелор не влияет на плазменные концентрации дилтиазема. Другие умеренные ингибиторы CYP3A4 (например, ампренавир, апрепитант, эритромицин, флуконазол) можно назначать одновременно с препаратом Брилинта®.
Циклоспорин (ингибитор P-gp и CYP3A4)
Совместное применение циклоспорина (600 мг) с тикагрелором увеличивает C max и AUC тикагрелора в 2,3 и 2,8 раз, соответственно. При этом отмечается увеличение AUC активного метаболита на 32% и снижение Cmax на 15%. Тикагрелор не влияет на плазменную концентрацию циклоспорина.
Индукторы CYP3A4
Совместное применение рифампицина с тикагрелором снижает C max и AUC тикагрелора на 73% и 86%, соответственно. Cmax активного метаболита не меняется, а AUC понижается на 46%. Другие индукторы CYP3A4 (например, фенитоин, карбамазепин и фенобарбитал), по-видимому, будут снижать экспозицию препарата Брилинта®. Мощные индукторы CYP3A4 могут уменьшать экспозицию и эффективность препарата Брилинта®.
Другие
По результатам фармакологических исследований взаимодействия сопутствующее применение тикагрелора с гепарином, эноксапарином и ацетилсалициловой кислотой или десмопрессином не влияет на фармакокинетику тикагрелора, его активного метаболита и АДФ-зависимую агрегацию тромбоцитов. В случае наличия клинических показаний к назначению препаратов, влияющих на гемостаз, они должны использоваться с осторожностью в комбинации с препаратом Брилинта® (см. раздел «С осторожностью»).
Нет данных о совместном применении препарата Брилинта® с мощными ингибиторами гликопротеина P (например, верапамил и хинидин), которые могут повысить экспозицию тикагрелора. Если нельзя избежать их совместного применения, оно должно осуществляться с осторожностью (см. разделы «С осторожностью», «Особые указания»).
Влияние препарата Брилинта® на другие лекарственные средства
Лекарственные препараты, метаболизируемые изоферментом CYP3A4
• Симвастатин: сопутствующее применение тикагрелора и симвастатина повышает C max и AUC симвастатина на 81% и 56%, соответственно, и увеличивает C max и AUC симвастатиновой кислоты на 64% и 52%, соответственно, при этом, в некоторых случаях эти показатели повышаются в 2-3 раза. Совместное применение симвастатина в дозе выше 40 мг/сут. с тикагрелором может приводить к развитию побочных эффектов симвастатина, и необходимо оценить соотношение потенциального риска и пользы. Не рекомендуется совместное применение препарата Брилинта® с симвастатином и ловастатином в дозе свыше 40 мг. Аторвастатин: сопутствующее применение аторвастатина и тикагрелора повышает Сmax и AUC метаболитов аторвастатиновой кислоты на 23% и 36%, соответственно. Подобное увеличение значений Cmax и AUC наблюдается для всех метаболитов аторвастатиновой кислоты. Эти изменения признаны клинически не значимыми.
• Сходные эффекты со статинами, метаболизирующимися CYP3A4, не могут быть исключены. В исследовании PLATO пациенты, получавшие тикагрелор, принимали различные статины при отсутствии каких-либо опасений относительно безопасности у 93% пациентов, принимавших эту группу препаратов.
Тикагрелор — умеренный ингибитор CYP3A4. Совместное применение препарата Брилинта® и субстратов CYP3A4 с узким терапевтическим индексом (например, цизаприд или алкалоиды спорыньи) не рекомендуется, так как тикагрелор может увеличивать экспозицию этих препаратов.
Лекарственные препараты, метаболизируемые изоферментом CYP2C9
Сопутствующее применение тикагрелора и толбутамида не меняло плазменные концентрации ни одного из этих препаратов, что говорит о том, что тикагрелор не является ингибитором изофермента CYP2C9, и, маловероятно, что он влияет на СУР2С9-опосредованный метаболизм препаратов, подобных варфарину и толбутамиду.
Оральные контрацептивы
Совместное применение тикагрелора, левоноргестрела и этинилэстрадиола увеличивает экспозицию этинилэстрадиола примерно на 20%, но не влияет на фармакокинетику левоноргестрела. Не ожидается клинически значимого воздействия на эффективность контрацепции при одновременном применении левоноргестрела, этинилэстрадиола и препарата Брилинта®.
Субстрат Р—др (включая дигоксин и циклоспорин)
Сопутствующее применение дигоксина с тикагрелором повышает Cmax и AUC дигоксина на 75% и 28%, соответственно. При совместном приеме с тикагрелором среднее значение самой низкой концентрации дигоксина увеличивалось на 30%, в некоторых индивидуальных случаях в два раза. Cmax и AUC тикагрелора при применении дигоксина не менялись. Поэтому рекомендуется проводить соответствующий клинический и/или лабораторный мониторинг при одновременном применении препарата Брилинта® и P-gp-зависимых препаратов с узким терапевтическим индексом, наподобие дигоксина и циклоспорина.
Другая сопутствующая терапия
При совместном применении препарата Брилинта® с препаратами, способными
вызвать брадикардию, должна соблюдаться осторожность. Однако в исследовании PLATO не наблюдалось клинически значимых нежелательных явлений при совместном применении с одним или более препаратами, способными вызвать брадикардию (например, 96% бета-адреноблокаторы, 33% антагонисты кальция, включая дилтиазем и верапамил, и 4% – дигоксин). В исследовании PLATO Брилинта® преимущественно назначалась совместно с ацетилсалициловой кислотой, ингибиторами протонной помпы, статинами, бета-адреноблокаторами, ингибиторами ангиотензинпревращающего фермента и антагонистами рецепторов ангиотензина в рамках длительного приема, а также с гепарином, низкомолекулярными гепаринами, ингибиторами гликопротеиновых IIb/IIIa рецепторов для внутривенного введения в рамках краткосрочной терапии. По результатам этих исследований не выявлено клинически значимых нежелательных взаимодействий.
Совместное применение препарата Брилинта® с гепарином, эноксапарином или десмопрессином не оказывало влияние на активированное частичное тромбопластиновое время (АЧТВ), активированное время свертывания (АВС) и исследование фактора Xa, однако вследствие потенциального фармакодинамического взаимодействия, требуется соблюдать осторожность при совместном применении с препаратами, влияющими на гемостаз.
В связи с сообщениями о подкожных кровоизлияниях на фоне селективных ингибиторов обратного захвата cеротонина, (например, пароксетин, сертралин и циталопрам), рекомендуется соблюдать осторожность при их совместном приеме с препаратом Брилинта ®.
При ежедневном употреблении больших объемов грейпфрутового сока (по 200 мл 3 раза в день) было отмечено 2-кратное увеличение экспозиции тикагрелора. Ожидается, что такое увеличение экспозиции тикагрелора не имеет клинического значения для большинства пациентов.
ОСОБЫЕ УКАЗАНИЯ
Риск развития кровотечения
У пациентов с острым коронарным синдромом, получавших терапию препаратом Брилинта® и ацетилсалициловой кислотой, отмечался повышенный риск несвязанных с АКШ больших кровотечений и кровотечений, требующих повышенного медицинского внимания, таких как большие + малые кровотечения по определению PLATO, но не увеличился риск летальных/угрожающих жизни кровотечений (см. раздел «Побочное действие»). При назначении препарата Брилинта® следует оценить соотношение пользы от профилактики атеротромботических событий и риска у пациентов с повышенным риском развития кровотечений.
При наличии клинических показаний Брилинта® должна использоваться с осторожностью в следующих группах пациентов:
• Предрасположенность пациентов к развитию кровотечения (например, в связи с недавно полученной травмой, недавно проведенной операцией, нарушениями свертываемости крови, активным или недавним желудочно-кишечным кровотечением). Использование препарата Брилинта® противопоказано у пациентов с активным патологическим кровотечением, внутричерепным кровоизлиянием в анамнезе, умеренной или тяжелой печеночной недостаточностью.
• Сопутствующее применение препаратов, которые могут повысить риск развития кровотечения (например, нестероидные противовоспалительные препараты, пероральные антикоагулянты и/или фибринолитики, принимаемые в течение 24 часов до приема препарата Брилинта®).
Отсутствуют данные о гемостатической эффективности трансфузий тромбоцитов при применении препарата Брилинта®; Брилинта® может ингибировать трансфузированные тромбоциты в крови. Так как при сопутствующем применении препарата Брилинта® и десмопрессина не уменьшалось стандартизированное время кровотечения, то маловероятно, что десмопрессин будет эффективно купировать кровотечение.
Антифибринолитическая терапия (аминокапроновая кислота или транексамовая кислота) и/или рекомбинантный фактор Vila могут усиливать гемостаз. После установления причины кровотечения и его купирования можно возобновить терапию препаратом Брилинта®.
Хирургические операции
Перед запланированной операцией или началом приема новых препаратов пациенту следует проинформировать врача о том, что он принимает препарат Брилинта®.
У пациентов, подвергающихся аортокоронарному шунтированию (АКШ), частота развития больших кровотечений при применении препарата Брилинта® была такой же, как при применении клопидогрела во все дни после отмены терапии, кроме дня 1, когда частота развития больших кровотечений была выше при приеме препарата Брилинта ® (см. раздел «Побочное действие»).
Если пациент подвергается плановой операции и не желателен
антитромботический эффект, то терапию препаратом Брилинта ® следует прекратить за 7 дней до операции.
Пациенты с риском развития брадикардии
В связи с выявлением в ранее проведенном клиническом исследовании, в основном, бессимптомных пауз, пациенты с повышенным риском развития брадикардии (например, больные без кардиостимулятора, у которых диагностирован синдром слабости синусового узла, атриовентрикулярная блокада сердца 2-ой или 3-ей степени; обморок, связанный с брадикардией) не были включены в основное исследование для оценки безопасности и эффективности препарата Брилинта®. Поэтому в связи с ограниченным клиническим опытом применения препарата у этих больных, рекомендуется с осторожностью назначать препарат Брилинта® таким пациентам (см. раздел «Фармакологические свойства»).
Дополнительная предосторожность должна соблюдаться при совместном применении препарата Брилинта® с препаратами, способными вызвать брадикардию. Однако не отмечалось клинически значимых побочных эффектов при совместном применении с одним или более препаратами, которые могут вызвать брадикардию (например, 96% бета-адреноблокаторы, 33% блокаторы кальциевых каналов, включая дилтиазем и верапамил, и 4% дигоксин) (см. раздел «Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия»).
В ходе под-исследования с использованием суточного мониторирования ЭКГ по Холтеру в группе тикагрелора по сравнению с клопидогрелом больше пациентов в острой фазе ОКС имели желудочковые паузы > 3 секунд. Повышение числа желудочковых пауз, зарегистрированных с помощью суточного мониторирования по Холтеру, на фоне приема тикагрелора отмечалось чаще у пациентов с хронической сердечной недостаточностью по сравнению с общей популяцией в острой фазе ОКС, но не на первом месяце. Паузы у этих пациентов не сопровождались последующими нежелательными клиническими последствиями (обмороки и установка кардиостимулятора).
Одышка
Одышка при применении препарата Брилинта® обычно слабая или умеренная по своей интенсивности, часто проходит по мере продолжения терапии препаратом. Пациенты с бронхиальной астмой/ХОБЛ могут иметь повышенный абсолютный риск одышки на приеме препарата Брилинта® (см. раздел «Побочное действие»). У пациентов с бронхиальной астмой/ХОБЛ тикагрелор должен использоваться с осторожностью. Механизм одышки на приеме тикагрелора не выяснен. Если у пациента развился новый эпизод одышки, сохраняется или усилилась одышка во время применения препарата Брилинта®, то необходимо провести полноценное обследование, и в случае непереносимости, прием препарата следует прекратить.
Повышение уровня
креатинина
На приеме препарата Брилинта® уровень креатинина может увеличиться (см. раздел «Побочное действие»). Механизм этого эффекта не известен. Оценку почечной функции необходимо производить через месяц от начала приема препарата, а в последующем в соответствии с рутинной клинической практикой, обращая особое внимание на пациентов от 75 лет и старше, пациентов с умеренной или тяжелой почечной недостаточностью и получающих терапию антагонистами рецепторов ангиотензина.
Повышение уровня мочевой кислоты
Пациенты на тикагрелоре имели более высокий риск гиперурикемии, чем
принимавшие клопидогрел (см. раздел «Побочное действие»). Необходимо соблюдать осторожность у пациентов с гиперурикемией или подагрическим артритом в анамнезе. В качестве превентивной меры следует избегать применения тикагрелора у пациентов с гиперурикемической нефропатией.
Другие
На основании наблюдаемого взаимодействия между поддерживающей дозой ацетилсалициловой кислоты и эффективностью тикагрелора по сравнению с клопидогрелом, совместное применение высокой поддерживающей дозы ацетилсалициловой кислоты (более 300 мг) и препарата Брилинта® не рекомендуется (см. разделы «Фармакологические свойства», «С осторожностью»).
Совместное применение препарата Брилинта® с мощными ингибиторами CYP3A4 (например, кетоконазол, кларитромицин, нефазодон, ритонавир и атазанавир) противопоказано (см. раздел «Противопоказания»), так как оно может привести к значительному повышению экспозиции препарата Брилинта® (см. раздел «Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия»).
Совместное применение препарата Брилинта® с мощными индукторами CYP3A4 (например, рифампицин, фенитоин, карбамазепин и фенобарбитал) не рекомендуется, так как их совместный прием может снижать экспозицию и эффективность тикагрелора (см. раздел «Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия»). Совместное применение препарата Брилинта® и субстратов CYP3A4 с узким терапевтическим индексом (например, цизаприд и алкалоиды спорыньи) не рекомендовано, так как тикагрелор может увеличить экспозицию этих препаратов.
Совместное применение препарата Брилинта® с симвастатином или ловастатином в дозе более 40 мг не рекомендуется (см. раздел «Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия»).
При совместном применении дигоксина и препарата Брилинта® рекомендован тщательный клинический и лабораторный мониторинг (частоты сердечных сокращений, и при наличии клинических показаний также ЭКГ и концентрации дигоксина в крови).
Нет данных о совместном применении тикагрелора с мощными ингибиторами гликопротеина P (например, верапамил и хинидин), которые могут повысить экспозицию тикагрелора. Если нельзя избежать их совместного применения, оно должно осуществляться с осторожностью (см. разделы «С осторожностью», «Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия»).
ВЛИЯНИЕ НА СПОСОБНОСТЬ УПРАВЛЯТЬ АВТОМОБИЛЕМ И ДРУГИМИ МЕХАНИЗМАМИ
Не проводилось исследований влияния препарата Брилинта® на способность к вождению автотранспорта и управлению механизмами. Брилинта® не влияет или в незначительной степени влияет на способность управлять транспортом и механизмами. Во время терапии острого коронарного синдрома сообщалось о головокружении и спутанности сознания. В случае развития данных явлений пациентам следует соблюдать осторожность при управлении автомобилем и другими механизмами.
ФОРМА ВЫПУСКА
Таблетки, покрытые плёночной оболочкой, 90 мг. По 14 таблеток в блистере из Ал/ПВХ/ПВДХ. 1, 4 или 12 блистеров с инструкцией по медицинскому применению в картонной пачке с контролем первого вскрытия.
УСЛОВИЯ ХРАНЕНИЯ
При температуре не выше 30°С, в недоступном для детей месте.
СРОК ГОДНОСТИ
3 года. Не применять по истечении срока годности, указанного на упаковке.
УСЛОВИЯ ОТПУСКА ИЗ АПТЕК
По рецепту.
Наименование и адрес юридического лица, на имя которого выдано регистрационное удостоверение
АстраЗенека АБ, SE-151 85 Содерталье, Швеция AstraZeneca AB, SE-151 85 Sodertalje, Sweden
Производитель и фасовщик (первичная упаковка)
АстраЗенека АБ, SE-151 85 Содерталье, Швеция AstraZeneca AB, SE-151 85 Sodertalje, Sweden
Упаковщик (вторичная (потребительская) упаковка) и выпускающий контроль качества
ООО «АстраЗенека Индастриз»
249006, Россия, Калужская область, Боровский район, деревня Добрино, 1-ый Восточный проезд, владение 8
Дополнительная информация предоставляется по требованию: ООО Астра Зенека Фармасьютикалз
125284 Москва, ул. Беговая д.3, стр. 1.
Купить Брилинта таблетки 90 мг в planetazdorovo.ru
*Цена в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)