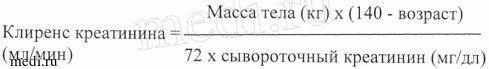Состав
В 1 флаконе находится 0,5 или 1 г активного компонента цефепим в виде цефепима гидрохлорида.
Форма выпуска
Медикамент выпускается в виде порошка, из которого готовят раствор для внутривенного, внутримышечного введения. Цефепим в таблетках не выпускается.
Фармакологическое действие
Антибиотик. Активное вещество является представителем класса цефалоспоринов 4-го поколения.
Фармакодинамика и фармакокинетика
Принцип основного воздействия направлен на разрушение клеточной стенки микробной клетки; препарат действует бактерицидно.
Лекарственное средство проявляется высокую антибактериальную активность в отношении штаммов, которые устойчивы к действию цефалоспоринов 3-го поколения, аминогликозидов. Активное вещество достаточно быстро проникает внутрь грамотрицательной микробной клетки, обладая при этом высокой устойчивостью к гидролизу многих бета-лактамаз. Главной мишенью внутри клетки для цефепима является пенициллин-связывающий белок.
Антибиотик Цефепим действует на грамположительную флору и грамотрицательные бактерии in vitro и in vivo: стрептококки, энтеробактерии, эшерихии коли, клебсиеллы, клостридии, протеи и др.
Показания к применению Цефепима
Антибиотик назначают при тяжелом и среднетяжелом течении пневмонии, вызванной стрептококками, энтерококками, клебсиеллами и другими чувствительными к действию препарата микроорганизмами.
Инструкция по применению Цефепима содержит следующие показания к применению препарата: инфекционные поражения мочевыделительного тракта (осложненные и неосложненные формы), фебрильная нейтропения, неосложненные инфекционные заболевания кожных покровов и прилежащих к ним мягких тканей.
Медикамент рекомендуется к применению при осложненных интраабдоминальных инфекционных поражениях (в комплексной терапии с метронидазолом).
Противопоказания
Цефепим не назначают при индивидуальной гиперчувствительности к активному компоненту, пенициллинам, цефалоспоринам, бета-лактамам.
Медикамент не назначают детям младше 2-х месяцев.
Побочные действия
Цефепим может вызывать аллергические реакции в виде лихорадки, зуда, эритематозных высыпаний на коже, токсического эпидермального некролиза, экссудативной мультиформной эритемы, анафилактоидных реакций.
На фоне лечения антибиотиком возможна регистрация положительной реакции Кумбса.
При внутримышечном введении отмечается болезненность и покраснение в зоне введения препарата; редко развиваются флебиты после внутривенного вливания.
Нервная система: судорожный синдром, головокружения, парестезии, спутанность сознания, ощущение тревоги и беспокойства, головная боль.
Мочевыделительный тракт: нарушения в функциональной работе почечной системы.
Пищеварительный тракт: диспепсические явления, псевдомембранозный колит, запоры, боли в эпигастрии, рвота, тошнота.
Органы кроветворения: редко отмечаются кровотечения на фоне антибактериальной терапии, анемия, лейкопения, снижение количества тромбоцитов, нейтрофилов.
Со стороны органов дыхательной системы наблюдается кашель.
Сердечно-сосудистая система: периферические отеки, учащенное сердцебиение, одышка.
Показатели лабораторно-инструментальных методов исследования: гиперкальциемия, повышение протромбинового времени, гипербилирубинемия, повышение уровня мочевины, ферментов печеночной системы и щелочной фосфатазы, регистрация гиперкреатининемии.
На фоне лечение возможно развитие орофарингеального кандидоза, астении, загрудинных болей, суперинфекции, боли в спине и горле.
Цефепим, инструкция по применению (Способ и дозировка)
Лекарство вводят инфузионно внутривенно (длительность вливания должна составлять не менее получаса). В некоторых случаях допускается внутримышечное введение медикамента (при заболеваниях мочеполовой системы, вызванных E. coli).
Лечение пневмонии: внутривенное введение 1-2 граммов антибиотика дважды в сутки в течение 10 дней.
Эмпирическая терапия фебрильной нейтропении: каждые 8 часов вводить по 2 грамма препарата внутривенно, лечение проводится до полного разрешения заболевания (в среднем 10 дней).
Лечение инфекционных поражений мочеполового тракта: внутривенное вливание 0,5-1 грамма цефепима каждые 12 часов, курс антибактериальной терапии рассчитан на 7-10 дней.
При тяжелом течении вышеуказанных заболеваний количество медикамента увеличивают до 2-х грамм, лечение рассчитано на 10 дней.
Пациентам, получающим гемодиализ, в первый день антибактериального лечения вводят 1 грамм цефепима, далее ежедневно вливают по 0,5 грамм (при фебрильной нейтропении дозу увеличивают до 1 грамма). Лекарственное средство рекомендуется вводить сразу после завершения сеанса гемодиализа.
Как разводить Цефепим для внутривенной инъекции: порошок перед вливанием растворяют в 5% растворе дектрозы (возможно применение раствора хлорида натрия 0,9%) до полного растворения. Перед внутримышечным введением препарат разводят в специальной воде для инъекции с бензиловым спиртом или парабеном. Возможно применение раствора лидокаина концентрации 0,5 и 1%.
Передозировка
Происходит усиление побочных эффектов. Симптомы передозировки: спутанность сознания, галлюцинации, ступор, кома, миоклония.
Лечение происходит по симптомам. Гемодиализ эффективен.
Взаимодействие
Цефепим способен повышать ототоксичность и усиливать побочное влияние на почечную систему при одновременном лечении аминогликозидами.
Антибиотик несовместим с гепарином и другими противомикробными препаратами. Лекарственное средство недопустимо вводить совместно с раствором метронидазола.
Условия продажи
Купить Цефепим можно в любой аптечной сети (обязательно предъявление рецептурного бланка с назначением врача).
Условия хранения
В недоступном для детей месте при температуре не более 25 градусов по Цельсию.
Готовый раствор антибиотика можно хранить не больше суток при комнатной температуре (при хранении в холодильнике срок увеличивается до 7 дней).
Срок годности
Не более трех лет.
Особые указания
Цефепим в таблетках не выпускается.
Медикамент отменяют при развитии псевдомембранозного колита с длительно протекающим диарейным синдромом (рекомендуется переход на метронидазол и ванкомицин).
У больных с аллергическими ответами в анамнезе на пенициллин возможно формирование перекрестной аллергической гиперчувствительности.
Пациентам с заболеваниями печеночной системы, почек требуется регулярный контроль над уровнем концентрации активного вещества в крови (коррекция режима дозирования проводится в соответствии с уровнем КК).
При смешанной форме анаэробно-аэробной инфекции рекомендуется дополнительное назначение антибактериальных препаратов до полной идентификации основных возбудителей.
На фоне лечения возможна регистрация ложноположительного результата при проведении теста на сахар в моче.
Антибактериальная активность лекарственного средства не теряется при изменении цвета приготовленного раствора.
Аналоги Цефепима
Совпадения по коду АТХ 4-го уровня:
Аналогами и синонимами можно назвать препараты: Максипим, Ладеф, Цепим, Мовизар, Эфипим.
Отзывы о Цефепиме
Отзывы о препарате указывают на хорошую переносимость и эффективность антибиотика при соблюдении предписаний лечащего врача.
Цена Цефепима, где купить
Цена Цефепима зависит от дозировки активного вещества (средняя стоимость 1 г флакона 100-200 рублей).
- Интернет-аптеки РоссииРоссия
ЛюксФарма* специальное предложение
-
Максипим 1г (Цефепим) фл. 1шт
ЗдравСити
-
Цефепим порошок для приг раствора для в/в и в/м введ. 1000мгПАО Биосинтез
-
Цефепим пор. д/приг. р-ра в/в и в/м введ. 1гБорисовский завод медицинских препаратов ОАО
-
Цефепим порошок для приг раствора для в/в и в/м введ. 1гПАО Красфарма
Аптека Диалог
-
Цефепим (фл. 1г в/в в/м)ДЕКО Компания
-
Цефепим (фл. 1г в/в в/м инд.уп.)БЗМП
-
Цефепим (фл. 1г в/в в/м инд.уп.)Красфарма ПАО
показать еще
Содержание
-
Структурная формула
-
Русское название
-
Английское название
-
Латинское название
-
Химическое название
-
Брутто формула
-
Фармакологическая группа вещества Цефепим
-
Нозологическая классификация
-
Код CAS
-
Фармакологическое действие
-
Характеристика
-
Фармакология
-
Применение вещества Цефепим
-
Противопоказания
-
Применение при беременности и кормлении грудью
-
Побочные действия вещества Цефепим
-
Взаимодействие
-
Передозировка
-
Способ применения и дозы
-
Меры предосторожности
-
Источники информации
-
Торговые названия с действующим веществом Цефепим
Структурная формула
Русское название
Цефепим
Английское название
Cefepime
Латинское название
Cefepimum (род. Cefepimi)
Химическое название
1-[[7-[[(2-Амино-4-тиазолил)(метоксиимино)ацетил]амино]-2-карбокси-8-оксо-5-тиа-1-азабицикло[4.2.0]окт-2-ен-3-ил]метил]-1-метилпирролидиния гидроксид (внутренняя соль)
Брутто формула
C19H24N6O5S2
Фармакологическая группа вещества Цефепим
Нозологическая классификация
Список кодов МКБ-10
-
A41.9 Септицемия неуточненная
-
G00.9 Бактериальный менингит неуточненный
-
J18 Пневмония без уточнения возбудителя
-
J20.9 Острый бронхит неуточненный
-
J42 Хронический бронхит неуточненный
-
K65 Перитонит
-
K81 Холецистит
-
L08.9 Местная инфекция кожи и подкожной клетчатки неуточненная
-
M60.0 Инфекционные миозиты
-
M65 Синовиты и тендосиновиты
-
M65.0 Абсцесс оболочки сухожилия
-
M71.0 Абсцесс синовиальной сумки
-
M71.1 Другие инфекционные бурситы
-
N12 Тубулоинтерстициальный нефрит, не уточненный как острый или хронический
-
N39.0 Инфекция мочевыводящих путей без установленной локализации
-
N73.9 Воспалительные болезни женских тазовых органов неуточненные
-
Z100* КЛАСС XXII Хирургическая практика
Код CAS
88040-23-7
Фармакологическое действие
—
антибактериальное, бактерицидное.
Характеристика
Цефепим в виде гидрохлорид представляет собой порошок от белого до бледно-желтого цвета, содержит в 1 мг не менее 825 и не более 911 мкг цефепима в расчете на безводное вещество. Хорошо растворим в воде.
Фармакология
Полусинтетическое цефалоспориновое антибактериальное средство для парентерального введения.
Механизм действия
Цефепим оказывает бактерицидное действие путем ингибирования синтеза бактериальной клеточной стенки. Цефепим обладает широким спектром активности in vitro в отношении многих грамположительных и грамотрицательных бактерий. В бактериальных клетках молекулярными мишенями цефепима являются ПСБ.
Фармакодинамика
Как и в случае с другими бета-лактамными противомикробными ЛС, было показано, что время, когда концентрация несвязанной формы цефепима в плазме превышает МПК для инфицирующего микроорганизма, наилучшим образом коррелирует с эффективностью на животных моделях инфекции. Однако взаимосвязь параметров фармакокинетики цефепима с его фармакодинамическими эффектами у пациентов не оценивалась.
Фармакокинетика
Выведение цефепима у здоровых добровольцев происходило главным образом путем почечной экскреции со средним T1/2 (± стандартное отклонение) (2±0,3) ч и общим клиренсом в организме (120±8) мл/мин. Фармакокинетика цефепима линейна в диапазоне доз от 250 мг до 2 г и не меняется в зависимости от продолжительности лечения. Отсутствуют доказательства накопления цефепима у здоровых взрослых добровольцев мужского пола (n=7), получавших клинически значимые дозы в течение 9 дней.
Фармакокинетические параметры после однократной 30-минутной в/в инфузий цефепима в дозах 500 мг, 1 и 2 г у здоровых взрослых добровольцев мужского пола (n=9) приведены в таблице 1.
Таблица 1
Средние фармакокинетические параметры (± стандартное отклонение) при в/в введении цефепима
| Параметр | 500 мг | 1 г | 2 г |
| Сmax, мкг/мл | 39,1 (3,5) | 81,7 (5,1) | 163,9 (25,3) |
| AUC, мкг·ч/мл | 70,8 (6,7) | 148,5 (15,1) | 284,8 (30,6) |
Фармакокинетические параметры после однократной в/м инъекции цефепима у здоровых взрослых добровольцев мужского пола (n=6) суммированы в таблице 2.
Таблица 2
Средние фармакокинетические параметры (± стандартное отклонение) при в/м введении цефепима
| Параметр | 500 мг | 1 г | 2 г |
| Сmax, мкг/мл | 13,9 (3,4) | 29,6 (4,4) | 57,5 (9,5) |
| Tmax, ч | 1,4 (0,9) | 1,6 (0,4) | 1,5 (0,4) |
| AUC, мкг·ч/мл | 60 (8) | 137 (11) | 262 (23) |
Абсорбция
После в/м введения цефепим полностью всасывается.
Распределение
Средний стационарный Vd цефепима составляет (18±2) л. Связывание цефепима с белками сыворотки крови составляет приблизительно 20% и не зависит от его концентрации в сыворотке. Цефепим выделяется с женским молоком в концентрации 0,5 мкг/мл. Грудной ребенок, потребляющий примерно 1000 мл женского молока в день, будет получать примерно 0,5 мг цефепима в день.
Таблица 3
Средняя концентрация цефепима в жидкостях и тканях организма
| Ткань или жидкость | Доза, путь введения | Количество пациентов | Среднее время забора проб после введения цефепима, ч | Средняя концентрация |
| Пузырная жидкость | 2 г, в/в | 6 | 1,5 | 81,4 мкг/мл |
| Слизистая оболочка бронхов | 2 г, в/в | 20 | 4,8 | 24,1 мкг/г |
| Мокрота | 2 г, в/в | 5 | 4 | 7,4 мкг/мл |
| Моча | 500 мг, в/в | 8 | 0–4 | 292 мкг/мл |
| 1 г, в/в | 12 | 0–4 | 926 мкг/мл | |
| 2 г, в/в | 12 | 0–4 | 3120 мкг/мл | |
| Желчь | 2 г, в/в | 26 | 9,4 | 17,8 мкг/мл |
| Перитонеальная жидкость | 2 г, в/в | 19 | 4,4 | 18,3 мкг/мл |
| Аппендикс | 2 г, в/в | 31 | 5,7 | 5,2 мкг/г |
| Желчный пузырь | 2 г, в/в | 38 | 8,9 | 11,9 мкг/г |
| Простата | 2 г, в/в | 5 | 1 | 31,5 мкг/г |
Метаболизм и выведение
Цефепим метаболизируется до N-метилпирролидона (NMП), который быстро превращается в N-оксид (NMП-N-оксид). Выведение неизмененного цефепима с мочой составляет примерно 85% от введенной дозы. Менее 1% введенной дозы определяется в моче в виде NMП, 6,8% в виде NMП-N-оксида и 2,5% в виде эпимера цефепима. Поскольку почечная экскреция является важным путем элиминации ЛС, пациентам с нарушением функции почек и пациентам, находящимся на гемодиализе, требуется коррекция дозы.
Особые группы пациентов
Пожилой возраст. Фармакокинетика цефепима была исследована у пожилых (65 лет и старше) мужчин (n=12) и женщин (n=12), средний Cl креатинина которых составлял (74±15) мл/мин. Наблюдалось снижение общего клиренса цефепима в организме в зависимости от Cl креатинина. Поэтому дозу цефепима у пожилых людей следует корректировать соответствующим образом, если Cl креатинина составляет ≤60 мл/мин.
Дети. Фармакокинетика цефепима была оценена у педиатрических пациентов от 2 мес до 11 лет после однократного и многократного введения каждые 8 (n=29) и каждые 12 ч (n=13) по назначению. После однократного в/в введения дозы общий клиренс в организме и Vss составили в среднем (3,3±1) мл/мин/кг и (0,3±0,1) л/кг соответственно. Выведение неизмененного цефепима с мочой составило (60,4±30,4)% от введенной дозы, а средний почечный клиренс — (2±1,1) мл/мин/кг. Не выявлено существенного влияния возраста или пола (25 пациентов мужского пола и 17 пациентов женского пола) на общий клиренс или Vd, скорректированные по массе тела. Не наблюдалось накопления при введении цефепима в дозе 50 мг/кг каждые 12 ч (n=13), в то время как Cmax, AUC и Т1/2 увеличивались примерно на 15% в равновесном состоянии после введения 50 мг/кг каждые 8 ч. Воздействие цефепима после в/в введения в дозе 50 мг/кг у детей сопоставимо с воздействием цефепима у взрослых при в/в дозе 2 г. Абсолютная биодоступность цефепима после в/м введения в дозе 50 мг/кг составила (82,3±15)% у 8 пациентов.
Нарушение функции почек. Фармакокинетика цефепима была исследована у пациентов с различной степенью нарушения функции почек (n=30). Средний T1/2 у пациентов, нуждающихся в гемодиализе, составлял (13,5±2,7) ч, а у пациентов, нуждающихся в непрерывном перитонеальном диализе, — (19±2) ч. Общий клиренс цефепима в организме снижался пропорционально Cl креатинина у пациентов с нарушением функции почек, что служит основой для рекомендаций по коррекции дозы у этой группы пациентов.
Нарушение функции печени. Фармакокинетика цефепима не изменялась у пациентов с нарушением функции печени, которые получали однократную дозу 1 г (n=11).
Микробиология
Антимикробная активность
Цефепим активен в отношении большинства изолятов следующих микроорганизмов, как in vitro, так и при клинических инфекциях.
Грамотрицательные бактерии: Enterobacter spp., Escherichia coli, Klebsiella pneumoniae, Proteus mirabilis, Pseudomonas aeruginosa.
Грамположительные бактерии: Staphylococcus aureus (только изоляты, чувствительные к метициллину), Streptococcus pneumoniae, Streptococcus pyogenes, стрептококки группы Viridans.
Имеются следующие данные in vitro, клиническая значимость которых неизвестна. По меньшей мере 90% следующих бактерий демонстрируют МПК in vitro, меньшую или равную пороговому значению чувствительности для цефепима в отношении изолятов аналогичного рода или группы организмов. Однако эффективность цефепима в лечении клинических инфекций, вызванных этими бактериями, не была установлена в ходе адекватных и хорошо контролируемых клинических исследований.
Грамположительные бактерии: Staphylococcus epidermidis (только изоляты, чувствительные к метициллину), Staphylococcus saprophyticus, Streptococcus agalactiae.
Большинство изолятов энтерококков, например Enterococcus faecalis, и метициллинрезистентных стафилококков устойчивы к цефепиму.
Грамотрицательные бактерии: Acinetobacter calcoaceticus, подвид lwoffii, Citrobacter diversus, Citrobacter freundii, Enterobacter agglomerans, Haemophilus influenzae, Hafnia alvei, Klebsiella oxytoca, Moraxella catarrhalis, Morganella morganii, Proteus vulgaris, Providencia rettgeri, Providencia stuartii, Serratia marcescens.
Цефепим неактивен в отношении многих изолятов Stenotrophomonas maltophilia.
Методы определения чувствительности
При наличии возможности лаборатория клинической микробиологии должна предоставлять врачу результаты тестов на чувствительность микроорганизмов in vitro к противомикробным ЛС, используемым в медицинских учреждениях (стационарах), в виде периодических отчетов, описывающих профиль чувствительности внутрибольничных и внебольничных патогенов. Эти отчеты должны помочь врачу в выборе соответствующего антибактериального ЛС для лечения.
Методы разведения
Для определения МПК антимикробных ЛС используются количественные методы. Эти МПК позволяют оценить чувствительность бактерий к противомикробным соединениям. МПК следует определять с использованием стандартизированного метода исследований (разведение в бульоне и/или агаре).
Диффузионые методы
Количественные методы, требующие измерения диаметра зоны, также дают предварительную оценку чувствительности бактерий к противомикробным соединениям. Размер зоны следует определять с использованием стандартизированного метода исследования. В этой процедуре для проверки чувствительности микроорганизмов к цефепиму используются бумажные диски, пропитанные 30 мкг цефепима.
Критерии интерпретации чувствительности микрорганизмов к цефепиму представлены в таблице 4.
Таблица 4
Критерии интерпретации тестов на чувствительность к цефепиму
| Патогенный микроорганизм | МПК, мкг/мл | Диаметр зоны по диско-диффузионному методу, мм | ||||
| Чувствительные | Умеренно резистентные | Резистентные | Чувствительные | Умеренно резистентные | Резистентные | |
| Enterobacteriaceae | ≤2 | 4–81 | ≥16 | ≥25 | 19–24 | ≤18 |
| Pseudomonas aeruginosa2 | ≤8 | − | ≥16 | ≥18 | − | ≤17 |
| Streptococcus pneumoniae3 (изоляты, не вызывающие менингита) | ≤1 | 2 | ≥4 | − | − | − |
| Streptococcus pyogenes | ≤0,5 | − | − | ≥24 | − | − |
| Стрептококки группы Viridans | ≤1 | 2 | ≥4 | ≥24 | 22–23 | ≤21 |
1 Для умеренно резистентных изолятов Enterobacteriaceae следует применять дозу 2 г каждые 8 ч у пациентов с нормальной функцией почек.
2 Для Pseudomonas aeruginosa следует применять дозу 2 г в/в каждые 8 ч у пациентов с нормальной функцией почек.
3 Для изолятов, не вызывающих менингита, МПК пенициллина <0,06 мкг/мл (или диаметр зоны для оксациллина >20 мм) может служить предиктором чувствительности к цефепиму.
Чувствительность стафилоккоков к цефепиму может быть оценена по тестам только с пенициллином и либо с цефокситином, или оксациллином.
Категория Чувствительные означает, что противомикробное ЛС, вероятно, будет подавлять рост возбудителя, если достигнет необходимой для этого концентрации в очаге инфекции. Результат Умеренно резистентный указывает на неоднозначность, и если микроорганизм не полностью чувствителен к альтернативным, клинически эффективным ЛС, тест следует повторить. Данная категория подразумевает возможность клинического применения в тех органах и тканях организма, где ЛС физиологически сконцентрировано, или в ситуациях, когда можно применять высокие дозы ЛС. Эта категория также обеспечивает буферную зону, которая предотвращает возникновение серьезных расхождений в интерпретации из-за небольших неконтролируемых технических факторов. Результат Резистентные указывает, что противомикробное ЛС вряд ли будет подавлять рост возбудителя при достижении концентрации, обычно наблюдаемой в очаге инфекции, и следует выбрать другую терапию.
Канцерогенез, мутагенез, влияние на фертильность репродуктивной функции
Исследования канцерогенности цефепима на животных не проводились.
В исследованиях хромосомных аберраций цефепим был положительным на кластогенность в первичных лимфоцитах человека, но отрицательным в клетках яичников китайского хомячка. В других тестах in vitro (мутация бактерий и клеток млекопитающих, восстановление ДНК в первичных гепатоцитах крыс и обмен хроматидами в лимфоцитах человека) цефепим был отрицательным на генотоксические эффекты. Кроме того, оценки цефепима in vivo у мышей (2 исследования на хромосомные аберрации и 2 микроядерных исследования) были отрицательными на кластогенность.
При п/к введении цефепима в дозах до 1000 мг/кг/сут (в 1,6 раза выше МРДЧ в рачете на площадь поверхности тела) у крыс не наблюдалось неблагоприятного воздействия на фертильность.
Клинические исследования
Фебрильная нейтропения
Безопасность и эффективность эмпирической монотерапии цефепимом у пациентов с фебрильной нейтропенией оценивали в двух многоцентровых рандомизированных исследованиях, в которых сравнивали применение монотерапии цефепимом (2 г в/в каждые 8 ч) и цефтазидимом (2 г в/в каждые 8 ч). В этих исследованиях приняли участие 317 пациентов, подлежавших оценке (таблица 5).
Таблица 5
Демографические данные пациентов, подлежавших оценке (только первые эпизоды)
| Показатель | Цефепим (n=164) | Цефтазидим (n=153) |
| Средний возраст, лет | 56 (от 18 до 82) | 55 (от 16 до 84) |
| Мужчины | 86 (52%) | 85 (56%) |
| Женщины | 78 (48%) | 68 (44%) |
| Лейкемия | 65 (40%) | 52 (34%) |
| Другие гематологические злокачественные новообразования | 43 (26%) | 36 (24%) |
| Сóлидная опухоль | 54 (33%) | 56 (37%) |
| Среднее абсолютное снижение числа нейтрофилов, клетки/мкл | 20 (диапазон от 0 до 500) | 20 (диапазон от 0 до 500) |
| Средняя продолжительность нейтропении, дни | 6 (диапазон от 0 до 39) | 6 (диапазон от 0 до 32) |
| Внутренний венозный катетер | 97 (59%) | 86 (56%) |
| Профилактический прием антибактериальных ЛС | 62 (38%) | 64 (42%) |
| Трансплантат костного мозга | 9 (5%) | 7 (5%) |
| сАД меньше 90 мм рт.ст. | 7 (4%) | 2 (1%) |
Таблица 6
Объединенные показатели ответа на эмпирическую терапию у пациентов с фебрильной нейтропенией
| Итоговый показатель | Доля ответа на эмпирическую терапию, % | |
| Цефепим (n=164) | Цефтазидим (n=153) | |
| Первичный эпизод разрешен без изменений в лечении, новых лихорадочных эпизодов или инфекции, а пероральный прием антибиотиков позволил завершить лечение | 51 | 55 |
| Первичный эпизод разрешен без изменений в лечении, новых лихорадочных эпизодов или инфекции и без перорального приема антибиотиков после лечения | 34 | 39 |
| Выживание, любая разрешенная модификация лечения | 93 | 97 |
| Первичный эпизод разрешен без изменений в лечении, и пероральный прием антибиотиков позволил завершить лечение | 62 | 67 |
| Первичный эпизод разрешен без изменений в лечении и без перорального приема антибиотиков после лечения | 46 | 51 |
Существует недостаточно данных, подтверждающих эффективность монотерапии цефепимом у пациентов с высоким риском развития тяжелой инфекции (включая пациентов с недавней трансплантацией костного мозга в анамнезе, артериальной гипотензией, обусловленной гематологической злокачественной опухолью, или с тяжелой или длительной нейтропенией). Данные о пациентах с септическим шоком отсутствуют.
Осложненные внутрибрюшные инфекции
Пациенты, госпитализированные с осложненными внутрибрюшными инфекциями, участвовали в рандомизированном двойном слепом многоцентровом исследовании, в котором сравнивали применение комбинации цефепима (2 г каждые 12 ч) с метронидазолом (в/в, 500 мг каждые 6 ч) и комбинации имипенем + циластатин (500 мг каждые 6 ч) в течение максимальной продолжительности терапии, равной 14 дням. Исследование было проведено для демонстрации эквивалентности двух методов лечения. Первичные анализы были проведены у популяции, состоящей из пациентов с хирургически подтвержденной осложненной инфекцией по крайней мере с одним изолятом патогена, выделенного до лечения, в течение 5 дней лечения и 4–6 нед наблюдения после лечения. Пациенты в группе получавших комбинацию имипенем + циластатин имели более высокие показатели по шкале APACHE II в исходном состоянии. В остальном группы лечения были в целом сопоставимы по своим характеристикам до лечения. Общая частота клинического излечения среди пациентов с первичным анализом составила 81% (51 вылеченных из 63 оцениваемых пациентов) в группе получавших комбинацию цефепим + метронидазол и 66% (62 из 94) в группе получавших комбинацию имипенем + циластатин. Наблюдаемые различия в эффективности, возможно, были обусловлены большей долей пациентов с высокими показателями по шкале APACHE II в группе получавших комбинацию имипенем + циластатин.
Применение вещества Цефепим
Пневмония (средней и тяжелой степени), вызванная чувствительными штаммами Streptococcus pneumoniae, включая случаи, связанные с одновременной бактериемией Pseudomonas aeruginosa, Klebsiella pneumoniae или видами Enterobacter.
Фебрильная нейтропения (эмпирическая монотерапия у пациентов с высоким риском развития тяжелой инфекции, включая пациентов с недавней трансплантацией костного мозга в анамнезе, артериальной гипотензией на момент первичного осмотра, гематологической злокачественной опухолью или тяжелой или длительной нейтропенией. Существует недостаточно данных, подтверждающих эффективность монотерапии цефепимом у таких пациентов).
Неосложненные и осложненные инфекции мочевыводящих путей (включая пиелонефрит), вызванные чувствительными изолятами Escherichia coli или Klebsiella pneumoniae, когда инфекция тяжелая, или Escherichia coli, Klebsiella pneumoniae или Proteus mirabilis, когда тяжесть инфекции от легкой до умеренной, включая случаи, связанные с одновременной бактериемией, вызванной этими бактериями.
Неосложненные инфекции кожи, вызванные золотистым стафилококком (только изоляты, чувствительные к метициллину) или Streptococcus pyogenes.
Осложненные внутрибрюшные инфекции (в комбинации с метронидазолом) у взрослых, вызванные чувствительными изолятами Escherichia coli, стрептококками группы Viridans, Pseudomonas aeruginosa, Klebsiella pneumoniae, Enterobacter species или Bacteroides fragilis.
Для уменьшения развития устойчивых к лечению бактерий и сохранения эффективности цефепима его следует использовать только для лечения инфекций, которые, как доказанно или сильно подозревается, вызваны чувствительными бактериями. Информацию о культуре и чувствительности следует учитывать при выборе или изменении антибактериальной терапии. В отсутствие таких данных эмпирическому выбору терапии могут способствовать местные эпидемиологические данные и особенности восприимчивости.
Противопоказания
Реакции гиперчувствительности немедленного типа к цефепиму или другим антибактериальным ЛС класса цефалоспоринов, пенициллинам или другим бета-лактамным антибиотикам.
Применение при беременности и кормлении грудью
Категория действия на плод по FDA — В.
Адекватных и хорошо контролируемых исследований применения цефепима у беременных женщин не проводилось. Поскольку исследования репродукции животных не всегда позволяют предсказать реакцию человека, цефепим следует применять во время беременности только в случае явной необходимости.
Цефепим не оказывал тератогенное или эмбриоцидное действие при введении в период органогенеза крысам в дозах до 1000 мг/кг/сут (в 1,6 раза выше МРДЧ в расчете на площадь поверхности тела) или мышам в дозах до 1200 мг/кг (примерно равна МРДЧ в расчете на площадь поверхности тела), или кроликам в дозе 100 мг/кг (0,3 МРДЧ в расчете на площадь поверхности тела).
Цефепим не изучался для применения во время родов. Лечение следует назначать только по строгим показаниям.
Цефепим выделяется с женским грудным молоком. Следует соблюдать осторожность при назначении цефепима кормящей женщине.
Побочные действия вещества Цефепим
Опыт клинических исследований
Поскольку клинические исследования проводятся в различных условиях, частота побочных реакций, наблюдаемых в одном клиническом исследовании ЛС, не может быть напрямую сопоставлена с данными, получеными в другом клиническом исследовании, и может не отражать показатели, наблюдаемые на практике.
В клинических исследованиях с применением нескольких доз цефепима 4137 пациентов получали рекомендованные дозы (от 500 мг до 2 г в/в каждые 12 ч). Не выявлено случаев смерти или постоянной инвалидности, предположительно связанных с побочными действиями цефепима. Из-за побочных реакций прекратили применение 64 (1,5%) пациента, 33 (51%) из них сделали это из-за сыпи. Доля пациентов, получавших цефепим, которые прекратили его применение из-за побочных реакций, была аналогичной при ежедневных дозах 500 мг, 1 и 2 г каждые 12 ч (0,8; 1,1 и 2% соответственно). Однако частота прекращения применения цефепима из-за сыпи увеличивалась с увеличением рекомендуемых доз.
Побочные реакции цефепима при введении в многократных дозах (данные клинических исследований в Северной Америке, n=3125), отмечавшиеся с частотой ≥1%, включали местные побочные реакции (3%), включая флебит (1,3%), боль и/или воспаление (0,6%) и сыпь (1,1%).
С частотой менее 1%, но более 0,1% отмечались колит (включая псевдомембранозный), диарея, эритема, лихорадка, головная боль, тошнота, монилиоз полости рта, зуд, крапивница, вагинит, рвота, анемия.
При более высокой дозе (2 г каждые 8 ч) частота побочных реакций была выше у 795 пациентов, получавших эту дозу цефепима. Побочные реакции представляли собой сыпь (4%), диарею (3%), тошноту (2%), рвоту (1%), зуд (1%), лихорадку (1%) и головную боль (1%).
Отклонения в результатах лабораторных обследований, отмечавшиеся с частотой ≥1%, включали положительный тест Кумбса (без гемолиза) (16,2%), снижение уровня фосфора (2,8%), повышение уровня АЛТ (2,8%), АСТ (2,4%), эозинофилию (1,7%), аномальное АЧТВ (1,6%) и ПВ (1,4%).
С частотой менее 1%, но более 0,1% отмечались повышенный уровень ЩФ, мочевины крови, кальция, креатинина, фосфора, калия, общего билирубина; снижение уровня кальция (гипокальциемия чаще наблюдалась у пожилых пациентов, не сообщалось о клинически значимых последствиях изменения уровня кальция или фосфора), гематокрита, количества нейтрофилов, тромбоцитов, лейкоцитов.
Опыт пострегистрационных наблюдений
Во время клинического применения цефепима после регистрации были выявлены приведенные ниже побочные реакции, однако поскольку эти реакции регистрируются в добровольном порядке в популяции неопределенного размера, не всегда возможно достоверно оценить их частоту или установить причинно-следственную связь с воздействием ЛС. В дополнение к побочным реакциям, о которых сообщалось в ходе клинических исследований, в ходе пострегистрационного применения были зарегистрированы следующие побочные реакции. Сообщалось о развитии энцефалопатии (нарушение сознания, включая спутанность сознания, галлюцинации, ступор и кому), афазии, миоклонуса, судорог и эпилептического состояния без судорог. Сообщалось о случаях анафилаксии, включая анафилактический шок, транзиторной лейкопении, нейтропении, агранулоцитоза и тромбоцитопении.
Побочные реакции, характерные для ЛС класса цефалоспоринов
В дополнение к перечисленным выше побочным реакциям, которые наблюдались у пациентов, получавших цефепим, сообщалось о следующих побочных реакциях и изменениях лабораторных параметров, отмечавшихся при применении антибактериальных ЛС класса цефалоспоринов: синдром Стивенса-Джонсона, мультиформная эритема, токсический эпидермальный некролиз, дисфункция почек, токсическая нефропатия, апластическая анемия, гемолитическая анемия, кровотечение, дисфункция печени, включая холестаз, и панцитопения.
Взаимодействие
Влияние на лабораторные тесты
Введение цефепима может привести к ложноположительной реакции на глюкозу в моче при определенных методах. Рекомендуется использовать тесты на глюкозу, основанные на ферментативных реакциях глюкозооксидазы.
Во время лечения цефепимом сообщалось о положительных прямых тестах Кумбса. При развитии гемолитической анемии необходимо прекратить применение цефепима и назначить соответствующую терапию. Положительный тест Кумбса может наблюдаться у новорожденных, матери которых получали ЛС цефалоспоринового ряда до родов.
Применение многих цефалоспоринов, включая цефепим, было связано со снижением активности протромбина. К группе риска относятся пациенты с почечной или печеночной недостаточностью или плохим питанием, а также получающие длительный курс противомикробной терапии. У пациентов из группы риска следует контролировать ПВ и назначать экзогенный витамин К по показаниям.
Лекарственные взаимодействия
Аминогликозиды. Необходимо контролировать функцию почек, если аминогликозиды должны вводиться одновременно с цефепимом из-за повышенного потенциала нефротоксичности и ототоксичности аминогликозидных антибактериальных ЛС.
Диуретики. Сообщалось о нефротоксичности после одновременного применения других цефалоспоринов с сильнодействующими диуретиками, такими как фуросемид. Необходимо контролировать функцию почек при одновременном применении цефепима с сильнодействующими диуретиками.
Передозировка
Симптомы: энцефалопатия (нарушение сознания, включая спутанность сознания, галлюцинации, ступор и кому), миоклонус, судороги, нервно-мышечная возбудимость и эпилептический неконвульсивный статус.
Лечение: пациенты при передозировке цефепима должны находиться под тщательным наблюдением и получать поддерживающее лечение. При наличии почечной недостаточности рекомендуется проводить гемодиализ или перитонеальный диализ, чтобы помочь в выведении цефепима из организма.
Способ применения и дозы
В/в, в/м. При в/в применении продолжительность введения должна составлять примерно 30 минут. Максимальная доза для педиатрических пациентов не должна превышать рекомендуемую дозу для взрослых.
Необходимо корректировать дозу у пациентов с Cl креатинина ≤60 мл/мин, чтобы компенсировать более медленную скорость выведения почками. У этих пациентов рекомендуемая начальная доза цефепима должна быть такой же, как у пациентов с Cl креатинина >60 мл/мин, за исключением пациентов, находящихся на гемодиализе.
У пациентов, проходящих непрерывный амбулаторный перитонеальный диализ, цефепим может вводиться в рекомендуемых дозах с интервалом дозирования каждые 48 ч. У пациентов, находящихся на гемодиализе, примерно 68% от общего количества цефепима, присутствующего в организме в начале диализа, будет удалено в течение 3 ч периода диализа.
Меры предосторожности
Реакции гиперчувствительности
Перед началом применения цефепима следует провести тщательное исследование, чтобы определить, были ли у пациента ранее реакции гиперчувствительности немедленного типа на цефепим, цефалоспорины, пенициллины или другие бета-лактамы. Необходимо соблюдать осторожность, если цефепим назначается пациентам, чувствительным к пенициллину, поскольку перекрестная гиперчувствительность к бета-лактамным антибактериальным ЛС была четко задокументирована и может возникать у пациентов с аллергией на пенициллин в анамнезе с частотой до 10%. Если возникает аллергическая реакция на цефепим, необходимо прекратить его применение и принять соответствующие поддерживающие меры.
Нейротоксичность
Сообщалось о серьезных побочных реакциях, включая опасные для жизни или смертельные случаи развития энцефалопатии (нарушение сознания, включая спутанность сознания, галлюцинации, ступор и кому), афазии, миоклонуса, судорог и эпилептического статуса без судорог. Большинство таких случаев наблюдалось у пациентов с нарушением функции почек, которые не получали соответствующей коррекции дозы. Однако некоторые случаи нейротоксичности отмечались у пациентов со скорректированной дозой, соответствующей степени их почечной недостаточности. В большинстве случаев симптомы нейротоксичности были обратимыми и исчезали после отмены цефепима и/или после гемодиализа. При возникновении нейротоксичности, связанной с терапией цефепимом, необходимо прекратить его применение и принять соответствующие поддерживающие меры.
Диарея, ассоциированная с Clostridium difficile
Сообщалось о развитии диареи, связанной с Clostridium difficile, при использовании почти всех антибактериальных ЛС, включая цефепим, которая может варьировать по степени тяжести от легкой диареи до смертельного колита. Лечение антибактериальными ЛС изменяет нормальную флору толстой кишки, приводя к чрезмерному росту Clostridium difficile, которая продуцирует токсины А и В, способствующие развитию диареи.
Штаммы Clostridium difficile, продуцирующие гипертоксин, вызывают повышенную заболеваемость и смертность, поскольку эти инфекции могут быть невосприимчивы к противомикробной терапии и потребовать проведения колэктомии. Диарею, ассоциированную с Clostridium difficile, необходимо учитывать у всех пациентов, у которых наблюдается диарея после применения антибактериальных ЛС. Необходим тщательный сбор анамнеза, поскольку сообщалось, что диарея, связанная с Clostridium difficile, может возникать в течение 2 мес после введения антибактериальных ЛС. При подозрении или подтверждении диареи, связанной с Clostridium difficile, возможно, потребуется прекратить постоянное применение антибактериальных ЛС, не направленных против Clostridium difficile. По клиническим показаниям следует назначить соответствующее дополнительное введение жидкости и электролитов, белковых добавок, а также лечение антибиотиками и хирургическое обследование.
Развитие устойчивых к ЛС бактерий
Назначение цефепима в отсутствие доказанной или сильно подозреваемой бактериальной инфекции не принесет пользу пациенту и увеличивает риск развития лекарственно-устойчивых бактерий. Как и в случае с другими противомикробными ЛС, длительное применение цефепима может привести к чрезмерному росту невосприимчивых микроорганизмов. Необходима повторная оценка состояния пациента. В случае возникновения суперинфекции во время терапии следует принять соответствующие меры.
Особые группы пациентов
Дети. Безопасность и эффективность применения цефепима при лечении неосложненных и осложненных инфекций мочевыводящих путей (включая пиелонефрит), неосложненных инфекций кожи и кожных структур, пневмонии, а также в качестве эмпирической терапии для пациентов с фебрильной нейтропенией были установлены в возрастных группах от 2 мес до 16 лет. Использование цефепима в этих возрастных группах подтверждается данными адекватных и хорошо контролируемых исследований цефепима у взрослых и дополнительными данными о фармакокинетике и безопасности, полученными в педиатрических исследованиях. Безопасность и эффективность у педиатрических пациентов в возрасте до 2 мес не установлены. Существует недостаточно клинических данных, подтверждающих применение цефепима у педиатрических пациентов для лечения серьезных инфекций в детской популяции, где подозреваемым или доказанным возбудителем является H.influenzae типа b. У тех пациентов, у которых имеется менингеальный посев из отдаленного очага инфекции или подозревается или задокументирован менингит, следует использовать альтернативное средство с доказанной клинической эффективностью в этих условиях.
Пожилой возраст. Из более чем 6400 взрослых, получавших цефепим в клинических исследованиях, 35% были старше 65 лет, а 16% — старше 75 лет. Когда пожилые пациенты получали обычную рекомендуемую дозу для взрослых, клиническая эффективность и безопасность были сопоставимы с клинической эффективностью и безопасностью у взрослых пациентов.
Серьезные побочные явления отмечались у пожилых пациентов с почечной недостаточностью, получавших нескорректированные дозы цефепима, включая опасные для жизни или смертельные случаи следующих заболеваний: энцефалопатия, миоклонус и судороги. Известно, что цефепим в значительной степени выводится почками, и риск побочных реакций на этот препарат может быть выше у пациентов с нарушением функции почек. Поскольку у пожилых пациентов более вероятно снижение функции почек, следует соблюдать осторожность при выборе дозы и контролировать функцию почек.
Нарушение функции почек. Необходимо скорректировать дозу цефепима у пациентов с Cl креатинина ≤60 мл/мин, чтобы компенсировать более медленную скорость выведения почками.
Источники информации
www.fda.gov и www.rxlist.com, 2021.
Торговые названия с действующим веществом Цефепим
| Торговое название | Цена за упаковку, руб. |
|---|---|
| Кефсепим |
439.00 |
| Цефепим |
от 155.30 до 218.00 |
| Цефомакс |
149.90 |
Цефепим — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-005926
Торговое наименование:
Цефепим
Международное непатентованное или группировочное наименование:
цефепим
Лекарственная форма:
порошок для приготовления раствора для внутривенного и внутримышечного введения
Состав
на 1 флакон:
| 0,5 г | 1,0 г | 2,0 г | |
|
Действующее вещество: |
|||
|
Цефепима гидрохлорида моногидрат |
0,5945 г |
1,1891 г |
2,3782 г |
|
(в пересчете на цефепим) |
0,5 г |
1,0 г |
2,0 г |
| Вспомогательное вещество: | |||
| L-аргинин |
0,3625 г |
0,725 г |
1,450 г |
Описание:
белый или белый с желтоватым оттенком кристаллический порошок
Фармакотерапевтическая группа:
антибиотик-цефалоспорин
Код ATX:
J01DE01
Фармакологические свойства
Фармакодинамика
Цефепим является цефалоспориновым антибиотиком широкого спектра действия. Цефепим подавляет синтез белков клеточной стенки бактерий, обладает широким спектром бактерицидного действия в отношении различных грамположительных и грамотрицательных бактерий, в том числе большинства штаммов, резистентных к аминогликозидам или цефалоспориновым антибиотикам третьего поколения, таким как цефтазидим. Цефепим высоко устойчив к гидролизу большинством бета-лактамаз, он имеет низкое сродство к бета-лактамазам и быстро проникает в клетки грамотрицательных бактерий. Доказано, что цефепим обладает очень высоким сродством к пенициллин-связывающему белку (ПСБ) типа 3, высоким сродством -к ПСБ типа 2 и умеренным сродством — к ПСБ типов 1а и 1б. Цефепим оказывает бактерицидное действие в отношении широкого спектра бактерий. Цефепим активен в отношении следующих микроорганизмов:
Грамположителъные аэробы:
Staphylococcus aureus (включая штаммы, продуцирующие бета-лактамазу);
Staphylococcus epidermidis (включая штаммы, продуцирующие бета-лактамазу);
другие штаммы Staphylococcus spp., включая Staphylococcus hominis, Staphylococcus saprophyticus;
Streptococcus pyogenes (стрептококки группы A);
Streptococcus agalactiae (стрептококки группы В);
Streptococcus pneumoniae (включая штаммы со средней устойчивостью к пенициллину — минимальная подавляющая концентрация от 0,1 до 1 мкг/мл);
другие бета-гемолитические Streptococcus spp. (группы С, G, F), Streptococcus bovis (группа D), Streptococcus spp. группы viridans.
Примечание: большинство штаммов энтерококков, например, Enterococcus faecalis, и стафилококки, резистентные к метициллину, устойчивы к действию большинства цефалоспориновых антибиотиков, включая цефепим.
Грамотрицательные аэробы:
Acinetobacter calcoaceticus (подштаммы anitratus, Iwoffii);
Aeromonas hydrophila;
Capnocytophaga spp.;
Citrobacter spp., включая Citrobacter diversus, Citrobacter freundii,
Campylоbасter jejuni;
Enterobacter spp., включая Enterobacter cloacae, Enterobacter aerogenes, Enterobacter sakazakii;
Escherichia coli;
Gardnerella vaginalis;
Haemophilus ducreyi;
Haemophilus influenzae (включая штаммы, продуцирующие бета-лактамазу);
Haemophilus parainfluenzae;
Hafnia alvei;
Klebsiella spp., включая Klebsiella pneumoniae, Klebsiella oxytoca, Klebsiella ozaenae;
Legionella spp.;
Morganella morganii;
Moraxella catarrhalis (Branhamella catarrhalis) (включая штаммы, продуцирующие бета-лактамазы);
Neisseria gonorrhoeae (включая штаммы, продуцирующие бета-лактамазу);
Neisseria meningitidis;
Pantoea agglomerans (ранее известный как Enterobacter agglomerans);
Proteus spp., включая Proteus mirabilis, Proteus vulgaris;
Providencia spp., включая Providencia rettgeri, Providencia stuartii;
Pseudomonas spp., включая Pseudomonas aeruginosa, Pseudomonas putida, Pseudomonas stutzeri, Salmonella spp.;
Serratia, включая Serratia marcescens, Serratia liquefaciens;
Shigella spp.;
Yersinia enterocolitica.
Примечание: цефепим неактивен в отношении многих штаммов Stenotrophomonas maltophilia, ранее известных как Xanthomonas maltophilia и Pseudomonas maltophilia).
Анаэробы:
Bacteroides spp.;
Clostridium perfringens;
Fusobacterium spp.;
Mobiluncus spp.;
Peptostreptococcus spp.;
Prevotella melaninogenica (известный как Bacteroides melaninogenicus);
Veillonella spp.
Примечание: цефепим неактивен в отношении Bacteroides fragilis и Clostridium difficile.
Фармакокинетика
Средние концентрации цефепима в плазме крови взрослых здоровых мужчин в различные сроки после однократного внутривенного введения в течение 30 мин до 12 ч и максимальная концентрация (Сmах) приведены ниже в таблице.
Средние концентрации цефепима в плазме (мкг/мл) после внутривенного введения
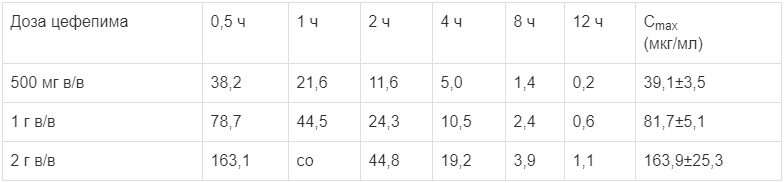
Сmах и время достижения максимальной концентрации (Тmах) после однократного внутримышечного введения приведены ниже в таблице.
Средние концентрации цефепима в плазме (мкг/мл) после внутримышечного введения
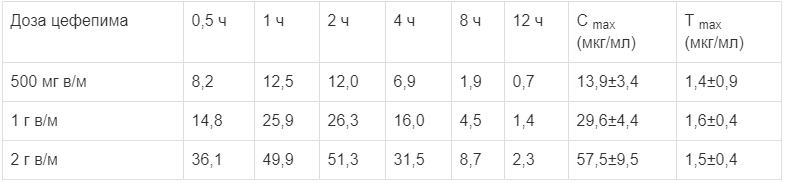
Цефепим метаболизируется в N-метилпирролидин, который быстро превращается в оксид N-метилпирролидина.
Цефепим выводится преимущественно почками, путем клубочковой фильтрации (почечный клиренс составляет в среднем 110 мл/мин). В моче обнаруживается приблизительно 85 % от введенной дозы неизмененного цефепима, менее 1 % N-метилпирролидина, около 6,8 % оксида N-метилпирролидина и около 2,5 % эпимера цефепима.
После введения доз от 250 мг до 2 г период полувыведения цефепима из организма составляет в среднем около 2 часов. Общий клиренс составляет в среднем 120 мл/мин. При внутривенном ведении препарата здоровым добровольцам в дозе 2 г каждые 8 часов в течение 9 дней кумуляции препарата не наблюдалось.
Пациенты с нарушениями функции почек
Период полувыведения из организма при почечной недостаточности увеличивается, при этом наблюдается линейная зависимость между общим клиренсом и клиренсом креатинина. При тяжёлых нарушениях функции почек, требующих проведения сеансов диализа, период полувыведения составляет в среднем 13 часов при гемодиализе и 19 часов при непрерывном перитонеальном диализе. При нарушенной функции почек требуется корректировка дозы.
Пациенты с нарушениями функции печени
Фармакокинетика цефепима у пациентов с нарушенной функцией печени не изменяется. Корректировки дозы для таких пациентов не требуется.
Пациенты старше 65 лет
После однократного внутривенного введения 1 г препарата здоровым добровольцам старше 65 лет отмечалось увеличение площади под кривой зависимости «концентрация-время» (AUC) и уменьшение почечного клиренса по сравнению с молодыми добровольцами. При нарушенной функции почек пациентам старшего возраста требуется корректировка дозы.
Дети
Фармакокинетика препарата исследовалась у детей в возрасте от 2 месяцев до 11 лет после однократного введения дозы 50 мг/кг массы тела внутривенно или внутримышечно, а также после повторного введения препарата (каждые 8-12 часов, в течение не менее 48 часов). После однократного внутривенного введения общий клиренс и объем распределения составляли 3,3 мл/мин/кг и 0,3 л/кг, соответственно. Период полувыведения из организма составлял в среднем 1,7 ч. Выведение цефепима в неизмененном виде почками составляло 60,4 % от введенной дозы, а почечный клиренс — в среднем 2,0 мл/мин/кг.
После многократного внутривенного введения концентрация цефепима в плазме крови в равновесном состоянии, а также другие фармакокинетические параметры не отличались от таковых после однократного введения. Возраст и пол пациентов не оказывали существенного влияния на общий клиренс и объем распределения с учетом поправки на массу тела. После внутримышечного введения максимальная концентрация цефепима в плазме крови в равновесном состоянии составляла в среднем 68 мкг/мл и достигалась в среднем за 0,75 ч. Через 8 ч после внутримышечного введения концентрации цефепима в плазме крови составляли в среднем 6 мкг/мл. Абсолютная биодоступность цефепима после внутримышечной инъекции составляла в среднем 82 %.
Концентрации препарата в спинномозговой жидкости (СМЖ) и в плазме крови у детей с бактериальным менингитом
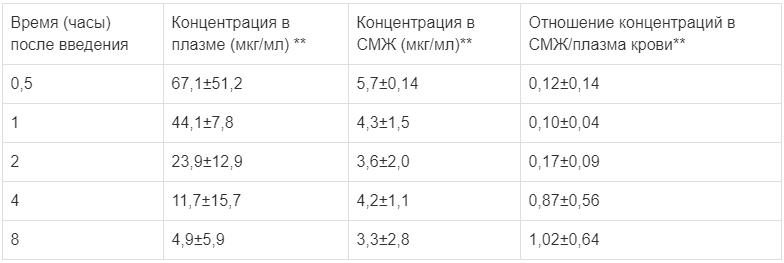
Показания к применению
Инфекционно-воспалительные заболевания, вызванные чувствительными к цефепиму микроорганизмами, у взрослых:
— Инфекции нижних дыхательных путей, включая пневмонию и бронхит;
— Инфекции мочевыводящих путей, как осложнённые, включая пиелонефрит, так и неосложнённые;
— Инфекции кожи и мягких тканей;
— Инфекции брюшной полости, включая перитонит и инфекции желчных путей;
— Гинекологические инфекции;
— Септицемия;
— Фебрильная нейтропения.
Профилактика возможных инфекций при проведении полостных хирургических операций.
Инфекционно-воспалительные заболевания, вызванные чувствительными к цефепиму микроорганизмами, у детей:
— Пневмония;
— Инфекции мочевых путей, как осложнённые, включая пиелонефрит, так и неосложнённые;
— Инфекции кожи и мягких тканей;
— Септицемия;
— Фебрильная нейтропения;
— Бактериальный менингит.
Противопоказания
Гиперчувствительность к цефепиму или L-аргинину, а также к антибиотикам цефалоспориновой группы, пенициллинам или другим бета-лактамным антибиотикам.
Детский возраст до 2-х месяцев.
С осторожностью
Заболевания желудочно-кишечного тракта в анамнезе (особенно колит), почечная недостаточность (клиренс креатинина менее 60 мл/мин).
Применение при беременности и в период грудного вскармливания
Адекватных и контролируемых клинических исследований у беременных женщин не проводилось. При беременности следует применять препарат только в том случае, если предполагаемая польза для матери превышает потенциальный риск для плода.
Цефепим обнаруживается в грудном молоке в очень низких концентрациях.
В период грудного вскармливания следует применять препарат только в том случае, если предполагаемая польза для матери превышает потенциальный риск для ребенка.
Способ применения и дозы
Цефепим может вводиться внутривенно (в/в) или внутримышечно (в/м). Дозы и путь введения зависят от чувствительности возбудителей, тяжести инфекции, состояния функции почек и общего состояния пациента. Внутривенный путь введения рекомендуется для пациентов с тяжёлыми или угрожающими жизни инфекциями, особенно при угрозе возникновения септического шока. Внутримышечно доза до 1 г (объем <3,1 мл) может быть введена как однократная инъекция. Максимальную дозу (2 г/6,2 мл) следует вводить в виде двух инъекций в разные места.
Для детей доза не должна превышать максимальную рекомендуемую дозу для взрослых (2 г в/в каждые 8 часов). Опыт внутримышечного введения цефепима детям ограничен.
Взрослым и детям с массой тела более 40 кг при нормальной функции почек
|
Инфекции мочевых путей, легкой и средней тяжести |
0,5 г-1 г в/в или в/м |
Каждые 12 часов |
|
Другие инфекции, легкой и средней тяжести |
1 г в/в или в/м |
Каждые 12 часов |
|
Тяжелые инфекции |
2 г в/в |
Каждые 12 часов |
|
Очень тяжелые и угрожающие жизни инфекции |
2 г в/в |
Каждые 8 часов |
Обычная продолжительность лечения составляет 7-10 дней; тяжёлые инфекции могут потребовать более продолжительного лечения.
В случае лечения фебрильной нейтропении обычная продолжительность лечения составляет 7 дней или до исчезновения нейтропении.
Профилактика возможных инфекций при проведении хирургических операций
За 60 минут до начала хирургической операции вводится 2 г препарата внутривенно в виде инфузии в течение 30 минут. Сразу после окончания инфузии вводится 500 мг метронидазола внутривенно. Вследствие несовместимости метронидазола и цефепима их не следует вводить одновременно или смешивать. Инфузионную систему перед введением метронидазола следует промыть (см. «Внутривенное введение»). Раствор метронидазола следует приготовить в соответствии с инструкцией по применению метронидазола. Во время длительных (более 12 часов) хирургических операций через 12 часов после первой дозы рекомендуется повторное введение в той же дозе препарата Цефепим с последующим введением метронидазола.
Дети от 2 месяцев с массой тела до 40 кг
Обычная рекомендуемая доза при инфекциях мочевых путей, инфекциях кожи и мягких тканей, пневмонии составляет 50 мг/кг каждые 12 часов в течение 10 дней. В случае тяжелых инфекций — каждые 8 часов. Пациентам с фебрильной нейтропенией, септицемией, бактериальным менингитом следует вводить 50 мг/кг каждые 8 часов в течение 7-10 дней.
Пациенты с нарушением функции почек
Пациентам с нарушенной функцией почек требуется корректировка дозировки цефепима с целью компенсации уменьшенной скорости выведения препарата с мочой. Режим дозирования должен назначаться в зависимости от степени почечной недостаточности, тяжести инфекции и чувствительности микроорганизмов. У пациентов со слабым или умеренным нарушением функции почек исходная доза препарата должна быть такой же, как у пациентов с нормальной функцией почек.
Рекомендуемые поддерживающие дозы цефепима представлены в таблице. Клиренс креатинина для мужчин можно рассчитать исходя из концентрации сывороточного креатинина по следующей формуле:
Клиренс креатинина для женщин можно рассчитать, умножив полученное значение на 0,85.
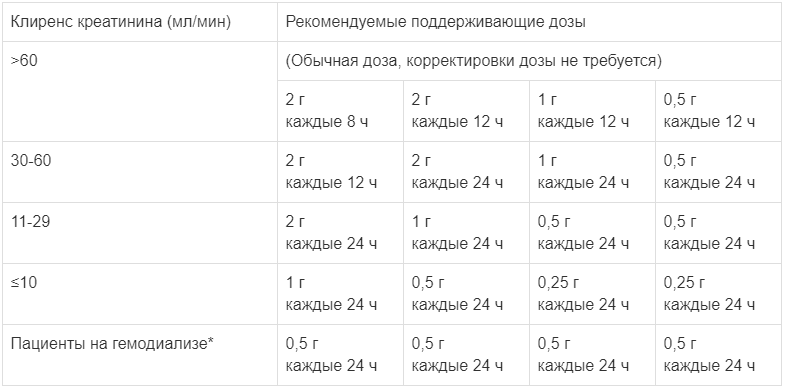
При гемодиализе за 3 часа удаляется из организма приблизительно 68 % введенной дозы препарата.
При непрерывном амбулаторном перитонеальном диализе препарат можно использовать в исходных рекомендованных дозах 0,5 г, 1 г или 2 г в зависимости от тяжести инфекции с интервалом между введением 48 часов.
Дети с нарушением функции почек
Детям при нарушенной функции почек рекомендуется уменьшение дозы или увеличение интервала между введениями, как указано выше в таблице. Клиренс креатинина вычисляется по следующим формулам:
Пациенты с нарушением функции печени
Коррекции дозы для пациентов с нарушением функции печени не требуется.
Внутривенное введение
Рекомендуется для пациентов с тяжёлыми или угрожающими жизни инфекциями, особенно при угрозе возникновения септического шока.
Приготовление раствора для внутривенного введения
Препарат растворяют в 5, 10 или 20 мл стерильной воды для инъекций, 5 % растворе декстрозы и 0,9 % растворе натрия хлорида для инъекций, как указано в приведенной ниже таблице, и вводят в течение 3-5 минут либо непосредственно в вену, либо в систему для внутривенного введения, через которую в организм пациента поступает совместимый раствор для внутривенного введения.
Приготовление раствора для внутривенной инфузии
Приготовленный раствор (см. выше) переносят в инфузионный сосуд с другими совместимыми растворам для внутривенных инфузий (см. ниже) и вводят в течение не менее 30 минут.

Внутримышечное введение: доза до 1 г (объем < 3,1 мл) может быть введена в виде однократной инъекции. Максимальную дозу (2 г/6,2 мл) следует вводить в виде двух инъекций в разные места.
Приготовление раствора для внутримышечного введения
Препарат растворяют в стерильной воде для инъекций, 5 % растворе декстрозы или 0,9 % растворе натрия хлорида для инъекций, бактериостатической воде для инъекций с парабенами или бензиловым спиртом, 0,5 % или 1 % растворе лидокаина, как указано ниже в таблице.

Приготовленные растворы препарата для внутримышечного и внутривенного введения стабильны в течение 24 часов при комнатной температуре или 7 дней при хранении в холодильнике (2-8°С).
Как и все растворы для парентерального применения, перед введением приготовленные растворы препарата следует проверить на отсутствие видимых механических включений. В противном случае запрещается использовать приготовленный раствор.
При хранении порошок и приготовленный раствор могут потемнеть, что не влияет на активность и качество препарата.
Побочное действие
Наиболее часто отмечаются побочные эффекты со стороны желудочно-кишечного тракта и аллергические реакции. Ниже перечислены побочные эффекты по органам и системам в соответствии с их частотой: очень часто (≥10 %); часто (≥1 % и <10 %); нечасто (≥0,1 % и <1 %); редко (≥0,01 % и <0,1 %); частота неизвестна (нет данных о частоте развития данного побочного эффекта).
Аллергические реакции
Часто — высыпания на коже;
Нечасто — эритема, крапивница, зуд;
Редко — анафилактические реакции;
Частота неизвестна — анафилактический шок, токсический эпидермальный некролиз, мультиформная эритема, синдром Стивенса-Джонсона, ангионевротический отек.
Инфекции
Нечасто — кандидоз слизистой оболочки полости рта, вагинальные инфекции;
Редко — кандидозы.
Со стороны центральной нервной системы
Нечасто — головная боль;
Редко — судороги, парестезии, дисгезии, головокружение;
Частота неизвестна (пострегистрационный опыт): энцефалопатия (нарушение сознания, включая спутанность сознания, галлюцинации, ступор и кома), миоклонус, судороги и бессудорожный эпилептический статус.
Несмотря на то, что большинство случаев отмечались у пациентов с почечной недостаточностью, которые получали цефепим в дозах, выше рекомендованных, в некоторых случаях нейротоксичность отмечалась у пациентов, которым проводилась коррекция дозы в зависимости от степени почечной недостаточности.
Со стороны мочевыделительной системы
Частота неизвестна — почечная недостаточность, токсическая нефропатия.
Со стороны пищеварительной системы
Часто — диарея;
Нечасто — тошнота, рвота, колит (включая псевдомембранозный колит);
Редко — абдоминальные боли, запор;
Частота неизвестна — нарушения пищеварения.
Со стороны дыхательной системы
Редко — одышка.
Со стороны сердечно-сосудистой системы
Редко — вазодилатация;
Частота неизвестна — кровотечения.
Общие реакции и реакции в месте введения
Часто — флебит в месте введения, боль в месте введения;
Нечасто — повышение температуры и воспаление в месте введения;
Редко — озноб.
Лабораторные показатели
Часто — повышение активности аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (ACT), щелочной фосфатазы (ЩФ), общего билирубина, анемия, эозинофилия, увеличение протромбинового времени или частичного тромбопластинового времени;
Нечасто — повышение азота мочевины крови, креатинина сыворотки, тромбоцитопения, лейкопения и нейтропения;
Частота неизвестна — апластическая анемия, гемолитическая анемия, агранулоцитоз.
Прочие
Редко — генитальный зуд, изменение вкуса, вагинит, эритема, ложноположительная проба Кумбса без гемолиза.
Передозировка
Симптомы: энцефалопатия (спутанность сознания, галлюцинации, ступор, кома), миоклонические судороги, повышенная нервно-мышечная возбудимость.
Лечение: симптоматическая и поддерживающая терапия. В случае значительного превышения рекомендованных доз, особенно у пациентов с нарушением функции почек, показан гемодиализ.
Взаимодействие с другими лекарственными средствами
Раствор препарата фармацевтически несовместим с растворами метронидазола, ванкомицина, гентамицина, тобрамицина сульфата, нетилмицина сульфата, поэтому их нельзя смешивать. Однако при одновременном назначении цефепима и вышеуказанных препаратов каждый из них можно вводить раздельно.
Данные по совместимости растворов цефепима и других лекарственных препаратов, а также их по их стабильности приведены в таблице ниже.
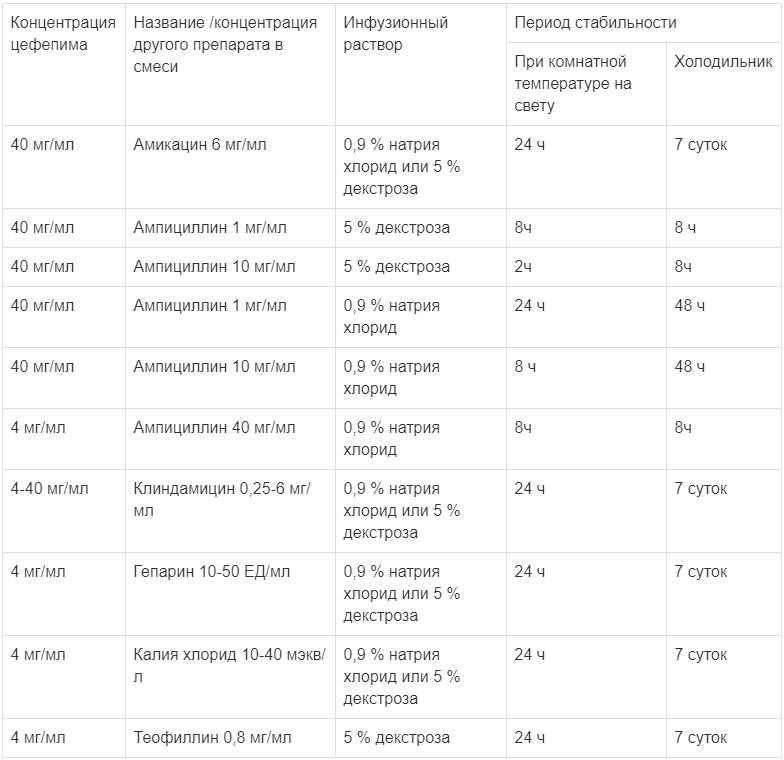
Особые указания
При наличии факторов, могущих вызвать нарушение функции почек, требуется корректировка дозы цефепима с целью компенсации уменьшенной скорости выведения препарата с мочой. Режим дозирования зависит от степени почечной недостаточности, тяжести инфекции и чувствительности микроорганизмов. При слабых или умеренных нарушениях функции почек начальная доза препарата такая же, как при нормальной функции почек. Риск развития токсических реакций особенно увеличивается у пожилых пациентов с нарушенной функцией почек.
Во время пострегистрационного наблюдения были зарегистрированы следующие серьезные нежелательные реакции, в том числе угрожающие жизни или приводящие к летальному исходу: энцефалопатия (нарушение сознания, включая спутанность сознания, галлюцинации, ступор и кома), миоклонус, судороги и бессудорожный эпилептический статус.
Большинство случаев отмечалось у пациентов с почечной недостаточностью, которым не проводилась коррекция дозы. Тем не менее, в некоторых случаях нейротоксичность отмечалась у пациентов, которым проводилась коррекция дозы в зависимости от степени почечной недостаточности. В большинстве случаев симптомы нейротоксичности были обратимы и исчезали после отмены препарата и/или после проведения гемодиализа. Если нейротоксичность связана с применением цефепима, следует рассмотреть вопрос о прекращении терапии цефепимом или корректировать дозу у пациентов с почечной недостаточностью. Перед началом лечения следует установить наличие в анамнезе у пациента аллергических реакций на цефепим, другие цефалоспориновые антибиотики, пенициллины и другие бета-лактамные антибиотики, а также других форм аллергии. При применении всех видов бета-лактамных антибиотиков отмечались случаи развития тяжелых реакций гиперчувствительности, иногда с летальным исходом.
Антибиотики группы цефалоспоринов могут быть причиной ложноположительной реакции на глюкозу в моче в тестах, основанных на восстановлении ионов меди (с растворами Бенедикта или Фелинга или с таблетками Клинитест), но не в ферментных тестах (с глюкозоксидазой). В связи с этим для определения глюкозы в моче рекомендуется применять ферментные тесты с глюкозоксидазой.
При развитии аллергической реакции следует прекратить лечение препаратом и предпринять соответствующие меры. При развитии тяжелой аллергической реакции (например, анафилактической реакции) непосредственно во время введения препарата может потребоваться применение эпинефрина и другой поддерживающей терапии.
При назначении эмпирического лечения необходимо принимать во внимание данные о приобретенной устойчивости микроорганизмов-возбудителей.
Устойчивость микроорганизмов может изменяться с течением времени и географического положения. Для идентификации микроорганизма-возбудителя и определения чувствительности к цефепиму следует провести соответствующие тесты. Цефепим может применяться в виде монотерапии даже до идентификации микроорганизма-возбудителя, так как он обладает широким спектром антибактериального действия в отношении грамположительных и грамотрицательных микроорганизмов. При риске смешанной аэробно/анаэробной инфекции (особенно, когда могут присутствовать нечувствительные к цефепиму микроорганизмы) лечение препаратом цефепим в комбинации с препаратом, действующим на анаэробы, можно начинать до идентификации возбудителя.
После идентификации возбудителя и определения чувствительности к антибиотикам лечение следует проводить в соответствии с результатами тестов.
Как и при применении других антибиотиков, лечение препаратом Цефепим может приводить к колонизации нечувствительной микрофлоры. При развитии суперинфекций во время лечения необходимо принятие соответствующих мер.
В исследованиях на крысах не было отмечено влияния на фертильность. Данные о влиянии на фертильность у людей при применении цефепима отсутствуют.
Clostridium difficile — ассоциированная диарея
При применении практически всех антибиотиков широкого спектра действия возможно возникновение диареи, ассоциированной с Clostridium difficile (CDAD — Clostridium difficile-associated diarrhea), которая может протекать как в легкой форме, так и в тяжелой, вплоть до летального исхода.
При возникновении диареи во время лечения препаратом необходимо подтвердить диагноз CDAD. Следует тщательно наблюдать за пациентом на предмет развития CDAD, поскольку регистрировались случаи ее возникновения спустя более двух месяцев после прекращения применения антибиотиков. При подозрении на CDAD или подтверждении данного диагноза необходимо прекратить применение антибиотиков, кроме тех, которые назначены для подавления Clostridium difficile. Нельзя применять лекарственные средства, тормозящие перистальтику кишечника.
Влияние на способность управлять транспортными средствами, механизмами
Изучение влияние препарата на способность к концентрации внимания не проводилось, однако, учитывая возможность развития побочных эффектов со стороны центральной нервной системы, во время лечения препаратом следует воздержаться от управления транспортными средствами и занятий другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Форма выпуска
Порошок для приготовления раствора для внутривенного и внутримышечного введения 0,5 г; 1,0 г; 2,0 г.
0,5 г или 1,0 г или 2,0 г действующего вещества во флаконы из трубки стеклянной для лекарственных средств вместимостью 10 мл, герметично укупоренные резиновыми пробками, обжатые колпачками алюминиевыми или комбинированными.
1; 5; 10 флаконов вместе с инструкцией по медицинскому применению укладывают в индивидуальную пачку из картона.
50 флаконов с приложением равного количества инструкций укладывают в коробку из картона (для стационаров).
Упаковка в комплекте с растворителем — водой для инъекций или 0,9 % раствором натрия хлорида. В комплект входят:
а) 1 флакон с препаратом по 0,5 г и 1 ампула с растворителем на 5 мл или 1 флакон с препаратом по 1,0 г или 2,0 г и 2 ампулы с растворителем на 5 мл;
б) 5 флаконов с препаратом по 0,5 г и 5 ампул с растворителем на 5 мл или 5 флаконов с препаратом по 1,0 г или 2,0 г и 10 ампул с растворителем на 5 мл;
в) 10 флаконов с препаратом по 0,5 г и 10 ампул с растворителем на 5 мл или 10 флаконов с препаратом по 1,0 г или 2,0 г и 20 ампул с растворителем на 5 мл.
Комплект укладывают в индивидуальную пачку из картона вместе с инструкцией по медицинскому применению, скарификатором ампульным.
При использовании ампул с надсечкой, кольцом излома или точкой излома скарификатор ампульный не вкладывают.
Условия хранения
В защищенном от света месте при температуре не выше 30°С.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности.
Условия отпуска
Отпускают по рецепту.
Владелец регистрационного удостоверения
ООО «ПРОМОМЕД РУС», Россия.
105005, г. Москва, ул. Почтовая М., дом 2/2, строение 1, пом I ком. 2.
Производитель
АО «Биохимик», Россия.
Юридический адрес: 430030, Республика Мордовия, г. Саранск, ул. Васенко, д. 15 А.
Адрес места производства: 430030, Республика Мордовия, г. Саранск, ул. Васенко, д. 15 А.
Организация, принимающая претензии потребителей
ООО «ПРОМОМЕД РУС», Россия.
129090, г. Москва, пр-т Мира, д.13, стр. 1.
Купить Цефепим в planetazdorovo.ru
*Цена в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Цефепим (Cefepime) инструкция по применению
💊 Состав препарата Цефепим
✅ Применение препарата Цефепим
Описание активных компонентов препарата
Цефепим
(Cefepime)
Приведенная научная информация является обобщающей и не может быть использована для принятия
решения о возможности применения конкретного лекарственного препарата.
Дата обновления: 2020.11.24
Владелец регистрационного удостоверения:
Лекарственные формы
| Цефепим |
Порошок д/пригот. р-ра д/в/в и в/м введения 0.5 г: 1 шт. рег. №: ЛП-008243 |
|
|
Порошок д/пригот. р-ра д/в/в и в/м введения 1 г: 1 шт. рег. №: ЛП-008243 |
||
|
Порошок д/пригот. р-ра д/в/в и в/м введения 2 г: 1 шт. рег. №: ЛП-008243 |
Форма выпуска, упаковка и состав
препарата Цефепим
Порошок для приготовления раствора для в/в и в/м введения белый или белый с желтоватым оттенком, кристаллический.
*Субстанция представляет собой стерильную смесь цефепима гидрохлорида моногидрата и L-аргинина. L-аргинин прибавляют в качестве регулятора pH восстановленного раствора в интервале значений от 4.0 до 6.0. Количество L-аргинина может меняться в зависимости от активности конкретной серии цефепима гидрохлорида.
Вспомогательные вещества: L-аргинин — 0.3625 г.
0.5 г — флаконы бесцветного стекла (тип I) (1) — пачки картонные.
0.5 г — флаконы (50) — коробки картонные (для стационаров).
0.5 г — флаконы (100) — коробки картонные (для стационаров).
0.5 г — флаконы (150) — коробки картонные (для стационаров).
Порошок для приготовления раствора для в/в и в/м введения белый или белый с желтоватым оттенком, кристаллический.
*Субстанция представляет собой стерильную смесь цефепима гидрохлорида моногидрата и L-аргинина. L-аргинин прибавляют в качестве регулятора pH восстановленного раствора в интервале значений от 4.0 до 6.0. Количество L-аргинина может меняться в зависимости от активности конкретной серии цефепима гидрохлорида.
Вспомогательные вещества: L-аргинин — 0.725 г.
1 г — флаконы бесцветного стекла (тип I) (1) — пачки картонные.
1 г — флаконы (50) — коробки картонные (для стационаров).
1 г — флаконы (100) — коробки картонные (для стационаров).
1 г — флаконы (150) — коробки картонные (для стационаров).
Порошок для приготовления раствора для в/в и в/м введения белый или белый с желтоватым оттенком, кристаллический.
*Субстанция представляет собой стерильную смесь цефепима гидрохлорида моногидрата и L-аргинина. L-аргинин прибавляют в качестве регулятора pH восстановленного раствора в интервале значений от 4.0 до 6.0. Количество L-аргинина может меняться в зависимости от активности конкретной серии цефепима гидрохлорида.
Вспомогательные вещества: L-аргинин — 1.45 г.
2 г — флаконы бесцветного стекла (тип I) (1) — пачки картонные.
2 г — флаконы (50) — коробки картонные (для стационаров).
2 г — флаконы (100) — коробки картонные (для стационаров).
2 г — флаконы (150) — коробки картонные (для стационаров).
Фармакологическое действие
Цефалоспориновый антибиотик IV поколения для парентерального применения. Оказывает бактерицидное действие, нарушая синтез клеточной стенки микроорганизмов.
Активен в отношении большинства грамотрицательных бактерий, в т.ч. продуцирующих β-лактамазы, включая Pseudomonas aeruginosa. Более активен, чем цефалоспорины III поколения, в отношении грамположительных кокков.
Не активен в отношении Enterococcus spp., Listeria spp., Legionella spp., некоторых анаэробных бактерий (Bacteroides fragilis, Clostridium difficile).
Цефепим характеризуется высокой стабильностью в отношении различных плазмидных и хромосомных β-лактамаз.
Фармакокинетика
Связывание с белками плазмы составляет менее 19% и не зависит от концентрации цефепима в сыворотке крови.
Терапевтические концентрации цефепима обнаруживаются в моче, желчи, перитонеальной жидкости, экссудате волдыря, слизистом секрете бронхов, мокроте, тканях предстательной железы, аппендиксе и желчном пузыре, спинномозговой жидкости при менингите.
У здоровых людей при в/в введении цефепима в дозе 2 г с интервалом 8 ч в течение 9 дней не наблюдалось кумуляции в организме.
Средний T1/2 из организма в среднем составляет около 2 ч, средний общий клиренс — 120 мл/мин. Цефепим выводится почками, главным образом путем клубочковой фильтрации (средний почечный клиренс — составляет 110 мл/мин). В моче обнаруживается приблизительно 85% введенного цефепима в неизмененном виде.
У больных в возрасте 65 лет или старше с нормальной функцией почек величина почечного клиренса меньше, чем у молодых больных.
У больных с нарушениями функции почек увеличивается T1/2. У больных с тяжелыми нарушениями функции почек, при которых требуется проведение гемодиализа, T1/2 в среднем составляет 13 ч, проведение перитонеального диализа — 19 ч.
Фармакокинетика цефепима у больных с нарушением функции печени, муковисцидозом не изменена.
Возраст и пол пациентов не оказывали существенного влияния на общий клиренс из организма и Vd с учетом поправки на массу тела каждого. При введении цефепима в дозе 50 мг/кг каждые 12 ч кумуляции не отмечалось, а при введении в этой же дозе каждые 8 ч в равновесном состоянии Cmax, AUC и T1/2 увеличивались примерно на 15%.
Показания активных веществ препарата
Цефепим
Лечение инфекционно-воспалительных заболеваний, вызванных чувствительными к цефепиму микроорганизмами: инфекции нижних отделов дыхательных путей (включая пневмонию и бронхит), инфекции мочевыводящих путей (как осложненные, так и неосложненные), инфекции кожи и мягких тканей, интраабдоминальные инфекции (включая перитонит и инфекции желчных путей), гинекологические инфекции, септицемия, нейтропеническая лихорадка (в качестве эмпирической терапии), бактериальный менингит у детей.
Профилактика инфекций при проведении полостных хирургических операций.
Открыть список кодов МКБ-10
| Код МКБ-10 | Показание |
| A40 | Стрептококковый сепсис |
| A41 | Другой сепсис |
| D70 | Агранулоцитоз |
| G00 | Бактериальный менингит, не классифицированный в других рубриках |
| J15 | Бактериальная пневмония, не классифицированная в других рубриках |
| J20 | Острый бронхит |
| J42 | Хронический бронхит неуточненный |
| K65.0 | Острый перитонит (в т.ч. абсцесс) |
| K81.0 | Острый холецистит |
| K81.1 | Хронический холецистит |
| K83.0 | Холангит |
| L01 | Импетиго |
| L02 | Абсцесс кожи, фурункул и карбункул |
| L03 | Флегмона |
| L08.0 | Пиодермия |
| L08.8 | Другие уточненные местные инфекции кожи и подкожной клетчатки |
| N10 | Острый тубулоинстерстициальный нефрит (острый пиелонефрит) |
| N11 | Хронический тубулоинтерстициальный нефрит (хронический пиелонефрит) |
| N30 | Цистит |
| N34 | Уретрит и уретральный синдром |
| N41 | Воспалительные болезни предстательной железы |
| N70 | Сальпингит и оофорит |
| N71 | Воспалительная болезнь матки, кроме шейки матки (в т.ч. эндометрит, миометрит, метрит, пиометра, абсцесс матки) |
| N72 | Воспалительная болезнь шейки матки (в т.ч. цервицит, эндоцервицит, экзоцервицит) |
| N73.5 | Тазовый перитонит у женщин неуточненный |
| T79.3 | Посттравматическая раневая инфекция, не классифицированная в других рубриках |
| Z29.2 | Другой вид профилактической химиотерапии (введение антибиотиков с профилактической целью) |
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Индивидуальный, в зависимости от чувствительности возбудителя, тяжести инфекции, возраста пациента, от состояния функции почек.
Вводят в/м или в/в. В/в путь введения предпочтителен для больных с тяжелыми или угрожающими жизни инфекциями, особенно при угрозе шока.
Побочное действие
Со стороны пищеварительной системы: возможны диарея, тошнота, рвота, колиты (включая псевдомембранозный колит); редко — боли в животе, запор, изменение вкуса.
Аллергические реакции: возможны — сыпь, зуд, крапивница; редко — анафилактические реакции.
Со стороны ЦНС и периферической нервной системы: возможны — головные боли; редко — головокружение, парестезии; в отдельных случаях — судороги.
Дерматологические реакции: редко — покраснение кожи. Наиболее часто у детей — сыпь.
Со стороны системы кроветворения: возможна анемия.
Со стороны показателей лабораторных исследований: возможны повышение активности АЛТ, АСТ, ЩФ, повышение общего билирубина, эозинофилия, увеличение протромбинового времени; редко — временное повышение азота мочевины крови и/или креатинина сыворотки, транзиторная тромбоцитопения, транзиторная лейкопения и нейтропения; часто — положительный результат теста Кумбса без гемолиза.
Прочие: возможны повышение температуры тела, вагинит, эритема; редко — генитальный зуд, неспецифический кандидоз.
Местные реакции: при в/в вливании возможны флебиты, редко — воспаление); при в/м введении возможно воспаление или боль.
Противопоказания к применению
Повышенная чувствительность к цефепиму или L-аргинину, а также к цефалоспориновым антибиотикам, пенициллинам или другим бета-лактамным антибиотикам.
Применение при беременности и кормлении грудью
Адекватных и строго контролируемых исследований безопасности применения цефепима при беременности не проведено; применение возможно только под наблюдением врача.
Цефепим выделяется с грудным молоком в очень низких концентрациях. В период лактации применять с осторожностью.
В экспериментальных исследованиях не выявлено влияния на репродуктивную функцию и фетотоксического действия цефепима.
Применение при нарушениях функции почек
При нарушениях функции почек (КК менее 30 мл/мин) необходима коррекция режима дозирования. Исходная доза цефепима должна быть такой же, как и для больных с нормальной функцией почек. Поддерживающие дозы определяют в зависимости от значений КК или концентрации креатинина сыворотки
Применение у детей
Безопасность и эффективность применения цефепима у детей в возрасте до 2 мес не установлены. Для детей старше 2 мес применение возможно согласно режиму дозирования. Детям с нарушениями функции почек рекомендуются такие же изменения режима дозирования, как и взрослым, поскольку фармакокинетика цефепима у взрослых и детей имеет сходный характер.
Особые указания
При применении у пациентов, находящихся в группе повышенного риска возникновения инфекции за счет смешанной аэробно/анаэробной микрофлоры (в т.ч. в случаях, когда одним из возбудителей является Bacteroides fragilis), до идентификации возбудителя рекомендуется одновременно с цефепимом назначить препарат, активный в отношении анаэробов.
С осторожностью применяют у пациентов с риском развития аллергических реакций, особенно на лекарственные препараты.
При развитии аллергических реакций цефепим следует отменить.
При серьезных реакциях гиперчувствительности немедленного типа может потребоваться применение эпинефрина (адреналина) и других форм поддерживающего лечения.
При появлении диареи на фоне лечения следует учитывать возможность развития псевдомембранозного колита. В таких случаях цефепим следует немедленно отменить и при необходимости назначить соответствующее лечение.
При развитии суперинфекции цефепим следует немедленно отменить и назначить соответствующее лечение.
Безопасность и эффективность применения цефепима у детей в возрасте до 2 мес не установлены.
С особой осторожностью применяют цефепим совместно с аминогликозидами и «петлевыми» диуретиками.
Лекарственное взаимодействие
При одновременном введении раствора цефепима с растворами метронидазола, ванкомицина, гентамицина, тобрамицина сульфата и нетилмицина сульфата возможно фармацевтическое взаимодействие.
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Аналоги препарата
Децефим
(ФАРМАСИНТЕЗ, Россия)
Кефсепим
(ДЖОДАС ЭКСПОИМ, Россия)
Максицеф®
(ПФК ПРЕБЕНД, Россия)
Мовизар
(YOUCARE PHARMACEUTICAL GROUP, Китай)
Цепим®
(БИОКОМ ТЕХНОЛОГИЯ, Республика Беларусь)
Цефепим
(SK MEDITECH, Индия)
Цефепим
(ПРОТЕК-СВМ, Россия)
Цефепим
(ФАРМГИД, Россия)
Цефепим
(КОМПАНИЯ ДЕКО, Россия)
Цефепим
(КРАСФАРМА, Россия)
Все аналоги
Цефепим, инструкция по применению
- Производитель
- Страна происхождения
- Группа препаратов
- Действующее вещество
- Формы выпуска
- Упаковка
- Состав
- Дозировка
- Показания к применению
- Передозировка
- Противопоказания
- Побочные действия
- Способ применения
- Применение при беременности и кормлении грудью
- Фармакологическое действие
- Синонимы
- Фармакокинетика
- Взаимодействие с другими лекарствами
- Лекарственная форма
- Условия хранения
- Срок годности
- Особые условия
- Условия отпуска из аптек
Цефепим — это цефалоспориновый антибиотик 4-го поколения. Обладает бактерицидным воздействием на организм. Активен в отношении грамположительных и грамотрицательных бактерий, в том числе большего количества различных штаммов, проявляющих устойчивость к аминогликозидам или цефалоспориновым антибиотикам третьего поколения, таким как цефтазидим. Назначается взрослым и детям при менингите, пневмонии, миозите, бронхите, перитоните, холецистите, инфекционных бурситах, воспалительных болезнях и инфекциях. Назначается исключительно по рецепту врача.
Производитель
Лекарство производится следующими фармацевтическими компаниями:
- Производитель: «Свисс Перентералс Пвт. Лтд», Индия.
- Производитель: АО «Лекхим», Украина, Киевская обл., 01033, г. Киев, ул. Шота Руставели, 23.
Телефон: +38 (044) 246-63-12.
Факс: +38 (044) 287-62-76.
Претензии или предложения от потребителей направлять по адресу производителя в Украине.
Страна происхождения
Владелец регистрационного удостоверения UA/13564/01/01 АО «Лекхим», Украина.
Группа препаратов
Лекарство Цефепим относится к цефалспоринам. Это антибиотики, в основе которых лежит 7-аминоцефалоспориновая кислота. Главной особенностью цефалоспоринов являются широкий спектр действия, высокая бактерицидность, относительно высокая, в сравнении с пенициллинами, резистентность по отношению к бета-лактамазам. Группа медикаментов оказывает на организм бактерицидные свойства, вызывает лизис клеток. Механизм данного воздействия взаимосвязан с повреждением клеточной мембраны делящихся бактерий.
Действующее вещество
Активным компонентом является одноименное вещество — цефепим, который является антибиотиком группы цефалоспоринов четвертого поколения. Обладает антибактериальным и бактерицидным воздействием на организм человека. Действие компонента основано на угнетении транспептидазы и нарушении биосинтеза мукопептида клеточных оболочек микроорганизмов.
Формы выпуска
Выпускается в виде порошка для приготовления инъекций.
Упаковка
Лекарственное средство находится в прозрачных стеклянных ампулах. В ячейковой упаковке из пластика содержится 10 флаконов. В картонной упаковке содержится один блистер, соответственно, 10 ампул.
Фармсредство находится в пачке, изготовленной из картона. Дополнительно прилагается инструкция, описывающая показания, способ применения, дозу и другую нужную информацию.
Состав
В 1 флаконе лекарственного препарата содержится активный компонент гидрохлорид цефепима — 0,6 грамм. Вспомогательным компонентом является L-аргинин.
Дозировка
Рекомендуемая дозировка для взрослых назначается индивидуально лечащим врачом. Стандартная дозировка для взрослых пациентов составляет 1000 миллиграмм, она вводится внутривенно или внутримышечно с интервалом в 12 часов. Средняя продолжительность терапевтического курса составляет 7-10 суток, в тяжелых случаях длительность лечения может быть увеличена.
Суточная дозировка и способ использования медикамента варьируются в зависимости от чувствительности микроорганизмов-возбудителей к активному веществу, степени тяжести заболевания, а также состояния почек пациента.
В целях профилактики возникновения инфекции при проведении хирургического вмешательства лекарство вводится за 1 час до начала операции в количестве 2 грамма для взрослого человека. При завершении дополнительно вводится 500 мг метронидазола внутривенно. При этом раствор последнего не рекомендуется вводить одновременно с медикаментом. Систему для инфузии перед употреблением необходимо тщательно промыть.
При проведении длительных хирургических операций, длящихся более 12 часов, спустя время после первой дозы рекомендуется повторно ввести ту же дозу лексредства с дальнейшим использованием метронидазола.
Для детей дозировка медикамента рассчитывается согласно массе тела:
- детям возрастом 1-2 месяцев медпрепарат назначается исключительно по жизненным показаниям в дозировке 30 мг на один килограмм массы тела каждые 8 или 12 часов в зависимости от тяжести недуга;
- детям возрастом от 2-х месяцев максимальная доза не должна превышать рекомендуемую для взрослых
- детям с массой тела 40 килограмм и более дозировка определяется как взрослым.
Окончательную частоту и длительность терапевтического курса определяет лечащий доктор.
Показания к применению
Взрослым медикамент назначается для лечения инфекций, вызванных чувствительной к препарату микрофлорой:
- пневмония;
- бронхит;
- заболевания кожи и подкожной клетчатки;
- перитонит;
- инфекции желчевыводящих путей;
- гинекологические заболевания;
- септицемия.
Используется при эмпирической терапии пациентов с нейтропенической лихорадкой, а также для профилактики послеоперационных осложнений в интраабдоминальной хирургии.
Детям лексредство назначается для лечения:
- пневмонии;
- инфекций мочевыводящих путей, в том числе пиелонефрита;
- инфекций кожи и подкожной клетчатки;
- септицемия;
- при эмпирической терапии пациентов с нейтропенической лихорадкой;
- бактериального менингита.
Начинать курс допускается только после консультации с лечащим врачом.
Передозировка
В случае передозировки возможны такие реакции, как:
- энцефалопатия;
- судороги у больных с почечной недостаточностью.
При проявлении любых из вышеперечисленных симптомов необходимо отменить медикамент. Для лечения симптомов необходим гемодиализ и поддерживающее лечение.
Противопоказания
Категорически запрещено принимать:
- при гиперчувствительности к основным или вспомогательным составляющим препарата;
- в детском возрасте до 2-х месяцев для внутривенного введения;
- в детском возрасте до 12-ти лет для внутримышечного введения.
Перед началом необходимо проконсультироваться с доктором на предмет наличия противопоказаний.
Побочные действия
Возможны побочные эффекты с различными системами организма:
- Нервной системы: головная боль, головокружение, расстройство сна, ощущение жжения и покалывания кожных покровов, повышенная тревожность, спутанность сознания, судороги, энцефалопатия.
- Мочеполовой: вагинит.
- Мочевыделительной: нарушение функции почек.
- Желудочно-кишечного тракта: диарея, тошнота, рвота, запор или понос, боль в области живота, диспепсия, псевдомембранозный колит.
- Кроветворения: анемия, тромбоцитопения, гемолитическая анемия, лейкопения, нейтропения, панцитопения, кровотечения.
- Дыхательной: беспричинный кашель, болевой синдром в области груди.
- Сердечно-сосудистой: учащенное сердцебиение, одышка, периферические отеки.
В качестве прочих побочных симптомов может возникнуть повышенное потоотделение, сыпь на кожных покровах, зуд, лихорадка, боль в горле, развитие суперинфекции.
Способ применения
Внутривенное введение предпочтительно для пациентов с тяжелыми или угрожающими жизни инфекциями. Перед инфузией место прокола необходимо обработать антисептиком. Вводить следует исключительно свежеприготовленный раствор.
Применение при беременности и кормлении грудью
Во время беременности лекарство используют только в том случае, если предполагаемая польза для матери выше потенциального риска для плода. Во время терапевтического курса медпрепаратом во время лактации грудное вскармливание следует прекратить.
Фармакологическое действие
Антибиотик цефалоспориновый четвертого поколения предназначен для парентерального применения. Обладает бактерицидным воздействием на организм, нарушает синтез клеточных стенок микроорганизмов.
Проявляет активность в отношении большей части грамотрицательных бактерий, в том числе продуцирующих бета-лактамазы.
Синонимы
Основными дженериками считаются фармсредства с похожим активным компонентом и эффектом. В каталогах интернет-аптек можно заказать с доставкой целый список лекарств из наличия, по доступной цене, считающихся актуальными аналогами с подробными отзывами. К ним относятся:
- Амоксициллин;
- Эфипим;
- Квадроцеф;
- Цефикад;
- Европим;
- Кефсепим;
- Димипра;
- Сервипим-1;
- Максипим.
Синонимы с названиями, приведенными выше, оказывают на здоровье человека такой же или близкий эффект.
Фармакокинетика
Биодоступность медикамента 100%. Максимальная концентрация в плазме крови после внутривенного или внутримышечного введения достигается через 60-120 минут. Средняя терапевтическая концентрация достигается через 12 часов. Высокие концентрации определяются в первую очередь в желчи, моче, перитонеальной жидкости, слизистом секрете бронхов, мокроте, предстательной железе, аппендиксе и желчном пузыре.
Время полувыведения составляет 120 минут. Из организма выводится при помощи почек с мочой, а также выделяется в грудное молоко.
Взаимодействие с другими препаратами
Одновременное введение раствора с растворами метронидазола, гентамицина, нетилмицина сульфата, ванкомицина и тобрамицина сульфата, может вызвать фармацевтическое взаимодействие.
Лекарственная форма
Выпускается в виде порошка, цвет от белого до бледно-желтого, достаточно легко растворяется в воде, не обладает специфическим ароматом.
Условия хранения
Препарат Цефепим нужно хранить в сухом месте, при температуре не более 25 градусов по Цельсию, в недоступном для ребенка месте. Не допускать попадания солнечных лучей, оказывающих разрушающее воздействие на средство. Хранить в оригинальной упаковке.
Срок годности
Срок годности в закрытой упаковке 2 года. После окончания срока годности, указанного на упаковке, использовать не рекомендуется, чтобы не нанести вред организму.
Особые условия
Пациентам, которые находятся в группе повышенного риска проявления инфекции за счет смешанной анаэробной или аэробной микрофлоры (в том числе в случаях, когда основным возбудителем является Bacteroides fragilis), до идентификации возбудителя следует одновременно с Цефепимом выписывать медсредство, активное в отношении анаэробов.
С особой осторожностью назначать пациентам, у который есть риск проявления аллергических реакций. В случае возникновения аллергии или побочных эффектов требуется отменить прием препарата.
При серьезный реакциях гиперчувствительности к составляющим компонентам немедленного типа может потребоваться адреналин (эпинефрин) и иные формы поддерживающей терапии.
В случае проявления диареи на фоне терапевтического лечения необходимо учитывать, что присутствует риск развития псевдомембранозного колита. В этом случае требуется незамедлительно отменить фармсредство и, при необходимости, выписать соответствующее лечение.
При развитии суперинфекции необходимо немедленно прекратить использование лексредства.
Во время использования иных антибиотиков группы цефалоспоринов могут проявиться:
- крапивница;
- многоформная эритема;
- колит;
- токсическая нефропатия;
- гемолитическая анемия;
- судороги;
- холестаз;
- синдром Стивенса-Джонсона;
- токсический эпидермальный некролиз;
- нарушение функции почек;
- апластическая анемия;
- кровоточивость;
- нарушение функции печени;
- ложноположительные результаты анализов на глюкозу мочи.
Эффективность и безопасность использования у детей до 2 месяцев не установлена.
С повышенной осторожностью применять с аминогликозидами и диуретиками.
Условия отпуска из аптек
Цефепим в аптеке отпускается исключительно по рецепту врача.