Сахарный диабет: диабетическая ретинопатия, диабетический макулярный отек
Версия: Клинические рекомендации РФ 2023 (Россия)
Категории МКБ:
Диабетическая ретинопатия (E10-E14+ с общим четвертым знаком .3) (H36.0*), Другие уточненные формы сахарного диабета с поражением глаз (E13.3), Инсулиннеозависимый сахарный диабет с поражением глаз (E11.3), Инсулинозависимый сахарный диабет с поражением глаз (E10.3), Сахарный диабет неуточненный с поражением глаз (E14.3), Сахарный диабет, связанный с недостаточностью питания, с поражением глаз (E12.3)
Разделы медицины:
Офтальмология, Эндокринология
Общая информация
Краткое описание
Разработчик клинической рекомендации:
- Общероссийская общественная организация «Ассоциация врачей-офтальмологов»
- Российская ассоциация эндокринологов
Одобрено Научно-практическим Советом Минздрава РФ
В соответствии с Правилами поэтапного перехода медицинских организаций к оказанию медицинской помощи на основе клинических рекомендаций, разработанных и утвержденных в соответствии с частями 3, 4, 6 –9 и 11 статьи 37 Федерального закона «Об основах охраны здоровья граждан в Российской Федерации», утвержденных постановлением Правительства Российской Федерации от 19.11.2021 № 1968, клинические рекомендации применяются следующим образом:
– размещенные в Рубрикаторе после 1 июня 2022 года – с 1 января 2024 года.
Клинические рекомендации
Сахарный диабет: ретинопатия диабетическая, макулярный отек диабетический
Возрастная категория: Взрослые
Пересмотр не позднее: 2025
Дата размещения: 15.02.2023
Статус: Действует
ID:115
Применение отложено
Определение заболевания или состояния (группы заболеваний или состояний)
Сахарный диабет (СД) – это группа метаболических (обменных) заболеваний, характеризующихся хронической гипергликемией, которая является результатом нарушения секреции инсулина, действия инсулина или обоих этих факторов [1, 2]. Хроническая гипергликемия при СД сопровождается повреждением, дисфункцией и недостаточностью различных органов, особенно глаз, почек, нервов, сердца и кровеносных сосудов.
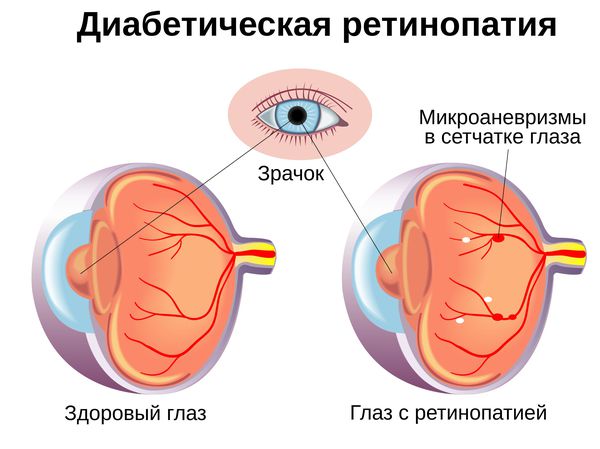
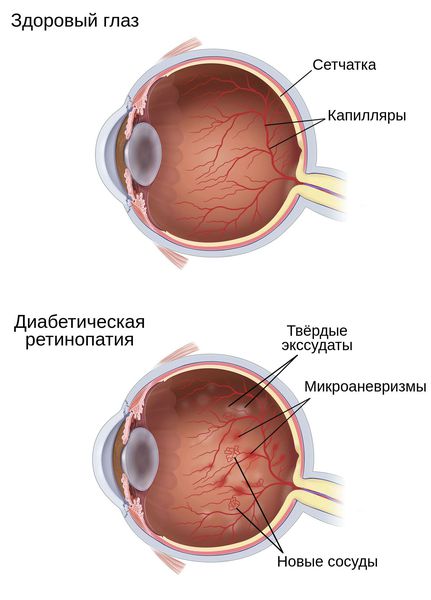
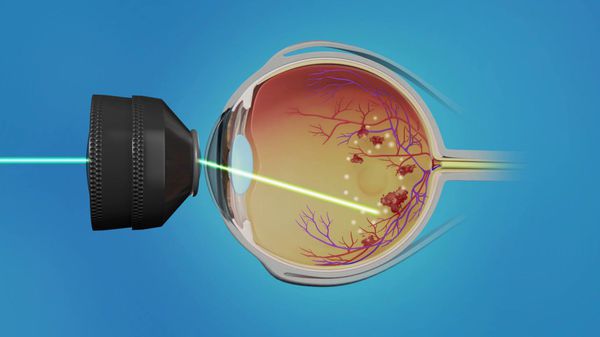
Диабетическая ретинопатия (ДР) – специфичное позднее нейромикрососудистое осложнение сахарного диабета, развивающееся, как правило, последовательно от изменений, связанных с повышенной проницаемостью и окклюзией ретинальных сосудов, до появления новообразованных сосудов и фиброглиальной ткани. Является одним из проявлений генерализованной микроангиопатии.
Диабетический макулярный отек (ДМО) – утолщение сетчатки, связанное с накоплением жидкости в межклеточном пространстве нейроэпителия вследствие нарушения гематоретинальных барьеров и несоответствия между транссудацией жидкости и способности к ее реабсорбции.
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статической класификации болезней и проблем, связанных со здоровьем
H36.0 — Диабетическая ретинопатия;
E10.3 — Инсулинозависимый сахарный диабет с поражением глаз;
E11.3 — Инсулиннезависимый сахарный диабет с поражением глаз;
Е12.3 — Сахарный диабет, связанный с недостаточностью питания с поражением глаз;
E13.3 — Другие уточненные формы сахарного диабета с поражением глаз;
Е14.3 — Сахарный диабет неуточненный с поражением глаз.
Облачная МИС «МедЭлемент»
Облачная МИС «МедЭлемент»

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
Классификация
Классификация заболевания или состояния (группы заболеваний или состояний)
Классификация ДР, предложенная Kohner E. и Porta M. (1991), выделяет три основных стадии заболевания [13]:
1. непролиферативная ДР;
2. препролиферативная ДР;
3. пролиферативная ДР.
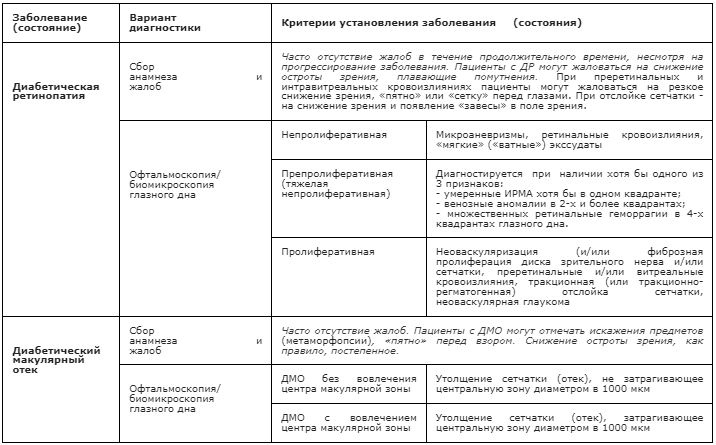
Клинические изменения, характерные для каждой стадии ДР, представлены в табл. 1.
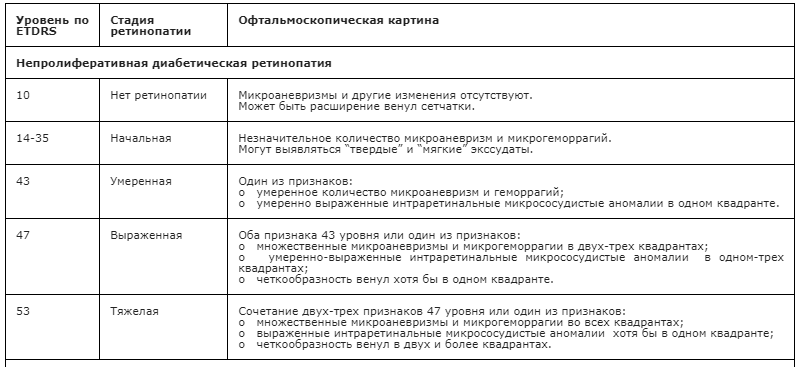
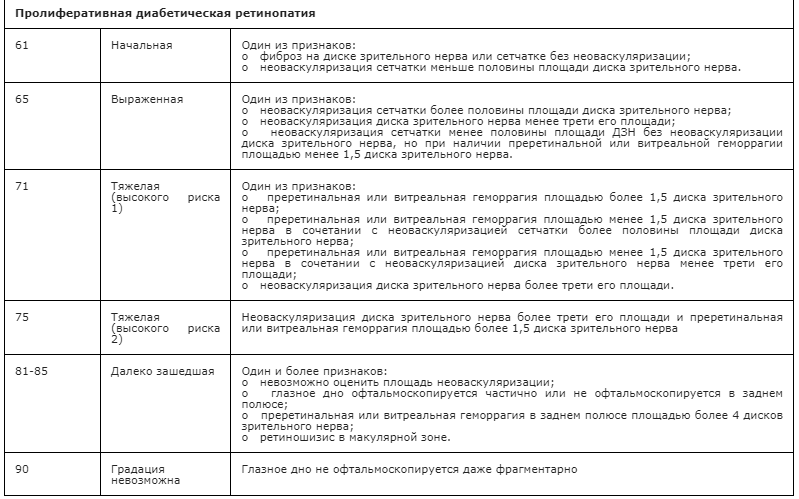
Таблица 1. Характеристика изменений на глазном дне при различных стадиях ДР
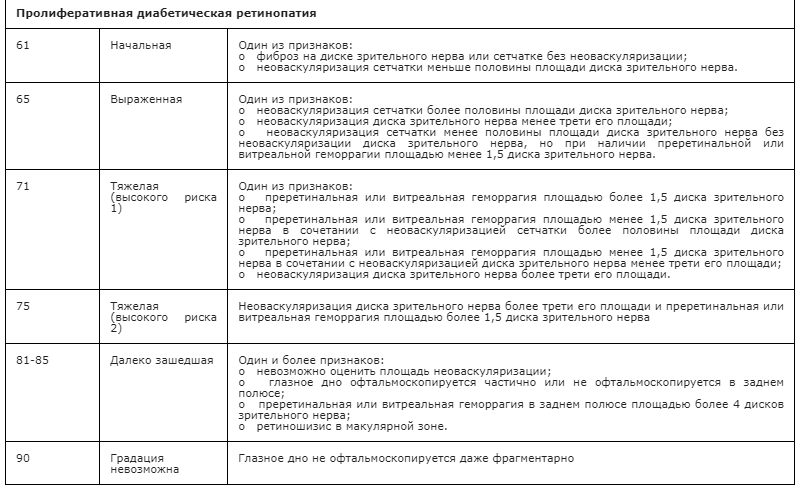
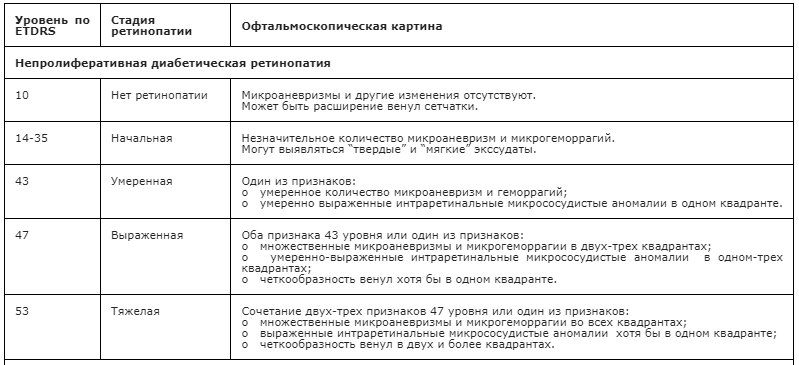
Самой полной на сегодняшний день является классификация Исследовательской группы по изучению раннего лечения ДР (Early Treatment Diabetic Retinopathy Study – ETDRS) 1991 года (табл. 2) [14], которая также может быть использована в клинической практике.
Таблица 2. Классификация и клинические проявления ДР ETDRS (1991)
Диабетическая макулопатия, в том числе ДМО, возможна на любой стадии ДР. В настоящее время не существует общепризнанной классификации диабетической макулопатии и ДМО. В то же время, в зависимости от того, какое из перечисленных ниже поражений является преобладающим, выделяют основные клинические формы поражения:
— ДМО или отечная макулопатия – локальный изолированный прорыв внутреннего гематоретинального барьера (группа микроаневризм) с нарушением ауторегуляции (фокальный отек) или гиперпроницаемость капилляров в сочетании с нарушением наружного гематоретинального барьера (диффузный отек);
— тракционная макулопатия – нарушение витреоретинальных взаимоотношений или плотности внутренней пограничной мембраны сетчатки (тракционный отек);
— ишемическая макулопатия – окклюзия капилляров (ишемический отек).
При значительных размерах интраретинальных полостей скопления жидкости отек называют кистовидным.
Исследовательской группой по изучению раннего лечения ДР (ETDRS) введено понятие клинически значимого ДМО, критериями которого являются [15]:
-утолщение сетчатки и/или твердые экссудаты, захватывающие центр макулы;
-утолщение сетчатки и/или твердые экссудаты, расположенные ближе 500 мкм от центра макулы, но на него не распространяющиеся
-утолщение сетчатки площадью 1 ДЗН или более, расположенное хотя бы частично, ближе 1 диаметра диска от центра макулы.
Кроме этого, принято выделять ДМО с вовлечением или без вовлечения центра. Макулярный отек с вовлечением центра определяется как утолщение сетчатки (ретинальный отек), затрагивающее центральную зону диаметром в 1000 мкм.
Этиология и патогенез
Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Диабетическая ретинопатия (ДР) является заболеванием, входящим в группу ишемических ретинопатий, которые характеризуются значительным нарушением капиллярной перфузии, развитием внутриглазных новообразованных сосудов и ретинальным отеком. Окклюзия и отек – это основные патологические проявления диабетического поражения сетчатки, причем окклюзия поражает в основном периферические отделы сетчатки, а отек преобладает в центральной ее части – в макулярной зоне. Окклюзия сосудов является причиной появления неперфузируемых зон сетчатки, которые стимулируют выброс ангиогенных факторов и воспалительных цитокинов.
В условиях гипергликемии возникает каскад патологических биохимических процессов, в результате которого образуются конечные продукты гликирования и активные формы кислорода, вызывающие повреждение сосудистой стенки и гибель эндотелиальных клеток. Поражению эндотелия сосудов способствует также резкое усиление ретинального кровотока, возникающее в условиях гипергликемии (эндотелиальный стресс), а также воздействие свободных радикалов. Оксидативный стресс, высокореактивные соединения кислорода и конечные необратимые продукты гликирования индуцируют экспрессию воспалительных цитокинов (таких как интерлейкин-6, интерлейкин-8, интерлейкин-1β и фактор некроза опухоли), хемокинов и молекул клеточной адгезии (intercellular adhesion molecule-1 – ICAM-1, vascular cell adhesion molecule-1 – VCAM-1), которые приводят к миграции лейкоцитов и лейкостазу. Повреждение эндотелия, усиление агрегации элементов крови, активация факторов коагуляции приводят к окклюзии капилляров и ретинальной ишемии, которая запускает повышенную экспрессию эндотелиального фактора роста сосудов (vascular endothelial growth factor – VEGF), что является одним из самых значимых звеньев в патогенезе диабетического макулярного отека (ДМО) и ДР. Открытие шунтов – интраретинальных микрососудистых аномалий (ИРМА) – в ответ на значительное снижение кровоснабжения лишь усугубляет ситуацию, поскольку перераспределяет кровоток в обход неперфузируемой сетчатки [3, 4].
Увеличение выработки VEGF выше критического уровня способствует развитию основных клинических проявлений диабетического поражения сетчатки – макулярного отека и неоваскуляризации [5, 6]. Воздействуя на эндотелиальные белки плотных межклеточных контактов, VEGF способствует повышению сосудистой проницаемости. Это усиливает экссудацию и накопление экстрацеллюлярной жидкости и белков в ткани сетчатки. Жидкость, которая проходит через стенку капилляров, в норме должна реабсорбироваться пигментным эпителием (наружный гематоретинальный барьер) и соседними капиллярами сетчатки. Когда диффузия превышает потенциальные возможности пигментного эпителия и капилляров к реабсорбции жидкостей, возникают клинические признаки макулярного отека. Значимое влияние на развитие ДМО оказывает увеличение выработки провоспалительных цитокинов выше критического уровня и активация мюллеровских клеток.
Повышенная экспрессия VEGF инициирует процесс ангиогенеза, представляющего собой упорядоченную последовательность сложных процессов:
— активация эндотелиальных клеток и изменение их формы;
— перицеллюлярная секреция протеаз и деградация внеклеточного матрикса;
— пролиферация и миграция эндотелиальных клеток, инвазия ими внеклеточного матрикса;
— дифференцировка тяжей мигрирующих эндотелиальных клеток в новообразованные сосуды, имеющие просвет, но лишенные базальной мембраны.
Новообразованные сосуды растут по задней поверхности стекловидного тела. Стенка новообразованного сосуда неполноценна, что приводит к выходу за его пределы как компонентов плазмы, так и цельной крови. Это стимулирует разрастание соединительной ткани в зонах неоваскуляризации. Поскольку соединительная ткань всегда стремится к сокращению, а адгезия фиброваскулярного конгломерата к задней поверхности стекловидного тела очень плотная, то развивается отслойка стекловидного тела. Как правило, в этот момент происходит разрыв новообразованных сосудов с развитием преретинальных (перед поверхностью сетчатки) или витреальных (в полость стекловидного тела) кровоизлияний. Рецидивирующие кровоизлияния, рубцевание задних отделов стекловидного тела ведут к образованию патологических витреоретинальных сращений, которые могут вызвать тракционную отслойку сетчатки. В дальнейшем возможно разрастание новообразованных сосудов по радужной оболочке (рубеоз) и в углу передней камеры, приводящее к развитию неоваскулярной глаукомы и к некупируемому повышению внутриглазного давления.
Таким образом, современные представления о патогенезе ДР позволяют выделить пять основных процессов в ее развитии:
— формирование микроаневризм;
— патологическая сосудистая проницаемость;
— сосудистая окклюзия;
— неоваскуляризация и фиброзная пролиферация;
— сокращение фибровоскулярной ткани и стекловидного тела.
Эпидемиология
Эпидемиология заболевания или состояния (группы заболеваний или состояний)
ДР является основной причиной слепоты у трудоспособного населения развитых стран и входит в число ведущих причин снижения зрения в возрастной группе старше 65 лет. Подсчитано, что слепота у больных СД развивается в 25 раз чаще, чем в среднем в популяции [7]. За последние три десятилетия распространенность СД (стандартизованная по возрасту) существенно возросла в странах с любым уровнем дохода, что отражает рост числа людей с избыточным весом или ожирением во всем мире. Глобальная распространенность диабета выросла с 4,7% в 1980 году до 8,5% в 2014 году [2].
Основными причинами снижения зрения у больных СД являются пролиферативная диабетическая ретинопатия (ПДР) и ДМО [2]. В Висконсинском эпидемиологическом исследовании была показана корреляция между ДР и типом, длительностью и тяжестью СД [7 — 10]. При СД 1 типа с длительностью заболевания более 20 лет ДР диагностируется более чем у 88% пациентов [7]. При СД 2 типа наибольшая распространенность (65,2%) отмечается в группе пациентов с 15-20-летним стажем диабета [8]. При некомпенсированном СД симптомы ДР встречаются практически в 2 раза чаще, чем при компенсированном СД [7 — 9]. Так или иначе, на каком-то этапе жизни более чем у трети людей с СД разовьется ДР [10]. Статистически достоверного различия частоты заболеваемости ДР между мужчинами и женщинами не выявлено. Несколько большее абсолютное число женщин с диагнозом ДР обусловлено их большей обращаемостью к врачам и заботой о собственном здоровье [7].
По результатам глобального метаанализа (в США, Европе, Австралии и Азии) было показано, что у каждого третьего больного СД (34,6%) наблюдалась какая-либо ДР, у каждого десятого (10,2%) была угрожающая потерей зрения форма (ПДР и/или ДМО) [11]. В 2010 г. в мире насчитывалось более 92 млн взрослых, имеющих какую-либо ретинопатию, 17 млн с ПДР, 20 млн с ДМО и 28 млн с угрожающей потерей зрения ДР. В 2015 г. 145 млн человек имели ДР, в том числе 45 млн человек – на стадии, угрожающей потерей зрения [10, 11]. В Российской Федерации в 2016 г. распространенность ДР составила: при СД 1 типа – 38,3% (3805,6 на 10 тыс. взрослых), при СД 2 типа – 15,0% (1497,0 на 10 тыс. взрослых) [12]. Структура новых случаев ДР: непролиферативная стадия при СД 1 типа – 71,4%, при СД 2 типа – 80,3%, препролиферативная ДР (ППДР) – 16,4% и 13,8%, соответственно, ПДР – 12,1% и 5,8%, соответственно, терминальная – 0,2% и 0,1%, соответственно [12]. По официальной статистике на 31.12.2017 года число пациентов с ДР в Российской Федерации превысило 580000 человек [12]. В большинстве регионов фактическая распространенность ДР превышает регистрируемую по обращаемости в несколько раз [12].
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний или состояний)
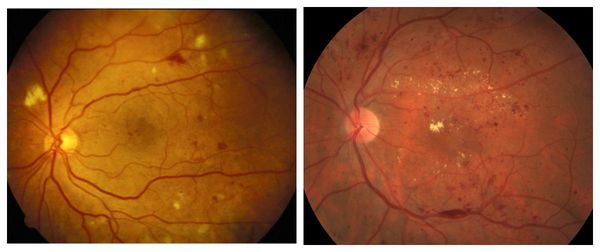
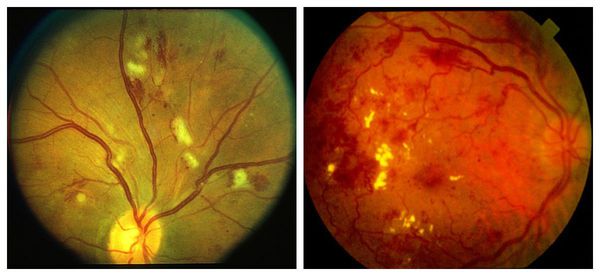
Изменения на глазном дне у больных СД развиваются последовательно от состояний, связанных с повышенной проницаемостью и окклюзией ретинальных сосудов, до появления новообразованных сосудов и фиброглиальной ткани. Детальное описание клинической картины в зависимости от стадии ДР представлены в табл. 1 и 2.
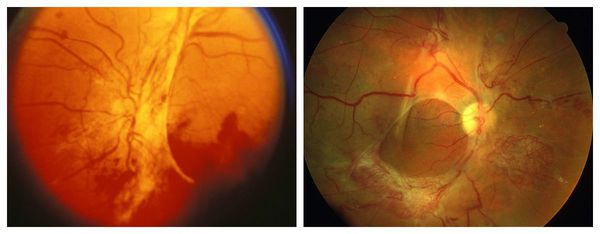
Осложненные формы пролиферативной ДР включают развитие рубеоза радужки и вторичной неоваскулярной глаукомы, преретинальных и интравитреальных кровоизлияний, тракционного синдрома и/или тракционной отслойки сетчатки вследствие образования витреоретинальных фиброглиальных шварт.
Клиническая картина диабетической макулопатии
На любой стадии заболевания может развиваться поражение области желтого пятна, называемое диабетической макулопатией и являющееся одной из основных причин снижения зрения. При биомикроскопии глазного дна выявляется деформация или утрата фовеолярного рефлекса, утолщение сетчатки в макулярной зоне и отложение липидных экссудатов. Длительно существующий макулярный отек может приводить к кистовидным, фиброзным и атрофическим изменениям сетчатки.
Ишемическая макулопатия связана с резким нарушением кровотока перифовеолярной зоны и практически не проявляет себя при офтальмоскопии. Предположить наличие такого варианта макулопатии позволяет несоответствие между низкой остротой зрения и незначительными изменениями на глазном дне в области желтого пятна. Достоверно оценить ишемическое поражение макулы позволяют дополнительные методы диагностики, такие как оптическое исследование сетчатки с помощью компьютерного анализатора в сосудистом режиме (ОКТ-ангиография) и флюоресцентная ангиография. Ишемическая макулопатия дает наихудший прогноз в отношении остроты зрения.
Тракционная макулопатия может развиваться вследствие нарушения витреоретинальных взаимоотношений (вертикальные тракции) или плотности внутренней пограничной мембраны сетчатки (горизонтальные тракции). При биомикроскопии выявляются патологические макулярные рефлексы и деформация ретинальных структур. Возможно появление ретинального отека (тракционный отек).
Клиническая картина транзиторной диабетической ретинопатии
На фоне быстрого снижения уровня гликемии у пациентов с выраженной декомпенсацией СД возможна транзиторная ретинопатия, которая характеризуется доброкачественным течением. Для правильной трактовки офтальмоскопической картины и постановки диагноза «транзиторная ретинопатия» необходим тщательный сбор анамнеза с выяснением эпизода (эпизодов) резкого снижения уровня гликемии.
Клинические проявления транзиторной ретинопатии достаточно вариабельны и могут проявляться как появлением, так и увеличением ретинальных геморрагий, «ватных» экссудатов и макулярного отека. Особое внимание необходимо уделять состоянию ДЗН, поскольку диабетический папиллит (иногда изолированный) является достаточно частым, но плохо фиксируемым проявлением транзиторной ретинопатии. Одним из тяжелых проявлений транзиторной ретинопатии является ишемическая макулопатия, лечение которой без наличия ретинального отека нецелесообразно. Изменения, как правило, подвергаются самопроизвольному регрессу в течение нескольких месяцев. Лазерная коагуляция сетчатки, как правило, не требуется [16].
Диабетическая папиллопатия (диабетический папиллит) характеризуется преходящим отеком диска зрительного нерва, наличием «мягких» экссудатов и ретинальных геморрагий в поверхностных слоях сетчатки по краю диска зрительного нерва. Течение обычно доброкачественное, и специфического лечения не требуется [16].
Другие поражения органа зрения диабетического генеза
У пациентов с СД (особенно декомпенсированным) вследствие метаболических нарушений отмечается раннее появление и более интенсивное прогрессирование катаракты.
Наиболее частым проявлением мононейропатии является поражение глазодвигательных и отводящих нервов. Пациенты могут жаловаться на отклонение глазного яблока, двоение и опущение верхнего века, что подтверждается при офтальмологическом осмотре.
Вследствие нарушения иннервации роговицы может развиться эпителиопатия роговицы, которая может приводить к рецидивирующим эрозиям роговицы.
Диагностика
Диагностика заболевания или состояния (группы заболеваний или состояний) медицинские показания и противопоказания к применению методов диагностики
Диагностика ДР и ДМО должна быть направлена на выявление начальных изменений, что особенно важно, принимая во внимание наличие в арсенале современной офтальмологии эффективных методов сохранения зрения при этом заболевании.
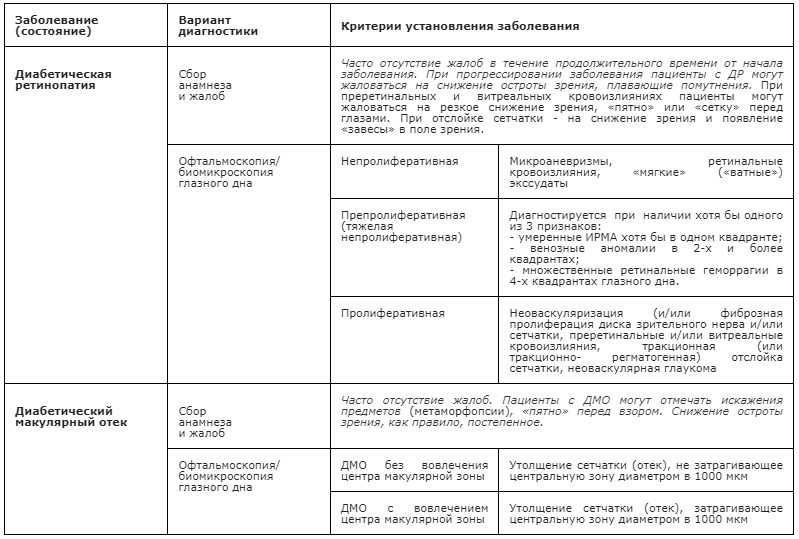
Таблица 3. Основные диагностические критерии установления ДР и ДМО
Жалобы и анамнез
-
Рекомендуется сбор анамнеза и жалоб при патологии глаза всем пациентам с подозрением на диабетическое поражение сетчатки с целью выяснения наличия функциональных зрительных расстройств [10, 17, 18, 19].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: возможно отсутствие жалоб в течение продолжительного времени, несмотря на прогрессирование заболевания. Пациенты с ДР могут жаловаться на снижение остроты зрения, плавающие помутнения. При ДМО пациенты отмечают искажения предметов (метаморфопсии), «пятно» перед взором, снижение остроты зрения [17]. При осложнениях ПДР (преретинальных и интравитреальных кровоизлияниях) пациенты могут жаловаться на снижение зрения, «пятно», «сетку» перед глазами, при отслойке сетчатки — на снижение зрения и появление «завесы» в поле зрения. Жалобы на снижение остроты зрения требуют, как правило, незамедлительного специализированного лечения. При развитии нейропатии с поражением III и VI пар черепномозговых нервов пациенты могут жаловаться на отклонение глазного яблока, двоение и опущение верхнего века. Из общего анамнеза важно уточнить давность СД и степень контроля заболевания (уровень сахара крови, гликированного гемоглобина), наличие артериальной гипертензии, показатели липидного обмена, наличие макрососудистых или иных микрососудистых осложнений СД [1, 2].
Физикальное обследование
-
Не рекомендуется физикальное обследование пациентам с целью диагностики и лечения ДР и ДМО [10, 18].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: физикальное обследование рекомендуется всем пациентам с СД в рамках ведения основного заболевания (в том числе для оценки риска возникновения или прогрессирования ДР и ДМО) и выполняется врачом терапевтического профиля (эндокринологом, терапевтом или врачом общей практики) согласно клиническим рекомендациям по ведению больных с различными типами СД [10, 17, 18, 19]. Также необходимо направлять к профильным специалистам за консультацией пациентов с иными сопутствующими системными заболеваниями и факторами риска системных осложнений перед выполнением лазерного или хирургического лечения (в том числе, интравитреального введения лекарственных препаратов) с целью выявления возможных противопоказаний к данным видам лечения и минимизирования риска осложнений [19]. Выбор профиля специалиста (эндокринолог, терапевт, отоларинголог, стоматолог и др.) определяется в зависимости от особенностей течения СД, планируемого лечения и наличия у пациента иного сопутствующего системного заболевания и фактора риска системных осложнений.
Лабораторные диагностические исследования
-
Рекомендуется исследование уровня глюкозы в крови, исследование уровня гликированного гемоглобина в крови (HbA1c), анализ крови по оценке нарушений липидного обмена биохимический, исследование уровня холестерина в крови, исследование уровня холестерина липопротеинов низкой плотности в крови, исследование уровня холестерина липопротеинов высокой плотности в крови, исследование уровня триглицеридов в крови, всем пациентам с диабетическим поражением сетчатки при отрицательной динамике состояния глазного дна, необходимости оценки общего статуса и степени риска прогресcирования поражений сетчатки, а также риска осложнений лечения при планировании или изменении тактики ведения пациента [18, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: выбор лабораторного исследования определяется в зависимости от особенностей течения СД и наличия у пациента сопутствующего системного заболевания и фактора риска системных осложнений. Также рекомендуется направлять на лабораторное исследование пациентов с сопутствующими системными заболеваниями и факторами риска системных осложнений до выполнения лазерного или хирургического лечения (в том числе, интравитреальному введению лекарственных препаратов) с целью выявления возможных противопоказаний к данным видам лечения [19, 20].
-
Рекомендуется общий (клинически) анализ крови, биохимический анализ крови общетерапевтический (исследование уровня общего белка в крови, исследование уровня глюкозы в крови, исследование уровня мочевины в крови, исследование уровня креатинина в крови, исследование уровня общего билирубина в крови, исследование уровня связанного (конъюгированного) билирубина в крови, определение активности аспартатаминотрансферазы в крови, определение активности аланинаминотрансферазы в крови, определение активности щелочной фосфатазы в крови, исследование уровня холестерина в крови, исследование уровня холестерина липопротеинов низкой плотности в крови, исследование уровня триглицеридов в крови, исследование уровня гликированного гемоглобина в крови (HbА1C), коагулограмма (ориентировочное исследование системы гемостаза), общий (клинический) анализ мочи, определение антител к бледной трепонеме (Treponema pallidum) иммуноферментным методом (ИФА) в крови, определение антигена (HbsAg) вируса гепатита B (Hepatitis B virus) в крови, определение антител к вирусу гепатита С (Hepatitis С virus) в крови, молекулярно-биологическое исследование крови на вирус иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV 1), определение антител классов М, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-1(Human immunodeficiency virus HIV 1) в крови, определение антител классов М, G (IgM, IgG) к вирусу иммунодефицита человека ВИЧ-2(Human immunodeficiency virus HIV 2) в крови, определение ДНК вируса иммунодефицита человека методом ПЦР, качественное исследование пациентам с ДР и ДМО при подготовке к хирургическому лечению (в том числе, интравитреальному введению лекарственных препаратов) или госпитализации с иной целью с кратностью в соответствии с действующими федеральными, региональными и локальными нормативными документами для оценки общего статуса, выявления сопутствующих заболеваний и возможных противопоказаний к данным видам лечения, минимизирования риска осложнений [19, 21 — 23].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: обследование проводится на основании добровольного согласия (санитарно-эпидемиологические правила СП 3.1.5.2826-10 «Профилактика ВИЧ-инфекции»). Выбор лабораторного исследования определяется в зависимости от наличия у пациента сопутствующего системного заболевания и фактора риска системных осложнений [21].
Инструментальные диагностические исследования
-
Рекомендуется визометрия всем пациентам с ДР и ДМО при диагностике заболевания, динамическом наблюдении и контроле за лечением с целью определения тяжести зрительных расстройств [10, 17 — 19].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
Рекомендуется рефрактометрия или определение рефракции с помощью набора пробных линз всем пациентам с ДР и ДМО при диагностике заболевания, динамическом наблюдении и контроле за лечением с целью определения максимально корригированной остроты зрения для точной оценки тяжести зрительных расстройств [10, 18].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
Рекомендуется офтальмотонометрия (в том числе, под местной анестезией с использованием раствора местного анестетика) всем пациентам с ДР и ДМО при диагностике заболевания, динамическом наблюдении и контроле за лечением с целью выявления нарушений офтальмотонуса [10, 17 – 19, 24].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
Рекомендуется биомикроскопия переднего отдела глаза и стекловидного тела всем пациентам с ДР и ДМО при диагностике заболевания, динамическом наблюдении и контроле за лечением с целью выявления неоваскуляризации радужки, оценки прозрачности оптических сред, наличия отслойки стекловидного тела [10, 17 — 19].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: биомикроскопию переднего отдела глазного яблока в обязательном порядке необходимо сначала проводить без мидриаза, поскольку расширение зрачка может затруднить выявление «ранней» неоваскуляризации радужки. Биомикроскопию стекловидного тела, наоборот, желательно проводить после медикаментозного мидриаза, что улучшает качество диагностики.
-
Рекомендуется гониоскопия под местной анестезией (с использованием раствора местного анестетика) пациентам с выявленным при биомикроскопии радужки рубеозом и/или нарушением регуляции офтальмотонуса при диагностике заболевания, динамическом наблюдении и контроле за лечением с целью определения причин повышения внутриглазного давления и выработки оптимальной тактики ведения [10, 17 — 19].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
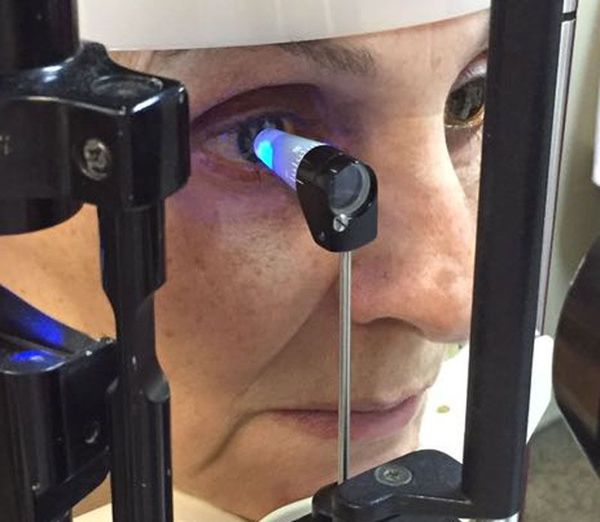
Рекомендуется биомикроскопия глазного дна или офтальмоскопия в условиях медикаментозного мидриаза (с использованием антихолинергических средств и симпатомиметиков (исключая противоглаукомные препараты), включая фиксированные комбинации) всем пациентам с ДР и ДМО при диагностике заболевания, динамическом наблюдении и контроле за лечением с целью выявления изменений на глазном дне, оценки их тяжести, мониторинга и выбора оптимальной тактики ведения [10, 17 — 19].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: биомикроскопия глазного дна с асферическими линзами при помощи щелевой лампы (или офтальмоскопия) является основным методом диагностики изменений глазного дна диабетического генеза в рамках офтальмологического приема при любом виде (первичная медико-санитарная помощь, специализированная помощь) и условии (стационарная, амбулаторная) оказания медицинской помощи. У больных СД она должна проводиться только с широким зрачком (в условиях медикаментозного мидриаза). Важно помнить, что до фармакологического расширения зрачка нужно оценить глубину передней камеры.
-
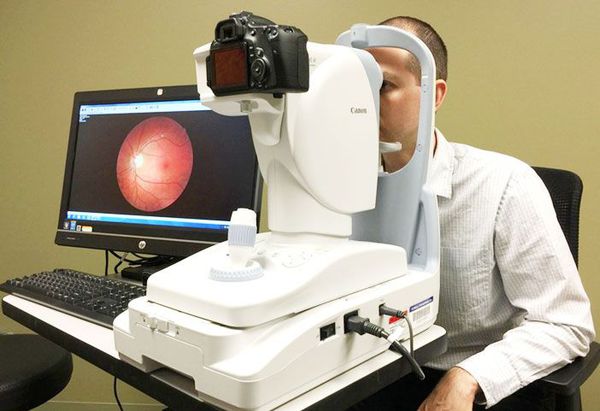
Рекомендуется биомикрофотография глазного дна с использованием фундус-камеры (при наличии технической возможности) пациентам в условиях медикаментозного мидриаза (с использованием антихолинергических средств и симпатомиметиков (исключая противоглаукомные препараты), включая фиксированные комбинации) при диагностике заболевания, динамическом наблюдении и контроле за лечением с целью скрининга, мониторинга и оценки эффективности лечения [10, 17 — 19].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: необходимость и частота фотографирования глазного дна с помощью фундус-камеры определяется врачом-офтальмологом в зависимости от особенностей течения ДР, ДМО и СД. Фотографирование глазного дна необходимо выполнять в условиях расширенного зрачка. Во многих исследованиях было показано, что фармакологический мидриаз значительно повышает качество фотографий. Именно поэтому в настоящее время съемку глазного дна рекомендуется выполнять в условиях медикаментозного мидриаза независимо от типа ретинальной камеры [10, 18, 19].
-
Рекомендуется оптическое исследование сетчатки с помощью компьютерного анализатора (оптическая когерентная томография, ОКТ) (при наличии технических возможностей) в условиях медикаментозного мидриаза (с использованием антихолинергических средств и симпатомиметиков (исключая противоглаукомные препараты), включая фиксированные комбинации) пациентам с ДМО или с подозрением на его наличие при диагностике заболевания, динамическом наблюдении и контроле за лечением с целью его количественной и качественной оценки, а также мониторирования эффективности лечения [10, 17 – 19, 25, 26].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: при оценке эффективности лечения интравитреальными введениями средств, препятствующих новообразованию сосудов, и глюкокортикоидов для местного применения следует оценивать количественные и качественные параметры томограмм. Анатомические параметры, наряду с остротой зрения являются ключевыми факторами активности заболевания, используемыми для мониторинга эффективности лечения и принятия решения о начале/возобновлении лечения пациента с ДМО. Оптическое исследование сетчатки с помощью компьютерного анализатора рекомендуется выполнять в условиях фармакологического мидриаза, поскольку это значительно повышает качество сканирования.
-
Рекомендуется оптическое исследование сетчатки с помощью компьютерного анализатора в режиме ангиографии (оптическая когерентная томография в режиме ангиографии, ОКТ-А) (при наличии технических возможностей) в условиях медикаментозного мидриаза (с использованием антихолинергических средств и симпатомиметиков (исключая противоглаукомные препараты), включая фиксированные комбинации) при диагностике заболевания, динамическом наблюдении и контроле за лечением пациентам со сниженным зрением, которое нельзя объяснить прозрачностью оптических сред и офтальмоскопической картиной с целью выявления и оценки площади ишемических зон в макулярной зоне, а также пациентам с ранней ретинальной неоваскуляризацией для ее точной локализации [26 — 28].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Комментарии: необходимость и частота ОКТ-А определяется врачом-офтальмологом в зависимости от особенностей течения заболевания. Оптическое исследование сетчатки с помощью компьютерного анализатора в режиме ангиографии рекомендуется выполнять в условиях фармакологического мидриаза, поскольку это значительно повышает качество исследования.
-
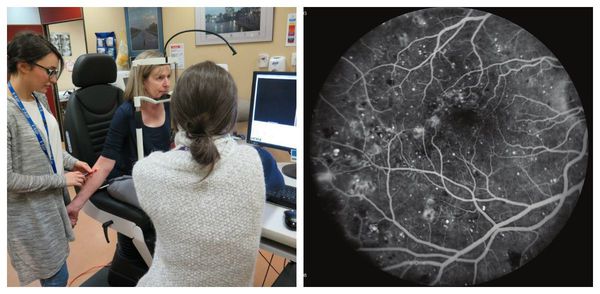
Рекомендуется флюоресцентная ангиография глаза (ФАГ) в условиях медикаментозного мидриаза (с использованием антихолинергических средств и симпатомиметиков (исключая противоглаукомные препараты), включая фиксированные комбинации) при диагностике заболевания, динамическом наблюдении и контроле за лечением пациентам с подозрением на нарушение перфузии сетчатки, внутреннего гемато-ретинального барьера с целью разработки тактики лечения, пациентам с необъяснимым снижением зрения с целью выявления ишемической макулопатии, пациентам с рефрактерным ДМО с целью выявления ишемии на периферии сетчатки как источника повышенной экспрессии сосудистого эндотелиального фактора роста, пациентам с рецидивирующими витреальными кровоизлияниями из необъяснимого источника с целью его локализации [10, 17, 18, 26].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
Рекомендуется ультразвуковое исследование глазного яблока всем пациентам с диабетическим поражением глаз и недостаточной прозрачностью оптических сред при диагностике заболевания, динамическом наблюдении и контроле за лечением с целью диагностики нарушений витреоретинальных взаимоотношений [17].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
Рекомендуется периметрия пациентам с диабетическим поражением глаз и подозрением на поражение зрительного нерва при диагностике заболевания, динамическом наблюдении и контроле за лечением с целью оценки функции сетчатки и проводящих путей [17].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
Рекомендуется электрофизиологическое исследование пациентам с необъяснимым снижением зрительных функций с целью оценки функции сетчатки и проводящих путей [17].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: решение о назначении иных дополнительных методов исследования принимает врач по результатам базового обследования.
Иные диагностические исследования
-
Рекомендуется флюорография легких (или флюорография легких цифровая) или рентгенография легких (или рентгенография легких цифровая) всем пациентам с ДР и ДМО при подготовке к хирургическому лечению (в том числе интравитреальному введению лекарственных препаратов) либо госпитализации с иной целью с кратностью в соответствии с действующими нормативными документами федерального, регионального и локального уровней для оценки общего статуса, выявления сопутствующих заболеваний и возможных противопоказаний к данным видам лечения, минимизирования риска осложнений [19, 21-23].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
-
Рекомендуется регистрация электрокардиограммы (с расшифровкой, описанием и интерпретацией электрографических данных) всем пациентам с ДР и ДМО при подготовке к хирургическому лечению (в том числе интравитреальному введению лекарственных препаратов) либо госпитализации с иной целью с кратностью в соответствии с действующими нормативными документами федерального, регионального и локального уровней для оценки общего статуса, выявления сопутствующих заболеваний и возможных противопоказаний к данным видам лечения, минимизирования риска осложнений [22, 23].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Лечение
Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
-
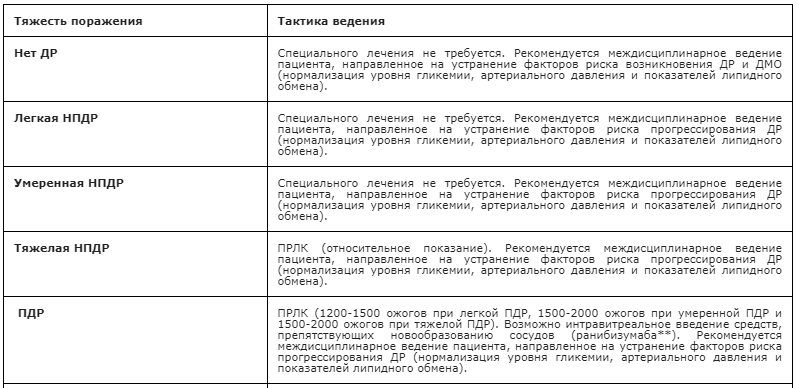
Рекомендуется междисциплинарное ведение пациента на всех стадиях ДР и ДМО с целью компенсации системных нарушений (нормализация уровня гликемии, артериального давления и показателей липидного обмена) [1, 18, 20, 29, 30].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: на всех стадиях ДР и ДМО должно проводиться лечение основного заболевания – СД, направленное на коррекцию метаболических нарушений [1, 2, 10, 18, 19, 29]. Согласно данным клинических и экспериментальных работ, существует четкая корреляция между степенью компенсации гликемии и развитием ДР. Исследование DCCT показало, что чем лучше проводился контроль гликемии, тем меньше был риск и частота развития ДР [29, 31]. Жесткий контроль уровня глюкозы крови, артериального давления и липидного обмена ассоциированы с меньшей вероятностью развития и меньшей скоростью прогрессирования ДР [17-19, 29 — 36].
-
Не рекомендуется специальное офтальмологическое лечение пациентам на стадии непролиферативной ДР (до 47 уровня включительно при применении классификации ETDRS) [1, 17].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
1. Консервативное лечение
-
Не рекомендуется консервативное лечение пациентам с ДР и ДМО [10, 17, 18, 26].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Коррекция липидного статуса при помощи гиполипидемического средства фенофибрата** может замедлять прогрессирование ДР [26, 34, 36].
2. Лазерное лечение
-
Рекомендуется проведение панретинальной лазерной коагуляции под местной анестезией (с использованием раствора местного анестетика) в условиях медикаментозного мидриаза (с использованием антихолинергических средств и симпатомиметиков (исключая противоглаукомные препараты), включая фиксированные комбинации) на стадии препролиферативной ДР (относительное показание) в случае невозможности регулярного мониторинга пациента с целью подавления экспрессии VEGF и профилактики развития неоваскуляризации, уменьшение клинических симптомов диабетической ретинопатии, стабилизации или повышения корригированной остроты зрения [14, 16 – 18, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: стандартная панретинальная лазеркоагуляция обычно осуществляется за несколько сеансов [10, 17, 18, 20]. Сеансы панретинальной лазеркоагуляции могут проводиться как в стационарных, так и в амбулаторных условиях при максимальном медикаментозном мидриазе [37 — 40].
-
Рекомендуется панретинальная лазерная коагуляция под местной анестезией (с использованием раствора местного анестетика) в условиях медикаментозного мидриаза (с использованием антихолинергических средств и симпатомиметиков (исключая противоглаукомные препараты), включая фиксированные комбинации), возможно, в сочетании с интравитреальным введением средства, препятствующего новообразованию сосудов — ранибизумаба** (см. раздел Хирургическое лечение) на стадии ПДР с целью подавления неоваскуляризации, уменьшение клинических симптомов диабетической ретинопатии, стабилизации или повышения корригированной остроты зрения [37 — 41].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2)
Комментарии: при уровне HbA1c более 10% и наличии ПДР панретинальная лазеркоагуляция должна проводиться, не дожидаясь существенного улучшения контроля гликемии.
У панретинальной лазеркоагуляции сетчатки существуют определенные побочные эффекты. Поэтому этот метод лазерного лечения выполняется, как правило, тогда, когда уже имеются новообразованные сосуды или риск их появления крайне высок. Вероятность развития слепоты при появлении новообразованных сосудов настолько высока, что оправдывает применение лазерного лечения, несмотря на побочные эффекты [17, 37 – 41].
Панретинальную лазерную коагуляцию сетчатки обычно начинают с нижних отделов средней периферии, так как эти зоны могут стать недоступными в случае возникновения кровоизлияния в стекловидное тело. Далее лазерное воздействие продолжают, нанося коагуляты на всю поверхность средней периферии глазного дна от височных сосудистых аркад. При наличии ПДР с неоваскуляризацией радужки и/или угла передней камеры необходимо коагулировать также крайние периферические отделы сетчатки.
Показанием к незамедлительному проведению панретинальной лазеркоагуляции является ПДР в сочетании с «факторами высокого риска снижения зрения», которые определяются как:
— неоваскуляризация сетчатки, размер которой превышает 1/2 площади ДЗН;
— неоваскуляризация ДЗН, размер которой превышает 1/3 площади ДЗН;
— витреальная или преретинальная геморрагия.
-
Рекомендуется проведение фокальной лазерной коагуляции глазного дна под местной анестезией (с использованием раствора местного анестетика) в условиях медикаментозного мидриаза (с использованием антихолинергических средств и симпатомиметико (исключая противоглаукомные препараты), включая фиксированные комбинации), в том числе в сочетании с интравитреальными введениями средств, препятствующих новообразованию сосудов или глюкокортикоидов для местного применения (см. раздел Хирургическое лечение) при наличии клинически значимого ДМО с целью стабилизации или повышения корригированной остроты зрения [15 – 18, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: при наличии ДМО наибольший эффект от лазерного лечения (фокальной или по типу «решетки» лазерной коагуляции сетчатки) ожидается в случае исходной центральной толщины сетчатки не более 350 мкм. В остальных случаях лазерное лечение ДМО существенно уступает по функциональному результату лечению средствами, препятствующими новообразованию сосудов (ингибиторами ангиогенеза) [42].
-
Рекомендуется проведение фокальной лазерной коагуляции глазного дна ретинальных новообразованных сосудов под местной анестезией (с использованием раствора местного анестетика) в условиях медикаментозного мидриаза (с использованием антихолинергических средств и симпатомиметиков (исключая противоглаукомные препараты), включая фиксированные комбинации), в том числе в сочетании с интравитреальным введением средства, препятствующего новообразованию сосудов (ранибизумаба**) при наличии активных новообразованных ретинальных сосудов, несмотря на ранее проведенную панретинальную лазерную коагуляцию с целью их прямого разрушения, уменьшения клинических симптомов диабетической ретинопатии и стабилизации корригированной остроты зрения [16, 18, 37, 38, 41].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
3. Хирургическое лечение
3.1 Интравитреальное введение лекарственных средств
-
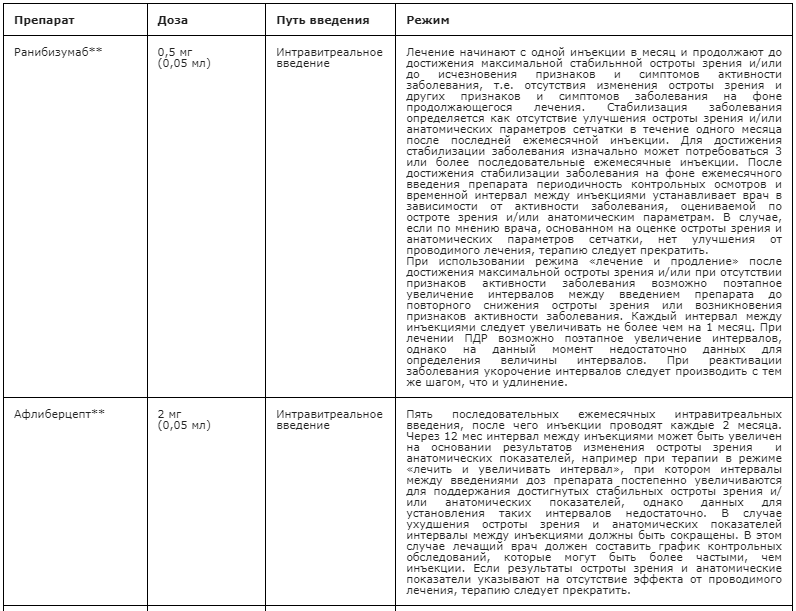
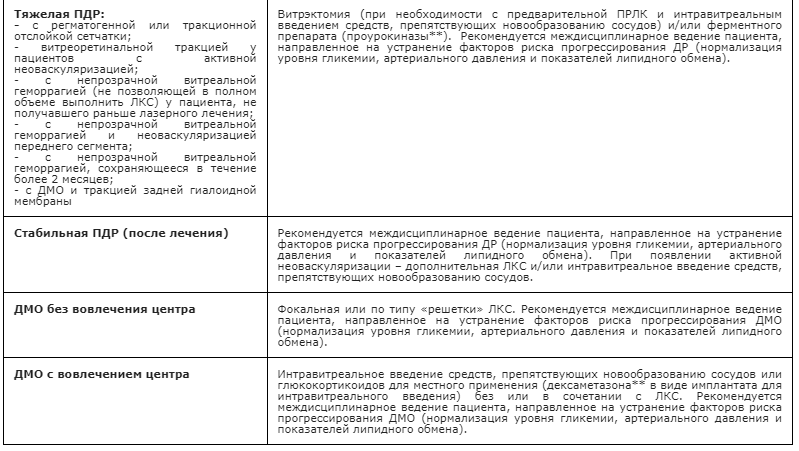
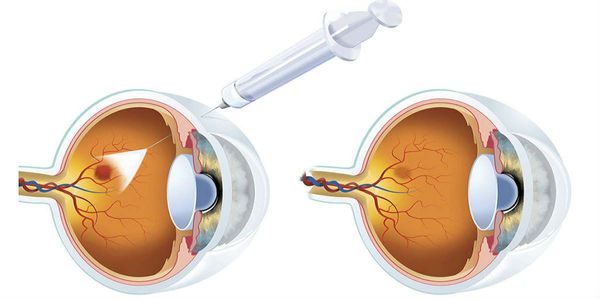
Рекомендуются интравитреальные инъекции (в условиях операционной, под местной анестезией, после обработки кожи век, области вокруг глаз и глазной поверхности антибактериальными препаратами для местного применения (включая антисептики и дезинфицирующие средства, включая препараты йода) средств, препятствующих новообразованию сосудов – препаратов ранибизумаб** [42], афлиберцепт** [43], бролуцизумаба** [44] или глюкокортикоидов для местного применения (дексаметазон** в виде имплантата для интравитреального введения)** [45], возможно в сочетании с лазерной коагуляцией сетчатки [46] при наличии клинически значимого ДМО с целью уменьшения толщины сетчатки, стабилизации или повышения корригированной остроты зрения.
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2).
Комментарии: в настоящее время интравитреальное введение средств, препятствующих новообразованию сосудов (ингибиторов ангиогенеза), является терапией первой линии при ДМО с вовлечением центра макулы. Необходимо учитывать, что при сочетании лазеркоагуляции сетчатки и интравитреальных введений средств, препятствующих новообразованию сосудов, функциональный эффект отсроченного лазерного лечения будет лучше [23, 46 — 50].
-
Ранибизумаб** – это фрагмент гуманизированного антитела к эндотелиальному фактору роста сосудов А (VEGF-A). Избирательно связывается с VEGF-А (VEGF110, VEGF121, VEGF165), предотвращая его взаимодействие с рецепторами на поверхности клеток эндотелия, что приводит к подавлению неоваскуляризации и пролиферации эндотелиальных клеток [42, 51, 52].
-
Афлиберцепт** – это рекомбинантный гибридный белок, состоящий из фрагментов внеклеточных доменов человеческих рецепторов VEGF, соединенных с Fc-фрагментом человеческого иммуноглобулина G. Действует как растворимый рецептор-ловушка, который связывает VEGF-А и плацентарный фактор роста с более высокой аффинностью, чем их естественные рецепторы, и, таким образом, может ингибировать связывание и активацию этих родственных VEGF рецепторов [43, 53, 54].
-
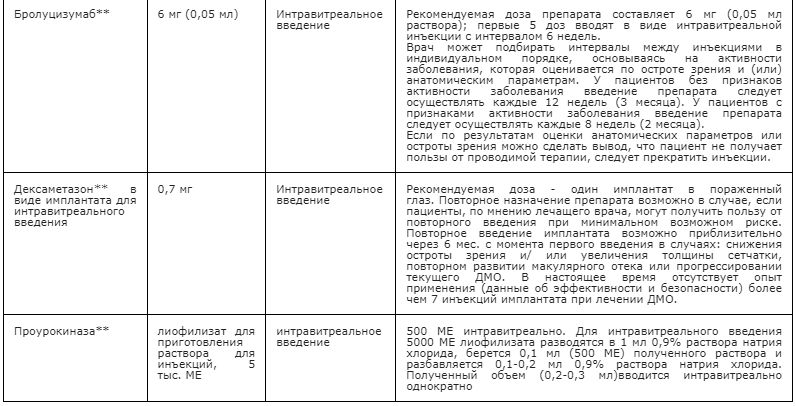
Бролуцизумаб** представляет собой одноцепочечный фрагмент гуманизированного антитела (ScFv, single-chain variable fragment) с молекулярной массой 26 кДа, который является наименьшей функциональной единицей антитела, что позволяет вводить в одной дозе больше молей вещества, чем при применении зарегистрированных ранее антител к VEGF, c потенциальной возможностью более длительного действия, более высокой пенетрацией в ткани [44]. Бролуцизумаб** с высокой аффинностью связывается с различными изоформами VEGF-A (в частности с VEGF110, VEGF121 и VEGF165), тем самым препятствуя связыванию VEGF-A с его рецепторами VEGFR-1 и VEGFR-2.
При лечении ранибизумабом** изначально может потребоваться 3 или более последовательные ежемесячные инъекции до достижения максимальной остроты зрения или до стабилизации заболевания, которая определяется как отсутствие улучшения остроты зрения и/или анатомических параметров сетчатки в течение одного месяца после последней ежемесячной инъекции. После достижения стабилизации периодичность контрольных осмотров и временной интервал между инъекциями устанавливает врач в зависимости от особенностей клинической картины. В случае выбора режима «Лечение и продление» интервал между инъекциями следует увеличивать не более, чем на 1 месяц.
При лечении афлиберцептом** начинают с пяти последовательных ежемесячных инъекций, затем выполняют по одной инъекции каждые два месяца. Через 12 месяцев лечения временной интервал между контрольными осмотрами и инъекциями может быть увеличен на основании оценки изменения остроты зрения и анатомических показателей, периодичность контроля состояния и лечения устанавливает врач в зависимости от течения заболевания. У пациентов с ДМО и исходной остротой зрения 0,4 и ниже наибольший функциональный результат ожидается при применении афлиберцепта** [26]. При лечении ДМО использование афлиберцепта** позволяет снизить необходимость применения лазеркоагуляции сетчатки [47, 48].
При лечении бролуцизумабом** первые пять инъекций производят с интервалом 6 недель. Далее врач может подбирать интервалы между инъекциями в индивидуальном порядке, основываясь на активности заболевания, которая оценивается по остроте зрения и (или) анатомическим параметрам. У пациентов без признаков активности заболевания введение препарата следует осуществлять каждые 12 недель (3 месяца). У пациентов с признаками активности заболевания введение препарата следует осуществлять каждые 8 недель (2 месяца) [44]. Если по результатам оценки анатомических параметров или остроты зрения можно сделать вывод, что пациент не получает пользы от проводимой терапии, следует прекратить инъекции.
В каждом клиническом случае окончательное решение о показаниях к лечению средствами, препятствующими новообразованию сосудов (ингибиторами ангиогенеза), выборе режима инъекций принимает врач на основе оценки особенностей клинической картины и течения заболевания.
Противопоказания к интравитреальному введению ранибизумаба**, афлиберцепта** или бролуцизумаба**:
-
повышенная чувствительность к компонентам препарата,
-
активные подтвержденные или предполагаемые инфекции глаза или инфекционные процессы периокулярной локализации,
-
активный интраокулярный воспалительный процесс,
-
беременность и период грудного вскармливания.
Глюкокортикостероид для местного применения (дексаметазон** в виде имплантата для интравитреального введения) обеспечивает длительное (до 6 месяцев) высвобождение действующего вещества в витреальной полости. Дексаметазон**, являясь сильнодействующим глюкокортикостероидом, подавляет воспаление, снижая выраженность отека, отложение фибрина, проницаемость капилляров и миграцию фагоцитов к месту воспаления. Глюкокортикостероиды подавляют экспрессию фактора роста эндотелия сосудов, а также предотвращают высвобождение простагландинов, часть из которых являются медиаторами кистовидного макулярного отека [45, 55 — 57].
Интравитреальное введение дексаметазона** в виде имплантата для интравитреального введения рекомендуется пациентам с ДМО, резистентному к лечению средствами, препятствующих новообразованию сосудов, и лазерному лечению, особенно в случаях артифакии, а также пациентам с высоким кардиоваскулярным риском [26]. Кроме этого, применение имплантата дексаметазона** целесообразно у тех пациентов, которые не могут соблюдать график частых визитов в лечебное учреждение, требуемых при лечении средствами, препятствующих новообразованию сосудов [58].
Применение дексаметазона** в виде имплантата для интравитреального введения требует длительного регулярного мониторинга ВГД. Повторное введение имплантата возможно приблизительно через 6 месяцев в случае снижения остроты зрения и/или увеличения толщины сетчатки.
Противопоказания к интравитреальному введению дексаметазона** в виде имплантата для интравитреального введения:
-
повышенная чувствительность к компонентам препарата;
-
активные подтвержденные или предполагаемые инфекции глаза или инфекционные процессы периокулярной локализации;
-
развитая стадия глаукомы с декомпенсацией ВГД, не купирующегося медикаментозной терапией;
-
афакия с разрывом задней капсулы хрусталика;
-
наличие переднекамерной ИОЛ, ирис-клипс ИОЛ, заднекамерной ИОЛ с транссклеральной фиксацией при одновременном наличии разрыва задней капсулы хрусталика.
При интравитреальном введении лекарственных средств, препятствующих новообразованию сосудов или дексаметазона** в виде имплантата для интравитреального введения следует учитывать потенциальный риск осложнений, таких как инфекционный и неинфенкционный эндофтальмит, ятрогеннная катаракта, гемофтальм, отслойка сетчатки и другие [19, 59].
При использовании лекарственных средств, препятствующих новообразованию сосудов или дексаметазона** в виде имплантата для интравитреального введения предупреждение снижения остроты зрения даже при отсутствии ее улучшения следует считать положительной динамикой по сравнению с естественным течением заболевания.
-
Рекомендуется интравитреальное введение (в условиях операционной, под местной анестезией, после обработки кожи век, области вокруг глаз и глазной поверхности антибактериальными препаратами для местного применения (включая антисептики и дезинфицирующие средства, включая препараты йода) ферментного препарата – проурокиназы** пациентам с ПДР и преретинальным кровоизлиянием и/или гемофтальмом с целью ускорения его резорбции (возможно в сочетании с интравитреальным введением средства, препятствующего новообразованию сосудов — ранибизумаба**) [41, 60].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Противопоказания к интравитреальному введению проурокиназы:
— индивидуальная гиперчувствительность к компонентам препарата;
— состояния с высоким риском развития кровотечения, в том числе заболевания крови;
— активные подтвержденные или предполагаемые инфекции глаза или инфекционные процессы периокулярной локализации;
— активный интраокулярный воспалительный процесс;
— беременность и период кормления грудью;
— хроническая почечная недостаточность (уровень креатинина сыворотки более 0,02 г/л, мочевины более 0,5 г/л);
— тяжелая гепатоцеллюлярная недостаточность (альбумин крови менее 30 г/л).
3.2 Витреоретинальная хирургия
-
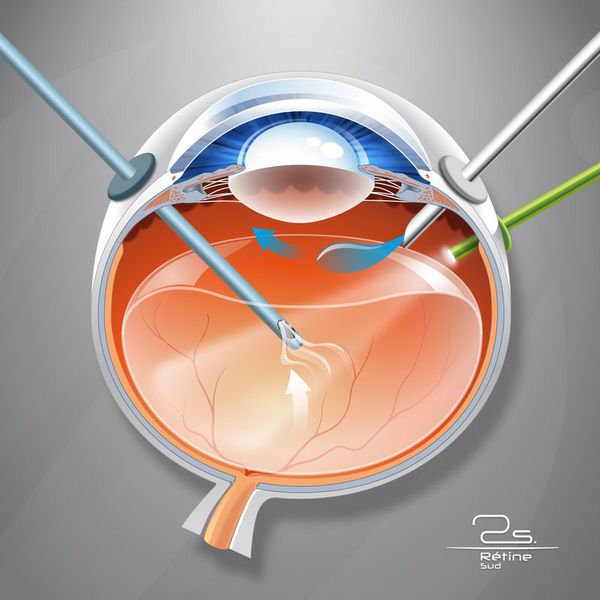
Рекомендуется микроинвазивная витреоэктомия или витреошвартэктомия (в условиях операционной; под местной анестезией (с использованием глазных капель местных анестетиков), при необходимости с пара- или ретробульбарной инъекцией местноанестезирующих препаратов (при необходимости – с использованием сочетанной анестезии), в условиях медикаментозного мидриаза (с использованием антихолинергических средств и симпатомиметиков (исключая противоглаукомные препараты), включая фиксированные комбинации), после обработки кожи век, области вокруг глаз и глазной поверхности антисептиками и дезинфицирующими средствами (включая препараты йода), с использованием противомикробных и противовоспалительных препаратов, при необходимости с сопутствующими манипуляциями, включая тампонаду витреальной полости (перфторорганическим или иным высокомолекулярным соединением), эндовитреальную замену перфторорганического соединения на силикон, эндовитреальное введение воздуха, силикона, эндолазеркоагуляцию, круговое или локальное эписклеральное пломбирование пациентам с ПДР, осложненной организовавшимся гемофтальмом и/или тракционной отслойкой сетчатки с захватом области макулы и/или тракционно-регматогенной отслойкой сетчаткой и/или тракцией области макулы, а также при тракционном ДМО с целью восстановления нормальных анатомических соотношений, стабилизации или повышения корригированной остроты зрения [61 — 63].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: в ходе микроинвазивной витреоэктомии или витреошвартэктомии, при наличии показаний, могут быть выполнены мембранопилинг, ретинотомия, эндолазеркоагуляция сетчатки, эндодиатермокоагуляция, эндотампонанада офтальмологическим газом, перфторорганическим соединением, силиконовым маслом и иные манипуляции. Подготовка пациента к хирургическому вмешательству осуществляется совместно с врачом-эндокринологом, врачом-терапевтом. При необходимости назначают консультацию врача-нефролога (при нарушении функции почек), врача-кардиолога (при наличии осложнений со стороны сердечно-сосудистой системы), врача-эндокринолога и/или врача-хирурга (при синдроме диабетической стопы).
Врач-офтальмолог, направляющий больного на витреальное вмешательство, должен обращать внимание на несколько моментов:
— степень выраженности патологических изменений для прогнозирования функционального результата операции;
— при кровоизлиянии в стекловидное тело необходимо оценить выраженность геморрагии (небольшое кровоизлияние, не затрудняющее проведение лазерного лечения и не приводящее к инвалидизации, не является показанием к операции);
— адекватность ранее выполненной лазерной коагуляции сетчатки (кровоизлияния могут возникать по причине недостаточной коагуляции);
— острота зрения другого глаза (витреоретинальное вмешательство можно рекомендовать раньше при инвалидизации пациента из-за низкой остроты зрения на другом глазу);
— тяжесть общего заболевания, предполагаемая продолжительность жизни пациента, риск анестезии.
-
Рекомендуется удаление силиконового масла (или иного высокомолекулярного соединения) из витреальной полости (в условиях операционной; под местной анестезией с использованием глазных капель местных анестетиков, при необходимости с пара- или ретробульбарной инъекцией местноанестезирующих препаратов, при необходимости с использованием сочетанной анестезии; в условиях медикаментозного мидриаза (с использованием антихолинергических средств и симпатомиметиков (исключая противоглаукомные препараты), включая фиксированные комбинации), после обработки кожи век, области вокруг глаз и глазной поверхности, антисептиками и дезинфицирующими средствами (включая препараты йода) с использованием противомикробных и противовоспалительных препаратов, при необходимости с сопутствующими манипуляциями, включая повторную тампонаду витреальной полости (перфторорганическим или иным высокомолекулярным соединением), эндовитреальную замену перфторорганического соединения на силикон, эндовитреальное введение воздуха, силикона, эндолазеркоагуляцию пациентам с ПДР в отдаленном периоде после операции витреоэктомии или витреошвартэктомии с целью предотвращения осложнений, связанных с чрезмерно длительной эндотампонадой силиконовым маслом [63, 64].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: продолжительность эндотампонады витреальной полости силиконовым маслом устанавливает врач на основе результатов динамического наблюдения пациента. Решение о необходимости повторной эндотампонады витреальной полости принимает врач на основе оценки состояния глаза пациента, риска рецидива кровоизлияния, отслойки сетчатки и др.
-
Рекомендуется до и после витреоретинального хирургического вмешательства инстилляции в конъюнктивальную полость противомикробных препаратов (включая антибиотики, фторхинолоны и противомикробные препараты другие), противовоспалительных препаратов (включая глюкокортикостероиды и нестероидные противовоспалительные препараты), противовоспалительных препаратов в комбинациии с противомикробными препаратами, при необходимости субконъюнктивальные и/или парабульбарные и/или внутримышечные и/или внутривенные инъекции антибактериальных препаратов или противомикробных препаратов системного действия (при отсутствии медицинских противопоказаний), включая антибактериальные препараты системного действия и кортикостероиды системного действия с целью профилактики послеоперационных осложнений [64].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: продолжительность инстилляций и инъекций лекарственных препаратов до и после витреоретинального хирургического вмешательства устанавливает врач на основе комплексной оценки клинической картины заболевания, особенностей течения операции и послеоперационного периода.
4. Диетотерапия
-
Рекомендуется количественная оценка усваиваемых углеводов по системе хлебных единиц всем пациентам с СД 1 типа для коррекции дозы инсулина и его аналогов перед едой [1, 65 — 69].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: общее потребление белков, жиров и углеводов при СД 1 типа не должно отличаться от такового у здорового человека. Рекомендуется определение соответствия дозы инсулина и его аналогов приему углеводов, уровню глюкозы в крови перед едой и ожидаемой физической активности пациентам с СД 1 для улучшения гликемического контроля [1]
-
Рекомендуется рассматривать питание как часть терапевтического плана у всех пациентов СД 2 при любом варианте медикаментозной сахароснижающей терапии с для достижения метаболических целей [70, 71].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: идеального процентного соотношения жиров белков, жиров и углеводов для всех пациентов с СД не существует. Рекомендации формируются на основе анализа актуального образца питания и метаболических целей. Всем пациентам с избыточной массой тела/ ожирением рекомендуется ограничение калорийности рациона с целью умеренного снижения массы тела. Достижение снижения массы тела наиболее эффективно при одновременном применении физических нагрузок и обучающих программ. Резкие нефизиологические ограничения в питании противопоказаны. Как правило, полезным для снижения массы тела может быть максимальное ограничение жиров (прежде всего животного происхождения) и сахаров, умеренное – продуктов, состоящих из сложных углеводов (крахмалов) и белков. Рекомендуется потребление углеводов в составе овощей, цельнозерновых, молочных продуктов, в отличие от источников углеводов, содержащих дополнительно насыщенные или транс жиры, сахара или натрий. Важно включать в рацион продукты богатые моно- и полиненасыщенными жирными кислотами (рыба, растительные масла). Питание должно быть частью терапевтического плана и должно способствовать достижению метаболических целей при любом варианте медикаментозной сахароснижающей терапии. Рекомендации по диетотерапии формируются врачом терапевтического профиля (эндокринологом, терапевтом или врачом общей практики) в рамках ведения основного заболевания. Рекомендуется оценка усваиваемых углеводов по системе хлебных единиц всем пациентам с СД 2 типа, получающим терапию инсулинами короткого действия и их аналогами для инъекционного введения, для коррекции дозы инсулинов и их аналогов перед едой [1].
Медицинская реабилитация
Медицинская реабилитация, медицинские показания и противопоказания к применению методов реабилитации
-
Рекомендуется подбор средств оптической коррекции слабовидения (очки, в том числе с дополнительным увеличением и встроенными монокулярами, специальные средства для получения информации для инвалидов с нарушением зрения) пациентам со слабовидением с целью повышения зрительных функций, качества жизни и социальной адаптации [1, 2, 10, 17].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Прогноз
Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
Пациент должен владеть информацией о необходимости нормализации уровня гликемии, артериального давления и показателей липидного обмена. Также необходимо настроить пациента на неукоснительное соблюдение всех назначений специалистов (врача-эндокринолога, врача-офтальмолога, врача-нефролога, врача-кардиолога, врача-терапевта, врача общей практики и т.д.).
Важно акцентировать внимание пациента с СД на необходимость осмотра врачом-офтальмологом не реже 1 раз в год (в случае СД 1 типа – через 5 лет от дебюта заболевания) даже при отсутствии жалоб со стороны органа зрения, а также безотлагательность обращения к врачу-офтальмологу при появлении жалоб со стороны органа зрения.
В случае наличия диабетических изменений со стороны глаз надо разъяснить пациенту рекомендуемую кратность обследования у врача-офтальмолога в зависимости от тяжести изменений, а также необходимость внеплановых осмотров при появлении любых новых зрительных расстройств.
Необходимо обсудить выявленные врачом-офтальмологом изменения со стороны глаз с врачами иных специальностей, курирующих пациента (врача-эндокринолога, врача-нефролога, врача-кардиолога, врача-терапевта, врача общей практики и т.д.).
Необходимо информировать пациентов, что эффективность лечения ДР и ДМО зависит от своевременности ее начала даже при отсутствии субъективных жалоб со стороны органа зрения.
В случае необратимой слепоты или слабовидения пациент должен владеть полной информацией о возможностях профессиональной, социальной, психологической реабилитации.
В случае применения метода интравитреального введения лекарственных средств необходимо обсудить с пациентом следующие моменты:
— перспективы лечения при помощи интравитреального введения лекарственных препаратов у пациентов с ДМО зависят от своевременного начала лечения и соблюдения оптимального режима инъекций в соответствии с инструкцией к препарату и клиническими рекомендациями на основе данных регулярного мониторинга;
— важно предупреждать пациентов, получающих интравитреальные инъекции, о необходимости незамедлительно сообщать о симптомах, при наличии которых можно заподозрить внутриглазное воспаление (эндофтальмит): боль в глазу или увеличение неприятных ощущений в глазу, усиление покраснения глаза, нечеткости или снижения зрения, увеличение светочувствительности, увеличение числа «летающих мушек» в поле зрения.
В случае проведения лазеркоагуляции сетчатки необходимо обсудить с пациентом следующие моменты:
— необходимость повторных осмотров и дополнительного лазерного лечения;
— панретинальная лазерная коагуляция сетчатки уменьшает риск слабовидения и слепоты, но может иметь побочные эффекты;
— лазерное лечение часто ухудшает периферическое зрение, кроме того, оно может умеренно снизить центральное зрение, но эти побочные эффекты лазеркоагуляции компенсируются долгосрочным снижением риска слабовидения и слепоты;
— у некоторых пациентов, несмотря на проводимое лазерное лечение, может возникнуть кровоизлияние в витреальную полость, которое происходит вследствие течения ДР, а не вызывается лазером (в этом случае пациенту может потребоваться дополнительное лазерное или оперативное лечение).
Госпитализация
Организация оказания медицинской помощи
Первичная специализированная медико-санитарная помощь оказывается врачом-офтальмологом в поликлиническом отделении медицинской организации.
Проведение лечения (лазерных вмешательств, интравитреальных введений лекарственных препаратов или витреальной хирургии) проводится врачом-офтальмологом в амбулаторных условиях, или в условиях дневного стационара, или в условиях круглосуточного стационара.
Показание для плановой госпитализации в медицинскую организацию:
· необходимость выполнения интравитреальных введений лекарственных препаратов или витреоретинальных хирургических вмешательств при невозможности проведения лечения в амбулаторных условиях.
Показание для неотложной госпитализации в медицинскую организацию:
· эндофтальмит как осложнение интравитреального введения лекарственных препаратов [38].
Показание к выписке пациента из медицинской организации:
1) завершение лечения или одного из этапов оказания специализированной, в том числе высокотехнологичной, медицинской помощи в условиях круглосуточного или дневного стационара при условии отсутствия осложнений лечения, требующих медикаментозной коррекции и/или медицинских вмешательств в стационарных условиях;
2) отказ пациента или его законного представителя от специализированной, в том числе высокотехнологичной, медицинской помощи в условиях круглосуточного или дневного стационара;
3) необходимость перевода пациента в другую медицинскую организацию.
Профилактика
Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
-
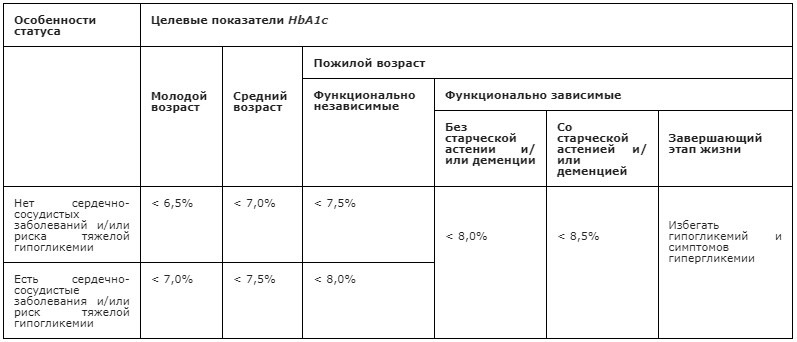
Рекомендуется устранение модифицируемых факторов риска возникновения и прогрессирования ДР и ДМО – компенсация СД (нормализация уровня гликемии согласно целевым показателям HbA1c (табл. 4), контроль артериального давления (табл. 5), и показателей липидного обмена согласно целевым показателям (табл. 6), изменение образа жизни (соблюдение диеты, сохранение двигательной активности) всем больным диабетом с целью профилактики диабетических поражений сетчатки [1, 72 — 106].
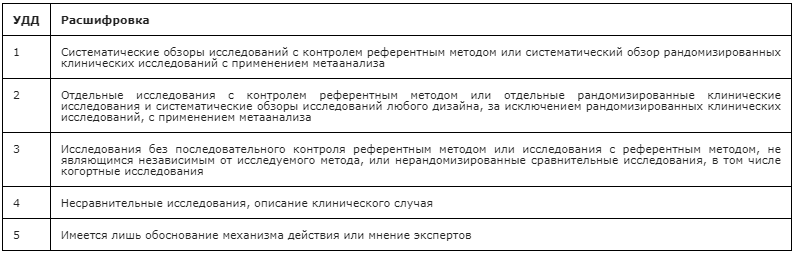
Уровень убедительности рекомендаций C (уровень достоверности доказательств — 4)
Таблица 4. Целевые показатели гликированного гемоглобина HbA1c у больных СД [1]
Комментарии: данные целевые значения не относятся к детям, подросткам и беременным. Сердечно-сосудистые заболевания: ишемическая болезнь сердца (инфаркт миокарда в анамнезе, шунтирование/стентирование коронарных артерий, стенокардия), нарушения мозгового кровообращения в анамнезе, заболевания артерий нижних конечностей в анамнезе (с симптоматикой). Основными критериями риска тяжелой гипогликемии являются: тяжелая гипогликемия в анамнезе, бессимптомная гипогликемия, большая продолжительность СД, хроническая болезнь почек – ХБП С 3-5, деменция.
Таблица 5. Целевые показатели артериального давления [1]
Комментарии: нижняя граница целевых значений АД относится к лицам на антигипертензивной терапии.
Таблица 6. Целевые уровни показателей липидного обмена у больных СД [1]
Комментарии: снижение HbA1c до 7% и ниже уменьшает риск микрососудистых осложнений. Более строгий гликемический контроль (HbA1c менее 6,5%) может быть рекомендован отдельным пациентам, если это достижимо без гипогликемических состояний и других нежелательных эффектов [1]. В настоящее время эндокринологами используется алгоритм индивидуализированного выбора целей терапии по HbA1c (табл. 3). В результате исследования DCCT был сделан вывод, что долгосрочные преимущества интенсивной терапии инсулином значительно перевешивают риски раннего ухудшения зрения. Ни один случай раннего ухудшения не был связан с серьезной угрозой зрению. Однако, когда интенсивное лечение начинается у пациентов с давним плохим гликемическим контролем, особенно если ретинопатия находится на стадии умеренной непролиферативной ДР или тяжелее, осмотр офтальмолога необходим до начала интенсивного лечения и с 3-месячными интервалами в течение 6-12 месяцев.
-
Рекомендуются осмотры врачом-офтальмологом всех пациентов СД с целью выявления диабетических изменений сетчатки [1, 18, 107, 108] с началом и периодичностью, указанными в табл. 7. Направление пациентов на обследование осуществляет врач-эндокринолог.
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5)
Таблица 7. Начало и периодичность осмотров больных СД врачом-офтальмологом [1]
Комментарии: внедрение скрининговых программ имеет принципиальное значение для профилактики слепоты и слабовидения вследствие диабетического поражения глаз. Идеальным методом скрининга ДР и ДМО является стереоскопическое фотографирование стандартных полей сетчатки. Выполнение процедуры проводится техническим персоналом, а оценка фотографий выполняется позже врачом-офтальмологом, специализирующимся в области ретинальной патологии [13].
При СД 1 типа риск развития ДР в течение первых 5 лет заболевания незначителен, поэтому осмотр врачом-офтальмологом должен быть проведен не позднее, чем через 5 лет от дебюта заболевания.
В связи с особенностью заболевания, отсутствием острого начала, СД 2 типа в течение нескольких лет может оставаться недиагностированным, что значительно увеличивает риск ДР. Около 20% больных СД 2 типа имеют признаки ДР в момент постановки диагноза СД. В связи с этим пациенты должны быть полноценно осмотрены врачом-офтальмологом сразу в момент постановки диагноза СД 2 типа.
Беременность ассоциируется с возможностью быстрого прогрессирования ДР при СД 1 и 2 типа. В связи с этим офтальмологическое обследование женщин, страдающих СД и планирующих беременность, необходимо проводить на этапе планирования беременности, во время первого триместра и далее каждые 3 месяца. Женщина также должна пройти полноценный офтальмологический осмотр в течение первого года после рождения ребенка.
Женщины с гестационным СД не нуждаются в осмотре врачом-офтальмологом с целью диагностики ДР, т.к. не имеют риска развития ДР.
Офтальмологическое обследование детей должно начинаться с 11-летнего возраста при длительности заболевания СД 1 типа более 2 лет или с началом пубертата при длительности заболевания СД более 2 лет [7, 10, 109].
Последующие осмотры при СД 1 и 2 типа у взрослых и детей проводятся в соответствии со стадией ДР, но не реже 1 раз в год.
-
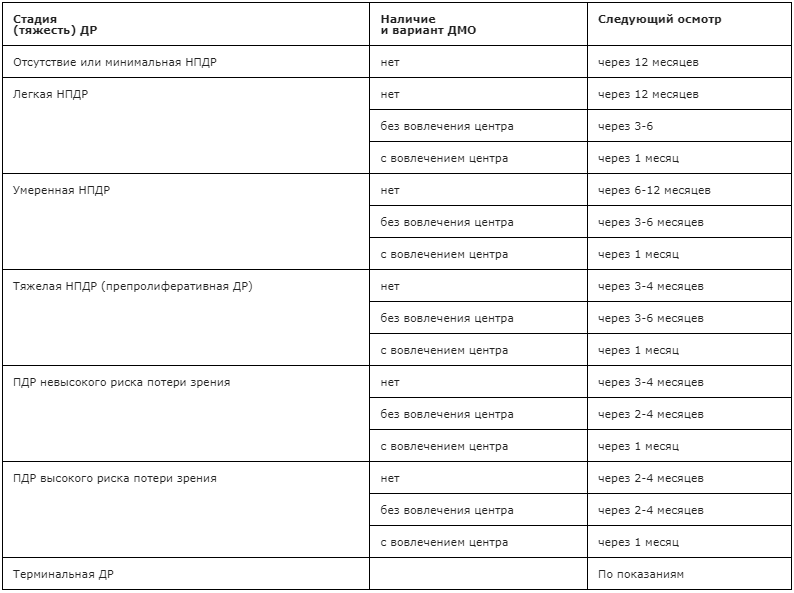
Рекомендуются регулярные офтальмологические осмотры с обязательной офтальмоскопией/биомикроскопией глазного дна всем пациентам с СД, частота которых зависит от особенностей клинической картины и течения заболевания (табл. 8), с целью выявления, оценки тяжести диабетических изменений сетчатки, их мониторинга и выработки тактики ведения пациента [20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Таблица 8. Частота офтальмологических осмотров пациентов с СД
Комментарии: при планировании периодичности осмотра врачом-офтальмологом следует учитывать, что риск развития и прогрессирования ДР и ДМО возрастает при определенных состояниях пациента, сопряженных с нарушениями гормонального статуса (беременность, состояние после искусственного прерывания беременности, пубертатный возраст и другие).
При неожиданном снижении остроты зрения или появлении каких-либо жалоб со стороны органа зрения, обследование у врача-офтальмолога должно быть проведено по возможности скорее, вне зависимости от сроков очередного визита к врачу.
Информация
Источники и литература
-
Клинические рекомендации общероссийской общественной организации Ассоциация врачей-офтальмологов
- 1. Дедов, И.И. Клинические рекомендации «Алгоритмы специализированной медицинской помощи больным сахарным диабетом» (9-й выпуск, дополненный) / ред. И.И. Дедов, М.В. Шестакова, А.Ю. Майоров // Сахарный диабет. – 2019. – Т. 22. № 1S1. – С. 1-144. DOI: 10.14341/DM221S1
2. Глобальный доклад по диабету [Global report on diabetes]. Женева: Всемирная организация здравоохранения. – 2018. – 88 с. Лицензия: CC BY-NC-SA 3.0 IGO.
3. Miller K., Fortun J.A. Diabetic macular edema: current understanding, pharmacologic treatment options and developing therapies / Asia-Pac J Ophthalmol. – 2018. – Vol. 7. – P. 28-35.
4. Romero-Aroca P. et al. Diabetic macular edema pathophysiology: vasogenic versus inflammatory (review article) / J Diabetes Res. – 2016. – Vol. 2016. – 17 p.
5. Haller J.A. et al. Update on the pathophisiology, molecular biology, and treatment of macular edema / Advanced studies in ophthalmology. – 2007. – Vol. 4. №7. – P. 178-190.
6. Aiello L.P. Vascular endothelial growth factor and the eye: biochemical mechanisms of action and implications for novel therapies / Ophthalmic. Res. – 1997. – Vol. 29. № 5. – P. 354-362.
7. Klein R. et al. The Wisconsin Epidemiologic Study of Diabetic Retinopathy: II. Prevalence and risk of diabetic retinopathy when age at diagnosis is less than 30 years / Arch Ophthalmol. – 1984. – V. 102. – P. 520-526.
8. Klein R. et al. The Wisconsin Epidemiologic Study of Diabetic Retinopathy: III. Prevalence and risk of diabetic retinopathy when age at diagnosis is 30 or more years / Arch Ophthalmol. – 1984. – V. 102. – P. 527-532.
9. Klein R. et al. The Wisconsin Epidemiologic Study of Diabetic Retinopathy: XI. The incidence of macular edema / Ophthalmology. – 1989. – V. 96. – P. 1501-1510.
10. Здоровье глаз и сахарный диабет. Руководство для медицинских работников. IDF и фонд Фреда Холлоуза. – Брюссель, Бельгия. – 2017. – 40 c.
11. Bourne RR, Stevens GA, White RA, Smith JL, Flaxman SR, Price H, et al. Causes of vision loss worldwide, 1990–2010: a systematic analysis / Lancet Glob Health. – 2013. – V. 1. – №6. – P.339-349.
12. Липатов Д.В. Эпидемиология диабетической ретинопатии в Российской Федерации по данным федерального регистра пациентов с сахарным диабетом / Д.В. Липатов, О.К. Викулова, А.В. Железнякова, М.А. Исаков, Е.Г. Бессмертная, А.А. Толкачева, Т.А. Чистяков, М.В. Шестакова, И.И. Дедов // Сахарный диабет. – 2018. – Т. 21. №4. – С. 230-240.
13. Porta M., Kohner E. M. Screening for diabetic retinopathy in Europe / Diabetic Medicine. – 1991. – V. 8. – P. 197-198.
14. Early Treatment Diabetic Retinopathy Study Research Group. Early photocoagulation for diabetic retinopathy. ETDRS report No 9 / Ophthalmology. – 1991. – V. 98. – P. 766-785.
15. Early Treatment Diabetic Retinopathy Study Research Group. Photocoagulation for diabetic macular edema. Early Treatment Diabetic Retinopathy Study (ETDRS) report No 1 / Arch Ophthalmol. – 1985. – Vol. 103. – P. 1796–806.
16. Руководство по клинической офтальмологии / ред. А.Ф. Бровкина, Ю.С. Астахов. – М.: Медицинское информационное агентство, 2014. – 955с.
17. Офтальмология: национальное руководство / ред. С.Э. Аветисов, Е.А. Егоров, Л.К. Мошетова, В.В.Нероев, Х.П. Тахчиди. – 2ое изд – М.: ГЭОТАР-Медиа, 2018. – 904с. – (Серия «Национальное руководство»).
18. International Council of Ophthalmology. Guidelines for Diabetic Eye Care. 2017. – 40 p.
19. Нероев В.В., Астахов Ю.С., Коротких С.А., Бобыкин Е.В., Зайцева О.В., Лисочкина А.Б., Бровкина А.Ф., Будзинская М.В., Гацу М.В., Григорьева Н.Н., Измайлов А.С., Карлова Е.В., Ковалевская М.А., Нечипоренко П.А., Панова И.Е., Рябцева А.А., Симонова С.В., Тульцева С.Н., Фурсова А.Ж., Шадричев Ф.Е., Шишкин М.М., Харлампиди М.П. Протокол выполнения интравитреального введения лекарственных препаратов. Консенсус Экспертного совета по заболеваниям сетчатки и зрительного нерва Общероссийской общественной организации «Ассоциация врачей-офтальмологов» // Вестник офтальмологии. – 2020. – Т.136. — №6. – С.251–263. https://doi.org/10.17116/oftalma2020136062251.
20. American Academy of Ophthalmology Preferred Practice Patterns Committee. Diabetic Retinopathy Preferred Practice Pattern®. AAO (2019); http://dx.doi.org/10.1016/j.ophtha.2019.09.025 ISSN 0161-6420/19.
21. Санитарно-эпидемиологические правила и нормативы СанПиН 2.1.3.2630-10 «Санитарно-эпидемиологические требования к организациям, осуществляющим медицинскую деятельность»: [постановление Главного государственного санитарного врача РФ от 18.05.2010 N 58 (ред. от 10.06.2016). : зарегистрировано в Минюсте России 09.08.2010, рег.номер 18094]. — М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора, 2010. — 255 с. ISBN 978— 5—7508—0925— 7.
22. Приказ Министерства здравоохранения и социального развития РФ от 29 декабря 2008 г. N 786н «О порядке формирования и утверждении государственного задания на оказание в 2009 году высокотехнологичной медицинской помощи гражданам Российской Федерации за счет ассигнований федерального бюджета» (с изменениями и дополнениями) : (зарегистрировано в Минюсте РФ 30 декабря 2008 г., рег. номер 13056).
23. Управление плановой госпитализацией в многопрофильной больнице. Методические рекомендации N 2001/144 : (утв. Минздравом РФ 09.11.2001).
24. Schields М.В. Glaucoma in diabetic patients / Ocular problems in diabetes mellitus // Blackwell Scientific Publ. – Boston. – 1992. – P. 307-319.
25. Virgili G. et al. Optical coherence tomography (OCT) for detection of macular oedema in patients with diabetic retinopathy / Cochrane Database Syst Rev. – 2015. – Vol. 7. – 57p.
26. Schmidt-Erfurth U. et al. Guidelines for the Management of Diabetic Macular Edema by the European Society of Retina Specialists (EURETINA) / Ophthalmologica. – 2017. – Vol. 237. № 4. – P. 185-222.
27. Kai Yuan Tey et al. Optical coherence tomography angiography in diabetic retinopathy: a review of current applications / Eye and Vision. – 2019. – Vol. 6. – P.37-47.
28. Johannesen S.K. et al. Optical coherence tomography angiography and microvascular changes in diabetic retinopathy: a systematic review / Acta Ophthalmol. – 2019. – Vol. 97. № 1. – P. 7-14.
29. Diabetes Control and Complication Trial Research Group. The effect of intensive treatment of diabetes on the development and progression of long-term complication in insulin dependent diabetes mellitus / N. Engl. J. Med.– 1993. – V. 329. – P. 977-86.
30. UK Prospective Diabetes Study Group. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes: UKPDS 33 / Lancet. – 1998. – V. 352. – P. 837-853.
31. Diabetes Control and Complication Trial Research Group. The relationship of glycemic exposure (HbA1с) to the risk of development and progression of retinopathy in the Diabetes Control and Complication Trial / Diabetes. – 1995. – V. 44. – P. 968-983.
32. Stephenson J. et al. Microvascular and acute complications in IDDM patients: the EURODIAB IDDM Complications Study / Diabetologia. – 1994. – V. 37. – P. 278-285.
33. Stratton I.M. et al. UKPDS 50: risk factors for incidence and progression of diabetic retinopathy in type 2 diabetes over 6 years from diagnosis / Diabetologia. – 2001. – V. 44. – P. 156-163.
34. Keech A.C. et al. FIELD study investigators. Effect of fenofibrate on the need for laser treatment for diabetic retinopathy (FIELD study): a randomised controlled trial / Lancet. – 2007. – V. 370. – P. 1687-1697.
35. Keech A.C. et al. FIELD study investigators. Effect of long-term fenofibrate therapy on cardiovascular events in 9795 people with type 2 diabetes mellitus (the FIELD study): randomised controlled trial / Lancet. – 2005. – V. 366. – P. 1849-1861.
36. ACCORD Study Group; ACCORD Study Eye Group, Effects of medical therapies on retinopathy progression in type 2 diabetes / N Enl J Med. – 2010. – Vol. 363. – P. 233-244.
37. Diabetic Retinopathy Study Research Group. Report No 8. Photocoagulation treatment of proliferative diabetic retinopathy. Clinical application of diabetic retinopathy study (DRS) findings / Ophthalmology. – 1981. – V. 88. – P. 583-600.
38. Diabetic Retinopathy Study Research Group. Report No 14. Indications for photocoagulation treatment of diabetic retinopathy / Int. Ophthalmol. Clin. – 1987. – V. 27. – P. 239-252.
39. Evans J.R., Michelessi M., Virqili G. Laser photocoagulation for proliferative diabetic retinopathy / Cochrane Database Syst Rev. – 2014. – Vol. 24. № 11. – 47 p.
40. Moutray T. et al. Different lasers and techniques for proliferative diabetic retinopathy / Cochrane Database Syst Rev. – 2018. – 104 p.
41. Gross J.G. et al. Panretinal Photocoagulation vs Intravitreous Ranibizumab for Proliferative Diabetic Retinopathy: A Randomized Clinical Trial / JAMA. – 2015. – Vol. 314. – № 20. – P.2137–2146.
42. Nguyen Q.D. et al. Ranibizumab for diabetic macular edema: Results from 2 phase III randomized trials: RISE and RIDE / Ophthalmology. – 2012. – Vol. 119. – P.789-801.
43. Do D.V. et al. One-year outcomes of the DA Vinci Study of VEGF Trap-Eye in eyes with diabetic macular edema / Ophthalmology. – 2012. – Vol. 119. – P. 1658-1665.
44. Brown D.M. et al. KESTREL and KITE: 52-week results from two Phase III pivotal trials of brolucizumab for diabetic macular edema / American Journal of Ophthalmology. – 2022. – Vol. 238. – P.157-172. doi: https://doi.org/10.1016/j.ajo.2022.01.004
45. Boyer D.S. et al. Ozurdex MEAD Study Group. Three-year, randomized, sham-controlled trial of dexamethasone intravitreal implant in patients with diabetic macular edema / Ophthalmology. – 2014. – Vol. 121. – P. 1904-1914.
46. Elman M.J. et al. Diabetic Retinopathy Clinical Research Network. Intravitreal Ranibizumab for diabetic macular edema with prompt versus deferred laser treatment: 5-year randomized trial results / Ophthalmology. – 2015. – Vol. 122. № 2. – P. 375-381.
47. Wells J.A. et al. Diabetic Retinopathy Clinical Research Network. Aflibercept, Bevacizumab, or Ranibizumab for Diabetic Macular Edema / N Engl J Med. – 2015. – Vol. 372. – P. 1193-1203.
48. Wells J.A. et al. Diabetic Retinopathy Clinical Research Network. Aflibercept, Bevacizumab, or Ranibizumab for Diabetic Macular Edema. Two-Year Results from a Comparative Effectiveness Randomized Clinical Trial / Ophthalmology. – 2016. – Vol. 123. № 6. – P. 1351-1359.
49. Papadopoulos N. et al. Binding and neutralization of vascular endothelial growth factor (VEGF) and related ligands by VEGF Trap, ranibizumab and bevacizumab / Angiogenesis. – 2012. – Vol. 15. – P. 171-185.
50. WHO. Prevention of blindness from diabetes mellitus / Report of a WHO consultation in Geneva 9-11 November 2005. – Switzerland. – WHO press. – 2005. – p. 39.
- 1. Дедов, И.И. Клинические рекомендации «Алгоритмы специализированной медицинской помощи больным сахарным диабетом» (9-й выпуск, дополненный) / ред. И.И. Дедов, М.В. Шестакова, А.Ю. Майоров // Сахарный диабет. – 2019. – Т. 22. № 1S1. – С. 1-144. DOI: 10.14341/DM221S1
Информация
Список сокращений
АД — артериальное давление
ВИЧ — вирус иммунодефицита человека
ВОЗ — Всемирная организация здравоохранения
ГКС — глюкокортикостероиды
ДЗН — диск зрительного нерва
ДМО — диабетический макулярный отек
ДР — диабетическая ретинопатия
ИРМА — интраретинальные микрососудистые аномалии
ИФА — иммуноферментный анализ
МКБ 10 — международная классификация 10-го пересмотра
НПДР — непролиферативная диабетическая ретинопатия
ОКТ — оптическая когерентная томография
ОКТ-А — оптическая когерентная томография в режиме ангиографии
ППДР — препролиферативная диабетическая ретинопатия
ПДР — пролиферативная диабетическая ретинопатия
ПЦР — полимеразная цепная реакция
РНК — рибонуклеиновая кислота
СД — сахарный диабет
ФАГ — флюоресцентная ангиография
ХБП — хроническая болезнь почек
ETDRS — Еarly Тreatment Diabetic Retinopathy Study – Исследование [по изучению] раннего лечения ДР
HbA1c — hemoglobin A1c, гликированный гемоглобин A1c
ICAM-1 — intercellular adhesion molecule-1, молекула межклеточной адгезии 1-го типа
PIGF — placental growth factor, плацентарный фактор роста
VCAM-1 — vascular cell adhesion molecule-1, молекула адгезии сосудистого эндотелия 1-го типа
VEGF — vascular endothelial growth factor, сосудистый эндотелиальный фактор роста
** — жизненно необходимые и важнейшие лекарственные препараты (ЖНВЛП)
Термины и определения
Биомикроскопия глаза — метод прижизненного визуального исследования оптических сред и тканей глаза, основанный на создании контраста между освещенными и неосвещенными участками, проводимый при помощи щелевой лампы и дополнительных диагностических линз (в частности, для биомикроскопии глазного дна).
Ватный (мягкий) экссудат (ватообразный фокус) — очаг фокальной ишемии внутренней сетчатки вследствие резкого нарушения ретинальной перфузии.
Гемофтальм — витреальное кровоизлияние (геморрагия), скопление крови в стекловидном теле или витреальной полости (при авитрии).
Интравитреальное введение (интравитреальная инъекция) — введение лекарственного вещества в стекловидное тело или витреальную полость (при авитрии).
Интраретинальные микрососудистые аномалии (ИРМА) — шунты в виде ветвящихся сосудов, располагающиеся по границе неперфузируемых зон сетчатки.
Микроаневризма — локальное расширение (выпячивание) капиллярной стенки.
Неоваскулярная глаукома — вторичная глаукома, возникающая в результате разрастания новообразованных сосудов и фиброзной ткани в углу передней камеры и на поверхности радужки.
Оптическая когерентная томография (ОКТ) — диагностический неинвазивный бесконтактный метод прижизненной визуализации, качественного и количественного анализа морфологических особенностей структур глазного дна, основанный на принципе световой интерферометрии.
Оптическая когерентная томография в режиме ангиографии (ОКТ-А) — диагностический неинвазивный бесконтактный метод прижизненной визуализации, качественного и количественного анализа микроциркуляции в структурах глазного дна с учетом сегментации слоев глазного дна.
Преретинальное кровоизлияние (геморрагия) — скопление крови в ретрогиалоидном пространстве.
Ретинальная неоваскуляризация — вариант патологического пролиферативного ответа на ишемию сетчатки, проявляющийся ростом по задней поверхности стекловидного тела новообразованных сосудов, источником которых являются собственные сосуды сетчатки.
Рубеоз радужки — рост новообразованных сосудов в радужке, как правило, сопровождается неоваскуляризацией структур угла передней камеры и является следствием выраженной ишемии сетчатки.
Твердый (липидный) экссудат — отложение белков и липидов в слоях нейроэпителия вследствие повышенной проницаемости сосуда и выхода компонентов плазмы крови за его пределы.
Тракционная отслойка сетчатки — отслойка сетчатки, связанная с сокращением соединительной ткани в составе пролиферативных мембран и ретракцией стекловидного тела, характеризуется скоплением жидкости между нейроэпителием и пигментным эпителием. При формировании вторичных разрывов сетчатки отслойка классифицируется как тракционно-регматогенная.
Флюоресцентная ангиография глаза (ФАГ, ангиография с флюоресцеином натрия) — диагностический метод, позволяющий выявить нарушения сосудистого русла на глазном дне, оценить состояние наружного и внутреннего гематоретинальных барьеров путем регистрации пассажа красителя (внутривенно вводимого флюоресцеина натрия) по сосудам глаза в режиме фото- и видеонаблюдения.
Критерии оценки качества медицинской помощи
Таблица 9.
Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
1. Астахов Ю.С., руководитель группы, д.м.н., профессор кафедры офтальмологии с клиникой ФБГОУ ВО «Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова», Вице-президент ООО «Ассоциация врачей-офтальмологов»;
2. Нероев В.В., д.м.н., академик РАН, директор ФГБУ «Национальный медицинский исследовательский центр глазных болезней им. Гельмгольца» Министерства здравоохранения Российской Федерации, Заслуженный врач Российской Федерации, Заслуженный деятель науки Российской Федерации, Президент ООО «Ассоциация врачей-офтальмологов»;
3. Шестакова М.В., со-руководитель группы, д.м.н., академик РАН, заместитель директора ФГБУ «Национальный медицинский исследовательский центр эндокринологии» Министерства здравоохранения Российской Федерации, Заслуженный деятель науки Российской Федерации, ученый секретарь «Российской ассоциации эндокринологов»;
4. Зайцева О.В., к.м.н., заместитель директора по организационно-методической работе ФГБУ «Национальный медицинский исследовательский центр глазных болезней им. Гельмгольца» Министерства здравоохранения Российской Федерации, ведущий научный сотрудник, исполнительный директор ООО «Ассоциация врачей-офтальмологов»;
5. Охоцимская Т.Д., к.м.н., врач ФГБУ «Национальный медицинский исследовательский центр глазных болезней им. Гельмгольца» Министерства здравоохранения Российской Федерации, член ООО «Ассоциация врачей-офтальмологов»;
6. Рябина М.В., к.м.н., старший научный сотрудник ФГБУ «Национальный медицинский исследовательский центр глазных болезней им. Гельмгольца» Министерства здравоохранения Российской Федерации, член ООО «Ассоциация врачей-офтальмологов».
7. Шадричев Ф.Е., к.м.н., заведующий офтальмологическим отделением Санкт-Петербургского территориального диабетологического центра СПбГБУЗ «ГКДЦ №1», ассистент кафедры офтальмологии с клиникой ФБГОУ ВО «Первый Санкт-Петербургский государственный медицинский университет им. акад. И.П. Павлова» Министерства здравоохранения Российской Федерации, член ООО «Ассоциация врачей-офтальмологов»;
8. Григорьева Н.Н., к.м.н., врач офтальмологического отделения Санкт-Петербургского территориального диабетологического центра СПбГБУЗ «ГКДЦ №1», ассистент кафедры оториноларингологии и офтальмологии ФГБОУ ВО «Санкт-Петербургский государственный университет», член ООО «Ассоциация врачей-офтальмологов»;
9. Липатов Д.В, д.м.н., заведующий отделением «Диабетическая ретинопатия и офтальмохирургия» ФГБУ «Национальный медицинский исследовательский центр эндокринологии» Министерства здравоохранения Российской Федерации, член «Российской ассоциации эндокринологов» и член ООО «Ассоциация врачей-офтальмологов»;
10. Кононенко И.В., к.м.н., врач ФГБУ «Национальный медицинский исследовательский центр эндокринологии» Министерства здравоохранения Российской Федерации, член «Российской ассоциации эндокринологов»;
11. Шкляров Е.Б., к.м.н., врач офтальмологического отделения Санкт-Петербургского территориального диабетологического центра СПбГБУЗ «ГКДЦ №1», ассистент кафедры семейной медицины ФГБОУ ВО «Северо-Западный государственный медицинский университет им. И.И. Мечникова» Министерства здравоохранения Российской Федерации, член ООО «Ассоциация врачей-офтальмологов».
Конфликт интересов отсутствует.
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций:
· Врачи-офтальмологи;
· Врачи-эндокринологи;
· Врачи общей практики (семейной медицины).
Методы, использованные для сбора/селекции доказательств: поиск в электронных базах данных; анализ современных научных разработок по проблеме ДР и ДМО в России и за рубежом; обобщение практического опыта российских и зарубежных специалистов. Описание методов, использованных для сбора/селекции доказательств: доказательной базой для рекомендаций являются публикации, вошедшие в Кохрайновскую библиотеку, базы данных EMBASE и MEDLINE, а также монографии и статьи в ведущих специализированных рецензируемых отечественных медицинских журналах по данной тематике. Методы, использованные для оценки качества и силы доказательств: консенсус экспертов, оценка значимости в соответствии с рейтинговой схемой.
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
Таблица 2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств)
Таблица 3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств)
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию – не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утверждённым клиническим рекомендациям, но не чаще 1 раза в 6 месяцев.
Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
1. Актуальные инструкции к лекарственным препаратам, упоминаемым в данных клинических рекомендациях, можно найти на сайте http://grls.rosminzdrav.ru
Таблица 1. Доза, путь введения и режимы применения лекарственных препаратов
2. Международная классификация болезней, травм и состояний, влияющих на здоровье, 10-го пересмотра (МКБ-10). Всемирная организация здравоохранения.
3. Номенклатура медицинских услуг. Приказ Министерства здравоохранения РФ от 13 октября 2017 г. N 804н «Об утверждении номенклатуры медицинских услуг».
4. Приказ Министерства здравоохранения РФ от 20.12.2012 № 1183н «Об утверждении Номенклатуры должностей медицинских работников и фармацевтических работников» (ред. от 01.08.2014)
5. Федеральный закон «Об основах охраны здоровья граждан в Российской Федерации» от 21.11.2011 № 323 Ф3.
6. Порядок оказания медицинской помощи взрослому населению при заболеваниях глаза, его придаточного аппарата и орбиты. Приказ Министерства здравоохранения России от 12.11.2012 № 902н «Об утверждении Порядка оказания медицинской помощи взрослому населению при заболеваниях глаза, его придаточного аппарата и орбиты».
7. Распоряжение Правительства РФ от 12.10.2019 N 2406-р (ред. от 30.03.2022) «Об утверждении перечня жизненно необходимых и важнейших лекарственных препаратов, а также перечней лекарственных препаратов для медицинского применения и минимального ассортимента лекарственных препаратов, необходимых для оказания медицинской помощи»
8. Приказ Министерства здравоохранения РФ от 24 декабря 2012 № 1492н «Об утверждении стандарта первичной медико-санитарной помощи при диабетической ретинопатии и макулярном отеке».
9. Приказ Министерства здравоохранения РФ от 10 мая 2017 г. № 203н «Об утверждении критериев оценки качества медицинской помощи».
10. Постановление Правительства РФ от 28 декабря 2021 г. N 2505 «О Программе государственных гарантий бесплатного оказания гражданам медицинской помощи на 2022 год и на плановый период 2023 и 2024 годов».
11. Санитарно-эпидемиологические правила и нормативы СП 2.1.3678-20 «Санитарно-эпидемиологические требования к эксплуатации помещений, зданий, сооружений, оборудования и транспорта, а также условиям деятельности хозяйствующих субъектов, осуществляющих продажу товаров, выполнение работ или оказание услуг» (постановление Главного государственного санитарного врача РФ от 24.12.2020 г. №44).
12. Санитарно-эпидемиологические правила и нормативы СанПиН 3.3686-21 «Санитарно-эпидемиологические требования по профилактике инфекционных болезней» (постановление Главного государственного санитарного врача РФ от 28.01.2021 г. № 2).
13. Управление плановой госпитализацией в многопрофильной больнице. Методические рекомендации № 2001/144: (утв. Министерством здравоохранения РФ 09.11.2001).
Приложение Б. Алгоритмы действий врача
Диабетическая ретинопатия
Диабетический макулярный отек
Приложение В. Информация для пациента
С целью профилактики слепоты и слабовидения вследствие диабетических осложнений со стороны глаз необходимо соблюдать все назначения эндокринолога, терапевта с целью компенсации углеводного обмена, артериальной гипертензии, показателей липидного обмена.
Даже при отсутствии жалоб со стороны органа зрения каждый пациент с СД должен проходить осмотры офтальмолога не реже 1 раз в год (в случае СД 1 типа – через 5 лет от дебюта заболевания). При появлении жалоб со стороны органа зрения требуется безотлагательное обращение к офтальмологу.
В случае наличия диабетических изменений со стороны глаз следует соблюдать необходимую кратность обследования у офтальмолога в зависимости от тяжести изменений, которая будет установлена врачом. При появлении новых жалоб со стороны органа зрения требуется безотлагательное обращение к офтальмологу.
ДР долгое время может протекать бессимптомно. Эффективность лечения ДР зависит от своевременности ее начала, даже при отсутствии субъективных жалоб со стороны органа зрения.
Лазерное лечение, как правило, требует повторных сеансов лечения, кратность и объем которых устанавливает врач. Внутриглазные кровоизлияния, возникающие во время или после лазеркоагуляции, связаны с наличием СД, но не с проводимым лазерным лечением, и, возможно, потребуют дополнительной лазеркоагуляции сетчатки.
Интравитреальные инъекции лекарственных препаратов требуют регулярных осмотров у офтальмолога и, как правило, повторных инъекций, кратность которых устанавливает врач. В случае появления симптомов, вероятно указывающих на воспаление (боль в глазу или увеличение неприятных ощущений в глазу, усиление покраснения глаза, усиление нечеткости или дальнейшее снижение зрения, увеличение светочувствительности, увеличение числа «летающих мушек» в поле зрения) в течение нескольких дней после инъекции, необходимо незамедлительно сообщить о них врачу.
Приложение Г1-ГN. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Таблица 1. Основные диагностические критерии установления ДР и ДМО
Таблица 2. Критерии определения стадии диабетической ретинопатии ETDRS (1991)
Таблица 3. Критерии выбора тактики ведения пациентов с ДР и ДМО
Прикреплённые файлы
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
Дата публикации 27 декабря 2019Обновлено 4 августа 2021
Определение болезни. Причины заболевания
Диабетическая ретинопатия (Diabetic retinopathy) — это наиболее тяжёлое осложнение сахарного диабета первого и второго типа, которое связано с поражением сосудов сетчатки глаза. Чаще всего оно приводит к снижению зрения и слепоте [1].
У диабетиков первого типа ретинопатия возникает в более раннем возрасте, у больных вторым типом диабета — на поздних сроках заболевания. Спрогнозировать время появления ретинопатии сложно, так как у каждого пациента оно индивидуально, но чаще всего при диабете второго типа ретинопатия развивается на 3-5 году болезни.
По данным Сент-Винсентской декларации 1992 года, которая была посвящена исследованию эпидемиологии диабетической ретинопатии при сахарном диабете первого типа, она возникает в 90 % случаев, при сахарном диабете второго типа — в 38,9 % [15].
Проблемы сахарного диабета сегодня выходят на первое место во всём мире. Этим заболеванием страдают примерно 5 % населения Земли всех национальностей и возрастов. В России число больных превышает 8 млн, причём ежегодно их число увеличивается на 5-7 % [15].
К факторам риска, которые приводят к ухудшению сахарного диабета, можно отнести:
- уровень глюкозы крови (показатели гипергликемии);
- артериальную гипертензию;
- хроническую почечную недостаточность;
- ожирение;
- молодой возраст;
- период беременности;
- генетическую предрасположенность (наследственность);
- вредные привычки (курение).
Но в первую очередь частота развития диабетической ретинопатии связана со стажем заболевания:
- при стаже сахарного диабета до 5 лет ретинопатия возникает в 9-17 % случаев;
- от 5 лет до 10 лет — в 44-80 % случаев;
- от 15 лет — в 87-99 % случаев [15].
Во время беременности риск появления ретинопатии отсутствует, так как срок гестационного диабета очень короткий, чтобы позволить ретинопатии развиться. Если же диабетическая ретинопатия развилась ещё до зачатия, то беременность может усугубить течение болезни [16].
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы диабетической ретинопатии
Внешне диабетическая ретинопатия никак себя не проявляет. Она начинает прогрессировать безболезненно и малосимптомно — в этом и есть её главное коварство. Только с течением времени проявляется первый признак заболевания — ухудшение чёткости зрения, из-за чего ретинопатию чаще всего выявляют уже на пролиферативной, т. е. самой поздней стадии болезни. Но при этом стоит помнить, что даже при запущенном заболевании зрение может оставаться в пределах нормы [16].
Когда отёк затрагивает центр сетчатки, пациент ощущает нечёткость зрения, ему становится трудно читать, писать, набирать текст, работать с мелкими деталями на близком расстоянии. При кровоизлияниях возникают плавающие серые или чёрные плотные пятна, которые движутся вместе с глазом, ощущение пелены или паутины перед глазами. Эти симптомы появляются из-за поражения сосудов на глазном дне.
Когда после лечения кровоизлияния рассасываются, пятна исчезают. Однако симптомы могут возникнуть вновь при нестабильном уровне глюкозы или скачке артериального давления. Поэтому пациент должен держать под контролем эти показатели и при появлении признаков болезни обратиться на приём к окулисту [2].
Патогенез диабетической ретинопатии
Сахарный диабет — это заболевание, при котором в организме возникает нехватка инсулина из-за невосприимчивости к нему тканей. Данное состояние в первую очередь влияет на внутренний слой сосудистых стенок — эндотелий. Он выполняет множество важных функций: участвует в процессе обмена веществ, обеспечивает непроницаемость сосудистой стенки, текучесть и свёртывание крови, появление новых сосудов и пр.
Изменения эндотелия на фоне сахарного диабета происходят из-за каскада нарушений, спровоцированных длительной гипергликемией — высоким уровнем глюкозы в крови. В избыточной концентрации глюкоза быстро вступает в химические реакции, которые пагубно воздействуют на клетки, ткани и органы. Такой длительный процесс называется глюкозотоксичностью [3].
Гипергликемия и глюкозотоксичность со временем приводят к гибели клеток в сосудах — перицитов, которые контролируют обмен жидкости, сужая и расширяя капилляры. После их разрушения проницаемость кровеносных сосудов сетчатки повышается, они становятся тоньше и растягиваются в связи с давлением скапливающейся жидкости под слоями сетчатки. Это приводит к образованию микроаневризм — небольших локальных расширений капилляров сетчатки, которые способствуют развитию ишемии (снижению кровоснабжения сетчатки) и появлению новых сосудов и тканей на глазном дне.
Таким образом, в развитии диабетической ретинопатии и её прогрессировании наиболее важное значение имеют два основных патогенетических механизма:
- Нарушение внутреннего барьера, который составляет эндотелий капилляров сетчатки. Из-за повышенной проницаемости стенок сосудов появляются отёки, твёрдые экссудаты (скопления жидкости) и кровоизлияния на глазном дне.
- Образование микротромбов и закупорка сосудов сетчатки. По этим причинам нарушается обмен веществ между кровью и тканью через стенки капилляров, появляются зоны ишемии и гипоксии сетчатки. Всё это, в свою очередь, приводит к появлению новых кровеносных сосудов на глазном дне.
Классификация и стадии развития диабетической ретинопатии
Согласно общепринятой классификации E. Kohner и M. Porta [14], в зависимости от патологических изменений выделяют три стадии диабетической ретинопатии:
- I стадия — непролиферативная;
- II стадия — препролиферативная;
- III стадия — пролиферативная.
Непролиферативную стадию диабетической ретинопатии ещё называют фоновой [16]. Её обычно диагностируют у диабетиков с большим стажем заболевания (от 10 до 13 лет). Она сопровождается закупоркой сосудов (чаще артерий) и повышением проницаемости капилляров (микрососудистой антипатией). В сетчатке образуются мелкие аневризмы (локальные расширения сосудов), отёки, экссудат и точечные кровоизлияния в центре или глубоких тканях сетчатки. Экссудат может быть мягким или твёрдым, белым или желтоватым, с чёткими или смазанными границами. Чаще всего он располагается в центре сетчатки и свидетельствует о наличии хронического отёка [16]. Качество зрения при этом не страдает.
Препролиферативная стадия сопровождается аномалиями сосудов, появлением экссудата различной консистенции, а также больших ретинальных кровоизлияниями. Она отличается тем, что:
- количество признаков, имеющихся на первой стадии, увеличивается;
- появляются субретинальные и преретинальные кровоизлияния;
- возникает гемофтальм — кровоизлияние в стекловидное тело;
- появляется макулопатия — поражение центральной зоны сетчатки;
- в макулярной зоне образуются участки ишемии и экссудации.
На препролиферативной стадии требуется тщательное обследование, чтобы обнаружить ишемические поражения сетчатки. Их наличие будет указывать на прогрессирование болезни и скорый переход к более тяжёлой стадии диабетической ретинопатии.
Пролиферативная стадия развивается при закупорке капилляров. Она приводит нарушению кровоснабжения в отдельных зонах сетчатки. Отличается появлением новых кровеносных сосудов в сетчатке или на диске зрительного нерва, обширными кровоизлияниями, наличием фиброзных спаек и плёнок.
Также существует классификация тяжести диабетической ретинопатии. Она чётко отражает стадии прогрессирования и распространённость болезни. Согласно ней, выделяют четыре степени тяжести:
- I степень — изменения только в зоне одной сосудистой аркады;
- II степень — фиброзные изменения диска зрительного нерва;
- III степень — наличие изменений I и II степени;
- IV степень — распространённые фиброзные поражения всего глазного дна [11].
Осложнения диабетической ретинопатии
Диабетическая ретинопатия приводит к возникновению следующих осложнений:
- Катаракта — потеря прозрачности хрусталика из-за образования плотных непрозрачных структур в его содержимом. Вследствие помутнения он не пропускает достаточное количество света, и человек перестаёт видеть отчётливую картинку. Из-за мутности хрусталика зрение становится как бы «затуманенным», очертания объектов — нечёткими и размытыми.
- Вторичная глаукома — повышение внутриглазного давления и поражение зрительного нерва, развивающееся на фоне другого заболевания — катаракты, кератита, травмы глаза, тромбоза вен сетчатки и др. При этом наблюдается прогрессирующее снижение остроты зрения и болевой синдром.
- Гемофтальм — кровоизлияние в полость стекловидного тела. Кровь так же, как и помутневший хрусталик, мешает попаданию света на сетчатку, из-за чего снижается чёткость зрения.
- Ретиношизис — расслоение сетчатки из-за нарушения кровообращения. Возникает чаще всего при сосудистых заболеваниях глаз, воспалительных процессах (хронических формах увеита, иридоциклита), онкологических заболеваниях сосудистой оболочки, в результате воздействия некоторых лекарств.
- Отслойка сетчатки — отделение сетчатки от сосудистой оболочки глаза. При этом возникает резкое снижение зрения, появляется пелена, «занавеска» перед глазом, сужаются поля зрения, появляются мушки, искры, молнии.
- Слепота. Она является необратимой и становится причиной инвалидизации.
Все эти состояния приводят к постоянному контролю со стороны эндокринолога, офтальмолога, терапевта и невропатолога. А такие осложнения, как катаракта, вторичная глаукома, гемофтальм и отслойка сетчатки, требуют проведения операции [12].
Диагностика диабетической ретинопатии
Диагноз диабетической ретинопатии выставляется на основании нескольких составляющих: анамнеза, результатов офтальмологического обследования и особенностей клинической картины глазного дна.
Для первичного обследования (скринига) проводятся определённые виды исследований:
- визометрия — проверка остроты зрения;
- периметрия — оценка состояния периферического зрения;
- биомикроскопия — изучение переднего отрезка глаза (роговицы, передней камеры, хрусталика, конъюнктивы и век);
- офтальмоскопия под мидриазом — осмотр глазного дна через расширенный зрачок с использованием линзы Гольдмана;
- контактная тонометрия — измерение внутриглазного давления тонометром Маклакова.
Данные обследования должны проходить все пациенты с сахарным диабетом любого типа минимум раз в год, а беременные пациентки — раз в триместр. Это позволит вовремя выявить ретинопатию и не допустить развитие осложнений [16].
Для отслеживания динамики изменений на сетчатке выполняется фотографирование глазного дня с помощью фундус-камеры. Иначе её называют ретинальной камерой. Она также помогает определить степень диабетической ретинопатии [16].
При наличии помутнений хрусталика и стекловидного тела показано проведение УЗИ глаза, чтобы оценить состояние этих структур. Для выявления признаков глаукомы выполняется гониоскопия, которая позволяет осмотреть переднюю камеру глаза.
Наиболее информативным методом визуализации сосудов сетчатки является флуоресцентная ангиография. Она помогает оценить состояние капилляров и качество кровообращения, благодаря чему можно обнаружить начальные проявления диабетической ретинопатии, а также закупорку капилляров, зоны ишемии сетчатки и образование новых сосудов. Эти данные позволяют определить степень тяжести диабетической ретинопатии и определиться с тактикой лечения [16].
Совместно с ангиографией проводят оптическую когерентную и лазерную сканирующую томографию сетчатки [13]. Эти исследования предназначены для оценки выраженности макулярного отека и эффективности проводимого лечения [16].
Лечение диабетической ретинопатии
Диабетическая ретинопатия при тяжёлой форме сахарного диабета неизбежно возникает и прогрессирует. Поэтому основная цель лечения ретинопатии заключается в том, чтобы как можно дольше избегать осложнений сахарного диабета и замедлить переход начальных проявлений ретинопатии к более серьёзным (пролиферативным) изменениям, которые приводят к значительному снижению зрения и инвалидизации [8].
Независимо от стадии диабетической ретинопатии необходимо провести соответствующее лечение основного заболевания, нормализовать артериальное давление и липидный обмен. Поэтому лечением ретинопатии занимаются сразу несколько специалистов: эндокринолог, офтальмолог, невролог и терапевт [9].
Медикаментозное лечение диабетической ретинопатии включает использование нескольких лекарственных групп:
- препараты, воздействующие на артериальную гипертензию, диабетическую нефропатию и ретинопатию;
- ангиоретинопротекторы и антиоксиданты, укрепляющие сосудистую стенку и иммунитет, препятствующие образованию микротромбов;
- препараты, улучшающие микроциркуляцию крови, её вязкость и текучесть;
- гиполипидемические препараты, нормализующие липидный обмен в организме;
- глюкокортикоиды, которые вводят в стекловидное тело для устранения отёка;
- ингибиторы VEGF, которые также вводят в стекловидное тело, чтобы не допустить или приостановить образование новых сосудов (например, афлиберцепт, ранибизумаб, бевацизумаб) [16].
При развитии третьей стадии диабетической ретинопатии, угрожающей жизни пациента, терапевтические возможности очень ограничены. В таких случаях может потребоваться лазерная коагуляция сетчатки. Показаниями к её выполнению служат:
- экссудативная (отёчная) макулопатия;
- ишемия сетчатки;
- появление новых сосудов на сетчатке или передней поверхности радужной оболочки;
- прогрессирование патологических изменений на глазном дне через 3-6 месяцев после компенсации сахарного диабета.
На данный момент существует три основных метода лазерной фотокоагуляции:
- Фокальная лазеркоагуляция (ФЛК) — нанесение коагулянта (вещества, «склеивающего» сетчатку с сосудистой оболочкой) на участки просачивания красителя (флуоресцеина), расположения микроаневризм, кровоизлияний и твёрдых экссудатов. Чаще применяется при макулярном отёке с повышенной проницаемостью сосудов.
- Барьерная лазеркоагуляция — нанесение коагулянтов на околомакулярную зону в несколько рядов. Чаще применяется при первой стадии диабетической ретинопатии в сочетании с макулярным отёком.
- Панретинальная лазеркоагуляция (ПРЛК) — нанесение коагулянтов на все зоны сетчатки, избегая макулярной области. Чаще применяется при второй стадии диабетической ретинопатии с обширными зонами ишемии. Правильно выполненная ПРЛК на ранних стадиях пролиферации является достаточно эффективным методом лечения диабетической ретинопатии.
В далеко зашедших случаях показано хирургическое вмешательство, а именно субтотальная витрэктомия (почти полное удаление стекловидного тела) с удалением задней пограничной мембраны, которая прикреплена по окружности диска зрительного нерва [6].
Показаниями для витрэктомии служат:
- витреальное кровоизлияние (постоянно кровоточащие сосуды);
- наличие спаек;
- отслойка сетчатки.
Для многих пациентов с тяжёлым течением диабетической ретинопатии витрэктомия является единственным вариантом сохранения зрения.
Прогноз. Профилактика
Во многом прогноз зависит от стадии диабетической ретинопатии и степени тяжести сахарного диабета. Наиболее неблагополучный вариант будущего возможен при пролиферативной стадии заболевания, так как на этом этапе возникают различные осложнения, которые приводят к значительной потере остроты зрения и слепоте.
Для сохранения зрения пациенту с сахарным диабетом крайне важно следить за основным заболеванием и артериальной гипертензией, строго следовать всем назначениям эндокринолога и терапевта, постоянно наблюдаться у офтальмолога. Если внезапно стала снижаться острота зрения или появились другие жалобы на состояние глаз, то необходимо незамедлительно обратиться к специалисту [10].
Diabetic retinopathy (conducting tactic)
Yu.S. Astahov, F.E. Shadrishev, A.B. Lisochkina
St.–Petersburg State Medical University of acad. Pavlov I.P.
St.–Petersburg territorial diabetic center
St.–Petersburg, Russia
Good results were reached in treatment and diagnostics of diabetic retinopthy during last 50 years. But it is still the main reason of blindness in economically developed countries. Authors give analysis of modern directions of medicamental treatment of DRP.
Диабетическая ретинопатия – это хорошо изученное в клиническом плане, угрожающее зрению хроническое заболевание глаз, которое развивается в какой–либо стадии практически у всех пациентов с сахарным диабетом 1 типа и у значительного количества лиц, страдающих диабетом 2 типа. Диабетическая ретинопатия характеризуется прогрессирующим изменением микрососудистой системы сетчатки, которое, как правило, происходит последовательно от небольших начальных проявлений, связанных с повышенной проницаемостью ретинальных сосудов (непролиферативная ретинопатия), до изменений, вызванных окклюзией сосудов (препролиферативная ретинопатия), а затем до наиболее тяжелой стадии диабетического поражения сетчатки, проявляющейся разрастанием новообразованных сосудов и фиброзной ткани (пролиферативная ретинопатия) [25]. Осложнения, связанные с увеличенной сосудистой проницаемостью и неконтролируемой неоваскуляризацией, часто приводят к значительному и необратимому снижению зрения.
Современная офтальмология обладает достаточным запасом знаний об этом грозном осложнении сахарного диабета. Доказано положительное влияние компенсации метаболических нарушений и нормализации артериального давления, получены данные о высокой эффективности лазерной коагуляции сетчатки и витрэктомии, оценена медицинская и экономическая эффективность скрининговых программ по раннему выявлению диабетических изменений сетчатки [1, 10, 11, 13, 16, 18, 21, 26, 32]. Однако, несмотря на это, ретинопатия продолжает оставаться одной из основных причин слепоты среди лиц трудоспособного возраста во всех развитых странах [6, 29, 34].
Национальные организации здравоохранения для создания системы профилактики слепоты вследствие диабетической ретинопатии должны решить следующие задачи:
– идентификация лиц с риском развития тяжелой диабетической ретинопатии;
– обеспечение систематического (и соответствующего) контроля гликемии;
– обеспечение пожизненной оценки состояния сетчатки;
– обеспечение доступным лазерным лечением лиц с риском снижения зрения;
– минимизация функциональных нарушений, связанных с лазерным лечением;
– реабилитация для пациентов, у которых произошло снижение зрения;
– обучение и вовлечение пациентов в управление их заболеванием.
Сент–Винсентская декларация, принятая в 1989 году под эгидой Всемирной Организации Здравоохранения (ВОЗ) и Международной Диабетологической Федерации, определив глобальную концепцию лечения и профилактики поздних осложнений сахарного диабета, обозначила и основные мероприятия, в частности – снижение на одну треть и более числа новых случаев слепоты, обусловленной диабетом [33]. Единственно эффективным способом ее предотвращения на сегодняшний день является лазерная коагуляция сетчатки. По мнению ВОЗ в настоящее время не существует лекарственных препаратов, способных предупредить развитие и прогрессирование диабетической ретинопатии у человека, поэтому при разработке и внедрении скрининговых стратегий не должны рассматриваться никакие лечебные воздействия, кроме лазеркоагуляции сетчатки [34].
Важно помнить, что организация четкой системы выявления и лечения диабетической ретинопатии должна привести к уменьшению случаев слепоты, что будет выражаться, в том числе, и в существенном экономическом эффекте. Достаточно сказать, что годовые затраты на лечение (лазерное) одного пациента с диабетической ретинонатией практически в 12 раз (!) ниже государственных социальных затрат (пенсии) на одного слепого [I]. Таким образом, организация доступной системы лечения ретинопатии лазерными методами, будет экономически выгодна, если учитывать материальные затраты на выплату пособий по инвалидности, которые несет государство, а также косвенные потери из–за невозможности принимать участие в производстве большому числу лиц трудоспособного возраста со слабовидением и слепотой вследствие диабетической ретинопатии. Разумеется, учесть в материальном эквиваленте моральные потери от человеческого страдания невозможно.
Все это указывает на то, что проблема предотвращения слепоты при диабете носит, в первую очередь, организационный характер и требует:
– четкого взаимодействия врачей различных специальностей при ведении больных сахарным диабетом;
– своевременного направления больного к офтальмологу;
– адекватного офтальмологического обследования;
– оценки степени риска прогрессирования и ухудшения зрения;
– своевременного начала лечения.
Эпидемиологические аспекты
диабетической ретинопатии
Эпидемиологии и прогрессированию диабетической ретинопатии посвящено очень большое количество исследований, проведенных в разных странах. Объем настоящей статьи не позволяет подробно останавливаться на этих вопросах. В то же время целесообразно привести данные некоторых исследований для того, чтобы еще раз подчеркнуть, что эта патология органа зрения в настоящее время является одной из серьезнейших медицинских проблем, уже хотя бы вследствие своей огромной распространенности (табл. 1).
Необходимо с осторожностью сравнивать результаты этих исследований, поскольку существует значительная разница в исследуемых популяциях (возраст, пол, длительность сахарного диабета, возраст в момент установления диагноза), в способах обследования (прямая офтальмоскопия, стереоскопическое цветное фотографирование стандартных полей сетчатки, флюоресцентная ангиография), в критериях оценки диабетических изменений сетчатки и использованных классификационных принципов.
Однако, несмотря на существенные различия в литературных данных, абсолютное большинство авторов к основным факторам риска, влияющим на уровень распространенности и прогрессирования диабетической ретинонатии, относят длительность и тип сахарного диабета, степень его компенсации, уровень артериального давления, состояние почек [1, 11, 21, 26, 32]. Все это должен учитывать офтальмолог, при выработке тактики ведения каждого пациента, страдающего этой тяжелой витреоретинальной патологией.
Классификация и клиника диабетической ретинопатии
Существуют множество классификаций диабетической ретинопатии, в основе которых лежат различные критерии. В настоящее время в большинсве европейских стран используется классификация, предложенная Е. Kohner и М. Porta (1991) [29]. Она проста и удобна в практическом применении, и вместе с тем, в ней четко определена стадийность процесса диабетического поражения сетчатки. Очень важно, что, пользуясь этой классификацией, можно достаточно точно установить, когда, на каком этапе диабетического поражения сетчатки, нужно проводить лазеркоагуляцию. Согласно этой классификации выделяются три основные формы (стадии) ретинопатии.
Непролиферативная ретинопатия характеризуется наличием микроаневризм, кровоизлияний, «твердых» и/или «мягких» экссудатов, отеком сетчатки (наиболее важный элемент непролиферативной ретинопатии – при локализации в макулярной области он может приводить к значительному снижению остроты зрения).
Препролиферативная ретинопатия характеризуется появлением венозных (выраженное расширение, неравномерность калибра – четкообразность, извитость, сосудистые петли) и интраретинальных микрососудистых аномалий. Выраженность этих изменений напрямую связана с риском развития пролиферации.
Пролиферативная ретинопатия характеризуется двумя видами пролиферации – сосудистой и фиброзной. Пролиферация, как правило, формируется в области диска зрительного нерва (ДЗН) или по ходу сосудистых аркад, но может располагаться в любых других участках глазного дна.
Новообразованные сосуды растут по задней поверхности стекловидного тела. Несостоятельность стенки новообразованных сосудов и их тракция ведет к частым геморрагиям, как преретинальным, так и к кровоизлияниям в стекловидное тело. Рецидивирующие кровоизлияния, происходящие вследствие прогрессирования задней отслойки стекловидного тела, и пролиферация глиальных клеток ведут к образованию витреоретинальных тракций, которые могут вызвать отслойку сетчатки. Степень выраженности фиброза (и витреоретинальных тракций) имеет большое значение для наблюдения за развитием процесса и для решения вопроса о целесообразности проведении лазеркоагуляции сетчатки.
Площадь неоваскуляризации как сетчатки, так и диска зрительного нерва, наличие или отсутствие витреальной или преретинальной геморрагии – эти изменения нужно тщательно оценивать, поскольку по ним можно прогнозировать степень прогрессирования пролиферативной диабетической ретинопатии. Большое внимание этому было уделено группой по изучению диабетической ретинопатии – Diabetic Retinopathy Study Research Group (DRS) [12]. Авторы этого исследования выделили в развитии пролиферативной ретинопатии основные патологические состояния, которые назвали факторами риска значительного снижения остроты зрения:
– преретинальная или витреальная геморрагии;
– неоваскуляризация ДЗН больше трети его площади;
– неоваскуляризация сетчатки по площади больше половины площади ДЗН.
Дальнейшие вазопролиферативные процессы могут привести к появлению новообразованных сосудов в радужной оболочке (рубеоз) и в углу передней камеры, который является зоной оттока внутриглазной жидкости. Эти изменения могут вызвать развитие неоваскулярной глаукомы.
Неоваскулярная глаукома – это вторичная глаукома, обусловленная пролиферацией новообразованных сосудов и фиброзной ткани в углу передней камеры и на радужке. В ходе своего развития эта фиброваскулярная мембрана сокращается, что приводит к формированию больших по протяженности гониосинехий и к некупируемому повышению внутриглазного давления.
Деление вторичной неоваскулярной глаукомы на стадии достаточно условно, в то же время оно целесообразно у больных сахарным диабетом, поскольку определяет тактику лечения. М.В. Schields (1992) предлагает выделять следующие основные стадии [31].
Стадия преглаукомы. Новообразованные сосуды выявляются клинически на радужке и в углу передней камеры, который открыт. Нарушение офтальмотонуса не выявляется (за исключением случаев, когда имеется сопутствующая первичная открытоугольная глаукома).
Стадия вторичной глаукомы с открытым углом передней камеры. Новообразованные сосуды расположены более плотно на поверхности радужки и в углу передней камеры, который все еще открыт. Внутриглазное давление повышено, часто имеется гифема (данная клиническая картина описывалась ранее как геморрагическая глаукома). На этой стадии наличие фиброваскулярной мембраны, покрывающей радужку и угол передней камеры, мешает эвакуации внутриглазной жидкости и объясняет повышение внутриглазного давления.
Стадия вторичной глаукомы с закрытым углом передней камеры. На этой стадии происходит сокращение фиброваскулярной мембраны, что ведет к изменениям на поверхности радужки и в углу передней камеры. Радужка смещена кпереди, строма ее уплощена, имеется выворот пигментного листка и механическое расширение зрачка. При гониоскопии выявляется смещение периферической части радужки кпереди, частичная или полная гониосинехия, которая ответственна за подъем внутриглазного давления. Эта стадия может сопровождаться выраженным болевым синдромом.
Поражение области желтого пятна при сахарном диабете называется диабетической макулопатией. Она возможна при любой стадии заболевания и представляет одну из основных причин снижения зрения, в связи с чем требует очень тщательной оценки. В основе диабетической макулопатии лежат два сопутствующих поражения:
– микроокклюзия капилляров (наиболее раннее проявление);
– гиперпроницаемость капилляров, связанная с прорывом внутреннего гематоретинального барьера (стенки капилляров сетчатки), иногда в сочетании с нарушением наружного гематоретинального барьера (пигментного эпителия сетчатки).
В настоящее время не существует общепризнанной классификации диабетической макулопатии, в то же время большинство исследователей, в зависимости от того, какое из перечисленных выше поражений является преобладающим, выделяют две основных клинических формы макулопатии:
– отечная (фокальная и диффузная);
– ишемическая.
Фокальный отек характеризуется локальной диффузией из микроаневризм или измененных сосудов. При биомикроскопии он выявляется как одна или несколько зон утолщения сетчатки, ограниченных липидными экссудатами. Резкое ухудшение зрения происходит чаще всего из–за расположения бляшки «твердого» экссудата в центре желтого пятна или вследствие пропотевания на границе фовеолы. При отсутствии лазерного лечения происходит прогрессирование процесса с формированием новых «твердых» экссудатов при одновременном рассасывании старых. Длительно существующие изменения такого типа приводят к необратимым изменениям в пигментном эпителии.
Диффузный отек обусловлен гиперпроницаемостью всей перимакулярной капиллярной сети. Ей сопутствует нарушение насосной функции, обеспечиваемой пигментным эпителием сетчатки (способность реабсорбировать жидкость, накапливающуюся в сетчатке, и транспортировать ее в подлежащие хориокапилляры). Диффузный отек при биомикроскопии определяется как утрата фовеолярного рефлекса и утолщение сетчатки в макулярной зоне.
Длительно существующий диффузный отек может приводить к кистозным изменениям сетчатки с формированием прозрачных микрокист (с центральной ячейкой или без нее). Кистозный макулярный отек часто сопровождается значительным снижением остроты зрения. Иногда наблюдается спонтанный регресс кистозного макулярного отека, но наиболее часто он дает тяжелые и необратимые осложнения: дистрофию пигментного эпителия сетчатки, ламеллярное макулярное отверстие, эпиретинальную мембрану. Оценивая влияние различных факторов на возникновение кистозного макулярного отека, необходимо учитывать не только местные (ишемическая капилляропатия, сопутствующая пролиферативная диабетическая ретинопатия, синдром ретиновитреального контакта), но и системные факторы (компенсация сахарного диабета, уровень артериальной гипертензии, наличие и тяжесть нефропатии, беременность).
Ишемическая макулопатия дает наихудший прогноз в отношении зрения. При этом перфузия перифовеолярной зоны отсутствует. На флюоресцентной ангиографии видно, что капилляры здесь как бы «обрублены», и терминальная часть их расширена. У молодых пациентов достаточно долго может сохраняться сравнительно высокая острота зрения, а у пожилых – быстро возникает тяжелая потеря зрения. Лазеркоагуляция при этом типе макулопатии не эффективна, а может привести и к ухудшению состояния.
Для определения показаний для лазерного лечения исследовательская группа по изучению раннего лечения диабетической ретинопатии – Early Treatment Diabetic Retinopathy Study Research Group (ETDRS) сформулировала критерии «клинически значимого макулярного отека», которые представлены в порядке уменьшения риска снижения остроты зрения [15]:
– утолщение сетчатки, расположенное в зоне до 500 мкм (1/3DP1) от центра макулы:
– наличие «твердых» экссудатов (при наличии утолщения сетчатки) в зоне до 500 мкм oт анатомического центра макулы;
– наличие утолщения сетчатки площадью, равной площади ДЗН, в зоне 500–1500 мкм от анатомического центра макулы.
Таким образом, снижение остроты зрения при диабетическом поражении сетчатки происходит в результате трех основных причин. Во–первых, из–за наличия макулопатии (макулярный отек или ишемия макулы) может страдать центральное зрение. Во–вторых, на стадии пролиферативной ретинопатии кровоизлияния (преретинальные или кровоизлияния в стекловидное тело), которые возникают из новообразованных сосудов, вызывают резкое ухудшение зрения. В–третьих, образование, разрастание и сокращение фиброваскулярной ткани ведет к тракции макулярной зоны или тракционной отслойке сетчатки, в результате чего происходит тяжелая и часто необратимая потеря зрения.
Быстрое снижение уровня сахара крови может привести к развитию транзиторной ретинопатии. Этот необычный, но важный клинический феномен, встречается в ряде случаев после достижения хорошей компенсации диабета у пациентов, у которых ранее диабет был декомпенсирован (например, после начала интенсивной инсулинотерапии и при трансплантации клеток поджелудочной железы у пациентов с сахарным диабетом) [10]. Развитием транзиторной диабетической ретинопатии также можно объяснить встречающееся в отдельных случаях значительное ухудшение состояния сетчатки при беременности, то есть в ситуации, когда многие женщины часто стремятся улучшить компенсацию диабета |24].
Возможно это связано с тем, что в условиях гипергликемии происходит значительное усиление ретинального кровотока. Резкое снижение уровня сахара крови приводит к его замедлению, что при наличии грубых структурных изменений ретинальных сосудов усиливает ишемизацию сетчатки (транзиторная ретинопатия характеризуется появлением большого количества «ватных» экссудатов). Причина этого, возможно, кроется и в связанном с гипергликемией повышенном синтезе сосудорасширяющих простагландинов, поддерживающих перфузию сетчатки даже в тех случаях, когда имеются значительные изменения капилляров. При достижении хорошей компенсации диабета этот синтез снижается, а, следовательно, уменьшается стимул для усиленного кровотока через сохранившиеся капилляры, что приводит к выраженной ишемии, за которой могут следовать пролиферативные изменения. Все это указывает на необходимость исключительно тщательного офтальмологического наблюдения пациентов в случаях быстрого снижение уровня сахара крови.
Диагностика диабетической ретинопатии
Очень важно помнить, что даже выраженные диабетические изменения со стороны глазного дна могут наблюдаться при сохраняющейся высокой остроте зрения. Больной не подозревает о них, пока у него не происходит ухудшения зрения, или пока он не будет осмотрен офтальмологом. Поэтому необходимо проводить осмотры, исходя из следующих основных принципов офтальмологического наблюдения, приведенных в таблице 2.
Идеальным методом выявления (скрининга) диабетической ретинонатии является офтальмологическое обследование с применением стереоскопического фотографирования стандартных полей сетчатки. Такое исследование позволяет получить объективную информацию о состоянии сетчатки. Выполнение процедуры проводится техническим персоналом, а оценка фотографий выполняется позже врачом–офтальмологом, специализирующимся в области ретинальной патологии. Правильная организация скрининга позволяет:
– быстро проводить оценку фотографий, а следовательно выявить группу риска по потере зрения и своевременно начать лечение;
– быстро проводить оповещение пациентов, нуждающихся в дальнейшем обследовании;
– получать, хранить и передавать заинтересованным специалистам объективную информацию о состоянии глазного дна.
Метод стереоскопического фотографирования стандартных полей сетчатки обладает наибольшей чувствительностью, однако, является очень дорогостоящим. Прямая офтальмоскопия несколько уступает по эффективности фотографическому методу, но при определенной оптимизации позволяет свести к минимуму количество случаев недиагностированной ретинопатии. Данный метод выявления диабетической ретинопатии (в сочетании с биомикроскопией сетчатки при помощи асферических линз) является оптимальным для нашей страны.
Независимо от использующегося метода, проведение скрининга ретинопатии в крупных городах Российской Федерации необходимо2, поскольку для создания оптимальной системы офтальмологической помощи больным сахарным диабетом необходимо располагать полной информацией о распространенности этого грозного осложнения сахарного диабета.
В Санкт–Петербурге пациенты, обследованные в результате скрининговых мероприятий, распределяются на три потока в зависимости от выраженности диабетических изменений сетчатки:
– пациенты с отсутствием диабетической ретинопатии или с минимальной непролиферативной ретинопатией, не грозящей снижением зрения, остаются под динамическим наблюдением офтальмолога поликлиники;
– пациенты с признаками диабетического поражения сетчатки, свидетельствующими о возможном снижении зрения (препролиферативная ретинопатия, непролиферативная ретинопатия без вовлечения макулы, но при наличии крупных конгломератов «твердых» экссудатов в пределах височных сосудистых аркад), направляются в межрайонные диабетологические центры;
– пациенты с изменениями сетчатки, свидетельствующими о высоком риске снижения зрения (пролиферативная ретинопатия и ретинопатия с вовлечением макулы), которые, как правило, нуждаются в лазеркоагуляции сетчатки или витрэктомии, направляются в территориальный диабетологический центр или офтальмологические стационары.
Лечение диабетической ретинопатии
Сахарный диабет – мультисистемное заболевание, требующее регулярного наблюдения врачами различных специальностей. Профилактика и лечение диабетической ретинопатии в настоящее время не имеют в своем арсенале специфических фармакологических средств, поэтому основными направлениями в ведении больных с диабетическими изменениями сетчатки являются:
– максимально стабильная компенсация сахарного диабета3 (гликироваиный гемоглобин НbА1С является показателем компенсации диабетических нарушений обмена веществ, поэтому имеет большое значение при прогнозировании появления и прогрессирования диабетической ретинопатии). При среднем уровне НbА1С выше 9% (норма от 3,6 до 7,0%) вероятность появления и прогрессирования диабетической ретинопатии крайне велика) [11, 20];
– лечение поражений сетчатки (лазерное и хирургическое).
Консервативная терапия. Понимание патогенетических механизмов развития диабетической ретинопатии должно привести к новым подходам в ее профилактике и лечении. К сожалению, пока они не будут найдены, диабетическая ретинопатия будет продолжать оставаться основной причиной потери зрения.
Клинические исследования потенциально возможных методов лечения остаются исключительно дорогими, так как включают лечение большого количества пациентов в течение многих лет. Наиболее перспективным решением проблемы была бы генетическая идентификация той группы больных сахарным диабетом, у которых со временем разовьется угрожающая зрению диабетическая ретинопатия (приблизительно треть пациентов). Возможность концентрировать исследования на пациентах, генетически предрасположенных к развитию осложнений, была бы исключительно полезной. Однако на сегодняшний день многочисленные попытки найти генетические маркеры не увенчались успехом.
Современные представления о патофизиологии диабетического поражения сетчатки позволяют выделить основные направления в консервативной терапии при диабетической ретинопатии: ингибиторы ангиотензин–превращающего фермента, игибиторы специфических изоформ протеин киназы С, аналоги соматостатина. В настоящее время ведутся большие и детальные исследования, в результате которых будет оценена эффективность этих препаратов.
Лазерная коагуляция сетчатки
Единственно эффективным способом лечения диабетической ретинопатии в настоящее время является лазеркоагуляция сетчатки. Это подтверждается данными многочисленных исследований, опубликованными за последние 30 лет. Именно информация о высокой эффективности лазеркоагуляции сетчатки, как средства предупреждения потери зрения, полученная в результате проведения широкомасштабных исследований, выполненных группой по изучению диабетической ретинопатии – DR–S и группой по изучению раннего лечения диабетической ретинопатии – ETDRS4, стала основой для разработки скрининговых программ по диабетической ретинопатии [2, 13–16].
Лазеркоагуляция при диабетическом поражении сетчатки направлена на выключение зон ретинальной ишемии, подавление неоваскуляризации и на облитерацию сосудов с повышенной проницаемостью, а также на образование хориоретинальных сращений, которые снижают риск тракционной отслойки.
Существуют три основных метода лазеркоагуляции:
– для лечения пролиферативной, а также препролиферативной ретинопатии. характеризующейся наличием обширных участков ишемии сетчатки с тенденцией к прогрессированию, используется панретинальная лазеркоагуляция сетчатки;
– для лечения макулопатии с локальной проницаемостью сосудов используется фокальная лазеркоагуляция;
– при диффузном макулярном отеке применяют коагуляцию по типу «решетки».
Панретинальная лазеркоагуляция сетчатки (ПРЛКС) заключается в нанесении коагулятов практически по всей площади сетчатки, исключая макулярную область. Основной задачей ПРЛКС является предупреждение или регрессия неоваскуляризации, что обеспечивается:
– уменьшением и ликвидацией зон ретинальной гипоксии, что, с одной стороны, приводит к уменьшению выработки вазопролиферативного фактора, а, с другой стороны, способствует улучшению питания оставшихся областей сетчатки, в том числе и макулярной;
– сближением сетчатки с хориокапиллярным слоем, что приводит к увеличению перфузии кислорода из хориоидеи в сетчатку;
– деструкцией сосудов с повышенной проницаемостью стенки и патологических сосудистых комплексов, что ведет к нормализации гемодинамики сетчатки.
Стандартная схема выполнении ПРЛКС. В подавляющем большинстве случаев для выполнения ПРЛКС используются большие размеры пятна (500 мкм для линзы Goldmann’a или 300 мкм для линзы Mainster’a 160°). На средней периферии сетчатки за 2–3 сеанса наносят 1500–2000 ожогов, оставляя свободной зону в 1 DP от носового края ДЗН, в 3 DP кверху и книзу и в 4 DP к височной стороны от анатомического центра макулы. При наличии препролиферативной и начальной пролиферативной диабетической ретинопатии в заднем полюсе можно оставить больше «свободного» места. Воздействие производят, постепенно продвигаясь от центральных отделов сетчатки к периферии (при наличии пролиферативной диабетической ретинопатии с неоваскуляризацией радужки и/или угла передней камеры вначале обрабатываются периферические отделы сетчатки). Необширные зоны плоской ретинальной неоваскуляризации обрабатываются сливающимися коагулятами, но несколько большей мощности (неоваскуляризация ДЗН не подвергается прямому воздействию). Воздействие распространяется до зон витреоретинальной тракции или тракционной отслойки сетчатки, отступая примерно на расстояние 1/2DP, но не производится поверх них.
При пролиферативной ретинопатии с высоким риском геморрагических осложнений ПРЛКС начинают с нижних квадрантов сетчатки. Такой порядок выполнения лазеркоагуляции связан с тем, что кровь, излившаяся в стекловидное тело, оседает вследствие законов гравитации в нижних его отделах, делая сетчатку в этих областях недоступной для лазерного лечения. Верхние же отделы стекловидного тела еще длительное время остаются относительно прозрачными.
Если препролиферативная и пролиферативная диабетическая ретинопатия протекает с явлениями макулопатии, то сначала необходимо выполнить вмешательство в макулярной зоне, а затем (через 3–4 недели) переходить непосредственно к ПРЛКС.
После проведения лазерной коагуляции сетчатки пациенту прописывают нестероидные противовоспалительные средства в каплях на несколько дней, особенно, если нанесено более 500 ожогов.
Основными критериями эффективности ПРЛКС служат исчезновение неоваскуляризации (или переход ее в неактивное состояние) и минимальные непролиферативные изменения оставшейся без воздействия сетчатки.
При стандартной методике лазерных вмешательств в макулярной зоне применяются в основном коагуляты размером 50–100 мкм, поскольку коагуляты большего размера увеличивают риск скотом и прогрессирующей атрофии пигментного эпителия сетчатки. Первоначально необходимо воздействовать на микроаневризму или на зону диффузного отека, расположенную на достаточно большом расстоянии от фовеолы. Постепенно мощность увеличивается до достижения необходимой интенсивности ожога. После получения требуемого эффекта начинается основное вмешательство. Сначала обрабатываются участки поражения, ближе всего расположенные к фовеоле, а затем производится воздействие кнаружи от этой зоны.
При локальном отеке, который обусловлен микроаневризмой, на нее наносится один ожог средней интенсивности. Если микроаневризма не белеет, то наносится повторный ожог большей интенсивности. После повторного воздействия, если пигментный эпителий сетчатки под микроаневризмой становится умеренно беловатым, даже если микроаневризма не меняет цвета, переходят к следующему участку поражения. При больших пропотевающих микроаневризмах обычно наносятся дополнительные коагуляты большей интенсивности. Положительным эффектом воздействия считается побеление микроаневризмы.
При диффузном отеке выполняется воздействие по типу «решетки» с использованием коагулятов размером 100 мкм. При небольших зонах отека коагуляты помещаются на расстоянии в два диаметра коагулята друг от друга. При скоплениях микроаневризм внутри колец «твердых» экссудатов ожоги наносятся еще плотнее. Интенсивность воздействия при выполнении «решетки» меньше, чем при фокальной коагуляции. Первоначальной зоной воздействия избирается менее отечная сетчатка, а затем мощность по мере необходимости увеличивается, и ожоги наносятся на более отечную ткань. Существует множество различных модификаций лазеркоагуляции по типу «решетки», однако основные правила, которые необходимо четко соблюдать при выполнении данного вмешательства, достаточно универсальны:
– ожоги должны быть слабыми по интенсивности, почти невидимыми в момент нанесения;
– расстояние между коагулятами должно составлять примерно 200 мкм, в случае обширных зон значительного отека коагуляты можно наносить плотнее – на расстоянии в один диаметр коагулята (100 мкм);
– центральная бессосудистая зона должна оставаться свободной (необходимо останавливаться в 200 мкм от краев перифовеолярной анастомотической аркады).
Перед проведением лазерной коагуляции больной должен быть информирован о том, что лечение направлено на предотвращение дальнейшего снижения остроты зрения, а не на восстановление нормальной остроты зрения.
Эффективность лазеркоагуляции сетчатки при диабетической ретинопатии не вызывает сомнений. Однако целый ряд клинических состояний ограничивает использование лазера и, в первую очередь, – это помутнение оптических сред. В таких случаях может быть произведена транссклеральная криоретинопексия [4].
Лечебный механизм криоретинопексии сходен с лазеркоагуляционным воздействием. Холодовая деструкция сетчатки (аппликаты наносятся через склеру) приводит к атрофии ишемизированных зон, а следовательно, – к улучшению обменных процессов и кровообращения в оставшейся сетчатке и даже к регрессу новообразованных сосудов.
Показания, обусловленные состоянием оптических сред. Не подлежит сомнению, что для лазеркоагуляции сетчатки необходимы прозрачность сред и хорошее расширение зрачка. Криотерапия имеет то преимущество, что может быть успешно проведена при менее благоприятных в оптическом отношении условиях под контролем бинокулярной офтальмоскопии, которая дает возможность яркого освещения и большого поля обзора, или под хронометрическим контролем.
Отсутствие эффекта от лазеркоагуляции сетчатки. Другим важным показанием для криовоздействия является отсутствие желаемого эффекта от ПРЛКС, когда после правильно проведенного лечения продолжается прогрессирование или отсутствует достаточный регресс неоваскуляризации (особенно радужки или угла передней камеры). Тогда панретинальная криоретинопексия является быстрым и эффективным методом разрушения дополнительных площадей гипоксичной сетчатки. В таком случае часто выбирают криоретинопексию передних отделов сетчатки.
Противопоказанием для этого вмешательства является выраженный фиброз, так как криоретинопексия может привести к тракционной отслойке сетчатки вследствие активации фиброваскулярной пролиферации. Поэтому до операции обязательно нужно провести ультразвуковое исследование глаза.
Несмотря на выполненную ПРЛКС, у некоторых пациентов может развиться тяжелая пролиферативная ретинопатия, осложненная кровоизлиянием в стекловидное тело, тракцией макулы или тракционной отслойкой сетчатки. В этих случаях, а также, когда выраженные новообразованные сосуды и кровоизлияние в стекловидное тело препятствуют осмотру глазного дна и лазерному лечению, витрэктомия через плоскую часть цилиарного тела становится единственно возможным вмешательством для предупреждения безвозвратной потери зрения. За последние 25 лет показания к витреоретинальной хирургии значительно расширились:
– тракционная отслойка сетчатки, захватывающая макулярную зону или угрожающая ей;
– регматогенная отслойка сетчатки;
– витреоретинальная тракция или преретинальное кровоизлияние у пациентов с активной неоваскуляризацией;
– непрозрачное (не позволяющее в полном объеме выполнить лазеркоагуляцию сетчатки) кровоизлияние в стекловидное тело у пациента, не получавшего ранее лазерного лечения;
– непрозрачное кровоизлияние в стекловидное тело вместе с тракцией сетчатки (выявляемой при эхографии) или с неоваскуляризацией переднего сегмента;
– непрозрачное кровоизлияние в стекловидное тело, сохраняющееся в течение 3 месяцев;
– диабетический макулярный отек с тракцией задней гиалоидной мембраны.
Врач, направляющий больного на витрэктомию, должен обращать внимание на несколько моментов:
– степень выраженности патологических изменений для определения вероятности положительного эффекта операции;
– при кровоизлиянии в стекловидное тело необходимо оценить выраженность геморрагии (небольшое кровоизлияние, не приводящее к инвалидизации, не является показанием к операции);
– адекватность ранее выполненной лазеркоагуляции сетчатки (кровоизлияния могут возникать по причине недостаточной коагуляции);
– острота зрения другого глаза (витреоретинальное вмешательство можно рекомендовать раньше при инвалидизации пациента из–за низкой остроты зрения на другом глазу);
– тяжесть общего заболевания, предполагаемая продолжительность жизни пациента, риск анестезии.
Лечение неоваскулярной глаукомы
Лечение на стадии рубеоза:
– ПРЛКС;
– транссклеральная криоретинопексия (если среды недостаточно прозрачны);
– их сочетание.
Лечение ни стадии вторичной глаукомы с открытым углом:
– ПРЛКС и/или транссклеральная криоретинопексия (если не были выполнены ранее);
– медикаментозное (бета–блокаторы, ингибиторы карбоангидразы, кортикостероиды);
– фистулизирующие операции как правило не очень эффективны из–за окклюзии зоны оттока фиброваскулярной тканью (в то же время возможно использование имплантатов).
Лечение на стадии вторичной глаукомы с закрытым углом:
– медикаментозное (бета–блокаторы, ингибиторы карбоангидразы, кортикостероиды, атропин);
– циклодеструктивные вмешательства (крио– или диод–лазерная циклодеструкция);
– интравитреальное введение кристаллических кортикостероидов.
В рамках одной журнальной статьи, естественно, невозможно отразить все аспекты диагностики и лечения больных с диабетической ретинопатией. В этой связи следует приветствовать выпуск тематических номеров журнала, которые позволяют дать разностороннюю информацию по какой–либо конкретной проблеме.