Эректильная дисфункция
Версия: Клинические рекомендации РФ 2021 (Россия)
Категории МКБ:
Импотенция органического происхождения (N48.4), Недостаточность генитальной реакции (F52.2)
Разделы медицины:
Урология
Общая информация
Краткое описание
Российское общество урологов
Клинические рекомендации
Эректильная дисфункция
Возрастная группа:
взрослые
Год утверждения (частота пересмотра): 2021 (не реже 1 раза в 3 года)
Определение заболевания или состояния (группы заболеваний или состояний)
Эректильная дисфункция (ЭД) — продолжающаяся более 3 месяцев неспособность достижения или поддержания эрекции, достаточной для проведения полового акта [1].
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
F52.2 — Недостаточность генитальной реакции
N48.4 — Импотенция органического происхождения
Облачная МИС «МедЭлемент»
Облачная МИС «МедЭлемент»

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
Классификация
Классификация заболевания или состояния (группы заболеваний или состояний)
Классификация ЭД по степени тяжести:
• лёгкая;
• умеренная;
• среднетяжелая;
• тяжёлая.
Патогенетическая классификация ЭД:
• психогенная — около 40% случаев;
• органическая — 29% случаев;
• смешанная (сочетание психических и органических факторов) — 25% случаев; неясного генеза — 6% случаев [4].
Этиология и патогенез
Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Факторы риска развития ЭД [2]:
• возраст;
• депрессия
• гиподинамия;
• ожирение;
• табакокурение;
• употребление наркотических средств;
• алкоголизм;
• дефицит витамина Д
• гиперлипидемия
• метаболический синдром;
• неблагоприятные внешние факторы — радиация, электромагнитное излучение.
Причинные факторы развития ЭД:
1. Психогенные факторы обуславливают психогенные нарушения эрекции, кодируемые в международной классификации болезней 10-го пересмотра (МКБ-10), как F52.2 — недостаточность генитальной реакции (эрекция — является одним из частных ее проявлений), не связанную с органическими факторами.
• ситуационные (особенности партнёра, чувство вины, тревога и т.д.);
• неврозы (тревожные, фобические). Зависимость от психоактивных веществ.
2 . Органические факторы вызывают органические формы ЭД. В М КБ-10 они кодируются как N48.4 — импотенция органического происхождения.
- Васкулогенные факторы:
— артериальная гипертензия;
— атеросклероз;
— сахарный диабет;
— гиперлипидемия;
— табакокурение (пенильный ангиоспазм);
— окклюзии подвздошных артерий;
— веноокклюзивные нарушения;
— оперативные вмешательства или лучевое воздействие в области таза и забрюшинного пространства.
- Нейрогенные факторы:
— болезнь Паркинсона;
— инсульт;
— новообразования центральной нервной системы;
— рассеянный склероз;
— травмы головного иили спинного мозга;
— поражения межпозвонковых дисков;
— периферические нейропатии вследствие:
• сахарного диабета;
• алкоголизма;
• хронической болезни почек;
• хронических болезней печени;
— полинейропатии;
— оперативные вмешательства или лучевая терапия в области забрюшинного пространства.
- Гормональные факторы:
— гипогонадизм (врождённый, приобретённый, возрастной);
— гиперпролактинемия;
— гипертиреоз, гипотиреоз;
— болезнь Иценко-Кушинга.
- Структурные факторы (болезни полового члена):
— опухоли полового члена;
— болезнь Пейрони;
— травма;
— врождённое искривление;
— склеротические изменения вследствие кавернита или приапизма;
— «малый» половой член;
— гипоспадия, эписпадия;
3. Лекарственно-индуцированные факторы
• Тиазидные диуретики
• Неселективные бета-адреноблокаторы
• Антидепрессанты
• Антиандрогены
• Психолептики
• Опиоиды [2].
Эпидемиология
Эпидемиология заболевания или состояния (группы заболеваний или состояний)
ЭД — распространённое заболевание в Российской Федерации, так как встречается у 48,9% мужчин в возрасте 20-77 лет. 34,6% мужчин страдают ЭД лёгкой степени, 7,2% — средней степени и 7,1% — тяжёлой степени [3].
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний или состояний)
ЭД проявляется либо недостаточной степенью исходной твердости полового члена иили ее спонтанным угасанием [2, 4].
Диагностика
Диагностика заболевания или состояния (группе заболеваний или состояний), медицинские показания и противопоказания к применению методов диагностики
Основным критерием установления ЭД является наличие жалоб на расстройства эрекции длительностью не менее 3 месяцев.
Диагностические мероприятия у пациентов, предъявляющих жалобы на ЭД, преследуют несколько целей:
• подтвердить наличие ЭД;
• определить степень её выраженности;
• выяснить причину этого расстройства, т.е. установить заболевание, вызвавшее его развитие;
• определить, страдает ли больной только ЭД или она сочетается с другими видами сексуальных расстройств (снижение полового влечения, нарушения эякуляции и оргазма) [5].
Жалобы и анамнез
- Рекомендуется при сборе жалоб и анамнеза выявлять сведения о сексологическом анамнезе пациента, а также состоянии копулятивной функции в прошлом и в настоящее время и его психическом статусе [6].
Уровень убедительности рекомендаций С (уровень достоверности доказательств — 5)
Комментарии:
Необходимо получить информацию о характере взаимоотношений с половым партнёром, предшествующих консультациях, о лечебных мероприятиях и их эффективности. Уточняют характер нарушения, его давность, стабильность проявления, влияние отдельных факторов и обстоятельств. Важно детально обсудить с пациентом качество адекватных и спонтанных эрекций, охарактеризовать половое влечение, продолжительность фрикционной стадии полового акта и оргазм.
Беседа с половым партнёром пациента весьма желательна и важна как для уточнения характера и степени выраженности нарушения, так и для успеха планируемой терапии [6].
- Рекомендуется с целью объективизации жалоб пациента, количественной характеристики сексуальных нарушений, включая ЭД, использовать одну из предложенных анкетных систем, например, наиболее распространённый опросник — сокращенный вариант Международного индекса эректильной функции (МИЭФ-5) [7, 8].
Уровень убедительности рекомендаций С (уровень достоверности доказательств — 5)
Комментарии: анализ полученных данных позволяет с высокой степенью достоверности судить о природе ЭД (табл. 1). Ситуационный, избирательный и преходящий характер расстройства, а также наличие спонтанных эрекций свидетельствуют о психогенном генезе нарушения. Количественное заключение о степени выраженности ЭД можно сделать по результатам заполненного пациентом опросника МИЭФ-5 (Приложение Г таблица 6).
- Рекомендуется всем пациентам с ЭД при сборе анамнеза выявлять наличие метаболических нарушений, так как выявлена связь между этими факторами риска и эректильной дисфункцией [9-12].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 2)
Комментарии: необходимо выяснить, страдает ли пациент сахарным диабетом гипогонадизмом, метаболическим синдромом, почечной недостаточностью [9-14].
Физикальное обследование
- Рекомендуется проводить оценку состояния сердечно-сосудистой системы пациентам с эректильной дисфункцией с помощью измерения артериального давления и характеристик пульса для оценки негативного влияния сердечно-сосудистых заболеваний на вероятность возникновения ЭД [15].
Уровень убедительности рекомендаций В (уровень достоверности доказательств — 2)
Комментарии: Учитывая высокую распространённость заболеваний сердечно-сосудистой системы и метаболического синдрома, объём обследования должен быть достаточным для заключения о допустимости сексуальной активности и об отсутствии противопоказаний к терапии ЭД.
Для стандартизации врачебных рекомендаций по сексуальной активности в случаях сердечного риска на международной конференции (Принстон, 2012) разработали рекомендации по лечению сексуальной дисфункции у пациентов с сердечно-сосудистыми заболеваниями [16]. Согласно Принстонскому консенсусу, пациентов разделяют на группы низкого, среднего и высокого риска (Приложение Г табл. 2).
При низкой степени риска сексуальную активность или лечение ЭД считают безопасным.
При средней и высокой степени рисков необходимо дообследование у врача-кардиолога.
Лабораторные диагностические исследования
- Рекомендуется всем пациентам с ЭД обязательное исследование уровня глюкозы, общего холестерина, ХС-ЛПВП, ХС-ЛПНП, триглицеридов в крови, а также уровня общего тестостерона в крови для диагностики сахарного диабета, атеросклероза артерий и гипогонадизма, обуславливающих ЭД [17].
Уровень убедительности рекомендаций С (уровень достоверности доказательств — 5)
Инструментальные диагностические исследования
- Рекомендуется проведение допплерографии сосудов полового члена с лекарственными препаратами при наличии у пациентов:
— первичной ЭД,
— перенесенной травмы или операций на органах таза или промежности в анамнезе, деформации полового члена,
— сложных эндокринных, психических и неврологических нарушения,
— а также перед фаллопластикой с протезированием [6, 18].
Уровень убедительности рекомендаций С (уровень достоверности доказательств — 5)
Комментарии: Ультразвуковую допплерографию артерий полового члена широко применяют для диагностики ЭД, хотя результаты исследования во многом зависят от технического совершенства аппаратуры. Этот метод более информативен, если исследование выполняют в состоянии покоя полового члена и индуцированной алпростадилом с последующим сравнением результатов. Основные количественные показатели при ультразвуковой допплерографии — максимальная (пиковая) систолическая скорость и конечная диастолическая скорость. На основе абсолютных показателей по стандартным формулам рассчитывают индекс резистентности. В норме пиковая систолическая скорость составляет более 30 см/с и индекс резистентности — более 0,8 [18-22].
Иные диагностические исследования
Иные диагностические исследования не рекомендуются.
Лечение
Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
- Рекомендуются перед началом медикаментозного лечения ЭД мероприятия по минимизации факторов риска заболевания и по нормализации образа жизни пациентов для улучшения эректильной функции и/или увеличения эффективности лечебных мероприятий [23].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 1)
Комментарии: корригирующие мероприятия и терапия, направленные на нормализацию артериального давления, уровня холестерина, глюкозы и общего тестостерона в крови, отмена и замена (в сотрудничестве со смежными специалистами) лекарственных препаратов, негативно влияющих на эрекцию. Нормализация питания, массы тела и регулярная физическая активность могут привести к улучшению эректильной функции даже без специфического ее лечения или увеличить эффективность лечебных мероприятий [24].
- Рекомендуется при лечении пациентов с ЭД руководствоваться принципом ступенчатого подхода в проведении лечебных мероприятий [25].
Уровень убедительности рекомендаций С (уровень достоверности доказательств — 5)
Комментарии: ступенчатый подход в лечении ЭД предполагает последовательное применение лечебных методов с увеличением их агрессивности от медикаментозной терапии ингибиторами фосфодиэстеразы 5 типа (по А ТХПрепараты для лечения нарушений эрекции) (альтернативной которым могут быть вакуумные эректоры и ударно-волновая терапия полового члена), до интракавернозных инъекций алпростадила и фаллопластики с протезированием. Смена ступени лечения производится при ее неэффективности или неприемлемости для пациента [25, 26].
1. Консервативное (медикаментозное) лечение
- Рекомендуется всем пациентам с ЭД назначение ингибиторов фосфодиэстеразы 5 типа (ФДЭ-5) (по АТХ Препараты для лечения нарушений эрекции) в качестве препаратов первой линии терапии [27,28].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 1)
Комментарии: в настоящее время в России доступны четыре препарата этой группы, выпускаемые в таблетированном виде в разных дозировках:
силденафил (следует учитывать, что по показанию лечения ЭД применяется только препарат в дозировке 25, 50 и 100 мг с кодом АТХ G04BE03; силденафил с дозировкой 2 0 мг, с кодом АТХ C02KX используют исключительно при лечении легочной артериальной гипертензии);
• тадалафил;
• варденафил;
• уденафил.
Их отличительная особенность — эффективность при всех формах ЭД и хорошая переносимость. Ингибиторы ФДЭ-5 используются эпизодически (по требованию) за определённое время перед половым актом, причём для наступления эффекта от препарата необходима сексуальная стимуляция. Дозы подбирают индивидуально. Ингибирование ФДЭ-5 приводит к релаксации гладких мышц, вазодилатации и эрекции. Профиль побочных эффектов варденафила, силденафила и тадалафила схож с плацебо [29, 30, 31].
Эффект силденафила может наблюдаться в течение 12 ч. После 24 недель его применения улучшение эректильной функции наблюдали у 56, 77 и 84% мужчин, принимавших 25, 50 и 100 мг силденафила соответственно, в сравнении с 25% улучшений у пациентов, принимавших плацебо. У пациентов с сахарным диабетом при использовании силденафила отмечалось 66,6% улучшения эрекции и 63% успешных соитий в сравнении с 28,6 и 33% у мужчин, принимавших плацебо, соответственно [29].
Варденафил помимо обычных таблетированных форм в дозировке 5, 10 и 20 мг выпускается также в варианте орально диспергированной таблетки, которая растворяется в ротовой полости без воды [30].
Принципиальное отличие тадалафила — его длительное действие: 36 ч. В премаркетинговых исследованиях после 12 недель применения тадалафила улучшение эрекции наблюдалось у 67 и 81% мужчин, принимавших 10 и 20 мг соответственно в сравнении с 35% мужчин, принимавших плацебо [31].
После 12 недель применения варденафила улучшение эрекций отметили в 66, 76 и 80% случаев при применении 5, 10 и 20 мг соответственно против 31% мужчин, принимавших плацебо. При приёме варденафила в сочетании с сахарным диабетом 78% пациентов подтвердит положительное изменение эректшьной функции, против 13% пациентов, получавших плацебо [30]. Исследования показали, что ежедневное применение тадалафша приводит к большему улучшению сексуальной функции, чем приём данного препарата по необходимости. В связи с этим данный препарат стали также выпускать в таблетированной форме с дозировкой 5 мг, предназначенной для ежедневного применения. Было выявлено, что длительное применение тадалафила улучшает эндотелиальные функции, данный эффект сохраняется после прекращения применения препарата [32].
Уденафил в дозировке 100 м г показал свою эффективность в мета-анализе у пациентов с ЭД. При его приеме было констатировано достоверное повышение показателя МИЭФ на 5,65 баллов, что было достоверно лучше плацебо (р<0,0001). Наиболее частыми побочными эффектами, связанными с приемом уденафила, были приливы крови к лицу и головная боль (уденафил по сравнению с плацебо, 5,6% против 1,8% и 3,1% против 0%, соответственно). [33].
Ни один из ингибиторов ФДЭ-5 не влияет отрицательно на продолжительность нагрузки или время до наступления ишемии при тестировании пациентов со стабильной стенокардией. Ингибиторы ФДЭ- 5 могут даже улучшать результаты данных тестов.
При сочетании ингибиторов ФДЭ-5 с антигипертензивными препаратами и альфа-адреноблокаторами наблюдается склонность к гипотензии.
Применение альфа-адреноблокаторов в сочетании с ингибиторами ФДЭ-5 может приводить к ортостатической гипотензии [34].
Сравнение фармакокинетики, клинической эффективности и нежелательных явлений ингибиторов ФДЭ-5 представлено в таблицах 3, 4, 5.
Ингибиторы ФДЭ-5 нельзя принимать параллельно с органическими нитратами из-за потенцирования гипотензивного действия. Согласно рекомендациям Американской кардиологической ассоциации, органические нитраты можно использовать не ранее чем через 24 ч после приёма короткодействующих ингибиторов ФДЭ-5 и не ранее чем через 48 ч после приёма тадалафила. При использовании ингибиторов ФДЭ-5 следует учитывать потенциальный риск осложнений, связанных с сексуальной активностью, в течение 90 дней после перенесённого инфаркта миокарда; при нестабильной стенокардии или стенокардии, возникающей во время полового акта; при развившейся в течение последних 6 мес сердечной недостаточности II функционального класса и выше по NYНА, неконтролируемых нарушениях сердечного ритма, артериальной гипотензии (АД ниже 90/50 мм рт. ст.) или неконтролируемой артериальной гипертензии, а также в течение 6 мес после инсульта [35]. Сочетание ингибиторов ФДЭ-5 с другими лекарственными средствами возможно.
- Рекомендуется в качестве препаратов второй линии терапии ЭД назначение интракавернозных инъекций алпростадила [5, 36].
Уровень убедительности рекомендаций С (уровень достоверности доказательств — 5)
Комментарии: при отсутствии эффекта от пероральных препаратов могут быть применены интракавернозные инъекции. Результативность данной терапии составляет около 85%. Для интракавернозного введения используют алпростадил.
Начальная доза алпростадила у пациентов с ЭД на фоне повреждений спинного мозга составляет 1,25 мкг. Дозировка второй и третьей инъекции в таких случаях составляет 2,5 и •5 мкг, соответственно. Шаг последующего увеличения доз у пациентов данной категории равен 5 мкг.
При ЭД сосудистого, психогенного и смешанного генеза начальная дозировка алпростадила составляет 2,5 мкг. Вторая инъекция может быть в дозе 5-7,5 мкг. Шаг последующего увеличения дозировок варьирует от 5 до 10 мкг. Препарат растворяют в 1 мл 0,9%-ного раствора натрия хлорида**.
Эрекция наступает через 5-15 мин после введения препарата, её продолжительность зависит от дозы, составляя в среднем около 90 мин. После подбора необходимого количества препарата и соответствующего обучения пациента переводят на выполнение аутоинъекций, частота их не более 3 раз в неделю. В генеральной группе пациентов с ЭД эффективность простагландина 70%, а в субгруппах до 94%. Осложнения: боль в половом члене у 50% пациентов после 11%, инъекций, сверхпролонгированная эрекция 5%, приапизм 1% и фиброз 2%,. Боль облегчается при использовании раствора натрия гидрокарбоната** и анестезии.
Данная терапия противопоказана пациентам:
• при повышенной чувствительностью к используемому препарату;
• с риском развития приапизма;
• с грубыми анатомическими дефектами полового члена.
К побочным эффектам относят:
• пролонгированную эрекцию;
• приапизм;
• боль в половом члене;
• развитие фиброза кавернозной ткани.
Пациента нужно предупредить, что в случае сохранения эрекции более 4 ч ему необходимо обратиться к врачу [37].
2. Консервативное немедикаментозное лечение
- Рекомендуется использовать вакуумные эректоры в качестве альтернативной терапии первой линии у хорошо информированных об особенностях данного лечения пожилых пациентов с низкой сексуальной активностью и сопутствующими заболеваниями, требующими немедикаментозного лечения [38].
Уровень убедительности рекомендаций С (уровень достоверности доказательств — 5)
Комментарии: сущность метода заключается в том, что половой член помещают в специальную колбу, где создают отрицательное давление с помощью вакуумного насоса. Это приводит к увеличению притока крови к пещеристым телам, что обусловливает эрекцию, для сохранения которой на основание полового члена накладывают специальное сжимающее кольцо, ограничивающее венозный отток. Достигаемая эрекция не физиологична. Показания к применению вакуумных устройств — невозможность лекарственной терапии или её неэффективность, а также предпочтение пациента. К данному виду терапии более склонны пожилые мужчины, которым свойственна низкая сексуальная активность. Эффективность метода и удовлетворённость им составляют от 27 до 94%. Примерно 30% пациентов отказываются от применения вакуумных устройств, в связи с возникновением боли, подкожных кровоизлияний, затруднённой эякуляции и снижения чувствительности головки полового члена [39].
- Рекомендуется применять низкоэнергетическую ударно-волновую терапию у пациентов в качестве альтернативной первой линии лечения у пациентов с легкой степенью ЭД или при отсутствии эффекта от ингибиторов ФДЭ-5 [40, 41,42,43].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 1)
Комментарии: низкоэнергетическая ударно-волновая терапия ЭД основана на воздействии на пещеристую ткань полового члена слабых акустических волн. Предполагается, что, проходя через биологические ткани разной плотности, акустические волны вызывают сдвиговое напряжение, которое увеличивает уровень сложных химических комплексов и окиси азота, стимулирующих процесс неоваскуляризации в кавернозных телах [44].
3. Оперативное лечение
- Рекомендуется в качестве третей линии лечения пациентов с ЭД применять фаллопластику с протезированием протезом полового члена ригидным или протезом полового члена трехкомпонентным наполняемым [2, 25, 26].
Уровень убедительности рекомендаций С (уровень достоверности доказательств — 5)
Комментарии: при неэффективности консервативной терапии ЭД, проявляющейся отсутствием положительной клинической динамики и прироста баллов при повторном анкетировании по опросникам МИЭФ или МИЭФ-5, а также в случае желания пациента, оптимальным лечением является осуществление фаллопластика с протезированием.
Существует два типа протезов полового члена: ригидные и трехкомпонентные, наполняемые. Большинство пациентов предпочитают протез полового ччена трехкомпонентный наполняемый в силу достижения более натуральной эрекции. Удовлетворенность половой жизнью после их имплантации отмечают свыше 90% оперированных и их партнерш.
Протез полового члена ригидный создает постоянную осевую твердость органа.
Фаллопластику с протезированием осуществляют через 3 оперативных доступа, мошоночный, подлобковый и завенечный. Мошоночный доступ обеспечивает хорошую визуализацию, позволяет при необходимости подойти к проксимальной части ножек полового члена, избегая повреждения дорсальных нервов, с возможностью установки помпы под контролем зрения. При сопутствующем тяжелом недержании мочи через этот же доступ мож но одномоментно установить искусственный сфинктер мочевого пузыря. При этом доступе резервуар устанавливается в позадилонное пространство без визуального контроля, что может быть чревато повреждением мочевого пузыря и подвздошных сосудов у больных, у которых в анамнезе были объемные операции на органах малого таза (радикальная простатэктомия или цистэктомия). В таких ситуациях безопаснее прибегать к эктопической субмускулярной установке резервуара над поперечной фасцией живота через основной кожный разрез.
Подлобковый доступ дает преимущество установки резервуара под контролем зрения, однако имплантация помпы может быть затруднительной и сопровождается повышенным риском повреждения дорсальных нервов полового члена.
Завенечный доступ предпочтителен в ситуациях, когда ЭД сочетается с выраженной деформацией полового члена (при болезни Пейрони) для осуществления одномоментной корпоропластики или при желании пациента увеличить длину органа при фаллопластике с протезированием (раскладывающая техника).
Наиболее тяжелым осложнением фаллопластики с протезированием является перипротезная инфекция. Ее частота существенно ниже у частооперирующих врачей-урологов. Антибактериальное покрытие протезов полового члена позволяет снизить вероятность данного осложнения с 5% до 2%.
Ресурс функционирования современных протезов превышает 15 лет. При их механической поломке проводится реимплантация нового [45, 46, 47, 48].
Медицинская реабилитация
Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
- Рекомендуется пациентам после радикальной простатэктомии начинать пенильную реабилитацию в ранние сроки с момента операции [49, 50, 51].
Уровень убедительности рекомендаций А (уровень достоверности доказательств — 1)
Госпитализация
Организация оказания медицинской помощи
Критерием эффективности консервативной терапии ЭД является увеличение баллов при повторном анкетировании по опроснике МИЭФ-5.
Показания для плановой госпитализации:
1) фаллопластика с протезированием
Показания для экстренной госпитализации:
1) не предусмотрена
Показания к выписке пациента из стационара:
1) отсутствие осложнений после фаллопластики с протезированием
Профилактика
Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
- Рекомендуются нормализация образа жизни и модификация факторов риска у пациентов с ЭД в качестве мер возможной профилактики расстройств эрекции [49, 50].
Уровень убедительности рекомендаций С (уровень достоверности доказательств — 5)
Комментарии: меры профилактики ЭД — нормализация образа жизни, достаточная физическая активность, исключение табакокурения, ограничение потребления алкоголя, контроль и коррекция массы тела, содержания глюкозы и липидов в крови, а также регулярная половая жизнь (не менее 3 раз в неделю) [52, 53].
Информация
Источники и литература
-
Клинические рекомендации Всероссийского общества урологов
- 2. Глыбочко П.В., Аляев Ю.Г., Чалый М.Е., Ахвледиани Н.Д. Половые расстройства у мужчин. — М.: ГЭОТАР- Медиа 2012. — С. 71-90.
4. Глыбочко П.В., Аляев Ю.Г. и соавт. Урология: учебник / под ред. — 3-е изд., перераб. и доп. — М.: ГЭОТАР- Медиа, 2013. — С. 543-558.
- 2. Глыбочко П.В., Аляев Ю.Г., Чалый М.Е., Ахвледиани Н.Д. Половые расстройства у мужчин. — М.: ГЭОТАР- Медиа 2012. — С. 71-90.
Информация
Список сокращений
АГ — артериальная гипертензия
ИБС — ишемическая болезнь сердца
мг — миллиграмм
МКБ-10 — международная классификация болезней 10-го пересмотра
мин — минут
см — сантиметр
сек — секунда
ТГ — триглицериды
ФДЭ-5 — фосфодиэстераза-5
ФК — функциональный класс
ХС-ЛПВП -холестерин липопротеинов высокой плотности
ХС-ЛПНП — холестерин липопротеинов низкой плотности
ЭД — эректильная дисфункция
МИЭФ — Международный индекс эректильной функции
МИЭФ-5 — сокращенная версия анкеты МИЭФ
IIEF — International Index of erectile function
Термины и определения
Эректильная дисфункция — продолжающаяся более 3 месяцев неспособность достижения или поддержания эрекции, достаточной для проведения полового акта.
Критерии оценки качества медицинской помощи
| № | Критерии качества |
Уровень достоверности доказательств |
Уровень убедительности рекомендаций |
| Этап | |||
| 1 |
Выполнено анкетирование по опроснику МИЭФ-5 |
5 | С |
| 2 |
Выполнено определение уровня глюкозы в крови |
5 | С |
| 3 |
Выполнено определение уровня общего холестерина в крови |
5 | С |
| 4 |
Выполнено определение уровня общего тестостерона в крови |
5 | С |
| 5 |
Выполнена допплерография сосудов полового члена с лекарственными препаратами |
5 | С |
| Этап | |||
| 1 |
Выполнено назначение рекомендации по изменению образа жизни перед началом медикаментозного лечения |
1 | А |
| 3 | Применен поэтапный принцип лечения ЭД | 5 | С |
| 4 |
Выполнено назначение ингибиторов ФДЭ-5 в качестве первой линии терапии ЭД |
1 | А |
| 5 |
Выполнено назначение интракавернозных инъекций алпростадила в качестве второй линии терапии ЭД |
5 | С |
| 6 |
Выполнение фаллопластики с протезированием лечения ЭД в качестве третей линии |
5 | С |
Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
1. Ахвледиани Ника Джумберович — доктор медицинских наук, профессор кафедры урологии Федерального государственного бюджетного образовательного учреждения высшего образования «Московский государственный медико-стоматологический университет имени А.И.Евдокимова» Министерства здравоохранения Российской Федерации
2 . Берников Александр Николаевич — кандидат медицинских наук, доцент кафедры урологии Федерального государственного бюджетного образовательного учреждения высшего образования «Московский государственный медико-стоматологический университет имени А.И.Евдокимова» Министерства здравоохранения Российской Федерации
3. Гвасалия Бадри Роинович — доктор медицинских наук, заведующий кафедрой урологии медицинского института непрерывного образования Федерального государственного бюджетного образовательного учреждения высшего образования «Московского государственного университета пищевых производств».
Все члены Рабочей группы подтвердили отсутствие финансовой поддержки/конфликта интересов, о которых необходимо сообщить.
Приложение А2. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций:
1. Врач — уролог
2 Врач — акушер-гинеколог
3. Студенты медицинских ВУЗов, ординаторы, аспиранты
В данных клинических рекомендациях все сведения ранжированы по уровню достоверности доказательности) в зависимости от количества и качества исследований по данной проблеме.
Таблица П1. Уровни достоверности доказательств (УДД) для диагностических вмешательств
| УДД |
Иерархия дизайнов клинических исследований по убыванию уровня достоверности доказательств от 1 до 5 |
| 1 |
Систематические обзоры исследований с контролем референсным методом1 |
| 2 | Отдельные исследования с контролем референсным методом |
| 3 |
Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода |
| 4 | Несравнительные исследования, описание клинического случая |
| 5 | Имеется лишь обоснование механизма действия или мнение экспертов |
1Общепринятым стандартом КИ диагностических вмешательств является одномоментный дизайн исследования, в котором к каждому включённому пациенту параллельно и в одинаковых условиях применяются исследуемый диагностический метод и референсный метод, являющийся «золотым стандартом» диагностики изучаемого заболевания или состояния, при этом исследуемый и референсный методы должны применяться независимо друг от друга (т.е. исследуемый метод не может быть частью референсного) и должны интерпретироваться исследователем без знания результатов применения другого метода (рекомендуется использовать ослепление).
Таблица П.2 — Уровни убедительности рекомендаций (УУР) для диагностических вмешательств
| УРР | Основания |
| А |
Однозначная (сильная) рекомендация (все исследования имеют высокое или удовлетворительное методологическое качеств, их выводы по интересующим исходам являются согласованными) |
| В |
Неоднозначная (условная) рекомендация (не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными) |
| С |
Низкая (слабая) рекомендация — отсутствие доказательств надлежащего качества (все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными) |
Таблица П.3 — УДД для лечебных, реабилитационных, профилактических вмешательств
| УДД | Иерархия дизайнов клинических исследований по убыванию уровня |
| 1 |
Систематический обзор рандомизированных клинических исследований РКИ с применением мета-анализа |
| 2 |
Отдельные РКИ и систематические обзоры исследований любого дизайна (помимо РКИ) с применением мета-анализа |
| 3 | Нерандомизированные сравнительные исследования, в т.ч. когортные |
| 4 |
Несравнительные исследования, описание клинического случая или серии случаев, исследования «случай-контроль» |
| 5 | Имеется лишь обоснование механизма действия вмешательства |
Таблица П.4 — УУР для лечебных, реабилитационных, профилактических вмешательств
| УРР | Основания |
| А |
Однозначная (сильная) рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными) |
| В |
Неоднозначная (условная) рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными) |
| С |
Низкая (слабая) рекомендация — отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными) |
Приложение АЗ. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов инструкции по применению лекарственного препарата
Данные клинические рекомендации разработаны с учётом следующих нормативно-правовых документов:
1. Стандарт медицинской помощи при эректильной дисфункции (Приказ Министерства здравоохранения Российской Федерации от 9 ноября 2012 г. № 778н «Об утверждении стандарта первичной медико-санитарной помощи при эректильной дисфункции»),
2. Клинические рекомендации Европейской ассоциации урологов [51].
Приложение Б. Алгоритмы действий врача
Приложение В. Информация для пациентов
Что такое эректильная дисфункция?
Эректильная дисфункция (ЭД) — продолжающаяся более 3 месяцев неспособность достижения илитподдержания эрекции, достаточной для проведения полового акта.
Каковы причины эректильной дисфункции?
Выделяют ряд факторов, которые повышают риск развития ЭД:
• возраст;
• депрессия;
• малоподвижный образ жизни;
• ожирение;
• табакокурение;
• употребление наркотических средств;
• алкоголизм;
• дислипидемия и метаболический синдром;
• сахарный диабет;
• операции на органах таза
Устранение неблагоприятных воздействий, связанных с особенностями образа жизни, приводит к уменьшению риска возникновения ЭД. В частности, увеличение физической активности снижает её вероятность у мужчин среднего возраста на 70% в течение 8 лет регулярных тренировок.
Причины развития ЭД делятся на психогенные (нарушения психологический сферы, приводящие к расстройствам эректильной функции) и органические (ряд заболеваний/патологических состояний организма, которые вызывают ЭД на структурном, органическом уровне). Кроме того, нарушения эрекции могут быть вызваны приемом ряда лекарственных препаратов: препараты тиазидных диуретиков и неселективных бета-адреноблокаторов, антиандрогенов, психолептиков, психоаналептиков и опиоидов.
Как часто встречается эректильная дисфункция?
Э Д — распространённое заболевание в Российской Федерации, так как встречается у 48,9% мужчин в возрасте 20-77 лет. Среди курильщиков ЭД встречается на 15-20% чаше, чем среди некурящих мужчин.
Как проводится диагностика эректильной дисфункции?
Основанием для постановки диагноза эректильной дисфункции являются жалобы пациента на неспособность достижения или поддержания эрекции, достаточной для проведения полового акта, длящееся в течение не менее 3 месяцев.
Для объективизации жалоб, уточнения степени тяжести заболевания применяют специальные анкеты-опросники. Наиболее широко применяемая анкета — сокращенный вариант Международного индекса эректильной функции (МИЭФ-5).
Для выявления сопутствующих заболеваний сердечно-сосудистой, эндокринной и половой систем, первым проявлением которых может стать ЭД, проводится осмотр пациента.
Характер и объём лабораторных исследований определяют индивидуально с учётом жалоб, расспроса и обследования в зависимости от объективной необходимости и желаний пациента. Основные лабораторные исследования, выполняемые в ходе обследования, включают: анализ уровня глюкозы в крови; анализ липидного профиля; анализ уровня общего тестостерона в утренней порции крови.
Ряд специальных инструментальных исследований (наиболее часто оценку кровообращения в половом члене с помощью допплерографии сосудов полового члена с лекарственными препаратами) проводится при наличии показаний.
Какие существуют методики лечения эректильной дисфункции?
Изменение образа жизни
Перед началом лечения необходимо максимального исключить факторы риска развития ЭД (депрессия; гиподинамия; ожирение; табакокурение; употребление опиоидов; злоупотребление алкоголем), нормализовать образ жизни, режим сексуальной активности, сна и отдыха. Следует решить вопрос о возможности отмены или замены получаемых пациентом лекарственных препаратов, способных отрицательно влиять на эрекцию.
Консервативное лечение
Первой линией терапии ЭД является назначение таблетированных лекарств, усиливающих приток крови к половому члену. Их отличает возможность назначения при всех формах ЭД и хорошая переносимость. Они могут быть использованы как ежедневно, так и эпизодически (по требованию) за определённое время перед половым актом, причём для наступления эффекта от препарата необходима сексуальная стимуляция. Дозы подбирают индивидуально.
При невозможности назначения или нежелании пациента применять вышеуказанные лекарства, в качестве альтернативы рекомендуется назначение лечения локальным отрицательным давлением (применение вакуумных эректоров) или ударно-волновая терапия полового члена.
Препараты второй линии терапии ЭД рекомендовано назначать в виде внутрипещеристых инъекций непосредственно в половой член.
Оперативное лечение
При безуспешности всех консервативных методов лечения, если пациент настаивает на кардинальном решении своей проблемы, выполняется фаллопластика с протезированием протезом полового члена ригидным или трехкомпонентным наполняемым, качественно имитирующим эрекцию.
Уровень удовлетворенности пациентов, подвергшихся фаллопластнке с протезированием члена тоехкомпонентным наполняемым составляет протезированием протезом полового члена свыше 90%.
Приложение Г1 — Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Таблица 1 — Различия органической и психогенной эректильной дисфункции
Таблица 2 — Принстонский консенсус по стратификации сердечно-сосудистого риска среди мужчин с эректильной дисфункцией
Таблица 3 — Основные параметры фармакокинетики ингибиторов ФДЭ-5 [271.
Приложение 1. Шаблон включения шкалы, опросника, других валидизированных методов оценки состояния пациента, прогноза рисков возникновения осложнений и прогноза заболевания
Название на русском языке: Международный индекс эректильной дисфункции (МИЭФ-5)
Тип:
-шкала
— опросник
— другое_________
Назначение: выявление и оценка степени тяжести ЭД.
Содержание: Оцените вашу эректильную функцию за последние 6 месяцев, ответив на нижеследующие 5 вопросов
Ключ:
22-25 баллов — ЭД отсутствует.
17-21 баллов — легкая степень ЭД.
12-16 баллов — умеренная (промежуточная степень между легкой и среднетяжелой ЭД).
8-11 баллов — среднетяжелая ЭД.
5-7 баллов — тяжелая ЭД.
Пояснения: пациенты отвечают на 5 вопросов одним из представленных 5 ответов. Каждому ответу соответствует указанный бал. По завершении анкетирования баллы за ответы суммируются и соотносятся с ключем. МИЭФ-5 позволяет исключить или подтвердить наличие ЭД, а так же определить ее выраженность.
Прикреплённые файлы
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
Дата публикации 25 декабря 2017Обновлено 26 апреля 2021
Определение болезни. Причины заболевания
Эректильная дисфункция — продолжительная (не менее 6 месяцев) неспособность мужчины достигать напряжения полового члена, достаточного для полноценного сексуального акта.
Человек — единственный биологический вид на нашей планете, который может поддерживать эрекцию достаточно длительное время. Нарушение этой способности является важной медицинской и социальной проблемой, ведёт к потере самоуважения, семейным конфликтам.
Внутренние причины эректильной дисфункции
- Нарушения сердечно-сосудистой системы. Разнообразные заболевания сердца и сосудов ведут к нарушению в интимной сфере (до 65% случаев) — ишемическая болезнь, нарушение сердечного ритма, гипертензия, состояния после инфарктов миокарда. Сужение сосудов (атеросклероз) в значительной степени присуще также сосудам фаллоса. Недаром некоторые учёные считают дисфункцию потенции предвестником сердечной патологии и рекомендуют начинать обследование сердца как можно раньше, если появились проблемы в интимной сфере. Имеет также значение повышенный холестерин и курение, приводящее к поражению стенки сосудов. Кроме того, препараты для лечения гипертонии и сердца могут сами по себе также вызывать значительные нарушения эрекции.[2]
- Травматический фактор — один из основных в развитии стойких нарушений потенции. Это переломы костей таза, разрывы уретры, травма головы, непосредственное повреждение кавернозных тел, состояния после операций на предстательной железе по поводу аденомы и рака.[3]
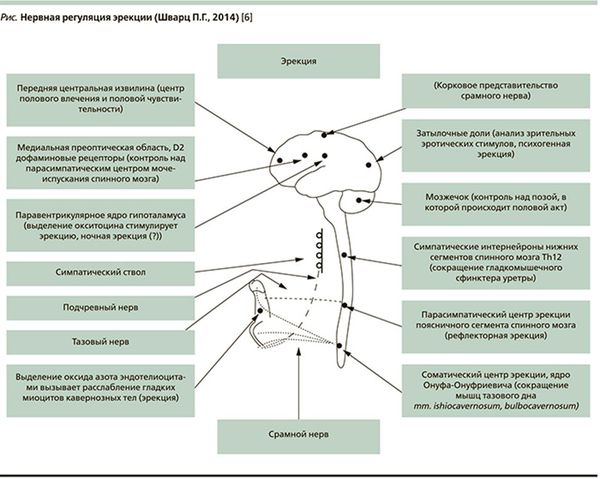
- Нарушения нервной проводимости. Чтобы осознать глубину проблемы, рекомендую просто взглянуть на схему нервной регуляции эрекции доктора П.Г. Шварца.
Работа организма в норме:
Согласно этой схеме, существует 14 структур регуляции эрекции. Нарушение на любом уровне может повлечь за собой разнообразные нарушения в интимной сфере мужчины. Данные структуры могут нарушаться в результате инсультов, травм, грыж межпозвоночных дисков, опухолей различных локализаций, рассеянного склероза, других неврологических заболеваний.[4]
Кроме того, выделяют группу причин, связанных с нарушением работы органов внутренней секреции (эндокринные причины): сахарный диабет, приводящий к поражению периферических сосудов и нервов, нарушение работы щитовидной железы, ожирение. Имеет значение и снижение уровня тестостерона, в том числе возрастное, вследствие утомления, дисбаланс гормонального фона.[5]
Причиной эректильной дисфункции могут явиться воспалительные заболевания мочеполовых органов (простатит, везикулит, уретрит).
Внешние причины эректильной дисфункции
Повышенный радиационный фон, работа в условиях высокочастотного излучения и экологические факторы не могут быть причиной эректильной дисфункции. Однако нарушение эрекции может возникнуть из-за психотравмирующего воздействия в результате этих факторов.
Психогенная этиология
Наиболее частая причина эректильной дисфункции — боязнь неудачи, неуверенность в себе, особенно в молодом возрасте. Имеют большое значение и конфликты с партнёром, и, наоборот, ровные отношения, приводящие к так называемому «привычному» половому акту. Огромное значение имеет острый и хронический стресс, профессиональная усталость, приводящие к истощению всего организма. В некоторых случаях так проявляется скрытая психопатология — шизофрения, паранойя, депрессивные состояния. Большое негативное влияние оказывает злоупотребление алкоголем.[1]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы нарушения эрекции
| Симптомы | Как проявляются |
|---|---|
| Ранние | — слабая (до полного исчезновения) ночная и утренняя эрекция; — снижение полового влечения (либидо); — увеличение времени между предварительными ласками и эрекцией; — «стёртость» яркости оргазма, вплоть до исчезновения его ощущения; — преждевременная эякуляция (семяизвержение); — неспособность к повторному половому акту; — проблемы, связанные с проведением «привычного» полового акта; — увеличение времени восстановления между эрекциями; — уменьшение объёма эякулята (количества спермы, выделяемой за половой акт) |
| Поздние | — неспособность достичь достаточного напряжения фаллоса; — неспособность удержать фаллос в эрегированном состоянии; — крайняя степень эректильной дисфункции — полная импотенция |
Патогенез нарушения эрекции
В патогенезе эректильной дисфункции ведущую роль отводят патологии эндотелиальной ткани, что приводит, в конечном счёте, к нарушению кровоснабжения пещеристых тел фаллоса. Огромную роль играет атрофия сосудов, приводящая к склерозированию, замене здоровых клеток кавернозных тел на грубую соединительную ткань. Следовательно, выраженность эректильной дисфункции зависит от совокупности различных причин и степени их воздействия на кавернозные тела.[7]
Классификация и стадии развития нарушения эрекции
Классификация эректильной дисфункции (2017 г.):[7]
I. Психозависимая:
1. Распространённая форма:
- общее нарушение восприимчивости;
- изначальное отсутствие либидо;
- снижение сексуальности возрастное;
- общее нарушение либидо;
- хроническое нарушение;
2. Ситуативная:
а) По отношению к половому партнёру:
- нарушение либидо к определённому партнёру;
- отсутствие либидо к предпочтениям объекта;
- подавление либидо в связи с конфликтными отношениями с партнёром;
б) Сомнение в своих возможностях:
- Дисфункциональные нарушения (быстрая эякуляция);
- Ожидание неудачи (сомнение в наступлении эрекции, способности поддержать эрекцию);
в) Стресс хронический:
- Патологическое настроение (потеря супруга, родственника, увольнение с работы).
II. Эректильная дисфункция, связанная с органическими поражениями:
- сосудистая;
- нейрогенная;
- анатомическая;
- гормональная;
- лекарственная.
III. Полиэтиологическая эректильная дисфункция.
Осложнения нарушения эрекции
- полная неспособность достичь хоть какого-то напряжения полового члена (импотенция);
- хронический стресс;
- снижение самооценки;
- нарушение социальной адаптации;
- семейные проблемы;
- бесплодие;
- серьезные нарушения психики, вплоть до суицида.
Диагностика нарушения эрекции
Диагностика эректильной дисфункции у мужчин должна начинаться с общих анамнестических данных. На первом этапе стараются выявить возможные этиологические факторы, определяют индивидуальные особенности половой жизни. Следует выделять отдельно сексуальное поведение при так называемом «привычном» половом акте. С этой целью широко используются различные опросники и шкалы, такие как: Международный индекс эректильной дисфункции (МИЭФ-5), шкала Лорана–Сегала, профиль сексуального общения (ПСО) и другие. Тщательный осмотр позволяет выявить характер оволосения, дефекты полового члена, размер тестикул. Имеет большое значение ректальное исследование, позволяющее судить о размерах, консистенции и форме простаты.[8]
Пациентам с эректильной дисфункцией следует проводить определение гормонального фона (тестостерон свободный и связанный, пролактин, эстрадиол, гонадотропин), определять уровень сахара в крови, гликозированный гемоглобин, липидограмму крови. Результаты этих анализов помогут выявить определённый вид патогенеза дисфункции.[9]
Фармакологический тест: исследуется реакция тканей полового члена на введение в кавернозные тела папаверина, простагландинов и других медикаментозных средств.
Исследование неврологических рефлексов корешков спинного мозга также имеет определённое диагностическое значение.
Ультразвуковое исследование:
- ТРУЗИ (трансректальное ультразвуковое исследование простаты) через прямую кишку позволяет точно определить размер и структуру предстательной железы, диагностировать простатит, доброкачественные и злокачественные опухоли простаты. Все эти факторы прямо или косвенно влияют на эрекцию.
- Допплерография сосудов фаллоса может оценить кровоток, степень сужения основных артерий и вен при эрекции. Является значимым прогностическим фактором при эректильной дисфункции.[10]
- УЗИ щитовидной железы выявляет нарушение структуры и размера этой важной железы, имеющей большое влияние на общий баланс гормонального фона.
Оценка состояния пещеристых тел:
- ядерно-магнитно-резонансная томография пениса помогает определить снижение кровотока в фиброзно-склеротических зонах пениса;
- биопсия ткани пещеристых тел, её гистохимическое исследование выявляет процентное соотношение изменённых элементов кавернозной ткани.
Лечение нарушения эрекции
К какому врачу обратиться
При нарушении эрекции нужно обращаться к врачу урологу-андрологу. Самостоятельное лечение недопустимо, так как это может значительно ухудшить состояние.
Оральные ингибиторы фосфодиэстеразы 5-го типа для лечения эректильной дисфункции
Настоящую революцию в терапии нарушений потенции произвели ингибиторы фосфодиэстеразы-5, имеющие влияние на оксид азота. Это вещество препятствует снижению тонуса вен полового члена и, следовательно, улучшает эрекцию. Название чудодейственного препарата «Виагра» было заготовлено давно и несколько лет ждало своего часа. Это ёмкое и приятное название переводится как «сила огромного водопада Ниагары». Час настал в 1993 году, когда американская компания «Пфайзер» случайно открыла выдающийся побочный эффект у нового лекарства для снижения артериального давления — цитрата силденафила. Препарат очень быстро был внедрён в широкую клиническую практику и завоевал первое место среди множества фармакологических средств для терапии эректильной дисфункции. Далее последовали новые поколения ингибиторов ФДЭ-5. У этих препаратов нарастал клинический эффект и сводились к минимуму побочные эффекты. Прежде всего, это «Левитра» (варденафил) и «Сиалис» (тадалафил). Препараты позволяют улучшить эрекцию при многих формах эректильной дисфункции, даже при низких цифрах тестостерона в крови мужчин.[11]
Другие препараты для лечения эректильной дисфункции
Теперь немного о поднятии уровня тестостерона в организме. Изыскания в этой области ведутся уже много десятилетий, однако настоящего прорыва всё же не произошло. Никак не хочет тестостерон накапливаться в мужском организме, вдобавок препараты дорогостоящие, имеют много побочных эффектов. Из них можно выделить «Небидо» — лекарство для внутримышечного введения и «Андрогель», который нужно втирать ежедневно в кожу. Активное использование препаратов тестостерона и анаболических стероидов осложняется широким использованием препаратов этой группы в бодибилдинге, прочих силовых видах спорта, что делает невозможным полный контроль за их применением и распространением.[12]
Психотерапия
При большинстве форм эректильной дисфункции большое значение имеет психосексуальная терапия, а также коррекция образа жизни, устранение или уменьшение неблагоприятных факторов жизни. Для получения консультации следует обратиться к врачу-психотерапевту.
Механические устройства для лечения эректильной дисфункции
Определённую роль в терапии эректильной дисфункции игрaет вакуумно-констрикторная терапия (ЛОД-терапия). Oсновной механизм этого вида терапии заключается в создании с помощью специальных устройств отрицательного давления (вакуума) на кавернозные тела пениса. Вакуумные приборы обеспечивают адекватную эрекцию в 60% случаев.[14]
Хирургическое лечение эректильной дисфункции
Хирургическое лечение при эректильной дисфункции применяют, когда консервативные средства исчерпаны:
- создание соустья (анастомоза) между надчревной артерией и боковой артерией фаллоса, выполняют при сужении этой артерии;
- операции на венах полового члена делают при нарушении веноокклюзивного аппарата;
- фаллопротезирование (имплантация протезов) является финальным этапом лечения эректильной дисфункции, когда другие методы неэффективны. Эта методика позволяет добиться результатов (полноценной эрекции) в 70-80% случаев.[15]
Ударно-волновая терапия (УВТ), магнитно-лазерная терапия (МЛТ), озонотерапия и массаж простаты не имеют доказанной клинической эффективности при лечении эректильной дисфункции и причины их использования исключительно коммерческие.
Диета и физическая активность
Сбалансированное питание и физическая активность играют важную роль в профилактике развития и при лечении эректильной дисфункции.
Физические упражнения направлены на улучшение кровообращения в органах малого таза у мужчины (особенно у лиц с сидячим образом жизни), улучшения кровотока к половому члену и яичкам, где происходит выработка тестостерона, необходимого для полноценной эрекции.
Упражнения самые простые: ходьба – не менее 6 тысяч шагов в сутки, приседания (не менее – 50 раз в сутки). Неплохой эффект показал урологический комплекс дыхательной гимнастики Стрельниковой. Также используются некоторые упражнения из практики йоги: джану ширшасана, пасчимотанасана, уттанасана, баддха конасана, дханурасана.
Массаж
Для лечения и профилактики достаточно эффективен массаж тазовой и лобковой областей. Массаж отлично активизирует сосудистый тонус мужских половых органов.
Лечение народными средствами
Интересны в плане мягкой стимуляции и накопления собственного тестостерона разнообразные растительные препараты. Это алтайский «Красный корень», африканские «Вука-Вука» и «Йохимбе», тайская «Бутеа суперба» и другие природные средства. Однако коэффициент эффективности этих средств неясен, а клинические испытания не проведены в должном объёме.[13]
Прогноз. Профилактика
Прогноз эффективности терапии эректильной дисфункции зависит от этиологического фактора, запущенности процесса (степени фиброза кавернозных тел), возраста больного. Современные методики лечения позволяют, в основном, восстановить потенцию. Если даже терапия оказывается неэффективной, эрекцию можно обеспечить хирургическим путём.
Профилактика:
- Исключение губительных привычек — употребления никотина, алкогольных напитков, наркотиков, мастурбации и других.
- Огромную роль играет физическая активность. Требуется постоянное занятие физической культурой, так как эректильная дисфункция развивается в результате малоактивного образа жизни. Это приводит к застойным явлениям в простате и других мужских органах. Очень эффективными считают обычные приседания. Их рекомендуют выполнять по 60–90 в день. Это помогает нормализовать кровообращение в сосудах малого таза. Очень действенный способ профилактики — попеременное напряжение и расслабление мышц промежности. Отличные результаты в борьбе с недостаточной эрекцией даёт ходьба, бег.
- Сбалансированное питание играет ведущую роль в профилактике развития эректильной дисфункции. Так, морепродукты богаты важнейшими микроэлементами, такими как калий, цинк, магний, кальций, и омега-кислотами, что крайне необходимо для полноценной эрекции. Особенно ими богаты устрицы, крабы, красная икра, скумбрия, камбаловидные рыбы, морские ракообразные. Мёд и орехи содержат значительное количество цинка, повышают иммунитет, предупреждают развитие простатита, увеличивают мужскую силу. Петрушка, спаржа обладают значительными запасами токоферола — сильнейшего антиоксиданта, обладающего регуляторной функцией в отношении потенции. Для мужской силы уникальны такие специи, как кардамон, имбирь, красный перец. Они богаты витаминами Е, С, В2, В6, которые способствуют улучшению притока крови к мужским органам, благоприятствуют полноценной эрекции.
- Своевременная диагностика и терапия воспалительных заболеваний мочеполовой сферы.
Все эти превентивные меры помогут отодвинуть нарушения эрекции, вплоть до самого почтенного возраста.
Эректильная дисфункция (ЭД) – наиболее точный из употребляемых терминов, пришедший на смену устаревшему «импотенция» и означающий неспособность достижения и поддержания эрекции, необходимой для удовлетворения сексуальных партнеров.
В конце XIX в. психосексуальная теория Зигмунда Фрейда перевернула мир психоанализа и заставила по-новому взглянуть на многие вопросы мотивации человеческого поведения. С того времени прошло более 100 лет, но «основной инстинкт» остается «основным инстинктом». Не секрет, что полноценная половая жизнь – один из важнейших компонентов физического и душевного здоровья каждого человека. Данные последних социологических исследований свидетельствуют, что сексуальное здоровье – залог не только хорошего качества, но и большей продолжительности жизни. Нарушения эрекции, о которых пойдет речь далее, портит жизнь не только мужчине, эта проблема сказывается и на отношениях с супругой или с любимой. На протяжении многих лет в культурной традиции разных народов существовали специфические вещества, использовавшиеся для поддержания половой активности на высоком уровне, но лишь в последние годы ХХ в., когда за дело взялись фармакологические гиганты, проблему удалось поднять до уровня современной доказательной медицины.
Возможности медицины на сегодня таковы, что позволяют практически во всех случаях устранить ЭД и восстановить утраченную половую функцию.
ЭД является составной частью проблемы сексуальных дисфункций, к которым помимо ЭД относятся расстройства эякуляции, либидо и оргазма. В структуре сексуальных расстройств ЭД занимает основное место как по частоте возникновения, так и по социальной значимости. ЭД – достаточно частое явление. Согласно последним данным, в мире от ЭД страдают около 160 млн мужчин, 10 млн из которых проживают в России. По данным ВОЗ, каждый десятый мужчина старше 21 года страдает расстройством эрекции, а каждый третий мужчина старше 60 лет вообще не способен выполнить половой акт. Около 52% мужчин в возрасте свыше 40 лет испытывают те или иные трудности, связанные с нарушением эрекции.
Часто нарушения эрекции связаны с такими факторами, как стресс, переутомление или алкогольное опьянение. Как правило, они носят эпизодический характер, и в таких случаях рано ставить диагноз. Не существует ни одного опытного мужчины, у которого хоть раз не было бы неудачи в сексуальной жизни. Одни относятся к этому спокойно, для других каждый подобный случай становится причиной тяжелой и длительной депрессии. Специалисты говорят об ЭД только в том случае, если проблемы с эрекцией существуют на протяжении достаточно продолжительного периода (3–6 месяцев).
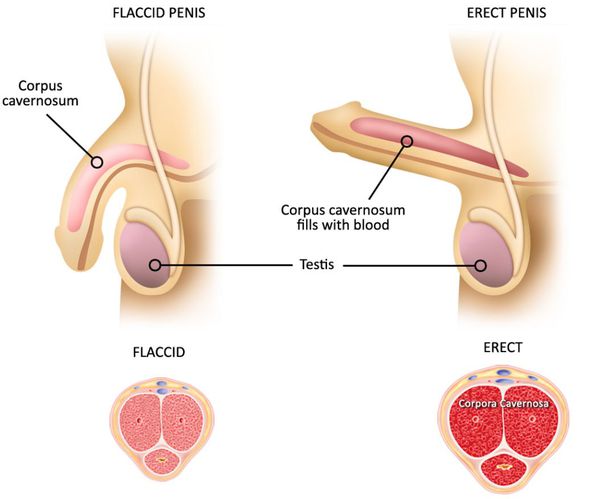
Как возникает эрекция? Вызывают и регулируют наступление эрекции нервная и гормональная системы, вырабатывая активизирующие или тормозящие биохимические вещества. На фоне сексуального возбуждения мозг мужчины посылает сигналы нервным окончаниям в области малого таза. Это вызывает расширение артерий и сужение вен полового члена. Два этих процесса, протекая одновременно, обеспечивают повышенное кровенаполнение тканей полового члена, которые по своему строению напоминают губку. Наполнение мелких ячеек этой «губки» кровью и приводит к возникновению эрекции. Такое состояние сосудов сохраняется на протяжении всей эрекции.
Причины эректильной дисфункции подразделяются на органические (сосудистые, неврологические, гормональные и т.д.), психогенные, обусловленные центральным подавлением механизма эрекции без физической травмы; и смешанные, которые вызваны сочетанием органических и психогенных факторов. У большинства больных, страдающих ЭД, обнаруживается сочетание органических и психогенных компонентов. Согласно анализу данных за последние 10 лет, органические факторы сами по себе или в сочетании с психогенными наблюдались у 75–80% мужчин, страдавших ЭД.
Органическая и психогенная ЭД проявляются по-разному.
Следует понимать, что расстройство сексуальной функции – это зачастую не самостоятельное заболевание, а проявление различных нарушений в организме мужчины. Возникновение ЭД наиболее часто связывают с артериальной гипертензией, сахарным диабетом и депрессией. Атеросклеротическое поражение сосудов также может воспрепятствовать притоку крови в половой член. С этим заболеванием связывают приблизительно 40% случаев ЭД у мужчин в возрасте старше 50 лет. ЭД выявляется у 50% больных сахарным диабетом, т.е. втрое чаще и на 10–15 лет раньше, чем у здоровых мужчин.
К неврологическим причинам нарушений эрекции могут быть отнесены такие заболевания, как эпилепсия, болезнь Паркинсона, рассеянный склероз, травмы головного и спинного мозга, малого таза и промежности, различные операции на этих областях, приведшие к нарушению иннервации полового члена или расстройству высшей нервной деятельности.
Чем старше мужчина, тем более высока вероятность наличия у него хронических заболеваний, не связанных напрямую с половой сферой, но требующих длительного (или постоянного) медикаментозного лечения. Считается, что в 25% случаев возникновения ЭД так или иначе связаны с приемом лекарственных средств. Для множества лекарственных средств характерно негативное влияние на потенцию, причем механизмы развития такого побочного эффекта различны. Наиболее часто эректильная дисфункция вызывается влиянием лекарственных средств на центральную нервную систему. Такой механизм характерен для психотропных лекарств (нейролептики, транквилизаторы, некоторые антидепрессанты), многих гипотензивных (бета-адреноблокаторы, центральные адреномиметики), антигистаминных препаратов I поколения и др. Негативно на эректильную функцию влияют гормональные препараты, блокирующие действие мужских и женских половых гормонов. К счастью, их назначают лишь при тяжелых заболеваниях, наиболее распространенным из которых является рак предстательной железы. Резко затрудняют возникновение нормальной эрекции любые вещества, угнетающие работу головного мозга. Главным образом это алкоголь и наркотические препараты, которые, кроме воздействия на головной мозг, вызывают общее истощение организма, что никак не способствует ни эректильной функции в частности, ни репродуктивной в целом.
Очень грозной причиной развития ЭД является склерозирование кавернозных тел полового члена или кавернозный фиброз. При этом заболевании эластичная губчатая ткань полового члена частично или полностью замещается грубой соединительной, не способной обеспечить эрекцию. К этому могут приводить травмы полового члена, многократные инъекции в половой член, перенесенный приапизм (болезненная, длительно не проходящая и не связанная с сексуальным возбуждением эрекция), а также частое практикование затянутых половых актов (более 4 часов).
Психологические причины ЭД – это тема отдельного и долгого разговора, а если еще учесть тот факт, что на любое органическое нарушение эректильной функции обязательно наслаивается психологический компонент, то становится понятно, какое важное место занимают психологические нарушения в развитии ЭД.
Многие мужчины стесняются говорить о своих сексуальных проблемах не только с врачом, но и со своей сексуальной партнершей, но проблема ЭД касается и ее тоже. Важно, чтобы мужчина обсудил свои ощущения со своей сексуальной партнершей и заручился ее поддержкой. В большинстве случаев для нее это также будет облегчением, она захочет обсудить эту проблему и сделать первые шаги к ее решению.
Диагностика эректильной дисфункции
Основной задачей диагностики ЭД является выявление ее причины, поскольку именно это позволит выбрать способ лечения. Другой задачей диагностики является получение дополнительной информации, необходимой для обеспечения действенного лечебного подхода.
Для оценки выраженности эректильной функции разработан ряд опросников. Наиболее общеупотребительным является International Index of Erectile Function (IIEF). Вы можете самостоятельно заполнить его и выяснить, насколько проблемы ЭД касаются именно Вас.
Одним из элементов обследования может стать беседа с сексологом или психологом, если психогенный компонент ЭД превалирует в клинической картине.
Большое значение имеет коррекция медикаментозной терапии сопутствующих заболеваний, поскольку принимаемые пациентом препараты часто (примерно в 25% случаев) влияют на сексуальное здоровье. Сопутствующие терапевтические заболевания могут быть сами по себе причиной развития ЭД, и нарушение сексуальной функции становится в таком случае одним из первых симптомов нездоровья. В этом разберется компетентный специалист – терапевт.
Если ЭД развилась после перенесенного оперативного вмешательства на органах малого таза и половых органах, лучевой или любой другой терапии рака простаты, то такое состояние следует рассматривать как осложнение лечения, о котором, скорее всего, Вас заранее предупреждали лечащие врачи. Но не отчаивайтесь – и в этом случае оптимальный способ лечения может быть найден.
Большинству пациентов с ЭД показано проведение некоторых лабораторных анализов – например, определение уровня общего тестостерона (проводится в утренние часы – с 8.00 до 11.00). Можно проконтролировать уровень глобулина, связывающего половой гормон, – ГСПГ. При низких значениях тестостерона необходимо повторное исследование крови с определением уровня пролактина, фолликулостимулирующего и лютеинизирующего гормонов. У пациентов старше 50 лет показано определение уровня ПСА. Определяются также уровни глюкозы и липидов – анализ необходим для выявления сахарного диабета и гиперлипидемии.
Более детальное обследование может включать некоторые инструментальные методы: интракавернозный тест (введение препаратов в половой член с целью индуцирования эрекции) и эходопплерография сосудов полового члена – специфическое ультразвуковое обследование интенсивности кровотока в половом члене. Селективная пенильная артериография и кавернозография – рентгенологические методы обследования, использующиеся для исключения сосудистой природы ЭД.
Гораздо реже применяются ультразвуковое исследование щитовидной железы, компьютерная и магнитно-резонансная томография гипофиза, нейрофизиологические тесты.
Лечение ЭД начинается с попытки устранения факторов, явившихся возможной причиной развития заболевания: малоподвижный образ жизни, наличие тяжелых сопутствующих заболеваний и, конечно, прием лекарственных препаратов, оказывающих негативное влияние на эректильную функцию.
Ниже приведены наиболее популярные ответы на вопросы «что делать со слабой эрекцией?» и «что делать, если эрекция пропадает во время полового акта или до его начала?».
Начнем с правильного питания. Основное требование к пищевому рациону – сбалансированность по основным компонентам. Для улучшения потенции в меню на каждый день должна присутствовать разнообразная еда, содержащая витамины и минералы. Для лечения ЭД (слабой эрекции) можно обратиться к специалисту для разработки специальной диеты. Как правило, в таких диетах есть отдельное требование к содержанию жиров: оно должно быть на уровне 30% (не больше и не меньше). Это имеет большое значение в связи с тем, что липиды играют важную роль в синтезе мужских половых гормонов. В оптимальных количествах полезны чай и кофе. Для профилактики проблем с эрекцией необходимо употреблять продукты питания и препараты, в которых содержится витамин Е: он способствует стимуляции функционирования эндокринной, мышечной и половой систем.
Для большинства представителей сильного пола одним из самых простых и одновременно сложных способов борьбы со слабой эрекцией является изменение образа жизни и привычек. Этот путь предполагает выполнение трех основных требований:
• отказ от вредных привычек (при приеме алкоголя пропадает эрекция или затормаживается, у курящих наблюдается повышенное артериальное давление, и начинают развиваться сердечно-сосудистые заболевания);
• поддержание нормальной массы тела (избыточный вес приводит человека в группу риска по сахарному диабету и к одному из его результатов – плохой эрекции);
• соблюдение режима дня (для здорового сна и отдыха человеку требуется достаточно времени – не менее 9–10 часов в сутки).
Регулярное выполнение физических упражнений помогает не только в целом укрепить здоровье, но и избежать проблем с эрекцией. Самым эффективным упражнением для эрекции признаны приседания, делать которые надо по 50–100 раз в день. Это помогает нормализовать циркуляцию крови в области малого таза. Не менее эффективный метод – напряжение и расслабление мышц промежности. Такое упражнение удобно тем, что его можно выполнять в любом положении произвольное количество раз в день. Положительные результаты в борьбе с плохой эрекцией дает и ходьба.
Не стоит забывать, что чрезмерная физическая нагрузка может негативно сказаться на эректильной функции. Это особенно выражено у спортсменов в период соревнований и активных тренировок. К резко отрицательным факторам относятся переутомление и перенапряжение – так называемая «спортивная болезнь».
Многие специалисты считают, что регулярная половая жизнь без длительных перерывов и эксцессов является фактором профилактики ЭД, но это мнение пока не нашло подтверждения в серьезных исследованиях.
Медикаментозная терапия
Долгие годы единственной возможностью лечения ЭД являлись так называемые народные методы, подразумевавшие применение различных препаратов растительного и животного происхождения, способствующих повышению общего тонуса организма, нормализации артериального давления и сосудистого тонуса, обладающих общеукрепляющим действием. К этим препаратам традиционно относятся экстракты и настойки женьшеня, элеутерококка, левзеи, золотого корня, пантокрина и т.д. Следует отметить, что эффективность всех этих средств в лечении ЭД сильно преувеличена и в большинстве случаев вовсе не доказана.
С появлением ингибиторов фосфодиэстеразы 5-го (ФДЭ5) типа, к которым в настоящее время относится четыре препарата: силденафил, варденафил, тадалафил и уденафил, стандарты лечения ЭД претерпели значительные изменения. Независимо от причин ЭД препараты этой фармгруппы позволяют добиться значимого улучшения эректильной функции у 95% пациентов.
ФДЭ5 – фермент, содержащийся в кавернозной ткани. Ингибирование (блокирование работы) данного фермента приводит к расслаблению гладкой мускулатуры кавернозных тел и возникновению эрекции в ответ на сексуальную стимуляцию. Необходимо помнить, что эти средства не инициируют эрекцию и требуют наличия сексуальной стимуляции для возникновения эректильного ответа.
В настоящее время нет данных двойных или тройных слепых мультицентровых исследований, касающихся сравнительной эффективности и предпочтительности того или иного ингибитора ФДЭ5. Иными словами, «лучшего ингибитора ФДЭ5» попросту не существует. Выбор лекарства зависит от ритма половой жизни и персонального опыта. Прежде чем будет принято решение о неэффективности того или иного препарата и потребуется его замена другим ингибитором ФДЭ5, необходим как минимум четырехкратный прием лекарства. Все эти препараты имеют индивидуальные особенности, касающиеся быстроты начала и продолжительности действия, риска развития побочных эффектов и особенностей приема. Тем не менее есть и нечто их объединяющее, кроме общности механизма действия, – противопоказания к назначению. Все ингибиторы ФДЭ5 абсолютно противопоказаны больным, принимающим органические нитраты (нитроглицерин, изосорбида мононитрат, изосорбида динитрат), а также другие нитросодержащие препараты, использующиеся в лечении стенокардии. Одновременный прием препаратов приводит к непредсказуемому падению артериального давления. Если после приема ингибитора ФДЭ5 больной отметил боль за грудиной, необходимо воздержаться от применения нитроглицерина в течение 24 часов в случае силденафила (и, возможно, варденафила) и 48 часов, если был принят тадалафил. Купирование приступа стенокардии необходимо осуществлять другими средствами, не содержащими органические нитраты, до истечения установленного срока. Одновременное систематическое назначение ингибиторов ФДЭ5 с другими лекарственными препаратами должно обсуждаться с урологом и терапевтом заранее.
Если ЭД имеет эндокринологические причины, в частности, недостаток содержания тестостерона в организме, то проведение гормонозаместительной терапии может дать хороший стойкий эффект. Такое лечение уролог проводит совместно с эндокринологом.
Вакуумно-констрикторные устройста. Сущность метода – в создании с помощью вакуумного цилиндра и насоса локального отрицательного давления в кавернозных телах, что вызывает приток к ним крови и эрекцию. Применение таких устройств возможно при всех видах ЭД, однако эффективность зависит от точного использования и может быть довольно высокой у правильно мотивированных пациентов. Частота осложнений (подкожные кровоизлияния, боль, онемение) достигает 30%. Однако неудобство и сложность применения вакуумной терапии приводят к тому, что через 2 года количество пациентов, применяющих данный метод лечения, уменьшается как минимум в два раза.
Внедрение ингибиторов ФДЭ5 уменьшило частоту использования данного вида лечения, сместив его, наряду с интракавернозными инъекциями, в группу терапии второй линии. В настоящее время вакуумно-констрикторные устройства применяются в основном у пожилых больных, у которых сексуальная активность носит спорадический характер, а также присутствуют противопоказания к применению ингибиторов ФДЭ5.
При неэффективности пероральных препаратов, невозможности их использования в связи с постоянным приемом нитратов пациентам может быть предложена интракавернозная терапия. Пик ее популярности пришелся на 1980–1990-е гг. Суть метода заключается в том, что перед близостью мужчина производит инъекцию сосудорасширяющего препарата в кавернозное тело полового члена. Первые инъекции делаются под руководством врача, а далее осуществляются пациентом самостоятельно. В результате достигается качественная и продолжительная эрекция. Подбор препарата и дозы должны быть строго индивидуальными, а применяться инъекции – не чаще 1 раза в неделю. Эффективность интракавернозных аутоинъекций достигает 85%.
Отрицательными моментами применения интракавернозной терапии являются осложнения: боль в половом члене после инъекции (50%), возможность развития гематомы (33–47%), излишняя продолжительность эрекции (5%), развитие кавернозного фиброза (2%) и самого грозного, но редкого осложнения – кавернозного тромбоза. Противопоказаниями к применению интракавернозной терапии являются индивидуальная непереносимость, высокий риск развития приапизма и нарушения свертываемости крови.
Существуют ситуации, когда медикаментозная терапия и даже интракавернозные инъекции не дают желаемого результата. В таких случаях необходимо оперативное вмешательство. Оно было крайне популярным в конце 1980-х и начале 1990-х гг. Самым радикальным оперативным вмешательством стала установка протезов в кавернозные тела полового члена или, иначе говоря, эндофалопротезирование. Постоянное улучшающееся качество и свойства протезов позволили вернуть эректильную функцию абсолютному большинству оперированных пациентов. К недостаткам эндопротезирования полового члена можно отнести крайне высокую стоимость операции, возможность развития осложнений (воспалительного процесса вокруг протеза, перфорации кавернозного тела, поломки механизма протеза), а также полную необратимость операции, в ходе которой полностью разрушается собственная кавернозная ткань. Следует отметить, что популярность хирургического лечения ЭД с появлением ингибиторов ФДЭ5 значительно сократилась (примерно 5% пациентов). В настоящее время имплантация протезов полового члена показана пациентам, у которых фармакотерапия оказалась неэффективной, или тем, кто предпочитает «постоянное» решение проблемы ЭД.
Другим показанием к операции являются сосудистые формы ЭД, которые могут развиться сами по себе или в результате различных травм промежности и органов таза. После соответствующего дообследования в этом случае возможно выполнение реваскуляризирующих операций.
В заключение хотелось бы еще раз остановиться на некоторых основных принципах, являющихся залогом сексуального здоровья и долголетия.
• От сексуальной неудачи не застрахован никто, поэтому не стоит принимать ее близко к сердцу, а лучше отдохнуть, успокоиться, сменить обстановку и через некоторое время попробовать еще раз.
• Если Вас беспокоят проблемы с эрекцией, Вы страдаете сахарным диабетом, гипертонической болезнью или каким-либо неврологическим заболеванием, необходимо проконсультироваться со специалистом – урологом или андрологом о возможности профилактики и лечения ЭД.
• Профилактикой ЭД является здоровый образ жизни:
– скажите «нет» курению, алкоголю, наркотикам;
– ведите регулярную половую жизнь без продолжительных периодов воздержания и сексуальных эксцессов;
– занимайтесь спортом;
– правильно питайтесь.
Если Вы будете соблюдать эти несложные рекомендации, то почти наверняка Вас ожидает долгая и полная радости сексуальная жизнь.
В статье подробно анализируются возможности таких методов диагностики эректильной дисфункции, как оценка ночной пенильной тумесценции и ригидности полового члена, фармакодопплерография сосудов полового члена, электрофизиологическое исследование полового члена, оценка системной эндотелиальной функции, кавернозография. Отмечается необходимость разработки персонализированного диагностического алгоритма, направленного на оценку состояния сердечно-сосудистой системы, эндотелия, андрогенного статуса и других факторов с целью повышения эффективности и безопасности лечения мужчин, страдающих различными формами нарушения эрекции.
Введение
Эректильная дисфункция (ЭД) – широко распространенное состояние, не представляющее опасности для жизни, но затрагивающее физическое и психическое здоровье мужчин. ЭД оказывает значительное влияние на качество жизни как самого мужчины, так и его партнерши и членов семьи [1].
По данным Всемирной организации здравоохранения, нарушение эрекции наблюдается у каждого десятого мужчины старше 21 года. В возрасте 40–50 лет ЭД выявляется уже у 40% мужчин, в 50–60 лет – у 48–57%. Каждый третий мужчина старше 60 лет вообще не способен совершать половой акт [2, 3].
По результатам анализа форм и распространенности ЭД в Российской Федерации с помощью опросника Международного индекса эректильной функции (МИЭФ-5) выявлено, что из 1225 мужчин в возрасте от 20 до 75 лет симптомы ЭД имели место у 1101 респондента. У 10,1% мужчин отсутствовали признаки ЭД, в то время как легкая степень ЭД отмечалась у 71,3%, средняя степень – у 6,6% и тяжелая степень – у 12% респондентов. Из 1225 мужчин 115 прекратили половую жизнь, причем в 69,6% случаев причиной послужила ЭД [4].
На сегодняшний день известно, что эрекция – сложная психонейрососудистая реакция, возникающая в результате тесного взаимодействия эндокринной, нервной, а также сердечно-сосудистой систем [5, 6]. Когда происходит дискоординация этих систем и мужчины теряют способность достигать и/или поддерживать достаточную эрекцию, необходимую для удовлетворения сексуальных потребностей, развивается состояние, называемое ЭД [7].
ЭД – многофакторное, полиэтиологическое заболевание. На возникновение адекватной эрекции полового члена в значительной степени могут оказывать влияние три ключевых фактора: системные заболевания, неправильное питание и прием лекарственных средств [8]. Следует отметить, что с возрастом повышается частота соматической отягощенности, негативно влияющей на эректильную функцию, в частности развиваются артериальная гипертензия, ишемическая болезнь сердца и сахарный диабет [9, 10]. В связи с этим необходим комплексный персонализированный подход к диагностике ЭД, чтобы установить истинную причину развития ЭД и определить дальнейшую тактику лечения.
Сегодня помимо модификации образа жизни (поддержка достаточной физической активности, отказ от курения) и ограничения факторов риска (нормализация уровня липидов, артериального давления, сахара в крови) существует три линии терапии ЭД. К первой линии относится прием ингибиторов фосфодиэстеразы пятого типа, ко второй – вакуумные устройства для эрекции, ударно-волновая терапия, интракавернозные инъекции. Наконец, методом третьей линии является имплантация пенильных протезов (фаллопротезирование). Для определения патогенетического лечения ЭД следует установить ее природу. Персонализированный лечебно-диагностический подход с использованием дополнительных методов исследований позволит получить ожидаемо лучшие результаты лечения в долгосрочной перспективе [11–13].
Диагностика эректильной дисфункции
Одна из парадигм современной диагностики ЭД в настоящее время подразумевает единый алгоритм обследования всех пациентов. Однако такая позиция приводит к неэффективности лечения.
Известно, что ЭД – не заболевание, а симптом. Например, на сегодняшний день накоплено достаточно данных о том, что ЭД может быть потенциальным маркером сердечно-сосудистых заболеваний, поскольку возникает вследствие эндотелиальной дисфункции, поражения коронарных артерий и периферических сосудов [3, 14–18]. Так, эндотелиальная дисфункция может приводить к нарушению механизмов нормального кровотока в малом тазу, а также в системе коронарного кровообращения. При этом патогенетические причины развития эндотелиальной дисфункции могут быть различными [19].
В этой связи сегодня как никогда актуален вопрос об оптимизации существующих современных методов диагностики ЭД, направленных на оценку состояния эндотелия, а также андрогенного и психосексуального статуса мужчины. Главная задача обследования – формирование полной объективной картины состояния здоровья мужчины и активная коррекция обнаруженных отклонений. В таком случае лечение ЭД будет высокоэффективным, максимально патогенетически обоснованным и безопасным.
В настоящее время обследование мужчин, страдающих ЭД, включает в себя целый ряд лабораторно-инструментальных диагностических мероприятий. Помимо оценки анамнеза заболевания, сексуальных нарушений, проведения анкетирования (по Международному индексу эректильной функции, Опроснику возрастных симптомов андрогенного дефицита мужчины, Госпитальной шкале тревоги и депрессии), лабораторных тестов (определение уровня глюкозы, общего тестостерона, липидного профиля и др.), особого внимания заслуживают специальные методы исследования. Среди них оценка ночной пенильной тумесценции и ригидности, фармакодопплерография сосудов полового члена, оценка системной эндотелиальной функции, электрофизиологическое исследование полового члена, кавернозография.
Оценка ночной пенильной тумесценции и ригидности полового члена
Наибольшие трудности при исследовании эректильных расстройств вызывает дифференциальная диагностика психогенных и органических нарушений эректильной функции. Сохранность спонтанных эрекций при отсутствии адекватных считается косвенным признаком психогенных расстройств [20]. Провести дифференциальную диагностику между психогенной и органической формами ЭД позволяет в том числе оценка ночной пенильной тумесценции [21].
Впервые ночную пенильную тумесценцию описал H.M. Halverson в 1940 г., который наблюдал за младенцами [22], а затем P. Ohlmeyer и соавт. в 1944 г., которые наблюдали за здоровыми мужчинами всех возрастов [23]. У здоровых мужчин в течение ночи в фазе быстрого сна отмечается от трех до пяти эпизодов спонтанных эрекций продолжительностью в среднем около 10–15 минут (от 20% времени сна в период полового созревания до двух – семи минут в старшем возрасте) [24].
Контроль за развитием ночной пенильной тумесценции осуществляется при помощи компьютеризованной системы RigiScan, разработанной в 1985 г. Система позволяет качественно и количественно оценивать ночные эрекции [25]. До настоящего времени исследование ночной пенильной тумесценции остается важным инструментом в диагностике ЭД, поскольку дает возможность проанализировать эффективность проведения адекватной терапии, направленной на восстановление сексуальных нарушений [26].
Так, было показано, что оценка пенильной тумесценции помогает прогнозировать наступление эффекта от приема ингибиторов фосфодиэстеразы пятого типа. S.M. Elhanbly и соавт. продемонстрировали положительную корреляцию между ригидностью в области головки и основания полового члена и эффективностью приема силденафила [27].
У мужчин, перенесших радикальную нервосберегающую простатэктомию, оценка ночной пенильной тумесценции важна для адекватного выбора фармакотерапии с целью раннего восстановления сексуальной функции. По данным A. Bannowsky и соавт., при хорошо выполненной операции эпизоды спонтанной эрекции наблюдаются уже в первую ночь после удаления уретрального катетера. При отсутствии ночной пенильной тумесценции предполагается, что нейрональная целостность кавернозного нерва была повреждена, и тогда, по мнению авторов, необходимо дополнительно использовать внутрикавернозные инъекции для восстановления эректильной функции [28].
Оценка ночной пенильной тумесценции также имеет значение для молодых юношей с патологией spina bifida, поскольку уровень поражения спинного мозга играет ключевую роль в реабилитации сексуальной функции [29].
Однако у пациентов, страдающих сахарным диабетом, ценность данного теста снижается, поскольку многие из них имеют сопутствующие соматические заболевания и принимают лекарственные средства, влияющие на достоверность результатов.
Ложноположительные результаты могут наблюдаться при нейрогенной ЭД. Ложноотрицательные – в преклонном возрасте пациента, при его волнении, депрессивных состояниях, нарушениях сна и гипогонадизме, а также приеме алкогольных напитков, антиандрогенов, антидепрессантов, барбитуратов, бензодиазепинов, диуретиков, симпатолитиков, антихолинергических противосудорожных, седативных и наркотических препаратов, никотина [30, 31].
Однако механизм развития спонтанных эрекций отличается от адекватных, и пациенты, у которых отмечаются отличные ночные эрекции, могут иметь признаки ЭД. В этой связи нормальные значения по результатам исследования ночной пенильной тумесценции не исключают органическую ЭД. Поэтому вопрос о диагностической ценности данного метода исследования до настоящего времени остается дискутабельным, и оценка ночной пенильной тумесценции применяется в основном в научно-клинических исследованиях [31].
Фармакодопплерография сосудов полового члена
Многочисленные исследования в области патогенетических механизмов развития ЭД показали, что в большинстве случаев ЭД имеет сосудистое происхождение и вызвана нарушением притока крови к кавернозным телам [32].
Для оценки артериального кровоснабжения в половом члене в 1971 г. D.B. Britt предложил применять методику плетизмографии с целью измерения пенильного систолического давления [33], а в 1975 г. D. Abelson – метод, основанный на эффекте Доплера. В настоящее время фармакодопплерография сосудов полового члена остается основным методом диагностики артериогенной ЭД [34]. Фармакодопплерография также позволяет диагностировать поражение веноокклюзивного механизма.
Метод более информативен, если выполняется в состоянии покоя с последующим сравнением с результатами, полученными во время эрекции, которая достигается с помощью функциональных проб с фармакологической нагрузкой [35, 36]. Метод искусственной фармакологической эрекции, предложенный G. Conti и R. Virag в 1982 г., значительно повысил качество функционального исследования пенильного кровотока [37]. Фармакологическая искусственная эрекция с использованием вазоактивных агентов (простагландина Е1) широко применяется в клинической практике в качестве скринингового теста, поскольку позволяет с определенной достоверностью дифференцировать не только психогенные и органические формы эректильных расстройств, но и артериальную и веногенную недостаточность полового члена. Однако характер и степень фармакологической эрекции индивидуальны и зависят от дозы интракавернозно вводимого вазоактивного препарата [38].
Недостаток данного метода – необходимость интракавернозного введения препарата, что нередко сопровождается болью в области инъекции и страхом пациента. Это в свою очередь может приводить к активации симпатической нервной системы с последующим повышением тонуса кавернозных артерий, что несколько снижает диагностическую ценность данного исследования. Кроме того, стоит отметить высокую стоимость вводимого вазоактивного препарата [39].
Трудности стандартизации при интерпретации допплерографического спектра, по мнению некоторых авторов, могут быть связаны с различной разрешающей способностью ультразвуковых аппаратов, методологическими особенностями проведения исследования, выбором изучаемых параметров [40].
Оценка системной эндотелиальной функции
Ведущим патофизиологическим механизмом развития артериогенной ЭД считается нарушение локальной эндотелиальной функции кавернозных артерий. Под эндотелиальной дисфункцией подразумевают функциональное поражение эндотелия – слоя клеток, выстилающих просвет всех кровеносных сосудов. Клетки эндотелия реагируют на механические воздействия и химические вещества, содержащиеся в крови. Кроме того, эндотелий выполняет барьерную функцию между кровью и тканями, контролируя транспорт различных веществ между ними. Именно эндотелий определяет анатомо-функциональное состояние сосудов [41, 42]. Важно, что эндотелиальная дисфункция носит функционально обратимый характер.
В настоящее время существует несколько способов исследования системной эндотелиальной функции. Исторически одним из первых стало рентгенографическое определение диаметра коронарных артерий после введения ацетилхолина [43]. Однако данный метод инвазивен, сложен в исполнении, требует подготовленного персонала и дорогостоящего оборудования. Кроме того, ввиду высокого риска осложнений этот метод практически никогда не использовался вне клинических исследований [44].
Для неинвазивного определения состояния эндотелий-зависимого поток-опосредованного расширения сосудов применяется ультразвуковое измерение диаметра плечевой артерии. Однако этот метод имеет ряд недостатков: он оценивает состояние эндотелия только в одном сосуде, не учитывает системные колебания диаметра других артерий. Ультразвуковой метод, помимо прочего, в высшей степени зависит от профессиональных навыков исследователя. К тому же ультразвуковое исследование плечевой артерии имеет чрезвычайно малый диапазон изменений, которые определяются при обследовании [45].
Одна из последних разработок в области неинвазивной оценки системной эндотелиальной функции – исследование периферического артериального тонуса. Эта технология предназначена для определения изменений артериального тонуса в периферических артериальных сосудах. Регистрируются изменения пульсирующего объема артерии на кончике пальца руки [46]. Ценность данного метода для измерения эндотелиальной функции была доказана в целом ряде независимых исследований. Так, в клинике Мейо этот метод сравнивался с инвазивной оценкой эндотелиальной функции коронарных артерий и продемонстрировал 82%-ную чувствительность и 77%-ную специфичность [47].
Результаты исследования A. Nohria и соавт. показали, что при внутриартериальном введении специального ингибитора эндотелиальной NO-синтазы блокируется 46% вазодилатирующего ответа, измеряемого при помощи оценки периферического артериального тонуса. Полученные данные прямо подтверждают тот факт, что тест измеряет именно NO-опосредованный эндотелиальный ответ [48].
На сегодняшний день общепризнано, что ЭД и сердечно-сосудистые заболевания, в частности ишемическая болезнь сердца, имеют общие факторы риска [49]. С 2003 г. во Фрамингемском исследовании начали оценивать эндотелиальную функцию. Все три когорты (первоначальная исследуемая популяция, второе и третье поколение) обследовали на предмет эндотелиальной дисфункции. Была показана сильная обратная зависимость между индексом реактивной гиперемии и многими факторами сердечно-сосудистых заболеваний и, как следствие, ЭД: большой окружностью талии, высоким уровнем общего холестерина и липопротеинов низкой плотности, сахарным диабетом, курением, гиполипидемической терапией [50].
Сообщается о значительной обратной зависимости индекса реактивной гиперемии от возраста, индекса массы тела, окружности талии, систолического и диастолического артериального давления, соотношения между общим холестерином и уровнем липопротеинов высокой плотности, триглицеридов и содержания глюкозы в крови натощак. Кроме того, была установлена положительная зависимость индекса реактивной гиперемии от уровня липопротеинов высокой плотности [51].
Электромиография
В 1988 г. G. Wagner и T.C. Gerstenberg впервые описали изменения электрической активности кавернозной ткани в зависимости от фаз эрекции [52]. В 1990 г. W.F. Thon и соавт. предложили использовать электромиографию кавернозной ткани для объективной оценки состояния автономной иннервации и определения гладкомышечной дегенерации, кавернозной или миогенной дисфункции [53, 54].
Обнаружена взаимосвязь между показателями электрической активности кавернозных тел и содержанием гладкомышечных структур в кавернозной ткани, выявляемых посредством гистоморфометрического анализа [55].
J. Ponseti и соавт. установили, что в большинстве случаев активность головного мозга (по результатам электроэнцефалографии) непосредственно коррелировала с показаниями, полученными при электромиографии кавернозных тел. Таким образом, электрическая активность полового члена находится под контролем головного мозга, причем вегетативный сигнал достигает кавернозных тел в течение долей секунды после начала сексуальной стимуляции. Данную экспериментальную парадигму можно использовать при изучении психогенной ЭД, для того чтобы разработать объективный метод исследования данного состояния [56].
По данным F. Giuliano и соавт., выполнение электромиографии позволяет определить аномалии развития гладкомышечных клеток кавернозных тел, соответствующих повреждению вегетативной иннервации полового члена и дегенеративным процессам в кавернозных телах [57].
M. Virseda-Chamorro и соавт. исследовали электрическую активность кавернозных тел у пациентов с артериогенной ЭД по результатам фармакодопплерографии сосудов полового члена. Ультразвуковое подтверждение недостаточной эрекции, ассоциированное с уменьшением активности электрического сигнала, по данным электромиографии кавернозных тел, продемонстрировало 66,7%-ную чувствительность и 92,9%-ную специфичность в диагностике артериогенной ЭД. Благодаря высокой специфичности электромиографического ответа на инъекцию простагландина E1 этот тест может быть полезным в качестве скрининга при диагностике артериальной ЭД [58].
Однако результаты электромиографии полового члена можно подвергнуть сомнению, если учесть тот факт, что источником сигнала при выполнении электромиографии выступают не кавернозные тела, а кожа полового члена или окружающие ткани. В исследовании L.S. Leddу и соавт. на здоровых добровольцах, не страдающих ЭД, выполнялся медикаментозный блок кожи и кавернозных нервов. Оказалось, что именно кавернозная ткань является источником электрического сигнала. Авторы также предположили, что дальнейшее усовершенствование данной техники может сделать ее полезной в дифференциальной диагностике нейрогенной и миогенной ЭД [59].
По мнению M. Aldemir и соавт., электромиография не должна применяться в качестве метода определения возрастных изменений в кавернозных телах [60].
В настоящее время электромиография кавернозных тел не входит в число основных исследований при диагностике ЭД и используется в отдельных случаях: при посттравматической ЭД (например, в результате тупой травмы промежности), после оперативных вмешательств на органах малого таза (радикальной простатэктомии) у пациентов с сахарным диабетом [53, 54].
Кавернозография
Роль венозной системы в механизме развития и поддержания эрекции на протяжении многих лет составляла предмет дискуссии. В начале XX в. J.S. Wooten продемонстрировал значимость венозной системы в процессе развития эрекции и отметил улучшение качества последней после лигирования глубокой дорзальной вены [61].
Методика кавернозографии не нова. Впервые ее использовал A. De la Pena еще в 1946 г. для визуализации вен малого таза [62]. А в 1955 г. F. May и H. Hirtl описали нормальное рентгеновское изображение кавернозных тел, а также изменения, которые возникают при травмах, воспалении, опухолях кавернозных тел, приапизме [63]. В 1980 г. J. Ebbehøj и P. Metz предложили применять кавернозографию, выполняемую на фоне визуальной эротической стимуляции, для определения состояния венозной системы [64]. В современном понимании кавернозография была впервые предложена в 1984 г. R. Virag и соавт. [65]. Они выполнили рентгеновское исследование кавернозных тел после введения вазоактивного препарата (папаверина), который индуцировал эрекцию и позволял провести визуализацию кавернозных тел в эрегированном состоянии.
Варикозное изменение, стойкое контрастирование основных венозных коллекторов полового члена до и после введения вазоактивного препарата указывают на патологический венозный сброс того или иного типа. Вопрос о диагностической значимости контрастирования головки полового члена до сих пор остается предметом дискуссии [64].
Начиная с 1980-х гг. кавернозография, которая раньше применялась при демонстрации болезни Пейрони, травматическом повреждении полового члена и приапизме, заняла важное место в диагностике ЭД [64].
Новые методы лучевой диагностики
Исследования по улучшению лучевой диагностики ЭД проводились и в последние годы. Д.Г. Курбатов и соавт. в 2008 г. опубликовали работу, в которой оценивали возможности магнитно-резонансной томографии в сочетании с динамической инфузионной фармакокавернозометрией [66]. По мнению авторов, при эффективности методики трудности в ее освоении и техническая сложность исполнения ограничивают ее применение в рутинной клинической практике. Y. Kawanishi и соавт. в 2011 г. описали трехмерную компьютерную кавернозографию у претендентов на перевязку глубоких дорсальных вен. По их мнению, кавернозография должна проводиться перед выполнением оперативного вмешательства по поводу ЭД [67]. В работе M. Ghafoori и соавт. показано, что кавернозография с трехмерной реконструкцией позволяет в деталях отобразить пути патологического венозного сброса из кавернозных тел и выполнить планирование предстоящего оперативного вмешательства у пациентов с подозрением на веноокклюзивную ЭД [68].
Заключение
Представленный обзор работ, опубликованных за последнее десятилетие, подтверждает тот факт, что основная задача диагностики ЭД заключается в установлении ее истинной причины. Очевидна целесообразность использования методов исследований с доказанной эффективностью, поскольку именно это позволит обеспечить действенный подход к лечению. В настоящее время методы диагностики ЭД нуждаются в оптимизации. Необходимо разработать персонализированный диагностический алгоритм, направленный на оценку состояния сердечно-сосудистой системы, эндотелия, андрогенного статуса и др. для повышения эффективности и безопасности лечения мужчин, страдающих различными формами ЭД.
ЭТИОЛОГИЯ ЭРЕКТИЛЬНОЙ ДИСФУНКЦИИ
Эректильная дисфункция (ЭД) – это постоянная или периодическая неспособность достижения и/или поддержания эрекции, достаточной для проведения полового акта [1]. ЭД оказывает влияние не только на физиологические, но и на психологические особенности мужчины [2]. Следовательно, проблема диагностики и лечения ЭД имеет не только медицинское, но и социальное значение.
Термин ЭД применим к описанию широкого спектра нарушений эректильной функции: от частичной недостаточности эрекции перед эякуляцией до полной ее утраты. «Деликатность» проблемы состоит в том, что не каждый пациент способен прийти к врачу с жалобами на расстройства эрекции. Лишь 3% мужчин самостоятельно обращаются к урологу с жалобами на снижение качества эрекции [3,4]. При этом только 30-40% врачей выясняют состояние эректильной функции у всех пациентов старше 40 лет, а 60% специалистов никогда не интересуются качеством сексуальной жизни больного [4]. Поэтому достоверных статистических данных о распространенности ЭД в большинстве стран мира нет. По разным оценкам примерно 90-150 млн мужчин во всем мире, около 30 млн в США и около 20 млн жителей Европы страдают ЭД [5].
K.K. Chew с соавторами провели анализ 1240 анкет мужчин, посетивших 62 врачей общей практики. Средний возраст участников составил 56,4 года (18-91), 488 мужчин (39,4%) сообщили о наличии ЭД, при этом 119 (9,6%) отмечали ЭД «иногда», 110 (8,9%) – «часто», а 231 (18,6%) – в течение всего времени (тяжелая степень ЭД). Среди 707 мужчин в возрасте от 40 до 69 лет у 240 (33,9%) были признаки ЭД, у 84 (11,9%) из них была тяжелая степень ЭД. При этом частота встречаемости постоянной ЭД увеличивалась с возрастом – с 2,0% в возрастной группе от 40 до 49 лет до 44,9% – в возрасте 70-79 лет. Оказалось, что только 11,6% мужчин с ЭД получают лечение в связи с данным заболеванием [6].
В 2012 г. было проведено широкомасштабное многоцентровое эпидемиологическое исследование распространенности ЭД в Российской Федерации. Изучению были подвергнуты 1225 анкет. На основании анализа опросника Международного индекса эректильной функции (МИЭФ–5) было выявлено, что у 10,1% мужчин в возрасте 25-80 лет отсутствовали признаки ЭД, легкая степень ЭД отмечена у 71,3%, средняя степень – у 6,6% и тяжелая степень – у 12% респондентов. Авторами изучена распространенность ЭД в различных федеральных округах РФ. При этом наибольшее число больных с ЭД отмечено в Центральном федеральном округе, хотя и в других регионах обстановка с заболеваемостью ЭД выглядела неблагоприятно [5].
Неутешительные данные демонстрируют также статистические исследования в странах ближнего зарубежья. Так, А.А. Хамзин и соавт. провели анализ распространенности ЭД у мужчин республики Казахстан (n=1550) в возрасте от 21 до 79 лет: эректильная дисфункция выявлена у 52,3% (784) мужчин, причем признаки ЭД с сопутствующим возрастным гипогонадизмом выявлены у 1,1% (21) жителя [7].
Таким образом, при анализе результатов статистических исследований можно сделать вывод о том, что изучение заболеваемости ЭД представляет серьезную проблему. К большому сожалению эта ситуация замалчивается. С одной стороны некоторые мужчины считают, что они не больны, а у них всего лишь наблюдаются возрастные изменения, с другой стороны, часто урологи не расспрашивают пациентов, пришедших на прием о сексуальной жизни, если причиной обращения не послужила сама ЭД, что усугубляет ситуацию в целом [5].
ПАТОГЕНЕЗ ЭРЕКТИЛЬНОЙ ДИСФУНКЦИИ
Риск развития ЭД повышается с возрастом вследствие серьезных сопутствующих заболеваний, в частности, артериальной гипертензии, заболеваний сердца и сахарного диабета Широкая распространенность ЭД объясняется неуклонным ростом факторов риска развития данного состояния, основными из которых являются пожилой возраст, хронические заболевания (сахарный диабет, сердечно-сосудистые заболевания, гипертоническая болезнь, заболевания почек, депрессивные состояния), применение различных лекарственных препаратов (гипотензивные средства, антидепрессанты), лучевая терапия и оперативные вмешательства на органах малого таза, повреждения спинного мозга, а также курение и малоподвижный образ жизни [8-14]. А.В. Амосов и соавт., Р.В. Роживанов с соавт. также выделяют такие факторы риска ЭД как сердечно-сосудистые и системные заболевания – хроническая почечная недостаточность, сахарный диабет(≈20%), эндокринные (≈10%), неврологические заболевания (≈20%), злоупотребление алкоголем (≈20%), побочные действия лекарственных средств (≈10%), психологические причины (≈20%) [15,16].
На сегодняшний день в зависимости от причины выделяют три вида эректильной дисфункции: психогенную, обусловленную психологическими проблемами, стрессами, психотравмами; органическую, в основе которой лежат соматические заболевания и смешанную форму.
Наиболее часто встречается органическая ЭД, которая подразделяется на неврогенную, гормональную, васкулогенную, ятрогенную и смешанную [17].
А. Carvalheira и соавт. ЭД была классифицирована на венозную (31%), артериогенную (23%), психогенную (18%), ятрогенную (13%), нейрогенную (8%) и диабетическую (7%) [18].
Органическая ЭД наиболее часто обусловлена недостаточностью артериального кровоснабжения полового члена различного генеза [19-23]. Работы В.И. Мустафиной и соавт. продемонстрировали, что у 23,9% мужчин с жалобами на ЭД были обнаружены допплерографические признаки артериальной, у 41,8% – венокорпоральной, а у 34,3% – признаки смешанной ЭД [13].
По мнению ряда авторов существенное значение в развитии ЭД принадлежит эндотелиальной дисфункции. Эндотелиальная дисфункция – это генерализованный процесс, возникающий вследствие оксидативного стресса, нарушения метаболизма оксида азота, процессов окислительно– восстановительного фосфорилирования стенки сосудов, в частности эндотелия. Проявлением эндотелиальной дисфункции могут быть нарушения механизмов нормального кровотока в органах малого таза, а также в системе коронарного кровообращения. Нарушение кровотока в сосудах может манифестировать эректильной дисфункцией, а также атеросклерозом коронарных артерий. При этом ЭД является проявлением нарушения функции эндотелия без промежуточных стадий, в то время как атеросклероз коронарных артерий может развиваться длительное время бессимптомно, без проявлений ИБС, диабетоа и другимх заболеваний [17,24].
Таким образом, вопросы патогенеза ЭД указывают на многообразие факторов, приводящих к ее развитию, а диагностика этиологии ЭД очень важна при выборе метода лечения.
ДИАГНОСТИКА ВАСКУЛОГЕННОЙ ЭРЕКТИЛЬНОЙ ДИСФУНКЦИИ
Известно, что диагностика васкулогенных нарушений эрекции на основании только клинико-анамнестических данных в абсолютном большинстве случаев представляет весьма сложную задачу и в ряде случаев требует применения инструментальных методов обследования [25,26].
Наиболее распространенные методами диагностики васкулогенной ЭД в современной урологии являются:
- ультразвуковое исследование (УЗИ) с использованием допплерографии сосудов полового члена;
- кавернозография;
- компьютерная томография полового члена (КТ);
- магнитно-резонансная томография (МРТ) полового члена.
Все вышеуказанные методы диагностики, как правило, применяются на фоне фармакологической стимуляции эрекции (при приеме пероральных ингибиторов фосфодиэстеразы 5 типа или интракавернозном введении папаверина, простагландина Е).
Применение допплерографии полового члена для диагностики эректильных расстройств началось в конце 70-х годов и получило развитие в конце девяностых годов двадцатого века в связи с внедрением эффективных фармакологических стимуляторов эрекции [20].
В настоящее время допплерография сосудов полового члена считается «золотым стандартом» диагностики ЭД. Российские и зарубежные авторы предлагают использовать УЗИ полового члена для скрининга этого заболевания из-за низкой его инвазивности, отсутствия лучевой нагрузки, достаточной эффективности и массовой доступности [27-28]. Ультразвуковую допплерографию артерий полового члена широко применяют для диагностики ЭД, хотя результаты исследования во многом зависят от технического совершенства аппаратуры [29]. Однако допплерография полового члена не лишена недостатков. Высокие ультразвуковые частоты, обеспечивая хорошее пространственное разрешение, обуславливают неточность измерения при высоких скоростях кровотока. Кроме того, на результаты исследования существенно влияет угол наклона датчика, что свойственно методу дифракции, и краевые артефакты. Более того, допплеровское исследование не позволяет оценить скорость кровотока во всем органе, поскольку измерения производят в специфичных сегментах отдельного сосуда в определенных точках. При этом требуется аппарат экспертного класса [30].
W. Hsiao и соавт. отмечают, что до сих пор не существует единого стандарта выполнения данной процедуры. Авторы считают, что признаками адекватной эрекции являются: пиковая систолическая скорость (Vmax) более 30 см/с, отсутствие венозной утечки и индекс резистентности (RI) более 0,8 [31]. А.В. Амосов и соавт. при выполнении допплерографии полового члена у 398 больных с жалобами на ЭД оценивали состояние кавернозных артерий до и после интракавернозного введения простагландина Е1. Патологический венозный отток подозревали в том случае, если при адекватном артериальном притоке развивалась эрекция, но ее продолжительность была невелика и при этом определялся постоянный антеградный диастолический кровоток на всем протяжении исследования. Одним из признаков венозного оттока является снижение индекса резистентности, характеризующий кавернозный венозный отток. При этом индекс резистентности менее 0,75 сопровождается венозным оттоком у 90% пациентов с ЭД. Индекс резистентности более 0,9 отмечается у 90% здоровых субъектов [20]. А. Aversa и соавт. для диагностики васкулогенной ЭД предлагают учитывать не только стандартные ультразвуковые показатели, такие как индекс резистентности и пульсационный индекс (PI), но и состояние стенки артерии и степень артериальной дилатации [32].
N. Caretta и соавт. провели ультрасонографическое исследование у 109 мужчин (84 – с ЭД, 25 – в группе контроля) для сравнения функциональных и морфологических параметров кавернозных артерий и изучения связи атеросклероза сосудов полового члена с системным атеросклерозом. Авторы показали, что увеличение толщины интима-медиа кавернозных артерий более 0,3 мм может предсказать развитие ЭД сосудистого происхождения с большей точностью, чем пиковая систолическая скорость, и может оказаться предиктором системного атеросклероза на ранней стадии [33].
А.Л. Верткин и соавт. сообщили о том, что чувствительность допплерографии полового члена при определении недостаточности артериального притока составляла 85-100%, а специфичность – лишь 50-70%. Чувствительность допплерографии полового члена при недостаточности веноокклюзивного механизма составляла 90%, специфичность – 70% [34]. В тоже время М.К. Михайлов и соавт. показали, что эффективность ультразвуковой диагностики патологической венозной утечки из кавернозного бассейна полового члена значительно ниже эффективности метода динамической кавернозографии. Кроме того, динамическая кавернозография позволяет диагностировать не только наличие патологической утечки, но также определять количество патологических коммуникантных вен, их уровень и бассейн сброса [35].
D. Prezioso и соавт. при исследовании 59 больных (32 с васкулогенной ЭД и 27 – без нее) предположили существование корреляции между значением толщины туника интима медиа (IMT) кавернозной артерии и IMT сонной артерии. Значения IMT кавернозной артерии у больных с васкулогенной ЭД были выше, чем у больных без нее (0,28 ± 0,06 мм против 0,17±0,07 мм). Значения IMT сонной артерии при васкулогенной ЭД группы были выше, чем в группе пациентов без таковой (0,74 ± 0,14 мм против 0,59±0,11 мм) и этот показатель может служить ранним предиктором системного атеросклероза [36]. М. Schipilliti и соавт. сообщили о том, что пациенты с кавернозной васкулопатией имеют повышенный кардиометаболический риск и скрининг данной группы пациентов может идентифицировать таких больных [37].
X. Zheng и соавт. при обследовании 37 пациентов учитывали при УЗИ полового члена не только стандартные показатели, но и измерения осевой и радиальной жесткости полового члена с помощью аппарата RigiScan [38].
В.И. Мустафина и соавт. считают, что комплексное УЗИ полового члена с использованием допплеровских методик обладает высокой информативностью при диагностике причин ЭД [13]. Позже эта же группа авторов провела оценку комплексной лучевой диагностики ЭД с применением ультразвукового исследования с допплеровскими методиками (цветной и энергетический допплер, режим Dynamic flow и оценка кривых скоростей кровотока), фармакологической и визуальной индукции эрекции, компьютерной томографии, магнитно-резонансной томографии, динамической кавернозографии. Изучены возможности различных методов в определении дисфункции веноокклюзивного аппарата полового члена. В результате оказалось, что комплексное УЗИ с использованием допплеровских методик обладает высокой информативностью в диагностике причин ЭД, но МРТ имеет большую разрешающую способность при исследовании мягких тканей. Однако несмотря на стремление авторов выполнить неинвазивную методику, контраст все же вводили интракавернозно [39].
А.Л. Кошкакарян изучал микроциркуляцию полового члена методом компьютерной капилляроскопии и лазерной допплеровской флоуметрии. Им показано, что при латентной и полной эрекции ее возрастание сопряжено с увеличением структурных параметров микрососудов преимущественно артериального звена, а в фазе детумесценции доминирует возрастание скорости эритроцитов в венозных звеньях микроциркуляторного русла. Биомикроскопическая техника позволяет также объективно оценить структурные параметры микрососудов и плотность функционирующих капилляров в поверхностных слоях головки полового члена. Методика обладает малой инвазивностью, однако характеризуется высокой погрешностью, а также охватывает только одну анатомическую область (головку полового члена) [40]. А.С. Баканова также рекомендовала определять характер капиллярного кровообращения методом лазерной флоуметрии у мужчин с ЭД. Основными нарушениями пенильной гемодинамики, по мнению автора, приводящими к развитию васкулогенной ЭД, являются структурные изменения сосудистой стенки и кавернозных тел, недостаточный артериальный приток, избыточный венозный дренаж. По данным лазерной флоуметрии основные микроциркуляторные нарушения в половом члене проявляются снижением интенсивности перфузии в кавернозной ткани, уменьшением объема кровотока в артериолах, застоем крови в капиллярном русле, гипоксией кавернозной ткани и повышением симпатической вазомоторной активности [41].
Учитывая недостатки тех или иных методов, ряд авторов пытались использовать комбинацию методик. X. Gamé и соавт. провели сравнительное исследование эффективности дуплексного ультразвукового сканирования полового члена и кавернозометрии в диагностике веноокклюзивной ЭД. Исследователи предложили в качестве первого этапа диагностики использовать УЗИ полового члена, а инвазивный метод (кавернозографию) применять на втором этапе при планировании оперативного лечения [42].
Кавернозография в современном понимании этого термина была впервые предложена в 1984 г. R.Virag и соавт., выполнявших рентгеновское исследование кавернозных тел после введения вазоактивного препарата папаверина, который индуцировал эрекцию и позволял провести визуализацию кавернозных тел в эрегированном состоянии [43].
Кавернозография — ангиографическое исследование сосудов полового члена, во время которого в кавернозные тела через небольшую иглу вводится рентгеноконтрастное вещество. Получаемая рентгенограмма позволяет определить состояние кровеносных сосудов полового члена. Данный метод применяется для подтверждения или исключения сосудистой природы ЭД. Используется главным образом в диагностически сложных случаях и позволяет определить недостаточность артериального притока, венозную окклюзию, а также локализацию сброса венозной крови в артериальное русло полового члена.
По мнению М.К. Михайлова и соавт. эффективность диагностики патологической венозной утечки из кавернозного бассейна полового члена методом УЗИ значительно ниже, чем при динамической кавернозографии. Кроме того динамическая кавернозография позволяет диагностировать не только наличие патологической утечки, но также определять количество патологических коммуникантных вен, их уровень и бассейн сброса [35].
Фармакокавернозография обычно выполняется в двух проекциях и демонстрирует контрастированные венозные сосуды, по которым преимущественно происходит сброс крови из кавернозных тел [44].
Я. В. Прокопьев изучил с 2005 по 2007 год данные 120 больных с эректильной дисфункцией и продемонстрировал, что кавернозография позволяет в 97,0±1,3% выявлять изменения в кавернозных телах полового члена (как структурные, так и анатомические), обуславливающие ЭД, и разработать оптимальные методы их коррекции. Автор показал, что основными бассейнами венозной утечки у больных с ЭД являются подвздошные, эпигастральные вены или сочетание этих путей. Динамическая кавернозография позволила автору установить причины ЭД: венозную утечку (76,9%); патологические шунты между головкой полового члена и кавернозными телами (30,7%); склерозирование кавернозных тел (38,4%); болезнь Пейрони (7,6%); патологическое строение кавернозного бассейна полового члена (23%). Автор считает, что динамическая кавернозография является достоверным, высокоэффективным методом диагностики ЭД по сравнению с ультразвуковой визуализацией сосудистой системы кавернозного бассейна полового члена [45]. В.В. Власов использовал разновидность кавернозографии – спонгиографию для выявления функциональных и патологических изменений вен полового члена и простатического венозного сплетения у мужчин с органической ЭД. Автор считает, что спонгиозография при ЭД целесообразна в случаях, когда стандартное обследование не дает однозначного ответа о причине нарушения эрекции. Также, по мнению автора, необходимо использовать этот метод для диагностики в случае неэффективности первичного лечения ЭД [46].
В.А. Брусенский полагает, что кавернозография более информативна при определении артериальной ЭД, а эффективность диагностики веногенной эректильной дисфункции с определением типа патологического венозного дренирования составляет лишь 54,8% при использовании этой методики [47]. В исследовании Д.Г. Курбатова и соавт. также продемонстрировано, что практически невозможно верифицировать венозную утечку при помощи фармакокавернозографии [48].
В настоящее время кавернозография из-за высокой инвазивности и лучевой нагрузки часто используется в сочетании с другими методиками.
D.V. Patel и соавт. предлагают для повышения диагностической ценности кавернозографии использовать ее в сочетании с манометрией. Авторы считают, что кавернозография эффективна для обнаружения анатомических дефектов в первую очередь при веноокклюзивной ЭД, то есть при так называемой «венозной утечке» и возможна для применения только по строгим показаниям у пациентов, которым планируется хирургическое вмешательство на половом члене [19].
Метод компьютерной томографии применяется у больных с подозрением на ЭД венозного генеза в сложных клинических случаях и при неэффективности скрининговой функциональной кавернозографии. Данный метод также позволяет выявить особенности патологического дренирования кавернозных тел полового члена, провести топическую диагностику с определением локализации венозной утечки. Возможность построения трехмерных изображений, получаемых при компьютерной томографии, позволяет представить имеющиеся патологические изменения и выбрать метод хирургического лечения [47].
Для визуализации анатомически «глубоко» расположенных сосудистых структур и оценки их объемного и пространственного взаимоотношения О.Б. Жуков и соавт. сообщили об опыте применения мультиспиральной компьютерной томографии органов малого таза, полового члена и органов мошонки у мужчин с ЭД. Для контрастирования сосудистых структур использовали омнипак 350 мг йода/мл с содержанием йогексикола 755 мг/мл (из расчета 1 мл контраста на 1 кг массы тела пациента), который вводили внутривенно болюсно. Мультиспиральную компьютерную томографию проводили как в покое, так и на фоне фармакологически индуцированной эрекции. Спиральная компьютерная томография позволила выявить множественные венозные соустья между половым членом и яичком, а именно между глубокими пенильными венами и веной семявыбрасывающего протока, между глубокой дорзальной веной и венами простатовезикального сплетения. К сожалению, данный метод, несмотря на его малую инвазивность и отсутствие необходимости интракавернозного введения контраста, не лишен таких недостатков как наличие лучевой нагрузки, дороговизна, быстрое прохождение сосудистой фазы при контрастировании, в связи с чем зачастую трудно получить изображения как магистральных, так мелких сосудов [49].
В.В Михайличенко и соавт., H.A. Feldman и соавт. для решения этой проблемы предлагают использовать функциональную кавернозографию (в качестве контраста используют йодсодержащие вещества) в сочетании с компьютерной томографией. Данный метод диагностики отвечает на некоторые вопросы поставленными авторами, но по нашему мнению, является слишком инвазивным и трудоемким [50, 51].
Другая группа российских авторов (Ефремов Е.А., Жуков О.Б. и соавт.) для диагностики ЭД использовала динамическую компьютерную кавернозографию. Ими обследовано 88 пациентов с подозрением на патологический венозный дренаж. При этом венозную «утечку» классифицировали на основании преобладающего пути венозного оттока. Авторы выделили 3 типа сброса крови из кавернозных тел: дистальный сброс – по системе глубокой дорсальной вены, проксимальный сброс – по глубоким пенильным венам и смешанный тип сброса крови. При обработке данных динамической компьютерной кавернозографии были получены следующие результаты: венозная утечка подтверждена у 72 (81,8%) пациентов, патологические шунты между спонгиозным телом полового члена и кавернозными телами у 26 (29,5%), склерозирование кавернозных тел полового члена у 19 (21,5%), болезнь Пейрони выявлена у 1 (1,14%), патологическое строение кавернозного бассейна полового члена у 13 (14,8%) пациентов. Сочетанные патологические состояния наблюдали у 57 (64,8%) больных. Наибольшая доля встречавшихся патологических состояний кавернозного бассейна приходилась на венозный сброс в подвздошные вены малого таза (55,7%), на долю сброса в эпигастральные вены приходилось до 18,2%. В течение исследования проведено сравнение диагностической ценности динамической компьютерной фармакокавернозографии с другими методами исследования состояния сосудов полового члена. Необходимо отметить, что чувствительность фармакодопплерографи, фармакокавернозографии, динамической компьютерной кавернозография при этом составила 71%, 73% и 95% соответственно, специфичность этих же методов – 85%, 93%; и 98%. Авторы сделали выводы о том, что среди имеющихся на сегодняшний день методов диагностики веногенной ЭД динамическая компьютерная фармакокавернозография имеет наилучшие показатели чувствительности и специфичности [52].
В.Н. Журавлев и соавт. для диагностики нарушений веноокклюзивного механизма при ЭД использовали плоскопанельную компьютерную томографию при обследовании 23 пациентов с ЭД и нарушением венооклюзионного механизма. Преимущества метода – использование небольшого количества контрастного вещества, возможность трехмерной реконструкции сосудистого русла из-за высокого пространственного разрешения, низкая доза облучения, отсутствие артефактов от металлических предметов. Однако отмечены следующие недостатки метода: необходимость применения сложного оборудования, интракавернозное введение контрастного вещества [53].
Брусенский В.А. продемонстрировал 97%-ую эффективность диагностики веногенной ЭД при определении типа патологического венозного дренирования с помощью мультисрезовой спиральной компьютерной томографии [47].
Магнитно-резонансная томография полового члена.
МРТ относится к дорогостоящим и технически сложным объективным лучевым методам диагностики, роль которых в диагностическом процессе, особенно в визуализации сосудистого компонента при ЭД венозного генеза, очень высока. Данный метод позволяет идентифицировать анатомические структуры, кавернозные ткани, визуализировать промежностные и пенильные артерии, однако более достоверно выявить сосудистую недостаточность при ЭД можно при помощи МР-ангиографии с контрастным усилением [54].
В работе Д.Г. Курбатова и соавт. МРТ полового члена проводили на фоне функциональной кавернозографии (в качестве контраста использовали парамагнитное вещество – гадолиний). Эффект контрастирования достигался за счет способности гадолиний-содержащих препаратов изменять релаксационные свойства экстрацелюлярной жидкости, что проявлялось укорочением времени Т1-релаксации и усилением интенсивности сигнала от крови при специальных импульсных последовательностях. Таким образом регистрировали эффект, аналогичный достигаемому при ангиографии [47]. МРТ полового члена помогает идентифицировать анатомические структуры полового члена, окружающие и патологически измененные ткани, позволяет качественно верифицировать состояние веноокклюзионного механизма вне зависимости от преобладания корпоральных и посткорпоральных факторов. Недостатком МРТ полового члена в диагностике веноокклюзивной ЭД является высокая инвазивность и дороговизна метода. В.А. Брусенский и соавт. полагают, что МРТ с интракавернозным контрастированием является методом выбора объективной визуализации патологических дренирующих вен полового члена у больных веногенной ЭД и его применение целесообразно в трудных диагностических случаях. Учитывая большую 100% эффективность МРТ и полное отсутствие ионизирующего излучения, данный метод исследования является основным в диагностике веногенной ЭД, особенно у молодых пациентов [47].
A. Kirkham считает МРТ полового члена дорогостоящим тестом, дополняющим клиническое обследование или УЗИ. МР-ангиография демонстрирует структуру внутренних подвздошных сосудов и может быть использована при планировании реваскуляризации органов малого таза, но не всегда обладает таким разрешением, чтобы достаточно визуализировать сосуды полового члена. По своим диагностическим возможностям данный метод превосходит «рутинную ангиографию» [55].
D. Prezioso и соавт. предложили учитывать не только структурные и скоростные характеристики артериального русла полового члена при УЗИ, но и архитектонику сосудов, определяемую при МРТ. Авторы показали, что МРТ является более чувствительным методом диагностики по сравнению с допплерографией (p< 0,001). К сожалению, данное исследование было выполнено при участии небольшого количества пациентов [36].
Таким образом, на сегодняшний день оптимальными методами топической диагностики веногенной ЭД следует считать МРТ и КТ с интракавернозным контрастированием.
Радионуклидные методы оценки кровоснабжения пениса были впервые предложены японскими учеными M. Shirai и M. Nakamura [56-57], которые использовали для этого серийную радиометрию проб крови из подкожных вен полового члена после внутривенной инъекции радиофармпрепарата (РФП). В 1982 г. N. Fanous и соавт. провели динамическую запись кровяного пула пениса с использованием 99тТс-пертехнетата и количественно рассчитали изменения объема крови в пенисе, вызванные внутривенным введением вазодилататора [58]. Измеренные параметры хорошо коррелировали с индексом кровяного давления в органе. Еще одной методикой радионуклидной диагностики эректильной дисфункции явилась оценка клиренса 33Хе после его подкожной инъекции в область заднего венечного шва полового члена. При этом оказалось, что у лиц с артериальной и смешанной формами импотенции клиренс индикатора снижается, а у пациентов с неваскулогенными и флебогенными нарушениями эрекции – не нарушается [59].
К сожалению, в настоящее время для радионуклидной оценки артериального и венозного компонентов васкулогенной ЭД недостаточно используют фаллосцинтиграфию с 99тТс-эритроцитами.
L.S. Zuckier также представил результаты радионуклидных методов исследования пенильной гемодинамики. Данный автор полагает, что эти методы являются простыми и рентабельными при диагностике ЭД [60].
В современной урологии методика радионуклидной диагностики ЭД не изменилась и не вызывает широких дискуссий авторов [61]. Однако на сегодняшний день отсутствуют масштабные сравнительные исследования в данной области. Большинство литературных данных представлены единичными описаниями. До сих пор не проводился анализ эффективности и специфичности радиоизотопной диагностики ЭД. В доступной нам литературе мы не нашли большого количества данных по этой проблеме.
Таким образом, в настоящее время микроциркуляция в половом члене при патологических состояниях изучена недостаточно, что определяет актуальность проведения исследований данной проблемы.
Многие специалисты полагают, что ЭД как проявление эндотелиальной дисфункции в ряде случаев является предвестником заболеваний сердечнососудистой системы. В связи с этим, ранняя диагностика ЭД может приводить к обнаружению этих нередко угрожающих жизни заболеваний, которые в противном случае могли бы остаться незамеченными [5].
На сегодняшний день в эру высоких медицинских технологий актуальным является внедрение в клиническую практику новых малоинвазивных, объективных, высокоинформативных и безвредных визуализационных методик диагностики эректильной дисфункции.
ЛИТЕРАТУРА
1. NIH Consensus Development Panel on Impotens. – Impotens. JAMA 1993;270: 83-90
2. Миронов С.А., Артифексов С.Б. Эректильная дисфункция. Патологическая связь с расстройством адаптации (обзор литературы). Вестник новых медицинских технологий 2013;(1):171.
3. Glina S, Cohen DJ, Vieira M. Diagnosis of erectile dysfunction. Curr Opin Psychiatry 2014;27(6):394-399.
4. Аляев Ю. Г., Винаров А. З., Ахвледиани Н. Д. Эффективность тадалафила в лечении преждевременного семяизвержения, ассоциированного с эректильной дисфункцией. РМЖ 2010;(5):273-276.
5. Пушкарь Д.Ю., Камалов А.А., Аль-Шукри С.Х., Еркович А.А., Коган М.И., Павлов В.Н., и др. Анализ результатов эпидемиологического исследования распространенности эректильной дисфункции в Российской Федерации. Урология 2012;(6):5-8.
6. Chew K.K. Earle CM, Stuckey BG, Jamrozik K, Keogh EJ. Erectile dysfunction in general medicine practice: prevalence and clinical correlates. Int J Impot Res 2000;12:41-45
7. Хамзин А.А., Фролов Р.А. Распространение эректильной дисфункции среди городского населения республики Казахстан в возрасте от 21 до 79 лет. Современная медицина: актуальные вопросы 2014;(30):89-93.
8. Раснер П.И., Пушкарь Д.Ю. Эректильная дисфункция – разные решения одной проблемы, или размышления на заданную тему. Медицинский совет 2014;(19):64-71.
9. Юдовский С.О., Пушкарь Д.Ю. Коррекция эректильной дисфункции у пациентов, перенесших радикальную простатэктомию. Урология 2014;(4):66-71.
10. Weinberg AE, Eisenberg M, Patel CJ, Chertow GM, Leppert JT. Diabetes severity, metabolic syndrome, and the risk of erectile dysfunction. J Sex Med 2013;(10):3102–3109.
11. Kumar J, Bhatia T, Kapoor A, Ranjan P, Srivastava A, Sinha A, et al. Erectile dysfunction precedes and is associated with severity of coronary artery disease among Asian Indians. J Sex Med 2013;10(5):1372–1379
12. Nehra A, Jackson G, Miner M, Billups KL, Burnett AL, Buvat J, et al. Diagnosis and treatment of erectile dysfunction for reduction of cardiovascular risk. J Urol 2013;189(6):2031–2038.
13. Мустафина В.И., Гурьев Э.Н., Лобкарев О.А. Комплексная лучевая диагностика эректильной дисфункции веноокклюзивного аппарата полового члена. Андрология и генитальная хирургия 2012;(4):18-24.
14. Давидович И.М., Маренин С.Н. Эректильная функция, андрогенный статус и эндотелиальнозависимая вазодилататция пенильных артерий у мужчин молодого возраста с гипертонической болезнью. Дальневосточный медицинский журнал 2013;(3):20-24.
15. Амосов А.В., Петровский Н.В., Демидко Ю.Л., Байдувалиев А.М. Индивидуальный подбор дозы силденафила в лечении эректильной дисфункциию. РМЖ. Фармакотерапия 2014;(17):1292-1297
16. Роживанов Р.В., Сунцов Ю.И., Курбатов Д.Г. Эректильная дисфункция у больных сахарным диабетом по данным контрольно – эпидемиологических исследований. Сахарный диабет 2009;(2):51-54.
17. Ахвледиани Н.Д., Алленов С.Н., Матюхов И.П., Иноятов Ж.Ш. Эректильная дисфункция: современной состояние проблемы. Медицинский совет 2015;(2):28-32.
18. Carvalheira A, Forjaz V, Pereira NM. Adherence to phosphodiesterase type 5 inhibitors in the treatment of erectile dysfunction in long-term users: how do men use the inhibitors? Sex Med 2014;2(2):96-102.
19. Patel D V, Halls J, Patel U. Investigation of erectile dysfunction. Br J Radiol 2012;85(1):69–78.
20. Амосов А.В., Петровский Н.В., Демидко Ю.Л., Байдувалиев А.М. Индивидуальный подбор дозы силденафила в лечении эректильной дисфункции. Русский медицинский журнал 2014;(17):1292-1297.
21. Кушниренко Н.П. Диагностика и хирургическое лечение болезни Пейрони, осложненной эректильной дисфункцией. Вестник Российской военно-медицинской академии 2011;(3):87-90.
22. Cander S, Coban S, Altuner S, Oz Gul O, Yetgin ZA, Akkurt A, et al. Prevalence and correlates of erectile dysfunction in type 2 diabetes mellitus: a cross-sectional single-center study among Turkish patients. Metab Syndr Relat Disord 2014;12(6): 324–329.
23. Qiu X1, Fandel TM, Lin G, Huang YC, Dai YT, Lue TF, et al. Cavernous smooth muscle hyperplasia in a rat model of hyperlipidaemia-associated erectile dysfunction. BJU Int 2011;108(11):1866-1872.
24. Lin G, Qiu X, Fandel TM, Albersen M, Wang Z, Lue TF, et al. Improved penile histology by phalloidin stain: circular and longitudinal cavernous smooth muscles, dual-endothelium arteries, and erectile dysfunction-associated changes. Urology 2011;78(4):970.
25. Hatzimouratidis K. I. Eardley, F. Giuliano, I. Moncada, A. Salonia. Guidelines on male sexual dysfunction: erectile dysfunction and premature ejaculation. Eur urol 2010; 57(5):804814
26. Кротовский Г.С, Зудин A.M. Виагра – 5 лет успеха. М. 2003, 189 с.
27. Костылев М.В., Егорова О.Н., Хохоля А.В., Дрюк Н.Ф. Диагностика эректильной дисфункции по данным ультразвукового исследования сосудов полового члена. Сердце и сосуды 2005;11(3):45-54.
28. Yildirim D, Bozkurt IH, Gurses B, Cirakoglu A. A new parameter in the diagnosis of vascular erectile dysfunction with penile Doppler ultrasound: cavernous artery ondulation index. Eur Rev Med Pharmacol Sci 2013;17(10):1382-1388
29. Щеплев П. А. , Данилов И.А., Колотинский А.Б., Гвасалия Б.Р., Гарин Н.Н. Клинические рекомендации эректильная дисфункция. Андрология и генитальная хирургия 2007;(1):59-65
30. Баев А.А., Громов А.И., Кульченко Н.Г. Лучевая диагностика и терапия в урологии [под ред. Громова А.И., Буйлова В.М.]. М. ГОЭТАР-Медиа 2011. 542 с.
31. Hsiao W, Shrewsberry AB, Moses KA, Pham D, Ritenour CW. Longer time to peak flow predicts better arterial flow parameters on penile Doppler ultrasound. Urology 2010;75(1):112-116.
32. Aversa A, Sarteschi LM. e role of penile color-duplex ultrasound for the evaluation of erectile dysfunction. J Sex Med 2007;4(5):1437-1447.
33. Caretta N, Palego P, Schipilliti M, Ferlin A, Di Mambro A, Foresta C. Cavernous artery intima-media thickness: a new parameter in the diagnosis of vascular erectile dysfunction. J Sex Med 2009;6(4):1117–1126
34. Верткин А.Л., Моргунов Л.Ю., Будылев С.А., Кривцова Е.В. Эректильная дисфункция: повторение и заметки. Медицинский совет 2011;(1-2):30-34.
35. Михайлов М.К., Лобкарев О.А., Прокопьев Я.В. Распространенность и структура эректильной дисфункции и роль динамической кавернозографии в ее диагностике. Общественное здоровье и здравоохранение 2008;(1):94-98.
36. Prezioso D, Iacono F, Russo U, Romeo G, Ruffo A, Russo N, Illiano E. Evaluation of penile cavernosal artery intima-media thickness in patients with erectile dysfunction. A new parameter in the diagnosis of vascular erectile dysfunction. Our experience on 59 cases. Arch Ital Urol Androl 2014;86(1):9-14.
37. Zheng X1, Ji P, Mao H, Wu J. Evaluation of penile erection rigidity in healthy men using virtual touch tissue quantification. Radiol Oncol 2012;46(2):114-118.
38. Schipilliti M, Caretta N, Palego P, Selice R, Ferlin A, Foresta C. Metabolic syndrome and erectile dysfunction: the ultrasound evaluation of cavernosal atherosclerosis. Diabetes Care 2011;34(8):1875-1877.
39. Мустафина В.И., Гурьев Э.Н. Возможности ультразвуковой диагностики артериальной эректильной дисфункции у мужчин. Медицинский вестник Башкортостана 2012;(7):45-49
40. Кошкакарян А. Л. Состояние кожной микроциркуляции полового члена и ее расстройства при хроническом простатите: автореф. дисс. … канд. мед. наук. Москва, 2010. М.. URL:http://medical-diss.com/medicina/sostoyanie-kozhnoy-mikrotsirkulyatsii-polovogo-chlena-i-ee-rasstroystva-pri-hronicheskom-prostatite
41. Баканова А.С. Пенильная гемодинамика и микроциркуляция в норме и при васкулогенной эректильной дисфункции. … автореф. дисс. канд. биол. наук. Барнаул, 2006. URL: http://www.dslib.net/fiziologia/penilnaja-gemodinamika-i-mikrocirkuljaci…
42. Gamé X1, Berrebi A, Lostes A, Malavaud B, Sarramon JP, Rischmann P. Comparison of cavernometry and duplex ultrasound in the diagnosis of veno-occlusive erectile dysfunction. Prog Urol 2006;16(4):470-473.
43. Virag R, Frydman D, Legman M, Virag H. Incavernous injection of papaverine as a diagnostic and therapeutic metod in erectile failure. Angiology 1984;35:79-87
44. Лоран, О. Б., Щеплев, П. А., Нестеров, С. Н., Кухаркин, С. А. Современные методы диагностики и лечения эректильных дисфункций. РМЖ 2000;8(3):130-134.
45. Прокопьев Я.В. Метод динамической кавернозорафии в диагностике заболеваний кавернозного бассейна полового члена. … дисс. канд. мед. наук., Казань, 2009. 110 с. URL: http://www.dissercat.com/content/metod-dinamicheskoi-kavernozorafii-v-di…
46. Власов В.В. Эректильная дисфункция. Венозная гемодинамика в механизме эрекции полового члена: дис. … канд. мед. наук. Н. Новгород; 2012, 123 с.
47. Брусенский В.А. Лучевые методы исследования в диагностике веногенной эректильной дисфункции: дисс. … канд. мед. наук. М.; 2008, 134 с. URL: http://medical-diss.com/medicina/luchevye-metody-issledovaniya-v-diagnos…
48. Курбатов Д.Г., Щетинин В.В., Китаев С.В. Роль магнитно-резонансной томографии в диагностике и лечении васкулогенной эректильной дисфункции. Медицинская визуализация 2005;(4):120-127.
49. Жуков О.Б., Зубарев А.Р., Кульченко Н.Г. Ультразвуковые параметры и морфологические критерии веноокклюзивной эректильной дисфункции при возрастном андрогеном дефиците. Андрология и генитальная хирургия 2009;(1):39-43.
50. Михайличенко В.В., Александров В.П., Фесенко В.Н., Кореньков Д.Г., Абд Али. Значение триплексной ультразвуковой допплерографии в диагностике эректильной дисфункции. Материалы конференции «Социальные и клинические проблемы сексологии и сексопатологии». – М., 2003г. – С. 1-2
51. Feldman HA, Goldstein I, Hatzichristou DG, Krane RJ, McKinlay JB. Impotence and its medical and psychosocial correlates: results of the Massachusetts male aging study. J Urol 1994;151(1):54-61
52. Ефремов Е.А., Жуков О.Б., Щербинин С.Н., Мельник Я.И., Красняк С.С., Симаков В.В. и др. Динамическая компьютерная кавернозография в диагностике веноокклюзивной эректильной дисфункции. Андрология и генитальная хирургия 2012;(1):62-69.
53. Журавлев В.Н., Коган О.С., Романенко Д.В., Кочмашев И.В., Шерстобитов В.Е. Плоскопанельная компьютерная томография (CONE-BEAM CT) в предоперационной диагностике нарушений вено-оклюзивного механизма при эректильной дисфункции. Медицинский вестник Башкортостана 2013;(2):293-295.
54. Жуков О.Б. Диагностика эректильной дисфункции. Клиническое руководство. Изд. Бином 2008, 77 c.
55. Kirkham A. MRI of the penis. Br J Radiol 2012;85(1):86-93.
56. Shirai M, Nakamura M. Diagnostic discrimination between organic and functional impotence by radioisotope penogram with 99mTcO4. Tohoku J Exp Med 1975;116(1):9-15.
57. Shirai M, Nakamura M. Differential diagnosis of organic and functional impotence by the use of 131-I-human serum albumin. Tohoku J Exp Med 1970;101(4):317-324.
58 Fanous HN, Jevtich MJ, Chen DC, Edson M. Radioisotope penogram in diagnosis of vasculogenic impotence. Urology 1982;20(5):499-502.
59 Лишманова Ю.Б., Чернова В.И. Радионуклидная диагностика для практических врачей // Томск :STT – 2004. – 394с.
60. Zuckier LS. Use of radoactive tracers in the evaluation of penile hemodynamics: History, methodology and measurements. Int J Impot Res 1997;9(2):99-108
61. Kandeel FR. Male Sexual Dysfunction: Pathophysiology and Treatment. CRS Press; 2007, 307 p.
| Прикрепленный файл | Размер |
|---|---|
| Скачать статью | 730.34 кб |
Ключевые слова:
эректильная дисфункция, диагностика, магнитно-резонансная томография, половой член, компьютерная томография, допплерография, радионуклидная диагностика, фаллосцинтиграфия