О препарате
Состав: экстракт каланхоэ перистого (Bryophyllum pinnatum extract), экстракт корней валерианы (Valeriana officinallis extract), экстракт корней солодки голой (Glycyrrhiza glabra extract).
В суточной дозе (1 капсула) содержится:
|
Ингредиент |
Содержание в суточной дозе не менее, мг |
% от рекомендуемого*/адекватного** уровня потребления |
|
Глициризиновая кислота |
20 |
200** |
|
Валереновая кислота |
0,3 |
15 |
|
Флавоноиды в пересчете на рутин |
7,5 |
25 |
|
Полифенольные соединения (в пересчете на галловую кислоту) |
15 |
15 |
*Согласно «Единым санитарно-эпидемиологическим и гигиеническим требованиям к товарам подлежащим санитарно-эпидемиологическому надзору (контролю)»
**Не превышает верхний допустимый уровень потребления (30 мг).
Показания к применению: способствует уменьшению частоты ночных мочеиспусканий, уменьшению ночного диуреза, снижению гиперактивности детрузора, улучшению качества сна.
Рекомендации по применению: взрослым по 1 капсуле 1 раз в день, во время еды. Перед применением рекомендуется проконсультироваться с врачом.
Форма выпуска: 30 капсул по 400 мг.
Противопоказания: индивидуальная непереносимость компонентов продукта, беременность, кормление грудью.
Условия хранения: хранить в недоступном для детей месте, при температуре не выше +25°С.
Срок годности: 2 года с даты изготовления.
СГР: RU.77.99.11.003.Е.004613.10.18
ТУ: 10.89.19-004-00145916-2018
Изготовитель: ООО «Витамер», 117623, г. Москва, вн.тер.г. муниципальный округ Южное Бутово, ул. 2-я Мелитопольская, д. 19, к. 2, кв. 57.
По заказу ООО «ЭСЭЙЧ ФАРМА».
Организация, уполномоченная принимать претензии от потребителей: ООО «ЭСЭЙЧ ФАРМА»,
109428, г. Москва, вн.тер.г. муниципальный округ Рязанский, пр-кт Рязанский, дом 10, строение 18, этаж 10, ком. 6А, тел.: 8 (495) 178 08 23, e-mail: info@shpharma.ru
Биологически активная добавка к пище. Не является лекарственным средством.
Действие компонентов
Каланхоэ перистое (Bryophyllum pinnatum)
Это вид цветковых растений рода Каланхоэ, родиной которого является Мадагаскар.
Экстракт Каланхоэ перистого снижает частоту мочеиспусканий в сутки на 17,8%. При использовании у женщин в менопаузе улучшает мочеиспускание у 80% пациентов. Результаты исследований Каланхоэ перистого показывают, что он расслабляет гладкую мускулатуру мочевого пузыря у людей и уменьшает активность центров мочеиспускания у модельных животных. Оба эффекта могут эффективно влиять на симптомы гиперактивности мочевого пузыря (ГАМП), так как предполагается, что в патогенезе ГАМП должны играть роль оба этих фактора.
Экстракт Каланхоэ перистого снижает сократимость мускулатуры мочевого пузыря in vitro на 18,7% в дозозависимом режиме. Его активность связана с разнонаправленным воздействием на различные подтипы мускариновых рецепторов.
Валериана лекарственная (Valeriana officinalis L.)
Валериана – это одно из самых известных лекарственных растений. Действие Валерианы обусловлено входящими в её состав эфирными маслами (изовалериановой и валереновой кислотами), тритерпеновыми гликозидами.
Считается, что Валериана взаимодействует с нейромедиатором гамма-аминомасляной кислотой (ГАМК) и его рецепторами. Валериана ингибирует поглощение ГАМК, а также стимулирует его высвобождение. Совсем недавно было показано, что Валериана является частичным стимулятором рецепторов аденозина и серотонина в головном мозге.
При неорганической бессоннице, экстракт Валерианы показывает в улучшении качества сна эффективность сходную со снотворным оксазепамом.
Полисомнографические исследования показали, что Валериана достоверно на 23% снижает частоту ночных пробуждение.
Экстракт валерианы накапливается в организме и демонстрирует усиление эффекта через 2 и 4 недели после начала приема. Таким образом, оптимальный курс лечения составляет 1 мес.
Это позволяет использовать экстракт Валерианы при ноктурии, связанной с расстройствами сна.
Солодка голая (Glycyrrhiza glabra)
Солодка голая или Лакрица – это многолетнее травянистое растение, произрастающее в Европе, России, Западной и Центральной Азии, Северной Африке.
Действие экстракта Солодки голой обусловлено наличием глицирризиновой кислоты, бета-ситостерина, флавоноидами (ликвиритином), Ликохалконом А.
Действие глицирризина может вызывать минералокортикоидные эффекты. Глицирретиновая кислота и сапонины Солодки могут ингибировать фермент 11-β-гидроксистероиддегидрогеназу, приводя к задержке жидкости ночью.
Исследования показали, что экстракт Солодки голой на 81% повышает секрецию Na-уретического пептида в течение 8 недель. Кроме того, Солодка достоверно уменьшает выделение натрия, что, в свою очередь, приводит к уменьшению выделения жидкости.
Другим механизмом уменьшения диуреза является снижение содержания гормона альдостерона в сыворотке крови.
Эти механизмы действия являются основанием для применения экстракта Солодки голой у пациентов с ноктурией с целью уменьшения диуреза.

|
||
|
||
|
||
|
||
|
||
|
||
|
||
|
||
|

Информация о лекарственных препаратах, размещенная на AptekaMos.ru, не должна использоваться неспециалистами для самостоятельного принятия решения об их покупке и применении без консультации врача.
Свидетельство о регистрации средства массовой информации ЭЛ № ФС77-44705 выдано Федеральной службой по надзору в сфере связи, информационных технологий и массовых коммуникаций (Роскомнадзор) 21 апреля 2011 года.
• Инструкция по применению Диунорм капсулы по 400мг.
• Способ применения и дозировка, состав, побочное действие и взаимодействие Диунорм капсулы по 400мг
Диунорм® в лечении симптомов гиперактивного мочевого пузыря у женщин (предварительные результаты)
https://doi.org/10.21886/2308-6424-2021-9-2-100-110
Полный текст:
- Статья
- Об авторах
Аннотация
Введение. Гиперактивный мочевой пузырь в сочетании или без ургентной инконтиненции прогрессирует с возрастом и не имеет гендерной принадлежности, составляя в женской популяции в среднем около 25%.
Цель исследования. Оценка эффективности препарата Диунорм® (капсулы) в лечении симптомов гиперактивного мочевого пузыря у женщин.
Материалы и методы. В статистический анализ включены результаты обследования 28 женщин с симптомами гиперактивного мочевого пузыря, средний возраст которых составил 35,3 года. Для лечения использован препарат Диунорм® по 400 мг 1 раз в день в течение 90 дней. Пациентки заполняли опросник Overactive Bladder Awareness Tool и дневник мочеиспускания. Дополнительно выполняли анализ мочи, бактериологическое исследование мочи, урофлоуметрию, УЗИ мочевого пузыря и цистоскопию.
Результаты. У всех женщин на протяжении исследования были отрицательные результаты посева мочи и отсутствовала пиурия, что исключало инфекционную этиологию нарушений мочеиспускания. На фоне терапии регистрировали статистически достоверное снижение ирритативной симптоматики по опроснику Overactive Bladder Awareness Tool. Сумма баллов через 1,5 и 3 месяца уменьшилась на 3,0 и 4,3 балла, соответственно (p < 0,05). Положительная динамика по сумме баллов отмечена у 75%, в отношении ноктурии у 82% пациенток (р < 0,01). Средняя скорость мочеиспускания увеличилась с 13,3 ± 0,7 мл/с до 15,1 ± 0,7 мл/с и 15,4 ± 0,5 мл/с через 1,5 и 3 месяца соответственно (р < 0,0001). Аналогичная тенденция отмечена для максимального потока мочи и объёма остаточной мочи. Максимальный поток мочи при приёме Диунорма® увеличился с 15,9 ± 0,6 мл/с до 17,4 ± 0,5 мл/с и 18,1 ± 0,4 мл/с (р < 0,001). Объём остаточной мочи уменьшался на протяжении всего исследования. При включении в исследование, через полтора и три месяца этот показатель составил 19,9 ± 1,4; 12,2 ± 1,6 и 6,4 ± 1,1 мл соответственно (p < 0,001).
Заключение. Препарат Диунорм® может стать достойной альтернативой традиционной терапии первой линии ГАМП. Для получения доказательной базы высокого уровня необходимо проведение сравнительных исследований.
Ключевые слова
Для цитирования:
Шкодкин С.В., Покровский М.В., Красняк С.С., Полищук А.В., Чирков С.В., Чурикова О.В., Кравцова Н.А. Диунорм® в лечении симптомов гиперактивного мочевого пузыря у женщин (предварительные результаты). Вестник урологии. 2021;9(2):100-110. https://doi.org/10.21886/2308-6424-2021-9-2-100-110
For citation:
Shkodkin S.V., Pokrovsky M.V., Krasnyak S.S., Polichuk A.V., Chirkov S.V., Churikova O.V., Kpavtsova N.A. Treatment of overactive bladder symptoms in women with Diunorm®: preliminary results report. Urology Herald. 2021;9(2):100-110.
(In Russ.)
https://doi.org/10.21886/2308-6424-2021-9-2-100-110
Введение
Проблемы гиперактивности мочевого пузыря (ГАМП) и связанной с этим инконтиненции длительное время сохраняют лидирующие позиции в публикационной активности как в отечественной, так и зарубежной научной периодической печати, что отражает их актуальность. Ориентируясь на эти исследования, можно констатировать, что гиперактивность детрузора в сочетании или без ургентной инконтиненции прогрессирует с возрастом и не имеет гендерной принадлежности, составляя в женской популяции в среднем около 25% [1][2][3]. Данная патология достаточно сильно социально дезадаптирует, так, в исследовании E.B. Rubin et al. (2016) продемонстрировали, что 68,9% респондентов предпочли бы фатальный исход проблемам с мочевым пузырём и инконтиненции [4][5][6][7]. Однако, несмотря на это, до 95% пациенток в России не получают адекватного лечения [8], а приверженность к фармакотерапии пока оставляет желать лучшего. Так, комплаентность через год от начала лечения не превышает 20% [9][10]. В данной плоскости проблемы лечения ГАМП не потеряли насущности.
Цель исследования: оценка эффективности препарата Диунорм® (капсулы) в лечении симптомов гиперактивного мочевого пузыря у женщин.
Материалы и методы
В данное клиническое проспективное наблюдательное исследование включены 30 женщин с симптомами ГАМП, 2 из них выбыли из исследования в связи с неявкой на контрольные визиты. В статистический анализ включены результаты обследования 28 женщин. В качестве фармакологического агента для лечения ГАМП использован препарат Диунорм® на регулярной основе по одной капсуле (400 мг) 1 раз в день. Длительность лечения составила 90 дней, таким образом, приверженность терапии Диунорм® в нашем исследовании превысила 93%.
В исследование включены женщины, средний возраст которых составил 35,3 года (95% ДИ: 31,6 – 38,8 лет). Самой молодой пациентке было 29 лет, максимальный возраст – 65 лет. Тест Колмогорова-Смирнова подтвердил нормальный характер распределения (D = 0,1645 при p = 0,0506). У всех пациенток на момент скрининга был установлен диагноз ГАМП, урокультура более 500 тыс. КОЕ/мл, стрессовая инконтиненция, снижение ёмкости мочевого пузыря, тазовый пролапс, отсутствовали воспалительные изменения мочи. Также к критериям исключения были отнесены следующие обстоятельства:
- трудовой распорядок с постоянной или периодической работой в ночное время;
- нуждаются в оперативном лечении или применении любого другого вида неотложного лечения интеркуррентных заболеваний с целью предотвращения прогрессирования заболевания и нанесения вреда здоровью пациента;
- отсутствие ноктурии среди СНМП, предъявляемых пациентам;
- регулярный прием лекарственных средств, приводящих к изменению параметров мочеиспускания в течение периода исследования или изменению исследуемых показателей;
- одновременный прием других препаратов, непосредственно предназначенных для лечения симптомов нижних мочевых путей;
- перенесённые операции на мочеиспускательном канале в течение 3 месяцев до включения в исследование, гистерэктомия или удаление обеих придатков или слинговая операция по поводу стрессовой инконтиненции в анамнезе;
- наличие опухоли мочевого пузыря сейчас или в анамнезе;
- хронический алкоголизм или наркомания;
- психические заболевания;
- острая или хроническая почечная недостаточность любой степени выраженности;
- неспособность пациента адекватно отвечать на вопросы исследователя, заполнять необходимые документы и принимать исследуемый препарат;
- наличие сопутствующих заболеваний в стадии декомпенсации, которые могут повлиять на проведение исследования;
- гиперчувствительность к любому из компонентов исследуемого препарата;
- участие пациента в других клинических исследованиях в течение последнего месяца или в настоящее время.
Кроме того, к неразрешённым к использованию препаратам, которые должны быть отменены как минимум за 2 недели до начала исследования, отнесены экстракты растительного и животного происхождения для лечения нарушений мочеиспускания, диуретики, м-холинолитики и препараты, влияющие на процесс засыпания или изменяющие структуру сна (снотворные, седативные, барбитураты, анксиолитики, антигистаминные, ноотропы).
На первом и вводном визите с разницей не более 5 суток проводили сбор анамнеза, физикальный осмотр (включая кольпоскопию и влагалищное исследование), пациентки заполняли опросник по ГАМП (Overactive Bladder Awareness Tool) и дневник мочеиспускания в течение 3 суток. Дополнительное лабораторное и инструментальное исследования включали анализ мочи, бактериологическое исследование мочи, урофлоуметрию, УЗИ мочевого пузыря (объём (см3), толщина передней стенки мочевого пузыря (мм), объём остаточной мочи (см3)) и цистоскопию.
На основании полученных данных определяли соответствия пациента критериям включения и наличие критериев исключения. При включении в исследование пациентки подписывали информированное согласие на участие и получали все необходимое количество препарата, таким образом, стоимость его не стала причиной выбора или отказа от терапии. Контроль эффективности терапии осуществляли в двух точках (45 и 90 сутки) с отклонением от даты запланированного визита не более 3 суток. Объём обследования включал опросник по ГАМП, дневник мочеиспускания, анализ мочи по Нечипоренко, бактериологическое исследование мочи, урофлоуметрию и УЗИ по протоколу, представленному таблице 1.
Таблица 1. График обследований пациентов
Table 1. Schedule of patient examinations
Примечания: * — допускается отклонение от даты запланированного визита ± 3 дня. СКР — скрининговый визит; ВВ — визит включения; В1 – визит № 1; В2 — визит № 2; ДЗ — досрочное завершение.
Notes: * — deviation from the date of the planned visit is allowed ± 3 days. SV — screening visit; IV — inclusion visit; V1 — visit 1; V2 — visit 2; EC — early completion.
Описание исследуемого препарата. Диунорм® – натуральный комплекс природного происхождения. Стандартная капсула 400 мг содержит: Каланхоэ перистого (Bryophyllum pinnatum) экстракт, Валерианы лекарственной экстракт (Valeriana officinalis L.), стандартизированный по содержанию валереновой кислоты, Солодки голой экстракт (Glycyrrhizia glabra), стандартизированный по содержанию глицирризиновой кислоты. Одна упаковка содержит 30 капсул.
Методы статистического анализа. Нормальность распределения переменных проверялась тестом Колмогорова-Смирнова. Для статистической обработки результатов применялся однофакторный дисперсионный анализ (ANOVA) в статистическом пакете SPSS Statistics v. 23.0. Достоверность различий для переменных с ненормальным распределением определяли непараметрическим критерием Манна-Уитни, статистически значимыми считали различия при вероятности больше 95%.
Результаты
У всех женщин на протяжении исследования были отрицательные результаты посева мочи и отсутствовала пиурия, что исключало инфекционную этиологию нарушений мочеиспускания.
С целью объективизации симптомов гиперактивного мочевого пузыря в нашем исследовании использована русскоязычная версия опросника Overactive Bladder Awareness Tool, которую пациентки заполняли на скрининговом и контрольных визитах на 45 и 90 сутки (табл. 1). Согласно данному опроснику, сумма баллов выше 7 предполагает высокую вероятность наличия гиперактивного мочевого пузыря. Для анализа оказались доступны данные анкетирования 27 пациенток. Все пациентки имели умеренную или выраженную симптоматику с медианой 20 баллов и 95% доверительным интервалом от 12 до 28 баллов (рис. 1). На фоне трехмесячной терапии препаратом Диунорм® мы регистрируем статистически достоверное снижение ирритативной симптоматики. Сумма баллов по опроснику ГАМП через 1,5 и 3 месяца уменьшилась на 3,0 и 4,3 балла, соответственно (p < 0,05, рис. 1). При детальном анализе данных анкетирования можно отметить, что в целом положительная динамика, определяемая по уменьшению суммы баллов, наблюдалась у 75% пациенток. Положительная динамика в отношении ноктурии отмечалась у 82% женщин (р < 0,01).
Рисунок 1. Динамика симптомов ГАМП по опроснику Overactive Bladder Awareness Tool на фоне приёма Диунорма® (СКР: 20,3 ± 4,2 vs Визит 1: 17,25 ± 4,3 vs Визит 2: 15,96 ± 5,4 баллов)
Figure 1. Dynamics of OAB symptoms according to the Overactive Bladder Awareness Tool questionnaire while Diunorm® intake (SV: 20.3 ± 4.2 vs Visit 1: 17.25 ± 4.3 vs Visit 2: 15.96 ± 5.4 points)
Всем пациенткам была выполнена урофлоуметрия на скрининговом визите и на 45 и 90 сутках исследования. При этом средняя скорость мочеиспускания через полтора месяца приёма Диунорма® увеличилась у всех пациенток в среднем на 1,8 мл/с (с 13,3 ± 0,7 до 15,1 ± 0,7 мл/с, р < 0,0001), а через три месяца – на 2,1 мл/с (до 15,4 ± 0,5 мл/с, р < 0,0001, рис. 2). Достоверного различия средних потоков мочи на сроках полтора и три месяца наблюдения обнаружено не было (p = 0,326, рис. 2). При этом эффективность препарата Диунорм® в отношении средней скорости мочеиспускания не зависела от возраста (r = 0,06432, p = 0,7451, рис. 3).
Рисунок 2. Средняя скорость мочеиспускания на фоне приёма Диунорма® (СКР vs Визит 1, p < 0,0001; СКР vs Визит 2, p < 0,0001; Визит 1 vs Визит 2, p = 0,326)
Figure 2. The average urination flow rate (Qave) while Diunorm® intake (SV vs Visit 1, p <0.0001; SV vs Visit 2, p <0.0001; Visit 1 vs Visit 2, p = 0.326)
Рисунок 3. Взаимосвязь средней скорости мочеиспускания и возраста
Figure 3. Relationship between average urination rate and age
Аналогичная тенденция отмечена для максимального потока мочи и объёма остаточной мочи. В первом случае отмечен статистически достоверный рост, во втором – снижение в течение первых полутора месяцев, которые оставались стабильными до конца исследования. Так, максимальный поток мочи при приёме Диунорма® увеличился на 1,5 и 2,2 мл/с через полтора и три месяца соответственно (15,9 ± 0,6 vs 17,4 ± 0,5 vs 18,1 ± 0,4 мл/с). Увеличение максимальной скорости мочеиспускания к завершению исследования составило 13,8%. Различие максимального потока мочи в начале исследования и через полтора месяца было статистически достоверным (p = 0,0025) и эффект сохранился на протяжении последующих полутора месяцев приёма препарата (р = 0,0963, рис. 4). При этом зависимости степени положительного эффекта препарата Диунорм® в отношении максимальной скорости мочеиспускания от возраста обнаружено не было (r = -0,1853 p = 0,3451, рис. 5).
Рисунок 4. Максимальная скорость мочеиспускания на фоне приёма Диунорма® (СКР vs Визит 1, p = 0,0025; СКР vs Визит 2, p < 0,001; Визит 1 vs Визит 2, р = 0,0963)
Figure 4. The maximum urination flow rate (Qmax) while Diunorm® intake (SV vs Visit 1, p = 0.0025; SV vs Visit 2, p <0.001; Visit 1 vs Visit 2, p = 0.0963)
Рисунок 5. Взаимосвязь максимальной скорости мочеиспускания и возраста
Figure 5. Relationship between maximum urination flow rate and age
Как уже было отмечено выше, объём остаточной мочи уменьшался на протяжении всего исследования. При включении в исследование, через полтора и три месяца этот показатель составил 19,9 ± 1,4; 12,2 ± 1,6 и 6,4 ± 1,1 мл соответственно. Таким образом, через три месяца приёма Диунорма® объём остаточной мочи уменьшился в 3,1 раза. Все изменения между контрольными и скрининговым визитами статистически достоверны (p < 0,001). Динамика объёма остаточной мочи отражена на рисунке 6.
Рисунок 6. Динамика объёма остаточной мочи на фоне приёма Диунорма® (СКР vs Визит 1, p < 0,0001; Визит 1 vs Визит 2, p = 0,001; Визит 1 vs Визит 2, p < 0,0001)
Figure 6. Dynamics of the post-void residual urine volume (PVR) during Diunorm® intake (SV vs Visit 1, p <0.0001; Visit 1 vs Visit 2, p = 0.001; Visit 1 vs Visit 2, p <0.0001)
Обсуждение
Достаточно серьёзный спектр нежелательных побочных эффектов, свойственный антимускариновым препаратам и бета-3-агонистам адренорецепторов, обусловил низкую комплаентность данного вида терапии ГАМП [9][10][11] с одной стороны и поиску альтернативных вариантов лечения с другой. За последние десятилетия представлено как минимум шесть исследований высокого уровня (слепые плацебо контролируемые), в которых показана эффективность различных вариантов фитотерапии [12][13][14][15][16]. Другой проблемой терапии первой линии ГАМП является узконаправленное воздействие препарата, а именно влияние на тонус детрузора мочевого пузыря, тогда как ГАМП является, скорее всего, полиэтиологичным синдромом, в формировании которого могут принимать участие корковые, подкорковые и спинальные отделы центральной нервной системы, уротелий и гладкая мускулатура мочевого пузыря, а если мы будем рассматривать причины развития ноктурии, то их количество будет ещё больше [7][17][18][19][20]. Исходя из этих позиций, использование фитопрепаратов открывает дополнительные возможности патогенерической терапии ГАМП.
В ходе трёхмесячного применения препарата Диунорм® мы получили хороший клинический эффект в отношении купирования симптомов нарушенного мочеиспускания. Так, суммарный балл опросника Overactive Bladder Awareness Tool снизился на 21,2%, что сопоставимо с результатами Швейцарского рандомизированного клинического исследования C. Betschart et al. (2013), в котором при использовании экстракта Каланхоэ перистого симптоматика регрессировала на 17,8% [15]. Авторы данного и ряда других экспериментальных исследований связывают эффекты использования экстракта Каланхоэ перистого с прямым миорелаксирующим, а также с возможным блокирующим М3 и агонистическим действием на М2 холинорецепторы стенки мочевого пузыря, что снижает сократимость детрузора на 18,7 – 21,3% от исходного [21][22][23]. Однако нами не отмечено признаков атонии детрузора, напротив, регистрировали достаточно быстрый рост среднего потока мочи, по данным урофлоуметрии (p <0 ,0001, рис. 2), который практически не менялся на промежутке между первым и вторым визитами (р > 0,05, рис. 2). При этом максимальный поток и объём остаточной мочи имели статистически достоверные различия на всех контрольных точках по сравнению со скриниговым визитом (р < 0,05). Полученные результаты мы объясняем достаточно быстрым (до полутора месяцев) достижением терапевтического эффекта, который обусловлен купированием гиперактивности детрузора и связан, с одной стороны, с ростом максимального потока за счёт увеличения ёмкости мочевого пузыря, а с другой – с сокращением времени мочеиспускания.
Возможно, что прирост ёмкости мочевого пузыря и урофлоуметрических показателей связан со стимулирующим эффектом на центральные рецепторы к аденозину, серотонину и ГАМК со стороны другого компонента Диунорм® – Валерианы лекарственной [24][25][26], что также подтверждает участие подкорковых структур в формировании синдрома ГАМП [18][19]. Другим вероятным механизмом компенсации миорелаксирующего и холинолитического действия экстракта Каланхоэ перистого и роста урофлоуметрических показателей может быть стимуляция выработки адипонектина жировой тканью, опосредованная все той же Валерианой лекарственной [27], последний в свою очередь, как было показано на экспериментальной модели in vivo, усиливает сократимость детрузора мочевого пузыря, опосредованную экспрессией кальцийзависимой изоформы ингибитора протеинкиназы C [28].
Рядом исследований показано, что бессонница и депрессия являются непосредственными спутниками детрузорной гиперактивности [7][17][19][29]. Однако авторы далеко не всегда ассоциируют ноктурию с синдромом ГАМП, считая, что ноктурия является следствием астенодепрессивного синдрома и бессонницы [29]. Соответственно, коррекция астено-депрессивного синдрома экстрактами Валерианы лекарственной – ещё один путь в лечении гиперактивности детрузора мочевого пузыря [30][31].
Ночная полиурия, обусловленная сердечнососудистой и почечной патологией, может выступать причиной ноктурии, особенно у пациентов старшей возрастной группы [17][20]. Поэтому определенный положительный эффект препарата Диунорм® вероятно связан с действием экстракта Солодки голой. В состав последнего входят глицирризиновая кислота, бета-ситостерин, флавоноиды (ликвиритином), ликохалконом А. Глицирризиновая кислота вызывает минералокортикоидоподобные эффекты. Глицирризиновая кислота и сапонины Солодки ингибируют 11-β-гидроксистероиддегидрогеназу, приводя к индуцированному кортизолом эффекту минералокортикоидов и, как следствие, к задержке жидкости [32]. Это, по-видимому, уменьшает экскрецию натрия почками [33][34], что приводит к снижению выделения жидкости у пациентов с ночной полиурией и, соответственно, выраженности ноктурии.
Заключение
Препарат Диунорм® показал эффективность в отношении симптомов ГАМП и может стать достойной альтернативой традиционной терапии первой линии ГАМП. Для получения доказательной базы высокого уровня необходимо проведение дальнейших многоцентровых сравнительных исследований.
Список литературы
1. Milsom I, Abrams P, Cardozo L, Roberts RG, Thuroff J, Wein AJ. How widespread are the symptoms of an overactive bladder and how are they managed? A populationbased prevalence study. BJU Int. 2001;87(9):760-6. DOI: 10.1046/j.1464-410x.2001.02228.x
2. Stewart WF, Van Rooyen JB, Cundiff GW, Abrams P, Herzog AR, Corey R, Hunt TL, Wein AJ. Prevalence and burden of overactive bladder in the United States. World J Urol. 2003;20(6):327-36. DOI: 10.1007/s00345-002-0301-4
3. Tubaro A, Palleschi G. Overactive bladder: epidemiology and social impact. Curr Opin Obstet Gynecol. 2005;17(5):507-11. DOI: 10.1097/01.gco.0000183529.26352.52
4. Rubin EB, Buehler AE, Halpern SD. States Worse Than Death Among Hospitalized Patients With Serious Illnesses. JAMA Intern Med. 2016;176(10):1557-1559. DOI: 10.1001/jamainternmed.2016.4362
5. Everaert K, Anderson P, Wood R, Andersson FL, Holm-Larsen T. Nocturia is more bothersome than daytime LUTS: Results from an Observational, Real-life Practice Database including 8659 European and American LUTS patients. Int J Clin Pract. 2018;72(6):e13091. DOI: 10.1111/ijcp.13091
6. Miller PS, Hill H, Andersson FL. Nocturia Work Productivity and Activity Impairment Compared with Other Common Chronic Diseases. Pharmacoeconomics. 2016;34(12):1277-1297. DOI: 10.1007/s40273-016-0441-9
7. Przydacz M, Golabek T, Dudek P, Skalski M, Sobanski J, Klasa K, Gronostaj K, Dudek D, Chlosta P. Overactive Bladder Symptoms Negatively Affect Sleep Quality of Patients With Depression. Int Neurourol J. 2021;25(1):59-68. DOI: 10.5213/inj.2040110.055
8. Пушкарь Д.Ю., Щавелева О.Б. Медикаментозное лечение императивных расстройств мочеиспускания. Фар-матека. 2002;10:9-16.
9. Makhani A, Thake M, Gibson W. Mirabegron in the Treatment of Overactive Bladder: Safety and Efficacy in the Very Elderly Patient. Clin Interv Aging. 2020;15:575-581. DOI: 10.2147/CIA.S174402
10. Vouri SM, Kebodeaux CD, Stranges PM, Teshome BF. Adverse events and treatment discontinuations of antimuscarinics for the treatment of overactive bladder in older adults: A systematic review and meta-analysis. Arch Gerontol Geriatr. 2017;69:77-96. DOI: 10.1016/j.archger.2016.11.006
11. Paquette A, Gou P, Tannenbaum C. Systematic review and meta-analysis: do clinical trials testing antimuscarinic agents for overactive bladder adequately measure central nervous system adverse events? J Am Geriatr Soc. 2011;59(7):1332-9. DOI: 10.1111/j.1532-5415.2011.03473.x
12. Cho A, Eidelberg A, Butler DJ, Danko D, Afshinnekoo E, Mason CE, Chughtai B. Efficacy of Daily Intake of Dried Cranberry 500 mg in Women with Overactive Bladder: A Randomized, Double-Blind, Placebo Controlled Study. J Urol. 2021;205(2):507-513. DOI: 10.1097/JU.0000000000001384
13. Noguchi M, Kakuma T, Tomiyasu K, Kurita Y, Kukihara H, Konishi F, Kumamoto S, Shimizu K, Kondo R, Matsuoka K. Effect of an extract of Ganoderma lucidum in men with lower urinary tract symptoms: a double-blind, placebo-controlled randomized and dose-ranging study. Asian J Androl. 2008;10(4):651-8. DOI: 10.1111/j.1745-7262.2008.00336.x
14. Palleschi G, Carbone A, Ripoli A, Silvestri L, Petrozza V, Zanello PP, Pastore AL. A prospective study to evaluate the efficacy of Cistiquer in improving lower urinary tract symptoms in females with urethral syndrome. Minerva Urol Nefrol. 2014;66(4):225-32. PMID: 25034330
15. Betschart C, von Mandach U, Seifert B, Scheiner D, Perucchini D, Fink D, Geissbuhler V. Randomized, doubleblind placebo-controlled trial with Bryophyllum pinnatum versus placebo for the treatment of overactive bladder in postmenopausal women. Phytomedicine. 2013;20(3-4):351-8. DOI: 10.1016/j.phymed.2012.10.007
16. Xiao DD, Lv JW, Xie X, Jin XW, Lu MJ, Shao Y. The combination of herbal medicine Weng-li-tong with Tolterodine may be better than Tolterodine alone in the treatment of overactive bladder in women: a randomized placebo-controlled prospective trial. BMC Urol. 2016;16(1):49. DOI: 10.1186/s12894-016-0167-1
17. Robinson D, Suman S. Managing nocturia: The multidisciplinary approach. Maturitas. 2018;116:123-129. DOI: 10.1016/j.maturitas.2018.08.007
18. Steers WD, Herschorn S, Kreder KJ, Moore K, Strohbehn K, Yalcin I, Bump RC; Duloxetine OAB Study Group. Duloxetine compared with placebo for treating women with symptoms of overactive bladder. BJU Int. 2007;100(2):337-45. DOI: 10.1111/j.1464-410X.2007.06980.x
19. Sakakibara R, Ito T, Yamamoto T, Uchiyama T, Yamanishi T, Kishi M, Tsuyusaki Y, Tateno F, Katsuragawa S, Kuroki N. Depression, Anxiety and the Bladder. Low Urin Tract Symptoms. 2013;5(3):109-20. DOI: 10.1111/luts.12018
20. Drake NL, Flynn MK, Romero AA, Weidner AC, Amundsen CL. Nocturnal polyuria in women with overactive bladder symptoms and nocturia. Am J Obstet Gynecol. 2005;192(5):1682-6. DOI: 10.1016/j.ajog.2004.11.033
21. Furer K, Eberli D, Betschart C, Brenneisen R, De Mieri M, Hamburger M, Mennet-von Eiff M, Potterat O, Schnelle M, Simoes-Wust AP, von Mandach U. Inhibition of porcine detrusor contractility by the flavonoid fraction of Bryophyllum pinnatum—a potential phytotherapeutic drug for the treatment of the overactive bladder syndrome. Phytomedicine. 2015;22(1):158-64. DOI: 10.1016/j.phymed.2014.11.009
22. Bachmann S, Betschart C, Gerber J, Furer K, Mennet M, Hamburger M, Potterat O, von Mandach U, Simoes-Wust AP. Potential of Bryophyllum pinnatum as a Detrusor Relaxant: An in Vitro Exploratory Study. Planta Med. 2017;83(16):1274-1280. DOI: 10.1055/s-0043-109097
23. Schuler V, Suter K, Furer K, Eberli D, Horst M, Betschart C, Brenneisen R, Hamburger M, Mennet M, Schnelle M, Simoes-Wust AP, von Mandach U. Bryophyllum pinnatum inhibits detrusor contractility in porcine bladder strips—a pharmacological study towards a new treatment option of overactive bladder. Phytomedicine. 2012;19(10):947-51. DOI: 10.1016/j.phymed.2012.05.003
24. Orhan IE. A Review Focused on Molecular Mechanisms of Anxiolytic Effect of Valerina officinalis L. in Connection with Its Phytochemistry through in vitro/in vivo Studies. Curr Pharm Des. 2021. DOI: 10.2174/13816128276662101191 05254. Online ahead of print.
25. Abad VC, Guilleminault C. Insomnia in Elderly Patients: Recommendations for Pharmacological Management. Drugs Aging. 2018;35(9):791-817. DOI: 10.1007/s40266-018-0569-8
26. Savage K, Firth J, Stough C, Sarris J. GABA-modulating phytomedicines for anxiety: A systematic review of preclinical and clinical evidence. Phytother Res. 2018;32(1):3-18. DOI: 10.1002/ptr.5940
27. Harada K, Kato Y, Takahashi J, Imamura H, Nakamura N, Nishina A, Phay N, Tadaishi M, Shimizu M, Kobayashi-Hattori K. The Effect of Methanolic Valeriana officinalis Root Extract on Adipocyte Differentiation and Adiponectin Production in 3T3-L1 Adipocytes. Plant Foods Hum Nutr. 2020;75(1):103-109. DOI: 10.1007/s11130-019-00790-2
28. Nobe K, Fujii A, Saito K, Negoro T, Ogawa Y, Nakano Y, Hashimoto T, Honda K. Adiponectin enhances calcium dependency of mouse bladder contraction mediated by protein kinase Calpha expression. J Pharmacol Exp Ther. 2013;345(1):62-8. DOI: 10.1124/jpet.112.202028
29. Savoie MB, Lee KA, Subak LL, Hernandez C, Schembri M, Fung CH, Grady D, Huang AJ. Beyond the bladder: poor sleep in women with overactive bladder syndrome. Am J Obstet Gynecol. 2020;222(6):600.e1-600.e13. DOI: 10.1016/j.ajog.2019.12.005
30. Choi JH, Lee MJ, Chang Y, Lee S, Kim HJ, Lee SW, Kim YO, Cho IH. Valeriana fauriei Exerts Antidepressant-Like Effects Through Anti-inflammatory and Antioxidant Activities by Inhibiting Brain-Derived Neurotrophic Factor Associated with Chronic Restraint Stress. Rejuvenation Res. 2020;23(3):245-255. DOI: 10.1089/rej.2018.2157
31. Amaral de Brito AP, Galvao de Melo IMDS, El-Bacha RS, Guedes RCA. Valeriana officinalis Counteracts Rotenone Effects on Spreading Depression in the Rat Brain in vivo and Protects Against Rotenone Cytotoxicity Toward Rat Glioma C6 Cells in vitro. Front Neurosci. 2020;14:759. DOI: 10.3389/fnins.2020.00759
32. Isbrucker RA, Burdock GA. Risk and safety assessment on the consumption of Licorice root (Glycyrrhiza sp.), its extract and powder as a food ingredient, with emphasis on the pharmacology and toxicology of glycyrrhizin. Regul Toxicol Pharmacol. 2006;46(3):167-92. DOI: 10.1016/j.yrtph.2006.06.002
33. Best R, Finney R. The anti-inflammatory and antidiuretic actions of fractions obtained from xanthoglabrol. J Pharm Pharmacol. 1961;13(Suppl):107-10. DOI: 10.1111/j.2042-7158.1961.tb10499.x
34. Morris DJ, Souness GW. Protective and specificityconferring mechanisms of mineralocorticoid action. Am J Physiol. 1992;263(5 Pt 2):F759-68. DOI: 10.1152/ajprenal.1992.263.5.F759
Об авторах
С. В. Шкодкин
Белгородская областная клиническая больница Святителя Иоасафа; Белгородский государственный национальный исследовательский университет Минобрнауки России
Россия
Шкодкин Сергей Валентинович — доктор медицинских наук, доцент; профессор кафедры госпитальной хирургии Медицинского института НИУ БелГУ; врач уролог урологического отделения БОКБ Святителя Иоасафа.
308007, Белгород, ул. Нкрасова, д. 8/9; 308015, Белгород, ул. Победы, д. 85.
Тел.: +7 (4722) 50-46-07
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
М. В. Покровский
Белгородский государственный национальный исследовательский университет Минобрнауки России
Россия
Покровский Михаил Владимирович — доктор медицинских наук, профессор; заведующий кафедрой фармакологии, руководитель центра доклинических и клинических исследований Медицинского института.
308015, Белгород, ул. Победы, д. 85.
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
С. С. Красняк
НИИ урологии и интервенционной радологии им. Н.А. Лопаткина -филиал ФГБУ «НМИЦ радиологии» Минздрава России
Россия
Красняк Степан Сергеевич — научный сотрудник отдела андрологии и репродукции человека.
105425, Москва, ул. Парковая 3-я, д. 51, стр. 1.
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
А. В. Полищук
Белгородский государственный национальный исследовательский университет Минобрнауки России; Клиника доктора Фомина — Белгород
Россия
Полищук Алексей Викторович — ассистент кафедры госпитальной хирургии Медицинского института НИУ БелГУ; врач-уролог ООО «КДФ-Белгород»
308015, Белгород, ул. Победы, д. 85; 308000, Белгород, Преображенская, д. 119.
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
С. В. Чирков
Белгородский государственный национальный исследовательский университет Минобрнауки России; Старооскольская окружная больница Святителя Луки Крымского
Россия
Чирков Сергей Викторович — аспирант кафедры госпитальной хирургии Медицинского института НИУ БелГУ; врач-уролог поликлиники №3 ОГБУЗ «Старооскольская окружная больница Святителя Луки Крымского».
308015, Белгород, ул. Победы, д. 85; 309506, Белгородская область, Старый Оскол, ул. Комсомольская, д. 81/14.
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
О. В. Чурикова
Белгородский государственный национальный исследовательский университет Минобрнауки России; Медицинский центр «Промедика»
Россия
Чурикова Ольга Викторовна — соискатель кафедры госпитальной хирургии Медицинского института НИУ БелГУ; врач-уролог медицинского центра ООО «Промедика»
308015, Белгород, ул. Победы, д. 85; 308036, Белгород, ул. Щорса, д. 48А.
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
Н. А. Кравцова
Белгородская областная клиническая больница Святителя Иоасафа
Россия
Кравцова Наталья Анатольевна — врач-уролог клинико-диагностического центра «Энергия жизни»
308027, Белгород, ул. Лермонтова, д. 47А.
Конфликт интересов:
Авторы заявляют об отсутствии конфликта интересов.
Рецензия
Для цитирования:
Шкодкин С.В., Покровский М.В., Красняк С.С., Полищук А.В., Чирков С.В., Чурикова О.В., Кравцова Н.А. Диунорм® в лечении симптомов гиперактивного мочевого пузыря у женщин (предварительные результаты). Вестник урологии. 2021;9(2):100-110. https://doi.org/10.21886/2308-6424-2021-9-2-100-110
For citation:
Shkodkin S.V., Pokrovsky M.V., Krasnyak S.S., Polichuk A.V., Chirkov S.V., Churikova O.V., Kpavtsova N.A. Treatment of overactive bladder symptoms in women with Diunorm®: preliminary results report. Urology Herald. 2021;9(2):100-110.
(In Russ.)
https://doi.org/10.21886/2308-6424-2021-9-2-100-110
Просмотров: 1372
- Шкодкин С.В. – д.м.н. доцент, профессор кафедры госпитальной хирургии Медицинского института ФГАОУ ВО «Белгородский государственный национальный исследовательский университет», врач уролог урологического отделения ОГБУЗ «Белгородская областная клиническая больница Святителя Иоасафа»; Белгород, Россия; РИНЦ AuthorID 482598
- Полищук А.В. – ассистент кафедры госпитальной хирургии Медицинского института ФГАОУ ВПО «Белгородский государственный национальный исследовательский университет», уролог медицинского центра «Клиники Фомина»; Белгород, Россия; РИНЦ AuthorID 1069331
- Чирков С.В. – аспирант кафедры госпитальной хирургии Медицинского института ФГАОУ ВПО «Белгородский государственный национальный исследовательский университет», уролог поликлиника №3 ОГБУЗ «Старооскольская окружная больница Святителя Луки Крымского»; Белгород, Россия
- Чурикова О.В. – соискатель кафедры госпитальной хирургии Медицинского института ФГАОУ ВО «Белгородский государственный национальный исследовательский университет», врач-уролог медицинского центра ООО «Промедика»; Белгород, Россия
- Кравцова Н.А. – врач-уролог медицинского центра «Энергия жизни»; Белгород, Россия
ВВЕДЕНИЕ
Естественный рост населения Земли и увеличение продолжительности жизни ведут к росту в популяции мужчин старшей возрастной группы, что делает проблему симптомов нарушенного мочеиспускания (СНМ) социально значимой [1]. Затраты на медикаментозную терапию в долгосрочной перспективе крайне велики, а используемые в настоящее время медикаментозные препараты, а тем более хирургические опции не лишены побочных эффектов и осложнений [2]. Это является причиной продолжающихся исследований по поиску альтернативных вариантов медикаментозной терапии [2].
Цель исследования: оценить эффективность и безопасность препарата Диунорм® капсулы, в профилактике и лечении нарушенного мочеиспускания у мужчин.
МАТЕРИАЛЫ И МЕТОДЫ
Данное клиническое исследование проведено как проспективное сравнительное наблюдательное когортное на 57 мужчинах с жалобами на СНМ. Пациенты рандомизированы по приему препарата для терапии СНМ. Основную группу наблюдения составили 42 первичных пациента в возрасте от 41 до 67 лет (51,4±7,9 года), для терапии у которых был использован препарат Диунорм® на регулярной основе по одной капсуле (400 мг) 1 раз в день. В контрольную группу вошли 15 пациентов в возрасте от 50 до 64 лет (58,4±3,9 года), в качестве инициальной терапии которым был назначен оригинальный Тамсулозин 0,4 мг 1 раз в сутки в соответствии с существующей рутинной клинической практикой. Длительность наблюдения в обеих группах составила 90 дней. В данное исследование пациенты включены по следующим критериям: объем предстательной железы до 50 см3; объем остаточной мочи менее 50 мл; максимальный поток по урофлоурограмме более 10 мл/сек; интравезикальная простатическая протрузия менее 10 мм; суммарный балл по IPSS 8-25 баллов; ПСА менее 4 нг/мл; отсутствие воспалительных изменений в анализе мочи и отрицательная урокультура.
Критериями исключения на момент 1 визита стали: трудовой распорядок с постоянной или периодической работой в ночное время; получаемая ранее терапия СНМ; необходимость оперативного лечения или применение любого другого вида неотложного лечения интеркуррентных заболеваний с целью предотвращения прогрессирования заболевания и нанесения вреда здоровью пациента; отсутствие ноктурии среди СНМ, предъявляемых пациентом; регулярный прием лекарственных средств, приводящих к изменению параметров мочеиспускания в течение периода исследования или изменению исследуемых показателей за исключением альфа-1-адреноблокаторов (АБ); перенесенные операции на предстательной железе или мочеиспускательном канале; наличие опухоли мочевого пузыря сейчас или в анамнезе; хронический алкоголизм или наркомания; психические заболевания; острая или хроническая почечная недостаточность любой степени выраженности; гиперчувствительность к любому из компонентов исследуемого препарата; нарушение пациентом протокола исследования. Все пациенты на момент включения в исследование подписали информированное согласие.
На первичном визите и до включения в исследование, помимо сбора анамнеза и физикального осмотра, больные заполняли шкалы опросники: Международная система суммарной оценки заболеваний предстательной железы (International Prostate Symptom Score, IPSS), Международный индекс эректильной функции (The international index of erectile function, IIEF-5), дневник мочеиспускания, который пациент вел в течение 3-х суток. Среди лабораторных методов использованы анализ мочи по Нечипоренко, бактериология мочи и определение уровня общего простатспецифического антигена (ПСА). Инструментальная диагностика включала выполнение урофлоуметрии и ультразвукового исследования (УЗИ) мочевого пузыря из трансабдоминального и предстательной железы из ректального доступа. При УЗИ регистрировали исходный объем (мл) и толщину передней стенки мочевого пузыря (мм), объем остаточной мочи (см3), объем предстательной железы (см3) и величину интравезикальной простатической протрузии (мм). Аналогичный лабораторноинструментальный контроль проведен на сроках 45 и 90 суток.
В настоящем исследовании изучена эффективность препарата Диунорм®, который представляет собой натуральный комплекс природного происхождения. Стандартная капсула 400 мг содержит: Каланхоэ перистого (Bryophyllum pinnatum) экстракт – 120 мг, Валерианы лекарственной экстракт (Valeriana officinalis L.) – 160 мг, Солодки голой экстракт (Glycyrrhizia glabra) – 120 мг.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Трое пациентов контрольной группы на сроках 14-е, 21-е и 45-е сутки отказались от приема тамсулозина в связи с эякуляторными расстройствами, что составило 20% от исходно включенных в исследование. Дальнейший анализ проведен для 12 пациентов контроля, закончивших исследование. Все 42 пациента основной группы наблюдения остались комплаентны на протяжении всего периода наблюдения (р<0,01). У пациентов обеих групп наблюдения не отмечено как манифестации симптоматической инфекции мочевыводящих путей, так и бессимптомной бактериурии, что потребовало бы коррекции терапии и исключения из протокола. Также не было отмечено существенной динамики по уровню ПСА, что, видимо, исключает влияние исследуемого препарата на метаболизм тестостерона. Однако для окончательного вывода стоит увеличить сроки наблюдения в основной группе до 12 месяцев.
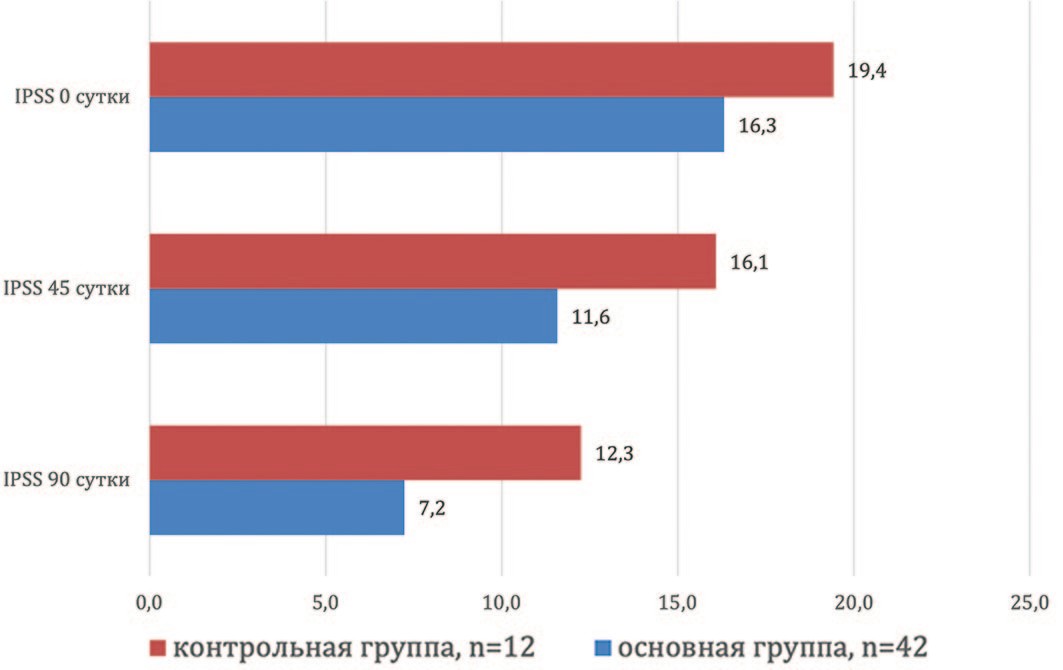
Консервативная терапия СНМ в обеих группах сопровождалась субъективным снижением симптоматики согласно суммарному баллу по шкале IPSS. Так, в основной группе наблюдения данный показатель составил 16,3±1,4, 11,6±1,5 и 7,2±0,8 балла на 0, 45 и 90 сутки исследования, соответственно. Таким образом, отмечено его снижение на 28,4±11,6% и 55,2±6,2% относительно исходного значения (р<0,0001) (рис. 1). Суммарный балл по шкале IPSS в группе контроля на аналогичных сроках наблюдения: 19,4±4,1, 16,1±3,6 и 12,3±5,6 балла. Это обеспечило следующие проценты снижения: 16,8±8,8% и 40,3±15,7% соответственно (р<0,0001) (рис. 1). И хотя относительные скорости снижения суммарного балла по шкале IPSS в группах наблюдения достоверно не различались, абсолютный показатель по шкале IPSS к выходу из эксперимента был ниже в основной группе наблюдения, составив 7,2±0,8 балла против 12,3±5,6 балла в контроле (р<0,05) (рис. 1). Однако полученные нами данные могут быть связаны с исходно более низким значением IPSS в основной группе наблюдения и эффектом малой выборки, что требует дополнительного набора пациентов и повторного анализа по анализируемому показателю
Рис. 1. Динамика снижения суммарного балла по шкале IPSS в группах наблюдения.
Fig. 1 The dynamics of the decrease in the total score on the IPSS scale in the observation groups.
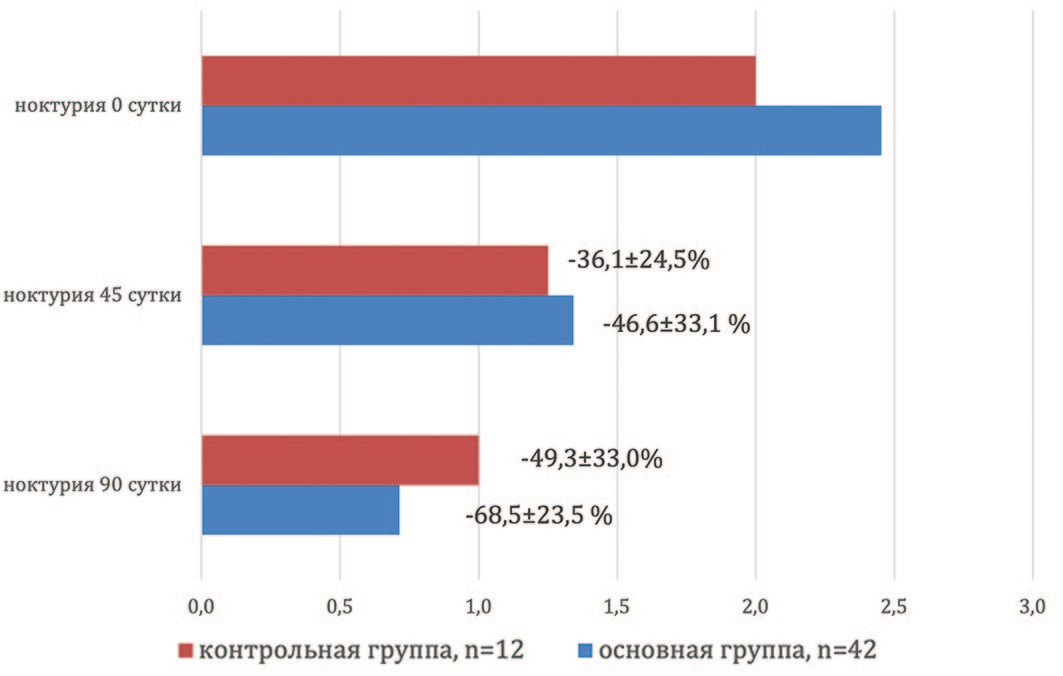
Еще одним из положительных моментов, с нашей точки зрения, является прогрессивное снижение частоты ноктурии в основной группе наблюдения на протяжении всего исследования. Средняя частота ночных мочеиспусканий при включении в исследование в этой группе составила 2,5±0,8 за ночь, через 1,5 месяца данный показатель уменьшился на 46,6±33,1% до 1,3±0,8 (р=0,0039) (рис. 2). Через 3 месяца приема Диунорма частота ночных мочеиспусканий относительно исходных значений уменьшилась на 68,5±23,5% до 0,7±0,5 (р=0,0001) (рис. 2). Подобная динамика имела место и у пациентов, принимающих тамсулозин. Частота ночных мочеиспусканий при контрольных обследованиях на 45-е и 90-е сутки снизилась на 36,1±24,5% и 49,3±33,0%, соответственно (р<0,001) (рис. 2), хотя механизмы воздействия на ноктурию у используемых препаратов различны, что мы попытаемся обсудить ниже.
Рис. 2. Динамика ноктурии в группах наблюдения
Fig. 2. Dynamics of nocturia in observation groups
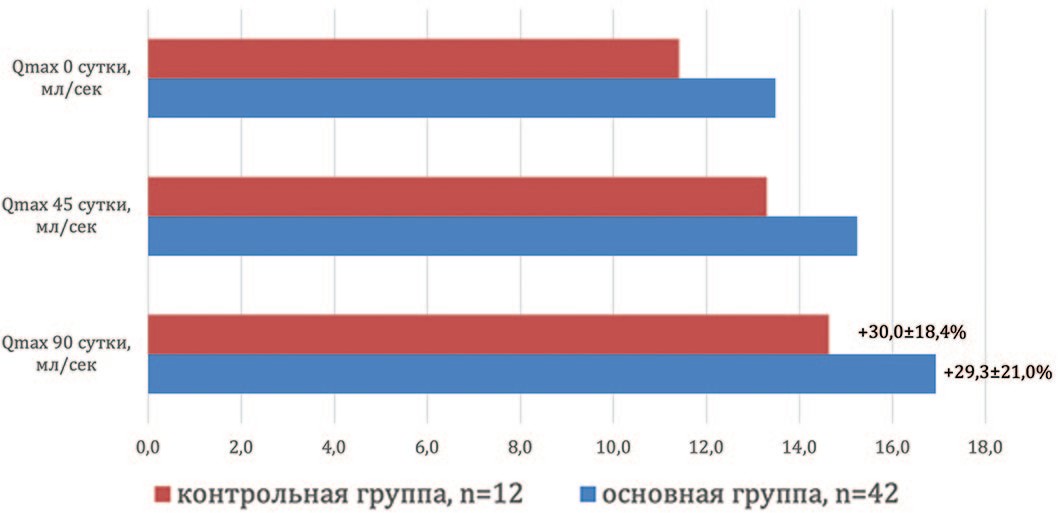
Стоит отметить, что сонографические показатели в обеих исследуемых группах не претерпели статистически достоверных колебаний за весь период наблюдения. Объем предстательной железы в основной группе на контрольных точках исследования составил 41,5±4,1 см3, 40,2±3,9 см3 и 38,7±4,2 см3 и не отличался от аналогичного показателя в контроле – 45,0±6,7 см3, 41,1±4,4 см3 и 40,0±4,0 см3 (р>0,05). Однако стоит остановиться на некоторых тенденциях. Так, в основной группе отмечен статистически недостоверный рост емкости мочевого пузыря с 299,3±64,5 мл при обращении пациента за помощью до 356,7±68,1 мл через 3 месяца терапии, что в среднем составило 31,1±19,4%. При этом в основной группе наблюдения не зарегистрировано роста объема остаточной мочи и снижения урофлоуметрических показателей, что говорит об отсутствии влияния «Диунорма» на контрактильную функцию детрузора. Более того, применительно к объему остаточной мочи для основной группы получено недостоверное снижение показателя, который составил на 0-ые, 45-е и 90-е сутки 29,5±9,8 мл, 21,0±9,2 мл и 12,7±7,7 мл, чего не наблюдалось в контроле 46,9±12,4 мл, 37,5±16,7 мл и 29,2±17,4 мл соответственно (р<0,05). А для максимального потока зарегистрирован достоверный рост у пациентов, принимавших Диунорм, что составило 13,4±0,7 мл/сек, 15,2±0,9 мл/сек и 16,9±0,7 мл/сек на контрольных точках. Таким образом, максимальная скорость мочеиспускания в основной группе увеличилась на 1,8 и 3,5 мл/сек через 1,5 и 3 месяца соответственно. Общий рост за весь период наблюдения в среднем составил 29,3±21,0% (р<0,001) (рис. 3).
Рис.3. Динамика увеличения максимальной скорости потока мочи Qmax в группах наблюдения
Fig. 3. The dynamics of the increase in the maximum flow Qmax in the observation groups
Анализ опросника IIEF-5 не выявил какой-либо динамики в группах наблюдения на протяжении 3 месяцев (p>0,05). Однако при оценке эякуляторной функции в контрольной группе еще 4 пациента пожаловались на анэякуляцию. Таким образом, с тремя пациентами, покинувшими исследование по этим же причинам, частота расстройств эякуляции на фоне приема тамсулозина составила 46,7%, что достоверно больше, чем в основной группе наблюдения (р<0,0001), при этом в 42,9% из них это стало причиной отказа от приема препарата.
Рандомизация в протоколе проводилась по желанию пациента после ознакомления с возможными вариантами лечения. Обращает внимание тот факт, что, несмотря на ограничительные по возрасту критерии включения, в основную группу вошла более молодая часть пациентов 51,4±7,9 лет против 58,4±3,9 лет в контроле. И хотя различия не являются статистически достоверными (р>0,05), можно заключить, что «молодые» пациенты не спешат прибегнуть к всесторонне исследованному фармакологическому препарату взамен на средство растительного происхождения.
В нашем исследовании в основной группе наблюдения отмечена более выраженная, хотя статистически не достоверная, тенденция по купированию ноктурии по сравнению с контролем (рис. 2).
Естественно, окончательные выводы о возможных преимуществах терапии препаратом Диунорм будет возможно сделать при увеличении числа наблюдений. Однако на этом этапе мы склонны ассоциировать положительное влияние на ноктурию не только с воздействием на гладкую мускулатуру детрузора за счет блокады М3-холинорецепторов и прямым миорелаксирующим действием, что показано в исследованиях [3-5] по экстракту Каланхоэ перистого (Bryophyllum pinnatum). Частота ночных микций может быть снижена вследствие нормализации сна и снижении диуретического эффекта. В ряде исследований было показано, что экстракт Валерианы (Valeriana officinalis L.), включающий масла изовалериановой и валериановой кислот и тритерпеновые гликозиды, способен улучшать высвобождение и нарушать обратный нейрональный захват гамма-аминомасляной кислоты (ГАМК) [6], а также выступать агонистом серотониновых и аденозиновых рецепторов в центральной нервной системе [7, 8]. Это способствует нормализации сна, снижая вероятность спонтанных пробуждений [9, 10]. Экстракт Солодки голой (Glycyrrhiza glabra) в качестве действующих веществ содержит глицирризиновую кислоту, бета-ситостерин, ликвиритин, ликохалкон А, у которых описаны минералокортикоидные эффекты и повышение секреции Na-уретического пептида [11, 12]. Это достоверно снижает экскрецию воды и натрия из организма [13].
Вышеописанные механизмы реализуют также снижение симптоматики по шкале IPSS. Достаточно позитивным моментом можно считать увеличение максимальной скорости потока мочи на фоне увеличения емкости мочевого пузыря в основной группе наблюдения, что, как уже отмечали выше, говорит о сохранности сократительной функции детрузора.
ВЫВОДЫ
Комплекс Диунорм достоверно и сопоставимо с альфа-блокатором тамсулозином снижает выраженность СНМ и частоту ноктурии у первичных молодых пациентов, не вызывая при этом эякуляторных расстройств. Мы не призываем экстраполировать полученные результаты на всех мужчин с СНМ, однако, в группе «молодых» пациентов с наличием ноктурии и желанием избежать анэякуляции данный подход может быть эффективным инструментом коррекции расстройств мочеиспускания.
ЛИТЕРАТУРА
- Vos T, Flaxman AD, Naghavi M, et al. Years lived with disability (YLDs) for 1160 sequelae of 289 diseases and injuries 1990-2010: a systematic analysis for the Global Burden of Disease Study 2010. Lancet 2012;(380):2163-96. https://doi.org/10.1016/S0140-6736(12)61729-2.
- Dahm P, Brasure M, MacDonald R, Olson CM, Nelson VA, Fink HA, Rwabasonga B, Risk MC, Wilt TJ. Comparative Effectiveness of Newer Medications for Lower Urinary Tract Symptoms Attributed to Benign Prostatic Hyperplasia: A Systematic Review and Meta-analysis. Eur Urol 2017 Apr;71(4):570-581. https://doi.org/10.1016/j.eururo.2016.09.032.
- Schuler V, et al. Bryophyllum pinnatum inhibits detrusor contractility in porcine bladder strips – A pharmacological study towards a new treatment option of overactive bladder. Phytomedicine 2012;19(10):947–951.
- Fürer K, et al. Inhibition of porcine detrusor contractility by the flavonoid fraction of Bryophyllum pinnatum – A potential phytotherapeutic drug for the treatment of the overactive bladder syndrome. Phytomedicine 2015;22(1):158–164.
- Bachmann S., et al. Potential of Bryophyllum pinnatum as a Detrusor Relaxant: An in Vitro Exploratory Study. Planta Med 2017; 83(16):1274–1280.
- Santos M.S., et al. Synaptosomal GABA release as influenced by valerian root extract—involvement of the GABA carrier. Arch Int Pharmacodyn. Thérapie 1994.
- Dietz B.M., et al. Valerian extract and valerenic acid are partial agonists of the 5-HT5areceptor in vitro. Mol Brain Res 2005;138(2):191–197.
- Müller C.E., et al. Interactions of valerian extracts and a fixed valerian-hop extract combination with adenosine receptors. Life Sci 2002;71(16):1939–1949.
- Ziegler G. et al. Efficacy and tolerability of valerian extract LI 156 compared with oxazepam in the treatment of non-organic insomnia—a randomized, double-blind, comparative clinical study. Eur J Med Res 2002; 71(16):1939–1949.
- Herrera-Arellano A., et al. Polysomnographic Evaluation of the Hypnotic Effect of Valeriana edulis Standardized Extract in Patients Suffering from Insomnia. Planta Med 2001;67(08):695–699.
- Isbrucker R.A., Burdock G.A. Risk and safety assessment on the consumption of Licorice root (Glycyrrhiza sp.), its extract and powder as a food ingredient, with emphasis on the pharmacology and toxicology of glycyrrhizin. Regul Toxicol Pharmacol 2006;46(3):167–192.
- FORSLUND T., et al. Effects of licorice on plasma atrial natriuretic peptide in healthy volunteers. J Intern Med 1989.
- Best R., Finney R. The anti-inflammatory and antidiuretic actions of fractions obtained from xanthoglabrol. J Pharm Pharmacol 1961; 13(Suppl):107–110.
Тематики и теги
Журнал
-
Артикул:
1000352817
-
Производитель:
ЭсЭйч Фарма
-
Страна происхождения:
США
-
Срок годности:
24 месяца
Доставка в аптеку
Доставка в любую аптеку бесплатно
Наличие в аптеках
Онлайн цены и цены в аптеках могут отличаться.
Найти в аптеке
Описание товара
«Диунорм» служит источником глицирризиновой кислоты и флавоноидов. Назначается как часть комплексной терапии при лечении нейрогенных расстройств мочеиспускания. Препарат поможет наладить работу мочевого пузыря, снижает его активность в ночные часы, обеспечит более спокойный сон ночью без позывов к мочеиспусканию. Состав препарата полностью растительный, это экстракты валерианы, солодки и каланхоэ.
Диунорм выпускается в капсулах, для эффекта рекомендуется курсовой прием в течение месяца. Не следует принимать в период беременности и кормления грудью.
Характеристики
Тип товара
Капсулы
Бренд
Направленность
Для почек
Форма выпуска
Капсулы
Описание лекарственной формы
Капсулы.
Показания препарата
Рекомендовано в качестве биологически активной добавки к пище, источника глицирризиновой кислоты, валереновой кислоты, флавоноидов и полифенольных соединений.
Противопоказания
Индивидуальная непереносимость компонентов продукта, беременность и кормление грудью. Перед применением необходимо проконсультироваться с врачом.
Применение при беременности/кормлении грудью
Противопоказано применение при беременности и в период грудного вскармливания.
Способ применения
Взрослым принимать по 1 капсуле 1 раз в день, во время еды. Продолжительность приема — 1 месяц. При необходимости прием можно повторить.
Фармакодинамика
Компоненты комплекса способствуют уменьшению числа ночных пробуждений, уменьшению выделения жидкости в ночное время, устранению гиперактивности мочевого пузыря.
Меры предосторожности
Перед применением рекомендуется проконсультироваться с врачом.
ОКПД2
10.89.19.210
Тип упаковки
картонная упаковка
Срок годности
2 года
Для цитирования:
Шкодкин С.В., Полищук А.В., Чирков С.В., Чурикова О.В., Кравцова Н.А. Коррекция симптомов нарушенного мочеиспускания у мужчин препаратом Диунорм®. Экспериментальная и клиническая урология 2020(4):76-80. https://doi.org/10.29188/2222-8543-2020-13-4-76-80
ВВЕДЕНИЕ
Естественный рост населения Земли и увеличение продолжительности жизни ведут к росту в популяции мужчин старшей возрастной группы, что делает проблему симптомов нарушенного мочеиспускания (СНМ) социально значимой [1]. Затраты на медикаментозную терапию в долгосрочной перспективе крайне велики, а используемые в настоящее время медикаментозные препараты, а тем более хирургические опции не лишены побочных эффектов и осложнений [2]. Это является причиной продолжающихся исследований по поиску альтернативных вариантов медикаментозной терапии [2].
Цель исследования: оценить эффективность и безопасность препарата Диунорм® капсулы, в профилактике и лечении нарушенного мочеиспускания у мужчин.
МАТЕРИАЛЫ И МЕТОДЫ
Данное клиническое исследование проведено как проспективное сравнительное наблюдательное когортное на 57 мужчинах с жалобами на СНМ. Пациенты рандомизированы по приему препарата для терапии СНМ. Основную группу наблюдения составили 42 первичных пациента в возрасте от 41 до 67 лет (51,4±7,9 года), для терапии у которых был использован препарат Диунорм® на регулярной основе по одной капсуле (400 мг) 1 раз в день. В контрольную группу вошли 15 пациентов в возрасте от 50 до 64 лет (58,4±3,9 года), в качестве инициальной терапии которым был назначен оригинальный Тамсулозин 0,4 мг 1 раз в сутки в соответствии с существующей рутинной клинической практикой. Длительность наблюдения в обеих группах составила 90 дней. В данное исследование пациенты включены по следующим критериям: объем предстательной железы до 50 см3; объем остаточной мочи менее 50 мл; максимальный поток по урофлоурограмме более 10 мл/сек; интравезикальная простатическая протрузия менее 10 мм; суммарный балл по IPSS 8-25 баллов; ПСА менее 4 нг/мл; отсутствие воспалительных изменений в анализе мочи и отрицательная урокультура.
Критериями исключения на момент 1 визита стали: трудовой распорядок с постоянной или периодической работой в ночное время; получаемая ранее терапия СНМ; необходимость оперативного лечения или применение любого другого вида неотложного лечения интеркуррентных заболеваний с целью предотвращения прогрессирования заболевания и нанесения вреда здоровью пациента; отсутствие ноктурии среди СНМ, предъявляемых пациентом; регулярный прием лекарственных средств, приводящих к изменению параметров мочеиспускания в течение периода исследования или изменению исследуемых показателей за исключением альфа-1-адреноблокаторов (АБ); перенесенные операции на предстательной железе или мочеиспускательном канале; наличие опухоли мочевого пузыря сейчас или в анамнезе; хронический алкоголизм или наркомания; психические заболевания; острая или хроническая почечная недостаточность любой степени выраженности; гиперчувствительность к любому из компонентов исследуемого препарата; нарушение пациентом протокола исследования. Все пациенты на момент включения в исследование подписали информированное согласие.
На первичном визите и до включения в исследование, помимо сбора анамнеза и физикального осмотра, больные заполняли шкалы опросники: Международная система суммарной оценки заболеваний предстательной железы (International Prostate Symptom Score, IPSS), Международный индекс эректильной функции (The international index of erectile function, IIEF-5), дневник мочеиспускания, который пациент вел в течение 3-х суток. Среди лабораторных методов использованы анализ мочи по Нечипоренко, бактериология мочи и определение уровня общего простатспецифического антигена (ПСА). Инструментальная диагностика включала выполнение урофлоуметрии и ультразвукового исследования (УЗИ) мочевого пузыря из трансабдоминального и предстательной железы из ректального доступа. При УЗИ регистрировали исходный объем (мл) и толщину передней стенки мочевого пузыря (мм), объем остаточной мочи (см3), объем предстательной железы (см3) и величину интравезикальной простатической протрузии (мм). Аналогичный лабораторноинструментальный контроль проведен на сроках 45 и 90 суток.
В настоящем исследовании изучена эффективность препарата Диунорм®, который представляет собой натуральный комплекс природного происхождения. Стандартная капсула 400 мг содержит: Каланхоэ перистого (Bryophyllum pinnatum) экстракт – 120 мг, Валерианы лекарственной экстракт (Valeriana officinalis L.) – 160 мг, Солодки голой экстракт (Glycyrrhizia glabra) – 120 мг.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Трое пациентов контрольной группы на сроках 14-е, 21-е и 45-е сутки отказались от приема тамсулозина в связи с эякуляторными расстройствами, что составило 20% от исходно включенных в исследование. Дальнейший анализ проведен для 12 пациентов контроля, закончивших исследование. Все 42 пациента основной группы наблюдения остались комплаентны на протяжении всего периода наблюдения (р<0,01). У пациентов обеих групп наблюдения не отмечено как манифестации симптоматической инфекции мочевыводящих путей, так и бессимптомной бактериурии, что потребовало бы коррекции терапии и исключения из протокола. Также не было отмечено существенной динамики по уровню ПСА, что, видимо, исключает влияние исследуемого препарата на метаболизм тестостерона. Однако для окончательного вывода стоит увеличить сроки наблюдения в основной группе до 12 месяцев.
Консервативная терапия СНМ в обеих группах сопровождалась субъективным снижением симптоматики согласно суммарному баллу по шкале IPSS. Так, в основной группе наблюдения данный показатель составил 16,3±1,4, 11,6±1,5 и 7,2±0,8 балла на 0, 45 и 90 сутки исследования, соответственно. Таким образом, отмечено его снижение на 28,4±11,6% и 55,2±6,2% относительно исходного значения (р<0,0001) (рис. 1). Суммарный балл по шкале IPSS в группе контроля на аналогичных сроках наблюдения: 19,4±4,1, 16,1±3,6 и 12,3±5,6 балла. Это обеспечило следующие проценты снижения: 16,8±8,8% и 40,3±15,7% соответственно (р<0,0001) (рис. 1). И хотя относительные скорости снижения суммарного балла по шкале IPSS в группах наблюдения достоверно не различались, абсолютный показатель по шкале IPSS к выходу из эксперимента был ниже в основной группе наблюдения, составив 7,2±0,8 балла против 12,3±5,6 балла в контроле (р<0,05) (рис. 1). Однако полученные нами данные могут быть связаны с исходно более низким значением IPSS в основной группе наблюдения и эффектом малой выборки, что требует дополнительного набора пациентов и повторного анализа по анализируемому показателю
Рис. 1. Динамика снижения суммарного балла по шкале IPSS в группах наблюдения.
Fig. 1 The dynamics of the decrease in the total score on the IPSS scale in the observation groups.
Еще одним из положительных моментов, с нашей точки зрения, является прогрессивное снижение частоты ноктурии в основной группе наблюдения на протяжении всего исследования. Средняя частота ночных мочеиспусканий при включении в исследование в этой группе составила 2,5±0,8 за ночь, через 1,5 месяца данный показатель уменьшился на 46,6±33,1% до 1,3±0,8 (р=0,0039) (рис. 2). Через 3 месяца приема Диунорма частота ночных мочеиспусканий относительно исходных значений уменьшилась на 68,5±23,5% до 0,7±0,5 (р=0,0001) (рис. 2). Подобная динамика имела место и у пациентов, принимающих тамсулозин. Частота ночных мочеиспусканий при контрольных обследованиях на 45-е и 90-е сутки снизилась на 36,1±24,5% и 49,3±33,0%, соответственно (р<0,001) (рис. 2), хотя механизмы воздействия на ноктурию у используемых препаратов различны, что мы попытаемся обсудить ниже.
Рис. 2. Динамика ноктурии в группах наблюдения
Fig. 2. Dynamics of nocturia in observation groups
Стоит отметить, что сонографические показатели в обеих исследуемых группах не претерпели статистически достоверных колебаний за весь период наблюдения. Объем предстательной железы в основной группе на контрольных точках исследования составил 41,5±4,1 см3, 40,2±3,9 см3 и 38,7±4,2 см3 и не отличался от аналогичного показателя в контроле – 45,0±6,7 см3, 41,1±4,4 см3 и 40,0±4,0 см3 (р>0,05). Однако стоит остановиться на некоторых тенденциях. Так, в основной группе отмечен статистически недостоверный рост емкости мочевого пузыря с 299,3±64,5 мл при обращении пациента за помощью до 356,7±68,1 мл через 3 месяца терапии, что в среднем составило 31,1±19,4%. При этом в основной группе наблюдения не зарегистрировано роста объема остаточной мочи и снижения урофлоуметрических показателей, что говорит об отсутствии влияния «Диунорма» на контрактильную функцию детрузора. Более того, применительно к объему остаточной мочи для основной группы получено недостоверное снижение показателя, который составил на 0-ые, 45-е и 90-е сутки 29,5±9,8 мл, 21,0±9,2 мл и 12,7±7,7 мл, чего не наблюдалось в контроле 46,9±12,4 мл, 37,5±16,7 мл и 29,2±17,4 мл соответственно (р<0,05). А для максимального потока зарегистрирован достоверный рост у пациентов, принимавших Диунорм, что составило 13,4±0,7 мл/сек, 15,2±0,9 мл/сек и 16,9±0,7 мл/сек на контрольных точках. Таким образом, максимальная скорость мочеиспускания в основной группе увеличилась на 1,8 и 3,5 мл/сек через 1,5 и 3 месяца соответственно. Общий рост за весь период наблюдения в среднем составил 29,3±21,0% (р<0,001) (рис. 3).
Рис.3. Динамика увеличения максимальной скорости потока мочи Qmax в группах наблюдения
Fig. 3. The dynamics of the increase in the maximum flow Qmax in the observation groups
Анализ опросника IIEF-5 не выявил какой-либо динамики в группах наблюдения на протяжении 3 месяцев (p>0,05). Однако при оценке эякуляторной функции в контрольной группе еще 4 пациента пожаловались на анэякуляцию. Таким образом, с тремя пациентами, покинувшими исследование по этим же причинам, частота расстройств эякуляции на фоне приема тамсулозина составила 46,7%, что достоверно больше, чем в основной группе наблюдения (р<0,0001), при этом в 42,9% из них это стало причиной отказа от приема препарата.
Рандомизация в протоколе проводилась по желанию пациента после ознакомления с возможными вариантами лечения. Обращает внимание тот факт, что, несмотря на ограничительные по возрасту критерии включения, в основную группу вошла более молодая часть пациентов 51,4±7,9 лет против 58,4±3,9 лет в контроле. И хотя различия не являются статистически достоверными (р>0,05), можно заключить, что «молодые» пациенты не спешат прибегнуть к всесторонне исследованному фармакологическому препарату взамен на средство растительного происхождения.
В нашем исследовании в основной группе наблюдения отмечена более выраженная, хотя статистически не достоверная, тенденция по купированию ноктурии по сравнению с контролем (рис. 2).
Естественно, окончательные выводы о возможных преимуществах терапии препаратом Диунорм будет возможно сделать при увеличении числа наблюдений. Однако на этом этапе мы склонны ассоциировать положительное влияние на ноктурию не только с воздействием на гладкую мускулатуру детрузора за счет блокады М3-холинорецепторов и прямым миорелаксирующим действием, что показано в исследованиях [3-5] по экстракту Каланхоэ перистого (Bryophyllum pinnatum). Частота ночных микций может быть снижена вследствие нормализации сна и снижении диуретического эффекта. В ряде исследований было показано, что экстракт Валерианы (Valeriana officinalis L.), включающий масла изовалериановой и валериановой кислот и тритерпеновые гликозиды, способен улучшать высвобождение и нарушать обратный нейрональный захват гамма-аминомасляной кислоты (ГАМК) [6], а также выступать агонистом серотониновых и аденозиновых рецепторов в центральной нервной системе [7, 8]. Это способствует нормализации сна, снижая вероятность спонтанных пробуждений [9, 10]. Экстракт Солодки голой (Glycyrrhiza glabra) в качестве действующих веществ содержит глицирризиновую кислоту, бета-ситостерин, ликвиритин, ликохалкон А, у которых описаны минералокортикоидные эффекты и повышение секреции Na-уретического пептида [11, 12]. Это достоверно снижает экскрецию воды и натрия из организма [13].
Вышеописанные механизмы реализуют также снижение симптоматики по шкале IPSS. Достаточно позитивным моментом можно считать увеличение максимальной скорости потока мочи на фоне увеличения емкости мочевого пузыря в основной группе наблюдения, что, как уже отмечали выше, говорит о сохранности сократительной функции детрузора.
ВЫВОДЫ
Комплекс Диунорм достоверно и сопоставимо с альфа-блокатором тамсулозином снижает выраженность СНМ и частоту ноктурии у первичных молодых пациентов, не вызывая при этом эякуляторных расстройств. Мы не призываем экстраполировать полученные результаты на всех мужчин с СНМ, однако, в группе «молодых» пациентов с наличием ноктурии и желанием избежать анэякуляции данный подход может быть эффективным инструментом коррекции расстройств мочеиспускания.
ЛИТЕРАТУРА
- Vos T, Flaxman AD, Naghavi M, et al. Years lived with disability (YLDs) for 1160 sequelae of 289 diseases and injuries 1990-2010: a systematic analysis for the Global Burden of Disease Study 2010. Lancet 2012;(380):2163-96. https://doi.org/10.1016/S0140-6736(12)61729-2.
- Dahm P, Brasure M, MacDonald R, Olson CM, Nelson VA, Fink HA, Rwabasonga B, Risk MC, Wilt TJ. Comparative Effectiveness of Newer Medications for Lower Urinary Tract Symptoms Attributed to Benign Prostatic Hyperplasia: A Systematic Review and Meta-analysis. Eur Urol 2017 Apr;71(4):570-581. https://doi.org/10.1016/j.eururo.2016.09.032.
- Schuler V, et al. Bryophyllum pinnatum inhibits detrusor contractility in porcine bladder strips – A pharmacological study towards a new treatment option of overactive bladder. Phytomedicine 2012;19(10):947–951.
- Fürer K, et al. Inhibition of porcine detrusor contractility by the flavonoid fraction of Bryophyllum pinnatum – A potential phytotherapeutic drug for the treatment of the overactive bladder syndrome. Phytomedicine 2015;22(1):158–164.
- Bachmann S., et al. Potential of Bryophyllum pinnatum as a Detrusor Relaxant: An in Vitro Exploratory Study. Planta Med 2017; 83(16):1274–1280.
- Santos M.S., et al. Synaptosomal GABA release as influenced by valerian root extract—involvement of the GABA carrier. Arch Int Pharmacodyn. Thérapie 1994.
- Dietz B.M., et al. Valerian extract and valerenic acid are partial agonists of the 5-HT5areceptor in vitro. Mol Brain Res 2005;138(2):191–197.
- Müller C.E., et al. Interactions of valerian extracts and a fixed valerian-hop extract combination with adenosine receptors. Life Sci 2002;71(16):1939–1949.
- Ziegler G. et al. Efficacy and tolerability of valerian extract LI 156 compared with oxazepam in the treatment of non-organic insomnia—a randomized, double-blind, comparative clinical study. Eur J Med Res 2002; 71(16):1939–1949.
- Herrera-Arellano A., et al. Polysomnographic Evaluation of the Hypnotic Effect of Valeriana edulis Standardized Extract in Patients Suffering from Insomnia. Planta Med 2001;67(08):695–699.
- Isbrucker R.A., Burdock G.A. Risk and safety assessment on the consumption of Licorice root (Glycyrrhiza sp.), its extract and powder as a food ingredient, with emphasis on the pharmacology and toxicology of glycyrrhizin. Regul Toxicol Pharmacol 2006;46(3):167–192.
- FORSLUND T., et al. Effects of licorice on plasma atrial natriuretic peptide in healthy volunteers. J Intern Med 1989.
- Best R., Finney R. The anti-inflammatory and antidiuretic actions of fractions obtained from xanthoglabrol. J Pharm Pharmacol 1961; 13(Suppl):107–110.
| Прикрепленный файл | Размер |
|---|---|
| Скачать статью | 938.24 кб |
Ключевые слова:
симптомы нарушенного мочеиспускания, симптомы нижних мочевых путей, СНМП, доброкачественная гиперплазия предстательной железы, ДГПЖ.
Описание препарата Диувер (таблетки, 10 мг) основано на официальной инструкции, утверждено компанией-производителем в 2022 году
Дата согласования: 28.03.2022
Особые отметки:
Содержание
- Фотографии упаковок
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Заказ в аптеках Москвы
- Отзывы
Фотографии упаковок

28.03.2022
Действующее вещество
ATX
Фармакологическая группа
Состав
| Таблетки | 1 табл. |
| активное вещество: | |
| торасемид | 5,00/10,00 мг |
| вспомогательные вещества: лактозы моногидрат — 58,44/116,88 мг; крахмал кукурузный — 14,56/29,12 мг; карбоксиметилкрахмал натрия — 0,80/1,60 мг; кремния диоксид коллоидный безводный — 0,60/1,20 мг; магния стеарат — 0,60/1,20 мг |
Описание лекарственной формы
Таблетки, 5 мг: белые или почти белые круглые двояковыпуклые таблетки с фаской, с риской на одной стороне и гравировкой «915» на другой стороне.
Таблетки, 10 мг: белые или почти белые круглые двояковыпуклые таблетки с фаской, с риской на одной стороне и гравировкой «916» на другой стороне.
Фармакологическое действие
Фармакологическое действие
—
диуретическое.
Фармакодинамика
Торасемид является петлевым диуретиком. Максимальный диуретический эффект развивается спустя 2–3 ч после приема препарата внутрь. Основной механизм действия препарата обусловлен обратимым связыванием торасемида с контранспортером ионов натрия/хлора/калия, расположенным в апикальной мембране толстого сегмента восходящей части петли Генле, в результате чего снижается или полностью ингибируется реабсорбция ионов натрия и уменьшается осмотическое давление внутриклеточной жидкости и реабсорбция воды. Блокирует альдостероновые рецепторы миокарда, уменьшает фиброз и улучшает диастолическую функцию миокарда.
Торасемид в меньшей степени, чем фуросемид, вызывает гипокалиемию, при этом он проявляет бóльшую активность, и его действие более продолжительно.
Применение торасемида является наиболее обоснованным выбором для проведения длительной терапии.
Фармакокинетика
После приема внутрь торасемид быстро и практически полностью всасывается в ЖКТ. Cmax торасемида в плазме крови отмечается через 1–2 ч после приема внутрь после еды. Биодоступность составляет 80–90% с незначительными индивидуальными вариациями.
Диуретический эффект сохраняется до 18 ч, что облегчает переносимость терапии из-за отсутствия очень частого мочеиспускания в первые часы после приема препарата внутрь, ограничивающего активность пациентов.
Связь с белками плазмы крови более 99%. Видимый Vd составляет 16 л.
Метаболизируется в печени с помощью изоферментов системы цитохрома Р450. В результате последовательных реакций окисления, гидроксилирования или кольцевого гидроксилирования образуются три метаболита (M1, М3 и М5), которые связываются с белками плазмы крови на 86, 95 и 97% соответственно.
T1/2 торасемида и его метаболитов составляет 3–4 ч и не изменяется при ХПН. Общий клиренс торасемида составляет 40 мл/мин, почечный клиренс — 10 мл/мин. В среднем около 83% от принятой дозы выводится почками: в неизмененном виде (24%) и в виде преимущественно неактивных метаболитов (M1 — 12%, М3 — 3%, М5 — 41%).
При почечной недостаточности T1/2 не изменяется, T1/2 метаболитов МЗ и М5 увеличивается. Торасемид и его метаболиты незначительно выводятся с помощью гемодиализа и гемофильтрации.
При печеночной недостаточности концентрация торасемида в плазме крови повышается вследствие снижения метаболизма препарата в печени. У пациентов с сердечной или печеночной недостаточностью T1/2 торасемида и метаболита М5 незначительно увеличен, кумуляция препарата маловероятна.
Показания
отечный синдром различного генеза, в т.ч. при хронической сердечной недостаточности, заболеваниях печени, легких и почек;
артериальная гипертензия.
Противопоказания
повышенная чувствительность к торасемиду или любому из компонентов препарата;
аллергия на сульфонамиды (сульфаниламидные противомикробные средства или препараты сульфонилмочевины);
почечная недостаточность с анурией;
печеночная кома и прекома;
выраженная гипокалиемия;
выраженная гипонатриемия;
гиповолемия (с артериальной гипотензией или без нее) или дегидратация;
резко выраженные нарушения оттока мочи любой этиологии (включая одностороннее поражение мочевыводящих путей);
гликозидная интоксикация;
острый гломерулонефрит;
декомпенсированный аортальный и митральный стеноз, гипертрофическая обструктивная кардиомиопатия;
повышение центрального венозного давления (свыше 10 мм рт. ст.);
гиперурикемия;
непереносимость лактозы, дефицит лактазы или глюкозо-галактозная мальабсорбция;
период лактации;
возраст до 18 лет.
С осторожностью: артериальная гипотензия; стенозирующий атеросклероз церебральных артерий; гипопротеинемия; предрасположенность к гиперурикемии; нарушения оттока мочи (доброкачественная гиперплазия предстательной железы, сужение мочеиспускательного канала или гидронефроз); желудочковая аритмия в анамнезе; острый инфаркт миокарда (увеличение риска развития кардиогенного шока); диарея; панкреатит; сахарный диабет (снижение толерантности к глюкозе); гепаторенальный синдром; подагра; анемия; беременность.
Применение при беременности и кормлении грудью
Торасемид не обладает тератогенным эффектом и фетотоксичностью, проникает через плацентарный барьер, вызывая нарушения водно-электролитного обмена и тромбоцитопению у плода.
Препарат Диувер во время беременности можно применять только в том случае, когда польза для матери превышает потенциальный риск для плода, только под контролем врача и только в минимальных дозах.
Неизвестно, проникает ли торасемид в грудное молоко. При необходимости применения препарата Диувер в период лактации необходимо прекратить грудное вскармливание.
Способ применения и дозы
Внутрь, один раз в день, после завтрака, запивая небольшим количеством воды.
Отечный синдром различного генеза, в т.ч. при ХСН, заболеваниях печени, легких и почек
Обычная терапевтическая доза составляет 5 мг внутрь один раз в день. При необходимости дозу следует постепенно увеличить до 20–40 мг один раз в день, в отдельных случаях — до 200 мг в день. Препарат назначают на длительный период или до момента исчезновения отеков.
Артериальная гипертензия
Начальная доза составляет 2,5 мг (1/2 табл. по 5 мг) один раз в день. При необходимости доза может быть увеличена до 5 мг один раз в день.
Пациентам пожилого возраста коррекция дозы не требуется.
Побочные действия
Со стороны водно-электролитного и кислотно-щелочного баланса: гипонатриемия, гипохлоремия, гипокалиемия, гипомагниемия, гипокальциемия, метаболический алкалоз. Симптомами, указывающими на развитие нарушений электролитного состояния и КЩС, могут быть головная боль, спутанность сознания, судороги, тетания, мышечная слабость, нарушения ритма сердца и диспепсические расстройства; гиповолемия и дегидратация (чаще у пациентов пожилого возраста), которые могут привести к гемоконцентрации с тенденцией к развитию тромбоза.
Со стороны ССС: чрезмерное снижение АД, ортостатическая гипотензия, коллапс, тахикардия, аритмии, снижение ОЦК.
Со стороны обмена веществ: гиперхолестеринемия, гипертриглицеридемия; преходящее повышение концентрации креатинина и мочевины в крови; повышение концентрации мочевой кислоты в крови, что может вызвать или усилить проявления подагры; снижение толерантности к глюкозе (возможна манифестация латентно протекающего сахарного диабета).
Со стороны мочевыделительной системы: олигурия, острая задержка мочи (например при гиперплазии предстательной железы, сужении мочеиспускательного канала, гидронефрозе); интерстициальный нефрит, гематурия, снижение потенции.
Со стороны пищеварительного тракта: тошнота, рвота, диарея, внутрипеченочный холестаз, повышение активности печеночных ферментов, острый панкреатит.
Со стороны ЦНС, органа слуха: нарушение слуха, обычно обратимое, и/или шум в ушах, особенно у пациентов с почечной недостаточностью или гипопротеинемией (нефротический синдром), парестезии.
Со стороны кожных покровов: кожный зуд, крапивница, другие виды сыпи или буллезное поражение кожи, полиморфная эритема, эксфолиативный дерматит, пурпура, лихорадка, васкулит, эозинофилия, фотосенсибилизация; тяжелые анафилактические или анафилактоидные реакции вплоть до шока, которые до настоящего времени были описаны лишь после в/в введения.
Со стороны периферической крови: тромбоцитопения, лейкопения, агранулоцитоз, апластическая или гемолитическая анемия.
Взаимодействие
Повышает концентрацию и риск развития нефро- и ототоксического действия цефалоспоринов, аминогликозидов, хлорамфеникола, этакриновой кислоты, цисплатина, амфотерицина В (вследствие конкурентного почечного выведения). Повышает эффективность диазоксида и теофиллина, снижает — гипогликемических средств, аллопуринола.
Прессорные амины и торасемид взаимно снижают эффективность.
Лекарственные средства, блокирующие канальцевую секрецию, повышают концентрацию торасемида в сыворотке крови.
При одновременном применении ГКС, амфотерицина В повышается риск развития гипокалиемии, с сердечными гликозидами — возрастает риск развития гликозидной интоксикации вследствие гипокалиемии (для высоко- и низкополярных) и удлинения T1/2 (для низкополярных).
Снижает почечный клиренс препаратов лития и повышает вероятность развития интоксикации.
НПВП, сукральфат снижают диуретический эффект вследствие ингибирования синтеза ПГ, нарушения активности ренина в плазме крови и выведения альдостерона. Усиливает гипотензивное действие гипотензивных средств, нервно-мышечную блокаду деполяризующих миорелаксантов (суксаметоний) и ослабляет действие недеполяризующих миорелаксантов (тубокурарин).
Одновременный прием больших доз салицилатов на фоне терапии торасемидом увеличивает риск проявления их токсичности (вследствие конкурентного почечного выведения).
Последовательное или одновременное применение торасемида с ингибиторами АПФ или антагонистами рецепторов ангиотензина II может привести к сильному снижению АД. Этого можно избежать, снизив дозу торасемида или временно отменив его. Одновременное использование пробенецида или метотрексата может уменьшать эффективность торасемида (одинаковый путь секреции). С другой стороны, торасемид может приводить к снижению почечной элиминации этих ЛС.
При одновременном применении циклоспорина и торасемида увеличивается риск развития подагрического артрита вследствие того, что циклоспорин может вызвать нарушение экскреции уратов почками, а торасемид — гиперурикемию. Сообщалось, что у пациентов с высоким риском развития нефропатии, принимающих торасемид внутрь, при введении рентгеноконтрастных средств нарушения функций почек наблюдались чаще, чем у пациентов с высоким риском развития нефропатии, которым перед введением рентгеноконтрастных средств проводили внутривенную гидратацию.
Передозировка
Симптомы: чрезмерно повышенный диурез, сопровождающийся снижением ОЦК и нарушением электролитного баланса крови, с последующим выраженным снижением АД, сонливостью и спутанностью сознания, коллапсом. Могут наблюдаться желудочно-кишечные расстройства.
Лечение: специфического антидота нет. Провокация рвоты, промывание желудка, активированный уголь. Лечение симптоматическое, снижение дозы или отмена препарата и одновременное восполнение ОЦК и коррекция показателей водно-электролитного баланса и кислотно-основного состояния под контролем сывороточных концентраций электролитов, гематокрита. Гемодиализ неэффективен.
Особые указания
Применять строго по назначению врача.
Пациенты с повышенной чувствительностью к сульфаниламидам и производным сульфонилмочевины могут иметь перекрестную чувствительность к препарату Диувер.
Пациентам, получающим высокие дозы препарата Диувер в течение длительного периода, во избежание развития гипонатриемии, метаболического алкалоза и гипокалиемии, рекомендуется диета с достаточным содержанием поваренной соли и применение препаратов калия.
Повышенный риск развития нарушений водно-электролитного баланса отмечается у больных с почечной недостаточностью. В ходе курсового лечения необходимо периодически контролировать концентрацию электролитов плазмы крови (в т.ч. натрия, кальция, калия, магния), кислотно-основное состояние, остаточный азот, креатинин, мочевую кислоту и проводить при необходимости соответствующую коррекционную терапию (с большей кратностью у больных с частой рвотой и на фоне парентерально вводимых жидкостей).
При появлении или усилении азотемии и олигурии у больных с тяжелыми прогрессирующими заболеваниями почек рекомендуется приостановить лечение.
Подбор режима доз больным с асцитом на фоне цирроза печени нужно проводить в стационарных условиях (нарушения водно-электролитного баланса могут повлечь развитие печеночной комы). Данной категории пациентов показан регулярный контроль электролитов плазмы крови.
У больных сахарным диабетом или со сниженной толерантностью к глюкозе требуется периодический контроль концентрации глюкозы в крови и моче.
У больных в бессознательном состоянии, с гиперплазией предстательной железы, сужением мочеточников необходим контроль диуреза в связи с возможностью острой задержки мочи.
В период лечения пациенты должны воздержаться от управления транспортными средствами и занятий другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Форма выпуска
Таблетки, 5 мг, 10 мг. По 10 табл. в блистере из пленки ПВХ/ПВДХ и алюминиевой фольги. По 2 или 6 блистеров вместе с инструкцией по применению в картонную пачку.
Производитель
1. Плива Хрватска д.о.о. Прилаз баруна Филиповича 25, 10000 Загреб, Республика Хорватия.
2. ООО «Р-Фарм Новосёлки», Российская Федерация, Ярославская обл., г. Ярославль, ул. 1-я Технологическая, 20.
Тел.: (4852) 77-21-36/37.
Юридическое лицо, на имя которого выдано РУ: Плива Хрватска д.о.о., Республика Хорватия.
Организация, принимающая претензии потребителей: ООО «Тева», 115054, Москва, ул. Валовая, 35.
Тел.: (495) 644-22-34; факс: (495) 644-22-35/36.
Условия отпуска из аптек
По рецепту.
DIUV-RU-00635-DOC/PHARM-02.2022
Условия хранения
При температуре не выше 25 °C.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Диаб-Норм (Diab-Norm)
💊 Состав препарата Диаб-Норм
✅ Применение препарата Диаб-Норм
⚠️ Государственная регистрация данного препарата отменена
Описание активных компонентов препарата
Диаб-Норм
(Diab-Norm)
Приведенная научная информация является обобщающей и не может быть использована для принятия
решения о возможности применения конкретного лекарственного препарата.
Дата обновления: 2020.11.24
Владелец регистрационного удостоверения:
Код ATX:
A10BG03
(Пиоглитазон)
Лекарственная форма
| Диаб-Норм |
Таб. 30 мг: 28 шт. рег. №: ЛС-001883 |
Форма выпуска, упаковка и состав
препарата Диаб-Норм
Таблетки белого или почти белого цвета, круглые, слегка двояковыпуклые, с фаской.
Вспомогательные вещества: лактозы моногидрат, гипролоза, кроскармеллоза натрия, магния стеарат.
7 шт. — упаковки ячейковые контурные (4) — пачки картонные.
Фармакологическое действие
Пероральное гипогликемическое средство, производное тиазолидиндионового ряда. Мощный, селективный агонист гамма-рецепторов, активируемых пролифератором пероксисом (PPAR-гамма). PPAR-гамма рецепторы обнаруживаются в жировой, мышечной тканях и в печени. Активация ядерных рецепторов PPAR-гамма модулирует транскрипцию ряда генов, чувствительных к инсулину, участвующих в контроле уровня глюкозы и в метаболизме липидов. Снижает инсулинорезистентность в периферических тканях и в печени, в результате этого происходит увеличение расхода инсулинозависимой глюкозы и уменьшение продукции глюкозы в печени. В отличие от производных сульфонилмочевины, пиоглитазон не стимулирует секрецию инсулина β-клетками поджелудочной железы.
При сахарном диабете 2 типа (инсулиннезависимом) уменьшение инсулинорезистентности под действием пиоглитазона приводит к снижению концентрации глюкозы в крови, снижению уровня инсулина в плазме и гемоглобина A1c (гликированный гемоглобин, HbA1c).
При сахарном диабете 2 типа (инсулиннезависимом) с нарушением липидного обмена на фоне применения пиоглитазона отмечается снижение уровня ТГ и увеличение уровня ЛПВП. При этом уровень ЛПНП и общего холестерина у таких пациентов не меняется.
Фармакокинетика
После приема внутрь натощак пиоглитазон обнаруживается в плазме крови через 30 мин. Cmax в плазме достигается через 2 ч. При приеме пищи наблюдалось незначительное увеличение времени достижения Cmax до 3-4 ч, но степень всасывания не изменялась.
После приема однократной дозы кажущийся Vd пиоглитазона составляет в среднем 0.63±0.41 л/кг. Связывание с белками сыворотки крови человека, в основном с альбумином, составляет более 99%; связывание другими белками сыворотки менее выраженное. Метаболиты пиоглитазона M-III и M-IV также в значительной степени связываются с альбумином сыворотки — более 98%.
Пиоглитазон интенсивно метаболизируется в печени путем гидроксилирования и окисления. Метаболиты М-II, М-IV (гидрокси-производные пиоглитазона) и M-III (кетопроизводные пиоглитазона) проявляют фармакологическую активность на моделях сахарного диабета 2 типа у животных. Метаболиты также частично превращаются в конъюгаты глюкуроновой или серной кислот.
Метаболизм пиоглитазона в печени происходит при участии изоферментов CYP2C8 и CYP3A4.
T1/2 неизмененного пиоглитазона составляет 3-7 ч, общего пиоглитазона (пиоглитазон и активные метаболиты) — 16-24 ч. Клиренс пиоглитазона составляет 5-7 л/ч.
После приема внутрь около 15-30% дозы пиоглитазона обнаруживается в моче. Почками выводится ничтожно малое количество пиоглитазона, в основном, в форме метаболитов и их конъюгатов. Считается, что при приеме внутрь большая часть дозы выделяется с желчью как в неизмененном виде, так и в виде метаболитов и выводится из организма с калом.
Концентрации пиоглитазона и активных метаболитов в сыворотке крови остаются на достаточно высоком уровне через 24 ч после однократного введения суточной дозы.
Показания активных веществ препарата
Диаб-Норм
Сахарный диабет 2 типа (инсулиннезависимый).
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Принимают внутрь в дозе 30 мг 1 раз/сут. Длительность лечения устанавливают индивидуально.
Максимальная доза при комбинированной терапии составляет 30 мг/сут.
Побочное действие
Со стороны обмена веществ: возможно развитие гипогликемии (от слабой до выраженной).
Со стороны системы кроветворения: возможны анемия, снижение гемоглобина и гематокрита.
Со стороны пищеварительной системы: редко — повышение активности АЛТ.
Противопоказания к применению
Сахарный диабет 1 типа (инсулинзависимый), диабетический кетоацидоз, беременность, лактация, повышенная чувствительность к пиоглитазону.
Применение при беременности и кормлении грудью
Пиоглитазон противопоказан к применению при беременности и в период лактации (грудного вскармливания).
У больных с инсулинорезистентностью и ановуляторным циклом в пременопаузном периоде лечение тиазолидиндионами, включая пиоглитазон, может вызвать овуляцию. Это повышает риск беременности, если не используются адекватные средства контрацепции.
Применение при нарушениях функции печени
Не следует применять пиоглитазон при наличии клинических проявлений заболевания печени в активной фазе или при увеличении активности АЛТ в 2.5 раза выше ВГН. При умеренно повышенной активности ферментов печени (АЛТ менее чем в 2.5 раза выше ВГН) до начала или во время лечения пиоглитазоном больных необходимо обследовать для определения причины повышения показателей. При умеренном повышении активности ферментов печени следует с осторожностью начинать или продолжать лечение. В этом случае рекомендуется более частый контроль клинической картины и исследование уровня активности печеночных ферментов.
В случае увеличения активности трансаминаз в сыворотке крови (АЛТ в >2.5 раза выше ВГН) контроль функции печени следует проводить чаще и до тех пор, пока уровень не вернется к норме или к показателям, которые наблюдались до проведения лечения. Если активность АЛТ в 3 раза превышает ВГН, то повторный тест по определению активности АЛТ следует провести как можно быстрее. Если активность АЛТ остается на уровне в 3 раза > ВГН пиоглитазон следует отменить.
В период лечения при подозрении на развитие нарушений функции печени (появление тошноты, рвоты, болей в животе, усталости, отсутствия аппетита, темной мочи) следует определить показатели функциональных тестов печени. Решение вопроса о продолжении терапии пиоглитазоном следует принимать на основании клинических данных с учетом лабораторных показателей. В случае возникновения желтухи пиоглитазон следует отменить.
Применение у детей
Применение пиоглитазона у детей не рекомендуется.
Особые указания
Не следует применять пиоглитазон при наличии клинических проявлений заболевания печени в активной фазе или при увеличении активности АЛТ в 2.5 раза выше ВГН. При умеренно повышенной активности ферментов печени (АЛТ менее чем в 2.5 раза выше ВГН) до начала или во время лечения пиоглитазоном больных необходимо обследовать для определения причины повышения показателей. При умеренном повышении активности ферментов печени следует с осторожностью начинать или продолжать лечение. В этом случае рекомендуется более частый контроль клинической картины и исследование уровня активности печеночных ферментов.
В случае увеличения активности трансаминаз в сыворотке крови (АЛТ в >2.5 раза выше ВГН) контроль функции печени следует проводить чаще и до тех пор, пока уровень не вернется к норме или к показателям, которые наблюдались до проведения лечения. Если активность АЛТ в 3 раза превышает ВГН, то повторный тест по определению активности АЛТ следует провести как можно быстрее. Если активность АЛТ остается на уровне в 3 раза > ВГН пиоглитазон следует отменить.
В период лечения при подозрении на развитие нарушений функции печени (появление тошноты, рвоты, болей в животе, усталости, отсутствия аппетита, темной мочи) следует определить показатели функциональных тестов печени. Решение вопроса о продолжении терапии пиоглитазоном следует принимать на основании клинических данных с учетом лабораторных показателей. В случае возникновения желтухи пиоглитазон следует отменить.
С осторожностью следует применять пиоглитазон у пациентов с отеками.
Применение пиоглитазона у детей не рекомендуется.
Лекарственное взаимодействие
При применении другого производного тиазолидиндиона одновременно с пероральными контрацептивами наблюдалось снижение концентрации этинилэстрадиола и норэтиндрона в плазме примерно на 30%. Поэтому при одновременном применении пиоглитазона и пероральных контрацептивов возможно снижение эффективности контрацепции.
Кетоконазол ингибирует метаболизм пиоглитазона в печени in vitro.
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код