Ганатон® (Ganaton) инструкция по применению
📜 Инструкция по применению Ганатон®
💊 Состав препарата Ганатон®
✅ Применение препарата Ганатон®
📅 Условия хранения Ганатон®
⏳ Срок годности Ганатон®
Описание лекарственного препарата
Ганатон®
(Ganaton)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для печатного издания справочника Видаль 2023 года.
Дата обновления: 2022.05.25
Код ATX:
A03FA
(Стимуляторы моторики ЖКТ)
Лекарственная форма
| Ганатон® |
Таб., покр. пленочной оболочкой, 50 мг: 40 или 70 шт. рег. №: ЛС-002513 |
Форма выпуска, упаковка и состав
препарата Ганатон®
Таблетки, покрытые пленочной оболочкой белого цвета, круглые, двояковыпуклые, с риской на одной стороне и гравировкой «HC 803» на другой стороне.
Вспомогательные вещества: лактозы моногидрат — 35 мг, крахмал кукурузный — 15 мг, кармеллоза — 20 мг, кремния диоксид коллоидный безводный — 4 мг, магния стеарат — 1 мг.
Состав пленочной оболочки: гипромеллоза 2910 — 4.4 мг, макрогол 8000 — 0.4 мг, титана диоксид (E171) — 0.2 мг, воск карнаубский — 0.025 мг.
10 шт. — упаковки ячейковые контурные (4) — пачки картонные с контролем первого вскрытия.
14 шт. — упаковки ячейковые контурные (5) — пачки картонные с контролем первого вскрытия.
Фармакологическое действие
Итоприда гидрохлорид — гастропрокинетик для приема внутрь. Лекарственная форма и состав таблеток обеспечивают немедленное высвобождение действующего вещества. Итоприд характеризуется двойным механизмом действия: антагонизм к D2-допаминовых рецепторам и ингибирование ацетилхолинэстеразы. В результате действия итоприда увеличивается концентрация ацетилхолина, что приводит к усилению моторики желудка, повышению тонуса нижнего пищеводного сфинктера (НПС), ускорению процесса опорожнения желудка и улучшению гастродуоденальной координации.
Итоприда гидрохлорид также оказывает противорвотный эффект за счет взаимодействия с D2-допаминовыми рецепторами, расположенными в хеморецепторной триггерной зоне продолговатого мозга. Итоприд вызывает дозозависимое подавление рвоты, вызванной апоморфином.
Действие препарата у пациентов с функциональной диспепсией приводит к снижению выраженности симптомов (общая оценка пациентом, постпрандиальная тяжесть в животе, раннее насыщение). Применение итоприда пациентами с диабетическим гастропарезом способствовало ускорению эвакуации из желудка жидкой и твердой пищи. У пациентов с гастроэзофагеальной рефлюксной болезнью (ГЭРБ) итоприд уменьшает количество преходящих расслаблений нижнего пищеводного сфинктера и уменьшает продолжительность времени с высокой кислотностью в пищеводе (pH<4).
При совместном применении итоприда гидрохлорида с альфа-липоевой кислотой наблюдалось ускорение процесса опорожнения желудка и снижение уровня гастрина и мотилина в сравнении с монотерапией итопридом.
Итоприда гидрохлорид оказывает высокоспецифичное действие на верхний отдел ЖКТ. Итоприда гидрохлорид ускоряет опорожнение желудка. Итоприда гидрохлорид не влияет на сывороточные уровни гастрина.
Фармакокинетика
Всасывание
Итоприда гидрохлорид быстро и практически полностью всасывается из ЖКТ. Относительная биодоступность составляет 60%, что связано с метаболизмом при «первом прохождении» через печень. Пища не оказывает влияния на биодоступность. Cmax в плазме крови (0.28 мкг/мл) достигается через 0.5-0.75 ч после приема 50 мг итоприда гидрохлорида.
При повторном приеме итоприда гидрохлорида внутрь в дозе 50-200 мг 3 раза/сут в течение 7 дней фармакокинетика препарата и его метаболитов была линейной, а кумуляция оказалась минимальной.
Распределение
Итоприда гидрохлорид на 96% связывается с белками плазмы крови, в основном с альбумином. Связывание с альфа1-кислым гликопротеином составляет менее 15% от общего связывания.
Итоприд активно распределяется в ткани (Vdβ=6.1 л/кг) и обнаруживается в высоких концентрациях в почках, тонком кишечнике, печени, надпочечниках и желудке. Проникновение в головной и спинной мозг минимальное. Итоприд проникает в грудное молоко.
Метаболизм
Итоприд подвергается активной биотрансформации в печени у человека. Идентифицированы 3 метаболита, только один из которых проявляет небольшую активность, которая не имеет фармакологического значения (примерно 2-3% от таковой итоприда). Первичным метаболитом у человека является N-оксид, который образуется в результате окисления третичной амино-N-диметильной группы.
Итоприд метаболизируется под действием флавин-зависимой монооксигеназы (FMО3). Количество и эффективность изоферментов FMO у человека может отличаться в зависимости от генетического полиморфизма, который в редких случаях приводит к развитию аутосомно-рецессивного состояния, известного под названием триметиламинурии (синдром рыбного запаха).
По данным фармакокинетических исследований CYP-опосредованных реакций in vivo итоприд не оказывает ингибирующего или индуцирующего действия на изоферменты CYP2C19 и CYP2E1. Терапия итопридом не влияет на CYP или активность уридиндифосфат-глюкуронилтрансферазы.
Выведение
Итоприда гидрохлорид и его метаболиты выводятся в основном с мочой. Почечная экскреция итоприда и его N-оксида после однократного приема препарата внутрь в терапевтической дозе (50 мг) у здоровых людей составляла 3.7 и 75.4% соответственно. Т1/2 итоприда гидрохлорида составляет около 6 ч.
Показания препарата
Ганатон®
- лечение желудочно-кишечных симптомов, связанных с нарушением моторики желудка или его замедленным опорожнением, таких как:
- вздутие живота;
- быстрое насыщение;
- чувство переполнения в желудке после приема пищи;
- боль или дискомфорт в эпигастральной области;
- снижение аппетита;
- изжога;
- тошнота;
- рвота.
- функциональная (неязвенная) диспепсия или хронический гастрит.
Режим дозирования
Взрослым назначают внутрь по 1 таб. препарата Ганатон® 50 мг 3 раза/сут до еды. Рекомендуемая суточная доза составляет 150 мг. Указанная доза может быть снижена с учетом возраста и симптомов больного.
В клинических исследованиях продолжительность лечения препаратом Ганатон® составляла до 8 недель.
Побочное действие
Следующие побочные эффекты наблюдались у 998 пациентов при применении итоприда в стандартной суточной дозе 150 мг или ниже в ходе 4 плацебо-контролируемых, 4 сравнительных и 13 неконтролируемых интервенционных клинических исследованиях с частотой [часто (≥1/100 и <1/10) и нечасто (≥1/1000 и <1/100)]. В категориях с частотой очень часто (≥1/10), редко (≥1/10000 и <1/1000) или очень редко (<1/10000) нежелательных реакций не наблюдалось.
Следующие побочные эффекты были выявлены в ходе пострегистрационного применения, исходя из имеющихся данных оценить их частоту не представляется возможным.
Со стороны системы кроветворения: лейкопения и тромбоцитопения.
Со стороны иммунной системы: реакции гиперчувствительности, включая анафилактоидную реакцию.
Со стороны эндокринной системы: повышение уровня пролактина в крови.
Со стороны нервной системы: головокружение, головная боль, тремор.
Со стороны ЖКТ: диарея, запор, боль в животе, повышенное слюноотделение и тошнота.
Со стороны печени и желчевыводящих путей: желтуха.
Со стороны кожи и подкожных тканей: сыпь, эритема и зуд.
Со стороны половых органов и молочной железы: гинекомастия.
Лабораторные и инструментальные данные: повышение активности ACT, АЛТ, ГГТ, ЩФ и уровня билирубина.
Противопоказания к применению
- повышенная чувствительность к итоприду или любому вспомогательному компоненту препарата;
- желудочно-кишечное кровотечение, механическая обструкция или перфорация ЖКТ;
- беременность;
- период грудного вскармливания;
- детский возраст до 16 лет (в связи с отсутствием данных по безопасности).
С осторожностью
Итоприда гидрохлорид усиливает действие ацетилхолина, что может вызывать холинергические побочные реакции. Препарат следует назначать с осторожностью пациентам, у которых появление таких реакций может усугубить течение основного заболевания.
Пациентам пожилого возраста итоприда гидрохлорид следует назначать с осторожностью, учитывая более высокую частоту снижения функции печени и почек, наличие сопутствующих заболеваний или другое лечение.
Применение при беременности и кормлении грудью
Беременность
На данный момент имеется ограниченное количество данных (менее 300 исходов беременности) по применению итоприда у беременных женщин. Экспериментальные исследования на животных не выявили признаков прямого или непрямого отрицательного влияния итоприда, указывающих на репродуктивную токсичность. В целях предосторожности противопоказано применение итоприда при беременности.
Период грудного вскармливания
Итоприд выделяется с молоком у животных, однако на данный момент отсутствует достаточное количество данных о выделении итоприда с грудным молоком у человека. При кормлении грудью нельзя исключать риск влияния препарата на ребенка. Решение о прекращении грудного вскармливания или отмене/перерыве в приеме препарата следует принимать, основываясь на оценке пользы грудного вскармливания для ребенка и пользы препарата для матери.
Фертильность
Данные о влиянии итоприда на фертильность у человека отсутствуют. Тем не менее, исследования на животных не выявили признаков отрицательного влияния препарата на фертильность.
Применение у детей
Противопоказано применение в детском возрасте до 16 лет (в связи с отсутствием данных по безопасности).
Применение у пожилых пациентов
Итоприд следует назначать с осторожностью пациентам пожилого возраста в связи с частым снижением функции печени и почек, наличием сопутствующих заболеваний или другого лечения.
Особые указания
Итоприд усиливает действие ацетилхолина и может вызвать холинэргические побочные реакции.
Данные о длительном применении препарата отсутствуют.
Влияние на способность к управлению автотранспортом и механизмами
Исследований относительно влияния итоприда на способность к управлению автомобилем и механизмами не проводилось. Однако в период лечения препаратом следует соблюдать осторожность при выполнении потенциально опасных видов деятельности, требующих повышенной концентрации внимания и быстроты психомоторных реакций (управление транспортными средствами, работа с движущимися механизмами, работа диспетчера и оператора), т.к. применение препарата может вызвать головокружение.
Передозировка
Лечение: при передозировке показаны промывание желудка и симптоматическая терапия.
Лекарственное взаимодействие
Метаболическое взаимодействие не ожидается, т.к. итоприд первично метаболизируется под действием флавиновой монооксигеназы, а не с участием системы цитохрома CYP450.
При одновременном применении варфарина, диазепама, диклофенака натрия, тиклопидина гидрохлорида, нифедипина и никардипина гидрохлорида изменений связывания с белками не наблюдалось.
Итоприд усиливает моторику желудка, поэтому он может повлиять на всасывание других препаратов, принимаемых внутрь. Особую осторожность следует соблюдать при применении препаратов с низким терапевтическим индексом, а также лекарственных форм с замедленным высвобождением или препаратов с кишечнорастворимой оболочкой.
Противоязвенные препараты, такие как циметидин, ранитидин, тепренон и цетраксат, не влияют на прокинетическое действие итоприда.
Антихолинергические средства могут ослабить эффект итоприда.
Условия хранения препарата Ганатон®
Препарат следует хранить в недоступном для детей месте при температуре не выше 25°С.
Срок годности препарата Ганатон®
Срок годности — 3 года. Не применять после истечения срока годности.
Условия реализации
Препарат отпускают по рецепту.
Контакты для обращений
ЭББОТТ ЛЭБОРАТОРИЗ ООО
(Россия)
|
|
125171 Москва, |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Эффективность применения препарата Ганатон в лечении больных ГЭРБ
Статьи
Опубликовано в журнале:
«Эффективная фармакотерапия в гастроэнтерологии», №3, октябрь 2008, с. 20-24
О.Н. Минушкин, Ю.Н. Лощинина
УНМЦ управления делами Президента РФ
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ) является заболеванием, обусловленным нарушением перистальтики органов эзофагогастродуоденальной зоны, часто повторяющимися забросами в пищевод желудочного или дуоденального содержимого, удлинением времени экспозиции рефлюктата в пищеводе, приводящих к повреждению дистальной части пищевода.
Из определения болезни видно, что основным патогенетическим механизмом, формирующим условия для раздражения, воспаления, повреждения слизистой, является расстройство моторики. Тем не менее, основным направлением терапии, используемым в лечении ГЭРБ, является блокада желудочной секреции. Это связано в значительной степени с тем, что эффективных препаратов, восстанавливающих нарушенную перистальтику, до настоящего времени не было, а те, которые присутствовали на фармакологическом рынке, обладали значительным количеством побочных эффектов.
Следует отметить, что в клинической практике блокада желудочной секреции не всегда эффективно решает задачу контроля над симптомами ГЭРБ. В таких случаях (а это, например, сочетание изжоги с симптомами диспепсии, резистентность к ингибиторам протонной помпы или ночные прорывы кислотности на фоне терапии этими препаратами, щелочной рефлюкс и др.) значение восстановления нормальной двигательной функции пищевода и желудка увеличивается.
В 2007 году в России зарегистрирован новый прокинетик с комбинированным механизмом действия – Ганатон (Ganaton – своеобразная аббревиатура от «gastric natural tone», т.е. восстанавливающий нормальный тонус желудка; международное название – итоприда гидрохлорид).
Ганатон (итоприда гидрохлорид) является одновременно антагонистом допаминовых рецепторов и блокатором ацетилхолинэстеразы. Препарат активирует освобождение ацетилхолина и препятствует его деградации.
Ганатон обладает минимальной способностью проникать через гематоэнцефалический барьер в центральную нервную систему, включая головной и спинной мозг. Метаболизм препарата позволяет избежать нежелательного лекарственного взаимодействия при приеме препаратов, метаболизирующихся ферментами системы цитохрома Р 450.
Взрослым Ганатон назначают внутрь по 1 таблетке (50 мг) 3 раза в сутки до еды. Рекомендуемая суточная доза составляет 150 мг.
В Японии, где Ганатон (итоприда гидрохлорид) применяется с 1995 г., было проведено многоцентровое двойное слепое сравнительное исследование эффективности применения в течение 2 недель у больных хроническим гастритом с симптомами диспепсии. Итоприд гидрохлорида назначался в дозе 50 мг 3 раза в сутки (у 111 пациентов), цизаприд – в дозе 2,5 мг 3 раза в сутки (у 114 пациентов) (3). Умеренное или значительное клиническое улучшение наблюдалось у 79,3% больных, получавших итоприда гидрохлорид, и у 71,9% пациентов, получавших цизаприд. Авторы сделали вывод о высокой эффективности применения итоприда гидрохлорида в лечении больных хроническим гастритом с симптомами диспепсии. Был отмечен также хороший эффект итоприда гидрохлорида у больных хроническим гастритом с сопутствующими симптомами гастроэзофагеальной рефлюксной болезни (2), а также у пациентов с диабетическим гастропарезом (5).
Во всех клинических исследованиях Ганатон (итоприда гидрохлорид) зарекомендовал себя как препарат, характеризующийся хорошей переносимостью и отсутствием серьезных побочных эффектов. Основными побочными эффектами при приеме итоприда гидрохлорида явились: диарея (0,7% случаев), боли в животе (0,3%), головная боль (0,3%). Проведенные постмаркетинговые исследования подтвердили безопасность итоприда гидрохлорида (1). Результаты применения этого препарата более чем у 10 млн больных не выявили ни одного случая удлинения интервала Q-T. При назначении препарата в обычных терапевтических дозах повышение уровня пролактина в крови встречается редко.
На специальном симпозиуме по лечению функциональной диспепсии, который проходил в 2005 г. в Монреале в рамках Всемирного конгресса гастроэнтерологов, Ганатон (итоприда гидрохлорид) был охарактеризован как высокоэффективный и безопасный представитель нового класса прокинетиков, который может с успехом применяться при лечении функциональной диспепсии, а в будущем, возможно, займет важное место и в лечении других гастроэнтерологических заболеваний, протекающих с нарушением двигательной функции желудка (идиопатического гастропареза, гастроэзофагеальной рефлюксной болезни и др.) (4).
На кафедре гастроэнтерологии ФГУ УНМЦ УД Президента РФ в период с апреля по июнь 2008 г. Было проведено изучение клинического применения, предусматривающее курсовое лечение Ганатоном по стандартной схеме в течение 4 недель больных ГЭРБ.
Цель изучения – оценка эффективности 4-недельного курса терапии Ганатоном в стандартном режиме в купировании симптомов ГЭРБ и влияния на качество жизни больных, а также на тонус ВНС (устранение дисфункции по симпатическому и парасимпатическому типу).
Критериями включения больных явились: наличие у пациентов умеренной или сильной изжоги (≥ 2 баллов по шкале Лайкерта), по крайней мере 1-2 раза в неделю, наличие дисфункции ВНС по симпатическому или парасимпатическому типу.
Всего к изучению было принято 20 пациентов мужского пола с ГЭРБ 0 – I стадии, в возрасте от 20 до 25 лет (средний возраст 22,8 ± 0,33 года), соответствующих критериям включения.
Перед включением проводились клинический анализ крови и мочи, ЭГДС. До и после лечения оценивали интенсивность и частоту симптомов, эндоскопическую картину у пациентов с эрозивной формой ГЭРБ и уровень качества жизни по данным опросника SF-36 и визуальной аналоговой шкалы (ВАШ).
Больные принимали Ганатон в дозе 1 таблетка 3 раза в день, за 15 минут до приема пищи в течение 25 дней.
Тип течения ГЭРБ имел рецидивирующий характер в 100% случаев. Средняя продолжительность ЭНРБ (эндоскопически негативной рефлюксной болезни) составляла 3,4 ± 0,65 лет.
Все пациенты на момент включения в группу лечения испытывали изжогу и другие симптомы ГЭРБ, значительно ухудшающие качество жизни.
Изжога оценивалась с помощью расчетного показателя в баллах (таблица 1).
Среднее значение изжоги составляло 7,0 ± 0,2 балла.
Эндоскопическая характеристика больных до начала лечения представлена в таблице 2.
Таблица 1. Оценка изжоги изученных больных
| Параметр | Характеристика | Балл |
|---|---|---|
| Частота | Отсутствует Менее 2 раз в неделю 2-6 раз в неделю Ежедневно |
0 1 2 3 |
| Время возникновения | Отсутствует Только днем Только ночью Днем и ночью |
0 1 1 2 |
| Интенсивность | Отсутствует Легкая Средняя Тяжелая |
0 1 2 3 |
| Продолжительность | Отсутствует Несколько минут Длительно |
0 1 2 |
Таблица 2. Результаты эндоскопического исследования до начала терапии
| Эндоскопический признак | Количество пациентов, N (%) |
|---|---|
| Отсутствие изменений слизистой | 8 (40%) |
| Катаральный эзофагит | 6 (30%) |
| Эрозивный эзофагит | 6 (30%) |
| Недостаточность кардии | 17 (85%) |
| ГПОД | 1 (2%) |
Исследование вегетативного статуса проводилось по данным специального вопросника (Вейн А.М., 1993 г.), объективного осмотра и по вычислению индекса Кердо: ВИ = (1 – Д/Р) × 100,
где ВИ – вегетативный индекс; Д – диастолическое давление; Р – частота сердечных сокращений в 1 минуту.
Результаты лечения больных
На фоне проводимой монотерапии препаратом Ганатон изжога уменьшилась на 1 и более баллов к 7 ± 0,62 дню лечения у всех больных и была полностью купирована на 8,5 ± 1,1 день терапии в 90% случаев. У 2 пациентов купирования симптомов ГЭРБ (изжога, отрыжка воздухом) по окончании терапии не наступило. Это может быть связано с тем, что механизм формирования клинических проявлений у них был иным – не связанным с расстройством моторики.
У пациентов с эрозивной формой ГЭРБ (6 пациентов) после окончания терапии проводилась контрольная ЭГДС, при которой была выявлена полная эпителизация эрозий пищевода в 100% случаев.
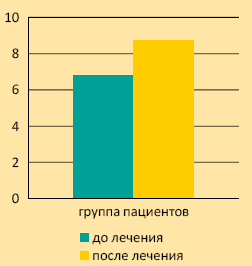
При оценке самочувствия визуальноаналоговой шкалы исходные данные ВАШ составили 6,8 ± 0,38 см, после курсовой терапии – 8,7 ± 0,19 см (р
График 1. Динамика самочувствия пациентов (оценка по ВАШ) до и после лечения
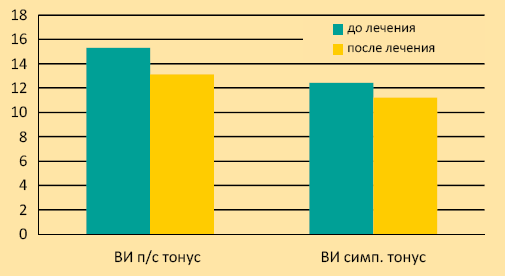
Было получено отчетливое влияние на вегетативный статус, что выражается в улучшении клинической симптоматики. Так, вегетативный индекс Кердо у пациентов с дисфункцией нервной системы по парасимпатическому типу до лечения составил 15,3 ± 1,8, после лечения – 13,1 ± 0,9. У пациентов с дисфункцией ВНС по симпатическому типу индекс Кердо до лечения – 12,4 ± 1,8, после лечения – 11,2 ± 1,2. Результаты представлены в графике 2.
График 2. Динамика вегетативного индекса Кердо до и после лечения Ганатоном
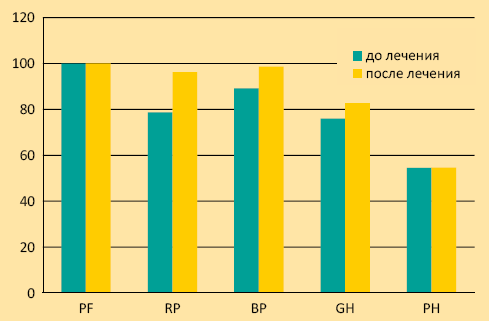
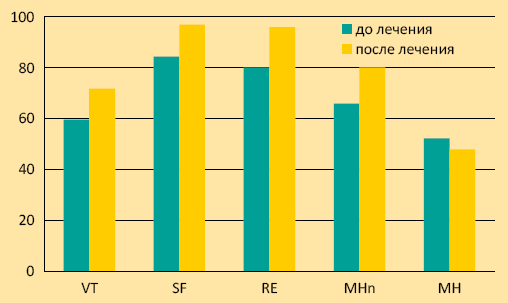
Динамика уровня качества жизни по данным опросника SF-36 показала, что среди показателей физического компонента здоровья (график 3) достоверно улучшились ролевое функционирование (RP), интенсивность боли (BP), общее состояние здоровья (GH). Среди показателей психологического компонента здоровья (график 4) наблюдалось достоверное улучшение жизненной активности (VT), социального (SF) и ролевого (RE) функционирования, психического здоровья (MHn).
График 3. Динамика уровня качества жизни (физическое здоровье) по данным опросника SF-36
График 4. Динамика уровня качества жизни (психическое здоровье) по данным опросника SF-36
Оценка безопасности и п ереносимости препарата Ганатон
За время лечения каких-либо побочных эффектов зарегистрировано не было. Препарат хорошо переносился и не вызывал органолептических неудобств.
Обсуждение
Изучена эффективность лечения 20 больных ГЭРБ (у 70% – НЭРБ, у 30% – эрозивный вариант). Больные характеризовались выраженным клиническим вариантом болезни (интенсивность изжоги составила 7 баллов), снижен уровень качества жизни; изменен вегетативный статус (поровну с преобладанием симпатического и парасимпатического отделов ВНС), причем у больных с преобладанием парасимпатического отдела – фиксировались более выраженные изменения слизистой пищевода – эрозивные и катаральные.
Больные получали только Ганатон и непродолжительным курсом (25 дней), при этом в обычные сроки были купированы клинические проявления и наступала эпителизация эрозий. Ни один больной ни потребовал усиления терапии антацидами или блокаторами секреции.
Эти результаты вселяют надежду, что новый (для нашей страны) прокинетик Ганатон может занять достойное место в лечении ГЭРБ.
Можно предположить, что для части больных Ганатон окажется препаратом выбора (не только в лечении, но и в поддержании ремиссии), для части – его использование поможет уменьшить дозу блокаторов секреции; сократить сроки лечения.
Препарат нуждается в дальнейшем изучении с целью определения его места в лечении наиболее распространенного гастроэнтерологического заболевания – ГЭРБ, которая и в условиях России становится болезнью № 1.
Выводы
- Ганатон является эффективным средством лечения ГЭРБ (как при эндоскопически негативном, так и при эрозивным варианте болезни) у молодых больных.
- Средний срок купирования симптомов на фоне монотерапии Ганатоном составил 7-9 дней, эрозивные изменения были эпителизированы за 25 дней лечения в 100% случаев.
- Препарат хорошо переносился и не вызывал побочных эффектов.
- Ганатон может быть рекомендован для лечения больных, страдающих ГЭРБ.
Литература
- Inoue K., Sanada Y., Fijimura J., Mihara O. Clinical effect of itopride hydrochloride on the digestive symptoms of chronic gastritis with reflux esophagitis // Clinical Medicine. 1999; Vol. 15: 1803-1808.
- Kahrilas P.J. Gastroesophageal reflux disease. JAMA 1996; 276: 983-8.
- Smout A.J.P.M., Akkermans L.M.A. Normal and disturbed motility of the gastrointestinal tract. – Wrightson Biomedical Publishing Ltd. – Petersfield, 1992.
- Talley N.J. Dyspepsia and functional dyspepsia. Motility. 1992; 20: 4-8.
- Physiological long-term treatment of gastro-oesophageal reflux disease. New perspectives with cisapride (Proceedings of symposium). J Drug Dev. 1993; 5: 1-28.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
таблетки, покрытые пленочной оболочкой
1 таблетка, покрытая пленочной оболочкой, содержит:
Действующее вещество: итоприда гидрохлорид 50 мг;
Вспомогательные вещества: лактозы моногидрат — 35 мг, крахмал кукурузный — 15 мг, кармеллоза — 20 мг, кремния диоксид коллоидный безводный — 4 мг, магния стеарат — 1 мг; пленочная оболочка: гипромеллоза 2910 — 4,4 мг, макрогол 8000 — 0,4 мг, титана диоксид (Е171) — 0,2 мг, воск карнаубский — 0,025 мг.
Белые, круглые двояковыгнутые таблетки, покрытые пленочной оболочкой, с риской на одной стороне и гравировкой «НС 803» на другой стороне.
Моторики ЖКТ стимулятор — ацетилхолина выброса стимулятор
АТХ A03FA Стимуляторы моторики ЖКТ
Фармакодинамика
Итоприда гидрохлорид — это гастропрокинетик для приема внутрь.
Лекарственная форма и состав таблеток обеспечивают немедленное высвобождение действующего вещества. Итопридхарактеризуется двойным механизмом действия: антагонизм к D2-дофаминовых рецепторам и ингибирование ацетилхолинэстеразы. В результате действия итоприда увеличивается концентрация ацетилхолина, что приводит к усилению моторики желудка, повышению тонуса нижнего пищеводного сфинктера (НПС), ускорению процесса опорожнения желудка и улучшению гастродуоденальной координации.
Итоприда гидрохлорид также оказывает противорвотный эффект за счет взаимодействия с D2-дофаминовыми рецепторами, расположенными в хеморецепторной триггерной зоне продолговатого мозга. Итоприд вызывает дозозависимое подавление рвоты, вызванной апоморфином.
Действие препарата у пациентов с функциональной диспепсией приводит к снижению выраженности симптомов (общая оценка пациентом, постпрандиальная тяжесть в животе, раннее насыщение).
Применение итоприда пациентами с диабетическим гастропарезом способствовало ускорению эвакуации из желудка жидкой и твердой пищи.
У пациентов с гастроэзофагеальной рефлюксной болезнью (ГЭРБ) итоприд уменьшает количество преходящих расслаблений нижнего пищеводного сфинктера и уменьшает продолжительность времени с высокой кислотностью в пищеводе (pH < 4).
При совместном применении итоприда гидрохлорида с альфа-липоевой кислотой наблюдалось ускорение процесса опорожнения желудка и снижение уровня гастрина и мотилина в сравнении с монотерапией итопридом.
Итоприда гидрохлорид оказывает высокоспецифичное действие на верхний отдел желудочно-кишечного тракта. Итоприда гидрохлорид ускоряет опорожнение желудка.
Итоприда гидрохлорид не влияет на сывороточные уровни гастрина.
Фармакокинетика
Всасывание
Итоприда гидрохлорид быстро и практически полностью всасывается в желудочно-кишечном тракте. Относительная биодоступность составляет 60 %, что связано с метаболизмом при первом прохождении через печень. Пища не оказывает влияния на биодоступность. Максимальная концентрация в плазме крови (Сmах 0,28 мкг/мл) достигается через 0,5-0,75 ч после приема 50 мг итоприда гидрохлорида.
При повторном приеме итоприда гидрохлорида внутрь в дозе 50-200 мг три раза в сутки в течение 7 дней фармакокинетика препарата и его метаболитов была линейной, а кумуляция оказалась минимальной.
Распределение
Итоприда гидрохлорид на 96% связывается с белками плазмы крови, в основном с альбумином. Связывание с альфа1-кислым гликопротеином составляет менее 15% от общего связывания.
Итоприд активно распределяется в ткани (объем распределения Vdβ = 6,1 л/кг) и обнаруживается в высоких концентрациях в почках, тонком кишечнике, печени, надпочечниках и желудке. Проникновение в головной и спинной мозг минимальное. Итоприд проникает в грудное молоко.
Метаболизм
Итоприд подвергается активной биотрансформации в печени у человека. Идентифицированы 3 метаболита, только один из которых проявляет небольшую активность, которая не имеет фармакологического значения (примерно 2-3% от таковой итоприда). Первичным метаболитом у человека является N-оксид, который образуется в результате окисления третичной амино-N-диметильной группы.
Итоприд метаболизируется под действием флавин-зависимой монооксигеназы (FMО3). Количество и эффективность изоферментов FMO у человека может отличаться в зависимости от генетического полиморфизма, который в редких случаях приводит к развитию аутосомно-рецессивного состояния, известного под названием триметиламинурии (синдром рыбного запаха).
По данным фармакокинетических исследований CYP-опосредованных реакций in vivo итоприд не оказывает ингибирующего или индуцирующего действия на изоферменты CYP2C19 и CYP2E1. Терапия итопридом не влияет на CYP или активность уридиндифосфат-глюкуронилтрансферазы.
Выведение
Итоприда гидрохлорид и его метаболиты выводятся в основном с мочой. Почечная экскреция итоприда и его N-оксида после однократного приема препарата внутрь в терапевтической дозе (50 мг) у здоровых людей составляла 3,7 и 75,4% соответственно. Период полувыведения итоприда гидрохлорида составляет около 6 ч.
Применяют для лечения желудочно-кишечных симптомов, связанных с нарушением моторики желудка или его замедленным опорожнением, таких как: вздутие живота, быстрое насыщение, чувство переполнения в желудке после приема пищи, боль или дискомфорт в эпигастральной области, снижение аппетита, изжога, тошнота и рвота; функциональная (неязвенная) диспепсия или хронический гастрит.
Повышенная чувствительность к итоприду или любому вспомогательному компоненту препарата; пациенты с желудочно-кишечным кровотечением, механической обструкцией или перфорацией; детский возраст до 16 лет (в связи с отсутствием данных по безопасности); беременность и период грудного вскармливания.
Итоприда гидрохлорид усиливает действие ацетилхолина, что может вызывать холинергические побочные реакции. Препарат следует назначать с осторожностью категории пациентов, для которых появление таких реакций может усугубить течение основного заболевания.
Пациентам пожилого возраста итоприд следует назначать с осторожностью, учитывая более высокую частоту снижения функции печени и почек, наличие сопутствующих заболеваний или другое лечение.
Фертильность
Данные о влиянии итоприда на фертильность у человека отсутствуют. Тем не менее исследования на животных не выявили признаков отрицательного влияния препарата на фертильность.
Беременность
На данный момент имеется ограниченное количество данных (менее 300 исходов беременности) по применению итоприда у беременных женщин. Исследования на животных не выявили признаков прямого или непрямого отрицательного влияния итоприда, указывающих на репродуктивную токсичность. В целях предосторожности следует избегать применения итоприда при беременности.
Период грудного вскармливания
Итоприд выделяется с молоком у животных, однако на данный момент отсутствует достаточное количество данных о выделении итоприда с грудным молоком у человека. При кормлении грудью нельзя исключать риск влияния препарата на ребенка. Решение о прекращении грудного вскармливания или отмене/перерыве в приеме препарата следует принимать, основываясь на оценке пользы грудного вскармливания для ребенка и пользы препарата для матери.
Взрослым назначают внутрь по 1 таблетке препарата Ганатон® 50 мг 3 раза в сутки до еды. Рекомендуемая суточная доза составляет 150 мг. Указанная доза может быть снижена с учетом возраста и симптомов больного.
В клинических исследованиях продолжительность лечения препаратом Ганатон® составляла до 8 недель.
Следующие побочные эффекты наблюдались у 998 пациентов при применении итоприда в стандартной суточной дозе 150 мг или ниже в ходе 4 плацебо-контролируемых, 4 сравнительных и 13 неконтролируемых интервенционных клинических исследованиях с частотой [часто (≥1/100 и <1/10) и нечасто (≥1/1000 и <1/100)]. В категориях с частотой очень часто (≥1/10), редко (≥1/10000 и <1/1000) или очень редко (< 1/10000) нежелательных реакций не наблюдалось.
| Система органов по классификации медицинского словаря для нормативно-правовой деятельности (MedDRA) | Частота | Нежелательные эффекты |
| Нарушения со стороны желудочно-кишечного тракта |
Часто Нечасто |
Боль в животе, диарея Повышенное слюноотделение |
| Лабораторные и инструментальные данные | Нечасто | Повышение активности аланинаминотрансферазы (АЛТ), снижение количества лейкоцитов |
| Нарушения со стороны нервной системы | Нечасто | Головокружение, головная боль |
| Нарушения со стороны кожи и подкожных тканей | Нечасто | Сыпь |
Следующие побочные эффекты были выявлены в ходе пострегистрационного применения, исходя из имеющихся данных оценить их частоту не представляется возможным.
Нарушения со стороны крови и лимфатической системы: лейкопения и тромбоцитопения.
Нарушения со стороны иммунной системы: реакции гиперчувствительности, включая анафилактоидную реакцию.
Нарушения со стороны эндокринной системы: повышение уровня пролактина в крови.
Нарушения со стороны нервной системы: головокружение, головная боль, тремор.
Нарушения со стороны желудочно-кишечного тракта: диарея, запор, боль в животе, повышенное слюноотделение и тошнота.
Нарушения со стороны печени и желчевыводящих путей: желтуха.
Нарушения со стороны кожи и подкожных тканей: сыпь, эритема и зуд.
Нарушения со стороны половых органов и молочной железы: гинекомастия.
Лабораторные и инструментальные данные: повышение активности аспартатаминотрансферазы (ACT), аланинаминотрансферазы (АЛТ), гамма-глютамилтранспептидазы, щелочной фосфатазы и уровня билирубина.
При передозировке показаны промывание желудка и симптоматическая терапия.
Метаболическое взаимодействие не ожидается, так как итоприд первично метаболизируется под действием флавиновой монооксигеназы, а не с участием системы цитохрома CYP450.
При одновременном применении варфарина, диазепама, диклофенака натрия, тиклопидина гидрохлорида, нифедипина и никардипина гидрохлорида изменений связывания с белками не наблюдалось.
Итоприд усиливает моторику желудка, поэтому он может повлиять на всасывание других препаратов, принимаемых внутрь.
Особую осторожность следует соблюдать при применении препаратов с низким терапевтическим индексом, а также лекарственных форм с замедленным высвобождением или препаратов с кишечнорастворимой оболочкой.
Противоязвенные препараты, такие как циметидин, ранитидин, тепренон и цетраксат, не влияют на прокинетическое действие итоприда.
Антихолинергические средства могут ослабить эффект итоприда.
Итоприд усиливает действие ацетилхолина и может вызвать холинэргические побочные реакции.
Данные о длительном применении препарата отсутствуют.
Исследований относительно влияния итоприда на способность к управлению автомобилем и механизмами не проводилось.
Однако в период лечения препаратом следует соблюдать осторожность при выполнении потенциально опасных видов деятельности, требующих повышенной концентрации внимания и быстроты психомоторных реакций (управление транспортными средствами, работа с движущимися механизмами, работа диспетчера и оператора), так как применение препарата может вызвать головокружение.
Таблетки, покрытые пленочной оболочкой, 50 мг.
По 10 или 14 таблеток в контурную ячейковую упаковку (блистер) из пленки ПВХ/ПВДХ/Аl фольги алюминиевой.
По 1, 2, 3, 4 или 5 в контурных ячейковых упаковок вместе с инструкцией по применению в пачку картонную с контролем первого вскрытия.
Хранить при температуре не выше 25 °С.
Хранить в недоступном для детей месте!
3 года.
Не применять после истечения срока годности.
По рецепту
Регистрационный номер
ЛС-002513
Дата регистрации
2011-09-09
Дата переоформления
2021-06-29
Владелец регистрационного удостоверения
ЭББОТТ ЛЭБОРАТОРИЗ ООО
Россия
Производитель
Представительство
ЭББОТТ ЛЭБОРАТОРИЗ ООО
Россия
Ганатон®
МНН: Итоприд
Производитель: Майлан ИПиДи Г.К.
Анатомо-терапевтическо-химическая классификация: Стимуляторы моторики ЖКТ
Номер регистрации в РК:
№ РК-ЛС-5№019454
Информация о регистрации в РК:
29.11.2017 — 29.11.2022
- Скачать инструкцию медикамента
Торговое название
Ганатон®
Международное непатентованное название
Итоприд
Лекарственная форма
Таблетки, покрытые пленочной оболочкой, 50 мг
Состав
Одна таблетка содержит
активное вещество — итоприда гидрохлорид 50 мг,
вспомогательные вещества — лактозы моногидрат, крахмал кукурузный, кармеллоза, кислота кремниевая слабая безводная, магния стеарат;
состав оболочки таблетки – гипромеллоза 2910, макрогол 6000, титана диоксид (Е 171), воск карнаубский.
Описание
Таблетки круглой формы, покрытые пленочной оболочкой белого цвета, с разделительной риской на одной стороне и выдавленным кодом «НС 803» — на другой стороне.
Фармакотерапевтическая группа
Препараты для лечения функциональных нарушений со стороны ЖКТ. Стимуляторы моторики ЖКТ. Итоприд.
Код АТХ А03 FA 07
Фармакологические свойства
Фармакокинетика
Абсорбция. Итоприда гидрохлорид быстро и практически полностью всасывается из желудочно-кишечного тракта. Его относительная биодоступность составляет 60%, что связано с эффектом «первого прохождения» через печень. Пища не влияет на биодоступность. После применения 50 мг итоприда гидрохлорида Сmax достигается через 0.5-0.75 ч и составляет 0.28 мкг/мл. При последующем применении лекарственного средства в дозах от 50 мг до 200 мг 3 раза в день на протяжении 7 дней фармакокинетика итоприда гидрохлорида и его метаболитов была линейной с минимальной кумуляцией.
Распределение. Приблизительно 96 % итоприда гидрохлорида связывается с белками плазмы (преимущественно с альбумином). Связывание с α1-кислым гликопротеином составляет менее 15 %.
Метаболизм. Итоприда гидрохлорид активно биотрансформируется в печени. Идентифицированы 3 метаболита, только один из которых обнаруживает незначительную активность, которая не имеет фармакологического значения (приблизительно 2-3% итоприда гидрохлорида). Первичным метаболитом является N-оксид, который образуется в результате окисления четвертичной амино-N-диметильной группы.
Итоприда гидрохлорид метаболизируется под действием флавин-зависимой монооксигеназы (FMO3). Количество и эффективность изоферментов FMO у человека может отличаться в зависимости от генетического полиморфизма, который в редких случаях приводит к развитию аутосомно-рецессивного состояния, известного под названием триметиламинурия (синдром «рыбного запаха»). У пациентов, страдающих триметиламинурией, Т1/2 увеличивается.
Согласно данным фармакокинетических исследований in vivo итоприда гидрохлорид не проявляет ингибирующего или индуцирующего действия по отношению к CYP2C19 и CYP2E1. Применение итоприда гидрохлорида не влияет на содержание CYP или активность уридиндифосфат-глюкуронизилтрансферазы.
Выведение. Итоприда гидрохлорид и его метаболиты выводятся преимущественно с мочой. Почечная экскреция итоприда гидрохлорида и его N-оксида составляла 3.7% и 75.4% соответственно после одноразового внутреннего применения лекарственного средства здоровыми добровольцами в терапевтической дозе.
Терминальный Т1/2 итоприда гидрохлорида составлял приблизительно 6 ч.
Фармакодинамика
Итоприда гидрохлорид активирует пропульсивную моторику желудочно-кишечного тракта благодаря антагонизму с допаминовыми D2-рецепторами и ингибирующей активности ацетилхолинэстеразы. Итоприда гидрохлорид активирует высвобождение ацетилхолина и ингибирует его распад.
Итоприда гидрохлорид также проявляет противорвотное действие благодаря взаимодействию с D2-рецепторами, локализованными в хеморецепторной триггерной зоне, что было продемонстрировано дозо-зависимым ингибированием апоморфин-индуцированной рвоты.
Итоприда гидрохлорид продемонстрировал ускорение опорожнения желудка в исследованиях у людей.
В исследованиях при применении одной дозы итоприда гидрохлорид продемонстрировал стимулирующее действие на опорожнение желудка.
Действие итоприда гидрохлорида является высокоспецифическим по отношению к верхним отделам желудочно-кишечного тракта.
Итоприда гидрохлорид не влияет на уровень гастрина в сыворотке крови.
Показания к применению
Купирование желудочно-кишечных симптомов функциональной неязвенной диспепсии (хронического гастрита), а именно:
— вздутие живота
— ощущение быстрого насыщения
— боль и дискомфорт в верхней части живота
— анорексия
— изжога
— тошнота
— рвота
Способ применения и дозы
Для взрослых рекомендованная доза составляет 150 мг в сутки (по 1 таблетке (50 мг) 3 раза в день перед приемом пищи). Указанная доза может быть снижена с учетом возраста пациента и симптомов (см. раздел «Особые указания»).
В клинических исследованиях длительность применения итоприда гидрохлорида у пациентов составляла до 8 недель.
Побочные действия
Побочные реакции, о которых сообщалось во время клинических исследований
Редко
— диарея, боль в животе
— головная боль
— снижение уровня лейкоцитов (лейкопения), повышение уровня пролактина
О следующих побочных реакциях сообщалось у пациентов, которые получали лечение итопридом гидрохлоридом (при практическом применении):
Редко
— лейкопения, тромбоцитопения
— анафилактоидная реакция
— повышение уровня пролактина, гинекомастия
— головокружение, головная боль, тремор
— повышенное слюноотделение, тошнота, боль в животе, диарея, запор
— желтуха
— сыпь, покраснение, зуд
— повышение уровней АСТ, АЛТ, ГГТ, щелочной фосфатазы, билирубина
Противопоказания
— повышенная чувствительность к итоприда гидрохлориду и другим компонентам препарата
— состояния, при которых повышение сократительной активности желудочно-кишечного тракта может быть вредным, например, при желудочно-кишечном кровотечении, механической обструкции или перфорации
Лекарственные взаимодействия
Метаболические взаимодействия не ожидаются в связи с тем, что итоприда гидрохлорид первично метаболизируется флавин-монооксигеназой, а не изоферментами системы цитохрома Р450.
Не наблюдалось никаких изменений связывания с белками при одновременном назначении с варфарином, диазепамом, диклофенаком натрия, тиклопидина гидрохлоридом, нифедипином и никардипина гидрохлоридом. В связи с тем, что итоприда гидрохлорид усиливает моторику желудка, он может влиять на процесс всасывания других лекарственных средств при одновременном назначении. Особенно осторожным необходимо быть при применении лекарственных средств с низким терапевтическим индексом, лекарственных форм с замедленным высвобождением или с кишечнорастворимой оболочкой.
Противоязвенные лекарственные средства такие, как циметидин, ранитидин, тепренон и цетраксат, не влияют на прокинетическое действие итоприда гидрохлорида.
Антихолинергические лекарственные средства могут снижать действие итоприда гидрохлорида.
Особые указания
Общие предостережения
Итоприда гидрохлорид усиливает действие ацетилхолина и может проявлять холинергичные побочные реакции. Данные о длительном применении отсутствуют.
Итоприда гидрохлорид следует назначать с осторожностью пациентам пожилого возраста и следить за их состоянием, поскольку у них чаще встречаются снижение функции почек, печени и сопутствующие заболевания или сопутствующая терапия другими лекарственными средствами.
Беременность и период лактации
Безопасность применения итоприда гидрохлорида в период беременности не установлена. Поэтому итоприда гидрохлорид не следует применять во время беременности за исключением случаев, когда ожидаемая польза от применения препарата превышает возможный риск.
В доклинических исследованиях тератогенный эффект не наблюдался.
Итоприда гидрохлорид выделяется в грудное молоко. С целью предотвращения возникновения побочных реакций у грудных детей должно быть принято соответствующее решение относительно прекращения грудного кормления или прекращения лечения, с учетом важности терапии для матери.
Дети
Безопасность применения итоприда гидрохлорида у детей в возрасте до 18 лет не установлена.
Особенности влияния лекарственного средства на способность управлять транспортным средством или потенциально опасными механизмами
Влияние маловероятно.
Передозировка
Симптомы: усиление побочных действий
Лечение: В случае чрезмерной передозировки необходимо принять обычные меры по промыванию желудка и симптоматическое лечение.
Форма выпуска и упаковка
По 10 таблеток помещают в контурную ячейковую упаковку из пленки поливинилхлоридной/поливинилдихлоридной (ПВХ/ПВДХ) и фольги алюминиевой. По 4 контурных упаковки вместе с инструкцией по медицинскому применению на государственном и русском языках вкладывают в картонную коробку.
Условия хранения
Хранить при температуре не выше 25 0С.
Хранить в недоступном для детей месте!
Срок хранения
3 года
Не применять препарат по истечении срока годности, указанного на упаковке.
Условия отпуска из аптек
По рецепту
Производитель
Майлан ИПиДи Г.К., Япония / Mylan EPD G.K., Japan
(2-1, Inokuchi 37, Katsuyama, Fukui 911-8555, Japan.)
Владелец регистрационного удостоверения
Абботт Лабораториз ГмбХ, Ганновер, Германия
Упаковщик
Майлан ИПиДи Г.К., Япония / Mylan EPD G.K., Japan
(2-1, Inokuchi 37, Katsuyama, Fukui 911-8555, Japan.)
Адрес организации, принимающей на территории Республики Казахстан претензии от потребителей по качеству продукции (товара) и ответственной за пострегистрационное наблюдение за безопасностью лекарственного средства.ТОО «Абботт Казахстан»
050059, г. Алматы, пр. Достык 117/6 БЦ Хан Тенгри 2
тел.: +7 727 244 75 44, факс: +7 727 244 76 44
эл. адрес: pv.kazakhstan@abbott.com
CCDS03440807
| 995672241477976970_ru.doc | 76 кб |
| 874954771477978130_kz.doc | 83 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники