05.09.2022
Описание препарата Газива® (концентрат для приготовления раствора для инфузий, 1000 мг/40 мл) основано на официальной инструкции, утверждено компанией-производителем в 2022 году
Дата согласования: 05.09.2022
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Заказ в аптеках Москвы
- Отзывы
Действующее вещество
ATX
Фармакологическая группа
Состав
| Концентрат для приготовления раствора для инфузий | 1 фл./1 мл |
| действующее вещество: | |
| обинутузумаб | 1000 мг/25 мг |
| вспомогательные вещества: L-гистидин — 57,6 мг; L-гистидина гидрохлорида моногидрат — 89,6 мг; α,α-трегалозы дигидрат — 3632,0 мг; полоксамер 188 — 8,0 мг; вода для инъекций — до 40 мл |
Описание лекарственной формы
Прозрачная или опалесцирующая жидкость от бесцветного до слегка коричневатого цвета.
Фармакологическое действие
Фармакологическое действие
—
противоопухолевое.
Фармакодинамика
Механизм действия. Обинутузумаб представляет собой рекомбинантное, гуманизированное, моноклональное антитело II типа с модифицированной схемой гликозилирования, принадлежащее к классу IgG1 и обладающее специфичностью к антигену CD20. Обинутузумаб избирательно взаимодействует с внеклеточным участком трансмембранного антигена СD20, расположенного на поверхности нормальных и злокачественных зрелых B-лимфоцитов и их предшественников, при этом не связывается со стволовыми гемопоэтическими клетками, про-В-лимфоцитами, плазматическими клетками, а также другими нормальными тканями.
Благодаря модификации схемы гликозилирования Fc-фрагмента, обинутузумаб обладает повышенным сродством к рецепторам FcγRIII на поверхности эффекторных клеток иммунной системы, в частности натуральных киллеров, макрофагов и моноцитов, по сравнению с антителами, не прошедшими такую модификацию.
Обинутузумаб напрямую индуцирует гибель клеток, опосредует антителозависимую клеточную цитотоксичность (АЗКЦ) и антителозависимый клеточный фагоцитоз (АЗКФ) путем привлечения FcγRIII-положительных эффекторных клеток иммунной системы. Кроме того, обинутузумаб в низкой степени индуцирует комплементзависимую цитотоксичность (КЗЦ). По сравнению с анти-CD20-антителами I типа обинутузумаб (антитело II типа) обладает повышенной способностью к прямой индукции гибели клеток на фоне пониженной способности вызывать КЗЦ. Благодаря модификации схемы гликозилирования, обинутузумаб более эффективно индуцирует АЗКЦ и АЗКФ по сравнению с анти-CD20-антителами, не прошедшими такую модификацию, что проявляется в более выраженном истощении пула B-клеток и повышенной противоопухолевой активности.
Истощение пула CD19+ B-клеток (до значений <0,07·109/L) наблюдалось у 91% пациентов с хроническим лимфолейкозом (ХЛЛ) после завершения терапии обинутузумабом в комбинации с хлорамбуцилом и сохранялось в течение 6 месяцев.
Восстановление числа В-клеток происходило в течение 12–18 месяцев у 35% пациентов при отсутствии прогрессирования и у 13% пациентов с прогрессированием заболевания.
В опорном клиническом исследовании у пациентов с индолентной неходжкинской лимфомой у 97% оцениваемых пациентов, получающих препарат Газива®, отмечалось истощение пула B-клеток в конце терапии, а у 97% пациентов истощение сохранялось более 6 месяцев после введения последней дозы. Восстановление числа B-клеток наблюдалось в течение 12–18 месяцев у 11% оцениваемых пациентов.
Иммуногенность. Тестирование на наличие антител к лекарственному препарату (антитерапевтических антител, AТA) проводилось в различных временных точках у пациентов с ХЛЛ. У 10 из 146 пациентов, получавших препарат Газива®, были обнаружены антитела к препарату через 12 месяцев после завершения последнего цикла терапии. У пациентов не выявлено случаев анафилаксии или реакций гиперчувствительности, связанных с AТA, или негативного влияния на клинический ответ.
У пациентов с индолентной неходжкинской лимфомой (иНХЛ) не отмечалось образования HAHA (антитела человека к антителам человеческого происхождения — Human Anti-Human Antibody) по сравнению с исходным уровнем. У 0,2% пациентов с ранее нелеченной фолликулярной лимфомой развивались HAHA на момент завершения индукции. Несмотря на то что клиническая значимость HAHA неизвестна, потенциальная взаимосвязь между развитием HAHA и клиническим течением заболевания не может быть исключена.
Результаты анализа иммуногенности в значительной степени зависят от различных факторов, таких как чувствительность и специфичность анализа, методология проведения анализа, чувствительность анализа к концентрации препарата Газива®/антител в сыворотке крови, манипуляции с забранными образцами, время забора образцов, сопутствующие препараты и характер основного заболевания. Таким образом, сравнение частоты обнаружения антител к препарату Газива® и частоты обнаружения антител к другим биологическим препаратам может оказаться неинформативным.
Фармакокинетика
Всасывание. Обинутузумаб вводится внутривенно. Другие пути введения препарата не изучались.
Рассчитанное значение медианы максимальной концентрации (Cmax) после инфузии в цикле 6, день 1-й, у пациентов с ХЛЛ составило 465,7 мкг/мл, а значение площади под кривой «концентрация-время» за период дозирования AUC(τ) составило 8961 мкг×д/мл и у пациентов с индолентной неходжкинской лимфомой (иНХЛ) — 539,3 мкг/мл и 10956 мкг×д/мл, соответственно.
Распределение. После внутривенного введения объем распределения в центральной камере (Vd) составляет 2,72 л и приблизительно равен объему сыворотки. Значения Vd и объема распределения обинутузумаба при равновесном состоянии (Vss) свидетельствуют о том, что распределение происходит только в плазме крови и внеклеточной жидкости.
Метаболизм. Отдельных исследований метаболизма обинутузумаба не проводилось. Как и другие антитела, обинутузумаб преимущественно подвергается катаболизму.
Выведение. Клиренс обинутузумаба у пациентов с ХЛЛ составлял примерно 0,11 л/день и у пациентов с иНХЛ примерно 0,08 л/день с медианой периода полувыведения (T1/2) 26,4 дня при ХЛЛ и 36,8 дня для иНХЛ.
Выведение обинутузумаба характеризуется как линейным, так и нелинейным клиренсом. В начальном периоде лечения зависящий от времени нелинейный клиренс является основным, но с продолжением терапии его вклад постепенно уменьшается, и доминирующим становится линейный путь. Это указывает на опосредованное мишенью распределение препарата (ОМРП), при котором избыток CD20+ В-клеток определяет резкое снижение концентрации обинутузумаба в сыворотке крови. Когда большинство CD20+ В-клеток связано с обинутузумабом, ОМРП оказывает минимальное влияние на фармакокинетику препарата.
Особые группы пациентов
Пол. По данным популяционного анализа, клиренс в равновесном состоянии (Clss) и Vd у мужчин выше на 18 и 19%, соответственно. Тем не менее, отличия в экспозиции обинутузумаба у мужчин и у женщин незначительны (при ХЛЛ медианы AUC и Cmax в 6-м цикле составили 11282 мкг×д/мл и 578,9 мкг/мл у женщин и 8451 мкг×д/мл и 432,5 мкг/мл у мужчин соответственно; при иНХЛ медианы AUC и Cmax составили 13172 мкг×д/мл и 635,7 мкг/мл у женщин и 9769 мкг×д/мл и 481,3 мкг/мл у мужчин соответственно), коррекции дозы в зависимости от пола не требуется.
Пожилой и старческий возраст. Не отмечено значительных различий в фармакокинетике обинутузумаба у пациентов в возрасте <65 лет, от 65 до 75 лет и у пациентов в возрасте >75 лет.
Нарушение функции почек. Значения фармакокинетических параметров обинутузумаба у пациентов с нарушением функции почек легкой (клиренс креатинина (Cl креатинина) 50–89 мл/мин) и средней (Cl креатинина 30–49 мл/мин) степени тяжести схожи с таковыми у пациентов с нормальной функцией почек (Cl креатинина ≥90 мл/мин). Данные по фармакокинетике у пациентов с нарушением функции почек тяжелой степени (Cl креатинина 15–29 мл/мин) ограничены, поэтому дать специальные указания по дозированию не представляется возможным.
Нарушения функции печени. Специальных исследований фармакокинетики у пациентов с нарушениями функции печени не проводилось.
Показания
хронический лимфолейкоз. В комбинации с хлорамбуцилом у взрослых пациентов с ранее нелеченным хроническим лимфолейкозом и с сопутствующими заболеваниями, при которых невозможно проведение терапии на основе флударабина в полной дозе.
фолликулярная лимфома (ФЛ). В комбинации с химиотерапией и последующей поддерживающей монотерапией препаратом Газива® (при достижении, как минимум, частичной ремиссии) у взрослых пациентов с ранее нелеченной ФЛ (стадия II с любыми нодальными или экстранодальными вовлечениями ≥7 см в диаметре, стадия III или IV).
в комбинации с бендамустином и последующей поддерживающей монотерапией препаратом Газива®у взрослых пациентов с фолликулярной лимфомой, не ответивших на лечение ритуксимабом или на лечение по содержащей ритуксимаб схеме, или у которых развилось прогрессирование заболевания во время или в течение 6 месяцев после такого лечения.
Противопоказания
гиперчувствительность к обинутузумабу и к другим компонентам препарата;
активный гепатит B и/или другие инфекции в активной фазе;
нарушения функции почек тяжелой степени при хроническом лимфолейкозе (Cl креатинина <30 мл/мин) и при фолликулярной лимфоме (Cl креатинина <40 мл/мин) (эффективность и безопасность применения не установлены);
нарушения функции печени (эффективность и безопасность применения не установлены);
вакцинация живыми вирусными вакцинами;
беременность;
период грудного вскармливания;
детский возраст до 18 лет (эффективность и безопасность применения у детей не установлены).
С осторожностью: хронические и рецидивирующие инфекции в анамнезе.
Применение при беременности и кормлении грудью
Беременность и период грудного вскармливания. Необходимо рассмотреть отсрочку проведения вакцинации живыми вакцинами у младенцев, чьи матери получали препарат Газива® во время беременности, до тех пор, пока число В-клеток у них не восстановится до нормы.
Обинутузумаб проникает в молоко животных. Грудное вскармливание не рекомендуется во время лечения и как минимум в течение 18 месяцев после введения последней дозы препарата Газива®.
Контрацепция. Женщины, обладающие репродуктивным потенциалом, должны использовать эффективные методы контрацепции в период лечения препаратом Газива® и в течение 18 месяцев после окончания терапии.
Способ применения и дозы
Внутривенно (в/в) капельно, через отдельный катетер. Вводить препарат в/в струйно или болюсно нельзя.
Препарат Газива® должен вводиться квалифицированным медицинским персоналом. Препарат предназначен для введения как в амбулаторно-поликлинических, так и в стационарных условиях.
Подготовка препарата к введению должна проводиться в асептических условиях, т.к. препарат Газива® не содержит антимикробных консервантов.
Для введения препарата Газива® следует использовать только 0,9% раствор натрия хлорида. Не следует использовать другие растворители, в частности раствор декстрозы (5%).
Совместимость. Препарат Газива® в виде раствора с концентрацией 0,4–20 мг/мл совместим с инфузионными пакетами из поливинилхлорида, полиэтилена, полипропилена или полиолефина, инфузионными системами из поливинилхлорида, полиуретана или полиэтилена, со встраиваемыми фильтрами из полиэфирсульфона, 3-ходовым запорным краном из поликарбоната, с катетерами из полиэфируретана.
Раствор препарата Газива® нельзя замораживать и встряхивать.
Премедикация и профилактика синдрома лизиса опухоли (СЛО). Пациентам с высокой опухолевой нагрузкой и/или высоким содержанием лимфоцитов в периферической крови (>25·109/л) и/или нарушением функции почек (Cl креатинина <70 мл/мин) требуется профилактика СЛО, поскольку они находятся в группе риска развития СЛО. Профилактика включает адекватную гидратацию и назначение гипоурикемических препаратов (например, аллопуринола или других альтернативных препаратов) перед инфузией препарата Газива® в соответствии со стандартной практикой. В случае если состояние пациента по-прежнему соответствует критериям СЛО, перед каждой последующей инфузией также необходимо проводить профилактику СЛО.
Премедикация и профилактика инфузионных реакций. Информация о проведении премедикации для снижения риска развития инфузионных реакций приведена в таблице 1. Премедикация глюкокортикостероидами (ГКС) рекомендована для пациентов с ФЛ и обязательна для пациентов с ХЛЛ при первой инфузии. Премедикацию при последующих инфузиях и другие виды премедикации следует проводить как описано ниже.
Учитывая то, что одним из проявлений инфузионных реакций может быть понижение артериального давления, следует рассмотреть возможность приостановки лечения антигипертензивными средствами в течение 12 часов перед каждой инфузией на протяжении инфузии и в течение 1 часа после ее окончания.
Таблица 1
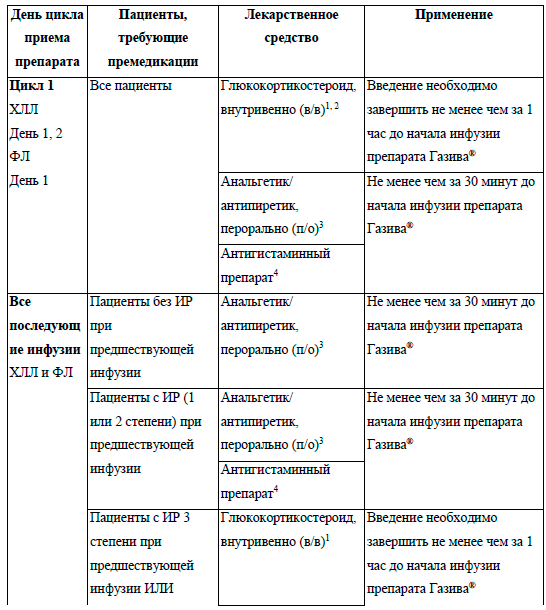
Премедикация перед введением препарата Газива®, необходимая для снижения риска развития инфузионных реакций (ИР)
| День цикла приема препарата | Пациенты, требующие премедикации | Лекарственное средство | Применение |
| Цикл 1-й | |||
| ХЛЛ, дни 1-й, 2-й | Все пациенты | ГКС (в/в)1,2 | Введение необходимо завершить не менее чем за 1 час до начала инфузии препарата Газива® |
| ФЛ, день 1-й | Анальгетик/антипиретик, перорально (п/о)3 | Не менее чем за 30 минут до начала инфузии препарата Газива® | |
| Антигистаминный препарат4 | |||
| Все последующие инфузии ХЛЛ и ФЛ | |||
| Пациенты без ИР при предшествующей инфузии | Анальгетик/антипиретик, перорально (п/о)3 | Не менее чем за 30 минут до начала инфузии препарата Газива® | |
| Пациенты с ИР (1-й или 2-й степеней) при предшествующей инфузии | Анальгетик/антипиретик, перорально (п/о)3 | Не менее чем за 30 минут до начала инфузии препарата Газива® | |
| Антигистаминный препарат4 | |||
| Пациенты с ИР 3-й степени при предшествующей инфузии или пациенты с числом лимфоцитов >25·109/л перед проведением инфузии | ГКС (в/в)1,2 | Введение необходимо завершить не менее чем за 1 час до начала инфузии препарата Газива® | |
| Анальгетик/антипиретик, перорально (п/о)3 | Не менее чем за 30 минут до начала инфузии препарата Газива® | ||
| Антигистаминный препарат4 |
1 100 мг преднизона/преднизолона или 20 мг дексаметазона или 80 мг метилпреднизолона. Не следует применять гидрокортизон, т.к. он не является эффективным для предотвращения ИР.
2 Профилактическое внутривенное введение ГКС не требуется в том случае, если препарат Газива® вводится в один день с комплексной химиотерапией, уже содержащей ГКС. В таком случае необходимо принять ГКС перорально как минимум за 60 минут до введения препарата Газива®.
3 Например 1000 мг ацетаминофена/парацетамола.
4 Например 50 мг дифенгидрамина.
Стандартный режим дозирования
ХЛЛ (в комбинации с хлорамбуцилом)
Цикл 1. Рекомендуемая доза препарата Газива®составляет 1000 мг в/в в течение 1-го и 2-го дней, далее в 8-й день и 15-й день 1-го 28-дневного цикла, как указано в таблице 2.
Для введения первой дозы препарата Газива®необходимо подготовить два инфузионных пакета, содержащих 100 мг препарата для первой инфузии и 900 мг — для второй.
В том случае, если при введении 100 мг препарата Газива®не потребуется снизить скорость или прервать введение препарата, то 900 мг препарата Газива®можно вводить в тот же день (без приостановки лечения) при условии, что в течение всей инфузии имеются соответствующие условия, необходимое время для проведения инфузии и медицинское наблюдение. Если введение 100 мг препарата пришлось прервать или изменить скорость, вводить 900 мг в тот же день нельзя (см. таблицу 2).
Циклы 2–6. Рекомендуемая доза препарата Газива® составляет 1000 мг с введением в 1-й день каждого 28-дневного цикла лечения, как указано в таблице 2.
Таблица 2
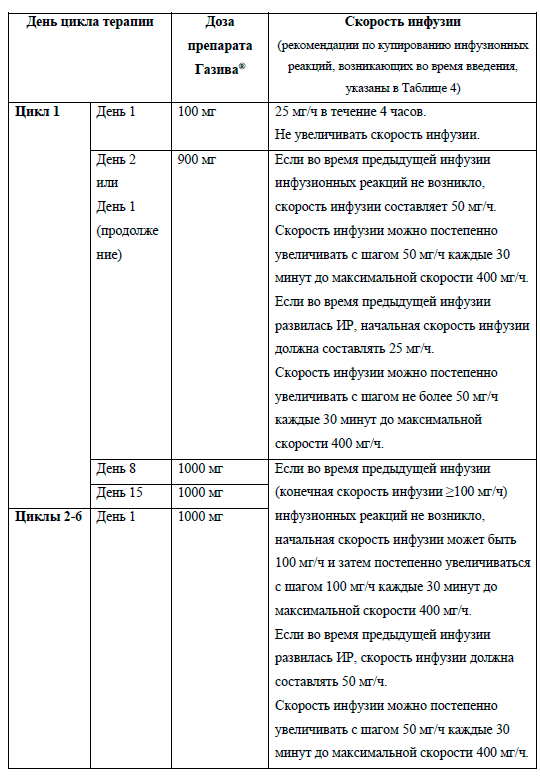
Введение препарата Газива®при ХЛЛ
| День цикла терапии | Доза препарата Газива® | Скорость инфузии (рекомендации по купированию инфузионных реакций, возникающих во время введения, указаны в Таблице 4) | |
| Цикл 1-й | День 1-й | 100 мг | 25 мг/ч в течение 4 часов. Не увеличивать скорость инфузии |
| День 2-й или День 1-й продолжение) |
900 мг | Если во время предыдущей инфузии ИР не возникло, скорость инфузии составляет 50 мг/ч. Скорость инфузии можно постепенно увеличивать с шагом 50 мг/ч каждые 30 минут до максимальной скорости 400 мг/ч. Если во время предыдущей инфузии развилась ИР, начальная скорость инфузии должна составлять 25 мг/ч. Скорость инфузии можно постепенно увеличивать с шагом не более 50 мг/ч каждые 30 минут до максимальной скорости 400 мг/ч |
|
| День 8-й | 1000 мг | Если во время предыдущей инфузии (конечная скорость инфузии ≥100 мг/ч) ИР не возникло, начальная скорость инфузии может быть 100 мг/ч и затем постепенно увеличиваться с шагом 100 мг/ч каждые 30 минут до максимальной скорости 400 мг/ч. Если во время предыдущей инфузии развилась ИР, скорость инфузии должна составлять 50 мг/ч. Скорость инфузии можно постепенно увеличивать с шагом 50 мг/ч каждые 30 минут до максимальной скорости 400 мг/ч |
|
| День 15-й | 1000 мг | ||
| Циклы 2–6-й | День 1-й | 1000 мг |
Режим дозирования хлорамбуцила. Применение препарата Газива®в комбинации с хлорамбуцилом изучено для режима дозирования хлорамбуцила 0,5 мг/кг перорально в день 1 и день 15 каждого цикла терапии (циклы 1–6-й).
Пропуск дозы (ХЛЛ). При пропуске запланированной дозы препарата Газива® необходимо ввести препарат как можно раньше; не следует ждать следующего запланированного введения. Между введениями следует выдерживать рекомендуемый интервал.
ФЛ
Рекомендуемая доза препарата Газива® составляет 1000 мг в/в как указано в таблице 3.
Ранее нелеченная ФЛ
— шесть 28-дневных циклов в комбинации с бендамустином или
— шесть 21-дневных циклов в комбинации с CHOP (циклофосфамид, доксорубицин, винкристин и преднизолон), затем — 2 дополнительных цикла препарата Газива®в монотерапии или
— восемь 21-дневных циклов в комбинации с CVP (циклофосфамид, винкристин, преднизолон).
Пациенты с ранее нелеченной ФЛ, ответившие на терапию препаратом Газива®в комбинации с химиотерапией с достижением полного или частичного ответа, должны продолжать поддерживающую терапию препаратом Газива®в виде монотерапии в дозе 1000 мг один раз в 2 месяца не более 2 лет. При прогрессировании заболевания терапию препаратом Газива® следует прекратить.
Рефрактерная/рецидивирующая ФЛ
Пациентам с ФЛ, не ответившим на ритуксимабсодержащую терапию или имевшим прогрессирование заболевания во время/после такой терапии, следует вводить препарат Газива® в комбинации с бендамустином в течение шести 28-дневных циклов.
Пациенты с рефрактерной/рецидивирующей ФЛ, которые достигли полного или частичного ответа, или пациенты со стабильным заболеванием должны продолжать поддерживающую терапию препаратом Газива®в виде монотерапии в дозе 1000 мг один раз в 2 месяца не более 2 лет. При прогрессировании заболевания терапию препаратом Газива® следует прекратить.
Препарат Газива® следует вводить со стандартной скоростью инфузии в цикле 1 (см. таблицу 3). Пациентам, у которых не возникает инфузионных реакций ≥3-й степени тяжести во время цикла 1-го, препарат Газива® может вводиться в виде короткой (приблизительно 90 минут) инфузии, начиная с цикла 2-го и далее (см. таблицу 4).
Таблица 3
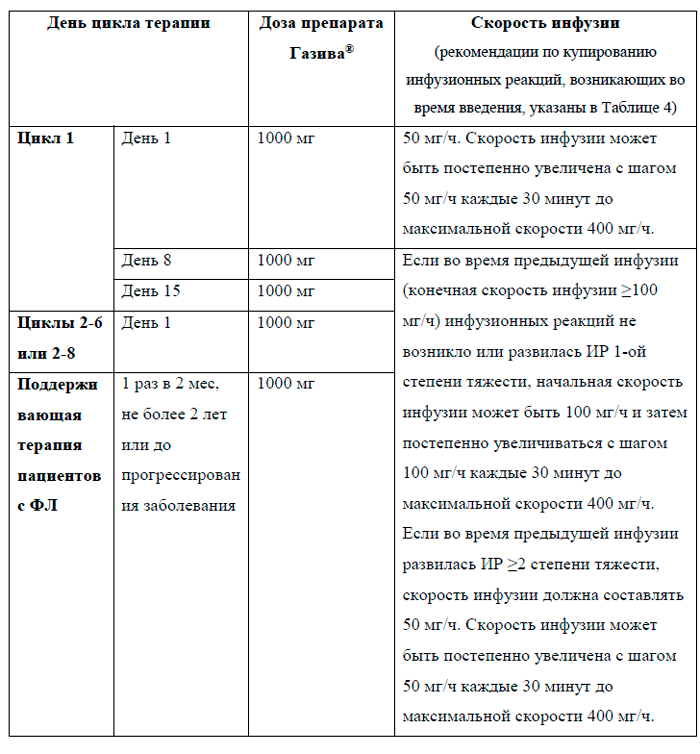
Введение препарата Газива®при ФЛ
| День цикла терапии | Доза препарата Газива® | Скорость инфузии (рекомендации по купированию инфузионных реакций, возникающих во время введения, указаны в таблице 5) | |
| Цикл 1-й | День 1-й | 1000 мг | 50 мг/ч. Скорость инфузии может быть постепенно увеличена с шагом 50 мг/ч каждые 30 минут до максимальной скорости 400 мг/ч |
| День 8-й | 1000 мг | Если во время предыдущей инфузии (конечная скорость инфузии ≥100 мг/ч) ИР не возникло или развилась ИР 1-й степени тяжести, начальная скорость инфузии может быть 100 мг/ч и затем постепенно увеличиваться с шагом 100 мг/ч каждые 30 минут до максимальной скорости 400 мг/ч. Если во время предыдущей инфузии развилась ИР≥2-й степени тяжести, скорость инфузии должна составлять 50 мг/ч. Скорость инфузии может быть постепенно увеличена с шагом 50 мг/ч каждые 30 минут до максимальной скорости 400 мг/ч |
|
| День 15-й | 1000 мг | ||
| Циклы 2-6-й или 2-8-й | День 1-й | 1000 мг | |
| Поддерживающая терапия пациентов с ФЛ | 1 раз в 2 мес не более 2 лет или до прогрессирования заболевания | 1000 мг |
Таблица 4
Введение препарата Газива®короткими инфузиями при ФЛ
| День цикла терапии | Доза препарата Газива® | Скорость инфузии (рекомендации по купированию инфузионных реакций, возникающих во время введения, указаны в Таблице 5) | |
| Циклы 2–6-й или 2–8-й | День 1-й | 1000 мг | Если во время цикла 1-го не возникло ИР ≥3-й степени тяжести: 100 мг/час в течение 30 минут, затем 900 мг/час в течение приблизительно 60 минут. Если во время предыдущей короткой инфузии развилась ИР 1–2-й степени тяжести с продолжающимися симптомами или ИР 3-й степени тяжести, то необходимо вводить препарат Газива® со стандартной скоростью (см. Таблицу 3) |
| Поддерживающая терапия | 1 раз в 2 мес., не более 2 лет или до прогрессирования заболевания | 1000 мг |
Режим дозирования бендамустина при рефрактерной/рецидивирующей и ранее нелеченной ФЛ. Применение препарата Газива®в комбинации с бендамустином изучено для режима дозирования бендамустина 90 мг/м2/сут внутривенно в дни 1 и 2 всех циклов терапии (циклы 1–6).
Режим дозирования циклофосфамида, винкристина, доксорубицина и преднизолона при ранее нелеченной ФЛ. Необходимо следовать рекомендациям по дозированию циклофосфамида, винкристина, доксорубицина и преднизолона (стандартные схемы CHOP и CVP), представленным в одобренных инструкциях по медицинскому применению данных препаратов и в специальной литературе.
Пропуск дозы (ФЛ). При пропуске запланированной дозы препарата Газива® необходимо ввести препарат как можно раньше; не следует ждать следующего запланированного введения или исключать пропущенную дозу.
Если проявления токсичности развиваются перед днем 8-м или днем 15-м цикла 1-го и возникает необходимость отложить введение, необходимо дождаться разрешения симптомов и после этого ввести соответствующую дозу. В таких случаях с учетом возникшей задержки должны быть перенесены все последующие визиты и начало цикла 2-го.
Во время поддерживающей терапии для введения последующих доз следует придерживаться изначального графика введения препарата.
Коррекция дозы (все показания)
Изменение дозы препарата Газива® не рекомендуется.
Рекомендации по изменению режима дозирования при возникновении симптоматических нежелательных явлений (включая инфузионные реакции) представлены в таблице 5 и в разделе «Особые указания».
Таблица 5
Рекомендации по коррекции скорости инфузии при развитии ИР (также см. «Особые указания»)
| Степень ИР | Рекомендации |
| 4-я степень (жизнеугрожающие ИР) | Остановить инфузию и полностью прекратить терапию |
| 3-я степень (тяжелые ИР) | Временно прекратить инфузию и провести симптоматическую терапию. При развитии ИР 3-й степени при стандартной скорости инфузии после разрешения симптомов возобновить инфузию со скоростью в два раза ниже, чем скорость предыдущей инфузии (скорость, с которой вводился препарат в то время, когда развились ИР). В дальнейшем при отсутствии каких-либо симптомов ИР скорость инфузии можно повышать с шагом и интервалом, рекомендованными в таблицах 2 и 3. При развитии ИР 3-й степени у пациентов с ФЛ при короткой инфузии после разрешения симптомов возобновить инфузию со скоростью в два раза ниже, чем скорость предыдущей инфузии (скорость, с которой вводился препарат в то время, когда развились ИР) и не более чем 400 мг/ч. Если инфузия завершается без повторного развития ИР 3-й степени, то следующую инфузию необходимо проводить со стандартной скоростью. В первом цикле терапии для пациентов с ХЛЛ, получающих первую дозу препарата Газива®, разделенную на два дня, в день 1 скорость инфузии может быть повышена через час после разрешения симптомов ИР, но не более чем до 25 мг/ч. При повторном развитии ИР 3-й степени тяжести инфузию следует остановить и полностью прекратить терапию |
| 1–2-я степень (ИР легкой и средней степени тяжести) | Снизить скорость инфузии и провести симптоматическую терапию. После разрешения симптомов продолжить инфузию. Если у пациента отсутствуют симптомы ИР, скорость инфузии можно повышать с шагом и интервалом, рекомендованными в таблице 2, 3 и 4. В первом цикле терапии для пациентов с ХЛЛ, получающих первую дозу препарата Газива®, разделенную на два дня, в день 1-й скорость инфузии может быть повышена через час после разрешения симптомов ИР, но не более чем до 25 мг/ч |
Особые указания по дозированию
Пожилой и старческий возраст. Коррекции дозы у пациентов пожилого и старческого возраста (≥65 лет) не требуется.
Дети. Эффективность и безопасность препарата Газива®у детей и подростков младше 18 лет не установлена.
Нарушение функции почек. Коррекции дозы препарата Газива®у пациентов с нарушением функции почек легкой и средней степени тяжести (Cl креатинина ≥30 мл/мин) не требуется. Эффективность и безопасность препарата Газива®у пациентов с нарушением функции почек тяжелой степени не установлены.
Нарушение функции печени. Эффективность и безопасность препарата Газива®у пациентов с нарушением функции печени не установлены.
Инструкция по приготовлению раствора для инфузий
Для введения первой дозы (1000 мг) препарата Газива® в первом цикле терапии ХЛЛ рекомендуется использовать 2 инфузионных пакета разного размера, что позволит различать дозу 100 мг, предназначенную для введения в цикле 1-м в день 1-й, и дозу 900 мг для введения в цикле 1-м в день 1-й или день 2-й (см. таблицу 6).
Из флакона отобрать 40 мл концентрата препарата Газива®.
Ввести 4 мл концентрата в инфузионный пакет объемом 100 мл, а оставшиеся 36 мл концентрата — в инфузионный пакет объемом 250 мл, содержащий стерильный апирогенный 0.9% раствор натрия хлорида. Промаркировать каждый инфузионный пакет.
Таблица 6
| Доза препарата Газива®, предназначенная для введения | Необходимое количество концентрата препарата Газива® | Объем инфузионного пакета |
| 100 мг | 4 мл | 100 мл |
| 900 мг | 36 мл | 250 мл |
| 1000 мг | 40 мл | 250 мл |
Введение препарата Газива® в 8-й день и 15-й день 1-го цикла и в 1-й день 2–6-го циклов терапии ХЛЛ и во все циклы терапии ФЛ
Из флакона отобрать 40 мл концентрата препарата Газива®и ввести в инфузионный пакет из ПВХ или полиолефина (неПВХ), содержащий стерильный апирогенный 0,9% раствор натрия хлорида.
Пакет следует осторожно перевернуть для перемешивания раствора, избегая избыточного образования пены.
Следует визуально проверить приготовленный раствор для инфузии на предмет механических включений и изменения окраски.
С точки зрения микробиологической чистоты, приготовленный раствор для инфузии следует использовать немедленно. В исключительных случаях приготовленный раствор может храниться не более 24 часов при температуре 2–8°C, если приготовление раствора для инфузий происходило в контролируемых и валидированных асептических условиях. При этом за условия хранения (правила хранения и продолжительность) отвечает специалист, готовивший раствор.
Приготовленный раствор препарата Газива® физически и химически стабилен в течение 24 часов при 2–8°C, затем в течение 24 часов при комнатной температуре (≤30 °C) и затем в течение не более 24 часов, во время которых должна быть завершена инфузия.
Побочные действия
Профиль безопасности препарата Газива® основан на данных клинического изучения препарата у пациентов с различными гематологическими заболеваниями (включая ХЛЛ и иНХЛ; всего около 4900 пациентов). Преимущественно препарат применялся в комбинации с режимами химиотерапии (CHOP, CVP, хлорамбуцил или бендамустин).
Наиболее серьезными нежелательными реакциями (НР) являлись:
— инфузионные реакции, наиболее часто встречавшиеся у пациентов с ХЛЛ (см. «Особые указания»);
— синдром лизиса опухоли, наиболее часто встречавшийся у пациентов с высокой опухолевой нагрузкой и/или высоким содержанием лимфоцитов в периферической крови и/или нарушением функции почек (см. «Особые указания»);
— тромбоцитопения, в некоторых случаях имевшая летальный исход в 1-м цикле (см. «Особые указания»).
Наиболее часто встречающимися НР у пациентов независимо от заболевания были ИР, нейтропения, диарея, запор и кашель.
В перечне ниже представлены нежелательные реакции, связанные с применением препарата Газива® в комбинации с различными режимами химиотерапии и по различным показаниям. Для описания частоты нежелательных реакций используется следующая классификация: очень часто (≥1/10), часто (≥1/100 и <1/10) и нечасто (≥1/1000 и <1/100). НР отнесены к той или иной категории на основании наиболее высокой частоты (различие ≥2% по сравнению с соответствующей группой сравнения), которая наблюдалась в любом из основных клинических исследований препарата Газива®.
Нежелательные реакции сгруппированы в соответствии с классами систем органов медицинского словаря для нормативно-правовой деятельности MedDRA.
В каждой категории нежелательные реакции указаны в порядке убывания частоты.
Травмы, интоксикации и осложнения манипуляций: очень часто — инфузионные реакции1.
Нарушения со стороны крови и лимфатической системы: очень часто — нейтропения, тромбоцитопения, лейкопения, анемия; часто – фебрильная нейтропения.
Инфекционные и паразитарные заболевания: очень часто — инфекции верхних дыхательных путей, синусит, инфекции мочевыводящих путей, опоясывающий лишай (Herpes Zoster), пневмония, назофарингит; часто — ринит, герпес слизистой оболочки полости рта, грипп, легочная инфекция, фарингит.
Общие расстройства и нарушения в месте введения: очень часто — утомляемость, повышение температуры тела, астения; часто — боль в груди.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения: очень часто — кашель; часто — боль в ротоглотке, заложенность носа, ринорея.
Нарушения обмена веществ и питания: часто — гипокалиемия, синдром лизиса опухоли, гиперурикемия.
Нарушения со стороны скелетно-мышечной системы и соединительной ткани: очень часто — артралгия, боль в спине, боли в конечностях; часто — боли в костях, скелетно-мышечные боли в грудной клетке.
Нарушения психики: очень часто — бессонница; часто — тревожность, депрессия.
Нарушения со стороны мочевыделительной системы: часто — недержание мочи, дизурия.
Нарушения со стороны сосудов: часто — повышение артериального давления.
Влияние на результаты лабораторных и инструментальных исследований: часто — снижение числа нейтрофилов, увеличение массы тела, снижение числа лейкоцитов.
Нарушения со стороны сердца: часто — фибрилляция предсердий.
Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы): часто — базальноклеточная карцинома, плоскоклеточная карцинома кожи.
Нарушения со стороны желудочно-кишечного тракта: очень часто — запор, диарея; часто — диспепсия, геморрой.
Нарушения со стороны кожи и подкожных тканей: очень часто — алопеция, зуд; часто — экзема.
Нарушения со стороны нервной системы: очень часто — головная боль.
1Определяется как любое связанное с терапией нежелательное явление, возникшее во время или в течение 24 часов после инфузии.
Описание отдельных нежелательных реакций
ИР
Наиболее часто (≥5%) наблюдались следующие симптомы ИР: тошнота, рвота, диарея, головная боль, головокружение, утомляемость, озноб, повышение температуры тела, понижение артериального давления, приливы, повышение артериального давления, тахикардия, одышка и дискомфорт в области грудной клетки. Кроме того, сообщалось о симптомах ИР со стороны дыхательной системы, таких как бронхоспазм, раздражение горла и гортани, хрипы, отек гортани и со стороны сердца: фибрилляция предсердий.
ХЛЛ. Частота инфузионных реакций составляет 65% при введении первой дозы (1000 мг). У 20% пациентов наблюдались ИР 3–4-й степени тяжести. У 7% пациентов ИР послужили причиной прекращения лечения препаратом Газива®. Частота ИР при последующих введениях составила соответственно 3% после 2-й дозы препарата Газива® (1000 мг) и 1% после введения последующих доз. ИР 3–4-й степени тяжести наблюдались только при введении первых 1000 мг препарата Газива®. При последующих введениях ИР 3–5-й степени не наблюдалось.
Комплекс мер по предупреждению ИР (см. «Способ применения и дозы») позволяет снизить частоту ИР за исключением ИР 3–4-й степени тяжести.
Неходжкинская лимфома. В цикле 1-м общая частота возникновения ИР была выше у пациентов, получавших препарат Газива® в комбинации с химиотерапией, по сравнению с пациентами из соответствующих групп сравнения. У пациентов, получавших препарат Газива®в комбинации с химиотерапией, частота возникновения ИР была самой высокой в день 1-й, постепенно снижалась при последующих инфузиях и продолжала снижаться во время поддерживающей монотерапии препаратом Газива®.
В целом у 4% пациентов развились ИР, послужившие причиной прекращения лечения препаратом Газива®.
В клиническом исследовании, разработанном для изучения профиля безопасности коротких (приблизительно 90 минут) инфузий после цикла 1 у пациентов с ранее нелеченной ФЛ, частота, тяжесть и типы симптомов ИР были аналогичны тем, что наблюдались у пациентов, получавших инфузии со стандартной скоростью введения.
Нейтропения и инфекции
ХЛЛ. Частота развития нейтропении на фоне терапии препаратом Газива® в комбинации с хлорамбуцилом составляет 40,7%, при этом частота развития инфекций составляет 38%. Нейтропения разрешалась спонтанно или после терапии гранулоцитарным колониестимулирующим фактором. Инфекционные осложнения 3–5-й степени тяжести наблюдались у 12% пациентов, а частота случаев с летальным исходом была <1%. Также сообщалось о случаях длительной нейтропении (2%) и нейтропении с поздней манифестацией (16%).
Неходжкинская лимфома. Нейтропения возникала чаще у пациентов, получавших лечение препаратом Газива® в комбинации с химиотерапией, по сравнению с пациентами из контрольных популяций, а риск ее развития был повышен в периоде индукции.
Частоты длительной нейтропении и нейтропении с поздним началом при лечении препаратом Газива® и химиотерапией составляли соответственно 3 и 7%. Частота возникновения инфекций составляла 78% при лечении препаратом Газива® в комбинации с химиотерапией (явления 3–5-й степени тяжести отмечались у 22%, и летальные исходы зарегистрированы у 3% пациентов).
Среди пациентов, получивших профилактическое лечение гранулоцитарным колониестимулирующим фактором, инфекции 3–5 степени тяжести встречались реже.
Тромбоцитопения и кровотечения
ХЛЛ. Общая частота развития тромбоцитопении на фоне терапии препаратом Газива® в комбинации с хлорамбуцилом составила 15,4%, при этом острая тромбоцитопения, развивающаяся в течение 24 часов после инфузии, наблюдалась у 4% пациентов. Частота кровотечений составила 8%. О фатальных случаях кровотечений сообщалось только в первом цикле терапии у 1% пациентов. Причинно-следственная связь между тромбоцитопенией и развитием кровотечений не установлена.
Неходжкинская лимфома. Тромбоцитопения возникала с повышенной частотой в 1-м цикле при лечении препаратом Газива® в комбинации с химиотерапией. Тромбоцитопения, развивающаяся в течение инфузии или не позднее 24 ч после инфузии (острая тромбоцитопения), чаще наблюдалась у пациентов, получавших терапию препаратом Газива® в комбинации с химиотерапией, чем у пациентов из групп сравнения.
Частота кровотечений всех степеней тяжести и кровотечений 3–5-й степени тяжести составила 12 и 4% соответственно. Частота случаев кровотечений с летальным исходом составила менее 1%, при этом в цикле 1 таких явлений не возникало.
Нарушение коагуляции, включая синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром). Собщалось о случаях развития ДВС-синдрома у пациентов с ФЛ и хроническим лимфолейкозом, получавших терапию препаратом Газива®. В некоторых случаях явления были связаны с ИР и/или СЛО. Специфичных исходных факторов риска развития ДВС-синдрома выявлено не было. Сообщалось о 3 пациентах, у которых развился ДВС-синдром (у одного пациента — серьезное явление, у 2 — несерьезное) среди 1135 пациентов, получавших терапию препаратом Газива® в трех крупнейших контролируемых исследованиях терапии ФЛ и хронического лимфолейкоза, спонсированных компанией. Все явления были отмечены в группе терапии обинутузумабом, в группах сравнения ни одного явления зарегистрировано не было. Все явления произошли в течение 1–2 дней после первой инфузии. Все пациенты продолжили лечение (см. «Особые указания»).
Прогрессирующая мультиочаговая лейкоэнцефалопатия (ПМЛ). ПМЛ зарегистрирована у пациентов, получавших препарат Газива®.
Реактивация вируса гепатита B. Сообщалось о случаях реактивации вируса гепатита B на фоне терапии препаратом Газива®.
Прогрессирование сопутствующих заболеваний сердца. На фоне терапии препаратом Газива® наблюдались случаи нарушения функции сердца, в т.ч. с летальным исходом.
Перфорация органов желудочно-кишечного тракта. Сообщалось о случаях перфорации органов желудочно-кишечного тракта у пациентов, получающих препарат Газива®, преимущественно по поводу неходжкинской лимфомы.
Поддерживающая терапия у пациентов с иНХЛ. У пациентов с рефрактерной/рецидивирующей иНХЛ во время поддерживающей монотерапии препаратом Газива®, проводимой после индукционной терапии препаратом Газива® в комбинации с бендамустином, самыми частыми НР были кашель (20,3%), нейтропения (12,7%), инфекции верхних дыхательных путей (12,0%), диарея (10,1%), бронхит (9,5%), синусит (9,5%), тошнота (8,9%), утомляемость (8,9%), ИР (8,2%), инфекция мочевыводящих путей (7,0%), назофарингит (7,0%), повышение температуры тела (7,0%), артралгия (6,3%), рвота (5,7%), сыпь (5,7%), пневмония (5,1%), одышка (5,1%) и боли в конечностях (5,1%). Самыми частыми нежелательными реакциями 3–5-й степени тяжести были нейтропения (10,8%), фебрильная нейтропения (1,9%) и анемия, тромбоцитопения, пневмония, сепсис, инфекция верхних дыхательных путей и инфекция мочевыводящих путей (все с частотой 1,3%).
Изменения лабораторных показателей. Транзиторное повышение активности печеночных ферментов (аспартатаминотрансферазы, аланинаминотрансферазы, щелочной фосфатазы) в сыворотке крови наблюдалось вскоре после первой инфузии препарата Газива®.
Взаимодействие
Специальных исследований взаимодействия с другими лекарственными средствами не проводилось.
Однако были проведены ограниченные подисследования межлекарственного взаимодействия препарата Газива® с бендамустином, препаратами схемы CHOP (циклофосфамид, доксорубицин, винкристин, преднизолон), препаратами схемы FC (флударабин, циклофосфамид) и хлорамбуцилом.
Совместное введение препарата Газива® не оказывало влияния на фармакокинетику бендамустина, FC или отдельных компонентов схемы CHOP; кроме того отсутствовало заметное влияние бендамустина, FC, хлорамбуцила или CHOP на фармакокинетику препарата Газива®.
Риск взаимодействия с одновременно применяемыми препаратами нельзя полностью исключить.
Передозировка
Опыт превышения рекомендованной дозы препарата Газива® отсутствует. Изучено применение доз от 50 до 2000 мг за одну инфузию. Степень тяжести и частота НР не зависели от дозы.
При случайном превышении дозы препарата Газива® необходимо немедленно прекратить инфузию или снизить дозу. В связи с увеличением риска инфекционных осложнений при истощении пула В-лимфоцитов следует тщательно наблюдать за пациентом и рассмотреть необходимость проведения развернутого общего анализа крови.
Особые указания
В медицинской документации пациента следует указывать торговое название препарата (Газива®) и номер серии. Замена препарата на какой-либо другой биологический лекарственный препарат требует согласования с лечащим врачом. Информация, представленная в данной инструкции, относится только к препарату Газива®.
Терапия препаратом Газива® должна назначаться онкологом или гематологом. Введение препарата проводится при наличии доступа к набору для оказания экстренной помощи. Врач, имеющий опыт применения химиотерапевтических препаратов, должен быть доступен в процессе проводимой терапии.
ИР. Наиболее часто наблюдаемыми нежелательными реакциями у пациентов, получающих препарат Газива®, были ИР, развившиеся преимущественно во время введения первых 1000 мг препарата. Комплекс мер по предупреждению ИР (применение подходящего ГКС, перорального анальгетика/антигистаминного препарата, пропуск приема антигипертензивного препарата) у пациентов с ХЛЛ позволяет снизить частоту ИР за исключением ИР 3–4-й степени.
Рекомендуется принимать меры по предупреждению ИР, описанные в разделе «Способ применения и дозы».
Частота и тяжесть инфузионных реакций существенно уменьшались после введения первых 1000 мг препарата Газива®, и при последующих инфузиях ИР у большинства пациентов не развивались.
В основном, независимо от показаний, наблюдались ИР легкой и средней степени тяжести, которые разрешались после замедления или временного прекращения первой инфузии, тем не менее известно также о тяжелых и жизнеугрожающих ИР, требующих симптоматической терапии. ИР могут клинически не отличаться от IgE-опосредованных аллергических реакций (например, анафилаксии). У пациентов с высокой опухолевой нагрузкой и/или с высоким содержанием циркулирующих лимфоцитов при ХЛЛ (>25·109/л) риск развития тяжелых ИР повышен. Меры по профилактике ИР описаны в разделе «Способ применения и дозы». Меры по купированию инфузионных реакций с учетом их степени тяжести описаны в разделе «Способ применения и дозы», таблица 5.
Терапию препаратом Газива® следует полностью прекратить в случае развития:
— жизнеугрожающих острых респираторных симптомов;
— ИР 4-й степени (угрожающих жизни);
— повторной (продолжающейся/рецидивирующей) ИР 3-й степени.
Пациенты с сопутствующими заболеваниями сердца или легких должны находиться под тщательным наблюдением во время инфузии и после нее. Во время инфузии препарата Газива® возможно понижение артериального давления. В связи с этим следует рассмотреть возможность приостановки лечения антигипертензивными препаратами в течение 12 часов перед каждой инфузией, на протяжении каждой инфузии и в продолжение 1 часа после введения препарата. Необходимо оценить пользу и возможный риск остановки приема антигипертензивных препаратов у пациентов с высоким риском развития гипертонического криза.
Реакции гиперчувствительности. На фоне терапии препаратом Газива® отмечались случаи реакций гиперчувствительности с немедленным (анафилаксия) и замедленным (сывороточная болезнь) развитием. Если во время или после инфузии подозревается развитие реакции гиперчувствительности (развитие симптомов происходит, как правило, при последующих введениях, очень редко симптомы развиваются во время первой инфузии), введение должно быть прекращено и терапию препаратом Газива® следует отменить и не возобновлять в дальнейшем. Пациентам с установленной гиперчувствительностью к препарату Газива® противопоказана терапия данным препаратом. Возможны затруднения при дифференциальной диагностике реакции гиперчувствительности и инфузионной реакции.
СЛО. Наблюдались случаи СЛО. Пациентам из группы риска развития СЛО (больные с высокой опухолевой нагрузкой и/или высоким содержанием лимфоцитов в периферической крови и/или нарушением функции почек (Cl креатинина <70 мл/мин) необходимо провести профилактику СЛО. Профилактика должна включать адекватную гидратацию и назначение гипоурикемических препаратов (например, аллопуринола или других альтернативных препаратов) до начала инфузии, как указано в разделе «Способ применения и дозы». Пациенты из группы риска развития СЛО должны находиться под тщательным наблюдением в первые дни терапии, при этом особое внимание следует уделять контролю функции почек, концентрации калия и мочевой кислоты. Дополнительные мероприятия должны проводиться в соответствии со стандартной практикой. При развитии СЛО необходимо тщательное наблюдение за функцией почек и водно-электролитным балансом с последующей коррекцией электролитных нарушений, а также проведением поддерживающих лечебных мероприятий, включая, если требуется, диализ.
Нейтропения. Наблюдались случаи серьезной и жизнеугрожающей нейтропении, включая фебрильную нейтропению. При развитии нейтропении пациенты нуждаются в тщательном наблюдении и проведении регулярного лабораторного обследования до полного разрешения симптомов. При необходимости следует провести терапию в соответствии с локально принятой практикой и рассмотреть необходимость применения гранулоцитарного колониестимулирующего фактора. При любом проявлении сопутствующей инфекции необходимо назначить соответствующее лечение. Возможно развитие нейтропении с поздней манифестацией (возникновение не раньше чем через 28 дней после окончания лечения) и длительной нейтропении продолжительностью более 28 дней после окончания или отмены терапии.
Тромбоцитопения. Наблюдались случаи серьезной и жизнеугрожающей тромбоцитопении, в том числе случаи острой тромбоцитопении, которые развивались в течение 24 часов после инфузии. В 1-м цикле терапии наблюдались случаи кровотечений с летальным исходом. Взаимосвязь между развитием кровотечений и тромбоцитопенией не установлена. В ходе лечения пациенты нуждаются в тщательном наблюдении на предмет развития тромбоцитопении, особенно в 1-м цикле. При выявлении тромбоцитопении необходимо регулярное проведение лабораторного обследования до тех пор, пока реакция не разрешится. В серьезных или жизнеугрожающих случаях следует рассмотреть возможность отложить введение препарата Газива®. Решение о проведении гемотрансфузии (трансфузии тромбоцитов) принимает лечащий врач в соответствии с практикой, установленной в лечебном учреждении. Необходимо принимать во внимание прием любых сопутствующих препаратов, способных усугубить тромбоцитопению, таких как ингибиторы агрегации тромбоцитов и антикоагулянты, особенно в 1-м цикле терапии.
Нарушение коагуляции, включая ДВС-синдром. Сообщалось о случаях развития ДВС-синдрома у пациентов с ФЛ и хроническим лимфолейкозом, получавших терапию препаратом Газива®. В большинстве случаев явления включали субклинические (бессимптомные) изменения лабораторных показателей тромбоцитов и коагулограммы после первой инфузии со спонтанным разрешением, как правило к 8-му дню. В некоторых случаях явления были связаны с ИР и/или СЛО. Специфичных исходных факторов риска развития ДВС-синдрома выявлено не было (см. «Побочные действия»).
Прогрессирование сопутствующих заболеваний сердца. У пациентов с сопутствующими заболеваниями сердца, получавших терапию препаратом Газива®, отмечалось развивитие аритмий (в частности, фибрилляции предсердий и тахиаритмии), стенокардии, острого коронарного синдрома, инфаркта миокарда и сердечной недостаточности (см. «Побочные действия»). Данные явления могут развиться как часть инфузионных реакций и иметь летальный исход. Таким образом, пациентов с заболеваниями сердца в анамнезе следует тщательно мониторировать. Кроме того, у таких пациентов следует соблюдать осторожность при проведении гидратации с целью избежать потенциального образования избытка жидкости.
Инфекции. Препарат Газива® не следует применять при наличии у пациента инфекции в активной стадии. Следует соблюдать осторожность при принятии решения о назначении препарата Газива® пациентам с периодически рецидивирующими и хроническими инфекциями в анамнезе. Возможно развитие серьезных бактериальных и грибковых инфекций, а также развитие или реактивация вирусных инфекций во время терапии и после ее окончания. Сообщалось о летальных случаях инфекционных заболеваний.
У пациентов с ФЛ зарегистрирована высокая частота развития инфекций на всех этапах клинических исследований, включая периоды последующего наблюдения. При этом наиболее высокая частота инфекций была характерна для периода поддерживающей терапии.
В периоде последующего наблюдения инфекции 3–5-й степеней тяжести чаще наблюдались у пациентов, которые на этапе индукции получали препарат Газива® в комбинации с бендамустином.
Реактивация вируса гепатита В. На фоне применения анти-CD-20 препаратов возможна реактивация вируса гепатита В, в некоторых случаях сопровождающаяся фульминантным гепатитом, печеночной недостаточностью, возможен летальный исход.
Перед назначением препарата Газива® всем пациентам следует пройти скрининг на вирус гепатита В, включая определение HBsAg-статуса, HBcAb-статуса, а также дополнительных маркеров согласно установленной местной практике. Препарат Газива® не следует применять пациентам с активным гепатитом B. Пациентам с положительными серологическими маркерами гепатита B следует проконсультироваться с врачом-гепатологом перед назначением препарата Газива®. В отношении таких пациентов необходимо проводить соответствующий мониторинг и принимать меры по профилактике реактивации вируса гепатита B в соответствии с местными стандартами.
ПМЛ. У пациентов, получавших терапию препаратом Газива®, отмечалась ПМЛ (см. «Побочные действия»). При развитии у пациентов новых неврологических симптомов или изменении уже имеющихся необходимо рассмотреть возможность диагноза ПМЛ. Симптомы ПМЛ не являются специфическими и могут варьировать в зависимости от локализации повреждения в головном мозге. Часто наблюдаются моторные симптомы с пирамидными нарушениями (например, мышечная слабость, паралич и нарушения чувствительности), аномалии чувствительности, мозжечковые нарушения и дефекты поля зрения. Могут развиться некоторые признаки/симптомы, считающиеся «корковыми» (например, афазия или визуально-пространственная дезориентация). Диагностика ПМЛ включает, но не ограничивается консультацией врача-невролога, проведением магнитно-резонансной томографии головного мозга и люмбарной пункцией (анализ спинно-мозговой жидкости на содержание ДНК JC-вируса). Терапию препаратом Газива® необходимо приостановить на время проведения обследования потенциальной ПМЛ и полностью ее прекратить, если диагноз ПМЛ подтвержден. Также следует рассмотреть возможность прекращения или сокращения любой сопутствующей иммуносупрессивной терапии или химиотерапии. Для оценки и лечения ПМЛ пациент должен быть направлен к врачу-неврологу.
Иммунизация. Безопасность иммунизации живыми или аттенуированными противовирусными вакцинами после окончания терапии препаратом Газива® не изучалась, вакцинация живыми противовирусными вакцинами во время терапии и до момента восстановления пула В-клеток не рекомендуется.
Внутриутробное воздействие препарата Газива® и вакцинация младенцев живыми вирусными вакцинами: в связи с потенциальным истощением пула В-клеток у младенцев, чьи матери получали препарат Газива®во время беременности, вопрос о безопасности и сроках вакцинации живыми вирусными вакцинами следует обсудить с врачом педиатром.
Необходимо рассмотреть возможность отсрочки вакцинации живыми вакцинами до тех пор, пока число В-клеток у ребенка не восстановится до нормы.
Пациенты с нарушением функции почек
ХЛЛ. У пациентов с ХЛЛ и нарушением функции почек средней степени тяжести (Cl креатинина <50 мл/мин), получающих лечение препаратом Газива® в комбинации с хлорамбуцилом, частота развития серьезных нежелательных явлений и нежелательных явлений с летальным исходом может быть выше по сравнению с пациентами с Cl креатинина ≥50 мл/мин.
Различия в эффективности между пациентами с Cl креатинина <50 мл/мин и ≥50 мл/мин отсутствуют.
Применение препарата Газива® у пациентов с Cl креатинина <30 мл/мин не изучалось.
НХЛ. В ходе изучения препарата Газива® в комбинации с химиотерапией у 7,7% пациентов с рефрактерной/рецидивирующей фолликулярной лимфомой и у 5% с ранее нелеченной фолликулярной лимфомой имелось нарушение функции почек средней степени тяжести (Cl креатинина <50 мл/мин). У этих пациентов развивалось большее число серьезных НР, НР, ведущих к отмене терапии (только у пациентов с ранее нелеченной фолликулярной лимфомой), и НР 3–5-й степени тяжести по сравнению с пациентами с Cl креатинина ≥50 мл/мин.
Применение препарата Газива® у пациентов с Cl креатинина <40 мл/мин не изучалось.
Пациенты пожилого и старческого возраста
ХЛЛ. У пациентов с ХЛЛ в возрасте ≥75 лет, получающих терапию препаратом Газива®в комбинации с хлорамбуцилом, частота развития серьезных нежелательных явлений и нежелательных явлений с летальным исходом была выше по сравнению с пациентами моложе 75 лет. Различия в эффективности терапии между пациентами в возрасте ≥75 лет и пациентами моложе 75 лет отсутствуют.
НХЛ. При изучении применения препарата Газива® в комбинации с химиотерапией при иНХЛ у пациентов в возрасте 65 лет и старше развивалось большее число серьезных НР, НР, ведущих к отмене терапии, и НР с летальным исходом по сравнению с пациентами моложе 65 лет. Клинически значимые различия в эффективности не наблюдались.
Инструкции по уничтожению неиспользованного препарата или препарата с истекшим сроком годности. Попадание лекарственного препарата Газива® в окружающую среду должно быть сведено к минимуму. Не следует утилизировать препарат с помощью сточных вод или вместе с бытовыми отходами. Уничтожение неиспользованного препарата или препарата с истекшим сроком годности должно проводиться в соответствии с требованиями лечебного учреждения.
Влияние на способность управлять транспортными средствами и механизмами. Влияние препарата Газива® на способность управлять автомобилем и работать с механизмами не изучалось. При развитии ИР и других НР рекомендуется воздержаться от управления транспортными средствами и механизмами до полного разрешения симптомов.
Форма выпуска
Концентрат для приготовления раствора для инфузий, 1000 мг/40 мл. По 1000 мг/40 мл препарата помещают во флакон бесцветного стекла (гидролитический класс 1 ЕФ), укупоренный пробкой из бутилкаучука, ламинированный фторполимером, обжатый алюминиевым колпачком и закрытый пластмассовой крышкой.
1 флакон с препаратом вместе с инструкцией по применению помещают в картонную пачку.
С целью контроля первого вскрытия на пачку наносится защитная голографическая наклейка.
В случае упаковки на ОАО «Фармстандарт-УфаВИТА»: с целью контроля первого вскрытия на пачку наклеивают самоклеящиеся стикеры с надписью «контроль вскрытия».
Производитель
Рош Диагностикс ГмбХ, Германия/Roche Diagnostics GmbH, Sandhofer Strasse 116, 68305 Mannheim, Germany.
ОАО «Фармстандарт-УфаВИТА», Россия. Россия, Республика Башкортостан, г. Уфа, ул. Худайбердина, 28.
Фасовщик (первичная упаковка). Рош Диагностикс ГмбХ, Германия/Roche Diagnostics GmbH, Sandhofer Strasse 116, 68305 Mannheim, Germany.
ОАО «Фармстандарт-УфаВИТА», Россия. Россия, Республика Башкортостан, г. Уфа, ул. Худайбердина, 28.
Упаковщик (вторичная/потребительская упаковка). Ф. Хоффманн-Ля Рош Лтд., Швейцария/F. Hoffmann-La Roche Ltd, Wurmisweg, 4303 Kaiseraugst, Switzerland.
ОАО «Фармстандарт-УфаВИТА», Россия. Россия, Республика Башкортостан, г. Уфа, ул. Худайбердина, 28.
Выпускающий контроль качества. Ф. Хоффманн-Ля Рош Лтд., Швейцария/F. Hoffmann-La Roche Ltd., Wurmisweg, 4303 Kaiseraugst, Switzerland.
Владелец регистрационного удостоверения. Ф. Хоффманн-Ля Рош Лтд., Швейцария/F. Hoffmann-La Roche Ltd, Grenzacherstrasse 124, 4070 Basel, Switzerland.
ОАО «Фармстандарт-УфаВИТА», Россия. Россия, Республика Башкортостан, г. Уфа, ул. Худайбердина, 28.
Организация, принимающая претензии потребителя. Претензии потребителей направлять в компанию АО «Рош-Москва» по адресу 107031, Россия, Москва, Трубная пл., 2, пом. 1, эт. 1-й, комн. 42.
Тел.: (495) 229-29-99; факс: (495) 229-79-99.
или через форму обратной связи на сайте:
www.roche.ru
В случае производства и упаковки на ОАО «Фармстандарт-УфаВИТА» претензии потребителей направлять по адресу:
450077, Россия, Республика Башкортостан, г. Уфа, ул. Худайбердина, 28.
Тел./факс (347) 272 92 85
www.pharmstd.ru
Условия отпуска из аптек
По рецепту.
Условия хранения
В защищенном от света месте, при температуре 2–8 °C (не замораживать).
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Газива — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер
ЛП-002867-071117
Торговое наименование
Газива®
Международное непатентованное наименование
Обинутузумаб
Лекарственная форма
Концентрат для приготовления раствора для инфузий
Состав
1 флакон содержит:
действующее вещество:
обинутузумаб – 1000 мг;
вспомогательные вещества:
L-гистидин – 57.6 мг, L-гистидина гидрохлорида моногидрат – 89.6 мг, α,α-трегалозы дигидрат – 3632.0 мг, полоксамер 188 – 8.0 мг, вода для инъекций до 40 мл.
1 мл концентрата содержит 25 мг обинутузумаба.
Описание
Прозрачная или опалесцирующая жидкость от бесцветного до слегка коричневатого цвета.
Фармакотерапевтическая группа
Противоопухолевое средство – антитела моноклональные.
Код АТХ [L01XC15]
Фармакологические свойства
Фармакодинамика
Механизм действия
Обинутузумаб представляет собой рекомбинантное, гуманизированное, моноклональное антитело II типа с модифицированной схемой гликозилирования, принадлежащее к классу IgG1 и обладающее специфичностью к антигену CD20. Обинутузумаб избирательно взаимодействует с внеклеточным участком трансмембранного антигена СD20, расположенного на поверхности нормальных и злокачественных зрелых B-лимфоцитов и их предшественников, при этом не связывается со стволовыми гемопоэтическими клетками, про-В-лимфоцитами, плазматическими клетками, а также другими нормальными тканями.
Благодаря модификации схемы гликозилирования Fc фрагмента обинутузумаб обладает повышенным сродством к FcγRIII рецепторам на поверхности эффекторных клеток иммунной системы, в частности натуральных киллеров, макрофагов и моноцитов, по сравнению с антителами, не прошедшими такую модификацию.
Обинутузумаб напрямую индуцирует гибель клеток, опосредует антителозависимую клеточную цитотоксичность (АЗКЦ) и антителозависимый клеточный фагоцитоз (АЗКФ) путем привлечения FcγRIII-положительных эффекторных клеток иммунной системы. Кроме того, обинутузумаб в низкой степени индуцирует комплемент-зависимую цитотоксичность (КЗЦ). По сравнению с анти-CD20 антителами I типа обинутузумаб (антитело II типа) обладает повышенной способностью к прямой индукции гибели клеток на фоне пониженной способности вызывать КЗЦ. Благодаря модификации схемы гликозилирования обинутузумаб более эффективно индуцирует АЗКЦ и АЗКФ по сравнению с анти-CD20 антителами, не прошедшими такую модификацию, что проявляется в более выраженном истощении пула B-клеток и повышенной противоопухолевой активности.
Истощение пула CD19+ B-клеток (до значений <0.07х109/L) наблюдалось у 91% пациентов с хроническим лимфолейкозом (ХЛЛ) после завершения терапии обинутузумабом в комбинации с хлорамбуцилом и сохранялось в течение 6 месяцев. Восстановление числа В-клеток происходило в течение 12-18 месяцев у 35% пациентов при отсутствии прогрессирования и у 13% пациентов с прогрессированием заболевания.
Иммуногенность
Тестирование на наличие антител к лекарственному препарату (ADA) проводилось в различных временных точках у пациентов с ХЛЛ. У 10 из 146 пациентов, получавших препарат Газива®, были обнаружены антитела к препарату через 12 месяцев после завершения последнего цикла терапии. У пациентов не выявлено случаев анафилаксии или реакций гиперчувствительности, связанных с ADA, или негативного влияния на клинический ответ.
У пациентов с индолентной неходжкинской лимфомой образование антител к препарату Газива® во время или после его применения не было зарегистрировано. Результаты анализа иммуногенности в значительной степени зависят от различных факторов, методологии проведения анализа, концентрации препарата Газива®/антител в сыворотке крови, сопутствующих препаратов и характера основного заболевания. Таким образом, сравнение частоты обнаружения антител к препарату Газива® и частоты обнаружения антител к другим биологическим препаратам может оказаться неинформативным.
Фармакокинетика
Всасывание
Обинутузумаб вводится внутривенно. Другие пути введения препарата не изучались.
Рассчитанное значение медианы максимальной концентрации Cmax после инфузии в цикле 6, день 1 у пациентов с хроническим лимфолейкозом составило 465.7 мкг/мл, а значение площади под кривой «концентрация-время» за период дозирования AUC(τ) составило 8961 мкг*д/мл и у пациентов с индолентной неходжкинской лимфомой (иНХЛ) – 539.3 мкг/мл и 10956 мкг*д/мл, соответственно.
Распределение
После внутривенного введения объем распределения в центральной камере (Vc) составляет 2.72 л и приблизительно равен объему сыворотки. Значения Vc и объема распределения обинутузумаба при равновесном состоянии (Vss) свидетельствуют о том, что распределение происходит только в плазме крови и внеклеточной жидкости.
Метаболизм
Отдельных исследований метаболизма обинутузумаба не проводилось. Как и другие антитела, обинутузумаб преимущественно подвергается катаболизму.
Выведение
Клиренс обинутузумаба у пациентов с ХЛЛ составлял примерно 0.11 л/день и у пациентов с иНХЛ примерно 0.08 л/день с медианой периода полувыведения tl/2 26.4 дня при ХЛЛ и 36.8 дня для иНХЛ.
Выведение обинутузумаба характеризуется как линейным клиренсом, так и нелинейным клиренсом. В начальном периоде лечения зависящий от времени нелинейный клиренс является основным, но с продолжением терапии его вклад постепенно уменьшается, и доминирующим становится линейный путь. Это указывает на опосредованное мишенью распределение препарата (ОМРП), при котором избыток CD20+ В-клеток определяет резкое снижение концентрации обинутузумаба в сыворотке крови. Когда большинство CD20+ В-клеток связано с обинутузумабом, ОМРП оказывает минимальное влияние на фармакокинетику препарата.
Фармакокинетика у особых групп пациентов
Пол
По данным популяционного анализа, клиренс в равновесном состоянии (CLss) и объем распределения (V) у мужчин выше на 18% и 19%, соответственно. Тем не менее, отличия в экспозиции обинутузумаба у мужчин и у женщин незначительны (при ХЛЛ медианы AUC и Cmax в 6 цикле составили 11282 мкг*д/мл и 578.9 мкг/мл у женщин и 8451 мкг*д/мл и 432.5 мкг/мл у мужчин, соответственно; при иНХЛ медианы AUC и Cmax составили 13172 мкг*д/мл и 635.7 мкг/мл у женщин и 9769 мкг*д/мл и 481.3 мкг/мл у мужчин, соответственно), коррекции дозы в зависимости от пола не требуется.
Пожилой и старческий возраст
Не отмечено значительных различий в фармакокинетике обинутузумаба у пациентов в возрасте <65 лет, от 65 до 75 лет и у пациентов в возрасте >75 лет.
Нарушение функции почек
Значения фармакокинетических параметров обинутузумаба у пациентов с нарушением функции почек легкой (клиренс креатинина (КК) 50-89 мл/мин) и средней (КК 30-49 мл/мин) степени тяжести схожи с таковыми у пациентов с нормальной функцией почек (КК ≥90 мл/мин). Данные по фармакокинетике у пациентов с нарушением функции почек тяжелой степени (КК 15-29 мл/мин) ограничены, поэтому дать специальные указания по дозированию не представляется возможным.
Нарушения функции печени
Специальных исследований фармакокинетики у пациентов с нарушениями функции печени не проводилось.
Показания к применению
Хронический лимфолейкоз
В комбинации с хлорамбуцилом у пациентов с ранее нелеченным хроническим лимфолейкозом (ХЛЛ) и с сопутствующими заболеваниями, при которых невозможно проведение терапии на основе флударабина в полной дозе.
Фолликулярная лимфома
В комбинации с химиотерапией и последующей поддерживающей монотерапией препаратом Газива® у пациентов с ранее нелеченной фолликулярной лимфомой (ФЛ).
В комбинации с бендамустином и последующей поддерживающей монотерапией препаратом Газива® у пациентов с фолликулярной лимфомой, не ответивших на лечение ритуксимабом или на лечение по содержащей ритуксимаб схеме, или у которых развилось прогрессирование заболевания во время или после такого лечения.
Противопоказания
- Гиперчувствительность к обинутузумабу и к другим компонентам препарата.
- Детский возраст до 18 лет (эффективность и безопасность применения у детей не установлены).
- Беременность и период грудного вскармливания.
- Активный гепатит B и/или другие инфекции в активной фазе.
- Нарушения функции почек тяжелой степени при хроническом лимфолейкозе (КК <30 мл/мин) и при фолликулярной лимфоме (КК <40 мл/мин) (эффективность и безопасность применения не установлены).
- Нарушения функции печени (эффективность и безопасность применения не установлены).
- Вакцинация живыми вирусными вакцинами.
С осторожностью
- Нарушения функции печени.
- Хронические и рецидивирующие инфекции в анамнезе.
- Применение при беременности и в период грудного вскармливания
- Беременность и период грудного вскармливания
- Необходимо рассмотреть отсрочку проведения вакцинации живыми вакцинами у младенцев, чьи матери получали препарат Газива® во время беременности, до тех пор, пока число В-клеток у них не восстановится до нормы.
Обинутузумаб проникает в молоко животных. Грудное вскармливание не рекомендуется во время лечения и, как минимум, в течение 18 месяцев после введения последней дозы препарата Газива®.
Контрацепция
Женщины, обладающие репродуктивным потенциалом, должны использовать эффективные методы контрацепции в период лечения препаратом Газива® и в течение 18 месяцев после окончания терапии.
Способ применения и дозы
Инфузии препарата Газива® следует проводить под тщательным наблюдением медицинского специалиста, имеющего опыт лечения анафилаксии, при наличии доступа к средствам для оказания экстренной помощи.
Препарат Газива® вводят только внутривенно (в/в) капельно, через отдельный катетер! Вводить препарат в/в струйно или болюсно нельзя!
Подготовка препарата к введению должна проводиться в асептических условиях, так как препарат Газива® не содержит антимикробных консервантов.
Разведение препарата Газива® должно проводиться высококвалифицированным медицинским персоналом.
Для введения препарата Газива® следует использовать только 0.9% раствор натрия хлорида. Не следует использовать другие растворители, в частности раствор декстрозы (5%).
Совместимость
Препарат Газива® в виде раствора с концентрацией 0.4 мг/мл — 20 мг/мл совместим с инфузионными пакетами из поливинилхлорида, полиэтилена, полипропилена или полиолефина, с инфузионными системами из поливинилхлорида, полиуретана или полиэтилена, со встраиваемыми фильтрами из полиэфирсульфона, 3-х ходовым запорным краном из поликарбоната, с катетерами из полиэфируретана.
Раствор препарата Газива® нельзя замораживать и встряхивать.
Премедикация и профилактика синдрома лизиса опухоли (СЛО)
Пациентам с высокой опухолевой нагрузкой и/или высоким содержанием лимфоцитов в периферической крови (>25х109/л) и/или нарушением функции почек (КК <70 мл/мин) требуется профилактика СЛО, поскольку они находятся в группе риска развития СЛО.
Профилактика включает адекватную гидратацию и назначение гипоурикемических препаратов (например, аллопуринола или других альтернативных препаратов) перед инфузией препарата Газива® в соответствии со стандартной практикой. В случае если состояние пациента по-прежнему соответствует критериям СЛО, перед каждой последующей инфузией также необходимо проводить профилактику СЛО.
Премедикация и профилактика инфузионных реакций
Информация о проведении премедикации для снижения риска развития инфузионных реакций приведена в Таблице 1. Премедикация глюкокортикостероидами рекомендована для пациентов с фолликулярной лимфомой (ФЛ) и обязательна для пациентов с хроническим лимфолейкозом (ХЛЛ) при первой инфузии. Премедикацию при последующих инфузиях и другие виды премедикации следует проводить как описано ниже.
Учитывая то, что одним из проявлений инфузионных реакций может быть понижение артериального давления, следует рассмотреть возможность приостановки лечения антигипертензивными средствами в течение 12 часов перед каждой инфузией на протяжении инфузии и в течение 1 часа после ее окончания.
Таблица 1. Премедикация перед введением препарата Газива®, необходимая для снижения риска развития инфузионных реакций (ИР).

1100 мг преднизона/преднизолона или 20 мг дексаметазона или 80 мг метилпреднизолона. Не следует применять гидрокортизон, так как он не является эффективным для предотвращения ИР.
2 Профилактическое внутривенное введение глюкокортикостероида не требуется в том случае, если препарат Газива® вводится в один день с комплексной химиотерапией, уже содержащей глюкокортикостероид. В таком случае необходимо принять глюкокортикостероид перорально как минимум за 60 минут до введения препарата Газива®.
3 например, 1000 мг ацетаминофена/парацетамола.
4 например, 50 мг дифенгидрамина.
Стандартный режим дозирования
Хронический лимфолейкоз (в комбинации с хлорамбуцилом)
Цикл 1
Рекомендуемая доза препарата Газива® составляет 1000 мг в/в в течение дня 1 и 2, далее в день 8 и день 15 1-го 28-дневного цикла, как указано в Таблице 2.
Для введения первой дозы препарата Газива® необходимо подготовить два инфузионных пакета, содержащих 100 мг препарата для первой инфузии и 900 мг для второй инфузии.
В том случае, если при введении 100 мг препарата Газива® не потребуется снизить скорость или прервать введение препарата, то 900 мг препарата Газива® можно вводить в тот же день (без приостановки лечения) при условии, что в течение всей инфузии имеются соответствующие условия, необходимое время для проведения инфузии и медицинское наблюдение. Если введение 100 мг препарата пришлось прервать или изменить скорость, вводить 900 мг в тот же день нельзя (см. Таблицу 2).
Циклы 2-6
Рекомендуемая доза препарата Газива® составляет 1000 мг с введением в день 1 каждого 28-дневного цикла лечения, как указано в Таблице 2.
Таблица 2. Введение препарата Газива® при ХЛЛ.
Режим дозирования хлорамбуцила
Применение препарата Газива® в комбинации с хлорамбуцилом изучено для режима дозирования хлорамбуцила 0.5 мг/кг перорально в день 1 и день 15 каждого цикла терапии (циклы 1-6).
Пропуск дозы (ХЛЛ)
При пропуске запланированной дозы препарата Газива® необходимо ввести препарат как можно раньше; не следует ждать следующего запланированного введения. Между введениями следует выдерживать рекомендуемый интервал.
Фолликулярная лимфома
Рекомендуемая доза препарата Газива® составляет 1000 мг внутривенно как указано в Таблице 3.
Ранее нелеченная фолликулярная лимфома
— 6 28-дневных циклов в комбинации с бендамустином или
— 6 21-дневных циклов в комбинации с CHOP (циклофосфамид, доксорубицин, винкристин и преднизолон), затем 2 дополнительных цикла препарата Газива® в монотерапии
или
— 8 21-дневных циклов в комбинации с CVP (циклофосфамид, винкристин, преднизолон).
Пациенты с ранее нелеченной ФЛ, ответившие на терапию препаратом Газива® в комбинации с химиотерапией с достижением полного или частичного ответа, должны продолжать поддерживающую терапию препаратом Газива® в виде монотерапии в дозе 1000 мг один раз в 2 месяца не более 2 лет. При прогрессировании заболевания терапию препаратом Газива® следует прекратить.
Рефрактерная/рецидивирующая фолликулярная лимфома
Пациентам с фолликулярной лимфомой, не ответившим на ритуксимаб-содержащую терапию или имевшим прогрессирование заболевания во время/после такой терапии, следует вводить препарат Газива® в комбинации с бендамустином в течение 6-ти 28-дневных циклов.
Пациенты с рефрактерной/рецидивирующей ФЛ, которые достигли полного или частичного ответа, или пациенты со стабильным заболеванием должны продолжать поддерживающую терапию препаратом Газива® в виде монотерапии в дозе 1000 мг один раз в 2 месяца не более 2 лет. При прогрессировании заболевания терапию препаратом Газива® следует прекратить.
Таблица 3. Введение препарата Газива® при ФЛ.
Режим дозирования бендамустина при рефрактерной/рецидивирующей и ранее нелеченной фолликулярной лимфоме
Применение препарата Газива® в комбинации с бендамустином изучено для режима дозирования бендамустина 90 мг/м2/сут внутривенно в дни 1 и 2 всех циклов терапии (циклы 1-6).
Режим дозирования циклофосфамида, винкристина, доксорубицина и преднизолона при ранее нелеченной фолликулярной лимфоме
Необходимо следовать рекомендациям по дозированию циклофосфамида, винкристина, доксорубицина и преднизолона (стандартные схемы CHOP и CVP), представленным в одобренных инструкциях по медицинскому применению данных препаратов и в специальной литературе.
Пропуск дозы (ФЛ)
При пропуске запланированной дозы препарата Газива® необходимо ввести препарат как можно раньше; не следует ждать следующего запланированного введения или исключать пропущенную дозу.
Если проявления токсичности развиваются перед днем 8 или днем 15 цикла 1 и возникает необходимость отложить введение, необходимо дождаться разрешения симптомов и после этого ввести соответствующую дозу. В таких случаях с учетом возникшей задержки должны быть перенесены все последующие визиты и начало цикла 2.
Во время поддерживающей терапии для введения последующих доз следует придерживаться изначального графика введения препарата.
Коррекция дозы (все показания)
Изменение дозы препарата Газива® не рекомендуется.
Рекомендации по изменению режима дозирования при возникновении симптоматических нежелательных явлений (включая инфузионные реакции) представлены в Таблице 4 и в разделе «Особые указания».
Таблица 4. Рекомендации по коррекции скорости инфузии при развитии инфузионных реакций (также смотри раздел «Особые указания»).
| 4 степень (жизнеугрожающие ИР) | Остановить инфузию и полностью прекратить терапию. |
| 3 степень (тяжелые ИР) | Временно прекратить инфузию и провести симптоматическую терапию.
— После разрешения симптомов возобновить инфузию со скоростью в два раза ниже, чем скорость, при которой развились инфузионные реакции. — В дальнейшем при отсутствии каких-либо симптомов ИР скорость инфузии можно повышать с шагом и интервалом, рекомендованными в таблице 2 и 3. • В первом цикле терапии для пациентов с ХЛЛ, получающих первую дозу препарата Газива®, разделенную на два дня, в день 1 скорость инфузии может быть повышена через час после разрешения симптомов ИР, но не более чем до 25 мг/час. — При повторном развитии ИР 3 степени тяжести инфузию следует остановить и полностью прекратить терапию. |
| 1-2 степень (ИР легкой и средней степени тяжести) | — Снизить скорость инфузии и провести симптоматическую терапию.
— После разрешения симптомов продолжить инфузию. — Если у пациента отсутствуют симптомы ИР, скорость инфузии можно повышать с шагом и интервалом, рекомендованными в таблице 2 и 3. • В первом цикле терапии для пациентов с ХЛЛ, получающих первую дозу препарата Газива®, разделенную на два дня, в день 1 скорость инфузии может быть повышена через час после разрешения симптомов ИР, но не более чем до 25 мг/час. |
Особые указания по дозированию
Пожилой и старческий возраст
Коррекции дозы у пациентов пожилого и старческого возраста не требуется.
Дети
Эффективность и безопасность препарата Газива® у детей и подростков младше 18 лет не установлена.
Нарушение функции почек
Коррекции дозы препарата Газива® у пациентов с нарушением функции почек легкой и средней степени тяжести (клиренс креатинина (КК) ≥30 мл/мин) не требуется.
Эффективность и безопасность препарата Газива® у пациентов с нарушением функции почек тяжелой степени не установлена.
Нарушение функции печени
Эффективность и безопасность препарата Газива® у пациентов с нарушением функции печени не установлены.
Инструкция по приготовлению раствора для инфузий
Для введения первой дозы (1000 мг) препарата Газива® в первом цикле терапии ХЛЛ рекомендуется использовать 2 инфузионных пакета разного размера, что позволит различать дозу 100 мг, предназначенную для введения в цикле 1 в день 1, и дозу 900 мг для введения в цикле 1 в день 1 или день 2 (см. Таблицу 5).
Из флакона отобрать 40 мл концентрата препарата Газива®.
Ввести 4 мл концентрата в инфузионный пакет объемом 100 мл, а оставшиеся 36 мл концентрата – в инфузионный пакет объемом 250 мл, содержащий стерильный апирогенный 0.9% раствор натрия хлорида. Промаркировать каждый инфузионный пакет.
Таблица 5.
| Доза препарата Газива®, предназначенная для введения | Необходимое количество концентрата препарата Газива® | Объем инфузионного пакета |
| 100 мг | 4 мл | 100 мл |
| 900 мг | 36 мл | 250 мл |
| 1000 мг | 40 мл | 250 мл |
Введение препарата Газива® в день 8 и день 15 цикла 1 и в день 1 циклов 2-6 терапии ХЛЛ и во все циклы терапии фолликулярной лимфомы
Из флакона отобрать 40 мл концентрата препарата Газива® и ввести в инфузионный пакет из ПВХ или полиолефина (не-ПВХ), содержащий стерильный апирогенный 0.9% раствор натрия хлорида.
Пакет следует осторожно перевернуть для перемешивания раствора, избегая избыточного образования пены.
Следует визуально проверить приготовленный раствор для инфузии на предмет механических включений и изменения окраски.
С точки зрения микробиологической чистоты приготовленный раствор для инфузии следует использовать немедленно. В исключительных случаях приготовленный раствор может храниться не более 24 часов при температуре 2-8°C, если приготовление раствора для инфузий происходило в контролируемых и валидированных асептических условиях.
При этом за условия хранения (правила хранения и продолжительность) отвечает специалист, готовивший раствор.
Приготовленный раствор препарата Газива® физически и химически стабилен в течение 24 часов при 2-8°C, затем в течение 24 часов при комнатной температуре (≤30°C) и затем в течение не более 24 часов, во время которых должна быть завершена инфузия.
Побочное действие
Хронический лимфолейкоз
Ниже приведены нежелательные реакции, наблюдавшиеся в клинических исследованиях с большей частотой (разница ≥2%) на фоне терапии препаратом Газива® в комбинации с хлорамбуцилом, по сравнению с таковой на фоне терапии только хлорамбуцилом или на фоне комбинированной терапии хлорамбуцилом и ритуксимабом. Нежелательные реакции сгруппированы в соответствии с классами систем органов медицинского словаря для нормативно-правовой деятельности MedDRA. Для описания частоты нежелательных реакций используется следующая классификация: очень частые (≥1/10),частые (≥1/100 и <1/10), нечастые (≥1/1000 и <1/100) редкие (≥1/10000 и <1/1000) и очень редкие (<1/10000), включая единичные случаи. В каждой категории нежелательные реакции указаны в порядке убывания частоты.
Травмы, отравления и осложнения манипуляций: очень часто – инфузионные реакции. Нарушения со стороны системы крови и лимфатической системы: очень часто – нейтропения, тромбоцитопения, анемия; часто – лейкопения.
Нарушения со стороны сосудов:
часто – повышение артериального давления.
Нарушения со стороны сердца:
часто – фибрилляция предсердий.
Инфекционные и паразитарные заболевания: часто – инфекции мочевыводящих путей, герпес слизистой оболочки полости рта, ринит*, назофарингит, фарингит.
Общие расстройства и нарушения в месте введения:
очень часто – повышение температуры тела.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения:
часто – кашель.
Нарушения обмена веществ и питания:
часто – синдром лизиса опухоли, гиперурикемия.
Нарушения со стороны скелетно-мышечной и соединительной ткани:
часто – артралгия, боль в спине, скелетно-мышечные боли в грудной клетке.
Нарушения со стороны лабораторных показателей: часто – снижение числа лейкоцитов, снижение числа нейтрофилов, увеличение массы тела.
Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы): часто – плоскоклеточная карцинома кожи.
Нарушения со стороны желудочно-кишечного тракта: очень часто – диарея*; часто – запор.
Нарушения со стороны кожи и подкожных тканей: часто – алопеция.
* Частота сообщений о данных нежелательных реакциях отличалась менее чем на 2% у пациентов, получающих лечение препаратом Газива® и хлорамбуцилом, по сравнению с пациентами, получающими только хлорамбуцил или хлорамбуцил в комбинации с ритуксимабом.
Не выявлено фатальных нежелательных реакций, частота развития которых была бы выше на ≥2% у пациентов, получающих лечение препаратом Газива® и хлорамбуцилом, по сравнению с пациентами, получающими только хлорамбуцил или хлорамбуцил в комбинации с ритуксимабом.
Неходжкинская лимфома
У пациентов с фолликулярной лимфомой (ФЛ) профиль нежелательных реакций соответствовал таковому в общей популяции пациентов с индолентной неходжкинской лимфомой (иНХЛ).
Ниже приведена информация о нежелательных реакциях, наблюдавшихся в периодах индукции лечения, поддерживающей терапии и последующего наблюдения при изучении препарата Газива® в комбинации с бендамустином, CHOP или CVP и последующей поддерживающей монотерапии препаратом Газива® в следующих популяциях:
• Пациенты с ранее нелеченной иНХЛ, 86% которых имели ФЛ. 92.7% таких пациентов в группе препарата Газива® получили от 6 до 8 циклов терапии препаратом Газива® в комбинации с химиотерапией (в зависимости от вида химиотерапии) на этапе индукции. Пациенты в контрольной группе получали ритуксимаб в комбинации с химиотерапией на этапе индукции и монотерапию ритуксимабом на этапе поддерживающей терапии.
• Пациенты с рефрактерной/рецидивирующей иНХЛ, 81% которых имели ФЛ. 79.4% таких пациентов в группе препарата Газива® получили 6 циклов терапии препаратом Газива® в комбинации с бендамустином на этапе индукции. Пациенты в контрольной группе получали бендамустин на этапе индукции.
Указаны НР, возникавшие с большей частотой (разница ≥2%) по сравнению с соответствующей контрольной группой хотя бы в одной из исследованных популяций.
Для каждой НР указана частота, являющаяся наибольшей из наблюдавшихся в обеих популяциях.
Нежелательные реакции сгруппированы в соответствии с классами систем органов медицинского словаря для нормативно-правовой деятельности MedDRAa.
Для описания частоты нежелательных реакций используется следующая классификация: очень частые (> 1/10),частые (> 1/100 и <1/10), нечастые (> 1/1000 и <1/100) редкие (> 1/10000 и <1/1000) и очень редкие (<1/10000), включая единичные случаи. В каждой категории нежелательные реакции указаны в порядке убывания частоты.
Травмы, отравления и осложнения манипуляций: очень часто — инфузионные реакции/
Нарушения со стороны системы крови и лимфатической системы: очень часто — нейтропения, тромбоцитопения; часто — болезненность лимфатических узлов.
Нарушения со стороны сердца: часто – сердечная недостаточность. Нарушения со стороны органа зрения: часто – гиперемия глаз.
Нарушения со стороны желудочно-кишечного тракта: очень часто – запор, диарея; часто – диспепсия, колит, геморрой.
Общие расстройства и нарушения в месте введения: очень часто – повышение температуры тела, астения; часто – боль в груди.
Инфекционные и паразитарные заболевания: очень часто – инфекции верхних дыхательных путей, назофарингит, синусит*, инфекции мочевыводящих путей, опоясывающий лишай Herpes zoster*; часто – пневмония*, ринит, грипп, фарингит, легочная инфекция.
Нарушения со стороны лабораторных показателей:
часто – гипокалиемия. Нарушения со стороны скелетно-мышечной и соединительной ткани: очень часто – артралгия*; часто – боль в конечностях, боль в костях.
Нарушения психики: очень часто – бессонница; часто – депрессия.
Нарушения со стороны мочевыделительной системы: часто – дизурия, недержание мочи.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения: очень часто – кашель; часто – заложенность носа, ринорея.
Нарушения со стороны кожи и подкожных тканей: очень часто – алопеция; часто – зуд, ночная потливость, экзема.
* — Наблюдались также в периоде поддерживающей терапии с большей частотой по сравнению с контрольной группой (разница ≥2%).
a Закодированные с помощью MedDRA нежелательные реакции, сообщенные исследователями (за исключением инфузионных реакций).
† Определяется как любое связанное с терапией нежелательное явление, возникшее во время или в течение 24 часов после инфузии.
Не выявлено фатальных нежелательных реакций, частота развития которых была бы выше на ≥2% у пациентов, получающих терапию препаратом Газива® в комбинации с химиотерапией, по сравнению с пациентами из соответствующих групп сравнения. У пациентов с рефрактерной/рецидивирующей иНХЛ во время поддерживающей монотерапии препаратом Газива® самыми частыми нежелательными реакциями были кашель (14.7%), инфекции верхних дыхательных путей (11.9%), нейтропения (10.5%), синусит (9.8%), диарея (8.4%), инфузионные реакции (8.4%), тошнота (7.7%), утомляемость (7.7%), бронхит (7.0%), артралгия (7.0%), назофарингит (6.3%), инфекция мочевыводящих путей (6.3%) и повышение температуры тела (5.6%). Самыми частыми нежелательными реакциями 3-5 степени тяжести были нейтропения (9.8%) и анемия, фебрильная нейтропения, тромбоцитопения, сепсис, инфекция верхних дыхательных путей и инфекция мочевыводящих путей (все с частотой 1.4%).
Описание отдельных нежелательных реакций
Инфузионные реакции
Наиболее часто (≥5%) наблюдались следующие симптомы инфузионных реакций (ИР): тошнота, рвота, диарея, головная боль, головокружение, утомляемость, озноб, повышение температуры тела, понижение артериального давления, «приливы», повышение артериального давления, тахикардия, одышка и дискомфорт в области грудной клетки.
Кроме того, сообщалось о симптомах ИР со стороны дыхательной системы, таких как бронхоспазм, раздражение горла и гортани, хрипы, отек гортани и со стороны сердца: фибрилляция предсердий.
Хронический лимфолейкоз
Частота инфузионных реакций составляет 65% при введении первой дозы (1000 мг). У 20% пациентов наблюдались ИР 3-4 степени тяжести. У 7% пациентов ИР послужили причиной прекращения лечения препаратом Газива®. Частота ИР при последующих введениях составила соответственно 3% после второй дозы препарата Газива® (1000 мг) и 1% после введения последующих доз. ИР 3-4 степени тяжести наблюдались только при введении первых 1000 мг препарата Газива®. При последующих введениях ИР 3-5 степени не наблюдалось.
Комплекс мер по предупреждению ИР (см. раздел «Способ применения и дозы») позволяет снизить частоту ИР за исключением ИР 3-4 степени тяжести.
Неходжкинская лимфома
В цикле 1 общая частота возникновения ИР была выше у пациентов, получавших препарат Газива® в комбинации с химиотерапией, по сравнению с пациентами из соответствующих групп сравнения. У пациентов, получавших препарат Газива® в комбинации с химиотерапией, частота возникновения ИР была самой высокой в день 1, постепенно снижалась при последующих инфузиях и продолжала снижаться во время поддерживающей монотерапии препаратом Газива®.
В целом у 3% пациентов развились ИР, послужившие причиной прекращения лечения препаратом Газива®.
Нейтропения и инфекции
Хронический лимфолейкоз
Частота развития нейтропении на фоне терапии препаратом Газива® в комбинации с хлорамбуцилом составляет 40.7%, при этом частота развития инфекций составляет 38%. Нейтропения разрешалась спонтанно или после терапии гранулоцитарным колониестимулирующим фактором. Инфекционные осложнения 3-5 степени тяжести наблюдались у 12% пациентов, а частота случаев с летальным исходом была <1%. Также сообщалось о случаях длительной нейтропении (2%) и нейтропении с поздней манифестацией (16%).
Неходжкинская лимфома
Нейтропения возникала чаще у пациентов, получавших лечение препаратом Газива® в комбинации с химиотерапией, по сравнению с пациентами из контрольных популяций, а риск ее развития был повышен в периоде индукции.
Частоты длительной нейтропении и нейтропении с поздним началом при лечении препаратом Газива® и химиотерапией составляли соответственно 3% и 7%.
Частота возникновения инфекций составляла 78% при лечении препаратом Газива® в комбинации с химиотерапией (явления 3-5 степени тяжести отмечались у 22%, и летальные исходы зарегистрированы у 3% пациентов).
Среди пациентов, получивших профилактическое лечение гранулоцитарнымколониестимулирующим фактором, инфекции 3-5 степени тяжести встречались реже.
Тромбоцитопения и кровотечения
Хронический лимфолейкоз
Общая частота развития тромбоцитопении на фоне терапии препаратом Газива® в комбинации с хлорамбуцилом составила 15.4%, при этом острая тромбоцитопения, развивающаяся в течение 24 часов после инфузии, наблюдалась у 4% пациентов. Частота кровотечений составила 8%. О фатальных случаях кровотечений сообщалось только в первом цикле терапии у 1% пациентов. Причинно-следственная связь между тромбоцитопенией и развитием кровотечений не установлена.
Неходжкинская лимфома
Тромбоцитопения возникала с повышенной частотой в цикле 1 при лечении препаратом Газива® в комбинации с химиотерапией. Тромбоцитопения, развивающаяся в течение инфузии или не позднее 24 ч после инфузии (острая тромбоцитопения), чаще наблюдалась у пациентов, получавших терапию препаратом Газива® в комбинации с химиотерапией, чем у пациентов из групп сравнения.
Частота кровотечений всех степеней тяжести и кровотечений 3-5 степени тяжестисоставила 11% и 5%, соответственно. Частота случаев кровотечений с летальным исходом составила менее 1%, при этом в цикле 1 таких явлений не возникало.
Прогрессирующая мулътиочаговая лейкоэнцефалопатия (ПМЛ)
Прогрессирующая мультиочаговая лейкоэнцефалопатия зарегистрирована у пациентов, получавших препарат Газива®.
Реактивация вируса гепатита B
Сообщалось о случаях реактивации вируса гепатита B на фоне терапии препаратом Газива®.
Прогрессирование сопутствующих заболеваний сердца
На фоне терапии препаратом Газива® наблюдались случаи нарушения функции сердца, в том числе с летальным исходом.
Перфорация органов желудочно-кишечного тракта
Сообщалось о случаях перфорации органов желудочно-кишечного тракта у пациентов, получающих препарат Газива®, преимущественно по поводу неходжкинской лимфомы.
Изменения лабораторных показателей
Транзиторное повышение активности печеночных ферментов (аспартатаминотрансферазы, аланинаминотрансферазы, щелочной фосфатазы) в сыворотке крови наблюдалось вскоре после первой инфузии препарата Газива®.
Передозировка
Опыт превышения рекомендованной дозы препарата Газива® отсутствует. Изучено применение доз от 50 мг до 2000 мг за одну инфузию. Степень тяжести и частота нежелательных реакций не зависели от дозы.
При случайном превышении дозы препарата Газива® необходимо немедленно прекратить инфузию или снизить дозу. В связи с увеличением риска инфекционных осложнений при истощении пула В-лимфоцитов следует тщательно наблюдать за пациентом и рассмотреть необходимость проведения развернутого общего анализа крови.
Взаимодействие с другими лекарственными средствами
Специальных исследований взаимодействия с другими лекарственными средствами не проводилось.
Однако были проведены ограниченные подисследования межлекарственного взаимодействия препарата Газива® с бендамустином, препаратами схемы CHOP (циклофосфамид, доксорубицин, винкристин, преднизолон), препаратами схемы FC (флударабин, циклофосфамид) и хлорамбуцилом. Совместное введение препарата Газива® не оказывало влияния на фармакокинетику бендамустина, FC или отдельных компонентов схемы CHOP; кроме того отсутствовало заметное влияние бендамустина, FC, хлорамбуцила или CHOP на фармакокинетику препарата Газива®. Риск взаимодействия с одновременно применяемыми препаратами нельзя полностью исключить.
Особые указания
В медицинской документации пациента следует указывать торговое название препарата (Газива®) и номер серии. Замена препарата на какой-либо другой биологический лекарственный препарат требует согласования с лечащим врачом. Информация, представленная в данной инструкции, относится только к препарату Газива®. Инфузионные реакции
Наиболее часто наблюдаемыми нежелательными реакциями у пациентов, получающих препарат Газива®, были инфузионные реакции (ИР), развившиеся преимущественно во время введения первых 1000 мг препарата. Комплекс мер по предупреждению ИР (применение подходящего глюкокортикостероида, перорального
анальгетика/антигистаминного препарата, пропуск приема антигипертензивного препарата) у пациентов с ХЛЛ позволяет снизить частоту ИР за исключением ИР 3-4 степени.
Рекомендуется принимать меры по предупреждению ИР, описанные в разделе «Способ применения и дозы».
Частота и тяжесть инфузионных реакций существенно уменьшались после введения первых 1000 мг препарата Газива®, и при последующих инфузиях ИР у большинства пациентов не развивались.
В основном, не зависимо от показаний, наблюдались ИР легкой и средней степени тяжести, которые разрешались после замедления или временного прекращения первой инфузии, тем не менее, известно также о тяжелых и жизнеугрожающих ИР, требующих симптоматической терапии. ИР могут клинически не отличаться от IgE-опосредованных аллергических реакций (например, анафилаксии). У пациентов с высокой опухолевой нагрузкой и/или с высоким содержанием циркулирующих лимфоцитов при ХЛЛ (>25×109/л) риск развития тяжелых ИР повышен. Меры по профилактике ИР описаны в разделе «Способ применения и дозы». Меры по купированию инфузионных реакций с учетом их степени тяжести описаны в разделе «Способ применения и дозы», Таблица 4.
Терапию препаратом Газива® следует полностью прекратить в случае развития:
- жизнеугрожающих острых респираторных симптомов;
- ИР 4 степени (угрожающих жизни);
- повторной (продолжающейся/рецидивирующей) ИР 3 степени.
Пациенты с сопутствующими заболеваниями сердца или легких должны находиться под тщательным наблюдением во время инфузии и после нее. Во время инфузии препарата Газива® возможно понижение артериального давления. В связи с этим следует рассмотреть возможность приостановки лечения антигипертензивными препаратами в течение 12 часов перед каждой инфузией, на протяжении каждой инфузии и в продолжение 1 часа после введения препарата. Необходимо оценить пользу и возможный риск остановки приема антигипертензивных препаратов у пациентов с высоким риском развития гипертонического криза.
Реакции гиперчувствительности
На фоне терапии препаратом Газива® отмечались случаи реакций гиперчувствительности с немедленным (анафилаксия) и замедленным (сывороточная болезнь) развитием. Если во время или после инфузии подозревается развитие реакции гиперчувствительности (развитие симптомов происходит, как правило, при последующих введениях, очень редко симптомы развиваются во время первой инфузии), введение должно быть прекращено и терапию препаратом Газива® следует отменить и не возобновлять в дальнейшем. Пациентам с установленной гиперчувствительностью к препарату Газива® противопоказана терапия данным препаратом. Возможны затруднения при дифференциальной диагностике реакции гиперчувствительности и инфузионной реакции.
Синдром лизиса опухоли (СЛО)
Наблюдались случаи синдрома лизиса опухоли (СЛО). Пациентам из группы риска развития СЛО (больные с высокой опухолевой нагрузкой и/или высоким содержанием лимфоцитов в периферической крови и/или нарушением функции почек (КК <70 мл/мин)) необходимо провести профилактику СЛО. Профилактика должна включать адекватную гидратацию и назначение гипоурикемических препаратов (например, аллопуринола или других альтернативных препаратов) до начала инфузии, как указано в разделе «Способ применения и дозы». Пациенты из группы риска развития СЛО должны находиться под тщательным наблюдением в первые дни терапии, при этом особое внимание следует уделять контролю функции почек, концентрации калия и мочевой кислоты. Дополнительные мероприятия должны проводиться в соответствии со стандартной практикой. При развитии СЛО необходимо тщательное наблюдение за функцией почек и водно-электролитным балансом с последующей коррекцией электролитных нарушений, а также проведением поддерживающих лечебных мероприятий, включая, если требуется, диализ.
Нейтропения
Наблюдались случаи серьезной и жизнеугрожающей нейтропении, включая фебрильную нейтропению. При развитии нейтропении пациенты нуждаются в тщательном наблюдении и проведении регулярного лабораторного обследования до полного разрешения симптомов. При необходимости следует провести терапию в соответствии с локально принятой практикой и рассмотреть необходимость применения гранулоцитарного колониестимулирующего фактора. При любом проявлении сопутствующей инфекции необходимо назначить соответствующее лечение. Возможно развитие нейтропении с поздней манифестацией (возникновение не раньше чем через 28 дней после окончания лечения) и длительной нейтропении продолжительностью более 28 дней после окончания или отмены терапии.
Тромбоцитопения
Наблюдались случаи серьезной и жизнеугрожающей тромбоцитопении, в том числе случаи острой тромбоцитопении, которые развивались в течение 24 часов после инфузии. В 1-м цикле терапии наблюдались случаи кровотечений с летальным исходом. Взаимосвязь между равзитием кровотечений и тромбоцитопенией не установлена. В ходе лечения пациенты нуждаются в тщательном наблюдении на предмет развития тромбоцитопении, особенно в 1-м цикле. При выявлении тромбоцитопении необходимо регулярное проведение лабораторного обследования до тех пор, пока реакция не разрешится. В серьезных или жизнеугрожающих случаях следует рассмотреть возможность отложить введение препарата Газива®. Решение о проведении гемотрансфузии (трансфузии тромбоцитов) принимает лечащий врач в соответствии с практикой, установленной в лечебном учреждении. Необходимо принимать во внимание прием любых сопутствующих препаратов, способных усугубить тромбоцитопению, таких как ингибиторы агрегации тромбоцитов и антикоагулянты, особенно в 1-м цикле терапии.
Прогрессирование сопутствующих заболеваний сердца
При наличии у пациентов сопутствующих заболеваний сердца возможно развивитие аритмий (в частности, фибрилляции предсердий и тахиаритмии), стенокардии, острого коронарного синдрома, инфакрта миокарда и сердечной недостаточности. Данные явления могут развиться во время инфузионных реакций и иметь летальный исход. Пациенты с заболеваниями сердца в анамнезе нуждаются в тщательном наблюдении. Кроме того, у таких пациентов следует соблюдать осторожность при проведении гидратации, избегая образования избытка жидкости в организме.
Инфекции
Препарат Газива® не следует применять при наличии у пациента инфекции в активной стадии. Следует соблюдать осторожность при принятии решения о назначении препарата Газива® пациентам с периодически рецидивирующими и хроническими инфекциями в анамнезе. Возможно развитие серьезных бактериальных и грибковых инфекций, а также развитие или реактивация вирусных инфекций во время терапии и после ее окончания. Сообщалось о летальных случаях инфекционных заболеваний.
У пациентов с фолликулярной лимфомой зарегистрирована высокая частота развития инфекций на всех этапах клинических исследований, включая периоды последующего наблюдения. При этом наиболее высокая частота инфекций была характерна для периода поддерживающей терапии.
В периоде последующего наблюдения инфекции 3-5 степеней тяжести чаще наблюдались у пациентов, которые на этапе индукции получали препарат Газива® в комбинации с бендамустином.
Реактивация вируса гепатита В
На фоне применения анти CD-20 препаратов возможна реактивация вируса гепатита В, в некоторых случаях сопровождающаяся фульминантным гепатитом, печеночной недостаточностью, возможен летальный исход.
Перед назначением препарата Газива® всем пациентам следует пройти скрининг на вирус гепатита В, включая определение HBsAg – статуса, HBcAb – статуса, а также дополнительных маркеров согласно установленной местной практике. Препарат Газива® не следует применять пациентам с активным гепатитом B. Пациентам с положительными серологическими маркерами гепатита B следует проконсультироваться с врачом-гепатологом перед назначением препарата Газива®. В отношении таких пациентов необходимо проводить соответствующий мониторинг и принимать меры по профилактике реактивации вируса гепатита B в соответствии с местными стандартами.
Прогрессирующая многоочаговая лейкоэнцефалопатия (ПМЛ)
При развитии новых неврологических симптомов или изменении уже имеющихся необходимо провести диагностику для исключения ПМЛ. Симптомы ПМЛ не являются специфическими и могут варьировать в зависимости от локализации повреждения. Часто наблюдаются моторные симптомы, ассоциированные с пирамидными нарушениями (в частности, мышечная слабость, паралич, нарушения чувствительности), мозжечковые нарушения и дефекты поля зрения, аномалии чуствительности. Возможны нарушения высших корковых функций, таких как афазия или визуально-пространственная дезориентация. Диагностика ПМЛ может включать консультацию врача-невролога, проведение магнитно-резонансной томографии головного мозга (МРТ) и люмбарную пункцию для анализа спинно-мозговой жидкости на содержание ДНК JC-вируса. Терапию препаратом Газива® необходимо остановить на время проведения обследования и полностью ее прекратить, если диагноз ПМЛ подвтержден. Также следует рассмотреть возможность приостановки или снижения интенсивности сопутствующей иммуносупрессивной терапии или химиотерапии. Для лечения ПМЛ пациент должен быть направлен к врачу-неврологу.
Иммунизация
Безопасность иммунизации живыми или аттенуированными противовирусными вакцинами после окончания терапии препаратом Газива® не изучалась, вакцинация живыми противовирусными вакцинами во время терапии и до момента восстановления пула В-клеток не рекомендуется.
Внутриутробное воздействие препарата Газива® и вакцинация младенцев живыми вирусными вакцинами: в связи с потенциальным истощением пула В-клеток у младенцев, чьи матери получали препарат Газива® во время беременности, вопрос о безопасности и сроках вакцинации живыми вирусными вакцинами следует обсудить с врачом педиатром.
Необходимо рассмотреть возможность отсрочки вакцинации живыми вакцинами до тех пор, пока число В-клеток у ребенка не восстановится до нормы.
Пациенты с нарушением функции почек
Хронический лимфолейкоз
У пациентов с ХЛЛ и нарушением функции почек средней степени тяжести (КК <50 мл/мин), получающих лечение препаратом Газива® в комбинации с хлорамбуцилом, частота развития серьезных нежелательных явлений и нежелательных явлений с летальным исходом может быть выше по сравнению с пациентами с КК ≥50 мл/мин.
Различия в эффективности между пациентами с КК <50 мл/мин и пациентами с КК ≥50 мл/мин отсутствуют.
Применение препарата Газива® у пациентов с КК <30 мл/мин не изучалось.
Неходжкинская лимфома
В ходе изучения препарата Газива® в комбинации с химиотерапией у 7.7% пациентов с рефрактерной/рецидивирующей фолликулярной лимфомой и у 5% с ранее нелеченной фолликулярной лимфомой имелось нарушение функции почек средней степени тяжести (КК <50 мл/мин). У этих пациентов развивалось большее число серьезных нежелательных явлений (НЯ), НЯ, ведущих к отмене терапии, и НЯ с летальным исходом по сравнению с пациентами с КК ≥50 мл/мин.
Применение препарата Газива® у пациентов с КК <40 мл/мин не изучалось.
Пациенты пожилого и старческого возраста
Хронический лимфолейкоз
У пациентов с ХЛЛ в возрасте ≥75 лет, получающих терапию препаратом Газива® в комбинации с хлорамбуцилом, частота развития серьезных нежелательных явлений и нежелательных явлений с летальным исходом была выше по сравнению с пациентами моложе 75 лет. Различия в эффективности терапии между пациентами в возрасте ≥75 лет и пациентами моложе 75 лет отсутствуют.
Неходжкинская лимфома
При изучении применения препарата Газива® в комбинации с химиотерапией при индолентной неходжкинской лимфоме у пациентов в возрасте 65 лет и старше развивалось большее число серьезных нежелательных явлений (НЯ), НЯ, ведущих к отмене терапии, и НЯ с летальным исходом по сравнению с пациентами моложе 65 лет.
Клинически значимые различия в эффективности не наблюдались.
Инструкции по уничтожению неиспользованного препарата или препарата с истекшим сроком годности
Попадание лекарственного препарата Газива® в окружающую среду должно быть сведено к минимуму. Не следует утилизировать препарат с помощью сточных вод или вместе с бытовыми отходами. Уничтожение неиспользованного препарата или препарата с истекшим сроком годности должно проводиться в соответствии с требованиями лечебного учреждения.
Влияние на способность управлять транспортными средствами и механизмами
Влияние препарата Газива® на способность управлять автомобилем и работать с механизмами не изучалось. При развитии инфузионных реакций и других нежелательных реакций рекомендуется воздержаться от управления транспортными средствами и механизмами до полного разрешения симптомов.
Форма выпуска и упаковка
Концентрат для приготовления раствора для инфузий 1000 мг/40 мл
По 1000 мг/40 мл препарата во флакон бесцветного стекла (гидролитический класс 1 ЕФ), укупоренный пробкой из бутилкаучука, ламинированного фторполимером, обжатый алюминиевым колпачком и закрытый пластмассовой крышкой.
1 флакон с препаратом вместе с инструкцией по применению помещают в картонную пачку.
Срок годности
3 года.
Не использовать по истечении срока годности, указанного на упаковке.
Условия хранения
Хранить при температуре 2-8°С в защищенном от света месте. Не замораживать.
Хранить в недоступном для детей месте.
Условия отпуска
Отпускают по рецепту.
Владелец Регистрационного удостоверения
Ф. Хоффманн-Ля Рош Лтд., Швейцария
F. Hoffmann-La Roche Ltd, Grenzacherstrasse 124, 4070 Basel, Switzerland
Производитель
Рош Диагностикс ГмбХ, Германия
Roche Diagnostics GmbH, Sandhofer Strasse 116, 68305 Mannheim, Germany
Претензии потребителей направлять в компанию ЗАО «Рош-Москва» по адресу:
107031, Россия, г. Москва, Трубная площадь, д. 2
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Газива® (Gazyva®) инструкция по применению
📜 Инструкция по применению Газива®
💊 Состав препарата Газива®
✅ Применение препарата Газива®
📅 Условия хранения Газива®
⏳ Срок годности Газива®
Описание лекарственного препарата
Газива®
(Gazyva®)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для печатного издания справочника Видаль 2023 года.
Дата обновления: 2022.11.01
Код ATX:
L01FA03
(Обинутузумаб)
Лекарственная форма
| Газива® |
Концентрат д/пригот. р-ра д/инф. 1000 мг/40 мл: фл. 1 шт. рег. №: ЛП-(001150)-(РГ-RU) Предыдущий рег. №: ЛП-002867 |
Форма выпуска, упаковка и состав
препарата Газива®
Концентрат для приготовления раствора для инфузий в виде прозрачной или опалесцирующей жидкости от бесцветного до слегка коричневатого цвета.
Вспомогательные вещества: L-гистидин, L-гистидина гидрохлорида моногидрат, α,α-трегалозы дигидрат, полоксамер 188, вода д/и.
40 мл — флаконы бесцветного стекла (1) — пачки картонные×.
× С целью контроля первого вскрытия на пачку наносится защитная голографическая наклейка.
C целью контроля первого вскрытия на пачку наклеивают самоклеящиеся круглые стикеры с надписью «контроль вскрытия» (в случае упаковки на ОАО «Фармстандарт-УфаВИТА»).
Фармакологическое действие
Механизм действия
Обинутузумаб представляет собой рекомбинантное, гуманизированное, моноклональное антитело II типа с модифицированной схемой гликозилирования, принадлежащее к классу IgG1 и обладающее специфичностью к антигену CD20. Обинутузумаб избирательно взаимодействует с внеклеточным участком трансмембранного антигена CD20, расположенного на поверхности нормальных и злокачественных зрелых В-лимфоцитов и их предшественников, при этом не связывается со стволовыми гемопоэтическими клетками, про-В-лимфоцитами, плазматическими клетками, а также другими нормальными тканями.
Благодаря модификации схемы гликозилирования Fc-фрагмента обинутузумаб обладает повышенным сродством к рецепторам FcγRIII на поверхности эффекторных клеток иммунной системы, в частности натуральных киллеров, макрофагов и моноцитов, по сравнению с антителами, не прошедшими такую модификацию.
Обинутузумаб напрямую индуцирует гибель клеток, опосредует антитело-зависимую клеточную цитотоксичность (АЗКЦ) и антителозависимый клеточный фагоцитоз (АЗКФ) путем привлечения FcγRIII-положительных эффекторных клеток иммунной системы. Кроме того, обинутузумаб в низкой степени индуцирует комплемент-зависимую цитотоксичность (КЗЦ). Применение обинутузумаба приводит к значительному угнетению B-клеток и противоопухолевой эффективности. По сравнению с анти-CD20 антителами I типа обинутузумаб (антитело II типа) обладает повышенной способностью к прямой индукции гибели клеток на фоне пониженной способности вызывать КЗЦ. Благодаря модификации схемы гликозилирования обинутузумаб более эффективно индуцирует АЗКЦ и АЗКФ по сравнению с анти-CD20 антителами, не прошедшими такую модификацию, что проявляется в более выраженном истощении пула В-клеток и повышенной противоопухолевой активности.
Истощение пула CD19+ В-клеток (до значений <0.07×109/л) наблюдалось у 91% пациентов с хроническим лимфолейкозом (ХЛЛ) после завершения терапии обинутузумабом в комбинации с хлорамбуцилом и сохранялось в течение 6 месяцев.
Восстановление числа В-клеток происходило в течение 12-18 месяцев у 35% пациентов при отсутствии прогрессирования и у 13% пациентов с прогрессированием заболевания.
В опорном клиническом исследовании у пациентов с индолентной неходжкинской лимфомой у 97% оцениваемых пациентов, получающих препарат Газива®, отмечалось истощение пула B-клеток в конце терапии, а у 97% пациентов истощение сохранялось более 6 месяцев после введения последней дозы. Восстановление числа B-клеток наблюдалось в течение 12-18 месяцев у 11% оцениваемых пациентов.
Иммуногенность
Тестирование на наличие антител к лекарственному препарату (антитерапевтических антител, АТА) проводилось в различных временных точках у пациентов с ХЛЛ. У 10 из 146 пациентов, получавших препарат Газива®, были обнаружены антитела к препарату через 12 месяцев после завершения последнего цикла терапии. У пациентов не выявлено случаев анафилаксии или реакций гиперчувствительности, связанных с АТА, или негативного влияния на клинический ответ.
У пациентов с индолентной неходжкинской лимфомой не отмечалось образования HAHA (антител человека к антителам человеческого происхождения — Human Anti-Human Antibody) по сравнению с исходным уровнем. У 0.2% пациентов с ранее нелеченной фолликулярной лимфомой развивались HAHA на момент завершения индукции.
Несмотря на то, что клиническая значимость HAHA неизвестна, потенциальная взаимосвязь между развитием НАНА и клиническим течением заболевания не может быть исключена
Результаты анализа иммуногенности в значительной степени зависят от различных факторов, таких как чувствительность и специфичность анализа, методология проведения анализа, чувствительность анализа к концентрации препарата Газива®/антител в сыворотке крови, манипуляции с забранными образцами, время забора образцов, сопутствующие препараты и характер основного заболевания. Таким образом, сравнение частоты обнаружения антител к препарату Газива® и частоты обнаружения антител к другим биологическим препаратам может оказаться неинформативным.
Фармакокинетика
Всасывание
Обинутузумаб вводят в/в. Другие пути введения препарата не изучались. Рассчитанное значение медианы Cmax после инфузии в цикле 6, день 1 у пациентов с хроническим лимфолейкозом составило 465.7 мкг/мл, а значение AUC за период применения AUC(t) составило 8961 мкг×д/мл и у пациентов с индолентной неходжкинской лимфомой (иНХЛ) — 539.3 мкг/мл и 10956 мкг×д/мл соответственно.
Распределение
После в/в введения объем распределения в центральной камере (Vc) составляет 2.72 л и приблизительно равен объему сыворотки. Значения Vc и Vd обинутузумаба при равновесном состоянии (Vss) свидетельствуют о том, что распределение происходит только в плазме крови и внеклеточной жидкости.
Метаболизм
Отдельных исследований метаболизма обинутузумаба не проводилось. Как и другие антитела, обинутузумаб преимущественно подвергается катаболизму.
Выведение
Клиренс обинутузумаба у пациентов с ХЛЛ составлял примерно 0.11 л/сут и у пациентов с иНХЛ примерно 0.08 л/сут с медианой Т1/2 26.4 сут при ХЛЛ и 36.8 сут для иНХЛ.
Выведение обинутузумаба характеризуется как линейным клиренсом, так и нелинейным клиренсом. В начальном периоде лечения зависящий от времени нелинейный клиренс является основным, но с продолжением терапии его вклад постепенно уменьшается, и доминирующим становится линейный путь. Это указывает на опосредованное мишенью распределение препарата (ОМРП), при котором избыток CD20+ В-клеток определяет резкое снижение концентрации обинутузумаба в сыворотке крови. Когда большинство CD20+ В-клеток связано с обинутузумабом, ОМРП оказывает минимальное влияние на фармакокинетику препарата.
Фармакокинетика у особых групп пациентов
Пол. По данным популяционного анализа клиренс в равновесном состоянии и Vd у мужчин выше на 18% и 19% соответственно. Тем не менее, отличия в экспозиции обинутузумаба у мужчин и у женщин незначительны (при ХЛЛ медианы AUC и Сmax в 6 цикле составили 11282 мкг×д/мл и 578.9 мкг/мл у женщин и 8451 мкг×д/мл и 432.5 мкг/мл у мужчин соответственно; при иНХЛ медианы AUC и Сmax составили 13172 мкг×д/мл и 635.7 мкг/мл у женщин и 9769 мкг×д/мл и 481.3 мкг/мл у мужчин соответственно), коррекция дозы в зависимости от пола не требуется.
Пожилой и старческий возраст. Не отмечено значительных различий в фармакокинетике обинутузумаба у пациентов в возрасте <65 лет, от 65 до 75 лет и у пациентов в возрасте >75 лет.
Нарушение функции почек. Значения фармакокинетических параметров обинутузумаба у пациентов с нарушением функции почек легкой (КК 50-89 мл/мин) и средней (КК 30-49 мл/мин) степени тяжести схожи с таковыми у пациентов с нормальной функцией почек (КК ≥90 мл/мин). Данные по фармакокинетике у пациентов с нарушением функции почек тяжелой степени (КК 15-29 мл/мин) ограничены, поэтому дать специальные указания по дозированию не представляется возможным.
Нарушения функции печени. Специальных исследований фармакокинетики у пациентов с нарушениями функции печени не проводилось.
Показания препарата
Газива®
Хронический лимфолейкоз
- в комбинации с хлорамбуцилом у взрослых старше 18 лет с ранее нелеченным хроническим лимфолейкозом (ХЛЛ) и с сопутствующими заболеваниями, при которых невозможно проведение терапии на основе флударабина в полной дозе.
Фолликулярная лимфома
- в комбинации с химиотерапией с последующей поддерживающей монотерапией препаратом Газива® (при достижении как минимум частичной ремиссии) у взрослых в возрасте старше 18 лет с ранее нелеченной распространенной фолликулярной лимфомой (ФЛ) (стадия II с любыми нодальными и экстранодальными вовлечениями ≥7 см в диаметре, стадия III или IV);
- в комбинации с бендамустином и последующей поддерживающей монотерапией препаратом Газива® у взрослых в возрасте старше 18 лет с ФЛ, не ответивших на лечение ритуксимабом или на лечение по содержащей ритуксимаб схеме, или у которых развилось прогрессирование заболевания во время или в течение 6 месяцев после такого лечения.
Режим дозирования
Препарат Газива® вводится квалифицированным медицинским персоналом.
Препарат предназначен для введения как в амбулаторно-поликлинических, так и в стационарных условиях.
Препарат Газива® вводят только в/в капельно, через отдельный катетер. Вводить препарат в/в струйно или болюсно нельзя!
Подготовку препарата к введению следует проводить в асептических условиях, т.к. препарат Газива® не содержит противомикробных консервантов.
Следует использовать стерильную иглу и шприц для приготовления раствора для инфузий препарата Газива®.
Для введения препарата Газива® следует использовать только 0.9% раствор натрия хлорида. Не следует использовать другие растворители, в частности раствор декстрозы (5%).
Совместимость
Препарат Газива® в виде раствора с концентрацией 0.4 мг/мл — 20 мг/мл совместим с инфузионными пакетами из поливинилхлорида, полиэтилена, полипропилена или полиолефина, с инфузионными системами из поливинилхлорида, полиуретана или полиэтилена, со встраиваемыми фильтрами из полиэфирсульфона, 3-ходовым запорным краном из поликарбоната, с катетерами из полиэфируретана.
Раствор препарата Газива® нельзя замораживать и встряхивать.
Премедикация и профилактика синдрома лизиса опухоли (СЛО)
Пациентам с высокой опухолевой нагрузкой и/или с высоким содержанием лимфоцитов (>25×109/л) и/или нарушением функции почек (КК <70 мл/мин) требуется профилактика СЛО, поскольку они находятся в группе риска развития СЛО. Профилактика включает адекватную гидратацию и назначение гипоурикемических препаратов (например, аллопуринола или других альтернативных препаратов) перед инфузией препарата Газива® в соответствии со стандартной практикой. В случае если состояние пациента по-прежнему соответствует критериям СЛО, перед каждой последующей инфузией также необходимо проводить профилактику СЛО.
Премедикация и профилактика инфузионных реакций
Информация о проведении премедикации для снижения риска развития инфузионных реакций приведена в Таблице 1. Премедикация ГКС рекомендована для пациентов с фолликулярной лимфомой (ФЛ) и обязательна для пациентов с хроническим лимфолейкозом (ХЛЛ) при первой инфузии. Премедикацию при последующих инфузиях и другие виды премедикации следует проводить как описано ниже.
Учитывая то, что одним из проявлений инфузионных реакций может быть понижение АД, следует рассмотреть возможность приостановки лечения антигипертензивными средствами в течение 12 ч перед каждой инфузией на протяжении инфузии и в течение 1 ч после ее окончания.
Таблица 1. Премедикация перед введением препарата Газива®, необходимая для снижения риска развития инфузионных реакций (ИР)
1 100 мг преднизона/преднизолона или 20 мг дексаметазона или 80 мг метилпреднизолона. Не следует применять гидрокортизон, т.к. он не является эффективным для предотвращения ИР.
2 Профилактическое в/в введение ГКС не требуется в том случае, если препарат Газива® вводится в один день с комплексной химиотерапией, уже содержащей ГКС. В таком случае необходимо принять ГКС перорально как минимум за 60 мин до введения препарата Газива®.
3 например, 1000 мг ацетаминофена/парацетамола.
4 например, 50 мг дифенгидрамина.
Стандартный режим дозирования
Хронический лимфолейкоз (в комбинации с хлорамбуцилом)
Цикл 1
Рекомендуемая доза препарата Газива® составляет 1000 мг в/в в течение дня 1 и 2, далее в день 8 и день 15 1-го 28-дневного цикла, как указано в Таблице 2.
Для введения первой дозы препарата Газива® необходимо подготовить два инфузионных пакета, содержащих 100 мг препарата для первой инфузии и 900 мг для второй инфузии.
В том случае, если при введении 100 мг препарата Газива® не потребуется снизить скорость или прервать введение препарата, то 900 мг препарата Газива® можно вводить в тот же день (без приостановки лечения) при условии, что в течение всей инфузии имеются соответствующие условия, необходимое время для проведения инфузии и медицинское наблюдение. Если введение 100 мг препарата пришлось прервать или изменить скорость, вводить 900 мг в тот же день нельзя (см. Таблицу 2).
Циклы 2-6
Рекомендуемая доза препарата Газива® составляет 1000 мг с введением в день 1 каждого 28-дневного цикла лечения, как указано в Таблице 2.
Таблица 2. Введение препарата Газива® при ХЛЛ
Режим дозирования хлорамбуцила
Применение препарата Газива® в комбинации с хлорамбуцилом изучено для режима дозирования хлорамбуцила перорально в дозе 0.5 мг/кг в день 1 и день 15 каждого цикла терапии (циклы 1-6).
Пропуск дозы (ХЛЛ)
При пропуске запланированной дозы препарата Газива® необходимо ввести препарат как можно раньше; не следует ждать следующего запланированного введения. Между введениями следует выдерживать рекомендуемый интервал.
Фолликулярная лимфома
Рекомендуемая доза препарата Газива® составляет 1000 мг в/в как указано в Таблице 3.
Ранее нелеченная фолликулярная лимфома
- 6 28-дневных циклов в комбинации с бендамустином
или
- 6 21-дневных циклов в комбинации с CHOP (циклофосфамид, доксорубицин, винкристин и преднизолон), затем 2 дополнительных цикла препарата Газива® в монотерапии
или
- 8 21-дневных циклов в комбинации с CVP (циклофосфамид, винкристин, преднизолон). Пациенты с ранее нелеченной ФЛ, ответившие на терапию препаратом Газива® в комбинации с химиотерапией с достижением полного или частичного ответа, должны продолжать поддерживающую терапию препаратом Газива® в виде монотерапии в дозе 1000 мг 1 раз в 2 месяца не более 2 лет. При прогрессировании заболевания терапию препаратом Газива® следует прекратить.
Рефрактерная/рецидивирующая фолликулярная лимфома
Пациентам с фолликулярной лимфомой, не ответившим на ритуксимаб-содержащую терапию или имевшим прогрессирование заболевания во время/после такой терапии, следует вводить препарат Газива® в комбинации с бендамустином в течение 6 28- дневных циклов.
Пациенты с рефрактерной/рецидивирующей ФЛ, которые достигли полного или частичного ответа, или пациенты со стабильным заболеванием должны продолжать поддерживающую терапию препаратом Газива® в виде монотерапии в дозе 1000 мг один раз в 2 месяца не более 2 лет. При прогрессировании заболевания терапию препаратом Газива® следует прекратить.
Препарат Газива® следует вводить со стандартной скоростью инфузии в цикле 1 (см. Таблицу 3). Пациентам, у которых не возникает инфузионных реакций ≥3 степени тяжести во время цикла 1, препарат Газива® может вводиться в виде короткой (приблизительно 90 мин) инфузии, начиная с цикла 2 и далее (см. Таблицу 4).
Таблица 3. Введение препарата Газива® при ФЛ
Таблица 4. Введение препарата Газива® короткими инфузиями при ФЛ
Режим дозирования бендамустина при рефрактерной/рецидивирующей и ранее нелеченной фолликулярной лимфоме
Применение препарата Газива® в комбинации с бендамустином изучено для режима дозирования бендамустина 90 мг/м2/сут в/в в дни 1 и 2 всех циклов терапии (циклы 1-6).
Режим дозирования циклофосфамида, винкристина, доксорубицина и преднизолона при ранее нелеченной фолликулярной лимфоме
Необходимо следовать рекомендациям по дозированию циклофосфамида, винкристина, доксорубицина и преднизолона (стандартные схемы CHOP и CVP), представленным в одобренных инструкциях по медицинскому применению данных препаратов и в специальной литературе.
Пропуск дозы (ФЛ)
При пропуске запланированной дозы препарата Газива® необходимо ввести препарат как можно раньше; не следует ждать следующего запланированного введения или исключать пропущенную дозу.
Если проявления токсичности развиваются перед днем 8 или днем 15 цикла 1 и возникает необходимость отложить введение, необходимо дождаться разрешения симптомов и после этого ввести соответствующую дозу. В таких случаях с учетом возникшей задержки должны быть перенесены все последующие визиты и начало цикла 2.
Во время поддерживающей терапии для введения последующих доз следует придерживаться изначального графика введения препарата.
Коррекция дозы (все показания)
Изменение дозы препарата Газива® не рекомендуется.
Рекомендации по изменению режима дозирования при возникновении симптоматических нежелательных явлений (включая инфузионные реакции) представлены в Таблице 5 и в разделе «Особые указания».
Таблица 5. Рекомендации по коррекции скорости инфузии при развитии инфузионных реакций (также см. раздел «Особые указания»)
Особые группы пациентов
У пациентов пожилого и старческого возраста (≥65 лет) коррекция дозы не требуется
Эффективность и безопасность препарата Газива® у детей и подростков младше 18 лет не установлена.
Коррекции дозы препарата Газива® у пациентов с нарушением функции почек легкой и средней степени тяжести (КК ≥ 30 мл/мин) не требуется. Эффективность и безопасность препарата Газива® у пациентов с нарушением функции почек тяжелой степени не установлены.
Эффективность и безопасность препарата Газива® у пациентов с нарушением функции печени не установлены.
Инструкция по приготовлению раствора для инфузий
Для введения первой дозы (1000 мг) препарата Газива® в первом цикле ХЛЛ рекомендуется использовать 2 инфузионных пакета из ПВХ или полиолефина (не-ПВХ) разного размера, что позволит различать дозу 100 мг, предназначенную для введения в цикле 1 в день 1, и дозу 900 мг для введения в цикле 1 в день 1 или день 2 (см. Таблицу 6).
Из флакона отобрать 40 мл концентрата препарата Газива®.
Ввести 4 мл концентрата в инфузионный пакет объемом 100 мл, а оставшиеся 36 мл концентрата — в инфузионный пакет объемом 250 мл, содержащий стерильный апирогенный 0.9% раствор натрия хлорида. Промаркировать каждый инфузионный пакет.
Таблица 6.
Введение препарата Газива® в день 8 и день 15 цикла 1 и в день 1 циклов 2-6 терапии ХЛЛ и во все циклы терапии фолликулярной лимфомы
Из флакона отобрать 40 мл концентрата препарата Газива® и ввести в инфузионный пакет из ПВХ или полиолефина (не-ПВХ), содержащий стерильный апирогенный 0.9% раствор натрия хлорида.
Пакет следует осторожно перевернуть для перемешивания раствора, избегая избыточного образования пены.
Следует визуально проверить приготовленный раствор для инфузий на предмет механических включений и изменения окраски.
С точки зрения микробиологической чистоты приготовленный раствор для инфузии следует использовать немедленно. В исключительных случаях приготовленный раствор может храниться не более 24 ч при температуре от 2° до 8°C, если приготовление раствора для инфузий происходило в контролируемых и валидированных асептических условиях. При этом за условия хранения (правила хранения и продолжительность) отвечает специалист, готовивший раствор.
Приготовленный раствор препарата Газива® физически и химически стабилен в течение 24 ч при температуре от 2° до 8°С, затем в течение 24 ч при комнатной температуре (≤30°С) и затем в течение не более 24 ч, во время которых должна быть завершена инфузия.
Побочное действие
Профиль безопасности препарата Газива® основан на данных клинического изучения препарата у пациентов с различными гематологическими заболеваниями (включая ХЛЛ и индолентную НХЛ; всего около 4900 пациентов). Преимущественно препарат применялся в комбинации с режимами химиотерапии (CHOP, CVP, хлорамбуцил или бендамустин). Наиболее серьезными нежелательными реакциями (НР) являлись:
- инфузионные реакции, наиболее часто встречавшиеся у пациентов с ХЛЛ (см. раздел «Особые указания»);
- синдром лизиса опухоли, наиболее часто встречавшийся у пациентов с высокой опухолевой нагрузкой и/или высоким содержанием лимфоцитов в периферической крови и/или нарушением функции почек (см раздел «Особые указания»);
- тромбоцитопения, в некоторых случаях имевшая летальный исход в цикле 1 (см раздел «Особые указания»).
Наиболее часто встречающимися нежелательным реакциями у пациентов независимо от заболевания были инфузионные реакции, нейтропения, диарея, запор и кашель.
В перечне ниже представлены нежелательные реакции, связанные с применением препарата Газива® в комбинации с различными режимами химиотерапии и по различным показаниям. Для описания частоты нежелательных реакций используется следующая классификация: очень часто (≥1/10), часто (≥1/100 и <1/10) и нечасто (≥1/1000 и <1/100). НР отнесены к той или иной категории на основании наиболее высокой частоты (различие ≥2% по сравнению с соответствующей группой сравнения), которая наблюдалась в любом из основных клинических исследований препарата Газива®. Нежелательные реакции сгруппированы в соответствии с классами систем органов медицинского словаря для нормативно-правовой деятельности MedDRA.
В каждой категории нежелательные реакции указаны в порядке убывания частоты.
Травмы, интоксикации и осложнения манипуляций: очень часто — инфузионные реакции*.
Со стороны крови и лимфатической системы: очень часто — нейтропения, тромбоцитопения, лейкопения, анемия; часто — фебрильная нейтропения.
Инфекционные и паразитарные заболевания: очень часто — инфекции верхних дыхательных путей, синусит, инфекции мочевыводящих путей, опоясывающий лишай (Herpes zoster), пневмония, назофарингит; часто — ринит, герпес слизистой оболочки полости рта, грипп, легочная инфекция, фарингит.
Со стороны дыхательной системы: очень часто — кашель; часто — боль в ротоглотке, заложенность носа, ринорея.
Со стороны обмена веществ: часто — гипокалиемия, синдром лизиса опухоли, гиперурикемия.
Со стороны скелетно-мышечной системы и соединительной ткани: очень часто — артралгия, боль в спине, боли в конечностях; часто — боли в костях, скелетно-мышечные боли в грудной клетке.
Нарушения психики: очень часто — бессонница; часто — тревожность, депрессия.
Со стороны мочевыделительной системы: часто — недержание мочи, дизурия.
Со стороны сосудов: часто — повышение АД.
Со стороны сердца: часто — фибрилляция предсердий.
Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы): часто — базальноклеточная карцинома, плоскоклеточная карцинома кожи.
Со стороны ЖКТ: очень часто — запор, диарея; часто — диспепсия, геморрой.
Со стороны кожи и подкожных тканей: очень часто — алопеция, зуд; часто — экзема.
Со стороны нервной системы: очень часто — головная боль.
Со стороны показателей лабораторных и инструментальных исследований: часто — снижение числа нейтрофилов, увеличение массы тела, снижение числа лейкоцитов.
Общие реакции и нарушения в месте введения: очень часто — утомляемость, повышение температуры тела, астения; часто — боль в груди.
*Определяется как любое связанное с терапией нежелательное явление, возникшее во время или в течение 24 ч после инфузии.
Описание отдельных нежелательных реакций
Инфузионные реакции
Наиболее часто (≥5%) наблюдались следующие симптомы инфузионных реакций (ИР): тошнота, рвота, диарея, головная боль, головокружение, утомляемость, озноб, повышение температуры тела, понижение АД, «приливы», повышение АД, тахикардия, одышка и дискомфорт в области грудной клетки.
Кроме того, сообщалось о симптомах ИР со стороны дыхательной системы, таких как бронхоспазм, раздражение горла и гортани, хрипы, отек гортани и со стороны сердца — фибрилляция предсердий
Хронический лимфолейкоз
Частота инфузионных реакций составляет 65% при введении первой дозы (1000 мг). У 20% пациентов наблюдались ИР 3-4 степени тяжести. У 7% пациентов ИР послужили причиной прекращения лечения препаратом Газива®. Частота ИР при последующих введениях составила соответственно 3% после второй дозы препарата Газива® (1000 мг) и 1% после введения последующих доз. ИР 3-4 степени тяжести наблюдались только при введении первых 1000 мг препарата Газива®. При последующих введениях ИР 3-5 степени не наблюдалось.
Комплекс мер по предупреждению ИР (см. раздел «Режим дозирования») позволяет снизить частоту ИР за исключением ИР 3-4 степени тяжести.
Неходжкинская лимфома
В цикле 1 общая частота возникновения ИР была выше у пациентов, получавших препарат Газива® в комбинации с химиотерапией, по сравнению с пациентами из соответствующих групп сравнения. У пациентов, получавших препарат Газива® в комбинации с химиотерапией, частота возникновения ИР была самой высокой в день 1, постепенно снижалась при последующих инфузиях и продолжала снижаться во время поддерживающей монотерапии препаратом Газива®.
В целом у 4% пациентов развились ИР, послужившие причиной прекращения лечения препаратом Газива®.
В клиническом исследовании, разработанном для изучения профиля безопасности коротких (приблизительно 90 мин) инфузий после цикла 1 у пациентов с ранее нелеченной ФЛ, частота, тяжесть и типы симптомов ИР были аналогичны тем, что наблюдались у пациентов, получавших инфузии со стандартной скоростью введения.
Нейтропения и инфекции
Хронический лимфолейкоз
Частота развития нейтропении на фоне терапии препаратом Газива® в комбинации с хлорамбуцилом составляет 40.7%, при этом частота развития инфекций составляет 38%. Нейтропения разрешалась спонтанно или после терапии гранулоцитарным колониестимулирующим фактором. Инфекционные осложнения 3-5 степени тяжести наблюдались у 12% пациентов, а частота случаев с летальным исходом была <1%. Также сообщалось о случаях длительной нейтропении (2%) и нейтропении с поздней манифестацией (16%).
Неходжкинская лимфома
Нейтропения возникала чаще у пациентов, получавших лечение препаратом Газива® в комбинации с химиотерапией, по сравнению с пациентами из контрольных популяций, а риск ее развития был повышен в периоде индукции.
Частота длительной нейтропении и нейтропении с поздним началом при лечении препаратом Газива® и химиотерапией составляла соответственно 3% и 7%.
Частота возникновения инфекций составляла 78% при лечении препаратом Газива® в комбинации с химиотерапией (явления 3-5 степени тяжести отмечались у 22%, и летальные исходы зарегистрированы у 3% пациентов).
Среди пациентов, получивших профилактическое лечение гранулоцитарным колониестимулирующим фактором, инфекции 3-5 степени тяжести встречались реже.
Тромбоцитопения и кровотечения
Хронический лимфолейкоз
Общая частота развития тромбоцитопении на фоне терапии препаратом Газива® в комбинации с хлорамбуцилом составила 15.4%, при этом острая тромбоцитопения, развивающаяся в течение 24 ч после инфузии, наблюдалась у 4% пациентов. Частота кровотечений составила 8%. О фатальных случаях кровотечений сообщалось только в первом цикле терапии у 1% пациентов. Причинно-следственная связь между тромбоцитопенией и развитием кровотечений не установлена.
Неходжкинская лимфома
Тромбоцитопения возникала с повышенной частотой в цикле 1 при лечении препаратом Газива® в комбинации с химиотерапией. Тромбоцитопения, развивающаяся в течение инфузии или не позднее 24 ч после инфузии (острая тромбоцитопения), чаще наблюдалась у пациентов, получавших терапию препаратом Газива® в комбинации с химиотерапией, чем у пациентов из групп сравнения. Частота нежелательных явлений кровотечений была схожей во всех группах лечения. Частота кровотечений всех степеней тяжести и кровотечений 3-5 степени тяжести составила 12% и 4%, соответственно. Частота случаев кровотечений с летальным исходом составила менее 1%, при этом в цикле 1 таких явлений не возникало.
Нарушения коагуляции, включая синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром)
Сообщалось о случаях развития ДВС-синдрома у пациентов с фолликулярной лимфомой и хроническим лимфолейкозом, получавших терапию препаратом Газива®. В некоторых случаях явления были связаны с ИР и/или СЛО. Специфичных исходных факторов риска развития ДВС-синдрома выявлено не было. Сообщалось о 3 пациентах, у которых развился ДВС-синдром (у одного пациента – серьезное явление, у 2 – несерьезное) среди 1135 пациентов, получавших терапию препаратом Газива® в трех крупнейших контролируемых исследованиях терапии фолликулярной лимфомы и хронического лимфолейкоза, спонсированных компанией. Все явления были отмечены в группе терапии обинутузумабом, в группах сравнения ни одного явления зарегистрировано не было. Все явления произошли в течение 1-2 дней после первой инфузии. Все пациенты продолжили лечение (см. раздел «Особые указания»).
Прогрессирующая мультиочаговая лейкоэнцефалопатия (ПМЛ)
Прогрессирующая мультиочаговая лейкоэнцефалопатия зарегистрирована у пациентов, получавших препарат Газива®.
Реактивация вируса гепатита В
Сообщалось о случаях реактивации вируса гепатита В на фоне терапии препаратом Газива®.
Прогрессирование сопутствующих заболеваний сердца
На фоне терапии препаратом Газива® наблюдались случаи нарушения функции сердца, в т.ч. с летальным исходом.
Перфорация органов ЖКТ
Сообщалось о случаях перфорации органов ЖКТ у пациентов, получающих препарат Газива®, преимущественно по поводу неходжкинской лимфомы.
Поддерживающая терапия у пациентов с индолентной НХЛ
У пациентов с рефрактерной/рецидивирующей иНХЛ во время поддерживающей монотерапии препаратом Газива®, проводимой после индукционной терапии препаратом Газива® в комбинации с бендамустином, самыми частыми нежелательными реакциями были кашель (20.3%), нейтропения (12.7%), инфекции верхних дыхательных путей (12.0%), диарея (10.1%), бронхит (9.5%), синусит (9.5%), тошнота (8.9%), утомляемость (8.9%), инфузионные реакции (8.2%), инфекция мочевыводящих путей (7.0%), назофарингит (7.0%), повышение температуры тела (7.0%), артралгия (6.3%), рвота (5.7%), сыпь (5.7%), пневмония (5.1%), одышка (5.1%) и боли в конечностях (5.1%). Самыми частыми нежелательными реакциями 3-5 степени тяжести были нейтропения (10.8%), фебрильная нейтропения (1.9%) и анемия, тромбоцитопения, пневмония, сепсис, инфекция верхних дыхательных путей и инфекция мочевыводящих путей (все с частотой 1.3%).
Изменения лабораторных показателей
Транзиторное повышение активности печеночных ферментов (АСТ, АЛТ, ЩФ) в сыворотке крови наблюдалось вскоре после первой инфузии препарата Газива®.
Противопоказания к применению
- повышенная чувствительность к обинутузумабу и к другим компонентам препарата;
- активный гепатит В и/или другие инфекции в активной фазе;
- нарушения функции почек тяжелой степени при хроническом лимфолейкозе (КК < 30 мл/мин) и при фолликулярной лимфоме (КК < 40 мл/мин) (эффективность и безопасность применения не установлены);
- нарушения функции печени (эффективность и безопасность применения не установлены);
- вакцинация живыми вирусными вакцинами;
- беременность;
- период грудного вскармливания;
- возраст до 18 лет (эффективность и безопасность применения у детей не установлены).
С осторожностью
Хронические и рецидивирующие инфекции в анамнезе.
Применение при беременности и кормлении грудью
Беременность и период грудного вскармливания
Необходимо рассмотреть отсрочку проведения вакцинации живыми вакцинами у младенцев, чьи матери получали препарат Газива® во время беременности, до тех пор, пока число В-клеток у них не восстановится до нормы.
Обинутузумаб выделяется с грудным молоком у животных. Грудное вскармливание не рекомендуется во время лечения и, как минимум, в течение 18 месяцев после введения последней дозы препарата Газива®.
Контрацепция
Женщины, обладающие репродуктивным потенциалом, должны использовать эффективные методы контрацепции в период лечения препаратом Газива® и в течение 18 месяцев после окончания терапии.
Применение при нарушениях функции печени
Противопоказано применение у пациентов с нарушениями функции печени (эффективность и безопасность применения не установлены).
Применение при нарушениях функции почек
Противопоказание: нарушения функции почек тяжелой степени при хроническом лимфолейкозе (КК < 30 мл/мин) и при фолликулярной лимфоме (КК < 40 мл/мин) (эффективность и безопасность применения не установлены).
Применение у детей
Применение препарата у пациентов в возрасте до 18 лет противопоказано (эффективность и безопасность применения у детей не установлены).
Применение у пожилых пациентов
Коррекция дозы у пациентов пожилого и старческого возраста не требуется.
Особые указания
В медицинской документации пациента следует указывать торговое название препарата (Газива®) и номер серии. Замена препарата на какой-либо другой биологический лекарственный препарат требует согласования с лечащим врачом. Информация, представленная в данном описании, относится только к препарату Газива®.
Терапию препаратом Газива® должен назначать онколог или гематолог. Введение препарата проводится при наличии доступа к набору для оказания экстренной помощи. Врач, имеющий опыт применения химиотерапевтических препаратов, должен быть доступен в процессе проводимой терапии.
Инфузионные реакции
Наиболее часто наблюдаемыми нежелательными реакциями у пациентов, получающих препарат Газива®, были ИР, развившиеся преимущественно во время введения первых 1000 мг препарата. Комплекс мер по предупреждению ИР (применение подходящего ГКС, перорального приема анальгетика/антигистаминного препарата, пропуск приема антигипертензивного препарата) у пациентов с ХЛЛ позволяет снизить частоту ИР, за исключением ИР 3-4 степени.
Рекомендуется принимать меры по предупреждению ИР, описанные в разделе «Режим дозирования».
Частота и тяжесть ИР существенно уменьшались после введения первых 1000 мг препарата Газива®, и при последующих инфузиях ИР у большинства пациентов не развивались.
В основном, независимо от показаний, наблюдались ИР легкой и средней степени тяжести, которые разрешались после замедления или временного прекращения первой инфузии, тем не менее, известно также о тяжелых и жизнеугрожающих ИР, требующих симптоматической терапии. ИР могут клинически не отличаться от lgE-опосредованных аллергических реакций (например, анафилаксии). У пациентов с высокой опухолевой нагрузкой и/или с высоким содержанием циркулирующих лимфоцитов при ХЛЛ (>25х109/л) риск развития тяжелых ИР повышен. Меры по профилактике ИР описаны в разделе «Режим дозирования». Меры по купированию инфузионных реакций с учетом их степени тяжести описаны в разделе «Режим дозирования», Таблица 5.
Терапию препаратом Газива® следует полностью прекратить, в случае развития:
- жизнеугрожающих острых респираторных симптомов;
- ИР 4 степени (угрожающих жизни);
- повторной (продолжающейся/рецидивирующей) ИР 3 степени.
Пациенты с сопутствующими заболеваниями сердца или легких должны находиться под тщательным наблюдением во время инфузии и после нее. Во время инфузии препарата Газива® возможно понижение АД. В связи с этим следует рассмотреть возможность приостановки лечения антигипертензивными препаратами в течение 12 ч перед каждой инфузией, на протяжении каждой инфузии и в продолжение 1 ч после введения препарата. Необходимо оценить пользу и возможный риск остановки приема антигипертензивных препаратов у пациентов с высоким риском развития гипертонического криза.
Реакции гиперчувствительности
На фоне терапии препаратом Газива® отмечались случаи реакций гиперчувствительности с немедленным (анафилаксия) и замедленным (сывороточная болезнь) развитием.
Если во время или после инфузии подозревается развитие реакции гиперчувствительности (развитие симптомов происходит, как правило, при последующих введениях, очень редко симптомы развиваются во время первой инфузии), введение должно быть прекращено и терапию препаратом Газива® следует отменить и не возобновлять в дальнейшем.
Пациентам с установленной гиперчувствительностью к препарату Газива® противопоказана терапия данным препаратом. Возможны затруднения при дифференциальной диагностике реакции гиперчувствительности и инфузионной реакции
Синдром лизиса опухоли (СЛО)
Наблюдались случаи СЛО. Пациентам из группы риска развития СЛО (больные с высокой опухолевой нагрузкой и/или высоким содержанием лимфоцитов в периферической крови (>25×109/л) и/или с нарушением функции почек (КК <70 мл/мин)) необходимо провести профилактику СЛО. Профилактика должна включать адекватную гидратацию и назначение гипоурикемических препаратов (например, аллопуринола или других альтернативных препаратов) до начала инфузии (как указано в разделе «Режим дозирования»). Пациенты из группы риска развития СЛО должны находиться под тщательным наблюдением в первые дни терапии, при этом особое внимание следует уделять контролю функции почек, концентрации калия и мочевой кислоты. Дополнительные мероприятия должны проводиться в соответствии со стандартной практикой. При развитии СЛО необходимо тщательное наблюдение за функцией почек и водно-электролитным балансом с последующей коррекцией электролитных нарушений, а также проведением поддерживающих лечебных мероприятий, включая, если требуется, диализ.
Нейтропения
Наблюдались случаи серьезной и жизнеугрожающей нейтропении, включая фебрильную нейтропению. При развитии нейтропении пациенты нуждаются в тщательном наблюдении и проведении регулярного лабораторного обследования до полного разрешения симптомов. При необходимости следует провести терапию в соответствии с локально принятой практикой и рассмотреть необходимость применения Г-КСФ. При любом проявлении сопутствующей инфекции необходимо назначить соответствующее лечение. Возможно развитие нейтропении с поздней манифестацией (возникновение не раньше чем через 28 дней после окончания лечения) и длительной нейтропении продолжительностью более 28 дней после окончания или отмены терапии.
Тромбоцитопения
Наблюдались случаи тяжелой и жизнеугрожающей тромбоцитопении, в т.ч. случаи острой тромбоцитопении, которые развивались в течение 24 ч после инфузии. В 1-м цикле терапии наблюдались случаи кровотечений с летальным исходом. Четкая взаимосвязь между развитием кровотечений и тромбоцитопенией не установлена.
В ходе лечения пациенты нуждаются в тщательном наблюдении на предмет развития тромбоцитопении, особенно в 1 цикле. При выявлении тромбоцитопении необходимо регулярное проведение лабораторного обследования до тех пор, пока реакция не разрешится. В тяжелых или жизнеугрожающих случаях следует рассмотреть возможность отложить введение препарата Газива®. Решение о проведении гемотрансфузии (трансфузии тромбоцитов) принимает лечащий врач в соответствии с практикой, установленной в лечебном учреждении. Необходимо принимать во внимание прием любых сопутствующих препаратов, способных усугубить тромбоцитопению, таких как ингибиторы агрегации тромбоцитов и антикоагулянты, особенно в 1 цикле терапии.
Нарушения коагуляции, включая ДВС-синдром
Сообщалось о случаях развития ДВС-синдрома у пациентов с фолликулярной лимфомой и хроническим лимфолейкозом, получавших терапию препаратом Газива®. В большинстве случаев явления включали субклинические (бессимптомные) изменения лабораторных показателей тромбоцитов и коагулограммы после первой инфузии со спонтанным разрешением, как правило к 8 дню. В некоторых случаях явления были связаны с ИР и/или СЛО. Специфичных исходных факторов риска развития ДВС-синдрома выявлено не было (см. раздел «Побочное действие»).
Прогрессирование сопутствующих заболеваний сердца
У пациентов с сопутствующими заболеваниями сердца, получавших терапию препаратом Газива®, отмечалось развитие аритмий (в частности, фибрилляции предсердий и тахиаритмии), стенокардии, острого коронарного синдрома, инфаркта миокарда и сердечной недостаточности (см. раздел «Побочное действие»). Данные явления могут развиться как часть инфузионных реакций и иметь летальный исход. Таким образом, пациентов с заболеваниями сердца в анамнезе следует тщательно мониторировать. Кроме того, у таких пациентов следует соблюдать осторожность при проведении гидратации с целью избежать потенциального образования избытка жидкости.
Инфекции
Препарат Газива® не следует применять при наличии у пациента инфекции в активной стадии. Следует соблюдать осторожность при принятии решения о назначении препарата Газива® пациентам с периодически рецидивирующими и хроническими инфекциями в анамнезе. Возможно развитие серьезных бактериальных и грибковых инфекций, а также развитие или реактивация вирусных инфекций во время терапии и после ее окончания. Сообщалось о летальных случаях инфекционных заболеваний.
У пациентов с фолликулярной лимфомой зарегистрирована высокая частота развития инфекций на всех этапах клинических исследований, включая периоды последующего наблюдения. При этом наиболее высокая частота инфекций была характерна для периода поддерживающей терапии.
В периоде последующего наблюдения инфекции 3-5 степеней тяжести чаще наблюдались у пациентов, которые на этапе индукции получали препарат Газива® в комбинации с бендамустином.
Реактивация вируса гепатита В
На фоне применения анти CD-20 препаратов возможна реактивация вируса гепатита В, в некоторых случаях сопровождающаяся фульминантным гепатитом, печеночной недостаточностью, возможен летальный исход.
Перед назначением препарата Газива® всем пациентам следует пройти скрининг на вирус гепатита В, включая определение HBsAg-статуса, HBcAb-статуса, а также дополнительных маркеров согласно установленной местной практике. Препарат Газива® не следует применять у пациентов с активным гепатитом В. Пациентам с положительными серологическими маркерами гепатита В следует проконсультироваться с врачом-гепатологом перед назначением препарата Газива®. В отношении таких пациентов необходимо проводить соответствующий мониторинг и принимать меры по профилактике реактивации вируса гепатита В в соответствии с местными стандартами.
Прогрессирующая многоочаговая лейкоэнцефалопатия (ПМЛ)
У пациентов, получавших терапию препаратом Газива®, отмечалась ПМЛ (см. раздел «Побочное действие»). При развитии у пациентов новых неврологических симптомов или изменении уже имеющихся необходимо рассмотреть возможность диагноза ПМЛ. Симптомы ПМЛ не являются специфическими и могут варьировать в зависимости от локализации повреждения в головном мозге. Часто наблюдаются моторные симптомы с пирамидными нарушениями (например, мышечная слабость, паралич и нарушения чувствительности), аномалии чувствительности, мозжечковые нарушения и дефекты поля зрения. Могут развиться некоторые признаки/симптомы, считающиеся корковыми (например, афазия или визуально-пространственная дезориентация).
Диагностика ПМЛ включает, но не ограничивается консультацией врача-невролога, проведением МРТ головного мозга и люмбальной пункцией (анализ спинномозговой жидкости на содержание ДНК JC-вируса). Терапию препаратом Газива® необходимо приостановить на время проведения обследования потенциальной ПМЛ и полностью ее прекратить, если диагноз ПМЛ подтвержден. Также следует рассмотреть возможность прекращения или сокращения любой сопутствующей иммуносупрессивной терапии или химиотерапии. Для оценки и лечения ПМЛ пациент должен быть направлен к неврологу.
Иммунизация
Безопасность иммунизации живыми или аттенуированными противовирусными вакцинами после окончания терапии препаратом Газива® не изучалась, вакцинация живыми противовирусными вакцинами во время терапии и до момента восстановления пула В-клеток не рекомендуется.
Внутриутробное воздействие препарата Газива® и вакцинация младенцев живыми вирусными вакцинами: в связи с потенциальным истощением пула В-клеток у младенцев, чьи матери получали препарат Газива® во время беременности, вопрос о безопасности и сроках вакцинации живыми вирусными вакцинами следует обсудить с педиатром. Необходимо рассмотреть возможность отсрочки вакцинации живыми вакцинами до тех пор, пока число В-клеток у ребенка не восстановится до нормы.
Пациенты с нарушением функции почек
Хронический лимфолейкоз. У пациентов с ХЛЛ и нарушением функции почек средней степени тяжести (КK<50 мл/мин), получающих лечение препаратом Газива® в комбинации с хлорамбуцилом, частота развития серьезных нежелательных явлений и нежелательных явлений с летальным исходом может быть выше по сравнению с пациентами с КК ≥50 мл/мин. Значимых различий в эффективности между пациентами с КК <50 мл/мин и пациентами с КК ≥50 мл/мин не отмечалось. Применение препарата Газива® у пациентов с КК <30 мл/мин не изучалось.
Неходжкинская лимфома. В ходе изучения препарата Газива® в комбинации с химиотерапией у 7.7% пациентов с рефрактерной/рецидивирующей фолликулярной лимфомой и у 5% с ранее нелеченной фолликулярной лимфомой имелось нарушение функции почек средней степени тяжести (КК<50 мл/мин). У этих пациентов развивалось большее число серьезных нежелательных явлений (НЯ), НЯ, ведущих к отмене терапии (только пациенты с ранее нелеченной фолликулярной лимфомой), и НЯ 3-5 степени тяжести по сравнению с пациентами с КК ≥50 мл/мин. Применение препарата Газива® у пациентов с КК <40 мл/мин не изучалось.
Пациенты пожилого и старческого возраста
Хронический лимфолейкоз. У пациентов с ХЛЛ в возрасте ≥75 лет, получающих терапию препаратом Газива® в комбинации с хлорамбуцилом, частота развития серьезных нежелательных явлений и нежелательных явлений с летальным исходом может быть выше по сравнению с пациентами моложе 75 лет. Различия в эффективности терапии между пациентами в возрасте ≥75 лет и пациентами моложе 75 лет отсутствуют.
Неходжкинская лимфома. При изучении применения препарата Газива® в комбинации с химиотерапией при индолентной неходжкинской лимфоме у пациентов в возрасте 65 лет и старше развивалось большее число серьезных НЯ, НЯ, ведущих к отмене терапии, и НЯ с летальным исходом по сравнению с пациентами моложе 65 лет. Клинически значимые различия в эффективности не наблюдались.
Инструкции по уничтожению неиспользованного препарата или препарата с истекшим сроком годности
Попадание лекарственного препарата Газива® в окружающую среду должно быть сведено к минимуму. Не следует утилизировать препарат с помощью сточных вод или вместе с бытовыми отходами. Уничтожение неиспользованного препарата или препарата с истекшим сроком годности должно проводиться в соответствии с требованиями лечебного учреждения.
Влияние на способность к управлению транспортными средствами и механизмами
Влияние препарата Газива® на способность управлять автомобилем и работать с механизмами не изучалось. При развитии инфузионных реакций и других нежелательных реакций рекомендуется воздержаться от управления транспортными средствами и механизмами до полного разрешения симптомов.
Передозировка
Опыт превышения рекомендуемой дозы препарата Газива® отсутствует. Изучено применение доз от 50 мг до 2000 мг за одну инфузию. Степень тяжести и частота нежелательных реакций не зависели от дозы.
Лечение: при случайном превышении дозы препарата Газива® необходимо немедленно прекратить инфузию или снизить дозу. В связи с увеличением риска инфекционных осложнений при истощении пула В-лимфоцитов следует тщательно наблюдать за пациентом и рассмотреть необходимость проведения развернутого общего анализа крови.
Лекарственное взаимодействие
Специальных исследований взаимодействия с другими лекарственными средствами не проводилось.
Однако были проведены ограниченные подысследования межлекарственного взаимодействия препарата Газива® с бендамустином, препаратами схемы CHOP (циклофосфамид, доксорубицин, винкристин, преднизолон), препаратами схемы FC (флударабин, циклофосфамид) и хлорамбуцилом. Совместное введение препарата Газива® не оказывало влияния на фармакокинетику бендамустина, FC или отдельных компонентов схемы CHOP; кроме того, отсутствовало заметное влияние бендамустина, FC, хлорамбуцила или CHOP на фармакокинетику препарата Газива®. Риск взаимодействия с одновременно применяемыми препаратами нельзя полностью исключить.
Условия хранения препарата Газива®
Препарат следует хранить в недоступном для детей, защищенном от света месте при температуре от 2° до 8°С. Не замораживать.
Срок годности препарата Газива®
Срок годности — 3 года. Не применять по истечении срока годности.
Условия реализации
Препарат отпускают по рецепту.
Контакты для обращений
Ф.ХОФФМАНН-ЛЯ РОШ ЛТД.
(Швейцария)

|
|
Претензии потребителей следует направлять |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Газива
МНН: Обинутузумаб
Производитель: Рош Диагностикс ГмбХ
Анатомо-терапевтическо-химическая классификация: Обинутузумаб
Номер регистрации в РК:
№ РК-ЛС-5№121935
Информация о регистрации в РК:
28.12.2020 — 28.12.2030
Информация о реестрах и регистрах
Информация по ценам и ограничения
Предельная цена закупа в РК:
1 720 456 KZT
- Скачать инструкцию медикамента
Торговое название
Газива
Международное непатентованное название
Обинутузумаб
Лекарственная форма
Концентрат для приготовления инфузионного раствора 1000 мг/40 мл
Состав
Один флакон содержит
активное вещество: обинутузумаб 1000 мг,
вспомогательные вещества: L-гистидин, L-гистидина гидрохлорида моногидрат, трегалозы дигидрат, полоксамер 188, вода для инъекций
Описание
Прозрачная или опалесцирующая жидкость от бесцветного до слегка коричневатого цвета
Фармакотерапевтическая группа
Противоопухолевые препараты. Моноклональные антитела. Обинутузумаб
Код АТХ L01XC15
Фармакологические свойства
Фармакокинетика
Фармакокинетические характеристика обинутузумаба при его использовании пациентами с хроническим лимфолейкозом (ХЛЛ) приведены на основании фармакокинетической модели, с помощью которой был проведен анализ фармакокинетических показателей 678 пациентов с неходжкинской лимфомой (НХЛ) и ХЛЛ, принимавших участие в исследованиях фаз I, II и III, где использовался обинутузумаб.
Абсорбция
При использовании популяционной фармакокинетической модели после инфузии, проведенной в 1-й день шестого цикла терапии, среднее значение Cmax составляло 473.2 мкг/мл, а значение AUC(τ) было равно 9516 мкг-сут/мл.
Распределение
После внутривенного введения объем распределения центральной камеры (2.76 л) приблизительно равен объему сыворотки, что указывает на ограниченность распределения, главным образом, плазмой и интерстициальной жидкостью.
Биотрансформация
Метаболизм обинутузумаба непосредственно не изучался. Клиренс антител происходит в основном через катаболизм.
Выведение
Клиренс обинутузумаба во время шестого цикла у пациентов с ХЛЛ составляет приблизительно 0.083 л/сут, а средний период полувыведения равен 30.3 суткам. Выведение препарата основано на модели динамически изменяющегося клиренса, протекающего параллельно двумя путями: линейный клиренс и нелинейный клиренс, который изменяется как функция от времени. На начальном этапе терапии преобладает нелинейный, меняющийся со временем клиренс. По мере продолжения лечения влияние данного пути клиренса снижается, и преобладать начинает линейный клиренс. Это свидетельствует о мишень-опосредованном распределении препарата, при котором первоначально большое число клеток белка CD20 приводит к быстрому снижению уровня обинутузумаба. Однако, после того как большая часть клеток CD20 связывается с обинутузумабом, влияние мишень-опосредованного распределения на фармакокинетику препарата снижается.
Взаимосвязь между фармакокинетическими и фармакодинамическими показателями
Популяционный фармакокинетический анализ показал, что пол является ковариатой, объясняющей определенную вариабельность фармакокинетических параметров у пациентов; у мужчин наблюдается более высокий клиренс в равновесном состоянии (на 22%) и более значительный объем распределения (на 18%). В то же время, результаты популяционного анализа говорят о том, что различия в уровне воздействия незначительны (средние значения AUC и Cmax во время 6-го цикла терапии составляют у женщин 11282 мкг-сут/мл и 578.0 мкг/мл, у мужчин – 8451 мкг-сут/мл и 432.5 мкг/мл, соответственно) и не требуют коррекции дозы в зависимости от пола пациента.
Фармакокинетика у пожилых пациентов
Популяционный фармакокинетический анализ показал, что возраст не влияет на фармакокинетику обинутузумаба. Между пациентами в возрасте до 65 лет (n=265), 65-75 лет (n=197) и старше 75 лет (n=128) не наблюдалось значительных различий в фармакокинетических показателях.
Фармакокинетика у детей
Исследования по оценке фармакокинетических параметров обинутузумаба у детей не проводились.
Почечная недостаточность
Популяционный фармакокинетический анализ показал, что клиренс креатинина не влияет на фармакокинетику обинутузумаба. Фармакокинетика препарата у пациентов с легкой степенью почечной недостаточности (клиренс креатинина 50-89 мл/мин, n=306) и средней степенью (клиренс креатинина 30-49 мл/мин, n=72) была аналогичной фармакокинетике обинутузумаба у пациентов с нормальной функцией почек (клиренс креатинина ≥ 90 мл/мин, n=207). Данные по фармакокинетике препарата у пациентов с тяжелой почечной недостаточностью (клиренс креатинина 15-29 мл/мин) ограничены (n=5), поэтому определенных рекомендаций для данной категории пациентов не существует.
Печеночная недостаточность
Формальные исследования фармакокинетики обинутузумаба у пациентов с печеночной недостаточностью не проводились.
Фармакодинамика
Газива – рекомбинантное моноклональное гуманизированое глико-инженерное антитело типа II, действующее против белка CD20, относящееся к изотипу IgG1. Обинутузумаб специфически связывается с внеклеточной петлей трансмембранного антигена CD20 на поверхности доброкачественных и злокачественных В-клеток-предшественников и зрелых В-лимфоцитов, не связываясь на поверхности гемопоэтических стволовых клеток, про-В-клеток, нормальных клеток плазмы и клеток других здоровых тканей. Сегмент Fc обинутузумаба, полученных с помощью гликоинженерии, обладает более высоким сродством к рецепторам FcγRIII иммунных эффекторов, таких как естественные клетки-киллеры, макрофаги и моноциты, по сравнению с антителами, в создании которых не использовались методы гликоинженерии.
В доклинических исследованиях обинутузумаб индуцирует непосредственную гибель клеток и опосредует антителозависимую клеточную цитотоксичность (АЗКЦ) и антителозависимый клеточный фагоцитоз (АЗКФ) через рекрутинг FcγRIII-положительных клеток-иммунных эффекторов. Обинутузумаб также опосредует комплементзависимую цитотоксичность (КЗЦ) низкой степени. По сравнению с антителами I типа, обинутузумаб (антитело типа II) характеризуется более интенсивной индукцией непосредственной гибели клеток с параллельным уменьшением КЗЦ при использовании эквивалентных доз. Являясь глико-инженерным антителом, обинутузумаб также характеризуется более высокой антителозависимой клеточной цитотоксичностью по сравнению с не глико-инженерными антителами, при использовании эквивалентных доз. В исследованиях с использованием моделей животных обинутузумаб опосредует интенсивное снижение числа В-клеток и противоопухолевую эффективность.
В базовом клиническом исследовании BO21004/CLL11 у 91% (40 из 44) поддающихся оценке пациентов, получавших препарат Газива, наблюдалось снижение уровней В-клеток (определяемое, как число CD19+B-клеток < 0.07 х 109/л) в конце курса терапии, сохранявшееся в течение 6 месяцев последующего наблюдения. Восстановление числа В-клеток имело место в течение 12-18 месяцев у 35% (14 из 40) пациентов, у которых не наблюдалось прогрессирования болезни, и у 13% (5 из 40) пациентов с прогрессированием заболевания.
Показания к применению
В комбинации с хлорамбуцилом для лечения взрослых пациентов с хроническим лимфолейкозом, ранее не получавших терапию и имеющих сопутствующие патологии, не позволяющие применять режимы терапии, основанные на флударабине.
Способ применения и дозы
Лечение должно проводиться под наблюдением квалифицированного врача, имеющего опыт применения противоопухолевых препаратов, а также при наличии необходимых условий для проведения реанимационных мероприятий в полном объеме.
Профилактика синдрома лизиса опухоли (СЛО)
При лечении пациентов с высоким количеством лимфоцитов в кровотоке (> 25 x 109/л) рекомендуется проведение профилактики с помощью адекватной гидратации и введения урикостатиков (например, аллопуринола) за 12-24 часа до начала терапии с целью снижения риска развития синдрома лизиса опухоли.
Профилактика инфузионных реакций и премедикация
Одним из симптомов инфузионных реакций, возникающих во время проведения внутривенной инфузии препарата, может являться снижение артериального давления. Поэтому следует рассмотреть возможность прекращения использования гипотензивных средств за 12 часов до начала инфузии и в течение ее проведения, а также в течение 1 часа после введения препарата.
Таблица 1. Премедикация для снижения риска развития инфузионных реакций
|
День цикла терапии |
Пациенты, которым требуется премедикация |
Премедикация |
Режим введения |
|
Цикл 1: День 1 |
Все пациенты |
Внутривенные кортикостероиды1 |
За 1 час до проведения инфузии |
|
Пероральные анальгетики/жаропонижающие средства2 |
Как минимум за 30 минут до инфузии |
||
|
Антигистаминные препараты3 |
|||
|
Цикл 1: День 2 |
Все пациенты |
Внутривенные кортикостероиды1 |
За 1 час до проведения инфузии |
|
Пероральные анальгетики/жаропонижающие средства2 |
Как минимум за 30 минут до инфузии |
||
|
Антигистаминные препараты3 |
|||
|
Цикл 1: День 8, День 15 Циклы 2-6: День 1 |
Пациенты, имевшие инфузионные реакции степени 3 во время предыдущей инфузии ИЛИ Пациенты с числом лимфоцитов > 25×109/л перед следующим курсом терапии |
Внутривенные кортикостероиды1 |
За 1 час до проведения инфузии |
|
Все пациенты |
Пероральные анальгетики/жаропонижающие средства2 |
Как минимум за 30 минут до инфузии |
|
|
Пациенты, имевшие инфузионные реакции (степени 1 и выше) во время предыдущей инфузии |
Антигистаминные препараты3 |
1 100 мг преднизона/преднизолона или 20 мг дексаметазона или 80 мг метилпреднизолона. Нельзя использовать гидрокортизон, т.к. он не помогает снизить частоту инфузионных реакций
2 например, 1000 мг ацетоминофена/парацетамола
3 например, 50 мг дифенгидрамина
Режимы дозирования
Рекомендуемые дозы указаны в Таблице 2.
Цикл 1
Рекомендуемая доза препарата составляет 1000 мг в 1-й, 2-й, 8-й и 15-й день первого цикла терапии продолжительностью 28 дней. Для инфузий, проводимых в 1-й и 2-й день необходимо подготовить два инфузионных мешка (100 мг в 1-й день и 900 мг – во 2-й день). Если введение первой инфузии не сопровождается прерываниями или изменениями скорости вливания, второй инфузионный мешок можно использовать в тот же день (не требуется отсрочка дозирования или повторная премедикация) при условии наличия надлежащих условий и медицинского наблюдения на протяжении всего периода проведения инфузии. В случае наличия изменений скорости введения инфузии или ее прерываний при вливании первых 100 мг, инфузия с помощью второго инфузионного мешка проводится на следующий день.
Циклы 2-6
Рекомендуемая доза препарата составляет 1000 мг в 1-й день каждого цикла.
Таблица 2. Дозы препарата, вводимые во время 6 циклов терапии (каждый продолжительностью 28 дней)
|
Цикл |
День |
Доза Газивы |
|
Цикл 1 |
День 1 |
100 мг |
|
День 2 (или продолжение в 1-й день) |
900 мг |
|
|
День 8 |
1000 мг |
|
|
День 15 |
1000 мг |
|
|
Циклы 2-6 |
День 1 |
1000 мг |
Продолжительность лечения
Шесть курсов терапии, каждый продолжительностью 28 суток.
Введение дозы позднее требуемого времени или пропуск дозы
В случае пропуска очередной дозы препарата ее следует ввести как можно скорее; следующей запланированной дозы ждать не следует. Между введением доз препарата необходимо соблюдать рекомендуемый интервал.
Модификация доз во время лечения
Дозы препарата снижать не рекомендуется.
Особые категории пациентов
Пожилые люди:
Коррекция дозы для лиц пожилого возраста не требуется.
Почечная недостаточность
Коррекция дозы для пациентов с почечной недостаточностью легкой или умеренной степени тяжести (клиренс креатинина 30-89 мл/мин) не требуется. Безопасность и эффективность препарата у пациентов с тяжелой почечной недостаточностью (клиренс креатинина < 30 мл/мин) не установлены.
Печеночная недостаточность
Безопасность и эффективность препарата у пациентов с нарушениями функций печени не установлены, поэтому специальных рекомендаций для таких пациентов нет.
Применение у детей
Безопасность и эффективность препарата у детей и подростков в возрасте до 18 лет не установлены. Информация на этот счет отсутствует.
Способ применения
Препарат предназначен для внутривенного введения. Газива, после разбавления, вводится в виде внутривенной инфузии через специальную инфузионную линию. Препарат нельзя вводить струйно или путем болюсного введения.
Инструкции по скорости введения инфузии даны в Таблице 3.
Таблица 3. Стандартная скорость введения инфузии при условии отсутствия инфузионных реакций/реакций гиперчувствительности
|
Цикл |
День |
Скорость введения |
|
Цикл 1 |
День 1 (100 мг) |
25 мг/ч в течение 4 часов. Не следует увеличивать скорость введения |
|
День 2 (или продолжение в 1-й день) (900 мг) |
50 мг/ч. Скорость вливания можно увеличивать на 50 мг/ч каждые 30 минут вплоть до достижения уровня в 400 мг/ч. |
|
|
День 8 |
Вливание можно начинать со скоростью 100 мг/ч и увеличивать на 100 мг/ч каждые 30 минут вплоть до достижения уровня в 400 мг/ч. |
|
|
День 15 |
||
|
Циклы 2-6 |
День 1 |
Для устранения инфузионных реакций может потребоваться временное прерывание инфузии, снижение ее скорости или полное прекращение терапии в зависимости от указанных ниже условий:
-
Степень 4 (угроза для жизни): инфузию останавливают и полностью прекращают проведение терапии препаратом.
-
Степень 3 (тяжелые реакции): инфузию временно приостанавливают и проводят симптоматическое лечение. После устранения симптомов проведение инфузии можно возобновить со скоростью, которая составляет не более 50% от скорости введения, при которой развилась инфузионная реакция, и, в случае отсутствия у пациента симптомов инфузионных реакций, скорость введения можно постепенно повышать согласно рекомендациям, указанным в Таблице 3. Скорость инфузии в 1-й день 1-го цикла можно увеличить до 25 мг/ч через 1 часа, не повышая ее в дальнейшем. При появлении у пациента второй инфузионной реакции 3-й степени инфузию останавливают и полностью прекращают проведение терапии препаратом.
-
Степени 1-2 (от слабых до умеренных реакций): скорость инфузии снижают и проводят симптоматическую терапию. После устранения симптомов проведение инфузии можно возобновить и, в случае отсутствия у пациента симптомов инфузионных реакций, скорость введения можно постепенно повышать согласно рекомендациям, указанным в Таблице 3. Скорость введения инфузии в 1-й день 1-го цикла можно увеличить до 25 мг/ч через 1 часа, не повышая ее в дальнейшем.
Побочные действия
Краткая характеристика профиля безопасности
Нежелательные реакции (НР) на препарат, описанные в данном разделе, были выявлены на этапе проведения терапии и последующего наблюдения в базовом клиническом исследовании BO21004/CLL11, в котором сравнивалось комбинированное применение препарата Газива и хлорамбуцила и монотерапия хлорамбуцилом (Стадия 1), или комбинация ритуксимаба и хлорамбуцила (Стадия 2). В группе комбинированной терапии обинутузумабом и хлорамбуцилом 81% пациентов получили все 6 циклов терапии по сравнению с 89% пациентов в группе «ритуксимаб+хлорамбуцил) и 67% в группе монотерапии хлорамбуцилом.
Самыми распространенными нежелательными реакциями у пациентов, получавших Газиву, являлись инфузионные реакции, наблюдавшиеся у большинства пациентов во время первого цикла лечения. Частота возникновения инфузионных симптомов резко падала с 65% после первой дозы в 1000 мг до менее 3% после последующих инфузий.
Нейтропения и тромбоцитопения наблюдались у 41% и 15% пациентов, соответственно, частота развития инфекций 3-5 степени в группе «Газива+хлорамбуцил» составила 16%.
К другим серьезным нежелательным реакциям, выявленным на этапе клинической разработки препарата, относились синдром лизиса опухоли, кардиологические явления и, очень редко, ПМЛ.
В Таблице 4 приведена сводная информация о нежелательных реакциях, возникавших чаще (разница в ≥2%) у пациентов, получавших Газиву в комбинации с хлорамбуцилом, по сравнению с пациентами из групп монотерапии хлорамбуцилом и комбинированной терапии «ритуксимаб+хлорамбуцил».
Частота возникновения реакций определяется следующим образом: очень часто (≥1/10), часто (≥1/100 — < 1/10), иногда (≥1/1000 — < 1/100), редко (≥1/10000 — < 1/1000) и очень редко (< 1/10000). Для каждой категории частоты нежелательные реакции перечислены в порядке убывания степени их тяжести.
Табличный список нежелательных реакций
Таблица 4. Нежелательные реакции, возникавшие чаще (разница в ≥2%) у пациентов, получавших Газиву в комбинации с хлорамбуцилом, по сравнению с пациентами из групп монотерапии хлорамбуцилом и комбинированной терапии «ритуксимаб+хлорамбуцил» (Исследование BO21004/CLL11)*
|
Частота |
Все степени % Газива + хлорамбуцил |
Степени 3-5† % Газива + хлорамбуцил |
|
Инфекционные и паразитарные заболевания |
||
|
Часто |
Инфекции мочевыводящих путей, назофарингит, герпес слизистой оболочки полости рта, ринит‡, фарингит |
Инфекции мочевыводящих путей |
|
Иногда |
Назофарингит |
|
|
Доброкачественные, злокачественные и неуточненные новообразования, включая полипы и кисты |
||
|
Часто |
Плоскоклеточный рак кожи |
Плоскоклеточный рак кожи |
|
Нарушения со стороны крови и лимфатической системы |
||
|
Очень часто |
Нейтропения, тромбоцитопения, анемия |
Нейтропения, тромбоцитопения |
|
Часто |
Лейкопения |
Анемия, лейкопения |
|
Нарушения со стороны обмена веществ и питания |
||
|
Часто |
Синдром лизиса опухоли, гиперурикемия |
Синдром лизиса опухоли |
|
Иногда |
Гиперурикемия |
|
|
Нарушения со стороны сердца |
||
|
Часто |
Фибрилляция предсердий |
|
|
Иногда |
Фибрилляция предсердий |
|
|
Нарушения со стороны сосудов |
||
|
Часто |
Повышенное артериальное давление |
Повышенное артериальное давление |
|
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения |
||
|
Часто |
Кашель |
|
|
Нарушения со стороны желудочно-кишечного тракта |
||
|
Очень часто |
Диарея |
|
|
Часто |
Запор |
Диарея |
|
Нарушения со стороны кожи и подкожных тканей |
||
|
Часто |
Алопеция |
|
|
Нарушения со стороны скелетно-мышечной и соединительной ткани |
||
|
Часто |
Артралгия, боль в спине, костно-мышечная боль в груди |
|
|
Иногда |
Артралгия, боль в спине, костно-мышечная боль в груди |
|
|
Общие расстройства и нарушения в месте введения |
||
|
Очень часто |
Повышение температуры тела |
|
|
Иногда |
Повышение температуры тела |
|
|
Лабораторные и инструментальные данные |
||
|
Часто |
Снижение уровня лейкоцитов‡, снижение числа нейтрофилов, снижение веса |
Снижение уровня лейкоцитов‡, снижение числа нейтрофилов |
|
Травмы, отравления и осложнения процедур |
||
|
Очень часто |
Инфузионные реакции |
Инфузионные реакции |
* Все степени или степени 3-5
† Между исследуемыми группами не наблюдалось разницы ≥2% в частоте развития нежелательных реакций степени 5
‡ Разница ≥2% в частоте возникновения явления между исследуемыми группами наблюдалась на Стадии 1, но обновленные данные для Стадии 1 и Стадии 2 не показали такой разницы.
Инфузионные реакции
Частота инфузионных реакций в группе «Газива+хлорамбуцил» была выше, чем в группе «ритуксимаб+хлорамбуцил». У 65% пациентов наблюдались инфузионные реакции после введения первой дозы препарата (у 20% пациентов были реакции 3-5 степени, летальных исходов не отмечено). В целом, только у 7% пациентов наблюдались инфузионные реакции, ставшие причиной прекращения терапии препаратом Газива. Частота развития инфузионных реакций при последующих инфузиях составила 3% для второй дозы в 1000 мг и 1% для последующих доз. После первого цикла терапии инфузионных реакций степеней 3-5 не наблюдалось.
Наиболее распространенными симптомами инфузионных реакций являлись тошнота, озноб, пониженное артериальное давление, повышение температуры тела, рвота, одышка, покраснение, повышение артериального давления, головная боль, тахикардия и диарея. Также сообщалось о симптомах со стороны сердца и органов дыхания, включая бронхоспазм, раздражение дыхательных путей, свистящее дыхание, отек гортани и фибрилляцию предсердий.
Нейтропения и инфекции
Частота возникновения нейтропении в группе «Газива+хлорамбуцил» была выше, чем в группе «ритуксимаб+хлорамбуцил»; нейтропения разрешалась спонтанным образом или благодаря использованию гранулоцитарных колониестимулирующих факторов. Частота развития инфекций составила 38% в группе «Газива+хлорамбуцил» и 37% в группе «ритуксимаб+хлорамбуцил» (явления степеней 3-5 имели место у 12% и 14% пациентов, соответственно; летальные исходы зафиксированы менее чем в 1% случаев в каждой группе). Также сообщалось о случаях продолжительной нейтропении (2% в группе «Газива+хлорамбуцил» и 4% в группе «ритуксимаб+хлорамбуцил») и отсроченной нейтропении (16% в группе «Газива+хлорамбуцил» и 12% в группе «ритуксимаб+хлорамбуцил»).
Тромбоцитопения
Частота возникновения тромоцитопении в группе «Газива+хлорамбуцил» была выше, чем в группе «ритуксимаб+хлорамбуцил», особенно во время первого цикла терапии. У 4% пациентов, получавших Газива в комбинации с хлорамбуцилом, наблюдалась острая тромбоцитопения (возникавшая в течение 24 часов после инфузии). Общая частота геморрагических явлений в обеих группах была сравнимой, также как и число летальных исходов; однако все случаи в группе препарата Газива имели место в течение первого цикла терапии. Однозначная связь между тромбоцитопенией и кровотечениями не была установлена.
Особые категории пациентов
Пожилые люди
В базовом исследовании 46% (156 из 336) пациентов с ХЛЛ, получавших препарат Газива в комбинации с хлорамбуцилом, были в возрасте 75 лет и старше (средний возраст 74 года). У этих пациентов чаще имели место серьезные нежелательные явления, приводившие к летальному исходу, по сравнению с пациентами в возрасте до 75 лет.
Почечная недостаточность
В базовом исследовании у 27% (90 из 336) пациентов с ХЛЛ, получавших препарат Газива в комбинации с хлорамбуцилом, имелась почечная недостаточность средней степени тяжести (клиренс креатинина <50 мл/мин). У этих пациентов чаще имели место серьезные нежелательные явления, приводившие к летальному исходу, по сравнению с пациентами с клиренсом креатинина ≥50 мл/мин.
Дополнительная информация о безопасности, полученная в клинических исследованиях
Прогрессирующая многоочаговая лейкоэнцефалопатия (ПМЛ)
Сообщалось о случаях ПМЛ у пациентов, получавших препарат Газива.
Реактивация гепатита В
Сообщалось о случаях реактивации гепатита В у пациентов, получавших препарат Газива.
Ухудшение предшествующих нарушений со стороны сердца
Сообщалось о случаях аритмии (фибрилляция предсердий, тахиаритмия), стенокардии, острого коронарного синдрома, инфаркта миокарда и сердечной недостаточности у пациентов, получавших препарат Газива. Эти явления могут возникать на фоне инфузионных реакций и приводить к летальному исходу.
Отклонения лабораторных показателей
Сообщалось о случаях транзиторных повышений уровней печеночных ферментов (аспартатаминотрансферазы (АСТ), аланинаминотрансферазы (АЛТ), щелочной фосфатазы), наблюдаемых сразу после первой инфузии препарата Газива.
Противопоказания
-
повышенная чувствительность к активному веществу или любому вспомогательному веществу
Лекарственные взаимодействия
Исследования взаимодействия препарата Газива с другими лекарственными средствами не проводились.
Обинутузумаб не является субстратом, ингибитором или индуктором цитохрома P450 (CYP450), ферментов и клеток-транспортеров уридинфосфат-глюкуронилтрансферазы (УГТ), таких как P-гликопротеин. Поэтому фармакокинетическое взаимодействие с препаратами, метаболизируемыми данными ферментными системами, маловероятно.
Во время терапии, а также до полного восстановления уровня В-клеток, не рекомендуется проводить вакцинацию живыми вирусными вакцинами, принимая во внимание иммуноподавляющее действие обинутузумаба.
Комбинированное использование обинутузумаба и хлорамбуцила может усиливать выраженность нейтропении.
Особые указания
В целях повышения качества отслеживаемости применения биологических лекарственных средств, торговое название назначаемого препарата должно быть надлежащим образом записано в истории болезни пациента.
Инфузионные реакции
Наиболее часто наблюдаемые нежелательными реакциями (НР) на препарат Газива являлись инфузионные реакции, которые в большинстве случаев возникали при введении первых 1000 мг препарата. У пациентов, получавших комбинированную профилактику инфузионных реакций (глюкокортикостероиды, пероральные анальгетики/антигистаминные средства, прерывание приема гипотензивных препаратов утром перед первой инфузией, введение первой дозы в течение 2 дней), наблюдалось снижение частоты развития инфузионных реакций всех степеней тяжести. Частота развития инфузионных реакций 3-4 степени (данные основаны на анализе относительно небольшого числа пациентов) была одинаковой до и после проведения профилактических мер. Частота и степень тяжести симптомов инфузионных реакций существенно снижались после введения первых 1000 мг препарата и при последующем ввеении препарата инфузионных реакций у большинства пациентов не наблюдалось.
У большинства пациентов инфузионные реакции были слабыми или умеренно выраженными и проходили при снижении скорости введения или временном приостановлении первой инфузии, хотя также имели место случаи тяжелых и опасных для жизни реакций, которые требовали проведения симптоматического лечения. С клинической точки зрения инфузионные реакции могут быть трудно отличимы от аллергических реакций, вызываемых иммуноглобулином Е (IgE) (например, анафилаксии). Пациенты с высокой опухолевой нагрузкой (число лимфоцитов в периферическом кровотоке > 25х109/л) имеют повышенный риск развития тяжелых инфузионных реакций. Более высокому риску развития инфузионных реакций, включая тяжелые реакции, подвержены пациенты с почечной недостаточностью (клиренс креатинина < 50 мл/мин) и пациенты, одновременно имеющие балл суммарной оценки тяжести заболевания (CIRS) > 6 и клиренс креатинина < 70 мл/мин.
В связи с применением препарата Газива также сообщалось о случаях развития синдрома высвобождения цитокинов.
Если у пациента наблюдается инфузионная реакция, лечение проводится исходя из степени ее тяжести. В случае реакций 4-й степени инфузию останавливают и терапию препаратом полностью прекращают. При развитии инфузионных реакций 3-й степени тяжести инфузию можно временно приостановить и провести медикаментозное лечение симптомов. В случае реакций 1-й и 2-й степени скорость инфузии снижают и проводят симптоматическую терапию. После регрессии симптомов инфузию возобновляют (за исключением инфузионных реакций 4-й степени) со скоростью, составляющей не более 50% от первоначальной, и, в случае отсутствия у пациентов аналогичных нежелательных явлений той же степени тяжести, можно постепенно повышать скорость инфузии в соответствии с рекомендациями, указанными выше. Если пациент плохо перенес предыдущую скорость введения препарата, следует придерживаться инструкции по проведению инфузий для 1-го и 2-го дня 1-го цикла терапии (см. Таблицу 3).
Терапию препаратом Газива необходимо прекратить в случае развития:
-
острых, угрожающих жизни симптомов со стороны дыхательных путей
-
инфузионных реакций 4-й степени (т.е. опасных для жизни)
-
повторного развития инфузионной реакции 3-й степени (после возобновления первой инфузии или во время последующих инфузий).
Пациенты с уже существующими нарушениями со стороны сердца или легких должны подвергаться тщательному наблюдению в течение всей инфузии и после нее. Внутривенные инфузии препарата Газива могут приводить к понижению артериального давления. Поэтому следует рассмотреть возможность прекращения использования гипотензивных средств за 12 часов до начала инфузии и во время ее проведения, а также в течение 1 часа после введения препарата. В отношении пациентов с высоким риском развития гипертонического криза следует провести оценку соотношения рисков и пользы от временного прекращения приема гипотензивных средств.
Реакции гиперчувствительности, включая анафилаксию
У пациентов, получавших препарат Газива, наблюдались случаи развития анафилаксии. Реакции гиперчувствительности могут быть схожи с инфузионными реакциями. Если при проведении инфузии возникает подозрение на развитие реакции гиперчувствительности (симптомы обычно возникают после предыдущей инфузии и очень редко во время первой инфузии), инфузию следует остановить и полностью прекратить терапию препаратом. Препарат Газива нельзя назначать пациентам с известной гиперчувствительностью к IgE.
Синдром лизиса опухоли (СЛО)
Сообщалось о случаях синдрома лизиса опухоли (СЛО) у пациентов, получавших препарат Газива. Пациентам, входящие в группу повышенного риска развития СЛО (например, пациенты с высокой опухолевой нагрузкой или высоким количеством лимфоцитов в кровотоке [> 25х109/л]), необходимо назначить профилактическое медикаментозное лечение урикостатическими средствами (например, аллопуринолом), а также провести гидратацию за 12-24 часа до проведения инфузии. Лечение СЛО включает в себя коррекцию электролитных нарушений, мониторинг функции почек и водного баланса, проведение поддерживающей терапии (включая диализ).
Нейтропения
В ряде случаев терапия препаратом Газива была связана с развитием нейтропении тяжелой и опасной для жизни формы, включая фебрильную нейтропению. Пациенты с нейтропенией должны проходить тщательное наблюдение с регулярным контролем лабораторных показателей вплоть до разрешения симптомов. При необходимости в лечении, оно должно проводиться согласно национальным клиническим рекомендациям; следует рассмотреть возможность применения гранулоцитарных колониестимулирующих факторов. При любом проявлении сопутствующей инфекции необходимо назначить соответствующее лечение. В случае развития нейтропении тяжелой и опасной для жизни степени возможна временная приостановка терапии. Настоятельно рекомендуется, чтобы пациенты с тяжелой и продолжительной (более 1 недели) нейтропенией получали профилактику противомикробными препаратами на протяжении всего курса лечения вплоть до снижения выраженности нейтропении до 1-й или 2-й степени. Также следует рассмотреть возможность проведения терапии противовирусными и противогрибковыми препаратами. Также сообщалось о случаях отсроченной нейтропении (через 28 дней после завершения терапии) и продолжительной нейтропении (длившейся более 28 дней после завершения/прекращения терапии). Пациенты с почечной недостаточностью (клиренс креатинина <50 мл/мин) в большей степени подвержены риску развития нейтропении.
Тромбоцитопения
Применение препарата Газива было связано со случаями тяжелой и опасной для жизни тромбоцитопении, включая острую тромбоцитопению (возникающую в течение 24 часов после проведения инфузии). Пациенты с почечной недостаточностью (клиренс креатинина <50 мл/мин) в большей степени подвержены риску развития тромбоцитопении. Также сообщалось о кровотечениях с летальным исходом, имевших место во время 1-го курса терапии препаратом Газива. Однозначная связь между тромбоцитопенией и кровотечениями не была установлена.
Необходимо тщательное наблюдение за пациентами на предмет развития тромбоцитопении, особенно в течение первого цикла терапии; вплоть до полного разрешения симптомов следует проводить регулярный контроль лабораторных показателей, а в случае тяжелой или угрожающей жизни пациента тромбоцитопении следует рассмотреть возможность временной приостановки лечения. Лечащий врач может принять решение о проведении переливания препаратов крови (т.е. тромбоцитов). Также следует принимать во внимание использование сопутствующих препаратов, которые потенциально могут усугубить реакции, связанные с тромбоцитопенией (например, ингибиторы агрегации тромбоцитов и антикоагулянты), особенно в течение первого курса терапии.
Ухудшение предшествующих нарушений со стороны сердца
У пациентов с уже существующими сердечными заболеваниями терапия препаратом Газива в ряде случаев приводила к развитию аритмии (фибрилляция предсердий и тахиаритмия), стенокардии, острому коронарному синдрому, инфаркту миокарда и сердечной недостаточности. Эти явления могут быть частью инфузионной реакции и приводить к летальному исходу. Поэтому необходим тщательный контроль за пациентами, имеющими в анамнезе заболевания сердца. Кроме этого, следует подходить с осторожностью к проведению гидратации у таких пациентов для того, чтобы не допустить развитие гиперволемии.
Инфекции
Терапию препаратом Газива нельзя проводить при наличии активного инфекционного процесса. Необходимо с осторожностью подходить к применению препарата для лечения пациентов с рецидивирующими или хроническими инфекциями в анамнезе. Во время и после терапии препаратом Газива могут возникать серьезные бактериальные, грибковые, а также новые или реактивированные вирусные инфекции. Сообщалось о случаях инфекций с летальным исходом. Пациенты с баллом CIRS >6 и клиренсом креатинина <70 мл/мин в большей степени подвержены риску развития инфекций, включая тяжелые формы инфекций.
Реактивация гепатита B
У пациентов, получающих антитела против белка CD20, включая Газива, может происходить реактивация вируса гепатита B, которая в ряде случаев приводит к развитию молниеносного (фульминантного) гепатита, печеночной недостаточности и летальному исходу. Перед началом терапии препаратом Газива все пациенты должны проходить скрининг на наличие вируса гепатита В. Как минимум, такой скрининг должен включать оценку статуса поверхностного антигена гепатита В (HBsAg) и статуса антител к ядерному антигену вируса гепатита B (HBcAb). Кроме этого, обследование может включать в себя использование других биомаркеров. Препарат нельзя назначать пациентам с активной формой гепатита В. Пациентам с положительными серологическими маркерами гепатита В следует проконсультироваться с врачом-гепатологом перед назначением препарата. В отношении таких пациентов необходимо проводить соответствующий мониторинг и принимать меры по профилактике реактивации вируса гепатита в соответствии с локальными стандартами.
Прогрессирующая многоочаговая лейкоэнцефалопатия (ПМЛ)
У пациентов, получавших лечение препаратом Газива, имели место случаи развития прогрессирующей многоочаговой лейкоэнцефалопатии (ПМЛ). Диагноз ПМЛ должен рассматриваться в качестве возможного у всех пациентов с рецидивом или изменениями существующих неврологических проявлений. Симптомы ПМЛ имеют неспецифический характер и могут различаться в зависимости от локализации пораженного участка головного мозга. Часто наблюдаются двигательные симптомы с поражением корково-спинномозгового пути (мышечная слабость, паралич и нарушения органов чувств), некорректная работа органов чувств, мозжечковые нарушения, дефекты поля зрения. Могут иметь место нарушения высших корковых функций (афазия, пространственная дезориентация). Обследование на предмет наличия ПМЛ включает в себя, помимо прочего, консультацию невролога, МРТ головного мозга, люмбальную пункцию (анализ спинномозговой жидкости на наличие ДНК вируса Джона Каннингема). В период проведения обследования на предмет наличия ПМЛ терапия препаратом Газива должна быть приостановлена и полностью прекращена в случае подтверждения ПМЛ. Также следует рассмотреть возможность прекращения или снижения доз сопутствующей химиотерапии или терапии иммунодепрессантами. Для обследования на предмет наличия ПМЛ и последующего лечения ПМЛ пациент должен быть направлен к неврологу.
Иммунизация
Безопасность иммунизации живыми или ослабленными вирусными вакцинами после терапии препаратом Газива не исследовалась, поэтому вакцинация живыми вирусными вакцинами в ходе лечения и вплоть до полного восстановления пула В-клеток не рекомендована.
Воздействие обинутузумаба на плод и вакцинация новорожденных живыми вирусными вакцинами
Учитывая возможное снижение числа пула В-клеток у новорожденных в результате воздействия обинутузумаба во время беременности, необходимо контролировать уровень В-клеток у новорожденных, а вакцинация должна быть отложена до восстановления нормального уровня пула В-клеток.
Беременность
Исследование репродуктивной функции у яванских макак не обнаружило признаков эмбриофетальной токсичности или тератогенных эффектов, но показало полное исчезновение В-лимфоцитов у потомства. Через 6 месяцев уровни В-клеток вернулись к нормальным значениям, и иммунологическая функция полностью восстановилась. Сывороточные концентрации обинутузумаба у потомства были сравнимы с концентрациями, наблюдаемыми у матерей через 38 дней после родов, что указывает на проникновение обинитузумаба через плаценту.
Данные относительно использования обинутузумаба беременными женщинами отсутствуют. Препарат Газива не рекомендован к применению беременными женщинами кроме случаев, когда возможная польза от терапии превышает потенциальный риск.
Грудное вскармливание
Исследования на животных показали, что обинутузумаб проникает в грудное молоко.
Так как человеческий иммуноглобулин G (IgG) проникает в грудное молоко, и возможная степень абсорбции и вреда для здоровья ребенка неизвестна, женщинами рекомендуется прекратить грудное вскармливание во время получения терапии препаратом Газива и в течение 18 месяцев после ее завершения.
Особенности влияния лекарственного средства на способность управлять транспортным средством или потенциально опасными механизмами
Препарат не оказывает или оказывает крайне незначительное влияние на способность к управлению автомобилем и работе с механизмами. Во время проведения первой инфузии препарата очень часто возникают инфузионные реакции и пациентам, имеющим симптомы, обусловленные такими реакциями, рекомендуется воздержаться от управления автомобилем или работы с механизмами.
Передозировка
Симптомы: в клинических исследованиях препарата Газива, в которых применялись дозы от 50 мг до 2000 мг на одну инфузию, случаев передозировки зарегистрировано не было. Частота возникновения и выраженность нежелательных реакций, наблюдавшихся в клинических исследованиях, не являются дозозависимыми.
Лечение: в случае передозировки необходимо немедленно остановить инфузию или снизить скорость введения препарата и осуществлять тщательное наблюдение за пациентом.
Следует рассмотреть возможность регулярного мониторинга показателей общего анализа крови и контроля на предмет повышенного риска развития инфекций в случае снижения уровня В-клеток.
Форма выпуска и упаковка
По 40 мл помещают во флаконы бесцветного стекла типа I вместимостью 50 мл, укупоренные резиновыми пробками с покрытием из фтористого полимера и алюминиевыми колпачками с пластиковыми крышками «flip-off».
По 1 флакону вместе с инструкцией по медицинскому применению на государственном и русском языках помещают в пачку из картона
Условия хранения
При температуре от 2 °С до 8 °С, в оригинальной упаковке для защиты от света. Не замораживать. Не встряхивать.
Хранить в недоступном для детей месте!
Срок хранения
3 года
Не применять по истечении срока годности, указанного на упаковке
Условия отпуска из аптек
По рецепту
Производитель
Рош Диагностикс ГмбХ, Германия
Sandhofer Strasse 116, D-68305 Mannheim, Germany
Владелец регистрационного удостоверения
Ф. Хоффманн-Ля Рош Лтд, Швейцария
Упаковщик
Ф. Хоффманн-Ля Рош Лтд, Швейцария
Адрес организации, принимающей на территории Республики Казахстан претензии от потребителей по качеству товара:
ТОО «Рош Казахстан»
050000, г.Алматы, ул. Кунаева, 77
Бизнес-центр «Park View Office Tower», 15 этаж
Тел.: +7 (727) 321 24 24
Факс: + 7 (727) 321 24 25
e-mail: kz.safety@roche.com, kz.quality@roche.com
Gazyvaro -EMEA/H/C/002799 -II/0003
6
, SmPC (last updated 17.08.2015)
| 239494201477976321_ru.doc | 194.5 кб |
| 001730941477977564_kz.doc | 258 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники
Товары из категории — Препараты для лечения онкологических заболеваний
Инструкция по применению
Цена в интернет-аптеке WER.RU: от 17 000
Немного фактов
Онкологические заболевания на данном этапе развития медицины являются одной из самых патологий. Сколько ко бы не разрабатывалось новых средств, люди все равно гибнут от данной болезни. Многим пациентам сложно даются длительные, изнурительные курсы лечения химиопрепаратами. Среди новообразований агрессивнее других себя ведут опухоли кровеносной и лимфатической системы. Препарат Газива разработан с для борьбы с лейкозами и лимфома. Благодаря своему составу, он способен прерывать патогенез и дальнейшее развитие патологического процесса. Специфичность активного компонента Газивы обуславливает эффективность лекарственного средства при хроническом лимфолейкозе и фолликулярной лимфоме.
Фармакодинамика
Главным компонентом лекарственного средства является обинутузумаб. Он относится к моноклональным антителам из класса иммуноглобулинов G. Терапевтический эффект достигается за счет сродства антитела к антигену, который находится на поверхности В-лимфоцитов и к другим иммунокомпетентным клеткам. В итоге взаимодействия комплекса антиген-антитело запускается система фагоцитоза и атипичные клетки погибают. Уничтожаются измененные и нормальные В-лимфоциты, это обуславливает возникновение побочных эффектов и снижение иммунитета пациента. Еще один механизм уничтожения опухолевых агентов представлен антигензависимой клеточной цитотоксичностью, в ходе которой клетки-мишени, помеченные иммуноглобулином G, погибают от эффекторных клеток с определенными рецепторами. Для синтеза обинутузумаба применяется механизм гликоинженеринга, поэтому его свойства во много раз сильнее, чем у его физиологических аналогов.
Применение лекарственного средства при лечении онкологических процессов позволяет замедлить развитие заболевания.
Фармакокинетика
В ходе ряда исследований выявлены данные, утверждающие о том, что распределение вещества ограничивается плазмой и межтканевой жидкостью. Биотрансформация антител происходит за счет катаболизма. В основном преобладает нелинейный путь клиренса, но при длительном использование фармакокинетика вещества растет и клиренс идет по линейному пути. Анализ результатов курса терапии у пожилых людей не выявил зависимости метаболизм компонентов Газивы от возраста. В отношении детей данное исследование не проводилось и информация отсутствует. Также анализ не проводился у людей с тяжелыми нарушениями в работе печени.
Состав препарата
Противовирусное средство Газива состоит из активного компонента (обинутузумаба) и вспомогательных веществ (аминокислоты, углеводы, вода для инъекций). Выпускается в форме концентрата для приготовления раствора, вводится с помощью инфузионной системы.
Показания к использованию
Применение лекарственного средства Газива целесообразно при неходжкинской лимфоме. Также же назначается пациентам с ранее нелеченным хроническим лимфолейкозом в комбинации с другими медикаментами, в случае непереносимости другой терапии. Эффективно использование при фолликулярной лимфоме, которая прогрессировала после приема других противоопухолевых лекарств.
Побочные эффекты
Препарат Газива может вызвать стойкую нейропению на фоне которой быстро развитие суперинфекция. Рекомендуется постоянный контроль показателей лейкоцитарной формулы. Пациентам целесообразно назначать профилактику антибактериальными, противовирусными и противомикозными лекарственными средствами.
Также существует риск развития тяжелой формы тромбоцитопении. Не рекомендуется совместный прием средства с антикоагулянтами и другими лекарствами, влияющими на свертывающую систему крови.
Возможно возникновение инфузионных реакций, что связано с масштабным высвобождением цитокинов. Существует ряд мер для предотвращения подобных осложнений. Необходимо назначить пациенту медикамент из группы глюкокортикостероидов, анальгетик и антипиретик. Обычно реакция возникает после первой инфузии, при легких проявлениях ее замедляют и устраняют симптомы. Средняя степень тяжести требует временной остановки инфузии и проведения тщательной симптоматической терапии. В тяжелых случая средство пациенту больше не вводится.
Еще одним осложнением может быть синдром лизиса опухоли. Профилактика заключается в контроле концентрации мочевой кислоты и назначении урикостатиков. Также необходимо следить за уровнем гидратации и при снижении восполнять его. Существенны также риски реактивации вирусного гепатита и прогрессирования заболеваний сердечно-сосудистой системы.
В связи с гиперчувствительностью пациента к компонентам средства могут возникнуть анафилактические реакции. При малейших проявлениях которой необходимо прекратить инфузионную терапию.
Противопоказанием является наличие активного инфекционного процесса в организме. Также лекарственное средство не назначают при тяжелой недостаточности почек и повышенной чувствительности к его составляющим.
Беременность и лактация
При приеме средства Газива женщины репродуктивного возраста должны придерживаться мер контрацепции с начала лечения и на протяжении 18 месяцев после последней дозы. При назначении во время беременности необходимо сопоставить возможные риски над пользой, так как у плода может возникнуть лимфоцитопения.
Как известно иммуноглобулины класса G способны проникать в грудное молоко у женщин. С помощью опытов на животных лекарственное средство также было выявлено в молоке. Необходимо прекратить грудное вскармливание на момент терапии и 1,5 года после последнего приема.
Инструкция
Курс терапии следует начать с профилактики таких осложнений как инфузионная реакция, синдром лизиса опухоли.
Инструкция по применению
Препарат следует вводить внутривенно капельно. Во время манипуляции должен быть доступ к средствам экстренной медицинской помощи. Средство Газива разводится специально обученным медперсоналом, в качестве растворителя применяют раствор натрия хлорида. Разработаны специальные циклы с точными дозами и днями инъекций. Интервал между инфузиями не должен нарушаться. Коррекция дозировка проводиться при появлении нежелательных реакций. В случае развития тяжелых осложнений введение лекарственного средства прекращается.
Особенности приема
В общем анализе крови следует контролировать уровень лимфоцитов, при снижении которого возрастает риск развития инфекционного процесса. Весь период терапии должен быть под контролем опытного в этой сфере специалиста. Не применяется в педиатрической практике из-за отсутствия необходимой информации об эффективности и безопасности средства для детского организма.
Нет данных о воздействии лекарства на способности управлять транспортным средством. При появлении побочных реакций не рекомендуется садится за руль до исчезновения всех симптомов.
Совместимость с алкоголем
Существует ряд весомых причин для отказа от употребления спиртных напитков на время проведения лечения средством Газива. Во-первых, алкоголь обладает высокой токсичностью по отношению к клеткам и поражает их. Это может стать причиной развития неопластического процесса. Во-вторых, терапия моноклональными антителами имеет множество побочных эффектов и при совместном приеме состояние пациента может усугубится. В-третьих, алкоголь может снизить эффективность лекарственного средства.
Взаимодействие с другими лекарствами
Не рекомендуется проводить во время терапии вакцинацию живыми вакцинами. Так как уровень В-лимфоцитов снижен, вместо адекватного ответа иммунной системы может возникнуть воспалительный процесс под действием вируса находящимся в вакцине.
Препарат Газива входит в медикаментозные схемы лечения онкозаболеваний и хорошо совместим с данными препаратами.
Передозировка
При малейших признаках передозировки следует приостановить инфузионную терапию, провести мониторинг жизненных показаний пациента. После стабилизации состояния больного можно продолжить инфузию в меньшем объеме. На время манипуляции необходимо постоянно контролировать инструментальные и лабораторные данные функционирования органов и систем.
Похожие препараты
Существует перечень аналогов Газивы, имеющих сходный терапевтический эффект. Лечение новообразований также можно производить представителем класса моноклональных антител – Авастином. Он показывает хорошие результаты при наличиях метастазов. Еще одно средство из этой группы – Ритуксим, используют при лечении опухолей и гранулематоза. Герцептин – лекарственное средство, активный компонент которого является аналогом иммуноглобулина класса G. Входит в комплексное лечение рака молочной железы на разных этапах заболевания.
Условия продажи
Препарат Газива возможно приобрести в аптечных сетях при наличии соответствующего рецепта от врача. Средство предназначено преимущественно для использования в стационаре медицинского учреждения.
Отзывы пациентов и врачей
По мнению докторов, практика подтверждает эффективность лечения онкологических заболеваний антинеопластическим средством Газива. Результативнее всего курс терапии, направленный на борьбу с хроническим лимфолейкозом. Препарат действует непосредственно на механизм развития новообразований и тормозит их рост. Пациенты, принимающие его при фолликулярной лимфоме, утверждают о существенном улучшении качества жизни и продлении ремиссии. При разумно подобранной дозировке побочные реакции практически отсутствуют.
Правила хранения
Сохранять лекарственное средство необходимо в оригинальной упаковке, изолировать от источников влаги и тепла. Запрещено замораживать. Температурный режим должен составлять от 2 до 8 градусов по Цельсию.
Цены на Газива в Москве
Заберите заказ в в аптеке
WER (г. Москва)
Цена: от 17 000 руб.