Состав
- вода очищенная,
- микрогранулированный хитозан,
- отдушка,
- ионное серебро.
Форма выпуска
Гель для наружного применения 50 г в тубе
Фармакологическое действие
Хитозан эффективно проникает через кожу и активирует в месте нанесения защитные реакции организма, способствует улучшению процессов обмена веществ и кровоснабжения. Кроме того, существенно ускоряет процессы регенерации и ранозаживления, улучшает микроциркуляцию и лимфоотток, выводит продукты клеточного обмена.
Ионное серебро в составе геля придает ему бактерицидные, противогрибковые и противовирусные свойства.
Показание к применению
Гель применяют для заживления ожогов, ран и обморожений, снятия болевых ощущений и ускорения процессов регенерации кожных покровов без образования спаек и рубцов.
Эффективен для заживления ран различного происхождения: механических, химических и термических (в т.ч. солнечных ожогов), а также послеоперационных швов, трофических язв различного генеза и пролежней.
В косметологии применяют для ухода за кожей лица и тела с целью стимуляции регенеративных процессов при угревой сыпи, герпесе, последствиях косметологических инъекций, депиляции, а также в качестве смягчающего средства после нанесения татуировок.
Способы применения и дозы
Нанести гель на поврежденную кожу и растереть легкими массирующими движениями. При открытых ранах обработку следует проводить с аккуратностью, захватывая околораневые поверхности. Образующаяся на месте нанесения газопроницаемая пленка удерживает влагу и предохраняет поврежденный участок от негативных внешних воздействий. Повторять процедуру 2-3 раза в день до полного заживления.
Наносить гель на чистую кожу.
При повышенной сухости кожи после применения геля рекомендуется использовать увлажняющие средства.
Противопоказания
Индивидуальная непереносимость компонентов геля.
Особые указания
Избегать попадания в глаза и на открытые раны.
В случае возникновения аллергических реакций применение геля прекратить.
Условия хранения
При температуре 2-25 °С (рекомендуется хранить в холодильнике при температуре 2-8 °С) в недоступном для детей месте. Предохранять от воздействия прямых солнечных лучей.
Примечание
Косметический продукт — не является лекарственным средством.
- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Федосов П.А.
1
Сливкин А.И.
1
Николаевский В.А.
1
Провоторова С.И.
1
Бузлама А.В.
1
Михайлов Е.В.
2
1 ФГБОУ ВПО «Воронежский государственный университет»
2 ФГБОУ ВПО «Воронежский государственный аграрный университет имени императора Петра I»
В скрининговых исследованиях на модели экспериментальных полнослойных ран изучены ранозаживляющие свойства геля на основе хитозана с таурином и аллантоином в сравнении с препаратами: гель «Солкосерил» и мазь «Левомеколь». Установлено, что гель на основе хитозана, содержащий таурин и аллантоин, оказывает выраженное ранозаживляющее действие, сокращает сроки регенерации на 4 дня, увеличивая скорость заживления ран в 1,5 раза относительно контроля и обеспечивает полную эпителизацию раневого дефекта. Заживление ран после применения геля на основе хитозана с таурином и аллантоином на 9-е сутки происходило более эффективно относительно геля «Солкосерил» и мази «Левомеколь» — на 25,38% и 40,24% (p<0,05) соответственно, без формирования грубой соединительной ткани рубца. По данным гистологических исследований установлено, что разработанный гель ускоряет ремоделирование рубцовой ткани, стимулирует регенераторные процессы и способствует трансформации рубцов в регенераты кожного типа.
хитозан
таурин
аллантоин
гель
заживление ран
1. Абаев Ю.К. Справочник хирурга. Раны и раневая инфекция / Ю.К. Абаев. – Ростов-на-Дону: Феникс, 2006. — 427 с.
2. Марченко Л.Г. Технология мягких лекарственных форм: учебное пособие для вузов / Л.Г. Марченко, А.В. Русак, И.Е. Смехова. – СПб.: СпецЛит, 2004. – 174 с.
3. Миронов А.Н. Руководство по проведению доклинических исследований лекарственных средств / А.Н. Миронов. – М.: Гриф и К, 2012. – 944 с.
4. Оценка эффективности применения инновационных раневых биопокрытий на основе хитозана при лечении ожоговых ран у крыс / Н.В. Островский и др. // Современные перспективы в исследовании хитина и хитозана: матер. одиннадцатой Международ. конф. – Мурманск, 2012. – С. 386–391.
5. Перспективы использования уникального биополимера хитозана при местном лечении ран кожи в хирургии / И.В. Ярема [и др.] // Хирург. – 2008. – № 4. – С. 40–46.
6. Сулейманов С.М. Методы морфологических исследований: метод. пособие / С.М. Сулейманов. – Воронеж: ВНИВИ патологии, фармакологии и терапии, 2012. – 103 с.
7. Экспериментальное исследование влияния хитозансодержащих композиций на ткани пародонта крыс / О.Н. Тумшевиц [и др.] // Сибирское медицинское обозрение. – 2006. – № 4. – С. 60–62.
8. Effect of taurine on wound healing / S. Dinger [et al.] // Amino Acids. – 1996. – Vol. 10. – P. 59–71
9. Profile of wound healing process induced by allantoin // Acta Cir. Bras. – 2010. – Vol. 25, № 5. – P. 460–461.
10. Study of cutaneous wound healing in rats treated with Lactobacillus plantarum on days 1, 3, 7, 14, and 21 / N. M. Heydari [et al.] // African Journal of Pharmacy and Pharmacology. – 2011. – Vol. 5. – P. 2395–2401.
Лечение ран является одной из важнейших проблем современной медицины. Каждый десятый житель России ежегодно подвергается травмам [1]. За последние десятилетия появилось большое количество раневых покрытий, разнообразных по составу действующих веществ, используемых основ или их комбинаций [4]. Среди множества основ особое внимание уделяется природным биополимерам. Так, хитозан, получаемый из панцирей ракообразных, используется в различных лекарственных формах, дает достоверные результаты в хирургии для ускорения очищения ран от мертвых клеток, кроме того, обладает антибактериальным действием и выступает в роли гелеобразующего средства [5]. В комбинации с лекарственными веществами хитозан способен пролонгировать их действие [7]. Использование гелей для местного лечения ран имеет определенные преимущества по сравнению с другими лекарственными формами: это длительный лечебный эффект, высокая биодоступность входящих в состав геля лекарственных веществ, а также возможность локального действия. Гели удобны и просты в применении, хорошо поглощают кожные экскреторные продукты, способствуют росту грануляционной ткани, не пачкают одежду и быстро образуют тонкую пленку на поверхности кожи [2]. Создание комбинации хитозана с другими веществами может способствовать повышению регенерации тканей. Такими веществами могут быть таурин и аллантоин. Таурин (2-аминоэтансульфоновая кислота) – условно незаменимая аминокислота, проявляющая антиоксидантное, мембраностабилизирующее действие, уменьшающая перекисное окисление липидов, стимулирующая репаративные процессы [8]. Аллантоин – низкомолекулярное гетероциклическое соединение, обладающее антиоксидантным, противомикробным, противовоспалительным, кератолитическим, регенераторным действием, что приводит к более быстрому заживлению ран [9]. В результате проведенного анализа литературы и патентного поиска не обнаружено сведений о комбинации геля на основе хитозана с таурином и аллантоином, в связи с чем актуальны и перспективны разработки геля на основе хитозана с таурином и аллантоином (ХТА) и изучение его фармакологического действия.
Цель исследования
Изучить ранозаживляющую активность комбинированного состава геля с хитозаном, таурином и аллантоином в сравнении с зарегистрированными лекарственными препаратами мазь «Левомеколь» и гель «Солкосерил» на модели экспериментальной полнослойной раны.
Материал и методы исследования
Определение влияния разработанного геля, его компонентов по отдельности и лекарственных препаратов мазь «Левомеколь» и гель «Солкосерил» на динамику заживления полнослойных ран выполнено в опытах на 49 половозрелых самцах мышей массой 18–25 г. Исследования были проведены с соблюдением этических принципов экспериментов над животными в соответствии с положением Европейской конвенции о защите позвоночных животных, используемых для экспериментов, и Приказа МЗ РФ от 19.06.2003 № 267. За день до эксперимента на месте предполагаемого нанесения ран у мышей удаляли шерстный покров с помощью депиляционного крема Deep depil (ООО «Флоресан», Россия). Под ингаляционным эфирным наркозом по трафарету с помощью хирургических ножниц с закругленными концами вырезали круглый лоскут кожи площадью 60 мм2 в шейно-затылочной области. Раны оставались открытыми до окончания эксперимента [3]. Мышей разделили на 7 групп по 7 животных в каждой. Первая группа была контрольной, рана оставалась открытой без нанесения геля, заживление раны происходило самостоятельно. Во второй группе на рану наносили мазь «Левомеколь» (ОАО «Нижфарм», Россия). В третьей группе на рану наносили гель «Солкосерил» (Legacy Pharmaceuticals Switzerland GmbH, Швейцария). В четвертой группе на раневую поверхность наносили гель на основе хитозана (Sigma-Aldrich, Япония) в монокомпозиции. В пятой группе животным наносили раствор таурина (ЗАО «Вектон», Россия) на рану. В шестой группе рану орошали раствором аллантоина (Acros Organics, Бельгия). В седьмой группе на рану наносили гель на основе хитозана с таурином и аллантоином. Экспериментальным группам мышей сразу после операции наносили изучаемое средство в дозе 0,2 г и затем ежесуточно в течение 14 дней. Измерение площади раны осуществляли 1 раз в сутки [10]. Об эффективности применения средств судили на основании наблюдений за динамикой процессов заживления ран. Оценивали общее состояние животных, наличие или отсутствие воспалительного процесса. Статистическую обработку данных проводили с использованием пакета прикладных программ «Microcoft Excel» и «Statistica». Достоверность отличий контрольных и экспериментальных результатов оценивали при помощи t-критерия Стьюдента.
Для выявления морфологических особенностей процесса заживления и способности исследуемых препаратов влиять на клеточный состав и качественно-количественное заполнение межклеточного вещества в самих рубцах были проведены гистоморфологические исследования. Для данного исследования на 14-е сутки после нанесения ран животных выводили из эксперимента и проводили забор кожного лоскута с раневой областью. Материал фиксировали в 10%-ном нейтральном растворе формалина (ЗАО «Вектон», Россия), обезвоживали в спиртовых растворах возрастающей концентрации и заливали в парафиновые блоки. Срезы толщиной 4–5 микрон получали на ротационном микротоме «МПС-2» (Точмедприбор, СССР) и окрашивали гематоксилин-эозином [6]. Микрофотографические снимки осуществляли с помощью микроскопа «Биомед-4» (Биомед, Россия), совмещенным с цифровой камерой для микроскопа «DCM510» (Scopetek, Китай) и компьютером.
Результаты исследования и их обсуждение
Результаты проведенных исследований показали, что мыши хорошо переносят применение геля на основе хитозана с таурином и аллантоином. Гель не оказывал раздражающего действия, не вызывал гиперемии и отека кожных покровов и не влиял на двигательную активность подопытных животных. За период наблюдения не было выявлено ни одного случая нагноения раны и осложненного течения раневого процесса у животных. Разработанный гель легко наносился на раны, сорбировал раневые выделения, не высушивая дно раны, останавливал кровотечение. На основании полученных данных были построены динамические кривые изменения площади (S) раны (рис. 1).
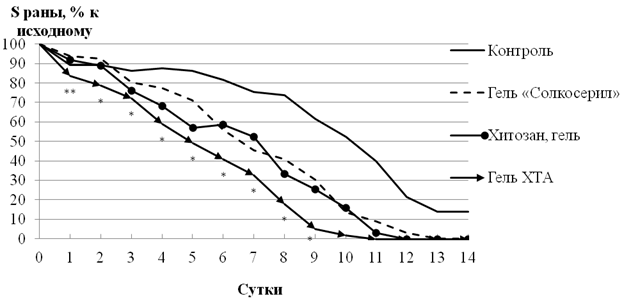
Рис. 1. Динамика изменения площади ран контрольных и леченных животных
(* — P<0,05; ** — P<0,01 – достоверность различий в группе ХТА по сравнению с контролем).
Анализ динамики изменения площади ран показал, что в контрольной группе наблюдалось последовательное уменьшение площади раны на протяжении всего периода наблюдения. Во второй группе применение мази «Левомеколь» достоверно уменьшало площадь раны на 9-е сутки на 16,38% относительно контроля. В третьей группе гель «Солкосерил» сокращал сроки заживления ран на 2 суток, оказывал положительное влияние на уменьшение площади ран на 7-е сутки на 29,93% относительно контроля (p<0,05). В четвертой группе, где раны обрабатывались гелем на основе хитозана, сокращались сроки заживления ран на 3 суток, на 6-е сутки наблюдалось уменьшение площади раны на 22,81% (p<0,05); на 8-е сутки максимальный эффект уменьшения площади ран составил 40,51% относительно контроля. В пятой группе после нанесения раствора таурина на место повреждения наблюдалось уменьшение площади ран на 5-е сутки на 21,07%, на 8-е сутки отмечено уменьшение на 35,75% по сравнению с контролем (p<0,05). В шестой группе животным наносили раствор аллантоина на рану, на 7-е сутки обнаружено ускоренное заживление ран на 25,38% (p<0,05).
Результаты исследования согласуются с известными сведениями о том, что растворы таурина и аллантоина обладают ранозаживляющим действием. В седьмой группе гель ХТА обеспечивает полное заживление ран на 4 дня раньше, чем в контроле, его ранозаживляющее действие проявлялось уже с 1-х суток после нанесения повреждения и характеризовалось уменьшением площади раны на 5,62%. За 7 суток наблюдений площадь раны уменьшилась на 42,60%, к 9-му дню площадь раны уменьшилась на 56,62% относительно контроля (p<0,05). Гель ХТА относительно мази «Левомеколь» сокращал время заживления ран на 4 дня и уменьшал площадь ран на 9-е сутки на 40,24% (p<0,05). Обработка ран гелем ХТА в сравнении с гелем «Солкосерил» ускорила процесс заживления ран на 9-е сутки на 25,38% (p<0,05).
Таблица 1
Периоды полузаживления полнослойных экспериментальных ран
|
Группа животных |
Период полузаживления, сут. |
|
Контроль |
10,43±0,98 |
|
Мазь «Левомеколь» |
8,86±0,38* |
|
Гель «Солкосерил» |
6,57±0,79* |
|
Гель хитозановый |
7,14±0,38* |
|
Раствор таурина |
7,43±0,53* |
|
Раствор аллантоина |
7,29±0,49* |
|
Гель ХТА |
5,43±0,54* |
Примечание: * — P<0,05; ** — P<0,01 – достоверность различий в опытной группе по сравнению с контролем.
Анализ динамики изменения площади ран контрольных и леченных животных позволил определить период полузаживления ран [10]. Полученные данные доказывают, что мазь «Левомеколь», гель «Солкосерил» и гель хитозановый сокращают сроки полузаживления ран на 15,05% и 37,01% и 31,54% (p<0,05) соответственно относительно контроля. Наибольшей активностью обладает гель ХТА, так как он уменьшает время полузаживления ран на 47,94% (p<0,05) относительно нелеченных животных. В сравнении с хитозановым гелем, гелем «Солкосерил» и мазью «Левомеколь» гель ХТА способствовал сокращению периода полузаживления ран на 23,95%, 17,35% и 38,71% (p<0,05) соответственно. На всех этапах течения раневого процесса наибольший эффект проявляется именно в группе ХТА, при этом на 14-й день эксперимента рубец от раны являлся значительно более тонким и менее грубым, чем в контрольной группе.
Анализ гистоморфологических исследований в контрольной группе животных показал, что на 14-й день эпидермис значительно увеличен, клетки всех слоев кожи приобрели атипичные формы и размеры. В шиповатом слое эпидермиса наблюдается вакуолизация клеток. Сосочковый слой дермы сглажен. Кровенаполнение сосудов неравномерное, одни сосуды в спавшемся состоянии, в виде «клеточных тяжей», другие — умеренно полнокровны со слабо выраженной лейкоцитарной инфильтрацией. Рост эпителия происходит по поверхности грануляционной и рыхлой соединительной ткани, которые образуются в ходе регенерации дермы. Клетки грануляционной ткани размножаются вокруг сосудов в виде небольших скоплений. В регенерирующей ткани преобладают пролиферативные процессы, в результате которых образуются очаговые клеточные инфильтраты с разрастанием грануляционной и волокнистой соединительной ткани (рис. 2).
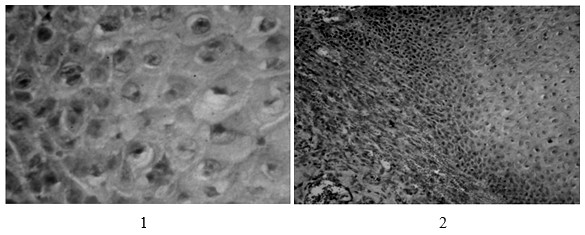
Рис. 2. Микроскопическое строение эпидермиса животных контрольной группы. Окраска гематоксилином и эозином, 1 – ув. × 400; 2 – ув. × 200.
В группе животных, где применяли гель «Солкосерил», раневой дефект замещается коллагеновыми волокнами. Наблюдается отсутствие экссудации и отека, грануляционная ткань заполняет весь дефект. Сразу после образования рубца происходит образование эластических волокон и новой фиброзной сети, в дерме по базальному слою образуется небольшое количество волосяных фолликулов. Роговой слой тонкий. Выявлялись мелкие группы эпителиальных клеток базального слоя в состоянии внутриклеточного отека. Базальные кератиноциты плотно сомкнуты между собой, имеют вытянутую форму, ядра четко очерчены. В фиброзной ткани коллагеновые волокна имеют небольшую извитость. Эластические волокна сформированы по всему объему рубца, ближе к краю регенерата и располагаются вдоль коллагеновых волокон, образуя очень тонкие, едва заметные ответвления (рис. 3).
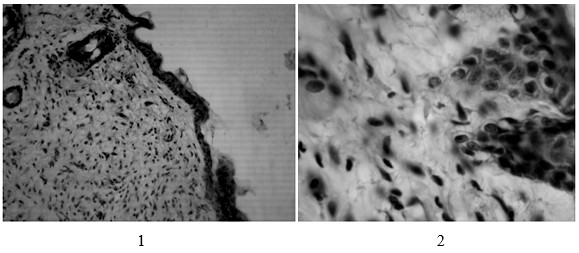
Рис. 3. Эпидермис кожи животных, после воздействия геля «Солкосерил». Окраска гематоксилином и эозином. 1 – ув. × 200; 2 – ув. × 400.
У животных, на раны которых наносили гель ХТА, происходила полная эпителизация области раневого дефекта. Наблюдаются гипертрофия эпителия и выросты базальной мембраны в подлежащую ткань, образована волокнистая соединительная ткань, полностью заполняющая объем раневого дефекта. Под эпителием сформирована рубцовая ткань. При этом происходит разрыхление рубцовой ткани и уменьшение числа сосудов. Преобладание фиброцитов и зрелых фибробластов над другими типами клеток может свидетельствовать об инволюции рубца. Отмечалось уменьшение пролиферативных воспалительных процессов в дерме и отсутствие очагов лейкоцитарной инфильтрации. На периферии бывшей раневой поверхности в дерме наблюдались процессы восстановления наружных эпителиальных влагалищ корней волос и сальных желез. Коллагеновые волокна формируют пучки различной толщины и направлений (рис. 4).
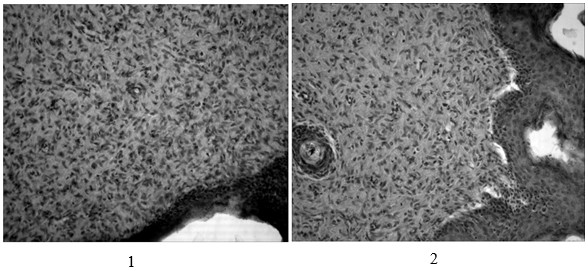
Рис. 4. Эпидермис кожи животных, после воздействия геля на основе хитозана с таурином и аллантоином. Окраска гематоксилином и эозином. 1,2 – ув. × 200;
Выводы
Местное применение геля на основе хитозана с таурином и аллантоином сокращает сроки регенерации на 4 дня и увеличивает скорость заживления ран в 1,5 раза относительно контроля. Заживление ран после применения геля ХТА на 9-е сутки происходило более эффективно относительно геля «Солкосерил» и мази «Левомеколь» на 25,38% и 40,24% (p<0,05) соответственно, без формирования грубой соединительной ткани рубца. По данным гистологических исследований установлено, что наибольшей эффективностью обладает гель ХТА, он ускоряет ремоделирование рубцовой ткани, стимулирует регенераторные процессы и способствует трансформации рубцов в регенераты кожного типа.
Рецензенты:
Булынин В.В., д.м.н., профессор кафедры госпитальной хирургии ГБОУ ВПО Воронежского государственного медицинского университета имени Н.Н. Бурденко Минздрава России, г. Воронеж;
Дьячкова С.Я., д.м.н., профессор кафедры фармакологии ФГБОУ ВПО Воронежского государственного университета, г. Воронеж.
Библиографическая ссылка
Федосов П.А., Сливкин А.И., Николаевский В.А., Провоторова С.И., Бузлама А.В., Михайлов Е.В. ИЗУЧЕНИЕ РАНОЗАЖИВЛЯЮЩЕГО ДЕЙСТВИЯ ГЕЛЯ НА ОСНОВЕ ХИТОЗАНА С ТАУРИНОМ И АЛЛАНТОИНОМ // Современные проблемы науки и образования. – 2015. – № 4.
;
URL: https://science-education.ru/ru/article/view?id=21247 (дата обращения: 19.05.2023).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Камская В.Е.
1
1 Башкирский государственный аграрный университет
В статье приводится информация по использованию хитозана, который представляет собой полидисперсный по молекулярной массе полимер D-глюкозамина содержащий 5-15% ацетамидных групп а также до 1% групп соединенных с аминокислотами и пептидами. Хитозан имеет уникальную биологическую активность, которая может индуцировать устойчивость к вирусным заболеваниям у растений, ингибировать вирусные инфекции у животных и предотвращать развитие фаговых инфекций в зараженной культуре микроорганизмов. Способность хитозана осветлять технологические жидкости используется в производстве соков, пива, вин, молочной сыворотке, промывных вод, фаршевого производства подпрессовых бульонов и других низко концентрированных жидкостей содержащих мелкодисперсные частицы органических соединений различной природы. Положительно заряженный хитозан взаимодействуют с отрицательно заряженной кожей и волосами. На этой биоадизивной способности основано их применение в составе косметических средств. Проявление свойств сорбента и частично эмульгата обусловливает липофильный эффект хитозана. В отличие от растительной клетчатки и других сорбентов природного происхождения, хитозан действует более эффективно благодаря своей уникальной молекулярной структуре. Первичные аминогруппы хитозана либо его комплексов по эффективности связывание ионов тяжелых металлов и радионуклидов в десятки раз превосходят ионообменные смолы. В обзоре приводятся данные по испытанию свойств хитозана в экспериментах с сельскохозяйственными животными, выращиваемыми на загрязнённых кормах. Полученные результаты показали, что хитозан, введённый в рацион животных, питавшихся загрязнёнными кормами, позволил понизить уровень загрязнения молока и мяса подопытных животных.
хитозан
энтеросорбент
профилактика инфекций
продуктивность
1. Авзалов Р.Х. Использование энтеросорбентов в рационах родительского стада уток/ Р.Х. Авзалов, Т.А. Седых, Р.С. Гизатуллин // Вестник Башкирского аграрного университета.- 2015. -№2 (34). — С.24-28. 1
2. Албулов А. И. Хитозан как новый природный энтеросорбент для ветеринарии и животноводства / А.И. Албулов, М.А. Фролова, Ж.Ю. Мурадян // Всероссийский научно-исследовательский и технологический институт биологической промышленности. -2007. — С.6-8 2
3. Андреева А.Е. Использование энтеросорбента приминкор в рационах ремонтного молодняка уток / А.Е. Андреева, Т.А. Седых, Ф.С. Хазиахметов, Р.С. Гизатуллин // Современные проблемы науки и образования. — 2015. — № 2. — С. 751.3
4. Бакаева Л.Н. Биологическая ценность мяса цыплят-бройлеров / Л.Н. Бакаева, Г.М. Топурия // Инновации, экобезопасность, техника и технологии в переработке с.-х. продукции: матер. 2 всерос. науч.-практич. конф. Уфа, 2011. — С. 109.4
5. Бакаева Л.Н. Показатели химического состава цыплят под действием хитинсодержащего препарата / Л.Н. Бакаева, Г.М. Топурия // Актуальные вопросы развития пищевой промышленности: матер. всерос. науч.- практич. конф. Челябинск, 2011. — С. 9-11. 5
6. Бикмиев Д.Р. Рост и развитие молодняка уток при включении в рацион энтеросорбента Приминкор (статья) / Д.Р. Бикмиев, Т.А. Седых // Современные наукоемкие технологии. — 2013. — № 9. — С. 10-11.
7. Братская С.Ю. Коллоидно-имические свойства хитозана / С.Ю. Братская, М.В. Шамов Д.В., Д.В. Червонецкий // Рыбохозяйственная наука на пути в XXI век. Тезисы докладов Всероссийской конференции молодых ученых. – Владивосток: ТИНРО- Центр, 2001. – С. 120–122. 6
8. Быкова, В.М. Сырьевые источники и способы получения хитина и хитозана: Хитин, его строение и свойства / В.М. Быкова, С.В. Немцев // Хитин и хитозан. Получение, свойства и применение. – М.: Наука, 2002. – C 7-10. 7
9. Гальбрайх Л.С. Модифицированные волокнистые и пленочные материалы / Л.С. Гальбрайх // Химические волокна. – 2005. — №5. – С.21-27. 8
10. Гамыгин Е.А. Новые комбикорма для аква- культуры / Журнал «Зооиндустрия» / Гамыгин Е.А., Передня А.А., Шоль А.В. // ВЕТТОРГ-портал: [сайт]. URL: www. vettorg.net/magazines/3/2001/30/84/ (дата обращения: 03.10.2016).9
11. Гладышев Д.Ю. Строение и фракционный состав карбоксиметилового эфира хитозана / Д.Ю. Гладышев и [др.] // Высокомолекулярные соединения. – 1990. – Т.32Б. — №7. – С.503-505. 10
12. Горовой Л.Ф. Сорбционные свойства хитина и его производных: Хитин его строение и свойства / Л.Ф. Горовой В.Н. Косяков // Хитин и хитозан. Получение свойства и применение. – М.: Наука 2002. – C.217-246. 11
13. Гумеров И.Р. Воспроизводительные качества уток при включении в рацион препаратов Микосорб и Приминкор (статья) / И.Р. Гумеров, Т.А. Седых // Современные наукоемкие технологии. — 2013. — № 9. — С. 12.
14. Гумеров И.Р., Воспроизводительные качества уток при включении в рацион препаратов микосорб и приминкор / И.Р. Гумеров, Т.А. Седых // Современные наукоемкие технологии. — 2013. — № 9. — С. 12. 12
15. Злобин, С.В. Оптимизация использования пробиотиков Субтилис в промышленном свиноводстве / С.В. Злобин // Веткорм. — 2008. — №5. – С. 26-27. 13
16. Интенсификация производства мяса уток (монография) / Р.Р. Гадиев, Т.Ф. Саитабаталов, Т.А. Седых / Уфа: Издательство БГАУ, 2009. – 208 с.
17. Кильдеева Н.Р. Получение материалов медицинского назначения из растворов биосовместимых полимеров / Н.Р. Кильдеева Л.С. Гальбрайх Г.А. Вихорева // Химические волокна. – 2005. — №6. – С.21-24. 14
18. Миронов А.В. Получение гранулированного хитозана / А.В. Миронов и [др.] // Химические волокна. – 2005. – №1. – С.26-29. 15
19. Пантюхин А.В. Разработка оптимальной технологии и исследование процесса микрокапсулирования гидрофобных веществ / // М.: Вестник ВГУ. – Серия: Химия, Биология, Фармация. – 2006. – № 2. – С. 338–339. 16
20. Седых Т.А. Мясная продуктивность уток при включении в рацион энтеросорбента Преминкор (статья) / Т.А. Седых // Аграрная наука – основа успешного развития АПК и сохранения экосистем. Материалы Международной научно-практической конференции (31 января – 2 февраля 2012 г.). – Волгоград: Волгоградский ГАУ, 2012. – С. 203-204.
21. Седых Т.А. Продуктивность и естественная резистентность уток при интенсивной технологии выращивания (статья) / Т.А..Седых // Аграрный вестник Урала. — №8. – 2012. – С. 33-37.
22. Система машин и оборудования для реализации инновационных технологий в растениеводстве и животноводстве Республики Башкортостан / под общ. ред. И.И. Габитова, С.Г. Мударисова, Г.П. Юхина, В.Г. Самосюка. – Уфа: Башкирский ГАУ, 2014. – С. 159-187
23. Степнова Е.А. биологически активные амфифильные производные хитозана / Е.А. Степнова и [др] // Химические волокна. – 2005. — №6. – С.57-58. 17
24. Топурия Л.Ю., Топурия Г.М. Эффективность применения хитозана в качестве иммуностимулятора для сельскохозяйственных животных и птиц/ // Ветеринарное дело. 2010. № 1. С. 61-68. 18
25. Шамшурин Д.В. Хроматографические свойства силикагелей модифицированных хитозаном и его производными / Д.В. Шамшурин Е.Н. Шаповалова О.А. Шпигун // Вестник Московского университета. – 2004. – Сер.2. – Химия. – Т.45. — №3. – С.180-185. 19
Хитозан – природный полимер XXI века. Уникальные свойства хитина и хитозана привлекают внимание большого числа специалистов самых разных специальностей. Роль полимеров в нашей жизни является общепризнанной, и все области их применения в быту, промышленном производстве, науке, медицине, культуре трудно даже просто перечислить. Если до XX века человеком использовались полимеры природного происхождения – крахмал, целлюлоза (дерево, хлопок, лен), природные полиамиды (шелк), природные полимерные смолы на основе изопрена – каучук, гуттаперча, то развитие химии органического синтеза в XX веке привело к появлению в различных областях деятельности человека огромного разнообразия полимеров синтетического происхождения – пластмасс, синтетических волокон и т.п. Происшедший технологический прорыв не только кардинально изменил нашу жизнь, но и породил массу проблем, связанных с охраной здоровья человека и защитой окружающей среды.
Поэтому закономерным является большой интерес науки и промышленности к поиску и использованию полимеров природного происхождения, таких как хитин и хитозан. Эти полимеры обладают рядом интереснейших свойств, высокой биологической активностью и совместимостью с тканями человека, животных и растений, не загрязняют окружающую среду, поскольку полностью разрушаются ферментами микроорганизмов, могут широко применяться в проведении природоохранных мероприятий.
В основе получения хитозана лежит реакция отщепления от структурной единицы хитина-N-ацетил-D-глюкозамина ацетильной группировки или реакция деацетилирования. Транс-расположение в элементарном звене макромолекулы хитина заместителей (ацетамидной и гидроксильной групп) у С2 и С3 обусловливает значительную гидролитическую устойчивость ацетамидных групп в том числе и в условиях щелочного гидролиза [18]. Поэтому отщепление ацетамидных групп удается осуществить лишь в сравнительно жестких условиях — при обработке 40-49% -ным водным раствором NaOH при температуре 110-1400С в течение 4-6 часов. Однако и в этих условиях степень деацетилирования (доля отщепившихся ацетамидных групп в расчете на одно элементарное звено) не достигает единицы, то есть не обеспечивается количественное удаление этих групп составляя обычно 0 8-0 9.
Реакция сопровождается одновременным разрывом гликозидных связей полимера т.е. уменьшением молекулярной массы изменением надмолекулярной структуры степени кристалличности и т.д. Таким образом, хитозан представляет собой полидисперсный по молекулярной массе полимер D-глюкозамина содержащий 5-15% ацетамидных групп а также до 1% групп соединенных с аминокислотами и пептидами. Процесс проводят обычно с помощью концентрированных щелочей при повышенных температурах. Первым опытом получения хитозана было сплавление хитина с твердой щелочью при 1800С. Этим способом получали продукт со степенью деацетилирования (СД) 95% но значительно деструктированный (до 20 единиц).
Хитин и хитозан по своему строению близки к целлюлозе — одному из основных волокнообразующих природных полимеров. Естественно поэтому что как и целлюлоза эти полимеры и их производные обладают волокно — и пленкообразующими свойствами [9]. Благодаря биосовместимости с тканями человека низкой токсичности способности усиливать регенеративные процессы при заживлении ран биодеградируемости такие материалы представляют особый интерес для медицины. При лечении гнойных и ожоговых ран широкое применение приобрели ферменты эффективность использования которых может быть повышена за счет их включения в структуру волокон и губок. Такие полимеры как хитин хитозан карбоксиметилхитин благодаря широкому набору функциональных групп обеспечивают возможность образования между полимером-носителем и ферментом связей различной прочности что создает предпосылки для регулирования активности и стабильности фермента скорости его диффузии в рану. В медицине для лечения и профилактики тромбозов используется природный антикоагулянт крови — гепарин по химическому строению являющийся смешанным полисахаридом. Наиболее близкий его структурный аналог — сульфат хитозана также обладает антикоагулянтной активностью возрастающей при увеличении степени сульфатирования. Возможность реализации синергического эффекта (усиления активности гепарина при введении добавок сульфата хитозана) делает это соединение перспективным для создания лекарственных препаратов антикоагулянтного и антисклеротического действия [4,8,13,23].
N- и О-сульфатированные производные частично деацетилированного карбоксиметилхитина не только препятствуют свертыванию крови благодаря селективной адсорбции антитромбина но и резко уменьшают интенсивность деления раковых клеток.
Одной из уникальных биологических активностей хитозана является его способность индуцировать устойчивость к вирусным заболеваниям у растений ингибировать вирусные инфекции у животных и предотвращать развитие фаговых инфекций в зараженной культуре микроорганизмов. Образование комплексов полимерными лигандами с различными металлами находит все более широкое применение в аналитической химии хроматографии биотехнологических процессах. Полимерные комплексообразователи в том числе хитин хитозан и их производные например карбоксиметиловые эфиры могут рассматриваться как реальная альтернатива традиционным методам очистки сточных вод промышленных предприятий от соединений металлов используемых для нанесения защитных покрытий (никель хром цинк) а также от таких металлов как ртуть и кадмий способных аккумулироваться живыми организмами [25]. Наличие электронодонорных амино — и гидроксильных групп широкие возможности введения различных ионогенных групп кислотного и основного характера делают производные хитина и хитозана весьма перспективными для использования в хроматографии при разделении и очистке биологически активных соединений (нуклеиновых кислот и продуктов их гидролиза стероидов аминокислот).
Весьма перспективно использование хитозана в бумажной промышленности: благодаря большей прочности при водных обработках ионных связей образующихся при нанесении хитозана на целлюлозное волокно при формировании бумаги по сравнению с существующими в обычной бумаге водородными связями заметно возрастает прочность бумажного листа особенно в мокром состоянии. При этом одновременно улучшаются и другие важные свойства (сопротивление продавливанию излому стабильность изображения). В последнее время все большее внимание уделяется исследованиям процессов образования изучению свойств и возможностей практического применения особого класса продуктов химических превращений полимеров — интерполимерных комплексов. Эти соединения образующиеся при взаимодействии макромолекул противоположно заряженных полиэлектролитов характеризуются высокой гидрофильностью что позволяет использовать их в качестве эффективных флокулянтов структурообразователей а в виде пленок в качестве полупроницаемых мембран и покрытий в том числе в медицине. Использование в качестве компонента интерполимерного комплекса сравнительно жесткоцепного хитозана способного благодаря наличию ионогенных групп к образованию межмолекулярных ион — ионных и ион — дипольных связей обеспечивает возможность улучшения физико-механических свойств получаемых пленок. Одним из направлений успешного использования таких пленок могут быть первапорационные процессы разделения водно-органических смесей. Так пленка на основе интерполимерного комплекса хитозан — полиакриловая кислота в процессе разделения методом первапорации водно — изопропанольной смеси не уступает по транспортным характеристикам пленкам из традиционных материалов (ацетат целлюлозы поливиниловый спирт) заметно превосходя их по селективности. Благодаря своим уникальным свойствам хитозан нашел применение в пищевой промышленности. Способность хитозана осветлять технологические жидкости используется в производстве соков пива вин молочной сыворотке промывных вод фаршевого производства подпрессовых бульонов и других низкоконцентрированных жидкостей содержащих мелкодисперсные частицы органических соединений различной природы. Проявление свойств сорбента и частично эмульгатора обусловливает липофильный эффект хитозана.
В технологии формованных изделий хитозан используется как структурообразующий агент повышающий значения реологических характеристик пищевых масс. Хитозан обладает редким свойством соединять в упорядоченную структуру фрагменты материалов различного влагосодержания: сухих с промежуточной влажностью и высоковлажных. Бактерицидное действие хитозана позволяет использовать его при хранении различных видов пищевой продукции. Наиболее широко показано защитное действие пленок из хитозана нанесенных на поверхность плодов и овощей — яблок апельсинов земляники томатов перца. Поскольку плоды и овощи остаются живым организмом будучи отделенными от материнского растения они обладают определенным иммунитетом и в них проходят обменные процессы [5,8,12].
Однородные гибкие не дающие трещин хитозановые пленки обладают избирательной проницаемостью подобно другим полимерным покрытиям на поверхности плодов и овощей играют роль микробного фильтра и/или регулируют состав газов у поверхности и в толще тканей влияя тем самым на активность и тип дыхания что в целом способствует продлению сроков хранения растительного сырья. Помимо этого покрытие из хитозана вызывает некоторые морфологические изменения в возбудителях порчи томатов и перца. Пленка хитозана способствующая продлению срока хранения мороженого тунца вероятнее всего играет роль барьера регулирующего проникновение кислорода воздуха и испарение воды. Хитозан присутствуя в составе пищевых продуктов положительно влияет на их биологическую ценность. Кроме того хитозан относится к диетическим волокнам которые не усваиваются организмом человека а в кислой среде желудка образует раствор высокой вязкости. Как компонент пищи или как лечебно профилактический препарат хитозан проявляет свойства энтеросорбента иммуномодулятора антисклеротического и антиартрозного фактора регулятора кислотности желудочного сока ингибитора пепсина и др. [11].
Хитозан отличается от большинства природных и химически синтезированных гелеобразователей применяемых в косметике тем что при биологических значениях рН они имеют положительный заряд т.е. является поликатионом (если рН < б). В этом заключается их преимущество перед полианионными гелеобразователями отрицательно заряженными при биологических значениях рН. Положительно заряженный хитозан взаимодействуют с отрицательно заряженной кожей и волосами. На этой их биоадизивной способности основано их применение в составе косметических средств. Кроме того биосовместимость хитозана с растительными экстрактами и другими компонентами используемыми в качестве полезных добавок и биологически активных ингредиентов открывает перспективы их использования для разработки новых средств для введения активных компонентов в косметические рецептуры. Примером может служить технология создания гранул внутри которых содержатся биологически активные субстанции нестабильные в обычных условиях косметических производств и при хранении готовых изделий.
В настоящее время применение в животноводстве и птицеводстве энтеросорбентов является весьма актуальным направлением, поскольку качеству кормов уделяется большое внимание [10].
С сорбирующими свойствами хитозана связаны многие из вышеперечисленных биологических эффектов. В отличие от растительной клетчатки и других сорбентов природного происхождения, хитозан действует более эффективно благодаря своей уникальной молекулярной структуре. Молекула хитозана содержит большое количество аминогрупп, что позволяет ему связывать ионы водорода и приобретать избыточный положительный заряд [6]. Кроме того, свободные аминогруппы и координационно связанные металлы определяют хелатообразующие (способность образовывать так называемые хелатные комплексы, прочно удерживающие металлы) и комплексообразующие свойства хитозана. Первичные аминогруппы хитозана либо его комплексов по эффективности связывание ионов тяжелых металлов и радионуклидов в десятки раз превосходят ионообменные смолы (Тесленко и др., 1992). Этим объясняют способность хитозана выводить из организма тяжёлые металлы и оказывать радиопротекторное действие за счёт разнообразных химических и электростатических взаимодействий. Свойство хитозана, связывать тяжёлые металлы и радионуклиды, было оценено в экспериментах с сельскохозяйственными животными, выращиваемыми на загрязнённых кормах. Полученные результаты показали, что хитозан, введённый в рацион животных, питавшихся загрязнёнными кормами, позволил понизить уровень загрязнения молока и мяса подопытных животных. Имея мощный положительный заряд молекула хитозана вступают в связь с отрицательно заряженными молекулами жирных кислот непосредственно в пищеварительном тракте – до их усвоения. Иными словами, попадая в организм, хитозан «притягивает» липиды, связывает их, делая недоступными для усвоения, и выводит из организма, препятствую тем самым образованию жировых отложений. Ученые называют хитозан «магнитом для жиров»: одна молекула хитозана способна связать молекул жира в 10-12 раз больше своего веса. Положительный заряд хитозана обеспечивает связывание поступающего с пищей холестерина. Кроме того хитозан” соединяется с желчной кислотой (с помощью которой происходит всасывание холестерина), выводит ее и холестерин пищи с каловыми массами. При этом холестерин крови, а также холестерин, поступающий с пищей, расходуется организмом для синтеза в печени желчной кислоты. Это еще один механизм снижения уровня холестерина при приеме хитозана.
Препараты хитозана в последнее время становятся все более востребованными в ветеринарии и животноводстве. Хитозан в ветеринарии применяется в двух направлениях: наружне в качестве ранозаживляющего и внутренне как энтеросорбент, противовоспалительный и бактериостатический агент, а также возможно его инъекционное введение в составе лекарственных и вакцинных препаратов. Из существующего в настоящее время широкого ассортимента полимерных покрытий на раны и ожоги рассасывающиеся покрытия в наибольшей степени отвечают всем медико-биологическим требованиям. Хитозан и его производные регулируют пролиферацию фибробластов и стимулируют нормальную регенерацию кожи. Болеутоляющее и антимикробное действие хитозана обусловлено его уникальной способностью неспецифически взаимодействовать с болевыми рецепторами и клеточной стенкой микроорганизмов. Одной из причин эффективности хитозана при заживлении ран является его стимулирующее воздействие на иммунную систему: его можно рассматривать как аналог липополисахаридов клеточных стенок микроорганизмов, выполняющих роль активаторов макрофагов. Для лечения желудочно-кишечных заболеваний молодняка сельскохозяйственных животных применяются антибиотики, которые помимо антимикробного обладают иммунодепрессивным действием, а со временем у животных развивается резистентность к ним, и лечебный эффект теряется [24].
Хитозан при применении внутрь обволакивает стенки слизистой кишечника, обладает способностью адсорбировать в желудочно-кишечном тракте токсины и способствует выведению их из организма животных, обладает бактериостатическим действием. Хитозановые препараты позволяют ускорить и удешевить курс лечения, исключить или значительно уменьшить использование антибиотиков и сульфаниламидов, обладающих кумулятивным эффектом. В последние годы учеными различных стран проведен цикл исследований по применению в качестве адъюванта хитозана и его модификатов в составе вакцин против листериоза, псевдомоноза, бруцеллеза, туберкулеза, ящура, гриппа и других инфекций [3]. Известен положительный опыт применения нанохитозана для повышения иммунного ответа при конструировании бруцеллезных вакцин [14]. Полученные результаты в большинстве случаев указывают на перспективность использования хитозана в иммунопрофилактике животных и человека.
Многочисленные научные исследования и производственный опыт свидетельствуют, что полноценная реализация генетического потенциала сельскохозяйственной птицы может быть достигнута за счет широкого использования биологически активных веществ и кормовых добавок природного происхождения [7-22]. С этой целью так же можно применить хитозан, обладающий рядом положительных свойств: иммунобиологической активностью, способностью улучшать обмен веществ, лечебно-профилактическим действием и т.д. [2-19].
Для стимуляции роста и микробиологической активности микроорганизмов- пробиотиков используют пребиотики- вещества приролного или искусственного происхождения. Таким является природный полисахарид хитозан [9].
Хитозан использовали в комплексе с прибиотическими кормовыми добавками «Муцинол» и «Проваген» при откорме телят и поросят. Для достижения поставленной цели, были проведены научно-хозяйственные опыты. За животными ежедневно вели наблюдения, а так же определяли массу тела, упитанность и сохраненность поголовья. В начале научно-хозяйственного опыта животные не имели существенных различий по живой массе, что свидетельствует об идентичности сформированных групп [1].
В результате исследований проведенных в ОАО «Аграрная группа РОСТ», было установлено, что скармливание поросятам опытной группы испытуемых кормовых добавок оказало блогоприятное влияние на клиничесие показатели крови. Комплекс пробиотика «Муцинол» с хитозаном положительно повлиял на белковый обмен поросят опытной группы. Повышение уровня белка в сыворотке крови поросят опытной группы свидетельствует о более интенсивных окислительно-восстановительных процессах в их организме и указывает на усиление белоксинтезирующей функции печени.
В опыте на телятах изучение микробиоценоза толстого кишечника подопытных животных показало, что выпивание в течении 7 суток пробиотика «Проваген» с хитозаном обусловило тенденцию к оптимизации в содержимом толстого кишечника телят уровня типичных эшерихий, кроме того, у животных опытной группы отмечено повышение вылового прироста на 9,59% и среднесуточных приростов живой массы на 9,62 %.
Таким образом, результаты двух научно-хозяйственных опытов свидетельствует об эффективности применения хитозана в комплексе с пробиотическими кормовыми добавками при откорме телят и поросят.
Так же в проведенном исследовании в ООО «Птицефабрикой «Орская» с использованием корма с добавкой хитозана, было выяснено, что он оказал позитивное влияние на массу мышц в тушках утят. Введение в рацион утят хитозана способствовало улучшению биологической ценности мяса [20].
Природный полимер добавляли и в корм козлятам. При выращивании и разведении козлят достаточно часто возникает необходимость предотвращения возникновения желудочно-кишечных заболеваний различной этиологии. Избежать подобных заболеваний, особенно часто проявляющихся в стрессовые периоды выращивания молодняка, предпочтительнее проведением профилактических мероприятий. Одним из них является добавление в рацион животных биологически активных кормовых добавок. В этом направлении определенный интерес представляет хитозан. В силу особенности химической структуры данный полимер способен во влажной среде при определенных значениях рН среды набухать и проявлять абсорбционные свойства. Эти способности в полной мере могут проявляться в кишечнике, хитозан, обволакивая ворсинки стенок, препятствует прикреплению и развитию неблагоприятной микрофлоры.
В Ставропольском НИИ животноводства и кормопроизводства разработана технология получения хитозан-меланинового комплекса (ХМК) из подмора пчёл. На основе ХМК, для усиления его действия при профилактике желудочно-кишечных заболеваний молодняка с.-х. животных и учитывая явление синергизма, разработана рецептура экспериментального препарата, включающего глюкозу, лактозу, пробиотик, витамин С, сухие экстракты трав. Действие полученного в лабораторных условиях хитозан-меланинового комплекса (ХМК) из подмора пчёл и препарата на его основе на молодняк с.-х. животных было исследовано при выпаивании их новорождённым козлятам зааненской породы. Полученные результаты свидетельствуют, что применение ХМК и препарата на его основе способствовало снижению заболеваемости и особенно повышению сохранности козлят. Так, если в опытных группах регистрировалось от 10 до 20% животных с признаками желудочно- кишечных расстройств, то среди козлят контрольной – 40,0%, соответственно профилактическая эффективность колебалась в разных опытных группах от 20,0 до 30,0%.
Лучшая сохранность животных, по-видимому, объясняется повышением защитных сил организма козлят при использовании ХМК и препарата на его основе, о чем свидетельствуют результаты биохимических исследований крови и уровня естественной резистентности. Выявлено, что у животных опытных групп достоверно повышалось содержание гемоглобина, лизоцимная, бактерицидная активность сыворотки крови и фагоцитарная активность нейтрофилов, в среднем соответственно на 11,4; 10,3; 35,4 и 56,3%. Положительным действие ХМК и препарата на его основе отмечали и при анализе динамики живой массы козлят до 2-месячного возраста. В ранний период онтогенеза (до 20 дней) наибольшая разница отмечена между контрольными животными и козлятами II и III групп: на 25,6 и 18,1% . В дальнейшем – в 40 дней и два месяца — животные опытных групп практически не отличались по живой массе между собой, достоверно (Р<0,01) превосходя козлят контрольной в среднем на 30,2 и 32,1%. При этом во все учтенные периоды животные опытных групп отличались от контрольных значительно большими среднесуточными приростами — в среднем на 47,9; 98,2 и 35,6% (Р<0,01)
Таким образом, для профилактики желудочно-кишечных заболеваний, повышения естественной резистентности, сохранности и живой массы козлят целесообразно выпаивание новорождённым козлятам хитозан-меланинового комплекса в дозе 15 мг на 1 кг живой массы и препарата на его основе [17].
В результате выше описанных исследований, можно сказать, что хитозан эффективен в примененении с комплексом пробиотических кормовых добавок при откорме телят и поросят, влияния при вскармливании на клинические показатели крови в состав рациона. Комплекс пробиотика «Муцинол» с хитозаном положительно повлиял на белковый обмен [21]. Так же повышение уровня белка в сыворотке крови поросят свидетельствует о более интенсивных окислительно-восстановительных процессах в их организме и указывает на усиление белоксинтезирующей функции печени. Применение хитозана на сельскохозяйственных животных и птицы оказывает положительное действие на обменные процессы в организме, что способствует увеличению продуктивности.
Библиографическая ссылка
Камская В.Е. ХИТОЗАН: СТРУКТУРА, СВОЙСТВА И ИСПОЛЬЗОВАНИЕ // Научное обозрение. Биологические науки. – 2016. – № 6.
– С. 36-42;
URL: https://science-biology.ru/ru/article/view?id=1020 (дата обращения: 19.05.2023).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Элентра Нутришн Хитозан+Хром (Elentra Nutrition Chitosan+Chromium) инструкция по применению
Описание биологически активной добавки
Элентра Нутришн Хитозан+Хром
(Elentra Nutrition Chitosan+Chromium)
Основано на официально утвержденных материалах и подготовлено для электронного издания справочника Видаль 2023 года, дата обновления: 2023.03.22
Владелец регистрационного удостоверения:
Контакты для обращений:
ГРОТЕКС ООО
(Россия)
Лекарственная форма
| БАД | Элентра Нутришн Хитозан+Хром |
Капс. 500 мг+83 мкг: 90 шт. рег. №: RU.77.99.11.003.R.000070.01.22 |
Форма выпуска, упаковка и состав
продукта Элентра Нутришн Хитозан+Хром
Капсулы массой 740 мг.
Вспомогательные вещества: капсула из гидроксипропилметилцеллюлозы (E464, носитель), целлюлоза микрокристаллическая (E460i, носитель), стеариновая кислота (E570, носитель), кремния диоксид (E551, агент антислеживающий).
90 шт. — флаконы полимерные (1) — пачки картонные.
Свойства
Поступление хитозана и хрома способствует:
- снижению усвоения углеводов и жиров;
- снижению избыточной массы тела;
- детоксикации организма.
Область применения
продукта Элентра Нутришн Хитозан+Хром
- в качестве биологически активной добавки к пище — источника хитозана, дополнительного источника хрома.
Рекомендации по применению
Принимают внутрь, во время еды.
Взрослым по 3 капс./сут. Следует принимать как минимум за 2-3 ч до или после приема жирорастворимых витаминов (A, D, E, K) или лекарств.
Продолжительность приема — 1 месяц. При необходимости прием можно повторить в течение года.
Противопоказания
- индивидуальная непереносимость компонентов БАД;
- беременность;
- период грудного вскармливания.
Применение при беременности и в период лактации
Противопоказано применение при беременности и в период грудного вскармливания.
Особые указания
Биологически активная добавка к пище, не является лекарственным средством.
Перед применением рекомендуется проконсультироваться с врачом.
Условия реализации
Места реализации определяются национальным законодательством государств-членов Евразийского экономического союза.
Условия хранения продукта Элентра Нутришн Хитозан+Хром
Продукт следует хранить в сухом, защищенном от прямых солнечных лучей, недоступном для детей месте, при температуре не выше 25°С.
Срок годности продукта Элентра Нутришн Хитозан+Хром
ГРОТЕКС ООО
(Россия)

|
|
195279 Санкт-Петербург, Индустриальный пр-т, |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код

