Диагностические лаборатории медицинских организаций, как правило, осуществляют работы с патогенными биологическими агентами (ПБА) III–IV групп патогенности. Чтобы обеспечить в лаборатории требования биологической безопасности, необходимо предусмотреть поточность технологических процессов, зонирование производственных помещений, своевременное проведение дезинфекционных мероприятий. Расскажем о том, как это сделать.
ПБА — это патогенные для человека микроорганизмами и гельминты, а также любые объекты и биологические материалы, подозрительные на их содержание. Классификация микроорганизмов по группам патогенности представлена в СП 1.3.2322-08 «Безопасность работы с микроорганизмами III–IV групп патогенности (опасности) и возбудителями паразитарных болезней».
Зонирование лаборатории
Лаборатория должна иметь 2 входа: один — для персонала, второй — для приема биологического материала на исследования. На входных дверях должно быть обозначено название лаборатории и размещен международный знак «Биологическая опасность».
Производственные помещения лаборатории разделяют на «заразную» и «чистую» зоны (см. схему). В «заразной» зоне выполняют любые виды работ с микроорганизмами и биологическим материалом. «Чистая» зона предназначена для тех видов деятельности, при которых невозможен контакт с патогенными биологическими агентами.
На границе «чистой» и «заразной» зон лаборатории целесообразно предусмотреть санитарный пропускник.
Рабочие столы, стеллажи, оборудование в «заразной» зоне маркируют с помощью международного знака «Биологическая опасность». Помещения «заразной» зоны оборудуют бактерицидными облучателями.
Обратите внимание!
Выносить за пределы лаборатории оборудование, лабораторную или хозяйственную посуду, реактивы, инструменты и прочие объекты можно только после их дезинфекции и с разрешения руководителя лаборатории.
Требования к отделке помещений лаборатории
Поверхности пола, стен, потолка, мебели, оборудования и прочих объектов в помещениях лаборатории должны быть гладкими, устойчивыми к влажной уборке с применением моющих и дезинфицирующих средств. Для пола необходимо предусмотреть гидроизоляцию и антискользящее покрытие.
Батареи отопления в «заразной» зоне располагают на достаточном расстоянии от стен, чтобы обеспечить возможность их дезинфекции.
Окна и двери помещений «заразной» зоны лаборатории должны быть герметичными, иметь запирающие устройства.
Если лаборатория располагается на первом этаже или в цоколе, то окна обязательно оснащают металлическими решетками, не нарушающими правил пожарной безопасности. Для защиты рабочих столов от попадания прямого солнечного света используют светозащитную пленку или жалюзи из материалов, устойчивых к воздействию дезсредств.
Доставка и прием биологического материала
Биологический материал для исследований в лабораторию должен доставляться в закрытых контейнерах, биксах или в сумках-холодильниках, промаркированных с помощью международного знака «Биологическая опасность».
На дно контейнера для транспортировки укладывают адсорбирующий материал (марлевую салфетку, ткань, вату).
Обратите внимание!
Не допускается доставка материала в хозяйственных сумках, чемоданах, портфелях и других предметах личного пользования.
Чтобы исключить контакт бланков-направлений с биологическим материалом, их вкладывают в отдельный полиэтиленовый пакет.
Важно!
Персонал лаборатории должен осуществлять прием и разбор биологического материала с использованием средств индивидуальной защиты: масок и резиновых перчаток.
Работа с патогенными биологическими агентами
Во время работы в «заразной» зоне лаборатории следует соблюдать максимальную осторожность и применять средства индивидуальной защиты. При пипетировании необходимо пользоваться резиновыми грушами или автоматическими устройствами.
Важно!
Запрещается пипетировать ртом и переливать жидкий инфекционный материал через край пробирки, покидать рабочее место во время манипуляций с ПБА, удалять необеззараженные сгустки крови из пробирок вытряхиванием, сливать жидкие отходы в канализацию без предварительного обеззараживания.
Работы с ПБА, представляющие наибольшую опасность для медицинского персонала и окружающей среды, должны выполняться в боксированных помещениях «заразной» зоны лаборатории или в боксах биологической безопасности II класса. К таким работам относятся:
- центрифугирование ПБА и другие манипуляции, вследствие которых образуются аэрозоли;
- приготовление суспензий;
- работа с лиофилизированными ПБА;
- работа по ведению коллекционных штаммов;
- работа по идентификации и изучению выделенных штаммов микроорганизмов.
- серологические исследования и ПЦР-исследованияпо детекции в клиническом материале возбудителей парентеральных вирусных гепатитов В и С, ВИЧ-инфекции и других микроорганизмов II группы патогенности.

Во время работ двери боксов и предбоксов должны быть закрыты. До момента окончания работ выход из боксов не допускается.
Перед началом работ с использованием боксов биологической безопасности включают вентиляцию, проверяют исправность оборудования, наличие аварийного запаса дезинфицирующих средств. Манипуляции с ПБА должны выполняться ближе к задней стенке бокса на поддонах с салфетками, смоченными дезинфицирующим раствором.
После окончания работ с ПБА переднюю панель бокса биологической безопасности опускают, внутри бокса включают бактерицидные лампы.
Обратите внимание!
Боксы биологической безопасности должны проверяться на защитную эффективность:
-
после монтажа и подготовки к использованию;
-
после перемещения или ремонта;
-
не реже одного раза в год при наличии фильтров предварительной очистки воздуха от крупнодисперсных частиц;
-
не реже 2 раз в год при отсутствии фильтров предварительной очистки воздуха от крупнодисперсных частиц.
При проверке боксов должны контролироваться параметры эффективности работы фильтров очистки воздуха и скорость воздушного потока в рабочем проеме бокса.
По окончании работ в «заразной» зоне все объекты, содержащие ПБА, должны быть убраны в холодильники, термостаты или лабораторные шкафы. При наличии коллекции культур микроорганизмов их хранилища опечатываются. Все рабочие поверхности дезинфицируются. Помещения «заразной» зоны лаборатории запираются и опечатываются.
Дезинфекционные мероприятия в лаборатории
При организации дезинфекционных мероприятий в лабораториях применяют физические и химические методы дезинфекции.
Для обеззараживания лабораторной посуды, защитной одежды персонала, бактериологических посевов, а также жидких отходов можно применять паровые стерилизаторы.
В воздушных стерилизаторах допускается обеззараживать лабораторную посуду из стекла, металлов или силикона, не загрязненную органическими веществами.
Обратите внимание!
Параметры паровой и воздушной стерилизации контролируют с помощью максимальных термометров, которые размещаются в контрольных точках. Количество контрольных точек зависит от объема камеры стерилизатора. Параметры паровой стерилизации дополнительно контролируются при помощи мановакуумметров.
Химический контроль термической стерилизации осуществляют при каждом цикле работы с использованием специальных тест-индикаторов, необходимое количество и точки расположения которых зависят от вида аппаратуры и объема стерилизационной камеры.
Контроль стерилизации с помощью бактериологических методов (биотестов) должен осуществляться не реже 2 раз в год, а также после ввода в эксплуатацию и ремонта аппаратуры. Биотесты, содержащие некоторое количество жизнеспособных микроорганизмов, обладающих высокой резистентностью, помещают в контрольные точки стерилизационной камеры. При качественно проведенном процессе стерилизации микроорганизмы погибают. Вид применяемых биотестов зависит от типа стерилизационного оборудования.
Химическими методами проводят обеззараживание различных поверхностей, медицинской мебели, оборудования, жидких отходов, спецодежды и других объектов.
К сведению
При выборе химических дезинфектантов предпочтение следует отдавать средствам с широким спектром антимикробной активности.
Объекты, загрязненные кровью, необходимо дезинфицировать растворами, обладающими активностью в отношении возбудителей парентеральных инфекций.
Рабочие растворы дезсредств готовят в специально отведенных помещениях или в вытяжном шкафу. Контейнеры (емкости) с растворами маркируют, указывая название дезсредства и его назначение, концентрацию раствора, дату приготовления и дату конечной реализации.
Дезсредства, применяемые для проведения текущих и генеральных уборок, должны обладать моющими свойствами. Текущую уборку проводят 2 раза в день. Обрабатывают полы, мебель, оборудование, подоконники, двери.
Генеральные уборки проводят не реже 1 раза в месяц, в боксированных помещениях — не реже 1 раза в неделю.
Во время генеральных уборок моют и дезинфицируют стены на высоту до 2 м, пол, плинтусы, двери, окна, мебель, аппараты, приборы. Для «чистой» и «грязной» зон используют отдельный уборочный инвентарь, который должен быть промаркирован и использоваться строго по назначению.
После влажной уборки включают бактерицидные облучатели. Их следует эксплуатировать в соответствии с действующими методическими документами и инструкциями по применению конкретного оборудования.
Обратите внимание!
Если в течение дня нужно экстренно обработать небольшие по площади или труднодоступные поверхности, следует использовать готовые к применению формы дезсредств, которые имеют небольшое время экспозиции и выпускаются в виде спреев или дезинфицирующих салфеток.
Медицинские изделия и посуду дезинфицируют способом полного погружения в рабочий раствор дезинфицирующего средства. Разъемные изделия обеззараживают в разобранном виде, каналы и полости изделий заполняют дезинфицирующим раствором.
Особенности обращения с отходами лабораторий
Все отходы, образующиеся в «заразной» зоне лаборатории, считаются эпидемиологически опасными, т. е. относятся к классу Б, и должны подвергаться обеззараживанию.
Твердые отходы, которые образуются в «заразной» зоне лаборатории, собирают в одноразовые пакеты или контейнеры желтого цвета или имеющие желтую маркировку, подвергают дезинфекции химическими или физическими методами.
Жидкие отходы из «заразной» зоны запрещено сливать в канализационную сеть без предварительного обеззараживания. Чаще всего их смешивают с растворами дезсредств в пропорциях, указанных в инструкциях по применению конкретных дезинфектантов.
Лабораторную посуду с культурами микроорганизмов, как правило, обеззараживают в паровых стерилизаторах.
Важно!
Пробирки со сгустками крови обеззараживают с использованием дезинфицирующих растворов или с применением физических методов дезинфекции. Вытряхивать необеззараженные сгустки крови из пробирок запрещено.
При погружении в дезинфицирующий раствор пробирок со сгустками крови необходимо соблюдать осторожность. Пробирку берут анатомическим пинцетом так, чтобы одна его бранша вошла немного внутрь, и погружают ее в наклонном положении до полного заполнения раствором. При правильном погружении воздушные пузыри не образуются, пробирка опускается на дно.
Техника безопасности и ликвидация аварийных ситуаций
Помещения лаборатории должны быть оборудованы пожарной сигнализацией и обеспечены средствами пожаротушения в соответствии с требованиями пожарной безопасности.
Сотрудники диагностических лабораторий должны быть обеспечены спецодеждой соответствующего размера: медицинскими халатами и костюмами, шапочками, медицинской обувью и средствами индивидуальной защиты, в том числе перчатками и масками, респираторами.
Для работы в боксированных помещениях используют отдельный халат, доходящий до нижней трети голени, и тапочки.
Рабочая одежда и обувь должны быть индивидуальными, храниться отдельно от личной одежды. Смена рабочей одежды проводится по мере загрязнения, но не реже 1 раза в неделю. Стирать спецодежду следует централизованно. Перед сдачей в стирку защитную одежду обеззараживают.
В лабораториях не допускается применение материалов и средств личной гигиены, раздражающих кожу. После окончания работ с ПБА, при переходе из «заразной» зоны в чистую, а также после уборочных работ и проведения дезинфекции персонал лаборатории должен выполнять гигиеническую обработку рук, используя кожные антисептики.
Важно!
На случай аварийных ситуаций, при которых создается угроза выделения ПБА в воздух рабочей зоны или есть риск заражения персонала, в лаборатории должен быть план ликвидации аварии и запас дезинфицирующих средств.
Объем мероприятий по ликвидации аварии зависит от характера выполняемой работы, вида и свойств ПБА, масштабов аварии.
Кроме того, в специально отведенном месте хранят аварийную аптечку, гидропульт, комплекты рабочей одежды для переодевания пострадавших и защитной одежды для сотрудников, ликвидирующих последствия аварии. Ответственным за комплектование аптечки и аварийной укладки является заведующий лабораторией.
Состав аварийной аптечки:
1. Спирт этиловый 70%-ный — 2 флакона по 100 мл.
2. Спиртовой раствор йода 5%-ный — 1 флакон.
3. Раствор борной кислоты 1%-ный — 1 флакон.
4. Нашатырный спирт — 1 флакон.
5. Бинт марлевый медицинский стерильный (5 м × 10 см) — 2 шт.
6. Лейкопластырь бактерицидный (не менее 1,9 см × 7,2 см) — 3 шт.
7. Салфетка марлевая медицинская стерильная (не менее 16 см × 14 см, № 10) — 1 уп.
8. Ножницы с закругленными браншами.
При аварии во время работы на центрифуге крышку медленно открывают только спустя 30–40 минут, чтобы сформировавшийся аэрозоль успел осесть. Центрифужные стаканы и разбитое стекло помещают в дезинфицирующий раствор, поверхность крышки, внутренние части центрифуги, ее наружную поверхность дезинфицируют (после отключения ее от электросети).
О каждом случае аварийной ситуации руководитель лаборатории обязан сообщить комиссии по контролю соблюдения требований биологической безопасности, а также руководителю медорганизации.
Не реже 1 раза в год в лаборатории должны проводиться тренировочные учения по ликвидации аварий.
Допуск персонала к работе с ПБА
Допуск персонала к работе с ПБА III–IV групп патогенности, а также допуск инженерно-технического персонала к обслуживанию лабораторного оборудования должен осуществляться на основании приказа главного врача. Приказ издается не реже одного раза в два года, корректируется по мере необходимости.
В лабораториях медорганизаций работу с ПБА могут выполнять специалисты не моложе 18 лет с высшим и средним медицинским или биологическим образованием, прошедшие необходимую профессиональную подготовку.
Лица, имеющие медицинские противопоказания к вакцинации, лечению специфическими препаратами, использованию средств индивидуальной защиты, к работам с ПБА не допускаются.
Не реже 1 раза в год медицинский персонал, работающий с ПБА, должен проходить инструктаж по соблюдению требований биологической безопасности. Инженерно-технический персонал, дезинфекторы и санитарки лаборатории также должны проходить вводные и периодические инструктажи по биологической безопасности.
При приеме на работу сотрудников лаборатории направляют на предварительный медицинский осмотр для выявления противопоказаний с учетом специфики трудовой деятельности[1].
Все сотрудники, которые привлекаются к работам с ПБА, должны быть привиты в соответствии с календарем профилактических прививок и календарем прививок по эпидемическим показаниям.
К работе с паровыми стерилизаторами (автоклавами) могут быть допущены лица, обученные, аттестованные и имеющие удостоверение на право обслуживания сосудов, работающих под давлением.
Организация работы комиссии по биологической безопасности
Для контроля за соблюдением мер биологической безопасности при работе с ПБА в медорганизации создается специальная комиссия. В ее состав, как правило, включают заведующего лабораторией, врача-эпидемиолога или его помощника, инженера по охране труда и других заинтересованных специалистов.
Задачи комиссии по биологической безопасности:
- организация и проведение постоянного контроля за соблюдением регламентированного порядка обеспечения биологической безопасности лаборатории;
- разработка комплекса мер по совершенствованию биологической безопасности;
- организация и проведение мероприятий, направленных на предупреждение аварийных ситуаций при работе с ПБА и ликвидацию их последствий;
- контроль за подготовленностью сотрудников к работе с ПБА и организация наблюдения за состоянием их здоровья.
Заседания комиссии проводятся не реже 2 раз в год. Решения комиссии доводятся до сведения руководителя медорганизации.
[1] Объем и порядок проведения медосмотра определяются Приказом Минздравсоцразвития России от 12.04.2011 № 302н (в ред. от 06.02.2018) «Об утверждении перечней вредных и (или) опасных производственных факторов и работ, при выполнении которых проводятся обязательные предварительные и периодические медицинские осмотры (обследования), и порядка проведения обязательных предварительных и периодических медицинских осмотров (обследований) работников, занятых на тяжелых работах и на работах с вредными и (или) опасными условиями труда».
Статья опубликована в журнале «Санэпидконтроль. Охрана труда» № 1, 2019.
ПРИ РАБОТЕ В БАКТЕРИОЛОГИЧЕСКОЙ ЛАБОРАТОРИИ
Подготовлено к печати:
д. б.н. Васильевым Д. А,
к б н Меркуловым А. В.,
в м н Нафеевым А. А,
к в н Золотухиным С. Н.
Ульяновск 2006
КАФЕДРА МИКРОБИОЛОГИИ, ВИРУСОЛОГИИ, ЭПИЗООТОЛОГИИ и ВСЭ
УЛЬЯНОВСКОЙ ГОСУДАРСТВЕННОЙ
СЕЛЬСКОХОЗЯЙСТВЕННОЙ АКАДЕМИИ
ПРАКТИЧЕСКОЕ РУКОВОДСТВО
ПО БИОЛОГИЧЕСКОЙ
БЕЗОПАСНОСТИ
В ЛАБОРАТОРНЫХ УСЛОВИЯХ
(ОБЩИЕ ПОЛОЖЕНИЯ)
БИОЛОГИЧЕСКИЕ ФАКТОРЫ
ПРОИЗВОДСТВЕННОЙ СРЕДЫ ______________________________
LABORATORY BIOSAFETY MANUAL
______________________________
Ульяновск 2006
ПРЕДИСЛОВИЕ
К персоналу лабораторий, осуществляющих деятельность с патогенными биологическими агентами (ПБА), по определению, относятся лица, работающие с инфекционными организмами или материалами, содержащими или могущими их содержать. Некоторые из этих микроорганизмов в зависимости от обстоятельств и дозы бывают патогенными или условно патогенными. Таким образом, существенным профессиональным навыком является умение избежать инфицирования. Безопасная работа – признак высочайшей квалификации персонала, которой он должен гордиться. В защите нуждаются не только сами микробиологи, их помощники и лица, находящиеся с ними в контакте, но и материалы, поскольку возможное перекрестное заражение способно исказить результаты экспериментов.
Данное руководство разработано группой экспертов. Оно носит практический характер, учитывает различное распространение и значимость патогенных организмов и технических особенностей, оснащения и ресурсов, уровня образования и обучения персонала. Оно содержит полезную информацию для лиц, осуществляющих разработку мероприятий по безопасности работ с патогенными биологическими агентами. В приложении 1 приведена классификация микроорганизмов по степени опасности для человека, полезная для специалистов, разрабатывающих или пересматривающих правила практической работы. Несмотря на обилие информации, данное руководство остается компактным и удобным практическим справочником.
Весьма важным является акцент на вопросы обучения персонала. Ни боксы, ни определенные методы сами по себе не гарантируют безопасности без правильной работы сотрудников, их информированности и адекватных знаний. Безопасное оборудование может вызвать ложное чувство защищенности и беспечности, что повышает риск, если это оборудование не спроектировано и установлено соответствующим образом, отсутствует его правильное материально-техническое обслуживание и эксплуатация. Необходим строжайший самоконтроль во время работы, также как и адекватное инспектирование и надзор.
В тоже время требуется и чувство меры. Абсолютная безопасность невозможна ни в одной области работы или жизни. Лаборатории, работа в которых налажена должным образом, не представляют собой опасности, что позволяет избежать чрезмерных предосторожностей или избыточного внимания к личной безопасности. Главным принципом биобезопасности является формирование рациональных навыков микробиологических исследований.
Д. А.Васильев
А. В.Меркулов
А. А. Нафеев
С. Н. Золотухин
1. Область применения
Методическое руководство предназначено для организаций, предприятий и иных хозяйствующих субъектов, проводящих работу с использованием микроорганизмов II-IV групп патогенности или материалом, подозрительным на их содержание, а также для учреждений, осуществляющих санитарно-эпидемиологический надзор за проведением этих работ.
2. Нормативные ссылки
В настоящем методическом руководстве использованы ссылки на следующие документы:
— Санитарные правила «Безопасность работы с микроорганизмами I-II групп патогенности (СП 1.3.1285-03).
— Санитарные правила «Безопасность работы с микроорганизмами III-IV групп патогенности» (СП 1.2.735-99)
— Санитарные правила «Порядок выдачи санитарно-эпидемиологического заключения о возможности проведения работ с возбудителями инфекционных заболеваний человека 1-4 групп патогенности (опасности)» (СП 1.3.1318-03)
— Сборник санитарных и ветеринарных правил «Профилактика и борьба с заразными болезнями, общими для человека и животных» (Бруцеллез, сальмонелез, кампилобактериоз, листериоз, сибирская язва, чума, лептоспироз, орнитоз, туберкулез, иерсиниозы, коксиеллез (лихорадка Ку), бешенство, туляремия, клещевой энцефалит, геморрагическая лихорадка с почечным синдромом). Москва, 1996.
Введение
Двойная цель техники лабораторной безопасности заключается в защите, как эксперимента, так и экспериментатора, но безопасность человека стоит, конечно, на первом месте.
Из того факта, что обычно используемые бактерии присутствуют в окружающей среде, как будто следует, что они безвредны для человека. Действительно, между непатогенностью и патогенностью нет резкой границы; фактически бактерии имеют широкий спектр степени вирулентности по отношению к человеку. Вчерашний сапрофит сегодня может стать паразитом, а завтра возбудителем заболевания (в качестве примеров можно назвать Escherichia coli, Proteus vulgaris, Pseudomonas aeruginosa, Serratia marcescens и Bacillus cereus). Никогда нельзя забывать, что со всеми бактериями следует работать как с потенциальным источником опасности для здоровья человека.
Предотвращение заражения
Основной принцип безопасной работы и функционирования бактериологической лаборатории заключается в достаточной организации данной безопасности. При этом необходимо иметь полное представление о степени риска, существующем при работе с микроорганизмами, знать механизмы, благодаря которым могут возникать опасные ситуации, использовать приёмы и способы безопасной работы, которые позволяют уменьшить или исключить возможность этих воздействий, и быть бдительными в отношении компромиссов и вероятных ошибок.
Общие сведения
В зарубежной литературе последних лет опубликованы сведения о 3921 случае инфекций, полученных в лаборатории. Из этих данных следует, что работающие с бактериями подвержены риску заражения, но из них трудно сделать выводы о степени риска, поскольку отчеты о заражениях неполны, а число людей, подвергшихся риску, не указывается. Но возможность бактериального заражения в лабораторных условиях очевидна, и это требует соблюдения мер предосторожности при обращении с любыми бактериями независимо от того, «патогенны» они или нет.
Таблица 1
Распределении случаев заболевания по источнику
бактериальной инфекции.
|
Источник инфекции |
Случаи |
|
|
число |
% |
|
|
Выявленное заболевание |
378 |
22,7 |
|
Аэрозоль |
101 |
6,1 |
|
Животное или эктопаразит |
149 |
8,9 |
|
Материал клинических проб |
90 |
5,4 |
|
Выброшенная стеклянная посуда |
34 |
2,0 |
|
Животные во время аутопсии (вскрытии) |
56 |
3,4 |
|
Умышленное заражение |
14 |
0,8 |
|
Возбудитель, при постановке опытов с ним в лаборатории |
381 |
22,8 |
|
Другие источники |
7 |
0,4 |
|
Неизвестные или не сообщенные |
459 |
27,5 |
|
Всего |
1669 |
100 |
Случая заражения, причины которых известны, составляют менее 25% от общего числа, тогда как в 75% случаев причины заражения неизвестны. В некоторых ситуациях по имеющейся информации можно предположить источник заражения только в 50% сообщённых случаев.
В следующей таблице (табл. 2) классифицированы известные несчастные случаи (происшествия), послужившие причиной зарегистрированного заболевания среди лабораторного персонала, имеющего дело с бактериями. Эти случаи разнообразны, причем среди них не отмечено какого-либо преобладания одной или нескольких инфекций. Следует помнить, что при проведении большинства бактериологических экспериментов возникают аэрозоли, которые либо оседают на поверхностях, либо непосредственно вдыхаются работающими. Отсутствие информации об источнике или причине многих лабораторных заражении часто объясняется тем, что возникновение аэрозолей остается незамеченнымМеждународный знак биологической опасности (рис. 1) употребляется для обозначения действительного или возможного присутствия биологической опасности, а также для обозначения оборудования, емкостей, комнат, материалов или экспериментальных животных, которые содержат или заражены жизнеспособными возбудителями. Плакат с этим знаком необходимо вывесить вместе с соответствующей информацией. Знак окрашен люминесцирующей оранжевой или оранжево-красной краской. К цвету фона никаких требований не предъявляется; он должен быть лишь достаточно контрастным, чтобы знак ясно выделялся. Знак должен быть заметным и практичным; он должен соответствовать по размеру тому оборудованию или материалу, к которому его прикрепляют, так чтобы его было видно отовсюду. Он указывает на действительную или возможную биологическую опасность. Рядом со знаком дается соответствующая информация о характере опасности, указывается фамилия ответственного за контроль над ней, а также меры, необходимые в случае аварии.
Таблица 2.
Известные происшествия в лабораториях,
приведшие к бактериальному заражению.
|
Вид происшествия |
число |
% |
|
Прокол или разбрызгивание при работе с иглой и шприцем |
83 |
22,1 |
|
Контакт с инфекционным материалом в результате проливания, разбрызгивания и т. д. |
82 |
21,7 |
|
Повреждение осколком стекла или другим острым предметом |
75 |
19,8 |
|
Засасывание через пипетку |
67 |
17,7 |
|
Укус или царапина, полученые от подопытного животного или эктопаразита |
41 |
10,8 |
|
Другие случаи |
3 |
0,8 |
|
Не установлен |
27 |
7,1 |
|
Всего |
378 |
100 |
Мероприятия по предотвращению заражения людей и контаминации окружающего оборудования.
При работе с бактериями необходимо тщательно выполнять следующие меры предосторожности.
1. Держать двери лаборатории закрытыми.
2. Дезинфицировать рабочие поверхности ежедневно и каждый раз после проливания растворов, содержащих бактерии.
3. Перед мытьем или повторным употреблением загрязненные предметы, такие, как лабораторная посуда, оборудование используемое в боксовой работе, клетки для животных должны быть автоклавированы или дезинфицированы.
4. Использовать механические устройства для набирания жидкости в пипетки.
5. Не есть, не пить и не курить в лаборатории.
6. Часто мыть руки и всегда-перед выходом из лаборатории.
7. Все процедуры и манипуляции выполнять осторожно, сводя к минимуму образование аэрозолей.
8. На соответствующих лабораторных дверях установить знаки биологической опасности. Морозильники, холодильники и другие места хранения патогенных бактерий также должны быть снабжены этим знаком.
9. Надевать нательное лабораторное белье, защитную одежду или халаты. Не носить эту одежду вне лаборатории.
10. Избегать по возможности использования игл и шприцев.
1 – Bio Hazard
2 – ADMITTANCE TO AUTHORIZED PERSONNEL ONLY
3 – Hazard identity:
4 – Responsible Investigator:
5 – In case of emergency call:
6 – Daytime phone
7 – Home phone
8 – Authorization for entrance must be obtained from the responsible Investigator named above.
Рис. 2. Знак биологической опасности, предназначенный
для вывешивания в местах возможного заражении.
Перевод с англ.: 1- биоопасность: 2-вход разрешен только сотрудникам, имеющим допуск; 3-вид опасности; 4-ответственный; 5- в экстренном случае звонить; 6-рабочий телефон; 7-домашний телефон; 8-допускаются только получившие разрешение у ответственного.
Специальные лабораторные процедуры безопасности
Личная гигиена
Еду, конфеты, жевательную резинку и напитки нельзя хранить и употреблять в лабораторных комнатах.
Курение в рабочих помещениях запрещено.
Нежелательно, чтобы работающие в лаборатории имели бороду, во-первых, потому что в бороде могут сохраняться частички с бактериями и, во-вторых, потому что маска или респиратор к чисто выбритому лицу прилегает гораздо лучше, чем к лицу с бородой.
Руки не следует подносить близко ко рту, носу, глазам, лицу и волосам, чтобы предотвратить самозаражение.
Личные вещи, такие, как пальто, шляпы, плащи, уличную обувь, зонты и кошельки, необходимо хранить вне лабораторных помещений.
После снятия защитных перчаток следует немедленно вымыть руки. Проверочные опыты показывают, что, даже когда используют перчатки, не исключено попадание на руки бактерий. Бактерии могут проникнуть через незаметные маленькие дырочки, трещины или разрывы или попасть через край перчатки, прилегающий к запястью.
Руки нужно мыть, сняв запачканную защитную одежду, перед выходом из лаборатории, перед едой иди курением и в течение дня через интервалы, определяемые. характером работы. Желательно мыть руки в дезинфицирующем растворе или погружать их в него, но при этом, конечно, не следует допускать огрубения, чрезмерного высушивания или раздражения кожи.
К работе с бактериями нельзя допускать людей со свежим или старым порезом, ссадиной, повреждением кожи или любой открытой раной, включая образовавшуюся после удаления зуба.
Работа с пипетками
Чтобы уменьшить возможность заражения, следует использовать безопасные способы применения пипеток. Насасывание раствора пипеткой было причиной бактериального заражения в лабораторных условиях более чем в 17% всех известных случаев.
Наиболее распространенный способ, при котором подвергаются опасности в работе с пипеткой – это насасывание ртом. Бактерии могут также попасть в рот, если загрязненным пальцем дотронуться до верхнего конца пипетки. Кроме того, если в пипетках нет ватных пробок, то заражение может произойти путем вдыхания аэрозолей, возникающих в процессе работы с жидкими суспензиями, даже в том случае, когда жидкость не попадает в рот. Дополнительная опасность действия аэрозолей возникает, когда жидкость из пипетки капают на рабочую поверхность, перемешивают культуру чередованием всасывания и выдувания, интенсивно выдувают культуру в чашку или выдувают последнюю каплю из пипетки.
Чтобы использование пипеток было безопасным, применяют дополнительные приспособления, предотвращающие опасность заглатывания, и стараются обращаться с ними осторожно. Существует множество приспособлений к пипеткам – от простых шаровидных груш и поршневых насасывателей до сложных конструкций, имеющих свои собственные насосы, создающие вакуум. При выборе приспособления надо иметь в виду тип операции, которую требуется выполнить, легкость выполнения, а также ее точность. Предварительно следует отработать технику использования пипеток, чтобы уменьшить возможность образования аэрозолей.
В верхнюю часть пипетки вставляют кусочки ваты и стараются избегать быстрого смешивания жидкостей путем чередования всасывания и выдувания их из пипеток. Нельзя с силой выдувать раствор из пипетки и допускать попадания пузырьков воздуха в жидкость, набираемую пипеткой. Предпочтительнее использовать пипетки, при работе с которыми не требуется выдувания последней капли. Необходимо также следить за тем, чтобы культуральный материал не капал из пипетки. Можно при работе с суспензиями, содержащими патогенные бактерии, на рабочую поверхность класть полотенце, пропитанное дезинфицирующим веществом. Жидкость из пипеток выливают таким образом, чтобы кончик пипетки находился почти над уровнем жидкости или агара в сосуде-приемнике или раствор стекал по его стенке. Нельзя вносить раствор из пипетки в сосуд каплями, падающими с высоты. Грязные пипетки помещают в емкости с дезинфицирующим раствором, полностью погружая в него.
Применение шприцев и игл
Причиной наибольшего количества из всех известных случаев бактериальных заражений в лабораторных условиях является использование игл и шприцев. Для того чтобы уменьшить вероятность неблагополучной инъекции, образования аэрозоля или проливания суспензий бактерий, лучше избегать их применения. Для введения суспензий бактерий животным через рот или нос рекомендуется пользоваться тупой иглой или канюлей на шприце и не рекомендуется применять шприц и иглу как заменитель пипетки.
Существуют следующие правила использования игл и шприцев для парентеральных инъекций.
Пользуются биологически безопасным боксом и избегают быстрых лишних движений рукой, держащей шприц.
Проверяют стеклянные шприцы на присутствие сколов и трещин, а иглы-на наличие зазубрин и проходимость. Это делают перед стерилизацией и перед употреблением.
Пользуются только шприцами с иглами и удостоверяются, что игла закреплена надежно. Используют хирургические или другие резиновые перчатки. Шприцы заполняют осторожно, чтобы в набираемом растворе было как можно меньше пузырьков воздуха и пены.
Излишки воздуха, жидкости и пузырьки удаляют, держа шприц в вертикальном положении, в ватный тампон, смоченный дезинфицирующим веществом, или в маленькую бутылочку, наполненную стерильной ватой.
Шприц не применяют для внесения инфекционной жидкости в открытый пузырек или пробирку с целью смешивания. Смешивание с помощью шприца разрешается только в том случае, если конец иглы находится ниже поверхности жидкости в пробирке.
Если раствор набирают шприцем из пробирки, то стараются не загрязнить втулку иглы, так как это может привести к попаданию инфекционного материала на пальцы.
Когда вынимают шприц и иглу из бутыли с резиновой пробкой, иглу и пробку заворачивают в ватный тампон, смоченный соответствующим дезинфектантом. Если есть опасность загрязнения дезинфектантом чувствительного к нему материала, используемого в эксперименте, применяют стерильный сухой тампон, который сразу же помещают в дезинфицирующий раствор.
Во время прививки животному руку держат сзади иглы во избежание укалывания.
Перед прививкой убеждаются в том, что животное хорошо фиксировано, и принимают меры предосторожности в случае неожиданных движений.
Место прививки перед инъекцией и особенно после нее протирают дезинфицирующим веществом.
После использования грязные стеклянные шприцы многоразового пользования с надетыми на них иглами погружают в емкость с дезинфицирующим раствором и затем автоклавируют. Чтобы уменьшить возможность заражения, иглы должны оставаться на шприцах до конца автоклавирования. Шприцы с надетыми на них иглами помещают в отдельный лоток, в котором нет других использованных материалов,
Иглы и шприцы одноразового пользования помещают в лоток с дезинфицирующим раствором и затем автоклавируют. Емкости с надписью «Шприцы и иглы» после соответствующей упаковки и разрушения содержимого можно выбрасывать в обычный контейнер для отходов. После стерилизации иглы и шприцы специально портят и разбивают, чтобы их не использовали наркоманы.
В тех случаях, когда после использования иглу нужно поместить в защитный футляр, ее берут пинцетом, чтобы уменьшить вероятность случайного укола пальца. Шприцы и иглы многоразового и одноразового пользования складывают в отдельные лотки с дезинфектантом, чтобы не возникало проблемы их сортировки. Шприцы и иглы никогда не кладут в лотки, содержащие пипетки и другую стеклянную посуду.
Вскрытие емкостей
С пробирками, содержащими бактериальные суспензии, необходимо обращаться осторожно. Такие простые операции, как удаление пробки из пробирки или перенесение культуры из одной емкости в другую, могут вызывать образование аэрозолей. Следует четко метить пробирки и штативы с пробирками, содержащими биологически опасный материал. Чтобы уменьшить проливание из разбитых пробирок, рекомендуется пользоваться безопасными подставками для пробирок вместо обычных штативов. В такой безопасной подставке каждая выемка для пробирки имеет достаточно высокие стенки, так что если пробирка разобьется, все ее содержимое останется в выемке. Аэрозоль с большим содержанием жидкости образуется при энергичном встряхивании жидких культур, тогда как при вращательном движении сосудов образование аэрозоля минимально, а получаемая суспензия достаточно гомогенна. По окончании ресуспендирования жидкой культуры следует несколько минут выждать и только затем открывать емкость; это способствует снижению образования аэрозоля.
Брызги аэрозоля могут появляться при погружении стерильной горячей петли или иглы в жидкую культуру или в косяк. Чтобы уменьшить образование аэрозолей, петле дают остыть либо на воздухе, либо при соприкосновении с внутренней стенкой емкости или поверхностью агара, где до этого заведомо не росла культура. После использования петли и иглы ее стерилизуют нагреванием на открытом пламени. В продаже имеются петли для внесения инокулята одноразового пользования, которые проще обеззараживать погружением в дезинфицирующий раствор, чем нагреванием.
При посеве штрихом на неровную поверхность агара происходит вибрация петли или иглы, что приводит к образованию аэрозоля. Как правило, этой проблемы не существует, если посев делают на гладкую поверхность агара, поэтому рекомендуется не высевать культуру в чашки с неровной поверхностью агара.
Вода, появляющаяся в чашках Петри в результате синерезиса, образует в перевернутой чашке пленку между ребром чашки и крышкой в которой могут содержаться жизнеспособные бактерии. При открывании чашки эта пленка разрывается, в результате чего возникают аэрозоли. Чашки следует открывать в боксе.
Менее вероятно высвобождение аэрозолей при открывании бутылей с завинчивающимися пробками или закрытых тампонами пробирок. Но все же это может произойти, когда во время открывания разрывается пленка между краем и прокладкой. Аэрозоли образуются при удалении ватных пробок или крышек с колб, бутылей и центрифужных стаканов сразу же после взбалтывания или центрифугирования. Опасно вынимать пробки, намокшие в результате невертикального положения колбы или центрифужного стакана. Пробки могут слегка увлажняться при центрифугировании, если в ходе его происходит незначительное вспенивание. В связи с этим все жидкие культуры с инфекционным материалом необходимо открывать в безопасном боксе, надев перчатки и лабораторную одежду с длинными рукавами.
Аэрозоль может образовываться при вскрытии запечатанной ампулы с лиофилизованной или жидкой культурой, поэтому ампулы следует вскрывать только в боксе. Собирая осколки ампулы, необходимо позаботиться о том, чтобы не порезать перчатки или руки, чтобы разбитое стекло не попало в глаза, на лицо или не осталось неубранным. После вскрытия ампулы суспензия бактерий не должна загрязняться посторонними микроорганизмами или дезинфицирующими веществами. Этого добиваются, работая в безопасном боксе в перчатках. Для того чтобы вскрыть ампулу, прежде всего делают насечку пилкой около шейки ампулы. Саму ампулу оборачивают ватой, пропитанной дезинфицирующим веществом, и вскрывают надломом в месте насечки, предварительно убедившись, что держат ее вертикально. Другим способом в месте насечки делают трещину, прикладывая к нему накаленную проволоку или стеклянную палочку, затем оборачивают ампулу пропитанной в дезинфицирующем веществе ватой и открывают ее надломом. Вату и верхушку ампулы немедленно бросают в дезинфицирующий раствор. Содержимое ампулы растворяют путем медленного добавления жидкости, стараясь не допускать образования аэрозоля. Раствор перемешивают, следя за тем, чтобы не было пузырьков, и переносят в приготовленную емкость.
Для удобства открывания выпускаются ампулы с предварительно нанесенной насечкой, однако такие ампулы менее надежны: они могут разбиваться во время работы с ними или при хранении. Ампулы с жидкими культурами вскрывают аналогичным образом.
Сбор культур, выращиваемых на куриных эмбрионах, весьма опасен. При его проведении сильно загрязняются скорлупа и подносы с яйцами, окружающая среда и руки экспериментатора. Работу подобного рода следует выполнять в безопасных боксах, часто пользуясь подходящим дезинфицирующим веществом.
Центрифугирование
При центрифугировании инфекционных бактериальных суспензий следует пользоваться безопасными центрифужными гильзами, а настольные центрифуги должны находиться только в боксах
Центрифужные стаканы и гильзы наполняют и открывают в безопасном боксе. Если центрифугируют вне бокса, то применяют защитную гильзу. После заполнения и запечатывания ее протирают или окунают в дезинфицирующий раствор. По истечении необходимого времени гильзу обмывают чистой водой, поскольку некоторые дезинфицирующие вещества вызывают коррозию.
Перед центрифугированием проверяют стаканы, и если находят трещины или сколотые края, то такими стаканами не пользуются. Внимательно осматривают внутреннюю поверхность гильз и ликвидируют шероховатости или приставшие частицы. Проверяют также состояние резиновых прокладок.
Между стаканом и гильзой заливают дезинфицирующий раствор, чтобы в том случае, если разобьется стакан, материал подвергся дезинфекции. К тому же это создает хорошую амортизацию. Следует позаботиться о том, чтобы культуральный материал не загрязнился дезинфицирующим веществом. Рекомендуется также не забывать о том, что если стакан разобьется, то из-за высокой концентрации клеток и большого разбавления дезинфицирующего вещества инфекционный материал может дезинфицироваться не полностью.
Надосадочную жидкость лучше не выливать из центрифужных стаканов, а отсасывать. Если ее необходимо слить, протирают внешний край стакана дезинфицирующим раствором, так как, если этого не сделать, на следующей стадии может образоваться аэрозоль.
Центрифужный стакан заполняют таким образом, чтобы край, крышка или ватная пробка не становились влажными от культуры. Завинчивающиеся крышки или крышки, охватывающие края сверху, безопаснее крышек, входящих внутрь. В последнем случае между крышкой и краем стакана обычно собирается некоторое количество жидкости. Даже стаканы с завинчивающимися крышками небезопасны: если края запачканы и неплотно прилегают к крышке, некоторое количество жидкости может попасть на внешнюю стенку стакана.
Не рекомендуется закрывать центрифужные стаканы алюминиевой фольгой, потому что при центрифугировании она часто слетает или рвется.
Стаканы и гильзы необходимо тщательно уравновешивать. Не следует смешивать гильзы, стаканы и пластмассовые вкладыши из разных наборов. Если на этих предметах не указан вес, удобно пометить каждый комплект своей краской.
Металл, из которого сделаны высокоскоростные роторы, постепенно изнашивается, и если их используют на разных центрифугах, то для каждого заводят тетрадь, в которой отмечают количество часов работы на предельной или пониженной скорости. Если это не соблюдается, может произойти опасная и дорогостоящая поломка. Чтобы предотвратить коррозию или другие дефекты, которые могут привести к развитию трещин, необходимы частые проверки роторов, их очистка и сушка. Если ротор обрабатывают дезинфицирующим раствором, то после этого его промывают водой и высушивают. Регулярно проверяют состояние резиновых колец и крышек центрифужных стаканов и смазывают их в соответствии с рекомендациями фирмы-изготовителя. Если стаканы сделаны из различных материалов {например, целлулоидные, полипропиленовые, из нержавеющий стали), следят за тем, чтобы использовались крышки, предназначенные для соответствующих типов. Крышки часто внешне похожи, но если их надевают на несоответствующие им стаканы, последние могут давать течь. При хорошем хранении стаканов и роторов и правильном с ними обращении этого не происходит.
Перемешивание и разрушение микроорганизмов
При использовании для разрушения бактерий смесителей, миксеров, ультразвуковых дезинтеграторов, коллоидных мельниц, струйных мельниц, дробилок, а также ступок с пестиками соблюдают следующие правила.
Используют биологически безопасный бокс.
Используют безопасное оборудование, в котором предотвращена утечка жидкости из сосуда. В случае отсутствия защиты от утечки перед работой необходимо убедиться в том, что ее нет. Для этого проводят предварительные испытания, используя стерильную воду, физиологический раствор или раствор метиленового синего.
Во время работы на смеситель вешают полотенце, смоченное дезинфицирующим раствором. Сразу после работы смеситель и остатки стерилизуют.
Для смешивания инфекционных материалов стараются не использовать стеклянные емкости.
Иногда для предотвращения разрушения рабочих деталей и уменьшения нагревания содержимого требуется охлаждать емкость смесителя. После прекращения работы смесителя емкость не открывают, по крайней мере, в течение 1 мин, давая возможность осесть аэрозолю.
Обращение с животными
Животные способны распространять патогенные микроорганизмы через слюну, мочу или экскременты. В отсутствие специальной информации все животные должны рассматриваться как разносчики инфекции. Чтобы уменьшить разнесение пыли и находящихся в клетке отходов, с ними обращаются очень осторожно. Использованные клетки, где содержались животные, стерилизуют автоклавированием вместе с отбросами, емкостями и поилками или же сами клетки дезинфицируют 10% раствором хлоромина.
Когда кормят, поят или забирают из клеток инфицированных животных, надевают плотные перчатки. Нельзя передвигать предметы в клетке голыми руками.
При инъекции животным бактерий надевают защитные перчатки. Следует ограничить движения животных (например, с помощью специальной небольшой клетки, подставки и т. п. ) или ввести им успокаивающие средства, чтобы избежать распространения опасного биологического материала или заражения других животных и персонала.
Двери в помещениях с животными всегда держат закрытыми, за исключением тех случаев, когда необходимо войти и выйти. В эти помещения нельзя допускать посторонних лиц.
В каждом помещении с животными должна находиться емкость с дезинфицирующим раствором, который следует ежедневно обновлять. Он предназначен для дезинфекции перчаток и рук, а также для общей дезинфекции. Руки, полы, стены и кормушки клеток регулярно моют проверенным дезинфицирующим раствором соответствующей концентрации.
Сточные желоба на полу помещений с животными периодически наполняют водой или дезинфицирующим раствором, чтобы газы, образующиеся в стоках, не поднимались вверх. Сбритые волосы и другие отходы нельзя бросать в сточный желоб на полу, поскольку они засоряют канализационные трубы.
Необходимо выполнять инструкцию по контролю зa насекомыми и грызунами в каждом помещении с животными и в местах, где хранится корм. Особое внимание обращают на то, чтобы живые животные, особенно мыши, не могли проникнуть к отходам.
Вскрытие зараженных животных производят в безопасном боксе. При этом поверх лабораторной одежды надевают хирургическую накидку, а на руки резиновые перчатки. Перед вскрытием шерсть животных обрабатывают подходящим дезинфицирующим раствором.
По окончании вскрытия весь биологически опасный материал помещают в подходящие емкости и немедленно стерилизуют, а грязные инструменты кладут на поднос и заливают дезинфицирующим раствором. Внутреннюю поверхность безопасного бокса и загрязненные поверхности дезинфицируют. Перед тем как снять с рук перчатки, их тщательно очищают в дезинфектанте, подготовив тем самым к стерилизации. Мертвых животных помещают в специальные непротекающие емкости, автоклавируют и надежно связывают перед кремацией.
Применение вакуумных систем
Вакуумная фильтрация суспензий и отсасывание культуральных сред и надосадочных жидкостей из центрифужных стаканов в приемные колбы – это обычные лабораторные процедуры. Чтобы предотвратить засасывание бактериальных аэрозолей или забрасывание жидкости в вакуумную систему, на пути к источнику вакуума устанавливают воздушный фильтр, а между приемной колбой и воздушным фильтром помещают колбу для забрасываемой жидкости.
Различные манипуляции
Водяные бани и бани с аппаратами Варбурга, используемые для инактивации, инкубирования бактерий или постановки опытов с ними, должны содержать дезинфицирующее вещество. Для бань с холодной водой рекомендуется использовать 70%-ный пропиленгликоль. Предупреждение. В качестве дезинфицирующего вещества не следует применять азид натрия, так как он взрывоопасен.
Морозильники, сосуды с жидким азотом, контейнеры с сухим льдом и холодильники необходимо периодически проверять, чистить и обеззараживать. Во время их чистки пользуются резиновыми перчатками и защитными респираторами. Все инфекционные материалы, хранящиеся в холодильниках или морозильниках, снабжают этикетками.
Опасные жидкие культуры или жизнеспособные порошковые инфекционные материалы в стеклянных сосудах следует транспортировать, инкубировать и хранить в удобных для обращения небьющихся непроницаемых контейнерах, достаточно больших для того, чтобы вместить всю жидкость или порошок в случае утечки содержимого или разбивания стеклянного сосуда.
Засеянные среды в чашках Петри или твердые среды в других емкостях переносят и инкубируют в непроницаемых лотках или контейнерах.
Проливание бактериальных суспензий
При проливании бактериальной суспензии внутри биологически безопасного бокса опасность для персонала, находящегося в помещении, невелика. Тем не менее, чтобы избежать распространения инфекции, рекомендуется сразу же провести химическую дезинфекцию, причем это делают при включенной вентиляционной системе бокса. Стены, рабочие поверхности и оборудование опрыскивают или протирают дезинфицирующим составом. Смесь дезинфектанта с детергентом очищает поверхности, как от грязи, так и от бактерий. Подходящим в данном случае является 3%-ный раствор какого-либо иодофора (например, вескодин) или разведенный в соотношении 1:100 отбеливатель, используемый в домашнем хозяйстве (например, хлорокс), с добавлением 0,7% неионного детергента. Все процедуры выполняют в перчатках. Для обработки используют достаточное количество дезинфицирующего раствора так, чтобы он попал в сточные лотки и емкости под рабочей поверхностью. Поднимают переднюю решетку и поддон и протирают все поверхности. Протирают также сточный резервуар и дезинфицирующий раствор из него сливают в контейнер. Дезинфицирующий раствор, перчатки, обтирочную ткань и губки помещают в лоток и автоклавируют. При этом не продезинфицированными остаются лишь фильтры, вентилятор, воздушные ходы и другие внутренние части бокса.
Если требуется продезинфицировать бокс изнутри, то это делают с помощью газообразного формальдегида. Отвешивают 0,3 г хлопьевидного параформальдегида на 0,03 м3 пространства бокса и на электроплитке вносят его внутрь бокса так, чтобы питающий шнур плитки выходил наружу. Влажность внутри бокса поднимают примерно до 70%, выпаривая на плитке воду. Температуру нагрева плитки с параформальдегидом поддерживают на уровне 292°С. Окно бокса закрывают полиэтиленовой пленкой, закрепляя ее клейкой лентой. Если воздух из бокса выходит в комнату, то к вытяжному отверстию бокса прикрепляют гибкий шланг и подводят его к вентиляционной решетке комнаты. Когда в здании используется система рециркуляции воздуха, шланг прикрепляют к открытому окну или двери. Если же воздух из бокса поступает непосредственно в вытяжную систему здания, то задвижку тяги закрывают. Для деполимеризации параформальдегида включают плитку. После того как деполимеризуется половина параформальдегида, примерно на 3 с, включают вентилятор бокса, чтобы формальдегид распространился по всему объему. После полной деполимеризации вновь включают вентилятор на 3 с. Затем оставляют бокс, по крайней мере, на 1 ч. После этого открывают задвижку тяги бокса, обеспечивая поступление воздуха в гибкий шланг, разрезают полиэтиленовую пленку, закрывающую окно, и включают вентилятор бокса. Бокс вентилируют в течение нескольких часов, чтобы удалить все следы формальдегида.
Проливание потенциально опасного биологического материала в лаборатории вне биологически безопасного бокса может подвергнуть риску тех, кто там находится. Если это произошло, прежде всего, надо избежать вдыхания любого материала, находящегося в воздухе, для чего задерживают дыхание и покидают лабораторию. Те, кто находился в помещении, предупреждают остальных об опасности и идут под душ или в раздевалку. Когда известно или есть подозрение, что заражена одежда, ее осторожно снимают, складывая зараженными местами внутрь, а затем кладут в мешок или загружают непосредственно в автоклав. Моют предположительно подвергшиеся заражению места, а также руки и лицо. Не заходят вновь в лабораторию в течение 30 мин, чтобы дать возможность осесть образовавшимся при проливании капелькам аэрозоля. Перед тем как войти в лабораторию, чтобы вымыть место, где была пролита суспензия, надевают защитную одежду (резиновые перчатки, обувь, которую можно автоклавировать, накидку и респиратор). Если суспензия была пролита на пол, не рекомендуется надевать хирургический халат, который может соприкасаться с полом при нагибании. Рядом с местом, где пролили суспензию, ставят контейнер для отходов, переносят туда крупные куски зараженного материала и закрывают его крышкой. Место, где виден пролитый материал, и вокруг него осторожно поливают раствором гипохлорита, содержащим 1000 ч. на млн. доступного хлора, раствором йодофора, содержащим 1600 ч. на млн. йода или другим подходящим дезинфицирующим агентом. Обработку производят в течение 15 мин, избегая брызг. Затем бумажным или матерчатым полотенцем вытирают дезинфицирующий раствор и пролитый материал по направлению к центру. Грязные полотенца сразу же бросают в контейнер для отходов. Контейнер для отходов, особенно дно, протирают снаружи полотенцем, смоченным в дезинфицирующем растворе, и помещают его и другие материалы в автоклав для стерилизации. Снимают обувь, верхнюю накидку, респиратор и перчатки и стерилизуют их в автоклаве. Моют руки и лицо и, если можно, принимают душ.
Инструменты
Зараженные шприцы, инструменты, термометры, пипетки и стеклянная посуда перед новым использованием должны быть обеззаражены. Если возможно, конечную обработку следует проводить паром для жаропрочных предметов или окисью этилена для неустойчивых к нагреванию и чувствительных к влаге материалов. В тех случаях, когда перед употреблением необходимо обеззараживание, для дезинфекции используют раствор 2%-ного глутарового альдегида. Предметы полностью погружают в раствор на 20-30 мин. При этом полная безопасность не гарантируется, если предмет не был предварительно вымыт или если раствор уже использовали ранее. Перед повторным употреблением инструменты необходимо тщательно прополоскать в дистиллированной воде, а если они предназначены для работы в полости тела животного или на его поверхности, то в стерильной дистиллированной воде.
Лабораторные пипетки обеззараживают погружением в дезинфицирующий раствор, например 2%-ный о-фенилфенол, налитый в вертикальную или горизонтальную емкость. Стеклянную посуду погружают полностью. Перед использованием стеклянную посуду стерилизуют паром.
Руки
Для обычного мытья рук в лаборатории, когда не имеют дела с инфекционными агентами, можно применять разные моющие средства. Тщательное мытье рук в течение 15-20 с дезинфектантом приводит к сокращению числа бактерий более чем на 50%.
Мыло в кусках использовать не рекомендуется не только из-за грязи в мыльнице, но также потому, что некоторые микроорганизмы сохраняют жизнеспособность на мыле в течение некоторого времени. Если в резервуар с жидким мылом не добавлять предохраняющих средств, то там могут постепенно вырасти многочисленные популяции бактерий. В этом случае резервуар следует вымыть обычным способом и налить туда новое мыло. Порошковые и листовые мыла имеют то преимущество, что они не загрязняются бактериями и бактерии не способны расти на них.
Быструю дезинфекцию рук после загрязнения производят одним из следующих способов:
1) моют руки щеткой 30-60 с смесью дезинфектанта и детергента и ополаскивают их водой;
2) моют руки щеткой 30-60 с смесью 4%-ного хлоргексидина и детергента и ополаскивают водой;
3) моют руки 20-30 с смесью фенольного дезинфектанта и детергента и затем ополаскивают водой (некоторые фенольные производные при слишком частом использовании в слишком больших концентрациях могут вызвать депигментацию смуглой кожи);
4) смачивают руки спиртом (50-70%) на 20-30 с, затем моют их щеткой с мылом в течение 10-15 с и ополаскивают водой.
3. Общие положения при работе.
Работа с патогенными биологическими агентами (ПБА) проводится в специфических условиях, которые могут отрицательно влиять на здоровье работающих. Важнейшей особенностью этой работы является риск заражения патогенными микроорганизмами лабораторных работников и лиц, непосредственно контактирующих с ними, а также загрязнения окружающей среды.
Все это обусловливает необходимость создания в лабораториях условий, обеспечивающих безопасность персонала и окружающей среды от возможного воздействия патогенных агентов. Поэтому параллельно развитию микробиологии постоянно разрабатываются и и совершенствуются методы безопасной работы и средства защиты персонала и окружающей среды.
Существующие в настоящее время приемы и правила работы с ПБА (защитные устройства, противоэпидемические и технические мероприятия, определенный уровень автоматизации) в значительной мере обеспечивают предотвращение внутрилабораторных заражений, но полностью исключить их не могут, на что указывают периодически возникающие случаи заболевания вследствие заражения при лабораторной работе.
Обеспечение биологической безопасности при работе с ПБА включает два основных фактора: человеческий и технический.
Правильность действий человека в комплексе мер, обеспечивающих безопасное проведение работ с биоматериалом, в значительной степени обусловлена уровнем профессиональной подготовки и характерологическими особенностями индивидуума. Готовность сотрудника к самостоятельным действиям в случаях непредвиденных обстоятельств (авариях) может быть повышена соответствующей подготовкой и тренировкой. Хорошее знание основ обеспечения биологической безопасности, представление о возможных источниках заражения, свойствах используемых агентов, принципах функционирования защитных устройств и приспособлений, причинах возникновения аварий, а также владение навыками предупреждения и устранения таких ситуаций позволяет свести к минимуму значение «человеческого фактора» в возникновении лабораторных заражений.
Технический осмотр (оборудование, планировка, защитные системы, средства индивидуальной защиты, безопасные методы работы и др.) поддается совершенствованию, ведению контроля и страховочных механизмов. Необходимость четкой регламентации условий и организации работы с ПБА обусловила потребность в разработке соответствующей классификации микроорганизмов по степени их опасности непосредственно работающему («индивидуальная опасность») и окружающим («общественная безопасность»).
В соответствии с санитарными правилами (СП 1.3.1285-03) все микроорганизмы разделены на 4 группы патогенности (отдельные микроорганизмы приведены в приложении 1):
I группа – высокая индивидуальная и общественная опасность (высокая контагиозность инфекции, отсутствие эффективного лечения и профилактики, тяжелое течение заболевания, высокая летальность);
II группа – высокая индивидуальная опасность (возможность распространения инфекции ограничена);
III группа – невысокая опасность для окружающих; IV группа – условно – патогенные микроорганизмы(как правило они не вызывают заболевания у работающих с ними лиц).
В ветеринарной практике кроме названной выше используется классификация микроорганизмов, основанная на степени их опасности для животных. При определении уровня защиты персонала необходимо руководствоваться классификацией микроорганизмов, патогенных для человека.
Классификация патогенных биологических агентов, принятая в РФ, отличается от классификации в других странах, где наиболее опасные агенты отнесены к IV группе, а наименее опасные к I группе.
3. Лабораторные заражения
Причина инфицирования – это совокупность условий, ведущих к нарушению изоляции инфекционного материала в результате аварий или несоблюдения правил работы, что создает возможность заражения персонала или распространения инфекции в лаборатории, а также ее выхода в окружающую среду.
Анализ случаев лабораторного заражения или аварий имеет важное практическое значение. Он позволяет выявить наиболее опасные процедуры, источники и причины инфицирования персонала, а также пути распространения инфекции. На основе анализа должна проводиться разработка необходимых мероприятий, направленных на обеспечение безопасности персонала и охрану окружающей среды.
Существенную роль в оценке опасности внутрилабораторных заражений играют пути и способы переноса и распространения патогенных агентов.
Источники, пути и причины заражения лабораторного персонала весьма разнообразны. Потенциальным источником инфекции в лабораторных условиях является любой инфекционный материал (культуры, пробы, экспериментальные животные, отработанный материал и т. д.).
Анализу источников инфекции при лабораторном заражении посвящено много публикаций, в основном зарубежных авторов (A. Wedum, R. Pike, C. Collins и д. р.). Источники инфекции могут быть разделены на две группы – первичные и вторичные. Первичные источники связаны непосредственно с объектами исследований; вторичные – опосредованно, как результат неконтролируемого выхода инфекции и загрязнения поверхностей, оборудования, воздуха и т. д.
Пути поступления патогенных агентов в организм человека различны (через рот, органы дыхания, кожу, слизистые).
Для оценки относительной опасности инфицирования человека различными патогенными агентами важно знать заражающую дозу каждого агента, то есть число микроорганизмов, вирусных частиц или других агентов, приводящее к заражению. Заражающие дозы варьируют в больших пределах, и величина дозы зависит от пути поступления и состояния организма человека.
ЗАРАЖАЮЩИЕ ДОЗЫ НЕКОТОРЫХ ПАТОГЕННЫХ
БИОЛОГИЧЕСКИХ АГЕНТОВ
R. Clarke, C. Collins
|
Патогенный биологический агент |
Путь заражения |
Доза |
|
Лихорадка Денге |
Ингаляционный |
2,0*100 |
|
Лихорадка Цуцугамуши |
Внутрикожный |
3,0*100 |
|
Лихорадка Ку |
Ингаляционный |
1,0*101 |
|
Туляремия |
Ингаляционный |
1,0*101 |
|
Шигелла Флекснера |
Скармливание |
1,8*102 |
|
Сибирская язва |
Ингаляционный |
1,3*103 |
|
Сап |
Ингаляционный |
3,2*103 |
|
Холера |
Скармливание |
1,0*108 |
|
Кишечная палочка |
Скармливание |
1,0*108 |
Заражение человека микроорганизмами, с которыми ведется работа в лаборатории, регистрируются на протяжении всего периода существования микробиологии и рассматриваются как убедительное подтверждение профессиональной опасности и профессионального риска, связанного с работой в лаборатории.
К сожалению, в России статистика лабораторных заражений в доступной литературе отсутствует.
Первые случаи документированных лабораторных заражений исследователей (брюшным тифом) относятся к 1885г., а сообщение о них было опубликовано в 1915г. В последующие годы число зарегистрированных случаев возрастало пропорционально расширению исследований с патогенным материалом.
R. Pike провел обстоятельный анализ 3921 случая внутрилабораторных заражений, имевших место в 1930-74 годы в США и некоторых европейских странах. Из опубликованных данных следует, что лабораторные заражения были вызваны более чем 160 видами микроорганизмов, в том числе бактериями – 37, вирусами – 90, риккетсиями – 9, хламидиями – 3, грибками – 9, простейшими – 16.
Заболевания, вызванные бактериями, составили 42,6% (1669 случаев, из них с летальным исходом – 4,1%); вирусами – 26,7% (1049 случаев, летальных – 5,1%); риккетсиями – 14,6% (573 случая, летальных – 5,6%). Наибольшее число заболеваний зарегистрировано вследствие заражения бруцеллезом – 423 человека (10,8%). Высокая летальность отмечена автором при лабораторных заражениях гепатитом В – 71%, чумой – 40%, холерой – 33%, желтой лихорадкой – 22%, пятнистой лихорадкой скалистых гор – 18%, лептоспирозом – 15%.
По данным R. Pike и J. Richardson отмечены редко встречающиеся групповые внутрилабораторные заражения в одной и той же лаборатории: из 423 случаев заражения бруцеллезом – 45, из 60 случаев болезни Кьясанурского леса – 53, из 45 случаев кожной формы сибирской язвы – 23.
Описаны вспышки заболеваний натуральной оспой в Англии (1979г.) и ФРГ (1980г.); туберкулеза – США (1980г.); лихорадки Ку – США и ФРГ (1982г.). Большинство из них связано с выносом инфекции за пределы лабораторий и заболеванием лиц, не имеющих непосредственного отношения к экспериментальным исследованиям.
Из всех лабораторных заражений на долю аварий пришлось только 17,9% и, таким образом, аварии не могут рассматриваться как ведущая причина их возникновения. Аэрозоль являлся причиной документально подтвержденных заражений в 13,3% случаев. Контакт с зараженными животными и эктопаразитами обусловил возникновение 16,8% случаев инфицирования; проливание и разбрызгивание инфицированной жидкости – 26,7%; аварии со шприцами и иглами – 25,2%. К настоящему времени показано, что при работе с животными одним из основных источников инфекции является аэрозоль, образующийся из-за распыления высыхающих инфицированных частиц выделений животных. В значительной части случаев (827 или 21,1%) в качестве заражения указан только факт работы с инфекционным материалом. С большей долей вероятности можно предположить, что источником заражений явился аэрозоль. Случаи лабораторных заражений, в которых аэрозоль явился установленной причиной заражения, или его роль можно предполагать, составляют большинство – 71,2% (по данным других авторов – 75%). Некоторые факторы риска, связанные с использованием технических средств и инструментов, приведены в таблицах (1,2)
Таблица 3
|
Вид оборудования, инструментария |
Фактор риска |
|
Шприцы для инъекций, иглы |
Укол, образование аэрозоля, утечка материала |
|
Центрифуга |
Аэрозоль, разбрызгивание материала, повреждение пробирок |
|
Анаэробные стаканы |
Взрыв, разбрызгивание инфекционного Материала |
|
Гомогенизаторы, измельчители Тканей |
Аэрозоль, протечка |
|
Культуральные мешалки и Шейкеры |
Аэрозоль, разбрызгивание, Разливание |
|
Аппараты лиофильной сушки |
Аэрозоль |
|
Ферментаторы |
Аэрозоль, разбрызгивание, разливание |
|
Пипетирующие средства |
Аэрозоль, разбрызгивание |
|
Боксы биологической безопасности |
Аэрозоль (при нарушении правил пользования) |
Многочисленными исследованиями показано, что образованием инфекционного аэрозоля сопровождается большинство манипуляций, проводимых и инфицированным материалом. По данным отдельных авторов при исследовании по определению количественных показателей образования инфекционного аэрозоля при выполнении различных видов лабораторных работ проведены расчёты для каждой манипуляции фактора распыления (отношение количества частиц вирусов или бактерий, выбрасываемых в воздух за 1 мин., к их концентрации в 1 мл исходного материала). Приводимые авторами факторы распыления для отдельных манипуляций имеют следующие значения: работа пипеткой с образованием пузырьков жидкости – 1*104, с каплями жидкого инфекционного материала – 3*105; внутриносовое заражение белых мышей – 2*107; удаление пробки из пробирки с инфекционным материалом – 2*109.
Ниже представлены следующие отдельные причины и частота лабораторных заражений при проведении различных работ.
Таблица 4
|
№ п/п |
Вид происшествия (аварийная ситуация) |
% |
|
1 |
2 |
3 |
|
1 |
Случайное попадание в организм заразного материала в результате укола или пореза (иглы, скальпели, бой посуды и т. д.) |
41,1 |
|
1 |
2 |
3 |
|
2 |
Заглатывание материала при пипетировании ртом, прием пищи в лабораториях, курение и т. д. |
13,1 |
|
3 |
Разбрызгивание инфицированной жидкости, что обычно бывает при нарушении правил работы с микроорганизмами (недостаточном закреплении иглы в шприце, падение капли с пипетки на рабочую поверхность стола, ненадлежащей фиксации животных и т. д. |
25,2 |
|
4 |
Работа с экспериментальными или экспериментально инфицированными животными: 1) приматы являются носителями гепатита В в 1-3%, и лабораторное заражение им характеризуется тяжелым течением и высокой летальностью; 2) кормление животных, перемещение, укусы, царапины, укус эктопаразитов, вдыхание высохших экскрементов, слюны и т. д. — укусы, царапины; — частота выделения микроорганизмов из мочи и фекалий лабораторных животных при — сибирской язве, бруцеллезе и мелиоидозе; — лихорадке Ку; — пситтакозе; — венесуэльском энцефаломиелите лошадей; — клещевом энцефалите |
87,5 13,5 100 72,7 75 50 80 |
|
5 |
Использование оборудования и инструментария, способных создать потенциальную опасность заражения |
|
|
6 |
Вторичные (опосредованные) источники заражения, к которым относятся: — контаминированный персонал; — аэрозоль, проникающий из других помещений; — средства индивидуальной защиты; — неисправное оборудование; — системы водоснабжения, вентиляции, кондиционирования воздуха, канализации; — жидкие отходы; — мусор; — и. т.д. |
Одними из наиболее опасных за последние годы (2004 – 2005 гг.), по официальным сообщениям (Приложение к ЕИКЗР «ООИ в мире» 2004 г.) внутрилабораторными заражениями явились случаи заражения связанные с вирусом Эбола:
— 2004 г. (февраль): Форт Детрик, Мэриленд (США) – ранение при проколе иглой (выздоровление);
— 2004 г. ( май): Государственный исследовательский центр вирусологии и биотехнологии (Вектор), Кольцово, РФ – ранение при проколе иглой (летальный исход 19 мая)
Таким образом, к настоящему времени достаточно изучены возможные источники и пути заражения персонала микробиологических лабораторий, а также пути попадания инфекционного агента в окружающую среду. Эти данные должны использоваться для оптимизации техники лабораторной работы и надлежащей организации технологического процесса с целью обеспечения соответствующего уровня биологической безопасности.
Необходимо отметить, что основной причиной, обеспечивающей эффективность мероприятий по профилактике внутрилабораторных заражений персонала и недопущения эпидемиологических осложнений, является «человеческий фактор», т. е. квалификация и дисциплинированность сотрудников.
Проблема профилактики внутрилабораторных заражений и предотвращение попадания контаминированного материала в окружающую среду имеет важное противоэпидемическое и социально-экономическое значение. Изучение и оценка различных аспектов опасности при работе с микроорганизмами должны являться одной из главных задач санитарно-эпидемиологической службы. Только на основе этих данных можно обоснованно и грамотно разрабатывать комплекс санитарно-гигиенических, профилактических и противоэпидемических мероприятий, направленных на защиту персонала и окружающей среды. Эти данные также могут служить основой для объективной оценки организации работ с микроорганизмами.
В России разработан комплекс организационных мероприятий по обеспечению биологической безопасности при работе с микроорганизмами I-II групп патогенности. Эти мероприятия изложены в документах, перечисленных в разделе 2 «Нормативные ссылки». В дополнение к регламентированному комплексу мероприятий в последние годы в учреждениях с целью своевременного выявления специфических заболеваний, ретроспективного подтверждения факта воздействия ПБА на персонал и контроля динамики уровня специфических антител за рубежом создаются банки сывороток крови сотрудников, а при оформлении на работу с ПБА – определяться чувствительность сотрудников к специфическим лечебным препаратам (антибиотикам, иммуноглобулинам и т. д.).
В настоящее время имеется реальная возможность использования ПБА в качестве биологического оружия в террористических целях. В учреждениях, проводящих работы с ПБА, имеются условия по наработке микробной массы. Для предупреждения наработки ПБА в непроизводственных целях и их несанкционированной передачи, для осуществления Госсанэпиднадзора на объектах, использующих микроорганизмы I-II групп патогенности, необходимо в обязательном порядке проводить контроль учета условий хранения, целевого использования ПБА согласно пояснительной записке по организации работ с ними.
4. Общие правила.
Базовые лаборатории – уровни
биологической безопасности 4 и 3
Работа с микроорганизмами 3-й и 4-й группами риска осуществляется согласно общим правилам и рекомендациям для базовых лабораторий с уровнями безопасности для этих групп. Хотя некоторые из мер предосторожности могут не потребоваться при работе с микроорганизмами группы риска 4, однако они желательны в учебных целях для обеспечения адекватной (т. е. безопасной) техники микробиологических исследований.
Поскольку ни в одной больничной или клинической лаборатории нет полного контроля за поступающими образцами, возможен случайный и неожиданный контакт персонала с агентами более высокого риска. Вероятность такого контакта следует предусматривать при разработке мер и действий по обеспечению безопасности.
Представленные общие рекомендации для 3-й группы биологической безопасности являются всеобъемлющими и подробными, поскольку служат основой для работы всех классов лабораторий. Общие правила для изолированной лаборатории – биологической безопасности 2-й группы и максимально изолированной лаборатории – биологической безопасности 1-й группы представляют собой правила для 3-й группы, модифицированные для работы с более опасными микроорганизмами.
Код практической работы
Представленный код – это перечень жизненно важных лабораторных процедур, которые служат основой безопасности лабораторной практики. В ряде лабораторий и национальных лабораторных программ такие коды могут иметь статус «Правил». В данной главе и других разделах публикации подробно изложены и разъяснены различные составляющие кода практической работы.
Правильно организованная работа – это основа биобезопасности лаборатории. Она не может быть заменена специальным оборудованием, которое лишь дополняет ее.
Перечисленные ниже важнейшие правила изложены в порядке, который необязательно соответствует степени их важности.
1. Международный код биологической опасности должен быть изображен на дверях комнат, где проводятся работы с микроорганизмами групп риска 1,2,3.
2. Не разрешается прием и хранение пищи и питья, курение и применение косметических средств в лабораторной зоне.
3. В лабораторных помещениях должны поддерживаться порядок и чистота, в них не должно быть материалов, не имеющих отношения к работе.
4. Рабочие поверхности следует немедленно дезинфицировать после загрязнения потенциально опасным материалом и в конце рабочего дня.
5. Работники лаборатории должны мыть руки после манипуляций с инфекционным материалом и в конце рабочего дня.
6. Все технические процедуры следует проводить таким образом, чтобы свести к минимуму возможность образования аэрозолей.
7. Все зараженные материалы, образцы и культуры должны быть обеззаражены перед удалением из лаборатории или повторным использованием. Они должны быть помещены в герметичные пластиковые пакеты с разноцветными метками (обозначает класс отходов) для автоклавирования или хранения. Эти емкости должны храниться в жестких контейнерах. При необходимости перемещения пакетов вне лаборатории для обеззараживания их следует поместить в герметичные (т. е. с твердым дном) контейнеры, которые необходимо закрыть перед выносом из лаборатории.
8. В лаборатории следует носить специальную одежду или халаты. В этой одежде нельзя находиться вне лабораторных помещений, а именно в офисах, библиотеках, комнатах персонала или хранилищах. Зараженная одежда должна быть дезинфицирована соответствующими средствами.
9. Нельзя носить обувь с открытым носом.
10. Защитная лабораторная одежда не должна храниться в тех же шкафчиках или ящиках, что и личная.
11. При необходимости предохранить глаза и лицо от брызг и попадания инфицированного материала следует надевать защитные очки, экраны, козырьки, маски и другие защитные средства.
12. В рабочую зону лаборатории должны допускаться лишь лица, которые прошли инструктаж по технике безопасности и выполнили специфические защитные требования (например, иммунизация); двери лаборатории должны быть закрыты во время работы; доступ в виварий разрешается только специальному персоналу; в рабочих зонах недопустимо пребывание детей.
13. Следует разработать программы, определяющие порядок работы с насекомыми и грызунами.
14. Животных, с которыми не производится непосредственная работа, следует содержать вне лаборатории.
15. Шприцы и иглы должны использоваться только для парентеральных инъекций и аспирации жидкости у лабораторных животных. Их использование для забора содержимого из емкостей должно быть ограничено (емкости следует открывать и использовать пипетки). Шприцы и иглы нельзя использовать как заменители автоматических пипеток при манипуляциях с инфицированными жидкостями. Там, где возможно, острые иглы следует заменить канюлями.
16. При всех процедурах, которые могут сопровождаться случайными прямыми контактами с кровью, инфекционным материалом или зараженными животными, необходимо надевать перчатки.
17. Обо всех случаях разлива инфекционного материала, ситуациях, чреватых неопределенными последствиями, подозрениях на контакт с инфекционными материалами следует немедленно доложить руководителю лаборатории. Необходимо подготовить письменное донесение (рапорт) о происшествии.
18. Необходимо обеспечить соответствующую медицинскую оценку, наблюдение, экстренную профилактику и лечение.
19. У всего лабораторного и другого, имеющего отношение к инфекционному материалу персонала, рекомендуется периодически собирать фоновые пробы сыворотки крови. Они должны храниться соответствующим образом. Дополнительные пробы следует периодически повторно собирать в зависимости от агентов, с которыми работают и лаборатории, и выполняемых задач (рекомендация).
20. Руководитель лаборатории отвечает за обучение персонала по технике безопасности лабораторных работ. Следует иметь инструкции по технике безопасности и лабораторные пособия, определяющие известную и потенциальную опасность работ, а также приемы и методы, сводящие к минимуму или исключающие такую опасность. Персонал должен быть информирован об особенностях работы с опасным материалом, а также обязан изучать соответствующие инструкции по применению стандартных правил и техники безопасности работ, и следовать им. Руководитель лаборатории должен быть уверен, что персонал их понимает.
Особенности проектирования и
оборудования базовых лабораторий
1. Для безопасного проведения лабораторных процедур необходимо обеспечить достаточное пространство.
2. Стены, потолок и полы должны быть гладкими, легко моющимися, непроницаемыми для жидкостей, устойчивыми для реактивов и дезинфицирующих средств, обычно употребляемых в лаборатории. Полы не должны быть скользкими. Выступающие и проходящие трубы должны располагаться на достаточном расстоянии от стен. С горизонтально расположенных поверхностей необходимо удалять пыль.
3. Для проведения любых работ необходимо обеспечить достаточное освещение. Следует избегать нежелательного отражения.
4. Поверхность сидений и полок должна быть водонепроницаемой и устойчивой к действию дезинфицирующих средств, кислот, щелочей, органических растворителей и достаточно жаропрочной.
5. Лабораторная мебель должна быть прочной. Открытые поверхности между и под полками, скамьями, шкафами и оборудованием должны быть доступны для уборки.
6. Для размещения приборов и оборудования первой необходимости следует выделить достаточное пространство, чтобы не создавать беспорядок на полках и в проходах. Необходимо обеспечить также достаточные складские помещения, которые следует удобно располагать вне рабочей зоны лаборатории.
7. Раковины, по возможности с проточной водой, следует размещать в каждой лабораторной комнате, предпочтительно ближе к выходу.
8. Двери должны соответствовать правилам противопожарной безопасности, быть самозакрывающимися и иметь окна для наблюдения.
9. Автоклав (или приемлемый его заменитель) для обеззараживания должен размещаться в том же здании, что и лаборатория.
10. Помещения для хранения верхней одежды и личных вещей, а также для приема пищи и курения должны располагаться вне рабочей зоны лаборатории.
11. Следует выделить помещения для безопасной работы с растворителями, радиоактивными материалами и сжиженными (или под давлением) газами и для их хранения.
12. Системы безопасности должны предусматривать противопожарную и электробезопасность, душ срочной обработки и средства промывания глаз.
13. Необходимо обеспечить готовность соответственно оборудованных помещений или зон для оказания первой помощи.
14. Важно, чтобы в лаборатории была регулируемая подводка воды хорошего качества. Не должно быть соединений между источниками воды для лабораторных целей и для питья.
15. Необходимо иметь надежный источник электропитания соответствующей мощности, а также дежурное освещение с указанием запасного выхода. Желательно наличие резервного генератора для обеспечения основного оборудования – инкубаторов, термостатов, холодильников и т. п.
16. Требуют специального внимания три аспекта удаления отходов в соответствии с требованиями контроля загрязнения окружающей среды:
— автоклавы для обработки твердых отходов нуждаются в специальных помещениях и обслуживании;
— печи для сжигания отходов должны быть специально спроектированы и оборудованы устройствами для сбора воды и дымоуловителями;
— отработанные и сточные воды, удаляемые из лаборатории, должны подвергаться специальной обработке.
17.Лаборатории и помещения для животных иногда бывают объектами актов
вандализма. Для исключения возможных конфликтов должны быть обес —
печены надежная защита и противопожарная безопасность. Из соображе-
ния безопасности необходимы прочные двери и зарешеченные окна, ко —
личество ключей должно быть ограничено.
5. Медицинский контроль и наблюдение за здоровьем
Целью медицинского контроля и наблюдения за здоровьем персонала лаборатории являются:
— выявление высокочувствительных к лабораторной инфекции лиц для предотвращения профессиональных заболеваний, а также регулярное обследование вновь принятых на работу;
— проведение в установленные сроки активной и пассивной иммунизации работающих;
— обеспечение ранней диагностики внутрилабораторной инфекции;
— оценка эффективности защитного оборудования и процедур.
Руководство лаборатории в лице ее заведующего несет ответственность за проведение медицинского контроля и наблюдения за здоровьем лабораторного персонала.
Принципы медицинского наблюдения сотрудников, работающих с
микроорганизмами группы риска 4
Данные микроорганизмы не вызывают заболеваний человека или инфекции лабораторных животных ветеринарного значения. В идеале, однако, персонал лаборатории должен подвергаться анамнестическому обследованию, относящемуся к периоду до принятия на работу. Желательна своевременная информация о заболеваниях и происшествиях в лаборатории, которые могут к ним привести; персонал лаборатории должен сознавать необходимость поддержания мер и средств техники безопасности на соответствующем уровне.
Принципы наблюдения сотрудников, работающих с
микроорганизмами группы риска 3
1. Необходим медицинский контроль лиц, вновь принимаемых на работу, или лиц, переходящих на новое рабочее место. Такой контроль должен предусматривать сбор анамнестических данных. Могут быть полезными, а в некоторых случаях и необходимыми, клиническое обследование и забор исходящих проб сыворотки крови.
2. В лаборатории должен быть список врачей, у которых наблюдаются члены семей сотрудников.
3. Руководитель лаборатории должен вести записи о заболеваниях сотрудников и пропусках ими рабочих дней; в обязанности каждого сотрудника и его лечащего врача входит информирование руководителя лаборатории обо всех пропусках работы, связанных с болезнью.
4. Женщины детородного возраста должны ясно осознавать риск бесплодия, связанный с лабораторным заражением такими микробиологическими агентами, как вирус краснухи. Необходимые меры защиты плода варьируют в зависимости от микроорганизма, с которым женщина находилась в контакте.
6. Организация предупредительного
санитарно-эпидемического надзора
Ответственным за организацию работы с ПБА по учреждению в целом является его руководитель, а по подразделениям – их заведующие.
Контроль выполнения требований биологической безопасности при работе с микроорганизмами I-IV групп патогенности осуществляют: в учреждении – комиссия по контролю за соблюдением требований биологической безопасности, в подразделении – лицо, определенное приказом по учреждению.
Государственный санитарно-эпидемиологический надзор за работой с патогенными биологическими агентами осуществляют учреждения госсанэпидслужбы, руководствуясь действующими нормативными документами, регламентирующими порядок организации и условия проведения исследований с ПБА. Общегигиенические параметры (площади рабочих помещений, освещенность, микроклимат и др.) регламентированы соответствующими санитарными правилами и нормами.
С целью адекватной оценкой условий труда лиц, работающих с ПБА, соблюдения требований биологической безопасности, профилактики внутрилабораторных заражений и охраны окружающей среды необходимо особо тщательно рассматривать предлагаемый порядок организации работ на этапе получения санитарно-эпидемиологического заключения и лицензии. При проведении санитарно-эпидемиологической экспертизы условий работы с ПБА необходимо тщательно изучить имеющиеся в подразделении следующие организационные и инструктивно-методические документы:
1. Пояснительную записку по организации работ с ПБА, в которой должно быть указано:
1.1. Наименование подразделения.
1.2. Перечень возбудителей, с которыми планируется проведение работ.
1.3. Место размещения подразделения. К текстовой части прилагается графический материал (схема планировочного решения подразделения с указанием назначения помещений, размещения оборудования, разводки систем вентиляции, отопления, канализации, водоснабжения и воздухообеспечения изолирующих средств индивидуальной защиты, а также схемы движения инфекционного материала, персонала и отходов).
1.4. Отделка помещений (стены, полы, герметизация оконных проемов, дверей и т. д.).
1.5. Краткое описание технологии работ, проводимых в каждом помещении (выполняемые операции).
1.6. Виды проводимых исследований (диагностические, экспериментальные, производственные). Объем биомассы, с которым будет проводиться работа. Используемые лабораторные животные, членистоногие и т. д., порядок их содержания.
1.7. Наличие и порядок использования защитных укрытий (боксы, ламинарные шкафы, стекла Фурко и т. д.).
1.8. Режим работы защитных вентилируемых укрытий (направленность воздушных потоков, очистка воздуха, обработка отходов, место выброса вытяжного воздуха и т. д.).
1.9. Методы, кратность и результаты оценки эффективности работы вытяжных вентиляционных систем, а также защитная эффективность используемых фильтров.
1.10. Наличие и порядок работы санитарных пропускников. Место надевания и снятия, а также порядок и метод дезинфекционной обработки отдельных видов средств индивидуальной защиты.
1.11. Порядок дезинфекционной обработки помещений, использованного материала, лабораторной посуды, оборудования, жидких и твердых отходов. Перечень используемых средств и методов дезинфекции. Методы и кратность контроля качества дезинфекции.
1.12. Организация контроля за контаминацией поверхностей, воздуха и стоков.
1.13. Условия и порядок транспортировки (переноса) ПБА.
1.14. Данные о специальной подготовке персонала по безопасности работ с патогенными биологическими агентами.
1.15. Сроки вакцинации сотрудников, методы и результаты контроля ее эффективности (уровень специфических антител в сыворотке крови, результаты аллергических проб и т. д.).
1.16. Порядок допуска персонала к работе с ПБА (номер приказа и дата). Наличие журнала регистрации ежедневной термометрии и медицинских осмотров и ответственных за их ведение.
1.17. Использование неутвержденных методов (не сертифицированные тест-системы) и методических приемов.
1.18. Наличие и дата утверждения документа о порядке организации работ с ПБА и соблюдению требований биологической безопасности в учреждении.
1.19. Порядок ведения и перечень используемых учетных форм.
1.20. Место и условия хранения патогенного материала (включая музейные культуры), порядок допуска в хранилище.
1.21. Организация медицинского наблюдения за состоянием здоровья работающих. Результаты прохождения периодического медицинского осмотра (последний акт и дата утверждения).
1.22. При работе с микроорганизмами 1-й – 2-й группами патогенности (опасности) требуется наличие плана мероприятий на случай выявления лиц, подозрительных на специфическое заболевание (кем утвержден, кем согласован, дата). Примерная схема плана дана в приложении 1.
1.23. Наличие документа о порядке проведения мероприятий при авариях или чрезвычайных ситуациях, а также материально-техническое обеспечение их проведения. Примерная схема плана дана в приложении 1.
1.24. Сведения о назначении ответственного за соблюдение требований биологической безопасности (номер приказа, дата).
1.25. Контроль качества проведения дезинфекционных мероприятий.
1.26. Наличие предыдущего санитарно-эпидемиологического заключения на проведение работ с ПБА (кем выдано, дата и номер).
1.27. Сведения о регистрации в подразделении в течение последнего года аварий (кратко причина и последствия).
2. Акт объектовой комиссии по контролю соблюдения требований биологической безопасности с заключением комиссии о готовности лаборатории к проведению работ, ограниченной готовности (с указанием причин), отсутствия готовности (с обоснованием заключения). При проведении обследования необходимо оценить и проверить:
2.1. Реальную возможность выполнения предполагаемого вида и объема работ в конкретных помещениях.
2.2. Соответствие планировочных решений и оснащения сведениям, указанным в пояснительной записке, подготовленной подразделением.
2.3. Соответствие положений имеющегося внутреннего документа по организации работ и соблюдению требований биологической безопасности требованиям действующих нормативных документов. Указанный внутренний документ должен быть утвержден руководителем учреждения и согласован с учреждением госсанэпиднадзора. В нем подробно излагается технология проведения работ с ПБА, операции, выполняемые в каждой комнате, меры безопасности персонала, мероприятия по защите окружающей среды, порядок организации медицинского наблюдения за персоналом в рабочие и выходные дни, сроки ревакцинации, объем и порядок проведения дезинфекционных мероприятий, контроль автоклавирования и т. д.
2.4. Реальность выполнения плана мероприятий по локализации и ликвидации возможных аварий и плана мероприятий на случай появления среди сотрудников специфических заболеваний с учетом имеющегося материально-технического, лечебно-профилактического и кадрового обеспечения (приложения 2 и 3).
2.5. Наличие необходимой учетной и иной документации, предусмотренной СП 1.3.1825-03, СП 1.2.735-99, СП 1.2.036-95 и другими нормативными документами.
2.6. Наличие документа о порядке проведения работ с зараженными животными или на отдельных видах потенциально опасного оборудования, разработанных с учетом соблюдения требований биологической безопасности.
2.7. Наличие в подразделении аптечки для оказания экстренной помощи пострадавшим в случае аварии, ее комплектность.
2.8. Эффективность функционирования систем вентиляции, оснащенность фильтрами тонкой очистки воздуха на вытяжке, методы, кратность и результаты оценки их защитной эффективности.
2.9. Наличие необходимого количества и номенклатуры используемых средств индивидуальной защиты. При использовании изолирующих средств и принудительной подачей воздуха оценить производительность системы воздухообеспечения, эффективность работы узлов воздухопроводки (очистка, подогрев, охлаждение).
2.10. Порядок и используемые методы контроля защитной эффективности противогазов, фильтрующих коробок, изолирующих костюмов и т. д.
2.11. Организацию обучения персонала правилам пользования средствами индивидуальной защиты, особенно изолирующими. Каждый сотрудник должен пройти теоретическую и практическую подготовку по их использованию.
2.12. Работу объектовой комиссии по контролю за соблюдением требований биологической безопасности (приложение 4).
2.13. Условия хранения и использования различных химических, радиоактивных и других веществ, применяемых при проведении отдельных операций в связи с угрозой сочетанного воздействия этих веществ и ПБА.
7. Организация
текущего санитарно-эпидемиологического надзора
При осуществлении текущего санитарно-эпидемиологического надзора необходимо обратить внимание на:
1. Соответствие организации проводимых работ данным, изложенным в пояснительной записке, представленной учреждению Госсанэпиднадзора для получения санитарно-эпидемиологического заключения на работу с ПБА (перечень ПБА, объём биоматериала и т. д.).
2. Работоспособность систем инженерного обеспечения (вентиляция, вентилируемые укрытия, обработка стоков, автоклавирование, герметичность ограждающих строительных конструкций, передаточные устройства, воздухоподготовка для шланговых средств индивидуальной защиты и т. д.), а также на организацию и методическую базу контроля эффективности их работы.
3. Порядок использования санитарных пропускников, средств индивидуальной защиты, наличие запаса средств индивидуальной защиты. Особое внимание следует обратить на порядок использования и организацию контроля защитной эффективности шланговых средств индивидуальной защиты, используемых при работе с аэрозолями и вирусами I группы патогенности.
4. Результаты и методы оценки контаминации ПБА воздуха рабочей зоны, поверхностей, оборудования, а также обработанных сточных вод (особенно при работе со споровыми формами).
5. Используемые дезинфицирующие средства, концентрации, условия и порядок приготовления рабочих растворов.
6. Наличие аварийных комплектов средств индивидуальной защиты, запасов дезинфекционных средств, распыливающих устройств, а также укомплектованность аптечек для оказания первой медицинской помощи пострадавшим при авариях.
7. Правильность ведения учетных форм и условия хранения ПБА.
8. Наличие и порядок ведения журналов медицинского наблюдения (термометрии), своевременность проведения инструктажей по соблюдению требований биологической безопасности и ревакцинации.
9. Наличие утвержденных инструкций по безопасной эксплуатации отдельных «опасных» видов оборудования и их знание сотрудниками.
10. Знание сотрудниками порядка обращения за медицинской помощью в случае заболевания на дому и их действия при возникновении аварий.
11. Использование в работе неутвержденных методик и приемов.
12. Наличие и реальность выполнения утвержденных планов мероприятий по ликвидации аварий и мероприятий при выявлении лиц, подозрительных на специфическое заболевание.
13. Организацию работы комиссии учреждения по контролю за соблюдением требований биологической безопасности в подразделениях.
14. Полноту, правильность и своевременность проведения мероприятий при имевших место авариях.
15. Использование лабораторной мебели и оборудования, отделка которых не позволяет проводить качественную дезинфекционную обработку.
16. Объем проводимых мероприятий, направленных на борьбу с грызунами и членистоногими.
17. Периодичность и полнота проверок, проводимых объектовой комиссией по контролю за противоэпидемиологическим режимом.
8. Техника обращения с центрифугами
Общие замечания
1. Техническая безопасность является необходимым условием микробиологической безопасности при использовании лабораторных центрифуг.
2. Работа с центрифугами должна проводиться в соответствии с инструкциями изготовителя.
3. Центрифуга должна быть расположена так, чтобы оператор даже ниже среднего роста мог видеть камеру и правильно размещать на ее дне стаканы и цапфы.
4. Вращающиеся части центрифуги и емкости должны ежедневно осматриваться для выявления возможных коррозии и трещин.
5. Центрифужные стаканы и цапфы, расположенные в центрифуге напротив друг друга, должны быть спарены по весу и тщательно уравновешены.
6. Для уравновешивания используется 70% пропанол. Во избежание коррозии металлических частей не разрешается использовать для уравновешивания раствор гипохлорита натрия.
7. По окончании центрифугирования емкостей, в которые помещаются пробирки, следует держать в вертикальном положении, чтобы полностью вытек балансировочный раствор.
8. При работе центрифуги могут образовываться взвешенные в воздухе частицы инфекционных материалов. Эти частицы двигаются слишком быстро, чтобы обеспечить их улавливание, если центрифуга помещена в обычные боксы I и II классов биологической безопасности.
9. Грамотное обращение с центрифугами и герметизация центрифужных пробирок («безопасные чашки») обеспечивают адекватную защиту от инфекционных аэрозолей и дисперсных частиц микроорганизмов агентов групп риска 3, 2 и 1.
Дополнительная информация на работе с центрифугами изложена в публикациях, указанных в списке литературы.
Центрифугирование микроорганизмов и материалов группы риска 3
1. Центрифужные пробирки и контейнеры с образцами, подлежащие центрифугированию, должны быть выполнены из толстостенного стекла или пластика; для выявления возможных дефектов их следует проверять перед центрифугированием.
2. Центрифужные пробирки и контейнеры для образцов должны быть снабжены крышками.
3. Внутреннюю поверхность центрифужной камеры следует ежедневно осматривать для выявления пятен грязи на уровне ротора. При их наличии результаты центрифугирования считаются неверными.
4. Угловые насадки не следует использовать для микробиологических исследований, за исключением случаев применения их в специальных высокоскоростных центрифугах.
5. За исключением ультрацентрифужных и малых протромбиновых пробирок уровень жидкости в обычной центрифужной пробирке должен быть ниже ее краев не менее чем на 2 см.
Центрифугирование микроорганизмов и материалов групп риска 1 и 2
1. Центрифугирование материалов, которые содержат микроорганизмы групп риска 2 и 1, должно производиться партиями, отдельными от остального материала.
2. Центрифужные пробирки или сосуды должны быть снабжены завинчивающимися крышками и маркированы с указанием принадлежности содержащегося в них материала к группам риска 2 и 1.
3. Необходимо использовать центрифужные стаканы с герметично закрывающимися предохранительными крышками.
4. Роторы следует загружать, закрывать и открывать в боксах биологической безопасности.
5. Роторы и центрифужные стаканы следунт регулярно деконтаминировать.
9. Безопасная транспортировка
образцов и инфекционных материалов.
Определения
В практическом руководстве по биологической безопасности в лабораторных условиях (ВОЗ, Женева 1994 г.) даны следующие определения принятые для использования с 1991 г.:
· Инфекционные материалы представляют собой субстанции, содержащие различные микроорганизмы, в том числе бактерии, вирусы, риккетсии, паразиты, грибы или рекомбинанты, гибриды или мутанты, которые могут вызывать заболевания или подозрительные на патогенные состояния у животных или людей.
Определение не относится к токсинам, не содержащим инфекционных субстанций. Транспорт генетически измененных микроорганизмов зависит от различных условий, и требования к нему должны быть согласованы.
· Диагностические образцы включают различные образцы экскретов, сектретов, крови и ее компонентов, тканей и тканевой жидкости и т. д., взятые для диагностических целей; исключение составляют живые инфицированные животные.
· Биологические продукты представляют собой приготовленные биологические продукты для использования у человека или ветеринарии, выполненные в соответствии с требованиями государственных служб здравоохранения и перевозимые по специальному разрешению или при наличии специальной лицензии этих служб; либо окончательно приготовленные биологические продукты, перевозимые до лицензирования для исследовательских целей с использованием в здравоохранении или ветеринарии; либо средства для экспериментального лечения животных, разработанные в соответствии с рекомендациями государственных служб здравоохранения. Сюда же относятся и не окончательно приготовленные биологические продукты, разработанные в соответствии с рекомендациями специальных правительственных комиссий. К биологическим продуктам относятся живые вакцины человека или животных, но не инфекционные субстанции.
Документации и требования к упаковке
Существуют определенные требования к документации при транспортировке инфекционных субстанций, биологических и диагностических образцов. Информация по их содержанию находится в соответствующих государственных учреждениях.
Инфекционные материалы и диагностические субстанции упаковываются в три этапа: а) первичный герметичный контейнер, содержащий образец; б) второй герметичный контейнер, содержащий достаточное количество адсорбента между его стенками и внутренним контейнером для адсорбции могущего пролиться материала; в) наружный контейнер, предназначенный для защиты второго от внешнего воздействия, например, физического повреждения или воды, во время перевозки.
Инфекционные субстанции классифицируются как биологически опасные. Тара, содержащая такие материалы, должна иметь метку с указанием инфекционной опасности.
Внутри третьего контейнера должна находиться одна копия регистрационной формы инфекционного материала (направление или иная информация, идентифицирующая или описывающая образец). Вторая копия посылается с нарочным по адресу лаборатории-получателя, третья остается у отправителя. Это позволяет лаборатории-получателю идентифицировать образец и решить, как с ним обращаться и работать.
Если материалы требуют хранения в жидком азоте или с иными предосторожностями против воздействия окружающей среды или более высокой температуры, все контейнеры и упаковочные материалы должны выдерживать очень низкие температуры, а первый и второй контейнеры – перепад давления по меньшей мере в 95 кПа и температуры от –40 0 С до +50 0 С.
Если культура живая и может погибнуть, соответствующее предупреждение должно быть внесено в сопроводительный документ, например «Хранить в прохладном месте при температуре от +2 0 С до +4 0 С».
Отправление материала
Эффективная пересылка инфекционных материалов требует хорошей координации действий отправителя, транспортных служб и лаборатории-получателя; в этом случае можно быть уверенным в том, что инфекционный материал доставлен безопасно, вовремя и в хорошем состоянии. От отправителя требуется выполнение следующего:
а) добиться договоренности между транспортными службами и получателем с тем, чтобы быть уверенным, что образцы будут получены и изучены должным образом – это следует делать по телефону;
б) приготовить сопроводительные документы для отправки;
в) вовремя отправить уведомление со всеми транспортными данными получателю.
Аварии при перевозке: действия персонала и неотложные мероприятия
Если упаковка с инфекционным материалом повреждена при перевозке или возникли подозрения об утечке материала или другие неполадки, перевозчик обязан сообщить об этом отправителю и получателю груза, а также органам общественного здравоохранения. Одновременно упакованный материал подвергается предварительным мерам безопасности, процедура которых описана ниже.
Предварительные процедуры, обеспечивающие безопасность (в случае повреждения упаковок, в отношении которых есть подозрение, что они содержат инфекционный материал)
1. При наличии осколков разбитого стекла или иных острых предметов, необходимо осторожно собрать их с помощью совка и маленькой щетки или пинцетом так, чтобы не порезать руки.
2. Надеть на руки пластиковый мешок как импровизированную рукавицу (класс Б – желтый цвет).
3. Защищенной таким образом рукой взять упаковку и поместить ее в пластиковый мешок подходящего размера.
4. Сбросить импровизированную рукавицу в тот же пакет.
5. Завязать мешок и поместить его под замок в безопасное место.
6. Дезинфицировать контаминированную поверхность, если имела место утечка инфекционного материала из упаковки.
7. Тщательно вымыть руки.
8. Последовательность операций изображена на следующих схемах (рис.2, 3).
Необходимые меры, предписываемые службами здравоохранения и/или ветеринарными службами по борьбе с распространением инфекции, по дезинфекции, изоляции, назначению вакцин или иммуноглобулинов и др., а также оповещению властей других районов, где могут иметь дело с этими материалами, в основном, сходны с теми, которые проводятся при авариях в лабораториях, и обеспечиваются в соответствии с планами на случай непредвиденной ситуации.
10. Действия и мероприятия в чрезвычайных ситуациях
Каждая лаборатория, работающая с биологическими инфекционными агентами, должна разработать и утвердить мероприятия по технике безопасности, соответствующие степени опасности работы с этими агентами.
Для специализированных лабораторий (базовая лаборатория – уровень биологической безопасности 3, изолированная лаборатория – уровень 2 и максимально изолированная лаборатория – уровень 1), работающих или хранящих агенты групп риска 2 или 1, необходимо принять письменный план действий на случай аварий. Поскольку эти агенты могут представлять опасность для населения, в разработке указанных мероприятий должны участвовать местные службы охраны здоровья.
Рис. 2
Примерная схема получения информации и принятия решения при лабораторной или транспортной аварии,
связанной с патогенными микроорганизмами I – II групп патогенности
Правительство Ульяновской области
Министерство сельского хозяйства

Координатор экстренных мер (определяет характер необходимых мероприятий, участие различных лиц и организаций в их проведении)
** ***
Руководитель учреждения
Руководитель режимной комиссии ***
Железнодорожный транспорт
|
Микробиологическая лаборатория учреждения |
Примечание: данная схема является ориентировочной и предназначена для своевременного оповещения заинтересованных ведомств и учреждений при возникновении аварийной ситуации (биотеррористического акта) и (или) обнаружение биологической субстанции с микроорганизмами 1-2 групп патогенности
Дополнительные обозначения:
* готовность ЛПУ:
· резерв оборудования, медикаментов и т. д.;
· транспортные средства для перевозки больных с инфекционным заболеванием, вызванным микроорганизмом 1-2 группы патогенности;
· госпитальная база для лечения больных с инфекционным заболеванием, вызванным микроорганизмом 1-2 группы патогенности
** Авария при транспортировке биологически опасного груза
***Авария или появление больного среди лабораторного персонала
Предпринять меры
безопасности*
|
Известен ли адресат и доступен ли в данном районе? |
|
|
Нет
|
|
|
|||
|
|
|
|||
|
Нет |
||||
|
Если доступна соответствующим образом оснащенная лаборатория, сначала необходимо идентифицировать находящийся в контейнере патогенный материал для последующей отсылки, затем автоклавировать или сжечь упаковку |
|
|
|
Если не забран в обозначенный срок |
||
|
|
|
|
|
|
Да
|
Группа 4? |
|
|
Никаких дальнейших действий |
Нет
|
|
|
Наблюдение за контактировавшими лицами (может включать пост-контактные лабораторные анализы и превентивное лечение) и предварительная изоляция в необходимых случаях. НЕМЕДЛЕННО ИНФОРМИРОВАТЬ ТЕРРИТОРИАЛЬНЫЕ УЧРЕЖДЕНИЯ ЗДРАВООХРАНЕНИЯ и ГОССАНЭПИДНАДЗОРА |
||
|
Группа 3, 2 или 1? |
||||
Рис.3 Действия при авариях, связанных с перевозкой инфекционных материалов
Планы действий в чрезвычайных ситуациях
План действий на случай непредвиденной ситуации должен определять мероприятия при перечисленных ниже обстоятельствах:
— предосторожности против стихийных бедствий, т. е. пожаров, наводнений, землетрясений;
— биологическая угроза;
— мероприятия при возникновении чрезвычайной ситуации и деконтаминация;
— экстренная медицинская помощь пострадавшим;
— медицинское наблюдение за пораженными;
— лечение пораженных в стационаре;
— эпидемиологические исследования.
В разрабатываемый план должны быть включены следующие меропрития:
— идентификация организмов высокого риска биологической опасности;
— локализация зон повышенного риска, например лабораторий или мест хранения материалов;
— определение круга лиц или групп лиц, подвергающихся риску;
— определение «кадрового резерва» и круга обязанностей лиц, входящих в него, т. е. лиц и персонала, ответственных за технику биологической и прочей безопасности, клиницистов, микробиологов, ветеринаров, эпидемиологов, сотрудников служб пожарной безопасности и охраны общественного порядка;
— перечень экстренных медицинских мер и средств изоляции, которые следует применять у инфицированных и пораженных лиц;
— транспортировка лиц, подвергшихся воздействию агента, и инфицированных лиц;
— перечень источников иммунной сыворотки, вакцин, необходимых медикаментов, специального оборудования и принадлежностей;
— обеспечение и местонахождение принадлежностей на случай чрезвычайного положения, т. е. защитной одежды, дезинфектантов, дезинфекционного оборудования.
Общие планы экстренных мероприятий в микробиологических лабораториях
Случайные инокуляции, порезы и ссадины
Сотрудник, допустивший их, должен снять защитную одежду, промыть руки и поврежденную поверхность тела, использовать дезинфектанты, пойти в медпункт и информировать руководство о причине раны и агенте, с которым он работал. При необходимости следует проконсультироваться с врачом и выполнять его советы. Имевший место случай подлежит регистрации.
Случайное попадание потенциально опасного агента
в желудочно-кишечный тракт
Сотрудник должен быть доставлен в медицинский пункт (комнату первой помощи) после снятия защитной одежды. Необходимо информировать врача об агенте, с которым работал сотрудник, и выполнять его рекомендации. соответствующие записи должны сохраняться.
Процедуры, проводимые в случае разбрызгивания
потенциально опасного агента в виде аэрозоля
за пределы бокса биологической безопасности
Всем лицам следует немедленно покинуть опасное место. Необходимо немедленно информировать об инциденте руководителя и ответственного за биологическую безопасность. В комнату запрещается вход кому бы то ни было в течение по меньшей мере 1 ч, что позволит устранить аэрозоль и обеспечит оседание более тяжелых частиц. Необходимо сделать плакаты, предупреждающие о запрещении входа. Спустя 1 ч проводят деконтаминацию под наблюдением лица, ответственного за технику безопасности. Для этого выдаются специальная защитная одежда и респираторы. Пораженные лица подвергаются медицинскому осмотру.
Разбитые емкости и пролитые культуры
Разбитые емкости и культуры необходимо накрыть куском ткани или бумажными полотенцами. После этого на них выливают дезинфектанты и оставляют по меньшей мере на 30 мин. Затем ткань, разлитая культура и полотенца должны быть убраны в контейнер; куски стекла следует собрать пинцетом. Контейнер с полотенцами, фрагментами емкостей следует автоклавировать или поместить в дезинфектант не менее чем на 24 ч. Все эти операции следует проводить в перчатках.
Разлитую культуру накрывают куском ткани или бумажными полотенцами, пропитанными дезинфектантом, не менее чем на 30 мин, прежде чем вытирают куском ткани, который затем помещают в контейнер для загрязненных отходов. Если заявки или иные печатные или рукописные материалы также подверглись загрязнению, то информацию переписывают на другой формуляр, а первый также помещается в контейнер для отходов.
Повреждение пробирок, содержащих потенциально опасный материал, в центрифугах, не имеющих специальных защитных крышек
Если повреждение произошло или подозреваются во время работы машины, двигатель следует выключить, а центрифугу не открывать в течение 30 мин. если место повреждения определено после остановки машины, крышку следует вернуть на место и оставить камеру закрытой в течение 30 мин. О поломке необходимо информировать ответственного по технике безопасности.
Все последующие операции выполняются в прочных перчатках (т. е. из толстой резины), надетых, или если необходимо, под разовые резиновые перчатки. Для извлечения стеклянных осколков необходимо использовать пинцеты или пинцеты с ватными тампонами.
Все битые пробирки, стеклянные осколки, люльки, спицы и ротор необходимо поместить в некоррозирующий дезинфектант, эффективный в отношении соответствующего инфекционного агента (не раствор гипохлорита, коррозирующего металлы), и оставить на 24 ч либо автоклавировать. Неразбитые закрытые пробирки можно поместить в отдельный контейнер с дезинфектантом и извлечь через 60 мин.
Камеру следует протереть тем же дезинфектантом в необходимом разведении, оставить на ночь, а затем снова протереть, промыть водой и высушить. Весь протирочный материал должен обрабатываться как инфекционные отходы.
Повреждение пробирок внутри центрифужных стаканов
Если повреждение подозревается в центрифужных стаканах, закрытых крышками, их открывают в боксах биологической безопасности. Если пробирка разбита, крышку центрифужного стакана надо заменить, а сам стакан автоклавировать.
Пожар, наводнение, стихийное бедствие
При возникновении чрезвычайной ситуации следует привлечь к ее ликвидации пожарные и иные службы. Их следует заранее проинформировать, в каких комнатах содержатся потенциально опасные инфекционные материалы.
При наводнениях или иных стихийных бедствиях (включая землетрясение) представители национальных или местных чрезвычайных служб должны быть поставлены в известность о наличии опасного материала в зданиях. Они должны входить внутрь только в сопровождении обученного сотрудника. культуры и инфекционный материал следует собрать в водонепроницаемые коробки или пластиковые мешки. На основе имеющейся информации персонал определяет возможность спасения материалов или дальнейшего их уничтожения.
Вандализм
Вандализм обычно выборочен и ориентирован на виварии. Защитой являются прочные тяжелые двери, хорошие замки и ограниченный доступ. Желательно экранировать окна и иметь сигнализацию на случай вторжения посторонних лиц. Действия в ситуациях, возникших в результате актов вандализма, те же, что и при прочих чрезвычайных происшествиях.
Службы экстренной помощи: к кому обращаться
У всех телефонных аппаратов должны быть разборчиво написаны следующие адреса и номера телефонов:
— точные адрес и местоположение лаборатории (адрес и местоположение могут быть неизвестны тому, кто звонит, и его абоненту);
— имя сотрудника, отвечающего за технику биологической безопасности;
— пожарная служба;
— служба скорой медицинской помощи/соответствующее отделение больницы (если прием при несчастных случаях, например, лиц, подвергшихся наибольшему риску, проводит определенная больница, то название отделений и имена врачей);
— милиция;
— директор института или заведующий лабораторией;
— инженер технической службы;
— санитарно-техническая, газовая и электротехническая служба.
Инвентарь для оказания экстренной помощи
Обязательным является наличие следующего оборудования:
— аптечка первой медицинской помощи, включая общие, противоцианидные и специальные антидоты;
— носилки.
Наличие следующих средств предполагается, однако они могут варьировать в зависимости от условий:
— полный комплект защитной одежды (комбинезон, перчатки и капюшон, очки (экраны) – для микроорганизмов групп риска 2 и 1);
— противогаз с соответствующими адсорбентами и фильтрами;
— оборудование для дезинфекции комнат, например, спреи и испарители с формальдегидом;
— дезинфектанты;
— инструменты – молотки, топоры, гаечные ключи, отвертки, лестницы, веревки;
— инвентарь для обозначения опасной зоны.
11. Комиссия по контролю биологической безопасности
В каждом учреждении осуществляющих деятельность с использованием возбудителей инфекционных заболеваний достаточно крупное (несколько лабораторий), необходимо организовать комиссию по безопасности труда с ПБА для разработки и реализации режима и программ безопасности на уровне учреждения и инструкций по технике безопасности, справочного пособия и программ обеспечения безопасности, которые могли бы служить основой соответствующей практики в отдельных лабораториях в количестве 3 человек, в достаточно крупных (несколько лабораторий) учреждениях состав комиссии может включать 5 человек.
Вопросы безопасной работы, встающие перед ответственным за технику безопасности, так же как и информацию о том, как эти вопросы решались, необходимо представлять для рассмотрения на регулярных заседаниях комитета по безопасности. Другие стороны деятельности комиссии могут касаться принятия планов исследовательской работы и арбитража в случае конфликтов по вопросам техники безопасности.
Состав и численность комиссии по контролю биологической безопасности зависят от величины и задач лаборатории, характера выполняемой работы и размещения подразделений или рабочих по лаборатории. Основу комиссии должны составлять:
Председатель – избирается из нижеуказанных членов*.
Члены — сотрудник ответственный за технику безопасности*;
врач-консультант;
представитель медицинского персонала;
представитель технического персонала;
представитель административного персонала*
*В небольших лабораториях (численность персонала 1 – 3 человека) комиссия включает 3 человека.
Комиссия по контролю биологической безопасности может также включать представителей ведомственных и специализированных служб (радиационной, промышленной, пожарной безопасности и др.) и периодически обращаться к специалистам из различных областей, местным экспертам и государственным служащим.
Численность и состав организационной структуры по технике безопасности должны изменяться в соответствии с задачами отдельной лаборатории и в некоторых случаях с национальным законодательством. Очевидно, что небольшие лаборатории не требуют организационных структур или профессионального штата сотрудников, занимающихся только вопросами безопасности. Во многих случаях, когда отдельные учреждения и лаборатории относительно невелики и работают с агентами групп риска 4 и 3, организационные структуры по безопасности могут быть созданы для обслуживания группы лабораторий.
Каждое крупное медико-биологическое учреждение имеет право создавать отдельный совет по биологической безопасности для нужд только данного учреждение с учетом специализированных аспектов собственной программы.
12. Технический персонал
Уборка лабораторных помещений должна (предпочтительно) производится персоналом, находящимся под наблюдением лабораторного руководства, а не лицами, работающими по контракту и подчиняющимися другим руководителям. Такая практика способствует безопасной работе и формирует производственные отношения между лабораторным и обслуживающим персоналом на основе сотрудничества. Это исключает неожиданные замены лиц, убирающих лабораторные помещения.
В изолированных – уровень биологической безопасности 2 – и максимально изолированных – уровень биологической безопасности 1 – лабораториях уборку помещений предпочтительнее производить силами лабораторного персонала. Если это невозможно, технический персонал приступает к работе после соответствующей проверки и под наблюдением ответственного за технику безопасности или руководителя лаборатории.
Технический персонал должен пройти обучение (приложение 5).
С целью предотвращения лабораторной инфекции для технического персонала разработаны следующие правила, которыми необходимо руководствоваться. Копии правил должны быть вручены каждому члену обслуживающих служб и вывешены в доступном месте.
____________________________________________________________________
Правила безопасности для технического и санитарного персонала
1. Постоянно носите защитную одежду согласно рекомендации надзирающего за безопасностью специалиста.
2. Снимайте защитную одежду при выходе из лаборатории в другую часть здания. Не носите защитную одежду в столовой или общей комнате.
3. Чаще мойте руки; мытье рук обязательно при выходе из лаборатории и входе в общую комнату для еды, питья или курения.
4. В лаборатории не принимайте пищу и питье, не курите и не пользуйтесь косметикой. Для этих целей есть комната персонала.
5. Не проводите чистку и мытьё рабочих полок без разрешения сотрудников лаборатории.
6. Если по вашей вине произошел какой-либо инцидент, если вы опрокинули или разбили бутыль, сосуд, пробирку или предмет оборудования, немедленно поставьте в известность ответственного за технику безопасности, вашего начальника или кого-либо из сотрудников лаборатории.
7. Если по вашей вине произошел какой-либо инцидент, не пытайтесь делать уборку без разрешения старшего сотрудника лаборатории. Не поднимайте осколки голыми руками. Пользуйтесь совком или щеткой. Следуйте инструкциям старших сотрудников лаборатории.
8. Не входите в комнату, на дверях которой имеется соответствующее предупреждение (например, биологическая или радиационная безопасность), пока вам не позволят сделать это.
9. Не опорожняйте ни каких контейнеров в лаборатории, пока не прочтете этикетку или инструкцию, позволяющую сделать это.
____________________________________________________________________
Приложение 1 (справочное)
Классификация
патогенных для человека микроорганизмов-возбудителей
инфекционных заболеваний, простейших, гельминтов и ядов
биологического происхождения
по группам патогенности (отдельные представители)
|
Бактерии |
||
|
I группа |
||
|
1. |
Yersinia pestis |
— чумы |
|
II группа |
||
|
1. |
Bacillus anthracis |
— сибирской язвы |
|
2. |
Brucella abortus Brucella melitensis Brucella suis |
— бруцеллеза |
|
3. |
Francisella rularensis |
— туляремии |
|
4. |
Burkholderia mallei |
— сапа |
|
5. |
Burkholderia pseudomallei |
— мелиоидоза |
|
6. |
Vibrio cholerae 01 токсигенный |
— холеры |
|
7. |
Vibrio cholerae non 01 (0139) токсигенный |
— холеры |
|
III группа |
||
|
1. |
Clostridium botulinum |
— ботулизма |
|
2. |
Clostridium tetani |
— столбняка |
|
3. |
Corynebacterium diphtheriae |
— дифтерии |
|
4. |
Mycobacterium tuberculosis Mycobacterium bovis Mycobacterium avium |
— туберкулеза |
|
5. |
Shigella spp. |
— дизентерии |
|
6. |
Treponema pallidum |
— сифилиса |
|
7. |
Vibrio cholerae 01 не токсигенный |
— диареи |
|
8. |
Vibrio cholerae non 01 (0139) не токсигенный |
— диареи, раневых инфекций, септицемии и др. |
|
IV группа |
||
|
1 |
Aerobacter aerogenes |
энтерита |
|
2 |
Salmonella spp. |
сальмонеллезов |
Вирусы |
||
|
II группа |
||
|
1 |
Вирус гепатита С |
Парентерального гепатита, гепатоцеллюлярной карциномы печени |
|
2 |
Род Hantavirus: вирусы Хантаан, Сеул, Пуумала, Чили, Аидо и др. |
Геморрагических лихорадок с почечным синдромом (ГЛПС) и с легочным синдромом |
|
3 |
Rhabdoviridae, род Lyssavirus: вирус уличного бешенства Дикования, Лагос-бат |
-бешенства — псевдобешенства и энцефалопатий |
|
4 |
Hepadnaviridae: вирусы гепатита В |
Парентеральных гепатитов |
|
5 |
Retroviridae: вирусы иммунодефицита человека (ВИЧ-1, ВИЧ-2), вирус Т-клеточного лейкоза человека (НТLV) |
— CПИДа — Т-клеточного лейкоза человека |
|
6 |
Nodaviridae: вирусы гепатитов Д (дельта) и Е |
Инфекционных гепатитов |
|
III группа |
||
|
1 |
Orthomyxoviridae: вирусы гриппа А, В и С |
Гриппа |
|
2 |
Picornaviridae, Род Enterovirus: Вирусы полиомиелита – дикие штаммы Вирусы гепатитов А и Е Вирус острого геморрагического конъюнктивита (АНС) |
— полиомиелита — энтеральных гепатитов — геморрагического конъюнктивита |
IV группа |
||
|
1 |
Adenoviridae: аденовирусы всех типов |
ОРВИ, пневмоний, конъюнктивитов |
|
2 |
Coronaviridae: коронавирусы человека |
ОРВИ (профузного насморка без температуры), энтериты |
Хламидии |
||
II группа |
||
|
1 |
Clamydophila psittaci |
Орнитоза-пситтакоза |
|
III группа |
||
|
1 |
Clamydia trachomatis |
Трахомы, урогенитольного хламидиоза |
|
2 |
Clamydophila pneumoniae |
Пневмонии, артритов |
Грибы |
||
|
II группа |
||
|
1 |
Blastomyces dermatitidis |
Бластомикоза |
|
2 |
Histoplasma capsulatum |
Гистоплазмоза |
|
3 |
Cjccidioides immitis |
Кокцидиоидомикоза |
|
4 |
Paracoccidioides brasiliensis |
Паракокцидиоидомикоза (южноамериканского бластомикоза) |
|
III группа |
||
|
1 |
Aspergillus flavus Aspergillus fumigatus |
Аспергиллеза |
|
2 |
Candida albicans |
Кандидоза |
|
3 |
Cryptococcus neoformans |
Криптококкоза |
|
IV группа |
||
|
1 |
Aspergillus niger Aspergillus nidulans |
Аспергиллеза |
|
2 |
Candida brumptii Candida crusei Candida intermedia Candida pseudotropicalis Candida tropicalis Candidaguillermondii |
Кандидоза |
Простейшие |
||
|
III группа |
||
|
1 |
Leishmania donovani |
Висцерального лейшманиоза |
|
2 |
Plasmodium vivax Plasmodium malariae Plasmodium falciparum |
Малярии |
|
3 |
Trichomonas vaginalis |
Мочеполового трихомониаза |
|
IV группа |
||
|
1 |
Babasia caucasica |
Бабезиоза |
|
2 |
Entamoeba hystolytica |
Амебиаза |
|
3 |
Toxoplasma gondii |
Токсоплазмоза |
Гельминты |
||
|
III группа |
||
|
1 |
Echinicoccus multilocularis |
Альвеолярного эхинококкоза |
|
2 |
Echinicoccus granulosis |
Гидатидозного эхинококкоза |
|
IV группа |
||
|
1 |
Enterobius vermicularis |
Энтеробиоза |
|
2 |
Trichinella spiralis |
Трихинеллеза |
|
3 |
Toxocara canis |
Токсокароза |
|
4 |
Ascaris lumbricoides |
Аскаридоза человека |
Яды биологического происхождения |
||
|
II группа |
||
|
1 |
Ботулинические токсины всех типов |
|
|
2 |
Холерный токсин |
|
|
3 |
Столбнячный токсин |
|
|
III группа |
||
|
1 |
Микотоксины |
Микотоксикозы |
|
2 |
Дифтерийный токсин |
|
|
3 |
Стрептококковый токсин группы А |
Приложение 2
Схема плана мероприятий при выявлении лиц,
подозрительных на специфическое заболевание
1. Схема и порядок передачи информации о подозрении на специфическое заболевание (в рабочие и выходные дни).
2. Порядок эвакуации, силы и средства для лечения и лабораторной диагностики, ответственные.
3. Порядок забора проб для лабораторной диагностики.
4. Перечень, состав укладок для забора проб и места их хранения.
5. Объем, порядок, сроки и ответственные за проведение противоэпидемических, профилактических и дезинфекционных мероприятий.
6. Перечень, количество и места хранения медикаментов для проведения симптоматической, патогенетической и этиотропной терапии.
7. Перечень и количество запаса дезинфекционных средств и средств индивидуальной защиты.
8. Функциональные обязанности работников на каждом этапе проведения мероприятий.
9. Подготовка кадров и проведение тренировочных занятий.
Приложение 3
Основные разделы плана
мероприятий по ликвидации последствий аварий
1. Введение
— дать перечень наиболее вероятных аварий;
— классификация аварий.
2. Организационные мероприятия:
— схема и порядок передачи информации об аварии в рабочее время и выходные дни;
— состав бригад по локализации и по ликвидации аварий;
— перечень сил и средств аварийной бригады и места хранения имущества;
— перечень и состав укладок для забора проб и места их хранения;
— порядок эвакуации персонала;
— мероприятия по организации медицинского наблюдения или профилактического лечения;
— перечень средств для укомплектования аптечек первой медицинской помощи, места хранения аптечек;
— силы и средства, используемые для медицинского наблюдения, лабораторной диагностики и лечения персонала, находящегося в зоне аварии;
— перечень и объем мероприятий, проводимых при аварии, и ответственные за их выполнение;
— план подготовки состава аварийных бригад и проведения тренировочных занятий;
— осуществление контроля, в том числе лабораторного, за правильностью, своевременностью и эффективностью проводимых мероприятий;
— порядок сбора аварийных бригад в рабочее и нерабочее время;
— проведение тренировочных учений по ликвидации последствий аварии.
Приложение 4
Схема проверки работы комиссии по контролю соблюдения
требований биологической безопасности
1. Наличие приказа о создании комиссии.
2. Отражение в утвержденном руководителем учреждения плане работы комиссии следующих вопросов:
— контроль подготовленности персонала к работе с инфекционным материалом, проверка знаний правил биологической безопасности;
— рассмотрение материалов по вопросу получения лицензии на работу с микроорганизмами;
— разработка (обсуждение) документов, регламентирующих проведение мероприятий по профилактике лабораторных заражений, по локализации и ликвидации аварий, а также при появлении больных или подозрительных на специфическое заболевание;
— заслушивание отчетов руководителей структурных подразделений об организации работы по соблюдению требований биологической безопасности;
— график проверок структурных подразделений и заслушивания результатов.
3. Контроль своевременности получения лицензии на работу с микроорганизмами и порядком выезда сотрудников в командировку (отпуск).
4. Контроль правильности использования дезинфекционных средств.
5. Контроль за организацией медицинского наблюдения за состоянием здоровья работающих и своевременностью вакцинации.
6. Контроль условий хранения ПБА (охрана, наличие рубежей охраны, порядок допуска в хранилище и т. д.)
7. Наличие материалов по анализу состояния биологической безопасности и разработке мероприятий по ее совершенствованию.
Приложение 5
Модуль подготовки вспомогательного персонала
Данный модуль, рассчитанный на один день, предназначен для следующих групп лабораторного вспомогательного персонала, которые обычно не имеют биологической практики:
Группа 1. Технический персонал, который убирает помещения, ликвидирует контаминированный и другой лабораторный мусор; моет и готовит стеклянные предметы и иное оборудование; готовит и стерилизует культуральные среды и реагенты.
Группа 2. Инженерный персонал и работники материально-технического обслуживания, которые обслуживают лабораторные помещения и ремонтируют оборудование.
Группа 3. Персонал, в обязанности которого входят получение и сортировка доставляемого в лабораторию материала; вскрытие почты; обработка заявок и лабораторной документации; упаковка инфекционных материалов для отправления по почте или перевозки; управление транспортом, перевозящим инфекционные материалы.
Содержание программы
1. Природа микроорганизмов и механизм возникновения инфекции, которые они вызывают (все группы).
2. Работа лаборатории (все группы).
3. Как избежать внутрилабораторного заражения; личная гигиена; защитная одежда, прием пищи и воды, курение; знаки биологической опасности и запретные зоны (все группы).
4. Использование и ограниченность применения дезинфектантов (все группы).
5. Опасность обращения с определенным оборудованием, таким, как боксы биологической безопасности, инкубаторами и рефрижераторами, гомогенизаторами и центрифугами.
6. Опасности, связанные с получением образцов, вскрытием посылок и ведением записей; правила упаковки инфекционных материалов для пересылки и транспортировки; экстренные меры безопасности, которые следует предпринять в случае аварии или утечки материалов до прибытия лица, ответственного за технику безопасности (группа 3).
7. Химическая, физическая, механическая и электрическая опасность в лаборатории (все группы).
8. Ответственный за технику безопасности и его (ее) обязанности; разъяснение отдельным работающим их прав и обязанностей в соответствии с национальными и местными правилами; необходимость доклада об авариях и иных происшествиях; безопасность и противопожарные меры на местах (все группы).
9. Первая помощь пострадавшим (все группы).
Справочная литература
1.Практическое руководство по биологической безопасности в лабораторных условиях. Второе издание. Женева, 1994 г.
2. Учебное пособие. Техника безопасности при работе в бактериологической лаборатории. УГСХА, 1998 г.
ВВОДНЫЙ ИНСТРУКТАЖ СТУДЕНТОВ
ПРАВИЛА ТЕХНИКИ БЕЗОПАСНОСТИ ПРИ РАБОТЕ В МИКРОБИОЛОГИЧЕСКИХ ЛАБОРАТОРИЯХ
1. Работа в лаборатории ведется исключительно в халатах и сменной обуви или бахилах.
2. Верхняя одежда и сумки не должны находиться в лаборатории.
3. Запрещается принимать пищу и пить воду в лаборатории.
4. Работу с биологическим материалом проводить только предварительно обработанным инструментом.
5. При случайном попадании биологического материала на стол, руки или другие поверхности необходимо сразу же оповестить об этом преподавателя и провести обработку загрязненной поверхности дезинфицирующим раствором.
6. После работы необходимо тщательно вымыть руки с использованием дезинфекционных средств.
7. Рабочее место следует поддерживать в чистоте, не загромождать его посудой и лишними вещами.
8. Студентам запрещается работать в лаборатории в отсутствие преподавателя или лаборанта, а также в неустановленное время без разрешения преподавателя.
9. К выполнению каждой лабораторной работы нужно приступать только после получения инструктажа по технике безопасности, ознакомления с методиками и разрешения преподавателя.
10. Лабораторную работу необходимо проводить в точном соответствии с описанием в методических указаниях.
11. Для проведения работы пользоваться только чистой, сухой лабораторной посудой; для отбора объемов реактивов нужно иметь мерную посуду (пипетки, бюретки, мензурку, мерный цилиндр или мерный стакан); нельзя выливать избыток налитого в пробирку реактива обратно в емкость.
12. Если в ходе опыта требуется нагревание, надо следовать предусмотренным методическими указаниями способам нагрева: на водяной бане, на электроплитке или на спиртовке.
13. Нагревание предметного стекла в пламени спиртовки при приготовлении некоторых препаратов следует проводить равномерно.
14. Запрещается работать с неисправными электроприборами. О любых неисправностях следует незамедлительно информировать преподавателя.
15. По окончании работы следует привести в порядок свое рабочее место: помыть посуду, протереть поверхность рабочего лабораторного стола, закрыть водопроводные краны, выключить электрические приборы.
P.S. По окончании инструктажа студенты должны расписаться в журнале!!!

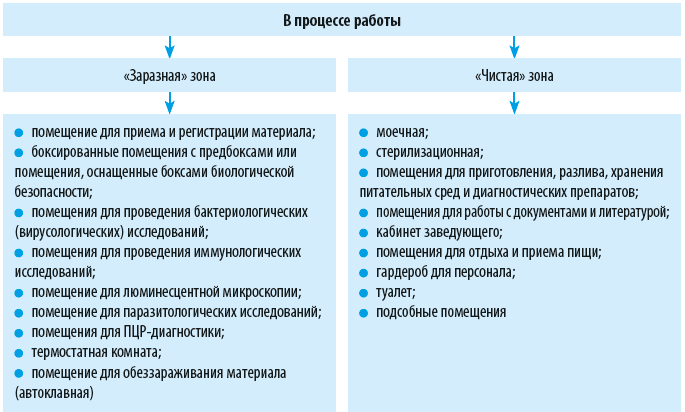






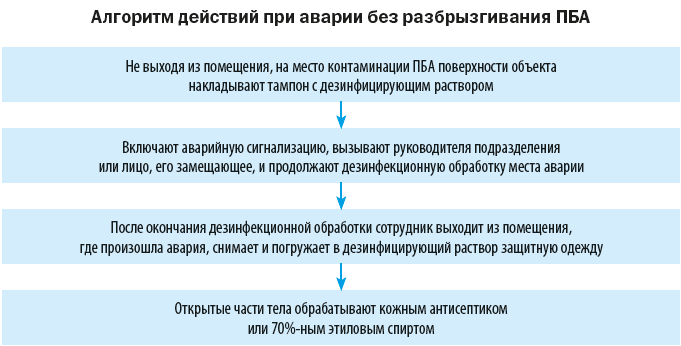




 Да
Да

 Нет
Нет