Управление рисками в лаборатории. Процедура — LINCO Platform
Материалы
Экономьте время на разработке,
используя свободные формы от LINCO
Управление рисками в лаборатории. Процедура
|
Открытая разработка документов | LINCO Open Source Управление рисками в лаборатории. Процедура Версия от 08.09.20 |
ВЕРНУТЬСЯ К ПЕРЕЧНЮ ДОКУМЕНТОВ ❯
ПЕРЕЙТИ К ТРЕБОВАНИЯМ ГОСТ 17025 ❯
Документ создается сообществом лабораторий и открыт для дополнения и редактирования.
Вы можете участвовать в корректировке и дополнении, а также направить нам свою версию
документа для включения её в состав данного материала. Для этой цели используйте
форму загрузки
внизу страницы.
Данный материал будет полезен для разработки документнов системы менеджмента своей лаборатории.
Содержание
1. Назначение и область применения
1.1.
Процедура устанавливает последовательность действий и ответственность при оценке рисков, выполнении контроля за текущими рисками и мониторинге эффективности методов управления рисками в испытательной лаборатории (испытательном лабораторном центре).
1.2.
Требования настоящей документированной процедуры распространяются на всех сотрудников лаборатории (центра).
2. Нормативные ссылки
2.2.
ГОСТ Р ИСО 9001-2015 «Системы менеджмента качества. Требования»;
2.3.
ГОСТ Р ИСО 31000-2019 «Менеджмент риска. Принципы и руководство»;
2.4.
ГОСТ Р 51897-2011 «Менеджмент риска. Термины и определения»;
2.5.
ГОСТ Р 51901.23-2012 «Реестр риска. Руководство по оценке риска событий для включения в реестр риска».
2.6. ГОСТ Р 70350-2022 » Менеджмент риска. Оценивание качества менеджмента риска организации»
Добавлен участником: 14 марта 2023
3. Определения
Анализ риска – процесс изучения природы и характера риска и определения уровня риска.
Владелец риска – лицо, несущее ответственность за управление риском. Владелиц риска отвечает за идентификацию, оценку и мониторинг управления риском.
Владелец процесса – руководитель процесса или подразделения лаборатории, на стратегические или операционные цели которого оказывает прямое влияние данное событие.
Идентификация риска – процесс определения, составления перечня и описания элементов риска (элементы риска могут включать в себя источники риска, события, их причины и возможные последствия).
Источник риска – объект или деятельность, которые самостоятельно или в комбинации с другими обладают возможностью вызывать повышение риска (источник может быть материальным и не материальным).
Корректирующее действие – действие, предпринятое для устранения причины несоответствия и предупреждения его повторного возникновения.
Несоответствие – невыполнение требования.
Последствие – результат воздействия события на объект.
Причина риска – явление или обстоятельство, в результате которого может возникнуть риск.
Потенциальное несоответствие – несоответствие, причина которого может привести к невыполнению требования или к другой нежелательной ситуации.
Предупреждающее действие – действие, предпринятое для устранения причины потенциального несоответствия или другой потенциально нежелательной ситуации.
Процесс – совокупность взаимосвязанных и(или) взаимодействующих видов деятельности, использующих входы для получения намеченного результата.
Результативность – степень реализации запланированной деятельности и достижения запланированных результатов.
Риск – влияние неопределенности на цели лаборатории, которое может привести не только к негативным последствиям, но и к положительным.
Управление рисками – это процесс разработки и выполнения управленческих решений, призванных максимально снизить возможность наступления негативного результата и свести к минимуму возможные потери, связанные с его реализацией.
4. Сокращения и обозначения
ВА – внутренний аудит
ВЛКК – внутрилабораторный контроль качества
ВП – владелец процесса
ИЛ – испытательная лаборатория
ИЛЦ – испытательный лабораторный центр
КД – корректирующее действие
МВИ – методика выполнения измерений
МСИ – межлабораторные сравнительные испытания
НД – нормативная документация
ПД – предупреждающее действие
СМ – система менеджмента
5. Процедура
5.1. Общие положения
5.1.1.
Цель управления рисками (ПД) — устранение причин потенциально возможных несоответствий для повышения результативности СМ и её непрерывного улучшения. Избегать появления несоответствий гораздо эффективнее, чем бороться с ними.
5.1.2.
Основой постоянного улучшения является активный поиск сотрудниками ИЛ (ИЛЦ) и ВП возможностей улучшения показателей процессов и результатов лабораторной деятельности, где это требуется:
- установление «слабых», «недостаточно надежных», «потенциально опасных» и т.п. направлений уже осуществляемой деятельности;
- организация мониторинга за такими видами деятельности и установление критериев, сигнализирующих о возможном в ближайшем будущем «выходе» этой деятельности за пределы приемлемого;
- выявление причин такого потенциально неблагоприятного явления;
- разработка, реализация и подтверждение результативности мероприятий по устранению предполагаемых причин (что является более предпочтительным, чем устранение несоответствий посредством КД, снижает вероятность возникновения несоответствий и минимизирует потери).
5.1.3.
Предупреждающие действия с целью уменьшения возможных потерь следует применять в основных и обеспечивающих процессах, а также в управляющих процессах для повышения удовлетворенности заказчика.
5.1.4.
Предупреждающие и корректирующие действия разграничивают следующим образом:
- когда несоответствие находится еще на стадии риска, применяется ПД;
- когда несоответствие зафиксировано, применяется КД;
- ПД и КД различаются моментом принятия решений;
- обучение, ознакомление, премирование (депремирование) и т.п. не являются ПД или КД, т.к. не изменяют СМ.
5.1.5.
Задача ВП – постоянное улучшение процессов ИЛ (ИЛЦ), закрепленных за ними. Делать это необходимо с точки зрения:
- повышения результативности (степени выполнения требований);
- повышения эффективности (например, через оптимизацию ресурсов);
- упорядочения воздействия на процесс (например, изменения процедур);
- применения лучших методов работы, передового опыта, не ожидая появления проблемы, чтобы выявить возможность улучшения.
5.1.6.
К ПД, выполняемым ИЛ (ИЛЦ) на постоянной основе, можно отнести:
- использование актуализированных НД, обеспечивающих качество проводимых лабораторией испытаний;
- повышение квалификации персонала;
- точное исполнение методик выполнения измерений;
- работа на поверенных (калиброванных) СИ;
- внутренние проверки и анализ со стороны руководства;
- проведение внутреннего и внешнего контроля качества результатов испытаний.
5.1.7.
Этапы управления рисками (ПД):
- установление потенциальных несоответствий и их причин;
- анализ причин потенциальных несоответствий (качественный: выявление, описание; количественный: оценка влияния риска);
- оценивание необходимости ПД и выбор метода ПД: снижение, сохранение, передача;
- разработка, проведение ПД и регистрация их результатов;
- контроль и анализ результативности предпринятых ПД;
- доведение до высшего руководства информации о предпринятых действиях для анализа.
5.1.8.
Для каждого риска или группы рисков во всех процессах СМ определена ответственность по управлению рисками (владелец риска). Ответственных за управление рисками назначают ВП распоряжением руководителя ИЛ (ИЛЦ).
5.1.9.
ПД должны проводится ответственными за управление рисками без лишней задержки. Срок организации и проведения ПД с момента определения причин потенциальных несоответствий должен не превышать один месяц или должен быть определен в распоряжении.
5.1.10.
ВП и персонал ИЛ (ИЛЦ) обязаны выявлять и регистрировать потенциальные несоответствия в своей работе. Данная обязанность включена в должностные инструкции.
5.2. Идентификация потенциальных несоответствий (рисков) и их причин
5.2.1.
«Потенциальное несоответствие» – это «необнаруженное несоответствие», т.е. такое, которое еще не выявлено. Это только риск несоответствия, а не оно само (если риск трактовать как возможность). Если несоответствия нет, то устранять причины можно, основываясь на прошлом опыте и опыте других.
5.2.2.
Ответственность за идентификацию потенциальных несоответствий в лабораторной деятельности, процессах, СМ в процессе ежедневного и периодического надзора за необходимыми для лабораторной деятельности факторами и применение ПД несут сотрудники ИЛ (ИЛЦ) и ВП.
5.2.3.
При обнаружении потенциального несоответствия в лабораторной деятельности, процессе, СМ лицо, обнаружившее несоответствие, оперативно доводит информацию до ВП и/или менеджера по качеству.
5.2.4.
Потенциальные несоответствия могут быть установлены при:
- входном контроле качества приобретаемых ресурсов (ВП, исполнитель);
- выполнении определения и проверке результата (исполнитель);
- систематическом надзоре за процессом получения результатов определений, состоянии оборудования, квалификации и компетентности персонала, условий проведения испытаний и др. (исполнитель, инженер, ВП);
- контроле выполнений требований МВИ (ВП, инженер);
- промежуточном и окончательном контроле результата (инженер, ВП);
- анализе несоответствующего результата (заказчик);
- анализе результатов ВЛКК и МСИ (ВП, менеджер по качеству);
- анализе ошибочных результатов определений (исполнитель, инженер, ВП);
- проведении внутренних и внешних аудитов, анализе СМ со стороны руководства (аудитор, менеджер по качеству, руководитель ИЛ (ИЛЦ));
- улучшении (ВП, менеджер по качеству, руководитель ИЛ (ИЛЦ)).
5.2.5.
Менеджер по качеству помогает сотрудникам, ВП правильно идентифицировать ПД в «Плане мероприятий«, П-NN-ГГ и не выдавать за них, в частности, мероприятия по плановой подготовке к новым видам деятельности, действия по улучшению и контрольную деятельность.
5.2.6.
После определения потенциального несоответствия дальнейшая деятельность по устранению причин несоответствия и проведению ПД проводится аналогично КД.
5.2.7.
Все потенциальные несоответствия должны быть проанализированы ВП, ответственным за область деятельности, в которой выявляются несоответствия, с привлечением, при необходимости, всех заинтересованных лиц и сотрудников подразделения лаборатории с целью установления причин их возникновения.
5.2.8.
ВП оперативно проводит ПД по устранению потенциального несоответствия, если причина потенциального несоответствия:
- заключается в нарушении или невыполнении последовательности операций, методов, режимов;
- известна и отражена в «Плане корректирующих и предупреждающих действий«, П-NN-ГГ;
- ясна без необходимости проведения комплексного анализа.
5.2.9.
ВП необходимо провести всесторонний анализ для разработки Плана мероприятий в случае, если:
- принятые меры не позволили устранить потенциальное несоответствие или однозначно определить причину его возникновения;
- в Плане корректирующих и предупреждающих действий отсутствует анализируемое на данный момент потенциальное несоответствие.
5.2.10.
ВП для исследования причин возможного возникновения потенциального несоответствия может быть проведен сбор дополнительной информации (данные аудитов СМ, данные по мониторингу, верификации и валидации, протоколы, акты, мнения сотрудников, имеющих отношение к рассматриваемой проблеме и др.).
5.2.11.
При невозможности проведения какого-либо этапа работ своими силами информацию о потенциальном несоответствии ВП сообщает менеджеру по качеству и/или руководителю ИЛ (ИЛЦ).
5.2.12.
Менеджер по качеству организует работы по проведению анализа причин потенциальных несоответствий. В случае необходимости при разработке мероприятий руководитель ИЛ (ИЛЦ) привлекает специалистов других подразделений лаборатории, в компетенции которых находится решение данной проблемы.
5.2.13.
Идентифицированные и установленные причины потенциальных несоответствий ИЛ (ИЛЦ) менеджер по качеству в электронной форме вносит в План корректирующих и предупреждающих действий. При этом менеджер по качеству учитывает:
- организационные обсуждения с сотрудниками ИЛ (ИЛЦ) потенциальных событий, которые могут влиять на ИЛ (ИЛЦ), на достижение ее целей и Политику качества ИЛ (ИЛЦ);
- перечень потенциальных событий, связанных с конфиденциальностью, беспристрастностью и лабораторной деятельностью, характерных для ИЛ (ИЛЦ);
- интервьюирование ключевых работников (аудиторов, руководителей подразделений ИЛ (ИЛЦ), руководителей процессов) для открытого обсуждения существующих и потенциальных рисков;
- анализ отчетов по ВА и прочих проверок;
- проверку соответствия имеющейся документации и фактически применяемых стандартов, нормативной базы и инструкций;
- результаты выполнения КД и ПД согласно Плану мероприятий.
5.3. Анализ причин потенциальных несоответствий (рисков)
5.3.1.
Цель анализа причин потенциального несоответствия – установить его действительную причину или ряд причин, при реализации которых будет отсутствовать риск его появления.
5.3.2.
При анализе причин потенциального несоответствия ВП, ответственному за область деятельности, в которой возникают риски, следует:
- установить возможное влияние всех фактических и потенциальных лабораторных факторов;
- определить место возникновения потенциального несоответствия, форму проявления и возможные последствия;
- проверить его содержание (организационное, техническое, экономическое, социально-психологическое);
- оценить потенциальное несоответствие по степени значимости (существенное, несущественное);
- определить уровень принятия решения о его устранении (уровень ИЛ (ИЛЦ), уровень процесса, уровень подразделения лаборатории, уровень исполнителя).
5.3.3.
Получив информацию о потенциальном несоответствии, ВП проводит всесторонний анализ состояния всех лабораторных факторов, действующих на:
- рабочем месте (сравнение с требованиям МВИ);
- процесс (сравнение с требованиями НД);
- СМ (сравнение с требованиями Руководства по качеству).
5.3.4.
ВП или комиссия, которую собирает ВП, устанавливает взаимосвязь между несоответствием и его причиной с учетом возможного влияния всех фактических и потенциальных факторов на потенциальное несоответствие и вносит предложение для изменения СМ.
5.3.5.
Анализ причин(ы) проводит ВП отдельно по каждому из идентифицированных рисков или группе рисков.
5.3.6.
Результатом проведенного анализа причин должно быть:
- определение причин(ы) возникновения потенциального несоответствия;
- разработка Плана мероприятий по предупреждению появления потенциального несоответствия (КД и ПД).
5.3.7.
Срок, в течение которого должен быть проведен анализ причин, не должен превышать трех дней с момента обнаружения и регистрации потенциального несоответствия.
5.3.9.
Потенциальные несоответствия, имеющие высокий уровень риска должны быть устранены в кратчайшие сроки. Если уровень риска признан низким, то допускается не проводить соответствующие ПД.
5.4. Разработка предупреждающих действий (ПД) и регистрация их результатов
5.4.1.
ПД направлены на устранение причин возникновения потенциальных несоответствий.
5.4.2.
ПД разрабатываются лицами, указанными в п. 6, в течении недели на основании установленных причин потенциального несоответствия и предложений по их устранению или снижению риска возникновения, тяжести последствий.
5.4.3.
ВП определяют содержание ПД в Плане мероприятий, включая исполнителей, сроки выполнения, и контролируют полноту и качество выполнения мероприятий. При необходимости привлекаются специалисты других подразделений.
5.4.4.
Основанием для разработки и проведения ПД являются решения ВП, менеджера по качеству, руководителя ИЛ (ИЛЦ) при анализе причин потенциальных несоответствий. Решения могут быть оформлены в виде:
- распоряжения – при распространении ПД на все или несколько подразделений ИЛ (ИЛЦ) и необходимости оперативного проведения ПД;
- Плана мероприятий – при распространении ПД на подразделение ИЛ (ИЛЦ), исполнителя или ресурсы;
- «Чек-листа«, Л-NN-ГГ – при определении ПД по результатам ВА;
- Плана корректирующих и предупреждающих действий – при распространении ПД на СМ ИЛ (ИЛЦ).
Руководитель ИЛ (ИЛЦ) и/или менеджер по качеству определяют, каким будет ПД: перспективным (мониторинг действий в течение длительного времени) или оперативным (реализуется в короткий срок).
5.4.5.
Для устранения причин потенциальных несоответствий ВП, менеджер по качеству могут:
- проводить обучение сотрудников, занятых в процессе, где ожидаются несоответствия, новым способам выполнения своих функций;
- готовить предложение об изменении СМ.
5.4.6.
В случае, если ПД принято к исполнению, то назначается ответственный исполнитель (владелец риска) и срок выполнения.
5.4.7.
После выполнения всех ПД владелец риска докладывает об их выполнении контролирующему лицу (ВП, ответственному за ВА аудитору, менеджеру по качеству, руководителю ИЛ (ИЛЦ)).
5.4.8.
Результаты выполнения ПД фиксируются:
- ВП – в Плане мероприятий, Отчете по анализу СМ, Журнале регистрации несоответствий и корректирующих действий;
- аудитором – в Чек-листе ВА, Отчете по ВА, Протоколе несоответствия;
- менеджером по качеству – в Плане корректирующих и предупреждающих действий, Отчете по функционированию СМ ИЛ (ИЛЦ);
- руководителем ИЛ (ИЛЦ) – в Анализе со стороны руководства или на исходном экземпляре документа в виде резолюции:
- «Решения выполнены. Причины потенциальных несоответствий устранены»;
- «Решения выполнены. Причины потенциальных несоответствий: (перечень причин) не устранены. Разработать новые мероприятия».
5.4.9.
ПД, направленные на снижение вероятности возникновения потенциальных несоответствий, установленных в критических точках процессов, и/или тяжести проявления их последствий, описаны в Руководстве по качеству, процедурах и инструкциях ИЛ (ИЛЦ), описывающих данные процессы.
5.5. Оценка результативности предпринятых ПД
5.5.1.
Оценка результативности мероприятий по управлению рисками проводится с целью обеспечения непрерывного совершенствования СМ. Своевременное проведение ПД обеспечивает сокращение затрат, обусловленных появлением несоответствий в результатах лабораторной деятельности, процессах и СМ.
5.5.2.
Результативность ПД оценивается по результатам наблюдений за состоянием качества результатов лабораторной деятельности, процессов и СМ после их проведения.
5.5.3.
Результативным может быть признано мероприятие, после проведения которого данное потенциальное несоответствие не появится, снижен (исключен) риск возникновения и/или тяжесть последствий.
5.5.4.
Для оценки результативности процесса используется индикатор – доля нерезультативных ПД в общем количестве запланированных.
5.5.5.
Оценка результативности ПД осуществляется:
- ВП – при проверке и контроле выполнения ПД;
- аудиторами – при проведении планового ВА;
- менеджером по качеству – при контроле выполнения Плана корректирующих и предупреждающих действий, ВЛКК, стандартизации и т. д.;
- руководителем ИЛ (ИЛЦ) – при анализе со стороны руководства.
5.5.6.
Если ПД признано результативным (т. е. было предупреждено появление несоответствия и получены какие-либо дополнительные выгоды), то должностным лицом, разработавшим и контролирующим качество и полноту выполнения мероприятий, в документе, содержащем ПД, делаются соответствующие отметки о необходимости продолжать выполнять ПД таким же образом или нет (риск устранен):
- в электронном Журнале регистрации несоответствий и корректирующих мероприятий;
- в электронном Плана корректирующих и предупреждающих действий;
- в Отчете по ВА;
- в «Сводной таблице итогов ВА за год«, Т-NN-ГГ;
- в годовых Отчетах по процессам и Отчете о функционировании системы менеджмента;
- в Анализе со стороны руководства.
5.5.7.
В случае, если мероприятия по устранению потенциальных несоответствий в лабораторной деятельности, процессе или СМ оказалось не результативным, ВП, менеджер по качеству информирует руководителя ИЛ (ИЛЦ) об отсутствии результата с указанием причин и проводит повторный анализ потенциального несоответствия и разработку ПД согласно п. 5.3 и п. 5.4 настоящей процедуры.
5.5.8.
Информация от ВП и/или менеджера по качеству о результативности ПД рассматривается на оперативных совещаниях.
5.5.9.
Результаты результативности ПД являются данными для анализа СМ со стороны руководства. Данные мониторинга ПД отражают ВП в годовом Отчете по процессу и менеджером по качеству в Отчете о функционировании системы менеджмента.
6. Ответственность
6.1.1.
Руководитель ИЛ (ИЛЦ) несет ответственность за:
- принятие решений о проведении ПД, направленных на устранение потенциальных несоответствий процессов, результатов лабораторной деятельности и СМ на уровне ИЛ (ИЛЦ);
- принятие окончательных решений по спорным вопросам в Плане корректирующих и предупреждающих действий.
6.1.2.
ВП несут ответственность за:
- идентификацию и своевременное определение потенциальных несоответствий в управляемом им процессе;
- проведение анализа причин потенциальных несоответствий;
- организацию, проведение и отчетность по выполнению ПД, направленных на устранение потенциальных несоответствий процессов СМ в целях поддержания стабильности результатов лабораторной деятельности;
- своевременное выполнение ПД и поддержание стабильной работы процесса;
- внесения предложений и изменений в СМ для улучшения работы процесса и исключения потенциальных несоответствий;
- своевременное информирование менеджера по качеству и/или руководителя ИЛ (ИЛЦ) о возможном невыполнении ПД в установленные сроки для принятия адекватных решений;
- проведение анализа результативности ПД и разработку повторных мероприятий (при необходимости).
6.1.3.
Менеджер по качеству несет ответственность за:
- помощь ВП в идентификации и определении причин потенциальных несоответствий в их процессах;
- своевременное внесение изменений в СМ для исключения потенциальных несоответствий в дальнейшей работе;
- контроль выполнения ПД, принятых к исполнению Планом мероприятий;
- мониторинг (ВА) эффективности выполнения ПД в подразделениях ИЛ (ИЛЦ);
- реестр всех потенциальных несоответствий и ПД в Плане корректирующих и предупреждающих действий.
6.1.4.
Аудиторы несут ответственность за свои действия согласно процедуре «Внутренний аудит«.
ВЕРНУТЬСЯ К ПЕРЕЧНЮ ДОКУМЕНТОВ ❯
ПЕРЕЙТИ К ТРЕБОВАНИЯМ ГОСТ 17025 ❯
Информация
В нашей стране с 1 сентября 2019 года Приказом Федерального агентства по техническому регулированию и метрологии от 15.07.2019 №385-ст был введён в действие стандарт ГОСТ ISO/IEC 17025-2019 «Общие требования к компетентности испытательных и калибровочных лабораторий». С 01.01.2021 вступили в силу новые критерии аккредитации, утверждённые Приказом Министерства экономического развития Российской Федерации от 26.10.2020 № 707 «Об утверждении критериев аккредитации и перечня документов, подтверждающих соответствие заявителя, аккредитованного лица критериям аккредитации». Согласно требованиям, приведённым в данных документах, лаборатории должны включать в свою систему менеджмента качества процедуры, описывающие действия по управлению рисками и возможностями.
Вопросы риск-менеджмента входили в систему менеджмента качества лабораторий и до введения указанных выше документов. Так, в действовавшем ранее ГОСТ ИСО/МЭК 17025-2009, риск упоминался в контексте необходимости учитывать его при принятии решений. Новая редакция стандарта переходит от требований учёта к управлению рисками и устанавливает необходимость разработки процедуры, объектом которой становятся риски.
В стандарте ГОСТ Р ИСО 31000-2019 риск определён как следствие влияния неопределённости на достижение поставленных целей. Риск часто связан с событием (результатом действия или процесса), в том числе с решением не предпринимать каких-либо действий. Риск всегда влечёт последствия, которые могут быть негативными, позитивными или ничтожными.
Под влиянием понимается отклонение события от ожидаемого. Влияние может быть как отрицательным, так и положительным.
Под неопределённостью понимается отсутствие достоверной информации о факторах, влияющих на результат действия или процесса. При этом может отсутствовать информация как об уровне влияния, так и о наличии влияющего фактора. При уменьшении неопределённости, можно уменьшить вероятность наступления события риска, но полностью исключить эту вероятность невозможно.
Под целями следует понимать цели организации. Цели могут иметь различные аспекты (финансовые, экологические, цели в отношении здоровья и безопасности) и могут применяться на различных уровнях (стратегических, в масштабах организации, проекта, продукта или процесса). Однако ГОСТ ISO/IEC 17025-2019 устанавливает требование к управлению рисками и возможностями только применительно к лабораторной деятельности (испытаниям, калибровке, отбору образцов). Управление рисками вне лабораторной деятельности не является требованием стандарта, но может быть включено в систему менеджмента качества лаборатории.
Принципы риск-менеджмента должны быть задекларированы в документах системы менеджмента качества лаборатории.
Процесс управления рисками должен начинаться с попытки понять внешние и внутренние факторы, которые могут влиять на успех лаборатории в достижении целей. Важно понимать место лаборатории на рынке услуг и место внутри организации, частью которой она является.
Чем больше факторов составляют внешний и внутренний контекст, тем больше рисков подлежит рассмотрению. Например, включение в контекст требований охраны труда влечёт за собой управление рисками в этой области. Для испытательных и калибровочных лабораторий, помимо лабораторной деятельности, характерно рассмотрение рисков в области аккредитации, сохранение государственной и коммерческой тайны, обращения с ядовитыми и радиоактивными веществами, обеспечение промышленной, пожарной, экологической, санитарной безопасности и т.д.
Процедура управления рисками и возможностями должна включать этапы, приведённые на Рис. 1.
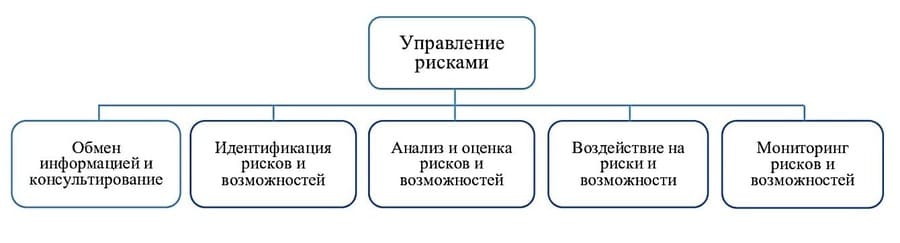
Рис.1 – Процедура управления рисками и возможностями
Обмен информацией и консультирование с заинтересованными сторонами (руководителями и работниками структурных подразделений, с которыми происходит взаимодействие в отношение риска или возможности) осуществляются на всех этапах риск-менеджмента.
Обмен информацией и консультирование должны гарантировать, что руководители структурных подразделений (владельцы процессов) и заинтересованные стороны принанимают решения, основанные на информации (свидетельствах), отражающей причины, которые указывают на необходимость воздействия на риск/возможность.
Обмен информацией и консультирование должны способствовать обмену объективной, существенной, точной и понятной информацией.
Для идентификации рисков и возможностей в лаборатории могут быть применены такие методы, как SWOT-анализ, мозговой штурм, метод Дельфи. В таблице 1 приведены примеры рисков, которые могут быть идентифицированы в лаборатории.
Таблица 1
Примеры рисков
|
№ п/п |
Содержание риска |
|
1 |
Нарушение принципа беспристрастности при проведении работ |
|
2 |
Увольнение (выход на пенсию) сотрудников лаборатории |
|
3 |
Болезнь сотрудников лаборатории |
|
4 |
Нарушение режима конфиденциальности |
|
5 |
Несоблюдение области аккредитации при проведении работ |
|
6 |
Несоблюдение процедур подтверждения компетентности |
|
7 |
Отсутствие заявок на проведение работ |
|
8 |
Ошибки при заключении договоров |
|
9 |
Нарушение сроков исполнения договорных обязательств |
|
10 |
Недостаточная компетентность персонала лаборатории |
|
11 |
Возникновение существенных негативных изменений в публичном мнении о лаборатории |
|
12 |
Неправильное публичное восприятие результатов лабораторной деятельности |
|
13 |
Потеря данных (информации) |
|
14 |
Отсутствие денежных ресурсов (финансовый риск) |
|
15 |
Несоблюдение времени проведения аудита |
|
16 |
Недостижение целей аудита |
|
17 |
Отсутствие необходимой нормативной документации |
|
18 |
Несоблюдение требований нормативных документов |
|
19 |
Поломка оборудования |
|
20 |
Несвоевременная поверка имеющихся средств измерений и аттестация испытательного оборудования |
Риски и возможности идентифицируются и по результатам идентификации оформляются паспорта рисков и возможностей. При идентификации рисков и возможностей определяется и документируется следующая информация:
-
название риска/возможности;
-
причина возникновения риска/возможности;
-
вероятность наступления риска/возможности;
-
возможные последствия риска/возможности.
На этапе анализа риска и возможности определяются последствия, вероятность возникновения и уровень риска и возможности, а также причины и факторы возникновения рисковых ситуаций. Анализ проводится отдельно по каждому из идентифицированных рисков и возможностей.
Пример определения значимости ущерба, причиняемого риском, приведён в Таблице 2.
Таблица 2
Определение уровня ущерба
|
№ п/п |
Последствия в баллах |
Уровень ущерба |
Влияние риска |
||
|
Время |
Сроки выполнение работ |
Удовлетворенность Заказчика |
|||
|
1 |
1 балл |
Несущественный |
Требуется время на устранение риска |
Зачастую не сдвигаются |
Удовлетворённость Заказчика не изменилась |
|
2 |
2 балла |
Низкий |
Требуется время на устранение риска |
Сдвигаются в пределах допустимых по договору |
Удовлетворённость Заказчика не изменилась |
|
3 |
3 балла |
Средний |
Требуется время на устранение риска |
Сроки сдвинуты выше указанных в договоре |
Удовлетворённость потребителя снижена из-за увеличения сроков работ |
|
4 |
4 балла |
Существенный |
Требуется время на устранение риска |
Сроки сдвинуты выше указанных в договоре |
Удовлетворённость потребителя снижена из-за увеличения сроков работ, получение претензий (жалоб) |
|
5 |
5 баллов |
Катастрофичес-кий |
Требуется время на устранение риска |
Сдвигаются сроки всех договорных обязательств |
Отказ Заказчика или появление информации, влияющей на репутацию организации |
После того как каждый выявленный риск оценен с точки зрения ущерба, проводится экспертная оценка вероятности наступления такого ущерба. В Таблице 3 приведен пример шкалы вероятности, которая может применяться для ранжирования рисков.
Таблица 3
Бальная система оценки вероятности наступления риска/возможности
|
№ п/п |
Вероятность наступления события |
Вероятность в баллах |
Характеристика |
|
1 |
Крайне маловероятно |
1 балл |
Возможно произойдёт в этом году |
|
2 |
Маловероятно |
2 балла |
Точно произойдёт 1-4 раза в год |
|
3 |
Возможно |
3 балла |
Разница в возникновении двух последовательных событий рассчитывается в месяцах |
|
4 |
Вероятно |
4 балла |
Разница в возникновении двух последовательных событий рассчитывается в неделях |
|
5 |
Весьма вероятно |
5 баллов |
Произойдёт 1 раз за день и чаще |
С помощью матрицы вероятности и последствий (Таблица 4) или путём умножения вероятности наступления события (риска) на уровень ущерба получают общую оценку риска.
Таблица 4
Матрица вероятности и последствий
|
Вероятность/баллы |
Уровень ущерба/баллы |
|||||
|
Несущест-венный |
Низкий |
Средний |
Сущест-венный |
Катастро-фический |
||
|
1 |
2 |
3 |
4 |
5 |
||
|
Весьма вероятно |
5 |
5 |
10 |
15 |
20 |
25 |
|
Вероятно |
4 |
4 |
8 |
12 |
16 |
20 |
|
Возможно |
3 |
3 |
6 |
9 |
12 |
15 |
|
Маловероятно |
2 |
2 |
4 |
6 |
8 |
10 |
|
Крайне маловероятно |
1 |
1 |
2 |
3 |
4 |
5 |
|
— низкий уровень риска (от 1 до 3 баллов) |
|
|
— средний уровень риска (от 4 до 9 баллов) |
|
|
— высокий уровень риска (от 10 до 16 баллов) |
|
|
— критический уровень риска (от 20 до 25 баллов) |
Любое событие риска может быть охарактеризовано по двадцати пяти бальной шкале. В матрице вероятности и последствий выделены четыре основных зоны. В зависимости от зоны, в которую попал риск, применяются разные стратегии реагирования на него.
Примеры стратегии реагирования на риски в зависимости от их уровня приведены в Таблице 5.
Таблица 5
Стратегия реагирования на риски
|
Уровень риска |
Стратегия реагирования |
|
Критический |
Неприемлемые. Незамедлительные действия, необходимые для снижения риска путем разработки мероприятий по его предотвращению или снижению |
|
Высокий |
Неприемлемые. Срочные действия, необходимые для снижения риска путем разработки мероприятий по его предотвращению или снижению |
|
Средний |
Необходим периодический мониторинг уровня риска. В случае экономической целесообразности лаборатория может принять решение о разработке мероприятий по минимизации рисков среднего уровня |
|
Низкий |
Риск приемлемый. Необходим периодический мониторинг уровня риска |
Риски, отнесенные к категории «низкие», считаются допустимыми и управляемыми в соответствии с существующей стратегией реагирования.
Риски, отнесенные к категории «средние», считаются допустимыми, но при этом требуется разработка и реализация организационных мероприятий для исключения или минимизации этих рисков и перевода их в категорию «низкие».
Риски, отнесенные к категории «высокие» и «критические», требуют незамедлительной разработки мер по управлению ими.
Для рисков, требующих управления, необходимо разработать мероприятия по снижению уровня рисков, определить необходимые ресурсы и назначить ответственного за реализацию этих мероприятий. Мероприятия по минимизации рисков позволяют исключить риски либо свести уровень рисков до категории «низкие».
Воздействия на риски включают выбор одного или нескольких вариантов мероприятий по минимизации вероятности возникновения рисков и их негативного влияния на цели процессов и максимизации вероятности возникновения возможностей и их позитивного влияния на цели процессов.
Воздействия на риски и возможности являются циклическим процессом, состоящим из следующих этапов:
-
планирование мероприятий по минимизации вероятности возникновения рисков и их негативного влияния на цели процессов и максимизации вероятности возникновения возможностей и их позитивного влияния на цели процессов;
-
реализация мероприятий по минимизации вероятности возникновения рисков и их негативного влияния на цели процессов и максимизации вероятности возникновения возможностей и их позитивного влияния на цели процессов;
-
оценка результативности мероприятий;
-
выявление причин и разработка необходимых мероприятия при отрицательном результате реализованных мероприятий;
-
определение достаточности реализованных мероприятий.
Планирование мероприятий по минимизации вероятности возникновения рисков и их негативного влияния на цели процессов и максимизации вероятности возникновения возможностей и их позитивного влияния на цели процессов производиться по итогам проведенного анализа и оценки рисков и возможностей.
Сотрудником лаборатории, ответственным за процесс, заполняется план мероприятий по минимизации вероятности возникновения рисков и их негативного влияния на цели процессов и максимизации вероятности возникновения возможностей и их позитивного влияния на цели процессов.
Реализация мероприятий по минимизации вероятности возникновения рисков и их негативного влияния на цели процессов и максимизации вероятности возникновения возможностей и их позитивного влияния на цели процессов должна проводится в соответствии с планом и в запланированные сроки.
После реализации мероприятий по минимизации вероятности возникновения рисков и максимизации вероятности возникновения возможностей, сотрудником лаборатории, ответственным за процесс, заполняется отчёт о реализации мероприятий по минимизации рисков и максимизации возможностей.
Результативность мероприятий оценивается определением того, наступил риск/возможность или нет.
Мониторинг и анализ рисков и возможностей являются составной частью процесса риск-менеджмента. Регулярное проведение мониторинга, анализа и управления рисками направлены на проверку:
-
достоверности предположений о рисках и возможностях;
-
достоверности предположений, на которых основана оценка рисков, включая внешние и внутренние области применения;
-
достижимости ожидаемых результатов;
-
соответствия результатов оценки рисков фактической информации о рисках;
-
правильности применения методов оценки рисков;
-
эффективности воздействия на риски и возможности.
Комплексное управление рисками позволяет более полно учитывать внутренние и внешние факторы рисков в деятельности лаборатории, определяет пути обеспечения устойчивости организации, ее способности противостоять неблагоприятным ситуациям.
Основные показатели эффективного управления рисками и возможностями – выполнение лабораторией договорных обязательств в срок и отсутствие жалоб и претензий со стороны потребителей.
Несмотря на то, что новая редакция межгосударственного стандарта ГОСТ ISO/IEC 17025-2019 не устанавливает требований к документированному процессу управления рисками, лабораториям настоятельно рекомендуется разработать и внедрить собственную документированную процедуру управления рисками, так как наличие такой процедуры является обязательным.
Приведённый пример оценки рисков и возможностей в лаборатории окажет несомненную помощь руководителям и сотрудникам лабораторий в понимании вопроса, что такое мышление, основанное на рисках.
Представленный в статье подход к построению риск-менеджмента может быть реализован любой лабораторией без существенных затрат.
Популярные статьи в категории:
Не нашли нужную информацию? Задайте вопрос менеджеру
05.06.2019
Добрый день, Уважаемые Коллеги!
Представляем Вашему вниманию новую статью по теме : «Управление рисками и возможностями»
Автор: Дмитрий Владимирович Фалкин
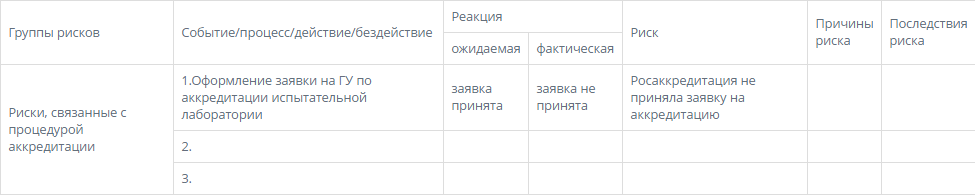
Одно из новых требований ISO/IEC 17025:2017 это «Управление рисками и возможностями». Одним из вариантов идентификации рисков является создание базы данных рисков. Так принято во многих отраслях: строительство, IT, машиностроение, энергетика и т.д. У каждого из вас есть свой жизненный опыт: много что случалось, много что могло случиться.
Я предлагаю создать общую базу рисков лабораторной и калибровочной деятельности. А мы с коллегами будем модерировать создание базы. Базу разместим в общем доступе и будем регулярно обновлять.
Прикрепляю образец реестра рисков. Присылайте мне описание рисков, можно сюда (+7927-692-01-12), можно в эл. почту (adar-rf@mail.ru). Анонимность гарантирую.
Скачать образец
Для удобства обработки прошу придерживаться правил:
1. Один риск — одно сообщение или отдельный файл.
2. Желательно заполнить эксель таблицу, но не обязательно все столбцы.