Описание препарата Изопринозин (таблетки, 500 мг) основано на официальной инструкции, утверждено компанией-производителем в 2022 году
Дата согласования: 28.03.2022
Особые отметки:
Содержание
- Фотографии упаковок
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Заказ в аптеках Москвы
- Отзывы
Фотографии упаковок

28.03.2022

28.03.2022
28.03.2022
Действующее вещество
ATX
Фармакологическая группа
Нозологическая классификация (МКБ-10)
Список кодов МКБ-10
- A60 Аногенитальная герпетическая вирусная инфекция [herpes simplex]
- B00 Инфекции, вызванные вирусом простого герпеса [herpes simplex]
- B01 Ветряная оспа [varicella]
- B02 Опоясывающий лишай [herpes zoster]
- B05 Корь
- B07 Вирусные бородавки
- B08.1 Контагиозный моллюск
- B25 Цитомегаловирусная болезнь
- B27 Инфекционный мононуклеоз
- B97.7 Папилломавирусы
- H19.1 Кератит, обусловленный вирусом простого герпеса, и кератоконъюнктивит (B00.5+)
- J06 Острые инфекции верхних дыхательных путей множественной и неуточненной локализации
- J11 Грипп, вирус не идентифицирован
- J38.1 Полип голосовой складки и гортани
- N73.9 Воспалительные болезни женских тазовых органов неуточненные
Состав
| Таблетки | 1 табл. |
| действующее вещество: | |
| инозин пранобекс (Изопринозин) | 500 мг |
| вспомогательные вещества: маннитол — 67,0 мг; крахмал пшеничный — 67,0 мг; повидон К30 — 10,0 мг; магния стеарат — 6,0 мг |
Описание лекарственной формы
Продолговатые двояковыпуклые таблетки белого или почти белого цвета с риской на одной стороне. Без запаха или с легким аминовым запахом.
Фармакологическое действие
Фармакологическое действие
—
иммуностимулирующее.
Фармакодинамика
Изопринозин — синтетическое комплексное производное пурина, обладающее иммуностимулирующей активностью и неспецифическим противовирусным действием.
Восстанавливает функции лимфоцитов в условиях иммунодепрессии, повышает бластогенез в популяции моноцитарных клеток, стимулирует экспрессию мембранных рецепторов на поверхности Т-хелперов, предупреждает снижение активности лимфоцитарных клеток под влиянием ГКС, нормализует включение в них тимидина. Изопринозин оказывает стимулирующее влияние на активность цитотоксических Т-лимфоцитов и естественных киллеров, функции Т-супрессоров и Т-хелперов, повышает продукцию IgG, интерферона-гамма, ИЛ-1 и ИЛ-2, снижает образование провоспалительных цитокинов — ИЛ-4 и ИЛ-10, потенцирует хемотаксис нейтрофилов, моноцитов и макрофагов.
Препарат проявляет противовирусную активность in vivo в отношении вирусов Herpes simplex, ЦМВ и вируса кори, вируса Т-клеточной лимфомы человека III типа, полиовирусов, гриппа А и В, ЕСНО-вируса (энтероцитопатогенный вирус человека), энцефаломиокардита и конского энцефалита. Механизм противовирусного действия препарата Изопринозин связан с ингибированием вирусной РНК и фермента дигидроптероатсинтетазы, участвующего в репликации некоторых вирусов, усиливает подавленный вирусами синтез мРНК лимфоцитов, что сопровождается подавлением биосинтеза вирусной РНК и трансляции вирусных белков, повышает продукцию лимфоцитов, обладающих противовирусными свойствами интерферонов альфа и гамма. При комбинированном назначении усиливает действие интерферона альфа, противовирусных средств ацикловира и зидовудина.
Фармакокинетика
После приема внутрь препарат хорошо всасывается из ЖКТ. Cmax ингредиентов в плазме крови определяется через 1–2 ч.
Быстро подвергается метаболизму и выделяется через почки. Метаболизируется аналогично эндогенным пуриновым нуклеотидам с образованием мочевой кислоты. N-N-диметиламино-2-пропранолон метаболизируется до N-оксида, а пара-ацетамидобензоат — до о-ацилглюкуронида. Не обнаружено кумуляции препарата в организме. T1/2 составляет 3,5 ч — для N-N-диметиламино-2-пропранолона и 50 мин — для пара-ацетамидобензоата. Элиминация препарата и его метаболитов из организма происходит в течение 24–48 ч.
Показания
лечение гриппа и других ОРВИ;
инфекции, вызываемые вирусом Herpes simplex 1, 2, 3 и 4-го типов: генитальный и лабиальный герпес, герпетический кератит, опоясывающий лишай, ветряная оспа, инфекционный мононуклеоз, вызванный вирусом Эпштейна-Барр;
подострый склерозирующий панэнцефалит;
цитомегаловирусная инфекция;
корь тяжелого течения;
папилломавирусная инфекция: папилломы гортани/голосовых связок (фиброзного типа), папилломавирусная инфекция гениталий у мужчин и женщин, бородавки;
контагиозный моллюск.
Противопоказания
повышенная чувствительность к компонентам препарата;
подагра;
мочекаменная болезнь;
аритмии;
хроническая почечная недостаточность;
беременность;
период грудного вскармливания;
детский возраст до 3 лет (масса тела до 15–20 кг).
С осторожностью: одновременное назначение изопринозина с лекарственными препаратами — ингибиторами ксантиноксидазы, диуретиками, зидовудином, острая печеночная недостаточность.
Применение при беременности и кормлении грудью
Беременность. Препарат противопоказан во время беременности, т.к. безопасность применения не исследовалась.
Период грудного вскармливания. Отсутствуют данные по экскреции изопринозина или его метаболитов с грудным молоком. Нельзя исключить риск для младенца. Во время лечения препаратом грудное вскармливание следует прекратить.
Фертильность. Отсутствуют данные о влиянии препарата на фертильность человека. Исследования у животных не показали влияния на фертильность.
Способ применения и дозы
Внутрь, после еды, запивая небольшим (около 1/2 стакана) количеством воды.
Рекомендуемая доза взрослым и детям с 3 лет (масса тела от 15–20 кг) составляет 50 мг/кг/сут, разделенная на 3–4 приема. Взрослым — по 6–8 табл./сут, детям — по 1/2 табл./5 кг/сут. При тяжелых формах инфекционных заболеваний доза может быть увеличена индивидуально до 100 мг/кг/сут, разделенная на 4–6 приемов. Максимальная суточная доза для взрослых — 3–4 г/сут, для детей — 50 мг/кг/сут.
Продолжительность лечения
При острых заболеваниях: продолжительность лечения у взрослых и детей обычно от 5 до 14 дней. Лечение необходимо продолжать до момента исчезновения клинических симптомов и в течение еще 2 дней уже при отсутствии симптомов. При необходимости длительность лечения может быть увеличена индивидуально под контролем врача.
При хронических рецидивирующих заболеваниях у взрослых и детей лечение необходимо продолжать несколькими курсами по 5–10 дней с перерывом в приеме в 8 дней.
Для проведения поддерживающей терапии доза может быть снижена до 500–1000 мг/сут (1–2 табл.) в течение 30 дней.
При герпетической инфекции взрослым и детям назначают в течение 5–10 дней до исчезновения симптомов заболевания, в бессимптомный период — по 1 табл. 2 раза в день в течение 30 дней для уменьшения числа рецидивов.
При папилломавирусной инфекции взрослым препарат назначают по 2 табл. 3 раза в день, детям — по 1/2 табл./5 кг/сут в 3–4 приема в течение 14–28 дней в виде монотерапии.
При рецидивирующих остроконечных кондиломах взрослым препарат назначают по 2 табл. 3 раза в день, детям — по 1/2 табл./5 кг/сут в 3–4 приема в день либо в качестве монотерапии, или в комбинации с хирургическим лечением в течение 14–28 дней, далее с трехкратным повторением указанного курса с интервалами в 1 мес.
При дисплазии шейки матки, ассоциированной с вирусом папилломы человека, назначают по 2 табл. 3 раза в день в течение 10 дней, далее проводят 2–3 аналогичных курса с интервалом в 10–14 дней.
Особые группы пациентов
Пожилой возраст. Коррекция дозы при применении у пожилых пациентов не требуется, препарат применяется так же, как у пациентов среднего возраста. Следует учитывать, что у пожилых пациентов чаще наблюдается повышение концентрации мочевой кислоты в сыворотке крови и в моче, чем у пациентов среднего возраста.
Дети. Препарат применяется у детей старше 3 лет.
Почечная и печеночная недостаточность. При лечении препаратом следует каждые 2 нед проводить контроль содержания мочевой кислоты в сыворотке крови и моче. Контроль активности печеночных ферментов рекомендуется проводить каждые 4 нед при длительных курсах лечения препаратом.
Побочные действия
В соответствии с классификацией ВОЗ все реакции распределены по системам органов и частоте развития: очень часто (>1/10); часто (>1/100 и <1/10); нечасто (>1/1000 и <1/100); редко (>1/10000 и <1/1000); очень редко (<1/10000); частота неизвестна (невозможно определить на основании доступных данных).
Со стороны иммунной системы: нечасто — крапивница, ангионевротический отек; частота неизвестна — реакции гиперчувствительности, анафилактические реакции, анафилактический шок.
Со стороны нервной системы: часто — головная боль, головокружение, утомляемость, плохое самочувствие, слабость; нечасто — нервозность, сонливость, бессонница.
Со стороны ЖКТ: часто — тошнота, рвота, боль в эпигастрии, снижение аппетита; нечасто — диарея, запор.
Со стороны печени и желчевыводящих путей: часто — временное повышение активности трансаминаз и ЩФ в плазме крови, повышение концентрации мочевины в плазме крови.
Со стороны кожи и подкожных тканей: часто — кожный зуд, сыпь; нечасто: макулопапулезная сыпь; частота неизвестна — эритема.
Со стороны почек и мочевыводящих путей: нечасто — полиурия.
Общие расстройства и нарушения в месте введения: часто — боль в суставах, обострение подагры.
Влияние на результаты лабораторных и инструментальных исследований: часто — повышение концентрации азота мочевины в крови.
Взаимодействие
Иммунодепрессанты ослабляют иммуностимулирующий эффект препарата. Изопринозин следует применять с осторожностью пациентам, принимающим одновременно ингибиторы ксантиноксидазы (например, аллопуринол) или урикозурические средства, включая диуретики — тиазидные диуретики (гидрохлоротиазид, хлорталидон, индапамид) или петлевые диуретики (фуросемид, торасемид, этакриновая кислота), т.к. при этом может наблюдаться повышение концентрации мочевой кислоты в сыворотке крови.
Совместное применение препарата с зидовудином приводит к увеличению концентрации последнего в плазме крови и удлиняет его T1/2 (при совместном применении может потребоваться коррекция дозы зидовудина).
Передозировка
При передозировке показано промывание желудка и симптоматическая терапия.
Особые указания
Изопринозин, как и другие противовирусные средства, наиболее эффективен при острых вирусных инфекциях, если лечение начато на ранней стадии болезни (предпочтительно с первых суток заболевания).
После двух недель применения препарата следует провести контроль концентрации мочевой кислоты в сыворотке крови и в моче.
Также при длительном применении рекомендуется периодически контролировать концентрацию мочевой кислоты в сыворотке крови и моче.
Пациенты со значительно повышенной концентрацией мочевой кислоты в организме могут одновременно принимать препараты, понижающие ее концентрацию. Необходимо контролировать концентрацию мочевой кислоты в сыворотке крови при назначении препарата одновременно с препаратами, увеличивающими концентрацию мочевой кислоты, или препаратами, нарушающими функцию почек.
При длительном применении после четырех недель приема целесообразно каждый месяц проводить контроль функции печени и почек (активность трансаминаз, уровень креатинина, мочевой кислоты в плазме крови). Препарат следует с осторожностью применять у пациентов с острой печеночной недостаточностью, поскольку он подвергается метаболизму в печени.
Влияние на способность управлять транспортными средствами, механизмами. Влияние изопринозина на психомоторные функции организма и способность управлять транспортными средствами и движущимися механизмами не исследовалось. При применении препарата следует учитывать возможность возникновения головокружения и сонливости.
Форма выпуска
Таблетки, 500 мг. По 10 табл. в блистере ПВХ/ПВДХ и фольги алюминиевой. По 2, 3 или 5 бл. вместе с инструкцией по применению помещают в пачку картонную. На пачку картонную дополнительно могут быть нанесены защитные наклейки.
Производитель
Техническое фармацевтическое общество «Лузомедикамента», С.А., Португалия, ул. Консильери Педрозу, 66, 69-В, Келуз де Байшу, 2730-055, Баркарена, Португалия.
Юридическое лицо, на имя которого выдано РУ: Тева Фармацевтические Предприятия Лтд., Израиль.
Организация, принимающая претензии потребителей ООО «Тева», 115054, Москва, ул. Валовая, 35.
Тел.: (495) 644-22-34; факс: (495) 644-22-35.
www.teva.ru
Условия отпуска из аптек
По рецепту.
ISPR-RU-00740-DOC-02.2022
Условия хранения
При температуре не выше 25 °C.
Хранить в недоступном для детей месте.
Срок годности
5 лет.
Не применять по истечении срока годности, указанного на упаковке.
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Изопринозин (Isoprinosine) инструкция по применению
📜 Инструкция по применению Изопринозин
💊 Состав препарата Изопринозин
✅ Применение препарата Изопринозин
📅 Условия хранения Изопринозин
⏳ Срок годности Изопринозин
Описание лекарственного препарата
Изопринозин
(Isoprinosine)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для печатного издания справочника Видаль 2019 года.
Дата обновления: 2018.11.28
Владелец регистрационного удостоверения:
Контакты для обращений:
ТЕВА
(Израиль)
Код ATX:
J05AX05
(Инозин пранобекс)
Активное вещество:
инозин пранобекс
(inosine pranobex)
BAN
принятое к употреблению в Великобритании
Лекарственная форма
| Изопринозин |
Таб. 500 мг: 20, 30 или 50 шт. рег. №: П N015167/01 |
Форма выпуска, упаковка и состав
препарата Изопринозин
Таблетки белого или почти белого цвета, продолговатые, двояковыпуклой формы, с легким аминовым запахом, с риской на одной стороне.
Вспомогательные вещества: маннитол, крахмал пшеничный, повидон, магния стеарат.
10 шт. — блистеры (2) — пачки картонные.
10 шт. — блистеры (3) — пачки картонные.
10 шт. — блистеры (5) — пачки картонные.
Фармакологическое действие
Изопринозин — синтетическое комплексное производное пурина, обладающее иммуностимулирующей активностью и неспецифическим противовирусным действием. Восстанавливает функции лимфоцитов в условиях иммунодепрессии, повышает бластогенез в популяции моноцитарных клеток, стимулирует экспрессию мембранных рецепторов на поверхности Т-хелперов, предупреждает снижение активности лимфоцитарных клеток под влиянием глюкокортикостероидов, нормализует включение в них тимидина. Изопринозин оказывает стимулирующее влияние на активность цитотоксических Т-лимфоцитов и естественных киллеров, функции Т-супрессоров и Т-хелперов, повышает продукцию IgG, интерферона гамма, интерлейкинов (ИЛ)-1 и ИЛ-2, снижает образование провоспалительных цитокинов — ИЛ-4 и ИЛ-10, потенцирует хемотаксис нейтрофилов, моноцитов и макрофагов.
Препарат проявляет противовирусную активность in vivo в отношении вирусов Herpes simplex, цитомегаловируса и вируса кори, вирус Т-клеточной лимфомы человека тип III, полиовирусов, гриппа А и В, ЕСНО-вирус (энтероцитопатогенный вирус человека), энцефаломиокардита и конского энцефалита. Механизм противовирусного действия Изопринозина связан с ингибированием вирусной РНК и фермента дигидроптероатсинтетазы, участвующего в репликации некоторых вирусов. Усиливает подавленный вирусами синтез мРНК лимфоцитов, что сопровождается подавлением биосинтеза вирусной РНК и трансляции вирусных белков, повышает продукцию лимфоцитами интерферонов альфа и гамма, обладающих противовирусными свойствами.
При комбинированном назначении усиливает действие интерферона альфа, противовирусных средств ацикловира и зидовудина.
Фармакокинетика
Всасывание
После приема внутрь хорошо всасывается из ЖКТ. Cmax активного вещества в плазме крови определяется через 1-2 ч.
Метаболизм
Быстро подвергается метаболизму. Метаболизируется аналогично эндогенным пуриновым нуклеотидам с образованием мочевой кислоты, N-N-диметиламино-2-пропранолон метаболизируется до N-оксида, а пара-ацетамидобензоат — до o-ацилглюкуронид. Не обнаружено кумуляции препарата в организме.
Выведение
T1/2 составляет 3.5 ч для N-N-диметиламино-2-пропранолона и 50 мин — для пара-ацетамидобензоата. Выводится почками. Элиминация препарата и его метаболитов из организма происходит в течение 24-48 ч.
Показания препарата
Изопринозин
- лечение гриппа и других ОРВИ;
- инфекции, вызываемые вирусом Herpes simplex типов 1, 2, 3 и 4: генитальный и лабиальный герпес, герпетический кератит;
- опоясывающий лишай, ветряная оспа;
- инфекционный мононуклеоз, вызванный вирусом Эпштейна-Барр;
- цитомегаловирусная инфекция;
- корь тяжелого течения;
- папилломавирусная инфекция: папилломы гортани/голосовых связок (фиброзного типа), папилломавирусная инфекция гениталий у мужчин и женщин, бородавки;
- контагиозный моллюск.
Режим дозирования
Таблетки принимают после еды, запивая небольшим количеством воды.
Рекомендуемая суточная доза для взрослых и детей в возрасте 3 лет и старше (с массой тела от 15-20 кг) составляет 50 мг/кг массы тела в 3-4 приема (для взрослых — 6-8 таб./сут, для детей — по 1/2 таб. на 5 кг массы тела/сут).
При тяжелых формах инфекционных заболеваний доза может быть увеличена индивидуально до 100 мг/кг массы тела/сут, разделенных на 4-6 приемов. Максимальная суточная доза для взрослых 3-4 г/сут, для детей — 50 мг/кг/сут.
Продолжительность лечения при острых заболеваниях у взрослых и детей обычно составляет от 5 до 14 дней. Лечение необходимо продолжать до момента исчезновения клинических симптомов и в течение еще 2 дней уже при отсутствии симптомов. При необходимости длительность лечения может быть увеличена индивидуально под контролем врача.
При хронических рецидивирующих заболеваниях у взрослых и детей лечение необходимо продолжать несколькими курсами по 5-10 дней с перерывом в приеме в 8 дней.
Для проведения поддерживающей терапии доза может быть снижена до 500-1000 мг/сут (1-2 таб.) в течение 30 дней.
При герпетической инфекции взрослым и детям препарат назначают в течение 5-10 дней до исчезновения симптомов заболевания, в бессимптомный период — по 1 таб. 2 раза/сут в течение 30 дней для уменьшения числа рецидивов.
При папилломавирусной инфекции взрослым препарат назначают по 2 таб. 3 раза/сут, детям — по 1/2 таб. на 5 кг/массы тела/сут в 3-4 приема в течение 14-28 дней в виде монотерапии.
При рецидивирующих остроконечных кондиломах взрослым препарат назначают по 2 таб. 3 раза/сут, детям — по 1/2 таб. на 5 кг/массы тела/сут в 3-4 приема, либо в качестве монотерапии или в комбинации с хирургическим лечением в течение 14-28 дней, далее с трехкратным повторением указанного курса с интервалами в 1 месяц.
При дисплазии шейки матки, ассоциированной с вирусом папилломы человека, назначают по 2 таб. 3 раза/сут в течение 10 дней, далее проводят 2-3 аналогичных курса с интервалом 10-14 дней.
Побочное действие
Частота развития побочных эффектов после применения препарата классифицирована согласно рекомендациям ВОЗ: часто (≥1%, <10%), иногда (≥0.1%, <1%).
Со стороны ЖКТ: часто — тошнота, рвота, боль в эпигастрии; иногда — диарея, запор.
Со стороны печени и желчевыводящих путей: часто — временное повышение активности трансаминаз и щелочной фосфатазы в плазме крови, повышение концентрации мочевины в плазме крови.
Дерматологические реакции: часто — зуд.
Со стороны нервной системы: часто — головная боль, головокружение, слабость; иногда — сонливость, бессонница.
Со стороны мочевыделительной системы: иногда — полиурия.
Со стороны опорно-двигательного аппарата и соединительной ткани: часто — боль в суставах, обострение подагры.
Противопоказания к применению
- мочекаменная болезнь;
- подагра;
- аритмии;
- хроническая почечная недостаточность;
- детский возраст до 3 лет (масса тела до 15-20 кг);
- повышенная чувствительность к компонентам препарата.
Применение при беременности и кормлении грудью
Безопасность применения Изопринозина при беременности и в период лактации не установлена, поэтому применение препарата не рекомендуется.
Применение при нарушениях функции печени
После 4 недель применения целесообразно каждый месяц проводить контроль функции печени (активность трансаминаз).
Применение при нарушениях функции почек
Противопоказан при хронической почечной недостаточности, мочекаменной болезни.
После 4 недель применения целесообразно каждый месяц проводить контроль функции почек (уровень креатинина, мочевой кислоты).
Применение у детей
Противопоказание: детский возраст до 3 лет (масса тела до 15-20 кг).
Особые указания
После 2 недель применения Изопринозина рекомендуется провести контроль содержания мочевой кислоты в сыворотке крови и в моче.
При длительном приеме после 4 недель применения целесообразно каждый месяц проводить контроль функции печени и почек (активность трансаминаз в плазме крови, уровень креатинина, мочевой кислоты).
Необходимо контролировать уровень мочевой кислоты в сыворотке крови при назначении Изопринозина в сочетании с препаратами, увеличивающими уровень мочевой кислоты или препаратами, нарушающими функцию почек.
Влияние на способность к управлению транспортными средствами и механизмами
Нет специальных противопоказаний.
Передозировка
Случаи передозировки Изопринозина не описаны.
Лекарственное взаимодействие
При одновременном применении иммунодепрессанты могут снижать эффективность Изопринозина.
Ингибиторы ксантиноксидазы и урикозурические средства (в т.ч. диуретики) могут способствовать риску повышения уровня мочевой кислоты в сыворотке крови пациентов, принимающих Изопринозин.
Условия хранения препарата Изопринозин
Препарат следует хранить в недоступном для детей, сухом, защищенном от света месте при температуре не выше 25°C.
Срок годности препарата Изопринозин
Условия реализации
Препарат отпускается по рецепту.
Контакты для обращений
ТЕВА
(Израиль)

|
|
Тева ООО 115054 Москва, Валовая ул. 35 |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Опыт применения Изопринозина при заболеваниях шейки матки на фоне папилломавирусной инфекции у подростков и молодых женщин
Статьи
Опубликовано в журнале:
«РУССКИЙ МЕДИЦИНСКИЙ ЖУРНАЛ»; ТОМ 16; № 19; 2008; стр. 1-4.
Л.И. Линаск, Е.Е. Григорьева
ГОУ ВПО «Алтайский государственный медицинский университет»
Комитет по делам здравоохранения администрации, Барнаул,
МУЗ «Детская городская поликлиника № 9», Барнаул
Последние десятилетия характеризуются высоким ростом вирусной инфекции, вследствие чего возрастает частота папилломавирусных поражений шейки матки. Вирус папилломы человека (ВПЧ) инициирует и поддерживает хронические воспалительные процессы нижнего отдела гениталий. Исследования отечественных и зарубежных авторов свидетельствуют о значимости вируса папилломы человека в развитии диспластических процессов шейки матки.
Главной особенностью ВПЧ-инфекции считают ее широкое распространение среди подростков и молодых женщин преимущественно до 25 лет [3]. Низкая сексуальная культура населения, частая смена половых партнеров, незащищенный секс, вредные привычки (курение, токсикомания, алкоголизм) увеличивают риск развития ВПЧ-инфекции, что способствует росту числа воспалительных заболеваний генитального тракта, нарушению репродуктивной функции, невынашиванию беременности и внутриутробного инфицирования плода, а также формированию цервикальной интраэпителиальной неоплазии шейки матки. Вместе с тем отмечено, что у подростков и молодых женщин происходит более быстрое самопроизвольное очищение (элиминация) от ВПЧ и регрессия имеющейся ВПЧ-ассоциированной патологии по сравнению с женщинами более позднего возраста. По результатам исследований, среднее время элиминации ВПЧ у подростков составляет 8 месяцев (CDC, 1999). По наблюдениям С.И. Роговской и В.Н. Прилепской (2006), в возрасте 18-25 лет этот период увеличивается до 1,5-2 лет у каждой второй пациентки. Локальные показатели инфицированности взаимосвязаны с другими генитальными инфекциями: трихомониазом, хламидиозом, микоуреаплазмозом, кандидозом и т.д. [7,8].
Большинство исследователей отмечают значительное разнообразие типов папилломавирусов. Чаще всего обнаруживается вирус 16 типа, следующим по частоте является вирус типа 18. На долю этих вирусов приходится около 50% от общего числа ВПЧ. Вирус папилломы человека может оказывать продуктивное (с образованием кондилом и папиллом) и непродуктивное действие на эпителий. Результатом непродуктивного действия являются внутриэпитеальные поражения, такие как цервикальная интраэпителиальная неоплазия, рак [3,11].
Наиболее уязвимым участком для воздействия вируса является зона трансформации — участок замещения цилиндрического эпителия плоским. Возможно, тропность ВПЧ к клеткам, претерпевающим метаплазию, связана с их повышенной чувствительностью к вирусной инфекции [9,11], поэтому наличие эктопии и других заболеваний на фоне вирусной инфекции является отягощающим обстоятельством для развития рака шейки матки.
Многообразие типов вирусов, возможность вызывать как продуктивное, так и непродуктивное действие на эпителий, формирование различных патологических процессов на шейке матки и наружных половых органах, сочетание вирусов с другими инфекционными агентами требуют дифференцированного подхода к консервативному лечению и избирательной оценке необходимости инвазивных методик.
По результатам исследований Е.Б. Рудаковой (2001), частота псевдоэрозий в структуре гинекологической заболеваемости женщин разных возрастных групп составляет 38,8%. При наличии гинекологических заболеваний этот процент повышается до 49,2, а у подростков и нерожавших женщин до 24 лет составляет от 52,2 до 90%. Наряду с нарушением гормонального баланса, воспалением, травмой, в генезе псевдоэрозий шейки матки существенное значение имеет нарушение местного иммунитета. Авторами доказана роль местного иммунитета в защите от возникновения и прогрессирования рака шейки матки.
По мнению В.А. Головановой и соавт. (1998), высокая частота патологии шейки матки у подростков и юных женщин связана с биологической незрелостью шейки матки, небольшим промежутком времени между менархе и началом половой жизни, ранним половым дебютом, наличием более 5 половых партнеров, что может стать фактором риска развития цервикальной интраэпителиальной неоплазии. Значимыми факторами риска для возникновения папилломавирусной инфекции являются эктопия и бактериальный вагиноз.
Комплексная диагностика ВПЧ-инфекции применительна к патологии шейки матки, хорошо разработана и предполагает использование следующих методов: клинико-визуальный, кольпоскопия, ВПЧ-тест и один из морфологических методов (цитологический -РАР-тест или гистологическое исследование прицельно взятого биоптата шейки матки).
Несмотря на расширение диапазона методов лечения (химио-, крио-, лазеро-, электродеструкция), которые применяются при доброкачественных заболеваниях шейки матки, не существует единых подходов к выбору метода и значимых критериев преимущества одной методики перед другой. Эффективность терапии во многом зависит от выбора метода лечения, использования иммунокорригирующей терапии и целесообразности комбинированного лечения с применением деструктивного воздействия на шейку матки. Большинство исследователей подчеркивают неудачу методов локальной деструкции, отмечают частые рецидивы ВПЧ инфекции на фоне иммунодефицита, обосновывают целесообразность иммунотерапии [2].
В.Н. Прилепская и С.И. Роговская предлагают комбинированное деструктивное лечение папилломавирусных поражений шейки матки проводить на фоне приема иммунопрепаратов, снижающих активность вируса и повышающих иммунитет. Разумная иммунокоррекция повышает эффективность терапии и снижает вероятность рецидива [3,4,7].
Наиболее широкое применение получили интерфероны и их индукторы, иммуномодуляторы. Эти препараты стимулируют неспецифический иммунитет, усиливают продукцию интерлейкинов, повышая синтез антител, стимулируют хемотаксическую и фагоцитарную активность моноцитов, макрофагов и полиморфно-ядерных клеток.
В настоящее время имеется большой выбор препаратов — активаторов иммунитета. Противовирусный препарат Изопринозин (производства «Тева фармацевтические предприятия Лтд.», Израиль), содержит активное вещество — инозин пранобекс, который подавляет репликацию ДНК и РНК вирусов посредством связывания с рибосомой клетки и изменения ее стереохимического строения. Кроме противовирусного действия, препарат обладает и иммуномодулирующим свойством за счет комплекса инозина, что повышает его доступность для лимфоцитов.
Целью настоящего исследования явилось изучение клинической эффективности препарата Изопринозин в монотерапии и комплексном лечении заболеваний шейки матки при ВПЧ-инфекции у подростков и юных женщин.
Материалы и методы
Всего обследовано 74 пациентки с патологией шейки матки на фоне ВПЧ-инфекции в возрасте от 15 до 25 лет (средний возраст 19,4±0,2 лет). Всем пациенткам проведено комплексное обследование, включающее изучение анамнеза, общий и гинекологический осмотр, расширенную кольпоскопию, бактериоскопию вагинальных мазков, окрашенных по Граму, ПЦР-типирование, цитологическое исследование соскобов с шейки матки.
Всем обследованным в монотерапии или при комбинированном лечении назначался Изопринозин.
Возрастная структура обследуемых: подростки в возрасте до 18 лет — 35 (47,3%), молодые женщины 19-25 лет — 38 (51,9%), в основном учащаяся молодежь (студентки ВУЗов и колледжей).
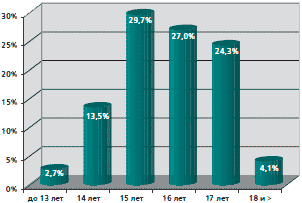
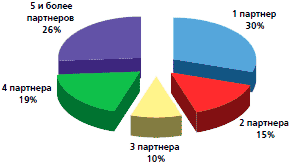
Нами проведена оценка среднего возраста начала половой жизни, количества и частоты смены половых партнеров. Анализ показал, что средний возраст начала половой жизни составил 15,9±0,1 лет. На рисунках 1 и 2 представлены диаграмма полового дебюта и полигамности половых связей. Только каждая третья имела постоянного полового партнера, у каждой четвертой отмечена полигамность половых связей (более 5 партнеров). У 52 (70,3%) менархе отмечено до 14 лет, у 22 (29,7%) после 14 лет, причем у каждой третьей наблюдалось позднее менархе. У большинства женщин — 54 (72,9%) менструальный цикл имел регулярный характер, у каждой пятой месячные были нерегулярные (опсо- или гиперполименореи).
Рис. 1. Возраст сексуального дебюта у девушек-подростков и молодых женщин (n=74)
Рис. 2. Число сексуальных партнеров у девочек-подростков и молодых женщин (n=74)
При изучении соматического анамнеза установлено, что хронический тонзиллит и другие очаги инфекции носоглотки имели место у 21 (28,4%) пациентки, заболевания желудочно-кишечного тракта — у 20 (27%), вегето-сосудистая дистония — у 25 (33,8%). Индекс соматических заболеваний составил 1,2 на 1 пациентку. Изучение анамнеза перенесенных детских инфекций показал, что каждая вторая девочка-подросток и молодая женщина переболела ветряной оспой, каждая третья — коревой краснухой; респираторно-вирусные инфекции были у 38 (51,3%) пациенток. Высокий инфекционный индекс, составляющий более 1,5 на 1 пациентку, свидетельствует о возможных изменениях иммунного статуса.
Особый интерес представляло изучение гинекологического анамнеза, при котором установлено, что воспалительные процессы наружных и внутренних половых органов составили более 85%. Несмотря на молодой возраст обследуемых, у 5 (6,8%) имел место острый эндометрит, у 3 (4,1%) — воспалительный процесс придатков матки и у 56 (75,7%) отмечался вульвовагинит. При всех эпизодах воспалительных заболеваний ранее проводилось лечение.
При гинекологическом осмотре в 100% выявлена патология шейки матки (эрозия, цервициты, лейкоплакии и т.д.). Определение инфекций, передаваемых половым путем, методом ПЦР и бактериоскопии, позволило установить не только различное типирование ВПЧ-инфекции, но и многофакторные причины воспалительных изменений на шейке матки. Моноинфекция имела место лишь у 18 (24,3%), два инфекционных фактора отмечены у 31(41,9%) пациентки, три и более инфекционных агента выявлены у 25 (33,8%) обследуемых. На одну пациентку приходится 2,4 возбудителя.
Как видно из таблицы 1, чаще всего определялся вирус папилломы человека 16,18 типа, который выявлен в 93,2%; ВПЧ 31,33 типа и ВПЧ 6,11 установлены в 14,9 и 17,6% соответственно. Следует отметить, что вирус папилломы человека, как моноинфекция, был только у каждой четвертой, у остальных 75% наиболее частыми сочетаниями являлись уреа — и микоплазменные возбудители. Процент микоплазмоза составил 28,4, а уреаплазмоза — 39,2. Хламидии определены у каждой пятой, трихомонады выявлены у 3 (4%), кандиды — у 11 (14,9%).
Таблица 1.
Основные виды ИППП
| Вид инфекции | Всего (n=74) | |
| абс. | % | |
| Трихомониаз | 3 | 4,1 |
| Микоплазмоз | 21 | 28,4 |
| Уреаплазмоз | 29 | 39,2 |
| Хламидиоз | 14 | 18,9 |
| ВПЧ 16,18 | 69 | 93,2 |
| ВПЧ 31,33 | 11 | 14,9 |
| ВПЧ 6,11 | 13 | 17,6 |
| ВПГ 1,2 | 5 | 6,8 |
| Кандидоз | 11 | 14,9 |
Всем пациенткам до начала лечения и после него проводилась простая и расширенная кольпоскопия. На начальном этапе обследования выявлены разнообразные кольпоскопические картины: эктопия с зоной трансформации, множественными открытыми и закрытыми протоками желез, признаки очагового и диффузного кольпита, зона трансформации с атипичным эпителием в виде лейкоплакии, йоднегативные зоны, мозаика в различных сочетаниях друг с другом. При цитологическом исследовании соскобов с шейки матки I тип цитограммы установлен у 39,2% обследованных, II тип — у 60,8%.
Высокий процент инфицированности, наличие цитограммы воспаления значительно повышают риск развития дисплазий. Учитывая молодой возраст пациенток, гистологическое исследование проводилось лишь по особым показаниям при осложненных формах эктопии, лейкоплакии и цитологически установленной дисплазии. Дисплазия установлена у 6 (8,1%), причем умеренно выраженная дисплазия составила 33,3%, то есть имела место у каждой третьей из шести. Также у каждой третей из всех обследованных имела место лейкоплакия. Проведенные углубленные исследования (кольпоскопическая визуализация и цитологическая диагностика) явились показанием для взятия гистологических исследований у 28 (37,8%) юных и молодых женщин. В подавляющем большинстве определена простая лейкоплакия, прогрессирующий эндоцервикоз.
Несмотря на то, что у всех пациенток выявлена ВПЧ инфекция, специфическая противовирусная терапия Изопринозином назначалась сразу только 18 пациенткам, остальным потребовались антибактериальная и санационная терапии, направленные на элиминацию возбудителей патогенной и условно-патогенной флоры. При верификации инфекции проводилась специфическая терапия основного инфекционного заболевания. При урео- и микоплазмозе, хламидиозе использовались антибактериальные препараты, при кандидозе -противогрибковые, при бактериальном вагинозе — коррекция биоценоза по общим терапевтическим схемам.
После проведения противовоспалительного лечения и контрольной кольпоскопии пациенткам назначался Изопринозин по 1,0 г 3 раза в сутки в течение 10 дней. По основному заболеванию шейки матки 31-й (41,9%) из обследованных женщин потребовалось комбинированное лечение с использованием радиоволновой терапии.
Эффективность монотерапии Изопринозином оценивалась по лабораторным исследованиям ПЦР-диагностики ВПЧ-инфекции через 1,5-2 месяца по окончанию терапии. Полученные результаты свидетельствуют, что полная элиминация вируса составила 95,3%, что подтверждено клинико-лабораторным выздоровлением в 41 случае из 43-х, что свидетельствует о высокой эффективности препарата.
При проведении комбинированной терапии с использованием радиоволновой методики воздействия на шейку матки и иммунокорригирующих препаратов эффективность лечения оценивалась через 2 месяца и полгода. Кольпоскопия показала, что у 30 (96,8%) обследуемых установлена нормальная кольпоскопическая картина, рецидив ВПЧ-инфекции имел место лишь в одном случае.
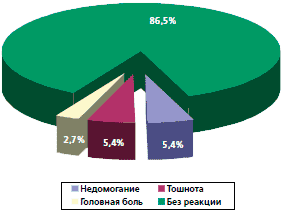
Кроме клинической эффективности, проведена оценка переносимости препарата Изопринозин. Установлено, что у 4 (5,4%) пациенток отмечалось легкое недомогание и тошнота, которые купировались на второй день приема препарата и не потребовали его отмены. Две пациентки жаловались на кратковременную головную боль, возможно, связанную с приемом препарата (рис. 3.). Других побочных проявлений и аллергических реакций не отмечено.
Рис. 3. Характер побочных реакций применения Изопринозина
Таким образом, исследование, проведенное в группе подростков и молодых женщин с заболеваниями шейки матки на фоне папилломавирусной инфекции, и оценка эффективности изопринозина в монотерапии и комбинированном лечении позволяет сделать следующие выводы:
1. Большинство пациенток с папилломавирусной инфекцией имели отягощенный соматический и гинекологический анамнезы.
2. Папилломавирусная инфекция чаще сочетается с уреаплазмозом, микоплазмозом и кандидозом, которые в совокупности составили более 80% всех других возбудителей.
3. Изопринозин является высокоэффективным препаратом для лечения ВПЧ-инфекции при заболеваниях шейки матки у подростков и молодых женщин.
4. Эффективность в монотерапии Изопринозином составляет 95,3%. При использовании Изопринозина в сочетании с радиоволновой терапией эффективность достигает 96,8% при контроле через полгода, несмотря на выраженные первоначальные морфологические изменения шейки матки.
5. Учитывая высокую эффективность препарата, хорошую переносимость и отсутствие побочных явлений, Изопринозин может быть использован при лечении девочек-подростков и юных женщин.
Литература
1. Голованова В.А., Гуркин Ю.А., Новик В.И. // Актуальные вопросы детской и подростковой гинекологии: материалы и тез. докл. Всерос. науч.-практ. конф. — Новосибирск, 1998. — С. 148-150.
2. Минкина Г.Н. Предрак шейки матки /Г.Н. Минкина, И.Б. Манухин, Г.А. Франк. — М., 2001. -С. 69-72.
3. Прилепская В.Н. Генитальные инфекции и патология шейки матки. Клинические лекции / B.Н. Прилепская, Е.Б. Рудакова. — Омск: ИПЦ ОмГМА, 2004. — 212 с.
4. Прилепская В.Н. Заболевания шейки матки, влагалища и вульвы/В.Н. Прилепская. — М.: МЕД пресс-информ, 2005. — 432 с.
5. Прилепская В.Н. Вирус папилломы человека: современный взгляд на проблему / В.Н. Прилепская // Медицинский вестник. — 2007. — № 29 (414). — С. 9-10.
6. Рудакова Е.Б. Псевдоэрозии шейки матки: автореф. дис…. д-ра мед. наук/Е.Б. Рудакова. — Омск, 1996. — 34 с.
7. Роговская С.И. Оптимизация лечения хронических цервицитов с помощью изопринозина / C.И. Роговская, В.Н. Прилепская//Гинекология. — 2006. — Т. 8, № 1. — С. 4-7.
8. Тихонова Л.И. Общий обзор ситуации с инфекциями, передаваемыми половым путем / Л.И. Тихонова// Вестн. дерматологии и венерологии. — 1999. — № 2. — С. 4-7.
9. Auborn K.J. Treatment of human papillomavirus gynecologic infections/K.J. Auborn, T.H. Carter // Clin Lab Med. — 2000. — Vol. 20, N 2. — P 407-422.
10. Guidelines 2002 for treatment of sexually transmitted diseases / CDC Alanta. — USA. — 400 p. Workowski, K.A. Sexually Transmitted Diseases Treatment Guidelines — 2002/K.A. Workowski, W.C. Levine//MMWR Recomm Rep. — 2002.-Vol. 51 (RR-6). — P. 1-78.
11. Nagai Y. Persistence of human papillomavirus infection after therapeutic conization for CIN 3: is it an alarm for disease recurrence?/ Y. Nagai, T. Maehama, T. Asato, K. Kanazawa // Gynecol Oncol. — 2000. — Vol. 79, N 2. — P. 294-299.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Заболевания, ассоциированные с вирусом папилломы человека (ВПЧ), являются одной из важнейших проблем в акушерстве и гинекологии. Вирус вызывает целый ряд заболеваний кожи и слизистых оболочек. В настоящее время известно уже более 200 типов папилломавирусов, причем 40 из них поражают мочеполовые органы. Инфицированность населения Земли папилломавирусом впечатляет – им инфицировано около 600 млн жителей планеты, причем у 28% зараженных в процессе задействованы онкогенные типы вирусов [16, 17].
В связи с резким ростом инфицированности населения ВПЧ, значительной его контагиозностью и способностью вызывать злокачественную патологию диагностика и лечение заболеваний, ассоциированных с папилломавирусной инфекцией, привлекают особое внимание акушеров-гинекологов. Согласно данным ВОЗ, папилломавирусная инфекция является наиболее распространенной инфекцией, передающейся половым путем; в Европе инфицированность ею населения репродуктивного возраста составляет 20–60% [1, 3, 14].
На сегодняшний день доказано, что папилломавирусная инфекция является ведущей причиной рака шейки матки [2, 15, 18, 20]. При инвазивном раке шейки матки в 95–100% случаев выявляется ВПЧ.
Как показали исследования последних лет, большинство женщин на протяжении жизни инфицируются ВПЧ. Так, например, более 80% женщин заражаются ВПЧ уже через 2 года после начала половой жизни, при этом даже при наличии одного полового партнера 20% женщин являются зараженными ВПЧ [10, 13]. Благодаря работе иммунной системы первичное заражение ВПЧ в большинстве случаев остается незамеченным и не сопровождается какими-либо последствиями. Однако тем, у кого самоэлиминации вируса не произошло, приходится жить с ВПЧ и бороться с его разрушающим действием. ВПЧ обнаруживают у 99,7% женщин с гистологически подтвержденным диагнозом рака шейки матки. При этом нередко определяется инфицированность различными типами ВПЧ, в т. ч. у женщин с нормальной цитологией.
Рак шейки матки представляет собой важную социальную проблему. На сегодняшний день он является одной из основных причин смерти от злокачественных опухолей у женщин в возрасте 15–40 лет. Особенно заметный рост наблюдается в группе моложе 29 лет, где прирост этого показателя за прошедшее десятилетие составил 150% [4].
Папилломавирусы передаются только от человека к человеку. Основным путем заражения ВПЧ является половой (включая орогенитальные и анальные контакты). Доказана возможность передачи папилломавирусной инфекции от матери плоду с поражением гортани (ларингеальный папилломатоз) и появлением аногенитальных бородавок у новорожденного, а также способность поражать клетки трофобласта, что может являться причиной прерывания беременности [15, 20].
Инкубационный период при заражении ВПЧ составляет от 3 мес. до нескольких лет.
Факторами риска инфицирования ВПЧ являются:
• раннее начало половой жизни;
• наличие более 3-х половых партнеров;
• наличие одного полового партнера, у которого множество половых партнеров;
• курение;
• наличие других инфекций, передающихся половым путем;
• нарушение иммунитета;
• факторы окружающей среды, условия жизни и работы.
По онкогенной опасности для человека условно выделяют три группы типов папилломавирусов (табл. 1):
• неонкогенные папилломавирусы ‒ никогда не приводят к озлокачествлению вызванного ими процесса;
• онкогенные папилломавирусы низкого риска – при определенных условиях (достаточно редко) могут приводить к озлокачествлению вызванного процесса;
• онкогенные папилломавирусы высокого онкогенного риска ‒ под влиянием различных факторов приводят к озлокачествлению вызванного ими процесса и являются доказанным этиологическим фактором рака шейки матки.
Течение папилломавирусной инфекции во многом зависит от состояния иммунной системы. В 70–80% случаев оно может быть транзиторным, и тогда наблюдается спонтанное очищение пораженной ткани от ВПЧ. Данный благоприятный исход возможен у молодых женщин с нормальным состоянием иммунной системы.
Латентное течение ВПЧ-инфекции характеризуется отсутствием каких-либо клинических и морфологических изменений при обнаружении ДНК вируса. В данном случае требуется наблюдение и постоянный контроль за состоянием эпителия шейки матки, влагалища и вульвы [11, 19].
В 20–30% случаев при ВПЧ-инфекции наблюдается прогрессирование заболевания. После элиминации вируса у части женщин сохраняются субклинические проявления инфекции, которые могут переходить в клиническую фазу у женщин с нарушением иммунитета [12]. ВПЧ довольно долго персистирует в многослойном плоском эпителии, что способствует рецидивированию заболевания.
По варианту течения и глубине поражения ВПЧ-ассоциированные заболевания нижнего отдела гениталий делятся на следующие формы [11, 12]:
1. Клинические (видимые невооруженным глазом):
– экзофитные кондиломы (остроконечные типичные, папиллярные, папуловидные);
– симптоматические цервикальные интраэпителиальные неоплазии.
2. Субклинические (невидимые невооруженным глазом и бессимптомные, выявляемые только при кольпоскопии и/или цитологическом либо гистологическом исследовании):
– плоские кондиломы (типичная структура с множеством койлоцитов);
– малые формы (различные поражения многослойного плоского эпителия и метапластического эпителия с единичными койлоцитами);
– кондиломатозный цервицит/вагинит.
3. Латентные (отсутствие клинических, морфологических или гистологических изменений при обнаружении ДНК ВПЧ).
4. Цервикальная интраэпителиальная неоплазия (CIN) или плоскоклеточные интраэпителиальные поражения (SIL) и рак шейки матки:
‒ CIN I – слабая дисплазия с койлоцитозом, дискератозом или без них;
‒ CIN II – умеренная дисплазия с койлоцитозом, дискератозом или без них;
‒ CIN III – тяжелая дисплазия или карцинома in situ с койлоцитозом, дискератозом или без них;
‒ микроинвазивная плоскоклеточная и железистая карцинома.
Субклинические формы – плоские кондиломы, вирусные цервициты и вагиниты – являются причиной частых обращений больных к врачам с жалобами на дискомфорт, обусловленный зудом, жжением, обильными выделениями, рецидивирующим бактериальным вагинозом и кандидозом. В большинстве случаев у таких пациенток возникают обострения клинических симптомов перед каждой менструацией. Клинические формы течения ВПЧ-инфекции – экзофитные кондиломы – могут быть незначительны по размерам и площади поражения, но вызывать нестерпимый зуд у пациенток, и наоборот, достаточно большие образования бывают врачебной находкой во время профилактического осмотра. Длительная персистенция ВПЧ в ткани органов нижнего отдела генитального тракта способна провоцировать развитие предраковых и раковых процессов.
Целый ряд онкологических заболеваний связан с высокоонкогенными типами ВПЧ, в первую очередь с 16 и 18 [19], в их числе рак шейки матки, прямой кишки, влагалища и вульвы, рак полового члена, гортани, ротовой полости.
Для диагностики ВПЧ-ассоциированных заболеваний применяются следующие методы исследования:
• клинические;
• цитологические (Pap-test);
• расширенная кольпоскопия;
• подтверждение наличия ДНК ВПЧ в цервикальном эпителии (ПЦР);
• определение вирусной нагрузки методом Hybride Capture (ВПЧ-Digene-тест), позволяющее выявить число копий ДНК онкогенных вирусов;
• ПЦР в режиме реального времени;
• жидкостная цитология;
• морфологическое исследование;
• определение онкомаркеров – онкобелков p16, Кi67;
• сканирование шейки матки в режиме реального времени (TruScreen) и др.
Клинико-визуальный метод является наиболее простым в диагностике ВПЧ-инфекции гениталий. С помощью рутинного осмотра вульвы, промежности, перианальной области, шейки матки и влагалища с использованием теста с раствором Люголя и 3–5% уксусной кислотой выявляется большинство клинических и субклинических форм инфекции. Однако данный метод не позволяет судить о характере и прогнозе течения патологического процесса [5].
Кольпоскопия представляет собой высокоинформативный и недорогой метод диагностики заболеваний шейки матки. Наиболее распространенной является расширенная кольпоскопия, которая включает осмотр и ревизию состояния слизистой оболочки шейки матки, влагалища и вульвы при увеличении микроскопа в 7–30 раз и применении некоторых эпителиальных тестов, при которых оценивается реакция тканей в ответ на их обработку различными медикаментозными средствами. Для более детального осмотра сосудистой сети применяются различные фильтры [5].
Диагностика типичных экзофитных кондилом не представляет особой сложности. Кольпоскопически они имеют характерный вид с пальцеобразными выпячиваниями и наличием петли сосуда в каждом из них. Большие трудности вызывает диагностика субклинических форм папилломавирусной инфекции и выявление кольпоскопических признаков, характеризующих вирусные поражения слизистой оболочки шейки матки, влагалища и вульвы. Это сложно еще и потому, что участки ВПЧ-инфекции могут сочетаться с другими доброкачественными и злокачественными образованиями эпителия. В связи с большим разнообразием проявлений субклинической инфекции специфического комплекса кольпоскопических признаков нет. Точно диагностировать внутриэпителиальные кондиломы с помощью одного кольпоскопического метода возможно только при выраженном ороговении или при сочетании плоских форм кондилом с экзофитными.
В настоящее время существует достаточно лекарственных средств для устранения симптомов заболевания, а также препаратов для повышения иммунитета, которые позволяют полностью избавиться от рецидивов и добиться такого результата, когда вирус не обнаруживается в анализах. Такой низкий уровень его концентрации поможет забыть о внешних проявлениях и предупредить развитие онкологических заболеваний, особенно часто встречающихся на фоне ВПЧ у женщин.
Выбор метода лечения при ВПЧ-ассоциированной патологии зависит от ряда факторов, включая морфологию, размеры, количество и локализацию кондилом, возраст больных и наличие беременности. В этом процессе немаловажную роль также играет собственный опыт врача и метод лечения, который он предпочитает. Основной целью терапии является элиминация кондилом, которые вызывают симптомы, сопряженные с физическим и психологическим дискомфортом. Тяжесть клинической манифестации ВПЧ-ассоциированной патологии слизистых оболочек и кожи урогенитальной и перианальной области широко варьирует, что требует тщательного выбора и обоснования целесообразности использования того или иного метода в каждом конкретном случае.
Доказательства преимущества какого-либо определенного метода перед остальными отсутствуют. Лечебное средство нужно выбирать индивидуально, исходя из того принципа, что лечебное воздействие не должно сопровождаться осложнениями, вызывающими более тяжелые страдания по сравнению с основной болезнью. При этом следует также учитывать выбор пациенток, исходя из стоимости и комфортности того или иного метода лечения для конкретного больного.
Арсенал средств:
• криодеструкция жидким азотом (пораженную область уничтожают замораживанием);
• радиоволновое удаление кандилом и лечение шейки матки;
• лазерная терапия – вариант, к которому желательно прибегать только в крайних случаях. Дело в том, что вирус, обработанный лазером, попадает в воздух и может заразить медперсонал, работающий без защитных масок;
• лекарственный метод – обработка пораженной области различными кремами, мазями, гелями, назначение иммуностимуляторов.
Целью настоящего исследования явилась оценка эффективности применения инозина пранобекса (Изопринозина) при остроконечных кондиломах, CIN, субклинических формах ВПЧ в комбинированном режиме.
Материал и методы. Проведен анализ эффективности применения и побочных эффектов инозина пранобекса (ИП) при ВПЧ-ассоциированных поражениях слизистых оболочек и кожи у 30 больных. ИП назначали 30 больным, из них 11 пациенток принимали ИП в монорежиме, а 19 – в комбинированном режиме. При этом сравнивали эффективность лечения ВПЧ-ассоциированных заболеваний по степени ликвидации жалоб на зуд и неприятные ощущения, по площади регрессии макроскопических изменений, при ВПЧ-ассоциированных заболеваниях шейки матки – по результатам ДНК ВПЧ-теста.
Далее побочные эффекты были проанализированы по результатам лечения пациенток, которые принимали ИП как в монорежиме, так и в комбинированном режиме.
Результаты исследования. Пациентки распределились по возрастным группам следующим образом: число пациенток до 20 лет составило 5; от 21 до 25 лет – 10; от 26 до 30 лет – 7; от 31 до 35 лет – 4; от 36 до 40 лет – 3; от 41 до 45 лет – 1.
Латентное течение ВПЧ-инфекции было зарегистрировано у 3 пациенток на основе ПЦР ДНК ВПЧ-тестов и клинических исследований. Различные проявления ВПЧ в виде высыпаний (остроконечных или плоских кондилом) в перианальной и урогенитальной области, области влагалища и шейки матки были обнаружены у 9 пациенток. Из них у 4 пациенток выявлены сочетанные вирусные инфекции (ВПГ 1, 2, ЦМВ) с ВПЧ-ассоциированными заболеваниями. При гинекологическом осмотре у 10 больных обнаружена эктопия, у 2 – истинная эрозия, у 5 женщин – цервициты и эндоцервициты. У 7 пациенток выявлен бактериальный вагиноз.
На основании цитологического, кольпоскопического и патоморфологического исследований у 2 пациенток установлена цервикальная интраэпителиальная неоплазия.
Результаты анализа в период 6-месячного наблюдения свидетельствуют о существенном снижении зуда и неприятных ощущений от первоначального осмотра к моменту повторных осмотров у всех пациенток, независимо от их возраста во всех группах. При этом также отмечено существенное снижение частоты жалоб после комбинированного применения ИП по сравнению с аналогичными показателями, как при применении традиционных методов лечения, так и ИП в монорежиме во всех возрастных группах (p<0,05).
Результаты визуальной оценки уменьшения площади ВПЧ-ассоциированных патологически измененных участков шейки матки, слизистых оболочек и кожи урогенитальной, анальной и перианальной областей после их лечения различными методами с и без применения ИП свидетельствуют, что наиболее значительное клиническое улучшение наступило после комбинированного лечения по сравнению с применением ИП в монорежиме (p<0,001). Результаты применения традиционных методов лечения оказались одинаковыми по эффективности с ИП в монорежиме (p<0,001) и ниже, чем таковые в группе с ИП в комбинированном режиме (p<0,001).
Результаты повторного анализа ПЦР ДНК ВПЧ-тестирования через 6 мес. у женщин, включенных в исследование, оказались положительными в среднем в 66,2±0,08% наблюдений, у женщин после традиционных методов лечения – в 52,6±0,09%, у пациенток после ИП в монорежиме – в 42,6±0,09%, у женщин после ИП в комбинированном режиме – в 25,3±0,08% наблюдений.
Анализ результатов свидетельствует, что применение ИП как в монорежиме, так и в комбинированном способствует существенной элиминации ВПЧ (p<0,05 и p<0,001 соответственно) по сравнению с аналогичным показателем спонтанной элиминации ВПЧ в группе наблюдения. При этом применение ИП в комбинированном режиме способствует значительному снижению ДНК ВПЧ-положительных результатов по сравнению с аналогичным показателем традиционных методов лечения (p<0,01), что не противоречит данным других исследователей [6–9].
Заключение. Инозин пранобекс (Изопринозин) – давно используемый в медицинской практике иммуностимулятор, который считается эффективным при различных вирусных инфекциях. ИП, по своей природе являясь производным пуринов и жизненно важным компонентом клеточного ядра, не дает выраженного токсического эффекта даже при назначении в высоких дозах. Обычно природные аналоги ИП поступают в организм из разнообразных пищевых продуктов. Поэтому при правильном назначении ИП в качестве иммуностимулятора с учетом противопоказаний к его применению частота побочных эффектов минимальна. Об этом свидетельствуют данные многолетнего использования ИП в медицинской практике во всем мире. Обнадеживающие результаты комбинированного применения ИП позволяют сделать вывод о целесообразности включения указанного иммуномодулятора в схемы традиционных методов лечения ВПЧ-ассоциированной патологии слизистых оболочек и кожи. Требуется дальнейшее изучение эффективности этого метода с точки зрения доказательной медицины.
Литература
1. Европейские стандарты диагностики и лечения заболеваний, передаваемых половым путем. М.: Медлит, 2004.
2. Качалина Т.С., Шахова Н.М., Качалина О.В. и др. Возможности диагностики и лечения ВПЧ-ассоциированных цервикальных неоплазий у женщин репродуктивного возраста в современных условиях // РМЖ. 2014. № 14. С. 1024–1028.
3. Краснопольский В.И. и др. Инфицированность вирусом папилломы человека среди девочек-подростков в Московской области // Рос. вестник акушера-гинеколога. 2010. № 5. С. 46–49.
4. Чиссов В.И., Старинский В.В., Петрова Г.В. Злокачественные новообразования в России в 2010 году (заболеваемость и смертность). М., 2012. 260 с.
5. Бауэр Г. Цветной атлас по кольпоскопии; пер. с нем. / Под ред. С.И. Роговской. М.: ГЭОТАР-МЕД, 2015. С. 288.
6. Елисеева Ю.Е., Мынбаев О.А. Роль вспомогательной иммунотерапии в решении проблем ВПЧ-ассоциированных патологических поражений слизистых оболочек и кожи // Акушерство и гинекология. 2011. № 4. С. 104–111.
7. Елисеева М.Ю., Мынбаев О.А. Роль иммунотерапии в решении проблем ВПЧ-ассоциированных патологических поражений слизистых оболочек и кожи // Акушерство и гинекология. 2011. Т. 4. С. 104–111.
8. Мынбаев О.А., Елисеева М.Ю. Вспомогательная иммунотерапия ВПЧ-ассоциированных поражений кожи и слизистых оболочек (обзор литературы) // Гинекология. 2011. Т. 13(3). С. 32–41.
9. Прилепская В.Н., Довлетханова Э.Р., Абакарова П.Р. Возможности терапии ВПЧ-ассоциированных заболеваний гениталий у женщин // Акушерство и гинекология. 2011. № 5. С. 123–128.
10. Потапов В.А., Демченко Т.В., Стрельцова Т.Р. и др. Клинико-лабораторная оценка эффективности Изопринозина в лечении папилломавирусной инфекции, ассоциированной с цервикальной интраэпителиальной неоплазией // Репродуктивное здоровье женщины. 2006. Т. 25, № 1. С. 134–135.
11. Прилепская В.Н., Роговская С.И. Возможности Изопринозина в лечении хронических цервицитов и вагинитов // РМЖ. 2008. Т. 16, № 1. С. 5–9.
12. Прилепская В.Н., Костава М.Н., Назарова Н.М. и др. Эффективность применения Изопринозина при лечении вульводинии, обусловленной инфекционно-воспалительными процессами // РМЖ. 2009. Т. 17, № 16. С. 1046–1048.
13. Роговская С.И. Папилломавирусная инфекция у женщин и патология шейки матки: в помощь практикующему врачу. М.: ГЭОТАР-Медиа, 2008.
14. Стратегический документ «Подготовка к внедрению вакцины против ВПЧ в Европейском регионе».‒ ВОЗ, 2008.
15. Шварц Г.Я., Прилепская В.Н., Мынбаев О.А. Изопринозин в лечении папилломавирусной инфекции в гинекологической практике. М., 2011.
16. Gaspar J. et al. Sociodemografic and clinical factors of women with HIV // Rev. lat. Am. Enfermagem. 2015. Vol. 23. № 1. P. 74–81.
17. Madeddu G.. et al. HPV infection in HPV-positive females: the need for cervical cancer screening including HPV-DNA defection despite successful HAART // Eur. Rev. Med. Pfarmacol. Sci. 2014. Vol. 18(8). P. 1277–1285.
18. Guidelines for treatment of sexually transmitted diseases. CDC reports 2006‒2008. MMWR, 2006. Vol. 55. RR‒ 11. P. 62‒67 http://www.cdc.gov/std
19. Russomano F., Reis A., Camargo M. et al. Efficacy in treatment of subclinical cervical HPV infections without CIN. Systemic review // Rev. Paul Med. 2000. Vol. 118, № 4. P. 109–115.
20. Nagai Y. Persistence of human papillomavirus infection after therapeutic conization for CIN 3: is it an alarm for disease recurrence? // Gynecol. Oncol. 2000. Vol. 79, № 2. P. 294–299.
Представлены результаты комплексного лечения 78 больных с обыкновенными, ладонно-подошвеннными, плоскими бородавками, остроконечными кондиломами. Помимо деструктивных методов терапии (криодеструкция, лазерная деструкция, местные цитотоксические препараты) применяли противовирусный и иммуностимулирующий препарат Изопринозин (инозин праногбекс). Эффективность комплексного лечения остроконечных кондилом составиоа — 93,6%, обыкновенных и плоских бородавок — 100%, ладонно-подошвенных бородавок — 83,4% (в целом 93,3%). Нежелательные побочные явления отмечены в 4,0% случаев, причем их развитие не требовало отмены Изопринозина.
Вирус папилломы человека (ВПЧ) повсеместно распространен и вызывает широкий спектр доброкачественных поражений кожи и слизистых оболочек, играя при этом немаловажную роль в патогенезе злокачественных новообразований, в частности плоскоклеточного рака кожи, шейки матки, полового члена, ареолы молочной железы и т. д. [1, 2]. К настоящему времени описано более 150 типов ВПЧ. По некоторым данным, инфицированность ВПЧ среди взрослой популяции составляет 20–60 % [2]. По данным Центра по контролю за инфекционными заболеваниями (Атланта, США), генитальными бородавками и кондиломами, возбудителями которых являются различные типы ВПЧ, в мире болеют около 630 млн человек, причем по распространенности ВПЧ в 3 раза превосходит генитальный герпес и не уступает гонорее [4]. Считается, что более 75 % сексуально активных мужчин и женщин на протяжении жизни были инфицированы минимум одним типом ВПЧ [3].
К заболеваниям, вызываемым ВПЧ, в настоящее время относят бородавки, остроконечные кондиломы, верруциформную эпидермодисплазию, папилломы, некоторые предраковые болезни и формы рака (см. выше) [4]. Первых два заболевания распространены наиболее широко. Так, например, простые бородавки выявляются у 20 % школьников, остроконечные кондиломы в развитых странах являются самыми распространенными заболеваниями, передающимися половым путем [1], а среди пациенток, обращающихся за помощью в гинекологические клиники, инфицированы ВПЧ 44,3 % женщин [1, 5, 9].
В связи с вышеизложенным поиск эффективных методов лечения больных ВПЧ-инфекцией является актуальной проблемой для всех стран мира.
На сегодняшний день в арсенале практических врачей имеется множество методик лечения вызываемых ВПЧ заболевания, например аногенитальных кондилом. Эффективность этих лечебных подходов варьируется в пределах от 30 до 90 %, но ни один из них не может рассматриваться как оптимальный, т. к. частота рецидивов даже при применении самых современных методов составляет 15–20 %. При этом установлено, что включение в комплекс лечебных мероприятий иммуностимулирующих препаратов повышает эффективность терапии, хотя и не решает проблему полностью [6–9].
Цель настоящего исследования состояла в оценке эффективности и безопасности включения в стандартную комплексную терапию больных бородавками и остроконечными кондиломами иммуностимулирующего и антивирусного препарата Изопринозин (инозин пранобекс).
Материал и методы
В исследование были включены 78 больных, в т. ч. 47 мужчин и 31 женщина. У 3 пациентов были выявлены обыкновенные бородавки, у 6 – ладонно-подошвенные бородавки, у 3 – плоские бородавки, у 66 – остроконечные кондиломы (см. таблицу).
Таблица. Нозологический состав и половая принадлежность больных.
Критерии включения:
- клинически верифицированный диагноз бородавок или остроконечных кондилом;
- возраст 3 года и старше;
- наличие информированного согласия на участие в исследовании пациента или его родителей. Критерии исключения:
- мочекаменная болезнь, сердечная аритмия, почечная недостаточность, беременность и лактация;
- возраст до 3 лет;
- индивидуальная непереносимость Изопринозина.
Критерии эффективности лечения (выздоровления):
- полное разрешение всех элементов высыпаний;
- отсутствие рецидивов в период наблюдения (9 месяцев).
Самую большую группу – 66 (84,6 %) человек – составили пациенты с остроконечными кондиломами. По возрасту они распределялись следующим образом: до 17 лет – 6, 18–20 лет – 16, 21–25 лет – 19, 26–30 лет – 9, 31–35 лет – 11, 36–40 – 4, 41–50 лет – 1 пациент. Таким образом, 50 больных (75,8 % от их общего числа в группе) заразились в возрасте до 30 лет. Замужние (10 человек) и женатые (15 человек) в этой группе составили 37,9 %. Пятнадцать пациентов (22,7 %) ранее получали лечение по поводу остроконечных кондилом (Циклоферон, аллокин-альфа, ферезол, криодеструкция), но у них развился рецидив. Из сопутствующих заболеваний в группе выявлены трихомониаз (19 человек – 28,8 %), гонорея (2 человека – 3,0 %), хламидиоз (8 человек – 12,1 %), кандидоз влагалища (13 человек – 19,7 %).
В составе комплексного лечения применялись криодеструкция высыпаний (с помощью аппарата “Азокриод”); Изопринозин (Тева) по 1000 мг (2 таблетки) 3 раза в сутки после еды в комбинации с местным цитотоксическим препаратом подофиллотоксин (Кондилин).
При обыкновенных и плоских бородавках криодеструкция элементов производилась на 5-й день на фоне приема Изопринозина в течение 10 дней.
При ладонно-подошвенных бородавках (из 6 больных четверо ранее получали лазеротерапиию – 1, криодеструкцию – 1, ферезол – 2) криодеструкция элементов производилась на 5-й день на фоне приема Изопринозина в течение 10 дней, затем после 8-дневного интервала проводили еще один 10-дневный курс лечения (очаги после обработки смазывали гелем панавир).
При остроконечных кондиломах проводили криодеструкцию на фоне приема изопринозина: три 5-дневных цикла с интервалами в месяц.
Продолжительность общего наблюдения за больными составила 9 месяцев.
Результаты
У пациентов с обыкновенными и плоскими бородавками рецидивов после проеденного лечения не возникало (эффективность – 100 %); из 6 пациентов с ладонно-подошвенными бородавками рецидив возник у 1 больного (эффективность – 83,4 %), ему был проведен дополнительный курс (криодеструкция + Изопринозин), после чего возникло клиническое излечение.
Среди пациентов с остроконечными кондиломами 3 человека после проведенного курса лечения на контрольное обследование не явились, а из оставшихся 63 больных полное клиническое излечение было достигнуто в 59 случаях (эффективность – 93,6 %). Рецидивы зарегистрированы у двух женщин на фоне наступившей беременности и у двух больных, признавших случайные незащищенные половые связи после лечения. В результате дополнительно проведенного курса комплексного лечения у них было достигнуто клиническое выздоровление.
Общая эффективность лечения во всей группе наблюдавшихся больных, полностью закончивших исследование (75 человек), составила 93,3 %.
Переносимость лечения в целом была хорошей: из общего числа больных 1 (1,3 %) пациент предъявил жалобы на тошноту, а 2 (2,7 %) – на вялость и сонливость. Отмены Изопринозина не потребовалось ни в одном из случаев. Изменений со стороны рутинных анализов крови, мочи, уровней мочевой кислоты, трансаминаз и креатинина также обнаружено не было.
Выводы
- Включение Изопринозина в комплексное лечение больных с обыкновенными, ладонно-подошвенными, плоскими бородавками и остроконечными кондиломами обеспечило выздоровление подавляющего большинства пациентов (93,3 %).
- Лечение Изопринозином хорошо переносится, редкие нежелательные явления (у 4 % больных) не требуют отмены препарата.
- Терапия Изопринозином в сочетании с деструктивными методами лечения может быть рекомендована при заболеваниях, вызванных ВПЧ, в первую очередь пациентам с остроконечными кондиломами.
Информация об авторах:
Родин Алексей Юрьевич – доктор медицинских наук, профессор, заведующий кафедрой дерматовенерологии
Волгоградского Государственного медицинского университета.
Тел. 36-13-88, E-mail: 2008@rambler.ru;
Заклякова Татьяна Николаевна – заместитель главного врача Краснооктябрьского кожвендиспансера Волгограда
1. Вульф К., Джонсон Р., Сюрмонд Д. Дерматология по Томасу Фицпатрику. Атлассправочник. Москва. 2007. С. 1248.
2. Ludicke E, Stalberg A, Vassilokos P, et al. High and intermediate risk human papfflomavirus infectionin sexually active adolescent females. J Pediatr Adolesc Gynecol 2001; 14(4):171–74.
3. Европейские стандарты диагностики и лечения заболеваний, передающихся половым путем. М., 2004. С. 274.
4. Краснов В., Кулова А., Кулова Е. и др. Реабилитация в закрытых детских учреждениях часто болеющих детей с маркерами активности герпетической инфекции // Врач. 2007. № 12. С. 68–70.
5. Роговская С.И., Прилепская В.Н. Оптимизация лечения хронических цервицитов с помощью изопринозина // Гинекология. 2006. Т. 8. № 1. С. 2–4.
6. Bigrigg MF, Colding BW, Pearson P, et al. Colposcopic diagnosis and treatment of cervical dysplasia at a single clinic visit. Lancet 1990;396:229–32.
7. Singer A, Monaghan JM. Lower genital tract precancer. Colposcopy, Pathology, Treatment. Blackwell Science. Inc. 1994.
8. Баррассо Р. Кольпоскопическая диагностика патологии шейки матки // ЗППП. 1995. № 5. С. 11–17.
9. Дубенский В.В. Интерфероны в комплексном лечении остроконечных кондилом // ЗППП. 1996. № 10. С. 28–9.