Дата публикации 16 октября 2017Обновлено 14 февраля 2022
Определение болезни. Причины заболевания
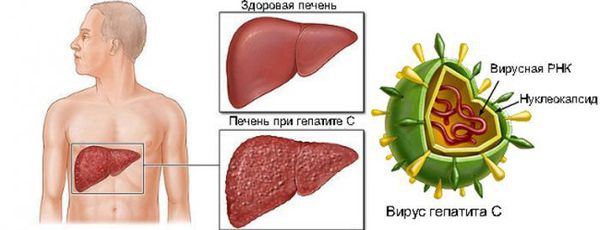
Вирусный гепатит С — острое или хроническое инфекционное заболевание, вызываемое различными типами вируса гепатита С, которые поражают в основном гепатоциты (клетки печени) и вызывают развитие воспалительного процесса в печени. При сочетании ряда факторов, образа жизни и отсутствии адекватного лечения вирусы гепатита С приводят к цирротической перестройке ткани и раку печени (гепатоцеллюлярной карциноме).
Краткое содержание статьи — в видео:
Этиологический агент — вирус гепатита С (ВГС). Вирус был впервые выделен американскими учёными в 1989 году.
Таксономическая структура:
- царство — вирусы
- семейство — Flaviviridae
- род — Hepacivirus
- вид — вирус гепатита С (hepatitis C virus, HCV) — 7 генотипов и 67 подтипов
Этиологические и морфологические свойства вируса
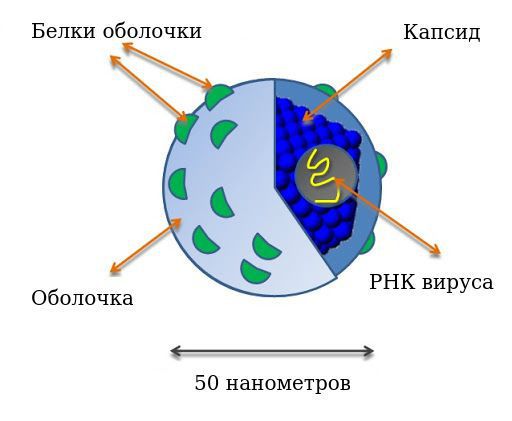
Диаметр вириона (вирусной частицы) — 50 нанометров. Имеет внешнюю белково-липидную оболочку. Оболочка вирусной частицы образуется в том числе за счёт взаимодействия вируса с липопротеидами низкой плотности хозяина, что позволяет ему ускользать из под иммунной атаки и проникать в клетки.
Генетическая структура представляет собой линейную однонитевую молекулу рибонуклеиновой кислоты (РНК), её размер примерно 9400 нуклеотидов. В ней выделяют следующие зоны: шифрующие структурные (Е1 и Е2 белки) и неструктурные (функциональные) белки — NS2, NS3, NS4A, NS4B, NS5A, NS5B, отвечающие за различные функции в жизни вируса. Структурные белки определяют прямой цитопатический эффект (повреждение клеток), полиморфизм (многообразие) вируса, участвуют в эффекте проникновения и выхода из клетки. Неструктурные белки участвуют в процессе развития и размножения вируса, определяют развитие резистентности (устойчивости) к интерферонам (NS5A). Встраивания вирусной РНК в геном клеток человека не замечено.
Вирус неоднороден (есть его различные подвиды — генотипы). Это обусловлено тем, что скорость его репликации огромна (за сутки 1011-1012) и в результате возникает большое число ошибок — вирус быстро мутирует. Такие мутации позволяют вирусу ускользать от иммунного ответа человека и длительно находиться в организме, а также сопротивляться воздействию лекарственных препаратов. Основной резервуар вируса — это клетки печени, однако он способен размножаться и в клетках иммунной системы (макрофагах, моноцитах и др.).
В целом вирус малоустойчив в окружающей среде. Под воздействием хлороформа, спирта, хлоргексидина и других дезинфицирующих средств погибает практически мгновенно, инактивируется при температуре 100 °С за 2 минуты, при температуре 60 °С за 30 минут. При комнатной температуре живёт не более четырёх суток, под действием ультрафиолета погибает за 30 минут. В плазме, эритроцитарной массе и др. может сохраняться до года. На культурах клеток не культивируется, не имеет гемагглютинирующей (склеивающей эритроциты) и гемолитической (разрушающей эритроциты) активности [2][8][10][11].
Передача вируса гепатита С
Передача вируса осуществляется только через кровь. Инфицирующая доза в несколько десятков раз больше, чем при гепатите В, т. е. для заражения нужны видимые следы крови. А вот пути заражения бывают различны:
- употребление наркотиков;
- медицинские манипуляции (в том числе пирсинг, тату и др.);
- половой путь (незащищённый половой контакт, в среднем около 1,5 % в гетеросексуальной семье);
- от матери к ребёнку в родах;
- бытовой путь (использование общих бритв, ножниц, зубных щёток).
При поцелуях, рукопожатиях, через посуду, сухие пятна крови на одежде, через воду, при кашле, чихании, потении, сидении рядом, по воздуху и т. д. гепатит С не передаётся. Заразиться через грудное молоко также нельзя, но заражение возможно при попадании крови матери на повреждённые губы ребёнка. Есть незначительный риск при попадании инфицированной крови в глаза, однако это единичные случаи. Заразиться при переливании крови практически невозможно, т. к. кровь на гепатит С тестируют методом ПЦР (полимеразной цепной реакции) с высокой чувствительностью.
Нет никаких научных оснований ограничивать выбор профессии, работы и круг общения людей с гепатитом С — передача осуществляется только через кровь, поэтому ограничений в работе (например учителем, врачом, няней), контактах с родственниками и т. п. быть не должно.
Территориальное распределение
Гепатит С распространен во всем мире. Наиболее часто он встречается в Регионе ВОЗ Восточного Средиземноморья и Европейском регионе ВОЗ, где в 2015 г. распространенность HCV, по оценкам, составила соответственно 2,3% и 1,5%. Общее количество больных вирусным гепатитом С в мире не менее 150 млн, в Российской Федерации — неизвестно (по некоторым данным ориентировочное количество больных — не менее 2 млн человек). По состоянию на 2016 год в США было заражено не менее 2,4 млн человек (по другим данным — не менее 4 млн). По самым скромным подсчётам в этой стране в 2018 году от гепатита С умерли не менее 15 тыс. человек. В РФ превалирующее распространение имеют генотипы 1b и За, но частота их выявления может значительно колебаться в зависимости от региона [4][7][9].
В настоящее время вирусный гепатит С распространяется в общей популяции, т. е. заболеванию подвержены люди всех возрастов и социальных слоёв, однако наибольший риск имеют следующие категории:
- потребители инъекционных наркотиков;
- ВИЧ-инфицированные;
- пациенты отделений гемодиализа;
- лица, подвергшиеся трансплантации органов (в настоящее время менее значимо);
- медработники;
- дети, рождённые от матерей с гепатитом С;
- маргинальные слои общества, работники секс-индустрии.
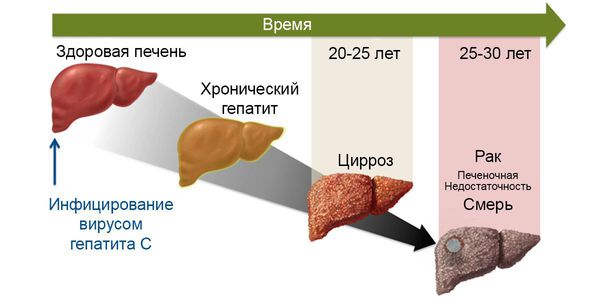
После перенесённого острого вирусного гепатита С примерно 30 % людей самоизлечиваются, т. е. полностью избавляются от вируса, в остальных случаях формируется хронический гепатит. Предикторы (прогностические параметры) самоизлечения — желтуха, высокий уровень АЛТ, молодой возраст, женский пол, 1 генотип вируса, наличие гепатита В с HbsAg (антигеном вируса гепатита В). У каждого 5-25 человека из 100 в течение 10-20 лет от момента инфицирования при хронизации развивается цирроз печени и у них имеется 1-4 % годовой вероятности развития рака печени.
Провоцирующие факторы развития цирроза печени:
- мужской пол;
- возраст более 50 лет;
- злоупотребление алкоголем;
- коинфекция ВИЧ, гепатита В или стеатогепатита;
- иммуносупрессивная терапия.
Гепатитом С можно заразиться после выздоровления от предыдущего случая (даже тем же генотипом), можно заразиться другим генотипом, даже если человек уже имеет гепатит С какого-либо генотипа (суперинфекция). В этом случае наблюдается борьба между генотипами за доминирование. Побеждает, как правило, какой-то один, а другой может сохраняться на минимальных степенях репликации. При этом существует риск ошибки при определении генотипа.
Иммуногенность вируса слабая, т. е. антитела, которые должны вырабатываться в ответ на заражение, появляются медленно (не ранее чем через 3 недели от заражения) и не обладают явным вируснейтрализующим действием [2][4][8][9].
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы гепатита С
Скрытый (инкубационный) период гепатита С может составлять от 2 недель до 6 месяцев. В это время может не быть никаких признаков заражения и развивающегося заболевания. Однако коварство гепатита С в том, что даже по прошествии этого времени может не возникнуть никаких явных симптомов и проявлений (большинство больных вообще не имеет симптомов или их нельзя связать с гепатитом). Даже если симптомы и возникают, то зачастую они настолько незначительны, что человек абсолютно не придаёт им значения и не обращается за медицинской помощью до развития осложнений. Чаще всего информация о болезни появляется после прохождения рутинных исследований для операции или донорства крови.
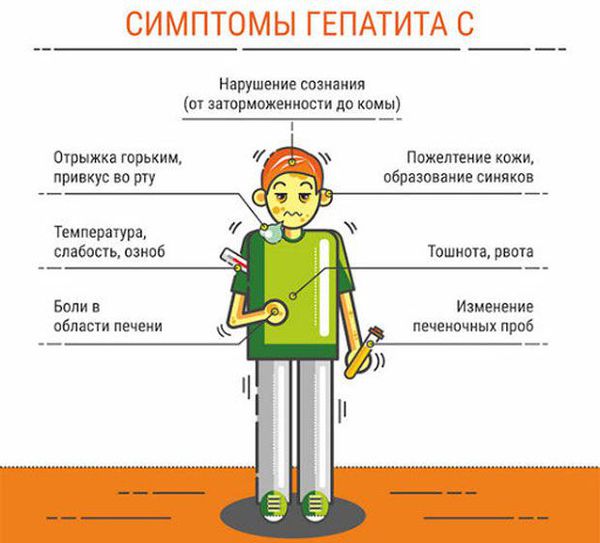
Симптомы вирусного гепатита С в остром и хроническом периоде:
- снижение или отсутствие аппетита;
- общая слабость, ухудшение самочувствия, повышенная утомляемость, депрессия (один из основных симптомов);
- тошнота;
- тяжесть и дискомфорт в правом подреберье;
- боли в животе, небольшое расстройство пищеварения;
- боли в суставах;
- в редких случаях — пожелтение склер глаз, кожи, потемнение мочи или осветление кала.
Повышение температуры отмечается редко. Возможен различный характер течения хронического заболевания, в большинстве случаев на протяжении десятков лет больной испытывает незначительную усталость, периодический дискомфорт в правом подреберье, иногда связанный с погрешностями в диете. Примечательно, что чёткого продолжительного периода ухудшения самочувствия обычно нет. Лишь на завершающей стадии заболевания (через несколько десятков лет) человек испытывает резкое ухудшение самочувствия, нарастание отёков, в том числе у него наблюдается накопление жидкости в брюшной полости (асцит), повышенная кровоточивость, похудание, желтуха. Зачастую толчком к этому служит принятие алкоголя на праздники в значительных дозах. В этом коварство вирусного гепатита С — мнимый период благополучия даже при высокоактивном инфекционном процессе («ласковый убийца», как длительное время его называли).
Гепатит С у беременных
Каких-либо значимых различий в течении вирусного гепатита С при беременности нет, как правило, происходит даже минимизация клинических и лабораторных изменений. Риск заражения ребёнка имеется лишь в родах, причём чем выше количество вируса в мл крови (вирусная нагрузка), тем выше риск. Выбор способа родоразрешения может влиять на риск передачи вируса при высокой вирусной нагрузке (свыше 8 х 10^5 МЕ/мл): при естественных родах риск до 8 %, при плановом кесаревом сечении — до 1 % (некоторые исследователи не подтверждают это). При коинфекции ВИЧ у матери риск передачи значительно возрастает — до 15 %.
Гепатит С у детей
После рождения от матерей с гепатитом С у 100 % детей выявляются материнские антитела к вирусу до 18 месяцев в максимальном исчислении (это нормально). Если заражения не произошло, в течение этого срока антитела исчезают и у ребёнка больше не будет никаких следов контакта. Если происходит заражение, то уже через 1-2 месяца в крови будет выявляться вирусная РНК в ПЦР исследовании (требует повторения даже при первичном отрицательном результате). Как правило, течение гепатита у детей малоактивное и не приводит к выраженным изменениям печени и самочувствия до момента возможного современного лечения и выражается только периодическим повышением АЛТ/АСТ [2][3][8][9].
Патогенез гепатита С
Проникая в организм, вирус гепатита С не оставляет никаких следов в месте внедрения. С током крови он быстро попадает в клетки печени, где оказывает неярко выраженное прямое разрушающее действие на клетки-мишени и в большей степени вызывает иммуноопосредованное поражение клеток на фоне репликации вируса. При использовании одного из исследований — ультрачувствительного ПЦР (полимеразной цепной реакции) — РНК вируса в крови может обнаруживаться уже через 2 недели от момента заражения. Значений, которые выявляются всеми тест-системами, как правило, вирусная нагрузка достигает через 1,5 месяца после заражения.
Нарушается баланс продукции цитокинов (белков, которые оказывают комплексное регулирующее влияние на воспаление и иммунитет):
- усиливается выработка интерлейкинов IL-4 и IL-10 (сигнальных веществ, которые вырабатываются клетками иммунной системы и служат для регуляции активности других клеток);
- снижается образование интерферонов IL-2 (белков с противовирусной и иммуномодулирующей активностью);
- подавляется активация СD4+ лимфоцитов (клеток, которые отражают работу иммунной системы).
Возможность нахождения и размножения вируса в клетках иммунной и нервной систем делает его недоступным для иммунного контроля. Главенствующая частота перехода вирусного гепатита С в хроническую форму (около 70 %) обусловлена не только различными особенностями самого вируса, но и обязательным участием (или вернее неадекватным участием) иммунной системы:
- наличием внепечёночного размножения вируса (главным образом в моноцитарной системе);
- наличием множества генотипов с подтипами и частыми мутациями (перестановками составляющих генома вируса);
- запуском иммунопатологических реакций, которые участвуют и во внепечёночных поражениях при гепатите С, в том числе в клетках эндотелия сосудов головного мозга;
- низкой иммуногенностью вируса;
- участием в патогенезе процессов перекисного окисления липидов.
После заражения и малосимптомного протекания острой фазы заболевания при отсутствии самоизлечения (около 30 %) наступает хронизация инфекции — длительный латентный период (до 10-30 лет, иногда более длительно). В течение этого периода человек ведёт обычный образ жизни, не испытывает никаких явных признаков заболевания, а появляющееся чувство усталости вполне логично списывает на интенсивный современный ритм жизни.
Длительность латентного периода зависит от свойств вируса, его реактивности, развития иммунопатологических реакций иммунной системы, образа жизни человека и других факторов. Однако рано или поздно наступает переломный момент в системе взаимодействия патогенного микроорганизма и восприимчивого человеческого макроорганизма. Несмотря на широкие регенераторные возможности печени происходит нарушение её восстановительных сил. Вследствие постоянного некупируемого воспалительного процесса активная функциональная ткань печени замещается жировой и далее соединительной тканью (рубцовой). При этом нарушается нормальное функционирование органа и по механизму обратной связи происходит прогрессирующее ухудшение работы печени и жизнедеятельности организма в целом [2][4][10][11].
Классификация и стадии развития гепатита С
Острый вирусный гепатит С
Периоды:
- Инкубационный период — от 3 недель до 4-6 месяцев. Полное отсутствие симптоматики.
- Преджелтушный (продромальный) период — от 4 суток до 3 недель. Симптомы малозаметны, может быть депрессивное настроение, слабость, дискомфорт в животе, неустойчивый стул.
- Период паренхиматозного гепатита (желтушный) — от 1 до 3 недель. Бывает редко, чаще отмечается незначительное желтушное окрашивание склер в совокупности с предыдущими признаками.
- Период выздоровления (реконвалесценции) или переход в малоактивное хроническое течение — от 3 до 6 месяцев.
По (МКБ-10): B17.1 Острый гепатит С.
По клинической форме:
- Манифестная:
- желтушная (типичная);
- безжелтушная.
- Бессимптомная:
- субклиническая (симптомы выражены очень слабо);
- инаппарантная (симптомов нет, возможны лишь лабораторные изменения).
По степени тяжести:
- Лёгкая — незначительная интоксикация до 5 дней, отсутствие или незначительная желтушность до 7 дней, отсутствие лихорадки, нормальные или незначительно увеличенные размеры печени, общий билирубин до 85-100 мкмоль/л, протромбиновый индекс (ПТИ) до 80 %, АЛТ до 500 ед/л.
- Средней тяжести — умеренная интоксикация до 7 дней, умеренная желтушность до 10 дней, субфебрилитет (повышение температуры тела в пределах от 37,1 до 38,0 °С) в начальном периоде до 5 дней, увеличение печени до 4 см, общий билирубин 100-170 мкмоль/л, ПТИ 80-60 %, АЛТ до 1000 ед/л.
- Тяжёлая — резко выраженная интоксикация 15 и более дней, интенсивная желтушность кожи 3 недели и более, фебрильная температура весь начальный и период разгара болезни, тахикардия, увеличение печени на 6 см и резкое её уменьшение в размерах на фоне прогресса болезни, общий билирубин от 170 мкмоль/л, ПТИ менее 60 %, АЛТ более 1000 ед/л.
По длительности течения:
- острый гепатит С (циклический — до 3 месяцев, острый затяжной — 3-6 месяцев);
- хронический гепатит С — продолжительностью более 6 месяцев.
Классификации хронических форм не разработаны, могут применяться различные составляющие на основании выраженности цитолитического синдрома, уровня повышения печёночных ферментов, морфологических изменений печени, наличию осложнений и др. [2][10][11].
Осложнения гепатита С
В остром периоде гепатита С возможно развитие «печёночной комы» — резкого выраженного угнетения функции печени вследствие массивной гибели печёночных клеток и накопления в организме токсичных продуктов обмена различных веществ. Это состояние характеризуется заторможенностью, потерей сознания, нарушением витальных (жизненно важных) функций. Однако встречаемость данного осложнения крайне низкая.
В хронической фазе болезни (или, по мнению части исследователей, конечной фазе заболевания) наиболее частым осложнением является развитие цирроза печени — замещения функционального долькового строения печёночной ткани грубым соединительнотканным образованием, что приводит к неадекватному функционированию органа. Определённое время печень способна выполнять функцию даже на стадии цирроза, но со временем при воздействии вируса наступает декомпенсация работы. Это состояние характеризуется нарушением кровотока в печени, повышением давления в системе воротной вены, расширением вен пищевода и желудка, увеличением селезёночной вены. Прогрессивно снижается уровень выработки белков, факторов свёртывания крови, фильтрационная способность. Появляются отёки, асцит (скопление жидкости в брюшной полости), кровотечения различной интенсивности, ухудшается общее состояние, интеллектуально-мнестические характеристики. В конечном итоге возможен летальный исход из-за массивного кровотечения и полиорганной недостаточности.
Не менее значимое осложнение хронической фазы гепатита С — развитие гепатоцеллюлярной карциномы (опухолевое перерождение). Согласно основной гипотезе, злокачественное перерождение возникает в результате повышенного распада клеток печени и последующего их восстановления, что приводит к повышенному числу мутаций. На ранних стадиях принципиальных отличий от течения хронического гепатита нет, в запущенных случаях возникает стремительное ухудшение состояния, нарастание асцита, желтухи, неспецифических желудочно-кишечных симптомов, потери веса, анорексии.
У 10-15 % больных с хроническим вирусным гепатитом С возможно развитие аутоиммунных заболеваний, наиболее частыми из которых являются аутоиммунный гепатит (АИГ) и криоглобулинемия. АИГ — это иммуноопосредованное поражение печени. Внешне оно мало отличается от проявлений гепатитов другой этиологии, но зачастую имеет более агрессивное течение и поддаётся терапии только длительными курсами иммуносупрессивных препаратов. Криоглобулинемия — накопление в малых и средних кровеносных сосудах специфических белков, которые вызывают затруднение в них тока крови и приводят к специфическим проявлениям.
Также определена связь гепатита С с развитием сахарного диабета, неходжкинской лимфомы и кожной порфирии Тарда [2][8][9][10].
Диагностика гепатита С
Вариантов первичного выявления вируса и заболевания множество, однако чаще всего гепатит С выявляется в ходе планового обследования при сопутствующем заболевании (операции или госпитализации). Как правило, обнаруживают повышенный уровень АЛТ или антитела к гепатиту С (HCVAb). Это служит поводом для направления такого пациента к врачу-инфекционисту для углублённого обследования.
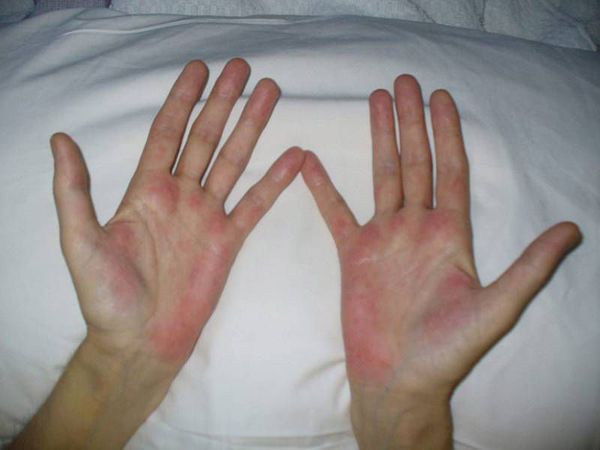
На приёме врач-инфекционист (гепатолог) осматривает пациента, в части случаев (в различных сочетаниях) выявляет характерное изменение цвета ладоней (печёночные ладони), увеличение размеров печени. В продвинутых случаях заболевания врач отмечает расширение вен области передней брюшной стенки («голова медузы»), отёчность (в том числе асцит как причина увеличения размеров живота), сосудистые звездочки и др.
Прохождение тестирования на гепатит С
При лабораторном обследовании в первую очередь должно быть назначено исследование на АЛТ, РНК вируса методом ПЦР качественно с чувствительностью 15-60 МЕ и антитела к вирусу гепатита С суммарные. При отрицательном результате ПЦР и положительном анализе на антитела диагноз гепатита С не подтверждается. Согласно действующему в РФ законодательству, такой человек должен быть поставлен на учёт к инфекционисту на срок 2 года с обязательным обследованием методом ПЦР раз в 6 месяцев. При отрицательном результате наблюдение прекращается с диагнозом паст-инфекция гепатита С (выздоровление). При положительном результате ПЦР происходит подтверждение диагноза — острый или хронический вирусный гепатит С — и назначается дополнительное обследование в целях уточнения текущего состояния. Необходимо помнить, что выявление суммарных антител в иммуноферментном анализе (ИФА) говорит лишь о прошлой встрече с инфекцией и не даёт практически никакой информации о наличии заболевания в текущий момент. Антитела могут сохраняться пожизненно.
Обязательно должны быть назначены следующие исследования:
- Развернутый клинический анализ крови + СОЭ (скорость оседания эритроцитов). Для гепатита С характерны: лейкопения (снижение количества лейкоцитов), лимфо- и моноцитоз (увеличение числа лимфоцитов и моноцитов), уменьшение СОЭ, тромбоцитопения (снижение количества тромбоцитов);
- Биохимический анализ крови:
- аланинаминотрансферраза (АЛТ) — возможен нормальный уровень или периодическое повышение;
- аспартатаминотрансферраза (АСТ) — норма или повышение;
- гамма-глутамилтранспептидаза (ГГТ) — норма или повышение;
- щелочная фосфатаза (ЩФ) — повышение при ухудшении процесса;
- общий билирубин — норма или повышение;
- общий белок — снижение при нарушении функции печени;
- протеинограмма — повышение гамма-глобулинов;
- протромбиновый индекс (ПТИ) — снижение при прогрессировании процесса;
- креатинин, амилаза, сахар.
- Онкомаркеры. Альфафетопротеин — повышение при прогрессировании процесса и развитии рака печени.
- Общий анализ мочи — появление уробилина, белка.
- УЗИ органов брюшной полости — возможно увеличение размеров печени и селезёнки, изменение структуры печени, размера внутренних сосудов.
- ФГДС — исследование пищевода, желудка и двенадцатиперстной кишки. Выявляется расширение вен пищевода при развитии портальной гипертензии — осложнение цирроза печени.
- Фиброскан — метод оценки фиброза печени, который позволяет определить тяжесть заболевания без биопсии (F0 – отсутствие фиброза, F4 — цирроз).
- ПЦР на гепатите С — качественный и при необходимости количественный тест.
- Генотипирование — определение генотипа вируса гепатита С.
- Мутации лекарственной резистентности NS3, NS5A и NS5B регионов генома вируса гепатита С (при неудаче в лечении препаратами прямого действия или высоком риске такой неудачи до лечения).
- Анализы на маркеры сопутствующих вирусных гепатитов (HbsAg, HbcorAb total, anti-Hbs).
- Анализ на ВИЧ.
При необходимости список исследований может расширяться. Стоит подчеркнуть, что грамотное назначение обследования и его интерпретация возможны исключительно врачом-инфекционистом (гепатологом). Врач назначит лишь необходимое, тем самым поможет пациенту сэкономить деньги, даст грамотную оценку полученных данных, что чрезвычайно важно в планировании дальнейшего лечения и его исхода [2][5][6][9][12].
Дифференциальная диагностика
- Вирусные и невирусные гепатиты другой этиологии. Связаны с путешествиями, любыми повреждениями кожи и слизистых, употреблением заражённых пищи и воды. Отличаются выраженностью симптоматики. Для уточнения диагноза проводятся специфические серологические тесты ИФА и ПЦР.
- Токсическое поражение печени. Связано с недавним значительным употреблением алкоголя или токсинов. Проводятся специфические серологические тесты ИФА и ПЦР, выявляется чрезмерное повышение ГГТ (фермент, маркер поражения печени).
- Паразитарные заболевания печени (например описторхоз, эхинококкоз). Связаны с проживанием в эндемичном регионе, употреблением плохо приготовленной рыбы, контактом с собаками. Характеризуются выраженной эозинофилией (увеличением уровня эозинофилов) периферической крови. Проводятся специфические серологические тесты, выявление яиц паразитов, инструментальные исследования.
- Первичный или метастатический рак печени. Изучаются данные анамнеза о сопутствующих заболеваниях, учитываются результаты инструментальной и лабораторной диагностики [2][4][10][11].
Надо ли проверяться на гепатит С здоровому человеку
Регулярное обследование на гепатит С при отсутствии симптомов следует проводить медработникам, пациентам отделений гемодиализа, частым посетителям стоматолога, больным хроническими заболеваниями с частыми парентеральными вмешательствами (внутривенно, подкожно и внутримышечно) и лицам, часто меняющим половых партнёров.
Лечение гепатита С
Основу любого лечебного воздействия составляет правильно подобранная диета. В отношении вируса гепатита С этот метод как никогда актуален, однако он зачастую игнорируется как пациентами, так и самими врачами.
Диета при гепатите С
Самое главное условие — полный отказ от алкоголя. Ничто так не вредит печени, как алкоголь. Именно он может стать тем фактором, который запускает цепь патологических реакций и переводит гепатит из вялотекущего процесса в высокоактивный, ускоряя наступление цирротической стадии гепатита. В отношении других продуктов питания и напитков следует соблюдать золотую середину: питание должно быть разнообразным, всего должно быть в меру, без злоупотреблений «тяжёлой» пищей (ограничение жирного, жареного, солёного, копчёного) с учётом отсутствия или наличия сопутствующих заболеваний.
Большое значение имеет поддержание разумной физической активности и контроль веса (индекс массы тела не должен превышать 25 кг/м2).
Какие врачи лечат гепатит С
Лечением гепатита С занимаются врачи-инфекционисты.
Медикаментозная терапия Гепатита С
Медикаментозное лечение гепатита С зависит от фазы развития заболевания, индивидуальных особенностей и возможностей организма. В остром периоде широко применяется инфузионная терапия (введение растворов) с привлечением различных дезинтоксикационных (очищение организма от вредных веществ) и питательных лечебных растворов.
Роль специфической противовирусной терапии острого гепатита С окончательно не решена и возможна лишь в индивидуальном порядке, например при угрозе хронизации или при фульминантном течении болезни (тяжёлом варианте воспалительно-некротического поражения печени). При невозможности радикального лечения гепатита С в хронической фазе вполне приемлема поддерживающая терапия так называемой группой гепатопротекторов (фосфолипиды, аминокислоты, антиоксиданты и др.). Данные средства не имеют чётко доказанной эффективности, однако широко применяются на практике и в некоторых случаях способны несколько задержать прогрессирование заболевания. Хороший эффект даёт нормализация функции ЖКТ и улучшение микрофлоры кишечника.
Попытки воздействия на вирус предпринимались с момента его открытия. Вначале это было изолированное применение препаратов интерферона короткого действия, затем комбинации интерферона короткого действия и рибавирина (препарата общевирусного действия). Их сменила комбинация интерферона пролонгированного действия и рибавирина.
К концу интерфероновой эпохи были достигнуты значительные успехи в процессе лечения и избавления человеческого организма от вируса гепатита С. Однако терапия была длительной, процент излечения достигал не более 70 % в среднем по генотипам, и курс лечения имел серьёзные побочные эффекты, иногда приводя к последствиям намного серьёзнее, чем сам гепатит С. Это обстоятельство дало толчок к разработке принципиально новых лекарственных средств, характеризующихся прямым противовирусным действием, сочетающих высокую эффективность (до 99 %), высокий профиль безопасности (минимальные побочные эффекты), простоту и удобство дозирования и небольшую длительность (2-3 месяца). В основу механизма действия легло подавление ключевых этапов размножения вируса, в первую очередь протеазы и полимеразы вируса гепатита С. Проведённые испытания препаратов показали высокие результаты, и, начиная с 2013 года, данная группа последних эффективных разработок с успехом применяется во всём мире. В некоторых странах одобрено лечение детей современными препаратами начиная с 3 лет (в зависимости от генотипа) с соответствующими взрослым показателями успеха.
Можно ли вылечить гепатит С полностью
В 2016 году Всемирная организация здравоохранения (ВОЗ) объявила гепатит С полностью излечимым заболеванием.
На 2020 год в мире доступны следующие виды и комбинации лекарственных препаратов прямого противовирусного действия для лечения гепатита С:
- Софосбувир.
- Даклатасвир.
- Элбасвир и Гразопревир.
- Глекапревир и Пибрентасвир.
- Ледипасвир и Софосбувир.
- Омбитасвир / Паритапревир / Ритонавир.
- Омбитасвир / Паритапревир / Питонавир / Дасабувир.
- Симепревир.
- Софосбувир и Велпатасвир.
- Софосбувир / Велпатасвир / Воксилапревир (комбинация не зарегистрирована в РФ).
Как лечить гепатит С в домашних условиях
Назначение противовирусной терапии должно осуществляться врачом, хорошо ориентирующимся в множестве применяемых для терапии гепатита С лекарств, после изучения всех составляющих процесса, возможных противопоказаний, взаимодействий с уже принимаемыми препаратами, особенностей диеты и образа жизни [1][5][8][9]. Гепатит С — тяжёлое инфекционное заболевание, которое может привести к циррозу и раку печени, поэтому самолечение опасно для жизни.
Схемы лечения гепатита С в России
В России на сегодняшний день для лечения гепатита С используется преимущественно устаревшее лечение интерферонами (чаще бесплатно или со скидкой), в редких случаях — препаратами прямого противовирусного действия (чаще платно со скидкой).
Прогноз. Профилактика
Если лечение гепатита начать до того, как разовьётся цирроз печени, то прогноз будет благоприятным: как правило, наступает полное излечение. При запущенных стадиях (цирроз и рак печени) прогноз зависит от множества факторов, обычно при начальном циррозе больные при должном лечении могут жить дальше без каких-либо серьёзных проблем со здоровьем, при декомпенсированном процессе прогноз неблагоприятный.
Прогноз при отсутствии лечения гепатита С
В среднем без лечения при отсутствии пагубных привычек и здоровом образе жизни в течение 20 лет примерно у 10-20 % больных разовьются цирроз и рак печени, при регулярном злоупотреблении алкоголем, наркотиками и токсинами (в том числе лекарствами) доля таких тяжёлых осложнений составит до 30-40%.
Из-за повышенной мутационной способности вируса существует ряд технических сложностей в создании вакцины — на данный момент её не существует (ведутся разработки). Поэтому меры профилактики распространения вируса гепатита С направлены на разрывы механизмов и путей передачи вируса, санитарное информирование и обучение населения.
Первичная профилактика
- Предупреждение возможности заражения в медицинских учреждениях:
- гигиена и обработка рук, инструментария, использование перчаток;
- тестирование донорской крови, плазмы и компонентов;
- тестирование донорских органов;
- надлежащее проведение медицинских инъекций;
- обучение медицинского персонала;
- обследование доноров, беременных, госпитализированных.
- Предупреждение полового пути заражения
- обучение правильному и своевременному использованию презервативов;
- тестирование перед вступлением в брак.
- Выдача стерильного инструментария потребителям инъекционных наркотиков (не во всех странах).
Вторичная профилактика
- Проведение противовирусной терапии (в идеале при выявлении заболевания, т. к. это предупреждает дальнейшее распространение инфекции).
- Матерям с гепатитом С (если он не был пролечен до беременности) следует внимательно следить за состоянием целостности кожи сосков и рта ребёнка, при наличии повреждений необходимо прекращать грудное вскармливание на время до их заживления [2][7][9][12].
Что делать, если член семьи болен гепатитом С
Самое важное, что следует сделать, чтобы предотвратить заражение вирусом — это избегать контакта с кровью инфицированного человека. Кровь может быть заразной, даже если она сухая. Надевайте перчатки, если вам нужно прикасаться к использованным бинтам. После контакта с кровью тщательно вымойте руки, даже если вы были в перчатках.
Некоторые предметы личной гигиены могут иногда содержать небольшое количество крови. Не следует совместно использовать зубную щётку, бритву или маникюрные ножницы.
Деятельность ВОЗ
В мае 2016 г. Всемирная ассамблея здравоохранения приняла первую «Глобальную стратегию сектора здравоохранения по вирусному гепатиту на 2016–2021 гг. Главной целью стратегии является снижение к 2030 г. числа новых случаев инфицирования вирусным гепатитом на 90 % и смертности от вирусного гепатита на 65 %. Для реализации этой стратегии ВОЗ занимается повышением осведомлённости о заболевании и его профилактике и расширяет охват услугами по скринингу, оказанию помощи и лечению гепатита С [13].
Хронический вирусный гепатит С у взрослых
Версия: Клинические рекомендации РФ 2021 (Россия)
Категории МКБ:
Хронический вирусный гепатит c (B18.2)
Разделы медицины:
Инфекционные и паразитарные болезни
Общая информация
Краткое описание
Разработчик клинической рекомендации
Некоммерческое партнерство «Национальное научное общество инфекционистов» (ННОИ)
Российское общество по изучению печени
Российская гастроэнтерологическая ассоциация
Клинические рекомендации
Хронический вирусный гепатит С у взрослых
Год утверждения (частота пересмотра): 2021
Возрастная категория: Взрослые
Определение заболевания или состояния (группы заболеваний или состояний)
Хронический вирусный гепатит С (ХВГС) – хроническое воспалительное заболевание в течение более 6 месяцев с преимущественным поражением ткани печени вследствие инфицирования вирусом гепатита С (ВГС или HСV – hepatitis С virus), которое может привести к тяжелым последствиям – циррозу (ЦП), раку печени (гепатоцеллюлярной карциноме, ГЦК) и летальному исходу [1].
Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
B18.2 – хронический вирусный гепатит С.
Применявшийся ранее код Z22.5 для носителей вирусного гепатита был исключен из последнего пересмотра МКБ 10.
Облачная МИС «МедЭлемент»
Облачная МИС «МедЭлемент»

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
Классификация
Классификация заболевания или состояния (группы заболеваний или состояний
Заболевание классифицируют в зависимости от ГТ ВГС, а также наличия ЦП и внепеченочных проявлений.
По стадиям:
0 – без фиброза;
1 – слабовыраженный фиброз;
2 – умеренный фиброз;
3 – выраженный фиброз;
4 – тяжелый фиброз.
По генотипу ВГС:
1 – генотип 1
— Генотип 1а
— Генотип 1b
2 – генотип 2 (в том числе 2k1b)
3 – генотип 3
4 – генотип 4
5 – генотип 5
6 – генотип 6
7 – генотип 7
8 – генотип 8
Этиология и патогенез
Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Возбудителем ХВГС является ВГС, который представляет собой небольшой гепатотропный РНК-вирус из семейства Flaviviridae. Вирус состоит из нуклеокапсида, состоящего из сердцевинного (ядерного) белка (HCVcAg) и одноцепочечной (+) РНК, и белково-липидной оболочки, содержащей аполипопротеин Е (апоЕ) человека и вирусные белки Е1 и Е2. Вирусный геном кодирует 10 различных белков, среди которых 3 описанных выше структурных и 7 неструктурных (p7, NS2, NS3, NS4A, NS4B, NS5A и NS5B) [2].
Выделяют 8 генотипов (ГТ) [3], которые обозначаются арабскими цифрами от 1 до 8, и несколько десятков субтипов ВГС, которые обозначаются латинскими буквами. Наибольшее клиническое значение имеют субтипы ГТ 1: а и b. Генотипы и субтипы различаются в последовательностях приблизительно на 30% и 20% соответственно. Вариабельность генома вируса обусловливает изменения в строении антигенных детерминант, которые определяют выработку специфических антител. Это препятствует элиминации вируса из организма и созданию эффективной вакцины против ВГС [4,5].
Инфицирование ВГС в большей доле случаев (55-85%) приводит к хроническому течению заболевания и примерно у четверти больных приводит в течение последующих десятилетий к развитию ЦП, что, в свою очередь, может служить основой для формирования ГЦК [6]. Довольно часто ввиду преимущественного бессимптомного течения инфекции заболевание впервые проявляется осложнениями ЦП.
Ведущим патогенетическим механизмом при ХВГС является нарушение взаимодействия иммунных клеток с инфицированными ВГС гепатоцитами. Повреждение печеночной ткани в большей степени является результатом реализации иммунного ответа в очаге воспаления, а не цитопатического действия вируса [7]. В печени накапливаются иммунокомпетентные клетки, часть из которых (NK-клетки, цитотоксические T-лимфоциты) обладают высокой цитотоксичностью и способностью повреждать гепатоциты [8]. В результате контакта инфицированных гепатоцитов с CTL-лимфоцитами (компонента адаптивного иммунного ответа) происходит запуск апоптоза. Отмечается дефицит Т-системы, депрессия макрофагов, ослабление системы интерфероногенеза, отсутствие специфического антителогенеза в отношении антигенов вирусов, что в конечном итоге нарушает адекватное распознавание и элиминацию иммунной системой антигенов вирусов на поверхности гепатоцитов [8-11].
У больных с выраженным Т-клеточным ответом происходит полная элиминация ВГС после перенесенного острого гепатита С. Вследствие взаимодействия вируса и иммунной системы происходит угнетение активности CTL-лимфоцитов белками вируса. В результате этого при ХВГС формируется иммунологическая толерантность к вирусу [12].
Действие вируса при ХВГС и вызванные им иммунологические реакции обусловливают не только повреждение печени, но и других органов и тканей. Концепция системных поражений при ХВГС заключается в возможности репликации вируса вне печени, а именно в тканях лимфоидного и нелимфоидного происхождения [13]. Размножение вируса в иммунокомпетентных клетках (лимфоцитах) приводит к нарушению их иммунологической функции. Сохранение ВГС в моноцитах является основной причиной реинфекции после трансплантации печени у больных тяжелыми формами ХВГС [10].
Среди факторов хозяина, влияющих на исход и течение ХВГС, имеет значение возраст на момент инфицирования, злоупотребление алкоголем, коинфицирование гепатотропными вирусами, нарушения липидного обмена и др. [14,15].
Эпидемиология
Эпидемиология заболевания или состояния (группы заболеваний или состояний)
По оценочным данным в мире у 1% населения (порядка 71 млн человек) выявляются антитела к ВГС (anti-HCV), среди которых 2/3 хронически инфицированы, и 1/3 выздоровели самостоятельно или вследствие излечения. Заболевание шире распространено в Африке и Азии (почти 3% населения), в то время как в Америке и Европе оно выявляется у 1,5-2,0% [17]. Достоверная распространённость ХВГС в РФ остаётся неизвестной, расчетное число пациентов может достигать 4,9 млн [16]. По данным Роспотребнадзора в субъектах РФ по состоянию на 01.01.2017 на диспансерном учёте состояло 591 830 пациентов с ХВГС [16].
В России самым распространенными являются ГТ 1 (52,6%, из них 3,7% приходятся на субтип 1а и 48,9% – на субтип 1b) и ГТ 3 (39,6%), гораздо реже встречается ГТ 2 (7,8%). Генотипы 4-6 встречаются менее чем в 0,01% случаев, ГТ 7 и 8 – крайне редко [16]. С появлением пангенотипных схем противовирусного лечения ХВГС клиническое значение ГТ ВГС постепенно утрачивается, однако остается еще ряд генотип-специфичных препаратов, перед применением которых необходимо уточнять ГТ ВГС.
Источником инфекции является больной человек. Наиболее значимым является парентеральный путь передачи (при употреблении внутривенных наркотических препаратов, медицинских манипуляциях, травмирующих косметических процедурах, включая маникюр и педикюр, нанесение татуировок и установку пирсинга), существенно реже – половой и вертикальный пути передачи [18].
Риск профессионального заражения медицинских работников при случайном уколе игрой, контаминированной инфицированной кровью, составляет около 1,8%. При попадании крови пациента на поврежденную кожу или неповрежденные слизистые медицинского работника риск инфицирования значительно меньше, а попадание ее на неповреждённую кожу безопасно. В связи с этим риск заражения для медицинского персонала мал. Риск инфицирования пациента от заражённого медицинского работника крайне мал [18]. Риск перинатальной передачи инфекции составляет 5-10% и мало зависит от способа родоразрешения, однако возрастает при наличии коинфекции ВИЧ у матери до 14-16% [18]. Низкая концентрация вируса в секретах половых желез и органах определяют низкий риск его передачи половым путем: около 0,5% в год при незащищенном половом контакте в моногамной гетеросексуальной паре, около 0,4-1,8% в год среди лиц, оказывающих сексуальные услуги [19], около 0,8% в год среди мужчин, практикующих секс с мужчинами с моноинфекцией ВГС (при коинфекции ВИЧ он выше в 4 раза) [20].
ВГС обладает сравнительно невысокой устойчивостью к воздействию факторов окружающей среды. Известно, что вирус устойчив к нагреванию до 500С, полная его инактивация наступает через 30 минут при температуре 600С и через 2 минуты при температуре 100С. Вирус чувствителен к ультрафиолетовому облучению и воздействию растворителей липидов [21].
Клиническая картина
Cимптомы, течение
Клиническая картина заболевания или состояния (группы заболеваний или состояний
У большинства пациентов заболевание протекает бессимптомно и выявляется при обследовании в рамках диспансеризации, догоспитальной подготовки, при посещении гастроэнтеролога по поводу диспепсических явлений (как правило, не связанных прямо с наличием ХВГС) и других специалистов (гинекологов, урологов, стоматологов и т.д.). От времени инфицирования до установления диагноза может пройти несколько лет. В ряде случаев первым проявлением заболевания являются В-клеточные лимфопролиферативные или иммунологически обусловленные внепеченочные заболевания (криоглобулинемический васкулит, в том числе с синдромом Рейно; интерстициальные заболевания легких; гломерулонефрит; синдром Шегрена; артрит и др.). У достаточного числа пациентов диагноз устанавливается только после манифестации осложнений ЦП: кровотечение из варикозно расширенных вен (ВРВ) пищевода и желудка и развития асцита [22,23].
При физикальном осмотре в отсутствии ЦП патологических проявлений, как правило, нет [22].
Активность трансаминаз может быть как повышенной, так и в пределах референсных значений. В некоторых случаях отмечается периодическое повышение активности АЛТ. В крови обнаруживаются anti-HCV и РНК ВГС. Активность АЛТ в пределах нормальных значений не свидетельствует об отсутствии изменений в печени, и пациенты не могут рассматриваться как «здоровые носители». Было показано, что 30-50% случаев у таких больных может быть диагностирован ЦП [24,25]. Часто в начальной стадии компенсированного ЦП отмечаются лишь похудание, астенизация, снижение работоспособности. При осмотре выявляют увеличение печени с ее уплотнением и спленомегалию. Однако у 20% больных в начальной стадии ЦП протекает бессимптомно, и его обнаруживают, как правило, случайно во время профилактического осмотра или обследования по поводу другого заболевания.
Цирроз печени развивается, как правило, в 25-35% случаев ХВГС. Вероятность его развития составляет 7,3% в год (5,1-9,5%). У многих пациентов ЦП в исходе ХВГС впервые диагностируется по данным гистологического исследования биоптата печени. Темпы декомпенсации ЦП составляют 5,5% в год. Вероятность развития в течение года синдрома портальной гипертензии у больных с компенсированным ЦП составляет 3,6%, печеночной энцефалопатии – 0,4%, ГЦК – 1,5% [24,26,27].
Диагностика
Диагностика заболевания или состояния (группы заболеваний или состояний, медицинские показания и противопоказания к применению методов диагностики
Диагноз ХВГС устанавливается на основании наличия антител к вирусу гепатита С (Определение суммарных антител классов M и G (anti-HCV IgG и anti-HCV IgM) к вирусу гепатита C (Hepatitis C virus) в крови, далее везде в тексте – anti-HCV) и РНК вируса гепатита С (Определение РНК вируса гепатита C (Hepatitis C virus) в крови методом ПЦР, качественное исследование, далее везде в тексте – РНК ВГС) или ядерного антигена ВГС (Определение Core-антигена вируса гепатита C (Hepatitis C virus) в крови, далее везде в тексте – HCVcAg) на протяжении более 6 месяцев [1].
Жалобы и анамнез
Специфических жалоб, характерных для ХВГС, нет. Заболевание, как правило, протекает бессимптомно, и довольно часто манифестирует осложнениями ЦП (асцит, кровотечение из ВРВ пищевода и желудка, печеночная энцефалопатия) [28]. В ряде случаев первыми проявлениями заболевания выступают иммунологически обусловленные внепеченочные проявления [23].
Физикальное обследование
При физикальном осмотре, как правило, никаких изменений не выявляется. Возможно наличие признаков ЦП (асцит, «печеночные ладони», ВРВ брюшной стенки, отеки, спленомегалия). При развитии иммунологически обусловленных внепеченочных проявлений имеют место соответствующие изменения [23].
Лабораторные диагностические исследования
Скрининг на наличие ХВГС основан на выявлении anti-HCV. Если обнаружены anti-HCV, следует обязательно провести анализ на РНК ВГС. В случае если анализ на РНК ВГС недоступен, допустимо провести тест на HCVcAg. Этот антиген в сыворотке или плазме крови также является маркером репликации ВГС. Анализ HCVcAg менее чувствителен, чем РНК ВГС (нижний предел обнаружения эквивалентен приблизительно 500-3000 МЕ/мл РНК ВГС, в зависимости от ГТ ВГС [28,29]). В редких случаях HCVcAg не обнаруживается при определяемой РНК ВГС [30].
- Рекомендуется обследование anti-HCV у лиц из группы повышенного риска для выявления потенциально инфицированных [1].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
Комментарии: отношение к группе повышенного риска устанавливается, как правило, на основании слов пациента (место работы, реципиент в анамнезе, введение инъекционных наркотиков, половые партнеры, семейный анамнез и т.д.).
К группе повышенного риска относятся:
— Беременные;
— Реципиенты крови и ее компонентов, органов и тканей;
— Персонал медицинских организаций;
— Пациенты центров и отделений гемодиализа, пересадки почки, сердечно-сосудистой и лёгочной хирургии, гематологии;
— Пациенты наркологических и кожно-венерологических кабинетов;
— Опекаемые и персонал учреждений с круглосуточным пребыванием детей или взрослых;
— Контактные лица в очагах острого и хронического гепатита С;
— Потребители инъекционных наркотиков и их половые партнеры;
— Лица, оказывающие услуги сексуального характера, и их половые партнеры;
— Мужчины, практикующие секс с мужчинами;
— Лица с большим количеством случайных половых партнеров;
— Лица, сделавшие татуаж;
— Лица, находящиеся в местах лишения свободы;
— Доноры крови (ее компонентов), органов и тканей, спермы;
— Пациенты с иммунодефицитом (пациенты с онкологическими заболеваниями, пациенты на гемодиализе, пациенты на лечении иммунодепрессантами и др.);
— Пациенты с заболеваниями печени неясной этиологии (в процессе первичного клинико-лабораторного обследования).
- Всем пациентам с выявленными anti-HCV рекомендуется провести анализ РНК ВГС или HCVcAg (в случае недоступности первого) для подтверждения наличия текущей инфекции [1].
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
- Всем пациентам с выявленными anti-HCV и отрицательной РНК ВГС (или HCVcAg) в случае недоступности первого) рекомендуется провести повторный анализ РНК ВГС через 12 и 24 недели, с тем чтобы подтвердить или опровергнуть наличие ХВГС [1].
Уровень убедительности рекомендации А (уровень достоверности доказательств – 5)
Комментарии: наличие anti-HCV в сочетании с РНК ВГС (или HCVcAg) характерно как для пациентов с ХВГС, так и пациентов с острым гепатитом С. Концентрация РНК ВГС (или HCVcAg) у больных с острым гепатитом С может значительно колебаться, вплоть до неопределяемого уровня. Таким образом, пациентам с неопределяемой РНК ВГС (или HCVcAg), необходимо повторно провести анализ РНК ВГС (или HCVcAg) через 12 и 24 недели после отрицательного результата, с тем чтобы убедиться в клиренсе ВГС (самостоятельное выздоровление от острого гепатита С) или подтвердить формирование ХВГС.
На этапе постановки диагноза:
- Определение генотипа вируса гепатита С (Определение генотипа вируса гепатита C (Hepatitis C virus), далее везде в тексте – ГТ ВГС) рекомендуется только пациентам с ХВГС для планирования генотип-специфичной схемы противовирусной терапии (ПВТ) [1].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 5)
Комментарии: ГТ ВГС имеет значение только при планировании генотип-специфичных противовирусных препаратов. При доступности пангенотипных препаратов это обследование не требуется.
- Всем пациентам с ХВГС с исходом в ЦП и/или признаками внепеченочных проявлений (лимфопролиферативные заболевания) рекомендуется проведение общего (клинического) анализа крови развернутого [23,36-38].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: течение ХВГС может влиять на клеточный состав крови, однако убедительных доказательств таких изменений в отсутствии ЦП и лимфопролиферативных заболеваний, индуцированных ВГС, нет. В случае формирования ЦП чаще всего наблюдается тромбоцитопения различной степени выраженности, реже другие варианты цитопений.
- Всем пациентам с ХВГС рекомендуется проведение анализа крови биохимического общетерапевтического для определения активности трансаминаз (аланинаминотрансфераза, аспартатаминотрансфераза), тяжести повреждения гепатоцитов, оценки функции печени и почек [39-41].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: в отсутствии признаков ЦП клиническое значение активности трансаминаз и других показателей функции печени (билирубин, альбумин) невелико. Оно приобретает большее значение, если имеет место сочетанная патология печени. У пациентов с ЦП в исходе ХВГС тяжесть поражения гепатоцитов и признаки декомпенсации имеют решающее значение в выборе тактики ведения пациента, препаратов ПВТ, прогнозе течения заболевания [39]. Кроме того, АЛТ и АСТ могут использоваться для самостоятельной оценки выраженности фиброза печени (например, индексы APRI, FIB-4) в отсутствии возможности выполнить инструментальное обследование [42] (см. Приложение Г). Оценка функции почек (креатинин) необходима при планировании схем ПВТ, содержащих софосбувир** [40,41].
- Всем пациентам с ХВГС с исходом в ЦП рекомендуется определение протромбинового (тромбопластинового) времени в крови или в плазме для оценки функции печени [46].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
- Рекомендуется исследование уровня альфа-фетопротеина (АФП) в сыворотке крови пациентам с ХВГС с выраженным и тяжелым фиброзом печени (F3-F4 по METAVIR) для своевременной диагностики ГЦК [44,45].
Уровень убедительности рекомендации А (уровень достоверности доказательств -1)
Комментарии: риск развития ГЦК на стадии ЦП составляет приблизительно 1-5% в год. Вероятность летального исхода в течение первого года после постановки диагноза у пациентов с ГЦК составляет 33%.
На этапе ПВТ:
- Лабораторный мониторинг не рекомендуется пациентам с ХВГС без ЦП во время ПВТ без применения рибавирина** [205,206].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2)
Комментарий: препараты современной ПВТ обладают высокой безопасностью и эффективностью, в связи с чем необходимости в лабораторном мониторинге во время ПВТ без применения рибавирина** нет.
- При применении РБВ** рекомендуется раз в 2-4 недели исследовать общий (клинический) анализ крови развернутый, с тем чтобы исключить вероятность частого побочного эффекта препарата – анемии [117].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
- Не рекомендуется определение РНК во время ПВТ для оценки ее эффективности [46-48] (см. Приложение Б).
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарий: закономерности между скоростью элиминации ВГС во время ПВТ и вероятностью УВО нет, в связи с чем необходимости в контроле РНК ВГС во время лечения нет [48].
На этапе диспансерного наблюдения:
- Не рекомендуется использовать анализ anti-HCV пациентам, выздоровевшим от ХВГС вследствие ПВТ, для контроля реинфицирования ВГС [49-51].
Уровень убедительности рекомендаций С (уровень достоверности доказательств –5)
Комментарий: после успешной ПВТ anti-HCV сохраняются длительно в подавляющем большинстве случаев, поэтому этот анализ не может использоваться для определения реинфицирования у пациентов с опытом элиминации ВГС. Доля пациентов, у которых anti-HCV постепенно исчезают, очень мала, и срок этого исчезновения неизвестен.
- Всем пациентам, получившим курс ПВТ ХВГС, рекомендуется определение РНК ВГС через 12 недель после окончания ПВТ для оценки ее эффективности (УВО12) [46-48] (см. Приложение Б).
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарий: отсутствие РНК ВГС через 12 недель после завершения ПВТ соответствует излечению от ХВГС, так как поздний рецидив возникает менее чем в 0,2% случаев [48].
- Рекомендуется определение уровня АФП пациентам с выраженным фиброзом печени (F3 по METAVIR) и с ЦП 1 раз в полгода для диагностики ГЦК [44,45].
Уровень убедительности рекомендаций А (уровень достоверности доказательств –1)
Комментарий: риск развития ГЦК на стадии ЦП составляет около 1-5% в год. Вероятность летального исхода в течение первого года после постановки диагноза у пациентов с ГЦК составляет 33%.
Инструментальные диагностические исследования
На этапе постановки диагноза:
- Всем пациентам с ХВГС рекомендуется выполнить УЗИ органов брюшной полости (комплексное) и забрюшинного пространства для выявления признаков ЦП и ГЦК [52,53].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2)
Комментарии: УЗИ органов брюшной полости и забрюшинного пространства проводится для диагностики ГЦК, признаков портальной гипертензии (увеличения селезенки, расширения вен портальной системы), асцита, исключения сопутствующей патологии желудочно-кишечного тракта, что в некоторых случаях может иметь решающее значение в определении стадии заболевания и тактики лечения. ЦП и ГЦК в исходе ХВГС могут протекать бессимптомно и выявляться только по данным УЗИ. При обнаружении в печени образования, подозрительного на ГЦК, следует продолжить исследования согласно клиническим рекомендациям по диагностике и лечению ГЦК.
- Всем пациентам с ХВГС рекомендуется выполнение неинвазивной диагностики фиброза, с тем чтобы определить тактику ПВТ и дальнейшее ведение пациента (в случае ЦП) [54-58].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: неинвазивная диагностика позволяет с высокой точностью определить стадию фиброза. Она может быть выполнена с помощью эластометрии печени (должна быть выполнена на валидизированном аппарате), либо с помощью сывороточных тестов. При недоступности эластометрии могут использоваться некоммерческие расчетные показатели, основанные на результатах лабораторного обследования (например, расчет индексов APRI, FIB-4, см. Приложения Г2, Г3).
- При получении противоречивых данных неинвазивной диагностики рекомендуется рассмотреть вопрос о проведении чрескожной биопсии печени, с тем чтобы определить тактику ПВТ и дальнейшее ведение пациента (в случае ЦП) [1].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Биопсия печени является инвазивной процедурой с риском развития осложнений, поэтому ее следует проводить только в случае, если не удается получить результат с помощью применения неинвазивных методов [1].
- Рекомендовано выполнение эзофагогастродуоденоскопии (ЭГДС) пациентам с ХВГС с исходом в ЦП для оценки наличия и степени ВРВ пищевода и желудка [59-61].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: Эндоскопический осмотр выполняется для диагностики степени ВРВ пищевода и желудка, а также при наложении клипс и лигатур при кровотечении или его профилактики из вен пищевода у пациентов с ЦП. Возможно проведение процедуры в условиях седации, что требует предварительной консультации и сопровождения анестезиолога.
- Компьютерная томография органов брюшной полости с внутривенным болюсным контрастированием или магнитно-резонансная томография органов брюшной полости с внутривенным контрастированием рекомендуется провести пациентам с ХВГС при обнаружении в печени образования по результатам УЗИ брюшной полости (комплексное) для уточнения его природы [62-65].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
На этапе диспансерного наблюдения:
- Рекомендуется выполнение неинвазивной диагностики стадии фиброза печени (эластометрия печени, при ее недоступности – сывороточные расчетные некоммерческие тесты APRI, FIB-4) пациентам с ХВГС 1 раз в год для динамического наблюдения [54,55,57,66].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
- Рекомендуется выполнение ЭГДС пациентам с ХВГС с исходом в ЦП для динамического наблюдения 1 раз в год [59-61,67].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
- После излечения от ХВГС пациентам с ЦП или выраженным фиброзом печени (F3 по METAVIR) рекомендуется пожизненно проводить скрининговое обследование для раннего выявления ГЦК (УЗИ брюшной полости комплексное каждые 6 месяцев) [53].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: у данных пациентов сохраняется риск развития ГЦК, несмотря на элиминацию вируса из организма, поэтому им рекомендовано проведение профилактического обследования для ее раннего выявления.
Лечение
Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
Цель лечения ХВГС – элиминация ВГС для профилактики осложнений ХВГС (включая ЦП, ГЦК, смерть), улучшение качества жизни и предотвращение дальнейшей передачи ВГС в популяции. Вирус гепатита С не образует высокостабильных внутриклеточных форм генетического материала, поэтому может быть элиминирован из организма полностью [1]. Показателем элиминации вируса из организма является стойкое достижение неопределяемого уровня РНК вируса в крови, которое оценивают через 12 недель после окончания терапии (УВО12) [29,30].
На выбор тактики лечения оказывают влияние следующие факторы [68]:
- стадия фиброза печени, наличие ЦП и его класс;
- ГТ ВГС;
- наличие некоторых сопутствующих заболеваний;
- опыт предыдущей ПВТ (если есть);
- прием лекарственных средств по поводу сопутствующей патологии.
1. Показания к началу противовирусной терапии
- Противовирусное лечение рекомендуется проводить всем пациентам с ХВГС, независимо от наличия ЦП, с целью излечения от инфекции (эрадикации ВГС) [1,69] (см. также Приложение А3).
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: лечение ХВГС показано всем больным, так как в настоящее время применяются высокоэффективные и безопасные препараты, которые позволяют добиться УВО в подавляющем большинстве случаев.
Для лечения ХВГС применяются противовирусные препараты прямого действия (ПППД). Те из них, которые входят в список ЖНЛВП, отмечаются знаком **. ПППД представляют собой ингибиторы различных неструктурных белков вируса. Второй корень названия ПППД указывает на то, какой конкретно белок он ингибирует: «-превир» – NS3/NS4A, «-асвир» – NS5А, «-бувир» – NS5B. Выбор препаратов для лечения и длительность лечения зависят от стадии фиброза, наличия и класса ЦП, ГТ вируса, опыта предшествующей терапии ХВГС, наличия сопутствующих заболеваний (в частности, хронической болезни почек (ХБП)), некоторых препаратов сопутствующей терапии. В зависимости от эффективности при различных ГТ выделяют пангенотипные схемы (эффективны при всех ГТ вируса) и генотип-специфические (эффективны только при определенных ГТ ВГС). В табл. 1 представлены лекарственные средства и их компоненты, применяющиеся в РФ.
Табл. 1. Компоненты, входящие в состав лекарственных средств прямого противовирусного действия, и лекарственные средства прямого противовирусного действия, одобренные для применения в РФ (представлены в алфавитном порядке).
Фиксированные комбинированные ПППД:
- Велпатасвир + софосбувир** (ВЕЛ+СОФ**)
- Глекапревир + пибрентасвир** (ГЛЕ+ПИБ**)
- Гразопревир + элбасвир** (ГРА+ЭЛБ**)
- Дасабувир; омбитасвир + паритапревир + ритонавирб** (ДСВ; ОБВ+ПТВ/р**)
- Ледипасвир + софосбувир (ЛЕД+СОФ)
а — входят в состав комбинированных препаратов;
б — ритонавир** (РТВ**) – фармакокинетический бустер, не обладает противовирусной активностью, используется с НРВ** и ПТВ для увеличения их концентрации в крови.
- Безотлагательно терапию рекомендуется рассмотреть в первую очередь у пациентов:
— с ХВГС с исходом в ЦП (включая декомпенсированный ЦП);
— с выраженным фиброзом (F3 по METAVIR);
— с клинически значимыми внепеченочными проявлениями;
— с рецидивом ХВГС после трансплантации печени;
— с риском быстрого развития заболевания печени по причине сопутствующих заболеваний (хронический вирусный гепатит В, ВИЧ-инфекция, сахарный диабет и
др., после трансплантации других органов кроме печени);
— с высоким риском передачи инфекции [1,69].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
- Перед применением ПППД рекомендуется проверить сочетаемость назначенной схемы с уже принимаемыми пациентом препаратами, используя любой специальный ресурс (например, https://www.hep-druginteractions.org). При выявлении значимого взаимодействия рекомендуется заменить схему или препарат, который пациент принимает при лечении сопутствующего заболевания. Если это невозможно, решение следует принимать в индивидуальном порядке, оценивая соотношение пользы и риска от данной комбинации и возможных последствий от ее применения [70].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: Большинство ПППД безопасно, но особенности их фармакокинетики могут приводить к значимому взаимодействию с другими препаратами, принимаемыми пациентом.
2. Лечение пациентов без цирроза печени и с компенсированным циррозом печени
Поскольку наличие опыта предшествующей терапии и ЦП существенно влияет на эффективность ПВТ, ее состав и длительность различается в зависимости от наличия этих факторов. В связи с этим пациентов с ХВГС принято разделять на несколько групп:
- Пациенты без опыта ПВТ и без ЦП;
- Пациенты без опыта ПВТ с компенсированным ЦП;
- Пациенты, не ответившие на предшествующую ПВТ (ПегИФН** + РБВ** ± СОФ** или СОФ** + РБВ**) без ЦП;
- Пациенты, не ответившие на предшествующую ПВТ (ПегИФН** + РБВ** ± СОФ** или СОФ** + РБВ**) с компенсированным ЦП.
Лечение пациентов с декомпенсированным ЦП рассматриваются отдельно в разделе «Трансплантация печени» и в Приложении А3.
Принципы перелечивания после неуспешного курса ПППД (ингибиторующими NS3/4А и/или ингибиторующими NS5A) рассматриваются в разделе Перелечивание.
- Лечение пациентов с ХВГС без ЦП, без опыта ПВТ и без трансплантации печени в анамнезе рекомендуется проводить по одной из альтернативных схем согласно табл. 2:
-Велпатасвир+Софосбувир** [76,79]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
-Глекапревир + Пибрентасвир** [85]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
-Даклатасвир** + Софосбувир** [105,107,208,218-220]
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 3)
-Гразопревир + Элбасвир** [93,207, 221-224]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
-Даклатасвир** + Нарлапревир** + Ритонавир** [109]
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
-Дасабувир; Омбитасвир + Паритапревир + Ритонавир** при генотипе 1b,
-Дасабувир; Омбитасвир + Паритапревир + Ритонавир** + Рибавирин** при генотипе 1а [98,99]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
-Ледипасвир + Софосбувир [90, 225]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
-Нарлапревир** + Софосбувир** + Ритонавир** [110,209]
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Табл. 2. Схемы ПВТ ХВГС для пациентов без предшествующего опыта ПВТ и без цирроза печени в зависимости от генотипа (лекарственные средства представлены в алфавитном порядке).
Примечания:
ВЕЛ+СОФ** – велпатасвир + софосбувир** (100/400 мг) 1 таб. 1р/д;
ГЛЕ+ПИБ** – глекапревир + пибрентасвир** (3 таб. одновременно, по 100/40 мг каждая) 1р/д;
ДАК** + СОФ** – даклатасвир** 60 мг 1 таб. 1р/д + софосбувир** 400 мг 1 таб. 1р/д;
ГРА+ЭЛБ** – гразопревир + элбасвир** 100/50 мг 1 таб. 1р/д;
ДАК** + НРВ**/р** – даклатасвир** 60 мг 1р/д + нарлапревир** 200 мг 1 р/д (2 таб. одновременно, по 100 мг каждая) + ритонавир** 100 мг 1р/д;
ДСВ; ОБВ+ПТВ/р** – дасабувир (1 таб. по 250 мг 2 р/д); омбитасвир + паритапревир + ритонавир** (2 таб. одновременно 1р/д, по 12,5/75/50 мг каждая);
ЛЕД+СОФ – ледипасвир + софосбувир 90/400 мг 1 таб. 1р/д;
НРВ**/р** + СОФ** – нарлапревир** 200 мг 1 р/д (2 таб. одновременно, по 100 мг каждая) + ритонавир** 100 мг 1р/д + софосбувир** 400 мг 1 таб. 1р/д;
а — при ВН не более 800 000 МЕ/мл срок лечения 12 недель; 16-недельный курс совместно с РБВ** следует рассмотреть при ВН ВГС >800 000 ME/мл и/или при наличии полиморфизмов NS5A;
б — у пациентов со слабовыраженным фиброзом (F0-2) 8 недель, с фиброзом F3-F4 по METAVIR – 12 недель.
в — у пациентов со слабовыраженным фиброзом (F0-2) и ВН менее 1 000 000 МЕ/мл можно рассмотреть длительность 8 недель по решению врачебной комиссии.
- Лечение пациентов с ХВГС с компенсированным ЦП без опыта ПВТ рекомендуется проводить по одной из альтернативных схем согласно табл. 3:
-Велпатасвир + Софосбувир** [76, 79]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
-Глекапревир + Пибрентасвир** [83-85,229]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 4)
-Даклатасвир** + Софосбувир** при генотипе 1, 2 и 4 [106,107,218]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
-Даклатасвир** + Софосбувир** + Рибавирин** при генотипе 3 [210, 218]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
-Гразопревир + Элбасвир** [93,207, 223, 226]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
-Дасабувир; Омбитасвир + Паритапревир + Ритонавир** при генотипе 1b,
-Дасабувир; Омбитасвир + Паритапревир + Ритонавир** + Рибавирин** при генотипе 1а [98, 102]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
-Ледипасвир + Софосбувир или Ледипасвир + Софосбувир + Рибавирин** [89-92,213-217]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
Табл. 3. Схемы ПВТ ХВГС для пациентов с компенсированным циррозом печени без предшествующего опыта ПВТ в зависимости от генотипа (лекарственные средства представлены в алфавитном порядке).
Примечания:
ВЕЛ+СОФ** – велпатасвир + софосбувир** (100/400 мг) 1 таб. 1р/д;
ГЛЕ+ПИБ** – глекапревир + пибрентасвир** (3 таб. одновременно, по 100/40 мг каждая) 1р/д;
ДАК**+СОФ** – даклатасвир** 60 мг 1 таб. 1р/д + софосбувир** 400 мг 1 таб. 1р/д;
ГРА+ЭЛБ** – гразопревир + элбасвир** 100/50 мг 1 таб. 1р/д;
ДСВ; ОБВ+ПТВ/р** – дасабувир (1 таб. по 250 мг 2 р/д); омбитасвир + паритапревир + ритонавир** (2 таб. одновременно 1р/д, по 12,5/75/50 мг каждая);
ЛЕД+СОФ – ледипасвир + софосбувир 90/400 мг 1 таб. 1р/д;
а — при ВН не более 800 000 МЕ/мл срок лечения 12 недель; 16-недельный курс совместно с РБВ** следует рассмотреть при ВН ВГС >800 000 ME/мл и/или при наличии полиморфизмов NS5A;
б — для ГТ 3 можно рассмотреть добавление РБВ**;
в — в случае недоступности иных схем лечения.
- Лечение пациентов с ХВГС, не ответивших на предшествующую терапию ПегИФН** + РБВ** ± СОФ** или СОФ** + РБВ**, без ЦП рекомендуется проводить по одной из альтернативных схем согласно табл. 4:
-Велпатасвир + Софосбувир** [76, 79]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
-Глекапревир + Пибрентасвир** [83-85]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
— Даклатасвир** + Софосбувир** [106,107,210,211,218]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
-Гразопревир + Элбасвир** [93,207, 223, 226]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
-Дасабувир; Омбитасвир + Паритапревир + Ритонавир** при генотипе 1b,
-Дасабувир; Омбитасвир + Паритапревир + Ритонавир** + Рибавирин** при генотипе 1а [98, 102]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
-Ледипасвир + Софосбувир или Ледипасвир+Софосбувир + Рибавирин** [89-92,213-217]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
Табл. 4. Схемы ПВТ ХВГС для пациентов, не ответивших на предшествующую терапию ПегИФН** + РБВ** ± СОФ** или СОФ** + РБВ**, без цирроза печени в зависимости от генотипа (лекарственные средства представлены в алфавитном порядке).
Примечания:
ВЕЛ+СОФ** – велпатасвир + софосбувир** (100/400 мг) 1 таб. 1р/д;
ГЛЕ+ПИБ** – глекапревир + пибрентасвир** (3 таб. одновременно, по 100/40 мг каждая) 1р/д;
ДАК** + СОФ** – даклатасвир** 60 мг 1 таб. 1р/д + софосбувир** 400 мг 1 таб. 1р/д;
ГРА+ЭЛБ** – гразопревир + элбасвир** 100/50 мг 1 таб. 1р/д;
ДСВ; ОБВ+ПТВ/р** – дасабувир (1 таб. по 250 мг 2 р/д); омбитасвир + паритапревир + ритонавир** (2 таб. одновременно 1р/д, по 12,5/75/50 мг каждая);
ЛЕД+СОФ – ледипасвир + софосбувир 90/400 мг 1 таб. 1р/д;
а – при ВН не более 800 000 МЕ/мл срок лечения 12 недель; 16-недельный курс совместно с РБВ** следует рассмотреть при ВН ВГС >800 000 ME/мл и/или при наличии полиморфизмов NS5A.
- Лечение пациентов с ХВГС, не ответивших на предшествующую терапию ПегИФН** + РБВ** ± СОФ** или СОФ** + РБВ**, с компенсированным ЦП рекомендуется проводить по одной из альтернативных схем согласно табл. 5:
-Велпатасвир + Софосбувир** [76, 79]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
-Глекапревир + Пибрентасвир** [84,85]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
-Даклатасвир** + Софосбувир** [106,107, 218, 227]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
-Даклатасвир** + Софосбувир** + Рибавирин** [108,210,211, 218]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
-Гразопревир + Элбасвир** [93,207]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
-Дасабувир; Омбитасвир + Паритапревир + Ритонавир** при генотипе 1b,
-Дасабувир; Омбитасвир + Паритапревир + Ритонавир** + Рибавирин** при генотипе 1а [98,102]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
-Ледипасвир + Софосбувир или Ледипасвир+Софосбувир + Рибавирин** [90-92,213-217]
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 3)
Табл. 5. Схемы ПВТ ХВГС для пациентов, не ответивших на предшествующую терапию, ПегИФН** + РБВ** ± СОФ** или СОФ** + РБВ**, с компенсированным циррозом печени в зависимости от генотипа (лекарственные средства представлены в алфавитном порядке).
Примечания:
ВЕЛ+СОФ** – велпатасвир + софосбувир** (100/400 мг) 1 таб. 1р/д;
ГЛЕ+ПИБ** – глекапревир + пибрентасвир** (3 таб. одновременно, по 100/40 мг каждая) 1р/д;
ДАК** + СОФ** – даклатасвир** 60 мг 1 таб. 1р/д + софосбувир** 400 мг 1 таб. 1р/д;
ГРА+ЭЛБ** – гразопревир + элбасвир** 100/50 мг 1 таб. 1р/д;
ДСВ; ОБВ+ПТВ/р** – дасабувир (1 таб. по 250 мг 2 р/д); омбитасвир + паритапревир + ритонавир** (2 таб. одновременно 1р/д, по 12,5/75/50 мг каждая);
ЛЕД+СОФ – ледипасвир + софосбувир 90/400 мг 1 таб. 1р/д;
а — при ВН не более 800 000 МЕ/мл срок лечения 12 недель; 16-недельный курс совместно с РБВ** следует рассмотреть при ВН ВГС >800 000 ME/мл и/или при наличии полиморфизмов NS5A;
б — для ГТ 3 можно рассмотреть добавление РБВ**;
в — в случае недоступности иных схем лечения.
Все схемы ПВТ для лечения пациентов с ХВГС (всех ГТ ВГС) с ЦП (в т.ч. декомпенсированным) или без него, с опытом предшествующей ПВТ или без него, суммированы также в Приложении А3.
3. Контроль терапии
- Всем пациентам, получившим ПВТ ХВГС, рекомендуется провести качественное определение РНК ВГС через 12 недель после окончания лечения, с тем чтобы оценить эффективность проведенной ПВТ. Рекомендуется использовать методы с высокой чувствительностью (≤15 МЕ/мл) [46-48,111]. Отсутствие РНК ВГС через 12 недель после окончания ПВТ означает излечение от ХВГС. Напротив, положительный результат РНК ВГС в эти сроки указывает на неудачу проведенного лечения.
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
- При применении РБВ** рекомендуется раз в 2-4 недели исследовать общий развернутый (клинический) анализ крови, и при снижении гемоглобина на 10 г/л от исходного и более уменьшить дозу препарата на 200 мг/сут, а при концентрации гемоглобина менее 85 г/л отменить терапию РБВ** [112-117].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Большинство современных препаратов ПВТ ХВГС хорошо переносятся, однако в ряде случаев необходимо добавлять РБВ** (для некоторых схем, особенно для пациентов с ЦП) – препарат, одним из основных побочных эффектов которого является не иммунный гемолиз. При применении РБВ** следует контролировать общий развернутый (клинический) анализ крови и при необходимости проводить коррекцию терапии.
- По решению лечащего врача, независимо от условий оказания медицинской помощи, для контроля ПВТ (в т.ч. оценки эффективности и безопасности) взрослых пациентов с ХВГС рекомендуется рассмотреть применение телемедицинских технологий [228,230].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3)
4. Перелечивание
В большинстве случаев (95-100%) применение ПППД приводит к УВО, однако в редких случаях достичь УВО не удается.
- При неэффективности терапии ПППД рекомендуется использовать схему с другими препаратами, а также комбинацию из трех препаратов различного механизма действия (препаратом, ингибирующим NS3/NS4A + препаратом, ингибирующим NS5A + препаратом, ингибирующим NS5B) без РБВ** или с добавлением его. Если доступно исследование мутаций резистентности ВГС к различным ПППД, рекомендуется выполнить его для рационального подбора новой схемы [71-76,167,212].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарии:
— Пациентам с ХВГС (ГТ 1-6) без ЦП или с компенсированным ЦП после неэффективной ПВТ препаратами, ингибирующими NS3/4А+/-NS5В: для перелечивания рекомендуется пангенотипная схема велпатасвир + софосбувир** 100/400 мг в течение 12 недель;
— Пациентам с ХВГС (ГТ 1-6) с декомпенсированным ЦП после неэффективной ПВТ препаратами, ингибирующими NS3/4А+/-NS5В: для перелечивания рекомендуется пангенотипная схема велпатасвир + софосбувир** 100/400 мг в комбинации с РБВ** (600 – 1200 мг/сут) в течение 12 недель;
— Пациентам с ХВГС (ГТ 1-6) без ЦП или с ЦП (компенсированным и декомпенсированным) после неэффективной ПВТ препаратами, ингибирующими NS5А: для перелечивания рекомендуется пангенотипная схема велпатасвир + софосбувир** 100/400 мг в комбинации с РБВ** (600 – 1200 мг/сут) в течение 24 недель;
— Пациентам с ХВГС (ГТ 1) без ЦП или с компенсированным ЦП после неэффективной ПВТ препаратами, ингибирующими NS3/4А без препаратамов, ингибирующих NS5A: для перелечивания рекомендуется схема глекапревир + пибрентасвир** (300/120 мг) в течение 12 недель;
— Пациентам с ХВГС (ГТ 1) без ЦП или с компенсированным ЦП после неэффективной
ПВТ препаратами, ингибирующими NS5A, без препаратов, ингибирующих NS3/4А: для перелечивания рекомендуется схема глекапревир + пибрентасвир** (300/120 мг) в течение 16 недель;
— Пациентам с ХВГС (ГТ 1-6) без ЦП или с компенсированным ЦП после неэффективной ПВТ препаратами, ингибирующими NS3/4А и NS5А: по решению врачебной комиссии для перелечивания можно рассмотреть #глекапревир + пибрентасвир** (300/120 мг 1р/д) в сочетании с софосбувиром** (400 мг 1 р/д) внутрь и/или РБВ** (1000-1200 мг/сут) в течение 12-24 недель. Длительность курса определяется индивидуально и зависит, в том числе, от стадии фиброза печени и наличия резистентных к ПППД вариантов ВГС.
5. Патогенетическая терапия
Патогенетической терапии для пациентов с ХВГС нет.
6. Симптоматическая терапия
Симптоматической терапии для пациентов с ХВГС нет.
7. Хирургическое лечение
- Рекомендуется проведение трансплантации печени при наличии стойких признаков декомпенсации функции печени пациентам с ЦП для сохранения жизни [118-120].
Уровень достоверности рекомендации С (уровень убедительности доказательств – 4)
Комментарий: дообследование проводится в соответствии с протоколом ведения пациентов из листа ожидания в трансплантологическом центре.
- Пациентам с ЦП рекомендуется выполнение эндоскопического лигирования или склерозирования ВРВ пищевода и желудка для профилактики кровотечения или его купирования [121-125].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
- Рекомендуется выполнение лапароцентеза пациентам с ЦП при наличии рефрактерного асцита для его купирования [126].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
- Рекомендуется выполнение трансъюгулярного внутрипеченочного порто-системного шунтирования пациентам при наличии выраженной портальной гипертензии [126].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
8. Внепеченочные проявления хронического вирусного гепатита С
- Пациентам с внепеченочными иммунологически обусловленными проявлениями ХВГС рекомендуется назначить ПППД по описанным выше схемам [23,127-129].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: ХВГС может проявиться внепеченочными иммунологически обусловленными состояниями (криоглобулинемический васкулит, в том числе с синдромом Рейно, интерстициальные заболевания легких, гломерулонефрит, синдром Шегрена, артрит и другие), а также неходжкинскими В-клеточными лимфомами. Во всех случаях следует назначить ПППД по описанным выше схемам. Раннее начало ПВТ значительно снижает риск развития внепеченочных проявлений.
9. Коинфекция
Пациенты с ХВГС и коинфекцией ВИЧ относятся к группе, требующей безотлагательной ПВТ ХВГС [1,69]. Течение ХВГС у ВИЧ-инфицированных зависит от степени выраженности иммунодефицита, обусловленного ВИЧ. Вероятность развития тяжелого поражения печени особенно высока при снижении CD4 лимфоцитов менее 200/мкл. Прогрессирование, связанное с поражением печени, обусловлено повышением концентрации вируса в крови (в 2-8 раз) на фоне выраженного иммунодефицита. Коинфекция ВИЧ и ВГС приводит к увеличению частоты развития осложнений, а также связанной с этими заболеваниями смертности.
Антиретровирусная терапия коинфицированных ВГС/ВИЧ больных ассоциирована с возможным риском нарушения функций печени вследствие ее гепатотоксичности [130,131].
- Для лечения ХВГС у больных, коинфицированных ВИЧ, рекомендуется использовать те же схемы ПВТ, что и для лечения моноинфекции ВГС, с целью эрадикации ВГС [132-137].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарии: все схемы ПВТ на основе ПППД требуют учета межлекарственных взаимодействий. Одним из удобных способов оценки межлекарственных взаимодействий является использование Ливерпульской таблицы лекарственных взаимодействий в Интернет ресурсе (http://www.hep-druginteractions.org).
9.2 Коинфекция ВГС/ВГВ
Пациенты с ХВГС и коинфекцией вирусом гепатита В (ВГВ) относятся к группе, требующей безотлагательной ПВТ ХВГС [1,69]. Коинфекция ВГС/ВГВ ускоряет прогрессирование заболевания и увеличивает риск развития ГЦК [138,139].
- Всем больным ХВГС рекомендуется провести тестирование на наличие перенесенной или текущей инфекции, вызванной ВГВ (HBsAg, anti-HBs, anti-HBc суммарные) [140-143].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4)
- Пациентам с коинфекцией ВГС/ВГВ рекомендуется назначить ПВТ нуклеозидами и нуклеотидами, кроме ингибиторов обратной транскриптазы, для профилактики реактивации инфекции, вызванной ВГВ. ПВТ нуклеозидами и нуклеотидами, кроме ингибиторов обратной транскриптазы, рекомендуется назначить на весь срок терапии ХВГС, а также на 12 недель после ее успешного завершения [142].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2)
Комментарии: поскольку ВГС, как правило, подавляет репликацию ВГВ, устранение первого вируса может привести к реактивации второго. Поэтому при лечении ХВГС следует тщательно контролировать маркеры активности ВГВ, и при их увеличении назначить ПВТ инфекции, вызванной ВГВ. Эту терапию также можно назначить с профилактической целью на срок лечение ХВГС и далее в течение 12 недель после ее успешного завершения.
- Пациентам с ХВГС и anti-HBc (в отсутствии HBsAg и anti-HBs) во время ПВТ ХВГС рекомендуется ежемесячный контроль АЛТ для исключения реактивации ВГВ [142].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2)
- При коинфекции ВГС/ВГВ для лечения ХВГС рекомендуется использовать стандартные схемы, описанные выше [1,138,142-145].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2)
10. Пациенты с хронической болезнью почек
- Для ПВТ ХВГС у пациентов с ХБП (включая тяжелую, с СКФ <30 мл/мин/1,73 м2) рекомендуется использование ПППД в соответствии с общими рекомендациями ПВТ ХВГС пациентов без ХБП [146-155] (см. подраздел 3.2 и Приложение А3).
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: на сегодня накоплено достаточно клинического опыта применения софосбувира** у пациентов с тяжелой ХБП [153-155], что позволяет рекомендовать софосбувир**-содержащие схемы ПВТ всем таким пациентам без коррекции доз ПППД.
- Для ПВТ ХВГС у пациентов с тяжелой ХБП (с СКФ <30 мл/мин/1,73 м2), тем не менее, рекомендуется по возможности отдавать предпочтение схемам, не содержащим софосбувир** [146-152]:
— Глекапревир + пибрентасвир** для всех ГТ ВГС;
— Дасабувир; омбитасвир + паритапревир + ритонавир** для ГТ 1;
— Элбасвир + гразопревир** для ГТ 1, 4;
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
- Пациентам с декомпенсированным ЦП (класс В или С по Child-Pugh) и тяжелой ХБП (с СКФ <30 мл/мин/1,73 м2) рекомендуется назначать следующие схемы ПВТ ХВГС в течение 24 недель [153,154,156,157]:
— Велпатасвир + софосбувир** (для всех ГТ);
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
— Даклатасвир** 1 таб. (60 мг) 1 р/д + #софосбувир** 1 таб. (400 мг) 1 р/д (для всех ГТ);
— Ледипасвир + cофосбувир (для ГТ 1 и 4).
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
11. Трансплантация печени
11.1 Противовирусная терапия ХВГС у больных с декомпенсированным циррозом печени, находящихся в Листе ожидания трансплантации печени
Целями ПВТ ХВГС у больных с декомпенсированным ЦП, находящихся в Листе ожидания ортотопической трансплантации печени (ОТП), являются:
- Предотвращение инфицирования трансплантата печени;
- Улучшение функции печени перед трансплантацией;
- Выведение пациента из Листа ожидания ОТП.
Улучшение функции печени оценивается по клиническим показателям, а также по шкалам Child-Pugh (см. Приложение Г) и MELD (для подсчета этого индекса можно использовать любой интернет-ресурс, например, https://www.mdcalc.com/meldna-meld-na-scoreliver-cirrhosis). Улучшение оценки MELD наблюдается у 60% больных с декомпенсированным ЦП, завершивших курс ПВТ. Это улучшение тем более вероятно и тем сильнее выражено, чем ниже оценка MELD до начала терапии.
До 25-30% больных с декомпенсированным ЦП могут иметь стойкое улучшение (компенсацию) ЦП, что позволяет вывести их из Листа ожидания ОТП. Выживаемость таких пациентов на протяжении 3-х лет не ниже, чем в группе реципиентов печени, которым была проведена ОТП, сопоставимых по исходной MELD [118,119,158-162].
- Больным с декомпенсированным циррозом в исходе ХВГС (Child-Pugh В или С) без ГЦК, ожидающим ОТП, рекомендуется назначать ПВТ, если MELD <20. ПВТ рекомендуется начинать как можно быстрее, чтобы завершить курс и оценить ответ до трансплантации [165,166].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1)
Комментарии: для ПВТ пациентов с декомпенсированным ЦП строго противопоказано использование препаратов, ингибирующих NS3/4.
- Больным с декомпенсированным ЦП в исходе ХВГС (Child-Pugh В или С) без ГЦК, ожидающим трансплантацию печени, с MELD ≥20 рекомендуется провести ОТП, не назначая ПВТ. ПВТ ХВГС рекомендуется провести после трансплантации [165,166].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1)
- Больным с декомпенсированным ЦП в исходе ХВГС (Child-Pugh В или С) без ГЦК, ожидающие ОТП, с MELD ≥20 могут начать лечение до ОТП, если предполагаемое время ожидания органа превышает 6 месяцев [165,166].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1)
11.2 Противовирусная терапия инфекции, вызванной вирусом гепатита С, у реципиентов печени
- ПВТ инфекции трансплантата, вызванной ВГС, рекомендуется проводить всем реципиентам, у которых выявляется РНК ВГС в крови, насколько это возможно по состоянию пациента [176,177].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
Комментарии: частота УВО у реципиентов печени с компенсированной болезнью трансплантата, получивших запланированный курс ПВТ, составляет более 95%. УВО ассоциируется с замедлением прогрессирования фиброза и улучшением выживаемости трансплантата и реципиентов.
12. Беременные
Беременность, по-видимому, не оказывает негативного влияния на течение ХВГС. Активность АЛТ в сыворотке крови снижается в течение I и III триместров беременности и повышаются после родов. Уровень РНК ВГС повышается в течение I и III триместров, достигая пика в течение III триместра, и снижается после родоразрешения. Эти события, вероятно, обусловлены иммуносупрессивными эффектами беременности и увеличением объема материнской плазмы [191,192]. Передача ВГС от матери ребенку встречается с общей частотой от 5% до 15% [193,194]. Убедительных данных о негативном влиянии ВГС на развитие плода и исход беременности нет. Есть отдельные сообщения о влиянии ЦП на течение беременности и ее исход. Так, беременные женщины с ЦП подвергаются повышенному риску неблагоприятных исходов для матери (например, преэклампсия, геморрагические осложнения и смерть) и для плода (например, преждевременные роды, низкая масса тела при рождении и неонатальная смерть). Женщины с ЦП в исходе ХВГС должны быть проинформированы об этих возможных осложнениях [195,196].
- Женщинам репродуктивного возраста рекомендуется ПВТ ХВГС до планирования беременности, с тем чтобы снизить риск передачи ВГС будущему ребенку [197].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
- Для выявления ХВГС рекомендуется проводить обследование беременных на anti-HCV крови (Определение суммарных антител классов M и G (anti-HCV IgG и anti-HCV IgM) к вирусу гепатита C (Hepatitis C virus) в крови) в I (при постановке на учет по беременности) и в III триместрах беременности [198].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
- Не рекомендуется проводить ПВТ ПППД во время беременности из-за отсутствия в настоящее время достаточных данных о безопасности и эффективности ПППД [199, 200].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: на сегодня не существует крупномасштабных клинических испытаний, оценивающих безопасность ПППД при беременности. Специальные исследования ПВТ СОФ** и ЛЕД+СОФ во время беременности продемонстрировали хорошую безопасность для плода. Данных об использовании пангенотипных схем во время беременности в настоящее время нет.
- Женщинам детородного возраста, получающим ПВТ ХВГС с РБВ**, не рекомендуется беременность во время приема ПВТ и в течение не менее 6 месяцев после прекращения ПВТ [201,202].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
- Мужчинам, получающим ПВТ ХВГС с РБВ**, не рекомендуется беременность их половых партнерш во время приема ПВТ и в течение не менее 6 месяцев после прекращения ПВТ [201,202].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: РБВ** обладает тератогенным свойством, то есть может вызвать аномалии развития и гибель плода. Его не следует назначать беременным женщинам или женщинам детородного возраста, которые могут забеременеть во время лечения РБВ** или в течение 6 месяцев после прекращения РБВ**. Кроме того, следует помнить, что РБВ** аналогичным образом может вызывать врожденные дефекты у плода, в случае если мужчина получал РБВ**, когда женщина забеременела от него. Таким образом, для избегания беременности во время лечения РБВ** и в течение не менее 6 месяцев после этого лицам с детородным потенциалом крайне важно использовать по крайней мере 2 формы эффективной контрацепции. Консультирующему врачу необходимо задокументировать обсуждение потенциальных тератогенных эффектов РБВ** в медицинской карте пациента.
- Женщинам с ХВГС не рекомендуется отмена грудного вскармливания, за исключением случаев повреждения сосков и кровотечения из этих повреждений [203,204].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4)
Комментарии: грудное вскармливание не представляет риска для передачи ВГС от матери ребенку, поскольку частота инфицирования детей по результатам исследований сопоставима в группах на грудном вскармливании и на искусственном вскармливании. Однако в случае повреждения сосков и кровотечения из этих повреждений возникает риск инфицирования ребенка от матери с ХВГС вследствие передачи ВГС через кровь.
Медицинская реабилитация
Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов медицинской реабилитации, в том числе основанных на использовании природных лечебных факторов
Для пациентов с ХВГС специализированные реабилитационные мероприятия не разработаны.
Госпитализация
Организация оказания медицинской помощи
Медицинская помощь оказывается в форме:
- экстренной медицинской помощи;
- неотложной медицинской помощи;
- плановой медицинской помощи.
Условия оказания медицинских услуг
Медицинская помощь оказывается в виде:
- первичной медико-санитарной помощи;
- скорой, в том числе скорой специализированной, медицинской помощи;
- специализированной, в том числе высокотехнологичной, медицинской помощи.
Медицинская помощь взрослым больным с ХВГС может оказываться в следующих условиях:
- амбулаторно (в условиях, не предусматривающих круглосуточное медицинское наблюдение и лечение);
- в дневном стационаре (в условиях, предусматривающих медицинское наблюдение и лечение в дневное время, не требующих круглосуточного медицинского наблюдения и лечения);
- стационарно (в условиях, обеспечивающих круглосуточное медицинское наблюдение и лечение).
Первичная медико-санитарная помощь пациентам оказывается в амбулаторных условиях и в условиях дневного стационара.
Первичная доврачебная медико-санитарная помощь в амбулаторных условиях осуществляется в фельдшерско-акушерских пунктах.
Первичная врачебная медико-санитарная помощь осуществляется врачом-терапевтом участковым, врачом общей практики (семейным врачом) в амбулаторных условиях.
Первичная специализированная медико-санитарная помощь осуществляется врачом-инфекционистом или врачом-гастроэнтерологом медицинской организации, оказывающим медицинскую помощь пациентам в амбулаторных условиях.
Специализированная, в том числе высокотехнологичная, медицинская помощь оказывается в условиях стационара врачами-инфекционистами и другими врачами-специалистами и включает в себя профилактику, диагностику, лечение заболеваний и состояний, требующих использования специальных методов и сложных медицинских технологий, а также медицинскую реабилитацию.
Лечение пациентов осуществляется в условиях круглосуточного или дневного стационара по направлению врача-терапевта участкового, врача общей практики (семейного врача), врача-инфекциониста, врача-гастроэнтеролога, медицинских работников, выявивших ХВГС.
Больные ХВГС должны находиться под наблюдением до достижения УВО12, а при наличии фиброза печени F3-4 по METAVIR пожизненно.
Показанием к экстренной госпитализации служит развитие острой печеночной недостаточности, в том числе печеночной энцефалопатии и острой печеночной недостаточности на фоне хронической.
Медицинская помощь пациентам ХВГС оказывается в соответствии с утвержденным стандартом специализированной медицинской помощи.
Профилактика
Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
1. Специфическая профилактика
Специфическая профилактика ХВГС в настоящее время не разработана.
- Пациентам с ХВГС рекомендуется вакцинация против гепатита А и В для предотвращения инфицирования этими вирусами [1,183-186].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
2. Неспецифическая профилактика
- Рекомендуется активное выявление источников инфекции (обследование лиц, подверженных повышенному риску инфицирования и/или имеющих особую эпидемиологическую значимость) для своевременного проведения ПВТ [31,32].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
- Рекомендуется профилактика искусственного механизма передачи (переливание крови только по жизненным показаниям, обоснованность инвазивных методов обследования, использование одноразового инструментария, строгое соблюдение режимов обработки медицинского инструментария и оборудования, использование защитных средств медработниками) для снижения риска распространения инфекции, вызванной ВГС [187-189].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1)
- Рекомендуется ПВТ больных, инфицированных ВГС, направленная на полную эрадикацию возбудителя, для профилактики распространения инфекции [17,32,190].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5)
3. Диспансерное наблюдение
- Пациентам с ХВГС, которым отложено проведение ПВТ, рекомендуется диспансерное наблюдение один раз в год с проведением комплексного клинико-лабораторного и инструментального обследования для динамического наблюдения [54,55,57,59-61,66,67] (см. также подразделы 2.3 Лабораторные диагностические исследования, 2.4 Инструментальные диагностические исследования, 2.4):
— Всем пациентам с ХВГС – анализ крови биохимический общетерапевтический, УЗИ органов брюшной полости (комплексное) и забрюшинного пространства, эластометрия печени (при ее недоступности могут использоваться некоммерческие расчетные показатели, основанные на результатах лабораторного обследования, например, расчет индексов APRI, FIB-4);
— Всем пациентам с ХВГС с исходом в ЦП в дополнение к вышеперечисленному — общий (клинический) анализ крови (развернутый), определение протромбинового (тромбопластинового) времени, ЭГДС.
Уровень убедительности рекомендации С (уровень достоверности доказательств – 4)
- Не рекомендуется диспансерное наблюдение пациентам с показаниями к безотлагательному началу ПВТ ХВГС [1,69] (см. подраздел 3.1 Показания к началу противовирусной терапии).
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
- Не рекомендуется диспансерное наблюдение пациентам без фиброза печени, со слабовыраженным и умеренным фиброзом печени (F0-F2 по METAVIR) после достижения УВО12 [46-48] (см. подраздел 2.3 Лабораторные диагностические исследования).
Уровень убедительности рекомендации С (уровень достоверности доказательств – 5)
Комментарий: пациенты с anti-HCV, у которых отсутствует РНК ВГС после проведенной ПВТ ХВГС в течение 12 недель, считаются излечившимся от ХВГС и подлежат снятию с диспансерного наблюдения.
- Рекомендуется диспансерное наблюдение пациентам с выраженным и тяжелым фиброзом печени (F3-F4 по METAVIR), получившим ПВТ ХВГС, даже после достижения УВО12 в связи с продолжающимся риском развития ГЦК (контроль АФП крови и УЗИ брюшной полости комплексное каждые полгода) [44,45,53] (см. подразделы 2.3 Лабораторные диагностические исследования, 2.4 Инструментальные диагностические исследования).
Уровень убедительности рекомендации A (уровень достоверности доказательств – 1)
Информация
Источники и литература
-
Клинические рекомендации Национального научного общества инфекционистов (ННОИ)
- 1. EASL recommendations on treatment of hepatitis C: Final update of the series. J
Hepatol 2020 Nov;73(5):1170-1218.
2. Dubuisson J, Cosset FL. Virology and cell biology of the hepatitis C virus life cycle: an
update. J Hepatol. 2014;61(1 Suppl):3-13.
3. Sergio M Borgia, et al. Identification of a novel hepatitis c virus genotype from punjab,
india: expanding classification of hepatitis c virus into 8 genotypes. J Infect Dis. 2018 Oct
20;218(11):1722-1729.
4. Дунаева, Н. В. Структурно-функциональная организация генома вируса гепатита
С. Вопросы вирусологии. – 2006. – № 51 (2). – С. 10 – 14.
5. Irshad M, Gupta P, Irshad K. Immunopathogenesis of liver injury during hepatitis c
virus infection. Viral Immunol. 2019;32(3):112-205.
6. Lingala S, Ghany MG. Natural history of hepatitis C. Gastroenterol Clin North Am.
2015;44(4):717-34.
7. Yamane, D. Liver injury and disease рathogenesis in chronic hepatitis C. Curr Top
Microbiology Immunology 2013;369:263-288.
8. Семенов, А. В. Особенности популяционного состава CXCRS-положительных
лимфоцитов периферической крови больных хроническим гепатитом С. Журнал
микробиологии, эпидемиологии и иммунобиологии. – 2013. –№ 6. – С. 69 – 76.
9. Елезов, Д. С. Анализ популяций Т-хелперных клеток памяти, экспрессирующих
хемокиновые рецепторы CXCR3 и CCR6, в периферической крови больных хроническим
вирусным гепатитом С. Бюллетень экспериментальной биологии и медицины. – 2015. – № 160
(8). – С. 204 – 208.
10. Lohr, H. F. HCV replication in mononuclear cells simulates anti-HCV-secreting B cells
and reflects nonresponsiveness to interferon-alfa. J. Med. Virol. 1995;46(4):314-21.
11. Арсентьева, Н. А. Хемокиновые рецепторы CXCR3 и CCR6 и их лиганды в
печени и крови больных хроническим вирусным гепатитом С. Бюллетень экспериментальной
биологии и медицины. – 2015. – № 8. – С. 218 – 222.
12. Давидович, Н. В. Иммунный ответ при вирусном гепатите С: ведущая роль
натуральных киллеров. Ж. «Вестник Северного (Арктического) федерального университета». –
2015. – №4. – C. 68 – 78.
13. Хронический вирусный гепатит. Под ред. В. В. Серова, З. Г. Апросиной. – М:
Медицина. – 2002. – 384 с.
14. Дудина, К. Р. Факторы прогрессирующего течения хронического гепатита С. Ж.
Лечащий врач. – 2013. – №10. – С. 36.
15. Сухорук, А. А. Цирроз печени как исход хронического гепатита С. Журнал
инфектологии. – 2014. –№ 6(1). – С. 67 – 71.
16. Пименов Н.Н., Комарова С.В., Карандашова И.В., Цапкова Н.Н., Волчкова Е.В.,
Чуланов В.П. Гепатит С и его исходы в России: анализ заболеваемости, распространенности и
смертности до начала программы элиминации инфекции. Инфекционные болезни, 2018, т.16,
№3, с. 37-45
17. WHO Global hepatitis report, 2018 https://www.who.int/news-room/factsheets/
detail/hepatitis-c Обращение к сайту в мае 2021.
18. Alter MJ. Epidemiology of hepatitis C virus infection. World J Gastroenterol.
2007;13(17):2436-41.
19. Terrault NA. Sexual activity as a risk factor for hepatitis C. Hepatology. 2002;36(5
Suppl 1):99-105.
20. Chan DP, Sun HY, Wong HT, Lee SS, Hung CC. Sexually acquired hepatitis C virus
infection: a review. Int J Infect Dis. 2016;49:47-58.
21. Жданов, К. В. Вирусные гепатиты. СПб.: Фолиант. – 2011. – 304 с.
22. Wang LS, D’souza LS, Jacobson IM. Hepatitis C – a clinical review. J Med Virol.
2016;88(11):1844-55.
23. Kuna L, Jakab J, Smolic R, Wu GY, Smolic M. HCV Extrahepatic Manifestations. J
Clin Transl Hepatol. 2019;7(2):172-182.
24. Ющук, Н. Д. Инфекционные болезни: национальное руководство – 2-е изд.,
переработанное и доп. М.: ГЭОТАР-Медиа, 2019. – 1104 с.
25. Майер, К. П. Гепатит и последствия гепатита. Практич. рук. Пер. с нем. – 2-е изд.//
М: ГЭОТАР- МЕД, 2004. – С. 265, 467 – 479; 491 – 503.
- 1. EASL recommendations on treatment of hepatitis C: Final update of the series. J
Информация
Список сокращений
** – указывается в конце названия лекарственного препарата или комбинации лекарственных препаратов, означает их принадлежность к списку ЖНЛВП
# – указывается в начале названия лекарственного препарата или схемы лекарственных препаратов, применяющихся не по медицинской инструкции (off-label)
Anti-HCV – антитела к вирусу гепатита С
Anti-HBc – антитела к ядерному антигену вируса гепатита В
HBcAg – hepatitis B core antigen, ядерный антиген вируса гепатита В
HBsAg – hepatitis B surface antigen, поверхностный антиген вируса гепатита В
HBV – hepatitis B virus, вирус гепатита В
HCVcAg – hepatitis C virus core antigen, ядерный антиген вируса гепатита С
HCV hepatitis C virus, вирус гепатита С
HIV – human immunogenicity virus, вирус иммунодефицита человека
MELD – model of end liver disease, расчетный индекс, характеристика тяжести терминальной стадии болезни печени
NS3/4A ингибиторы – противовирусные средства для лечения гепатита C, блокируют неструктурные белки NS3 и NS4A вируса гепатита С (J05AЕ ингибиторы протеаз)
NS5A ингибиторы – противовирусные средства для лечения гепатита C, блокируют неструктурный белок NS5A вируса гепатита С (J05AХ прочие противовирусные препараты)
АЛТ – аланиновая аминотрансфераза
АСТ – аспарагиновая аминотрансфераза
АФП – альфа-фетопротеин
ВГВ – вирус гепатита В
ВГС – вирус гепатита С
ВЕЛ+СОФ** – велпатасвир + софосбувир**
ВН – вирусная нагрузка
ВИЧ – вирус иммунодефицита человека
ВРВ – варикозно расширенные вены
ГГТ – гамма-глутамилтрансфераза
ГЛЕ+ПИБ** – глекапревир + пибрентасвир**
ГРА+ЭЛБ** – гразопревир + элбасвир**
ГТ – генотип
ГЦК – гепатоцеллюлярная карцинома
ДАК** – даклатасвир**
ДСВ; ОБВ+ПТВ/р** – дасабувир; омбитасвир + паритапревир + ритонавир**
ДНК – дезоксирибонуклеиновая кислота
ЖНЛВП – жизненно необходимые и важнейшие лекарственные препараты
ЛЕД+СОФ – ледипасвир + софосбувир
МЕ – международная единица
МКБ 10 – Международная классификация болезней 10-го пересмотра
НРВ** – нарлапревир**
НРВ**/р**– нарлапревир**, бустированный ритонавиром**
ОТП – ортотопическая трансплантация печени
ПегИФН** – Пэгинтерферон альфа-2a (40 кДа)** или Пэгинтерферон альфа 2b **
ПППД – противовирусные препараты прямого действия
ПТИ – протромбиновый индекс
РБВ** – рибавирин**
РНК – рибонуклеиновая кислота
р/д – раз в день
СКФ – скорость клубочковой фильтрации
СОФ** – софосбувир**
таб. – таблетка
УЗИ – ультразвуковое исследование
УВО – устойчивый вирусологический ответ
УВО12 – устойчивый вирусологический ответ через 12 недель после окончания терапии
ХБП – хроническая болезнь почек
ХВГС – хронический вирусный гепатит С
ЦП – цирроз печени
Термины и определения
Вирусная нагрузка (ВН) – количество вирусной РНК в крови, измеряется в МЕ/мл.
Генотипы вируса гепатита С – варианты вируса гепатита С, разделяются на основании различий в нуклеотидной последовательности определенных областей генома вируса. В клинической практике имеют большое значение для подбора схемы противовирусного лечения, в случае если применяются генотип-специфические препараты.
Гепатит – воспаление в ткани печени, характеризуется наличием некровоспалительных изменений в биоптате печени.
Гепатоцеллюлярная карцинома – злокачественное образование печени, является
одним из возможных неблагоприятных исходов хронического вирусного гепатита С, возникает,
как правило, на фоне сформированного цирроза печени.
Коинфекция – инфицирование двумя и более инфекционными агентами. В случае хронического вирусного гепатита С обычно применяется в отношении сочетания с вирусами гепатита В, Д и ВИЧ.
Пангенотипный – характеристика лекарственного средства или группы средств, эффективных в отношении всех наиболее распространенных генотипов вируса гепатита С.
Устойчивый вирусологический ответ (УВО) – отсутствие в крови РНК вируса гепатита С через 12 после окончания терапии.
Фиброз печени – процесс замещения паренхиматозной ткани печени соединительной тканью, является универсальной реакцией организма на хроническое повреждение.
Цирроз печени – терминальная стадия хронического заболевания печени, характеризуется замещением паренхимы соединительной тканью и нарушением архитектуры органа. На ранних этапах при сохраненной функции печени называется компенсированным, при потере функции – декомпенсированным.
APRI – некоммерческий расчетный индекс фиброза печени, метод неинвазивной диагностики. Может использоваться в качестве альтернативного при недоступности эластометрии печени.
FIB-4 – некоммерческий расчетный индекс фиброза печени, метод неинвазивной диагностики. Может использоваться в качестве альтернативного при недоступности эластометрии печени.
METAVIR – популярная система оценки степени воспаления (от А0 до А3) и фиброза (от F0 по F4) в ткани печени. Применяется как для характеристики биоптата печени, так и для оценки фиброза печени неинвазивными методами (например, при эластометрии печени или расчете индекса фиброза) (см. Приложение Г).
Критерии оценки качества медицинской помощи
Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
Ивашкин Владимир Трофимович – д.м.н., профессор, академик РАН, Президент Российской гастроэнтерологической ассоциации и Российского общества по изучению печени, заведующий кафедрой пропедевтики внутренних болезней, гастроэнтерологии и гепатологии ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет), заслуженный врач РФ, заслуженный деятель науки РФ.
Ющук Николай Дмитриевич – д.м.н., профессор, академик РАН, Президент ФГБОУ ВО МГМСУ им. А.И. Евдокимова Минздрава России, заведующий кафедрой инфекционных болезней и эпидемиологии ФГБОУ ВО МГМСУ им. А.И. Евдокимова Минздрава России, заслуженный деятель науки РФ.
Богомолов Павел Олегович – к.м.н., руководитель отделения гепатологии ГБУЗ МО МОНИКИ им. М.Ф. Владимирского.
Волчкова Елена Васильевна – д.м.н., профессор, заведующая кафедрой инфекционных болезней Института клинической медицины им. Н.В. Склифосовского ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет).
Дмитриев Александр Сергеевич – к.м.н., руководитель Центра эпидемически значимых инфекционных болезней ФГБУ «НМИЦ ФПИ» Минздрава России, врач-инфекционист.
Жаркова Мария Сергеевна – к.м.н., заведующая отделением гепатологии Клиники пропедевтики внутренних болезней, гастроэнтерологии и гепатологии им. В.Х. Василенко ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет).
Жданов Константин Валерьевич –д.м.н., профессор, член-корр. РАН, начальник кафедры инфекционных болезней (с курсом медицинской паразитологии и тропических заболеваний) ФГКВОУ ВПО «ВМА им. С. М. Кирова» Минобороны России.
Знойко Ольга Олеговна – д.м.н., профессор кафедры инфекционных болезней и эпидемиологии ФГБОУ ВО МГМСУ им. А.И. Евдокимова Минздрава России.
Климова Елена Анатольевна – д.м.н., профессор кафедры инфекционных болезней и эпидемиологии ФГБОУ ВО МГМСУ им. А.И. Евдокимова Минздрава России.
Козлов Константин Вадимович – д.м.н., доцент кафедры инфекционных болезней (с курсом медицинской паразитологии и тропических заболеваний) ФГКВОУ ВПО «ВМА им. С. М. Кирова» Минобороны России.
Кравченко Ирина Эдуардовна – д.м.н. доцент, профессор кафедры инфекционных болезней ФГБОУ ВО Казанский ГМУ Минздрава России.
Маевская Марина Викторовна – д.м.н., профессор ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет), консультант ЛДО3 УКБ 2.
Малинникова Елена Юрьевна – д.м.н., доцент, заведующая кафедрой вирусологии ФГБОУ ДПО РМАНПО Минздрава России.
Мамонова Нина Алексеевна – научный сотрудник лаборатории генетических технологий и трансляционных исследований ФГБУ «НМИЦ ФПИ» Минздрава России.
Масленников Роман Вячеславович – к.м.н., ассистент кафедры пропедевтики
внутренних болезней, гастроэнтерологии и гепатологии ФГАОУ ВО Первый МГМУ им. И.М.
Сеченова Минздрава России (Сеченовский Университет).
Михайлов Михаил Иванович – д.м.н., профессор, член-корреспондент РАН, заведующий лабораторией вирусных гепатитов ФГБНУ НИИВС им. И.И. Мечникова.
Новак Ксения Егоровна – к.м.н., доцент кафедры инфекционных болезней взрослых и эпидемиологии ФГБОУ ВО СПбГПМУ Минздрава России.
Никитин Игорь Геннадиевич – д.м.н., профессор, заведующий кафедрой госпитальной терапии №2 лечебного факультета ФГАУ ВО «Российский национальный исследовательский университет им. Н.И. Пирогова» Минздрава России, директор ФГАУ НМИЦ «Лечебно-реабилитационный центр» Минздрава России.
Сюткин Владимир Евгеньевич – д.м.н., ведущий научный сотрудник отделения трансплантации печени ГБУЗ «НИИ скорой помощи им. Н.В. Склифосовского ДЗМ», профессор кафедры хирургии с курсами онкохирургии, эндоскопии, хирургической патологии, клинической трансплантологии и органного донорства ФГБУ ГНЦ ФМБЦ им. А.И. Бурназяна ФМБА России.
Тихонов Игорь Николаевич – ассистент кафедры пропедевтики, гастроэнтерологии и гепатологии ИКМ Н.В. Склифосовского ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет), врач-гастроэнтеролог отделения гепатологии УКБ 2.
Чуланов Владимир Петрович – д.м.н., профессор, главный внештатный специалист по инфекционным болезням Минздрава России, заместитель директора по научной работе и инновационному развитию ФГБУ «НМИЦ ФПИ» Минздрава России.
Шептулин Аркадий Александрович – д.м.н., профессор кафедры пропедевтики внутренних болезней гастроэнтерологии и гепатологии ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет).
Широкова Елена Николаевна – д.м.н., профессор кафедры пропедевтики внутренних болезней ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет).
Эсауленко Елена Владимировна – д.м.н., профессор, заведующая кафедрой инфекционных болезней взрослых и эпидемиологии ФГБОУ ВО СПбГПМУ Минздрава России.
Приложение А2. Методология разработки клинических рекомендаций
Предлагаемые рекомендации имеют своей целью довести до практических врачей современные представления об этиологии и патогенезе ХВГС, а также ознакомить их с применяющимся в настоящее время алгоритмами ее диагностики и лечения.
Целевая аудитория данных клинических рекомендации:
1. Врачи-инфекционисты;
2. Врачи-гастроэнтерологи;
3. Врачи общей практики (семейные врачи);
4. Врачи-терапевты.
Табл. П1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств)
Табл. П2. Уровни достоверности доказательств с указанием использованной классификации уровней достоверности доказательств (УДД)
Табл. П3. Уровни убедительности рекомендаций (УУР) с указанием использованной классификации уровней убедительности рекомендаций
Порядок обновления клинических рекомендаций
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию – не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений и/или замечаний к ранее утверждённым клиническим рекомендациям, но не чаще 1 раза в 6 месяцев.
Приложение А3. Справочные материалы
Данные клинические рекомендации разработаны с учетом следующих нормативно-правовых документов:
1. Приказ Министерства здравоохранения и социального развития Российской Федерации от 31 января 2012 г. № 69н «Об утверждении Порядка оказания медицинской помощи взрослым больным при инфекционных заболеваниях»;
2. Приказ Министерства здравоохранения и социального развития Российской Федерации от 02.06.2010 № 415н “Об утверждении Порядка оказания медицинской помощи населению при заболеваниях гастроэнтерологического профиля”;
3. Приказ Министерства здравоохранения Российской Федерации от 10 мая 2017 г. N 203н «Об утверждении критериев оценки качества медицинской помощи»;
4. Приказ Минздрава России от 07.11.2012 N 685н «Об утверждении стандарта специализированной медицинской помощи при хроническом вирусном гепатите C».
Схемы противовирусной терапии хронического вирусного гепатита С с учетом генотипа, опыта предшествующей терапии, наличия цирроза печени (названия лекарственных средств указаны в алфавитном порядке)
Приложение Б. Алгоритмы действий врача
Диагностика, лечение ХВГС
Приложение В. Информация для пациента
Уважаемый пациент! У Вас гепатит С. Современными лекарствами возможно полностью излечиться от данного заболевания. Это позволит не допустить развитие таких осложнений, как цирроз и рак печени. Обычно болезнь протекает без симптомов и выявляется при случайном обследовании. Однако это не значит, что ее не следует лечить. Объем терапии определит Ваш лечащий врач. Он же определит перечень необходимых исследований и их периодичность. Вам не следует самостоятельно отменять или заменять препараты, даже если Вы чувствуете себя лучше или считаете себя здоровым человеком. По всем появляющимся вопросам обращайтесь к лечащему врачу.
Приложение Г. Шкалы оценки, приведенные в клинических рекомендациях
Приложение Г1. Оценка степени тяжести цирроза печени по шкале Child-Pugh
Название на русском языке: Оценка степени тяжести цирроза печени по шкале Child-Pugh
Источник: Durand F., Valla D. Assessment of the prognosis of cirrhosis: Child–Pugh versus MELD //Journal of hepatology. – 2005. – Т. 42. – №. 1. – С. S100-S107.
Тип: шкала оценки
Назначение: оценка степени тяжести цирроза печени
Содержание:
Ключ (интерпретация):
Баллы выставляются в зависимости от значения каждого из параметров от 1 до 3, после чего суммируются. Оценка выживаемости больных ЦП в зависимости от полученных баллов:
Приложение Г2. Расчет индекса фиброза APRI
Название: Расчет индекса фиброза APRI
Источник: Yen Y. H. et al. APRI and FIB-4 in the evaluation of liver fibrosis in chronic
hepatitis C patients stratified by AST level //PloS one. – 2018. – Т. 13. – №. 6. – С. e0199760.Тип: индекс
Содержание: Расчетная формула:
APRI = (АСТ/(ВГН АСТ)) * 100 / тромбоциты (109/л)
АСТ – значение аспарагиновой аминотрансферазы пациента
ВГН АСТ – верхняя граница нормы АСТ
Тромбоциты (109/л) – число тромбоцитов пациента в 1 л крови
Ключ (интерпретация):
Приложение Г3. Расчет индекса фиброза FIB-4
Название: Расчет индекса фиброза FIB-4
Источник: Yen Y. H. et al. APRI and FIB-4 in the evaluation of liver fibrosis in chronic
hepatitis C patients stratified by AST level //PloS one. – 2018. – Т. 13. – №. 6. – С. e0199760.
Тип: индекс
Содержание: Расчетная формула:
FIB-4 = Возраст (лет)) * АСТ / тромбоциты (109/л) * √АЛТ
Возраст – возраст пациента (лет)
АСТ – значение аспарагиновой аминотрансферазы пациента
Тромбоциты (109/л) – число тромбоцитов пациента в 1 л крови
√АЛТ – квадратный корень значения АЛТ пациента
Ключ (интерпретация):
Приложение Г4. Стадии фиброза печени по шкале METAVIR
Название: Шкала METAVIR
Источник: Shiha G., Zalata K. Ishak versus METAVIR: terminology, convertibility and correlation with laboratory changes in chronic hepatitis C //Liver biopsy. – 2011. – Т. 10. – С. 155-170.
Тип: шкала
Содержание и ключ (интерпретация):
Прикреплённые файлы
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
Вирусные гепатиты (ВГ) остаются одной из актуальных проблем в инфекционной патологии человека. Достижения в области вирусологии и изучения тонких механизмов патогенеза ВГ позволили не только по-новому оценить этапы и варианты взаимодействия вируса и макроорганизма, но и выработали новые подходы к терапии ВГ, включая разработку и внедрение в практику действенной этиотропной противовирусной терапии. Вместе с тем основные принципы терапии ВГ, разработанные С. П. Боткиным, Е. М. Тареевым, А. Ф. Блюгером и другими ведущими отечественными гепатологами-инфекционистами еще в XIX–XX веках, остаются актуальными и обязательными и в настоящее время.
Острые вирусные гепатиты (ОВГ)
Основой терапии ОВГ является создание охранительно-щадящего режима и соблюдение диеты. Больные ОВГ подлежат госпитализации в инфекционные стационары как по эпидемиологическим показаниям, так и для диагностики, оценки тяжести и динамического наблюдения с целью ранней диагностики развития тяжелых форм гепатита и осложнений. В острый период заболевания рекомендуется назначение постельного режима, а больным с угрозой развития острой печеночной энцефалопатии — соблюдение строгого постельного режима. В периоды спада желтухи и реконвалесценции пациенты переходят на палатный режим.
После выписки из стационара больные становятся на учет врача-инфекциониста поликлиники. В амбулаторный период наблюдения рекомендации по режиму учитывают индивидуальные особенности жизнедеятельности пациента. Во всех случаях рекомендуется ограничивать активные занятия спортом (для учащихся — освобождение от физкультуры), избегать работы в ночную смену, ограничить трудоемкую физическую работу (с переводом на легкие виды труда). Исключаются виды спорта и физические упражнения, предусматривающие длительные или резкие усилия. Физзарядка также не должна вызывать чувство усталости и продолжаться не более 10 минут. Не рекомендуется подъем тяжестей свыше 3 кг и длительная физическая нагрузка — пешие прогулки не более одного часа в день или не более 2 км. Занятия спортом после перенесенного гепатита разрешаются врачом при наличии нормальных клинико-лабораторных показателей не ранее чем через три месяца.
Нежелательными являются длительные командировки, изменение климатического пояса, требующее адаптации. Ограничиваются посещение бани, сауны, загорание на пляже и в соляриях. Неблагоприятными факторами также являются длительное вождение автомобиля, психоэмоциональные нагрузки, длительная работа на компьютере.
Вопрос возобновления половой жизни решается индивидуально с учетом наличия или отсутствия вируса в крови и динамики нормализации лабораторных показателей.
Следует подчеркнуть, что нарушение режима, особенно в амбулаторный период, нередко лежит в основе клинико-лабораторных обострений ВГ и способствует, в ряде случаев, формированию хронической патологии печени.
Диета при ВГ, как острых, так и хронических, в базисной терапии занимает важное место. Регулярность приема пищи, качество продуктов, их пищевая полноценность и щадящий характер являются основой питания при заболеваниях печени. В медицинской практике эта диета обозначается как стол № 5 или 5а. Если в условиях стационара вопрос о питании больных ВГ решается путем применения соответствующей нормативной документации на пищеблоках, то при курации больных в амбулаторных условиях и домашнем питании необходимо как можно подробнее обсудить с пациентом основные принципы и регулярность лечебного питания, ассортимент продуктов и примерный перечень блюд.
Необходимо принимать пищу в строго определенные часы и не реже 4–5 раз в сутки (1-й и 2-й завтраки, обед, полдник и ужин).
Следует избегать употребления продуктов, оказывающих сильное раздражающее действие на слизистую оболочку желудка, двенадцатиперстной кишки и верхних отделов тонкой кишки: приправы и пряности, копчености, блюда, содержащие уксус, овощи, богатые эфирными маслами, — редис, лук, чеснок, редька, щавель и др., а также продуктов, содержащих тугоплавкие жиры (бараний, гусиный, свиной и т. д.).
Ограничивается употребление томатов, кислой квашеной капусты. Исключаются: грибы (в любом виде), горох и фасоль (т. к. возможно повышенное газообразование!), однако допускается употребление небольшого количества зеленого консервированного горошка в качестве добавки к салатам, супам и т. д. Не следует есть сырые незрелые и кислые сорта ягод и фруктов (кислые, зеленые яблоки, красная смородина, клюква и т. п.).
Разрешается небольшое количество зелени укропа и петрушки, тмин, лавровый лист.
Не рекомендуется употреблять практически любые пищевые продукты, предназначенные для длительного хранения (содержащие консерванты, концентраты, вкусовые добавки): консервы, сублимированные продукты, супы и бульоны быстрого приготовления, концентрированные и сухие соки и напитки, кондитерские изделия, рассчитанные на длительное хранение.
Из питания исключаются:
-
шоколад и его производные, кондитерские изделия, содержащие кремы (торты, пирожные, мороженное);
-
изделия из слоеного и сдобного теста;
-
все виды кофе, крепкий чай, какао;
-
алкоголь в любом виде;
-
майонезы, кетчупы, острые соусы, уксус и маринованные продукты, все виды перца, горчица, хрен.
Из продуктов животного происхождения исключаются жирные сорта мяса, птицы и рыбы; печень, почки и др. субпродукты; сало, шпик, корейка, грудинка и т. д., копченая птица, балыки, острая, соленая рыба, морепродукты, крабы, раки.
При приготовлении пищи рекомендуется исключить крепкие мясные, рыбные и овощные бульоны, для чего при варке продуктов, доведя их до кипения, первый бульон следует слить, залить новой порцией воды и варить до готовности.
Запрещаются жареные блюда. Продукты рекомендуется готовить на пару, отваривать или запекать в духовом шкафу после варки, не допуская образования пригорелой корочки.
Полезно приготовление блюд из фарша, дважды пропущенного через мясорубку — это уменьшает механическую нагрузку на желудок и способствует более полноценному перевариванию пищи.
Следует ограничить количество употребляемых яиц до трех в неделю, причем желательно использовать их для приготовления блюд, а не употреблять их целиком или в сыром виде.
Из молочных продуктов необходимо исключить цельное молоко и острые сорта сыра. Ограничивается прием сметаны, творожных сырков, жирного творога, ряженки, йогурта. Желательно использование молочных продуктов пониженной жирности.
Рекомендуется употребление кисломолочных продуктов: кефир, бифидок, бифидум-кефир, бифилайф, ацидофилин и др. Вместе с тем следует учитывать индивидуальную переносимость и в случае появления метеоризма (повышение бродильных процессов и газообразования), болей в животе, жидкого стула, тошноты или других симптомов употребление этих продуктов следует уменьшить или прекратить.
При заболеваниях печени необходимо ограничить употребление соли и соленых продуктов.
При ОВГ или в периоды обострения хронических заболеваний печени рекомендуем обязательную механическую обработку (протертые, мелкорубленые или дважды пропущенные через мясорубку продукты) и строгое соблюдение графика дробного приема пищи.
Питание должно быть обязательно разнообразным — не следует устраивать разгрузочные дни. При расширении ассортимента питания следует вводить новый продукт небольшими порциями и не больше одного продукта в день — при появлении дискомфорта нетрудно будет определить его причину и исключить неподходящий продукт.
Хлеб. Черный и белый, хорошо пропеченный, без подгорелых корок, «вчерашний», не более 500 г в сутки. Сухарики (сушеные, а не жареные!) сухое печенье, сухой бисквит.
Супы. Овощные, рыбные, мясные (на слабом бульоне) с добавлением различных круп и овощей. Молочные и фруктовые супы, борщи, щи.
Блюда из мяса, птицы, рыбы. Нежирные сорта говядины, телятины, кролик, курица, индейка. Изредка — мясная (постная) свинина. Мясо, очищенное от пленок, сухожилий и жира, без костей. Птица без кожи. Порции куском, или рубленые, или в виде фарша, в отварном или паровом виде, можно с последующим запеканием их в духовом шкафу. Колбасы: молочная, докторская, диетическая. Сосиски молочные. Рыба нежирных сортов: судак, треска, окунь, лещ, хек и т. д. — отварная, запеченная, заливная, куском или в виде фарша.
Блюда из овощей. Картофель, свекла, морковь, тыква, белокочанная капуста, кабачки, огурцы, помидоры (в ограниченном количестве). Лучше избегать применения томатной пасты. Овощи в вареном, запеченном и сыром виде. Самостоятельно и в виде гарниров.
Фрукты и ягоды. Яблоки не кислые (лучше запеченные), груши, абрикосы, персики, бананы (лучше перезревшие), киви, хурма, айва, сливы, вишня, чернослив, инжир, финики, курага (лучше в составе компота), урюк, изюм, гранаты, арбузы, дыни, клубника, смородина, виноград, черника. Полезно небольшое количество орехов (кроме арахиса) в натуральном виде, очень тщательно очищенных и измельченных. Употреблять фрукты и ягоды можно в натуральном виде и в виде компотов, киселей, желе, разбавленных соков.
Крупы и макаронные изделия. Различные каши на воде или разбавленном наполовину молоке (цельном, сухом, сгущенном), отварные или приготовленные на пару (водяная баня), запеченные. Мелкие макаронные изделия, вермишель или рубленые макароны и т. п. — отварные, запеченные.
Сладкие блюда. Сахар, немного меда (1–2 чайных ложки в день — если нет предрасположенности к аллергии!), мармелад, зефир, пастила, карамель, ирис, варенье, джемы. Количество сахара (и сахарсодержащих продуктов) следует по возможности ограничивать или частично заменить ксилитом или сорбитом.
Закуски. Заливные рыба, язык, нежирное мясо, отварная курица (все без специй). Холодец и студень не рекомендуется. Нежирная ветчина, вымоченная сельдь, черная икра в ограниченном количестве, неострые сыры, салаты из сырых и вареных овощей с растительным маслом или сметаной (заправку сметаной не выше 10% жирности ограничивать до 1–2 раз в неделю).
Масло. Сливочное масло не более 40 г в сутки, используя его в приготовлении пищи. Подсолнечное рафинированное, салатное, кукурузное, кубанское, оливковое и др. могут использоваться для приготовления блюд и заправок.
Напитки. Объем жидкости не должен превышать 2–2,5 литра в сутки, включая первые блюда. Чай не крепкий, фруктовые, ягодные, овощные соки свежеприготовленные и обязательно разбавленные кипяченой водой в соотношении 1:2, компоты, кисели домашнего приготовления. Очень полезен настой шиповника. Минеральные воды (2–3 стакана в день, не чаще 3 раз в неделю) комнатной температуры, без газа. Не рекомендуется пить воду и другие напитки охлажденными. Не следует пить всевозможные газированные (фруктовые) напитки и консервированные фруктовые напитки. Натуральные соки (предпочтительно нектары) следует разводить кипяченой водой.
Базисная терапия ОВГ включает в себя дезинтоксикационную терапию и применение энтеросорбентов. При легкой и среднетяжелой формах ОВГ дезинтоксикация может проводиться перорально — для этого суточный объем жидкости увеличивается на 1–1,5 литра за счет приема минеральной воды. При наличии тошноты и тем более рвоты (в острый период гепатита) проводят парентеральную (внутривенную) дезинтоксикационную терапию в объеме 800–1200 мл в сутки. В качестве инфузионных растворов применяют 5% раствор глюкозы, физиологический раствор, Плазмалит, Гемодез и его аналоги, кристаллоидные растворы. Во всех случая проведения дезинтоксикационной терапии следует контролировать диурез. При тяжелых формах ОВГ и особенно при развитии острой печеночной энцефалопатии применяют методы форсированного диуреза с увеличением объема вводимой жидкости до 2–2,5 л в сутки. В тех же ситуациях используют плазмоферез.
В настоящее время имеется обширный арсенал энтеросорбентов — препаратов, способных связывать и выводить токсины из организма: Фильтрум-СТИ, Лактофильтрум, Полифепан, Энтеросгель, Нормазе, Дюфалак и др.
В патогенетическую терапию ВГ могут быть включены также и другие препараты гепатопротективного действия: Гептрал, Рибоксин, Тыквеол, Хофитол, Дипана, Фосфоглив, Карсил, Легалон и др. Могут применяться препараты группы глутоксима, избирательно действующие на вируспораженные и непораженные клетки и регулирующие процессы тиолового обмена (Глутоксим, Моликсан и др.).
В случаях тяжелого течения ОВГ к терапии добавляют глюкокортикоиды (преднизолон 60–90 мг per os в сутки или 240–300 мг внутривенно), белковые препараты (альбумин, плазма), аминокислотные смеси (Гепастерил А и Б, Гепасол А, Аминостерил Н-Гепа и др.), противогеморрагические средства (Викасол, Дицинон, Аминокапроновую кислоту и др.), ингибиторы протеаз (Контрикал, Гордокс и аналоги), энтеросорбенты, среди которых наиболее предпочтительным является Дюфалак. Эффективным методом терапии тяжелых форм остается плазмоферез. Наряду с общепринятой базисной терапией возможно назначение этиотропного лечения — индукторов интерферонов и иммуномодуляторов (Амиксин, Неовир, Циклоферон, Имунофан, Полиоксидоний и др.).
При развитии холестатического варианта течения назначают Урсофальк (урсодеоксихолевая кислота) по 10–15 мг/кг массы тела в сутки один раз вечером в течение 15–30 дней, энтеросорбенты (Полифепан, Энтеросгель и т. п.), в ряде случаев наблюдается положительный эффект при проведении неоднократных дуоденальных зондирований, ГБО, ингаляционного введения гепарина в сочетании с лазерной терапией, сеансов плазмафереза.
Учитывая тот факт, что при патологии печени всегда имеются различной степени выраженности нарушения микрофлоры кишечника, рекомендуется назначение бактерийных препаратов, нормализующих микрофлору кишечника: Бифидумбактерин и его комбинации, Лактобактерин, Хилак форте и пр. В период разрешения холестаза (нормализация цвета стула и мочи) можно рекомендовать желчегонные препараты растительного происхождения.
В терапии острого гепатита С желательно назначение 3–6-месячного курса интерферонов с нуклеозидами по схеме, применяемой для терапии хронического гепатита С. Раннее назначение противовирусных препаратов значительно снижает частоту или даже исключает переход острого гепатита в затяжной и хронический. Представляется обоснованным также назначение в начальном периоде острого гепатита С препаратов, обладающих определенной противовирусной активностью (препараты глицирризиновой кислоты — Виусид, Фосфоглив, лекарственные средства группы амантадинов — Ремантадин, ПК-Мерц и др.).
Лечение обострений ОВГ, протекающих с аутоиммунным компонентом, предусматривает назначение глюкокортикоидов. В этом случае используется иммунодепрессивный эффект препаратов гормонов коры надпочечников.
Хронические вирусные гепатиты (ХВГ)
При ХВГ соблюдаются те же основные принципы терапии, что и при ОВГ: режим и диета являются обязательными компонентами терапии.
Лечение ХВГ, как правило, проводится в амбулаторных условиях, требует индивидуального подхода и включает в себя ряд аспектов, среди которых следует выделить в первую очередь деонтологический. Так, больные хроническими гепатитами С должны быть обязательно подробно информированы по определенному кругу вопросов, связанных с их заболеванием, в частности, касательно особенностей клинического течения, правил поведения больного в быту, санитарно-эпидемиологического характера, возможных исходов, использования терапевтических мероприятий и средств, в том числе специфических противовирусных препаратов и связанных с этим сложностей и проблем (длительность и дороговизна терапии, нежелательные побочные проявления, ожидаемая эффективность лечения). Результатом такого собеседования врача с пациентом должно быть осознанное желание пациента лечиться, а также оптимистическое отношение к предстоящей длительной и упорной терапии.
В настоящее время в мировой практике используется целый ряд медикаментозных средств, противовирусная активность которых в той или иной степени доказана.
Первую и основную группу противовирусных препаратов, применяемых для лечения хронического гепатита С (ХГС), составляют альфа-интерфероны (рекомбинантные и природные) — такие как: Интерферон лейкоцитарный человеческий, Альфаферон, Вэллферон, Виферон, Реаферон, Роферон-А, Интрон А, Интераль, Реальдирон, Альтевир, Альфарона, Эберон альфа Р и др. (табл. 1). Считается, что их противовирусное действие основано на торможении вирусной репродукции и стимуляции многих факторов иммунной системы организма.
Вторую группу противовирусных средств составляют ингибиторы обратной транскриптазы и, в частности, аналоги нуклеозидов (ламивудин, ацикловир, рибавирин (Копегус, Рибамидил, Ребетол, Веро-Рибавирин), видарабин, лобукавир, соривудин и др.), блокирующие синтез вирусных ДНК и РНК путем замены собой натуральных нуклеозидов и тем самым тормозящие репликацию вируса (табл. 2).
Третья серия препаратов представлена интерфероногенами (Циклоферон, Неовир, Амиксин и др.), механизм действия которых заключается в индукции выработки макроорганизмом дополнительных количеств своих собственных интерферонов (табл. 4). Противовирусным эффектом обладают также препараты группы амантадинов (Ремантадин, ПК-Мерц и др.).
Несомненно, полезными в комплексной терапии хронических гепатитов являются гепатопротекторы, применение которых, с одной стороны, способствует восстановлению нарушенных структур и функций печени, с другой стороны, предотвращает возможное токсическое действие мощных противовирусных препаратов (табл. 3).
Лечение любого заболевания и особенно хронической формы гепатита С требует исключительно индивидуального подхода, поскольку характер патологического процесса у каждого конкретного больного определяется целым рядом составляющих, как то: возраст больного, характер сопутствующей патологии, длительность заболевания, генотип вируса и уровень вирусной нагрузки, переносимость препаратов, наличие и выраженность побочных явлений, связанных с проводимой терапией и, в конце концов (а в ряде случаев и в начале) — с финансовыми возможностями конкретного пациента.
Тем не менее уместно отметить, что первоначально использовавшаяся у больных ХГС монотерапия препаратами интерферона по литературным данным (1999–2000 гг.) — по 3 млн ME 3 раза в неделю в течение 12 месяцев давала положительный результат в 13–48% случаев (имелась в виду нормализация уровня аминотрансфераз и исчезновение PHK HCV в крови по данным ПЦР). Такая разница в результатах зависела от генотипов возбудителей, включались ли в их число и т. н. положительные нестабильные ответы, т. е. новое появление РНК в крови у пациентов в процессе 6–12-месячного наблюдения за ними после завершения курса лечения.
В настоящее время в целях повышения эффективности лечения ХГС применяется комплексная противовирусная терапия — как правило, сочетанное использование альфа-интерферонов и аналогов нуклеозидов (рибавирин (Копегус, Ребетол, Рибамидил), видарабин, лобукавир, соривудин и др.). К примеру, комбинированное применение Интрона А по 3–5 млн ME 3 раза в неделю и рибавирина ежедневно в дозе 1000–1200 мг в течение 12 месяцев позволило получить стабильный, устойчивый ответ у 43% больных, т. е. отсутствие РНК вируса гепатита С в крови, по данным ПЦР в динамике, на протяжении 12 месяцев после прекращения терапии. Вместе с тем следует учитывать, что аналоги нуклеозидов сами по себе обладают целым спектром побочных реакций, проявляющихся при длительном приеме препаратов. Об этих реакциях нуклеозидов также следует предупредить пациента.
Существующие рекомендации по противовирусной терапии предусматривают 2 варианта начальной стадии лечения: ежедневное введение интерферонов в дозе 3–5 млн МЕ в течение 4 недель, затем через день в той же дозировке. Другой вариант — назначение повышенных доз интерферонов 6–10 млн МЕ через день в первый месяц с последующим снижением дозы. Помимо прочих факторов, недостаточно высокий положительный стабильный эффект даже такой комбинированной терапии объяснялся некоторыми авторами тем, что применяемые схемы интерферонотерапии не создавали постоянства терапевтической концентрации активного вещества в крови и в тканях, поскольку период полураспада введенного в организм интерферона составляет 8 часов, в то время как вирусу достаточно в промежутках между инъекциями интерферона всего нескольких часов, чтобы достигнуть вновь своей исходной концентрации. Замена препарата Интрон А в приведенной выше схеме лечения больных ХГС на пэгинтерферон альфа-2а (Пегасис) в дозе 1,5 мкг/кг в виде 1 инъекции в неделю (присоединение к молекуле интерферона полиэтиленгликоля приводит к удлинению периода полураспада активного вещества в организме до 168 часов) позволила авторам получить устойчивый терапевтический ответ в среднем у 72% всех таким образом пролеченных больных, из них у 94% с генотипом возбудителя 2 и 3.
Надо добавить, что оптимистические результаты, полученные при использовании пэгинтерферонов на начальном этапе клинических исследований, в последующем при более широком применении несколько снизили процент положительных результатов, а высокая цена препаратов значительно уменьшила их практическое использование.
Вместе с тем в последнее время появились убедительные данные о том, что положительный эффект от проводимой терапии в большей степени зависит от длительности курса, а не от дозировки интерферонов. Показана эффективность и от схем, постепенно увеличивающих дозу интерферонов после получения отрицательного результата ПЦР на РНК HCV.
Общепринятое стандартное лечение ХГС препаратами интерферона и аналогами нуклеозидов должно быть дополнено терапией сопровождения, включающей различные группы препаратов.
Патогенетически обоснованным в терапии ХГС является применение иммуномодулирующих препаратов — интерлейкинов (ИЛ). Интерлейкин-1 бета (Беталейкин) перестраивает иммунопоэз, активирует нейроэндокринную систему, стимулирует костно-мозговое кроветворение, активируя нейтрофильные гранулоциты, пролиферативную и функциональную активность Т- и В-лимфоцитов. Он также индуцирует синтез ростовых факторов и ряда цитокинов, таких как ИЛ-2 и ИЛ-4, усиливает экспрессию их рецепторов и вызывает повышение содержания эндогенного интерферона альфа, а также подавляет внутриклеточную репликацию вируса гепатита С.
Наиболее перспективным в настоящее время представляется применение Беталейкина в комплексе с интерферонами и аналогами нуклеозидов.
Лечение гепатита С является довольно сложным мероприятием, поэтому при назначении и проведении специфической терапии уместно руководствоваться следующими принципами:
-
Необходимо проводить терапию у врача, имеющего достаточный практический опыт ведения таких больных.
-
Лечение предпринимается только при условии обнаружения РНК вируса в крови по данным ПЦР, определения его генотипа и уровня виремии (количественным или полуколичественным методом — титр).
-
Провести комплексное лабораторное обследование — развернутый анализ периферической крови, возможно полный спектр функциональных проб печени и другие биохимические исследования: сахар крови, амилаза, железо и пр. при необходимости в каждом конкретном случае. Желательны, кроме того, определение естественного интерферонового уровня у больного, исследование чувствительности к интерферонам и индукторам интерферонов, а также морфофункциональное состояние щитовидной железы.
-
Оценить характер сопутствующей патологии, например: почечной с нарушением выделительной функции, сердечно-сосудистой, аутоиммунных заболеваний, патологии щитовидной железы, психических заболеваний, выраженных отклонений со стороны периферической крови (анемия, тромбоцитопения, лейкопения) и пр., что может явиться даже противопоказанием для планируемого противовирусного лечения.
-
Специфическая терапия запрещается во время беременности и кормления ребенка грудным молоком.
-
Подлежат лечению как острые (и даже предпочтительно), так и хронические формы вирусного гепатита С, включая и те, когда при наличии в крови РНК возбудителя регистрируется стабильно нормальный уровень аминотрансфераз.
-
Рекомендуется комбинированное (одновременно 2–3 и более препаратов) использование противовирусных средств.
-
Учитывая возможность развития толерантности к применяемым медикаментам, образования к ним антител, время от времени на определенных этапах лечения желательно изменять комбинации лечебных средств.
-
Эффективность лечения больше зависит от длительности его проведения, чем от дозы препарата (в зависимости от конкретных особенностей пациента продолжительность лечения колеблется от 6 до 18 месяцев, в среднем — 12 месяцев).
-
В случаях гепатита С, вызванного генотипами 1а и 1b, а также при длительности процесса более 3 лет и при повторных курсах противовирусной терапии продолжительность лечения должна быть не менее 12 месяцев (а чаще и более), при этом терапия усиливается на последнем этапе.
-
Обязателен ежемесячный, а при необходимости и более частый контроль клинико-лабораторных данных, в том числе развернутого анализа периферической крови в целях коррекции возможных побочных, нежелательных эффектов.
-
Следует помнить и информировать пациента о том, что при проведении терапии возможны ознобы, лихорадка, миальгии, аллергические и токсико-аллергические явления, анорексия, депрессии, тиреоидиты, облысение, анемия, лейкопения, тромбоцитопения, агранулоцитоз и пр.
A priori надо ожидать меньшую эффективность лечения гепатита С, а подчас ее полное отсутствие в следующих случаях: у лиц с иммуносупрессией различного происхождения, у пациентов с ожирением, при сочетанном хроническом процессе, вызванном вирусами гепатитов С (могут, в частности, одновременно идентифицироваться разные его генотипы), В и D, у больных с генотипом вируса 1а и 1b, в случаях высокой концентрации HCV-PHK в крови, при большой длительности хронического процесса (многие годы. Напротив, замечено, что терапия наиболее эффективна с длительностью хронического процесса до 2 лет), у пациентов, где хронический гепатит С протекает с элементами цирроза печени, при наличии аутоиммунных заболеваний, в случаях, когда терапия протекает на фоне приема алкоголя и наркотических средств, а также когда лечение производится лишь у одного из двух половых партнеров, больных вирусным гепатитом С (возможность реинфицирования вирусом того же генотипа).
Среди побочных реакций со стороны крови, сопровождающих длительную противовирусную терапию, часто отмечаются анемия, лейко- и тромбоцитопения. Коррекция анемии может успешно проводится препаратами, стимулирующими эритропоэз, например Эпокрином. При лейкопении можно рекомендовать назначение Беталейкина (рекомбинантного Интерлейкина-1 бета).
Следует отметить, что в настоящее время активно изучаются возможности использования других препаратов противовирусного действия, способных заменить интерфероны. Противовирусное действие продемонстрировано у препаратов, содержащих соли глицирризиновой кислоты, получаемых из корня солодки, — Фосфоглив, Виусид и др. (табл. 3).
Противовирусное лечение хронического гепатита В показано лицам с активностью инфекционного процесса — при наличии в крови DNA HBV. Применяют препараты интерферона-альфа совместно с нуклеозидами: интерфероны 3–5 млн МЕ 3 раза в неделю внутримышечно или подкожно (Пегасис по 180 мкг 1 раз в неделю) в сочетании с Зеффиксом ежедневно по 100 мг перорально (табл. 1, табл. 2). Возможно применение только Зеффикса в дозе 100 мг перорально. В то же время известно, что монотерапия Зеффиксом относительно быстро приводит к формированию мутаций в геноме HBV и потере контроля над репликацией. В среднем курс такой терапии проводится в течение 12 месяцев. При формировании устойчивости к ламивудину (Зеффикс) показано назначение энтекавира (Бараклюд) в дозе 1 мг ежедневно (табл. 2). Бараклюд эффективен и против «дикого» штамма вируса в дозе 0,5 мг. В отличие от аналогов нуклеозидов пегелированные интерфероны не вызывают мутации вируса и одинаково эффективны как в виде монотерапии, так и в комбинации с аналогами нуклеозидов. Терапия может быть дополнена назначением индукторов интерферона, иммуностимуляторов типа Тактивина, Неоминофагена С, Имунофана и пр. (табл. 4). Лечение проводится под ежемесячным контролем функциональных проб печени, клинического анализа крови, вирусной нагрузки.
Интегративные формы (HBe-негативные) ХГВ характеризующиеся, как правило, нормальными или невысокими уровнями активности трасфераз (АЛТ/АСТ) и низкой концентрацией ДНК ГВ (или отсутствием ДНК), противовирусной терапии не подлежат. В этих случаях задачей терапии является проведение комплекса мер, ограничивающих либо исключающих возможность обострений заболевания, таких как: соблюдение диеты, режима, использование гепатопротекторов (табл. 3).
Необходимо иметь в виду, что, помимо высокой стоимости, лечение является достаточно агрессивным, сопровождается целым рядом побочных эффектов, требующих коррекции, и, к сожалению, при этом далеко не у всех пациентов дает стабильный положительный результат, т. е. постоянно нормальные уровни АЛТ, сероконверсию HBe — anti-HBe, исчезновение HBsAg, неоднократные отрицательные результаты определения ДНК вируса в течение года от момента прекращения терапии.
Практически абсолютным противопоказанием для противовирусной терапии ХГВ является наличие у больного сопутствующих аутоиммунных заболеваний, заболеваний системы крови, алкоголизм, беременность.
Следует подчеркнуть, что лечение ХГВ должно проводиться врачом, имеющим достаточный практический опыт ведения таких больных.
К сожалению, в настоящее время эффективной специфической терапии хронических форм HDV-инфекции пока не существует. Имеются отдельные сообщения об эффективности использования в этих случаях высоких доз интерферонов — 10 и более млн МЕ в сутки.
Наконец, следует остановиться на стоимости «лекарственной корзины». Практический врач не может не учитывать экономической составляющей противовирусной терапии, поскольку используемые как отечественные, так и зарубежные противовирусные средства в России пока не входят в реестр медикаментов, предоставляемых бесплатно. Представляется очевидным, что основная масса пациентов просто не в состоянии приобретать дорогостоящие зарубежные препараты на полный курс. В этой связи практическую значимость приобретает изучение и обобщение опыта работы с отечественными противовирусными препаратами как наиболее доступными и достаточно эффективными.
C. Н. Жаров, доктор медицинских наук, профессор Б. И. Санин, кандидат медицинских наук, доцент РГМУ, Москва
Таблица 1. Препараты группы интерферона для лечения ВГ
Таблица 2. Препараты из группы синтетических аналогов нуклеозидов для лечения ВГ
Таблица 3. Препараты из группы гепатопротекторов для лечения ВГ
Таблица 4. Препараты с иммуномодулирующей, противовирусной и интерфероногенной активностью для лечения ВГ