Дата публикации 28 марта 2023Обновлено 10 мая 2023
Определение болезни. Причины заболевания
Пролежни (Pressure sores) — это язвенно-некротическое повреждение кожи, которое возникает у лежачих пациентов и вызвано нарушением кровообращения в областях, подверженных длительному давлению, трению или сдвигу тканей [1].
Распространённость
Пролежни очень распространены и возникают примерно у 15 % госпитализированных пациентов, чаще в отделениях интенсивной терапии [8]. Однако эта патология развивается в 2–3 раза реже, если за больным ухаживают специально обученные санитарки и сиделки [12].
Причины пролежней
Пролежни развиваются из-за сдавления кожи между двумя точками — как правило, между поверхностью кровати и костными выступами. Наибольшее давление возникает в области пяток, крестца, затылка, локтей, вертелов бедренных костей (бугорков бедренной кости вблизи сочленения с тазобедренной костью) [3][6][10].
Основная причина развития пролежней — это ограничение подвижности при параличе, коме, травмах и заболеваниях спинного мозга, онкологических болезнях, длительном периоде после операции, продолжительном пребывании в реанимации или отделении интенсивной терапии [2][5].
Можно выделить внутренние и внешние, а также на обратимые и необратимые факторы риска развития пролежней.
Обратимые внутренние факторы:
- истощение и обезвоживание;
- ожирение;
- снижение или отсутствие активных движений;
- нарушение психомоторной активности (двигательное беспокойство, апатия, возбуждение или бессонница);
- анемия;
- сердечная недостаточность;
- пониженное артериальное давление;
- недержание мочи или кала;
- нарушение периферического кровообращения по артериям или венам, например при сахарном диабете;
- болевой синдром;
- курение.
Необратимые внутренние факторы:
- пожилой или старческий возраст;
- тяжёлое состояние организма;
- сухая, истончённая, легко травмируемая или повреждённая кожа;
- нарушения нервной системы (чувствительности или движений);
- патологические состояния сознания — спутанность, оглушение, сопор, кома.
Обратимые внешние факторы:
- недостаточный гигиенический уход — кожа становится более уязвимой при длительном воздействии мочи и стула;
- неподходящие способы и средства ухода — перцовые пластыри, йодные «сетки», пиявки и другие подобные методы;
- неправильная методика массажа и использование масел и средств, содержащих вредные или прижигающие компоненты;
- складки на постельном белье или одежде пациента;
- недостаток в организме белков и/или аскорбиновой кислоты при плохом аппетите, диетах или нарушенном режиме питания;
- действие некоторых цитостатических препаратов, гормонов и нестероидных противовоспалительных средств;
- отсутствие поручней у кровати (некоторые пациенты пытаются приподняться или повернуться, но не могут это сделать без опоры на поручни);
- несоблюдение правил нахождения, расположения и передвижения пациента на кушетке, кровати или в кресле;
- неправильное использование противопролежневых подушек, матрасов и прокладок;
- перегрев, переохлаждение, избыточная влажность или сухость кожи.
Необратимые внешние факторы риска:
- предшествующая операция, которая длилась больше двух часов;
- обширные травмы позвонков, костей малого и большого таза, органов брюшной полости;
- травмы и повреждения головного и/или спинного мозга.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы пролежней
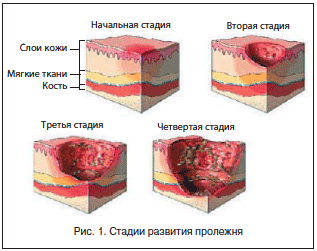
Клинические проявления пролежней зависят от стадии развития [1].
Всего выделяют четыре стадии:
- Бледность или устойчивое покраснение кожи, которое сохраняется после прекращения сдавления.
- Устойчивый синюшно-красноватый оттенок отграниченного участка кожи. На этой стадии поверхностный слой кожи отслаивается и появляются неглубокие повреждения (язвы, натёртости или пузыри с жидкостью), которые могут распространяться на подкожно-жировую клетчатку.
- Разрушение кожи (некроз), которое распространяется до мышечного слоя — на дне язв можно увидеть мышечную ткань, язвы могут проникать и в сами мышцы. Могут быть жидкие выделения из области пролежня.
- Некроз всех слоёв мягких тканей — развивается полость или кратер, в котором можно увидеть фрагменты сухожилий или даже костей.
Длительность каждой стадии варьирует от нескольких дней до нескольких недель и зависит от положения пациента, отягощающих факторов и особенностей ухода.
Патогенез пролежней
На развитие пролежней влияет множество факторов: длительное механическое давление на кожу и ткани, нарушение кровоснабжения, инфекция и недостаток питательных веществ.
Пролежни обычно развиваются в области костных выступов: лопаток, локтей, ягодиц, крестца, кистей, лодыжек и пяток. Из-за продолжительного давления в этих областях нарушается кровоснабжение тканей и возникает дефицит кислорода. Мышечные волокна более чувствительны к нехватке кислорода, чем кожа, из-за чего изменения развиваются прежде всего в мышечном слое над костным выступом [1].
Длительное давление (больше 1–2 часов) ведёт к закупорке крупных кровеносных артерий и вен, сдавливанию нервных стволов и мягких тканей, что усугубляет уже имеющееся нарушение кровотока в мелких сосудах тканей. В результате развиваются дистрофические процессы, которые в дальнейшем распространяются по направлению к коже.
Повреждение мягких тканей может возникать при соприкосновении кожи со швами на одежде, складками на постельном белье и крошками. Также важную роль в образовании язв играют силы смещения давления, например при поднятом изголовье кровати, когда больной сползает вниз, давление перемещается на крестец и глубокую фасцию. В результате мышцы и глубоколежащие ткани смещаются вниз под действием силы тяжести, в то время как кожа остаётся неподвижной [3]. Длительное давление, действие сил смещения и трения, а также мокнутие и попадание бактерий в повреждённую кожу приводит к развитию пролежневых язв [2].
Ещё один важный фактор в развитии пролежней — это нехватка белка в организме, что способствует появлению отёка и снижению тургора, или эластичности, мягких тканей.
Классификация и стадии развития пролежней
Существует несколько классификаций пролежней.
По глубине поражения:
- поверхностные пролежни — вызваны локальным воздействием на кожу;
- глубокие — изменены лежащие глубже ткани; такие пролежни могут долго не диагностироваться, пока не достигнут поверхностных слоёв кожи [4].
В зависимости от причины поражения:
- экзогенные пролежни — возникают от непосредственного физического воздействия в области костных выступов или инородных предметов, например мочевых катетеров или гипсовых повязок;
- эндогенные — вызваны поражением нервной системы, приводящей к нарушению обменных процессов и микроциркуляции в тканях, часто возникают из-за поражения головного или спинного мозга.
Стадии развития пролежней
В российской литературе и клинической медицине долго использовалась классификация пролежней В. П. Балича и О. Г. Когана.
В ней выделяется пять последовательных этапов развития патологии:
- Поверхностный пролежень, т. е. поражающий поверхностные ткани.
- Глубокий пролежень с поражением мышц.
- Глубокий пролежень с боковыми карманами.
- Глубокий пролежень, который распространяется до костной ткани и приводит к развитию остеомиелита.
- Пролежень рубцовой ткани [3].
Профессор М. Д. Дибиров выделяет три стадии пролежневого процесса:
- В мелких сосудах в месте сдавливания нарушается кровообращение, из-за чего кожа сначала бледнеет, затем краснеет, а потом становится синеватого оттенка.
- Возникает некроз (омертвение ткани), появляется поверхностная рана или глубокая язва, может отделяться гной. Некроз может поражать кожу, подкожно-жировую клетчатку и мышцы, а также распространяться на суставы и кости, что приводит к развитию артрита и остеомиелита. Поверхность пролежня может быть как сухой с чёткими краями, так и с нечёткими и гнойным отделяемым — это признак того, что поражение распространяется на окружающие ткани.
- Происходит заживление тканей. Явы или поверхностные раны затягиваются, кожа восстанавливается и/или в области пролежня формируется рубцовая ткань [3][4].
Осложнения пролежней
При неэффективности или отсутствии лечения пролежни прогрессируют и могут появиться осложнения. Крайне опасным из них является сепсис — распространение инфекции по организму. При этом часто выявляют гнилостную и/или неклостридиальную инфекцию, поражающую мягкие ткани (например, некротизирующие формы целлюлита, фасциита и миозита) [4].
Также пролежни могут осложниться:
- флегмоной — воспалением мягких тканей, не имеющим чётких границ;
- абсцессом — чётко отграниченным воспалением;
- гнойным тендовагинитом — воспалением по ходу сухожилий;
- артритом — воспалением суставов;
- остеомиелитом — воспалением костей.
Диагностика пролежней
При диагностике пролежней обычно проводится сбор анамнеза (истории болезни), жалоб и осмотр. Дополнительно могут применяться лабораторные и инструментальные методы, но они используются гораздо реже: клиническая картина часто однозначна и врач уже при осмотре может поставить диагноз.
Пролежни часто появляются в местах контакта костных выступов с твёрдой поверхностью: в области затылка, ушей, грудного отдела позвоночника, рёбер, локтей, крестца, таза, бёдер, голеней и пяток [1]. Реже пролежни появляются в области сосцевидного отростка (который расположен позади уха), лопаток и пальцев стоп. При длительном вынужденном положении, например после инсульта, обширных травм или при сдавлении гипсовыми повязками и медицинскими шинами, пролежни могут появляться в нехарактерных местах, например на боковых поверхностях стоп или тыльной стороне пальцев руки и ног.
Лабораторная диагностика
При выявлении в анализе крови агранулоцитоза (выраженного снижения уровня лейкоцитов) обязательно проводится бактериологическое подтверждение заболевания, даже если нет видимых симптомов воспаления. Для этого у пациента берут мазок или делают пункцию раневой поверхности. При исследовании выделяют и высеивают инородную или условно-патогенную микрофлору (в норме она не вызывает болезни и проявляется только при ослабленной иммунной системе).
Дифференциальная диагностика
Пролежни следует отличать от контактного дерматита, связанного с местной реакцией на недержание мочи или кала [1]. Пролежни в основном развиваются из-за сдавления между костным выступом и твёрдой поверхностью, а контактный дерматит может появляться в тканях, не сдавливаемых извне.
Лечение пролежней
Лечение пролежней комплексное: нужно исключить длительное сдавливание, восстановить кровоснабжение, проводить местное лечение язв и терапию основного заболевания.
Также очень важен адекватный уход:
- соблюдение асептики (инфицирование пролежней сильно замедляет заживление);
- соблюдение правил гигиены;
- периодическое изменение положения больного;
- использование противопролежневых матрасов или специализированных кроватей;
- контроль за повреждающими поверхностями вокруг пролежня (например, швами на белье);
- наложение защитных повязок и послеоперационных наклеек;
- адекватное питание с достаточным количеством белка и необходимых витаминов.
На первой и второй стадии пролежневого процесса нужно исключить сдавление тканей, восстановить и улучшить кровоснабжение. Для этого применяются антикоагулянтные препараты, которые уменьшают свёртываемость крови. Их используют как в виде уколов или капельниц, так и в мазях или гелях [7]. На этих стадиях важно защитить рану от патогенных микробов с помощью тканевых или марлевых повязок, специальных пластырей и плёнок, а также исключить другие опасные факторы (например, соблюдать гигиену при недержании мочи и кала).
Кроме того, необходимо лечить сопутствующие заболевания, которые могут приводить к появлению и развитию пролежней. Среди таких болезней особенно выделяют сахарный диабет (проводится терапия инсулином или гипогликемическими препаратами в таблетках и контроль сахара в крови) и заболевания, связанные с закупоркой или сужением артериальных сосудов. Также необходимо проводить своевременное и эффективное обезболивание, контролировать водно-солевой баланс, корректировать нарушение кровообращения в мелких сосудах.
На третьей и четвёртой стадиях пролежневого процесса погибшие ткани иссекают и удаляют, проводят местное лечение пролежневых язв и стимулируют процессы восстановления тканей.
К безоперационным методам лечения относятся:
- очищение раны;
- стимуляция роста грануляционной ткани, например методом гипербарической оксигенации — пациент находится в специальной камере с повышенным атмосферным давлением и вдыхает 100%-й кислород;
- наложение повязки или наклейки для защиты ткани от высыхания и развития в ней инфекции.
При хирургическом лечении проводится иссечение и удаление омертвевших тканей. Также применяют методы для защиты обнажённых тканей, например частичную трансплантацию кожного лоскута. На третьей и четвёртой стадии важно удалить омертвевшие ткани, очистить язву от гноя (в том числе вскрыть гнойные затёки и карманы) и остатков погибших тканей и защитить заживающую рану от высыхания. Чтобы оперативное лечение было эффективным, на стадии воспаления проводится санация области пролежня местными средствами, в том числе антисептиками.
Послеоперационные осложнения подразделяются на ранние и поздние.
Ранние осложнения:
- накопление жидкости под кожным лоскутом, закрывающим пролежневый дефект;
- несостоятельность послеоперационных швов и расхождение краёв раны;
- некроз краёв кожного лоскута;
- формирование гнойного отделяемого с расплавлением стенки сосуда.
К поздним осложнениям относится формирование свища с образованием полости и повторное развитие пролежня. Причиной этих осложнений может стать как недостаточный послеоперационный уход, так и неэффективная или неудавшаяся операция [4].
Прогноз. Профилактика
При поверхностных, вызванных внешними факторами пролежнях прогноз, как правило, благоприятный: после прекращения давления на ткани и лечения кожа достаточно быстро восстанавливается. Более непредсказуемы внутренние, или глубокие, пролежни, так как они могут сопровождаться опасными для жизни повреждениями стенок сосудов и полых органов. При пролежнях, вызванных поражением нервной системы, прогноз неблагоприятный: пациенты уже страдают тяжёлым основным заболеванием, которое ещё и усугубляется гнойно-некротическим процессом, что снижает шансы на положительный результат.
Профилактика пролежней
Мероприятия по предотвращению развития пролежней проводят медсёстры, которые обладают необходимыми знаниями и навыками, или люди, которые ухаживают за пациентом, например родственники [9].
Чтобы предупредить развитие пролежней, следует:
- Своевременно оценивать риск развития пролежней. Часто к медицинской карте пациента прикладывается или ведётся на компьютере журнал, в котором медсёстры ежедневно оценивают риск развития пролежней или динамику их состояния.
- Уменьшить механические воздействия — трение, давление и силу смещения в области костных выступов, а также в участках, наиболее подверженных развитию пролежней. Такой контроль также важен при перемещении и транспортировке пациента.
- Регулярно изменять положение тела больного — обычно рекомендуют делать это раз в два часа.
- Контролировать положение пациента в кровати или кресле — важно, чтобы человек не скользил и не сползал. Если больной находится в сидячем или полусидячем положении и сползает, его тело нужно зафиксировать.
- Использовать правильно подобранные матрасы или противопролежневые системы (матрасы с компрессором). При риске развития пролежней матрас нужно использовать сразу, а не тогда, когда они уже появились [11]. При низкой вероятности развития пролежней и небольшом весе больного, как правило, достаточно матраса из поролона толщиной 10 см. При этом важно, чтобы вес человека равномерно распределялся по поверхности кровати. Если риск развития пролежней высок или они уже появились, необходимы специальные матрасы. При длительном нахождении пациента в сидячем положении в кресле-каталке или обычном кресле под спину или ягодицы желательно помещать противопролежневые подушки толщиной 10 см. При положении на боку такие подушки нужно подкладывать между коленками.
- Стимулировать адекватное кровообращение с помощью ручного массажа или массажёров в местах, где часто возникают пролежни.
- Контролировать целостность кожи на этих участках кожи.
- Поддерживать чистоту кожи и правильно ухаживать за ней. Рекомендуется, чтобы гигиенические средства, в том числе моющие губки и пенообразующие или волокнистые перчатки, были одноразовыми. Также желательно, чтобы все средства по уходу за кожей были гипоаллергенными: у них зачастую есть некоторые защитные свойства, к примеру они могут поглощать влагу или формировать защитную плёнку на коже.
- Поддерживать нормальную влажность и температуру кожи.
- Правильно использовать массажёры и аппараты электростимуляции при проведении реабилитации. Применять их можно только после консультации с врачом.
- Обеспечить пациента необходимым питьём и питанием.
- Устранить или уменьшить влияние других негативных факторов, например ослабить боль, зуд, бессонницу, стрессы и помочь с решением психологических проблем.
- Обучить пациента или его родственников правилам ухода — важно знать, в каких областях чаще всего появляются пролежни, каким должно быть положение тела и как правильно перемещать пациента, разбираться в гигиенических средствах. Также нужно знать, что недопустимо длительное мокнутие от слюнотечения и неконтролируемого мочеиспускания, и важно своевременно менять подгузники и следить за сухостью одежды или постельного белья.
Таким образом, для профилактики пролежней нужно своевременно и адекватно оценивать вероятность их развития, а также вовремя и правильно проводить профилактические мероприятия [1][6].
Пролежни
Версия: Клинические протоколы МЗ РК — 2022 (Казахстан)
Категории МКБ:
Декубитальная язва (пролежень) и место давления неуточненные (L89.9), Декубитальная язва (пролежень) и область давления, стадия I (L89.0), Декубитальная язва (пролежень), стадия II (L89.1), Декубитальная язва (пролежень), стадия III (L89.2), Декубитальная язва (пролежень), стадия IV (L89.3), Декубитальная язва и область давления (L89)
Разделы медицины:
Паллиативная помощь, Хирургия
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «13» января 2023 года
Протокол №177
КЛИНИЧЕСКИЙ ПРОТОКОЛ ПАЛЛИАТИВНОЙ МЕДИЦИНСКОЙ ПОМОЩИ
ПРОЛЕЖНИ
Пролежни – это патологическое состояние мягких тканей, которое связано с некрозом. Обуславливается оно тем, что на ткани постоянно осуществляется давление – это часто встречается у лежачих больных, которые не двигаются. В результате питание клеток нарушается, образуется некроз.
Длительно незаживающая рана – рана, не заживающая в течение периода, который является нормальным для ран подобного типа или локализации. На практике длительно незаживающей раной (хронической) принято считать рану, существующую более 4 недель без признаков активного заживления (исключение составляют обширные раневые дефекты с признаками активной репарации).
ВВОДНАЯ ЧАСТЬ
Код(ы) МКБ-10:
Дата разработки/пересмотра протокола: 2022 г.
Сокращения используемые в протоколе:
Пользователи протокола: ВОП поликлиники, комбустиологи, нейрохирурги, травматологи-ортопеды, общие хирурги, средний и младший медицинский персонал.
Категория пациентов для оказания паллиативной медицинской помощи: взрослые пациенты с пролежнями III, IV стадии.
Шкала уровня доказательности:
Облачная МИС «МедЭлемент»
Облачная МИС «МедЭлемент»

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
Классификация
Классификация [3]:
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Диагностические критерии
Жалобы на образование пролежней или других поражений кожи
Анамнез: сроки появления поражений кожи, проводимые в домашних условиях мероприятия, наличие хронического прогрессирующего заболевания.
Физикальное обследование:
— осмотр кожных покровов (внешний вид кожи, пастозность, инфекции, периодическое воспаление), оценка по шкале Карновского, Нортон.
Лабораторные исследования, необходимые для определения синдрома, проведенные до госпитализации в организацию по оказанию паллиативной медицинской помощи [6]:
ОАК (при длительно незаживающих ранах, особенно гигантских): умеренное снижение гемоглобина, повышение СОЭ, эозинофилия,
Коагулограмма: увеличение уровня фибриногена до 6 г/л.
Биохимический анализ крови: гипопротеинемия.
анализ крови на ВИЧ методом ИФА;
определение маркеров вирусного гепатита В методом ИФА;
определение маркеров вирусного гепатита С методом ИФА.
Группа крови и резус фактор
С-реактивный белок
Бак посев из раны (посев гнойного отделяемого для определения вида возбудителя и чувствительности возбудителя к антибиотикам)
Инструментальные исследования, необходимые для определения синдрома, проведенные до госпитализации в организацию по оказанию паллиативной медицинской помощи [7]:
ЭКГ (при наличие патологии со стороны сердечно-сосудистой системы)
Эхокардиография (при наличие патологии со стороны сердечно-сосудистой системы)
Флюорография (при наличие патологии со стороны легких)
Фиброэзофагогастродуоденоскопия (при наличие патологии со стороны ЖКТ)
Рентгенография (при наличие патологии со стороны ЖКТ)
Ультразвуковое исследование (при наличии деструкции костной ткани)
Компьютерная томография (область поражения) (при наличии деструкции костной ткани)
Диагноз подтверждается бактериологически при выделении микроорганизма в посевах образцов жидкости, полученных методом мазка или пункции из краев раны.
Подтверждение имеющегося осложнения «инфекции пролежней» бактериологически должно проводиться у всех пациентов, страдающих агранулоцитозом даже при отсутствии внешних признаков воспаления (боль, отечность краев раны, гнойное отделяемое).
Инфекции пролежней, развившиеся в стационаре, регистрируются как внутрибольничные инфекции.
Паллиативная помощь
Цели оказания паллиативной медицинской помощи:
- Восстановление целостности покровных тканей
- Улучшение качества жизни.
ТАКТИКА ОКАЗАНИЯ ПАЛЛИАТИВНОЙ МЕДИЦИНСКОЙ ПОМОЩИ [2,3,4, 21]
Немедикаментозное лечение [8,9,10]:
Режим общий, в послеоперационном периоде – постельный, диета – 15 стол.
Соблюдение общей гигиены, уход за кожей, избегать травмирующих воздействий (растирание полотенцем и пр.), использование увлажняющих кремов в зонах с риском развития поражения кожи, исключить длительный контакт кожи с мокрым бельем (при непроизвольных физиологических отправлениях).
Пассивная мобилизация каждые 2 часа.
Использование противопролежневых матрасов, постельное белье, на котором лежит больной, должно быть сухим и чистым, мягким и не иметь складок (простыню нужно натягивать, фиксируя края матрасом или как-нибудь иначе), следить, чтобы в постели не было крошек.
Физиолечение [11,12]:
• вакуум–терапия;
• магнитотерапия;
• лазеротерапия;
• гипербарическая оксигенация
Медикаментозное лечение [13,14,15]
Перечень основных лекарственных средств
NB! Антибактериальная терапия назначается эмпирически. При наличии клинических признаков инфекции нечувствительной к лечению рекомендуется проведение антибактериальной терапии с учетом чувствительности микрофлоры к антибактериальным препаратам [21].
Хирургическое вмешательство [16,17]:
свободная аутодермопластика; при наличии ограниченных или обширных дефектов кожи;
Хирургическая обработка гранулирующей раны: при наличии патологически измененных тканей;
аллотрансплантация кожи; при наличии обширных дефектах кожных покровов, обширных язв различного происхождения;
ксенотрансплантация при наличии ограниченных или обширных дефектов кожи, с целью предоперационной подготовки;
трансплантация культивированных клеток кожи при наличии обширных дефектах кожных покровов, обширных язв различного происхождения;
комбинированная трансплантация и применение факторов роста при наличии обширных дефектах кожных покровов, обширных язв различного происхождения;
Пластика местными тканями: при наличии ограниченных дефектов кожных покровов.
пластика лоскутами на питающей ножке: При наличии рубцов или дефектов тканей в области крупных суставов, при обнажении сухожилий, костных структур на протяжении, при дефектах тканей кистей и на опорных поверхностях стоп, с целью реконструкции дефектов в области головы, шеи, туловища, области таза;
При отсутствии положительной динамики основных вмешательств или как дополнение к ним возможна трансплансплантация культивированных аллогенных или аутологичных клеток кожи, в целях подготовки раны для оперативного вмешательства применение ваккум – терапии.
Противопоказания к хирургическому вмешательству [18]:
Сепсис
Отсутствие сознания
Эндокардит
Менингит
Свищи
Бактериемия
Дальнейшее ведение [19]:
При наличии остаточных ран на уровне ПМСП наблюдение осуществляется хирургом не менее 2-х раз в неделю до полной эпителизации ран;
динамическое наблюдение врачом общим хирургом должно осуществляться в сроки 3-х месяцев после выписки, 6 месяцев и 12 месяцев с целью определения дальнейшей тактики лечения.
Индикаторы эффективности паллиативного лечения [20]:
восстановление или увеличение объема движений;
уменьшение площади дефекта;
отсутствие воспалительных процессов в ране;
заживление раневого дефекта;
восстановление целостности кожного покрова.
Госпитализация
Показания для госпитализации в организацию по оказанию паллиативной медицинской помощи:
- пролежни 3 и 4 стадии;
- стерильный бак посев из пролежневой раны.
Условия для госпитализации в организацию по оказанию паллиативной медицинской помощи:
- пролежни 1 и 2 стадии.
Информация
Источники и литература
-
Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2022
- 1.Treuillet S., Albouy B., Lucas Y. Three-dimensional assessment of skin wounds using a standard digital camera. IEEE Trans Med Imaging. 2009; 28(5):752-762. doi: 10.1109/TMI.2008.2012025
2.Ахтямова Н.Е. Лечение пролежней у малоподвижных пациентов. Русский медицинский журнал. 2015; (26):1549–1552. [Ahtyamova N.Е. Lechenie prolezhney u malopodvizhnyh pacientov. Russkiy medicinskiy zhurnal. 2015;(26): 1549–1552. (In Russ).]
3.Xie H., Peel N.M., Hirdes J.P. et al. Validation of the interRAI Pressure Ulcer Risk Scale in acute care hospitals. J Am Geriatr Soc. 2016; 64(6):1324-1328. doi: 10.1111/jgs.14131.
4.Cushing C.A., Phillips L.G. Evidence-based medicine: pressure sores. Plast Reconstr Surg. 2013; 132(6):1720- 1732. doi: 10.1097/PRS.0b013e3182a808ba
5.Pattanshetty R.B., Prasade P.M., Aradhana K.M. Risk assessment of decubitus ulcers using four scales among patients admitted in medical and surgical intensive care units in a tertiary care set up: a crosssectional study. Int J of Physiother Res. 2015; 3(2):971-977. doi: 10.16965/ijpr.2015.117
6.Agrawal K., Chauhan N. Pressure ulcers: Back to the basics. Indian J Plast Surg. 2012; 45(2):244. doi: 10.4103/0970-0358.101287
7.Bliss M.R. Acute pressure area care: Sir James Paget’s legacy. Lancet. 1992; 339(8787):221-223.
8.Климиaшвили А.Д. Профилактика и лечение пролежней. Lancet. 1990;335:1311-1312 [Klimiashvili A.D. Profilaktika i lechenie prolezhney [Prophylaxis and treatment of pressure bedsores]. Lancet. 1990;(335):1311-1312 (In Russ).]
9.Jiang Q, Li X, Qu X et al. The incidence, risk factors and characteristics of pressure ulcers in hospitalized patients in China. Int J Clin Exp Pathol. 2014; 7(5):2587.
10.Edsberg L.E., Black J.M., Goldberg M. et al. Revised National Pressure Ulcer Advisory Panel pressure injury staging system: revised pressure injury staging system. J Wound Ostomy Continence Nurs. 2016; 43(6):585. doi: 10.1097/WON.0000000000000281
11.National Pressure Ulcer Advisory Panel, European Pressure Ulcer Advisory Panel and Pan Pacific Pressure Injury Alliance. International Guideline Treatment of Pressure Ulcers: Quick Reference Guide. 2009 [updated 2014 Oct 16, cited 2019 Sep 05]. Available from: https://www.npuap.org/wp-content/uploads/2014/08/ Updated-10-16-14-Quick-Reference-Guide-DIGITAL-NPUAP-EPUAP-PPPIA-16Oct2014.pdf.
12.The National Pressure Ulcer Advisory Panel. 2014 Prevention and Treatment of Pressure Ulcers: Clinical Practice Guideline. [updated 2014, cited 2019 Sep 05] Available from: http://internationalguideline.com/guideline.
13.Пшениснов К.П. Курс пластической хирургии. Руководство для врачей. 2010;(2):982. [Pshenisnov K.P. Kurs plasticheskoy hirurgii. Rukovodstvo dlya vrachey. [Course of the Plastic Surgery. Guide]. 2010;(2):982 (In Russ).]
14. Государственный стандарт Российской Федерации (ГОСТ) Р 56819-2015 Надлежащая медицинская практика. Инфологическая модель. Профилактика пролежней. Введ. 2015-11-30. Межрегиональная общественная организация «Общество фармакоэкономических исследований»; М.: Стандартинформ, 2016:4.
15.Anders J., Heinemann A., Leffmannet C. et al. Decubitus ulcers: pathophysiology and primary prevention. Dtsch Arztebl Int. 2010; 107(21):371. doi: 10.3238/arztebl.2010.0371.
16.Дибиров М.Д. Пролежни: профилактика и лечение. Медицинский совет. 2013; (5-6) [Dibirov M.D. Prolezhni: profilaktika i lechenie [Pressure bedsores: prevention and treatment]. Medicinskiy sovet. 2013; (5-6) (In Russ).]
17.Rahim K, Saleha S, Zhuet X et al. Bacterial contribution in chronicity of wounds. Microb Ecol. 2017; 73(3):710- 721. doi: 10.1007/s00248-016-0867-9
18.Об утверждении отраслевого стандарта «Протокол ведения больных. Пролежни»: приказ Министерства Здравоохранения Российской Федерации от 17.04.2002 г. № 123 [Ob utverzhdenii otraslevogo standarta “Protokol vedeniya bol’nyh. Prolezhni”: prikaz Ministerstva Zdravoohraneniya Rossijskoj Federacii ot 17.04.2002 № 123 (In Russ).] Доступно по: https://normativ.kontur.ru/document?moduleId=1&documentId=74654. Ссылка активна на 20.05.2019.
19.Webster J., Coleman K., Mudge A. et al. Pressure ulcers: effectiveness of risk-assessment tools. A randomised controlled trial (the ULCER trial). BMJ Qual Saf. 2011(4): 297-306. doi: 10.1136/bmjqs.2010.043109
20.Compton F., Hoffmann F., Hortig T. et al. Pressure ulcer predictors in ICU patients: nursing skin assessment versus objective parameters. J Wound Care. 2008;17: 417–424. doi: 10.12968/jowc.2008.17.10.31304
21. BMJ BestPractice Pressure ulcer Last reviewed: 8 Nov 2022, Last updated: 03 Aug 2021 https://bestpractice.bmj.com/topics/ru-ru/378
- 1.Treuillet S., Albouy B., Lucas Y. Three-dimensional assessment of skin wounds using a standard digital camera. IEEE Trans Med Imaging. 2009; 28(5):752-762. doi: 10.1109/TMI.2008.2012025
Информация
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА
Список разработчиков протокола с указание квалификационных данных:
1) Мурадов Мисмил Исламович – кандидат медицинских наук, заведующий отделением реконструктивно-пластической микрохирургии АО «Национальный научный центр хирургии им. А.Н. Сызганова».
2) Мухамедкерим Канат Базарбекович – старший сотрудник отделения реконструктивно-пластической микрохирургии АО «Национальный научный центр хирургии им. А.Н. Сызганова».
3) Кошкарбаев Данияр Жамбылұлы — сотрудник отделения реконструктивно-пластической микрохирургии АО «Национальный научный центр хирургии им. А.Н. Сызганова».
4) Саршаев Марат Амангалиевич – врач нейрохирург первой категории Центральной Клинической Больницы Медицинского Центра Управления Делами Президента Республики Казахстан
5) Қазантаев Кымбат Ерикович – ассистент кафедры травматологии и ортопедии НАО «Казахский национальный медицинский университет имени С.Д. Асфендиярова»
6) Ильясова Бибигуль Сапарбековна — кандидат медицинских наук ассоцированный профессор, сотрудник кафедры клинической фармакологии НАО «Казахский национальный медицинский университет имени С.Д. Асфендиярова»
Указание на отсутствие конфликта интересов: нет.
Рецензенты: Ибадильдин Амангельды Сейтказинович – доктор медицинских наук, профессор кафедры хирургических болезней НАО «Казахский национальный медицинский университет имени С.Д. Асфендиярова»
Указание условий пересмотра протокола: пересмотр протокола через 5 лет после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Прикреплённые файлы
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
Pressure ulcers: new approaches to treatment / Igor N. Pasechnik1, ORCID: 0000-0002-8121-4160, pasigor@yandex.ru / Tatiana V. Novikova2, ORCID: 0000-0003-2732-3873, tatyana.novikova@danone.com / 1 Federal State Budgetary Institution of Additional Professional Education Central State Medical Academy of the Administrative Department of the President of the Russian Federation; 19 b.1A Marshal Timoshenko str., Moscow, 121359, Russia / 2 Nutricia Advanced LLC; block B BC Riga Land, 26 km Novorizhskoe highway, Kr
Abstract. The urgency of the problem of pressure ulcers does not decrease, despite the achievements of modern medicine. Pressure ulcers occur both in hospital patients and in patients receiving treatment at home or in long-stay institutions. The main reason for the high prevalence of pressure ulcers is the aging of the population and an increase in patients with comorbid pathology. A pressure sore is a localized injury to the skin and/or underlying tissue that typically occurs over a bony prominence, usually as a result of long-term pressure or pressure combined with shear or friction. The most common sites for pressure ulcers are the skin covering the sacrum, coccyx, heels, and thighs, although other areas may be affected: knees, ankles, back of the shoulders, or back of the skull. From a clinical point of view, a bedsore can be described as an ulcer resulting from pressure. It is believed that the most important factors contributing to the formation of pressure ulcers are continuous pressure, displacement forces, friction and moisture. A large role in the development of ulcers is also played by the limited motor activity of patients, inadequate nutrition and care. In this article, pressure ulcers are considered as a multidisciplinary problem that doctors of various specialties must face. The most effective method of dealing with pressure sores is preventive measures. Modern prevention of bedsores includes a number of areas and should take into account the patient’s condition, as well as the capabilities and qualifications of medical personnel. The main goal of the treatment of bedsores is to restore the integrity of the skin, while the tactics of management are largely determined by the staging of the pathological process. Complex treatment of pressure ulcers depends on their stage and includes both pharmacological effects and surgical intervention. One of the components of the treatment of pressure ulcers is to provide nutritional support with integral mixtures enriched with arginine, vitamins, antioxidants, and the micronutrient zinc.
For citation: Pasechnik I. N., Novikova T. V. Pressure ulcers: new approaches to treatment // Lechaschi Vrach. 2022; 4 (25): 38-43. DOI: 10.51793/OS.2022.25.4.007
Резюме. Актуальность проблемы пролежней не уменьшается, несмотря на достижения современной медицины. Пролежни встречаются как у больных стационара, так и у пациентов, получающих лечение в домашних условиях или учреждениях длительного пребывания. Основная причина высокой распространенности пролежней – старение населения и увеличение пациентов с коморбидной патологией. Пролежни представляют собой локализованное повреждение кожи и/или подлежащей ткани, которое обычно возникает над костным выступом в результате, как правило, долгосрочного давления или давления в сочетании со сдвигом или трением. Наиболее распространенными участками развития пролежней являются кожа, покрывающая крестец, копчик, пятки и бедра, хотя могут быть затронуты и другие участки: колени, лодыжки, задняя часть плеч или затылок. C клинических позиций пролежень можно обозначить как язву, образующуюся вследствие давления. Считается, что наиболее важными факторами, способствующими образованию пролежневых язв, являются непрерывное давление, силы смещения, трение и влажность. Большую роль в развитии язв также играют ограниченная двигательная активность больных, недостаточные питание и уход. В этой статье пролежни рассматриваются как мультидисциплинарная проблема, с которой приходится сталкиваться врачам различных специальностей. Наиболее эффективным методом борьбы с пролежнями являются профилактические мероприятия. Современная профилактика пролежней включает целый ряд направлений и должна учитывать состояние пациента, а также возможности и квалификацию медицинского персонала. Основная цель лечения пролежней – восстановление целостности кожного покрова, при этом тактика ведения во многом определяется стадийностью патологического процесса. Комплексное лечение пролежней зависит от их стадии и включает как фармакологическое воздействие, так и хирургическое вмешательство. Одним из компонентов лечения пролежней является проведение нутритивной поддержки энтеральными смесями, обогащенными аргинином, витаминами, антиоксидантами и микронутриентом цинком.
Увеличение продолжительности жизни в современном мире связано с улучшением условий проживания людей в большинстве стран и успехами здравоохранения. Обратной стороной старения населения является возрастание числа лиц пожилого и старческого возраста в стационарах. В отделениях реанимации и интенсивной терапии (ОРИТ), где концентрируются наиболее тяжелые пациенты в критических состояниях (КС) с полиорганной недостаточностью (ПОН), средний возраст больных превышает 65 лет [1]. Лечение пациентов в КС с ПОН предусматривает замещение жизненно важных функций: коррекцию нарушений гемодинамики, проведение искусственной вентиляции легких, экстракорпоральную детоксикацию и пр. Эффективность таких методов лечения наиболее демонстративна, позволяет стабилизировать состояние больного и перевести его в профильное отделение. Однако у большинства больных, перенесших КС и ПОН, развивается так называемый синдром последствий интенсивной терапии – ПИТ-синдром. Это собирательное понятие включает совокупность ограничивающих повседневную жизнь пациента соматических, неврологических и социально-психологических последствий пребывания в ОРИТ [2].
В многочисленных публикациях подробно разбираются причины и последствия ПИТ-синдрома, формирование которого начинается в ОРИТ, а лечебные мероприятия приходится проводить уже в профильном отделении. Важными предрасполагающими факторами возникновения ПИТ-синдрома являются длительная иммобилизация пациента, нарушение пищевого статуса, неадекватная нутритивная поддержка. Стоит также подчеркнуть, что в остром периоде КС акцент лечебных мероприятий смещается в сторону жизнеспасающих технологий. Однако именно в этот момент возникают осложнения, профилактике которых не уделяется должное внимание. Речь идет о пролежнях. Развитие пролежней неблагоприятно сказывается на результатах лечения и прогнозе заболевания, их инфицирование может приводить к манифестации сепсиса. Многие клиницисты считают, что наличие специальных противопролежневых матрасов в ОРИТ – гарантия от их возникновения. К сожалению, это не так. Пролежни относятся к мультидисциплинарной проблеме, так как с ними приходится сталкиваться и заниматься их лечением большинству клиницистов – анестезиологам-реаниматологам, хирургам, травматологам, неврологам, терапевтам и другим специалистам.
Обширные операции, требующие длительного соблюдения постельного режима, травмы, длительно (иногда навсегда) ограничивающие подвижность пациента, коматозные состояния, при которых человек может дни и месяцы находиться без сознания, реабилитация после острого нарушения мозгового кровообращения (ОНМК) – вот далеко неполный перечень ситуаций, при которых могут возникать пролежни. Важно помнить, что это не только проблема стационаров, но и амбулаторных длительно лежащих больных.
Пролежни как мультидисциплинарная проблема
Пролежни (код в МКБ-10 – L89), а в англоязычной литературе – pressure ulcer – представляют собой локализованное повреждение кожи и/или подлежащей ткани, которое обычно возникает над костным выступом в результате, как правило, долгосрочного давления или давления в сочетании со сдвигом или трением. Наиболее распространенными участками развития пролежней являются кожа, покрывающая крестец, копчик, пятки и бедра, хотя могут быть затронуты и другие участки: колени, лодыжки, задняя часть плеч или черепа [3]. Происхождение термина пролежень (decubitus) связывают с латинским словом decumbere (лежать), что не совсем корректно, так как создается впечатление, что пролежни образуются только при лежании пациента [4]. На самом деле пролежень может возникать при любом сдавлении извне. Патогенез пролежней связан не только с механическим воздействием на поверхность тела человека, но и с другими факторами, которые будут рассмотрены ниже.
Локализация пролежней зависит от положения больного (рис. 1-3) [3]. В лежачем положении наибольшее давление приходится на ткани человека, находящиеся в области крестца, ягодиц, пяток и затылка (40-60 мм рт. ст.), в прон-позиции (положении лежа на животе) до 50 мм рт. ст. приходится на область коленей и груди, в сидячем положении при опоре ногами на твердую поверхность наибольшее давление (примерно 10 мм рт. ст.) испытывают ткани в области седалищных бугров. Наиболее типичным местом образования пролежней (до 60% частоты встречаемости) являются крестец и седалищные бугры. Стоит отметить, что при приподнятом головном конце кровати давление на крестец увеличивается. У больных с избыточной массой тела возможно образование пролежней в течение 2 часов [5].
C клинических позиций пролежень можно обозначить как язву, образующуюся вследствие давления. Считается, что наиболее важными факторами, способствующими образованию пролежневых язв, являются непрерывное давление, силы смещения, трение и влажность. Большую роль в развитии язв также играют ограниченная двигательная активность больных, недостаточные питание и уход. Кроме того, к существенным факторам риска относятся возраст старше 70 лет, мужской пол, сахарный диабет, параплегия, кахексия и др. [2, 4].
Длительное (более 1-2 часов) действие давления приводит к обструкции сосудов, сдавлению нервов и мягких тканей. В тканях, подвергающихся давлению, сдвигу и трению, особенно в уязвимых местах над костными выступами, нарушаются микроциркуляция и трофика, развивается гипоксия с последующим появлением некроза и изъязвлений (пролежней) [3]. Факторы риска развития пролежней делятся на обратимые (гипотензия, гиповолемия, гипопротеинемия) и необратимые (возраст). В задачи клиницистов входит профилактика возникновения пролежней. Для этого разработаны специальные шкалы, позволяющие прогнозировать их развитие. Наиболее известными являются шкалы Нортон (Norton, 1962) [6] (табл. 1) и Меддлей (Meddley, 1991). Вероятность образования пролежней (по Шкале Нортон):
- 12 баллов или меньше – высокая;
- 14 баллов или меньше – средняя;
- более 14 баллов – низкая.
Шкала Нортона не требует значительных усилий и позволяет при минимальных затратах времени оценить степень риска развития пролежней. Поэтому она наиболее часто используется в клинической практике. Шкала Меддлей наибольшее распространение получила в отделениях неврологии, что связывают с ее универсальностью и простотой применения.
Кроме того, используются шкалы Ватерлоу (Waterlow, 1985) и Брейден (Braden, 1987) [7, 8], которые учитывают дополнительные риски, влияющие на развитие пролежней, включая оценку нутритивного статуса (табл. 2). Приведенные шкалы позволяют не только оценить риск развития пролежней, но также указывают на пути их предотвращения. Во время комы больному следует обеспечить «пассивную подвижность» (повороты пациента, кинезотерапия), правильный уход за кожей, сбалансированное питание, поддержание гомео-стаза (в том числе лечение сопутствующих заболеваний).
В настоящий момент принято выделять 4 стадии пролежней, имеющих характерную картину и требующих соответствующего лечения [4, 7, 8]:
I стадия – появление бледного участка кожи или устойчивая гиперемия кожи, не проходящая после прекращения давления; кожные покровы не нарушены;
II стадия – появление синюшно-красного цвета кожи с четкими границами, стойкая гиперемия кожи, отслойка эпидермиса, поверхностное (неглубокое) нарушение целостности кожных покровов (поверхностная язва, которая клинически проявляется в виде потертости, пузыря или плоского кратера) с распространением на подкожную клетчатку;
III стадия проявляется некротическим поражением кожи на всю глубину с вовлечением подкожной жировой клетчатки до фасции;
IV стадия характеризуется не только обширным поражением кожи и подкожной клетчатки, но и некрозом глубжележащих тканей – мышц, костей, сухожилий и суставных капсул.
Профилактика пролежней
Наиболее эффективным методом борьбы с пролежнями являются профилактические мероприятия. При этом состоянии в полной мере реализуется положение, высказанное еще Гиппократом: «Предупредить легче, чем лечить». В большинстве стран с высоким уровнем развития медицины широко распространено мнение, что профилактикой пролежней должен заниматься средний медицинский персонал. Врачи чаще всего не вникают должным образом в решение этого вопроса. Большинство современных научных исследований направлено на разработку новых методов лечения уже образовавшихся пролежней [8].
Современная профилактика пролежней включает целый ряд направлений и должна учитывать состояние пациента, а также возможности и квалификацию медицинского персонала. Обязательным является оценка риска возникновения пролежней. Общепринятыми становятся следующие мероприятия:
- уменьшение давления в местах костных выступов и зонах риска развития пролежней, в том числе за счет использования противопролежневых систем, контроль за положением больного, смена положения;
- улучшение кровоснабжения и микроциркуляции в зонах риска развития пролежней;
- контроль за положением пациента в кровати, предупреждение неправильного положения («сползание» с подушек при положении сидя в кровати или кресле);
- наблюдение за кожей в зонах риска развития пролежней;
- гигиенический уход, поддержание чистоты кожи и ее умеренной влажности;
- обеспечение нормальной температуры кожи;
- правильный подбор, обеспечение и использование технических средств реабилитации и ухода;
- контроль гидратации пациента и проведение адекватной нутритивной поддержки;
- обучение больных, способных ухаживать за собой, или их родственников;
- устранение сопутствующих проблем (борьба с кожным зудом, болью, бессонницей, нормализация психологического статуса и т. д.).
Лечение пролежней
Основная цель лечения пролежней – восстановление целостности кожного покрова, при этом тактика ведения во многом определяется стадийностью патологического процесса [8-10]. На I-II стадиях показаний для хирургического вмешательства нет. Основная задача клиницистов – профилактика прогрессирования патологического процесса. Проводятся мероприятия, направленные на устранение сдавления тканей, восстановление нормального кровообращения и микроциркуляции. Одной из важнейших задач лечения на I-II стадиях является предотвращение инфицирования раны. Возникновение воспалительного процесса в месте пролежня чревато генерализацией инфекционного процесса вплоть до развития сепсиса и ПОН. Неотъемлемый компонент терапии пролежней не только на ранних стадиях, но и при прогрессировании процесса – курация сопутствующих заболеваний и синдромов, относящихся к факторам риска: сахарного диабета, облитерирующих заболеваний артерий, сердечной недостаточности и др. Кроме того, необходимо устранять водно-электролитные отклонения, являющиеся важным компонентом нарушения микроциркуляции, адекватно обезболивать пациентов. Считается, что ведущий фактор консервативного лечения пролежней – устранение длительного непрерывного давления на ткани проблемной зоны.
На III-IV стадиях пролежней лечение направлено на удаление некротизированных тканей. Объем операции определяется обширностью и глубиной патологического процесса. Антибактериальная терапия проводится с учетом выявленного возбудителя и его чувствительности к препаратам. Для стимуляции быстрого заживления и очищения раны используются различные фармакологические средства и методы физического воздействия.
Перспективным методом лечения пролежней является применение отрицательного давления в области раны – вакуум-терапия [9]. В работе С. А. Шляпникова с соавт. было показано, что применение вакуум-терапии в комбинации с адекватным системным назначением антибактериальных препаратов в лечении пролежней предотвращает прогрессирование раневого процесса, значительно снижает срок перехода раневого процесса от стадии воспаления к фазе регенерации за счет увеличения кровотока в пораженном участке, снижения микробной контаминации раневой поверхности. Такой подход сопровождается уменьшением срока госпитализации и экономических затрат при лечении пролежней [10].
Вне зависимости от способа лечения пролежней, пристальное внимание уделяется правильно организованному уходу: тщательному соблюдению асептики (инфицирование раны значительно замедляет заживление пролежня), изменению положения тела больного, применению противопролежневых матрацев, предотвращению травматизации грануляционной ткани пролежневой раны, надлежащему гигиеническому уходу за больным, полноценному питанию с достаточным количеством белка и витаминов.
Роль нутритивной поддержки в лечении пролежней
Особая роль в лечении пролежней отводится коррекции пищевого статуса. Это связано с двумя аспектами. Исходная нутритивная недостаточность является фактором риска развития пролежней, инфицирования ран и их замедленного заживления [2, 11]. Кроме того, неадекватная доставка энергии, макро- и микронутриентов задерживает грануляцию и заживление ран [12, 13]. При возникновении пролежней на фоне ПИТ-синдрома у пациентов с ОНМК, больных после обширных операций потребности в нутриентах и энергии невозможно обеспечить обычным приемом пищи, поэтому им необходимо пероральное дополнительное питание или назначение энтеральных смесей через зонд.
В целом ряде работ отмечено позитивное влияние нутритивной поддержки на результаты лечения пролежней, при этом потребности в белке и энергии зависят от стадии патологического процесса.
В систематическом обзоре и метаанализе 15 исследований (из них 8 рандомизированных клинических) было показано, что назначение высокобелкового перорального дополнительного и энтерального питания ассоциировано со снижением риска развития пролежней на 25% [14].
В большинстве исследований было показано, что потребность в белке у больных с пролежнями I и II стадии составляет 1-1,4 г/кг/сут, с пролежнями III и IV – 1,5-2,0 г/кг/сут, и в некоторых случаях может достигать 2,2 г/кг/сут (B1 ↑↑) [14, 15]. В числе необходимых мер по профилактике и лечению пролежней международным альянсом (EPUAP/NPIAP/PPPIA, 2019) рекомендовано проведение оценки нутритивного статуса для лиц с пролежнями и риском их развития, в том числе разработка и внедрение индивидуального плана питания для лиц с пролежневой травмой или риском ее возникновения, страдающих от недоедания [16].
Пациентам с нутритивной недостаточностью и наличием пролежней II стадии и выше рекомендовано питание высококалорийными смесями с высоким содержанием белка, повышенным содержанием аргинина, цинка и антиоксидантов (уровень рекомендаций B1) [16]. Кроме того, необходимо обеспечить потребление 30-35 ккал/кг в сутки взрослыми с пролежнями, которые недоедают или подвержены риску недоедания (B1↑) [16].
Действительно, белок является важнейшим компонентом нутритивной поддержки, так как необходим для восстановления пораженных тканей. Аминокислоты участвуют в репаративных процессах на всех этапах заживления ран, включая пролиферацию фибробластов, синтез коллагена, ангиогенез и иммунный ответ.
Позитивные результаты нутритивной поддержки больных с пролежнями легли в основу изучения методов коррекции пищевого статуса с использованием питательных смесей, обогащенных компонентами, ранее доказавшими эффективность при заживлении ран и пролежней (аргинин, витамины А, Е, С, антиоксиданты и микроэлемент Zn) [11].
Аргинин – частично заменимая аминокислота, однако в условиях КС, сепсиса, развития пролежней и стрессовой реакции организма больного становится незаменимой, так как резко возрастает ее потребление в защитных метаболических процессах. Сообщается о том, что аргинин способствует улучшению микроциркуляции, ускоряет заживление ран и предотвращает развитие пролежней. Аргинин является субстратом для синтеза белка, стимулирует транспорт аминокислот в клетки тканей и способствует образованию белков в клетке. Известен его позитивный эффект на пролиферацию клеток, репарацию коллагена и иммуномодулирующее действие [17].
Аргинин является биологическим предшественником оксида азота, который обладает мощными сосудорасширяющими, антибактериальными и ангиогенными свойствами, что положительно сказывается на заживлении ран [18]. При использовании аргинина, особенно его внутривенных форм, необходимо учитывать возможность развития гипотензии, что связано с образованием оксида азота. Однако это актуально в основном для гемодинамически нестабильных больных сепсисом [19].
Успешное заживление раны требует серии скоординированных процессов, включая гемокоагуляцию, редукцию воспаления, ангиогенез, образование новой ткани и ремоделирование внеклеточного матрикса. Цинк является кофактором для многих металлоэнзимов, необходимых для восстановления клеточных мембран, пролиферации клеток, их роста и функционирования иммунной системы. Дефицит Zn сопровождается повреждением кожи, нарушением иммунной функции и заживления ран [20].
В обзорной публикации, посвященной изучению эффективности витаминов и антиоксидантов у больных с ранами, было показано, что включение в нутритивную поддержку витамина С и Zn позволяет уменьшить развитие пролежней у пациентов с факторами риска, а также способствует их более быстрому заживлению [21].
В пилотном исследовании у 16 больных с пролежнями II-IV стадий изучили влияние пероральных добавок [22]. Пациенты дополнительно к обычному питанию получали аргинин – 9 г/сут, витамин С – 500 мг/сут и Zn – 30 мг/сут. Возраст пациентов составил 37-92 года, индекс массы тела – 16,4-28,1 кг/м2. Было установлено, что обогащение пищи аргинином, витамином С и Zn сопровождалось быстрейшим заживлением пролежневых ран. Авторы делают вывод о необходимости дальнейших исследований влияния специализированной нутритивной поддержки на течение раневого процесса.
С учетом данных клинических исследований компанией Nutricia был разработан инновационный продукт специализированного питания для нутритивной поддержки пациентов с пролежнями и хроническими ранами – Нутризон Эдванст Кубизон. Он является полноценным средством для энтерального питания и обогащен компонентами, играющими важную роль в заживлении ран, – аргинином, витаминами А, С и Е, микроэлементом цинком.
Эффективность препарата Нутризон Эдванст Кубизон была изучена у пациентов пожилого и старческого возраста с пролежнями. Больных рандомизировали в две группы в зависимости от особенностей нутритивной поддержки, исследование длилось 12 недель. Различий по стадиям пролежней (II-IV стадии) и методам лечения между группами не было. Больные 1-й группы получали стандартную больничную диету или энтеральную смесь Нутризон, больным 2-й группы больничную пищу комбинировали с Кубизоном (1000 мл) или пероральным дополнительным питанием (400 мл Кубитана – препарат, схожий по составу с Кубизоном, в РФ не зарегистрирован). Общая калорийность питания по группам не различалась и составила 30 ккал/кг/сут. Состояние пролежней оценивали по специальным шкалам. Установили, что включение в состав нутритивной поддержки Кубизона способствует более быстрому заживлению пролежней, что проявлялось в значимом уменьшении их площади через 8 и 12 недель от начала лечения в сравнении с контрольной группой [23]. Авторы делают вывод о целесообразности назначения больным с пролежнями энтерального питания, обогащенного аргинином, витаминами, антиоксидантами и Zn.
Углубленное изучение данных об эффективности специфических смесей с высоким содержанием белка, обогащенных аргинином, цинком и антиоксидантами, предназначенных для пациентов с пролежнями (PU), было проведено группой исследователей на основе рандомизированных контролируемых испытаний, результаты которых были опубликованы с января 1997 г. по октябрь 2015 г. в электронных базах данных (EMBASE, Medline, PubMed и CINAHL) (рис. 4) [24]. На графиках квадраты обозначают точечные оценки эффекта (средняя разница), при этом размер квадрата представляет вес, приписываемый каждому исследованию, а горизонтальные столбцы указывают 95% ДИ [24]. Систематический обзор показывает, что использование пероральных/зондовых смесей, обогащенных аргинином, цинком и антиоксидантами, не менее чем в течение 8 недель связано с улучшением заживления пролежней по сравнению со стандартными смесями.
Заключение
Проблема профилактики и лечения пролежней далека от своего решения. Несмотря на отсутствие полноценной статистики, создается впечатление, что количество случаев развития пролежней не снижается. Это заметно как по стационарам, так и у больных, получающих лечение на дому. Основные причины сохранения высокой частоты развития пролежней – общее старение населения, увеличение числа больных с коморбидной патологией и, соответственно, с факторами риска. Основа терапии пролежней – профилактика их возникновения. В профильной литературе подробно описаны подходы к лечению пролежней в зависимости от их стадии.
В последние годы опубликованы результаты исследований, доказывающие важную роль нутритивной поддержки в лечении пролежней. Наилучшие результаты получены при использовании специализированных высокобелковых продуктов для перорального дополнительного питания и энтеральных смесей зондового питания, обогащенных аргинином, витаминами, антиоксидантами и микронутриентом цинком.
КОНФЛИКТ ИНТЕРЕСОВ. Статья подготовлена при участии ООО «Нутриция». Это никак не повлияло на мнение авторов.
CONFLICT OF INTERESTS. The article was prepared with the participation of Nutricia LLC. This did not affect the author’s opinion in any way.
Литература/References
- Flaatten H., de Lange D. W., Artigas A., et al. The status of intensive care medicine research and a future agenda for very old patients in the ICU // Intensive Care Med. 2017, 43 (9): 1319-1328.
- Белкин А. А. Синдром последствий интенсивной терапии (ПИТ-синдром) // Вестник интенсивной терапии имени А. И. Салтанова. 2018; 2: 12-23. [Belkin A. A. Syndrome of consequences of intensive care (PICS) // Vestnik intensivnoy terapii imeni A. I. Saltanova. 2018; 2: 12-23.]
- Grey J. E., Harding K. G., Enoch S. Pressure ulcers // BMJ. 2006; 7539 (332): 472-475.
- Климиашвили А. Д. Профилактика и лечение пролежней // Русский медицинский журнал. 2004; 12 (12): 40-45. [Klimiashvili A. D. Prevention and treatment of bedsores // RMJ. 2004. T. 12, № 12. P. 40-45.]
- Leigh I. H., Bennett G. Pressure Ulcers: Prevalence, Etiology, and Treatment Modalities: A Review // American J. Surgery. 1994; 167: 25S-30S. doi.org/10.1016/0002-9610(94)90007-8.
- Norton D., McLaren R., Exton-Smith A. N. An Investigation of Geriatric Nursing Problems in Hospital. Churchill Livingstone, London, 1962. Р. 193-224.
- Дибиров М. Д. Пролежни: профилактика и лечение. Стационаро-замещающие технологии // Амбулаторная хирургия. 2016; 1-2: 55-63. [Dibirov M. D. Bedsores: prevention and treatment. Stationary-replacing technologies // Ambulatory surgery. 2016. № 1-2. P. 55-63.]
- Климиашвили А. Д. Профилактика и лечение пролежней // Медицина неотложных состояний. 2007; 5 (12): 99-103. [Klimiashvili A. D. Prevention and treatment of bedsores // Meditsina neotlozhnykh sostoyaniy. 2007; 5 (12): 99-103.]
- Hsu К.-F., Kao L. T., Chu P.-Y. et al. Simple and Efficient Pressure Ulcer Reconstruction via Primary Closure Combined with Closed-Incision Negative Pressure Wound Therapy (CiNPWT)-Experience of a Single Surgeon // J Pers Med. 2022; 12 (2): 182. DOI: 10.3390/jpm12020182.
- Шляпников С. А., Насер Н. Р., Бородина М. А. и соавт. Современные подходы к лечению пролежней // Журнал МедиАль. 2019; 1 (23): 40-41. [Shlyapnikov S. A., Naser N. R., Borodina M. A. i soavt. Modern approaches to the treatment of bedsores // Zhurnal MediAl’. 2019; 1 (23): 40-41.]
- Yap J. W., Holloway S. Evidence-based review of the effects of nutritional supplementation for pressure ulcer prevention // Int Wound J. 2021; 18 (6): 805-821. DOI: 10.1111/iwj.13584.
- Zhong J. X., Kang K., Shu X. L. Effect of nutritional support on clinical outcomes in perioperative malnourished patients: a meta-analysis // Asia Pac J Clin Nutr. 2015; 24 (3): 367-378. DOI: 10.6133/apjcn.2015.24.3.20.
- Munoz N., Posthauer M. E., Cereda E. et al. The Role of Nutrition for Pressure Injury Prevention and Healing: The 2019 International Clinical Practice Guideline Recommendations // Adv Skin Wound Care. 2020; 33 (3): 123-136. DOI: 10.1097/01.ASW.0000653144.90739.ad.
- Cox J., Rasmussen L. Enteral nutrition in the prevention and treatment of pressure ulcers in adult critical care patients // Crit Care Nurse. 2014; 34 (6): 15-27; quiz 28. DOI: 10.4037/ccn2014950.
- Stratton R. J., Ek A. C., Engfer M., et al. Enteral nutritional support in prevention and treatment of pressure ulcers: A systematic review and meta-analysis // Ageing Res Rev. 2005; 4 (3): 422-450. DOI: 10.1016/j.arr.2005.03.005.
- Prevention and Treatment of Pressure Ulcers/Injuries: Quick Reference Guide. Emily Haesler (Ed.). EPUAP/NPIAP/PPPIA: 2019.
- Chu A. S., Delmore B. Arginine: What You Need to Know for Pressure Injury Healing // Adv Skin Wound Care. 2021; 34 (12): 630-636. DOI: 10.1097/01.ASW.0000795900.25030.5e.
- Stechmiller J., Childress B., Cowan L. Arginine supplementation and wound healing // Nutr Clin Pract. 2005; 20 (1): 52-61. DOI: 10.1177/011542650502000152.
- Luiking Y. C., Deutz N. E. P. Exogenous arginine in sepsis // Crit Care Med. 2007; 35 (9 Suppl): S557-563. DOI: 10.1097/01.CCM.0000279191.44730.A2.
- Lin P.-H., Sermersheim M., Li H. et al. Zinc in Wound Healing Modulation // Nutrients. 2017; 10 (1): 16. DOI: 10.3390/nu10010016.
- Ellinger S., Stehle P. Efficacy of vitamin supplementation in situations with wound healing disorders: results from clinical intervention studies // Curr Opin Clin Nutr Metab Care. 2009; 12 (6): 588-95. DOI: 10.1097/MCO.0b013e328331a5b5.
- Desneves K. J., Todorovic B. E., Cassar A., Crowe T. C. Treatment with supplementary arginine, vitamin C and zinc in patients with pressure ulcers:a randomised controlled trial // Clin Nutr. 2005; 24 (6): 979-987. DOI: 10.1016/j.clnu.2005.06.011.
- Cereda E., Gini A., Pedrolli C., Vanotti A. Disease-specific, versus standard, nutritional support for the treatment of pressure ulcers in institutionalized older adults: a randomized controlled trial // J Am Geriatr Soc. 2009; 57 (8): 1395-1402. DOI: 10.1111/j.1532-5415.2009.02351.x.
- Cereda E., Neyens J. C. L., Caccialanza R. et al. Efficacy of a Disease-Specific Nutritional Support for Pressure Ulcer Healing: A Systematic Review and Meta-Analysis // J Nutr Health Aging. 2017; 21 (6): 655-661. DOI: 10.1007/s12603-016-0822-y.
И. Н. Пасечник1, ORCID: 0000-0002-8121-4160, pasigor@yandex.ru
Т. В. Новикова2, ORCID: 0000-0003-2732-3873, tatyana.novikova@danone.com
1 Федеральное государственное бюджетное учреждение дополнительного профессионального образования Центральная государственная медицинская академия Управления делами Президента Российской Федерации; 121359, Россия, Москва, ул. Маршала Тимошенко, 19, стр. 1А
2 Медицинский отдел Департамента cпециализированного питания Danone CIS; 143421, Россия, Московская область, Красногорский район, Новорижское шоссе 26 км, БЦ «Рига Ленд», блок В
Сведения об авторах:
Пасечник Игорь Николаевич, д.м.н., профессор, заведующий кафедрой анестезиологии и реаниматологии Федерального государственного бюджетного учреждения дополнительного профессионального образования Центральная государственная медицинская академия Управления делами Президента Российской Федерации; 121359, Россия, Москва, ул. Маршала Тимошенко, 19, стр. 1А; pasigor@yandex.ru
Новикова Татьяна Валериановна, медицинский менеджер направ-ления интенсивной терапии и неврологии, Медицинский отдел Департамента cпециализированного питания Danone CIS; 143421, Россия, Московская область, Красногорский район, Новорижское шоссе 26 км, БЦ «Рига Ленд», блок В; tatyana.novikova@danone.com
Information about the authors:
Igor N. Pasechnik, Dr. of Sci. (Med.), Professor, Head of department of Anesthesiology and Intensive Care at the Federal State Budgetary Institution of Additional Professional Education Central State Medical Academy of the Administrative Department of the President of the Russian Federation; 19 b.1A Marshal Timoshenko str., Moscow, 121359, Russia; pasigor@yandex.ru
Tatiana V. Novikova, М.D., Adult Medical Manager Critical Care& Neurology Danone Specialized Nutrition CIS, Nutricia Advanced LLC; block B BC Riga Land, 26 km Novorizhskoe highway, Krasnogorsky district, MR, 143421, Russia; tatyana.novikova@danone.com
Пролежни: новые подходы к лечению/ И. Н. Пасечник, Т. В. Новикова
Для цитирования: Пасечник И. Н., Новикова Т. В. Пролежни: новые подходы к лечению // Лечащий Врач. 2022; 4 (25): 38-43. DOI: 10.51793/OS.2022.25.4.007
Теги: пожилые пациенты, стационар, постельный режим, длительно лежащие больные
Для цитирования. Ахтямова Н.Е. Лечение пролежней у малоподвижных пациентов // РМЖ. 2015. № 26. С. 1549–1552.
По данным отечественной и зарубежной литературы, частота возникновения пролежней у малоподвижных пациентов составляет от 3 до 40%, достигая 80% у спинальных больных [1–10]. К группе риска возникновения пролежней относятся все люди с ограниченной подвижностью вследствие многообразных причин: заболеваний или травм спинного мозга, параличей, комы, онкологической патологии, длительного послеоперационного периода, продолжительного пребывания в отделениях реанимации и интенсивной терапии.
Во многих работах последних лет пролежни определяются как участки ишемии и некроза тканей вследствие нейротрофических нарушений. Этим подчеркиваются отсутствие иннервации в зоне поражения, низкая резистентность тканей и их слабая репаративная способность [4, 5]. К числу факторов, повышающих риск возникновения пролежней, относятся: пожилой возраст, дефицит питания, мышечная атрофия, курение, недержание мочи или кала, заболевания, сопровождающиеся нарушением микроциркуляции в тканях (облитерирующий атеросклероз, сахарный диабет).
Независимо от причины в основе патогенеза пролежней лежат нарушения трофики и защитных свойств кожи, развивающиеся вследствие тканевой гипоксии. Пролежни обычно развиваются в тех местах, где ткани испытывают интенсивное и продолжительное давление, особенно в области подкожных костных выступов. В лежачем положении у человека наибольшее давление – 40–60 мм рт. ст. испытывают области крестца, ягодиц, пяток и затылка. Согласно результатам экспериментальных исследований, имевших целью количественную оценку сдавливающего действия внешних факторов, установлено, что непрерывное давление 70 мм рт. ст. в течение 2 ч вызывает необратимые изменения в тканях. В то же время при прекращении давления каждые 5 мин в тканях возникают минимальные изменения без каких-либо последствий [5].
В ответ на давление первоначально ишемические изменения вследствие большей чувствительности к гипоксии развиваются прежде всего в мышечном слое над костным выступом. В условиях тканевой гипоксии увеличивается проницаемость капилляров с нарастанием тканевого отека, снижается напряжение кислорода в тканях, развиваются грубые нарушения структуры. Все это в итоге приводит к развитию трофических нарушений, которые впоследствии распространяются по направлению к коже. Последующая травматизация вследствие трения, смещения, мацерации и бактериальная контаминация кожи приводят к быстрому прогрессированию воспаления и некрозу [3–7].
В зависимости от расположения пациента (на спине, на боку, сидя в кресле) места сдавления тканей изменяются. Чаще всего это области ушной раковины, грудного отдела позвоночника, крестца, большого вертела бедренной кости, выступа малоберцовой кости, седалищного бугра, локтя, пяток. Реже пролежни появляются в области затылка, сосцевидного отростка, акромиального отростка лопатки, ости лопатки, латерального мыщелка, пальцев стоп. Наиболее типичной локализацией пролежней является крестцовая область. Около 36% случаев пролежней у малоподвижных пациентов развивается в этой области, 21% случаев приходится на области ягодиц, 25% – на пяточные области, 2–4% – на другие области [4, 11].
Длительно незаживающая раневая поверхность становится причиной хронической интоксикации, ведущей к анемии, гипопротеинемии, амилоидозу органов [1, 4, 5]. Являясь входными воротами для инфекции, пролежни часто становятся причиной сепсиса, в 20% заканчивающегося летальным исходом [4]. Летальность у больных с пролежневыми язвами, по данным различных авторов, колеблется в широких пределах – от 21 до 88,1% [1–8].
Течение пролежня подчиняется общим закономерностям раневого процесса, однако имеется и ряд особенностей, связанных с его развитием в условиях нервно-трофической дисфункции. Для определения исходного состояния пролежня и контроля за динамикой лечения оцениваются размер, форма пролежня, характер его краев и дна, состояние окружающих тканей. С целью объективизации данных о выраженности трофических расстройств была разработана классификация пролежней Pressure Ulcer Advisoriy Panel (1989), согласно которой выделяют 4 стадии пролежня (рис. 1) [9]:
• I стадия – кожный покров без повреждения, эпидермис интактен, отмечается эритема кожи в месте формирования пролежня, сохраняющаяся в течение 30 мин после изменения положения тела;
• II стадия – поверхностный дефект кожи в виде поражения эпидермиса, иногда с захватом дермы, что может проявляться в виде пузыря, который наполнен содержимым бурого цвета, на фоне эритемы кожи или в виде очага воспаления;
• III стадия – поражение кожи на всю ее толщину, образование язв с боковыми карманами; в центре язвенного образования, которое обращено внутрь, отмечаются очаги некроза и формирования свища за счет истончения кожного покрова;
• IV стадия – деструкция кожи и глубжележащих расположенных тканей; процесс некротизации захватывает подкожные структуры: фасции, мышцы и сухожилия, элементы сустава и костные образования.
В течении заболевания выделяют также этап первичной реакции, некротически-воспалительный этап и этап регенерации.
Проблема лечения пролежней у малоподвижных больных была и остается не только актуальной медицинской, но и социальной проблемой. При развитии пролежневых язв увеличивается продолжительность госпитализации пациента, появляется потребность в дополнительных перевязочных и лекарственных средствах, инструментарии, оборудовании. В ряде случаев требуется хирургическое лечение пролежней. Помимо экономических затрат, связанных с лечением пролежней, нужно учитывать и нематериальные затраты – тяжелые физические и моральные страдания, испытываемые пациентом.
Лечению пролежней посвящено большое количество работ как в отечественной, так и в зарубежной литературе [2–7, 9–11, 13, 14]. В них достаточно глубоко и подробно отражен патогенез развития пролежней, предлагаются многообразные классификации, методы профилактики и лечения, в т. ч. и хирургического, что свидетельствует о сложности и неоднозначности решения данной проблемы.
В лечении пролежней всегда необходим комплексный подход, направленный прежде всего на устранение основной причины – заболевания, вызвавшего появление пролежня, а также факторов, способствующих развитию пролежней. На каждой степени развития пролежня важно проводить профилактику его прогрессирования. Выбор локального лечения пролежней зависит от стадии процесса.
Пациенты с пролежнями I стадии не нуждаются в хирургическом лечении. Главными задачами лечения на этой стадии являются защита раны от инфекции и активная профилактика прогрессирования некротического изменения тканей. С целью предотвращения дальнейшего воздействия повреждающих факторов необходимо переворачивать пациента в кровати каждые 2 ч либо применять специальные средства для уменьшения локального давления на ткани. К последним относятся специальные кровати, матрацы, подушки, заполненные пеной, водой, воздухом, гелем или комбинацией этих материалов, оснащенные системами регулируемого давления и вибрации, обеспечивающие прерывистость давления. Следует соблюдать простые гигиенические правила ухода за лежачими больными, следить за чистотой и состоянием их кожи. Местное лечение формирующейся пролежневой язвы требует грамотного подхода и включает тщательную обработку области измененной кожи средствами, не обладающими ионообменными свойствами (физиологический раствор, камфорный спирт). Данный выбор средств имеет принципиальное значение, поскольку препараты, обладающие ионообменными свойствами (хлоргексидин, йодинол, повидон-йод и др.) нарушают проницаемость клеточных мембран, подавляют защитные функции клеток и создают благоприятные условия для развития микрофлоры и дальнейшего прогрессирования пролежня. После обработки пролежня важно применение средств, улучающих местное кровообращение и трофическое обеспечение тканей.
Пациенты с пролежнями II стадии также не нуждаются в хирургическом лечении. На этой стадии продолжается проведение активной профилактики прогрессирования некротического изменения тканей, достаточно ограничиться тщательной обработкой пролежневого дефекта, которая заключается в удалении общего загрязнения и эпидермиса в местах образования пузырей. Деэпителизированные участки кожи (так же как и на I стадии пролежневого процесса) не следует обрабатывать ионообменными антисептиками. Допустимо промывание раны физиологическим раствором, перекисью водорода. Для эпителизации измененных участков кожи в настоящее время в арсенале врача имеется широкое многообразие повязок, отличающихся по физическим свойствам, химическому составу, добавляемым в них лекарственным веществам [2] для лечения пролежневой раневой поверхности с учетом стадии, наличия или отсутствия некроза, площади поражения. Это и прозрачные пленочные повязки с клеящейся поверхностью, вафельные гидроколлоидные гидрогелевые повязки, полупроницаемые повязки на основе гидрополимера, губчатые повязки с верхним слоем из воздухопроницаемого полиуретана, который препятствует проникновению бактерий и жидкости.
Задачами лечения пролежней III стадии являются предупреждение дальнейшего прогрессирования некротического изменения подкожных тканей и удаление некрозов хирургическим путем, очищение пролежневой язвы от гнойного экссудата и остатков некроза, абсорбция отделяемого и предохранение заживающей раны от высыхания. Для местного лечения пролежней на этой стадии существует несколько групп препаратов, применение которых зависит от фазы раневого процесса. На этапе некротически-воспалительных изменений применяют местные антисептики (раствор Бeтaдина, мирамистин, перекись водорода, хлоргексидин), некролитические препараты (трипсин, химотрипсин, террилитин, коллагеназа), гиперосмолярные препараты и противовоспалительные средства (гидрокортизон, дексаметазон).
Значительное ослабление неприятного запаха из пролежневых язв достигается применением в качестве перевязочного материала 0,75% метронидазолового геля.
На этапе регенерации применяют стимуляторы репарации тканей (диоксометилтетрагидропиримидин, винилин, цинка гиалуронат, декспантенол).
На IV стадии формирования пролежня происходит глубокий некроз с вовлечением в патологический процесс мышц, сухожилий, суставных капсул и костей. Лечение заключается в некрэктомии, очищении пролежневой раны и стимуляции регенерации заживающей язвы. Медикаментозная терапия схожа с таковой, применяемой при лечении пролежней III стадии. Полное хирургическое иссечение всех мертвых тканей невозможно и нецелесообразно, поскольку точно определить границы некроза довольно сложно. Хирургическое очищение раны проводится с максимально возможным сохранением живых тканей в зонах суставных сумок, сосудисто-нервных пучков [4, 7].
В большинстве развитых стран мира, в т. ч. и у нас, пролежни у малоподвижных больных предпочитают лечить консервативно, что обусловлено экономическими причинами. Другой причиной низкой хирургической активности является высокий процент послеоперационных осложнений, обусловленных плохой подготовленностью пролежня к операции, остеомиелитом подлежащей кости, наличием высокопатогенной флоры, резистентной к большинству антибиотиков, большим натяжением краев раны, недостаточным уходом за больным после операции. В среднем, по данным разных авторов, только 50–75% пролежней после операции заживает первично. В остальных случаях необходима дополнительная, достаточно длительная консервативная терапия или повторная операция [2, 7, 9]. В ведущих клиниках мира, занимающихся проблемой лечения пролежней, пролежни II и III степени лечатся консервативно, операция выполняется только у больных с пролежнями IV степени.
По опыту лечения 695 пациентов с пролежнями различной локализации на фоне повреждения спинного мозга за период 1993–1997 гг. было показано, что основой лечения пролежней IV степени, длительно не заживающих или часто рецидивирующих пролежней II и III степени является оперативное вмешательство, что позволяет в десятки раз быстрее ликвидировать длительно существующие кожные язвы и значительно улучшить качество и продолжительность жизни пациентов [5]. Выбор метода хирургического лечения определяется размерами пролежня. Применяются иссечение пролежня с сопоставлением краев раны, свободная кожная пластика (аутодермопластика), пластика местными тканями, перемещенным кожным или кожно-мышечным лоскутом.
Обязательным условием для хирургического лечения пролежня является его тщательная комплексная предоперационная подготовка, которая может продолжаться от 2–3 мес. до 1 года.
Комплексное применение средств с рациональной антибактериальной терапией позволяет добиться быстрого очищения язвы и стабилизации состояния больного. Особенно эффективны мази на водорастворимой основе, поскольку они позволяют обеспечить выраженный дегидратационный эффект и положительно влияют на процессы заживления. Одним из эффективных антибактериальных препаратов является средство Бeтaдин, представляющее собой комплекс поливинилпирролидона и йода. Препарат обладает универсальным спектром активности: подавляет грамположительные бактерии, включая энтерококки и микобактерии, грамотрицательные бактерии, в т. ч. псевдомонады, ацинетобактерии, клебсиеллы, протей, споры бактерий, грибы, вирусы, включая вирусы гепатита В и С, энтеро- и аденовирусы, а также анаэробные, спорообразующие и аспорогенные бактерии [14–17].
Бактерицидное действие оказывает за счет образования белковых соединений йодаминов при контакте с белками бактериальной стенки или ферментными белками, в результате чего блокируется жизнедеятельность микроорганизмов. Благодаря большому размеру комплексной молекулы Бeтaдин плохо проникает через биологические барьеры, поэтому практически не проявляется системное действие йода. Проникновение в ткани на глубину около 1 мм не препятствует нормальным процессам регенерации. За счет постепенного высвобождения йода препараты Бeтaдина действуют длительно. Препарат выпускается в виде 10% раствора в зеленых пластмассовых флаконах по 30, 120 и 1000 мл; 10% мази в тубе по 20 г [17].
Исследования доказали высокую эффективность препарата Бeтaдин в сравнении с другими антисептиками (табл. 1) [17, 18].
Бeтaдин эффективнее других антисептиков подавляет размножение микроорганизмов даже в большом разведении (рис. 2). Физико-химические условия в ране и очаге воспаления (рН, белок, кровь, ферменты) мало влияют на действие Бeтaдина (рис. 3) [19].
При стационарном лечении пролежней неэффективность консервативной терапии и предоперационной подготовки, а также большинство послеоперационных осложнений, как правило, связаны с высокопатогенной флорой, резистентной к большинству антибиотиков. Исследования 1998 г. подтверждают исключительно высокую эффективность Бeтaдина в профилактике и лечении инфекционных осложнений, вызванных высокорезистентной патогенной микрофлорой (рис. 4) [17].
В одно из исследований по оценке эффективности применения препарата Бeтaдин при лечении 156 больных с инфицированными ранами были включены пациенты с пролежнями. Бeтaдин продемонстрировал эффективность, способствовал отчетливому регрессу воспалительного процесса в течение первых 5–7 сут. На фоне лечения исследуемым препаратом исчезал отек тканей вокруг участка поражения, уменьшалось количество гнойного отделяемого, исчезали или становились менее интенсивными боли в ране, уменьшались размеры ран. При применении Бeтaдина отмечено снижение обсемененности ран ниже критического уровня – менее 103 КОЕ/г к 7,2 сут. Появление первых грануляций зафиксировано к 10,2 и 13,5 сут. Первые признаки краевой эпителизации в 1-й группе возникали через 13,9 сут. Клиническое исследование показало, что Бeтaдин является эффективным средством при лечении инфицированных ран в I–II фазах раневого процесса. Побочных эффектов, таких как аллергические общие и местные реакции, при использовании Бeтaдина не наблюдалось, препарат хорошо переносился пациентами [13].
Эффективность препарата Бeтaдин, помимо его применения в терапии пролежней, показана в лечении пациентов с ожогами, трофическими язвами, суперинфекционными дерматитами, вирусными заболеваниями кожи, в т. ч. вызванными вирусом герпеса и вирусом папилломы человека, у гинекологических больных и подтверждена многочисленными клиническими исследованиями [15, 17].
В настоящий момент проблема лечения пролежней у малоподвижных пациентов является трудной задачей. Дифференцированный подход к лечению в зависимости от стадии процесса, а также комбинированный способ ведения ран с использованием сочетанного применения групп препаратов в соответствии с фазой раневого процесса могут быть использованы в клинической практике как эффективный подход к лечению пролежней у малоподвижных больных.
Хирургические методы лечения пролежней являются методами выбора у пациентов с пролежнями IV степени и длительно не заживающими или часто рецидивирующими пролежнями II и III степени. Обязательным условием для хирургического лечения пролежня является тщательная его подготовка к операции, включающая рациональную антибиотикотерапию.
Среди антибактериальных препаратов местного применения Бeтaдин выделяют за счет его универсального спектра активности, что делает его незаменимым при лечении пролежней у малоподвижных пациентов. Высокая эффективность даже при разведении и изменении физико-химических условий в ране позволяет с успехом использовать препарат для лечения пролежневых ран. Удобные формы препарата Бeтaдин (раствор, мазь) позволяют широко применять его в клинической практике.

![Пролежни [13] Пролежни [13]](https://probolezny.ru/media/bolezny/prolezhen/prolezhni-13_s.jpeg)
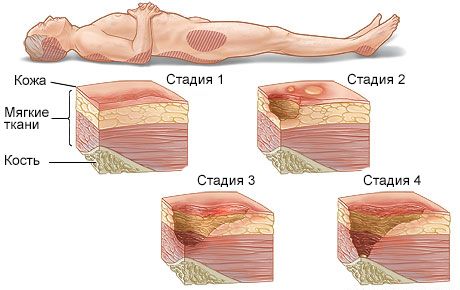
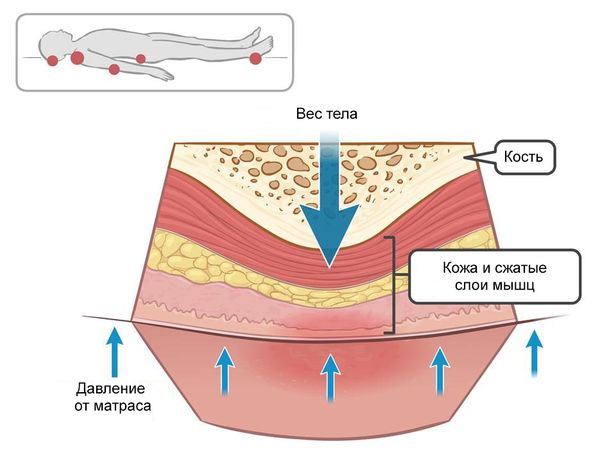

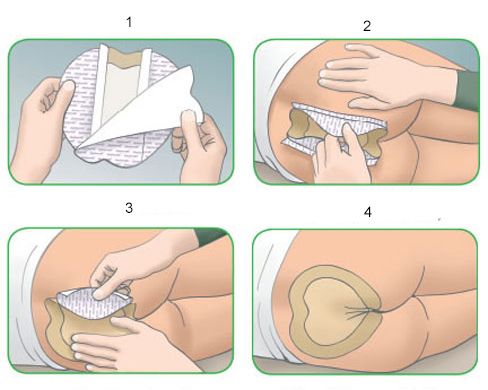
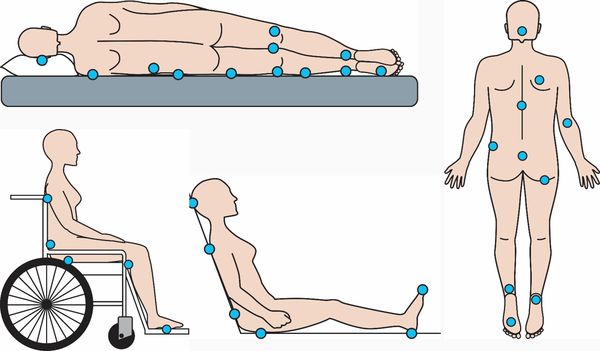





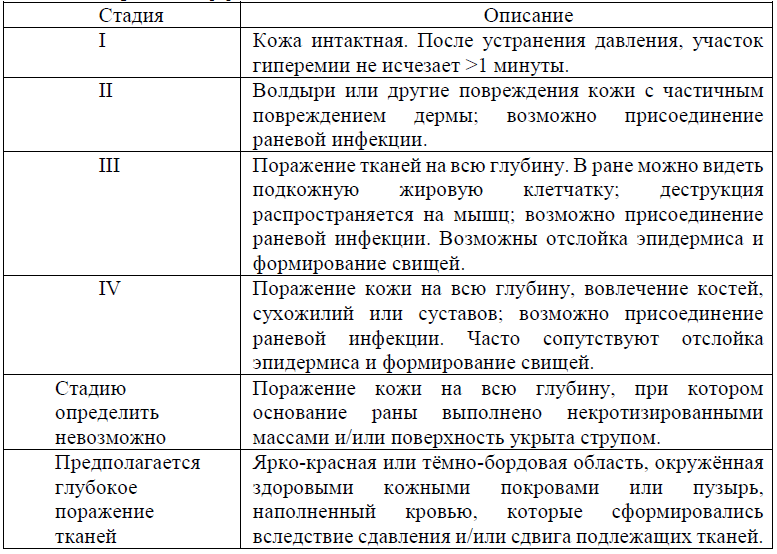
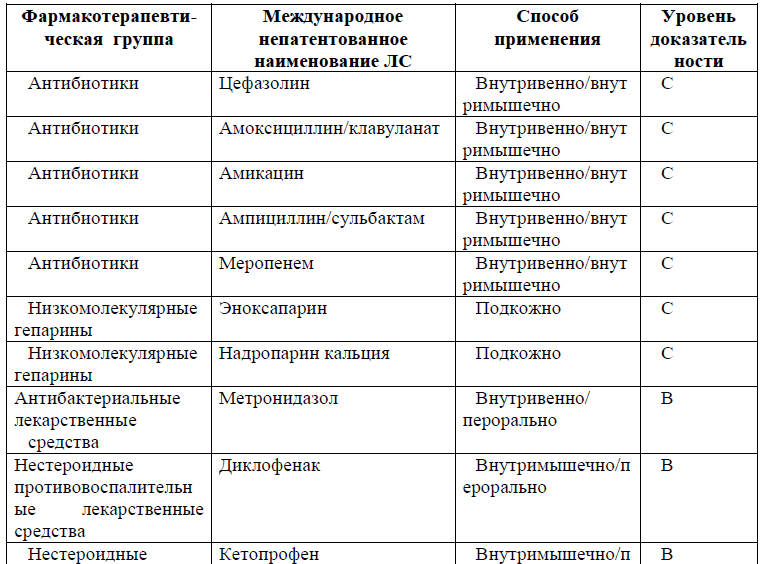
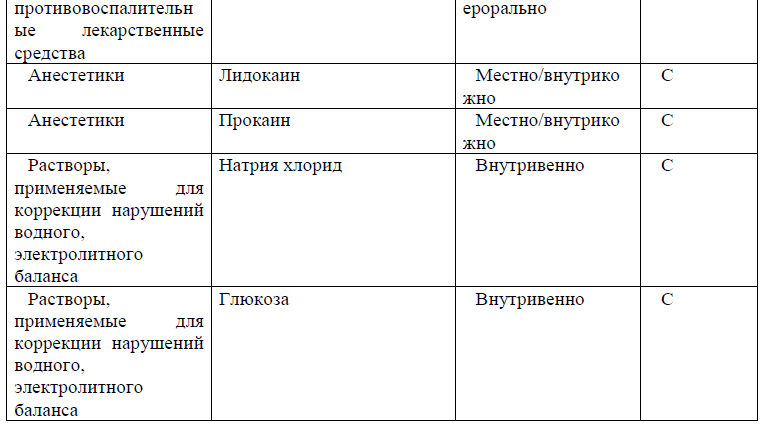
.png)
.png)
.png)
_575x.gif)
.png)
.gif)