МНН: Валсартан
Производитель: КРКА, д.д., Ново Место
Анатомо-терапевтическо-химическая классификация: Valsartan
Номер регистрации в РК:
№ РК-ЛС-5№019063
Информация о регистрации в РК:
23.10.2017 — 23.10.2022
Номер регистрации в РБ:
9941/12/17
Информация о регистрации в РБ:
06.09.2017 — бессрочно
Информация о реестрах и регистрах
- Скачать инструкцию медикамента
Торговое название
ВАЛЬСАКОР®
Международное непатентованное название
Валсартан
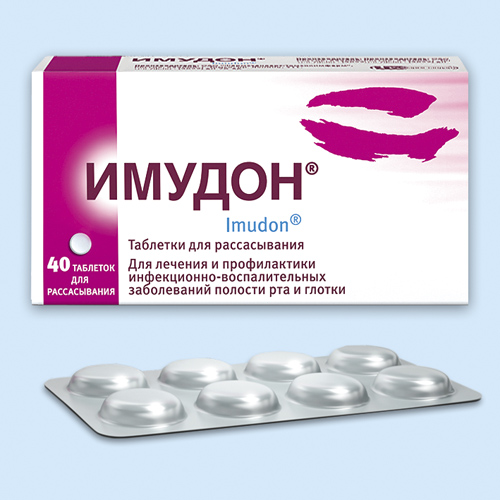
Лекарственная форма
Таблетки, покрытые пленочной оболочкой 320 мг
Состав
Одна таблетка содержит
активное вещество — валсартан 320.00 мг,
вспомогательные вещества: лактозы моногидрат, целлюлоза микрокристаллическая, повидон К-25, кроскармелоза натрия, кремния диоксид коллоидный безводный, магния стеарат,
состав оболочки: гипромеллоза 6 ср, титана диоксид (Е171), ), железа (III) оксид желтый (Е172), железа (III) оксид красный (Е172)? макрогол 4000.
Описание
Таблетки капсуловидной формы, с двояковыпуклой поверхностью, риской на одной стороне, покрытые пленочной оболочкой светло-коричневого цвета
Фармакотерапевтическая группа
Препараты, влияющие на систему ренин-ангиотензин. Ангиотензина II антагонисты.
Код АТС С09СА03
Фармакологические свойства
Фармакокинетика
Всасывание:
После приема Cmax валсартана достигается в течение 2-4 часов. Средняя абсолютная биодоступность составляет 23%. При назначении с пищей AUC уменьшается на 40%, и Cmax на 50%, однако, спустя 8 часов после приема концентрация валсартана в крови становится одинаковой у пациентов, принимавших препарат с пищей и у тех, кто получал препарат отдельно. Уменьшение AUC не сопровождается клинически значимым снижением терапевтического эффекта препарата. Поэтому валсартан можно принимать не зависимо от приема пищи.
Распределение
Равновесный объем распределения валсартана после внутривенного введения составляет приблизительно 17 литров, который указывает на то, что валсартан активно не проникает в ткани. Валсартан имеет высокую связь с сывороточными белками (94-97%), в основном с сывороточным альбумином.
Биотрансформация
Валсартан не подвергается активной биотрансформации, только 20% вещества распадается на метаболиты. Гидроксиметаболиты обнаруживаются в плазме крови в низких концентрациях (менее 10% AUC валсартана). Данный метаболит не является фармакологически активным.
Выведение
Кинетика валсартана носит многоэкспоненциальный характер ((t1/2α<1 ч. и t1/2β около 9 ч).).
Валсартан выделяется с желчью и выводится с калом (около 83% дозы) и через почки с мочой (около 13% дозы) в основном в неизмененном виде. После внутривенного введения клиренс плазмы составляет около 2 л/ч и почечный клиренс 0.62 л/ч (около 30% общего клиренса). Период полураспада валсартана составляет 6 часов.
Пожилые пациенты
У пожилых пациентов было отмечено немного более высокое системное воздействие валсартана по сравнению с молодыми испытуемыми. Однако, эта разница не имеет клинической значимости.
Нарушение функции почек
Как и в случае с веществами, где клиренс составляет всего 30% от общего клиренса плазмы, связи между функцией почек и системным воздействием валсартана не было установлено. Поэтому для пациентов с нарушениями функции почек не требуется специальный подбор дозы препарата (клиренс креатина <10 мл/мин). На сегодняшний день нет данных по безопасности валсартана для пациентов с клиренсом креатина >10 мл/мин, а также пациентов, которым проводится диализ. Поэтому в случае с этими пациентами необходимо соблюдать осторожность при назначении валсартана. Валсартан хорошо связывается с белками плазмы и не выводится диализом.
Печеночная недостаточность
Примерно 70% усвоенной дозы препарата выводится с желчью в неизмененной форме. В отличие от здоровых испытуемых, у пациентов с легкой и средней степенью печеночной недостаточности наблюдалось увеличение AUC вдвое. Однако, связи между концентрацией валсартана в плазме и тяжестью нарушений функции печени не было выявлено.
Фармакодинамика
Валсартан является активным при пероральном введении, сильнодействующим, специфическим антагонистом рецепторов ангиотензина II (Ang II). Он действует избирательно на AT1 тип рецепторов, которые отвечают за известные эффекты ангиотензина II. Повышение в плазме уровня ангиотензина II после блокады валсартаном рецепторов AT1 типа, может стимулировать незаблокированный рецептор AT2, нейтрализующий действие рецептора AT1. Валсартан не оказывает эффекта частичного антагониста на рецептор AT1 и гораздо быстрее (примерно в 20 000 раз) связывается с рецептором AT1, чем с AT2 рецептором. Валсартан также связывает или блокирует другие рецепторы гормонов или ионных каналов, которые играют важную роль в работе сердечно-сосудистой системы.
Валсартан не подавляет действие ангиотензинпревращающего фермента (также известного как кининаза II), который превращает Ang I в Ang II и осуществляет распад брадикинина. Из-за отсутствия влияния на ангиотензинпревращающий фермент и потенцирование брадикинина или вещества Р, антагонисты рецепторов ангиотензина II не вызывают кашля. В клинических исследованиях, где действие валсартана сравнивалось с действием ингибитора ангиотензинпревращающего фермента, число случаев появления сухого кашля было значительно меньше (P<0.05) среди пациентов, которые получали валсартан по сравнению с теми, кто принимал ингибитор ангиотензинпревращающего фермента (2.6% против 7.9%). В клинических исследованиях среди пациентов, у которых в прошлом был сухой кашель во время лечения ингибитором ангиотензинпревращающего фермента, кашель наблюдался у 19.5% исследуемых, получающих валсартан и 19.0%, получающих тиазидный диуретик, в сравнении с 68.5% исследуемых, получавших ингибитор ангиотензинпревращающего фермента (P<0.05).
Прием валсартана пациентами с гипертензией ведет к понижению артериального давления, не влияя на частоту пульса.
У большинства пациентов после приема однократной дозы антигипертензивный эффект развивается в течение 2 часов, достигая пика снижения артериального давления через 4-6 часов и сохраняется в течение 24 часов. При регулярном приеме значительный антигипертензионный эффект наблюдается в течение 2 недель, достигает максимального эффекта в течение 4 недель и сохраняется при длительном лечении. При одновременном приеме с гидрохлоротиазидом достигается дополнительный значительный антигипертензионный эффект. При резком прекращении приема валсартана не возникает «рикошетная» гипертензия или какие-либо другие нежелательные реакции.
У пациентов с гипертензией, диабетом 2 типа и микроальбуминурией, прием валсартана вызывает понижение количества альбумина в моче. Исследования эффективности валсартана в понижении содержания альбумина в моче у пациентов гипертензией (АД=150/88 мм рт. ст) с диабетом 2 типа, альбуминурией (среднее значение=102 мг/мин; 20-700 мг/мин) и сохраненной функцией почек (средний креатинин в сыворотке крови = 80 ммоль/л), показали, что прием валсартана влияет на снижение альбумина в моче у пациентов с гипертензией и диабетом 2 типа в дозе 160-320 мг.
Показания к применению- эссенциальная гипертензия
Способ применения и дозы
Рекомендуемая начальная доза валсартана составляет 80 мг один раз вдень. Понижение высокого артериального давления наблюдается в течение 2-х недель, максимальный эффект от приема препарата достигается в течение 4-х недель. Пациентам, у которых артериальное давление не контролируется должным образом, следует увеличить дозу до 160 мг или максимум до 320 мг.
Валсартан можно принимать с другими антигипертензивными препаратами. Одновременный прием диуретиков, таких как гидрохлоротиазид, способствует большему снижению артериального давления.
Валсартан принимают, запивая водой, не зависимо от приема пищи.
У пациентов пожилого возраста коррекция дозы не требуется.
Пацентам с нарушенной функцией почек
Коррекция дозы у пациентов с клиренсом креатинина >10 мл/мин или 0.167 мл/с не требуется.
Пациентам с нарушенной функцией печени
У пациентов с легкой и умеренной печеночной недостаточностью без холестаза, доза валсартана не должна превышать 80 мг. Валсартан противопоказан пациентам с тяжелыми нарушениями функции печени и пациентам с холестазом.
Побочные действия
Показатели безопасности, полученные в контролируемых клинических исследованиях среди пациентов, перенесших инфаркт миокарда и/или с сердечной недостаточностью, отличаются от общих показателей безопасности для пациентов с гипертензией. Это может иметь отношение к основному заболеванию этих пациентов.
Побочные эффекты, возникающие у пациентов с гипертензией:
Не часто (от >1/1,000 до <1/100):
-головокружение
-кашель
-боль в области живота
— утомляемость
Частота возникновения не известна:
— снижение уровня гемоглобина и гематокрита, нейтропения,
тромбоцитопения
— реакции повышенной чувствительности, включая сывороточную болезнь
— повышение содержания калия в сыворотке крови
— васкулит
— повышение показателей функции печени, включая увеличение уровня
билирубина в сыворотке крови
— отек Квинке, сыпь, зуд
-мышечные боли
-почечная недостаточность и нарушения функции почек, повышение креатинина в сыворотке крови
Побочные эффекты, возникающие у пациентов, перенесших инфаркт миокарда и/или с сердечной недостаточностью:
Часто (от >1/100 до <1/10):
-головокружение, постуральное головокружение
-гипотензия, ортостатическая гипотензия
-почечная недостаточность и нарушения функции почек
Не часто (от >1/1,000 до <1/100):
-гиперкалиемия
-обморок, головная боль
-вертиго
— сердечная недостаточность
-кашель
-тошнота, диарея
-отек Квинке
-острая почечная недостаточность, повышение уровня креатинина в сыворотке крови
-астения, слабость
Частота возникновения не известна:
— васкулит
— повышение показателей функции печени
— сыпь, зуд
— мышечные боли
— повышение уровня мочевины в крови
Противопоказания
— повышенная чувствительность к любому компоненту препарата
— тяжелые нарушения функции печени, билиарный цирроз и холестаз
— беременность и период лактации
— детский и подростковый возраст до 18 лет (безопасность и
эффективность не установлены)
Лекарственные взаимодействия
Одновременный прием с другими ЛС не рекомендуется.
Литий
Сообщалось о повышения соли лития в сыворотке крови во время одновременного приема валсартана с ингибиторами ангиотензинпревращающего фермента. В виду недостаточного опыта одновременного применения валсартана и соли лития, комбинация данных препаратов не рекомендуется. В случае, если одновременный прием данных препаратов необходим, следует проводить тщательный мониторинг уровня соли лития в сыворотке крови.
Калиевые добавки, калийсберегающие диуретики, заменители соли, содержащие калий и другие препараты, повышающие уровень калия
В случае, если при приеме валсартана требуется прием ЛС, влияющих на уровень калия, необходим мониторинг уровня калия в плазме крови.
Меры предосторожности при совместном применении
Нестероидные противовоспалительные препараты (НПВП), включая селективные ингибиторы СОХ-2, ацетилсалициловой кислоты( > 3 г/ в день) и неселективные НПВП.
При одновременном приеме антагонистов ангиотензина II и НПВП, может возникнуть уменьшение антигипертензивного эффекта. Кроме того, при одновременном применении антагонистов ангиотензина II и НПВП существует повышенный риск ухудшения функции почек и увеличения уровня калия в сыворотке крови. Поэтому, в начале лечения рекомендуется проводить мониторинг функции почек и адекватной гидратации пациента.
Другие ЛС
В исследовании взаимодействия валсартана с другими лекарственными средствами, не было выявлено клинически значимого взаимодействия со следующими препаратами: циметидин, варфарин, фуросемид, дигоксин, атенолол, индометацин, гидрохлортиазид, амлодипин, глибенкламид.
Особые указания
Гиперкалиемия
Одновременный прием с калиевыми добавками, калийсберегающими диуретиками, заменителями соли, содержащими калий или другими препаратами, повышающими уровень калия (гепарин и др.) не рекомендуется. Следует проводить мониторинг уровня калия.
Пациенты с пониженным уровнем натрия и/или межклеточной жидкости
У пациентов с пониженным уровнем натрия и/или межклеточной жидкости, получающих высокие дозы диуретиков, после начала лечения валсартаном в редких случаях может появиться симптоматическая гипотензия. Перед началом лечения валсартаном необходимо произвести корректировку уровня натрия и/или межклеточной жидкости, например, снизив дозу диуретика.
Стеноз почечной артерии
Для пациентов с двусторонним или односторонним стенозом почечной артерии безопасность применения валсартана не установлена.
Прием валсартана в течение короткого времени 12 пациентами с вазоренальной гипертензией вследствие одностороннего стеноза почечной артерии значительно не повлиял на почечную гемодинамику, уровень креатинина в сыворотке крови или мочевину крови. Однако, другие препараты, влияющие на ренин-ангиотензиновую систему могут повысить мочевину крови и уровень креатинина у пациентов с односторонним стенозом почечной артерии, поэтому во время лечения валсартаном рекомендуется проводить мониторинг функции почек.
Трансплантация почек
В настоящее время достаточного опыта применения валсартана для пациентов, недавно перенесшим трансплантацию почки, нет.
Первичный гиперальдостеронизм
Пациенты с первичным гиперальдостеронизмом не должны принимать валсартан, поскольку их ренин-ангиотензиновая система не активизирована.
Стеноз устья аорты и митрального клапана, гипертрофическая обструктивная кардиомиопатия
Как и в случае с другими сосудорасширяющими средствами при лечении валсартаном пациентов со стенозом устья аорты и митрального клапана, гипертрофической обструктивной кардиомиопатией (ГОКМ) требуется особая осторожность.
Нарушение функции почек
Для пациентов с клиренсом креатинина >10 мл/мин или 0.167 мл/с корректировка дозы не требуется. В настоящее время опыт безопасного применения препарата для пациентов с клиренсом кретинина <10 мл/мин или 0.167 мл/с и пациентов, проходящих диализ, отсутствует. Поэтому в лечении валсартаном этой категории пациентов следует соблюдать осторожность.
Печеночная недостаточность
В лечении препаратом пациентов с легкой или средней степенью печеночной недостаточности без холестаза следует соблюдать осторожность.
Беременность
Во время беременности противопоказан прием антагонистов рецепторов ангиотензина II (АРА II). До тех пор, пока лечение антагонистами рецепторов ангиотензина II является необходимым, пациентки, планирующие беременность, должны перейти на прием альтернативных антигипертензивных препаратов для снижения артериального давления, которые безопасны для применения во время беременности. После подтверждения беременности лечение антагонистами рецепторов ангиотензина II следует прекратить немедленно, и при необходимости следует начать альтернативное лечение.
Другие условия при стимуляции ренин-ангиотензиновой системы
В случае с пациентами, у которых функция почек зависит от активности ренин-ангиотензиновой системы (например, у пациентов с тяжелой застойной сердечной недостаточностью) лечение ингибиторами ангиотензинпревращающих ферментов приводит к олигурии и/или прогрессирующей азотемии, а в редких случаях к острой почечной недостаточности и/или смерти. В виду того, что валсартан является антагонистом ангиотензина II, нельзя исключать вероятность того, что он может вызвать почечную недостаточность.
Лактоза
Вальсакор содержит лактозу. Пациенты с редкими наследственными формами непереносимости галактозы, лактазной недостаточностью или глюкозо-галактозной мальабсорбцией не должны принимать данный препарат.
Особенности влияния лекарственного средства на способность управлять транспортным средством или потенциально опасными механизмами
При управлении автотранспортом или другими механизмами, следует учитывать вероятность возникновения головокружения и утомления.
Передозировка
Симптомы — артериальная гипотензия, угнетенный уровень сознания, сосудистая недостаточность и/или шок.
Лечение: если препарат был принят внутрь недавно, рекомендуется спровоцировать рвоту и промыть желудок. При развитии артериальной гипотензии пациент должен находиться в положении лежа на спине, при этом необходимо провести коррекцию объема циркулирующей крови ( внутривенно вводят изотонический раствор натрия хлорида).
Гемодиализ не эффективен.
Форма выпуска и упаковка
По 14 таблеток помещают в контурную ячейковую упаковку из пленки PVC/PE/PVDC и фольги алюминиевой.
По 2 контурных ячейковых упаковок вместе с инструкцией по медицинскому применению на государственном и русском языках помещают в пачку из картона.
Условия хранения
Хранить в оригинальной упаковке при температуре не выше 25 ºС.
Хранить в недоступном для детей месте!
Срок хранения
2 года
Не применять по истечении срока хранения.
Условия отпуска из аптек
По рецепту
Производитель
КРКА, д.д. Ново место, Словения
Владелец регистрационного удостоверения
КРКА, д.д., Ново Место, Словения
Адрес организации, принимающей на территории Республики Казахстан претензии от потребителей по качеству продукции (товара)
Представительство «КРКА, д.д. Ново место» в РК
РК, 050059, г. Алматы, пр. Аль-Фараби, 5/1, секция 1б, 2-й этаж
тел.: +7 (727) 311 08 09
факс: +7 (727) 311 08 12
www.krka.si
| 735793441477977023_ru.doc | 81.5 кб |
| 269178581477978200_kz.doc | 94 кб |
| 9941_12_17_p.pdf | 0.38 кб |
| 9941_12_17_s.pdf | 1.09 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники. «Центр экспертиз и испытаний в здравоохранении» МЗ РБ
1 таблетка, покрытая оболочкой, содержит:
Активное вещество: валсартан 40 мг, 80 мг, 160 мг или 320 мг
Вспомогательные вещества: лактоза моногидрат, целлюлоза микрокристаллическая, кроскармеллоза натрия, повидон К29-32, тальк, магния стеарат, кремния диоксид коллоидный.
Оболочка:
Для таблеток 40 мг: Опадрай II 85G32407 Желтый (поливиниловый спирт, тальк, титана диоксид (Е171), макрогол — 3350, краситель железа оксид желтый (Е172), лецитин (Е322)).
Для таблеток 80 мг: Опадрай II 85G34643 Розовый (поливиниловый спирт, тальк, титана диоксид (Е171), макрогол — 3350, краситель железа оксид желтый (Е172), краситель железа оксид красный (Е172), лецитин (Е322)).
Для таблеток 160 мг: Опадрай II 85G32408 Желтый (поливиниловый спирт, тальк, титана диоксид (Е171), макрогол — 3350, краситель железа оксид желтый (Е172), краситель железа оксид красный (Е172), лецитин (Е322)).
Для таблеток 320 мг: Опадрай II 85G20236 Коричневый (поливиниловый спирт, тальк, титана диоксид (Е171), макрогол — 3350, лецитин (Е322), краситель солнечный закат желтый алюминиевый лак (Е110), краситель железа оксид черный (Е172)).
Антагонисты ангиотензина II, валсартан.
Код ATX: С09СА03
Для таблеток 40 мг: овальные двояковыпуклые таблетки желтого цвета, покрытые оболочкой, с риской с одной стороны, боковыми рисками и маркировкой «V» с другой стороны, с размерами около 9,0*4,5 мм.
Для таблеток 80 мг: круглые двояковыпуклые таблетки розового цвета, покрытые оболочкой, с риской с двух сторон, боковыми рисками и маркировкой «V» с одной стороны, диаметром около 8,0 мм.
Для таблеток 160 мг: овальные двояковыпуклые таблетки желтого цвета, покрытые оболочкой, с риской с одной стороны, боковыми рисками и маркировкой «V» с другой стороны, с размерами около 15,0*6,5 мм.
Для таблеток 320 мг: овальные двояковыпуклые таблетки коричневого цвета, покрытые оболочкой, с риской с одной стороны, боковыми рисками и маркировкой «V» с другой стороны, с размерами 19,0*8,2 мм.
Фармакологическое действие
Фармакодинамика
Валсартан является активным специфическим блокатором (антагонистом) рецепторов ангиотензина II (БРА), предназначенным для приема внутрь. Он действует избирательно на рецепторы подтипа АТ1, которые ответственны за действие ангиотензина II. Повышенные уровни ангиотензина II в плазме вследствие блокады АТ1-рецепторов валсартаном могут стимулировать незаблокированные АТ2-рецепторы, которые ypaвновешивают эффект АТ1-рецепторов. Валсартан не проявляет какой-либо активности агониста в отношении АТ1-рецепторов, но обладает большим (примерно в 20000 раз) сродством к AT1-рецепторам, чем к АТ2-рецепторам.
Валсартан не угнетает ангиотензинпревращающий фермент (АПФ), известный также под названием кининазы II, который превращает ангиотензин I в ангиотензин II и влияет на систему брадикинина. В клинических испытаниях, в которых валсартан сравнивали с ингибитором АПФ, частота развития сухого кашля была значительно ниже (р<0,05) у пациентов, получавших валсартан, чем у пациентов, получавших ингибитор АПФ (2,6% против 7,9% соответственно). В клинических исследованиях у пациентов с кашлем в анамнезе во время терапии ингибиторами АПФ сухой кашель отмечался у 19,5% пациентов, переведенных на валсартан и 19,0% пациентов, получавших тиазидные диуретики по сравнению с 68,5% пациентов, получавших ингибитор АПФ.
Применение лекарственного средства у пациентов с артериальной гипертензией приводит в итоге к снижению артериального давления без влияния на частоту пульса.
Начало эффекта отмечается через 2 ч после приема внутрь, максимум — через 4-6 ч; продолжительность действия — более 24 ч. После регулярного приема максимальное снижение артериального давления (АД) наступает через 2-4 недели. Отсутствует синдром «отмены» при внезапном прекращении приема.
Фармакокинетика
После приема внутрь абсорбция — быстрая, степень всасывания вариабельна. Среднее значение абсолютной биодоступности — 23%. Фармакокинетическая кривая валсартана имеет нисходящий мультиэкспоненциальный характер (t½α <1 ч и t½β около 9 ч).
В диапазоне изученных доз кинетика валсартана имеет линейный характер. При повторном применении валсартана изменений кинетических показателей не отмечалось. При приеме дозы 1 раз в день наблюдалась незначительная кумуляция валсартана. Концентрация валсартана в плазме крови не имеет различий у мужчин и женщин.
Валсартан хорошо связывается с белками плазмы крови (94-97%), преимущественно с сывороточными альбуминами. При достижении равновесного состояния объем распределения — 17 л. По сравнению с печеночным кровотоком (около 30 л/ч), плазменный клиренс валсартана происходит относительно медленно (около 2 л/ч). Лекарственное средство выводится с желчью и почками, преимущественно в неизменном виде. При нормальном уровне гломерулярной фильтрации (120 мл/мин) почечный клиренс составляет около 30% от общего плазменного клиренса. Гидроксиметаболит обнаруживается в плазме крови в низких концентрациях (менее 10% от площади под кривой «концентрация-время» (AUC) для валсартана). Данный метаболит фармакологически не активен. После приема внутрь 83% валсартана выводится через кишечник и 13% через почки, преимущественно в неизменном виде.
При приеме лекарственного средства с пищей AUC валсартана уменьшается на 48%, хотя, начиная примерно с 8-го часа после приема лекарственного средства, концентрации валсартана в плазме крови как в случае приема его натощак, так и в случае приема с пищей, одинаковые. Уменьшение AUC не сопровождается клинически значимым уменьшением терапевтического эффекта валсартана, поэтому лекарственное средство можно применять независимо от приема пищи.
Выведение
Для валсартана наблюдается многоэкспоненциональная динамика распада (t½α <1 ч, t½β около 9 ч). Валсартан выводится главным образом с каловыми массами 83% и с мочой 13%, в основном в виде неизмененного вещества.
После внутривенного введения клиренс валсартана в плазме составляет 2 л/ч, его почечный клиренс составляет 0,62 л/ч (около 30% от общего клиренса).
Период полураспада валсартана составляет 6 часов.
Фармакокинетика отдельных групп пациентов
Пожилые пациенты
У некоторых пациентов пожилого возраста (>65 лет) системное воздействие валсартана было несколько более выражено, чем у пациентов молодого возраста; но это не имело клинического значения.
Пациенты с нарушением функции почек
Для соединений, почечный клиренс которых составляет менее 30% общего плазменного клиренса, отсутствует корреляция между функцией почек и системным воздействием. Поэтому у пациентов с нарушением функции почек коррекция дозы лекарственного средства не требуется. В настоящее время отсутствует опыт по безопасному применению валсартана у пациентов на диализе. Валсартан сильно связан с белками плазмы и его удаление в ходе диализа маловероятно.
Пациенты с нарушением функции печени
Приблизительно 70% дозы после всасывания выводится с желчью, преимущественно в неизмененной форме. Валсартан не подвергается биотрансформации, поэтому до сих пор не доказана связь между концентрацией валсартана в плазме и степенью нарушения функции печени. Поэтому не требуется корректировка дозы у пациентов с нарушением функции печени небилиарного происхождения и без холестаза. У пациентов с билиарным циррозом или холестазом AUC валсартана увеличивался в два раза. (см. разделы «Противопоказания», «Способ применения и дозы», «Меры предосторожности»).
Пациенты с сердечной недостаточностью
У пациентов с сердечной недостаточностью время достижения максимального уровня в плазме и период полувыведения валсартана аналогичны у здоровых добровольцев. Значения AUC и Сmax валсартана линейно увеличиваются в диапазоне клинических доз (от 40 мг до 160 мг два раза в день) и почти пропорционально увеличению дозы. Средний коэффициент накопления составляет около 1,7. Клиренс валсартана составляет приблизительно 4,5 л/ч после перорального введения. Возраст не влияет на клиренс у пациентов с сердечной недостаточностью.
Педиатрические пациенты
В исследовании у 26 детей с артериальной гипертензией (в возрасте от 1 до 16 лет), получавших однократную дозу суспензии валсартана (в среднем 0,9-2 мг/кг, максимальная доза 80 мг), клиренс (л/час/кг) валсартана был сопоставим у детей разного возраста внутри возрастной группы 1-16 лет и аналогичен таковому у взрослых, получавших лекарственное средство в той же лекарственной форме (см. раздел «Меры предосторожности»).
— Артериальная гипертензия (40 мг, 80 мг, 160 мг, 320 мг) у взрослых и детей от 6 до 18 лет (см. разделы Противопоказания, Меры предосторожности, Взаимодействие с другими лекарственными средствами, Фармакодинамика).
Сердечная недостаточность (40 мг, 80 мг, 160 мг): лечение сердечной недостаточности с клинической симптоматикой у взрослых пациентов, с непереносимостью ингибиторов ангиотензинпревращающего фермента (иАПФ), или в качестве дополнительной терапии к иАПФ у пациентов, с непереносимостью бета-блокаторов, если нельзя использовать антагонисты минералокортикоидных рецепторов (см. разделы Способ применения и дозы, Меры предосторожности, Взаимодействие с другими лекарственными средствами, Фармакодинамика).
Недавно перенесенный инфаркт миокарда (40 мг, 80 мг, 160 мг) (у клинически стабильных взрослых пациентов с клиническими проявлениями сердечной недостаточности или бессимптомной систолической дисфункцией левого желудочка после перенесенного (12 часов — 10 дней) инфаркта миокарда).
Повышенная чувствительность к валсартану или к вспомогательным веществам, входящим в состав лекарственного средства. Валз противопоказан пациентам с наследственной ангиодистрофией или с историей развития ангионевротического отека при лечении ингибиторами АПФ или антагонистами рецептора ангиотензина II.
Тяжелые нарушения функции печени, билиарный цирроз и холестаз.
Беременность (см. раздел «Применение при беременности и в период лактации»).
Одновременное применение блокаторов рецепторов ангиотензина II, в том числе, валсартана, с алискиреном у пациентов с сахарным диабетом или почечной недостаточностью (СКФ <60 мл/мин/1,73м2).
Применение в период беременности или грудного вскармливания
Как и другие лекарственные средства, напрямую воздействующие на ренин-ангиотензин-альдостероновую систему (РААС), Валз нельзя применять при беременности (см. раздел Противопоказания).
Пациенткам, планирующим беременность, в случае необходимости должно быть назначено альтернативное антигипертензивное лечение, которое имеет установленный профиль безопасности для применения во время беременности. Когда беременность обнаружена, лечение блокаторами рецепторов ангиотензина II (БРА) должно быть немедленно прекращено и, при необходимости, должно быть назначено альтернативное лечение. Эпидемиологические данные показали повышенный риск тератогенного воздействия при применении иАПФ в первом триместре беременности. Подобный риск может существовать также при приеме БРА.
Известно, что прием БРА во втором и третьем триместрах беременности вызывает фетотоксичность (снижение функции почек, маловодие, задержка окостенения черепа) и неонатальную токсичность (почечная недостаточность, артериальная гипотензия, гиперкалиемия).
Если женщина принимала БРА во втором триместре беременности, необходимо УЗИ контроль функции почек и черепа плода. Новорожденные, матери которых принимали БРА, должны внимательно наблюдаться из-за возможной артериальной гипотензии.
Не рекомендуется применять Валз во время грудного вскармливания, так как отсутствует информация о применении валсартана во время кормления грудью. Предпочтительно использовать альтернативные методы лечения с установленным профилем безопасности, особенно если ребенок новорожденный или недоношенный.
Внутрь, независимо от приема пищи, запивая достаточным количеством жидкости. Риска на таблетках предназначена для деления на две равные дозы.
Артериальная гипертензия
Рекомендуемая начальная доза лекарственного средства составляет 80 мг 1 раз в день. Гипотензивный эффект развивается в первые 2 недели терапии. Максимальный эффект достигается после 4-х недель приема лекарственного средства. У пациентов, для которых суточная доза 80 мг не дает желаемого терапевтического эффекта, рекомендуется увеличить суточную дозу до 160 мг, или, максимально, до 320 мг.
Дополнительно может быть назначено другое антигипертензивное средство (например, диуретик).
Сердечная недостаточность (СН)
Рекомендуемая начальная доза лекарственного средства Валз составляет 40 мг 2 раза в сутки. При недостаточном терапевтическом эффекте требуется постепенное повышение дозы до 80 мг 2 раза в сутки и при хорошей переносимости — до 160 мг 2 раза в сутки. От момента начала лечения лекарственным средством Валз до момента достижения приема максимальной дозировки должен быть интервал не менее двух недель. Максимальная суточная доза — 320 мг в 2 приема. Возможно снижение доз при одновременном приеме диуретиков.
Валз может применяться в комбинации с другими лекарственными средствами, предназначенными для лечения хронической сердечной недостаточности. Однако не рекомендуется тройная комбинация ингибитора АПФ, валсартана и бета-блокатора или калийсберегающего диуретика (см. разделы «Фармакодинамика», «Меры предосторожности»). Оценка состояния пациентов с сердечной недостаточностью должна всегда включать мониторинг функции почек.
После перенесенного инфаркта миокарда
При стабильных показателях гемодинамики лечение можно начинать в течение 12 ч после острого инфаркта миокарда. Начальная доза — ½ таблетки 40 мг (20 мг) 2 раза в сутки, с последующим увеличением дозы до 40 мг, 80 мг, 160 мг 2 раза в сутки в течение нескольких недель, до достижения максимальной суточной дозы 160 мг 2 раза в сутки.
Достижение дозы 80 мг 2 раза в сутки рекомендуется к концу 2-й недели лечения, 160 мг 2 раза в сутки — к концу 3-го месяца терапии. Дозу следует повышать, основываясь на переносимости лекарственного средства пациентом.
В случае симптоматической артериальной гипотензии или при нарушении функции почек дозу лекарственного средства Валз следует снизить.
Оценка состояния пациентов после инфаркта всегда должна включать мониторинг функции почек.
Валсартан может использоваться у пациентов, получавших другие лекарственные средства, рекомендованные после инфаркта миокарда (такие, как тромболитики, ацетилсалициловая кислота, бета-блокаторы, статины и диуретики). Комбинация с ингибиторами АПФ не рекомендуется (см. разделы «Меры предосторожности», «Фармакодинамика»).
Применение у особых категорий пациентов
Артериальная гипертензия у детей и подростков
Дети от 6 до 18 лет
Для детей с массой тела менее 35 кг начальная доза составляет 40 мг один раз в день. Для детей с массой тела 35 кг и более начальная доза составляет 80 мг один раз в день. Дозу следует корректировать в зависимости от действия на артериальное давление. Максимальные дозы, изученные в клинических испытаниях, приведены в таблице ниже. Дозы, превышающие указанные, не были изучены и поэтому не рекомендуются.
| Масса тела | Максимальные дозы, изученные в клинических испытаниях |
| ≥ 18 кг … < 35 кг | 80 мг |
| ≥ 35 кг … < 80 кг | 160 мг |
| ≥ 80 кг … < 160 кг | 320 мг |
Дети до 6 лет
Безопасность и эффективность Валза у детей младше 6 лет не установлена.
Сердечная недостаточность и недавно перенесенный инфаркт миокарда у детей и подростков
Валз не рекомендуется для лечения сердечной недостаточности или недавно перенесенного инфаркта миокарда у детей и подростков в возрасте до 18 лет в связи с отсутствием данных о безопасности и эффективности.
Пациенты пожилого возраста
Нет необходимости в коррекции дозы у пациентов пожилого возраста.
Пациенты с нарушением функции почек
Дети от 6 до 18 лет
Применение у детей с клиренсом креатинина <30 мл/мин или находящихся на диализе не изучалось, поэтому таким пациентам валсартан не рекомендуется. Не требуется коррекции дозы у детей с клиренсом креатинина более 30 мл/мин. Следует тщательно контролировать функцию почек и уровень калия в сыворотке крови (см. разделы Меры предосторожности и Фармакокинетика).
Взрослые
Нет необходимости коррекции дозы у взрослых пациентов с клиренсом креатинина более 10 мл/мин.
Пациенты с нарушением функции печени
Валсартан противопоказан пациентам с тяжелой печеночной недостаточностью, билиарным циррозом печени или обструкцией желчных путей. У пациентов с легкой и умеренной печеночной недостаточностью без холестаза доза валсартана не должна превышать 80 мг (см. раздел Меры предосторожности).
Если Вы забыли принять Валз
Нельзя удваивать дозировку лекарственного средства для компенсации пропущенной!
Если Вы забыли принять дозу, примите её как можно скорее, пока не приблизилось время очередного приема. Если подошло время для приема следующей дозы лекарственного средства, не принимайте пропущенную дозу.
Частота побочных эффектов: очень часто (≥1/10); часто (≥1/100, но <1/10); нечасто (≥1/1000, но <1/100) редко (≥1/10000, но <1/1000), очень редко (<1/10000).
Нарушения со стороны сердца: нечасто — сердечная недостаточность*; очень редко — сердечная аритмия.
Нарушения со стороны сосудов: часто — ортостатическая гипотензия; нечасто — снижение АД*#; очень редко — васкулит.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения: нечасто — кашель.
Нарушения со стороны желудочно-кишечного тракта: нечасто — диарея, абдоминальная боль; очень редко — тошнота##.
Нарушения со стороны нервной системы» и представить в редакции: «часто: постуральные головокружения#, нечасто — обмороки*, редко – головокружение##, очень редко — головная боль#.
Нарушения со стороны органа слуха и лабиринтные нарушения: нечасто — вертиго.
Нарушения со стороны крови и лимфатической системы: часто — нейтропения; очень редко — тромбоцитопения.
Нарушения со стороны иммунной системы: редко — сывороточная болезнь, повышенная чувствительность; очень редко — ангионевротический отек**, кожная сыпь, зуд.
Нарушения со стороны скелетно-мышечной и соединительной ткани: нечасто — боль в спине, судороги мышц, артрит, миалгия; очень редко — артралгия.
Нарушения со стороны почек и мочевыводящих путей: очень редко — нарушение функции почек**##, острая почечная недостаточность**.
Нарушения со стороны обмена веществ и питания: нечасто — гиперкалиемия*#.
Инфекционные и паразитарные заболевания: часто — вирусные инфекции; нечасто — инфекции верхних дыхательных путей, фарингит, синусит, конъюнктивит; очень редко — ринит, гастроэнтерит.
Общие расстройства и нарушения в месте введения: нечасто — чувство усталости, астения, носовое кровотечение, отеки.
Влияние на результаты лабораторных и инструментальных исследований: снижение уровня гемоглобина и гематокрита, гиперкреатининемия, гипербилирубинемия, повышение активности «печеночных» трансаминаз, повышение концентрации азота мочевины сыворотки крови.
Нарушения психики: нечасто — бессонница, снижение либидо.
Побочное действие у детей:
Гипертензия
Антигипертензивный эффект валсартана оценивали в двух рандомизированных, двойных слепых клинических исследованиях у 561 детей от 6 до 18 лет. Не было выявлено значимых отличий по типу, частоте и тяжести побочных эффектов между профилем безопасности для детей в возрасте от 6 до 18 лет и ранее известным профилем безопасности у взрослых пациентов.
Оценка нейрокогнитивной функции и развития у детей в возрасте от 6 до 16 лет не выявила клинически значимого отрицательного влияния после лечения валсартаном продолжительностью до одного года.
В двойном слепом рандомизированном исследовании у 90 детей в возрасте от 1 года до 6 лет, за которым последовало открытое продление на один год, два человека умерли и наблюдались отдельные случаи выраженного повышения печеночных трансаминаз, связь этих случаев с валсартаном не была установлена, т.к. имело место наличие сопутствующих заболеваний. Во втором исследовании, в котором были рандомизированы 75 детей в возрасте от 1 года до 6 лет, не было ни одного случая смерти или выраженного повышения печеночных трансаминаз.
Эти случаи имели место в популяции пациентов со значительными сопутствующими заболеваниями. Не было установлено причинно-следственной связи с приемом валсартана.
У детей и подростков в возрасте от 6 до 18 лет с хроническими заболеваниями почек чаще наблюдалась гиперкалиемия.
* Сообщалось в период лечения после острого инфаркта миокарда.
# Сообщалось при лечении СН.
** Нечасто сообщалось в период лечения после острого инфаркта миокарда.
## Наиболее часто встречающееся в период лечения СН (часто: головокружение, нарушение функции почек, гипотензия; иногда: головная боль, тошнота).
Пациент должен быть информирован о необходимости обратиться к врачу в случае возникновения любых из перечисленных побочных реакций, а также побочных реакций, не указанных в данной инструкции.
Вследствие передозировки валсартаном может развиться выраженная артериальная гипотензия, что может привести к угнетению сознания, коллапсу и/или шоку. Если лекарственное средство было принято недавно, следует вызвать рвоту. При артериальной гипотензии обычным методом терапии является внутривенное введение солевого раствора. Выведение валсартана из организма путем гемодиализа маловероятно.
В клинических исследованиях не обнаружено имеющих клиническое значение взаимодействий валсартана со следующими лекарственными средствами: циметидин, варфарин, фуросемид, дигоксин, атенолол, индометацин, гидрохлоротиазид, амлодипин, глибенкламид.
Литий
При одновременном применении иАПФ или БРА с лекарственными средствами лития наблюдалось обратимое повышение концентрации лития в сыворотке крови и появление токсических эффектов. Если существует необходимость совместного приема данных лекарственных средств, необходим тщательный мониторинг сывороточных концентраций лития. Если мочегонное средство также используется, можно предположить увеличение риска токсичности лития при применении валсартана.
Лекарственные средства, влияющие на СУР 450
Поскольку валсартан не подвергается существенному метаболизму, клинически значимого взаимодействия с другими лекарственными средствами в виде метаболической индукции или угнетения системы цитохрома Р450 при совместном применении с валсартаном не наблюдалось. Несмотря на то, что валсартан имеет высокую степень связывания с белками плазмы, исследования in vitro не продемонстрировали никакого взаимодействия на этом уровне с рядом молекул, которые также имеют высокую степень связывания с белками, а именно — диклофенаком, фуросемидом и варфарином.
Калийсберегающие диуретики, лекарственные средства калия, лекарственные средства, содержащие калий в виде солей и другие лекарственные средства, способные повысить уровень калия
Совместное применение с калийсберегающими диуретиками (например, спиронолактон, триамтерен, амилорид), лекарственными средствами калия, калийсодержащими заменителями поваренной соли, либо с другими лекарственными средствами, которые могут увеличить уровень калия (напр., гепарин), может привести к повышению уровня калия в сыворотке крови, а у пациентов с сердечной недостаточностью может повышать уровень сывороточного креатинина. Следует контролировать уровень калия в случае необходимости совместного введения данных лекарственных средств.
Нестероидные противовосполительные препараты (НПВП), включая селективные ингибиторы ЦОГ-2, ацетилсалициловой кисслоты (>3 г/сут) и неселективные НПВП
Одновременное применение НПВП и БРА может привести к ослаблению антигипертензивного эффекта. Кроме того, одновременный прием БРА и НПВП может привести к повышению риска ухудшения функции почек и увеличение уровня калия в сыворотке крови. В связи с этим рекомендуется контроль функции почек в начале лечения и адекватная гидратация пациента.
Транспортеры
Одновременный прием ингибиторов переноса (напр., рифампин, циклоспорин) или эффлюксных транспортеров (напр., ритонавир) может усиливать действие валсартана. Двойная блокада ренин-ангиотензин-альдостероновой системы (РААС)
На основе имеющихся данных, двойная блокада РААС с применением иАПФ, БРА или лекарственных средств, содержащих алискирен, не может быть рекомендована любому пациенту, особенно пациентам с диабетической нефропатией.
У пациентов с сахарным диабетом или умеренной/тяжелой почечной недостаточностью (СКФ <60 мл/мин/1,73м2) одновременное применение лекарственных средств, содержащих алискирен, с иАПФ или БРА противопоказано.
В отдельных случаях, когда совместное применение иАПФ и БРА абсолютно показано, необходимо тщательное наблюдение специалиста и обязательный мониторинг функции почек, водно-электролитного баланса, артериального давления.
Пациенты с дефицитом в организме натрия и/или объема циркулирующей крови (ОЦК). У пациентов с выраженным дефицитом натрия в организме и/или сниженным ОЦК, например, вследствие приема больших доз диуретиков, в редких случаях может в начале терапии валсартаном развиться выраженная артериальная гипотензия. Перед началом терапии лекарственным средством Валз рекомендуется восстановить содержание электролитов и жидкости в организме, в частности, путем уменьшения доз диуретиков.
Лекарственное средство Валз можно применять совместно с другими лекарственными средствами, предназначенными для лечения инфаркта миокарда, такими как тромболитики, ацетилсалициловая кислота, бета-адреноблокаторы, статины и диуретики. Совместный прием ингибиторов АПФ не рекомендуется.
При реноваскулярной гипертонии необходим регулярный контроль содержания мочевины и креатинина в крови.
Гиперкалиемия. При совместном применении с лекарственными средствами, содержащими калий, его соли, и лекарственными средствами, относящимися к группе калийсберегающих диуретиков, проводят регулярный контроль уровня калия в плазме крови.
Стеноз почечной артерии. Кратковременное применение валсартана у 12 пациентов с вазоренальной гипертензией, являющейся вторичной вследствие одностороннего стеноза почечной артерии, не вызвало никаких существенных изменений гемодинамических параметров почек, креатинина сыворотки или азота мочевины крови. Поскольку другие лекарственные средства, влияющие на ренин-ангиотензин-альдостероновую систему (РААС), могут повышать уровень мочевины крови и креатинина сыворотки у пациентов с односторонним или двусторонним стенозом почечной артерии, как мера безопасности рекомендуется мониторинг этих показателей.
Нарушение функции почек. У пациентов с нарушением функции почек коррекция дозы не требуется. Однако в тяжелых случаях (клиренс креатинина <10 мл/мин) следует соблюдать осторожность, поскольку опыт применения лекарственного средства в этих случаях отсутствует. С осторожностью применять у пациентов, находящихся на гемодиализе. В настоящее время отсутствует опыт по безопасному применению валсартана у пациентов, находящихся на гемодиализе. Однако, валсартан имеет высокую степень связывания с белками плазмы, поэтому его выведение при гемодиализе маловероятно. Опыт применения лекарственного средства Валз у пациентов с трансплантацией почки отсутствует. Следует избегать одновременного применения антагонистов рецепторов ангиотензина, в том числе валсартана, или ингибиторов АПФ с алискиреном у пациентов с тяжелой почечной недостаточностью (клиренс креатинина <30 мл/мин).
Нарушение функции печени. У пациентов с легкой и умеренной печеночной недостаточностью без халестаза Валз должен применяться с осторожностью (см. разделы «Противопоказания» и «Фармакокинетика»).
Сердечная недостаточность/Постинфарктное состояние. У пациентов с сердечной недостаточностью или постинфарктным состоянием, принимающих валсартан в обычных дозах, наблюдается незначительное снижение артериального давления, но прекращение терапии из-за длительной симптоматической гипотензии, как правило, не требуется, если соблюдать инструкции по дозировке лекарственного средства. Необходимо соблюдать осторожность пациентам с сердечной недостаточностью или в постинфарктном состоянии, начинающим терапию.
Как следствие угнетения ренин-ангиотензин-альдостероновой системы (РААС), у лиц с повышенной чувствительностью могут наблюдаться нарушения функции почек. У пациентов с тяжелой сердечной недостаточностью, у которых функция почек зависит от активности ренин-ангиотензин-альдостероновой системы, лечение ингибиторами АПФ или антагонистами рецепторов ангиотензина могло стать причиной олигурии и/или прогрессирующей азотемии, острой почечной недостаточности (редко) и/или летального исхода. Оценка состояния пациентов с сердечной недостаточностью или в постинфарктном состоянии всегда должна включать мониторинг функции почек. Не рекомендуется одновременный прием тройной комбинации ингибиторов АПФ, бета-блокаторов и валсартана.
Стеноз аортального и митрального клапанов, гипертрофическая кардиомиопатия. Как и при применении других вазодилататоров следует соблюдать особую осторожность при назначении лекарственного средства пациентам с аортальным или митральным стенозом, а также гипертрофической кардиомиопатией.
Ангионевротический отек. Сообщалось о случаях ангионевротического отека, в том числе отека гортани и голосовой щели, что приводит к обструкции дыхательных путей и/или отеку лица, губ, глотки и/или языка у пациентов, получавших валсартан; у некоторых из этих пациентов ранее развивался отек Квинке при приеме других лекарственных средств, в том числе ингибиторов АПФ. Следует немедленно прекратить прием Валза пациентам, у которых развивается ангионевротический отек, и лекарственное средство не должно назначаться снова.
Первичный гиперальдостеронизм. Не рекомендовано назначать валсартан пациентам с первичным гиперальдостеронизмом.
Двойная блокада ренин-ангиотензиновой системы (РАС). Необходимо соблюдать осторожность во время совместного применения антагонистов рецепторов ангиотензина, в том числе валсартана, с другими средствами, блокирующими РАС, такими как ингибиторы АПФ или алискирен.
Беременность
Не следует инициировать прием антагонистов рецепторов ангиотензина II во время беременности. Пациенткам, планирующим беременность, следует назначить альтернативные антигипертензивные средства, которые имеют установленный профиль безопасности для использования во время беременности. В случае наступления беременности применение валсартана следует немедленно прекратить и, при необходимости, начать альтернативную терапию.
Детский возраст.
Применение у детей с клиренсом креатинина <30 мл/мин и у детей на диализе не изучалось, поэтому у таких пациентов валсартан применять не рекомендуется. Не требуется коррекции дозы у детей с клиренсом креатинина >30 мл/мин. Следует тщательно контролировать функцию почек и содержание калия в сыворотке. Это особенно касается случаев, когда валсартан применяется при наличии других состояний (напр., лихорадка, обезвоживание), способных вызвать нарушение функции почек.
Противопоказано одновременное применение блокаторов рецепторов ангиотензина II (в т.ч. Валза) или иАПФ с лекарственными средствами, содержащими алискирен, у пациентов с умеренной/тяжелой почечной недостаточностью (СКФ <60 мл/мин/1,73 м2).
Применение у детей с нарушением функции печени
Как и у взрослых, Валз противопоказан у детей при тяжелой печеночной недостаточности, билиарнам циррозе печени и при холестазе. Существует ограниченный клинический опыт применения валсартана у детей с легкой и умеренной печеночной недостаточностью. У таких пациентов доза валсартана не должна превышать 80 мг.
Вспомогательные вещества.
Лекарственное средство содержит лактозу, поэтому его не следует применять пациентам с такими редкими наследственными заболеваниями, как непереносимость галактозы, дефицит лактазы Лаппа, или мальабсорбция глюкозы-галактозы.
В составе таблеток 320 мг содержится краситель солнечный закат желтый алюминиевый лак (Е110), который может вызвать аллергические реакции.
Влияние на способность управлять транспортными средствами и выполнять работы, требующие повышенного внимания
В период лечения необходимо соблюдать осторожность при вождении автотранспорта и занятия другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты двигательных и психических реакций из-за возможности возникновения головокружения или слабости.
Таблетки покрытые оболочкой 40 мг, 320 мг в упаковках №7×4.
Таблетки покрытые оболочкой 80 мг, 160 мг в упаковках №7×4, №14×7.
По 7 или 14 таблеток в блистер из ПВХ/ПЭ/ПВДХ/Алюминиевая фольга.
По 4 блистера или 7 блистеров вместе с инструкцией по применению в пачке картонной.
При температуре не выше 30°С. Хранить в недоступном для детей месте.
3 года. Не использовать по истечении срока годности, указанного на упаковке.
Условия отпуска из аптек
По рецепту.
Заявитель
Актавис Лтд, Мальта
Производитель
Балканфарма-Дупница АД, Болгария
ул. «Самоковское шоссе» 3,
2600, г. Дупница
тел.: +359/701 58 196
факс: +359/701 58 555
Синонимы, аналоги
Статьи
Регистрационный номер
ЛП-003177
Торговое наименование препарата
Вальсакор® Н320
Международное непатентованное наименование
Валсартан + Гидрохлоротиазид
Лекарственная форма
таблетки, покрытые пленочной оболочкой
Состав
На 1 таблетку, покрытую пленочной оболочкой, 320 мг+12,5 мг:
Ядро:
Действующие вещества: валсартан 320,00 мг, гидрохлоротиазид 12,50 мг
Вспомогательные вещества: целлюлоза микрокристаллическая 164,00 мг, лактозы моногидрат 106,00 мг, магния стеарат 18,00 мг, кроскармеллоза натрия 9,50 мг, повидон-К25 6,00 мг, кремния диоксид коллоидный 4,00 мг.
Оболочка пленочная: гипромеллоза 2910 11,20 мг, титана диоксид (Е171) 3,50 мг, макрогол-4000 1,20 мг, краситель железа оксид красный (EI72) 0,10 мг.
На 1 таблетку, покрытую пленочной оболочкой, 320 мг + 25 мг:
Ядро:
Действующие вещества: валсартан 320.00 мг, гидрохлоротиазид 25 мг
Вспомогательные вещества: целлюлоза микрокристаллическая 164,00 мг, лактозы моногидрат 93,50 мг, магния стеарат 18,00 мг, кроскармеллоза натрия 9,50 мг, повидон-К25 6,00 мг, кремния диоксид коллоидный 4,00 мг.
Оболочка пленочная: гипромеллоза 2910 11,20 мг, титана диоксид (Е171) 3,30 мг, макрогол-4000 1,20 мг, краситель железа оксид желтый (Е172) 0,30 мг.
Описание
Таблетки 320 мг+12,5 мг. Овальные, двояковыпуклые таблетки, покрытые пленочной оболочкой розового цвета. Вид на изломе: белая или почти белая шероховатая масса с пленочной оболочкой розового цвета.
Таблетки 320 мг+25 мг. Овальные, двояковыпуклые таблетки, покрытые пленочной оболочкой светлого коричневато-желтого цвета, с риской на одной стороне. Вид на изломе: белая или почти белая шероховатая масса с пленочной оболочкой светлого коричневато-желтого цвета.
Фармакотерапевтическая группа
Гипотензивное средство комбинированное (ангиотензина II рецепторов антагонист+диуретик)
Код АТХ
C09DA03
Фармакодинамика:
Препарат Вальсакор® Н 320 — комбинированный гипотензивный препарат, в состав которого входят антагонист рецепторов ангиотензина II (АРА II) и тиазидный диуретик.
Валсартан
Валсартан является селективным АРА II для приема внутрь, небелковой природы. Избирательно блокирует АТ1-рецепторы, ответственные за вазопрессорное действие ангиотензина II. Следствием блокады AT1-рецепторов является повышение концентрации ангиотензина II в плазме крови, которое может стимулировать незаблокированные АТ2-рецепторы, что уравновешивает вазопрессорные эффекты, связанные с озбуждением AT1-рецепторов. Валсартан не имеет агонистической активности в отношении АТ1-рецепторов. Его сродство к АТ1-рецепторам примерно в 20 000 раз выше, чем к АТ2-рецепторам.
Валсартан не ингибирует ангиотензинпревращающий фермент (АПФ), известный также как кининаза II, который превращает ангиотензин I в ангиотензин II и разрушает брадикинин. В связи с отсутствием влияния на АПФ, не потенцируются эффекты брадикинина и субстанции Р. Частота развития сухого кашля ниже у пациентов, получавших АРА II, в сравнении с пациентами, получавшими ингибиторы АПФ.
Валсартан не вступает во взаимодействие и не блокирует рецепторы других гормонов или ионные каналы, участвующие в регуляции функций сердечно-сосудистой системы.
При лечении артериальной гипертензии (АГ) валсартан снижает артериальное давление (АД), не влияя на частоту сердечных сокращений (ЧСС).
После приема внутрь разовой дозы валсартана антигипертензивный эффект развивается в течение 2-х часов, а максимальное снижение АД достигается через 4-6 часов. Антигипертензивный эффект валсартана сохраняется в течение 24 часов после его применения. При постоянном применении валсартана максимальное снижение АД, вне зависимости от дозы, достигается через 2-4 недели и поддерживается на достигнутом уровне в ходе длительной терапии. Одновременное применение с гидрохлоротиазидом позволяет достичь значимого дополнительного снижения АД.
Внезапная отмена валсартана не сопровождается резким повышением АД или другими нежелательными клиническими последствиями.
Гидрохлоротиазид (ГХТЗ)
Точкой приложения действия тиазидных диуретиков являются дистальные извитые почечные канальцы. При воздействии тиазидных диуретиков на высокочувствительные рецепторы дистальных канальцев коркового слоя почек происходит подавление реабсорбции ионов натрия (Na+) и хлора (С1—). Подавление ко-транспортной системы Na+ и С1—, по-видимому, происходит за счет конкуренции за участки связывания С1— в данной системе, что приводит к увеличению экскреции Na+ и С1— примерно в одинаковой степени. В результате диуретического действия наблюдается уменьшение объема циркулирующей крови (ОЦК), вследствие чего повышается активность ренина, секреция альдостерона, выведение почками калия и, следовательно, снижение содержания калия в сыворотке крови. Связь между ренином и альдостероном опосредуется ангиотензинном II, поэтому снижение содержания калия в сыворотке крови при одновременном применении ГХТЗ с валсартаном менее выражено, чем при монотерапии ГХТЗ.
Фармакокинетика:
Валсартан
Всасывание
После приема валсартана внутрь максимальная концентрация (Сmах) в плазме крови достигается в течение 2-4 часов. Средняя абсолютная «недоступность составляет 23%. При приеме валсартана с пищей площадь под кривой «концентрация-время» (AUC) и Сmах в плазме крови уменьшаются на 40% и 50% соответственно. Тем не менее через 8 часов после приема валсартана, принятого натощак и с пищей, его плазменные концентрации одинаковы. Уменьшение AUC не сопровождается клинически значимым снижением терапевтического эффекта валсартана, поэтому препарат можно принимать независимо от времени приема пищи.
Распределение
Объем распределения (Vd) валсартана в период равновесного состояния после внутривенного введения составлял около 17 л, что указывает на отсутствие выраженного распределения валсартана в тканях. Валсартан активно связывается с белками плазмы крови (94-97%), преимущественно с альбумином.
Метаболизм
Валсартан не подвергается существенной биотрансформации, только около 20% дозы, принятой внутрь, выводится в виде метаболитов. Гидроксильный метаболит определяется в плазме крови в низких концентрациях (менее 10% от AUC валсартана). Этот метаболит не обладает фармакологической активностью.
Выведение
Валсартан выводится двухфазно: α-фаза с периодом полувыведения (Т1/2α) менее 1 часа и β-фаза с Т1/2β — около 9 часов. Валсартан выводится в основном в неизмененном виде через кишечник (около 83%) и почками (около 13%). После внутривенного введения плазменный клиренс валсартана составляет около 2 л/час, почечный клиренс — 0,62 л/час (около 30% от общего клиренса). Т1/2 валсартана составляет 6 часов.
Фармакокинетика валсартана в диапазоне терапевтических доз носит линейный характер. При повторном применении валсартана изменений фармакокинетических показателей не отмечалось. При приеме валсартана 1 раз в сутки кумуляция незначительна. Плазменные концентрации валсартана одинаковы у мужчин и женщин.
ГХТЗ
Всасывание
При приеме внутрь ГХТЗ всасывается быстро. Сmах в плазме крови достигается через 2 часа после приема внутрь. Фармакокинетика (AUC) линейна в терапевтическом диапазоне доз. Одновременный прием с пищей может привести к увеличению или уменьшению системной доступности но сравнению с приемом натощак, данные изменения не имеют клинического значения. При приеме внутрь абсолютная биодоступность ГХТЗ составляет 70%.
Распределение
Видимый Vd составляет 4-8 л/кг. Связывание с белками плазмы крови (преимущественно с альбуминами) составляет около 40-70%. ГХТЗ накапливается в эритроцитах в концентрации, примерно в 3 раза превышающей плазменную.
Метаболизм, выведение
ГХТЗ элиминируется практически в неизмененном виде. T1/2 конечной фазы составляет 6-15 часов. При повторном применении фармакокинетика ГХТЗ не изменяется. При приеме 1 раз в сутки накопление ГХТЗ незначительно. Более 95% всосавшейся дозы выводится в неизмененном виде почками.
Валсартан/гидрохлоротиазид
При одновременном применении с валсартаном системная биодоступность ГХТЗ уменьшается на 30%, а биодоступность валсартана существенно не изменяется. Отмеченное взаимодействие не оказывает влияние на эффективность комбинированного применения валсартана и ГХТЗ. В контролируемых клинических исследованиях был выявлен отчетливый антигипертензивный эффект данной комбинации, который превышал эффект каждого из компонентов препарата в отдельности или эффект плацебо.
Фармакокинетика особых групп пациентов
Пациенты пожилого возраста (старше 65 лет)
AUC валсартана у некоторых пациентов пожилого возраста больше, чем у добровольцев молодого возраста. Данные изменения клинического значения не имеют. Предположительно, у пациентов пожилого возраста с нормальным уровнем АД и АГ системный клиренс ГХТЗ ниже, чем у здоровых молодых добровольцев.
Пациенты с нарушением функции почек
У пациентов с нарушением функции почек с клиренсом креатинина (КК) 30-70 мл/мин коррекции дозы препарата Вальсакор® Н 320 не требуется. Нет данных по применению препарата у пациентов с тяжелым нарушением функции почек (КК менее 30 мл/мин) и у пациентов, находящихся на гемодиализе. Валсартан не выводится с помощью гемодиализа, в отличие от ГХТЗ.
При наличии почечной недостаточности Сmax и AUC ГХТЗ увеличиваются, а скорость выведения снижается. У пациентов с нарушением функции почек легкой и средней степени тяжести Т1/2 ГХТЗ удлиняется практически в два раза.
Пациенты с нарушением функции печени
У пациентов с легкими (5-6 баллов по шкале Чайлд-Пью) или умеренными (7-9 баллов по шкале Чайлд-Пью) нарушениями функции печени AUC валсартана в 2 раза больше, чем у здоровых добровольцев. Нет данных по применению препарата у пациентов с тяжелыми (более 9 баллов по шкале Чайлд-Пью) нарушениями функции печени.
Заболевания печени не оказывают существенного влияния на фармакокинетику гидрохлоротиазида, поэтому коррекции его дозы в данном случае не требуется.
Показания:
Артериальная гипертензия (пациентам, которым показана комбинированная терапия).
Противопоказания:
— Повышенная чувствительность к валсартану, гидрохлоротиазиду и к другим производным сульфонамида или любым другим компонентам препарата;
— тяжелые нарушения функции печени (более 9 баллов по шкале Чайлд-Пью), билиарный цирроз и холестаз;
— анурия, тяжелые нарушения функции почек (КК менее 30 мл/мин);
— рефрактерные гипокалиемия, гипонатриемия, гиперкальциемия и симптоматическая гиперурикемия;
— одновременное применение с алискиреном у пациентов с сахарным диабетом или умеренными и тяжелыми нарушениями функции почек (КК менее 60 мл/мин);
— беременность и планирование беременности, период грудного вскармливания;
— возраст до 18 лет (эффективность и безопасность у детей не доказаны);
— дефицит лактазы, непереносимость лактозы, синдром глюкозо-галактозной мальабсорбции, так как в состав препарата Вальсакор® Н 320 входит лактоза.
С осторожностью:
— Одновременное применение калийсберегающих диуретиков, препаратов калия, калийсодержащих пищевых добавок или других лекарственных препаратов, способных повышать содержание калия в сыворотке крови (например, гепарин);
— состояния, сопровождающиеся водно-электролитными нарушениями: нефропатия с потерей солей и переренальным (кардиогенным) нарушением функции почек, гипокалиемия, гипомагниемия, гиперкальциемия;
— хроническая сердечная недостаточность (ХСН) III-IV функционального класса по классификации NYHA;
— выраженная гипонатриемия и/или состояния, сопровождающиеся снижением ОЦК (в том числе диарея, рвота, терапия высокими дозами диуретиков);
— двусторонний или односторонний стеноз почечных артерий или стеноз артерии единственной почки, состояние после трансплантации почки;
— первичный гиперальдостеронизм;
— стеноз аортального и/или митрального клапана, гипертрофическая обструктивная кардиомиопатия (ГОКМП);
— системная красная волчанка (СКВ);
— сахарный диабет (СД);
— гиперхолестеринемия;
— гипертриглицеридемия;
— закрытоугольная глаукома;
— у пациентов с наследственным ангионевротическим отеком, либо ангионевротическим отеком на фоне предшествующей терапии АРА II или ингибиторами АПФ.
Беременность и лактация:
Беременность
Валсартан
Применение АРА II в I триместре беременности не рекомендуется. Применение АРА II противопоказано во II-III триместрах беременности, поскольку применение во II-III триместрах беременности может вызвать фетотоксические эффекты (снижение функции почек, маловодие, замедление окостенения костей черепа плода) и неонатальные токсические эффекты (почечную недостаточность, артериальную гипотензию, гиперкалиемию). Имеются сообщения о самопроизвольных абортах, маловодии и нарушении функции почек у новорожденных, матери которых во время беременности неумышленно получали валсартан.
Если все же применяли препарат во II-III триместрах беременности, то необходимо провести ультразвуковое исследование почек и костей черепа плода.
При планировании беременности рекомендуется пациентку перевести на альтернативную гипотензивную терапию с учетом профиля безопасности.
Новорожденные, матери которых получали АРА II во время беременности, нуждаются в медицинском наблюдении, так как существует риск развития артериальной гипотензии.
ГХТЗ
Опыт применения ГХТЗ во время беременности, особенно в I триместре, ограничен. ГХТЗ проникает через плаценту. При применении тиазидных диуретиков во II-III триместре беременности возможно развитие тромбоцитопении, нарушение водно-электролитного баланса, желтухи у плода или новорожденного.
При подтверждении беременности препарат Вальсакор® Н 320 необходимо отменить как можно раньше.
Период грудного вскармливания
Нет данных о выделении валсартана в грудное молоко. ГХТЗ выделяется с грудным молоком у женщин. При необходимости применения препарата Вальсакор® Н 320 в период лактации необходимо прекратить грудное вскармливание.
Способ применения и дозы:
Перед началом терапии необходимо скорректировать водно-электролитные нарушения (препарат не показан пациентам со сниженным ОЦК).
Препарат Вальсакор® Н 320 назначают по 1 таблетке внутрь, 1 раз в сутки, ежедневно, независимо от времени приема пищи, таблетку следует проглатывать целиком, запивая достаточным количеством жидкости.
В зависимости от клинической ситуации рекомендуемая суточная доза — 1 таблетка препарата, содержащая фиксированную комбинацию валсартан/гидрохлоротиазид в дозах 80/12,5 мг, 160/12,5 мг, 160/25 мг, 320/12,5 мг или максимально 320/25 мг.
Максимальное снижение АД обычно достигается за 2-4 недели терапии.
Пациентам со слабо или умеренно выраженными нарушениями функции почек (скорость клубочковой фильтрации > 30 мл/мин) изменений дозы препарата не требуется.
У пациентов с легкими (5-6 баллов по шкале Чайлд-Пью) и умеренными нарушениями функции печени без сопутствующих явлений холестаза доза валсартана не должна превышать 80 мг.
Побочные эффекты:
Классификация частоты развития побочных эффектов Всемирной организации здравоохранения (ВОЗ):
очень часто ≥ 1/10
часто от ≥ 1/100 до < 1/10
нечасто от ≥ 1/1000 до < 1/100
редко от ≥ 1/10000 до < 1/1000
очень редко < 1/10000
частота неизвестна — не может быть оценена на основе имеющихся данных.
При применении комбинации валсартан/гидрохлоротиазид
Нарушения со стороны обмена веществ и питания:
нечасто: дегидратация.
Нарушения со стороны нервной системы:
часто: головная боль;
нечасто: парестезия;
очень редко: головокружение;
частота неизвестна: обморок.
Нарушения со стороны органа зрения:
нечасто: снижение остроты зрения.
Нарушения со стороны органа слуха и лабиринтные нарушения:
нечасто: шум в ушах.
Нарушения со стороны сосудов:
нечасто: выраженное снижение АД, периферические отеки.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения:
нечасто: кашель;
частота неизвестна: некардиогенный отек легких.
Нарушения со стороны желудочно-кишечного тракта:
нечасто: тошнота;
очень редко: диарея.
Нарушения со стороны скелетно-мышечной и соединительной ткани:
нечасто: миалгия;
очень редко: артралгия.
Нарушения со стороны почек и мочевыводящих путей:
частота неизвестна: нарушение функции почек.
Общие расстройства и нарушения в месте введения:
нечасто: повышенная утомляемость.
Лабораторные и инструментальные данные:
частота неизвестна: повышение концентрации мочевой кислоты в сыворотке крови, повышение концентрации билирубина в сыворотке крови, повышение концентрации креатинина в сыворотке крови, гипонатриемия, гипокалиемия, нейтропения, повышение концентрации остаточного азота мочевины в сыворотке крови.
При изучении клинического применения фиксированной комбинации валсартан/гидрохлоротиазид у пациентов с АГ наблюдались следующие нежелательные явления (НЯ) без очевидной связи с приемом препарата: боль в животе, боль в верхней части живота, тревога, артрит, астения, боль в спине, бронхит (в том числе острый), боль в груди, постуральное головокружение, диспепсия, одышка, сухость слизистой оболочки полости рта, носовые кровотечения, эректильная дисфункция, гастроэнтерит, головная боль, повышенное потоотделение, гипостезия, гриппоподобное состояние, бессонница, растяжение связок, мышечные спазмы, мышечный гипертонус, заложенность носа, назофарингит, тошнота, боль в шее, периферические отеки, средний отит, боль в конечностях, учащенное сердцебиение, боль в гортани и глотке, пирексия, поллакиурия, гипертермия, синусит, сонливость, инфекции верхних дыхательных путей, инфекции мочевыводящих путей, вертиго, вирусные инфекции, нарушение зрения.
При применении комбинации валсартан/гидрохлоротиазид возможно возникновение НЯ, отмечавшихся как при применении валсартана и ГХТЗ в монотерапии, так и не выявленных в ходе клинических исследований.
При применении валсартана
Нарушения со стороны крови и лимфатической системы:
частота неизвестна: снижение гемоглобина, снижение гематокрита, тромбоцитопения.
Нарушения со стороны иммунной системы:
частота неизвестна: реакции повышенной чувствительности/аллергические реакции, включая сывороточную болезнь.
Нарушения со стороны обмена веществ и питания:
частота неизвестна: повышение содержания калия в сыворотке крови, гипонатриемия.
Нарушения со стороны органа слуха и лабиринтные нарушения:
нечасто: вертиго.
Нарушения со стороны сосудов:
частота неизвестна: васкулит.
Нарушения со стороны желудочно-кишечного тракта:
нечасто: боль в животе.
Нарушения со стороны печени и желчевыводящих путей:
частота неизвестна: повышение активности «печеночных» ферментов.
Нарушения со стороны кожи и подкожных тканей:
частота неизвестна: ангионевротический отек, кожная сыпь, кожный зуд, буллезный дерматит.
Нарушения со стороны почек и мочевыводящих путей:
частота неизвестна: почечная недостаточность.
Следующие НЯ наблюдались при изучении клинического применения валсартана у пациентов с АГ независимо от их причинной связи с применением валсартана: артралгия, астения, боль в спине, диарея, головокружение, головная боль, бессонница, снижение либидо, тошнота, отеки, фарингит, ринит, синусит, инфекции верхних дыхательных путей, вирусные инфекции.
При применении тиазидных диуретиков, включая ГХТЗ
Нарушения со стороны крови и лимфатической системы:
редко: тромбоцитопения, иногда с пурпурой;
очень редко: агранулоцитоз, угнетение костномозгового кроветворения, гемолитическая анемия, лейкопения;
частота неизвестна: апластическая анемия.
Нарушения со стороны иммунной системы:
очень редко: реакции повышенной чувствительности.
Нарушения со стороны обмена веществ и питания:
очень часто: гипокалиемия, повышение концентрации липидов в плазме крови (особенно на фоне высоких доз ГХТЗ);
часто: гипонатриемия, гипомагниемия, гиперурикемия;
редко: гиперкальциемия, гипергликемия, глюкозурия и ухудшение течения СД;
очень редко: гипохлоремический алкалоз.
Нарушения психики:
редко: нарушение сна, депрессия.
Нарушения со стороны нервной системы:
редко: головная боль, головокружение, парестезия.
Нарушения со стороны органа зрения:
редко: нарушение зрения (особенно в первые несколько недель лечения);
частота неизвестна: острый приступ закрытоугольной глаукомы.
Нарушения со стороны сердца:
редко: аритмии.
Нарушения со стороны сосудов:
часто: ортостатическая гипотензия (может усиливаться при одновременном применении с этанолом, седативными или обезболивающими средствами).
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения:
очень редко: респираторный дистресс-синдром, включая отек легких и пневмонит.
Нарушения со стороны пищеварительной системы:
часто: снижение аппетита, умеренно выраженная тошнота и рвота;
редко: дискомфорт в животе, запор, диарея;
очень редко: панкреатит.
Нарушения со стороны печени и желчевыводящих путей:
редко: внутрипеченочный холестаз или желтуха.
Нарушения со стороны почек и мочевыводящих путей:
частота неизвестна: нарушение функции почек, острая почечная недостаточность.
Нарушения со стороны кожи и подкожных тканей:
часто: крапивница и другие формы кожной сыпи;
редко: фотосенсибилизация;
очень редко: некротизирующий васкулит и токсический эпидермальный некролиз, волчаноподобные реакции, обострение кожных проявлений СКВ;
частота неизвестна: мультиформная эритема.
Нарушения со стороны скелетно-мышечной и соединительной ткани:
частота неизвестна: мышечные спазмы.
Нарушения со стороны половых органов и молочной железы:
часто: импотенция.
Общие расстройства и нарушения вместе введения:
частота неизвестна: гипертермия, астения.
Передозировка:
Симптомы: основным ожидаемым проявлением передозировки валсартана является выраженное снижение АД, которое может привести к нарушению сознания, коллапсу и/или шоку. При передозировке ГХТЗ возможно развитие следующих симптомов: тошнота, сонливость, снижение ОЦК, нарушения ритма сердца и спазмы мышц, вызванные нарушением водно-электролитного баланса.
Лечение: симптоматическое и зависит от времени, прошедшего с момента приема препарата, и от степени тяжести симптомов. В случае ранней диагностики передозировки рекомендовано вызвать рвоту и/или промыть желудок. Следует стабилизировать показатели гемодинамики. При выраженном снижении АД необходимо перевести пациента в горизонтальное положение с приподнятыми вверх ногами и восполнить ОЦК (внутривенно ввести 0,9% раствор натрия хлорида) под контролем показателей гемодинамики и диуреза. Валсартан не выводится с помощью гемодиализа, так как значительно связывается с белками плазмы крови. ГХТЗ выводится с помощью гемодиализа.
Взаимодействие:
Общие лекарственные взаимодействия для валсартана и гидрохлоротиазида
Одновременное применение не рекомендуется
Препараты лития
При одновременном применении ингибиторов АПФ, АРА II или тиазидных диуретиков с препаратами лития отмечалось обратимое повышение концентрации лития в плазме крови и развитие интоксикации. Риск токсических проявлений, связанных с применением препаратов лития, может дополнительно увеличиваться при одновременном применении с препаратом Вальсакор® Н 320, поскольку почечный клиренс препаратов лития снижается под действием тиазидных диуретиков. При необходимости одновременного применения с препаратами лития следует тщательно контролировать концентрацию лития в плазме крови.
Одновременное применение с осторожностью
Другие гипотензивные препараты
Возможно усиление антигипертензивного эффекта при одновременном применении с другими лекарственными средствами, снижающими АД (например, ингибиторы АПФ, бета-адреноблокаторы, блокаторы «медленных» кальциевых каналов (БМКК), гуанетидин, метилдопа, вазодилататоры, прямые ингибиторы ренина, АРА II).
Прессорные амины (например, норэпинефрин и эпинефрин)
Возможно ослабление действия прессорных аминов, не требующее прекращения одновременного применения валсартана и ГХТЗ.
Нестероидные противовоспалительные препараты (НПВП), включая селективные ингибиторы циклооксигеназы-2 (ЦОГ-2)
При одновременном применении АРА II и ГХТЗ с НПВП возможно ослабление диуретического и антигипертензивного действия. В условиях гиповолемии возможно развитие острой почечной недостаточности (ОПН), рекомендуется контролировать функцию почек в начале терапии, а также адекватное восполнение ОЦК у пациента.
Лекарственные взаимодействия для валсартана
Одновременное применение противопоказано
Одновременное применение АРА II, включая валсартан, с алискиреном противопоказано у пациентов с СД или умеренными и тяжелыми нарушениями функции почек (КК менее 60 мл/мин).
Одновременное применение не рекомендуется
Калийсберегающие диуретики (спиронолактон, эплеренон, триамтерен, амилорид), препараты калия, калийсодержащие заменители пищевой соли и другие лекарственные средства и вещества, которые могут вызвать повышение содержания калия в сыворотке крови (например, гепарин)
При необходимости одновременного применения с препаратами, влияющими на содержание калия, рекомендуется контролировать содержание калия в плазме крови.
Одновременное применение с осторожностью
При одновременном применении АРА II, включая валсартан, с лекарственными средствами, оказывающими влияние на ренин-ангиотензин-альдостероновую систему (РААС), такими как, ингибиторы АПФ или алискирен повышается частота возникновения случаев артериальной гипотензии, гиперкалиемии, нарушения функции почек.
Необходимо контролировать АД, функцию почек, содержание электролитов в плазме крови у таких пациентов.
Белки-переносчики
Исследования in vitro на культурах печени показали, что валсартан является субстратом для белков-переносчиков ОАТР1В1/ОАТР1В3 и MRP2. Одновременное применение валсартана с ингибиторами белка-переносчика OATP1B1/OATP1В3 (рифампицин, циклоспорин) или MRP2 (ритонавир) может увеличить системную экспозицию валсартана (Сmах и AUC). Необходимо соблюдать осторожность в начале одновременного применения с вышеуказанными препаратами или после их отмены.
Отсутствие лекарственного взаимодействия
Не выявлено клинически значимых взаимодействий со следующими лекарственными средствами: циметидин, варфарин, фуросемид, дигоксин, атенолол, индометацин, ГХТЗ, амлодипин и глибенкламид.
Лекарственные взаимодействия для ГХТЗ
Одновременное применение с осторожностью
Лекарственные препараты, влияющие на содержание калия в плазме крови
При одновременном применении с «петлевыми» диуретиками, глюкокортикостероидами (ГКС), адренокортикотропным гормоном (АКТГ), амфотерицином В, бензатина бензилпенициллином, карбеноксолоном, слабительными средствами, ацетилсалициловой кислотой или ее производными риск снижения содержания калия в плазме крови и гипокалиемии увеличивается. В этом случае рекомендовано контролировать содержание калия в плазме крови.
Лекарственные препараты, способные вызывать полиморфную желудочковую тахикардию типа «пируэт»
При одновременном применении антиаритмических средств IA и III классов и некоторых антипсихотических препаратов (нейролептиков) с ГХТЗ следует соблюдать осторожность, так как существует риск развития аритмии типа «пируэт» на фоне возможной гипокалиемии. Рекомендован контроль содержания калия в плазме крови.
Миорелаксанты недеполяризующие периферического действия (тубокурарин)
ГХТЗ потенцирует действие миорелаксантов.
Гипогликемические средства (для приема внутрь и инсулин)
При одновременном применении может потребоваться коррекция дозы гипогликемических средств.
Метформин следует принимать с осторожностью, гак как возможно развитие лактоацидоза, индуцированного почечной недостаточностью на фоне приема ГХТЗ.
Лекарственные препараты, влияющие на содержание натрия в плазме крови
При длительном одновременном применении с антидепрессантами, противосудорожными, антипсихотическими (нейролептиками) препаратами (например, карбамазепин) и т. д. следует соблюдать осторожность, так как увеличивается риск развития гипонатриемии. Рекомендовано регулярно контролировать содержание натрия в плазме крови.
Сердечные гликозиды
Гипокалиемия и гипомагниемия на фоне приема тиазидных диуретиков могут способствовать развитию нарушений сердечного ритма у пациентов, получающих сердечные гликозиды.
Н- и м-холиноблокатары
Н- и м-холиноблокаторы (атропин, бипериден) могут повышать биодоступность тиазидных диуретиков за счет снижения перистальтической активности желудочно-кишечного тракта (ЖКТ) и замедления опорожнения желудка. Соответственно, стимуляторы моторики ЖКТ (цизаприд) могут снижать биодоступность тиазидных диуретиков.
Анионообменные смолы (колестирамин и колестипол)
Всасывание тиазидных диуретиков, в том числе ГХТЗ, уменьшается при одновременном применении колестирамина и колестипола. Поэтому ГХТЗ следует принимать за 4 часа либо через 4-6 часов после приема анионообменных смол.
Метилдопа
Описаны отдельные случаи развития гемолитической анемии при одновременном применении метилдопы и ГХТЗ.
Витамин D и соли кальция
Одновременное применение тиазидных диуретиков, включая ГХТЗ, с витамином D или солями кальция может приводить к повышению содержания кальция в плазме крови в результате усиления реабсорбции кальция.
Циклоспорин
При одновременном применении ГХТЗ и циклоспорина увеличивается риск развития гиперурикемии и симптомов, схожих с обострением течения подагры.
Рентгеноконтрастные средства, содержащие йод
При гиповолемии, развившейся па фоне приема диуретиков, увеличивается риск развития ОПН. Следует восполнить ОЦК перед применением средств с высоким содержанием йода (например, рентгеноконтрастных средств, содержащих йод).
Лекарственные средства для лечения подагры (пробенецид, сульфинпиразон и аллопуринол)
При применении ГХТЗ возможно повышение концентрации мочевой кислоты в плазме крови, что может потребовать коррекции доз лекарственных средств для лечения подагры (например, увеличение дозы сульфинпиразона и пробенецида). Одновременное применение с тиазидными диуретиками, включая ГХТЗ, может привести к увеличению частоты реакций повышенной чувствительности на аллопуринол.
Амантадин
Одновременное применение с тиазидными диуретиками, включая ГХТЗ, увеличивает риск развития побочных аффектов амантадина.
Бета-адреноблокаторы и диазоксид
Одновременное применение с тиазидными диуретиками, включая ГХТЗ, увеличивает риск развития гипергликемии.
Цитотоксические препараты (циклофосфамид, метотрексат)
Одновременное применение с тиазидными диуретиками, включая ГХТЗ, снижает выведение цитотоксических препаратов почками, что приводит к потенцированию их миелосупрессивного действия.
Этанол, барбитураты и наркотические средства
Одновременное применение с тиазидными диуретиками, включая ГХТЗ, может потенцировать развитие ортостатической гипотензии.
Особые указания:
Нарушение функции почек
У пациентов с нарушением функции почек (КК более 30 мл/мин) не требуется изменения дозы препарата. При применении препарата Вальсакор® Н 320 у пациентов с нарушением функции почек рекомендуется регулярно контролировать содержание калия, концентрации креатинина и мочевой кислоты в плазме крови.
Состояние после перенесенной трансплантации почки
Безопасность препарата Вальсакор® Н 320 у пациентов, недавно перенесших трансплантацию почки, не установлена.
Стеноз аортального и/или митрального клапанов, ГОКМП
Препарат Вальсакор® Н 320 необходимо с осторожностью применять у пациентов с гемодинамически значимым стенозом аортального и/или митрального клапанов или с ГОКМП.
Нарушение функции печени
Препарат Вальсакор® Н 320 не рекомендуется пациентам с нарушением функции печени. Максимально рекомендованная суточная доза валсартана у пациентов с легкими или умеренными нарушениями функции печени без явлений холестаза — 80 мг.
Нарушения водно-электролитного баланса
При применении тиазидных диуретиков, включая ГХТЗ, отмечались случаи развития гипокалиемии, гипонатриемии и гипохлоремического алкалоза, гипомагниемии (так как увеличивается выведение магния почками) и гиперкалиемии (так как снижается выведение кальция почками). Рекомендуется при применении препарата Вальсакор® Н 320 регулярно контролировать содержание электролитов в сыворотке крови, в особенности калия.
Гипонатриемия и/или снижение ОЦК
У пациентов с выраженной гипонатриемией и/или при сниженном ОЦК (например, при приеме высоких доз диуретиков) в редких случаях в начале терапии препаратом Вальсакор® Н 320 возможно выраженное снижение уровня АД с клиническими проявлениями. Поэтому в начале лечения следует провести коррекцию содержания натрия в сыворотке крови и/или восполнить ОЦК.
В случае развития выраженного снижения АД пациента следует перевести в горизонтальное положение с приподнятыми ногами и, при необходимости, провести внутривенную инфузию 0,9% раствора натрия хлорида. После стабилизации уровня АД лечение препаратом Вальсакор® Н 320 может быть продолжено.
Хроническая сердечная недостаточность III-IV функционального класса (по классификации NYHA) или другие заболевания, сопровождающиеся стимуляцией РААС
У пациентов, функция почек которых зависит от состояния РААС (например, ХСН II-IV функционального класса по классификации NYHA), терапия ингибиторами АПФ может сопровождаться олигурией и/или прогрессирующей азотемией, в редких случаях — ОПН. Невозможно исключить развитие нарушений функции почек вследствие подавления активности РААС на фоне приема препарата Вальсакор® Н 320. Терапию препаратом Вальсакор® Н 320 следует проводить с осторожностью, под контролем функции почек.
Первичный гиперальдостеронизм
Препарат Вальсакор® Н 320 неэффективен для лечения АГ у пациентов с первичным гиперальдостеронизмом по причине отсутствия активации РААС.
Стеноз почечной артерии
У пациентов с односторонним или двусторонним стенозом почечной артерии или стенозом артерии единственной почки препарат должен применяться с осторожностью, так как возможно повышение концентраций креатинина и мочевины в плазме крови.
Системная красная волчанка
При применении тиазидных диуретиков (в том числе ГХТЗ) описаны случаи развития обострений и ухудшения течения заболеваний соединительной ткани (например, СКВ).
Другие метаболические нарушения
Тиазидные диуретики, включая ГХТЗ, могут вызывать изменение толерантности к глюкозе и повышение концентрации холестерина, триглицеридов и мочевой кислоты в плазме крови.
Пациентам с СД может потребоваться коррекция дозы инсулина или гипогликемических средств для приема внутрь.
Тиазидные диуретики снижают экскрецию кальция почками и могут вызывать незначительное повышение содержания кальция в плазме крови при отсутствии сопутствующих нарушений метаболизма кальция. Выраженная гиперкалиемия на фоне применения тиазидного диуретика может свидетельствовать о гиперпаратиреозе. Перед исследованием функции паращитовидных желез следует отменить тиазидные диуретики, включая ГХТЗ.
Фоточувствительность
Описаны случаи развития фоточувствительности на фоне приема ГХТЗ. В случае развития проявлений фоточувствительности рекомендовано прекратить терапию. При необходимости продолжения терапии рекомендуется защищать открытые участки тела от воздействия солнечных и ультрафиолетовых лучей.
Антидопинговый тест
ГХТЗ может давать положительный результат при проведении допинг-контроля.
Реакции повышенной чувствительности
Реакции повышенной чувствительности на фоне применения ГХТЗ наиболее часто отмечались у пациентов с аллергическими реакциями и бронхиальной астмой в анамнезе.При применении валсартана у пациентов наблюдалось развитие ангионевротического отека, в том числе отека гортани и голосовых связок, приводящего к обструкции дыхательных путей, и/или отека лица, губ, глотки и/или языка, у некоторых из этих пациентов в анамнезе отмечалось развитие ангионевротического отека на фоне применения других лекарственных средств, включая ингибиторы АПФ. В случае развития ангионевротического отека следует немедленно отменить препарат Вальсакор® Н 320 и не возобновлять лечение препаратом.
Острый приступ закрытоугольной глаукомы
На фоне применения ГХТЗ отмечались случаи транзиторной миопии и острого развития закрытоугольной глаукомы. Симптомы включают в себя внезапное начало, резкое снижение остроты зрении или боль в глазу, обычно возникают в период от нескольких часов до недели после начала терапии. Нелеченная закрытоугольная глаукома может привести к стойкой потере зрения.
В первую очередь необходимо как можно быстрее отменить прием ГХТЗ. Если внутриглазное давление остается неконтролируемым, может потребоваться экстренное медикаментозное или хирургическое лечение. Фактором риска развития острой закрытоугольной глаукомы может быть наличие у пациента в анамнезе аллергических реакций на сульфонамиды или пенициллин.
Специальная информация по вспомогательным веществам
Препарат Вальсакор® Н 320 содержит лактозу, поэтому не следует применять при следующих состояниях: непереносимость лактозы, дефицит лактазы или синдром глюкозо-галактозной мальабсорбции.
Влияние на способность управлять транспортными средствами и механизмами:
В связи с возможностью возникновения головокружения или слабости на фоне применения препарата Вальсакор® Н 320 необходимо соблюдать осторожность при управлении транспортными средствами и работе с другими техническими устройствами, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Форма выпуска/дозировка:
Таблетки, покрытые пленочной оболочкой, 320 мг+12,5 мг, 320 мг+25 мг.
Упаковка:
По 14 или 15 таблеток в блистере из комбинированного материала ПВХ/ПЭ/ПВДХ — алюминиевой фольги.
По 2, 4, 6 или 7 блистеров (по 14 таблеток), или по 2, 4 или 6 блистеров (по 15 таблеток) помещают в пачку картонную вместе с инструкцией по применению.
Условия хранения:
В защищенном от света месте, при температуре не выше 25 °С, в оригинальной упаковке.
Хранить в недоступном для детей месте.
Срок годности:
5 лет.
Не использовать препарат после истечения срока годности.
Условия отпуска
По рецепту
Производитель
АО «КРКА, д.д., Ново место», Smarjeska cesta 6, 8501, Novo mesto, Slovenia, Словения
Владелец регистрационного удостоверения/организация, принимающая претензии потребителей:
АО «КРКА, д.д., Ново место»
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Состав раствора Рингера
В одном миллилитре раствора Рингера содержится 8,6 грамм натрия хлорида, 0,3 г калия хлорида, 0,33 г кальция хлорида.
Также в состав препарата входят: кислота хлористоводородная, гидроксид натрия, вода.
Форма выпуска
Средство – прозрачная жидкость без цвета.
Продается во флаконах из пластика, емкостью 500 мл (10 штук); бутылках по 200 или 400 мл; контейнерах емкостью 250 мл (40 штук) или 500 мл (20 штук); в контейнерах по 100 мл по 1 или 50 контейнерах в упаковке; в контейнерах емкостью один литр.
Фармакологическое действие
Восполняет недостаток энергетических субстратов, возмещает дефицит электролитов и экстрацеллюлярной жидкости.
Фармакодинамика и фармакокинетика
Активные компоненты раствора Рингера оказывают дезинтоксикационное, восполняющее дефицит крови и электролитов действие.
Благодаря тому, что р-р увеличивает объем крови и разжижает ее, концентрация токсинов значительно уменьшается.
Эффект восполнения объема потерянной пациентом крови быстро проходит, р-р Рингера быстро выводится из сосудистого русла в близлежащие ткани. При оказании первой помощи следует помнить, что такой эффект продлится не более 30-40 минут.
Также существует раствор Рингера для собак, кошек и других животных. Состав такого средства несколько отличается. Например, процентное содержание хлорида натрия для млекопитающих составляет менее одной десятитысячной доли процента, хлорида калия – 0,042%, хлорида кальция – 0,024%.
Показания к применению
Препарат используют для оказания экстренной помощи пострадавшему при нарушении электролитного баланса или потери крови.
В том числе:
- при коллапсе или шоке;
- после ожогов, обморожений, электротравм;
- для восполнения баланса электролитов в организме вследствие диареи (острые кишечные инфекции), рвоты, различных отравлений;
- при остром перитоните, кишечной непроходимости, кишечном свище;
- для проведения лечебного плазмофереза;
- при метаболическом алкалозе, в процессе которого было потеряно много жидкости.
Противопоказания
Препарат противопоказан:
- при отеке мозга или легких;
- лицам, страдающим хронической почечной или сердечной недостаточностью;
- при гиперволемии, ацидозе, гипернатриемии и гиперхлоремии;
- если у пострадавшего аллергия на какой-либо из компонентов лекарства.
Побочные эффекты
Если использовать р-р Рингера согласно инструкции, то побочные реакции проявляются крайне редко. Чаще всего какие-либо проявления нежелательных эффектов связаны с передозировкой средством.
Могут проявиться: аллергия, недостаточность калия в плазме крови, гипергидратация.
Если во время введения раствора началась аллергия, то процедуру следует немедленно прервать и произвести специфические мероприятия. Для устранения прочих эффектов достаточно уменьшения дозировки.
Раствор Рингера, инструкция по применению (Способ и дозировка)
Р-р Рингера вводят внутривенно, с использованием капельницы или струйно (по показаниям, оказание экстренной помощи). Скорость введения составляет около 60-80 капель/мин.
Инструкция по применению Рингера
Суточная дозировка устанавливается индивидуально.
Для детей расчет дозы происходит по формуле 5-10 мл на кг веса тела. Скорость введения до 60 капель/минута. В тяжелых случаях дозировку можно увеличить до 30 мл на кг веса ребенка.
Капельница для взрослого человека рассчитывается: 20 мл на кг веса (до 50 мл на кг).
Продолжительность лечения в зависимости от заболевания и его тяжести составляет 3-5 дней.
Иногда целесообразно применять раствор Рингера для кошек, собак и прочих домашних животных, приобретенный в обычной аптеке (не ветеринарной). В таком случае рекомендуется проконсультироваться с ветеринаром о режиме дозирования препарата.
Передозировка
Передозировка средством встречается крайне редко. Как правило, это приводит к повышению частоты и силы побочных реакций. В таком случае рекомендуется прекратить ввод раствора и скорректировать дозировку.
Взаимодействие
При сочетании лекарства с нестероидными противовоспалительными средствами, анаболиками, кортикотропином, вазодилататорами, андрогенными средствами, эстрогенами, минералокортикоидами, ганглиоблокаторами возможна задержка натрия в организме.
Совместный прием с сердечными гликозидами повышает их токсичность.
Сочетание раствора с ингибиторами АПФ, препаратами калия и диуретиками способствует развитию гиперкалиемии.
Условия продажи
Для приобретения лекарства в аптеке могут потребовать рецепт на латыни. Средство разрешено к применению под контролем специалиста.
Условия хранения
Препарат необходимо хранить в темном, прохладном месте (от 15 до 25 градусов). При этом, если во время хранения лекарство было заморожено, то его можно использовать при условии, что внешний вид раствора не изменился (не помутнел, нет хлопьев или осадка), упаковка не повреждена.
Беречь от детей.
Срок годности
2 года.
Особые указания
При длительном применении р-ра необходимо контролировать количество электролитов в крови, рН крови.
Нельзя использовать препарат по истечению срока годности, если упаковка повреждена, раствор помутнел или выпал осадок, изменился цвет.
Аналоги
Совпадения по коду АТХ 4-го уровня:
Дарроу, Физ. раствор, Ацесоль, Дисоль, Йоностерил, Раствор Рингера-Локка, Трисоль, Хлосоль.
При беременности и лактации
В связи с ограниченным опытом применения лекарства беременными и кормящими женщинами рекомендуется воздержаться от применения средства.
Отзывы
Существует масса положительных отзывов о растворе Рингер. Капельницы с этим препаратам ставят и детям, и беременным женщинам, и даже животным. Некоторые просто в восторге от данного средства.
Вот несколько отзывов:
- “Девчонки, Рингер – чудесное средство. Только он один и помог. Я месяц мучилась. Сейчас второй день его капают и мне уже намного лучше. Советую всем …”
- “Моя кошка была одной лапой в могиле, только этим раствором и спасались …”
- “Мне как раз Рингер и помог. Начала хоть немного кушать, потому что до этого полторы недели не ела вообще …”
Цена раствора Рингера
Цена Рингера варьируется в зависимости от производителя. На данный момент невозможно указать примерную стоимость препарата.
Имудон® (Imudon®) инструкция по применению
📜 Инструкция по применению Имудон®
💊 Состав препарата Имудон®
✅ Применение препарата Имудон®
📅 Условия хранения Имудон®
⏳ Срок годности Имудон®
Описание лекарственного препарата
Имудон®
(Imudon®)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для электронного издания справочника Видаль 2023
года, дата обновления: 2022.12.21
Код ATX:
L03AX
(Другие иммуностимуляторы)
Лекарственная форма
| Имудон® |
Таб. д/рассасывания: 24 или 40 шт. рег. №: П N014990/01 |
Форма выпуска, упаковка и состав
препарата Имудон®
Таблетки для рассасывания белого или почти белого цвета, плоскоцилиндрической формы, с гладкой блестящей поверхностью, со скошенными краями, с мятным запахом, допускается незначительная мраморность.
Вспомогательные вещества: натрия дезоксихолат — 0.53 мг, тиомерсал — не более 0.0125 мг, глицин — 49.3 мг, лактозы моногидрат — 350 мг, маннитол — 100 мг, натрия сахаринат — 1.12 мг, повидон — 10 мг, натрия гидрокарбонат — 30 мг, лимонная кислота безводная — 23 мг, ароматизатор мятный — 8 мг, магния стеарат — 4.88 мг.
8 шт. — упаковки ячейковые контурные (3) — пачки картонные.
8 шт. — упаковки ячейковые контурные (5) — пачки картонные.
Фармакологическое действие
Иммуностимулирующий препарат бактериального происхождения для местного применения в оториноларингологии, стоматологии. Представляет собой поливалентный антигенный комплекс, смесь лизатов бактерий, состав которой соответствует возбудителям, наиболее часто вызывающим воспалительные процессы в полости рта и глотки.
Имудон® активирует фагоцитоз, способствует увеличению количества иммунокомпетентных клеток, повышает выработку лизоцима и интерферона, иммуноглобулина А в слюне.
Фармакокинетика
Данные о фармакокинетике не предоставлены.
Показания препарата
Имудон®
Лечение и профилактика инфекционно-воспалительных заболеваний полости рта и глотки:
- фарингит;
- хронический тонзиллит;
- предоперационная подготовка и послеоперационный период после тонзиллэктомии;
- поверхностные и глубокие пародонтозы, пародонтит, стоматит (в т.ч. афтозный), глоссит;
- эритематозный и язвенный гингивит;
- дисбактериоз полости рта;
- инфекции после удаления зубов, имплантации искусственных зубных корней;
- изъязвления, вызванные зубными протезами.
Режим дозирования
Взрослым и подросткам старше 14 лет при острых воспалительных заболеваниях полости рта и глотки и обострении хронических заболеваний препарат назначают в дозе 8 таб./сут. Таблетки рассасывают (не разжевывая) в полости рта с интервалом 1-2 ч. Средняя продолжительность курса лечения — 10 дней.
Для профилактики обострения хронических воспалительных заболеваний полости рта и глотки препарат назначают в дозе 6 таб./сут. Таблетки рассасывают (не разжевывая) в полости рта с интервалом 2 ч. Продолжительность курса лечения — 20 дней.
Рекомендуется проводить профилактические курсы 3-4 раза в год.
Детям в возрасте от 3 до 14 лет при лечении острых и обострении хронических воспалительных заболеваний полости рта и глотки препарат назначают в дозе 6 таб./сут. Таблетки рассасывают (не разжевывая) в полости рта с интервалом 1-2 ч. Продолжительность курса лечения при острых заболеваниях — 10 дней, для профилактики обострения хронических заболеваний — 20 дней.
Курс профилактического применения рекомендуется повторять 3-4 раза в год.
Побочное действие
Аллергические реакции: редко — кожная сыпь, крапивница, ангионевротический отек.
Со стороны пищеварительной системы: редко — тошнота, рвота, боли в животе.
Со стороны дыхательной системы: редко — обострение бронхиальной астмы, кашель.
Дерматологические реакции: очень редко — узловатая эритема.
Со стороны свертывающей системы крови: очень редко — геморрагический васкулит, тромбоцитопения.
Прочие: редко — повышение температуры тела.
Противопоказания к применению
- повышенная индивидуальная чувствительность к препарату или его компонентам;
- аутоиммунные заболевания;
- детский возраст до 3 лет.
Применение при беременности и кормлении грудью
Информация о применении препарата Имудон® при беременности недостаточна. Соответствующие данные экспериментов на животных и эпидемиологические исследования отсутствуют.
Не рекомендуется принимать Имудон® при беременности и в период лактации (грудного вскармливания).
Применение у детей
Противопоказано применение препарата в детском возрасте до 3 лет.
Дети в возрасте от 3 до 6 лет должны рассасывать таблетки под обязательным наблюдением взрослых.
Особые указания
Не следует принимать пищу и воду, а также полоскать рот в течение 1 ч после применения Имудона, чтобы не снижать терапевтическую эффективность препарата.
При назначении препарата пациентам, соблюдающим бессолевую или малосолевую диету, необходимо учитывать, что 1 таб. Имудона содержит 15 мг натрия.
Пациентам с бронхиальной астмой, у которых прием препаратов, содержащих бактериальные лизаты, вызывает обострение заболевания (приступ бронхиальной астмы), применять препарат не рекомендуется.
Использование в педиатрии
Дети в возрасте от 3 до 6 лет должны рассасывать таблетки под обязательным наблюдением взрослых.
Влияние на способность к управлению транспортными средствами и механизмами
Нет данных, свидетельствующих о необходимости каких-либо ограничений деятельности, связанной с управлением автомобилем или другими механизмами в период лечения.
Передозировка
Случаев передозировки препарата Имудон® не описано.
Лекарственное взаимодействие
Лекарственное взаимодействие не отмечено. Имудон® можно применять одновременно с другими лекарственными препаратами.
Условия хранения препарата Имудон®
Препарат следует хранить в недоступном для детей месте при температуре не выше 25°С.
Срок годности препарата Имудон®
Срок годности — 2 года.
Препарат не пригоден к применению при нарушении целостности упаковки (блистера), нечеткой маркировке, после окончания срока годности.
Условия реализации
Препарат отпускают без рецепта.
Контакты для обращений
ЭББОТТ ЛЭБОРАТОРИЗ ООО
(Россия)
|
|
125171 Москва, |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код