Новое об использовании метформина для лечения синдрома поликистозных яичников (СПКЯ).
Применение антидиабетического препарата метформина является одним из основных направлений лечения гормональных нарушений при синдроме поликистозных яичников на Западе. К сожалению, этот вид терапии пока очень мало распространен в нашей стране. В Центре иммунологии и репродукции мы применяем метформин (сиофор, глиформин) с целью дополнительного средства восстановления овуляции и достижения беременности при СПКЯ с 1998 г. За это время мы на своем опыте убедились в благотворном действии препарата на гормональные и клинические показатели у больных. Данная подборка является переводом резюме нескольких недавних публикаций на эту тему.
Терапия метформином ведет к уменьшению проявлений гиперандрогении и гиперинсулинемии у пациенток с синдромом поликистозных яичников (СПКЯ).
Цель исследования: оценить влияние 12-недельной терапии метформином на клинические и гормональные показатели при СПКЯ.
Вид исследования: проспективное.
Группа пациентов: 39 женщин с СПКЯ и гиперинсулинемией натощак.
Методы: 12 недель перорального приема метформина (500 мг 3 раза в день).
Главные критерии оценки результатов: уровень инсулина, тестостерона, ДЭА-сульфата, инсулиноподобного фатора роста-1 (ИФР-1), гонадотропинов, секс-стероидсвязывающего глобулина (СССГ) и клинические признаки, такие как: акне (угревая сыпь), гирсутизм, продолжительность менструального цикла. Была проведена оценка клинических признаков и уровня гормонов до начала терапии метформином и после ее окончания.
Результаты: Результатом терапии метформином явилось существенное снижение концентрации инсулина натощак и уровня общего тестостерона и повышение уровня СССГ, которое привело к уменьшению показателя свободного тестостерона. Кроме того, отмечалось существенное прогрессирующее снижение индекса массы тела, соотношения окружности талии/бедер, уменьшение проявлений гирсутизма, акне и нормализация менструального цикла. Не было отмечено изменений в уровне ЛГ и соотношения ЛГ/ФСГ. Множественный регрессионный анализ продемонстрировал, что наиболее существенное снижение и показателей общего и свободного тестостерона после терапии метформином наблюдалось у пациенток с выраженной гиперандрогенией. Ответ на применение метформина в группе пациенток с повышенным и нормальным уровнями ДЭА-сульфата был различным. В группе женщин с повышенным уровнем ДЭА-сульфата отмечалось меньшее количество случаев нормализации менструального цикла, увеличение уровня ИФР-1 после лечения и не отмечалось уменьшения проявлений гирсутизма.
Заключение: результатом терапии метформином у пациенток с СПКЯ явилось снижение концентрации инсулина, а также общего и биодоступного тестостерона, что привело к заметному клиническому уменьшению проявлений гиперандрогении. Реакция на лечение метформином зависит от степени гиперандрогении и функции надпочечников.
Влияние метформина на резистентность к инсулину и стероидогененез в яичниках у женщин с синдром поликистозных яичников (СПКЯ).
Unluhizarci K, Kelestimur F, Bayram F, et al // Clin Endocrinol. (Oxf.) 1999 Aug; 51(2):231-6
Цель исследования: Синдром поликистозных яичников является разновидностью функциональной яичниковой гиперандрогении и встречается приблизизительно у 5-10% женщин репродуктивного возраста. Инсулинорезистентность и гиперандрогенемия представляются почти универсальными составляющими синдрома поликистозных яичников. Нарушенная регуляция фермента цитохром Р450с17альфа вызывает повышенную выработку андрогенов яичниками при СПКЯ. Целью настоящего исследования было установить, повлияет ли снижение концентрации инсулина в результате воздействия метформина на снижение уровней ФСГ, ЛГ, 17-гидроксипрогестерона (17-ОНП) и андростендиона, а также на гиперреактивность теста с бусерелином у женщин с СПКЯ.
Методы: Наличие гиперинсулинемии у 16 женщин с СПКЯ было подтверждено пероральным тестом на толерантность к глюкозе (ПТТГ), и результаты были сравнены с показателями 13 здоровых женщин. Уровни ФСГ, ЛГ, 17-ОНП и андростендиона в пробе с бусерелином были измерены у всех женщин с СПКЯ до и после 12 недельной терапии метформином (500 мг дважды в день перорально).
Результаты: Результаты в группе пациенток с гиперинсулинемией сравнивались с результатами, полученными у здоровых женщин. Терапия метформином нормализовала менструальную функцию у 25% женщин с СПКЯ, а также улучшила чувствительность к инсулину и снизила базальный уровень инсулина и его уровень после нагрузки глюкозой. Однако ответные уровни гормонов (ФСГ, ЛГ, 17-ОНП и андростендиона) в пробе с бусерелином остались без изменений.
Выводы: очевидно, что СПКЯ часто связан с выраженным повышением резистентности к инсулину и гиперинсулинемией. Эти расстройства объясняют широкую распространенность нарушенной толерантности к глюкозе у женщин с СПКЯ, и в такой ситуации метформин оказывает благотворное действие на чувствительность к инсулину. Уменьшение гиперинсулинемии существенным образом не сказывается на активности фермента цитохром Р450с17альфа в яичниках. Однако метформин может быть использован для лечения пациенток с ожирением и СПКЯ в качестве адъювантной терапии. Желательно проведение долгосрочных исследований, направленных на выяснение механизма эндокринологических эффектов метформина у женщин, страдающих СПКЯ.
Инсулинорезистентность, синдром поликистозных яичников (СПКЯ) и терапия метформином.
Pugeat M, Ducluzeau PH // Drugs. 1999; Suppl 1:41-6; discussion 75-82
Синдром поликистозных яичников (СПКЯ) — одно из наиболее часто встречающихся нарушений функции яичников у женщин репродуктивного возраста. СПКЯ характеризуется хронической ановуляцией и избыточной продукцией андрогенов, клинически проявляющейся нерегулярным характером менструаций, гирсутизмом и появлением угревой сыпи. Инсулинорезистентность и как следствие этого гиперинсулинемия были выявлены у пациенток с СПКЯ, независимо от наличия просто избытка массы тела или явного ожирения. Поскольку инсулин оказывает прямое воздействие на продукцию андрогенов в яичниках in vitro, инсулинорезистентность может играть решающую роль в патофизиологии СПКЯ. И хотя молекулярные механизмы резистентности к инсулину при СПКЯ до конца неясны, у некоторых пациенток с СПКЯ было обнаружено избыточное инсулин-независимое фосфорилирование серина бета-субъединицы рецептора к инсулину, что позволило предложить новый механизм развития инсулинорезистентности. В последнее время был проведен ряд исследований влияния коротких курсов лечения препаратами, повышающими чувствительность к инсулину, на инсулинорезистентность при СПКЯ. Исследования с контрольными группами показали, что прием метформина, обеспечивая уменьшение массы тела, может снижать уровни инсулина натощак и после нагрузки. Другие исследования показали, что применение метформина в дозировке 500 мг три раза в день уменьшает секрецию инсулина и продукцию 17-альфа-гидроксипрогестерона яичниками с восстановлением самостоятельной или индуцированной кломифеном овуляции, независимо от потери веса. Эти данные позволяют рассматривать применение метформина и других повышающих чувствительность к инсулину лекарств в качестве нового подхода к лечению гиперандрогении яичникового генеза и нарушенной овуляции при СПКЯ. Они также позволяют предполагать, что длительный прием метформина может быть полезным в лечении инсулинорезистентности в плане снижения риска развития сахарного диабета (СД) 2 типа (инсулиннезависимого СД) и сердечно-сосудистых осложнений у этой группы пациенток.
Связь приема метформина, и наступления беременности при синдроме поликистозных яичников (СПКЯ): сообщение о трех клинических случаях.
Seal FG, Robinson RD, Neal GS // J Reprod Med. 2000 Jun; 45(6):507-510
Обоснование: Бесплодие — одно из основных проявлений СПКЯ, состояния, характеризующегося хронической ановуляцией, гиперинсулинемией и гиперандрогенемией. Гиперинсулинемия приводит к повышенной выработке андрогенов в яичниках, вызывая атрезию фолликулов и ановуляцию. Метформин, препарат, повышающий чувствительность к инсулину в тканях и снижающий уровень инсулина в сыворотке крови, восстанавливает овуляторную функцию и повышает фертильность у женщин с СПКЯ. Мы приводим три случая из нашей клиники, подтверждающих данную гипотезу.
Описание случаев. В клинике репродуктивной эндокринологии наблюдались три пациентки с документально подтвержденным диагнозом СПКЯ, длительно существующим бесплодием и клинически диагностированной инсулинорезистентностью.
У первой пациентки отмечалась гиперандрогения, кожные проявления инсулинорезистентности в виде acantosis nigricans, а также устойчивость к многочисленным курсам стимуляции овуляции кломифен-цитратом. У второй пациентки наряду с ановуляцией были выявлены гипертензия, гиперлипидемия и нарушение толерантности к глюкозе. Третья пациентка очень желала наступления беременности, но при этом она страдала плохо управляемым сахарным диабетом II типа.
Все больные получали метформин, в результате чего овуляция восстановилась, и наступила беременность.
Выводы: Три описанных случая отражают гетерогенную природу СПКЯ. Коррекция фонового нарушения — инсулинорезистентности — метформином привела к наступилению беременности. Эти наблюдения позволяют сделать предположение, что терапия метформином является полезным дополнительным компонентом лечения бесплодия у пациенток с СПКЯ.
Терапия метформином снижает реакцию цитохрома Р-450с17альфа в яичниках на стимуляцию хорионическим гонадотропином человека (ХГЧ) у женщин с инсулинорезистентным СПКЯ.
la Marca A, Egbe TO, Morgante G, et al // Hum Reprod. 2000 Jan;15(1):21-3
Недавно было сделано предположение, что две составляющие СПКЯ: гиперинсулинемическая инсулинорезистентность и повышенная активность цитохрома Р-450с17альфа в яичниках — патогенетически взаимосвязаны друг с другом. Целью данного исследования явилась проверка гипотезы о взаимосвязи гиперинсулинемиии и повышенной активности цитохрома Р-450с17альфа. При этом использовался тест с ХГЧ, который является более приемлемым стимулятором функции яичников, чем гонадотропин-рилизинг гормон (Гн-РГ), в плане выявления изменений стероидогенеза в яичниках. В исследовании приняли участие 11 женщин с СПКЯ в сочетании с гиперинсулинемией. В/м им вводился ХГЧ (10000 ед.) и проводилось взятие крови в момент введения препарата и спустя 8, 12, 16 и 24 часа. На следующий день начинался курс приема метформин (500 мг трижды в день) продолжительностью 30 — 32 дня. По окончании курса повторно проводился тест с ХГЧ. У двух женщин после приема метформина восстановилась овуляция. Применение метформина вызвало уменьшение площади под кривой концентрации инсулина в пробе на толерантность к глюкозе (75 г глюкозы per os ) в течении 2ч, снижение уровня свободного тестостерона и увеличение концентрации секс-стероидсвязывающего глобулина (СССГ) в плазме крови. Уровень 17-гидроксипргестерона в плазме в ответ на введение ХГЧ оказался значительно ниже после применения метфомина . Данное исследование наглядно продемонстрировало, что применение метфомина ведет к снижению стимулированной активности цитохрома Р-450с17альфа в яичниках у женщин с СПКЯ.
Влияние метформина на инсулиноподобный фактор роста -1 (ИФР-1) и ИФР-1-связывающий белок при СПКЯ.
De Leo V, La Marca A, Orvieto R, et al // J Clin Endocrinol Metab. 2000 Apr;85(4):1598-600
Целью данного исследования была проверка возможного влияния метформина на плазменную концентрацию ИФР-1 и ИФР-1-связывающего глобулина при СПКЯ. Это было открытое исследование, проводимое кафедрой акушерства и гинекологии университета города Сиены в Италии. 17 женщин с СПКЯ получали метформин в дозе 500 мг трижды в день. Терапия продолжалась 30-32 дня, после чего которой проводились контрольные измерения учитываемых параметров (плазменные концентрации ЛГ, ФСГ, эстрадиола, свободного тестостерона, ИФР-1, ИФР-1-связывающего глобулина, секс-стероидсвязывающего глобулина и инсулина). Терапия метформином привела к заметному уменьшению площади под кривой концентрации инсулина, снижению уровня свободного тестостерона и повышению концентрации секс-стероидсвязывающего белка в плазме крови. Также было отмечено статистически незначимое повышение уровня ИФР-1-связывающего глобулина и значимое увеличение концентрации ИФР-1 в плазме. Соотношение ИФР-1/ИФР-1-связывающий белок заметно снизилось по окончании курса терапии по сравнению с исходным значением этого показателя.
Представляется целесообразным применение препаратов, повышающих чувствительность к инсулину, таких как метформин, с целью разрыва патогенетической взаимосвязи между гирепинсулинемией и гормональными нарушениями при СПКЯ.
Влияние метформина на стероидогенез в надпочечниках у женщин с СПКЯ.
la Marca A, Morgante G, Paglia T, et al // Fertil Steril. 1999 Dec;72(6):985-9
Цель исследования: определить, вызывает ли применение метформина изменения в надпочечниковом стероидогенезе у женщин с СПКЯ.
Вид исследования: проспективное.
Место проведения: кафедра акушерства и гинекологии университета города Сиена, Италия.
Контингент исследуемых: 14 женщин с диагнозом СПКЯ.
Объект исследования: пробы крови, полученные за 15 мин. до начала введения АКТГ, непосредственно перед введением препарата и спустя 15, 30, 45 и 60 мин. после его введения. После терапии метформином в течении 30-32 дней (ежедневно 500 мг трижды в день) был проведен повтор вышеназванной пробы с АКТГ.
Основные оцениваемые параметры: уровень андрогенов надпочечникового происхождения перед началом пробы с АКТГ и после нее.
Результаты: овуляция в ответ на терапию метформином произошла у 2 женщин (14%). Было отмечено существенное снижение концентрации свободного тестостерона и повышение уровня секс-стероидсвязывающего белка в плазме крови. Применение метфомина вызвало заметное снижение уровней 17-альфагидроксипрогестерона, тестостерона, свободного тестостерона и андростендиона в ответ на введение АКТГ по сравнению с исходными показателями. Соотношение 17-альфагидроксипрогестерон/прогестерон, отражающее акативность 17альфа-гидроксилазы, и соотношение андростендион/17-альфагидроксипрогестерон, отражающее активность 17,20-лиазы, были заметно уменьшены после месяца применения метформина, что указывает на снижение активности данных ферментов.
Выводы: применение метформина у женщин с СПКЯ, которые не были специально отобраны по каким-либо дополнительным параметрам, привело к снижению активности стероидогенеза в ответ на введение АКТГ по сравнению с исходными показателями. Эти данные подтверждают предположение, что высокая концентрация инсулина при СПКЯ может вызывать повышение уровня андрогенов надпочечникового происхождения в плазме крови.
ВВЕДЕНИЕ
Эндометриоз — хроническое воспалительное гормонозависимое гинекологическое заболевание доброкачественного течения, характеризующееся наличием ткани, подобной эндометрию, за пределами полости матки. Эндометриоидные очаги в большинстве случаев обнаруживаются на брюшине малого таза, яичниках и маточно-крестцовых связках, в ректовагинальной перегородке и пузырно-маточной складке, реже в кишечнике, диафрагме, пупке, перикарде и плевре. У некоторых женщин эндометриоз может протекать бессимптомно, однако зачастую это заболевание становится причиной бесплодия или различных вариантов болевого синдрома, таких как дисменорея, диспареуния, хроническая тазовая боль (ХТБ)[1].
Болевой синдром является одним из самых частых клинических проявлений эндометриоза и крайне негативно влияет на качество жизни, сексуальную функцию, эффективность работы и социальную жизнь женщины. Хирургическое удаление очагов эндометриоза значительно уменьшает болевой синдром[2], однако может быть связано с интра- и постоперационными осложнениями и снижением овариального резерва. Кроме того, после оперативного лечения ассоциированного с эндометриозом болевого синдрома наблюдается значительная частота рецидивов[3]. Таким образом, ключевую роль в долгосрочном лечении и предупреждении рецидивов эндометриоза играет медикаментозная терапия[4, 5].
Ряд авторов считает, что современные гормональные методы лечения практически не повышают частоту наступления беременности при ассоциированном с эндометриозом бесплодии и направлены преимущественно на уменьшение болевого синдрома[6]1. При этом в период, когда пациентки прекращают гормональную терапию заболевания в связи с побочными эффектами или для реализации репродуктивной функции, боли могут возобновиться[6]2. Общепризнано, что эстрогены имеют первостепенное значение в развитии и прогрессировании эндометриоза. Большинство гормональных препаратов, используемых в настоящее время для лечения боли, связанной с эндометриозом, в первую очередь оказывают влияние на подавление секреции эстрадиола яичниками, модулируя гипоэстрогенное состояние[6]. Гормональная терапия первой линии, используемая для лечения ассоциированного с эндометриозом болевого синдрома, сегодня представлена прогестагенами и агонистами гонадотропин-рилизинг-гормона3.
Однако после первоначального описания предполагаемого патогенеза эндометриоза, сделанного J.A. Sampson[7], знания о молекулярных путях развития заболевания значительно расширились. На основании результатов молекулярных исследований для его лечения было протестировано (in vitro и на животных моделях хирургически индуцированного экспериментального эндометриоза) несколько новых лекарственных средств[8].
Одним из этих средств стал бигуанид метформин. Предполагаемый механизм лечебного действия метформина при эндометриозе заключается в снижении активности фермента ароматазы и подавлении пролиферации железистого компонента эндометрия[9]. Поступление холестерина в митохондрии контролируется стероидогенным острым регуляторным белком (англ. Steroidogenic Acute Regulatory protein, StAR), уровень которого в стромальных клетках эндометриоидных гетеротопий в 264 раза выше, чем в эутопическом эндометрии[10]. В литературе представлены данные о супрессивном влиянии метформина на продукцию StAR, регулирующего биосинтез эстрогенов[10, 11]. Содержание эстрадиола, циркулирующего в крови, снижается в ответ на повышение уровня глобулина, связывающего половые гормоны, и это приводит к уменьшению очагов эндометриоза[12].
Кроме того, установлено, что метформин оказывает прямое влияние на стероидогенез в ткани яичников, подавляя выработку ФСГ, прогестерона и эстрадиола в гранулезных клетках[13]. Таким образом, метформин может подавлять эндометриоидные гетеротопии за счет ингибирования как овариальной, так и локальной продукции эстрогенов. При использовании метформина зафиксировано увеличение количества рецепторов к прогестерону в клетках карциномы эндометрия[14].
Исходя из известных механизмов действия метформина на процессы стероидогенеза, воспаления и пролиферации, которые играют существенную роль в патогенезе эндометриоза, можно предположить, что данный бигуанид перспективен для патогенетического лечения эндометриоза.
Ранее нами на основании экспериментальной модели эндометриоза на крысах было продемонстрировано уменьшение размеров (61%) или полная резорбция (39%) эндометриоидных имплантатов на фоне применения метформина, причем его эффективность была сопоставима с эффективностью диеногеста — классического прогестагена для лечения эндометриоза, который в настоящее время рассматривается в качестве первой линии терапии заболевания[15].
Цель исследования: оценить клиническую эффективность метформина в комбинированной и монотерапии наружного генитального эндометриоза (НГЭ).
МАТЕРИАЛЫ И МЕТОДЫ
Открытое проспективное рандомизированное неконтролируемое исследование в параллельных группах проведено в центре «Диагностика и лечение эндометриоза» ФГБНУ «Научно-исследовательский институт акушерства, гинекологии и репродуктологии им. Д.О. Отта» (директор НИИ АГиР им. Д.О. Отта — член-корреспондент РАН, д. м. н., профессор И.Ю. Коган) в 2017–2018 гг. Набор пациенток осуществлялся в течение 1,5 года, общая продолжительность работы составила 2 года.
Дизайном исследования предусматривалось сравнение экспериментального лечения ассоциированного с эндометриозом болевого синдрома метформином в дозе 1500 мг/день
«вне инструкции» со стандартной гормональной терапией диеногестом в дозе 2 мг/день, а также схем комбинированного применения стандартной гормональной терапии диеногестом в дозе 2 мг/день с метформином в дозах 750 и 1500 мг/день. Нулевая гипотеза заключалась в утверждении, что использование метформина в терапии ассоциированного с эндометриозом болевого синдрома не способствует изменению частоты и интенсивности дисменореи, диспареунии и ХТБ.
В исследование были отобраны 146 женщин с ассоциированным с эндометриозом болевым синдромом.
Критериями включения являлись:
– подписанное и датированное информированное согласие на применение метформина «вне инструкции» для терапии НГЭ;
– возраст от 18 до 45 лет;
– регулярный менструальный цикл;
– диагноз НГЭ, установленный во время органосохраняющей операции, выполненной лапароскопическим доступом, с последующим гистологическим подтверждением;
– наличие ассоциированного с эндометриозом болевого синдрома, документально подтвержденное регистрацией одного или нескольких симптомов: дисменореи; болей в области малого таза, не связанных с менструальным циклом; диспареунии.
В исследование не включались женщины с ожирением, миомой матки, синдромом поликистозных яичников, сахарным диабетом, гипер- или гипогонадотропной недостаточностью яичников, гиперчувствительностью к любому компоненту используемых препаратов, нарушением функции почек или печени, хроническими соматическими заболеваниями в стадии декомпенсации.
Из 146 участниц исследования были сформированы четыре группы:
– в группе 1 (n = 32; 21,9%) применяли стандартную терапию диеногестом в дозе 2 мг/день;
– группа 2 (n = 61; 41,8%) получала комбинированную терапию в составе 2 мг диеногеста и 1500 мг метформина ежедневно;
– в группу 3 (n = 29; 19,9%) входили пациентки с дефицитом массы тела или отказавшиеся от прохождения перорального глюкозотолерантного теста, которым была назначена комбинированная терапия из 2 мг диеногеста и 750 мг метформина ежедневно;
– к группе 4 (n = 24; 16,4%) относились пациентки с противопоказаниями к назначению гормономодулирующей терапии, планировавшие беременность или воздерживавшиеся от приема гормональных препаратов, у которых проводилась монотерапия метформином в дозе 1500 мг/день.
Распределение женщин в группы 1 и 2 происходило случайным образом. Для рандомизации использовался блочный метод.
Все препараты назначались перорально 1 раз в день. Для уменьшения побочных эффектов метформин в группах 2 и 4 вводился с постепенной титрацией: в дозе 750 мг/день в течение 1-й недели с последующим переходом на 1500 мг/день. Применение терапии в группах пациенток, получавших диеногест или комбинацию диеногеста и метформина, было рекомендовано с 5-го дня менструального цикла. Продолжительность лечения во всех группах составила 6 месяцев.
Обследование включало опрос, сбор акушерско-гинекологического и соматического анамнеза пациенток. В ходе опроса особое внимание уделялось оценке интенсивности болевого синдрома по визуально-аналоговой шкале (ВАШ). Всем пациенткам проводили стандартное физикальное и специальное гинекологическое обследование.
В качестве основного исхода оценивалась динамика дисменореи, диспареунии и ХТБ у больных НГЭ по ВАШ с выделением двух контрольных точек — на этапе включения в исследование и через 6 месяцев терапии.
Для статистического анализа данных было использовано программное обеспечение Jamovi с открытым исходным кодом (Сидней, Австралия). Проверку нормальности распределения проводили с помощью критерия Шапиро — Уилка. Описание количественных данных с нормальным распределением выполнено с применением среднего значения (M) и стандартного отклонения (SD), данные с распределением, отличавшимся от нормального, описаны медианой (Me) и квартилями (Q1; Q3). Для сравнения количественных данных между группами использованы t-критерий Стьюдента и критерий Манна — Уитни, для анализа номинальных данных — критерий хи-квадрат (χ2) Пирсона с определением отношения шансов (OR) и 95%-ного доверительного интервала (ДИ). Различия считались статистически значимыми при p < 0,05.
Исследование одобрено локальным этическим комитетом ФГБНУ «НИИ АГиР им. Д.О. Отта» (протокол № 80 от 11.10.2016).
РЕЗУЛЬТАТЫ
Клинические характеристики участниц исследования
Возраст включенных в исследование женщин с НГЭ (n = 146) составлял 31,3 ± 6,4 года (от 22 до 44 лет). Все пациентки имели ассоциированный с эндометриозом болевой синдром. Наиболее распространенной являлась дисменорея, отмечавшаяся у 137 (93,8%) больных НГЭ, ее выраженность составляла 6 (4; 
У большинства (n = 133; 91,1%) пациенток ИМТ находился в пределах нормальных значений, у 6 (4,1%) был отмечен избыток массы тела, у 7 (4,8%) — дефицит массы тела. Средний показатель ИМТ составил 22,49 ± 3,26 кг/м2.
Средний возраст наступления менархе — 12,9 ± 3,8 года (от 10 до 16 лет). Средняя продолжительность менструального цикла — 26,3 ± 4,4 дня (от 20 до 38 дней). Регулярный менструальный цикл отмечен у 124 (84,9%) женщин. Среди нарушений менструального цикла ведущими были аномальные маточные кровотечения по типу перименструальных кровянистых выделений (n = 77; 52,7%). Отмечались также олигоменорея (n = 44; 30,1%), межменструальные мажущие кровянистые выделения (n = 25; 17,1%), обильные менструальные кровотечения (n = 7; 4,8%).
Основные результаты исследования
После окончания курса лечения частота встречаемости исследуемых проявлений болевого синдрома — дисменореи, диспареунии, ХТБ — статистически значимо уменьшилась во всех группах (p < 0,001) (рис.).
Рис. Изменение частоты встречаемости болевого синдрома на фоне различных видов медикаментозной терапии, %
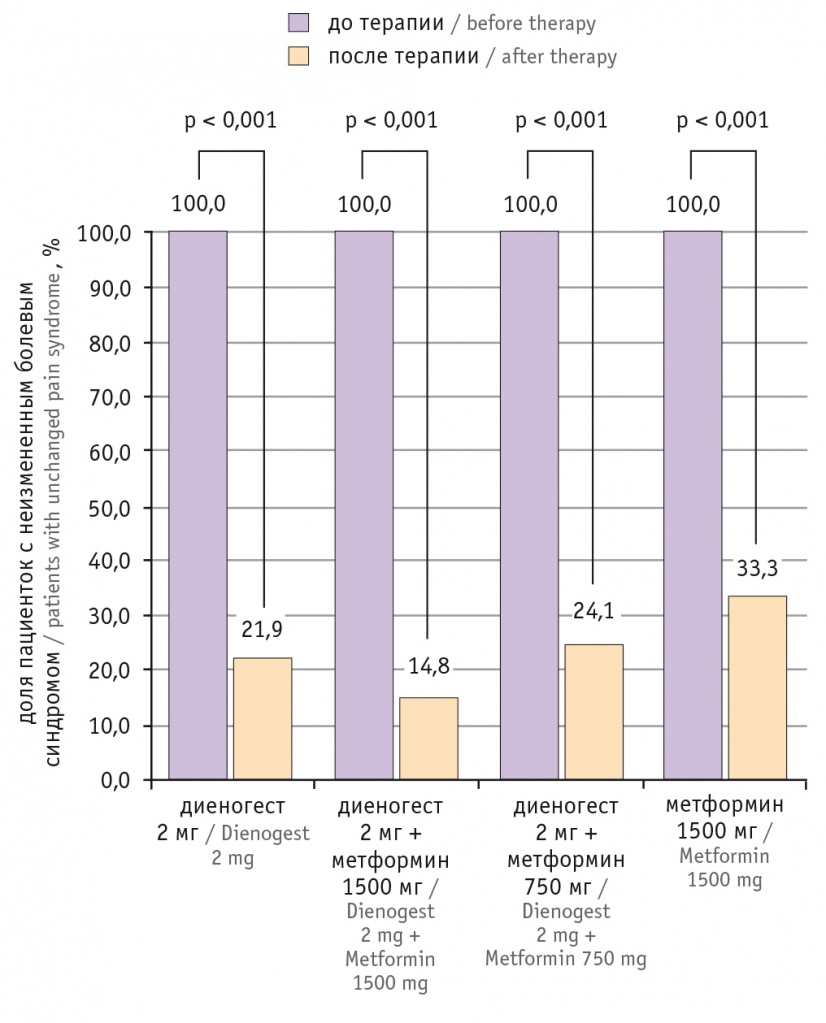
При применении комбинации 2 мг диеногеста с 1500 мг метформина (группа 2) у 85,2% (52/61) больных отмечено уменьшение болевого синдрома: 24 пациентки перестали предъявлять жалобы на боли; у остальных выраженность дисменореи по ВАШ снизилась в 2,6 раза, диспареунии — в 1,3 раза, ХТБ — в 2,5 раза. Применение комбинации 2 мг диеногеста с 750 мг метформина (группа 3) характеризовалось уменьшением болевого синдрома у 75,9% (22/29) больных с полным исчезновением боли у 17 пациенток и ослаблением у 5 женщин, среди которых выраженность дисменореи снизилась в 2,0 раза, диспареунии — в 2,9 раза, ХТБ — в 1,6 раза. В группах пациенток, получавших монотерапию диеногестом в дозе 2 мг/день (группа 1) или метформином в дозе 1500 мг/день (группа 4), болевой синдром уменьшился у 78,1% (25/32) и 66,7% (16/24) женщин соответственно. Болевой синдром в группе 1 перестал беспокоить 19 пациенток, у остальных выраженность дисменореи снизилась в 2,4 раза, диспареунии — в 3,3 раза, ХТБ — в 1,5 раза. В группе 4 болевой синдром исчез у 9 пациенток, у остальных выраженность дисменореи снизилась в 1,8 раза, диспареунии — в 1,5 раза, ХТБ — в 1,5 раза (см. рис., табл.).
Таблица
Динамика болевого синдрома у больных наружным генитальным эндометриозом на фоне различных видов медикаментозной терапии, баллы по визуально-аналоговой шкале, Me (Q1; Q3)
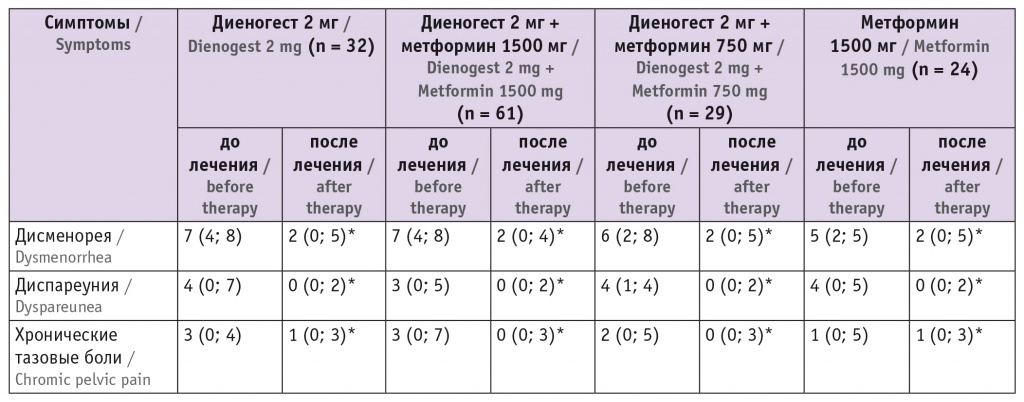
Примечание. Знаком (*) отмечены статистически значимые различия с исходными данными (p < 0,05).
При анализе исходов с помощью критерия χ2 Пирсона выявлены статистически значимые улучшения у пациенток, получавших комбинированную терапию в составе 2 мг диеногеста и 1500 мг метформина (группа 2), по сравнению с пациентками, получавшими только диеногест в дозе 2 мг/день (группа 1). Уменьшение дисменореи в группе 2 наблюдалось чаще (OR = 2,87; 95%-ный ДИ: 1,07–7,66; p = 0,031), а снижение интенсивности ХТБ было более выраженным, чем при монотерапии диеногестом (p = 0,027). Однако шансы и степень уменьшения диспареунии в этих группах не имели статистически значимых различий (χ2 = 0,03; p = 0,858).
Статистически значимых отличий исходов лечения в группах 3, 4 от исходов монотерапии диеногестом обнаружено не было, однако небольшой объем выборки не позволяет сделать окончательный вывод о сопоставимой эффективности этих схем.
Нежелательные явления
На фоне лечения диеногестом в дозе 2 мг/день у 37,5% (n = 12) пациенток побочных эффектов не возникло, 59,4% (n = 19) женщин отмечали нерегулярные мажущие кровянистые выделения, 12,5% (n = 4) предъявляли жалобы на мастодинию, у 3,1% (n = 1) появились приливы. При проведении терапии у 12,5% (n = 4) больных были обнаружены функциональные образования яичников размерами от 20 до 35 мм. В одном случае пациентка прекратила прием диеногеста в связи с появлением аллергической реакции.
На фоне сочетанного применения 2 мг диеногеста с 1500 мг метформина у 45,9% (n = 28) больных побочных эффектов не возникло, 34,4% (n = 21) женщин отмечали нерегулярные мажущие кровянистые выделения, 8,2% (n = 5) — мастодинию, 6,6% (n = 4) — появление приливов. У 8,2% (n = 5) пациенток при динамическом наблюдении в течение лечения были обнаружены функциональные кисты яичников размерами от 30 до 42 мм.
В группе, получавшей комбинированную терапию из 2 мг диеногеста и 750 мг метформина, у 17,2% (n = 5) пациенток побочных эффектов не возникло, нарушения менструального цикла по типу нерегулярных мажущих кровянистых выделений отмечали 65,5% (n = 19) женщин, мастодинию — 17,2% (n = 5), у 10,3% (n = 3) пациенток при проведении УЗИ органов малого таза были обнаружены функциональные образования яичников размерами до 40 мм.
Среди всех пациенток, получавших метформин в режиме монотерапии или в комбинации с диеногестом (группы 2, 3, 4), 21,1% (24/114) женщин отмечали эпизоды тошноты, металлического привкуса во рту, диспепсических явлений в начале курса лечения, однако данные побочные явления носили транзиторный характер и не явились основанием для отмены терапии.
ОБСУЖДЕНИЕ
Результаты настоящего исследования демонстрируют статистически значимое уменьшение частоты и выраженности ассоциированного с эндометриозом болевого синдрома на фоне терапии метформином. Высокая эффективность препарата, вероятно, обусловлена его антипролиферативным и противовоспалительным эффектом, влиянием на активность овариальной ароматазы и стероидные половые гормоны.
Комбинированное применение 2 мг диеногеста и 1500 мг метформина у больных НГЭ сопровождалось статистически значимым уменьшением частоты и интенсивности болевого синдрома. По сравнению с шестимесячным курсом лечения диеногестом в дозе 2 мг/день, сочетанная терапия с включением 1500 мг метформина характеризовалась более частым уменьшением выраженности дисменореи (OR = 2,87; 95%-ный ДИ: 1,07–7,66; p = 0,031) и более выраженным снижением интенсивности ХТБ (p = 0,027).
Немногочисленные литературные данные также подтверждают перспективность применения метформина в лечении эндометриоза как на экспериментальных моделях[16, 17], так и в клинических исследованиях[18, 19].
Нами впервые разработаны персонифицированные схемы комбинированного применения диеногеста с метформином в различных дозировках. Комбинация прогестагена с 1500 мг метформина в день продемонстрировала более высокую эффективность по сравнению со стандартной гормономодулирующей терапией диеногестом в дозе 2 мг/день.
78,9% (90/114) пациенток отметили удовлетворительную переносимость метформина, на фоне его использования не было зафиксировано серьезных побочных эффектов, что подтверждает безопасность использования препарата.
Период наблюдения не позволяет сделать выводы о влиянии метформина на рецидивы эндометриоза. Необходимо проведение дальнейших исследований с увеличением длительности использования препарата для уточнения данных о его эффективности и безопасности.
ЗАКЛЮЧЕНИЕ
Полученные данные свидетельствуют об обоснованности применения метформина в комбинированной терапии ассоциированного с эндометриозом болевого синдрома. Наиболее эффективно сочетанное использование 1500 мг метформина с 2 мг диеногеста 1 раз в день. При наличии противопоказаний к приему гормональных препаратов может применяться монотерапия метформином в дозе 1500 мг/день, которая также характеризуется статистически значимым уменьшением выраженности болевого синдрома у больных генитальным эндометриозом. В случаях плохой переносимости 1500 мг метформина, дефицита массы тела или отказа от проведения глюкозотолерантного теста возможно использование 750 мг метформина в комбинации с 2 мг диеногеста 1 раз в день.
Перспективным направлением является персонализированная патогенетически обоснованная терапия генитального эндометриоза с индивидуальным подбором комбинации препаратов и дозы метформина.
Поступила: 12.03.2021
Принята к публикации: 31.03.2021
________
1 Endometriosis: diagnosis and management. NICE Guideline [NG73]. Published: Sept. 6, 2017. URL: https://www.nice.org.uk/guidance/ng73 (дата обращения — 01.03.2021).
2 Там же.
3 Эндометриоз: Клинические рекомендации МЗ РФ. URL: https://roag-portal.ru/recommendations_gynecology (дата обращения — 01.03.2021).
МЕТФОРМИН — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер
ЛП-005456
Торговое наименование препарата
Метформин
Международное непатентованное наименование
Метформин
Лекарственная форма
таблетки, покрытые пленочной оболочкой
Состав
На одну таблетку:
действующее вещество: метформина гидрохлорид — 500,0 мг или 850,0 мг, или 1000,0 мг;
вспомогательные вещества (ядро): повидон К-30 — 20,0 мг или 34,0 мг или 40,0 мг, магния стеарат — 5,0 мг или 8,5 мг или 10,0 мг, глицерила дибегенат — 20,0 мг или 34,0 мг или 40,0 мг, гипролоза (низкозамещенная) — 30,0 мг или 51,0 мг или 60,0 мг;
вспомогательные вещества (пленочная оболочка): гипромеллоза — 3,75 мг или 5,94 мг или 7,5 мг, макрогол 4000 (полиэтиленгликоль 4000) — 0,90 мг или 1,42 мг или 1,80 мг, титана диоксид — 1,35 мг или 2,14 мг или 2,7 мг.
Описание
Круглые, двояковыпуклой формы таблетки, покрытые пленочной оболочкой, белого или почти белого цвета.
Фармакотерапевтическая группа
Гипогликемическое средство для перорального применения группы бигуанидов
Код АТХ
A10BA02
Фармакодинамика:
Метформин снижает гипергликемию, не приводя к развитию гипогликемии. В отличие от производных сульфонилмочевины, не стимулирует секрецию инсулина и не оказывает гипогликемического эффекта у здорового человека. Повышает чувствительность периферических рецепторов к инсулину и утилизацию глюкозы клетками. Тормозит глюконеогенез в печени. Задерживает всасывание углеводов в кишечнике. Стимулирует синтез гликогена, активируя гликогенсинтазу. Увеличивает транспортную емкость всех типов мембранных переносчиков глюкозы.
Кроме того, оказывает благоприятный эффект на метаболизм липидов: снижает концентрацию общего холестерина, липопротеинов низкой плотности и триглицеридов.
На фоне приема метформина масса тела пациента либо остается стабильной, либо умеренно снижается.
Клинические исследования показали также эффективность метформина для профилактики сахарного диабета у пациентов с предиабетом с дополнительными факторами риска развития явного сахарного диабета 2 типа, у которых изменения образа жизни не позволили достичь адекватного гликемического контроля.
Фармакокинетика:
Абсорбция
После приема внутрь метформин абсорбируется из желудочно-кишечного тракта достаточно полно. Доля невсосавшегося метформина, обнаруженного в кале, составляет 20-30%. Процесс всасывания метформина характеризуется насыщаемостью. Предполагается, что фармакокинетика его всасывания нелинейна.
Максимальная концентрация (Сmах) (примерно 2 мкг/мл или 15 мкмоль) в плазме крови достигается через 2,5 ч. При применении в рекомендуемых дозах равновесная концентрация метформина в плазме крови достигается в течение 24-48 ч и, как правило, не превышает 1 мкг/мл.
Абсолютная биодоступность у здоровых добровольцев составляет 50-60%. При одновременном приеме пищи абсорбция метформина снижается и задерживается.
Распределение
Метформин быстро распределяется в ткани, практически не связывается с белками плазмы. Сmах в крови ниже Сmах в плазме крови и достигается примерно за то же время.
Метформин проникает в эритроциты. Вероятно, эритроциты представляют собой вторичный компартмент распределения метформина. Средний объем распределения составляет 63-276 л.
Метаболизм и выведение
Подвергается метаболизму в очень слабой степени, метаболитов в организме не обнаружено. Выводится преимущественно почками в неизмененном виде. Клиренс метформина у здоровых добровольцев составляет более 400 мл/мин (в 4 раза больше, чем клиренс креатинина), что свидетельствует о наличии активной канальциевой секреции.
Период полувыведения составляет приблизительно 6,5 ч.
Нарушение функции почек
При нарушении функции почек клиренс метформина уменьшается пропорционально клиренсу креатинина, соответственно, период полувыведения увеличивается, концентрация метформина в плазме крови повышается, повышается риск его кумуляции.
Дети
При однократном применении в дозе 500 мг у детей фармакокинетические параметры метформина были сходны с таковыми у здоровых взрослых.
При многократном применении в дозе 500 мг 2 раза в сутки в течение 7 дней у детей Сmах и площадь по кривой «концентрация-время» (AUC0-t) метформина были снижены примерно на 33% и 40% соответственно, по сравнению со взрослыми пациентами с сахарным диабетом, которые получали метформин в дозе 500 мг 2 раза в сутки в течение 14 дней. Поскольку доза метформина подбирается индивидуально на основании показателей гликемического контроля, полученные данные имеют ограниченную клиническую значимость.
Показания:
Сахарный диабет 2 типа, особенно у пациентов с ожирением, при неэффективности диетотерапии и физических нагрузок:
- у взрослых в качестве монотерапии или в сочетании с другими пероральными гипогликемическими средствами, или с инсулином;
- у детей с 10 лет в качестве монотерапии или в сочетании с инсулином.
Профилактика сахарного диабета 2 типа у пациентов с предиабетом с дополнительными факторами риска развития сахарного диабета 2 типа, у которых изменения образа жизни не позволили достичь адекватного гликемического контроля.
Противопоказания:
— Повышенная чувствительность к метформину и/или любому вспомогательному веществу препарата;
— диабетический кетоацидоз, диабетическая прекома, кома;
— почечная недостаточность или нарушение функции почек (клиренс креатинина менее 45 мл/мин);
— острые состояния, протекающие с риском развития нарушения функции почек: дегидратация (при диарее, рвоте), тяжелые инфекционные заболевания, шок;
— клинически выраженные проявления острых и хронических заболеваний, которые могут приводить к развитию тканевой гипоксии (в том числе, острая сердечная недостаточность, хроническая сердечная недостаточность с нестабильными показателями гемодинамики, дыхательная недостаточность, острый инфаркт миокарда);
— обширные хирургические операции и травмы, когда показано проведение инсулинотерапии (см. раздел «Особые указания»);
— печеночная недостаточность, нарушение функции печени;
— хронический алкоголизм, острое отравление алкоголем;
— беременность;
— лактоацидоз (в т.ч. и в анамнезе);
— применение в течение менее 48 ч до и в течение 48 ч после проведения радиоизотопных или рентгенологических исследований с введением йодсодержащего контрастного вещества;
— соблюдение низкокалорийной диеты (менее 1000 ккал/сут);
— детский возраст до 10 лет.
С осторожностью:
Применять препарат у детей в возрасте от 10 до 12 лет, лиц старше 60 лет, выполняющих тяжелую физическую работу, что связано с повышенным риском развития у них лактоацидоза; у пациентов с почечной недостаточностью (клиренс креатинина 45-59 мл/мин); в период грудного вскармливания.
Беременность и лактация:
Декомпенсированный сахарный диабет во время беременности связан с повышенным риском возникновения врожденных пороков и перинатальной смертности.
Ограниченное количество данных свидетельствует о том, что прием метформина у беременных женщин не увеличивает риск развития врожденных пороков у детей.
При планировании беременности, а также в случае наступления беременности на фоне приема метформина при предиабете или сахарном диабете 2 типа, препарат должен быть отменен, и назначена инсулинотерапия. Необходимо поддерживать содержание глюкозы в плазме крови на уровне, наиболее близком к норме для снижения риска возникновения пороков развития плода.
Метформин проникает в грудное молоко. Побочные эффекты у новорожденных при грудном вскармливании на фоне приема метформина не наблюдались. Однако в связи с ограниченным количеством данных, применение препарата в период грудного вскармливания не рекомендовано. Решение о прекращении грудного вскармливания должно быть принято с учетом пользы от грудного вскармливания и потенциального риска возникновения побочных эффектов у ребенка.
Способ применения и дозы:
Препарат Метформин принимают внутрь, во время или после еды, не разжевывая, запивая достаточным количеством воды.
Взрослые
Монотерапия и комбинированная терапия в сочетании с другими пероральными гипогликемическими средствами при сахарном диабете 2 типа
— Обычная начальная доза составляет 500 мг или 850 мг 2-3 раза в сутки после или во время приема пищи. Возможно дальнейшее постепенное увеличение дозы в зависимости от концентрации глюкозы в крови.
— Через каждые 10-15 дней рекомендуется корректировать дозу на основании результатов измерения концентрации глюкозы в плазме крови.
— Поддерживающая доза препарата обычно составляет 1500-2000 мг/сут. Для уменьшения побочных явлений со стороны ЖКТ суточную дозу следует разделить на 2-3 приема. Максимальная доза составляет 3000 мг/сут, разделенная на 3 приема.
— Медленное увеличение дозы может способствовать уменьшению нежелательных реакций со стороны ЖКТ.
— Пациенты, принимающие метформин в дозах 2000-3000 мг/сут, могут быть переведены на прием препарата 1000 мг. Максимальная рекомендованная доза составляет 3000 мг/сут, разделенная на 3 приема.
В случае планирования перехода с другого гипогликемического препарата необходимо прекратить прием этого препарата и начинать прием препарата Метформин в дозе, указанной выше.
Комбинация с инсулином
Для достижения лучшего контроля глюкозы в крови метформин и инсулин можно применять в виде комбинированной терапии. Обычная начальная доза препарата Метформин в дозировках 500 мг или 850 мг составляет одну таблетку 2-3 раза в сутки, в то время как дозу инсулина подбирают на основании концентрации глюкозы в крови.
Дети и подростки
С 10-летнего возраста препарат может применяться как в монотерапии, так и в сочетании с инсулином. Обычная начальная доза составляет 500 мг или 850 мг 1 раз в сутки после или во время приема пищи. Через 10-15 дней дозу необходимо скорректировать на основании концентрации глюкозы крови. Максимальная суточная доза составляет 2000 мг, разделенная на 2-3 приема.
Монотерапия при предиабете:
Обычная доза составляет 1000-1700 мг в сутки после приема пищи, разделенная на 2 приема.
Рекомендуется регулярно проводить гликемический контроль для оценки необходимости дальнейшего применения препарата.
Пациенты пожилого возраста
Из-за возможного снижения функции почек дозу препарата Метформин необходимо подбирать под регулярным контролем показателей функции почек (определять концентрацию креатинина в сыворотке крови не менее 2-4 раз в год).
Пациенты с нарушением функции почек
Метформин может применяться у пациентов с почечной недостаточностью средней степени тяжести (клиренс креатинина 45-59 мл/мин) только в случае отсутствия состояний, которые могут увеличивать риск развития лактоацидоза.
Пациенты с клиренсом креатинина 45-59 мл/мин: начальная доза составляет 500 мг или 850 мг один раз в сутки. Максимальная доза составляет 1000 мг в сутки, разделенная на 2 приема. Функция почек должна тщательно контролироваться (каждые 3-6 месяцев). Если клиренс креатинина ниже 45 мл/мин, прием препарата должен быть немедленно прекращен.
Длительность лечения
Препарат Метформин следует принимать ежедневно, без перерыва. В случае прекращения лечения пациент должен сообщить об этом врачу.
Побочные эффекты:
Частота побочных эффектов препарата расценивается следующим образом: очень часто: > 1/10; часто: 1/10-1/100; нечасто: 1/100-1/1000; редко: 1/1000-1/10000; очень редко: <1/10000.
Нарушения со стороны обмена веществ и питания
Очень редко: лактоацидоз (см. раздел «Особые указания»).
При длительном приеме метформина может наблюдаться снижение всасывания витамина В12. При обнаружении мегалобластной анемии необходимо учитывать возможность такой этиологии.
Нарушения со стороны нервной системы
Часто: нарушение вкуса.
Нарушения со стороны желудочно-кишечного тракта
Очень часто: тошнота, рвота, диарея, отсутствие аппетита, боль в животе.
Данные побочные эффекты часто возникают в начальный период лечения и в большинстве случаев, при продолжении приема, они спонтанно проходят. Для уменьшения побочных эффектов рекомендуется принимать препарат во время или после приема пищи. Медленное увеличение дозы может улучшить желудочно-кишечную переносимость.
Нарушения со стороны печени и желчевыводящих путей
Очень редко: нарушение показателей функции печени и гепатит. После отмены метформина эти нежелательные явления полностью исчезают.
Нарушения со стороны кожи и подкожных тканей
Очень редко: кожные реакции, такие как эритема, зуд, сыпь.
Опубликованные постмаркетинговые данные, а также контролируемые клинические исследования в ограниченной детской популяции в возрастной группе 10-16 лет показывают, что побочные эффекты у детей по характеру и тяжести схожи с таковыми у взрослых пациентов.
Передозировка:
Симптомы: при применении метформина в дозе 85 г (в 42,5 раз превышающей максимальную суточную дозу) гипогликемии не наблюдалось, однако отмечалось развитие лактоацидоза. Значительная передозировка метформина или сопряженные факторы риска могут привести к развитию лактоацидоза (см. раздел «Особые указания»).
Лечение: в случае появления признаков лактоацидоза лечение препаратом необходимо немедленно прекратить, пациента срочно госпитализировать и, определив концентрацию лактата, уточнить диагноз. Наиболее эффективным мероприятием по выведению из организма лактата и метформина является гемодиализ. Проводят также симптоматическое лечение.
Взаимодействие:
Противопоказанные комбинации
Йодсодержащие рентгеноконтрастные средства: на фоне функциональной почечной недостаточности у пациентов с сахарным диабетом радиологическое исследование с применением йодсодержащих рентгеноконтрастных средств может вызывать развитие лактоацидоза. Лечение метформином необходимо отменить в зависимости от функции почек за 48 ч до или на время рентгенологического исследования с применением йодсодержащих рентгеноконтрастных средств и не возобновлять ранее 48 ч после, при условии, что в ходе обследования функция почек была признана нормальной.
Нерекомендуемые комбинации
Алкоголь: при острой алкогольной интоксикации возрастает риск развития лактоацидоза, особенно в случае:
- недостаточного питания;
- соблюдения низкокалорийной диеты;
- печеночной недостаточности.
Во время приема препарата следует избегать приема алкоголя и лекарственных средств, содержащих этанол.
Комбинации, требующие применения с осторожностью
Даназол: не рекомендуется одновременный прием даназола во избежание гипергликемического действия последнего. При необходимости лечения даназолом и после прекращения приема последнего требуется коррекция дозы препарата метформин под контролем концентрации глюкозы в крови.
Хлорпромазин: при приеме в больших дозах (100 мг в день) повышает концентрацию глюкозы в крови, снижая высвобождение инсулина. При лечении нейролептиками и после прекращения приема последних требуется коррекция дозы препарата метформин под контролем концентрации глюкозы в крови.
Глюкокортикостероиды (ГКС) системного и местного действия снижают толерантность к глюкозе, повышают концентрацию глюкозы в крови, иногда вызывая кетоз. Во время лечения ГКС и после прекращения приема последних требуется коррекция дозы препарата метформин под контролем концентрации глюкозы в крови.
Диуретики: одновременный прием «петлевых» диуретиков может привести к развитию лактоацидоза из-за возможной функциональной почечной недостаточности. Не следует назначать метформин, если клиренс креатинина ниже 60 мл/мин.
Бета2-адреномиметики, назначаемые парентерально: повышают концентрацию глюкозы в крови вследствие стимуляции бета2-адренорецепторов. В этом случае необходим контроль концентрации глюкозы в крови. При необходимости рекомендуется назначение инсулина.
При одновременном применении вышеперечисленных лекарственных средств может потребоваться более частый контроль содержания глюкозы в крови, особенно в начале лечения. При необходимости доза метформина может быть скорректирована в процессе лечения и после его прекращения.
Гипотензивные лекарственные средства, за исключением ингибиторов ангиотензинпревращающего фермента могут снижать концентрацию глюкозы в крови. При необходимости следует скорректировать дозу метформина.
При одновременном применении метформина с производными сульфонилмочевины, инсулином, акарбозой, салицилатами возможно развитие гипогликемии.
Нифедипин повышает абсорбцию и Сmах метформина.
Катионные лекарственные средства (амилорид, дигоксин, морфин, прокаинамид, хинидин, хинин, ранитидин, триамтерен, триметоприм и ванкомицин), секретирующиеся в почечных канальцах, конкурируют с метформином за канальцевые транспортные системы и могут приводить к увеличению его Сmах.
Гипогликемическое действие метформина могут снижать фенотиазиды, глюкагон, эстрогены, пероральные контрацептивы, фенитоин, симпатомиметики, никотиновая кислота, изониазид, блокаторы «медленных» кальциевых каналов, левотироксин натрия.
Одновременное применение с циметидином снижает скорость выведения метформина, что может приводить к развитию лактоацидоза.
У здоровых добровольцев при одновременном применении метформина и пропранолола, а также при применении метформина и ибупрофена не наблюдалось изменения их фармакокинетических показателей.
Метформин может снижать действие антикоагулянтов непрямого действия.
Субстраты транспортера органических катионов 1 и 2 (ОСТ1 и ОСТ2)
Метформин является субстратом органических катионов ОСТ1 и ОСТ2.
При совместном применении с метформином:
- ингибиторы ОСТ1 (такие как верапамил) могут снизить гипогликемическое действие метформина;
- индукторы ОСТ1 (такие как рифампицин) могут увеличить всасывание метформина в желудочно-кишечном тракте и усилить его гипогликемическое действие;
- ингибиторы ОСТ2 (такие как циметидин, долутегравир, ранолазин, триметоприм, вандетаниб, изавуконазол) могут снизить выведение метформина почками и привести к увеличению его концентрации в плазме крови;
- ингибиторы ОСТ1 и ОСТ2 (такие как кризотиниб, олапарид) могут снизить гипогликемическое действие метформина.
Особые указания:
Лактоацидоз
Лактоацидоз является редким, но серьезным (высокая смертность при отсутствии неотложного лечения) осложнением, которое может возникнуть из-за кумуляции метформина. Случаи лактоацидоза при приеме метформина возникали в основном у пациентов с сахарным диабетом с выраженной почечной недостаточностью.
Следует учитывать и другие сопряженные факторы риска, такие как декомпенсированный сахарный диабет, кетоз, продолжительное голодание, алкоголизм, печеночная недостаточность и любое состояние, связанное с выраженной гипоксией. Это может помочь снизить частоту случаев возникновения лактоацидоза. Следует учитывать риск развития лактоацидоза при появлении неспецифических признаков, таких как мышечные судороги, сопровождающиеся диспепсическими расстройствами, болью в животе и выраженной астенией. Лактоацидоз характеризуется ацидотической одышкой, болью в животе и гипотермией с последующей комой. Диагностическими лабораторными показателями являются снижение pH крови (менее 7,25), содержащие лактата в плазме крови свыше 5 ммоль/л, повышенные анионный промежуток и отношение лактат/пируват. При подозрении на метаболический ацидоз необходимо прекратить прием препарата и немедленно обратиться к врачу.
Хирургические операции
Применение метформина должно быть прекращено за 48 ч до проведения плановых хирургических операций и может быть продолжено не ранее чем через 48 ч после, при условии, что в ходе обследования почечная функция была признана нормальной.
Функция почек
Поскольку метформин выводится почками, перед началом лечения и регулярно в последующем, необходимо определять клиренс креатинина:
- не реже одного раза в год у пациентов с нормальной функцией почек;
- не реже 2-4 раз в год у пожилых пациентов, а также у пациентов клиренсом креатинина на нижней границе нормы.
В случае клиренса креатинина менее 45 мл/мин применение препарата противопоказано. Следует проявлять особую осторожность при возможном нарушении функций почек у пожилых пациентов, при одновременном применении гипотензивных лекарственных средств, диуретиков или нестероидных противовоспалительных препаратов.
Сердечная недостаточность
Пациенты с сердечной недостаточностью имеют более высокий риск развития гипоксии и почечной недостаточности. Пациентам с хронической сердечной недостаточностью следует регулярно проводить мониторинг сердечной функции и функции почек во время приема метформина. Прием метформина при сердечной недостаточности с нестабильными показателями гемодинамики противопоказан.
Дети и подростки
Клинический опыт применения метформина у детей в возрасте от 10 до 12 лет ограничен, поэтому у детей в указанной возрастной группе необходим наиболее тщательный контроль. Диагноз сахарного диабета 2 типа должен быть подтвержден до начала лечения метформином. В ходе клинических исследований продолжительностью 1 год было показано, что метформин не влияет на рост и половое созревание. Однако, ввиду отсутствия долгосрочных данных, рекомендован тщательный контроль последующего влияния метформина на эти параметры у детей, особенно в период полового созревания.
Другие меры предосторожности
Пациентам рекомендуется продолжать соблюдать диету с равномерным потреблением углеводов в течение дня. Пациентам с избыточной массой тела рекомендуется продолжать соблюдать гипокалорийную диету (но не менее 1000 ккал/сут).
Рекомендуется регулярно проводить стандартные лабораторные анализы для контроля сахарного диабета.
Метформин при монотерапии не вызывает гипогликемию, однако рекомендуется проявлять осторожность при его применении в комбинации с инсулином или другими гипогликемическими средствами (например, производными сульфонилмочевины, репаглинидом и др.).
Применение препарата у пациентов с предиабетом рекомендовано при наличии дополнительных факторов риска развития явного сахарного диабета 2 типа, к которым относятся:
- возраст менее 60 лет;
- индекс массы тела (ИМТ) >30 кг/м2;
- гестационный сахарный диабет в анамнезе;
- семейный анамнез сахарного диабета у родственников первой степени родства;
- повышенная концентрация триглицеридов;
- сниженная концентрация холестерина ЛПВП;
- артериальная гипертензия.
Метформин не влиял на фертильность самцов или самок крыс при применении в дозах, втрое превышающих максимальную рекомендованную суточную дозу для человека.
Влияние на способность управлять транспортными средствами и механизмами:
Монотерапия препаратом не вызывает гипогликемии, поэтому не влияет на способность управлять транспортными средствами и механизмами. Следует предостеречь пациентов о риске развития гипогликемии при применении метформина в сочетании с другими гипогликемическими средствами (производными сульфонилмочевины, репаглинидом, инсулином и др.), при которых ухудшается способность к управлению транспортными средствами и занятиями другими потенциально опасными видами деятельности, требующими повышенного внимания и быстрых психомоторных реакций.
Форма выпуска/дозировка:
Таблетки, покрытые пленочной оболочкой, 500 мг, 850 мг и 1000 мг.
Упаковка:
По 10 таблеток в контурную ячейковую упаковку из пленки поливинилхлоридной и фольги алюминиевой печатной лакированной.
По 30 таблеток в банку из полиэтилена низкого давления.
3 или 6 контурных ячейковых упаковок или банку с инструкцией по медицинскому применению помещают в пачку из картона.
Условия хранения:
Хранить при температуре не выше 25 °С.
Хранить в недоступном для детей месте.
Срок годности:
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Условия отпуска
По рецепту
Производитель
Открытое акционерное общество «Ирбитский химико-фармацевтический завод» (ОАО «Ирбитский химфармзавод»), 623856, Свердловская область, г. Ирбит, ул. Карла Маркса, д. 124-а, Россия
Владелец регистрационного удостоверения/организация, принимающая претензии потребителей:
ОАО «Ирбитский химфармзавод»
Купить МЕТФОРМИН в planetazdorovo.ru
*Цена в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Актуальность:
Рак эндометрия является одним из самых распространенных гинекологических раков в мире. Частота рака эндометрия увеличивается, отчасти, из-за увеличения частоты ожирения. Гиперплазия эндометрия -предраковое состояние у женщин, которое может привести к раку эндометрия в случае отсутствия лечения. Гиперплазия эндометрия встречается чаще, чем рак эндометрия. Частота побочных эффектов при применении прогестагенов per os, используемых в настоящее время для лечения гиперплазии эндометрия, составляет до 84%. Внутриматочное средство с левоноргестрелом («Мирена», Bayer HealthCare Pharmaceuticals, Inc., Инк., Уиппани, Нью-Джерси, США) может улучшить приверженность лечению, но является инвазивным средством, не является приемлемым для всех женщин и связано с нерегулярными вагинальными кровотечениями в 82% случаев. Поэтому необходимо альтернативное лечение для женщин с гиперплазией эндометрия. Метформин – препарат, который часто применяется для лечения сахарного диабета. В некоторых исследованиях было показано, что его использование нивелирует гиперплазию эндометрия. Однако эффективность и безопасность метформина для лечения гиперплазии эндометрия остаются неопределенными.
Цель исследования:
Определить эффективность и безопасность применения метформина в лечении женщин с гиперплазией эндометрия.
Методы поиска:
Был выполнен поиск в специализированном регистре Кокрейн по гинекологии и фертильности, Центральном Кокрановском регистре контролируемых исследований (CENTRAL), базах данных MEDLINE, Embase, в совокупном Индексе для медсестер и сопутствующих медицинской литературе (CINAHL), PubMed, Google Scholar, OpenGrey, LILACS и двух регистров исследований от момента их создания до 10 января 2017 года. Был выполнен поиск в библиографии всех включенных исследований и отзывов на эту тему. Вручную был выполнен поиск в тезисах конференции Европейского общества репродукции и эмбриологии человека (ESHRE) 2015 г. и Американского общества репродуктивной медицины (ASRM) 2015 г.
Критерии отбора:
Включали рандомизированные контролируемые исследования (РКИ) и перекрестные исследования, сравнивающих применение метформина (отдельно или в комбинации с другими препаратами) с плацебо или отсутствием лечения, с каким-либо общепринятым лечением или с любым другим активным вмешательством у женщин с гистологически подтвержденной гиперплазией эндометрия любого типа.
Сбор и анализ данных:
Два автора обзора независимо друг от друга оценивали исследования на предмет соответствия критериям, извлекали данные из включенных исследований и оценивали систематическую ошибку включенных исследований. Разногласия разрешали путем обсуждения или привлечения третьего автора обзора. Когда детали исследования отсутствовали, авторы обзора связывались с авторами исследований. Первичной конечной точкой данного обзора явилась регрессия гиперплазии эндометрия (с атипией или без нее) по данным гистологического исследования до нормы. Вторичные конечные точки: рецидивирование гиперплазии эндометрия, прогрессирование гиперплазии эндометрия до рака эндометрия, частота гистерэктомии, аномальное маточное кровотечение, качество жизни, связанное со здоровьем и неблагоприятные эффекты во время лечения.
Основные результаты:
Было включено три РКИ, в которых приняли участие в общей сложности 77 пациенток. Мы оценили качество доказательств как очень низкое для всех результатов из-за очень серьезной систематической ошибки (связанной с плохой отчетностью, выбыванием пациенток из исследованиий и ограничениями в дизайне исследований) и неточностью. Был выполнен мета-анализ двух исследований с 59 участницами. При сравнении применения метформина и мегестрола ацетата у женщин с гиперплазией эндометрия было недостаточно данных, чтобы определить, имеются ли различия между группами для следующих результатов: регресса гиперплазии эндометрия по данным гистологического исследования до нормы (отношение шансов (ОШ) 3,34; 95% доверительный интервал (ДИ) 0,97 до 11,57, два РКИ, n=59, доказательство очень низкого качества), частоты гистерэктомии (ОШ 0,91; 95% ДИ 0,05 до 15,52, два РКИ, n=59, доказательство очень низкого качества) и частоты аномальных маточных кровотечений (ОШ 0,91; 95% ДИ 0,05 до 15,52, два РКИ, n=44, доказательство очень низкого качества). Мы не нашли данных о рецидиве гиперплазии эндометрия или качестве жизни, связанном со здоровьем. Оба исследования (n=59) приводят данные о прогрессировании гиперплазии эндометрия в рак эндометрия, а также в одном (n=16) сообщается о побочных эффектах метформина, в частности, тошнота, тромбозы, лактатацидоз, нарушение функции печени и почек. Еще в одном исследовании, включающем 16 пациенток, сравнили применение метформина плюс мегестрола ацетат и применение только мегестрола ацетата у женщин с гиперплазией эндометрия. Было недостаточно данных, чтобы определить, имеются ли различия между группами для следующих результатов: регресса гиперплазии эндометрия по данным гистологического исследования до нормы (ОШ 9,00; 95% ДИ от 0,94 до 86,52, одно РКИ, n=16, доказательство очень низкого качества), рецидива гиперплазии эндометрия среди пациенток, которые достигли ремиссии (ОШ не оценено, нет зарегистрированных данных, одно РКИ, n=8, доказательство очень низкого качества), прогрессирования гиперплазии эндометрия в рак эндометрия (ОШ не оценено, нет зарегистрированных событий, одно РКИ, n=13, доказательство очень низкого качества) или частоты гистерэктомии (ОШ 0,29; 95% ДИ 0,01-8,37, одно РКИ, n=16, доказательство очень низкого качества). Исследователи не представили данных об аномальных маточных кровотечениях или качестве жизни, связанном со здоровьем. С точки зрения побочных эффектов, три из восьми пациенток исследования (37,5%), принимавших метформин плюс мегестрола ацетат, сообщили о тошноте.
Заключение авторов:
В настоящее время недостаточно данных, чтобы поддержать или опровергнуть применение метформина виде монотерапии или в комбинации со стандартным лечением, в частности, с мегестрола ацетатом — по сравнению с использованием только мегестрола ацетата, для лечения гиперплазии эндометрия. Для решения этого клинического вопроса необходимы надежные и адекватно разработанные рандомизированные контролируемые исследования, дающие данные о долгосрочных результатах.
Metformin for endometrial hyperplasia.
Clement NS1, Oliver TR, Shiwani H, Sanner JR, Mulvaney CA, Atiomo W.
Cochrane Database Syst Rev. 2017 Oct 27;10:CD012214. doi: 10.1002/14651858.CD012214.pub2.
https://www.ncbi.nlm.nih.gov/pubmed/29077194
У женщин с СПКЯ) наблюдается хроническая овуляторная дисфункция или отсутствие овуляции (ановуляция) и чрезмерная выработка мужских гормонов (гиперандрогения).
Основными симптомами заболевания являются нерегулярные менструации, бесплодие, гирсутизм (чрезмерный рост волос на лице и теле) и угревая сыпь.
СПКЯ — наиболее распространенное эндокринное заболевание у женщин, которым страдают от 5% до 10% женщин репродуктивного возраста.
ЭКО может быть эффективным вариантом лечения бесплодия у женщин с СПКЯ, которые не реагируют на процедуры индукции овуляции. В первой части лечения ЭКО стимуляция яичников с использованием гонадотропинов необходима для развития более зрелых ооцитов, чтобы произвести больше эмбрионов хорошего качества для переноса в матку. Такая чрезмерная стимуляция увеличивает риск развития серьезного осложнения, известного как синдром гиперстимуляции яичников (СГЯ). Стратегии, используемые во время лечения ЭКО для снижения риска СГЯ, включают: стимуляцию яичников низкими дозами гонадотропина, терапию метформином, использование протокола антагониста гонадотропин-рилизинг-гормона (ГнРГ) вместо агониста ГнРГ и использование агониста ГнРГ в качестве триггера окончательного созревания ооцитов вместо хорионического гонадотропина человека (ХГЧ).
Материалы и методы
Было включено 13 рандомизированных контролируемых испытаний с участием 1132 женщин, которым был назначен метформин (570) или плацебо / без лечения (563).
Анализ был разделен по типу протокола стимуляции яичников, используемого во время ЭКО («длинный» протокол с использованием агониста ГнРГ или «короткий» с антагонистом ГнРГ), чтобы определить, влияет ли тип используемой стимуляции на результаты.
Поиск данных был произведен в Специализированном регистре Кокрановской группы по гинекологии и репродуктивной медицине, CENTRAL, через Кокрановский реестр исследований в Интернете (CRSO), MEDLINE, Embase, PsycINFO, LILACS, регистры текущих испытаний и списки ссылок статей (по 13 февраля 2020 г.).
Критерии отбора:
Типы исследований: рандомизированные контролируемые испытания (РКИ), сравнивающие лечение метформином и плацебо или отсутствие лечения у женщин с СПКЯ, подвергшихся лечению ЭКО или ИКСИ (интрацитоплазматическая инъекция сперматозоида в яйцеклетку).
Типы участников: женщины репродуктивного возраста с ановуляцией в связи с СПКЯ с сопутствующими факторами бесплодия или без них.
Типы вмешательств: прием метформина до и во время проведения ЭКО или ИКСИ.
Первичные критерии оценки: рождаемость, частота СГЯ.
Два автора обзора независимо друг от друга извлекли данные из выбранных исследований в соответствии с протоколом и оценили качество исследований. Общее качество доказательств было оценено с использованием подхода GRADE.
Результаты
Общее качество доказательств по первичным исходам — коэффициент живорождения и развитие СГЯ — было низким.
В подгруппе «длинного» протокола объединенные данные показали, что нет убедительной информации о влиянии метформина на частоту живорождений на одну женщину по сравнению с плацебо / отсутствием лечения (отношение рисков (ОР) 1,30, 95% доверительный интервал (ДИ) От 0,94 до 1,79; 6 РКИ; 651 женщина; I2 = 47%; доказательства низкого качества). Вероятность живорождения после приема плацебо / отсутствие лечения составила 28%, вероятность после метформина составляет 27%-51%.
Только в одном исследовании использовался «короткий» протокол с применением антагониста ГнРГ. Метформин может снизить частоту живорождений по сравнению с плацебо / отсутствием лечения (ОР 0,48, 95% ДИ от 0,29 до 0,79; 1 РКИ; 153 женщины; доказательства низкого качества). Вероятность живорождения в группе плацебо / без лечения составила 43%, вероятность в группе метформина 13%-34% (короткий антагонист-протокол).
Метформин может снижать частоту СГЯ (ОР 0,46, 95% ДИ от 0,29 до 0,72; 11 РКИ; 1091 женщина; I2 = 38%; доказательства низкого качества). Это говорит о том, что для женщины с 20% риском СГЯ без метформина соответствующий риск при использовании метформина будет снижен на 6% — 14%. Используя «длинный» протокол стимуляции агонистами гонадолиберина, метформин может увеличить частоту развития клинической беременности на женщину по сравнению с плацебо / отсутствием лечения (ОР 1,32, 95% ДИ 1,08–1,63; 10 РКИ; 915 женщин; I2 = 13%; доказательства низкого качества). При проведении «короткого» протокола нет убедительных данных о влиянии метформина на частоту развития клинической беременности на женщину по сравнению с плацебо / отсутствием лечения (ОР 1,38, 95% ДИ 0,21–9,14; 2 РКИ; 177 женщин; I2 = 87%; доказательства низкого качества).
Также нет убедительных данных о влиянии метформина на частоту выкидышей по сравнению с плацебо / отсутствием лечения (ОР 0,86, 95% ДИ 0,56–1,32; 8 РКИ; 821 женщина; I2 = 0%; доказательства низкого качества).
Метформин может вызывать усиление побочных эффектов по сравнению с плацебо / отсутствием лечения (ОР 3,35, 95% ДИ от 2,34 до 4,79; 8 РКИ; 748 женщин; I2 = 0%; доказательства низкого качества).
Общее качество доказательств варьировалось от очень низкого до низкого. Основными ограничениями были риск систематической ошибки и неточные результаты.
Заключение
В целом, метформин может снизить частоту СГЯ по сравнению с плацебо / отсутствием лечения. Для женщины с 20% риском СГЯ без метформина соответствующий риск при использовании метформина будет снижаться до 6% — 14%. Побочные эффекты (в основном желудочно-кишечные) могут чаще реализовываться при приеме метформина. Нет убедительных данных о влиянии метформина на частоту выкидышей по сравнению с плацебо / отсутствием лечения.
Метформин снижает гиперинсулинемию и подавляет чрезмерную выработку андрогенов яичниками. Предполагается, что, как следствие, метформин может улучшить результаты вспомогательных репродуктивных технологий, таких как СГЯ, беременность и уровень живорождений.
Источник:
cochrane.org/CD006105/MENSTR_metformin-women-polycystic-ovary-syndrome-pcos-improving-fe…
