Описание препарата Мирцера® (раствор для внутривенного и подкожного введения, 100 мкг/мл) основано на официальной инструкции, утверждено компанией-производителем в 2010 году
Дата согласования: 31.08.2010
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав и форма выпускa
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Условия хранения
- Срок годности
- Заказ в аптеках Москвы
- Отзывы
Действующее вещество
ATX
Фармакологическая группа
Состав и форма выпускa
| Раствор для внутривенного и подкожного введения | 1 фл. |
| метоксиполиэтиленгликоль-эпоэтин бета | 50 мкг |
| 100 мкг | |
| 200 мкг | |
| 300 мкг | |
| 400 мкг | |
| 600 мкг | |
| 1000 мкг | |
| вспомогательные вещества: L-метионин; натрия сульфат безводный; натрия дигидрофосфата моногидрат; маннитол; полоксамер 188; кислота хлористоводородная разбавленная или раствор натрия гидроксида; вода для инъекций |
во флаконах по 1 мл; в пачке картонной 1 флакон.
| Раствор для внутривенного и подкожного введения | 1 шпр.-тюб. |
| метоксиполиэтиленгликоль-эпоэтин бета | 30 мкг |
| 40 мкг | |
| 50 мкг | |
| 60 мкг | |
| 75 мкг | |
| 100 мкг | |
| 120 мкг | |
| 150 мкг | |
| 200 мкг | |
| 250 мкг | |
| вспомогательные вещества: L-метионин; натрия сульфат безводный; натрия дигидрофосфата моногидрат; маннитол; полоксамер 188; кислота хлористоводородная разбавленная или раствор натрия гидроксида; вода для инъекций |
в шприц-тюбиках по 0,3 мл (в комплекте со стерильной иглой); в упаковке контурной ячейковой 1 комплект.
| Раствор для внутривенного и подкожного введения | 1 шпр.-тюб. |
| метоксиполиэтиленгликоль-эпоэтин бета | 360 мкг |
| 400 мкг | |
| 600 мкг | |
| 800 мкг | |
| вспомогательные вещества: L-метионин; натрия сульфат безводный; натрия дигидрофосфата моногидрат; маннитол; полоксамер 188; кислота хлористоводородная разбавленная или раствор натрия гидроксида; вода для инъекций |
в шприц-тюбиках по 0,6 мл (в комплекте со стерильной иглой); в упаковке контурной ячейковой 1 комплект.
Описание лекарственной формы
Прозрачная, бесцветная или слегка желтоватого цвета жидкость.
Фармакологическое действие
Фармакологическое действие
—
гемопоэтическое.
Фармакодинамика
Препарат Мирцера — химически синтезированный представитель нового класса активаторов рецепторов эритропоэтина длительного действия. Метоксиполиэтиленгликоль-эпоэтин бета является ковалентным конъюгантом белка, полученного методом рекомбинантной ДНК, и линейного метоксиполиэтиленгликоля (ПЭГ). Метоксиполиэтиленгликоль-эпоэтин бета отличается от эритропоэтина наличием амидной связи между N-концевой аминогруппой или ε-аминогруппой лизина, преимущественно Lys52 и Lys45, и метоксиполиэтиленгликольбутановой кислотой. Молекулярная масса метоксиполиэтиленгликоль-эпоэтин бета составляет примерно 60 кДа, включая 30 кДа молекулярную массу ПЭГ.
Препарат Мирцера обладает отличной от эритропоэтина активностью на уровне рецептора и характеризуется более длительной ассоциацией с рецептором и более быстрой диссоциацией от рецептора, сниженной специфической активностью in vitro и повышенной активностью in vivo, а также увеличенным Т1/2, что позволяет вводить препарат Мирцеру 1 раз в месяц.
Механизм действия. Препарат Мирцера стимулирует эритропоэз при взаимодействии с эритропоэтиновыми рецепторами на клетках-предшественниках костного мозга.
Клиническая эффективность. У 97,5% пациентов с хроническими заболеваниями почек, не находящихся на диализе, и у 93,3% пациентов с хроническими заболеваниями почек, находящихся на диализе, при терапии препаратом Мирцера отмечена коррекция анемии. У пациентов, находящихся на диализе, при переводе с терапии дарбэпоэтином альфа или эпоэтином на терапию препаратом Мирцера сохраняется стабильный целевой уровень гемоглобина (Hb).
Фармакокинетика
T1/2 после в/в введения препарата Мирцера в 15–20 раз продолжительнее, чем при введении рекомбинантного человеческого эритропоэтина.
Клиренс и объем распределения метоксиполиэтиленгликоль-эпоэтина бета не зависят от дозы.
Длительное назначение не влияет на клиренс, объем распределения и биодоступность метоксиполиэтиленгликоль-эпоэтина бета. Введение метоксиполиэтиленгликоль-эпоэтина бета 1 раз в 4 нед не приводит к значимой кумуляции препарата, коэффициент кумуляции равен 1,03 при введении 1 раз в 4 нед и 1,12 — при введении 1 раз в 2 нед. Не выявлено различий в фармакокинетике препарата у больных, получающих и не получающих диализ. Гемодиализ не оказывает влияние на фармакокинетику метоксиполиэтиленгликоль-эпоэтина бета.
Фармакокинетика, фармакодинамика и местная переносимость не зависят от места п/к инъекции препарата (плечо, передняя поверхность бедра, передняя брюшная стенка).
Абсорбция после п/к введения. Время достижения Сmax метоксиполиэтиленгликоль-эпоэтина бета в сыворотке при п/к введении — 72 ч.
Абсолютная биодоступность метоксиполиэтиленгликоль-эпоэтина бета у пациентов, находящихся на диализе, и у пациентов, не находящихся на диализе, составляет 62 и 54% соответственно.
Распределение. Объем распределения составляет 5 л.
Экскреция. Т1/2 метоксиполиэтиленгликоль-эпоэтина бета при в/в введении 134 ч (или 5,6 дней), при п/к введении — 139 ч (или 5,8 дней), полный системный клиренс 0,494 мл/ч/кг.
Фармакокинетика у специальных групп пациентов
Печеночная недостаточность: фармакокинетика метоксиполиэтиленгликоль-эпоэтина бета у пациентов с тяжелой печеночной недостаточностью и у здоровых пациентов не отличается.
Пол, раса, пожилой возраст: не требуется коррекции начальной дозы метоксиполиэтиленгликоль-эпоэтина бета.
Показания
Анемия при хронической почечной недостаточности (по классификации NKF K/DOQI — при хроническом заболевании почек).
Противопоказания
повышенная чувствительность к метоксиполиэтиленгликоль-эпоэтину бета или к любом другому компоненту препарата;
неконтролируемая артериальная гипертензия;
детский возраст до 18 лет (безопасность и эффективность не установлены).
С осторожностью (поскольку безопасность и эффективность препарата Мирцера для данных групп изучены недостаточно):
беременность;
период кормления грудью;
гемоглобинопатии;
эпилепсия;
тромбоцитоз (число тромбоцитов >500·109/л).
Применение при беременности и кормлении грудью
Безопасность и эффективность препарата Мирцера для данных групп изучены недостаточно. При беременности и в период кормления грудью препарат Мирцера следует назначать только в том случае, если предполагаемая польза для матери превышает потенциальный риск для плода или ребенка.
На животных препарат Мирцера не оказывает прямого или косвенного вредного действия в отношении беременности, эмбрионального/фетального развития, родов или постнатального развития.
Неизвестно, выводится ли метоксиполиэтиленгликоль-эпоэтин бета с грудным молоком у человека. В исследовании на животных показано, что метоксиполиэтиленгликоль-эпоэтин бета выводится с материнским молоком.
Способ применения и дозы
П/к и в/в.
Учитывая более длительный Т1/2, препарат Мирцера должна вводиться реже, чем другие стимуляторы эритропоэза.
Лечение препаратом Мирцера необходимо начинать только под наблюдением специалиста.
Правила хранения раствора в амбулаторных и стационарных условиях
Раствор препарата Мирцера стерилен и не содержит консервантов. Применять следует только прозрачный, бесцветный или слегка желтоватого цвета раствор, не содержащий видимых примесей. Перед введением раствор доводят до комнатной температуры, если раствор хранился в холодильнике.
Шприц-тюбик может храниться в течение 1 мес при комнатной температуре (не выше 25 °C) и должен быть использован в течение месяца.
Флакон может храниться в течение 7 дней при комнатной температуре (не выше 25 °C) и должен быть использован в течение 7 дней.
Неиспользованный раствор должен быть уничтожен. Каждый флакон или шприц-тюбик можно использовать только однократно. Не встряхивать.
Способ применения. Препарат следует вводить п/к в область плеча, переднюю поверхность бедра или переднюю брюшную стенку.
Содержание Нb следует контролировать 1 раз в 2 нед до его стабилизации и периодически после стабилизации.
Стандартный режим дозирования
Пациенты, не получающие стимулятор эритропоэза в настоящее время. Рекомендуемая начальная доза — 0,6 мкг/кг в/в или п/к 1 раз в 2 нед, целевой показатель гемоглобина >110 г/л (6,83 ммоль/л).
Дозу препарата Мирцера можно увеличить на 25–50% от предыдущей, если спустя 1 мес повышение Нb составляет <10 г/л (0,621 ммоль/л). Дальнейшее увеличение дозы примерно на 25–50% можно проводить с интервалами 1 раз в месяц до достижения индивидуального целевого содержания Нb.
Дозу препарата Мирцера уменьшают на 25–50% от предыдущей, если спустя 1 мес увеличение Hb составляет >20 г/л (1,24 ммоль/л). Если Нb превышает 130 г/л (8,07 ммоль/л), то терапию необходимо прервать до снижения Нb <130 г/л (8,07 ммоль/л) и затем возобновить в дозе 50% от предыдущей. При целевом Нb 120 г/л доза препарата изменяется на 25%.
После прекращения терапии Нb снижается примерно на 3,5 г/л (0,22 ммоль/л) в неделю.
Коррекцию дозы препарата проводят не чаще 1 раза в месяц.
Пациенты, получающие стимулятор эритропоэза в настоящее время. Пациентов, получающих другой стимулятор эритропоэза, можно перевести на терапию препаратом Мирцера с режимом введения 1 раз а месяц или 1 раз в 2 нед п/к или в/в.
Начальная доза: зависит от недельной дозы ранее вводимого препарата — дарбэпоэтина альфа или эпоэтина (альфа или бета) (см. табл. 1 и 2). Первую инъекцию препарата Мирцера проводят в день следующей запланированной инъекции ранее применявшегося дарбэпоэтина альфа или эпоэтина (альфа или бета).
Таблица 1
Переход с эпоэтина (альфа или бета)
| Предшествующая недельная доза эпоэтина (ЕД/нед) |
Доза препарата Мирцера | |
| 1 раз в месяц (мкг/месяц) | 1 раз в 2 нед (мкг/2 нед) |
|
| <8000 | 120 | 60 |
| 8000–16000 | 200 | 100 |
| >16000 | 360 | 180 |
Таблица 2
Переход с дарбэпоэтина альфа
| Предшествующая недельная доза дарбэпоэтина альфа (мкг/нед) |
Доза препарата Мирцера |
|
| 1 раз в месяц (мкг/мес) | 1 раз в 2 нед (мкг/2 нед) | |
| <40 | 120 | 60 |
| 40–80 | 200 | 100 |
| >80 | 360 | 180 |
Если для поддержания целевого Нb выше 110 г/л (6,83 ммоль/л) требуется коррекция дозы, то месячную дозу можно изменить на 25%.
Дозу препарата Мирцера уменьшают на 25–50% от предыдущей, если спустя 1 мес увеличение Нb составляет более 20 г/л (1,24 ммоль/л). Если Нb превышает 130 г/л (8,07 ммоль/л), то терапию необходимо прервать до снижения Нb до уровня менее 130 г/л (8,07 ммоль/л) и затем возобновить в дозе 50% от предыдущей.
При целевом Нb 120 г/л доза препарата изменяется на 25%.
После прекращения терапии Нb снижается примерно на 3,5 г/л (0,22 ммоль/л) в неделю.
Коррекцию дозы препарата проводят не чаще 1 раза в месяц.
Перерыв в лечении. Лечение анемии, в т.ч. и терапия препаратом Мирцера, обычно бывает долговременным. Но при необходимости терапия препаратом Мирцера может быть прервана в любой момент.
Пропущенная доза. Пропущенную однократную инъекцию препарата Мирцера необходимо ввести как можно скорее и далее вводить препарат с предписанной частотой дозирования.
Дозирование в особых случаях
У пациентов с печеночной недостаточностью любой степени тяжести коррекции начальной дозы препарата и режима дозирования не требуется.
В пожилом возрасте (старше 65 лет) коррекции начальной дозы препарата не требуется.
Инструкция по обращению со шприц-тюбиком
1. Вынуть прозрачную контурную ячейковую упаковку с лекарственным препаратом из картонной пачки, не вскрывая защитную пленку.
2. Тщательно вымыть руки теплой водой с мылом.
3. Снять защитную пленку с контурной ячейковой упаковки, достать шприц-тюбик и прозрачный пластмассовый контейнер с иглой.
4. Удерживая контейнер с иглой, отсоединить колпачок, сделав вращательное движение по часовой стрелке, как показано на рисунке 1. Снять колпачок с верхней части контейнера с иглой.
Рисунок. 1. Техника удаления колпачка.
5. Удерживая шприц-тюбик, снять резиновый наконечник, предварительно согнув и потянув, как показано на рисунке 2.
Рисунок. 2. Техника удаления резинового наконечника.
6. Удерживая прозрачный контейнер с иглой, плотно вставить иглу в шприц-тюбик, как показано на рисунке 3.
Рисунок. 3. Техника насадки иглы на шприц-тюбик.
Подготовка и проведение инъекции
1. Для введения лекарственного препарата выбрать одно из рекомендуемых мест как показано на рисунке 4: передняя брюшная стенка (исключая область вокруг пупка), передняя поверхность середины бедра или наружная поверхность плеча. Не вводить лекарственный препарат в родимые пятна, ткани рубцов, гематомы или пупок, места с уплотнениями и/или реакцией после предшествующих инъекций. Следует каждый раз менять место введения препарата. Избегать участков, которые могут подвергаться раздражению ремнем или поясом одежды.
Рисунок. 4. Рекомендуемые места инъекций.
2. Тщательно обработать кожу в месте инъекции тампоном, смоченным спиртом, как показано на рисунке 5. Подождать пока обработанный участок подсохнет.
Рисунок. 5. Техника обработки места инъекции.
3. Аккуратно удерживая шприц-тюбик, не нажимая на поршень, осторожно снять прозрачный контейнер с иглы.
4. Двумя пальцами собрать кожу в складку в месте предполагаемой инъекции. Ввести иглу в кожную складку под прямым углом, как показано на рисунке 6.
Рисунок. 6. Техника проведения инъекции.
5. Медленно ввести весь лекарственный препарат, плавно нажимая на поршень, как показано на рисунке 7. Не следует прекращать давить на поршень шприц-тюбика, пока игла не будет извлечена из кожи!
Рисунок. 7. Техника введения ЛС.
6. После введения всей дозы вынуть иглу из кожи, не отпуская поршень шприц-тюбика, как показано на рисунке 8.
Рисунок. 8. Техника извлечения иглы.
7. Отпустить поршень, в результате чего высвободится защитное устройство и закроет иглу, как показано на рисунке 9.
Рисунок. 9. Техника применения защитного устройства.
8. Прижать ватным тампоном место введения лекарственного препарата. При необходимости заклеить место инъекции пластырем.
Побочные действия
Следующие категории используются для описания частоты нежелательных реакций: часто (≥1/100 и <1/10), редко (≥1/1000 и <1/100) и очень редко (≥1/10000 и <1/1000).
Примерно у 6% пациентов, получающих препарат Мирцера, возможно возникновение побочных эффектов. Наиболее частым из них является артериальная гипертензия (часто).
Побочные реакции легкой или средней степени тяжести, встречающиеся у пациентов, получавших препарат Мирцера
Со стороны сердечно-сосудистой системы: артериальная гипертензия (часто); тромбоз шунта (редко); приливы (очень редко).
Со стороны нервной системы: головная боль (редко), гипертензивная энцефалопатия (очень редко).
Со стороны иммунной системы: реакции гиперчувствительности (очень редко).
Со стороны кожи и ее придатков: макулопапулезная сыпь (очень редко).
Изменения лабораторных показателей: у 7,5% пациентов, получавших терапию препаратом Мирцера, и у 4,4% пациентов, получавших терапию другими стимуляторами эритропоэза, наблюдалась тромбоцитопения (количество тромбоцитов <100·109/л).
Взаимодействие
Исследований по изучению взаимодействия с другими ЛС не проводилось. Полученные до настоящего времени данные не выявили каких-либо взаимодействий препарата Мирцера с другими препаратами.
Проведенный популяционный анализ не выявил признаков влияния других препаратов на фармакокинетику и фармакодинамику Мирцеры.
Не следует смешивать метоксиполиэтиленгликоль-эпоэтин бета с другими ЛС или инъекционными растворами.
Передозировка
Максимально переносимая доза у пациентов не определялась.
Симптомы: возможен чрезмерный фармакодинамический ответ, т.е. чрезмерный эритропоэз.
Лечение: при высоком уровне гемоглобина необходимо временно прервать терапию препаратом Мирцера (см. «Способ применения и дозы»). При необходимости может быть проведена флеботомия.
Особые указания
До начала и во время лечения препаратом Мирцера необходимо исключить дефицит железа.
Дополнительная терапия железом рекомендуется, если содержание ферритина в сыворотке крови ниже 100 мкг/л или насыщение трансферрина железом ниже 20%.
Отсутствие эффекта: наиболее частыми причинами неполного ответа на лечение средствами, стимулирующими эритропоэз, являются дефицит железа, воспаление, хроническая кровопотеря, фиброз костного мозга, резкое увеличение концентрации алюминия, обусловленное гемодиализом, дефицит фолиевой кислоты или витамина В12, гемолиз. Если все перечисленные состояния исключены и у больного наблюдается внезапное снижение гемоглобина, ретикулоцитопения и обнаруживаются антитела к эритропоэтину, необходимо провести исследование костного мозга для исключения парциальной красноклеточной аплазии (ПККА). При развитии ПККА терапию препаратом Мирцера необходимо прекратить и пациентов не следует переводить на терапию другими стимуляторами эритропоэза.
Сообщалось о случаях развития ПККА, вызванной антителами к эритропоэтину, на фоне терапии стимуляторами эритропоэза. Антитела обладают перекрестной реакцией со всеми стимуляторами эритропоэза. Не рекомендуется переводить на терапию Мирцерой пациентов с подтвержденными антителами к эритропоэтину или подозрением на их наличие.
Артериальная гипертензия: до начала и во время лечения препаратом Мирцера, как и другими стимуляторами эритропоэза, необходимо контролировать АД. Если АД не удается контролировать медикаментозно, необходимо снизить дозу или приостановить терапию препаратом Мирцера (см. «Способ применения и дозы»).
Эффект на опухолевый рост: препарат Мирцера, как и другие ЛС, стимулирующие эритропоэз, является фактором роста, который в основном стимулирует образование эритроцитов. Эритропоэтиновые рецепторы могут присутствовать на поверхности различных опухолевых клеток. Возможно, что средства, стимулирующие эритропоэз, могут стимулировать рост злокачественного образования любого типа.
В клинических исследованиях, в которых эпоэтины применялись у пациентов с различными злокачественными опухолями, в т.ч. головы и шеи, молочной железы, наблюдалось увеличение летальности, причины которой неясны.
Влияние на способность управлять автомобилем и работу с механизмами. Исследования по изучению влияния препарата на способность управлять автомобилем и работать с механизмами не проводились. Исходя из механизма действия и профиля безопасности, препарат Мирцера не обладает таким действием.
Условия хранения
раствор для внутривенного и подкожного введения 100 мкг/мл флакон, 600 мкг/0.6 мл шприц-тюбик, 600 мкг/мл флакон, 60 мкг/0.3 мл шприц-тюбик, 50 мкг/мл флакон, 400 мкг/0.6 мл шприц-тюбик, 400 мкг/мл флакон, 40 мкг/0.3 мл шприц-тюбик, 360 мкг/0.6 мл шприц-тюбик, 300 мкг/мл флакон, 30 мкг/0.3 мл шприц-тюбик, 250 мкг/0.3 мл шприц-тюбик, 200 мкг/0.3 мл шприц-тюбик, 200 мкг/мл флакон, 150 мкг/0.3 мл шприц-тюбик, 120 мкг/0.3 мл шприц-тюбик, 1000 мкг/мл флакон —
В защищенном от света месте, при температуре 2–8 °C (не замораживать).
раствор для внутривенного и подкожного введения 75 мкг/0.3 мл шприц-тюбик, 50 мкг/0.3 мл шприц-тюбик, 100 мкг/0.3 мл шприц-тюбик —
При температуре 2–8 °C, не замораживать, в картонной пачке для защиты от света.
Хранить в недоступном для детей месте.
Срок годности
раствор для внутривенного и подкожного введения 100 мкг/мл флакон, 600 мкг/мл флакон, 50 мкг/мл флакон, 400 мкг/мл флакон, 300 мкг/мл флакон, 200 мкг/мл флакон, 1000 мкг/мл флакон — 1 год.
раствор для внутривенного и подкожного введения 75 мкг/0.3 мл шприц-тюбик, 600 мкг/0.6 мл шприц-тюбик, 60 мкг/0.3 мл шприц-тюбик, 50 мкг/0.3 мл шприц-тюбик, 400 мкг/0.6 мл шприц-тюбик, 40 мкг/0.3 мл шприц-тюбик, 360 мкг/0.6 мл шприц-тюбик, 30 мкг/0.3 мл шприц-тюбик, 250 мкг/0.3 мл шприц-тюбик, 200 мкг/0.3 мл шприц-тюбик, 150 мкг/0.3 мл шприц-тюбик, 120 мкг/0.3 мл шприц-тюбик, 100 мкг/0.3 мл шприц-тюбик — 3 года.
Не применять по истечении срока годности, указанного на упаковке.
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Фармакологическое действие
Стимулятор гемопоэза. Препарат Мирцера® — химически синтезированный представитель нового класса активаторов рецепторов эритропоэтина длительного действия. Метоксиполиэтиленгликоль-эпоэтин бета является ковалентным конъюгантом белка, полученного методом рекомбинантной ДНК, и линейного метоксиполиэтиленгликоля (ПЭГ). Метоксиполиэтиленгликоль-эпоэтин бета отличается от эритропоэтина наличием амидной связи между N-концевой аминогруппой или ε-аминогруппой лизина, преимущественно Lys52 и Lys45, и метоксиполиэтиленгликольбутановой кислотой. Молекулярная масса метоксиполиэтиленгликоль-эпоэтин бета составляет примерно 60 кДа, включая 30 кДа молекулярную массу ПЭГ.
Препарат Мирцера® обладает отличной от эритропоэтина активностью на уровне рецептора и характеризуется более длительной ассоциацией с рецептором и более быстрой диссоциацией от рецептора, сниженной специфической активностью in vitro и повышенной активностью in vivo, а также увеличенным T1/2, что позволяет вводить препарат Мирцера® 1 раз в месяц.
Механизм действия
Препарат Мирцера® стимулирует эритропоэз при взаимодействии с эритропоэтиновыми рецепторами на клетках-предшественниках костного мозга.
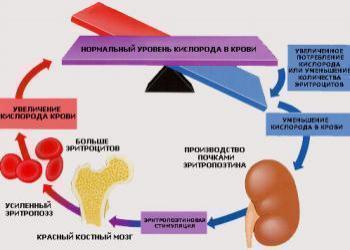
Являясь основным фактором роста, необходимым для созревания эритроцитов, естественный эритропоэтин вырабатывается почками и высвобождается в кровяное русло в ответ на гипоксию. В ответ на гипоксию эритропоэтин взаимодействует с клетками предшественниками эритроцитов и приводит к повышению образования эритроцитов.
Клиническая эффективность
Коррекция анемии отмечена у 97.5% и 94.1% пациентов с хронической болезнью почек (ХБП), не находящихся на диализе, при терапии препаратом Мирцера® 1 раз в 2 недели и 1 раз в месяц, соответственно. В первые 8 недель терапии уровень гемоглобина превышал 130 г/л у 11.4% пациентов, получавших препарат Мирцера® 1 раз в 2 недели, и у 34% пациентов, получавших дарбэпоэтин альфа, и превышал 120 г/л у 25.8% пациентов, получавших препарат Мирцера® 1 раз в месяц, и у 47.7% пациентов, получавших дарбэпоэтин альфа. У 93.3% пациентов с ХБП, находящихся на диализе, при терапии препаратом Мирцера® отмечена коррекция анемии. У пациентов, находящихся на диализе, при переводе с терапии дарбэпоэтином альфа или эпоэтином на терапию препаратом Мирцера® сохраняется стабильный целевой уровень гемоглобина.
В группе поддерживающей терапии препаратом Мирцера® 1 раз в месяц доля пациентов с ХБП, находящихся на гемодиализе, с ответом на терапию была значительно выше по сравнению с группой поддерживающей терапии дарбэпоэтином альфа 1 раз в месяц (р<0.0001).
Фармакокинетика
Фармакокинетические и фармакологические параметры позволяют вводить препарат Мирцера® 1 раз месяц в связи с увеличенным T1/2.
T1/2 после в/в введения препарата Мирцера® в 15-20 раз продолжительнее, чем при введении рекомбинантного человеческого эритропоэтина.
Фармакокинетические параметры препарата изучались у здоровых добровольцев и у пациентов с анемией и ХБП, находящихся и не находящихся на диализе.
У пациентов с ХБП клиренс и Vd метоксиполиэтиленгликоль-эпоэтина бета не зависят от дозы.
Фармакокинетика препарата Мирцера® изучалась у пациентов с ХБП после однократного введения на 9 неделе и 19 или 21 неделе. Многократное введение не влияет на клиренс, Vd и биодоступность метоксиполиэтиленгликоль-эпоэтина бета. Введение метоксиполиэтиленгликоль-эпоэтина бета 1 раз в 4 недели пациентам с ХБП не приводит к значимой кумуляции препарата, коэффициент кумуляции равен 1.03 при введении 1 раз в 4 недели. Коэффициент кумуляции при введении 1 раз в 2 недели равен 1.12. Результаты сравнения сывороточных концентраций метоксиполиэтиленгликоль-эпоэтина бета до и после проведения гемодиализа у пациентов с ХБП показали, что гемодиализ не оказывает влияние на фармакокинетику препарата. У больных с ХБП, получающих и не получающих диализ, различия в фармакокинетике отсутствовали.
Фармакокинетика, фармакодинамика и местная переносимость не зависят от места п/к инъекции препарата (плечо, передняя поверхность бедра, передняя брюшная стенка), что подтверждается результатами исследования, проведенного на здоровых добровольцах. На основании данных результатов эти места одинаково подходят для п/к введения препарата Мирцера®.
Всасывание
Время достижения Cmax в сыворотке метоксиполиэтиленгликоль-эпоэтина бета при п/к введении пациентам с ХБП, находящимся на диализе, — 72 ч (медиана) и 95 ч — после введения пациентам, не находящимся на диализе. Абсолютная биодоступность метоксиполиэтиленгликоль-эпоэтина бета у пациентов, находящихся на диализе, и у пациентов, не находящихся на диализе, составляет 62% и 54% соответственно.
Распределение
У пациентов с ХБП Vd составляет 5 л.
Выведение
T1/2 метоксиполиэтиленгликоль-эпоэтина бета при в/в введении составляет 134 ч (или 5.6 сут), а полный системный клиренс 0.494 мл/ч/кг. Т1/2 препарата при п/к введении — 139 ч у пациентов, находящихся на диализе, и 142 ч — у пациентов, не находящихся на диализе.
Фармакокинетика у специальных групп пациентов
Печеночная недостаточность: фармакокинетика метоксиполиэтиленгликоль-эпоэтина бета у пациентов с тяжелой печеночной недостаточностью и у здоровых добровольцев не отличается.
Другие особые группы пациентов: не требуется коррекции начальной дозы метоксиполиэтиленгликоль-эпоэтина бета в зависимости от расы, пола и возраста пациента. У пациентов 65 лет и старше изменение начальной дозы не требуется.
У пациентов, находящихся и не находящихся на диализе, различия в фармакокинетике препарата отсутствуют.
Показания препарата
Мирцера®
- анемия при хронической почечной недостаточности (по классификации NKF K/DOQI — при хронической болезни почек).
Режим дозирования
Учитывая более длительный T1/2, препарат Мирцера® должен вводиться реже, чем другие стимуляторы эритропоэза.
Лечение препаратом Мирцера® необходимо начинать только под наблюдением специалиста.
Правила хранения раствора в амбулаторных и стационарных условиях
Раствор препарата Мирцера® стерилен и не содержит консервантов. Применять следует только прозрачный бесцветный или слегка желтоватого цвета раствор, не содержащий видимых примесей. Перед введением раствор доводят до комнатной температуры, если препарат хранился в холодильнике.
Шприц-тюбик может храниться в течение 1 месяца при комнатной температуре (не выше 30°C) и должен быть использован в течение этого месяца.
Флакон может храниться в течение 7 дней при комнатной температуре (не выше 25°С) и должен быть использован в течение этих 7 дней.
Неиспользованный раствор должен быть уничтожен. Каждый флакон или шприц-тюбик можно использовать только однократно. Не встряхивать.
Флаконы и шприц-тюбики следует хранить в картонной пачке в соответствии с требованиями по хранению.
Способ применения
Препарат можно вводить как п/к, так и в/в, в зависимости от клинических предпочтений.
П/к препарат вводят в область плеча, переднюю поверхность бедра или переднюю брюшную стенку. Все указанные области введения одинаково подходят для п/к инъекций.
Содержание гемоглобина следует контролировать 1 раз в 2 недели до его стабилизации и периодически после стабилизации.
Стандартный режим дозирования
Пациенты, не получающие стимулятор эритропоэза в настоящее время
Пациенты, не находящиеся на диализе. Рекомендуемая начальная доза: 1.2 мкг/кг п/к 1 раз в месяц, целевой гемоглобин >110 г/л (6.83 ммоль/л). Возможен альтернативный режим дозирования препарата Мирцера® в начальной дозе 0.6 мкг/кг в/в или п/к 1 раз в 2 недели, целевой гемоглобин >110 г/л (6.83 ммоль/л).
Пациенты, находящиеся на диализе. Рекомендуемая начальная доза: 0.6 мкг/кг в/в или п/к 1 раз в 2 недели, целевой гемоглобин >110 г/л (6.83 ммоль/л).
Дозу препарата Мирцера® можно увеличить на 25-50% от предыдущей, если спустя месяц повышение гемоглобина составляет менее 10 г/л (0.621 ммоль/л). Дальнейшее увеличение дозы примерно на 25-50% можно проводить с интервалами 1 раз в месяц до достижения индивидуального целевого гемоглобина.
Дозу препарата Мирцера® уменьшают на 25-50% от предыдущей, если спустя месяц увеличение гемоглобина составляет более 20 г/л (1.24 ммоль/л). Если гемоглобин превышает 130 г/л (8.07 ммоль/л), то терапию необходимо прервать до снижения гемоглобина менее 130 г/л (8.07 ммоль/л) и затем возобновить, в дозе 50% от предыдущей. При целевом гемоглобине 120 г/л доза препарата изменяется на 25%.
После прекращения терапии гемоглобин снижается примерно на 3.5 г/л (0.22 ммоль/л) в неделю. При достижении целевого гемоглобина >110 г/л (6.83 ммоль/л) пациентов, получающих терапию препаратом Мирцера® 1 раз в 2 недели, можно перевести на режим введения препарата 1 раз в месяц в дозе, превышающей предыдущую в 2 раза. Коррекцию дозы препарата проводят не чаще 1 раза в месяц.
Пациенты, получающие стимулятор эритропоэза в настоящее время
Пациентов, получающих другой стимулятор эритропоэза, можно перевести на терапию препаратом Мирцера® с режимом введения 1 раз в месяц или 1 раз в 2 недели п/к или в/в.
Начальная доза зависит от недельной дозы ранее вводимого препарата — дарбэпоэтина альфа или эпоэтина (альфа или бета) (Таблицы 1 и 2). Первую инъекцию препарата Мирцера® проводят в день следующей запланированной инъекции ранее применявшегося дарбэпоэтина альфа или эпоэтина (альфа или бета).
Таблица 1. Переход с эпоэтина (альфа или бета).
Таблица 2. Переход с дарбэпоэтина альфа.
Если для поддержания целевого гемоглобина выше 110 г/л (6.83 ммоль/л) требуется коррекция дозы, то месячную дозу можно изменить на 25%.
Дозу препарата Мирцера® уменьшают на 25-50% от предыдущей, если спустя месяц увеличение гемоглобина составляет более 20 г/л (1.24 ммоль/л). Если гемоглобин превышает 130 г/л (8.07 ммоль/л), то терапию необходимо прервать до снижения гемоглобина до уровня менее 130 г/л (8.07 ммоль/л) и затем возобновить, в дозе 50% от предыдущей.
При целевом гемоглобине 120 г/л доза препарата изменяется на 25%.
После прекращения терапии гемоглобин снижается примерно на 3.5 г/л (0.22 ммоль/л) в неделю.
Коррекцию дозы препарата проводят не чаще 1 раза в месяц.
Перерыв в лечении
Лечение анемии, в т.ч. и терапия препаратом Мирцера®, обычно бывает долговременным. Но при необходимости терапия препаратом Мирцера® может быть прервана в любой момент.
Пропущенная доза
Пропущенную однократную инъекцию препарата Мирцера® необходимо ввести как можно скорее и далее вводить препарат с предписанной частотой дозирования.
Дозирование в особых случаях
У пациентов с печеночной недостаточностью любой степени тяжести не требуется коррекции начальной дозы препарата и режима дозирования.
У пациентов пожилого возраста (65 лет и старше) не требуется коррекции начальной дозы препарата.
Применение препарата Мирцера® у детей и подростков в возрасте до 18 лет не рекомендуется, в связи с недостаточными данными по безопасности и эффективности препарата у данной категории пациентов.
Инструкция по обращению со шприц-тюбиком
1.Вынуть прозрачную контурную ячейковую упаковку с лекарственным препаратом из картонной пачки, не вскрывая защитную пленку.
2.Тщательно вымыть руки теплой водой с мылом.
3.Снять защитную пленку с контурной ячейковой упаковки, достать шприц-тюбик и прозрачный пластмассовый контейнер с иглой.
4.Удерживая контейнер с иглой, отсоединить колпачок, сделав вращательное движение по часовой стрелке. Снять колпачок с верхней части контейнера с иглой.
5.Удерживая шприц-тюбик, снять резиновый наконечник, предварительно согнув и потянув.
6.Удерживая прозрачный контейнер с иглой, плотно вставить иглу в шприц-тюбик.
Подготовка и проведение инъекции
1.Для введения лекарственного препарата выбрать одно из рекомендуемых мест: передняя брюшная стенка, исключая область вокруг пупка, передняя поверхность середины бедра или наружная поверхность плеча. Не вводить лекарственный препарат в родимые пятна, ткани рубцов, гематомы или в пупок, в места с уплотнениями и/или реакцией после предшествующих инъекций. Следует каждый раз менять места введения препарата. Избегать участков, которые могут подвергаться раздражению ремнем или поясом одежды.
2.Тщательно обработать кожу в месте инъекции тампоном, смоченным спиртом. Подождать пока обработанный участок подсохнет.
3.Аккуратно удерживая шприц-тюбик, не нажимая на поршень, осторожно снять прозрачный контейнер с иглы.
4.Двумя пальцами собрать кожу в складку в месте предполагаемой инъекции. Ввести иглу в кожную складку под прямым углом.
5.Медленно ввести весь лекарственный препарат, плавно давя на поршень. Не прекращать давить на поршень шприц-тюбика, пока не извлечется игла из кожи.
6.После введения всей дозы вынуть иглу из кожи, не отпуская поршень шприц-тюбика.
7.Отпустив поршень, высвободится защитное устройство и закроет иглу.
8.Прижать ватным тампоном место введения лекарственного препарата. При необходимости заклеить место инъекции пластырем.
Побочное действие
Клинические исследования
При применении препарата Мирцера® возникновение нежелательных реакций возможно примерно у 6% пациентов. Наиболее частой из них является повышение АД (часто).
Для описания частоты нежелательных реакций используются следующие категории: часто (≥1/100 и <1/10), нечасто (≥1/1000 и <1/100), редко (≥1/10 000 и <1/1000).
Нежелательные реакции, связанные с терапией препаратом Мирцера®, зарегистрированные в контролируемых клинических исследованиях у пациентов с ХБП
Со стороны сердечно-сосудистой системы: часто — повышение АД; нечасто – тромбоз шунта; редко — приливы.
Со стороны ЦНС: нечасто – головная боль; редко — гипертензивная энцефалопатия.
Со стороны иммунной системы: редко — реакции гиперчувствительности.
Со стороны кожи и ее придатков: редко — макуло-папулезная сыпь (серьезная нежелательная реакция).
Все другие нежелательные реакции, связанные с терапией препаратом Мирцера®, сообщались редко и в большинстве случаев были легкой или средней степени тяжести. Данные нежелательные реакции могут быть обусловлены сопутствующими заболеваниями.
Изменения лабораторных показателей
В клинических исследованиях в ходе терапии препаратом Мирцера® наблюдалось незначительное снижение числа тромбоцитов в пределах нормальных значений. У 7.5% пациентов, получавших терапию препаратом Мирцера®, и у 4.4% пациентов, получавших терапию другими стимуляторами эритропоэза, наблюдалась тромбоцитопения (количество тромбоцитов <100×109/л).
Постмаркетинговые наблюдения
При применении препарата Мирцера® сообщалось о парциальной красноклеточной аплазии (ПККА), вызванной образованием нейтрализующих антител к эритропоэтину. В остальном профиль безопасности препарата соответствовал нежелательным реакциям, зарегистрированным при применении препарата Мирцера® в клинических исследованиях.
Противопоказания к применению
- неконтролируемая артериальная гипертензия;
- гиперчувствительность к метоксиполиэтиленгликоль-эпоэтину бета или любому другому компоненту препарата.
С осторожностью следует применять при беременности, в период грудного вскармливания, при гемоглобинопатии, эпилепсии, тромбоцитозе (число тромбоцитов более 500×109/л), поскольку безопасность и эффективность препарата Мирцера® для данных групп изучены недостаточно.
Применение при беременности и кормлении грудью
Безопасность и эффективность применения препарата Мирцера® при беременности изучены недостаточно.
Результаты исследований, проведенных на животных, свидетельствуют о том, что препарат Мирцера® не оказывает прямого или косвенного вредного действия в отношении беременности, эмбрионального/фетального развития, родов или постнатального развития. Следует соблюдать осторожность при назначении препарата Мирцера® беременным.
Неизвестно, выводится ли метоксиполиэтиленгликоль-эпоэтин бета с грудным молоком у человека. В исследовании на животных показано, что метоксиполиэтиленгликоль-эпоэтин бета выводится с грудным молоком. Вопрос о прекращении кормления грудью или отмене терапии должен решаться в зависимости от важности лечения для матери и грудного вскармливания для ребенка.
Применение при нарушениях функции печени
Фармакокинетика метоксиполиэтиленгликоль-эпоэтина бета у пациентов с печеночной недостаточностью не изучена.
Применение при нарушениях функции почек
У пациентов с печеночной недостаточностью любой степени тяжести не требуется коррекция дозы препарата.
Применение у детей
Применение препарата Мирцера® у детей и подростков до 18 лет не рекомендуется, в связи с недостаточными данными по безопасности и эффективности препарата у данной категории пациентов.
Применение у пожилых пациентов
У пациентов пожилого возраста (старше 65 лет) не требуется коррекции начальной дозы препарата.
Особые указания
До начала и во время лечения препаратом Мирцера® необходимо исключить дефицит железа.
Дополнительная терапия железом рекомендуется, если содержание ферритина в сыворотке крови ниже 100 мкг/л или насыщение трансферрина железом ниже 20%.
Отсутствие эффекта: наиболее частыми причинами неполного ответа на лечение средствами, стимулирующими эритропоэз, являются дефицит железа, воспаление, хроническая кровопотеря, фиброз костного мозга, резкое увеличение концентрации алюминия, обусловленное гемодиализом, дефицит фолиевой кислоты или витамина В12, гемолиз. Если все перечисленные состояния исключены и у больного наблюдается внезапное снижение гемоглобина, ретикулоцитопения и обнаруживаются антитела к эритропоэтину, необходимо провести исследование костного мозга для исключения ПККА.
При развитии ПККА терапию препаратом Мирцера® необходимо прекратить и пациентов не следует переводить на терапию другими стимуляторами эритропоэза.
На фоне терапии стимуляторами эритропоэза, в т.ч. при применении препарата Мирцера®, сообщалось о случаях развития ПККА, вызванной антителами к эритропоэтину. Антитела обладают перекрестной реакцией со всеми стимуляторами эритропоэза. Не следует переводить на терапию препаратом Мирцера® пациентов с подтвержденными антителами к эритропоэтину или подозрением на их наличие.
Повышение АД: до начала и во время лечения препаратом Мирцера®, как и другими стимуляторами эритропоэза, необходимо контролировать АД. Если АД не удается контролировать медикаментозно, необходимо снизить дозу или приостановить терапию препаратом Мирцера®.
Эффект на опухолевый рост: препарат Мирцера®, как и другие лекарственные средства, стимулирующие эритропоэз, является фактором роста, который в основном стимулирует образование эритроцитов. Эритропоэтиновые рецепторы могут присутствовать на поверхности различных опухолевых клеток. Возможно, что средства, стимулирующие эритропоэз (как и другие факторы роста), могут стимулировать рост злокачественного образования любого типа.
При применении эпоэтинов у пациентов с различными злокачественными опухолями, в т.ч. головы и шеи, молочной железы, наблюдалось увеличение летальности, причины которой неясны.
Следует проявлять осторожность при применении препарата Мирцера® у пациентов с гемоглобинопатиями, эпилепсией, тромбоцитозом (число тромбоцитов более 500×109/л), поскольку безопасность и эффективность препарата для данных групп не изучены.
Попадание лекарственных препаратов в окружающую среду должно быть сведено к минимуму. Не следует утилизировать препарат с помощью сточных вод или вместе с бытовыми отходами. По возможности необходимо использовать специальные системы для утилизации лекарственных препаратов.
Доклинические данные по безопасности
Канцерогенность: долгосрочные исследования по изучению канцерогенности у животных не проводились. Препарат Мирцера® не вызвал пролиферативного ответа in vitro, при этом связывание препарата Мирцера® наблюдалось только в клетках-мишенях (клетках предшественниках в костном мозге).
Нарушение фертильности: исследования на животных не выявили какого-либо отрицательного влияния препарата на фертильность.
Влияние на способность к управлению транспортными средствами и механизмами
Исследования по изучению влияния препарата на способность управлять транспортными средствами и заниматься другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций, не проводились. Исходя из механизма действия и профиля безопасности, препарат Мирцера® не обладает таким действием.
Передозировка
Препарат Мирцера® обладает широким терапевтическим диапазоном, при инициации терапии следует принимать во внимание индивидуальный ответ на терапию. Возможен чрезмерный фармакодинамический ответ, т.е. чрезмерный эритропоэз. При высоком уровне гемоглобина необходимо временно прервать терапию препаратом Мирцера®. При необходимости может быть проведена флеботомия.
Лекарственное взаимодействие
Исследований по изучению взаимодействия с другими лекарственными средствами не проводилось. Полученные до настоящего времени данные не выявили какого-либо взаимодействия препарата Мирцера® с другими препаратами, а также не выявлено признаков влияния других препаратов на фармакокинетику и фармакодинамику препарата Мирцера®.
Фармацевтическое взаимодействие
Не следует смешивать метоксиполиэтиленгликоль-эпоэтин бета с другими лекарственными средствами или инъекционными растворами.
Условия хранения препарата Мирцера®
Препарат следует хранить в недоступном для детей, защищенном от света месте при температуре от 2° до 8°C; не замораживать.
Срок годности препарата Мирцера®
Срок годности — 3 года.
Препарат не следует использовать по истечении срока годности, указанного на упаковке.
Условия реализации
Препарат отпускается по рецепту.
Состав Один флакон (1 мл) содержит: метоксиполиэтиленгликоль-эпоэтин бета 50 мкг, 100 мкг, 200 мкг, 300 мкг, 400 мкг, 600 мкг, 1000 мкг вспомогательные вещества: L-метионин, натрия сульфат безводный, натрия дигидрофосфата моногидрат, маннитол, полоксамер 188, кислота хлористоводородная разбавленная или раствор натрия гидроксида, вода для инъекций. Один шприц-тюбик (0.3 мл) содержит: метоксиполиэтиленгликоль-эпоэтин бета 50 мкг, 75 мкг, 100 мкг, 150 мкг, 200 мкг, 250 мкг вспомогательные вещества: L-метионин, натрия сульфат безводный, натрия дигидрофосфата моногидрат, маннитол, полоксамер 188, кислота хлористоводородная разбавленная или раствор натрия гидроксида, вода для инъекций. Один шприц-тюбик (0.6 мл) содержит: метоксиполиэтиленгликоль-эпоэтин бета 400 мкг, 600 мкг, 800 мкг вспомогательные вещества: L-метионин, натрия сульфат безводный, натрия дигидрофосфата моногидрат, маннитол, полоксамер 188, кислота хлористоводородная разбавленная или раствор натрия гидроксида, вода для инъекций. Описание Прозрачная бесцветная или слегка желтоватого цвета жидкость.
Фармакотерапевтическая группа:
Гемопоэза стимулятор
Код ATX: [BO3XA03]
Фармакологическое действие
Фармакодинамика
Мирцера — химически синтезированный представитель нового класса активаторов рецепторов эритропоэтина длительного действия. Метоксиполиэтиленгликоль-эпоэтин бета является ковапентным конъюгантом белка, полученного методом рекомбинантной ДНК, и линейного метоксиполиэтиленгликоля (ПЭГ). Метоксиполиэтиленгликоль-зпоэтин бета отличается от эритропоэтина наличием амидной связи между N-концевой аминогруппой или ε-аминогруппой лизина, преимущественно Lys52 и Lys45, и метоксиполиэтиленгликольбутановой кислотой. Молекулярная масса метоксиполиэтилен-гликоль-эпоэтин бета составляет примерно 60 кДа, включая 30 кДа молекулярную массу ПЭГ.
Мирцера обладает отличной от эритропоэтина активностью на уровне рецептора и характеризуется более длительной ассоциацией с рецептором и более быстрой диссоциацией от рецептора, сниженной специфической активностью in vitro и повышенной активностью in vivo, а также увеличенным периодом полувыведения, что позволяет вводить Мирцеру 1 раз в месяц.
Механизм действия
Мирцера стимулирует эритропоэз при взаимодействии с эритропоэтиновыми рецепторами на клетках предшественниках костного мозга.
Клиническая эффективность
У 97.5% пациентов с хроническими заболеваниями почек, не находящихся на диализе, при терапии Мирцерой отмечена коррекция анемии. У 93.3% пациентов с хроническими заболеваниями почек, находящихся на диализе, при терапии Мирцерой отмечена коррекция анемии. У пациентов, находящихся на диализе, при переводе с терапии дарбэпоэтином альфа или эпоэтином на терапию Мирцерой сохраняется стабильный целевой уровень гемоглобина (Нb).
Фармакокинетика
Период полувыведения (T½) после в/в введения Мирцеры в 15-20 раз продолжительнее, чем при введении рекомбинантного человеческого эритропоэтина.
Клиренс и объём распределения метоксиполиэтиленгликоль-эпоэтина бета не зависят от дозы.
Длительное назначение не влияет на клиренс, объём распределения и биодоступность метоксиполиэтиленгликоль-эпоэтинабета. Введение метоксиполиэтиленгликоль-эпоэтина бета 1 раз в 4 недели не приводит к значимой кумуляции препарата, коэффициент кумуляции равен 1,03 при введении 1 раз в 4 недели и 1.12- при введении 1 раз в 2 недели. Не выявлено различий в фармакокинетике препарата у больных, получающих и не получающих диализ.
Гемодиализ не оказывает влияниет на фармакокинетику метоксиполиэтиленгликоль-эпоэтина бета.
Фармакокинетика, фармакодинамика и местная переносимость не зависят от места подкожной инъекции препарата (плечо, передняя поверхность бедра, передняя брюшная стенка).
Абсорбция после подкожного введения
Время достижения максимальной сывороточной концентрации метоксиполиэтилен- гликоль-эпоэтина бета при п/к введении — 72 часа.
Абсолютная биодоступность метоксиполиэтиленгликоль-эпоэтина бета у пациентов, находящихся на диализе, и у пациентов, не находящихся на диализе, составляет 62% и 54%, соответственно.
Распределение
Объём распределения составляет 5 литров.
Экскреция
Период полувыведения (T½) метоксиполиэтиленгликоль-эпоэтина бета при в/в введении 134 часа (или 5.6 дней), при п/к введении -139 часов (или 5.8 дней), полный системный клиренс 0.494 мл/ч/кг.
Фармакокинетика у специальных групп пациентов
Печёночная недостаточность: фармакокинетика метоксиполиэтцленгликоль-эпоэтина бета у пациентов с тяжелой печёночной недостаточностью и у здоровых пациентов не отличается.
Пол, раса, пожилой возраст: не требуется коррекции начальной дозы метоксиполи-этиленгликоль-эпоэтина бета.
Показания
Анемия при хронической почечной недостаточности (по классификации NKF K/DOQI -при хроническом заболевании почек).
Противопоказания
Повышенная чувствительность к метоксиполиэтиленгликоль-эпоэтину бета или к любому другому компоненту препарата.
Неконтролируемая артериальная гипертензия.
Детский возраст до 18 лет (безопасность и эффективность не установлены).
С осторожностью
Беременность, период кормления грудью, гемоглобинопатии, печеночная недостаточность, эпилепсия, тромбоцитоз (число тромбоцитов более 500 × 109/л) , поскольку безопасность и эффективность Мирцеры для данных групп изучены недостаточно.
Беременность и период кормления грудью
Безопасность и эффективность Мирцеры для данных групп изучены недостаточно. При беременности и в период кормления грудью Мирцеру следует назначать только в том случае, если предполагаемая польза для матери превышает потенциальный риск для плода или ребенка.
На животных Мирцера не оказывает прямого или косвенного вредного действия в отношении беременности, эмбрионального/фетального развития, родов или постнатального развития. Неизвестно, выводится ли метоксиполиэтиленгликоль-эпоэтин бета с грудным молоком у человека. В исследовании на животных показано, что метокси полиэтилен гли коль-эпоэти н бета выводится с материнским молоком.
Способ применения и дозы
Учитывая более длительный период полувыведения, Мирцера должна вводиться реже, чем другие стимуляторы эритропоэза.
Лечение препаратом Мирцера необходимо начинать только под наблюдением специалиста.
Правша хранения раствора в амбулаторных и стационарных условиях Раствор Мирцеры стерилен и не содержит консервантов. Применять следует только прозрачный бесцветный или слегка желтоватого цвета раствор, не содержащий видимых.примесей. Перед введением раствор доводят до комнатной температуры, если препарат хранился в холодильнике. Шприц-тюбик может храниться в течение 1 месяца при комнатной температуре (не выше 30°С) и должен быть использован в течение этого месяца. Флакон может храниться в течение 7 дней при комнатной температуре (не выше 25°С) и должен быть использован в тече-ние этих 7 дней.
Неиспользованный раствор должен быть уничтожен. Каждый флакон или шприц-тюбик можно использовать только однократно. Не встряхивать. Способ применения Препарат можно вводить как подкожно (п/к), так и внутривенно (в/в). Препарат следует вводить п/к в область плеча, переднюю поверхность бедра или переднюю брюшную стенку. Содержание Hb следует контролировать 1 раз в две недели до его стабилизации и периодически после стабилизации. Стандартный режим дозирования Пациенты, не получающие стимулятор эритропоэза в настоящее время Рекомендуемая начальная доза: 0.6 мкг/кг в/в или п/к 1 раз в 2 недели, целевой показатель гемоглобина >110 г/л (6.83 ммоль/л).
Дозу Мирцеры можно увеличить на 25-50% от предыдущей, если спустя месяц повышение Hb составляет менее Юг/л (0.621 ммоль/л). Дальнейшее увеличение дозы примерно на 25-50% можно проводить с интервалами 1 раз в месяц до достижения индивидуального целевого содержания Hb.
Дозу Мирцеры уменьшают на 25-50% от предыдущей, если спустя месяц увеличение Hb составляет более 20 г/л (1.24 ммоль/л). Если Hb превышает 130 г/л (8.07 ммоль/л), то терапию необходимо прервать до снижения Hb менее 130 г/л (8.07 ммоль/л) и затем возобновить, в дозе 50% от предыдущей. При целевом Hb 120 г/л доза препарата изменяется на 25%. После прекращения терапии Hb снижается примерно на 3.5 г/л (0.22 ммоль/л) в неделю.
Коррекцию дозы препарата проводят не чаще 1 раза в месяц.
Пациенты, получающие стимулятор эритропоэза в настоящее время Пациентов, получающих другой стимулятор эритропоэза, можно перевести на терапию Мирцерой с режимом введения 1 раз в месяц или 1 раз в 2 недели п/к или в/в.
Начальная доза: зависит от недельной дозы ранее вводимого препарата — дарбэпо-этина альфа или эпоэтина (альфа или бета) (см. Таблицы1 и 2). Первую инъекцию Мирцеры проводят в день следующей запланированной инъекции ранее применявшегося дарбэпоэтина альфа или эпоэтина (альфа или бета).
| Предшествующая недельная доза эпоэтина (ЕД/неделя) |
Доза Мирцеры | |
| Один раз в месяц (мкг/месяц) |
Один раз в две недели (мкг/2 недели) |
|
| <8000 | 120 | 60 |
| 8000-16000 | 200 | 100 |
| >16000 | 360 | 180 |
| Предшествующая недельная цоза дарбэпоэтина альфа (мкг/неделя) | Доза Мирцеры | |
| Один раз в месяц (мкг/месяц) |
Один раз в две недели (мкг/2 недели) |
|
| <40 | 120 | 60 |
| 40-80 | 200 | 100 |
| >80 | 360 | 180 |
Если для поддержания целевого Hb выше 110 г/л (6.83 ммоль/л) требуется коррекция дозы, то месячную дозу можно изменить на 25%.
Дозу Мирцеры уменьшают на 25-50% от предыдущей, если спустя месяц увеличение Hb составляет более 20 г/л (1.24 ммоль/л). Если Hb превышает 130 г/л (8.07 ммоль/л), то терапию необходимо прервать до снижения Hb до уровня менее 130 г/л (8.07 ммоль/л) и затем возобновить, в дозе 50% от предыдущей. При целевом Hb 120 г/л доза препарата изменяется на 25%.
После прекращения терапии Hb снижается примерно на 3.5 г/л (0.22 ммоль/л) в неделю.
Коррекцию дозы препарата проводят не чаще 1 раза в месяц.
Перерыв в лечении
Лечение анемии, в том числе и терапия препаратом Мирцера, обычно бывает долговременным. Но при необходимости терапия препаратом Мирцера может быть прервана в любой момент.
Пропущенная доза
Пропущенную однократную инъекцию Мирцеры необходимо ввести как можно скорее и далее вводить препарат с предписанной частотой дозирования. Дозирование в особых случаях Печёночная недостаточность: не требуется коррекции начальной дозы препарата и режима дозирования у пациентов с печёночной недостаточностью любой степени тяжести.
Пожилой возраст (старше 65 лет): не требуется коррекции начальной дозы препарата.
Инструкция по обращению со шприц-тюбиком
- Вынуть прозрачную контурную ячейковую упаковку с лекарственным препаратом из картонной пачки, не вскрывая защитную пленку.
- Тщательно вымыть руки теплой водой с мылом.
- Снять защитную пленку с контурной ячейковой упаковки, достать шприц-тюбик и прозрачный пластмассовый контейнер с иглой.
- Удерживая контейнер с иглой, отсоединить колпачок, сделав вращательное движение по часовой стрелке, как показано на рисунке. Снять колпачок с верхней части контейнера с иглой.
- Удерживая шприц-тюбик, снять резиновый наконечник, предварительно согнув и потянув, как показано на рисунке.
- Удерживая прозрачный контейнер с иглой, плотно вставить иглу в шприц-тюбик, как показано на рисунке.
Подготовка и проведение инъекции
- Для введения лекарственного препарата выбрать одно из рекомендуемых мест: передняя брюшная стенка, исключая область вокруг пупка, передняя поверхность середины бедра или наружная поверхность плеча. Не вводить лекарственный препарат в родимые пятна, ткани рубцов, гематомы или в пупок, в места с уплотнениями и/или реакцией после предшествующих инъекций. Следует каждый раз менять места введения препарата. Избегать участков, которые могут подвергаться раздражению ремнем или поясом одежды.
- Тщательно обработать кожу в месте инъекции тампоном, смоченным спиртом. Подождать пока обработанный участок подсохнет.
- Аккуратно удерживая шприц-тюбик, не нажимая на поршень, осторожно снять прозрачный контейнер с иглы.
- Двумя пальцами собрать кожу в складку в месте предполагаемой инъекции. Ввести иглу в кожную складку под прямым углом.
- Медленно, ввести весь лекарственный препарат, плавно давя на поршень. Не прекращайте давить на поршень шприц-тюбика пока не извлечете иглу из кожи!
- После введения всей дозы вынуть иглу из кожи, не отпуская поршень шприц-тюбика, как показано на рисунке.
- Отпустив поршень, высвободится защитное устройство и закроет иглу.
- Прижать ватным тампоном место введения лекарственного препарата. При необходимости заклеить место инъекции пластырем.
Побочное действие
Следующие категории используются для описания частоты нежелательных реакций: Часто (21/100 и 1/1000 и со стороны сердечно-сосудистой системы: артериальная гипертензия (часто); тромбоз шунта (редко);
со стороны нервной системы: головная боль (редко), гипертензивная энцефалопатия (очень редко);
со стороны иммунной системы: реакции гиперчувствительности (очень редко); со стороны кожи и ее придатков: макулопапулезная сыпь (очень редко).
Изменения лабораторных показателей У 7.5% пациентов, получавших терапию Мирцерой, и у 4.4 % пациентов, получавших терапию другими стимуляторами эритропоэза, наблюдалась тромбоцитопения (количество тромбоцитов 9/л).
Передозировка
Максимально переносимая доза у пациентов не определялась. Возможен чрезмерный фармакодинамический ответ, т.е. чрезмерный эритропоэз. При высоком уровне гемоглобина необходимо временно прервать терапию Мирцерой (см. «Способ применения и дозы»). При необходимости может быть проведена флеботомия.
Взаимодействие с другими лекарственными средствами
Исследований по изучению взаимодействия с другими лекарственными средствами не проводилось. Полученные до настоящего времени данные не выявили каких-либо взаимодействий Мирцеры с другими препаратами. Проведенный популяционный анализ не выявил признаков влияния других препаратов на фармакокинетику и фармакодинамику Мирцеры. Не следует смешивать метоксиполиэтиленгликоль-эпоэтин бета с другими лекарственными средствами или инъекционными растворами.
Особые указания
До начала и во время лечения Мирцерой необходимо исключить дефицит железа.
Дополнительная терапия железом рекомендуется, если содержание ферритина в сыворотке крови ниже 100 мкг/л или насыщение трансферрина железом ниже 20%.
Отсутствие эффекта: наиболее частыми причинами неполного ответа на лечение средствами, стимулирующими эритропоэз, являются дефицит железа, воспаление, хроническая кровопотеря, фиброз костного мозга, резкое увеличение концентрации алюминия, обусловленное гемодиализом, дефицит фолиевой кислоты или витамина В12, гемолиз. Если все перечисленные состояния исключены и у больного наблюдается внезапное снижение гемоглобина, ретикулоцитопения и обнаруживаются антитела к эритропоэтину, необходимо провести исследование костного мозга для исключения парциальной красноклеточной аплазии (ПККА). При развитии ПККА терапию Мирцерой необходимо прекратить и пациентов не следует переводить на терапию другими стимуляторами эритропоэза.
Сообщалось о случаях развития ПККА, вызванной антителами к эритропоэтину, на фоне терапии стимуляторами эритропоэза. Антитела обладают перекрестной реакцией со всеми стимуляторами эритропоэза. Не следует переводить на терапию Мирцерой пациентов с подтвержденными антителами к эритропоэтину или подозрением на их наличие.
Артериальная гипертензия: до начала и во время лечения Мирцерой, как и другими стимуляторами эритропоэза, необходимо контролировать АД. Если АД не удаётся контролировать медикаментозно, необходимо снизить дозу или приостановить терапию Мирцерой (см. «Способ применения и дозы»).
Эффект на опухолевый рост: Мирцера, как и другие лекарственные средства, стимулирующие эритропоэз, является фактором роста, который в основном стимулирует образование эритроцитов, Эритропоэтиновые рецепторы могут присутствовать на поверхности различных опухолевых клеток. Возможно, что средства, стимулирующие эритропоэз, могут стимулировать рост злокачественного образования любого типа. В двух клинических исследованиях, в которых эпоэтины применялись у пациентов с различными злокачественными опухолями, в том числе головы и шеи, молочной железы, наблюдалось увеличение летальности, причины которой неясны.
Влияние на способность управлять автомобилем и работу с механизмами
Исследования по изучению влияния препарата на способность управлять автомобилем и работать с механизмами не проводились. Исходя из механизма действия и профиля безопасности, Мирцера не обладает таким действием.
Форма выпуска и упаковка
Раствор для подкожного и внутривенного введения, флаконы.
По 50 мкг/1 мл, 100 мкг/1 мл, 200 мкг/1 мл, 300 мкг/1 мл, 400 мкг/1 мл, 600 мкг/1 мл, 1000 мкг/1 мл препарата во флаконы, изготовленные из бесцветного стекла (гидролитический класс 1 по ЕФ), укупоренные крышкой из бутилкаучука, обжатые алюминиевым колпачком и закрытые пластмассовой крышкой; цвет крышки соответствует цвету, которым выделена дозировка препарата на этикетке флакона и на пачке. Каждый флакон вместе с инструкцией по применению помещают в картонную пачку; на пачке имеется контроль вскрытия упаковки с указанием места вскрытия.
Раствор для подкожного и внутривенного введения, шприц-тюбики
По 50 мкг/0.3 мл, 75 мкг/0.3 мл, 100 мкг/0.3 мл, 150 мкг/0.3 мл, 200 мкг/0.3 мл, 250 мкг/0.3 мл, 400 мкг/0.6 мл, 600 мкг/0.6 мл, 800 мкг/0.6 мл в шприц-тюбики, корпус которых изготовлен из стекла (гидролитический класс 1 по ЕФ), поршень — из пластмассы, с пробкой из бутилкаучука, ламинированного фторполимером. Цвет поршня соответствует цвету, которым выделена дозировка препарата на этикетке шприц-тюбика и на пачке. На круглой рукоятке поршня имеется логотип . С другой стороны шприц-тюбики укупорены наконечником из бутилкаучука, ламинированного фторполимером. Шприц-тюбик помещен в прозрачный защитный пластмассовый контейнер с пружиной. 1 стерильная игла для инъекций помещена в герметично укупоренный пластмассовый контейнер с контролем вскрытия.
1 шприц-тюбик вместе с контейнером с иглой для инъекций помещен в прозрачную контурную ячейковую упаковку, герметично укупоренную. Контурная ячейковая упаковка вместе с инструкцией по применению помещена в картонную пачку.
Условия хранения
Хранить при температуре 2-8°С, в защищенном от света месте. Не замораживать. Хранить в недоступном для детей месте.
Срок годности
Флаконы — 1 год.
Шприц-тюбики — 3 года.
Препарат не следует использовать по истечении срока годности, указанного на упаковке.
Условия отпуска из аптек:
По рецепту.
Производитель
Ф. Хоффманн-Ля Рош Лтд, Швейцария (флаконы) Рош Диагностике ГмбХ, Германия (шприц-тюбики)
Юридический адрес производителя:
Ф. Хоффманн-Ля Рош Лтд, Грензахерштрассе 124, 4070 Базель, Швейцария F. Hoffmann-La Roche Ltd, Grenzacherstrasse 124,4070 Basel, Switzerland
Рош Диагностике ГмбХ, Сандхоферштрассе 116, 68305 Маннхайм, Германия Roche Diagnostics GmbH, Sandhoferstrasse 116, 68305 Mannheim, Germany
Претензии потребителей направлять no адресу Представительства в Москве: 125445, ул.Смольная, д.24Д
Товары из категории — Лекарства от болезней крови
Инструкция по применению
Цена в интернет-аптеке WER.RU: от 1 600
Фармакологические свойства
Препарат Мирцера относится к фармакологической группе медикаментов, действие которых направлено на стимуляцию эритро-и лейкопоэз. Это синтетический медикамент, представляющий из себя новое поколение активаторов гемопоэтина продолжительного действия. Основной действующий компонент препарата — метоксиполиэтиленгликоль-эпоэтин бета.
Медикамент Мирцера оказывает стимулирующее воздействие на процесс кроветворения, в ходе которого образуются эритроциты. Процесс образования эритроцитов происходит в почках, поэтому действие медикамента распространяется, в первую очередь, на этот орган.
Препарат эффективно борется с признаками малокровия при заболевании почек, нормализуя уровень гемоглобина.
Медикаментозное средство назначается только после проведения всех обследований пациента лечащим врачом, сбора анализов и определения точной клинической картины заболевания. При обнаружении гиперчувствительности к компонентам препарата использовать медикамент для терапии нельзя и необходимо выбрать другой способ лечения.
Медикаментозное средство используется для инъекций, которые могут быть введены под кожу или внутривенно. Способ введения препарата выбирается врачом по согласованию с пациентом.
Состав и форма выпуска
Медикамент Мирцера выпускается в форме растворимой жидкости, имеющей светло-желтый оттенок, который вводится внутривенно или под кожу пациента при помощи инъекций.
В состав Мирцеры входят следующие компоненты:
Продается медикамент во флаконах в виде шприца объемом 0,3 мл. В упаковке идет инструкция, игла для укола и сам раствор с медикаментом.
Показания к применению
Медикаментозное средство Мирцера назначается пациентам при малокровии, сопровождающемся болезнями почек, при котором нарушена нормальная работоспособность органа.
Международная классификация болезней (МКБ-10)
D63.8 Анемия при других хронических болезнях, классифицированных в других рубриках.
Побочные эффекты
Применение Мирцеры может стать причиной развития и проявления нежелательных побочных признаков:
Противопоказания
Медикамнтозное средство не рекомендуется использовать при неподдающейся контролю гипертонической болезни и чрезмерной восприимчивости к составляющим медикаментозного средства.
С осторожностью лечащий врач назначает медикамент Мирцера детям, пожилым людям, пациентам с заболеваниями печени, кормящим матерям, беременным женщинам, при нарушении структуры белка гемоглобина, риске появления эпилептических припадков, увеличенном числе тромбоцитов в крови.
Применение при беременности
Нет точных сведений и показаний о воздействии компонентов Мирцеры на развивающийся в утробе матери плод, поэтому принимать медикамент во время беременности следует только при невозможности отказаться от терапии медикаментом и исключительно под наблюдением врача.
Так как сведений о проникновении компонентов медикамента в организм младенца через грудное вскармливание нет, необходимо в период терапии препаратом отказаться от кормления ребенка грудью продолжить его только после завершения курса лечения.
Способ и особенности применения
Оказываясь в организме пациента, медикамент имеет длительный период воздействия, поэтому частота инъекций должна составлять не более одного раза в месяц. Назначается лекарственное средство только лечащим врачом после проведения всех необходимых обследований пациента, сбора анализов и установления точного анамнеза. Ставить инъекции должен также только лечащий врач в специально подобранных условиях.
Медикамент стерилен, без добавления консервантов. Медикамент, готовый для инъекции, должен иметь желтоватый оттенок или быть прозрачным, без осадков. Перед уколом медикамент необходимо согреть до температуры помещения, если он до этого лежал в холодильной камере. Медикаментозное средство с раствором сохраняет свои свойства и может быть использовано на протяжении месяца при температуре, не превышающей 30°C. По истечении месяца использовать препарат нельзя и его необходимо утилизировать. Использовать каждый флакон можно исключительно один раз, после чего остатки средства выбрасываются. Нельзя встряхивать тюбик перед использованием. Необходимо соблюдать все правила и нормы хранения медикамента, указанные в действующей инструкции по применению.
Медикамент Мирцера используется для инъекций в вену и под кожу. Если препарат вводится под кожу, то укол необходимо делать в плечевую область, живот или бедренную часть.
При прохождении курса медикаментом нужно следить за гемоглобином.
Продолжительность курса и рекомендуемую дозировку Мирцеры назначает лечащий врач, учитывая клиническую картину заболевания и индивидуальные особенности пациента. Решение об отмене препарата, а также о корректировке дозы принимается также лечащим врачом, который наблюдает за состоянием пациента на протяжении всего времени прохождения терапии.
Если инъекция была пропущена по какой-либо причине, то ее необходимо поставить как можно быстрее после пропуска, а затем следовать установленному графику.
Не следует назначать медикамент Мирцера детям, не достигшим 18-летнего возраста, так как нет точных данных о воздействии компонентов препарата на растущий и развивающийся организм.
Пожилым людям, пациентам с болезнями печени корректировка дозы или продолжительности курса лечения не нужна.
Рекомендации по использованию медикамента Мирцера:
Медикамент может быть введен под кожу или в вену. Необходимо тщательно выбирать место введения препарата. Ставить инъекции с раствором медикамента можно в плечевую область, переднюю часть живота, не затрагивая район пупочной зоны, или бедренную область. Следует избегать попадания иглы в родинки, шрамы, рубцы, раздражения, гематомы, припухлости. Место инъекции необходимо менять, нельзя ставить укол дважды в одно место. Перед уколом место для инъекции обрабатывают специальным обеззараживающим раствором во избежание попадания инфекции через место прокола. После инъекции место укола также обрабатывается и при необходимости на ранку накладывается пластырь.
Вводить препарат Мирцера может только медицинский персонал, имеющий должную квалификацию и терапевтический опыт.
Взаимодействие с другими лекарствами
Нет данных и сведений о взаимодействии медикамента Мирцера с другими препаратами. При использовании других медикаментов любой этиологии и назначения, пациенту необходимо сообщить об этом лечащему врачу, который примет решение об отмене какого-либо из препаратов или изменении дозировки.
Передозировка
Медикаментозное средство Мирцера имеет широкий спектр воздействия. После первой инъекции лечащий врач пациент должны проследить за реакцией организма на компоненты препарата. В случае проявления побочных признаков или других неприятных симптомов, необходимо принять решение об отмене препарата или изменении дозировки. При повышенном уровне гемоглобина необходимо прекратить употребление препарата.
Аналоги
Аналогами медикаментозного средства Мирцера по составу и фармакологическому воздействию являются Epoetinum beta и Methoxypolyaethylenglycolum-epoetinum beta.
Условия продажи
Медикаментозное средство отпускается в аптечных пунктах только по назначению лечащего врача при наличии рецептурного листа.
Условия хранения
Хранить медикамент следует в изолированном от досягаемости детьми и проникновения света месте при температуре от 2 до 8 °C, нельзя хранить медикамент в холодильнике во избежание заморозки. Срок хранения медикамента составляет три года с момента изготовления. По истечении срока годности и хранения, указанного на упаковке, медикамент использовать нельзя и его следует утилизировать в соответствии с правилами.
Цены на Мирцера в Москве
Заберите заказ в в аптеке
WER (г. Москва)
Цена: от 1 600 руб.
Сертификаты и лицензии
Один флакон (1 мл) содержит:
активное вещество: метоксиполиэтиленгликоль-эпоэтин бета 50 мкг, 100 мкг, 200 мкг, 300 мкг, 400 мкг, 600 мкг, 1000 мкг;
вспомогательные вещества: L-метионин — 1.49 мг, натрия сульфат безводный — 5.68 мг, натрия дигидрофосфата моногидрат — 1.38 мг, маннитол — 30.00 мг, полоксамер 188-0.10 мг, кислота хлористоводородная разбавленная или раствор натрия гидроксида (q.s. до pH 6.2), вода для инъекций.
Один шприц-тюбик (0.3 мл) содержит:
активное вещество: метоксиполиэтиленгликоль-эпоэтин бета 30 мкг, 40 мкг, 50 мкг, 60 мкг, 75 мкг, 100 мкг, 120 мкг, 150 мкг, 200 мкг, 250 мкг;
вспомогательные вещества: L-метионин — 0.447 мг, натрия сульфат безводный — 1.704 мг, натрия дигидрофосфата моногидрат — 0.414 мг, маннитол — 9.000 мг, полоксамер 188-
0. 030 мг, кислота хлористоводородная разбавленная или раствор натрия гидроксида (q.s. до pH 6.2), вода для инъекций.
Один шприц-тюбик (0.6 мл) содержит:
активное вещество: метоксиполиэтиленгликоль-эпоэтин бета 360 мкг, 400 мкг, 600 мкг, 800 мкг;
вспомогательные вещества: L-метионин — 0.894 мг, натрия сульфат безводный — 3.408 мг, натрия дигидрофосфата моногидрат — 0.828 мг, маннитол — 18.000 мг, полоксамер 188 — 0. 060 мг, кислота хлористоводородная разбавленная или раствор натрия гидроксида (q.s. до pH 6.2), вода для инъекций.
Прозрачная бесцветная или слегка желтоватого цвета жидкость.
Препарат Мирцера® — химически синтезированный представитель нового класса активаторов рецепторов эритропоэтина длительного действия. Метоксиполиэтиленгликоль- эпоэтин бета является ковалентным конъюгантом белка, полученного методом рекомбинантной ДНК, и линейного метоксиполиэтиленгликоля (ПЭГ). Метоксиполиэтиленгли- коль-эпоэтин бета отличается от эритропоэтина наличием амидной связи между N- концевой аминогруппой или s-аминогруппой лизина, преимущественно Lys52 и Lys45, и метоксиполиэтиленгликольбутановой кислотой. Молекулярная масса метоксиполиэтилен- гликоль-эпоэтин бета составляет примерно 60 кДа, включая 30 кДа молекулярную массу ПЭГ.
Препарат Мирцера® обладает отличной от эритропоэтина активностью на уровне рецептора и характеризуется более длительной ассоциацией с рецептором и более быстрой диссоциацией от рецептора, сниженной специфической активностью in vitro и повышенной активностью in vivo, а также увеличенным периодом полувыведения, что позволяет вводить препарат Мирцера® 1 раз в месяц.
Механизм действия
Препарат Мирцера® стимулирует эритропоэз при взаимодействии с эритропоэтиновыми рецепторами на клетках-предшественниках костного мозга.
Являясь основным фактором роста, необходимым для созревания эритроцитов, естественный эритропоэтин вырабатывается почками и высвобождается в кровяное русло в ответ на гипоксию. В ответ на гипоксию эритропоэтин взаимодействует с клетками- предшественниками эритроцитов и приводит к повышению образования эритроцитов. Клиническая эффективность
Коррекция анемии отмечена у 97.5% и 94.1% пациентов с хронической болезнью почек (ХБП), не находящихся на диализе, при терапии препаратом Мирцера® 1 раз в 2 недели и 1 раз в месяц, соответственно. В первые 8 недель терапии гемоглобин (НЬ) превышал 130 г/л у 11.4% пациентов, получавших препарат Мирцера® 1 раз в 2 недели, и у 34% пациентов, получавших дарбэпоэтин альфа, и превышал 120 г/л у 25.8% пациентов, получавших препарат Мирцера® 1 раз в месяц, и у 47.7% пациентов, получавших дарбэпоэтин альфа.
У 93.3% пациентов с ХБП, находящихся на диализе, при терапии препаратом Мирцера® отмечена коррекция анемии. У пациентов, находящихся на диализе, при переводе с терапии дарбэпоэтином альфа или эпоэтином на терапию препаратом Мирцера® сохраняется стабильный целевой НЬ.
В группе поддерживающей терапии препаратом Мирцера®, 1 раз в месяц, доля пациентов с ХБП, находящихся на гемодиализе, с ответом на терапию была значительно выше по сравнению с группой поддерживающей терапии дарбэпоэтином альфа, 1 раз в месяц (pO.OOOl).
Фармакокинетические и фармакологические параметры позволяют вводить препарат Мирцера® 1 раз месяц в связи с увеличенным периодом полувыведения.
Период полувыведения (Т щ) после внутривенного (в/в) введения препарата Мирцера® в 15-20 раз продолжительнее, чем при введении рекомбинантного человеческого эритропоэтина.
Фармакокинетические параметры препарата изучались у здоровых добровольцев и у пациентов с анемией и ХБП, находящихся и не находящихся на диализе.
У пациентов с ХБП клиренс и объем распределения метоксиполиэтиленгликоль-эпоэтина бета не зависят от дозы.
Фармакокинетика препарата Мирцера® изучалась у пациентов с ХБП после однократного введения на 9 неделе и 19 или 21 неделе. Многократное введение не влияет на клиренс, объем распределения и биодоступность метоксиполиэтиленгликоль-эпоэтина бета. Введение метоксиполиэтиленгликоль-эпоэтина бета 1 раз в 4 недели пациентам с ХБП не приводит к значимой кумуляции препарата, коэффициент кумуляции равен 1.03 при введении 1 раз в 4 недели. Коэффициент кумуляции при введении 1 раз в 2 недели равен 1.12. Результаты сравнения сывороточных концентраций метоксиполиэтиленгликоль-эпоэтина бета до и после проведения гемодиализа у пациентов с ХБП показали, что гемодиализ не оказывает влияние на фармакокинетику препарата. У больных с ХБП, получающих и не получающих диализ, различия в фармакокинетике отсутствовали.
Фармакокинетика, фармакодинамика и местная переносимость не зависят от места подкожной (п/к) инъекции препарата (плечо, передняя поверхность бедра, передняя брюшная стенка), что подтверждается результатами исследования, проведенного на здоровых добровольцах. На основании данных результатов эти места одинаково подходят для п/к введения препарата Мирцера®.
Абсорбция после подкожного введения
Время достижения максимальной сывороточной концентрации метоксиполиэтилен- гликоль-эпоэтина бета при п/к введении пациентам с ХБП, находящимся на диализе, — 72 часа (медиана) и 95 часов после введения пациентам, не находящимся на диализе. Абсолютная биодоступность метоксиполиэтиленгликоль-эпоэтина бета у пациентов, находящихся на диализе, и у пациентов, не находящихся на диализе, составляет 62% и 54%, соответственно.
Распределение
У пациентов с ХБП объем распределения составляет 5 литров.
Экскреция
Тi/2 метоксиполиэтиленгликоль-эпоэтина бета при в/в введении 134 часа (или 5.6 дней), а полный системный клиренс 0.494 мл/ч/кг. Т1/2 препарата при п/к введении — 139 часов у пациентов, находящихся на диализе, и 142 часа, у пациентов, не находящихся на диализе. Фармакокинетика у специальных групп пациентов
Печеночная недостаточность’, фармакокинетика метоксиполиэтиленгликоль-эпоэтина бета у пациентов с тяжелой печеночной недостаточностью и у здоровых добровольцев не отличается (см. раздел «Способ применения и дозы», подраздел «Дозирование в особых случаях»).
Другие особые группы пациентов: коррекции начальной дозы метоксиполиэтиленгликоль- эпоэтина бета в зависимости от пола, расы, возраста не требуется.
У пациентов 65 лет и старше изменение начальной дозы не требуется.
У пациентов, находящихся и не находящихся на диализе, различия в фармакокинетике препарата отсутствуют.
Доклинические данные по безопасности
Канцерогенность: долгосрочные исследования по изучению канцерогенности у животных не проводились. Препарат Мирцера® не вызвал пролиферативного ответа in vitro, при этом связывание препарата Мирцера® наблюдалось только в клетках-мишенях (клетках- предшественниках в костном мозге).
Нарушение фертильности: исследования на животных не выявили какого-либо отрицательного влияния препарата на фертильность.
Анемия при хронической почечной недостаточности (по классификации NKF K/DOQI — при хронической болезни почек).
Повышенная чувствительность к метоксиполиэтиленгликоль-эпоэтину бета или к любому другому компоненту препарата.
Неконтролируемая артериальная гипертензия.
Беременность, период кормления грудью, гемоглобинопатии, эпилепсия, тромбоцитоз (число тромбоцитов более 500 х 109/л), поскольку безопасность и эффективность препарата Мирцера® для данных групп изучены недостаточно.
Безопасность и эффективность применения препарата Мирцера® у беременных изучены недостаточно.
Результаты исследований, проведенных на животных, свидетельствуют о том, что препарат Мирцера® не оказывает прямого или косвенного вредного действия в отношении беременности, эмбрионального/фетального развития, родов или постнатального развития. Следует соблюдать осторожность при назначении препарата Мирцера® беременным. Неизвестно, выводится ли метоксиполиэтиленгликоль-эпоэтин бета с грудным молоком у человека. В исследовании на животных показано, что метоксиполиэтиленгликоль-эпоэтин бета выводится с материнским молоком. Вопрос о прекращении кормления грудью или отмене терапии должен решаться в зависимости от важности лечения для матери и грудного вскармливания для ребенка.
Учитывая более длительный период полувыведения, препарат Мирцера® должен вводиться реже, чем другие стимуляторы эритропоэза.
Лечение препаратом Мирцера® необходимо начинать только под наблюдением специалиста.
Правша хранения раствора в амбулаторных и стационарных условиях Раствор препарата Мирцера® стерилен и не содержит консервантов. Применять следует только прозрачный бесцветный или слегка желтоватого цвета раствор, не содержащий видимых примесей. Перед введением раствор доводят до комнатной температуры, если препарат хранился в холодильнике.
Шприц-тюбик может храниться в течение 1 месяца при комнатной температуре (не выше 30°С) и должен быть использован в течение этого месяца.
Флакон может храниться в течение 7 дней при комнатной температуре (не выше 25 °С) и должен быть использован в течение этих 7 дней.
Неиспользованный раствор должен быть уничтожен. Каждый флакон или шприц-тюбик можно использовать только однократно. Не встряхивать.
Флаконы и шприц-тюбики следует хранить в картонной пачке в соответствии с требованиями по хранению (см. раздел «Условия хранения»).
Способ применения
Препарат можно вводить как п/к, так и в/в, в зависимости от клинических предпочтений. Препарат следует вводить п/к в область плеча, переднюю поверхность бедра или переднюю брюшную стенку. Все вышеуказанные области введения одинаково подходят для п/к инъекций.
Содержание НЬ следует контролировать 1 раз в 2 недели до его стабилизации и периодически после стабилизации.
Стандартный режим дозирования
Патенты, не получающие стимулятор эритропоэза в настоящее время Пациенты, не находящиеся на диализе
Рекомендуемая начальная доза: 1.2 мкг/кг п/к 1 раз в месяц, целевой НЬ >110 г/л (6.83 ммоль/л). Возможен альтернативный режим дозирования препарата Мирцера® в начальной дозе 0.6 мкг/кг в/в или п/к 1 раз в 2 недели, целевой НЬ >110 г/л (6.83 ммоль/л).
Пациенты, находящиеся на диализе
Рекомендуемая начальная доза: 0.6 мкг/кг в/в или п/к 1 раз в 2 недели, целевой НЬ >110 г/л (6.83 ммоль/л).
Дозу препарата Мирцера® можно увеличить на 25-50% от предыдущей, если спустя месяц повышение НЬ составляет менее 10 г/л (0.621 ммоль/л). Дальнейшее увеличение дозы примерно на 25-50% можно проводить с интервалами 1 раз в месяц до достижения индивидуального целевого НЬ.
Дозу препарата Мирцера® уменьшают на 25-50% от предыдущей, если спустя месяц увеличение НЬ составляет более 20 г/л (1.24 ммоль/л). Если НЬ превышает 130 г/л (8.07 ммоль/л), то терапию необходимо прервать до снижения НЬ менее 130 г/л (8.07 ммоль/л) и затем возобновить, в дозе 50% от предыдущей. При целевом НЬ 120 г/л доза препарата изменяется на 25%.
После прекращения терапии НЬ снижается примерно на 3.5 г/л (0.22 ммоль/л) в неделю. При достижении целевого НЬ >110 г/л (6.83 ммоль/л) пациентов, получающих терапию препаратом Мирцера® 1 раз в 2 недели, можно перевести на режим введения препарата 1 раз в месяц в дозе, превышающей предыдущую в два раза. Коррекцию дозы препарата проводят не чаще 1 раза в месяц.
Пациенты, получающие стимулятор эритропоэза в настоящее время Пациентов, получающих другой стимулятор эритропоэза, можно перевести на терапию препаратом Мирцера® с режимом введения 1 раз в месяц или 1 раз в 2 недели п/к или в/в. Начальная доза: зависит от недельной дозы ранее вводимого препарата — дарбэпоэтина альфа или эпоэтина (альфа или бета) (см. Таблицы 1 и 2). Первую инъекцию препарата Мирцера® проводят в день следующей запланированной инъекции ранее применявшегося дарбэпоэтина альфа или эпоэтина (альфа или бета).
Если для поддержания целевого НЬ выше 110 г/л (6.83 ммоль/л) требуется коррекция дозы, то месячную дозу можно изменить на 25%.
Дозу препарата Мирцера® уменьшают на 25-50% от предыдущей, если спустя месяц увеличение НЬ составляет более 20 г/л (1.24 ммоль/л). Если НЬ превышает 130 г/л (8.07 ммоль/л), то терапию необходимо прервать до снижения НЬ до уровня менее 130 г/л (8.07 ммоль/л) и затем возобновить, в дозе 50% от предыдущей.
При целевом НЬ 120 г/л доза препарата изменяется на 25%.
После прекращения терапии НЬ снижается примерно на 3.5 г/л (0.22 ммоль/л) в неделю. Коррекцию дозы препарата проводят не чаще 1 раза в месяц.
Перерыв в лечении
Лечение анемии, в том числе и терапия препаратом Мирцера®, обычно бывает долговременным. Но при необходимости терапия препаратом Мирцера® может быть прервана в любой момент.
Пропущенная доза
Пропущенную однократную инъекцию препарата Мирцера® необходимо ввести как можно скорее и далее вводить препарат с предписанной частотой дозирования.
Дозирование в особых случаях
Печеночная недостаточность: не требуется коррекции начальной дозы препарата и режима дозирования у пациентов с печеночной недостаточностью любой степени тяжести (см. раздел «Фармакологическое действие», подраздел «Фармакокинетика у специальных групп пациентов»).
Пожилой возраст (65 лет и старше): не требуется коррекции начальной дозы препарата (см. раздел «Фармакологическое действие», подраздел «Фармакокинетика у специальных групп пациентов).
Дети: применение препарата Мирцера® у детей до 18 лет не рекомендуется, в связи с недостаточными данными по безопасности и эффективности препарата у данной категории пациентов.
При применении препарата Мирцера® возникновение нежелательных реакций возможно примерно у 6% пациентов. Наиболее частой из них является повышение артериального давления (часто).
Для описания частоты нежелательных реакций используются следующие категории: часто (>1/100 и <1/10), нечасто (>1/1000 и <1/100) и редко (>1/10000 и <1/1000).
Все другие нежелательные реакции, связанные с терапией препаратом Мирцера®, сообщались редко и в большинстве случаев были легкой или средней степени тяжести. Данные нежелательные реакции могут быть обусловлены сопутствующими заболеваниями. Изменения лабораторных показателей
В клинических исследованиях в ходе терапии препаратом Мирцера® наблюдалось незначительное снижение числа тромбоцитов в пределах нормальных значений.
У 7.5% пациентов, получавших терапию препаратом Мирцера®, и у 4.4% пациентов, получавших терапию другими стимуляторами эритропоэза, наблюдалась тромбоцитопения (количество тромбоцитов <100 х 109/л).
Постмаркетинговые наблюдения
При применении препарата Мирцера® сообщалось о парциальной красноклеточной аплазии (ПККА), вызванной образованием нейтрализующих антител к эритропоэтину (см. раздел «Особые указания»), В остальном профиль безопасности препарата соответствовал нежелательным реакциям, зарегистрированным при применении препарата Мирцера® в клинических исследованиях (см. раздел «Особые указания» и раздел «Фармакологическое действие», подраздел «Клиническая эффективность»).
Препарат Мирцера® обладает широким терапевтическим диапазоном, при инициации терапии следует принимать во внимание индивидуальный ответ на терапию. Возможен чрезмерный фармакодинамический ответ, т.е. чрезмерный эритропоэз. При высоком уровне НЬ необходимо временно прервать терапию препаратом Мирцера® (см. раздел «Способ применения и дозы»). При необходимости может быть проведена флеботомия.
Исследований по изучению взаимодействия с другими лекарственными средствами не проводились. Полученные до настоящего времени данные не выявили каких-либо взаимодействий препарата Мирцера® с другими препаратами, а также признаков влияния других препаратов на фармакокинетику и фармакодинамику препарата Мирцера®. Не следует смешивать метоксиполиэтиленгликоль-эпоэтин бета с другими лекарственными средствами или инъекционными растворами.
До начала и во время лечения препаратом Мирцера® необходимо исключить дефицит железа.
Дополнительная терапия железом рекомендуется, если содержание ферритина в сыворотке крови ниже 100 мкг/л или насыщение трансферрина железом ниже 20%.
Отсутствие эффекта: наиболее частыми причинами неполного ответа на лечение средствами, стимулирующими эритропоэз, являются дефицит железа, воспаление, а также хроническая кровопотеря, фиброз костного мозга, резкое увеличение концентрации алюминия, обусловленное гемодиализом, дефицит фолиевой кислоты или витамина В12, гемолиз. Если все перечисленные состояния исключены и у больного наблюдается внезапное снижение НЬ, ретикулоцитопения и обнаруживаются антитела к эритропоэтину, необходимо провести исследование костного мозга для исключения ПККА. При развитии ПККА терапию препаратом Мирцера® необходимо прекратить и пациентов не следует переводить на терапию другими стимуляторами эритропоэза.
На фоне терапии стимуляторами эритропоэза, в том числе при применении препарата Мирцера , сообщалось о случаях развития ПККА, вызванной антителами к эритропоэтину. Антитела обладают перекрестной реакцией со всеми стимуляторами эритропоэза. Не следует переводить на терапию препаратом Мирцера® пациентов с подтвержденными антителами к эритропоэтину или подозрением на их наличие.
Повышение артериального давления: до начала и во время лечения препаратом Мирцера®, как и другими стимуляторами эритропоэза, необходимо контролировать артериальное давление. Если артериальное давление не удается контролировать медикаментозно, необходимо снизить дозу или приостановить терапию препаратом Мирцера® (см. раздел «Способ применения и дозы»).
Эффект на опухолевый рост: препарат Мирцера®, как и другие лекарственные средства, стимулирующие эритропоэз, является фактором роста, который в основном стимулирует образование эритроцитов. Эритропоэтиновые рецепторы могут присутствовать на поверхности различных опухолевых клеток. Возможно, что средства, стимулирующие эритропо- эз (как и другие факторы роста), могут стимулировать рост злокачественного образования любого типа.
При применении эпоэтинов у пациентов с различными злокачественными опухолями, в том числе головы и шеи, молочной железы, наблюдалось увеличение летальности, причины которой неясны.
Следует проявлять осторожность при применении препарата Мирцера® у пациентов с гемоглобинопатиями, эпилепсией, тромбоцитозом (число тромбоцитов более 500 х 109/л), поскольку безопасность и эффективность препарата для данных групп не изучены. Попадание лекарственных препаратов в окружающую среду должно быть сведено к минимуму. Не следует утилизировать препарат с помощью сточных вод или вместе с бытовыми отходами. По возможности необходимо использовать специальные системы для утилизации лекарственных препаратов.
Исследования по изучению влияния препарата на способность управлять транспортными средствами и заниматься другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций, не проводились. Исходя из механизма действия и профиля безопасности, препарат Мирцера® не обладает таким действием.
Раствор для подкожного и внутривенного введения, флаконы
По 50 мкг/1 мл, 100 мкг/1 мл, 200 мкг/1 мл, 300 мкг/1 мл, 400 мкг/1 мл, 600 мкг/1 мл, 1000 мкг/1 мл препарата во флаконы, изготовленные из бесцветного стекла (гидролитический класс 1 по ЕФ), укупоренные крышкой из бутилкаучука, обжатые алюминиевым колпачком и закрытые пластмассовой крышкой; цвет крышки соответствует цвету, которым выделена дозировка препарата на этикетке флакона и на пачке.
Каждый флакон вместе с инструкцией по применению помещают в картонную пачку; на пачке имеется контроль вскрытия упаковки с указанием места вскрытия.
Раствор для подкожного и внутривенного введения, шприц-тюбики
По 30 мкг/0.3 мя, 40 мкг/0.3 мл, 50 мкг/0.3 мл, 60 мкг/0.3 мл, 75 мкг/0.3 мл, 100 мкг/0.3 мл, 120 мкг/0.3 мл, 150 мкг/0.3 мл, 200 мкг/0.3 мл, 250 мкг/0.3 мл, 360 мкг/0.6 мл, 400 мкг/0.6 мл, 600 мкг/0.6 мл, 800 мкг/0.6 мл в шприц-тюбики, корпус которых изготовлен из стекла (гидролитический класс 1 по ЕФ), поршень — из пластмассы, с пробкой из бутилкаучука, ламинированного фторполимером. Цвет поршня соответствует цвету, которым выделена дозировка препарата на этикетке шприц-тюбика и на пачке. На круглой рукоятке поршня имеется логотип <^Д>. С другой стороны шприц-тюбики укупорены наконечником из бутилкаучука, ламинированного фторполимером.
Шприц-тюбик помещен в прозрачный защитный пластмассовый контейнер с пружиной.
1 стерильная игла для инъекций помещена в герметично укупоренный пластмассовый контейнер с контролем вскрытия.
1 шприц-тюбик вместе с контейнером с иглой для инъекций помещен в прозрачную контурную ячейковую упаковку, герметично укупоренную. Контурная ячейковая упаковка вместе с инструкцией по применению помещена в картонную пачку.
Хранить при температуре 2-8°С в защищенном от света месте. Не замораживать.
Хранить в недоступном для детей месте.
Флаконы — 1 год.
Шприц-тюбики — 3 года.
Не использовать по истечении срока годности, указанного на упаковке.