Описание препарата Номидес® (капсулы, 30 мг) основано на официальной инструкции, утверждено компанией-производителем в 2017 году
Дата согласования: 18.04.2017
Содержание
- Фотографии упаковок
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Заказ в аптеках Москвы
- Отзывы
Фотографии упаковок
18.04.2017

18.04.2017

18.04.2017
Действующее вещество
ATX
Фармакологическая группа
Состав
| Капсулы | 1 капс. |
| активное вещество: | |
| осельтамивира фосфат | 39,4/59,1/98,5 мг |
| соответствует осельтамивиру 30/45/75 мг | |
| вспомогательные вещества: кремния диоксид коллоидный (аэросил) — 6/9/15 мг; коповидон — 3,6/5,4/9 мг; крахмал прежелатинизированный — 65,6/98,4/164 мг; кроскармеллоза натрия — 1,84/2,76/4,6 мг; натрия стеарилфумарат — 0,92/1,38/2,3 мг; тальк — 2,64/3,96/6,6 мг | |
| твердые желатиновые капсулы | |
| дозировка 30 мг, корпус капсулы: вода очищенная — 14–15 мг; натрия лаурилсульфат — 0,12 мг; титана диоксид — 2,05 мг; желатин — до 100 мг; крышечка капсулы: вода очищенная — 14–15 мг; натрия лаурилсульфат — 0,12 мг; титана диоксид — 2,05 мг; желатин — до 100 мг | |
| для дозировки 45 мг: корпус капсулы: вода очищенная — 14–15 мг; натрия лаурилсульфат — 0,08 мг; титана диоксид — 0,97524 мг; краситель бриллиантовый голубой — 0,2626 мг; желатин — до 100 мг; крышечка капсулы: вода очищенная — 14–15 мг; натрия лаурилсульфат — 0,08 мг; титана диоксид — 0,97524 мг; краситель бриллиантовый голубой — 0,2626 мг; желатин — до 100 мг | |
| для дозировки 75 мг: корпус капсулы: вода очищенная — 14–15 мг; натрия лаурилсульфат — 0,12 мг; титана диоксид — 1,50038 мг; желатин — до 100 мг; крышечка капсулы: вода очищенная — 14–15 мг; натрия лаурилсульфат — 0,12 мг; титана диоксид — 1,50038 мг; краситель «Солнечный закат» желтый (Е110) — 1,2753 мг; краситель пунцовый Понсо 4R (Е124) — 0,2401 мг; желатин — до 100 мг |
Описание лекарственной формы
Капсулы, 30 мг: твердые, желатиновые №3, корпус белого цвета, крышечка белого цвета.
Капсулы, 45 мг: твердые желатиновые №2, корпус голубого цвета, крышечка голубого цвета.
Капсулы, 75 мг: твердые, желатиновые, корпус белого цвета, крышечка оранжевого цвета.
Содержимое капсул: белый или белый с желтоватым оттенком порошок.
Фармакологическое действие
Фармакологическое действие
—
противовирусное.
Фармакодинамика
Противовирусный препарат — осельтамивира фосфат — является пролекарством, его активный метаболит (осельтамивира карбоксилат, ОК) — эффективный и селективный ингибитор нейраминидазы вирусов гриппа типа А и В — фермента, катализирующего процесс высвобождения вновь образованных вирусных частиц из инфицированных клеток, их проникновение в клетки эпителия дыхательных путей и дальнейшего распространения вируса в организме. Тормозит рост вируса гриппа in vitro и подавляет репликацию вируса и его патогенность in vivo, уменьшает выделение вирусов гриппа А и В из организма. Исследования клинических изолятов вируса гриппа показали, что IC50 ОК составляет 0,1–1,3 нМ для вируса гриппа А и 2,6 нМ для вируса гриппа В. Согласно данным опубликованных исследований, медиана значений IC50 для вируса гриппа В несколько выше и составляет 8,5 нМ.
Резистентность
Клинические исследования. Риск появления вирусов гриппа со сниженной чувствительностью или резистентностью к препарату изучался в клинических исследованиях. У всех пациентов-носителей ОК-резистентного вируса носительство имело временный характер, не влияло на элиминацию вируса и не вызывало ухудшения клинического состояния.
|
Популяция пациентов |
Пациенты с мутациями, приводящими к резистентности |
|
|
Фенотипирование* |
Гено- и фенотипирование* |
|
| Взрослые и подростки | 4/1245 (0,32%) | 5/1245 (0,4%) |
| Дети (1–12 лет) | 19/464 (4,1%) | 25/464 (5,4%) |
*Полное генотипирование не было проведено ни в одном из исследований.
При приеме осельтамивира с целью постконтактной профилактики (7 дней), профилактики контактировавших в семье (10 дней) и сезонной профилактики (42 дня) у лиц с нормальной функцией иммунной системы случаев резистентности к препарату не отмечено. В 12-недельном исследовании по сезонной профилактике у лиц с ослабленным иммунитетом случаев возникновения резистентности также не наблюдалось.
Данные отдельных клинических случаев и наблюдательных исследований
У пациентов, не получавших осельтамивир, обнаружены возникающие в природных условиях мутации вирусов гриппа А и В, которые обладали сниженной чувствительностью к осельтамивиру. В 2008 году мутация по типу замены H275Y, приводящая к резистентности, была обнаружена более чем у 99% штаммов вируса 2008 H1N1, циркулирующих в Европе. Вирус гриппа 2009 H1N1 в большинстве случаев был чувствителен к осельтамивиру. Устойчивые к осельтамивиру штаммы обнаружены у лиц с нормальной функцией иммунной системы и лиц с ослабленным иммунитетом, принимавших осельтамивир. Степень снижения чувствительности к осельтамивиру и частота встречаемости подобных вирусов может отличаться в зависимости от сезона и региона. Устойчивость к осельтамивиру обнаружена у пациентов с пандемическим гриппом H1N1, получавших препарат как для лечения, так и для профилактики.
Частота встречаемости резистентности может быть выше у более молодых пациентов и пациентов с ослабленным иммунитетом. Устойчивые к осельтамивиру лабораторные штаммы вирусов гриппа и вирусы гриппа от пациентов, получавших терапию осельтамивиром, несут мутации нейраминидазы N1 и N2. Мутации, приводящие к устойчивости, часто являются специфическими для подтипа нейраминидазы.
При принятии решения о применении осельтамивира следует учитывать сезонную чувствительность вируса гриппа к препарату (последнюю информацию можно найти на сайте ВОЗ).
Доклинические данные
Доклинические данные, полученные на основании стандартных исследований по изучению фармакологической безопасности, генотоксичности и хронической токсичности, не выявили особой опасности для человека.
Канцерогенность: результаты 3 исследований по выявлению канцерогенного потенциала (2-летних исследований на крысах и мышах для осельтамивира и одного 6-месячного исследования на трансгенных мышах Tg:AC для активного метаболита) были отрицательными.
Мутагенность: стандартные генотоксические тесты для осельтамивира и активного метаболита были отрицательными.
Влияние на фертильность: осельтамивир в дозе 1500 мг/кг/сут не влиял на репродуктивную функцию самцов и самок крыс.
Тератогенность: в исследованиях по изучению тератогенности осельтамивира в дозе до 1500 мг/кг/сут (на крысах) и до 500 мг/кг/сут (на кроликах) влияние на эмбриональное развитие не обнаружено. В исследованиях по изучению антенатального и постнатального периодов развития у крыс при введении осельтамивира в дозе 1500 мг/кг/сут наблюдалось увеличение периода родов: предел безопасности между экспозицией у человека и максимальной, не оказывающей эффекта, дозой у крыс (500 мг/кг/сут) для осельтамивира выше в 480 раз, а для его активного метаболита — в 44 раза. Экспозиция у плода составляла 15–20% от таковой у матери.
Прочее: осельтамивир и активный метаболит проникают в молоко лактирующих крыс. Согласно ограниченным данным, осельтамивир и его активный метаболит проникают в грудное молоко человека. По результатам экстраполяции данных, полученных в исследованиях у животных, их количество в грудном молоке может составлять 0,01 и 0,3 мг/сут соответственно.
Примерно у 50% протестированных морских свинок при введении максимальных доз активной субстанции осельтамивира наблюдалась сенсибилизация кожи в виде эритемы. Также выявлено обратимое раздражение глаз у кроликов.
В то время как очень высокие пероральные однократные дозы (657 мг/кг и выше) осельтамивира фосфата не оказывали влияние на взрослых крыс, данные дозы оказывали токсическое действие на незрелых 7-дневных детенышей крыс, в т.ч. приводили к гибели животных. Нежелательных эффектов не наблюдалось при хроническом введении в дозе 500 мг/кг/сут с 7-го по 21-й день постнатального периода.
Фармакокинетика
Абсорбция. Осельтамивира фосфат легко всасывается в ЖКТ и в высокой степени превращается в активный метаболит под действием печеночных и кишечных эстераз.
Концентрация активного метаболита в плазме определяется в пределах 30 мин, Tmax — 2–3 ч и более чем в 20 раз превышают концентрацию пролекарства. Не менее 75% принятой внутрь дозы попадает в системный кровоток в виде активного метаболита, менее 5% — в виде исходного препарата. Плазменные концентрации как пролекарства, так и активного метаболита пропорциональны дозе и не зависят от приема пищи.
Распределение. Vd активного метаболита — 23 л.
По данным исследований, проведенных на животных, после приема внутрь осельтамивира фосфата его активный метаболит обнаруживался во всех основных очагах инфекции (легких, промывных водах бронхов, слизистой оболочки полости носа, среднем ухе и трахее) в концентрациях, обеспечивающих противовирусный эффект.
Связь активного метаболита с белками плазмы — 3%. Связь пролекарства с белками плазмы 42%, что недостаточно, чтобы служить причиной существенных лекарственных взаимодействий.
Метаболизм. Осельтамивира фосфат в высокой степени превращается в активный метаболит под действием эстераз, находящихся преимущественно в печени. Ни осельтамивира фосфат, ни активный метаболит не являются субстратами или ингибиторами изоферментов системы цитохрома P450.
Выведение. Выводится (>90%) в виде активного метаболита преимущественно почками. Активный метаболит не подвергается дальнейшей трансформации и выводится почками (>99%) путем КФ и канальцевой секреции. Почечный клиренс (18,8 л/ч) превышает СКФ (7,5 л/ч), что указывает на то, что препарат выводится еще и путем канальцевой секреции. Через кишечник выводится менее 20% принятого препарата. T1/2 активного метаболита 6–10 ч.
Фармакокинетика в особых группах пациентов
Пациенты с поражением почек. При применении осельтамивира (100 мг 2 раза в сутки в течение 5 дней) у больных с различной степенью поражения почек величина AUC осельтамивира карбоксилата обратно пропорциональна снижению функции почек.
Фармакокинетика осельтамивира у пациентов с терминальной стадией почечной недостаточности (Cl креатинина ≤10 мл/мин), не находящихся на диализе, не изучалась. В связи с этим рекомендации по дозированию у данной группы пациентов отсутствуют.
Пациенты с поражением печени. Полученные in vitro и в исследованиях на животных данные об отсутствии значительного повышения AUC осельтамивира фосфата при нарушении функции печени легкой и средней степени тяжести были подтверждены и в клинических исследованиях. Безопасность и фармакокинетика осельтамивира фосфата у пациентов с тяжелым нарушением функции печени не изучалась.
Пациенты пожилого и старческого возраста. У пациентов пожилого и старческого возраста (65–78 лет) экспозиция метаболита в равновесном состоянии на 25–35% выше, чем у более молодых пациентов при назначении аналогичных доз осельтамивира. T1/2 препарата у больных пожилого и старческого возраста существенно не отличался от такового у более молодых пациентов. С учетом данных по экспозиции препарата и его переносимости пациентами пожилого и старческого возраста, коррекция дозы при лечении и профилактике гриппа не требуется.
Дети. У детей младшего возраста выведение пролекарства и активного метаболита происходит быстрее, чем у взрослых, что приводит к более низким AUC по отношению к конкретной дозе. Прием препарата в дозе 2 мг/кг обеспечивает такую же AUC осельтамивира карбоксилата, какая достигается у взрослых после однократного приема капсулы с 75 мг препарата (что эквивалентно примерно 1 мг/кг). Фармакокинетика осельтамивира у детей старше 12 лет такая же, как у взрослых.
Показания
лечение гриппа у взрослых и детей в возрасте старше 3 лет;
профилактика гриппа у взрослых и подростков в возрасте старше 12 лет, находящихся в группах повышенного риска инфицирования вирусом (в больших коллективах, у ослабленных пациентов);
профилактика гриппа у детей старше 3 лет.
Противопоказания
повышенная чувствительность к осельтамивира фосфату или любому компоненту препарата;
терминальная стадия почечной недостаточности (Cl креатинина ≤10 мл/мин);
тяжелая печеночная недостаточность;
детский возраст до 3 лет.
С осторожностью: беременность; период грудного вскармливания.
Применение при беременности и кормлении грудью
Контролируемых исследований у беременных женщин не проводилось. Однако результаты постмаркетинговых и наблюдательных исследований продемонстрировали пользу предлагаемого стандартного режима дозирования для данной популяции пациентов. Результаты фармакокинетического анализа показали более низкую экспозицию активного метаболита (приблизительно на 30% в течение всех триместров беременности) у беременных женщин по сравнению с небеременными. Тем не менее значение расчетной экспозиции остается выше ингибирующих концентраций (значение IC95) и терапевтических значений для многих штаммов вируса гриппа. Изменение режима дозирования у беременных женщин при проведении терапии или профилактики не рекомендуется. Не обнаружено прямого или опосредованного неблагоприятного влияния препарата на беременность, эмбриофетальное или постнатальное развитие (см. «Фармакодинамика», Доклинические данные). При назначении осельтамивира беременным женщинам следует учитывать как данные по безопасности, так и течение беременности и патогенность циркулирующего штамма вируса гриппа.
Во время доклинических исследований осельтамивир и активный метаболит проникали в молоко лактирующих крыс. Данные по экскреции осельтамивира с грудным молоком у человека и применению осельтамивира кормящими женщинами ограничены. Осельтамивир и его активный метаболит в небольших количествах проникают в грудное молоко (см. «Фармакодинамика», Доклинические данные), создавая субтерапевтические концентрации в крови грудного ребенка. При назначении осельтамивира кормящим женщинам следует также учитывать сопутствующее заболевание и патогенность циркулирующего штамма вируса гриппа.
При беременности и в период грудного вскармливания осельтамивир применяют только в случае, если предполагаемая польза для матери превышает потенциальный риск для плода и ребенка.
Способ применения и дозы
Внутрь, независимо от приема пищи или во время еды.
Лечение
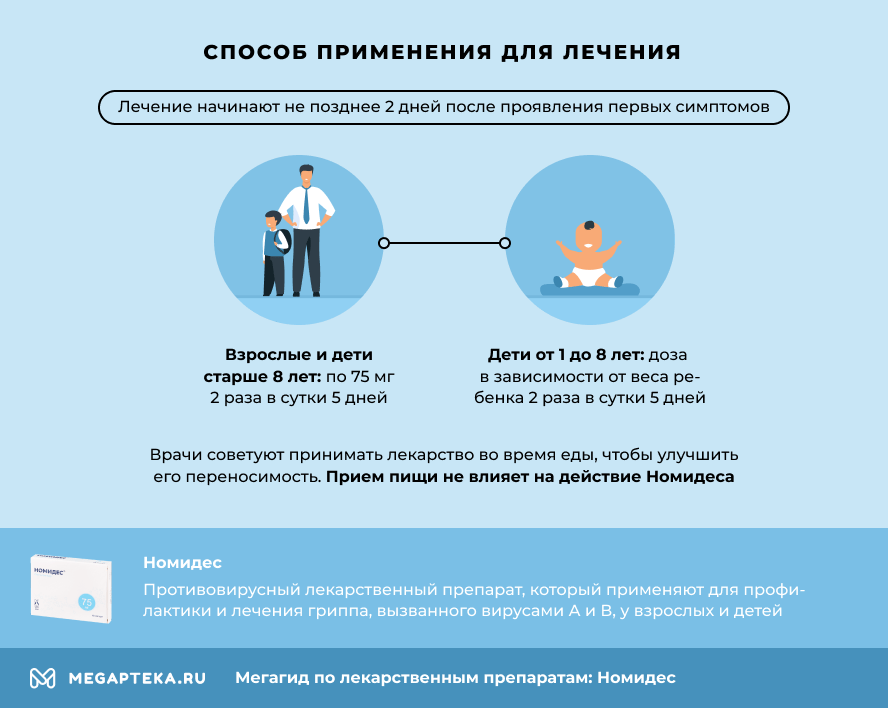
Прием препарата необходимо начинать не позднее 2 сут с момента развития симптомов заболевания.
Взрослые и подростки ≥12 лет. Рекомендуемая суточная доза составляет 150 мг. Препарат назначают в дозе 75 мг (1 капс. 75 мг или 1 капс. 30 мг + 1 капс. 45 мг) 2 раза в сутки внутрь в течение 5 дней.
Дети с массой тела более 40 кг или ≥8 лет. Дети, которые умеют проглатывать капсулы, также могут получать лечение, принимая по 75 мг (1 капс. 75 мг или 1 капс. 30 мг + 1 капс. 45 мг) 2 раза в сутки в течение 5 дней.
Дети ≥3 лет. Рекомендованный режим дозирования осельтамивира в капсулах 30 и 45 мг (в течение 5 дней): у пациентов с массой тела ≤15 кг доза составляет 30 мг 2 раза в сутки; >15–23 кг — 45 мг 2 раза в сутки; >23–40 кг — 60 мг 2 раза в сутки.
Профилактика
Прием препарата необходимо начинать не позднее 2 сут после контакта с больными.
Взрослые и подростки ≥12 лет. По 75 мг (1 капс. 75 мг или 1 капс. 30 мг + 1 капс. 45 мг) 1 раз в сутки внутрь в течение не менее 10 дней после контакта с больным. Во время сезонной эпидемии гриппа — по 75 мг 1 раз в сутки в течение 6 нед. Профилактическое действие продолжается столько, сколько длится прием препарата.
Дети с массой тела более 40 кг или ≥8 лет. Дети, которые могут проглатывать капсулы, также могут получать профилактическую терапию, принимая по 75 мг (1 капс. 75 мг или 1 капс. 30 мг + 1 капс. 45 мг) 1 раз в сутки в течение 10 дней.
Дети ≥3 лет. Рекомендованный режим дозирования осельтамивира в капсулах 30 и 45 мг (в течение 10 дней): у пациентов с массой тела ≤15 кг доза составляет 30 мг 1 раз в сутки; >15–23 кг — 45 мг 1 раз в сутки; >23–40 кг — 60 мг 1 раза в сутки.
Дозирование в особых случаях
Пациенты с нарушением функции почек
Лечение. Больным с Cl креатинина более 60 мл/мин коррекция дозы не требуется. У больных с Cl креатинина от 30 до 60 мл/мин дозу осельтамивира следует уменьшить до 30 мг 2 раза в сутки в течение 5 дней; от 10 до 30 мл/мин дозу осельтамивира следует уменьшить до 30 мг 1 раз в сутки в течение 5 дней; пациентам, находящимся на постоянном гемодиализе, осельтамивир в первоначальной дозе 30 мг можно принять до начала диализа, если симптомы гриппа появились в течение 48 ч между сеансами диализа. Для поддержания плазменной концентрации на терапевтическом уровне осельтамивир следует принимать по 30 мг после каждого сеанса диализа. Пациентам, находящимся на перитонеальном диализе, осельтамивир следует принимать в первоначальной дозе 30 мг до начала проведения диализа, затем по 30 мг каждые 5 дней.
Фармакокинетика осельтамивира у пациентов с терминальной стадией ХПН (с Cl креатинина ≤10 мл/мин), не находящихся на диализе, не изучалась. В связи с этим рекомендации по дозированию у данной группы пациентов отсутствуют.
Профилактика. Больным с Cl креатинина более 60 мл/мин коррекция дозы не требуется. У больных с Cl креатинина от 30 до 60 мл/мин дозу осельтамивира следует уменьшить до 30 мг 1 раз в сутки. У больных с Cl креатинина от 10 до 30 мл/мин рекомендуется уменьшить дозу осельтамивира до 30 мг через день. Пациентам, находящимся на постоянном гемодиализе, осельтамивир в первоначальной дозе 30 мг можно принимать до начала диализа. Для поддержания плазменной концентрации на терапевтическом уровне осельтамивир следует принимать по 30 мг после каждого последующего нечетного сеанса диализа. Пациентам, находящимся на перитонеальном диализе, осельтамивир следует принимать в первоначальной дозе 30 мг до начала проведения диализа, затем — по 30 мг каждые 7 дней.
Фармакокинетика осельтамивира у пациентов с терминальной стадией ХПН (с Cl креатинина ≤10 мл/мин), не находящихся на диализе, не изучалась. В связи с этим рекомендации по дозированию у данной группы пациентов отсутствуют.
Пациенты с нарушением функции печени
Коррекция дозы при лечении и профилактике гриппа у пациентов с нарушением функции печени легкой и средней степени тяжести не требуется. Безопасность и фармакокинетика осельтамивира у пациентов с тяжелыми нарушениями функции печени не изучалась.
Пациенты пожилого и старческого возраста
Коррекция дозы для профилактики или лечения гриппа не требуется.
Пациенты с ослабленным иммунитетом (после трансплантации)
Для сезонной профилактики гриппа у пациентов с ослабленным иммунитетом в возрасте ≥3 лет — в течение 12 нед, коррекция дозы не требуется.
Побочные действия
В исследованиях по лечению гриппа у взрослых/пациентов подросткового возраста самыми частыми нежелательными реакциями (НР) были тошнота, рвота и головная боль. Большинство НР возникали в 1-й или 2-й день лечения и проходили самостоятельно в течение 1–2 дней. В исследованиях по профилактике гриппа у взрослых и подростков самыми частыми НР были тошнота, рвота, головная боль и боль. У детей наиболее часто встречалась рвота. Описанные НР в большинстве случаев не требовали отмены препарата.
Лечение и профилактика гриппа у взрослых и подростков
В таблице 1 представлены НР, возникавшие наиболее часто (?1%) при приеме рекомендованной дозы осельтамивира в исследованиях по профилактике и лечению гриппа у взрослых и подростков (75 мг 2 раза в сутки в течение 5 дней — для лечения и 75 мг 1 раз в сутки до 6 нед — для профилактики), и частота которых как минимум на 1% выше по сравнению с плацебо. В исследования по лечению гриппа вошли взрослые/подростки без сопутствующей патологии и больные группы риска, т.е. пациенты с высоким риском развития осложнений гриппа (пациенты пожилого и старческого возраста, пациенты с хроническими заболеваниями сердца или органов дыхания). В целом профиль безопасности у пациентов группы риска соответствовал таковому у взрослых/пациентов подросткового возраста без сопутствующей патологии.
В исследованиях по профилактике гриппа профиль безопасности у пациентов, получавших рекомендованную дозу препарата (75 мг 1 раз в сутки до 6 нед), не отличался от такового в исследованиях по лечению гриппа, несмотря на более длительный прием препарата.
Таблица 1
Процент взрослых/подростков с НР, возникавшими с частотой ?1% в группе осельтамивира в исследованиях по лечению и профилактике гриппозной инфекции (различие с плацебо ?1%)
| Системно-органный класс/НР | Лечение | Профилактика | Категория частотыа | ||
| Осельтамивир (75 мг 2 раза/сут) n=2647, % | Плацебо n=1977, % | Осельтамивир (75 мг 1 раз/сут) n=1945, % | Плацебо n=1588, % | ||
| Со стороны ЖКТ | |||||
| Тошнота | 0 | 6 | 8 | 4 | очень часто |
| Рвота | 8 | 3 | 2 | 1 | часто |
| Со стороны нервной системы | |||||
| Головная боль | 2 | 1 | 17 | 16 | очень часто |
| Общие расстройства | |||||
| Боль | <1 | <1 | 4 | 3 | часто |
а Категория частоты представлена только для группы осельтамивира. Для оценки частоты НР использованы следующие категории частоты: очень часто (?1/10); часто (?1/100, <1/10).
Далее представлены НР, которые возникали с частотой ?1% у взрослых и подростков, получавших осельтамивир в качестве терапии и профилактики гриппозной инфекции. Данные нежелательные явления либо более часто наблюдались у пациентов, получавших плацебо, либо различия в частоте между группами осельтамивира и плацебо составили менее 1%.
Со стороны ЖКТ (осельтамивир против плацебо): лечение — диарея (6 против 7%), боль в животе (включая боль в верхней части живота, 2 против 3%); профилактика — диарея (3 против 4%), боль в верхней части живота (2 против 2%), диспепсия (1 против 1%).
Инфекции и инвазии (осельтамивир против плацебо): лечение — бронхит (3 против 4%), синусит (1 против 1%), простой герпес (1 против 1%); профилактика — назофарингит (4 против 4%), инфекции верхних дыхательных путей (3 против 3%), гриппозная инфекция (2% против 3%).
Общие расстройства (осельтамивир против плацебо): лечение — головокружение (включая вертиго, 2 против 3%); профилактика — усталость (7 против 7%), пирексия (2 против 2%), гриппоподобное заболевание (1 против 2%), головокружение (1 против 1%), боль в конечности (1 против 1%).
Со стороны нервной системы (осельтамивир против плацебо): лечение — бессонница (1 против 1%); профилактика — бессонница (1 против 1%).
Со стороны дыхательной системы, органов грудной клетки и средостения (осельтамивир против плацебо): лечение — кашель (2 против 2%), заложенность носа (1 против 1%); профилактика — заложенность носа (7 против 7%), ангина (5 против 5%), кашель (5 против 6%), ринорея (1 против 1%).
Со стороны скелетно-мышечной системы и соединительной ткани (осельтамивир против плацебо): профилактика — боль в спине (2 против 3%), артралгия (1 против 2%), миалгия (1 против 1%).
Со стороны половых органов и молочной железы (осельтамивир против плацебо): профилактика — дисменорея (3 против 3%).
Лечение и профилактика гриппозной инфекции лиц пожилого и старческого возраста
Профиль безопасности у 942 пациентов пожилого и старческого возраста, получавших осельтамивир или плацебо, клинически не отличался от такового у лиц более молодого возраста (до 65 лет).
Профилактика гриппозной инфекции у пациентов с ослабленным иммунитетом
В 12-недельном исследовании по профилактике гриппа с участием 475 пациентов с ослабленным иммунитетом (включая 18 детей в возрасте от 1 года до 12 лет), у пациентов, принимавших осельтамивир (n=238), профиль безопасности соответствовал описанному ранее в исследованиях по профилактике гриппа.
Лечение и профилактика гриппозной инфекции у детей без сопутствующих заболеваний в возрасте 1–12 лет и пациентов с бронхиальной астмой
В исследованиях по лечению естественной гриппозной инфекции у детей в возрасте от 1 года до 12 лет НР при применении осельтамивира (n=858), отмеченной с частотой ?1% и как минимум на 1% чаще по сравнению с плацебо (n=622), была рвота. У детей, получавших рекомендованную дозу препарата 1 раз в сутки в качестве постконтактной профилактики в домашних условиях, наиболее часто встречалась рвота (8% в группе осельтамивира против 2% в группе пациентов, не получавших профилактическое лечение). Осельтамивир хорошо переносился, зарегистрированные нежелательные явления соответствовали описанным ранее при проведении лечения гриппа у детей.
Далее представлены НР, отмеченные у детей с частотой ?1% в исследованиях по лечению гриппа (n=858) или с частотой ?5% в исследованиях по профилактике гриппа (n=148). Данные нежелательные явления более часто наблюдались в группе плацебо/отсутствие профилактики, различия между группами осельтамивира и плацебо/отсутствие профилактики составили менее 1%.
Cо стороны ЖКТ (осельтамивир против плацебо): лечение — диарея (9 против 9%), тошнота (4 против 4%), боль в животе (включая боль в верхней части живота, 3 против 3%).
Инфекции и инвазии (осельтамивир против плацебо): лечение — средний отит (5 против 8%), бронхит (2 против 3%), пневмония (1 против 3%), синусит (1 против 2%).
Со стороны дыхательной системы, органов грудной клетки и средостения (осельтамивир против плацебо): лечение — астма (включая обострение, 3 против 4%), носовое кровотечение (2 против 2%); профилактика — кашель (12 против 26%), заложенность носа (11 против 20%).
Со стороны кожи и подкожных тканей (осельтамивир против плацебо): лечение — дерматит (включая аллергический и атопический дерматит, 1 против 2%).
Со стороны органа слуха и лабиринтные нарушения (осельтамивир против плацебо): лечение — боль в ухе (1 против 1%).
Со стороны органа зрения (осельтамивир против плацебо): лечение — конъюнктивит (включая покраснение глаз, выделения из глаза и боль в глазах, 1 против <1%).
Дополнительные НР, отмеченные при проведении лечения гриппа у детей, не соответствовавшие описанным выше критериям
Со стороны крови и лимфатической системы (осельтамивир против плацебо): лечение — лимфоаденопатия (<1 против 1%).
Со стороны органа слуха и лабиринтные нарушения (осельтамивир против плацебо): лечение — повреждение барабанной перепонки (<1 против 1%).
Постмаркетинговое наблюдение
Далее представлены НР при применении осельтамивира, которые наблюдались в период постмаркетингового наблюдения. Частота развития данных НР и/или причинно-следственная связь с применением препарата не может быть установлена, т.к. неизвестен истинный размер популяции в виду добровольного характера сообщений.
Со стороны кожи и подкожных тканей: реакции гиперчувствительности — дерматит, кожная сыпь, экзема, крапивница, мультиформная экссудативная эритема, синдром Стивенса-Джонсона и токсический эпидермальный некролиз, аллергия, анафилактические и анафилактоидные реакции, отек Квинке.
Со стороны печени и желчевыводящих путей: гепатит, увеличение активности печеночных ферментов у пациентов с гриппоподобными симптомами, получавших осельтамивир; фульминантный гепатит (в т.ч. с фатальным исходом), печеночная недостаточность, желтуха.
Со стороны нервно-психической сферы: гриппозная инфекция может ассоциироваться с различными неврологическими симптомами и изменениями поведения, включая такие симптомы, как галлюцинации, бред и анормальное поведение. В некоторых случаях они могут привести к смертельному исходу. Такие явления могут возникать как на фоне развития энцефалопатии или энцефалита, так и без проявления данных заболеваний. У пациентов (в основном детей и подростков), принимавших осельтамивир с целью лечения гриппа, были зарегистрированы судороги и делирий (включая такие симптомы, как нарушение сознания, дезориентация во времени и пространстве, анормальное поведение, бред, галлюцинации, возбуждение, тревога, ночные кошмары). Эти случаи редко сопровождались опасными для жизни действиями. Роль осельтамивира в развитии этих явлений неизвестна. Подобные психоневрологические нарушения также отмечены у пациентов с гриппом, не получавших осельтамивир.
Со стороны ЖКТ: желудочно-кишечные кровотечения после приема осельтамивира (в частности, нельзя исключить связь между явлениями геморрагического колита и приемом осельтамивира, поскольку указанные явления исчезали как после выздоровления пациента от гриппа, так и после отмены препарата).
Со стороны органа зрения: нарушение зрения.
Со стороны сердца: аритмия.
Взаимодействие
Клинически значимые лекарственные взаимодействия маловероятны по данным фармакологических и фармакокинетических исследований. Осельтамивира фосфат в высокой степени превращается в активный метаболит под действием эстераз, в основном расположенных в печени. Лекарственные взаимодействия, обусловленные конкуренцией за связывание с активными центрами эстераз, в литературных источниках широко не представлены. Низкая степень связывания осельтамивира и активного метаболита с белками плазмы не дают оснований предполагать наличие взаимодействий, связанных с вытеснением ЛС из связи с белками.
Исследования in vitro показывают, что ни осельтамивира фосфат, ни его активный метаболит не являются предпочтительным субстратом для полифункциональных оксидаз системы цитохрома P450 или для глюкуронилтрансфераз. Оснований для взаимодействия с пероральными контрацептивами нет.
Циметидин, неспецифический ингибитор изофермента системы цитохрома P450 и конкурирующий в процессе канальцевой секреции с препаратами щелочного типа и катионами, не влияет на плазменные концентрации осельтамивира и его активного метаболита.
Маловероятны клинически значимые межлекарственные взаимодействия, связанные с конкуренцией за канальцевую секрецию, принимая во внимание резерв безопасности для большинства подобных препаратов, пути выведения активного метаболита осельтамивира (КФ и анионная канальцевая секреция), а также выводящую способность каждого из путей.
Пробенецид приводит к увеличению AUC активного метаболита осельтамивира примерно в 2 раза (за счет снижения активной канальцевой секреции в почках). Однако коррекция дозы при одновременном применении с пробенецидом не требуется, учитывая резерв безопасности активного метаболита.
Одновременный прием с амоксициллином не влияет на плазменные концентрации осельтамивира и его компонентов, демонстрируя слабую конкуренцию за выведение путем анионной канальцевой секреции.
Одновременный прием с парацетамолом не влияет на плазменные концентрации осельтамивира и его активного метаболита или парацетамола.
Фармакокинетических взаимодействий между осельтамивиром, его основным метаболитом, не обнаружено при одновременном приеме с парацетамолом, ацетилсалициловой кислотой, циметидином или антацидными средствами (магния и алюминия гидроксид, кальция карбонат), варфарином, римантадином или амантадином.
При использовании осальтемивира с часто применяемыми препаратами, такими как ингибиторы АПФ (эналаприл, каптоприл), тиазидные диуретики (бендрофлуметиазид), антибиотики (пенициллин, цефалоспорины, азитромицин, эритромицин и доксициклин), блокаторы Н2-гистаминовых рецепторов (ранитидин, циметидин), бета-адреноблокаторы (пропранолол), ксантины (теофиллин), симпатомиметики (псевдоэфедрин), опиаты (кодеин), ГКС, ингаляционные бронхолитики и ненаркотические анальгетики (ацетилсалициловая кислота, ибупрофен и парацетамол), изменений характера или частоты нежелательных явлений не наблюдалось.
Применять осельтамивир в комбинации с препаратами, имеющими узкую широту терапевтического действия (например хлорпропамид, метотрексат, бутадион), необходимо с осторожностью.
Передозировка
В большинстве случаев передозировка в ходе клинических исследований и при постмаркетинговом применении осельтамивира не сопровождалась какими-либо нежелательными явлениями. В остальных случаях симптомы передозировки соответствовали НР, представленным в разделе «Побочные действия».
Особые указания
Нарушения психики. У пациентов (в основном детей и подростков), принимавших осельтамивир с целью лечения гриппа, были зарегистрированы судороги и делирийподобные психоневрологические нарушения. Эти случаи редко сопровождались опасными для жизни действиями. Роль осельтамивира в развитии этих явлений неизвестна. Подобные психоневрологические нарушения также отмечены у пациентов с гриппом, не получавших осельтамивир. Риск развития психоневрологических нарушений у пациентов, получающих осельтамивир, не превышает таковой у пациентов с гриппом, не получающих противовирусные препараты.
Рекомендуется тщательное наблюдение за состоянием и поведением пациентов, особенно детей и подростков, с целью выявления признаков анормального поведения и оценки риска продолжения приема препарата при развитии данных явлений.
Данных по эффективности осельтамивира при любых заболеваниях, вызванных другими возбудителями, кроме вирусов гриппа A и B, нет.
Осельтамивир не является заменой вакцинации.
Профилактический прием препарата возможен по эпидемиологическим показаниям.
Рекомендации по коррекции дозы у больных с поражением почек представлены в подразделе «Дозирование в особых случаях» (см. также Фармакокинетика в особых группах пациентов).
Влияние на способность управлять транспортными средствами и механизмами. Исследования по изучению влияния препарата на способность управлять транспортными средствами и заниматься другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций, не проводились. Исходя из профиля безопасности, влияние осельтамивира на данные виды деятельности маловероятно.
Форма выпуска
Капсулы, 30 мг; 45 мг; 75 мг.
Первичная упаковка лекарственного препарата. По 5 или 10 капс. в контурной ячейковой упаковке из пленки ПВХ и фольги алюминиевой печатной лакированной. По 20, 30 капс. в банке полимерной с крышкой, натягиваемой с контролем первого вскрытия. Свободное пространство заполняют ватой медицинской. На банки наклеивают этикетки из бумаги этикеточной или писчей или из полимерных материалов, самоклеющиеся.
Вторичная упаковка лекарственного препарата. По 1 или 2 контурной ячейковой упаковке помещают в пачку из картона для потребительской тары. Пачки помещают в групповую упаковку. По 1 банке помещают в пачку из картона для потребительской тары. Пачки помещают в групповую упаковку.
Производитель
АО «Фармасинтез», Россия.
Юридический адрес: 664007, Россия, г. Иркутск, ул. Красногвардейская, 23, оф. 3.
Адрес производственной площадки; 664040, Россия, г. Иркутск, ул. Розы Люксембург, 184.
Тел.: (3952) 55-03-55; факс: (3952) 55-03-25.
Эксклюзивный дистрибьютор. ООО «Фармасинтез-Ритейл»
Юридический адрес: 664040, Россия, Иркутская обл., г. Иркутск, ул. Розы Люксембург, 184, оф. 448.
Тел.: (3952) 55-03-55; факс: (3952) 55-03-25.
Фактический адрес: 123100, Москва, Пресненская наб., 12, башня «Федерация», 42 эт.
Тел.: (495) 750-54-37.
www. http://nomides.ru
Претензии потребителей направлять по адресу: ООО «Фармасинтез-Ритейл».
Условия отпуска из аптек
По рецепту.
Условия хранения
В защищенном от света месте, при температуре не выше 25 °C.
Хранить в недоступном для детей месте.
Срок годности
5 лет.
Не применять по истечении срока годности, указанного на упаковке.
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Капсулы твердые желатиновые капсулы №3, корпус белого цвета, крышечка белого цвета; содержимое капсул — белый или белый с желтоватым оттенком порошок.
Вспомогательные вещества: кремния диоксид коллоидный (аэросил) — 6 мг, коповидон — 3.6 мг, крахмал прежелатинизированный — 65.6 мг, кроскармеллоза натрия — 1.84 мг, натрия стеарилфумарат — 0.92 мг, тальк — 2.64 мг.
Состав корпуса капсулы: титана диоксид — 2%, желатин — до 100%.
Состав крышечки капсулы: титана диоксид — 2%, желатин — до 100%.
5 шт. — упаковки контурные ячейковые (1) — пачки картонные.
5 шт. — упаковки контурные ячейковые (2) — пачки картонные.
10 шт. — упаковки контурные ячейковые (1) — пачки картонные.
10 шт. — упаковки контурные ячейковые (2) — пачки картонные.
20 шт. — банки полимерные (1) — пачки картонные.
30 шт. — банки полимерные (1) — пачки картонные.
Капсулы твердые желатиновые капсулы №2, корпус голубого цвета, крышечка голубого цвета; содержимое капсул — белый или белый с желтоватым оттенком порошок.
Вспомогательные вещества: кремния диоксид коллоидный (аэросил) — 9 мг, коповидон — 5.4 мг, крахмал прежелатинизированный — 98.4 мг, кроскармеллоза натрия — 2.76 мг, натрия стеарилфумарат — 1.38 мг, тальк — 3.96 мг.
Состав корпуса капсулы: краситель бриллиантовый голубой — 0.15%, титана диоксид — 1.8817%, желатин — до 100%.
Состав крышечки капсулы: краситель бриллиантовый голубой — 0.15%, титана диоксид — 1.8817%, желатин — до 100%.
5 шт. — упаковки контурные ячейковые (1) — пачки картонные.
5 шт. — упаковки контурные ячейковые (2) — пачки картонные.
10 шт. — упаковки контурные ячейковые (1) — пачки картонные.
10 шт. — упаковки контурные ячейковые (2) — пачки картонные.
20 шт. — банки полимерные (1) — пачки картонные.
30 шт. — банки полимерные (1) — пачки картонные.
Капсулы твердые желатиновые капсулы №1, корпус белого цвета, крышечка оранжевого цвета; содержимое капсул — белый или белый с желтоватым оттенком порошок.
Вспомогательные вещества: кремния диоксид коллоидный (аэросил) — 15 мг, коповидон — 9 мг, крахмал прежелатинизированный — 164 мг, кроскармеллоза натрия — 4.6 мг, натрия стеарилфумарат — 2.3 мг, тальк — 6.6 мг.
Состав корпуса капсулы: титана диоксид — 2%, желатин — до 100%.
Состав крышечки капсулы: краситель пунцовый [Понсо 4R] — 0.2401%, титана диоксид — 1.5004%; краситель солнечный закат желтый — 1.2753%, желатин — до 100%.
5 шт. — упаковки контурные ячейковые (1) — пачки картонные.
5 шт. — упаковки контурные ячейковые (2) — пачки картонные.
10 шт. — упаковки контурные ячейковые (1) — пачки картонные.
10 шт. — упаковки контурные ячейковые (2) — пачки картонные.
20 шт. — банки полимерные (1) — пачки картонные.
30 шт. — банки полимерные (1) — пачки картонные.
Номидес — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-006702
Торговое наименование:
Номидес®
Международное непатентованное или группировочное наименование:
осельтамивир
Лекарственная форма:
порошок для приготовления суспензии для приема внутрь
Состав:
Один грамм порошка для приготовления суспензии для приема внутрь содержит:
Действующее вещество: осельтамивира фосфат (в пересчете на осельтамивир) – 39,4 мг (30,0 мг);
Вспомогательные вещества: мальтитол – 841,0 мг, кальция гидрофосфат – 15,0 мг, натрия бензоат – 2,5 мг, повидон К17 – 15,1 мг, камедь ксантановая – 15,0 мг, натрия цитрат – 55,0 мг, натрия сахаринат – 2,0 мг, ароматизатор земляничный – 12,0 мг, ароматизатор цитрусовый – 3,0 мг.
Описание:
Порошок: мелкий гранулированный порошок от белого до светло-желтого цвета, с фруктовым запахом. Допускается комкование.
Суспензия: непрозрачная суспензия от белого до светло-желтого цвета, с фруктовым запахом.
Фармакотерапевтическая группа:
противовирусное средство
Код ATX:
J05AH02
Фармакологические свойства
Фармакодинамика
Механизм действия
Противовирусный препарат. Осельтамивир является пролекарством, его активный метаболит (осельтамивира карбоксилат, ОК) – эффективный и селективный ингибитор нейраминидазы вирусов гриппа типа А и В – фермента, катализирующего процесс высвобождения вновь образованных вирусных частиц из инфицированных клеток, их проникновения в неинфицированные клетки эпителия дыхательных путей и дальнейшего распространения вируса в организме. Тормозит рост вируса гриппа in vitro и подавляет репликацию вируса и его патогенность in vivo, уменьшает выделение вирусов гриппа А и В из организма. Концентрации ОК, необходимая для ингибирования нейраминидазы на 50% (IC50), составляет 0,1-1,3 нМ для вируса гриппа А и 2,6 нМ для вируса гриппа В. Медиана значений IC50 для вируса гриппа В несколько выше и составляет 8,5 нМ.
Клиническая эффективность
В проведенных исследованиях осельтамивир не оказывал влияния на образование противогриппозных антител, в том числе на выработку антител в ответ на введение инактивированной вакцины против гриппа.
Исследования естественной гриппозной инфекции
В клинических исследованиях, проведенных во время сезонной инфекции гриппа, пациенты начинали получать осельтамивир не позднее 40 ч после появления первых симптомов гриппозной инфекции. 97% пациентов были инфицированы вирусом гриппа А и 3% пациентов – вирусов гриппа В. Осельтамивир значительно сокращал период клинических проявлений гриппозной инфекции (на 32 ч). У пациентов с подтвержденным диагнозом гриппа, принимавших осельтамивир, тяжесть заболевания, выраженная как площадь под кривой для суммарного индекса симптомов, была на 38% меньше по сравнению с пациентами, получавшими плацебо. Более того, у молодых пациентов без сопутствующих заболеваний осельтамивир снижал примерно на 50% частоту развития осложнений гриппа, требующих применения антибиотиков (бронхита, пневмонии, синусита, среднего отита). Были получены доказательства эффективности препарата в отношении вторичных критериев эффективности, относящихся к антивирусной активности: осельтамивир вызывал как укорочение времени выделения вируса из организма, так и уменьшение площади под кривой «вирусные титры — время».
Данные, полученные в исследовании по терапии осельтамивиром у пациентов пожилого и старческого возраста, показывают, что прием осельтамивира в дозе 75 мг 2 раза в сутки в течение 5 дней сопровождался клинически значимым уменьшением медианы периода клинических проявлений гриппозной инфекции, аналогичным таковому у взрослых пациентов более молодого возраста, однако различия не достигали статистической значимости. В другом исследовании пациенты с гриппом старше 13 лет, имевшие сопутствующие хронические заболевания сердечно-сосудистой и/или дыхательной систем, получали осельтамивир в том же режиме дозирования или плацебо. Отличий в медиане периода до уменьшения клинических проявлений гриппозной инфекции в группах пациентов, получавших осельтамивир и плацебо не было, однако период повышения температуры при приеме осельтамивира сокращался примерно на 1 день. Доля пациентов, выделяющих вирус на 2-ой и 4-ый день, становилась значительно меньше. Профиль безопасности осельтамивира у пациентов группы риска не отличался от такового в общей популяции взрослых пациентов.
Лечение гриппа у беременных женщин
Контролируемых исследований у беременных женщин не проводилось. Однако результаты постмаркетинговых и ретроспективных наблюдательных исследований продемонстрировали пользу предлагаемого режима дозирования для данной популяции пациентов в отношении снижения заболеваемости/смертности. Результаты фармакокинетического анализа показали более низкую экспозицию активного метаболита, тем не менее, изменение режима дозирования у беременных женщин при проведении терапии или профилактики не рекомендуется (см. раздел «Фармакологические свойства», подраздел «Фармакокинетика в особых группах пациентов», пункт «Беременные женщины»).
Лечение гриппа у детей
У детей в возрасте 1-12 лет (средний возраст 5,3 года), имевших лихорадку (>37,8 °С) и один из симптомов со стороны дыхательной системы (кашель и ринит) в период циркуляции вируса гриппа среди населения, было проведено двойное слепое плацебоконтролируемое исследование. 67% пациентов были инфицированы вирусом гриппа А и 33% пациентов – вирусом гриппа В. Осельтамивир (при приеме не позднее 48 ч после появления первых симптомов гриппозной инфекции) значительно снижал продолжительность заболевания (на 35,8 ч) по сравнению с плацебо. Продолжительность заболевания определялась как время до купирования кашля, заложенности носа, исчезновения лихорадки, возвращения к обычной активности. В группе детей, получавших осельтамивир, частота острого среднего отита снижалась на 40% по сравнению с группой плацебо. Выздоровление и возвращение к обычной активности наступало почти на 2 дня раньше у детей, получавших осельтамивир, по сравнению с группой плацебо.
В другом исследовании участвовали дети в возрасте 6-12 лет, страдающие бронхиальной астмой; 53,6% пациентов имели гриппозную инфекцию, подтвержденную серологически и/или в культуре. Медиана продолжительности заболевания в группе пациентов, получавших осельтамивир, значительно не снижалась. Но к последнему 6-му дню терапии осельтамивиром объем форсированного выхода за 1 сек (ОФВ1) повышался на 10,8% по сравнению с 4,7% у пациентов, получавших плацебо (р = 0,0148).
Профилактика гриппа у взрослых и подростков
Профилактическая эффективность осельтамивира при естественной гриппозной инфекции А и В была доказана в 3 отдельных клинических исследованиях III фазы. На фоне приема осельтамивира гриппом заболели около 1% пациентов. Осельтамивир значительно уменьшал частоту выделения вируса и предотвращал передачу вируса от одного члена семьи к другому.
Взрослые и подростки, которые были в контакте с заболевшим членом семьи, начинали прием осельтамивира в течение двух дней после возникновения симптомов гриппа у членов семьи и продолжали его в течение 7 дней, что достоверно уменьшало частоту случаев гриппа у контактировавших лиц на 92%.
У непривитых и в целом здоровых взрослых в возрасте 18-65 лет прием осельтамивира во время эпидемии гриппа существенно снижал заболеваемость гриппом (на 76%). Пациенты принимали осельтамивир в течение 42 дней.
У лиц пожилого и старческого возраста, находившихся в домах престарелых, 80% из которых были привиты перед сезоном, когда проводилось исследование, осельтамивир достоверно снижал заболеваемость гриппом на 92%. В том же исследовании осельтамивир достоверно (на 86%) уменьшал частоту осложнений гриппа: бронхита, пневмонии, синусита. Пациенты принимали осельтамивир в течение 42 дней.
Профилактика гриппа у детей
Профилактическая эффективность осельтамивира при естественной гриппозной инфекции была продемонстрирована у детей от 1 года до 12 лет после контакта с заболевшим членом семьи или с кем-то из постоянного окружения. Основным параметром эффективности была частота лабораторно подтвержденной гриппозной инфекции.
Профилактика гриппа у лиц с ослабленным иммунитетом
У лиц с ослабленным иммунитетом при сезонной гриппозной инфекции и при отсутствии вирусовыделения исходно, профилактическое применение осельтамивира приводило к снижению частоты лабораторно подтвержденной гриппозной инфекции, сопровождающейся клинической симптоматикой, до 0,4% (1/232) по сравнению с 3% (7/231) в группе плацебо. Лабораторно подтвержденная гриппозная инфекция, сопровождающаяся клинической симптоматикой, диагностировалась при наличии температуры в полости рта выше 37,2 °С, кашля и/или острого ринита (все зарегистрированные в один и тот же день во время приема осельтамивира/плацебо), а также положительного результата обратно-транскриптазной полимеразной цепной реакции на РНК вируса гриппа.
Лечение гриппа у взрослых пациентов с ослабленным иммунитетом
В рандомизированном двойном слепом исследовании оценки профиля безопасности осельтамивира и его влияния на развитие резистентности вируса гриппа (первичный анализ) у пациентов с ослабленным иммунитетом и гриппозной инфекцией принимал участие 151 пациент. Эти пациенты (n=151) были пригодны также и для оценки эффективности осельтамивира (вторичный небустерный анализ).
В исследование были также включены пациенты после трансплантации солидных органов, гематопоэтических стволовых клеток, ВИЧ+ пациенты с числом CD4+ клеток <500 клеток/мм³, пациенты, получавшие иммуносупрессивную терапию, а также пациенты со злокачественным гемобластозом.
Пациенты были рандомизированы в группу лечения осельтамивиром на протяжении 10 дней (группа стандартной дозы – 73 пациента, группа двойной дозы – 78 пациентов) в течение 96 часов с момента развития симптомов гриппа.
Среднее время разрешения симптомов гриппа было сопоставимо в группе стандартной дозы (103 часа, 90% доверительный интервал 75,4-110,0) и в группе двойной дозы (104 часа, 90% доверительный интервал 65,8-131,0). Соотношение пациентов с вторичными инфекциями было также сопоставимо (8,2% в группе стандартной дозы и 5,1% в группе двойной дозы).
Резистентность
Клинические исследования
Риск появления вирусов гриппа со сниженной чувствительностью или явной резистентностью к осельтамивиру изучался в клинических исследованиях.
Появление резистентности вируса к осельтамивиру чаще наблюдалось у детей чем у взрослых пациентов (18% у младенцев в возрасте <1 года и <1% у взрослых пациентов).
У детей с резистентным к осельтамивиру вирусом носительство, как правило, имело более продолжительный характер по сравнению с субъектами с вирусом, обладающим чувствительностью.
Однако, вызванная терапией резистентность к осельтамивиру не влияла на терапевтический ответ и не вызывала продления симптомов гриппа.
У взрослых пациентов с ослабленным иммунитетом, получавших осельтамивир в стандартной дозе (14,9%, 10 пациентов из 67) или двойной дозе (2,8%, 2/71) на протяжении 10 дней, частота развития резистентности к осельтамивиру, в среднем, была выше чем у взрослых пациентов с нормальным иммунитетом, также получавших осельтамивир.
Большинство пациентов с резистентностью перенесли трансплантацию (8/10 пациентов в группе стандартной дозы и 2/2 пациента в группе двойной дозы).
Большая часть пациентов-носителей осельтамивир-резистентного вируса была инфицирована вирусом гриппа типа А; носительство имело продолжительный характер. Частота развития резистентности к осельтамивиру в клинических исследованиях.
| Популяция пациентов | Пациенты с мутациями, приводящими к резистентности | |
| Фенотипирование* | Гено- и фенотипирование* | |
| Взрослые и подростки | 21/2377 (0,88%) | 27/2391 (1,12%) |
| Дети (1-12 лет) | 66/1698 (3,89%) | 72/1698 (4,24%) |
| Младенцы (<1 года) | 13/71 (18,31%) | 13/71 (18,31%) |
* Полное генотипирование не было проведено ни в одном из исследований.
Профилактика гриппа
При приеме осельтамивира с целью постконтактной профилактики (7 дней), профилактики контактировавших в семье (10 дней) и сезонной профилактики (42 дня) улиц с нормальной функцией иммунной системы случаев резистентности не отмечено.
В 12-недельном исследовании по сезонной профилактике у лиц с ослабленным иммунитетом случаев возникновения резистентности также не наблюдалось.
Данные отдельных клинических случаев и наблюдательных исследований
У пациентов, не получавших осельтамивир, обнаружены возникающие в природных условиях мутации вирусов гриппа А и В, которые обладали сниженной чувствительностью к осельтамивиру. В 2008 году мутация по типу замены H275Y, приводящая к резистентности, была обнаружена более чем у 99% штаммов вируса 2008 H1N1, циркулирующих в Европе. Вирус гриппа 2009 H1N1 («свиной грипп») в большинстве случаев был чувствителен к осельтамивиру. Устойчивые к осельтамивиру штаммы вируса гриппа обнаружены у лиц с нормальной функцией иммунной системы и лиц с ослабленным иммунитетом, принимавших осельтамивир. Степень снижения чувствительности к осельтамивиру и частота встречаемости подобных вирусов может отличаться в зависимости от сезона и региона. Устойчивость к осельтамивиру обнаружена у пациентов с пандемическим гриппом H1N1, получавших осельтамивир как для лечения, так и для профилактики.
Частота встречаемости резистентности может быть выше у более молодых пациентов и пациентов с ослабленным иммунитетом. Устойчивые к осельтамивиру лабораторные штаммы вирусов гриппа и вирусы гриппа от пациентов, получавших терапию осельтамивиром, несут мутации нейраминидазы N1 и N2. Мутации, приводящие к устойчивости, часто являются специфическими для подтипа нейраминидазы.
При принятии решения о применении осельтамивира следует учитывать сезонную чувствительность вируса гриппа к препарату (последнюю информацию можно найти на сайте ВОЗ).
Доклинические данные
Доклинические данные, полученные на основании стандартных исследований по изучению фармакологической безопасности, генотоксичности и хронической токсичности, не выявили особой опасности для человека.
Канцерогенность: результаты 3-х исследований по выявлению канцерогенного потенциала (двух 2-х летних исследований на крысах и мышах для осельтамивира и одного 6-ти месячного исследования на трансгенных мышах Tg:AC для активного метаболита) были отрицательными.
Мутагенность: стандартные генотоксические тесты для осельтамивира и его активного метаболита были отрицательными.
Влияние на фертильность: осельтамивир в дозе 1500 мг/кг/сут не влиял на генеративную функцию самцов и самок крыс.
Тератогенность: в исследованиях по изучению тератогенности осельтамивира в дозе до 1500 мг/кг/сут (на крысах) и до 500 мг/кг/сут (на кроликах) влияния на эмбриофетальное развитие не обнаружено. В исследованиях по изучению антенатального и постнатального периодов развития у крыс при введении осельтамивира в дозе 1500 мг/кг/сут наблюдалось увеличение периода родов: предел безопасности между экспозицией для человека и максимальной не оказывающей эффекта дозой у крыс (500 мг/кг/сут) для осельтамивира выше в 480 раз, а для его активного метаболита – в 44 раза. Экспозиция у плода составляла 15-20% от таковой у матери.
Прочее: осельтамивир и активный метаболит проникают в молоко лактирующих крыс. Согласно ограниченным данным осельтамивир и его активный метаболит проникают в грудное молоко человека. По результатам экстраполяции данных, полученных в исследованиях у животных, их количество в грудном молоке может составлять 0,01 мг/сутки и 0,3 мг/сутки, соответственно.
Примерно у 50% протестированных морских свинок при введении максимальных доз активной субстанции осельтамивира наблюдалась сенсибилизация кожи в виде эритемы. Также выявлено обратимое раздражение глаз у кроликов.
В то время как очень высокие пероральные однократные дозы (657 мг/кг и выше) осельтамивира не оказали влияния на взрослых крыс, данные дозы оказывали токсическое действие на незрелых 7-дневных детенышей крыс, в том числе приводили к гибели животных. Нежелательных эффектов не наблюдалось при хроническом введении в дозе 500 мг/кг/сут с 7 по 21 день постнатального периода.
Фармакокинетика
Всасывание
Осельтамивир легко всасывается в желудочно-кишечном тракте и экстенсивно превращается в активный метаболит под действием печеночных и кишечных эстераз. Концентрация активного метаболита в плазме определяются в пределах 30 мин, время достижения максимальной концентрации 2-3 ч, и более чем в 20 раз превышают концентрации пролекарства. Не менее 75% принятой внутрь дозы попадает в системный кровоток в виде активного метаболита, менее 5% – в виде исходного препарата. Плазменные концентрации как пролекарства, так и активного метаболита пропорциональны дозе и не зависят от приема пищи.
Распределение
Объем распределения (Vss) активного метаболита – 23 л.
По данным исследований, проведенных на животных, после приема внутрь осельтамивира его активный метаболит обнаруживался во всех основных очагах инфекции (легких, промывных водах бронхов, слизистой оболочке полости носа, среднем ухе и трахее) в концентрациях, обеспечивающих противовирусный эффект.
Связь активного метаболита с белками плазмы крови – 3%. Связь пролекарства с белками плазмы крови – 42%, что недостаточно, чтобы служить причиной существенных лекарственных взаимодействий.
Метаболизм
Осельтамивир экстенсивно превращается в активный метаболит под действием эстераз, находящихся преимущественно в печени. Ни осельтамивир, ни активный метаболит не являются субстратами или ингибиторами изоферментов системы цитохрома Р450.
Выведение
Выводится (>90%) в виде активного метаболита преимущественно почками. Активный метаболит не подвергается дальнейшей трансформации и выводится почками (>99%) путем клубочковой фильтрации и канальцевой секреции. Почечный клиренс (18,8 л/ч) превышает скорость клубочковой фильтрации (7,5 л/ч), что указывает на то, что препарат выводится еще и путем канальцевой секреции. Через кишечник выводится менее 20% принятого осельтамивира. Период полувыведения активного метаболита 6-10 ч.
Фармакокинетика в особых группах пациентов
Пациенты с поражением почек
При применении осельтамивира (100 мг два раза в сутки в течение 5 дней) у пациентов с различной степенью поражения почек площадь под кривой «концентрация активного метаболита в плазме – время» (AUC осельтамивира карбоксилата) обратно пропорциональна снижению функции почек.
Фармакокинетика осельтамивира у пациентов с терминальной стадией почечной недостаточностью (с клиренсом креатинина <10 мл/мин), не находящихся на диализе, не изучалась.
Пациенты с поражением печени
Полученные in vitro и в исследованиях на животных данные об отсутствии значительного повышения AUC осельтамивира или его активного метаболита при нарушении функции печени легкой и средней степени тяжести были подтверждены и в клинических исследованиях (см. «Дозирование в особых случаях»). Безопасность и фармакокинетика осельтамивира у пациентов с тяжелым нарушением функции печени не изучалась.
Пациенты пожилого и старческого возраста
У пациентов пожилого и старческого возраста (65-78 лет) экспозиция активного метаболита в равновесном состоянии на 25-35% выше, чем у более молодых пациентов при назначении аналогичных доз осельтамивира. Период полувыведения препарата у пациентов пожилого и старческого возраста существенно не отличался от такового у более молодых пациентов. С учетом данных по экспозиции препарата и его переносимости пациентами пожилого и старческого возраста коррекции дозы при лечении и профилактике гриппа не требуется.
Дети в возрасте от 1 года до 8 лет и подростки
Фармакокинетику осельтамивира изучали у детей от 1 до 16 лет в фармакокинетическом исследовании с однократным приемом препарата и в клиническом исследовании по изучению многократного приема препарата у небольшого числа детей в возрасте 3-12 лет. Скорость выведения активного метаболита с поправкой на массу тела у детей младшего возраста выше, чем у взрослых, что приводит к более низким AUC по отношению к конкретной дозе. Прием препарата в дозе 2 мг/кг и однократных доз 30 мг или 45 мг в соответствии с рекомендациями по дозированию для детей и экстемпоральному приготовлению суспензии, приведенными в разделе «Способ применения и дозы», обеспечивает такую же AUC осельтамивира карбоксилата, какая достигается у взрослых после однократного приема капсулы 75 мг препарата (что эквивалентно примерно 1 мг/кг). Фармакокинетика осельтамивира у детей старше 12 лет такая же, как у взрослых.
Беременные женщины
В ходе объединенного анализа популяционной фармакокинетики было выявлено, что применение препарата в дозе, указанной в разделе «Способ применения и дозы», приводи т к более низкой экспозиции активного метаболита (в среднем на 30% в течение всех триместров беременности) у беременных женщин по сравнению с небеременными женщинами. Наименьшая расчетная экспозиция, тем не менее, остается выше ингибирующих концентраций (значения IC95), одновременно находясь на уровне терапевтического воздействия для ряда штаммов вируса гриппа. Кроме того, результаты наблюдательных исследований выявляют пользу существующего режима дозирования в указанной популяции пациентов. Таким образом, изменение режима дозирования у беременных женщин при проведении терапии или профилактики гриппа не рекомендуется (см. раздел «Фармакологические свойства», подраздел «Фармакодинамика», пункт «Лечение гриппа у беременных женщин»).
Пациенты с ослабленным иммунитетом
Анализ популяционной фармакокинетики указывает на увеличение экспозиции (до 50%) активного метаболита осельтамивира у взрослых пациентов с ослабленным иммунитетом по сравнению с пациентами с нормальным иммунитетом (как указано в разделе «Способ применения и дозы»). При этом клиренс креатинина в этих группах остается сопоставимым. Наличие сниженного иммунитета у взрослых пациентов не требует коррекции дозы осельтамивира, благодаря высокому пределу безопасности активного метаболита. Тем не менее, у взрослых пациентов с поражением почек дозы необходимо корректировать в соответствии с информацией, представленной в разделе «Способ применения и дозы».
Показания к применению
- Лечение гриппа у взрослых и детей в возрасте старше 1 года.
- Профилактика гриппа у взрослых и подростков в возрасте старше 12 лет, находящихся в группах повышенного риска инфицирования вирусом (в воинских частях и больших производственных коллективах, у ослабленных пациентов).
- Профилактика гриппа у детей старше 1 года.
Противопоказания
- Повышенная чувствительность к осельтамивиру или любому компоненту препарата.
- Терминальная стадия почечной недостаточности (клиренс креатинина <10 мл/мин).
- Детский возраст до 1 года.
- Тяжелая печеночная недостаточность.
С осторожностью
- Беременность.
- Период грудного вскармливания.
- Применение в комбинации с препаратами, имеющими узкую широту терапевтического действия (например, хлорпропамид, метотрексат, бутадион).
Применение при беременности и в период грудного вскармливания
Беременность
Неблагоприятный исход беременности и аномалии развития плода, а также риск серьезных врожденных пороков развития, в том числе врожденных пороков сердца, связаны с заболеванием гриппом.
Большое количество данных о воздействии осельтамивира у беременных женщин в ходе постмаркетингового применения и наблюдательных исследований (более 1000 пациентов на первом триместре беременности) не указывают ни на пороки развития, ни на фето/неонатальную токсичность осельтамивира.
Однако в одном наблюдательном исследовании результаты оценки риска развития тяжелых врожденных пороков сердца, диагностированных в течение 12 месяцев после рождения, не были однозначными, хотя общий риск пороков развития и не был увеличен.
В данном исследовании частота развития тяжелых врожденных пороков сердца после применения осельтамивира в течение первого триместра беременности составляла 1,76% (7 младенцев из 397 беременностей) по сравнению с 1,01% при беременности в общей популяции без применения осельтамивира (отношение рисков 1,75, 95% доверительный интервал 0,51 до 5,98).
Клиническое значение данного результата до конца не ясно, так как исследование имело ограниченную мощность.
Кроме того, исследование было недостаточно объемным, чтобы провести достоверную оценку отдельных категорий тяжелых пороков развития; при этом данные у женщин, принимавших и не принимавших осельтамивир, не могли быть полностью сопоставимы, независимо от того, болели ли они гриппом.
Исследования на животных не указывают на репродуктивную токсичность осельтамивира (см. раздел «Фармакологические свойства», подраздел «Доклинические данные»). Применение препарата при беременности возможно в случае необходимости и после оценки имеющейся информации о безопасности и пользе (информацию о пользе применения препарата у беременных женщин см. в подразделе «Фармакодинамика», пункт «Лечение гриппа у беременных женщин»), а также патогенности циркулирующего штамма вируса гриппа.
Грудное вскармливание
Во время доклинических исследований осельтамивир и активный метаболит проникали в молоко лактирующих крыс. Данные по экскреции осельтамивира с грудным молоком у человека и применению осельтамивира кормящими женщинами ограничены. Ограниченные данные показывают, что осельтамивир и его активный метаболит в небольших количествах проникают в грудное молоко, создавая субтерапевтические концентрации в крови грудного ребенка. При назначении осельтамивира кормящим женщинам следует также учитывать их сопутствующие заболевания и патогенность циркулирующего штамма вируса гриппа. При беременности и в период грудного вскармливания осельтамивир применяют только в случае, если ожидаемая явная польза для кормящей матери превышает риск для ребенка.
Фертильность
На основании доклинических данных не ожидается, что препарат влияет на фертильность мужчин или женщин (см. раздел «Фармакологические свойства», подраздел «Доклинические данные»).
Способ применения и дозы
Внутрь, во время еды или независимо от приема пищи. Переносимость осельтамивира можно улучшить, если принимать его во время еды.
Желательно, чтобы приготовлением суспензии занимался фармацевт или провизор.
Приготовление суспензии
- Осторожно несколько раз постучать пальцем по закрытому флакону с тем, чтобы порошок распределился на дне флакона.
- Отмерить 55 мл воды. Используя мерный стаканчик. Заполняя его до указанного уровня.
- Добавить 55 мл воды во флакон, закрыть колпачком и хорошо встряхивать в течение 15 секунд.
- Снять колпачок и вставить в горлышко флакона адаптер.
- Плотно завинтить флакон колпачком для обеспечения правильного расположения адаптера.
На этикетке флакона следует указать дату приготовления суспензии. Перед применением флакон с приготовленной суспензией необходимо взбалтывать. Для дозировки суспензии прилагается дозирующий шприц с метками, указывающими уровни доз 30 мг, 45 мг, 60 мг и 75 мг (см. раздел «Форма выпуска и упаковка»).
Стандартный режим дозирования
Лечение
Прием препарата необходимо начинать не позднее 2 суток с момента развития симптомов заболевания.
Взрослые и дети в возрасте >8 лет
По 75 мг 2 раза в сутки внутрь в течение 5 дней. Увеличение дозы более 150 мг/сутки не приводит к усилению эффекта.
Дети в возрасте от 1 года до 8 лет
Рекомендованный режим дозирования осельтамивира:
| Масса тела | Рекомендованная доза в течение 5 дней | Количество суспензии |
| ≤15 кг | 30 мг два раза в сутки | 2,50 мл |
| >15-23 кг | 45 мг два раза в сутки | 3,75 мл |
| >23-40 кг | 60 мг два раза в сутки | 5,00 мл |
| >40 кг | 75 мг два раза в сутки | 6,25 мл |
Для дозирования суспензии использовать прилагающийся шприц. Необходимое количество суспензии отобрать из флакона дозирующим шприцем, перенести в мерный стаканчик и принимать внутрь.
Профилактика
Прием препарата необходимо начинать не позднее 2 суток после контакта с заболевшим человеком.
Взрослые и подростки в возрасте >12 лет
По 75 мг 1 раз в сутки внутрь в течение не менее 10 дней после контакта с заболевшими лицами. Во время сезонной эпидемии гриппа – 75 мг 1 раз в сутки в течение 6 недель.
Профилактическое действие продолжается столько, сколько длится прием препарата.
Дети в возрасте от 8 до 12 лет
По 75 мг 1 раз в сутки внутрь в течение 10 дней
Дети в возрасте от 1 года до 8 лет
Рекомендованный режим дозирования осельтамивира:
| Масса тела | Рекомендованная доза в течение 10 дней | Количество суспензии |
| ≤15 кг | 30 мг один раз в сутки | 2,50 мл |
| >15-23 кг | 45 мг один раз в сутки | 3,75 мл |
| >23-40 кг | 60 мг один раз в сутки | 5,00 мл |
| >40 кг | 75 мг один раз в сутки | 6,25 мл |
Для дозирования суспензии использовать прилагающийся шприц с метками. Необходимое количество суспензии отобрать из флакона дозирующим шприцем, перенести в мерный стаканчик и принимать внутрь.
Дозирование в особых случаях
Пациенты с поражением почек
Лечение
Пациентам с клиренсом креатинина более 60 мл/мин коррекции дозы не требуется. У пациентов с клиренсом креатинина от 30 до 60 мл/мин дозу осельтамивира следует уменьшить до 30 мг два раза в сутки в течение 5 дней.
У пациентов с клиренсом креатинина от 10 до 30 мл/мин дозу осельтамивира следует уменьшить до 30 мг один раз в сутки в течение 5 дней. Пациентам, находящимся на постоянном гемодиализе, осельтамивир в первоначальной дозе 30 мг можно принять до начала диализа, если симптомы гриппа появились в течение 48 ч между сеансами диализа. Для поддержания плазменной концентрации на терапевтическом уровне осельтамивир следует принимать по 30 мг после каждого сеанса диализа. Пациентам, находящимся на перитонеальном диализе, осельтамивир следует принимать в первоначальной дозе 30 мг до начала проведения диализа, затем по 30 мг каждые 5 дней. Фармакокинетика осельтамивира у пациентов с терминальной стадией почечной недостаточности (с клиренсом креатинина <10 мл/мин), не находящихся на диализе не изучалась. В связи с этим рекомендации по дозированию у данной группы пациентов отсутствуют.
Профилактика
Пациентам с клиренсом креатинина более 60 мл/мин коррекции дозы не требуется. У пациентов с клиренсом креатинина от 30 до 60 мл/мин дозу осельтамивира следует уменьшить до 30 мг один раз в сутки.
У пациентов с клиренсом креатинина от 10 до 30 мл/мин рекомендуется уменьшить дозу осельтамивира до 30 мг через день. Пациентам, находящимся на постоянном гемодиализе, осельтамивир в первоначальной дозе 30 мг можно принять до начала диализа («1-й сеанс»). Для поддержания плазменной концентрации на терапевтическом уровне осельтамивир следует принимать по 30 мг после каждого последующего нечетного сеанса диализа.
Пациентам, находящимся на перитонеальном диализе, осельтамивир следует принимать в первоначальной дозе 30 мг до начала проведения диализа, затем по 30 мг каждые 7 дней. Фармакокинетика осельтамивира у пациентов с терминальной стадией почечной недостаточности (с клиренсом креатинина <10 мл/мин), не находящихся на диализе, не изучалась. В связи с этим рекомендации по дозированию у данной группы пациентов отсутствуют.
Пациенты с поражением печени
Коррекции дозы осельтамивира при лечении и профилактике гриппа у пациентов с нарушениями функции печени легкой и средней степеней тяжести не требуется. Безопасность и фармакокинетика осельтамивира у пациентов с тяжелыми нарушениями функции печени не изучалась.
Пациенты пожилого и старческого возраста
Коррекции дозы для профилактики или лечения гриппа не требуется.
Пациенты с ослабленным иммунитетом (после трансплантации
Лечение
Рекомендованная доза осельтамивира составляет 75 мг 2 раза в сутки внутрь у взрослых пациентов (см. разделы «Особые указания», «Побочное действие» и «Фармакологические свойства»). Прием препарата необходимо начинать не позднее 2 суток с момента развития симптомов заболевания.
Сезонная профилактика
Для сезонной профилактики гриппа у пациентов с ослабленным иммунитетом в возрасте >1 года – в течение 12 недель, коррекция дозы не требуется.
Дети
Осельтамивир не следует назначать детям до 1 года.
Побочное действие
Обзор профиля безопасности
Общий профиль безопасности осельтамивира основан на данных 6049 взрослых пациентов/подростков и 1473 детей с гриппом, получавших осельтамивир или плацебо, а также на данных 3990 взрослых пациентов/подростков и 253 детей, получающих осельтамивир или плацебо/не получавших терапии в клинических исследованиях по профилактике гриппа.
Кроме того, 199 взрослых пациентов с ослабленным иммунитетом получили осельтамивир для лечения гриппа, и 475 пациентов с ослабленным иммунитетом (в том числе 18 детей, 10 из которых получали осельтамивир и 8 – плацебо) получили осельтамивир или плацебо для профилактики гриппа.
У взрослых пациентов/подростков наиболее частыми нежелательными реакциями (HP) в ходе клинических исследований лечения гриппа были тошнота и рвота, а в ходе исследований по профилактике – тошнота.
Большинство указанных HP были зарегистрированы однократно в первый или второй день терапии и спонтанно разрешались в течение последующих 1-2 дней.
У детей наиболее часто встречающейся HP была рвота.
У большинства пациентов данные HP не приводили к отмене терапии осельтамивиром.
Серьезные HP, перечисленные ниже, редко отмечались с момента выхода осельтамивира на рынок: анафилактические и анафилактоидные реакции, нарушения со стороны печени (фульминантный гепатит, нарушение функции печени и желтуха), ангионевротический отек, синдром Стивенса-Джонсона и токсический эпидермальный некролиз, желудочно-кишечное кровотечение и нарушения со стороны нервной системы и психики (см. раздел «Особые указания»).
Список нежелательных реакций представлен в табличном формате ниже.
Для описания частоты нежелательных реакций используется следующая классификация: очень частые (≥1/10), частые (≥1/100 и <1/10), нечастые (≥1/1000 и <1/100), редкие (≥1/10000 и <1/1000) очень редкие (<1/10000). Соответствующая категория присваивается нежелательным реакциям на основании объединенного анализа клинических исследований.
Лечение и профилактика гриппа у взрослых и подростков
В таблице 1 представлены HP, возникавшие наиболее часто при приеме рекомендованной дозы осельтамивира в исследованиях по профилактике и лечению гриппа у взрослых и подростков (75 мг 2 раза в сутки в течение 5 дней для лечения и 75 мг 1 раз в сутки до 6 недель для профилактики).
В исследованиях по профилактике гриппа профиль безопасности у пациентов, получавших рекомендованную дозу осельтамивира (75 мг 1 раз в сутки до 6 недель), качественно не отличался от такового в исследованиях по лечению гриппа, несмотря на более длительный прием препарата.
Таблица 1. Нежелательные реакции, выявленные в ходе клинических исследований по профилактике и лечению гриппа осельтамивиром у взрослых пациентов и подростков или в ходе постмаркетингового наблюдения.
| Класс систем органов | Нежелательные реакции, распределенные согласно частоте выявления | |||
| Очень часто | Часто | Нечасто | Редко | |
| Инфекционные и паразитарные заболевания | Бронхит, Herpes simplex, назофарингит, инфекции верхних дыхательных путей, синусит | |||
| Нарушения со стороны крови и лимфатической системы | Тромбоцитопения | |||
| Нарушения со стороны иммунной системы | Реакции гиперчувствительности | Анафилактические реакции, анафилактоидные реакции | ||
| Нарушения психики | Беспокойство, анормальное поведение, тревожность, спутанность сознания, бред, делирий, галлюцинации, ночные кошмары, причинение себе телесного повреждения | |||
| Нарушения со стороны нервной системы | Головная боль | Бессонница | Изменение сознания, судороги | |
| Нарушения со стороны органа зрения | Нарушение зрения | |||
| Нарушения со стороны сердца | Аритмия | |||
| Нарушения со стороны дыхательной системы, органов грудной клетки и средостения | Кашель, боль в горле, ринорея | |||
| Нарушения со стороны желудочно-кишечного тракта | Тошнота | Рвота, боль в животе (включая боль в верхней части живота), диспепсия | Желудочно-кишечные кровотечения, геморрагический колит | |
| Нарушения со стороны печени и желчевыводящих путей | Повышение активности «печеночных» ферментов | Фульминантный гепатит, печеночная недостаточность, гепатит | ||
| Нарушения со стороны кожи и подкожных тканей | Экзема, дерматит, сыпь, крапивница | Ангионевротический отек, мультиформная эритема, синдром Стивенса-Джонсона, токсический эпидермальный некролиз | ||
| Общие расстройства и нарушения в месте введения | Боль, головокружение (включая вертиго), утомляемость, лихорадка, боль в конечностях |
Лечение и профилактика гриппа у детей
В клинических исследованиях осельтамивира при лечении гриппа принимали участие 1473 ребенка (включая в целом здоровых детей в возрасте от 1 до 12 лет и детей с астмой в возрасте от 6 до 12 лет). Из них 851 ребенок получал терапию осельтамивиром в лекарственной форме «суспензия». Всего 158 детей получали рекомендованную дозу осельтамивира 1 раз в сутки в исследованиях постконтактной профилактики в домашних условиях (n=99), в 6-недельных исследованиях сезонной профилактики (n=49) и 12-недельных исследованиях сезонной профилактики у пациентов с ослабленным иммунитетом (n=10).
В таблице 2 представлены HP, наиболее часто сообщаемые в ходе клинических исследований у детей.
Таблица 2. Нежелательные реакции, выявленные в ходе клинических исследований по профилактике и лечению гриппа осельтамивиром у детей (доза от 30 мг до 75 мг в зависимости от возраста/веса).
| Класс систем органов | Нежелательные реакции, распределенные согласно частоте выявления | |||
| Очень часто | Часто | Нечасто | Редко | |
| Инфекционные и паразитарные заболевания | Средний отит | |||
| Нарушения со стороны нервной системы | Головная боль | |||
| Нарушения со стороны органа зрения | Конъюнктивит (включая покраснения глаз, выделения и боль) | |||
| Нарушения со стороны органа слуха и лабиринтные нарушения | Боль в ухе | Нарушения со стороны барабанной перепонки | ||
| Нарушения со стороны дыхательной системы, органов грудной клетки и средостения | Кашель, заложенность носа | Ринорея | ||
| Нарушения со стороны желудочно-кишечного тракта | Рвота | Боль в животе (включая боль в верхней части живота), диспепсия, тошнота | ||
| Нарушения со стороны кожи и подкожных тканей | Дерматит (включая аллергический и атопический дерматит) |
Описание отдельных нежелательных реакций
Нарушения со стороны нервной системы и психики
Гриппозная инфекция может ассоциироваться с различными неврологическими симптомами и изменениями поведения, включая такие симптомы, как галлюцинации, делирий, и анормальное поведение. В некоторых случаях они могут привести к смертельному исходу.
Данные явления могут возникать как на фоне развития энцефалопатии или энцефалита, так и отдельно, без явного тяжелого заболевания.
В постмаркетинговых сообщениях у пациентов, которые получали осельтамивир для лечения гриппа, отмечались судороги и делирий (включая такие симптомы, как нарушение сознания, спутанность сознания, анормальное поведение, бред, галлюцинации, беспокойство, тревожность, ночные кошмары). Эти случаи редко сопровождались опасными для жизни активностями или летальным исходом. Данные явления были зарегистрированы в основном среди детей и подростков и часто имели внезапное начало и быстрое разрешение.
Роль осельтамивира в развитии данных явлений неизвестна. Указанные психоневрологические нарушения также были зарегистрированы у пациентов с гриппом, не получавших осельтамивир.
Нарушения со стороны печени и желчевыводящих путей
Нарушения со стороны печени и желчевыводящих путей, включая гепатит и повышение активности «печеночных» ферментов, отмечались у пациентов с гриппоподобным заболеванием. Указанные явления также включали фульминантный гепатит/печеночную недостаточность с фатальным исходом.
Прочие особые популяции пациентов
Дети (до 1 года)
В двух исследованиях фармакокинетики, фармакодинамики и профиля безопасности осельтамивира, в которых принимали участие 135 детей в возрасте до 1 года с гриппом, профиль безопасности препарата был сопоставим в различных возрастных группах.
Наиболее часто сообщаемыми нежелательными явлениями при этом были рвота, диарея и опрелость (см. раздел «Фармакологические свойства», подраздел «Фармакокинетика»).
Данные о детях в постконцептуальном возрасте до 36 недель недостаточны.
Данные по безопасности применения осельтамивира при лечении у детей в возрасте до 1 года получены из проспективных и ретроспективных наблюдательных исследований (включали более 2400 детей данного возраста), исследований эпидемиологических баз данных и постмаркетингового наблюдения. Профиль безопасности у детей до 1 года сопоставим с известным профилем безопасности у детей в возрасте 1 года и старше.
Пожилые пациенты и пациенты с хронической сердечной и/или дыхательной недостаточностью
Популяция, включенная в исследования по лечению гриппа, состояла из в целом здоровых взрослых/подростков и пациентов группы риска (риск развития осложнений гриппа, например, популяция пожилых пациентов и пациентов с хронической сердечной или дыхательной недостаточностью). В целом профиль безопасности препарата у пациентов группы риска был сопоставим с таковым у в целом здоровых взрослых/подростков.
Пациенты с ослабленным иммунитетом
В двойном слепом исследовании 199 взрослых пациентов с ослабленным иммунитетом (которые отвечали критериям для оценки профиля безопасности) были рандомизированы для получения осельтамивира на протяжении 10 дней для лечения гриппа: 98 пациентов получали стандартную дозу (75 мг 2 раза в сутки) и 101 пациент получал двойную дозу (150 мг 2 раза в сутки). Профиль безопасности препарата, наблюдаемый в данном исследовании, был сопоставим с таковым в предыдущих клинических исследованиях, в которых осельтамивир применялся для лечения пациентов с нормальным иммунитетом (здоровые пациенты или пациенты из группы риска, например, с дыхательной и/или сердечной недостаточностью). Соотношение пациентов, у которых отмечались нежелательные явления, было ниже в группе стандартной дозы по сравнению с группой двойной дозы (49,0% и 59,4%, соответственно) (см. раздел «Фармакологические свойства», подраздел «Фармакодинамика»).
В ходе 12-недельного исследования по профилактике гриппа у 475 пациентов с ослабленным иммунитетом (включая 18 детей в возрасте от 1 до 12 лет и старше) профиль безопасности в группе осельтамивира (238 пациентов) был сопоставим с ранее наблюдаемым профилем осельтамивира в клинических исследованиях по профилактике.
Дети с бронхиальной астмой в анамнезе
В целом профиль нежелательных реакций у детей с бронхиальной астмой в анамнезе был сопоставим с таковым в целом у здоровых детей.
Передозировка
В большинстве случаев передозировка в ходе клинических исследований и при постмаркетинговом применении осельтамивира не сопровождалась какими-либо нежелательными явлениями. В остальных случаях симптомы передозировки соответствовали нежелательным явлениям, предоставленным в разделе «Побочное действие».
Взаимодействие с другими лекарственными средствами
Фармакокинетические свойства осельтамивира, такие как его низкая степень связывания с белками и метаболизм, не зависимый от изофермента CYP450 и системы глюкуронидаз (см. раздел «Фармакологические свойства», подраздел «Фармакокинетика»), не дают оснований предполагать наличие клинически значимых взаимодействий по указанным механизмам.
Пробенецид
Коррекция дозы при одновременном применении с пробенецидом у пациентов с нормальной функцией почек не требуется. Одновременное применение с пробенецидом, мощным ингибитором анионной канальцевой секреции в почках, приводит к-2-кратному увеличению экспозиции активного метаболита осельтамивира.
Амоксициллин
Кинетическое взаимодействие осельтамивира и амоксициллина (выводящегося тем же путем, что и осельтамивир) отсутствует. Предполагается, что конкуренция осельтамивира за выделение почками слабая.
Выведение с мочой
Маловероятны клинически значимые межлекарственные взаимодействия, связанные с конкуренцией за канальцевую секрецию, принимая во внимание резерв безопасности для большинства подобных препаратов, пути выведения активного метаболита осельтамивира (клубочковая фильтрация и анионная канальцевая секреция), а также выводящую способность каждого из путей. Однако, применять осельтамивир в комбинации с препаратами, имеющими узкую широту терапевтического действия (например, хлорпропамид, метотрексат, бутадион), необходимо с осторожностью.
Дополнительная информация
Не обнаружено фармакокинетических взаимодействий между осельтамивиром или его основным метаболитом при одновременном приеме с парацетамолом, ацетилсалициловой кислотой, циметидином, антацидными средствами (магния и алюминия гидроксид, кальция карбонат), римантадином или варфарином (у пациентов без гриппа, стабильных на варфарине).
Особые указания
Осельтамивир эффективен только в отношении заболевания, вызванного вирусом гриппа. Данные об эффективности осельтамивира при терапии заболеваний, вызванных иными агентами, отсутствуют (см. раздел «Фармакологические свойства», подраздел «Фармакодинамика»).
Осельтамивир не является заменой вакцинации.
Использование осельтамивира не должно влиять на оценку пациентов при проведении ежегодной вакцинации против гриппа.
Защита от гриппа длится только до тех пор, пока применяется осельтамивир.
Препарат следует использовать только для лечения и профилактики гриппа и только в случае, если достоверные эпидемиологические данные указывают на то, что вирус гриппа циркулирует в общей популяции.
Чувствительность циркулирующих штаммов вируса гриппа к осельтамивиру может сильно варьировать (см. раздел «Фармакологические свойства», подраздел «Фармакодинамика», пункт «Резистентность»).
Таким образом, при назначении препарата необходимо учитывать самую последнюю доступную информацию о чувствительности циркулирующего вируса к осельтамивиру.
Тяжелое сопутствующее заболевание
Данные о безопасности и эффективности применения осельтамивира у пациентов с достаточно тяжелым сопутствующим заболеванием или нестабильным состоянием, предполагающим госпитализацию, отсутствуют.
Пациенты с ослабленным иммунитетом
Эффективность осельтамивира при лечении или профилактике гриппа у пациентов с ослабленным иммунитетом четко не установлены (см. раздел «Фармакологические свойства»), подраздел «Фармакодинамика»). Однако у взрослых пациентов с ослабленным иммунитетом лечение гриппа следует проводить на протяжении 10 дней, так как клинические исследования при более коротком курсе терапии не проводились.
Сердечная/дыхателъная недостаточность
Эффективность осельтамивира при лечении или профилактике гриппа у пациентов с хронической сердечной и/или дыхательной недостаточностью не установлена. В данной популяции пациентов частота возникновения осложнений была сопоставима в группе лечения и группе плацебо.
Дети
Данные для определения дозы у недоношенных детей (постконцептуальный возраст <36 недель) отсутствуют.
Почечная недостаточность тяжелой степени тяжести
У взрослых пациентов и подростков (13-17 лет) с тяжелой степенью почечной недостаточности при лечении и профилактике гриппа рекомендуется коррекция дозы.
Клинические данные для коррекции дозы у младенцев и детей (в возрасте от 1 года и старше) с почечной недостаточностью отсутствуют (см. разделы «Способ применения и дозы» и «Фармакологические свойства», подраздел «Фармакокинетика»).
Психоневрологические нарушения
У пациентов (в основном у детей и подростков), принимавших осельтамивир, были зарегистрированы психоневрологические нарушения. Подробные психоневрологические нарушения так же отмечены у пациентов с гриппом, не получавших осельтамивир.
Следует тщательно мониторировать пациентов на предмет изменений в поведении, риск и польза продолжения терапии должны быть оценены для каждого пациента индивидуально (см. раздел «Побочное действие»).
Инструкции по применению, обращению и уничтожению
Попадание лекарственных препаратов в окружающую среду должно быть сведено к минимуму. Не следует утилизировать препарат с помощью сточных вод или вместе с бытовыми отходами. По возможности необходимо использовать специальные системы для утилизации лекарственных препаратов.
Влияние на способность управлять транспортными средствами, механизмами
Исследования по изучению влияния препарата на способность управлять транспортными средствами и заниматься другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций, не проводились. Исходя из профиля безопасности, влияние осельтамивира на данные виды деятельности маловероятно.
Форма выпуска
Порошок для приготовления суспензии для приема внутрь 12 мг/мл
Первичная упаковка лекарственного препарата.
30 г препарата во флакон светозащитного стекла типа III (USP/Ph.Eur), вместимостью 100 мл, укупоренный полипропиленовой или полиэтиленовой крышкой винтовой, обеспечивающей контроль первого вскрытия и защиту от вскрытия флакона детьми. Способ открытия флакона приведен в виде схемы.
На каждый флакон наклеивают этикетки.
Вторичная упаковка лекарственного препарата.
По 1 флакону вместе с адаптером для шприца из полиэтилена низкой плотности, шприцем-дозатором, состоящим из полипропиленового корпуса и поршня из полиэтилена низкой плотности (помещенные в герметичную упаковку из полиэтилена), полипропиленовым мерным стаканчиком и инструкцией по применению помещают в пачку из картона. Пачки помещают в групповую упаковку.
Условия хранения
При температуре не выше 25 °С. После приготовления суспензию хранить при температуре 2-8 °С в течение 17 дней или при температуре не выше 25 °С в течение 10 дней.
Хранить в недоступном для детей месте.
Срок годности
2 года. Не применять по истечении срока годности.
Условия отпуска
Отпускают по рецепту.
Производитель
АО «Фармасинтез», Россия
Юридический адрес: 664007, г. Иркутск, ул. Красногвардейская, д. 23, оф. 3;
Адрес производственной площадки: г. Иркутск, ул. Р. Люксембург, д. 184.
Владелец регистрационного удостоверения/ Организация, принимающая претензии потребителей
АО «Фармасинтез», Россия
Юридический адрес: 664007, г. Иркутск, ул. Красногвардейская, д. 23, оф. 3;
Адрес производственной площадки: г. Иркутск, ул. Р. Люксембург, д. 184.
Купить Номидес в planetazdorovo.ru
*Цена в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
МНН: Осельтамивир
Производитель: АО Фармасинтез
Анатомо-терапевтическо-химическая классификация: Oseltamivir
Номер регистрации в РК:
РК-ЛС-5№023153
Информация о регистрации в РК:
03.08.2017 — 03.08.2022
- Скачать инструкцию медикамента
Торговое название
Номидес
Международное непатентованное название
Осельтамивир
Лекарственная форма
Капсулы,
30 мг, 45 мг, 75 мг
Фармакотерапевтическая группа
Противоинфекционные
препараты для системного использования. Противовирусные препараты для
системного применения. Противовирусные препараты прямого действия.
Ингибиторы нейраминидазы. Осельтамивир.
Код
АТХ J05AH02
Показания к применению
Лечение
гриппа
-
Препарат
Номидес показан для лечения взрослых у которых наблюдаются
характерные симптомы гриппа во время вспышки гриппа. Доказано, что
препарат обеспечивает терапевтический эффект, если лечение
начинается в течение первых двух дней с момента появления симптомов.
Профилактика
гриппа
-
постконтактная
профилактика у взрослых после контакта с больным с подтвержденным
клиническим диагнозом гриппа во время вспышки заболевания. -
соответствующий
порядок применения препарата Номидес для профилактики гриппа
определяется в каждом конкретном случае, исходя из конкретных
обстоятельств и характеристик популяции, требующей профилактической
защиты. В исключительных случаях (например, если имеет место
несовпадение циркулирующего штамма вируса и штамма, содержащегося в
вакцине, или в случае пандемии) можно рассмотреть возможность
назначения сезонной профилактики.
Препарат
Номидес не является заменой вакцинации.
Применение
противовирусных препаратов для лечения и профилактики гриппа должно
проводиться на основании официальных рекомендаций. Решение об
использовании осельтамивира для лечения и профилактики гриппа должно
приниматься с учетом известных характеристик циркулирующих штаммов
вируса, имеющейся информации о лекарственной чувствительности для
каждого сезона и влиянии, оказываемом заболеванием в различных
географических регионах и популяциях пациентов.
Перечень сведений,
необходимых до начала применения
Противопоказания
-
Повышенная
чувствительность к активному веществу или к любому компоненту
препарата -
Терминальная
стадия почечной недостаточности (клиренс креатинина ≤10 мл/мин) -
Тяжелая
печеночная недостаточность -
Дети
и подростки до 18 лет
Необходимые
меры предосторожности при применении
С осторожностью
применять во время беременности и в период грудного вскармливания.
Взаимодействия
с другими лекарственными препаратами
Клинически
значимые лекарственные взаимодействия маловероятны. Осельтамивира
фосфат в высокой степени превращается в активный метаболит под
действием эстераз, в основном расположенных в печени. Лекарственные
взаимодействия, обусловленные конкуренцией за связывание с активными
центрами эстераз, в литературных источниках широко не представлены.
Низкая степень связывания осельтамивира и активного метаболита с
белками плазмы не дают оснований предполагать наличие взаимодействий,
связанных с вытеснением лекарственных средств из связи с белками.
Ни
осельтамивира фосфат, ни его активный метаболит не являются
предпочтительным субстратом для полифункциональных оксидаз системы
цитохрома P450
или для глюкуронилтрансфераз. Оснований для взаимодействия с
пероральными контрацептивами нет.
Циметидин,
неспецифический ингибитор изофермента системы цитохрома P450
и конкурирующий в процессе канальцевой секреции с препаратами
щелочного типа и катионами, не влияет на плазменные концентрации
осельтамивира и его активного метаболита.
Маловероятны
клинически значимые межлекарственные взаимодействия, связанные с
конкуренцией за канальцевую секрецию, принимая во внимание резерв
безопасности для большинства подобных препаратов, пути выведения
активного метаболита осельтамивира (клубочковая фильтрация и анионная
канальцевая секреция), а также выводящую способность каждого из
путей.
Пробенецид
приводит к увеличению AUC
активного метаболита осельтамивира примерно в 2 раза (за счет
снижения активной канальцевой секреции в почках). Однако коррекции
дозы при одновременном применении с пробенецидом не требуется,
учитывая резерв безопасности активного метаболита.
Одновременный
прием с амоксициллином
не
влияет на плазменные концентрации осельтамивира и его компонентов,
демонстрируя слабую конкуренцию за выведение путем анионной
канальцевой секреции.Одновременный прием с парацетамолом
не влияет на плазменные концентрации осельтамивира и его активного
метаболита или парацетамола.
Фармакокинетических
взаимодействий между осельтамивиром, его основным метаболитом не
обнаружено при одновременном приеме с парацетамолом,
ацетилсалициловой кислотой, циметидином или антацидными средствами
(магния и алюминия гидроксид, кальция карбонат), варфарином,
римантадином или амантадином.
При
использовании осальтемивира с часто применяемыми препаратами, такими
как ингибиторы ангиотензинпревращающего фермента (эналаприл,
каптоприл), тиазидные диуретики (бендрофлуметиазид), антибиотики
(пенициллин, цефалоспорины, азитромицин, эритромицин и доксициклин),
блокаторы Н2-гистаминовых
рецепторов (ранитидин, циметидин), бета-адреноблокаторы
(пропранолол), ксантины (теофиллин), симпатомиметики (псевдоэфедрин),
опиаты (кодеин), глюкокортикостероиды, ингаляционные бронхолитики и
ненаркотические анальгетики (ацетилсалициловая кислота, ибупрофен и
парацетамол), изменений характера или частоты нежелательных явлений
не наблюдалось.
Применять
осельтамивир в комбинации с препаратами, имеющими узкую широту
терапевтического действия (например, хлорпропамид, метотрексат,
бутадион), необходимо с осторожностью.
Специальные
предупреждения
Осельтамивир
эффективен только при заболеваниях, вызванных вирусами гриппа.
Отсутствуют доказательства эффективности осельтамивира в отношении
заболеваний, вызванных агентами, отличными от вируса гриппа.
Номидес не является
заменителем вакцины против гриппа. Применение осельтамивира не должно
влиять на определение лиц для ежегодной вакцинации против гриппа.
Защита от гриппа длится только во время приема осельтамивира.
Лекарственное средство Номидес следует применять для лечения и
профилактики гриппа только при наличии надежных эпидемиологических
данных, подтверждающих факт циркуляции гриппа в популяции.
Чувствительность циркулирующих штаммов гриппа к осельтамивиру очень
вариабельна. Следовательно, медицинские работники, назначающие
рецептурные препараты, должны учитывать наиболее свежую информацию о
характере чувствительности циркулирующих в данный момент вирусов к
осельтамивиру при принятии решения об использовании лекарственного
средства Номидес.
Сопутствующие
тяжелые состояния
Отсутствуют данные о
безопасности и эффективности осельтамивира у пациентов с любыми в
достаточной степени тяжелыми или нестабильными медицинскими
состояниями. При которых риск госпитализации рассматривается как
неизбежный.
Пациенты с
иммунодефицитом
Эффективность
осельтамивира как для лечения, так и для профилактики гриппа у
пациентов с ослабленным иммунитетом не была четко установлена. Однако
у взрослых пациентов с ослабленным иммунитетом лечение гриппа следует
проводить на протяжении 10 дней, так как клинические исследования при
более коротком курсе терапии не проводилось.
Сердечные/респираторные
заболевания
Эффективность
осельтамивира для лечения пациентов, страдающих хроническим
заболеванием сердца и/или дыхательных путей, не была установлена. У
таких пациентов не отмечалось различий в частоте возникновения
осложнений между группами, получавшими лекарственное средство и
плацебо.
Тяжелая почечная
недостаточность
Рекомендуется
коррекция дозы при лечении и профилактике у пациентов с тяжелой
почечной недостаточностью. Чтобы дать
рекомендации по дозированию
см. раздел «Режим дозирования».
Нейропсихиатрические
расстройства
Нейропсихиатрические
расстройства во время приема осельтамивира отмечались у пациентов,
больных гриппом, особенно у подростков. Подобные проявления
наблюдались также у пациентов, больных гриппом, не принимавших
осельтамивир. Следует тщательно контролировать пациентов на предмет
поведенческих изменений и тщательно оценивать пользу и риск
продолжения лечения для каждого пациента.
Вспомогательные вещества
Лекарственное
средство Номидес содержит натрий в количестве менее 1 ммоль (23
мг) в дозе, т.е. практически «не содержит натрия»
Во время
беременности или лактации
При беременности и в
период грудного вскармливания осельтамивир применяют только в случае,
если предполагаемая польза для матери превышает потенциальный риск
для плода и ребенка.
Беременность
Заболевание гриппом
связано с неблагоприятным течением беременности, может вызывать
аномалии развития плода, а также является риском развития серьезных
врожденных пороков, в том числе пороков сердца. Большое количество
данных о применении осельтамивира у беременных женщин не указывает на
наличие фето/неонатальной токсичности осельтамивира и влияния на риск
пороков развития.
Отсутствуют данные о
влиянии осельтамивира на репродуктивную токсичность.
Применение препарата
Номидес при беременности возможно в случае необходимости и после
оценки имеющейся информации о безопасности и преимуществ терапии, а
также патогенности циркулирующего штамма вируса гриппа.
Кормление
грудью
Осельтамивир и
активный метаболит проникают в молоко. Данные по экскреции
осельтамивира с грудным молоком у человека и применению осельтамивира
кормящими женщинами ограничены. Ограниченные данные показывают, что
осельтамивир и его активный метаболит в небольших количествах
проникают в грудное молоко, создавая субтерапевтические концентрации
в крови младенца. При назначении осельтамивира кормящим женщинам
следует также учитывать имеющиеся сопутствующие заболевания и
патогенность циркулирующего штамма вируса гриппа. В период грудного
вскармливания осельтамивир применяют только в случае, если явные
ожидаемые преимущества лечения для кормящей матери превышают риски
для ребенка.
Особенности
влияния препарата на способность управлять транспортным средством или
потенциально опасными механизмами
Исследования по
изучению влияния лекарственного средства на способность управлять
транспортными средствами и заниматься другими потенциально опасными
видами деятельности, требующими повышенной концентрации внимания и
быстроты психомоторных реакций, не проводились. Исходя из профиля
безопасности, влияние осельтамивира на данные виды деятельности
маловероятно.
Рекомендации по
применению
Режим
дозирования
Взрослые
Лечение
Рекомендованная
доза для приема внутрь составляет 75 мг осельтамивира два раза в
сутки в течение 5 дней.
|
Масса |
Рекомендуемая |
|
˃ |
75 |
Лечение
необходимо начинать не позднее 2 суток с момента развития симптомов
гриппа.
Постконтактная
профилактика:
Рекомендованная
доза для профилактики гриппа после тесного контакта с больным гриппом
составляет 75 мг осельтамивира один раз в сутки в течение 10 дней.
Лечение необходимо начинать не позднее 2 суток от момента контакта с
больным.
|
Масса |
Рекомендуемая |
|
˃ |
75 |
Профилактика
во время эпидемии гриппа в сообществе:
для профилактики гриппа во время вспышки эпидемии рекомендовано
применение 75 мг осельтамивира один раз в сутки в течение 6 недель.
Инструкции по разовому
приготовлению суспензии приведены в разделе «Экстемпоральное
приготовление суспензии Номидес».
Особые
группы пациентов
Почечная
недостаточность
Лечение
гриппа: Для пациентов с почечной
недостаточностью средней и высокой степенью тяжести рекомендуется
снижение дозы препарата. В следующей таблице приведены рекомендации
по коррекции дозы у данных пациентов.
|
Клиренс |
Рекомендуемая |
|
>60 |
75 |
|
>30 |
30 |
|
>10 |
30 |
|
≤10 |
Не |
|
Пациенты, |
30 |
|
Пациенты, |
30 |
* ожидается,
что клиренс осельтамивира карбоксилата повышается при использовании
режима автоматического перитонеального диализа (АПД). Режим терапии
можно менять с ХАПД на АПД, если это необходимо по мнению нефролога.
Профилактика
гриппа: в следующей таблице содержатся
рекомендации по коррекции дозы препарата при профилактике гриппа у
пациентов со средней и тяжелой почечной недостаточностью.
|
Клиренс |
Рекомендуемая |
|
>60 |
75 |
|
>30 |
30 |
|
>10 |
30 |
|
≤10 |
Не |
|
Пациенты, |
30 |
|
Пациенты, |
30 |
* Данные
получены в исследованиях с участием пациентов, находящихся на
хроническом амбулаторном перитонеальном диализе (ХАПД); ожидается,
что клиренс осельтамивира карбоксилата повышается при использовании
режима автоматического перитонеального диализа (АПД). Режим терапии
можно менять с ХАПД на АПД, если это необходимо по мнению нефролога.
Пациенты
с печеночной недостаточностью
Коррекции
дозы при лечении и профилактике гриппа у пациентов с нарушением
функции печени легкой и средней степени тяжести не требуется.
Безопасность и фармакокинетика осельтамивира у пациентов с тяжелыми
нарушениями функции печени не изучалась.
Больные
пожилого и старческого возраста
Коррекции
дозы для профилактики или лечения гриппа не требуется.
Пациенты
с ослабленным иммунитетом (после трансплантации)
Лечение
Рекомендованная
доза осельтамивира составляет 75 мг 2 раза в сутки внутрь у взрослых
пациентов. Прием препарата необходимо начинать не позднее 2 суток с
момента развития симптомов заболевания.
Сезонная
профилактика
Для
сезонной профилактики гриппа у больных с ослабленным иммунитетом в
течение 12 недель, коррекции дозы не требуется.
Метод
и путь введения
Препарат
предназначен для приема внутрь.
Пациентам,
которые не могут проглотить капсулу, можно назначать соответствующие
дозы препарата Номидес в виде суспензии для приема внутрь (6 мг/мл).
Экстемпоральное приготовление
суспензии Номидес
В
случаях, когда у взрослых существует проблема с проглатыванием капсул
и отсутствует доступ к готовой пероральной суспензии, то необходимо
открыть капсулу и смешать её содержимое не более чем с одной чайной
ложкой подходящего подслащенного продукта питания (сахарная вода) для
того, чтобы скрыть горький вкус. Смесь необходимо тщательно
перемешать и дать пациенту целиком. Следует проглотить смесь сразу же
после приготовления.
Капсулы
75 мг
Если
пациентам требуется доза 75
мг, то
необходимо следовать следующим инструкциям:
1.
Держа одну капсулу 75 мг Номидес над маленькой емкостью,
аккуратно раскрыть капсулу и высыпать порошок в емкость.
2.
Добавить небольшое количество (не более 1 чайной ложки) подходящего
подслащенного продукта питания (чтобы скрыть горький вкус) и хорошо
перемешать.
3.
Тщательно перемешать смесь и выпить ее сразу же после приготовления.
Если в емкости осталось небольшое количество смеси, то следует
ополоснуть емкость небольшим количеством воды и выпить оставшуюся
смесь.
Если
пациентам требуются дозы 30-60
мг, то для
правильного дозирования необходимо следовать следующим инструкциям:
1.
Держа одну капсулу 75 мг препарата Номидес над маленькой
емкостью, аккуратно раскрыть капсулу и высыпать порошок в емкость.
2.
Добавить в порошок 5 мл воды с помощью шприца с метками,
показывающими количество набранной жидкости. Тщательно перемешать в
течение 2 минут.
3.
Набрать в шприц необходимое количество смеси из емкости согласно
нижеприведенной таблице:
|
Масса |
Рекомендованная |
Количество |
|
>23-40 |
60 |
4 |
Нет
необходимости в заборе нерастворенного белого порошка, поскольку он
является неактивным наполнителем. Нажав на поршень шприца, ввести все
его содержимое во вторую емкость. Оставшуюся неиспользованную смесь
необходимо выбросить.
4.
Во вторую емкость добавить небольшое количество (не более 1 чайной
ложки) подходящего подслащенного продукта питания, чтобы скрыть
горький вкус, и хорошо перемешать.
5.
Тщательно перемешать смесь и выпить ее сразу же после приготовления.
Если в емкости осталось небольшое количество смеси, то следует
ополоснуть емкость небольшим количеством воды и выпить оставшуюся
смесь.
Данную
процедуру следует повторять перед каждым приемом препарата.
Капсулы
30 мг и 45 мг
Для
правильного дозирования необходимо следовать следующим инструкциям:
1.
Определить необходимое количество капсул Номидес, требующееся для
приготовления смеси:
|
Масса |
Количество |
Количество |
|
>23-40 |
2 |
2 |
*Пациенты
с массой тела >40 кг в возрасте от 18 лет и взрослые могут
получать Номидес, используя для приготовления смеси одну капсулу 45
мг + одну капсулу 30 мг 2 раза в сутки для лечения или 1 раз в
сутки для профилактики.
2.
Убедитесь, что используется правильная доза препарата (в соответствии
с вышеприведенной таблицей). Держа одну или несколько капсул
Номидес над маленькой емкостью, аккуратно раскрыть одну или
несколько капсул и высыпать порошок в емкость.
3.
Добавить небольшое количество (не более 1 чайной ложки)
подходящего подслащенного продукта питания, чтобы скрыть горький
вкус, и хорошо перемешать.
4.
Тщательно перемешать смесь и выпить ее сразу же после приготовления.
Если в емкости осталось небольшое количество смеси, то следует
ополоснуть емкость небольшим количеством воды и выпить оставшуюся
смесь.
Повторяйте
данную процедуру перед каждым приемом препарата.
Меры,
которые необходимо принять в случае передозировки
Большинство
случаев передозировки, о которых сообщалось, не сопровождалось
какими-либо нежелательными явлениями. Нежелательные реакции в случаях
передозировки были аналогичны и сопоставимы по частоте возникновения
с нежелательными реакциями, наблюдавшимися при применении препарата в
терапевтических дозах, перечисленными в разделе «Нежелательные
реакции».
Специфический
антидот неизвестен.
Рекомендации
по обращению за консультацией к медицинскому работнику для
разъяснения способа применения лекарственного препарата
Рекомендовано
обратиться за консультацией к медицинскому работнику для разъяснения
способа применения лекарственного препарата.
Описание
нежелательных реакций, которые проявляются при стандартном применении
ЛП и меры, которые следует принять в этом случае
Очень
часто
—
головная боль
—
тошнота
Часто
—
бронхит, простой герпес, назофарингит, инфекции верхних дыхательных
путей, синусит
—
бессонница
—
кашель, боль в горле, ринорея
—
рвота, боль в животе (включая боль в верхнем отделе брюшной полости),
диспепсия
-
боль, головокружение (включая
вестибулярное), усталость, гипертермия, боль в конечностях
Нечасто
—
реакции гиперчувствительности
—
помутнение сознания, судороги
—
нарушения сердечного ритма
—
экзема, дерматит, сыпь, крапивница
Редко
—
тромбоцитопения
—
анафилактические реакции, анафилактоидные реакции
—
возбуждение, необычное поведение, тревожность, спутанность сознания,
мания, бред, галлюцинации, кошмары, членовредительство
—
зрительное расстройство
—
желудочно– кишечные кровотечения, геморрагический колит
—
ангионевротический отек, мультиформная эритема, синдром
Стивенса-Джонсона, токсический эпидермальный некролиз
При
возникновении нежелательных лекарственных реакций обращаться к
медицинскому работнику, фармацевтическому работнику или напрямую в
информационную базу данных по нежелательным реакциям (действиям) на
лекарственные препараты, включая сообщения о неэффективности
лекарственных препаратов
РГП
на ПХВ «Национальный центр экспертизы лекарственных средств и
медицинских изделий» Комитет контроля качества и безопасности
товаров и услуг Министерства здравоохранения Республики Казахстан
http://www.ndda.kz
Дополнительные
сведения
Состав
лекарственного препарата
Одна
капсула содержит
активное
вещество – осельтамивир, 30 мг,
45 мг, 75 мг
(в
виде осельтамивира фосфата, 39,4 мг, 59,1 мг, 98,5 мг)
вспомогательные
вещества: кремния диоксид коллоидный
(аэросил), коповидон, крахмал прежелатинизированный, кроскармеллоза
натрия, натрия стеарилфумарат, тальк.
состав
капсул:
для
дозировки 30 мг: натрия лаурилсульфат, титана диоксид (Е171), вода
очищенная, желатин;
для
дозировки 45 мг: натрия лаурилсульфат, титана диоксид (Е171),
краситель бриллиантовый голубой (Е133), вода очищенная, желатин;
для
дозировки 75 мг: натрия лаурилсульфат, титана диоксид (Е171),
краситель солнечный закат желтый (Е110), краситель пунцовый
[Понсо 4R] (Е124), вода очищенная, желатин.
Описание
внешнего вида, запаха, вкуса
Для
дозировки 30 мг: твердые желатиновые капсулы № «3»,
корпус белого цвета, крышечка белого цвета.
Для
дозировки 45 мг: твердые желатиновые капсулы № «2»,
корпус голубого цвета, крышечка голубого цвета.
Для
дозировки 75 мг: твердые желатиновые капсулы № «1»,
корпус белого цвета, крышечка оранжевого цвета.
Содержимое
капсул – белый или белый с желтоватым оттенком порошок.
Форма выпуска и упаковка
По
5 или 10 капсул в контурную ячейковую упаковку из пленки
поливинилхлоридной и фольги алюминиевой печатной лакированной
По
20, 30 капсул в банку полимерную из полиэтилена низкого давления с
крышкой натягиваемой с контролем первого вскрытия из полиэтилена
высокого давления. Свободное пространство заполняют ватой
медицинской. На банки наклеивают этикетки из бумаги этикеточной или
писчей или из полимерных материалов, самоклеющиеся.
По
1 или 2 контурной ячейковой упаковке вместе с инструкцией по
применению помещают в пачку из картона для потребительской тары.
Пачки помещают в групповую упаковку. Пачки помещают в групповую
упаковку.
По
1 банке вместе с инструкцией по применению помещают в пачку из
картона для потребительской тары. Пачки помещают в групповую упаковку
Срок хранения
Срок
хранения 3 года.
Не
применять по истечении срока годности!
Условия хранения
Хранить
в оригинальной упаковке при температуре не выше 25 °С.
Хранить
в недоступном для детей месте!
Условия отпуска из аптек
По
рецепту.
Сведения
о производителе
АО
«Фармасинтез», Россия.
Юридический
адрес: 664007, г. Иркутск, ул. Красногвардейская,
д. 23, оф. 3.
тел.:
+7 (3952) 550-355
факс:
+7 (3952) 550-325
адрес
электронной почты: info@pharmasyntez.com
Владелец регистрационного удостоверения
АО
«Фармасинтез», Россия.
Юридический
адрес: 664007, г. Иркутск, ул. Красногвардейская,
д. 23, оф. 3.
тел.:
+7 (3952) 550-355
факс:
+7 (3952) 550-325
адрес
электронной почты info@pharmasyntez.com
Наименование,
адрес и контактные данные (телефон, факс, электронная почта)
организации на территории Республики Казахстан, принимающей претензии
(предложения) по качеству лекарственных средств от потребителей и
ответственная ответственной за пострегистрационное наблюдение за
безопасностью лекарственного средства
г.
Алматы,
ТОО
«СonsultAsia»
ул.
Шевченко 165 Б
адрес
электронной почты: registration@consultingasia.kz
pv@consultingasia.kz
Тел/факс:
+77051708825/+727-3794258
| ЛВ_Номидес_итог_рус.docx | 0.06 кб |
| Номидес_каз.docx | 0.06 кб |
Отправить прикрепленные файлы на почту
Одна капсула содержит
активное вещество – осельтамивир, 30 мг, 45 мг, 75 мг
(в виде осельтамивира фосфата, 39,4 мг, 59,1 мг, 98,5 мг)
вспомогательные вещества: кремния диоксид коллоидный (аэросил), коповидон, крахмал прежелатинизированный, кроскармеллоза натрия, натрия стеарилфумарат, тальк.
состав капсул:
для дозировки 30 мг: натрия лаурилсульфат, титана диоксид (Е171), вода очищенная, желатин;
для дозировки 45 мг: натрия лаурилсульфат, титана диоксид (Е171), краситель бриллиантовый голубой (Е133), вода очищенная, желатин;
для дозировки 75 мг: натрия лаурилсульфат, титана диоксид (Е171), краситель солнечный закат желтый (Е110), краситель пунцовый [Понсо 4R] (Е124), вода очищенная, желатин.
Для дозировки 30 мг: твердые желатиновые капсулы № «3», корпус белого цвета, крышечка белого цвета.
Для дозировки 45 мг: твердые желатиновые капсулы № «2», корпус голубого цвета, крышечка голубого цвета.
Для дозировки 75 мг: твердые желатиновые капсулы № «1», корпус белого цвета, крышечка оранжевого цвета.
Содержимое капсул – белый или белый с желтоватым оттенком порошок.
Противоинфекционные препараты для системного использования. Противовирусные препараты для системного применения. Противовирусные препараты прямого действия. Ингибиторы нейраминидазы. Осельтамивир.
Код АТХ J05AH02
Лечение гриппа
Препарат Номидес показан для лечения взрослых и детей, включая доношенных новорожденных, у которых наблюдаются характерные симптомы гриппа во время вспышки гриппа (за исключением капсул препарата Номидес, 75 мг, поскольку содержат краситель солнечный закат желтый (E110), который противопоказан к применению детям в возрасте до 18 лет). Доказано, что препарат обеспечивает терапевтический эффект, если лечение начинается в течение первых двух дней с момента появления симптомов.
Профилактика гриппа
– постконтактная профилактика у детей старше 1 года и старше после контакта с больным с подтвержденным клиническим диагнозом гриппа во время вспышки заболевания (за исключением капсул препарата Номидес, 75 мг, поскольку содержат краситель солнечный закат желтый (E110), который противопоказан к применению детям в возрасте до 18 лет).
– соответствующий порядок применения препарата Номидес для профилактики гриппа определяется в каждом конкретном случае, исходя из конкретных обстоятельств и характеристик популяции, требующей профилактической защиты. В исключительных случаях (например, если имеет место несовпадение циркулирующего штамма вируса и штамма, содержащегося в вакцине, или в случае пандемии) можно рассмотреть возможность назначения сезонной профилактики некоторым детям в возрасте от 1 года и старше (за исключением капсул препарата Номидес, 75 мг, поскольку содержат краситель солнечный закат желтый (E110), который противопоказан к применению детям в возрасте до 18 лет).
– препарат Номидес показан для постконтактной профилактики гриппа у детей в возрасте до 1 года во время вспышки пандемии гриппа (за исключением капсул препарата Номидес, 75 мг, поскольку содержат краситель солнечный закат желтый (E110), который противопоказан к применению детям в возрасте до 18 лет).
Препарат Номидес не является заменой вакцинации.
Применение противовирусных препаратов для лечения и профилактики гриппа должно проводиться на основании официальных рекомендаций. Решение об использовании осельтамивира для лечения и профилактики гриппа должно приниматься с учетом известных характеристик циркулирующих штаммов вируса, имеющейся информации о лекарственной чувствительности для каждого сезона и влиянии, оказываемом заболеванием в различных географических регионах и популяциях пациентов.
— гиперчувствительность к действующему веществу или к любому из вспомогательных веществ.
— противопоказано детям до 18 лет в дозировке 75 мг (капсулы содержат краситель солнечный закат желтый (E110), который противопоказан к применению детям в возрасте до 18 лет).
С осторожностью применять во время беременности и в период грудного вскармливания.
Клинически значимые лекарственные взаимодействия маловероятны. Осельтамивира фосфат в высокой степени превращается в активный метаболит под действием эстераз, в основном расположенных в печени. Лекарственные взаимодействия, обусловленные конкуренцией за связывание с активными центрами эстераз, в литературных источниках широко не представлены. Низкая степень связывания осельтамивира и активного метаболита с белками плазмы не дают оснований предполагать наличие взаимодействий, связанных с вытеснением лекарственных средств из связи с белками.
Ни осельтамивира фосфат, ни его активный метаболит не являются предпочтительным субстратом для полифункциональных оксидаз системы цитохрома P450 или для глюкуронилтрансфераз. Оснований для взаимодействия с пероральными контрацептивами нет.
Циметидин, неспецифический ингибитор изофермента системы цитохрома P450 и конкурирующий в процессе канальцевой секреции с препаратами щелочного типа и катионами, не влияет на плазменные концентрации осельтамивира и его активного метаболита.
Маловероятны клинически значимые межлекарственные взаимодействия, связанные с конкуренцией за канальцевую секрецию, принимая во внимание резерв безопасности для большинства подобных препаратов, пути выведения активного метаболита осельтамивира (клубочковая фильтрация и анионная канальцевая секреция), а также выводящую способность каждого из путей.
Пробенецид приводит к увеличению AUC активного метаболита осельтамивира примерно в 2 раза (за счет снижения активной канальцевой секреции в почках). Однако коррекции дозы при одновременном применении с пробенецидом не требуется, учитывая резерв безопасности активного метаболита.
Одновременный прием с амоксициллином не влияет на плазменные концентрации осельтамивира и его компонентов, демонстрируя слабую конкуренцию за выведение путем анионной канальцевой секреции.Одновременный прием с парацетамолом
не влияет на плазменные концентрации осельтамивира и его активного метаболита или парацетамола.
Фармакокинетических взаимодействий между осельтамивиром, его основным метаболитом не обнаружено при одновременном приеме с парацетамолом, ацетилсалициловой кислотой, циметидином или антацидными средствами (магния и алюминия гидроксид, кальция карбонат), варфарином, римантадином или амантадином.
При использовании осальтемивира с часто применяемыми препаратами, такими как ингибиторы ангиотензинпревращающего фермента (эналаприл, каптоприл), тиазидные диуретики (бендрофлуметиазид), антибиотики (пенициллин, цефалоспорины, азитромицин, эритромицин и доксициклин), блокаторы Н2-гистаминовых рецепторов (ранитидин, циметидин), бета-адреноблокаторы (пропранолол), ксантины (теофиллин), симпатомиметики (псевдоэфедрин), опиаты (кодеин), глюкокортикостероиды, ингаляционные бронхолитики и ненаркотические анальгетики (ацетилсалициловая кислота, ибупрофен и парацетамол), изменений характера или частоты нежелательных явлений не наблюдалось.
Применять осельтамивир в комбинации с препаратами, имеющими узкую широту терапевтического действия (например, хлорпропамид, метотрексат, бутадион), необходимо с осторожностью.
Осельтамивир эффективен только в отношении заболевания, вызванного вирусом гриппа.
Данные об эффективности осельтамивира в терапии заболеваний, вызванных иными агентами, отсутствуют.
Применение препарата Номидес не является заменой вакцинации
. Использование препарата Номидес не должно влиять на оценку пациентов при проведении ежегодной вакцинации против гриппа. Защита от гриппа длится только до тех пор, пока применяется препарат Номидес. Препарат следует использовать только для лечения и профилактики гриппа и только в случае, если достоверные эпидемиологические данные указывают на то, что вирус гриппа циркулирует в общей популяции. Чувствительность циркулирующих штаммов вируса гриппа к осельтамивиру может сильно варьировать. Таким образом, при назначении препарата необходимо учитывать самую последнюю доступную информацию о чувствительности циркулирующего вируса к осельтамивиру.
Тяжелые сопутствующие заболевания
Данные о безопасности и эффективности применения осельтамивира у пациентов с достаточно тяжелым сопутствующим заболеванием или нестабильным состоянием, предполагающим госпитализацию, отсутствуют.
Пациенты с ослабленным иммунитетом
Эффективность осельтамивира при лечении или профилактике гриппа у пациентов с ослабленным иммунитетом четко не установлена. Однако у взрослых пациентов с ослабленным иммунитетом лечение гриппа следует проводить на протяжении 10 дней, так как исследований применения препарата при менее продолжительном курсе терапии не проводилось.
Заболевания сердца и органов дыхания
Эффективность осельтамивира при лечении или профилактике гриппа у пациентов с хроническими заболеваниями сердца и/или органов дыхания не установлена. В данной популяции пациентов частота возникновения осложнений была сопоставима с таковой в группе лечения осельтамивиром и в группе плацебо.
Дети
Данные для определения дозы у недоношенных детей (постконцептуальный возраст <36 недель) отсутствуют.
Тяжелая почечная недостаточность
У взрослых пациентов и подростков (13-17 лет) с тяжелой степенью почечной недостаточности при лечении и профилактике гриппа рекомендуется коррекция дозы. Клинических данных для коррекции дозы у младенцев и детей (в возрасте от 1 года и старше) с почечной недостаточностью недостаточно, поэтому определить режим дозирования для данной категории пациентов не представляется возможным (см. раздел «Режим дозирования»).
Психоневрологические нарушения
У пациентов (в основном у детей и подростков), принимавших осельтамивир, были зарегистрированы психоневрологические нарушения. Подобные психоневрологические нарушения так же отмечены у пациентов с гриппом, не получавших осельтамивир.
Следует тщательно мониторировать пациентов на предмет изменений в поведении, риск и польза продолжения терапии должны быть оценены для каждого пациента индивидуально.
Натрий
Данный лекарственный препарат содержит менее 1 ммоль (23 мг) в одной капсуле, т. е. практически не содержит натрия.
Лекарственное средство Номидес, 75 мг, капсулы, содержит краситель солнечный закат желтый (E110), запрещенный к применению в лекарственных препаратах для детей. В этой связи детям и подросткам в возрасте до 18 лет осельтамивир следует принимать в виде капсул в дозировке 45 мг и 30 мг, или в виде суспензии для приема внутрь 6 мг/мл (см. раздел «Экстемпоральное приготовление суспензии Номидес»).
При беременности и в период грудного вскармливания осельтамивир применяют только в случае, если предполагаемая польза для матери превышает потенциальный риск для плода и ребенка.
Беременность
Заболевание гриппом связано с неблагоприятным течением беременности, может вызывать аномалии развития плода, а также является риском развития серьезных врожденных пороков, в том числе пороков сердца. Большое количество данных о применении осельтамивира у беременных женщин не указывает на наличие фето/неонатальной токсичности осельтамивира и влияния на риск пороков развития.
Отсутствуют данные о влиянии осельтамивира на репродуктивную токсичность.
Применение препарата Номидес при беременности возможно в случае необходимости и после оценки имеющейся информации о безопасности и преимуществ терапии, а также патогенности циркулирующего штамма вируса гриппа.
Кормление грудью
Осельтамивир и активный метаболит проникают в молоко. Данные по экскреции осельтамивира с грудным молоком у человека и применению осельтамивира кормящими женщинами ограничены. Ограниченные данные показывают, что осельтамивир и его активный метаболит в небольших количествах проникают в грудное молоко, создавая субтерапевтические концентрации в крови младенца. При назначении осельтамивира кормящим женщинам следует также учитывать имеющиеся сопутствующие заболевания и патогенность циркулирующего штамма вируса гриппа. В период грудного вскармливания осельтамивир применяют только в случае, если явные ожидаемые преимущества лечения для кормящей матери превышают риски для ребенка.
Исследования по изучению влияния лекарственного средства на способность управлять транспортными средствами и заниматься другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций, не проводились. Исходя из профиля безопасности, влияние осельтамивира на данные виды деятельности маловероятно.
Режим дозирования
Взрослым, которые по каким-либо причинам не могут глотать капсулы, или которым требуются меньшие дозы препарата, а также детям и подросткам в возрасте до 18 лет, препарат Номидес следует принимать в виде суспензии для приема внутрь 6 мг/мл (см. раздел «Экстемпоральное приготовление суспензии Номидес»). Детям и подросткам в возрасте до 18 лет также можно принимать капсулы препарата Номидес в дозировке 30 мг и 45 мг.
Взрослые и подростки в возрасте 13 лет и старше
Лечение:
Рекомендуемая пероральная доза осельтамивира для взрослых и подростков (13-17 лет): 75 мг два раза в сутки в течение 5 дней.
| Масса тела | Рекомендуемая доза в течение 5 дней |
| ˃ 40 кг | 75 мг два раза в сутки |
Лечение следует начинать как можно быстрее в течение первых двух дней после возникновения симптомов гриппа.
Постконтактная профилактика:
Рекомендуемая профилактическая доза после близкого контакта с больным гриппом для взрослых и подростков (13-17 лет): 75 мг осельтамивира один раз в сутки в течение 10 дней.
| Масса тела | Рекомендуемая доза в течение 10 дней |
| ˃40 кг | 75 мг два раза в сутки |
Лечение следует начинать как можно быстрее в течение первых двух дней после возникновения симптомов гриппа.
Постконтактная профилактика: Рекомендуемая профилактическая доза после близкого контакта с больным гриппом для взрослых и подростков (13-17 лет): 75 мг осельтамивира один раз в сутки в течение 10 дней.
| Масса тела | Рекомендуемая доза в течение 10 дней |
| >40 кг | 75 мг один раз в сутки |
Лечение следует начинать как можно быстрее в течение первых двух дней после контакта с заболевшим.
Профилактика во время эпидемии гриппа: Рекомендуемая профилактическая доза во время вспышек гриппа: 75 мг осельтамивира один раз в сутки в течение максимум 6 недель.
Дети
Дети в возрасте 1-12 лет
Для лечения и профилактики детей в возрасте от 1 года и старше могут использоваться капсулы Номидес 75 мг, 40 мг и 30 мг и суспензия для приема внутрь (6 мг/мл) (см. раздел «Экстемпоральное приготовление суспензии Номидес»).
Лечение: Для лечения детей младшего и среднего возраста (от 1 года и старше) рекомендуется использовать следующие режимы дозирования в зависимости от веса ребенка:
| Масса тела | Рекомендуемая доза в течение 5 дней |
| 10 — 15 кг | 30 мг два раза в сутки |
| от >15 кг до 23 кг | 45 мг два раза в сутки |
| от >23 кг до 40 кг | 60 мг два раза в сутки |
| >40 кг | 75 мг два раза в сутки |
Лечение следует начинать как можно быстрее в течение первых двух дней после возникновения симптомов гриппа.
Постконтактная профилактика: Рекомендуемая доза препарата Номидес после контакта с больным:
| Масса тела | Рекомендуемая доза в течение 10 дней |
| 10 — 15 кг | 30 мг один раз в сутки |
| от >15 кг до 23 кг | 45 мг один раз в сутки |
| от >23 кг до 40 кг | 60 мг один раз в сутки |
| >40 кг | 75 мг один раз в сутки |
Профилактика во время эпидемии гриппа: Исследования профилактического применения препарата во время эпидемии гриппа у детей в возрасте до 12 лет не проводились.
Младенцы в возрасте 0 – 12 месяцев
Лечение: Рекомендуемая доза для лечения младенцев в возрасте 0-12 месяцев: 3 мг/кг два раза в сутки. Рекомендации по дозированию основаны на результатах исследований фармакокинетики и безопасности осельтамивира, согласно которым доза 3 мг/кг у детей указанного возраста позволяет получить такие концентрации пролекарства и активного метаболита в плазме, которые, предположительно, являются клинически эффективными и обеспечивают профиль безопасности, сравнимый с профилем, наблюдаемым у детей и подростков более старшего возраста. Для лечения младенцев в возрасте 0-12 месяцев рекомендуется использовать следующий режим дозирования:
| Масса тела* | Рекомендуемая доза в течение 5 дней |
| 3 кг | 9 мг два раза в сутки |
| 4 кг | 12 мг два раза в сутки |
| 5 кг | 15 мг два раза в сутки |
| 6 кг | 18 мг два раза в сутки |
| 7 кг | 21 мг два раза в сутки |
| 8 кг | 24 мг два раза в сутки |
| 9 кг | 27 мг два раза в сутки |
| 10 кг | 30 мг два раза в сутки |
* Данная таблица может не содержать все возможные варианты массы тела для указанной популяции. Для всех пациентов во возрасте до 1 года доза должна определяться исходя из соотношения 3 мг/кг массы тела.
Лечение следует начинать как можно быстрее в течение первых двух дней после возникновения симптомов гриппа.
Рекомендации, приведенные выше, не применимы для недоношенных младенцев (возраст после зачатия <36 недель). Для данной популяции пациентов отсутствует достаточный объем данных, учитывая, что таким детям может потребоваться иной режим дозирования по причине несовершенства физиологических функций.
Постконтактная профилактика: Рекомендуемая профилактическая доза у детей в возрасте до 1 года во время вспышки гриппа: половина суточной дозы, используемой для лечения гриппа. Рекомендации по дозированию основана на клинических данных, полученных у младенцев в возрасте 0-12 месяцев, детей старше 1 года и взрослых, согласно которым профилактическая доза, эквивалентная половине суточной дозы, используемой для лечения гриппа, является клинически эффективной для профилактики гриппа. Для младенцев в возрасте 0-12 месяцев рекомендуется профилактический режим дозирования, из расчета массы тела ребенка:
| Возраст | Рекомендуемая доза в течение 10 дней |
| 0 — 12 месяцев | 3 мг/кг один раз в сутки |
Рекомендации, приведенные выше, не применимы для недоношенных младенцев (возраст после зачатия <36 недель). Для данной популяции пациентов отсутствует достаточный объем данных, учитывая, что таким детям может потребоваться иной режим дозирования по причине несовершенства физиологических функций.
Профилактика во время эпидемии гриппа: Исследования профилактического применения препарата во время эпидемии гриппа у детей в возрасте 0-12 месяцев не проводились.
Инструкции по разовому приготовлению суспензии приведены в разделе «Экстемпоральное приготовление суспензии Номидес».
Особые группы пациентов
Печеночная недостаточность
Коррекция дозы препарата при лечении и профилактике гриппа у пациентов с нарушением функции печени не требуется. Исследования с участием пациентов детского возраста с печеночной недостаточностью не проводились.
Почечная недостаточность
Лечение гриппа: Для взрослых и подростков (13-17 лет) с почечной недостаточностью средней и высокой степенью тяжести рекомендуется снижение дозы препарата. В следующей таблице приведены рекомендации по коррекции дозы у данных пациентов.
| Клиренс креатинина | Рекомендуемая доза (лечение) |
| >60 (мл/мин) | 75 мг два раза в сутки |
| >30 — 60 (мл/мин) | 30 мг (суспензия) два раза в сутки |
| >10 — 30 (мл/мин) | 30 мг (суспензия) один раз в сутки |
| £10 (мл/мин) | Не рекомендуется (данные отсутствуют) |
| Пациенты, получающие гемодиализ | 30 мг после каждого сеанса гемодиализа |
| Пациенты, получающие перитонеальный диализ* | 30 мг (суспензия) – разовая доза |
* Данные получены в исследованиях с участием пациентов, находящихся на хроническом амбулаторном перитонеальном диализе (ХАПД); ожидается, что клиренс осельтамивира карбоксилата повышается при использовании режима автоматического перитонеального диализа (АПД). Режим терапии можно менять с ХАПД на АПД, если это необходимо по мнению нефролога.
Профилактика гриппа: в следующей таблице содержатся рекомендации по коррекции дозы препарата при профилактике гриппа у взрослых и подростков (13-17 лет) со средней и тяжелой почечной недостаточностью.
| Клиренс креатинина | Рекомендуемая доза (лечение) |
| >60 (мл/мин) | 75 мг два раза в сутки |
| >30 — 60 (мл/мин) | 30 мг (суспензия) один раз в сутки |
| >10 — 30 (мл/мин) | 30 мг (суспензия) через день |
| ≤10 (мл/мин) | Не рекомендуется (данные отсутствуют) |
| Пациенты, получающие гемодиализ | 30 мг после каждого второго сеанса гемодиализа |
| Пациенты, получающие перитонеальный диализ* | 30 мг (суспензия) – один раз в неделю |
* Данные получены в исследованиях с участием пациентов, находящихся на хроническом амбулаторном перитонеальном диализе (ХАПД); ожидается, что клиренс осельтамивира карбоксилата повышается при использовании режима автоматического перитонеального диализа (АПД). Режим терапии можно менять с ХАПД на АПД, если это необходимо по мнению нефролога.
Существует недостаточно клинических данных по применению осельтамивира у младенцев и детей младшего возраста (до 12 лет) с почечной недостаточностью. Рекомендации по дозированию у данной группы пациентов отсутствуют.
Пожилые
Коррекция дозы не требуется за исключением случаев, когда у пациента имеются признаки умеренной или тяжелой степени почечной недостаточности.
Пациенты с ослабленным иммунитетом
Лечение: взрослым рекомендуемая доза составляет 75 мг 2 раза в сутки в течение 10 дней. Лечение следует начать как можно быстрее в течение первых двух дней после возникновения симптомов гриппа.
Сезонная профилактика: у пациентов с ослабленным иммунитетом оценивалась долговременная сезонная профилактика продолжительностью до 12 недель.
Метод и путь введения
Препарат предназначен для приема внутрь.
Пациентам, которые не могут проглотить капсулу, можно назначать соответствующие дозы препарата Номидес в виде суспензии для приема внутрь (6 мг/мл).
Экстемпоральное приготовление суспензии Номидес
В случаях, когда у взрослых существует проблема с проглатыванием капсул и отсутствует доступ к готовой пероральной суспензии, то необходимо открыть капсулу и смешать её содержимое не более чем с одной чайной ложкой подходящего подслащенного продукта питания (сахарная вода) для того, чтобы скрыть горький вкус. Смесь необходимо тщательно перемешать и дать пациенту целиком. Следует проглотить смесь сразу же после приготовления.
Капсулы 75 мг
Если пациентам требуется доза 75 мг, то необходимо следовать следующим инструкциям:
1. Держа одну капсулу 75 мг Номидес над маленькой емкостью, аккуратно раскрыть капсулу и высыпать порошок в емкость.
2. Добавить небольшое количество (не более 1 чайной ложки) подходящего подслащенного продукта питания (чтобы скрыть горький вкус) и хорошо перемешать.
3. Тщательно перемешать смесь и выпить ее сразу же после приготовления. Если в емкости осталось небольшое количество смеси, то следует ополоснуть емкость небольшим количеством воды и выпить оставшуюся смесь.
Если пациентам требуются дозы 30-60 мг, то для правильного дозирования необходимо следовать следующим инструкциям:
1. Держа одну капсулу 75 мг препарата Номидес над маленькой емкостью, аккуратно раскрыть капсулу и высыпать порошок в емкость.
2. Добавить в порошок 5 мл воды с помощью шприца с метками, показывающими количество набранной жидкости. Тщательно перемешать в течение 2 минут.
3. Набрать в шприц необходимое количество смеси из емкости согласно нижеприведенной таблице:
|
Масса тела |
Рекомендованная доза |
Количество смеси Номидес на один прием |
| >23-40 кг | 60 мг | 4 мл |
Нет необходимости в заборе нерастворенного белого порошка, поскольку он является неактивным наполнителем. Нажав на поршень шприца, ввести все его содержимое во вторую емкость. Оставшуюся неиспользованную смесь необходимо выбросить.
4. Во вторую емкость добавить небольшое количество (не более 1 чайной ложки) подходящего подслащенного продукта питания, чтобы скрыть горький вкус, и хорошо перемешать.
5. Тщательно перемешать смесь и выпить ее сразу же после приготовления. Если в емкости осталось небольшое количество смеси, то следует ополоснуть емкость небольшим количеством воды и выпить оставшуюся смесь.
Данную процедуру следует повторять перед каждым приемом препарата.
Капсулы 30 мг и 45 мг
Для правильного дозирования необходимо следовать следующим инструкциям:
1. Определить необходимое количество капсул Номидес, требующееся для приготовления смеси:
| Масса тела* | Количество капсул Номидес для обеспечения рекомендованной дозы с целью лечения в течение 5 дней | Количество капсул Номидес для обеспечения рекомендованной дозы с целью профилактики |
| >23-40 кг | 2 капсулы 30 мг 2 раза/сут | 2 капсулы 30 мг 1 раз/сут |
*Пациенты с массой тела >40 кг в возрасте от 18 лет и взрослые могут получать Номидес, используя для приготовления смеси одну капсулу 45 мг + одну капсулу 30 мг 2 раза в сутки для лечения или 1 раз в сутки для профилактики.
2. Убедитесь, что используется правильная доза препарата (в соответствии с вышеприведенной таблицей). Держа одну или несколько капсул Номидес над маленькой емкостью, аккуратно раскрыть одну или несколько капсул и высыпать порошок в емкость.
3. Добавить небольшое количество (не более 1 чайной ложки) подходящего подслащенного продукта питания, чтобы скрыть горький вкус, и хорошо перемешать.
4. Тщательно перемешать смесь и выпить ее сразу же после приготовления. Если в емкости осталось небольшое количество смеси, то следует ополоснуть емкость небольшим количеством воды и выпить оставшуюся смесь.
Повторяйте данную процедуру перед каждым приемом препарата.
Большинство случаев передозировки, о которых сообщалось, не сопровождалось какими-либо нежелательными явлениями. Нежелательные реакции в случаях передозировки были аналогичны и сопоставимы по частоте возникновения с нежелательными реакциями, наблюдавшимися при применении препарата в терапевтических дозах, перечисленными в разделе «Нежелательные реакции».
Специфический антидот неизвестен.
Рекомендации по обращению за консультацией к медицинскому работнику для разъяснения способа применения лекарственного препарата
Рекомендовано обратиться за консультацией к медицинскому работнику для разъяснения способа применения лекарственного препарата.
Очень часто
– головная боль
– тошнота
Часто
– бронхит, Herpes simplex, назофарингит, инфекции верхних дыхательных путей, синусит
– бессонница
– кашель, боль в горле, ринорея
– рвота, боль в животе (включая боль в верхней части живота), диспепсия
– боль, головокружение (включая вертиго), утомляемость, лихорадка, боль в конечностях
Нечасто
– реакции гиперчувствительности
– изменение сознания, судороги
– аритмия
– повышение активности «печеночных» ферментов
– экзема, дерматит, сыпь, крапивница
Редко
– тромбоцитопения
– анафилактические реакции, анафилактоидные реакции
– беспокойство, аномальное поведение, тревожность, спутанность сознания, бред, делирий, галлюцинации, ночные кошмары, причинение себе телесного повреждения
– нарушение зрения
– желудочно-кишечные кровотечения, геморрагический колит
– фульминантный гепатит, печеночная недостаточность, гепатит
– ангионевротический отек, мультиформная эритема, синдром Стивенса-Джонсона, токсический эпидермальный некролиз
Дополнительные нежелательные реакции у детей
Очень часто
– кашель, заложенность носа
– рвота
Часто
– средний отит
– головная боль
– конъюнктивит (включая покраснение глаз, выделения и боль)
– боль в ухе
– ринорея
– боль в животе (включая боль в верхней части живота), диспепсия, тошнота
Иногда
– нарушения со стороны барабанной перепонки
– дерматит (включая аллергический и атопический дерматит)
При возникновении нежелательных лекарственных реакций обращаться к медицинскому работнику, фармацевтическому работнику или напрямую в информационную базу данных по нежелательным реакциям (действиям) на лекарственные препараты, включая сообщения о неэффективности лекарственных препаратов
РГП на ПХВ «Национальный центр экспертизы лекарственных средств и медицинских изделий» http://www.ndda.kz
По 5 или 10 капсул в контурную ячейковую упаковку из пленки поливинилхлоридной и фольги алюминиевой печатной лакированной.
По 20, 30 капсул в банку полимерную с крышкой натягиваемой с контролем первого вскрытия.
По 1 или 2 контурной ячейковой упаковке вместе с инструкцией по применению помещают в пачку из картона для потребительской тары.
По 1 банке вместе с инструкцией по применению помещают в пачку из картона для потребительской тары.
5 лет.
Не применять по истечении срока годности!
Хранить в защищенном от света месте при температуре не выше 25 °С.
Хранить в недоступном для детей месте!
По рецепту.
Сведения о производителе
АО «Фармасинтез», Россия.
Юридический адрес: 664007, Иркутская обл., г. Иркутск, ул. Красногвардейская, д. 23, офис 3.
тел.: +7 (3952) 550-355
факс: +7 (3952) 550-325
адрес электронной почты: info@pharmasyntez.com
Держатель регистрационного удостоверения
АО «Фармасинтез», Россия.
Юридический адрес: 664007, Иркутская обл., г. Иркутск, ул. Красногвардейская, д. 23, офис 3.
тел.: +7 (3952) 550-355
факс: +7 (3952) 550-325
адрес электронной почты info@pharmasyntez.com
Наименование, адрес и контактные данные (телефон, факс, электронная почта) организации на территории Республики Казахстан, принимающей претензии (предложения) по качеству лекарственных средств от потребителей и ответственной за пострегистрационное наблюдение за безопасностью лекарственного средства
ТОО «Adalan»
Республика Казахстан, 050057, г. Алматы, ул. Тимирязева, 42, пав. 23, оф. 202.
Тел: +(727) 269 54 59, +(727) 269 54 18
Моб. (24 часа): +7 (701) 217 24 57
Адрес электронной почты: b.satova@adalan.kz; pv@adalan.kz
ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. ВОЗМОЖНЫ ПОБОЧНЫЕ ЭФФЕКТЫ. НЕОБХОДИМА КОНСУЛЬТАЦИЯ СПЕЦИАЛИСТА.В сезон простудПри простудеПротивовирусные каплиСредства от простуды
Автор статьи
Диплом о фармацевтическом образовании: 105924 1197876, рег. номер 30353
Все авторы
Содержание статьи
- Номидес: дозировка
- Номидес при ковиде
- Номидес: аналоги
- Номидес или Арбидол: что лучше?
- Краткое содержание
- Задайте вопрос эксперту по теме статьи
Противовирусные лекарства эффективны в первые дни после заражения. Они останавливают размножение вируса в организме и стимулируют иммунитет для успешной борьбы с ним. Препарат Номидес относится к средствам с прямым антивирусным действием. Он подавляет фермент, который отвечает за проникновение вируса в клетки и предотвращает его размножение.
Провизор Наталья Зотина рассказывает, как принимать Номидес, назначают ли его при коронавирусе, есть ли у лекарства аналоги и сравнивает с Арбидолом.
Номидес: дозировка
Препарат применяют для профилактики и лечения гриппа у взрослых и детей старше 1 года. Врачи советуют принимать лекарство во время еды, чтобы улучшить его переносимость. Прием пищи не влияет на действие Номидеса
Детский Номидес выпускают в виде порошка для приготовления суспензии для приема внутрь с дозировкой 12 мг/мл. Для удобства применения в комплект входит специальный дозирующий шприц. Для взрослых есть капсулы с дозировками 30 мг, 45 мг и 75 мг. Таблетки Номидес не производят.
Лечение начинают не позднее 2 дней после проявления первых симптомов. Схемы приема:
- взрослые и дети старше 8 лет — по 75 мг 2 раза в сутки 5 дней
- дети от 1 до 8 лет — рекомендованная доза в зависимости от веса ребенка 2 раза в сутки 5 дней
Для профилактика гриппа следует принимать Номидес не позднее двух суток после контакта с заболевшим:
- взрослые и дети старше 12 лет — 75 мг один раз в сутки не менее 10 дней, в период эпидемии гриппа — 6 недель
- дети от 8 до 12 лет — 75 мг один раз в сутки 10 дней
- дети от 1 года до 8 лет — рекомендованную дозу в зависимости от веса ребенка один раз в сутки 10 дней
Номидес при ковиде
Осельтамивир — действующее вещество Номидеса. Его эффективность доказана только в отношении вирусов гриппа А и В. Препарат подавляет фермент нейраминидазу, который помогает именно вирусам гриппа проникать в клетки. Осельтамивир не затрагивает сериновые протеазы, с помощью которых коронавирус попадает в клетки для размножения.
Номидес не включен Минздравом РФ во Временные методические рекомендации по лечению коронавирусной инфекции от 22.02.2022. Его эффективность при Covid-19 не доказана. Имеющиеся отзывы применения при коронавирусе носят субъективный и не научный характер.
Номидес: аналоги
Активное вещество Номидеса осельтамивир содержат следующие средства:
- Тамифлю (оригинальный препарат)
- Гриптера
- Осмивир Медисорб
- Инфлюцеин
- Осельтамивир (Акрихин, Канон, Авексима)
- Флустоп
- Флутавир-эйч
Аналоги выпускают в капсулах по 75 мг, за исключением Осельтамивира производителей Авексима, Изварино, Атолл и Флутавир-эйч с дозировками 30 мг, 45 мг и 75 мг. При соблюдении дозировок препараты взаимозаменяемы. Детская форма в виде порошка для суспензии есть только у Номидеса.
Хотите разбираться в аналогах лекарств, чтобы умело подбирать препараты на свой бюджет? Наша методичка от экспертов-провизоров «Аналоги популярных лекарств» поможет вам в этом! Получить методичку просто: подпишитесь на наши соцсети и напишите в сообщения «аналоги».
Мегаптека в соцсетях: ВКонтакте, Telegram, OK
Номидес или Арбидол: что лучше?
Арбидол содержит активное вещество умифеновир. Он подавляет поверхностный белок вируса гемагглютинин, с помощью которого тот прикрепляется к клетке. Кроме этого, Арбидол стимулирует иммунитет и повышает выработку интерферона.
Таким образом, он относится к средствам с прямым противовирусным и иммуностимулирующим действием.
Арбидол имеет показания для профилактики и лечения гриппа А и В, других ОРВИ, в комплексной терапии ротавирусной инфекции, бронхита, пневмонии, герпеса. Его используют для профилактики инфекционных послеоперационных осложнений. Он разрешен для применения детям с 2 лет и имеет лекарственную форму в виде порошка для приготовления детской суспензии.
Умифеновир включен в российские Временные методические рекомендации по лечению коронавирусной инфекции.
Эффективность Арбидола не подтверждена достаточным количеством клинических исследований согласно принципам доказательной медицины. Эффективность Номидеса против вируса гриппа подтверждена.
Краткое содержание
- Номидес принимают для лечения и профилактики гриппа. Дозировки для детей старше 1 года зависят от веса ребенка и указаны в инструкции по применению.
- Эффективность Номидеса при Covid-19 не доказана. Препарат активен против фермента, помогающего вирусу гриппа проникать в клетку. Номидеса нет в последних Методических рекомендациях МЗ РФ по лечению коронавирусной инфекции.
- Аналоги Номидеса: Тамифлю, Инфлюцеин, Гриптера, Осельтамивир и др. Лекарственная форма в виде детской суспензии для детей от 1 года есть только у Номидеса.
- Арбидол с действующим веществом умифеновир имеет более широкий спектр действия. Разрешен детям с 2 лет. Не имеет доказанной эффективности. Умифеновир включен в российские Методические рекомендации по лечению коронавируса.
Задайте вопрос эксперту по теме статьи
Остались вопросы? Задайте их в комментариях ниже – наши эксперты ответят вам. Там же Вы можете поделиться своим опытом с другими читателями Мегасоветов.
Поделиться мегасоветом
Понравилась статья? Расскажите маме, папе, бабушке и тете Гале из третьего подъезда
Аналоги Номидес
Товары из категории — Противовирусные препараты
Инструкция по применению
Цена в интернет-аптеке WER.RU: от 362
Немного фактов
Номидес – препарат противовирусной направленности, применяемый при лечении симптомов гриппа, а также острых вирусных инфекций. Обладает катализирующим действием, препятствуя образованию и развитию вирусов в организме человека, а также замедляя их дальнейшее распространение.
Немного фактов
Номидес – препарат противовирусной направленности, применяемый при лечении симптомов гриппа, а также острых вирусных инфекций. Обладает катализирующим действием, препятствуя образованию и развитию вирусов в организме человека, а также замедляя их дальнейшее распространение.
Лечебное действие Номидеса основано на осельтамивире, относящемуся к группе ингибиторов нейраминидаз, блокирующих размножение вирусов гриппа типа А и Б. Более известен в мире под торговой маркой Тамифлю и используется начиная с 1999-го года. Производится российской фармацевтической корпорацией АО «Фармасинтез», главный офис которой находится в городе Иркутск.
Лекарственная форма и фармакологические свойства
Лекарственное средство выпускается в виде желатиновых капсул разных цветов: белого цвета по 30 мг, голубого цвета по 45 мг и оранжевого цвета по 75 мг. Внутри каждая капсула содержит белый порошок с желтым оттенком. Основным действующим веществом, входящим в состав Номидеса является осельтамивир. Кроме того, в составе препарата находятся такие компоненты как коллоидный диоксид кремния, крахмал, коповидон, стеарилфумарат и тальк. Капсулы состоят из желатина, воды, диоксида титана, лаурилсульфата натрия и красителей.
В упаковке находится блистер с десятью капсулами лекарственного препарата, а вместе с ними инструкция по применению.
Показания к применению
Благодаря осельтамивиру, находящемуся в составе лекарственного средства и оказывающему антивирусное действие, препарат целесообразно использовать для борьбы с вирусами гриппа, а также для профилактики возникновения вирусных инфекций среди групп людей, находящихся в местах с высоким риском заражения – работающих в больших коллективах, среди студентов и школьников. В целом, можно принимать в профилактических целях среди детей старше трех лет.
Способ применения и дозировка
Для борьбы против уже начавшихся вирусных заболеваний среди подростков и взрослых следует принимать внутрь, в любое время суток, по 75 мг лекарства два раза в день. Желательно начать прием не позднее чем через два дня после проявления симптомов. У детей доза лекарства составляет 75 мг один раз в день.
В случае применения препарата в качестве профилактического средства суточная дозировка Номидеса составляет 75 мг у взрослых и детей в период сезонной эпидемии гриппа.
Профилактический прием препарата можно вести постоянно, а курс приема для уже заболевших гриппом – 5 дней. Если не наблюдается улучшений в состоянии после прохождения этого периода времени нужно проконсультироваться с врачом по поводу дальнейшего лечения либо возможной замены препарата другим лекарственным средством.
Передозировка и побочные действия
В ходе клинических испытаний не было выявлено каких-либо симптомов передозировки препаратом.
Касаемо побочных действий инструкция отмечает следующие возможные неприятные последствия: тошнота и рвота, нарушения режима сна, головокружение, утомляемость, кашель, боли в желудке. Частота возникновения данных симптомов является незначительной.
Противопоказания к использованию
Номидес не рекомендовано использовать в случае наличия высокой восприимчивости входящих в состав препарата компонентов.
Существуют показания по осторожному приему препарата среди беременных, а также в период кормления грудью. Необходима дополнительная консультация у лечащего врача.
Противопоказания приема лекарственного средства имеются для пациентов с наличием заболеваний печени.
Следует осуществлять тщательное наблюдение за состоянием детей младше 12-ти лет в период приема медпрепарата для избегания возможных осложнений.
В период приема лучше воздержаться от вождения автомобиля и других транспортных средств, так как не исключено влияние на скорость реакции.
Взаимодействие с алкоголем и лекарственными препаратами
Следует воздержаться от приема алкоголя в период использования Номидеса, так как этанол понижает позитивный эффект лекарственного средства.
Необходимо соблюдать осторожность в случае одновременного приема препарата вместе с метотрексатом, бутадионом и хлорпропамидом.
Не обнаружено каких-либо отклонений в случае комбинирования лекарственного средства с другими препаратами, в частности допустим прием совместно с парацетамолом, ранитидином, кодеином, теофиллином, антибиотиками, тиазидными диуретками.
Аналоги
Номидес имеет следующие аналоги: по лечебным компонентам – осельтамивир, тамифлю и флустоп. Среди препаратов со сходным лечебным действием можно выделить амизон, амиксин, анаферон, арбидол, виферон, ибупрофен, лавомакс, либексин, нурофен, фервекс, циклоферон, эргоферон и другие. Следует внимательно отнестись к выбору средства из этой группы, чтобы компоненты, входящие в лекарственное средство, позволили достигнуть наивысшей эффективности.
Условия продажи и хранения
Отпускается только при наличии рецепта врача. Хранить фармацевтическое средство необходимо в месте, с ограниченным для детей доступом, температура в котором не превышает 25-ти градусов по Цельсию. Срок хранения препарата – 3 года. Не рекомендовано использовать после того как истек указанный на упаковке срок годности.
Цены на Номидес в Москве
Заберите заказ в в аптеке
WER (г. Москва)
Цена: от 362 руб.