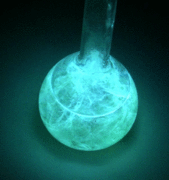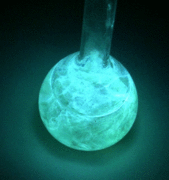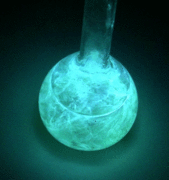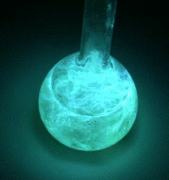
Набор для экспериментов «Волшебный фонарь» позволит провести увлекательный научный опыт, а игрушка, созданная собственными руками, будет наградой юному ученому.
Яркая и подробная инструкция позволяет проводить эксперименты играючи. Все действия подробно описаны, все ингредиенты наглядно показаны, а все важные действия продублированы подробными пошаговыми иллюстрациями.
Видеообзоры набора
Посмотрите, из чего состоит набор, а также ознакомьтесь со всеми этапами выполнения опыта в нашей видеоинструкции.
Для того, чтобы провести эксперимент, достаточно ознакомиться с инструкцией и следовать указанным в ней рекомендациям. Тем не менее, для вашего удобства мы приготовили удобные видео-инструкции по каждому набору.
Ниже вы можете посмотреть краткий видеообзор набора, а также подробную и детальную видеоинструкцию по проведению всех входящих в него экспериментов.
Для того, чтобы провести эксперимент, достаточно ознакомиться с инструкцией и следовать указанным в ней рекомендациям. Тем не менее, для вашего удобства мы приготовили удобные видео-инструкции по каждому набору.
Ниже вы можете посмотреть краткий видеообзор набора, а также подробную и детальную видеоинструкцию по проведению всех входящих в него экспериментов.
Подробная видеоинструкция
Подробнее о наборе
В данном разделе вы можете ознакомиться с подробным описанием набора и посмотреть его детальные фотографии.
Именно опыты и эксперименты двигали науку вперед, а этот набор опытов будет двигать научный интерес ребенка, представляя эксперименты по химии совсем в другом свете — буквально. Фонарик не только подарит атмосферу праздника, но и удивит свечением от химической реакции.
Именно опыты и эксперименты двигали науку вперед, а этот набор опытов будет двигать научный интерес ребенка, представляя эксперименты по химии совсем в другом свете — буквально. Фонарик не только подарит атмосферу праздника, но и удивит свечением от химической реакции.
В наборе уже есть все, чтобы провести увлекательный химический опыт. Состав набора:
Гексацианоферрат (III) калия, 3 г
Гидроперит
Гидроксид натрия, 0,8 г
Люминол, 0,06 г
Пластиковая пробирка
Защитные перчатки
Инструкция
Фотографии: Depositphotos / Иллюстрации: Юлия Замжицкая
Последний урок химии в уходящем году должен стать запоминающимся для школьников. Рассказываем, какие несложные, но яркие опыты можно провести в классе.
1. Зима в стакане
Опыт заключается в сублимации бензойной кислоты и ее оседании на еловой ветке. Бензойная кислота является органическим веществом, которое может переходить из твердого состояние в газообразное без жидкой фазы и благодаря этому давать красивые эффекты.
Что нужно:
- Термостойкая или боросиликатная стеклянная посуда.
- Еловая ветка.
- Бензойная кислота.
- Спиртовка.
Инструкция:
- Насыпьте небольшое количество кислоты в стакан.
- Положите внутрь стакана еловую ветку, чтобы на ней оседали пары бензойной кислоты.
- Подожгите спиртовку и поставьте на нее стакан для нагревания. Через некоторое время кислота начинает сублимироваться, и стакан наполняется парами.
- Снимите стакан с огня, чтобы он остыл.
- После остывания пары бензойной кислоты начинают оседать на еловой ветке и стенках стакана и создавать эффект пушистого снега
Еще больше полезных материалов — в Телеграм-канале Педсовета. Подписывайтесь, чтобы не пропускать свежие статьи и новости.
Подписаться
2. «Золотой дождь»
В ходе реакции образуется йодид свинца, который дает красивый золотой цвет с перламутровым переливом. Эксперимент можно повторять неограниченное количество раз — достаточно только нагреть раствор, чтобы йодид растворился.
Что нужно:
- Нерастворимая соль свинца (1г).
- Йодид калия (1г).
- Уксусная кислота.
- 250 мл дистиллированной воды.
- Емкость для проведения опыта.
- Стакан для приготовления раствора.
Инструкция:
- Засыпьте йодид калия в колбу.
- Нитрат засыпьте в стакан для приготовления раствора.
- Добавьте уксусную кислоту в нитрат.
- Вскипятите 250 мл дистиллированной воды и добавьте поровну в обе емкости.
- Постоянно перемешивая жидкость, дождитесь полного растворения вещества.
- Добавьте нитрат свинца к йодиду калия небольшими порциями.
3. Снежная лавина
При взаимодействии с водой абсорбент начинает раздуваться и создает эффект пушистого снега. Получившимся веществом можно засыпать елку или использовать как элемент декора.
Что нужно:
- Полиакрилат натрия (он, например, содержится в подгузнике).
- Ножницы.
- Емкость для приготовления раствора.
- Вода.
Инструкция:
- Заполните 1/ 3 стакана водой.
- Высыпьте в стакан полиакрилат натрия.
- Дождитесь полного разбухания абсорбента и вытащите получившийся «снег» из стакана.
4. Фейерверк в стакане
Опыт демонстрирует реакцию серной кислоты и спирта на кристалл перманганата калия. В итоге у вас получается яркий фейерверк на дне стакана.
Что нужно:
- Серная кислота.
- Прозрачная емкость.
- Перманганат калия.
- Спирт.
- Прозрачная емкость для приготовления раствора.
Инструкция:
- Налейте серную кислоту в емкость.
- Добавьте туда спирт в пропорции 1:1.
- Засыпьте кристаллы перманганата калия.
- Выключите свет (иначе опыт будет недостаточно яркий).
5. Горячий лёд
Опыт показывает, как с помощью простых веществ — соды и уксуса — образовывается «горячий лед». Полученный раствор кристаллизуется с выделением большого количества тепла. Благодаря этому получившиеся кристаллы можно переплавить и вновь использовать в опыте.
Что нужно:
- Уксусная кислота 70% (100 гр.).
- Сода пищевая (97,8 гр.).
- Вода (20 мл).
- Высокая емкость.
- Кристаллы ацетата натрия.
Инструкция:
- Налейте уксусную кислоту в емкость.
- Добавьте к ней соду и воду.
- Подождите, пока образуется тригидрат ацетата натрия (понадобится около 10 часов). Он будет похож на талый снег.
- Поставьте емкость на плиту и, постоянно помешивая, растворите содержимое до прозрачной жидкости.
- Охладите раствор до комнатной температуры.
- Нанесите небольшое количество кристаллов ацетата натрия на кончики пальцев и опустите их в емкость.
- Дождитесь реакции. Вокруг вашей руки начнут образовываться кристаллы, похожие на треснувший лед.
Материалы по теме:
- Необычные новогодние «ёлки» России: огонь, вода и джем-сейшен на барабанах;
- Как мотивировать детей на учебу в конце года. Советы учителям «началки»;
- Что посмотреть в кино с детьми на новогодних каникулах.
Если вам нравятся материалы на Педсовете, подпишитесь на наш канал в Телеграме, чтобы быть в курсе событий раньше всех.
Подписаться
Редкие дети не проявляют повышенный интерес к огню. Он для них и страшен и прекрасен одновременно. Чтобы удовлетворить детское любопытство и при этом направить его в конструктивное русло, я устраиваю для моих детей опыты – в ходе них можно и с чудесами огня познакомиться поближе, и все это происходит с моими пояснениями и под моим присмотром. Помните, я совсем недавно рассказывала, как в домашних условиях сделать цветной огонь? Но на этом наши эксперименты с огнем не закончились. Сегодня я покажу три очень простых опыта, все необходимые составляющие для которых можно легко найти дома или в ближайшей аптеке. А для их проведения не понадобиться никакой специальной огнезащиты, кроме металлического противня, на котором лучше устраивать все поджоги. Ну, и конечно, не забывайте о технике безопасности – хороший повод еще раз поговорить о ней с детьми!
ОПЫТ 1. Химический фитиль.
Этот способ дистанционно поджигать запалы для бомб использовали еще в конце 19 века террористы-народовольцы при организации покушений на государственных чиновников. Но не бойтесь, мы ничего взрывать не будем:) Мы просто посмотрим, как огонь может рождаться не только от искры, но и просто от смешания некоторых веществ, которые по отдельности совершенно безобидны. Это хороший урок для юных химиков, которые так и норовят все порошки из разных пробирок смешать в одной, совершенно не задумываясь о том, что может в результате получиться не только безобидная коричневая бурда, но и небольшой взрыв (это у нас дома однажды проделал Витя со своим другом).
Нам понадобится:
- Марганцовка (перманганат калия) – продается в аптеке
- Глицерин- продается в аптеке
- Бумага
Ход эксперимента:
Тетрадный листок бумаги нужно скомкать и насыпать на него небольшую кучку марганцовки, где-то 1/3 чайной ложки (см. фото).
После этого надо капнуть на нее буквально 2-3 капли глицерина, не больше! (Мы отмеряли пипеткой, сделанной из коктейльной трубочки).
Проходящая химическая реакция является экзотермической. Это значит, что при соединении веществ выделяется большое количество теплоты. Поэтому надо будет подождать около полминуты, пока от реакции разогреется бумага. Сначала порошок зашипит и начнет пузыриться, от него пойдет дым.
А как только бумага достаточно нагреется – она загорится сама собой.
ОПЫТ 2. Мини-фейерверк
Смотря, как на праздники взрывают салюты, редкий ребенок не захочет попробовать сделать что-то подобное. Легко! Только, чур, под присмотром мамы 🙂
Нам понадобится:
- Марганцовка (перманганат калия) – продается в аптеке
- Железные опилки – продаются в магазинах с учебными пособиями и входят в состав химических наборов для детей.
- Растолченный в порошок древесный уголь (подойдет и растолченная таблетка активированного угля)
Ход эксперимента:
Сначала нам надо найти тигль, в котором мы будем устраивать наш фейерверк. Это должна быть какая-то небольшая огнеупорная емкость с длинной ручкой, которую не жалко испортить продуктами горения. Например, мы с детьми используем жестяной колпачок от бутылочки аптечного спирта, к которому прикрутили длинную ручку, сделанную из проволоки. А чтобы руки точно не обжечь, я еще и держу ее над огнем, используя плоскогубцы.
Потом на лист бумаги насыпаем три небольшие одинаковые кучки мелко растолченных порошков: марганцовки, опилок и угля. Мы брали в такой пропорции, чтобы остальных ингредиентов было столько же, сколько порошка от одной таблетки активированного угля.
После этого складываем лист бумаги пополам так, чтобы порошки ссыпались в одну кучку. Обязательно надо обратить внимание детей на тот способ, которым мы получили смесь порошков. Дело в том, что при перетирании марганцовки с железными опилками (если бы мы мешали какой-то ложкой или палочкой), смесь может вспыхнуть сама-собой.
Полученную смесь высыпаем в наш тигль.
Подносим тигль к пламени (например, газовой конфорки, сухого спирта или свечки) и ждем несколько секунд. Когда смесь прогреется, она начнет искрить и гореть фейерверком, похожим на бенгальский огонь.
Реакция длится всего десяток секунд, поэтому смотрите во все глаза 🙂 И будьте осторожнее – если у вас в порошке встретятся крупные частицы, они будут разлетаться по сторонам горячими искрами и могут оставить следы на мебели и других вещах.
ОПЫТ 3. Фараонова змея из глюконата кальция
Разные вещества в огне ведут себя по разному. Что-то просто загорается (например, бумага), что-то взрывается (например, газ углеводород), что-то искрит (как смесь в предыдущем опыте), что-то плавится (как пластмасса), что совсем не горит (например, металл). А что-то ведет себя уж совсем экзотически – вспухает и превращается в пористое вещество, объем которого во много раз превышает объем исходного вещества.
Для таких химических реакций есть даже специальное название – “фараонова змея”. “Змея” – потому что вещество, увеличиваясь в объеме как бы выползает из огня. А вот почему “фараонова” я так и не нашла 🙂 Может среди моих читателей найдется химик или филолог по образованию, который сможет это объяснить?
Нам понадобится:
- Таблетка сухого спирта (продается в отделах магазинов с туристским снаряжением)
- Таблетка глюконата кальция (продается в аптеке)
Ход эксперимента:
Кладем глюконат кальция на сухой спирт
Поджигаем спирт и через несколько секунд наблюдаем за тем, как обычная таблетка медленно превращается в настоящую змею!
P.S. Предупреждая все вопросы, сразу скажу: да, эти опыты опасны, особенно с марганцовкой. Но я специально показываю их детям. Во-первых, им надо знать, что с огнем не все так просто. А то привыкли видеть его в “прирученном” виде на плите под чайником. А во-вторых, лучше пусть они их проделают со мной и удовлетворят свою тягу к фейерверкам и взрывам, чем где-нибудь с друзьями под гаражом без всякой техники безопасности.
Но тут каждый решает за своих детей сам – есть такие ребячьи натуры, что, наоборот, будут потом пытаться самостоятельно проделать то, что нельзя. Лучше вас ваших детей не знает никто 🙂
Еще опыты и эксперименты по химии для детей в моем блоге:
- Химические опыты для детей – большая подборка простых опытов и экспериментов для детей
- Цветные опыты по химии (получаем всевозможные разноцветные жидкости в результате химических реакций)
- “Волшебное зелье” – опыты по смешению жидкостей разного цвета и плотности
- Как сделать цветной огонь? (химические опыты с окрашиванием пламени)
- Опыты с огнем – зажигаем бумагу с помощью лупы и несгораемая купюра.
- Опыты с молоком
- Проявляющаяся валентинка
- Выращивание кристаллов: Снежинки мастер-класс
- ТОП-10 невидимых чернил
- Цветные опыты с капустой
Ох уж эти джедаи с их световыми мечами, взволновали умы миллионов, не обошли и нас. В кино всё выглядело более чем эффектно, и лет 10 назад разноцветные светящиеся палочки, привезённые с китайской барахолки и лишь очень отдалённо напоминающие орудие упомянутых рыцарей, произвели фурор. Практичные люди, вроде рыбаков и исследователей, сразу оценили такие светильники не только в качестве средства создания подходящего антуража, но и как альтернативный источник света. Химический способ получения видимого излучения отличается очень низкой теплоотдачей. К тому же он может быть применён в условиях, где другие светильники не могут работать. Пытливые умы экспериментаторов сразу задались вопросом о том, насколько сложно изготовить такой химический источник света своими руками.
Разновидности ХИС
ХИС — химический источник света заводского изготовления можно встретить не только в магазинах игрушек и украшений. Модели побольше и, конечно, посильнее встречаются в специальном оборудовании спасателей, подводников, спелеологов и других специалистов, связанных с необычными условиями труда. Ингредиенты, участвующие в реакции, довольно труднодоступны для обывателя, а некоторые обходятся в серьёзную сумму. Некоторые реактивы могут быть небезопасными, а этого хотелось бы избежать в кустарном производстве. В общем, экспериментальным путём было выявлено несколько способов, в том числе и безрезультатных.
Провал с лимонадом
С прискорбием можно констатировать, что известный трюк с напитком Mountain Dew не работает. Если быть совсем точным, то он не работает с ингредиентами, использованными в известном опыте, потому что светильник в пластиковой бутылке на основе этого напитка вполне реализуем. Об этом несколько позже.
Простейший светильник на ацетоне
Каталитическое окисление ацетона можно рассматривать как источник света, химический принцип которого не отличается от обычного горения. Отличием будет лишь отсутствие открытого пламени. Вкратце, в прозрачную ёмкость наливают незначительное количество ацетона. Важно лишь создать место для образования и скопления паров горючего и смешивания их с кислородом воздуха. Медную проволоку сворачивают пружинкой или другим способом, чтобы витки были поближе друг к другу для создания большей площади реакции в меньшем объёме. Этот конец проволоки нагревают до красноты и опускают в ёмкость с парами ацетона, и на поверхности меди ацетон вступает в реакцию с кислородом, выделяя дополнительное тепло. Полученная энергия поддерживает температуру реакции и дополнительно нагревает металл до состояния свечения. Такой светильник выделяет много тепла, да и свет получается из-за нагрева меди, но необычность и химическая составляющая имеются, поэтому мы не могли обойти его вниманием.
Химический свет путём окисления люминола
Поиски подходящих ингредиентов и работающего рецепта привели наконец к удовлетворительному результату. Люминол используется в судебной медицине для обнаружения остатков крови: ионы железа в плазме действуют как катализатор, и люминол окисляется с выделением светового излучения. Найти это вещество не составит труда, препарат «Галавит» содержит натриевую соль люминола в достаточном количестве для нескольких опытов с изготовлением веществ, используемых как источник света. Химический аспект всего действия подразумевает, что ёмкости для светильника не будут использованы в быту, чтобы исключить отравления или повреждения кожи агрессивными веществами. Будьте аккуратны при проведении опытов, используйте защитные перчатки, очки и респиратор при необходимости.
Изготовление химических источников света (ХИС) в водных растворах
Итак, мы определились с основным реагентом, нужно подумать об идеальных условиях реакции. В качестве жидкой среды понадобится растворитель. В его роли может выступить обычная вода из крана, однако люминол практически нерастворим в ней. Чтобы реакция протекала равномерно, «Галавит» придётся мелко растереть и приготовить суспензию, а также понадобится катализатор с большим выделением ионов железа или меди в растворе. Сульфат меди или медный купорос, как его называют, будет отличным усилителем реакции в воде. Для создания щелочной среды потребуется нашатырный спирт, а лучше гидроксид натрия или калия. Окислителем послужит перекись водорода, пропорции следующие:
-
100 мл воды смешать с 2-3 растёртыми таблетками «Галавита»;
-
добавить 50 мл пероксида водорода;
-
3-5 г медного купороса или красной кровяной соли;
-
30 мл нашатырного спирта или 15 мл раствора КОН или NaOH.
Свечение появится почти сразу после смешивания и сохранится на несколько часов. Для продолжения действия нужно добавлять тёртый «Галавит» и пероксид водорода в раствор и слегка взболтать.
Опыты с «Димексидом»
Эксперименты с водой дают результат слабее ожидаемого, вследствие плохой растворимости люминола, стоит поискать среду получше. Диметилсульфоксид отлично справляется с задачей растворения реагентов, приобрести его можно в аптеках под названием «Димексид». Соблюдайте осторожность при работе с этим препаратом, потому что проникающая способность его делает кожу проницаемой для различной грязи, которая в обычных условиях успешно сдерживается нашей естественной защитной оболочкой. Катализатор реакции придётся убрать, потому что с купоросом и кровяной солью реакция протекает слишком бурно и кратковременно. Опытным путём рассчитаны следующие пропорции:
-
около 20 г КОН или NaOH в сухом виде (следует полностью отказаться от воды для чистоты эксперимента);
-
100 мл «Димексида», полностью растворять гидроксид нет необходимости, на поверхности его осадка реакция и начнётся;
-
1 таблетка «Галавита», растёртая в порошок, чтобы растворилась быстрее.
К слову, такой раствор можно приготовить заранее и засыпать люминол при необходимости, главное — убедиться в надёжности и герметичности емкости. Стоит предупредить, что едкая смесь щёлочи и «Димексида» разъедает пластиковые бутылки дня за 3-4, поэтому целесообразно только разовое и недолгое использование таких емкостей для приготовления химических источников света.
Другие варианты
Существует немало рецептов создания таких жидкостей, как источник света химический, есть варианты использования стиральной жидкости как среды и даже человеческой крови в качестве катализатора, но большинство из них являются лишь вариантами рассмотренных нами рецептов. Вы и сами можете подобрать собственные реагенты и их соотношения для опыта, в том числе и с газировкой Mountain Dew.
ХЕМИЛЮМИНЕСЦЕНЦИЯ, ИЛИ Как сделать светящуюся жидкость.
Для начала стоит отметить, что создание светящейся жидкости в домашних условиях это не самый легкий процесс. Он так же не является очень уж чистым с точки зрения домохозяек, а значит, придется, как следует отмывать посуду после его изготовления.
Очевидно, что если жидкость светится, значит, в ней происходят определенные химические процессы (глубокая мысль, да? )))).
Но очень уж сильно углубляться в дебри химии не будем. Достаточно просто знать, что некоторые вещества, находясь в кислой среде, могут излучать свет в результате процесса окисления.
Также стоит отметить, что существуют с добрый десяток способов изготовления светящейся жидкости. Рассмотрим некоторые из наиболее часто встречающихся.
Как сделать светящуюся воду
I Способ
Вам понадобится:
— люминол (его можно найти в магазинах, специализирующихся на химреактивах) — 2-3 г
— перекись водорода 3% (можно найти в аптеке) — 80 мл
— вода — 100 мл
— медный купорос — 3 г
— раствор едкого натра — 10 мл
— флуоресцентные красители, например рубрен (но можно использовать и такие как бриллиантовый зеленый)
— прозрачная стеклянная емкость.
Люминол является порошком желтого цвета. Если насыпать его в кислые и нейтральные растворы, он начнет светиться голубым цветом. Именно он является главным ингредиентом в данном эксперименте.
Процесс:
1. Налейте в стеклянную емкость воду и растворите в ней люминол.
2. Добавьте в емкость перекись водорода.
3. Добавьте медный купорос (можно его заменить хлорным железом или красной кровяной солью).
* В случае, если у вас нет ни одного и трех ингредиентов, можете использовать подручные средства. Выдавите из куриного окорока немного крови и разведите ее в воде, после чего добавьте 1 ст. ложку данного раствора к смеси в емкости.
4. Добавьте едкий натр.
Теперь можете выключить свет и любоваться голубым свечением из емкости.
* В случае, если вам хочется другой цвет, кроме голубого, можете добавить в раствор любой органический краситель.
II Способ
Вам понадобится:
— люминол — 0,15 г
— сухая щелочь (КОН) — 35 г
— димексид — 30 мл
— стеклянная емкость с пробкой — 500 мл
— флуоресцентный краситель
Процесс:
1. Смешайте в емкости люминол, щелочь и димексид.
2. Закройте емкость крышкой и взболтайте. У вас должно получиться голубое свечение. Его вы можете перекрасить, с помощью любого флуоресцентного красителя.
* В случае, если свечение ослабло, откройте крышку, чтобы набрать в емкость воздуха. После этого жидкость снова станет излучать свет.
III Способ
Вам понадобится:
— один высокий стакан
— раствор стирального порошка — 20 мл
— перекись водорода 3% — 10 мл
— раствор люминола 3% — 5 мл
— немного кристаллов марганцовки
Процесс:
1. Приготовьте в стакане раствор стирального порошка.
2. Добавьте перекись водорода.
3. Добавьте раствор люминола.
4. Разотрите несколько кристаллов марганцовки и добавьте их в ту же емкость.
* Если начать перемешивать смесь, она начнет пениться, и будет искриться.
* Так как вода в кране хлорированная, то под воздействием хлора раствор люминола будет светиться.