Магний, как и другие макроэлементы, встречается во всех тканях. Являясь внутриклеточным ионом, магний занимает четвертое место по содержанию в организме человека, принимает участие в терморегуляции, процессах углеводного, липидного, белкового и фосфорного обменов, контролирует процессы деления и очищения клеток. Участвуя в обменных процессах, магний, тесно взаимодействуя с калием, натрием, кальцием, является активатором для множества ферментов, стимулирует образование белков, служит одним из важнейших компонентов в регуляции большинства физиологических процессов. Его поступление, наряду со многими другими минеральными веществами и витаминами, необходимо для нормальной жизнедеятельности. В организме взрослого человека содержится примерно 20–30 г магния: приблизительно 60% в костях, около 20% – в мышцах и менее 1% – в плазме крови и эритроцитах. Значительное количество магния встречается в нервных клетках, миокарде, почках. Суточная потребность в данном микроэлементе колеблется от 250 до 450 мг, иногда до 600 мг, в зависимости от пола, возраста и других факторов. Потребность в магнии существенно возрастает при физических нагрузках, стрессе, в условиях жаркого климата, при частом посещении бани, в период роста, беременности и лактации, при несбалансированных ограничительных диетах, заболеваниях ЖКТ, продолжительной диарее, полиурии, злоупотреблении алкоголем и синдроме хронической усталости. В этих ситуациях потребность повышается в среднем на 150 мг/сут [1–3].
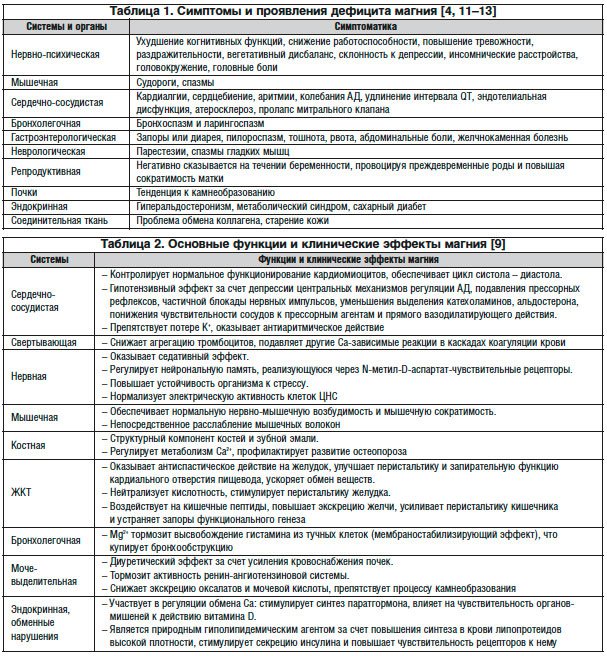
Магний поступает в организм с пищей. Основными источниками его поступления в организм являются бобовые и злаковые, шпинат, салаты (в т. ч. руккола), брокколи, ревень. Много магния в тыквенных семечках и кунжуте. Особенно богаты магнием миндальные, кедровые орехи и арахис, какао и шоколад, но существенное увеличение потребления данных продуктов может привести к прибавке в весе в связи с их высокой калорийностью. Кроме этого, необходимо помнить, что усваивается не более 30–40% магния, поступающего с пищей. При этом для его хорошей усвояемости также требуется поступление в организм в достаточном количестве кофакторов: молочной, аспарагиновой, оротовой кислот и витамина В6. В развитии алиментарного дефицита магния важную роль играют такие факторы, как его низкое содержание в пище, воде, а также избыточное потребление кальция, натрия, белка или жира с пищей, что существенно снижает поступление магния в организм из-за образования его невсасывающихся комплексов. Частота гипомагниемии достаточна высокая и составляет от 10 до 40%. Для обозначения нарушений обмена магния используют 2 термина: «магниевый дефицит», под ним понимают снижение общего содержания магния в организме, и «гипомагниемия» – подразумевается снижение концентрации магния в сыворотке (в норме 0,8–1,2 ммоль/л). Умеренной недостаточности магния в организме соответствует его уровень в сыворотке крови 0,5–0,7 ммоль/л, выраженной (угрожающей жизни) – ниже 0,5 ммоль/л. Выделяют первичный (генетически обусловленный) и вторичный (алиментарный, физиологический и т. д.) дефицит магния. Причинами дефицита магния могут быть различные эндокринные нарушения (гиперкальциемия, гиперальдостеронизм и др.), диабет, состояние хронического стресса, алкоголизм, а также медикаментозное лечение, в т. ч. длительный прием диуретиков. Экскреция магния значительно возрастает при повышении уровня катехоламинов и глюкокортикостероидов. Также существенные потери магния могут иметь место при усиленном потоотделении [1, 4–6]. Основные проявления недостатка магния в организме представлены в таблице 1.
Нормальный уровень магния в организме человека признан основополагающей константой, контролирующей здоровье человека. При изучении внутриклеточной молекулярной биокинетики установлено наличие не менее 290 генов и белковых соединений в последовательности генома человека, которые способны связывать Mg2+ как кофактор множества ферментов, участвующих в более чем 300 внутриклеточных биохимических реакциях. Ионы магния стабилизируют молекулы субстрата – нейтрализуют отрицательный заряд субстрата, активного центра фермента, способствуют поддержанию третичной и четвертичной структур белковой молекулы фермента, облегчают присоединение субстрата к ферменту и тем самым облегчают протекание химической реакции, комплекс «магний – аденозинтрифосфат (ATФ)», стабилизируя молекулу АТФ, способствует ее присоединению и «правильной» ориентации в активном центре фермента, ослабляя фосфоэфирную связь и облегчая перенос фосфата на глюкозу. В ряде случаев ион магния может помогать присоединению кофермента, способствуя активации металлоэнзимов. Магний способствует устойчивости структуры клетки в процессе роста, принимает участие в процессе регенерации клеток организма. Mg2+ – естественный физиологический антагонист Са2+, что обусловливает наличие у него миотропного, спазмолитического и дезагрегационного эффектов, способствует фиксации К+ в клетках, обеспечивая поляризацию клеточных мембран, контролирует спонтанную электрическую активность нервной ткани и проводящей системы сердца. Магний оказывает влияние на функциональное состояние практически всех органов и систем (табл. 2) [4, 7–9].
Установлена важная роль магния в развитии эндотелиальной дисфункции. Было показано, что назначение препаратов магния способно через 6 мес. существенно улучшить (почти в 3,5 раза больше по сравнению с плацебо) эндотелийзависимую дилатацию плечевой артерии. При этом также была выявлена прямая линейная корреляция – зависимость между степенью эндотелийзависимой вазодилатации и концентрацией внутриклеточного магния. Одним из возможных механизмов, объясняющих благоприятное влияние магния на эндотелиальную функцию, может быть его антиатерогенный потенциал [4, 10].
В настоящее время препараты магния широко применяются в лечении сердечно-сосудистых заболеваний. Экспериментальные данные указывают на важную роль ионов магния в регуляции сосудистого тонуса и АД. Магний оказывает гипотензивный эффект за счет отрицательного хроно- и инотропного действия, снижения тонуса сосудов, угнетения передачи в вегетативных ганглиях, угнетения вазомоторного центра. Установлена обратная зависимость между уровнем альдостерона и ренина плазмы, свидетельствующая о том, что низкий уровень магния связан с повышением активности ренин-ангиотензин-альдостероновой системы. Ионы магния подавляют активность ренин-ангиотензин-альдостероновой системы, поэтому на фоне гипомагниемии часто имеет место выраженная вазоконстрикция. Напротив, при парентеральном введении магния наблюдается выраженная вазодилатация, сопоставимая с эффектом антагонистов кальция. Следовательно, дополнительный прием магния можно рекомендовать больным с артериальной гипертензией (АГ), у которых имеется высокий риск гипомагниемии (например, при терапии тиазидными диуретиками) [4, 8, 14–19].
Также оправданным является применение магнийсодержащих препаратов при ишемической болезни сердца (ИБС). Антиишемический эффект магния обусловлен восстановлением эндотелийзависимой вазодилатации, нормализацией показателей липидного спектра, улучшением реологических свойств крови, уменьшением агрегационной активности тромбоцитов, депрессорного влияния на инотропную функцию сердца. По данным эпидемиологических исследований, дефицит магния в питьевой воде повышает риск развития сердечно-сосудистых заболеваний (особенно ИБС) и внезапной смерти. Известно, что миокард больных, умерших от сердечно-сосудистой патологии, содержит почти в 2 раза меньше магния, чем у пациентов, скончавшихся от других причин. Дефицит магния ассоциируется с повышением уровня атерогенных липидов. По данным исследования ARIC (The Atherosclerosis Risk in Communities), частота развития ИБС выше у тех лиц, у которых выявляется более низкий уровень магния в крови. В Финляндии в результате реализации правительственной программы по профилактике магниевого дефицита у населения страны в течение последних 15 лет удалось снизить частоту инфарктов миокарда (ИМ) в популяции почти в 2 раза. Анализ обобщенных данных 7 рандомизированных исследований у 1301 больного острым ИМ выявил благоприятное влияние магния на больничную летальность. В многоцентровом исследовании LIMIT-II (2316 пациентов) было выявлено снижение риска смерти на 24%, риска развития сердечной недостаточности – на 25% (в группе больных острым ИМ, которые в течение первых 28 дней получали дополнительно к стандартной терапии инфузии сульфата магния). Дефицит магния был обнаружен при сердечной недостаточности, развившейся на фоне АГ и ИБС. Следовательно, дополнительный прием магния в составе комплексной терапии можно рекомендовать больным с ИБС и хронической сердечной недостаточностью [4, 8, 20–27].
Кроме того, показано, что на фоне дефицита магния гораздо чаще развиваются нарушения ритма и проводимости при терапии сердечными гликозидами. Препараты магния широко используются при лечении аритмий на фоне дигиталисной интоксикации благодаря способности восстанавливать функцию калий-натриевой помпы. По данным исследования FHS (Framinghem Heart Study), экстрасистолы выявлены у 5,5% пациентов (n=3327, средний возраст 44 года). При этом длительная гипомагниемия коррелирует с высокой частотой возникновения желудочковых экстрасистол, тахикардии, фибрилляции желудочков (р=0,01). Эта закономерность оставалась значимой даже после учета поправок на массу левого желудочка, в т. ч. и у добровольцев без клинически выраженного заболевания. В исследовании PROMISE Study были выявлены большая частота желудочковой экстрасистолии и высокая летальность в группе пациентов с гипомагниемией в сравнении с группами, в которых отмечалась нормо- и гипермагниемия [28–30].
Препараты магния давно используются как антиаритмические средства, сочетающие свойства антиаритмиков I (мембраностабилизирующие) и IV (антагонисты кальция) классов. Магний оказывает мембраностабилизирующее действие, депрессорное влияние на возбудимость и проводимость клетки. Истощение запасов магния вызывает выраженное неблагоприятное воздействие на миокард. Нарушение содержания ионов калия и магния и их соотношения является существенным фактором риска развития аритмий. Магний предотвращает потерю калия клеткой и уменьшает вариабельность длительности интервала QT, которая является прогностически неблагоприятным фактором развития фатальных аритмий. Кроме того, магний способен ингибировать симпатические влияния на сердце. В качестве антиаритмика соли магния наиболее эффективны (препарат выбора) при пируэт-желудочковой аритмии (torsades de pointes) благодаря способности угнетать развитие следовых деполяризаций и укорачивать длительность интервала QT. Магний также используется как при врожденном синдроме удлиненного интервала QT, так и при его удлинении вследствие применения антиаритмиков I класса. Результаты рандомизированного многоцентрового плацебо-контролируемого двойного слепого исследования MAGICA позволили рассматривать препараты магния и калия как общепринятый европейский стандарт при лечении аритмий у пациентов на фоне приема сердечных гликозидов, диуретиков, антиаритмиков. Антиаритмический эффект препаратов магния проявляется спустя 3 нед. от начала лечения и позволяет снизить число желудочковых экстрасистол на 12% и общее число экстрасистол на 60–70% [4, 6, 8, 28, 31–35].
Применение препаратов магния эффективно при пролапсе митрального клапана. Так, у больных, регулярно принимавших магния оротат, установлено достоверное изменение эхокардиографических параметров, свидетельствующее о положительном влиянии магния на диспластические изменения: уменьшение глубины пролабирования митрального клапана, степени митральной регургитации, размера левого предсердия и частоты миксоматозной дегенерации створок митрального клапана [11, 36, 37].
Сегодня в клинической практике применяются несколько лекарственных препаратов, содержащих магний. Одним из наиболее удачных является препарат Магнерот (фармацевтическая компания «Верваг Фарма», Германия) – магниевая соль оротовой кислоты. Одна таблетка содержит 500 мг оротата магния (32,8 мг магния). К настоящему времени накоплен значительный клинический материал об эффективности этого препарата в различных областях медицины, и в первую очередь в кардиологии и неврологии. Оротовая кислота стимулирует синтез АТФ. Поскольку 90% внутриклеточного магния связано с АТФ, относительное увеличение внутриклеточного депо АТФ посредством оротовой кислоты улучшает фиксацию магния в клетках. Перспективным в клинической практике считается использование препаратов на основе именно органических солей магния, характеризующихся более высокой биодоступностью по сравнению с неорганическими солями. Оротат магния в отличие от неорганических оксида или сульфата магния более эффективен при коррекции дефицита магния, особенно у больных с острым коронарным синдромом и сердечной недостаточностью, протекающими с нарушениями ритма сердечной деятельности. Кардиопротективный эффект оротовой кислоты опосредован через регуляцию фермента N-ацетилглюкозаминтрансферазы, ингибирование внутриклеточной фосфодиэстеразы и модулирование кофермента PQQ с противовоспалительным, антиоксидантным и нейропротекторным эффектами [7, 9, 38, 39].
При уровне магния в сыворотке крови ниже 0,5 ммоль/л имеют место различной степени тяжести нарушения со стороны ЦНС, что требует интенсивной возместительной терапии препаратами магния, такими как Магнерот для перорального применения до 3–6 г/сут [7].
Таким образом, включение препаратов магния, в т. ч. оротата магния (Магнерот), в комбинированную терапию сердечно-сосудистых заболеваний способствует более эффективному снижению метаболических нарушений, нормализации гликемического и липидного профилей, реологических свойств крови, что суммарно ведет к снижению АД, профилактике атеросклероза и сердечно-сосудистых осложнений. Препарат магния оротата Магнерот следует считать препаратом выбора в комплексном лечении и профилактике стенокардии, ИМ, хронической сердечной недостаточности, аритмий сердца, вызванных дефицитом магния, спастических состояний, атеросклероза, дислипидемий. Многолетний опыт клинического применения препаратов магния свидетельствует об их хорошей эффективности и высоком профиле безопасности в профилактике и лечении пациентов с различной кардиологической, неврологической патологией, а также другими заболеваниями, обусловленными дефицитом магния.
Литература
1. Dreosti E. Magnesium status and health // Nutr. Rev. 1995. Vol. 53. P. 23–27.
2. Городецкий В.В., Талибов О.Б. Препараты магния в медицинской практике. Малая энциклопедия магния. М.: Медпрактика, 2008. 43 с.
3. Petroianu A., Barquete J., Plentz E. G. Acute effects of alcohol ingestion on the human serum concentrations of calcium and magnesium // J. Int. Med. Res. 1991. Sep.-Oct. Vol. 19 (5). P. 410–413.
4. Недогода С.В. Роль препаратов магния в ведении пациентов терапевтического профиля // Лечащий врач. 2009. №.6. C. 16–19.
5. Schimatchek H.F., Rempis R. Prevalence of hypomagnesemia in an unselected German population of 16,000 individuals // Magnes. Res. 2001. Vol. 14. P. 283–290.
6. Школьникова М.А., Чупрова С.Н., Калинин Л.А. и др. Метаболизм магния и терапевтическое значение его препаратов. Пособие для врачей. М.: Медпрактика, 2002. 32 с.
7. Шилов А.М., Осия А.О. Препараты магния (Магнерот) и сердечно-сосудистые заболевания в практике врача первичного звена здравоохранения // Трудный пациент. 2013. № 12. С.12–19.
8. Морозова Т.Е., Дурнецова О.С. Препараты магния в кардиологической практике // Лечащий врач. 2014. № 4. С. 95–99.
9. Коровина Н.А., Творогова Т.М., Гаврюшева Л.П. Применение препаратов магния при сердечно-сосудистых заболеваниях у детей // Лечащий врач. 2006. № 3. С.10–13.
10. Shechter M., Sharir M., Labrador M. J. et al. Oral magnesium therapy improves endothelial function in patients with coronary artery disease // Circulation. Nov. 2000. Vol. 102. P. 2353–2358.
11. Мартынов А.И., Урлаева И.В., Акатова Е.В., Николин О.П. Значение дефицита магния в кардиологии // Consilium Medicum. 2014. № 01. С. 43–46.
12. Акарачкова Е.С. Дефицит магния. Случаи из практики врача-невролога // РМЖ. 2010. № 26 (1628).
13. Шилов А.М., Авшалумов А.Ш., Синицина Е.Н. и др. Метаболический синдром и «дефицит магния»: особенности течения и лечения // Врач. 2008. № 9.С. 44–48.
14. Cappuccio F.P., Markandu N.D., Beynon G.W. et al. Lack of effect of oral magnesium on high blood pressure: a double blind study // BMJ. 1985. Vol. 291. P. 235–238.
15. Ekmekci O.B., Donma O., Tunckale A. Angiotensin-converting enzyme and metals in untreated essential hypertension // Biol. Trace Elem. Res. 2003. Vol. 95 (3). P. 203–210.
16. Geleijnse J.M., Witteman J.C., Bak A.A. et al. Reduction in blood pressure with a low sodium, high potassium, high magnesium salt in older subjects with mild to moderate hypertension // BMJ. 1994. Vol. 309 (6952). P. 436–440.
17. Mizushima S., Cappuccio F.P., Nichols R., Elliott P. Dietary magnesium intake and blood pressure – a qualitative overview of the observational studies // J. Hum. Hypertens. 1998. Vol. 12. P. 447–453.
18. Shechter M., Sharir M., Labrador M.J. et al. Oral magnesium therapy improves endothelial function in patients with coronary artery disease // Circulation. Nov. 2000.Vol.102. P. 2353–2358.
19. Wirell M.P., Wester P.O., Segmayer B.J. Nutritional dose of magnesium in hypertensive patients on beta blockers lowers systolic blood pressure: a double-blind, cross-over study // J. Intern. Med. 1994. Vol. 236. P. 189–195.
20. Liao F., Folsom A.R., Brancati F.L. Is low magnesium concentration a risk factor for coronary heart disease? The Atherosclerosis Risk in Communities (ARIC) Study // Am. Heart J. 1998. Vol. 136 (3). P. 480–490.
21. Shechter M. Does magnesium have a role in the treatment of patients with coronary artery disease? // Am. J. Cardiovasc. Drugs. 2003. Vol. 3 (4). P. 231–239.
22. Лазебник Л.Б., Дроздова С.Л. Коррекция магниевого дефицита при сердечно-сосудистой патологии // Кардиология. 1997. № 5. С. 103–104.
23. Diaz R., Paolasso E.C., Piegas L.S. et al. on behalf of the ECLA (Estudios Cardiologicos Latinoamerica) collaborative group. Metabolic modulation of acute myocardial infarction. The ECLA glucose-insulin-potassium pilot trial // Circulation. 1998. Vol. 98. P. 2227–2234.
24. Fath-Ordoubadi F., Beatt K.J. Glucose-insulin-potassium therapy for treatment of acute myocardial infarction. An overview of randomized placebo – controlled trials // Circulation. 1997. Vol. 96. P. 1152–1156.
25. Shechter M., Hod H., Chouraqui P. et al. Magnesium therapy in acute myocardial infarction when patients are not candidates for thrombolytic therapy // Am. J. Cardiol. 1995. Vol. 75. P. 321–323.
26. Teo K.K., Yusuf S., Collins R. et al. Effects of intravenous magnesium in suspected acute myocardial infarction. Overview of randomised trials // Brit. Med. J. 1991. Vol. 303. P. 1499–1503.
27. Woods K.L., Fletcheer S., Foffe C., Haider Y. Intravenous magnesium sulphate in suspected acute myocardial infarction. Results of the second Leicester Intravenous Magnesium Intervention Trial (LIMIT – 2) // Lancet. 1992. Vol. 343. P. 816–819.
28. Zehender M., Meinertz T., Just H. Magnesium deficiency and magnesium substitution. Effect on ventricular cardiac arrhythmias of various etiology // Herz. 1997. Jun. 22 (Suppl. 1). P. 56–62.
29. Tsuji H., Venditti F.J. Jr, Evans J.C. et al. The associations of levels of serum potassium and magnesium with ventricular premature complexes (the Framingham Heart Study) // Am. J. Cardiol. 1994. Vol. 74. P. 232–235.
30. Eichhorn E.J., Tandon P.K., Dibianco R. et al. The Study Group Clinical and prognostic significance of serum magnesium concentration in patients with severe chronic congestive heart failure: The Promise Study // J. Am. Coll. Cardiol. 1993. Vol. 21 (3). P. 634–640.
31. Давыдова С., Яровой С. Препараты магния в лечении и профилактике суправентрикулярных тахиаритмий у больных урологического профиля // Врач. 2011. № 9. С. 44–49.
32. Chakraborti S., Chakraborti T., Mandal M. et al. Protective role of magnesium in the cardiovascular diseases: A review // Mol. Cell. Biochem. 2002. Vol. 238. P. 163–179.
33. Sueta C.A., Clarke S.W., Dunlap S.H. Effect of acute magnesium administration on the frequency of ventricular arrhythmia in patients with heart failure // Circulation. 1994. Vol. 89. P. 660–666.
34. Шилов А.М. и др. Применение препаратов магния для профилактики нарушений ритма сердца у больных острым инфарктом миокарда // Рос. кардиол. журн. 2002. № 1. С. 16–19.
35. Hoshino K., Ogawa K., Hishitani T. et al. Successful uses of magnesium sulfate for torsades de pointes in children with long QT syndrome // Pediatr. Int. 2006. Vol. 48 (2). P. 112–117.
36. Мартынов А.И., Акатова Е.В., Николин О.П. Клиническая эффективность оротата магния у пациентов с нарушениями ритма и артериальной гипертонией при пролапсе митрального клапана // Кардиоваск. терапия и профилактика. 2009. № 8. С. 8–12.
37. Мартынов А.И., Акатова Е.В. Опыт пятнадцатилетнего применения препаратов магния у больных с пролапсом митрального клапана // Кардиология. 2011. № 6. С. 60–65.
38. Торшин И.Ю., Громова О.А., Федотова Л.Э. и др. Хемоинформационный анализ молекулы оротовой кислоты указывает на противовоспалительные, нейропротективные и кардиопротективные свойства лиганда магния // Фарматека. 2013. № 13. С. 95–103.
39. Jellinek H., Takacs E. Morphological aspects of the effects of orotic acid and magnesium // Arzneimittelforschung. 1995. Vol. 45 (8). P. 836–842.
40. Altura B.M. Basic biochemistry and physiology of magnesiym; A brief reviem // Mag-nesium and Frace Elements. 1991. Vol. 10. P. 167–171.
При дисплазиях соединительной ткани одним из наиболее частых патологических нарушений со стороны сердечно-сосудистой системы является аритмический синдром, который, проявляясь уже с 5–6-летнего возраста и максимально прогрессируя в подростковом, может приводить к развитию жизнеугрожающих нарушений ритма сердца у молодых лиц [1, 2]. Ведущую роль среди модифицируемых факторов риска формирования клинически значимых аритмий при дисплазиях соединительной ткани (ДСТ) отводят дисбалансу вегетативной нервной системы [3]. При этом, согласно результатам большинства исследований, посвященных изучению роли симпатического тонуса при патологии сердечно-сосудистой системы, ассоциированной с ДСТ, сложилось представление о прогностически неблагоприятном значении гиперсимпатикотонии, в том числе как независимого фактора риска развития фатальных нарушений ритма [3–5]. Необходимо отметить, что концентрация катехоламинов в плазме крови лишь косвенно характеризует активность симпатической нервной системы. Выраженность физиологического эффекта катехоламинов во многом определяется степенью их связывания с адренорецепторами, локализованными на мембранах клеток органов и тканей, а также — эритроцитов [6, 7]. Данные обстоятельства послужили основанием считать β-адренореактивность мембраны эритроцитов (β-АРМ) системным показателем адренореактивности организма [7, 8].
Между тем установлены корреляционные взаимосвязи между содержанием магния в слюне и наличием жизнеугрожающих аритмий [9]. Кроме того, литературные данные свидетельствуют об эффективности магния оротата дигидрата в снижении средней и максимальной частоты сердечных сокращений, количества эпизодов тахикардии и частоты пароксизмов суправентрикулярной тахикардии, а также уменьшении выраженности синдрома вегетативной дисфункции, в том числе — у пациентов с пролапсом митрального клапана (ПМК) [10–13].
Целью данного исследования было изучение влияния магния оротата дигидрата на состояние адренореактивности у пациентов с аритмическим синдромом, ассоциированным с ДСТ.
Материал и методы исследования
В исследование включено 72 пациента с нарушением ритма на фоне ДСТ (38 мужчин и 32 женщины) в возрасте от 18 до 35 лет. Критерии включения в исследование: пациенты с нарушением сердечного ритма при наличии признаков дисплазий соединительной ткани; возраст пациентов от 18 до 40 лет; добровольное информированное согласие пациента на участие в исследовании. Критерии исключения: пациенты с повышенным давлением по малому кругу кровообращения, травматические повреждения грудной клетки в анамнезе, заболевания сердечно-сосудистой системы (кардиомиопатия, врожденные и приобретенные пороки сердца, миокардиты, сердечная недостаточность и др.), заболевания щитовидной железы, заболевания крови, электролитные нарушения, острые или обострение хронических воспалительных заболеваний, алкоголизм, наркомания, использование препаратов, которые могут повлиять на результаты исследования, противопоказания к применению магния оротата дигидрата, беременность и лактация, нежелание пациента участвовать в исследовании.
Всем пациентам, принимавшим участие в исследовании, проведены: общеклиническое обследование (жалобы, анамнез, полное физикальное обследование), электрокардиография (ЭКГ) по общепринятой методике (электрокардиограф Schiller), мониторирование ЭКГ по Холтеру в течение 24 часов (монитор МТ-200 фирмы Schiller (Швейцария)), оценка уровня β-адренореактивности организма методом изменения осморезистентности эритроцитов под влиянием β-адреноблокаторов с использованием диагностического набора реактивов («АГАТ Мед», Москва) [6, 8].
По результатам электрокардиографических методов исследования были сформированы группы пациентов с учетом расположения эктопического очага: I группа — 23 пациента (11 мужчин и 12 женщин), медиана возраста — 23 года (Р25–75% = 22 ± 32), с зарегистрированными полиморфными желудочковыми экстрасистолами (n = 11), мономорфными парными желудочковыми экстрасистолами (n = 7), полиморфными парными желудочковыми экстрасистолами (n = 5); II группа — 20 пациентов (9 мужчин и 11 женщин), медиана возраста — 27,5 лет (Р25–75% = 23,5 ± 33), с зарегистрированной желудочковой экстрасистолией в виде мономорфной одиночной с частотой не более 30 эктопических комплексов за любой час мониторирования (n = 13) и мономорфной одиночной с частотой более 30 экстрасистолических комплексов за любой час мониторирования (n = 7); III группа — 29 пациентов (20 мужчин и 9 женщин), медиана возраста 25 лет (Р25–75% = 21 ± 29), с мономорфной одиночной суправентрикулярной экстрасистолией (СВЭ) с частотой менее 100 комплексов за любой час мониторирования (n = 3), мономорфной частой СВЭ (n = 12), политопной одиночной СВЭ (n = 6), монофокусной пароксизмальной суправентрикулярной тахикардией (n = 5), неустойчивым пароксизмом суправентрикулярной тахикардии (n = 2), атриовентрикулярной пароксизмальной тахикардией (n = 1). Группу контроля составили 30 здоровых добровольцев (20 мужчин и 10 женщин), медиана возраста составила 23 года (Р25–75% = 21 ± 29).
Пациенты исследуемых групп (I–III) после проведенного обследования в течение 4 месяцев принимали магния оротат дигидрат согласно инструкции по применению препарата (по 2 табл. 3 раза в сутки в течение 7 дней, затем — по 1 табл. 3 раза в сутки ежедневно до 4 месяцев). После приема магния оротат дигидрата вновь была проведена оценка уровня адренореактивности в исследуемых группах с целью изучения восстановления чувствительности β-адренорецепторов эритроцитов.
Анализ на однородность групп по возрасту и полу проводился с использованием непараметрического критерия Манна–Уитни U Test для числовых данных (возраст) и критерия χ2 с учетом поправки Yates, для дихотомических данных (пол). Сравниваемые группы были сопоставимы по полу и возрасту.
Для обработки данных использовался пакет статистических программ Statistica 7.0 и стандартные математические таблицы Microsoft Exel. Во всех процедурах статистического анализа критический уровень значимости р принимался равным 0,05.
Для определения типа распределения изучаемых выборок применялся графический метод построения гистограмм с визуальной оценкой полученного распределения и с применением теста Шапиро–Уилка W. При получении значимых показателей критерия, нулевая гипотеза о соответствии анализируемых данных закону нормального распределения отвергалась. В случае несоответствия данных закону нормального распределения, для описания данных вместо среднего арифметического использовалась медиана (Ме), с указанием межквартильного размаха (интервал между 25-м и 75-м процентилями). Для выявления различий между анализируемыми группами был применен метод Крускала–Уоллиса ANOVA, для уточнения выявленных различий был применен метод попарного сравнения групп с использованием непараметрического критерия Манна–Уитни U Test. Учитывая множественность сравнений, применялась поправка Бонферрони, уточняющая уровень значимости, при котором значения р ниже рассчитанного расценивались как достоверные.
Результаты и обсуждение
С целью восстановления чувствительности β-адренорецепторов у пациентов с аритмическим синдромом, ассоциированным с ДСТ, был выбран магния оротат дигидрат, имеющий ряд преимуществ: ионы магния участвуют в процессах возбуждения клетки, являясь физиологическим антагонистом кальция; при дефиците ионов магния нарушается обмен катионов на мембране клеток, нередко приводя к электрической перевозбудимости; ионы магния необходимы для нормального обмена нейромедиаторов (катехоламинов, тирозина, дофамина, норадреналина, серотонина, γ-аминомасляной кислоты). Кроме того, в ряде работ был доказан дефицит данного макроэлемента у пациентов с ДСТ [12, 13].
В целом пациенты отмечали хорошую переносимость препарата, не было зарегистрировано ни одного случая нежелательных явлений. По окончании курса терапии у пациентов исследуемых групп была отмечена достоверная положительная динамика по ряду субъективных проявлений. Так, уменьшилась частота регистрации жалоб астенического характера (p < 0,01), на сердцебиение жаловались меньше трети пациентов, перебои в работе сердца стали реже, и их отмечали меньше половины пациентов, кардиалгии беспокоили лишь каждого четвертого пациента, а также достоверно улучшилась переносимость умеренной физической нагрузки (p < 0,001).
По данным суточного мониторирования ЭКГ, уменьшение количества желудочковых экстрасистол в группах I и II отмечено у трети пациентов, у каждого седьмого пациента из I группы исчезли экстрасистолы высокой градации, у четверти пациентов из II группы желудочковые экстрасистолы после лечения не зарегистрированы (р < 0,05). В III группе у 10 пациентов вместо политопных и парных суправентрикулярных экстрасистол были отмечены монотопные и одиночные эктопии. На наш взгляд, антиаритмическая активность оротата магния в данном случае была связана прежде всего с тем, что магний, являясь естественным антагонистом кальция, обладает мембраностабилизирующим свойством, присущим антиаритмическим препаратам I класса, способствуя тем самым замедлению потери калия клеткой, уменьшению дисперсии длины интервала QT на ЭКГ, а также ингибированию симпатического влияния на сердце [12, 14].
В ходе исследования β-адренорецепции мембран эритроцитов методом оценки изменения осморезистентности эритроцитов под влиянием β-адреноблокаторов у пациентов исследуемых групп было выявлено, что медиана показателя β-адренореактивности мембран эритроцитов (β-АРМ) в I группе составила 52,07 условных единицы (Р25–75% = 48,03 ± 55,22), у пациентов II группы 43,54 условных единицы (Р25–75% = 39,56 ± 45,75), в III группе 36,7 условных единицы (Р25–75% = 35,1 ± 40,64), в то время как в группе здоровых добровольцев значимо ниже — 17,43 условных единицы (Р25–75% = 13,22 ± 22,08), не выходя за пределы нормальных значений (2–20 условных единиц). При проведении попарного сравнения между группами были получены следующие результаты. Наибольшие значения показателя β-АРМ зарегистрированы у пациентов с желудочковыми нарушениями сердечного ритма, с максимальными значениями в группе пациентов с высокой градацией экстрасистол по Lown, что достоверно отличало их от группы с суправентрикулярными нарушениями ритма и группы контроля (табл.).
Таким образом, у пациентов с ДСТ были выявлены более высокие значения показателя β-АРМ мембран эритроцитов, чем в группе здоровых добровольцев, что соответствовало десентизации адренорецепторов (р < 0,001).
После курсового приема магния оротата дигидрата в течение 4 месяцев было отмечено снижение β-АРМ у пациентов с аритмическим синдромом на фоне ДСТ (группы I–III), что могло свидетельствовать о процессе ресенситизации адренорецепторов. Так, в I группе медиана показателя β-АРМ составила 40,42 условных единицы (Р25–75% = 35,1 ± 45,7), во II группе — 32,73 условных единицы (Р25–75% = 28,83 ± 36,62), в III группе — 28,05 условных единицы (Р25–75% = 24,3 ± 31,09). В целом в I и II исследовательских группах целевых уровней β-АРМ, при котором клетки чувствительны к β-адреноблокаторам, удалось достигнуть больше чем у половины пациентов, однако у каждого 10-го пациента, несмотря на снижение индивидуальных значений АРМ, была необходима дальнейшая коррекция десенситизации адренорецепторов. По окончании курса терапии в III группе не зарегистрировано ни одного случая со значениями β-АРМ выше 40 условных единиц, между тем у трети пациентов данный показатель был в пределах 30–40 условных единиц. При сравнении показателя β-АРМ во всех исследуемых группах (I–III) до и по окончании курса лечения отмечена статистически достоверная положительная динамика (Wilcoxon Test, p = 0,00000), однако нормальных значений (по условиям метода) достигнуть не удалось, что говорит о необходимости дальнейшего поиска способов ранней фармакологической коррекции процесса десенситизации адренорецепторов.
Таким образом, у пациентов с ДСТ выявляются более высокие значения показателя β-адренорецепции мембран эритроцитов, чем в группе здоровых добровольцев, что соответствует десентизации адренорецепторов. Причины десентизации в большинстве случаев точно не установлены. В ряде работ приводятся данные, что на потерю чувствительности адренорецепторов оказывает влияние стресс [15, 17]. Причем скорость десентизации и ресентизации адренорецепторов во многом сопоставима с продолжительностью воздействия стрессорного фактора [17]. Кроме того, у пациентов с ДСТ, по мнению ряда исследователей, повышены процессы перекисного окисления липидов [5, 18, 19], приводящие к более стремительному процессу десентизации адренорецепторов у данных пациентов. Между тем, согласно результатам проведенного исследования, применение магния оротата дигидрата у пациентов с аритмическим синдромом на фоне ДСТ патогенетически обоснованно и эффективно. Назначение магния оротата дигидрата привело к улучшению субъективного самочувствия и электрофизиологических показателей сердечной деятельности (уменьшило выраженность и частоту регистрации аритмических эпизодов) у большинства пациентов; увеличило осморезистентность эритроцитов в присутствии β-адреноблокаторов, что может свидетельствовать о процессе ресентизации адренорецепторов, что очень важно при ведении пациентов с аритмическим синдромом.
Выводы
- У пациентов с аритмическим синдромом на фоне ДСТ присутствует десенситизация адренорецепторов с максимальными значениями показателя в группе пациентов с желудочковыми экстрасистолами высоких градаций (p < 0,001).
- Прием магния оротата дигидрата в течение 4 месяцев восстанавливает чувствительность адренорецепторов (Wilcoxon Test, p = 0,0000) у пациентов с нарушениями сердечного ритма на фоне ДСТ.
- В программу обследования больных с нарушениями сердечного ритма на фоне ДСТ целесообразно включение метода оценки адренореактивности организма по величине β-АРМ, что позволит индивидуализировать подбор и оценку эффективности антиаритмической терапии у данной категории пациентов.
Литература
- Клинические рекомендации российского научного медицинского общества терапевтов по диагностике, лечению и реабилитации пациентов с дисплазиями соединительной ткани (первый пересмотр) // Медицинский вестник Северного Кавказа. 2018; 1.2 (13): 137–210. https://doi.org/10.14300/mnnc.2018.13037.
- Шилова М. А., Мамедов М. Н. Внезапная сердечная смерть лиц молодого возраста: факторы риска, причины, морфологические эквиваленты // Кардиология. 2015; 7 (55): 78–83. https://dx.doi.org/10.18565/cardio.2015.7.78–83.
- Друк И. В., Нечаева Г. И., Осеева О. В. и др. Персонифицированная оценка риска развития неблагоприятных сердечно-сосудистых осложнений у пациентов молодого возраста с дисплазией соединительной ткани // Кардиология. 2015; 3: 75–84. 10.18565/cardio.2015.3.75–84.
- Земцовский Э. В., Тихоненко В. М., Реева С. В. Функциональная диагностика состояния вегетативной нервной системы. СПб: ИНКАРТ, 2004.
- Нечаева Г. И., Яковлев В. М., Друк И. В. Тихонова О. В. Нарушения ритма сердца при недифференцированной дисплазии соединительной ткани // Лечащий Врач. 2008; 6: 43–47.
- Сергеев П. В., Шимановский Н. Л. Рецепторы физиологически активных веществ. М., 1987. 400 с.
- Bristow M. R. β-Adrenergic receptor blockade in chronic heart failure // Circulation. 2000; vol. 10: 558–569.
- Малкова М. И., Булашова О. В., Хазова Е. В. Определение адренореактивности организма по адренорецепции клеточной мембраны при сердечно-сосудистой патологии // Практическая медицина. 2013; 3 (71): 20–23.
- Тихонова О. В., Дрокина О. В., Моисеева Н. Е., Нечаева Г. И., Мартынов А. И. Оценка информативности методов определения содержания магния в организме на примере пациентов с признаками дисплазии соединительной ткани // Архив внутренней медицины. 2014; 1 (15): 19–24.
- Мартынов А. И., Акатова Е. В., Николин О. П., Урлаева И. В. Влияние магния оротата на кардиоваскулярные риски // Терапия. 2016; 5: 52–57.
- Мартынов А. И., Акатова Е. В. Опыт пятнадцатилетнего применения препаратов магния у больных с пролапсом митрального клапана // Кардиология. 2011; 6: 60–65.
- Torshin I. Y., Gromova O. A., Kalacheva A. G., Oshchepkova E. V., Martynov A. I. Meta-analysis of clinical trials of cardiovascular effects of magnesium orotate // Ter. Archive. 2015; 87 (6): 88–97. 10.17116/terarkh201587688–97.
- Сологова С. С., Максимов М. Л., Тарасов В. В. Фармакологическая эффективность препаратов магния. Оротат магния (Магнерот) в клинической практике // РМЖ. Медицинское обозрение. 2014; 127: 1966.
- Городецкий В. В., Талибов О. Б. Препараты магния в медицинской практике. Малая энциклопедия магния. М.: Медпрактика, 2003. 44 с.
- Torda T., Yamaguchi I., Kopin I.J., Axelrod J Quinacrine-blocked desensitization of adrenoreceptors after immobilization stress or repeated injection of isoproterenol in rats // J. Pharmacol. Exp. Ther. 1981; vol. 216: 334–338
- Земцовкий Э. В. Спортивная медицина. СПб: Гиппократ, 1995. 448 с.
- Стрюк Р. И., Длусская И. Г. Адренореактивность и сердечно-сосудистая система. М.: Медицина, 2003. 160 с.
- Пономарева Д. А., Нагаева Т. А., Балашева И. И. Особенности состояния органов пищеварительного тракта и системы перекисного окисления липидов при дисплазии соединительной ткани у школьников по результатам скрининговых осмотров // Сибирский вестник гепатологии и гастроэнтерологии. 2007; 21: 71–73.
- Нечаева Г. И., Мартынов А. И. Дисплазия соединительной ткани: сердечно-сосудистые изменения, современные подходы к диагностике и лечению. М: ООО «Медицинское информационное агентство». 2017; 400.
Е. Н. Логинова1, кандидат медицинских наук
Ю. В. Москвина, кандидат медицинских наук
Г. И. Нечаева, доктор медицинских наук, профессор
И. В. Друк, доктор медицинских наук, профессор
А. А. Семенкин, доктор медицинских наук, профессор
М. И. Шупина, кандидат медицинских наук
Ю. В. Терещенко, кандидат медицинских наук
ФГБОУ ВО ОмГМУ МЗ РФ, Омск
1 Контактная информация: osma-genpract@yandex.ru
Роль оротата магния в лечении аритмического синдрома на фоне дисплазий соединительной ткани/ Е. Н. Логинова, Ю. В. Москвина, Г. И. Нечаева, И. В. Друк, А. А. Семенкин, М. И. Шупина, Ю. В. Терещенко
Для цитирования: Лечащий врач № 12/2018; Номера страниц в выпуске: 50-53
Теги: сердечно-сосудистая система, аритмический синдром, молодые пациенты
Содержание
-
Структурная формула
-
Русское название
-
Английское название
-
Латинское название
-
Химическое название
-
Брутто формула
-
Фармакологическая группа вещества Магния оротат
-
Нозологическая классификация
-
Код CAS
-
Фармакологическое действие
-
Фармакология
-
Применение вещества Магния оротат
-
Противопоказания
-
Применение при беременности и кормлении грудью
-
Побочные действия вещества Магния оротат
-
Взаимодействие
-
Передозировка
-
Способ применения и дозы
-
Меры предосторожности
-
Торговые названия с действующим веществом Магния оротат
Структурная формула
Русское название
Магния оротат
Английское название
Magnesium orotate
Латинское название
Magnesii orotas (род. Magnesii orotatis)
Химическое название
2,6-Диоксо-3H-пиримидин-4-карбоксилат магния
Брутто формула
C10H6MgN4O8
Фармакологическая группа вещества Магния оротат
Нозологическая классификация
Список кодов МКБ-10
-
E63 Физические и умственные перегрузки
-
E78 Нарушения обмена липопротеинов и другие липидемии
-
I21 Острый инфаркт миокарда
-
I49.9 Нарушение сердечного ритма неуточненное
-
I50.0 Застойная сердечная недостаточность
-
I70 Атеросклероз
-
I73.9 Болезнь периферических сосудов неуточненная
Код CAS
27067-77-2
Фармакологическое действие
—
антиагрегационное, антиаритмическое, восполняющее дефицит магния и оротовой кислоты, спазмолитическое.
Фармакология
Магний участвует в переносе, хранении и утилизации энергии, синтезе белка и нуклеиновых кислот, ряде митохондриальных процессов. Является кофактором многих ферментативных реакций: гидролиз и перенос фосфатной группы, функционирование Na+-K+-АТФазного, Ca2+-АТФазного и протонного насосов. Контролирует баланс внутриклеточного калия. При остром инфаркте миокарда магний несколько снижает системное сосудистое сопротивление, увеличивает коронарный кровоток, предупреждает коронароспазм, выступает как кардиопротектор, устраняя внутриклеточный дефицит не только магния, но и калия, фосфатов (одновременно уменьшается содержание кальция и натрия), редуцирует зону инфаркта и выраженность сердечной недостаточности. Снижает синтез тромбоксана B2 и угнетает агрегацию тромбоцитов, в т.ч. тромбининдуцированную. Оротовая кислота — эндогенный метаболит, участвующий в построении пиримидиновых оснований, входящих в состав нуклеиновых кислот. Улучшает процессы регенерации, стимулирует синтез сократительных белков миокарда, способствует клеточной утилизации магния и проявлению его эффектов.
Применение вещества Магния оротат
Комплексное лечение и профилактика следующих заболеваний и состояний: инфаркт миокарда, хроническая сердечная недостаточность; аритмия, вызванная дефицитом магния; спастические состояния (в т.ч. ангиоспазм), атеросклероз, дислипидемии. При повышенных физических нагрузках.
Противопоказания
Гиперчувствительность, нарушение функции почек, мочекаменная болезнь, цирроз печени с асцитом.
Применение при беременности и кормлении грудью
В периоды беременности и грудного вскармливания возможно с осторожностью и строго по показаниям, поскольку в это время потребность в магнии значительно возрастает. Если его содержание не сбалансировано, это может привести к серьезным осложнениям, в т.ч. невынашиванию беременности.
Побочные действия вещества Магния оротат
Со стороны органов ЖКТ: неустойчивый стул и диарея (при приеме высоких доз), которые обычно проходят самостоятельно при снижении дозы.
Прочие: аллергический дерматит.
Взаимодействие
Снижает абсорбцию железа, тетрациклина, фторида натрия. Уменьшает степень дефицита магния и риск связанных с ним осложнений при приеме диуретиков, аминогликозидов, цисплатина, циклоспорина, амфотерицина, пентамидина, метотрексата, слабительных.
Передозировка
Симптомы: возможно усиление побочных реакций.
Лечение: симптоматическая терапия.
Способ применения и дозы
Внутрь, по 1 г 3 раза в день в течение 7 дней, затем по 0,5 г 2–3 раза в сутки ежедневно, продолжительность курса не менее 4–6 нед. Повторные курсы возможны после консультации врача. При ночных судорогах икроножных мышц рекомендуется принимать по 1–1,5 г по вечерам.
Меры предосторожности
При лечении препаратами железа, тетрациклина и натрия фторида прием магния оротата должен быть отсрочен не менее чем на 2 ч. При возникновении признаков кишечной диспепсии (неустойчивый стул, диарея) дозу необходимо уменьшить.
Магния оротат можно применять длительное время. Следует учитывать, что к дефициту магния в организме могут приводить заболевания ЖКТ, потребление пищевых продуктов со сниженным содержанием магния, хронический алкоголизм (из-за уменьшения резорбции магния в почечных канальцах и усиления выведения магния из организма), прием некоторых лекарственных препаратов (пероральные контрацептивы, диуретики, миорелаксанты, глюкокортикоиды, инсулин), состояния, требующие повышенного потребления магния (гиподинамия, стресс, беременность).
Торговые названия с действующим веществом Магния оротат
| Торговое название | Цена за упаковку, руб. |
|---|---|
| Магнемакс |
от 477.00 до 477.00 |
| Магнерот® |
от 289.00 до 1372.00 |
Фармакологическое действие
Средство, содержащее магний. Магний является важнейшим макроэлементом. Необходим для обеспечения многих энергетических процессов, участвует в обмене белков, жиров, углеводов и нуклеиновых кислот.
Магний принимает участие в процессе нервно-мышечного возбуждения, угнетая нервно-мышечную передачу. Особый интерес магний представляет как естественный физиологический антагонист кальция. Особый интерес магний представляет как естественный физиологический антагонист кальция. Магний контролирует нормальное функционирование клеток миокарда; участвует в регуляции сократительной функции миокарда. В стрессовых ситуациях выводится повышенное количество свободного ионизированного магния, в связи с чем дополнительное количество магния способствует повышению резистентности к стрессу.
Дефицит магния приводит к нейромышечным нарушениям (моторной и сенсорной повышенной возбудимости, судорогам, парестезии), психологическим изменениям (состоянию депрессии, спутанности сознания и галлюцинациям), сердечно-сосудистым заболеваниям (желудочковой экстрасистолии, тахикардии, повышенной чувствительности к сердечным гликозидам). Дефицит магния при беременности увеличивает вероятность токсикоза и преждевременных родов.
Соли оротовой кислоты участвуют в процессе обмена веществ. Кроме того соли оротовой кислоты необходимы для фиксации магния на АТФ в клетке и проявления его действия.
Фармакокинетика
Всасывается приблизительно 35-40% от принятой дозы. Гипомагниемия стимулирует всасывание ионов магния. Присутствие солей оротовой кислоты, способствуют улучшению всасывания магния.
Магний выводится почками, выведение уменьшается при дефиците магния и увеличивается при его избытке.
Показания активного вещества
МАГНИЯ ОРОТАТ
В составе комплексной терапии и для профилактики следующих заболеваний: инфаркт миокарда, стенокардия; хроническая сердечная недостаточность; аритмии, вызванные дефицитом магния; спастические состояния — боли и спазмы мышц (в т.ч. ангиоспазм); атеросклероз; артериит; нарушения липидного обмена.
Режим дозирования
Принимают внутрь по 1 г 3 раза/сут в течение 7 дней, затем — по 200 мг 2-3 раза/сут ежедневно. Продолжительность курса лечения — не менее 4-6 недель.
При ночных судорогах икроножных мышц рекомендуют принимать вечером 1-1.5 г.
Побочное действие
Со стороны пищеварительной системы: неустойчивый стул и диарея (при приеме препарата в высоких дозах), которые обычно проходят самостоятельно при снижении дозы.
Прочие: возможны аллергические реакции.
Противопоказания к применению
Мочекаменная болезнь; нарушения функции почек; предрасположенность к образованию кальциево-магниево-аммониево-фосфатных камней; цирроз печени с асцитом; детский и подростковый возраст до 18 лет; повышенная чувствительность к активному веществу.
Применение при беременности и кормлении грудью
Применение при беременности и в период лактации возможно по показаниям, если потенциальная польза для матери превышает потенциальный риск для плода и ребенка. Если содержание магния не сбалансировано, то это может привести к серьезным осложнениям, в т.ч. невынашиванию беременности.
Особые указания
При необходимости можно применять длительно.
Лекарственное взаимодействие
При одновременном приеме магнийсодержащих препаратов с препаратами железа, натрия фторида и тетрациклинами может снижаться абсорбция последних. Поэтому следует принимать препараты с интервалом 2-3 ч.
Пероральные контрацептивы, диуретики, миорелаксанты, ГКС, инсулин снижают эффект магния.
Применение магния (Магнерот) в лечении сосудистых заболеваний
Статьи
Е.И. Чуканова
Кафедра неврологии и нейрохирургии РГМУ, Москва
В настоящее время не вызывает сомнения роль микроэлементов в многообразных функциях организма и каждой клетки в отдельности. Фундаментальные науки (биохимия, фармакология, физиология, генетика) в XX веке дали начало нейрохимии, нейрофармакологии, нейрофизиологии. В последние годы сформировалась новая наука – клиническая элементология. Применение знаний этой новой дисциплины для диагностики и лечения заболеваний нервной системы — насущная необходимость для постановки диагноза, оценки прогноза заболевания и достижения более высоких клинических результатов при лечении больных [1].
Магний относится к жизненно необходимым элементам. К сожалению, на протяжении длительного периода времени магнию (Mg2+) не уделялось должного внимания, что во многом было обусловлено трудностями в установлении его концентрации в плазме и тем, что, будучи полученным, данный показатель косвенно отражал сложную схему распределения Mg2+ в организме [1, 2].
К настоящему времени физиологическая активность магния изучена достаточно хорошо. Являясь универсальным регулятором обменных процессов в организме, Mg2+ участвует в энергетическом (комплексирование с АТФ и активация АТФ-аз, окислительное фосфорилирование, гликолиз), пластическом (синтез белка, липидов, нуклеиновых кислот), электролитном обменах [3]. Выполняя роль естественного антагониста кальция, магний принимает участие в расслаблении мышечного волокна, снижает агрегационную способность тромбоцитов, поддерживает нормальный трансмембранный потенциал в электровозбудимых тканях [4]. Рассмотрим подробнее роль магния в функционировании органов системы кровообращения.
Суточная потребность в Mg2+ составляет 300 мг для женщин, 350 мг для мужчин и возрастает при беременности, занятиях спортом. Наиболее богаты магнием злаковые культуры, бобовые, зелень, орехи, шоколад. Усвояемость магния из пищевых продуктов составляет 30-35 %. Она может увеличиваться под влиянием витамина В6, молочной, аспарагиновой, оротовой кислот [16, 17].
Несмотря на то, что магний широко распространён в природе, его дефицит в человеческой популяции встречается в 16–42 % [18]. Это связано с составом пищи: часть продуктов располагает малым содержанием магния, другие – первоначально достаточным его количеством, но не выгодным в плане сопутствующих ионов кальция и фосфатов, некоторых липидов и протеинов, уменьшающих абсорбцию магния из кишечника. Возрастное замедление моторики желудочно-кишечного тракта, дисбактериозы, полиэтиологичный синдром мальабсорбции дополнительно снижают всасывание Mg2+. К другим факторам, способствующим гипомагниемии, относят пребывание в помещениях с жарким микроклиматом, злоупотребление алкоголем, беременность, лактацию, нерациональную гипокалорийную диету, стресс и синдром хронической усталости [19]. Среди важных причин развития дефицита магния можно выделить причины, связанные:
- с повышенным выведением (через желудочно-кишечный тракт при рвоте, диарее, через почки при нефротическом синдроме, у больных с сахарным диабетом, при диуретической терапии, лечении циклоспорином);
- с эндокринными нарушениями (гипертиреоидизм, гиперальдестеронизм);
- с повышенной потребностью магния (беременность, кормление грудью, стресс, период реконвалесценции, период роста, повышенное потоотделение)
- со сниженным потреблением (диета, алкоголизм, парентеральное питание с низким содержанием магния и др.);
- со сниженной кишечной резорбцией (энтеропатии, состояния после обширных резекций кишечника, синдром мальабсорбции, продолжительная диарея).
Клинические проявления отражают патогенетическую сущность магниевого дефицита и разделяются исследователями на группы: эндокринно-обменные проявления, психические, неврологические, сердечно-сосудистые заболевания.
Магний влияет на эндотелий, который играет ключевую роль в сосудистом гомеостазе, в частности, за счёт продукции оксида азота и участия в управлении агрегацией тромбоцитов. Доказано, что дефицит ионов магния увеличивает активность тромбоксана А2, что сопровождается повреждением сосудистой стенки. В рандомизированном двойном слепом исследовании была изучена эндотелий-зависимая дилатация плечевой артерии на фоне приёма препарата магния по сравнению с группой контроля. В исследовании показано, что через 6 месяцев приёма препаратов магния этот показатель увеличился на 15,5 ± 12,0 % (р 2+ [5].
Представляет интерес вопрос об антиатерогенной активности магния. Длительный дефицит магния — одно из необходимых условий для манифестации и развертывания генетически детерминированной программы атеросклероза. В условиях атерогенной диеты недостаток в пище магния способствует прогрессированию склеротического поражения сосудов, и, наоборот, назначение магния приводит к регрессу гиперхолестеринемии. При дефиците магния в крови повышено содержание триглицеридов, липопротеидов низкой плотности и очень низкой плотности и, наоборот, снижен уровень липопротеидов высокой плотности. Согласно результатам исследования The Atherosclerosis Risk in Communities (ARIC), гипомагниемия сопровождает развитие ишемической болезни сердца (ИБС). Подобный вывод был сделан на основании наблюдения 13 922 пациентов на протяжении 4-7 лет с учётом социодемо-графических характеристик, вредных привычек, уровней холестерина, фибриногена и других факторов [6]. В дополнение известно, что наиболее выраженный дефицит магния имеется у лиц с повышенным содержанием атерогенных липидов [7].
Исследования [8] показали, что длительно существующий дефицит магния, особенно на фоне эссенциальной гипертонии, является достоверным фактором риска возникновения острых нарушений мозгового кровообращения. Кровеносные сосуды, снабжающие ткань мозга, чрезвычайно чувствительны к магниевому балансу.
Недостаток магния при сердечной недостаточности свидетельствует в пользу того, что это заболевание является, как правило, результатом прогрессирования ИБС и/или АГ, а также их осложнений [9]. Степень гипомагниемии может служить показателем тяжести заболевания и отчасти объяснять выраженность симптоматики [10]. Назначение магний-содержащих препаратов особенно оправдано при длительном приёме сердечных гликозидов, которые провоцируют гипомагниемию и последующие нарушения ритма, связанные с дефицитом иона. Считается, что ионы Mg2+ тормозят активность ренин-ангиотензин-альдостероновой системы (РААС), и при их дефиците создаются более благоприятные условия для системной вазоконстрикции [11].
Несмотря на отсутствие единого подхода к оценке роли гипомагниемии при АГ, необходимость коррекции электролитного обмена, особенно нарушений, связанных с приёмом диуретиков, является очевидной [12].
Гипомагниемия усиливается при сахарном диабете 2 типа, который стал частым спутником больных с кардиоваскулярной патологией старших возрастов [13]. Недостаток магния сопряжён с нарушенной толерантностью к глюкозе [14], а препараты магния способны улучшать инсулинозависимую утилизацию.
Дефицит цитозольного магния в нейронах является наиболее ранним и точным маркером апоптоза нервных клеток. В последние годы появилось огромное количество литературных данных относительно апоптоза. Огромное количество исследований, проведённых за последние годы привнесло новое понимание в молекулярные механизмы программированной смерти клетки; уточнило её роль в процессах гистогенеза и атрофии. Оценка этих механизмов подвела исследователей к пониманию терапевтических направлений в манипуляции апоптозом и в осуществлении терапевтического воздействия биотехнологическими методами. В последние годы было доказано, что микроэлементы (МЭ) способны модулировать программу апоптоза посредством определённых механизмов [15]. Ряд МЭ играет существенную роль в росте клетки и обмене веществ. Их транспорт и накопление в различных клетках определены в соответствии с функциональными требованиями компонентов клетки и генетических стимулов или патологически развивающимися механизмами проходимости. Поэтому даже умеренный дефицит или избыток МЭ в различных токсикологических моделях может иметь длительные эффекты на процессы репопуляции клеток и апоптоза [1]. Недавние открытия показали, что сутью механизма, лежащего в основе апоптоза, спровоцированного избытком или дефицитом МЭ, являются фундаментальные процессы митохондриального повреждения и активация каскада каспаз. Микроэлементы вовлечены в самосборку, синтез и регулирование митохондриальных ферментов, что вносит вклад в целостность комплексов дыхательной цепи.
Магний и другие микроэлементы являются структурными компонентами многих ферментов. Они влияют на кальций-зависимый синтез NO, косвенно регулируют пролиферацию нервных клеток и их пластичность. Доказано участие ионов магния в работе глутаматных и NMDA-рецепторов: при дефиците магниевого ионного окружения эти рецепторы возбуждаются.
В эксперименте на крысах доказана нейропротекторная роль сульфата магния, введённого за 30 минут до моделируемой гипоксии мозга. Многоцентровые эпидемиологические исследования выявили повышение частоты мозгового инсульта в биогеохимических провинциях со сниженным содержанием магния и кальция в мягкой воде.
Одним из важных эффектов магния является торможение процессов возбуждения в коре головного мозга и связанная с этим реализация наркотического, снотворного, седативного, аналитического и противосудорожного эффекта. Экспериментальными исследованиями доказана роль магния в качестве модулятора эффектов возбуждающих аминокислот в ЦНС. При дефиците магния снижается способность к концентрации внимания и функции памяти. Классикой нейрохимии стало воззрение на магний как на ион с чёткими седативными свойствами. Синтез ацетилхолина в головном мозге возможен только в присутствии ионов магния. Кора головного мозга обладает выраженной реактивностью, поэтому расстройства высшей нервной деятельности сопровождаются не только нарушениями энергетического обмена, но и изменениями трансмембранного транспорта ионов, в первую очередь магния. На большом экспериментальном и клиническом материале показана зависимость выраженности эпилептиформной готовности в коре головного мозга от уровня ионов магния.
Дефицит магния в организме — обычное явление для людей, подвергающихся хроническим стрессам, страдающим депрессией и аутизмом.
Стрессы различной природы (физические, психические) увеличивают потребность в магнии и служат причиной внутриклеточной магниевой недостаточности. Стресс и магниевая недостаточность являются взаимообуславливаемыми процессами, обоюдно усугубляющими друг друга. Состояние острого и хронического стресса ведёт к истощению внутриклеточного пула магния и его потерям с мочой, так как в стрессовой ситуации выделяется большое количество адреналина и норадреналина, способствующих выведению магния из клеток. При нормальном снабжении клеток магнием эти катехоламиновые воздействия удаётся снизить. В результате чего повышается резистентность к стрессу. По данным А.В. Кудрина и Громовой [1], дефицит магния встречается у 70 % детей с синдромом дефицита внимания с гиперактивностью и у больных с ранними формами цереброваскулярных заболеваний.
Дефицит магния со стороны ЦНС ведёт к повышению активности глубоких сухожильных рефлексов, атаксии, тремору, дезориентации, судорожным состояниям, нистагму, парестезии.
Доказано, что нормальный уровень магния в организме обеспечивает активность нейромедиаторной аминокислоты глицина, участвующей в таких важных неврологических функциях, как тонкая моторика, точность движений, поддержание позы и ходьбы. Препарат глицин на фоне дефицита магния не может в полной мере реализовывать нейропротекторные эффекты, так как глицин должен быть активирован магнием.
Необходимость коррекции магниевого дефицита бесспорна. Однако это весьма затруднительно в связи с тем, что магний представляет собой главным образом внутриклеточные ионы. Именно поэтому целесообразно использование комплексной терапии дефицита этих ионов с компонентами, способствующими проникновению ионов магния во внутриклеточное пространство, или комплексными препаратами.
Назначение препаратов магния представляет собой своеобразную заместительную терапию и в качестве цели преследует коррекцию его нормального уровня и восстановление физиологических процессов, в которых Mg2+ принимает активное участие [15].
Заслуживает внимания препарат Магнерот, в состав которого входит оротовая кислота. Оротовая кислота необходима для фиксации магния на АТФ в клетке, что приводит к терапевтической активности магния. Помимо этого, оротовая кислота способствует росту клеток, участвуя в процессе обмена веществ. Магнерот успешно применяется в составе комплексной терапии в лечении и профилактике сердечно-сосудистых заболеваний: ишемической болезни сердца, магний-зависимых сердечных аритмий, различных спастических состояниях (в т. ч. ангиоспазмов), инфаркта миокарда, атеросклероза и гиперлипидемий.
Применение оротата магния началось в 60-х годах прошлого века. Преимущественно препарат использовался в терапии сердечной недостаточности, в т. ч. вызванной алкогольной кардиомиопатией. На модели алкогольного повреждения сердца у животных было показано, что одной из причин заболевания является нарушение синтеза РНК в кардиомиоцитах, а оротовая кислота необходима для нормального хода данного процесса. Оротовая кислота (которую называют так же витамином В13), помимо участия в обмене магния, обладает собственной метаболической активностью: соединение является одним из метаболических предшественников пиримидиновых нуклеотидов, т. е. в конечном счёте необходимо для нормального хода анаболических процессов. На уровне сердечной мышцы эффект выражается в повышении синтеза белка и АТФ [20]. Анаболическая активность оротовой кислоты с успехом используется, например, у спортсменов с целью повышения работоспособности и конкурирует с таковой у стероидных препаратов. Установлено, что оротовая кислота поддерживает холестерин в коллоидном состоянии, что, возможно, препятствует его отложению в сосудистой стенке. Положительно и то, что магниевая соль оротовой кислоты слабо растворима в воде, поэтому практически не обладает послабляющим эффектом, хорошо всасывается.
Оротат магния (Магнерот) сочетает в себе все описанные выше свойства Mg2+ и оротовой кислоты [21], чем предопределяется широта его терапевтических эффектов. Так, в комплексной терапии ИБС на фоне приёма препарата урежается частота приступов стенокардии и потребность в сублин-гвальном нитроглицерине. Препарат используется в комбинированном лечении некоторых видов нарушений сердечного ритма, АГ, сердечной недостаточности различного генеза, благоприятно влияет на уровень глюкозы крови при сахарном диабете и на качественный состав липидов.
Во всем мире пероральные препараты магния в комбинированной терапии сердечно-сосудистой патологии приобретают всё большее значение, поскольку они эффективны, хорошо переносятся больными и достаточно дешевы. В нашей стране накоплен большой опыт применения Магнерота, особенно в использовании препарата при наиболее распространённых в кардиологии нозологиях. Можно выделить группы пациентов, у которых назначение препарата Магнерот в качестве компонента комбинированной терапии будет наиболее успешным [22]:
- дефицит ионов Mg2+ (клиническая картина, гипо-магниемия, снижение экскреции Mg2+ с мочой);
- сочетание АГ с гиперлипидемией, проявлениями ишемии миокарда;
- сочетание АГ с нарушением толерантности к глюкозе или сахарным диабетом 2 типа;
- наличие хронической алкогольной интоксикации, хронический стресс (профилактика стресс-индуцированных сердечно-сосудистых осложнений).
В одном из исследований были включены больные со стенокардией и АГ. При лечении данных больных Магнеротом в дозе 6 табл./сут в течение 6 недель в комплексной терапии с антиангинальными и антигипертензивными средствами получено статистически достоверное снижение уровня АД с 157,8/88,3 мм рт. ст. до 125,6/82,8 мм рт. ст. [23], что сочеталось с урежением сердечного ритма [24].
Эффективность Магнерота была продемонстрирована в лечении пожилых пациентов обоего пола со стенокардией III функционального класса и АГ II степени в комплексной терапии с основными препаратами. Назначение Магнерота в течение 5 недель данным пациентам привело к уменьшению частоты приступов стенокардии в среднем с 11,2 до 1,9 в неделю и снижению потребности в нитросорбите с 80 до 32 мг/сут. Количество нитроглицерина, использованного каждым больным за время комплексного лечения с Магнеротом, составило, в среднем, 29 таблеток, в то время как в контрольной группе за этот же период больные приняли по 53 таблетки. Достигнутый терапевтический эффект сохранялся в течение 2 недель после отмены Магнерота [25].
Во многих исследованиях Магнерот демонстрировал эффективность в комбинированной терапии больных после перенесённого инфаркта миокарда [26], причём особого внимания заслуживает профилактическая активность в отношении аритмий, нормализация фракции выброса и уменьшение конечного систолического и диастолического объёма [27], что особенно важно в восстановительный период после перенесённого инфаркта миокарда.
Магнерот хорошо переносится, процент побочных эффектов весьма невелик (немного более одного процента) и выражается в нарушениях со стороны пищеварительной системы (диарея, запоры), что, как правило, возникает при приёме препарата в высоких дозах и обычно проходит при снижении дозы. Единственным противопоказанием для назначения данного препарата является наличие почечной патологии — мочекаменная болезнь и нарушения почечной функции. Важно отметить, что Магнерот может применяться в период беременности и лактации. Магнерот, назначаемый в дозе по 2 таблетки 3 раза в сутки в течение 7 дней, с переходом на 1 таблетку 2-3 раза в сутки ежедневно можно применять длительное время.
Таким образом, многочисленные исследования дают основание считать применение препарата Магнерот эффективным в кардиологической практике.
Литература
- Кудрин А.В., Громова О.А. Микроэлементы в неврологии. М.: 2006; 303.
- Фогорос Р.Н. Антиаритмические средства. Изд. 2е, исп. Пер. с англ. М.: Спб.: «Издательство БИНОМ» – «Невский Диалект», 2002; 190.
- Стуров Н.В. Кафедра общей и клинической фармакологии РУДН, Москва. Препараты магния – обоснование применения в кардиологической практике. Medi. Ru «Подробности о лекарствах». Woerwad Pharma.
- Физиология человека. Под редакцией Агаджаняна Н.А., Циркина В.И. Спб.: Сотис 1998; 528.
- Метелица В.И. Справочник по клинической фармакологии сердечнососудистых лекарственных средств. 2е изд., перераб. и доп. М.: Издательство Бином – Спб.: Невский Диалект, 2002; 926.
- Метаболизм магния и терапевтическое значение его препаратов. М.: ИД Медпрактика – М. 2002; 28.
- Применение магния и оротовой кислоты в кардиологии. М.: ИД Медпрактика – М. 2002; 20.
- Shechter M., Sharir M., Labrador M.J. et al. Oral magnesium therapy improves endothelial function in patients with coronary artery disease // Circulation. Nov 2000; 102: 2353–2358.
- Liao F., Folsom A.R., Brancati F.L. Is low magnesium concentration a risk factor for coronary heart disease? The Atherosclerosis Risk in Communities (ARIC) Study // Am Heart J. 1998 Sep;136: 3: 480–90.
- Ueshima K. Magnesium and ischemic heart disease: a review of epidemiological, experimental, and clinical evidences // Magnes Res. 2005 Dec; 18: 4: 275–84.
- Suter P.M. The effects of potassium, magnesium, calcium and fiber on risk of stroke // Nutr. Rev. 1999; 57: 84–88.
- Witte K.K., Clark A.L. Micronutrients and their supplementation in chronic cardiac failure. An update beyond theoretical perspectives // Heart Fail Rev. 2006 Mar; 11: 1: 65–74.
- Sueta C.A., Clarke S.W., Dunlap S.H. Effect of acute magnesium administration on the frequency of ventricular arrhythmia in patients with heart failure // Circulation. Feb 1994; 89: 660–666.
- Lezhitsa I.N. Potassium and magnesium depletions in congestive heart failurepathophysiology, consequences and replenishment // Clin Calcium. 2005 Nov; 15: 11: 123–33.
- Hadj A., Pepe S., Marasco S., Rosenfeldt F. The principles of metabolic therapy for heart disease // Heart Lung Circ. 2003; 12: Suppl 2: S55–62.
- Head K.A. Peripheral neuropathy: pathogenic mechanisms and alternative therapies // Altern Med Rev. 2006 Dec; 11: 4: 294–9.
- Ma B., Lawson A.B., Liese A.D. et al. Dairy, magnesium, and calcium intake in relation to insulin sensitivity: approaches to modeling a dosedependent association // Am J Epidemiol. 2006; Sep 1; 164: 5: 449–58.
- Kudrin A.V. Trans elements and apoptosis // J. Trans Element Med. Biol. 1998; 12: 65–76.
- Engstrom A.M., Tobelmann R.C. Nutritional consequences of reducing sodium intake // Ann Intern Med. 1983 May; 98: 5 Pt 2: 870–2.
- Bourre J.M. Effects of nutrients (in food) on the structure and function of the nervous system: update on dietary requirements for brain. Part 1: micronutrients // J Nutr Health Aging. 2006 SepOct;10: 5: 377–85.
- Rosenfeldt F.L. Metabolic supplementation with orotic acid and magnesium orotate // Cardiovasc Drugs Ther. 1998; 12: Suppl 2: 147–52.
- Classen H.G. Magnesium orotateexperimental and clinical evidence // Rom J Intern Med. 2004; 42: 3: 491–501.
- Лазебник Л.Б., Дроздова С.Л. Коррекция магниевого дефицита при сердечнососудистой патологии // Кардиология. 1997; 5: 103–104.
- Погорелко О.И., Орлов В.А., Шутько В.Ю. и др. Применение препарата магнерот в терапии больных ишемической болезнью сердца с метаболическим кардиоваскулярным синдромом // Актуал. вопр. клинич. ж.д. медицины. Мво путей сообщ., Центр. клинич. больница. 2000; 5: 223–233.
- Терапия магнезиуморотатом. Таблетки Магнерот. Научный обзор. Медпрактика. 2001; 31.
- Ежов А.В., Пименов Л.Т., Замостьянов М.В. Клиническая эффективность магнерота в лечении стабильной стенокардии напряжения в сочетании с артериальной гипертензией у лиц пожилого возраста // Рос. мед. вести. 2001; 1: 71–74.
- Шилов А. М. и др. Применение препаратов магния для профилактики нарушений ритма сердца у больных острым инфарктом миокарда // Рос. кардиол. журн. 2002; 1: 16–19.
- Рагозина Н.П., Чурин К.В., Чурина С.К. Пероральные препараты магния при остром инфаркте миокарда: влияние на течение заболевания и развитие аритмий // Вестн. аритмологии. 2000; 19: 23–28.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)