В соответствии с рекомендациями ВОЗ термин «острые кишечные инфекции»
(ОКИ) объединяет более 30 заболеваний бактериальной, вирусной или
протозойной этиологии, основным симптомом которых является острая
диарея (рис. 1).
На практике все зарегистрированные ОКИ принято разделять на три основные группы:
- заболевания, вызываемые неустановленным возбудителем (около 70% случаев);
- острые кишечные инфекции, вызываемые установленным возбудителем (около 20%);
- бактериальная дизентерия (около 10%).
Тот факт, что 70% случаев ОКИ приходится на заболевания с
неустановленным возбудителем, можно считать следствием общепринятого
для ОКИ «синдромального» принципа формирования диагноза, который
полностью оправдывает себя при заболеваниях, не носящих эпидемического
характера. В самом деле, при спорадических ОКИ (а их большинство)
сходство клинической картины и течения заболеваний различной этиологии
позволяет не тратить время на точное определение возбудителя, поскольку
это существенно не влияет на выбор стратегии и тактики лечения. При
эпидемических ОКИ как можно более раннее выделение и идентификация
возбудителя болезни, напротив, становятся важнейшей задачей, требующей,
к сожалению, значительных затрат времени и наличия хорошо оснащенной
лаборатории.
Важно, что в наиболее обширную группу ОКИ неустановленной этиологии
входят и большинство так называемых пищевых токсикоинфекций (ПТИ) — эту
группу составляют приблизительно 20 этиологически разных, но
патогенетически и клинически сходных заболеваний, не представляющих
эпидемической опасности.
Более чем в половине случаев этиологию ОКИ не удается установить ни
клинически, ни лабораторно. Эта задача, равно как и выбор
патогенетического лечения, тем более не может быть решена (да и не
ставится) на этапе догоспитальной помощи. Усилия врача скорой
медицинской помощи (СМП) должны быть направлены на:
- коррекцию тяжелых нарушений жизненно важных функций организма больного;
- дифференцирование инфекционного, терапевтического или хирургического генеза заболевания;
- решение
вопроса о необходимости госпитализации больного для специализированного
лечения или проведения противоэпидемических мероприятий.
Клиническая картина ОКИ
ОКИ — заболевания различной этиологии и семиотики — объединяют общий
для всех этих состояний, преимущественно фекально-оральный, способ
передачи возбудителя и развитие вследствие этого характерного
симптомокомплекса острой диареи (табл. 1).
В то же время выраженность диарейного синдрома, равно как и степень
тяжести общего состояния, возможные исходы и стратегия лечения
заболевания определяются возбудителем инфекции. При всей
относительности синдромальной доклинической диагностики ОКИ можно
выделить признаки, наиболее характерные для диареи различной этиологии.
Так, бактериальную диарею (БД) отличают более тяжелое клиническое
течение и более неблагоприятный прогноз по сравнению с вирусной
диареей, поскольку патофизиологические механизмы БД заключаются в
повреждении слизистой оболочки желудочно-кишечного тракта
бактериальными энтеротоксинами или в результате инвазии микроорганизмов
в клетки эпителия. Инкубационный период при БД может длиться от 6-8
часов до 7-10 суток, однако чаще всего он составляет около 3 дней.
Самый короткий инкубационный период — у кокковых инфекций и
сальмонеллеза. Дебют БД сопровождается выраженной интоксикацией,
значительным ухудшением общего самочувствия, дегидратацией, головной
болью, лихорадкой до 38-39°С, тошнотой и рвотой. При генерализации
инфекции возможно появление симптомов раздражения мозговых оболочек,
мышечных и костно-суставных болей. БД всегда сопровождается
болезненными тенезмами и схваткообразной сильной болью в животе, а при
дизентерии приводит к появлению кровавого стула. Нередко у мужчин при
БД развивается синдром Рейтера (артрит, конъюнктивит, уретрит). В
острой фазе болезни проявляются и специфические симптомы того или иного
возбудителя БД. Прогноз БД всегда тревожный, и при клинически
очерченном течении заболевание во всех случаях требует госпитализации и
эпидемиологической оценки.
ПТИ также относятся к БД, так как вызываются условно-патогенными
бактериями и в ряде случаев имеют групповой, эксплозивный характер.
Однако в подавляющем большинстве случаев ПТИ протекают спорадически с
развитием острого гастрита, гастроэнтерита или гастроэнтероколита, с
той или иной степенью обезвоживания и интоксикации и имеют
благоприятный прогноз.
При диарее вирусной этиологии (ВД) целостность слизистой оболочки
желудочно-кишечного тракта в большинстве случаев не нарушается и в
процесс редко вовлекается толстая кишка. Инкубационный период, как
правило, более короткий, чем при эпидемической БД. Острый вирусный
гастроэнтерит, хотя и сопровождается лихорадкой и нарушением общего
состояния больного, редко приводит к тяжелой интоксикации, развитию
выраженной воспалительной реакции и дегидратации организма больного. К
числу значимых дифференциальных критериев ВД можно отнести отсутствие
при этих заболеваниях выраженной боли в животе, водянистый, а не
слизисто-гнойный и кровавый характер испражнений. ВД нередко
сопровождается острым респираторным заболеванием, особенно у детей.
Продолжительность ВД редко превышает 3 дня, и в целом заболевание имеет
благоприятный прогноз. Пациенты с относительно легким течением ВД в
госпитализации не нуждаются.
Из ОКИ паразитарного происхождения (ПД) наибольшее клиническое
значение имеют амебиаз и лямблиоз. Известно, что клиническая картина
амебной дизентерии развивается приблизительно у 10% инфицированных
амебой больных. Амебный колит характеризуется сильнейшей болью в
животе, лихорадкой и кровавой диареей, которая чревата перфорацией
толстой кишки. Генерализация амебиаза сопровождается септикопиемией с
образованием абсцессов печени, легких или головного мозга и крайне
неблагоприятным прогнозом для жизни больного. Заболевание носит
эндемичный характер. Лямблиоз на территории России распространен очень
широко и в 25-50% случаев приводит к развитию острого или хронического
энтерита, сопровождающегося диареей. Наибольшую помощь в постановке
доклинического диагноза при ПД может оказать тщательный сбор анамнеза
настоящего заболевания и анамнеза жизни пациента, поскольку особую
группу риска образуют лица, практикующие анальные сексуальные контакты.
В современной классификации ОКИ выделяют так называемые особые формы заболевания:
- диарея путешественников;
- диарея у мужчин-гомосексуалов;
- диарея у ВИЧ-инфицированных;
- антибиотико-ассоциированная диарея;
- синдром избыточного роста бактерий в желудочно-кишечном тракте.
Из особых форм ОКИ для практики врача СМП имеет значение лишь один
из вариантов антибиотико-ассоциированной диареи — псевдомембранозный
колит. Это заболевание развивается во время или значительно после
приема антибактериальных препаратов и связано с колонизацией кишечника
условно-патогенным микроорганизмом сlostridium difficile. Протекает
псевдомембранозный колит с высокой лихорадкой, кровавой диареей, болью
в животе и сопровождается существенной интоксикацией со всеми
возможными осложнениями острой профузной диареи. При подозрении на
псевдомембранозный колит больной должен быть госпитализирован в
инфекционный стационар.
Доклиническая и дифференциальная диагностика ОД
Всестороннее изучение анамнеза настоящего заболевания является
первым шагом в обследовании пациентов, имеющих характерные признаки ОКИ
(табл. 1).
У больных необходимо выяснить:
- когда и как началось заболевание (например, внезапное или
постепенное развитие заболевания, наличие инкубационного или
продромального периода); - характер испражнений (водянистые, кровянистые, с примесью слизи или гноя, жирные и т. д.);
- частоту стула, количество и болезненность испражнений;
- наличие симптомов дизентерии (лихорадка, тенезмы, примесь крови и/или гноя в испражнениях).
В беседе с больным очень важно установить наличие и, что особенно
существенно, развитие субъективных и объективных проявлений
обезвоживания (жажды, тахикардии, ортостатических реакций, уменьшения
диуреза, вялости и нарушений сознания, судорог, снижения тургора кожи)
и интоксикации (головной боли, тошноты, рвоты, мышечных болей).
Кроме того, во всех случаях необходимо выявить возможные факторы
риска ОКИ: поездки в страны с неблагополучной по инфекционным диареям
эпидобстановкой; род занятий; недавнее употребление в пищу небезопасных
продуктов (например, недостаточно термически обработанного мяса, сырых
яиц или моллюсков, непастеризованного молока и соков); купание в
загрязненных водоемах или использование для питья воды из них
(например, воды из озера или реки); пребывание в сельской местности,
посещение «детских» зоопарков, контакт с дикими или домашними
животными; наличие в окружении больных, имеющих сходные симптомы;
регулярный или недавний прием лекарств (антибиотиков, антацидных
препаратов, противодиарейных средств); наличие медицинских факторов,
предрасполагающих к развитию инфекционной диареи (ВИЧ, прием
иммунодепрессантов, гастрэктомия в анамнезе, ранний детский или
старческий возраст); пристрастие к анальному сексу; принадлежность к
декретированным группам населения (работники питания, воспитатели
детских учреждений).
На догоспитальном этапе ОКИ необходимо дифференцировать с рядом
острых неинфекционных заболеваний хирургического, терапевтического,
гинекологического и иного профиля. Единственной целью дифференциального
диагноза в данном случае является выбор направления госпитализации
больного. Основные критерии для проведения дифференциального диагноза
отражены в предлагаемом нами алгоритме догоспитальной медицинской
помощи (рис. 2).
Распространенность ошибочной диагностики ОКИ иллюстрируют данные
DuPont H. L. (1997). Предоставленные автором данные анализа более 50
тысяч случаев госпитализации больных с ОКИ констатируют, что в 7,4%
случаев этот диагноз был установлен при таких заболеваниях, как острый
аппендицит, острый холецистопанкреатит, странгуляционная кишечная
непроходимость, тромбоз мезентериальных сосудов, инфаркт миокарда,
крупозная пневмония, декомпенсация сахарного диабета, гипертонический
криз. Напротив, указанные выше заболевания были ошибочно
диагностированы у больных с ОКИ в 11,1% случаев.
Догоспитальная терапия ОД
Наибольшую угрозу для пациентов с ОКИ представляет развитие
дегидратации и ассоциированной с ней артериальной гипотензии на фоне
интоксикации, провоцирующей падение артериального давления и нарушение
функции центральной нервной системы. Объем догоспитальной терапии при
ОКИ базируется на мониторинге жизненно важных функций организма
больного: состоянии сознания и функции внешнего дыхания, уровне АД и
гидратации пациента. При наличии соответствующего оснащения бригады СМП
терапия клинически значимой гиповолемической и инфекционно-токсической
артериальной гипотензии должна осуществляться под контролем
центрального венозного давления. В соответствии со стандартными
рекомендациями терапия на этом этапе направлена:
- на восстановление сердечного ритма;
- на оптимизацию объема циркулирующей крови;
- на устранение гипоксии и нормализацию кислотно-щелочного равновесия;
- на проведение инотропной/вазопрессорной терапии.
Для устранения гипоксии больному назначают оксигенотерапию газовой смесью с 35%-ным содержанием кислорода.
Регидратацию больного начинают с диагностики обезвоживания, тяжесть которой может варьировать от I до IV степени (табл. 2).
При дегидратации I и II степеней (85-95% больных ОКИ) восполнение
потери жидкости может и должно осуществляться оральным путем. ВОЗ
рекомендует применять для оральной регидратации растворы следующей
прописи: 3,5 г NaCl, 2,5 г NaHCO3
(или 2,9 г цитрата натрия), 1,5 г KCl и 20 г глюкозы или ее полимеров
(например, 40 г сахарозы, или 4 столовые ложки сахара, или 50-60 г
вареного риса, кукурузы, сорго, проса, пшеницы или картофеля) на 1 л
воды. Это позволяет получить раствор, содержащий приблизительно 90
ммоль Na, 20 ммоль K, 80 ммоль Cl, 30 ммоль HCO3 и 111 ммоль глюкозы.
Можно с успехом использовать любой из готовых растворов для оральной
регидратации (цитроглюкосалан, регидрон, гастролит). Количество выпитой
жидкости должно в 1,5 раза превышать ее потери с испражнениями и мочой.
Компенсация обезвоживания сопровождается очевидным уменьшением жажды,
нормализацией диуреза и улучшением общего состояния больного.
Дегидратация III и IV степеней, выраженная тошнота или рвота, а
также бессознательное состояние больного требуют неотложной инфузионной
терапии. Для внутривенной регидратации используют полиионные
кристаллоидные растворы: трисоль, квартасоль, хлосоль, ацесоль. Менее
эффективно введение моноионных растворов (физиологического раствора
хлорида натрия, 5%-ного раствора глюкозы), а также несбалансированных
полиионных растворов (раствора Рингера, мафусола, лактасола).
Коллоидные растворы (гемодез, реополиглюкин, рефортан) вводят только в
случаях упорной гипотонии, после восстановления объема циркулирующей
крови в целом. В тяжелых случаях инфузия водно-электролитных смесей
начинается с объемной скоростью 70-90 мл/мин, при средней тяжести
состояния больного — с объемной скоростью 60-80 мл/мин. В ряде случаев
необходимая скорость инфузии обеспечивается путем одновременного
вливания в 2-3 вены. После стабилизации артериального давления скорость
инфузии снижается до 10-20 мл/мин. Для предотвращения прогрессирования
обезвоживания, развития гемодинамической недостаточности, отека легких,
пневмонии, ДВС-синдрома и острой почечной недостаточности объем
жидкости, вводимой после стабилизации состояния больного, может
составлять 50-120 мл на 1 кг веса.
Назначение антибактериальной терапии среднетяжелых и тяжелых ОКИ на
доклиническом этапе не только не входит в задачи врача СМП, но и
категорически противопоказано, поскольку может существенно ухудшить
состояние больного и затруднить лабораторную верификацию возбудителя
заболевания. Возрастающая угроза инфекций, вызванных
антибиотико-резистентными штаммами микроорганизмов, наличие
нежелательных реакций при применении антимикробных препаратов,
суперинфекция, связанная с эрадикацией нормальной микрофлоры
антибактериальными средствами, и возможность индукции антибиотиками
некоторых факторов вирулентности у энтеропатогенов (например, индукция
фторхинолонами фага, ответственного за продукцию шигеллезного токсина),
заставляют тщательно взвешивать все за и против при решении вопроса об
антимикробной терапии и назначать ее только после точной диагностики
возбудителя ОКИ. В связи с вышеизложенным антибактериальные препараты
особенно не рекомендуются при гастроэнтеритическом варианте ОД любой
степени тяжести, при легком, стертом течении колитического варианта и в
период реконвалесценции при любой форме кишечного заболевания.
Эмпирическое назначение антибиотиков возможно в случае
легкопротекающей и среднетяжелой ОКИ любой этиологии, а также при
диарее путешественников, наиболее вероятным возбудителем которой
являются энтеротоксигенные штаммы E.coli или другие бактериальные
патогены. В этом случае взрослым назначают фторхинолоны, а детям —
ко-тримоксазол, применение которых позволяет сократить длительность
заболевания с 3-5 до 1-2 дней. Этой категории больных, как правило, не
нуждающихся в госпитализации, можно рекомендовать амбулаторный прием
антисептиков кишечного действия: эрцефурила, интетрикса или
энтероседива в стандартных дозах в течение 5-7 дней, а также препаратов
неантимикробного действия, облегчающих течение диареи (табл. 3).
Столь же опасным, как антибиотики, в отношении усугубления интоксикации
является применение при ОКИ любого клинического течения сильных
противодиарейных препаратов (имодиума) и противотошнотных средств
(церукала, торекана).
Особое значение при ОКИ имеет коррекция микробиоценоза кишечника
пробиотиками, проводимая на различных этапах лечения: в остром периоде
— в целях конкурентного вытеснения патогенной микрофлоры, у
реконвалесцентов — для обеспечения реабилитационных процессов. Весьма
эффективно раннее, не позже второго дня болезни, назначение
бифидумбактерина форте в ударных дозах (по 50 доз 3 раза каждые 2 часа
в первый день лечения) с последующим приемом поддерживающих доз (30 доз
в день, по показаниям — до 6 дней).
Пробиотик IV поколения бифидумбактерин форте обеспечивает высокую
локальную колонизацию слизистой оболочки кишечника, элиминацию
патогенной и условно-патогенной микрофлоры. Положительный клинический
эффект при сальмонеллезе средней тяжести отмечен через 1-2 дня, при
тяжелом течении сальмонеллеза и дизентерии — к окончанию курса. Из
пробиотиков, приготовленных на основе микроорганизмов рода Bacillus,
препаратом выбора является биоспорин, назначаемый по 2 дозы 2-3 раза в
день в течение 5-7 дней. Препарат обладает выраженным
антибактериальным, антитоксическим и иммуномодуляторным действием,
индуцирует синтез эндогенного интерферона, стимулирует активность
лейкоцитов крови, синтез иммуноглобулинов. При преобладании
энтеритического синдрома рекомендуется энтерол, получаемый из
сахаромицетов Буларди. Он назначается по 250 мг 2 раза в день в течение
5 дней. В периоде реконвалесценции наряду с традиционными
патогенетическими средствами (стимуляторами репарации, общего и
местного иммунного ответа) целесообразно применение препаратов
облигатной флоры, оптимально — бифидумбактерина форте, оказывающего
стабилизирующее влияние на микробиоценоз кишечника и гомеостатические
процессы.
Несмотря на расширение возможностей по верификации возбудителя и
большой выбор методов этиопатогенетической терапии, появившихся в
арсенале врача за последние 20 лет, ОКИ и сегодня по-прежнему сопряжены
с высокой летальностью. Так, по данным Н. Д. Ющука, при ПТИ и
сальмонеллезе летальность составляет около 0,1%, а при дизентерии —
1,4%, при этом причиной 20% летальных исходов при бактериальной
дизентерии и 44,4% летальных исходов при всех остальных ОКИ является
инфекционно-токсический шок. Причины столь высокой летальности,
вероятно, кроются в неадекватной оценке прогноза и тяжести состояния
больного ОКИ и неоказании ему, в том числе по причинам недостаточного
инструментального, медикаментозного и информационного обеспечения,
неотложной помощи именно на догоспитальном этапе. Хочется надеяться,
что предложенный нами простой алгоритм догоспитальной медицинской
помощи при ОД (рис. 2) окажется небесполезным для практикующих врачей и
их пациентов.
Литература
- DuPont H. L. // Am. J. Gastroenterol. 1997; 92: 1962-75.
- Kehl K. S., Havens P., Behnke C. E., Acheson D. W. // J. Clin. Microbiol. 1997; 35: 2051-4.
- Лобзин
Ю. В., Корвякова Е. Р., Литусов Н. В., Захаренко С. М. Современная
фармакотерапия острых кишечных инфекций. Центр ВТП БЗ МО РФ. - Mc Qbaid K. R. Diarrhea. Current medical diagnosis and treatment. 38th ed. Appleton & Lange, 1999, p. 546.
- Спрингис Д. и др. Неотложная терапия. Гэотар, Медицина, 2000. С. 30.
- Ющук Н. Д., Бродов Л. Е. Принципы диагностики и лечения острых кишечных инфекций // Лечащий Врач. 1999. № 7. С. 40.
Таблица 1. Типичные клинические проявления ОКИ
- Острая профузная диарея
- Обезвоживание
- Интоксикация
- Боль в животе
- Лихорадка
- Примесь крови в испражнениях
назад
- Авторы
- Файлы
Хунафина Д.Х.
Шамсиева А.М.
Бурганова А.Н.
Кутуев О.И.
Галиева А.Т.
Хабелова Т.А.
Сыртланова Г.Р.
Тема и ее актуальность
Острые кишечные инфекции (ОКИ) до настоящего времени занимают ведущее место в инфекционной патологии детей и взрослых, уступая по заболеваемости только гриппу и острым респираторным инфекциям. По данным ВОЗ ежегодно в мире регистрируются до 1-1,2 млрд. диарейных заболеваний, и около 5 млн. детей умирает от кишечной инфекции. Уровень заболеваемости в России остается постоянно высоким в течение последнего десятилетия. Это определяет первостепенное значение всесторонней оценки синдрома диареи в ранней диагностике и первичной дифференциальной диагностике острых кишечных инфекций на врачебном участке. В учебном пособии представлены следующие темы: пищевые токсикоинфекции (ПТИ), сальмонеллез — обширная группа кишечных инфекций, развивающихся после употребления в пищу продуктов, инфицированных патогенными или условно патогенными микроорганизмами, характеризуются внезапным началом, синдромом интоксикации, гастроэнтерита, развитием обезвоживания различной степени. На их долю приходится 1/3 всех острых кишечных заболеваний. ПТИ вследствие их бурного и скоротечного течения являются заболеваниями, с которыми чаще встречаются врачи общей практики, службы скорой помощи. От умелой и правильной тактики ведения больных зависит исход и прогноз после кишечных инфекций.
Шигеллез — относится к числу распространенных антропонозных кишечных инфекций. Вызывается бактериями рода шигелла, протекающая с преимущественным поражением дистального отдела толстого кишечника. Заболеваемость регистрируется в виде групповых и спорадических вспышек. Клинической особенностью течения шигеллеза на современном этапе является значительная частота стертых вариантов, трудных в диагностике. Функциональные и морфологические изменения в кишечнике, обусловленные инфекционным процессом, сдвиги в составе кишечной микрофлоры приводят к формированию стойкого дисбактериоза, обострения хронических болезней органов пищеварения.
Холера — острое инфекционное заболевание из группы карантинных инфекций. Характеризуется способностью к пандемическому распространению. При несвоевременной диагностике и запаздывании патогенетической терапии заболевание протекает в тяжелой форме с развитием гиповолемического шока (летальность — от 20 до 70%). Прогноз заболевания во многом зависит от своевременной диагностики и проведения адекватных неотложных мероприятий врачами первичной медицинской сети.
Ведущий путь передачи ОКИ: пищевой, водный и контактно-бытовой. Для большинства ОКИ бактериальной этиологии характерен летне-осенний подъем заболеваемости. Входными воротами и органом «мишенью» является желудочно-кишечный тракт. Клинически ОКИ характеризуются симптомами интоксикации, развитием диарейного синдрома, нередким развитием гиповолемического и инфекционно-токсического шока. Особенности клинических проявлений каждой нозологической формы ОКИ определяются наличием у возбудителя факторов патогенности: способность к инвазии, продукции экзотоксинов, их тропизм к эпителию желудочно-кишечного тракта.
Цель учебного пособия: научить студентов проводить на догоспитальном и госпитальном этапах диагностику кишечных инфекций на основании анамнестических, эпидемиологических и клинических данных. Уметь правильно интерпретировать данные вспомогательных и лабораторных методов обследования для назначения адекватной терапии в зависимости от этиологии, локализации, степени тяжести ведущего клинического синдрома. Оказывать экстренную медицинскую помощь при осложнениях, приобрести навыки ведения больного в стационаре, познакомить с принципами реабилитации реконвалесцентов, правильно организовать противоэпидемические мероприятия в очаге.
В учебном пособии представлены:
- Таксономия, строение и основные свойства возбудителей кишечных инфекций; эпидемиология кишечных инфекций; анатомо-физиологические особенности ЖКТ, почек; патофизиология основных клинических синдромов: интоксикации, гастроэнтерита, энтероколита, механизм развития гиповолемического, инфекционно-токсического шока.
- Клинические ситуационные задачи с эталонами ответов.
- Схемы ориентировочной основы действий врача при обследовании на ОКИ.
- Таблицы дифференциально-диагно-стических признаков холеры, дизентерии, ПТИ, ротавирусного гастроэнтерита.
- Таблица дифференциально-диагности-ческих признаков холеры и отравлений химическими веществами.
- Таблица степеней обезвоживания при ОКИ.
- Приложения: приказ МЗ СССР № 475; забор материала при кишечных инфекциях, макроскопическое исследование кала.
- Список основной и дополнительной литературы.
Область применения: учебное пособие предназначено для студентов, обучающихся по специальности: лечебное дело, медико-профилактическое дело.
Учебное пособие подготовлено в соответствие с типовой программой по дисциплине «инфекционные болезни». Издание является инструкцией к усвоению и закреплению знаний студентов по теме «Острые кишечные инфекции» во внеаудиторное время и содержит основные данные по этиологии, патогенезу, клинике, диагностике, дифференциальной диагностике и лечению кишечных инфекций, и является дополнением к основной литературе.
Библиографическая ссылка
Хунафина Д.Х., Шамсиева А.М., Бурганова А.Н., Кутуев О.И., Галиева А.Т., Хабелова Т.А., Сыртланова Г.Р. ОСТРЫЕ КИШЕЧНЫЕ ИНФЕКЦИИ (учебное пособие) // Успехи современного естествознания. – 2010. – № 9.
– С. 35-36;
URL: https://natural-sciences.ru/ru/article/view?id=8710 (дата обращения: 21.05.2023).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
В обзоре представлены современные методы диагностики и лечения острых кишечных инфекций. Подробно изложены методики клинической диагностики, клинико-лабораторного обследования, рекомендации по этиотропной, патогенетической и симптоматической терапии. Проведен обзор основных групп препаратов, рекомендованных на каждом из этапов лечения.
Эпидемиологическая ситуация в мире по заболеваемости острыми кишечными инфекциями (ОКИ) остается на стабильно неблагоприятном уровне. С января по июнь 2015 г. в Российской Федерации был зарегистрирован 16 491 случай сальмонеллезной инфекции, более половины приходилось на детей в возрасте до 14 лет (8161 пациент). Показатель заболеваемости на 100 тыс. населения другими ОКИ, вызванными установленными бактериальными, вирусными возбудителями, а также пищевые токсикоинфекции установленной этиологии, составил в указанный период 98,3, а для детского населения – 511,8. Для ОКИ неустановленной этиологии этот показатель за первые 6 месяцев 2015 г. равнялся 170,0, а для детей – 556,6 на 100 тыс. населения. Высокие показатели заболеваемости (от 13,06 до 44,98 на 100 тыс. населения) зарегистрированы в Ненецком, Ханты-Мансийском, Ямало-Ненецком автономных округах, в Томской, Тамбовской, Липецкой, Иркутской, Новосибирской, Амурской, Оренбургской, Кемеровской, Калининградской областях, республиках Коми, Мордовия, Саха [1].
Этиологическая структура ОКИ в настоящее время характеризуется преобладанием вирусных агентов над бактериальными. При этом доминирующими возбудителями являются рота- и норовирусные инфекции. Следует отметить, что норовирусная инфекция играет большую роль во вспышках ОКИ, а также в случае развития инфекций, связанных с оказанием медицинской помощи. Среди бактериальных инфекций лидирующие позиции в этиологической структуре занимают сальмонеллез и кампилобактериоз [2].
К сожалению, в рутинной клинической практике этиология ОКИ в большинстве случаев остается неустановленной. В таких случаях диагноз выставляется посиндромно: гастрит, гастроэнтерит, энтерит, энтероколит, колит, гемоколит или тотальное поражение всего желудочно-кишечного тракта (ЖКТ) – гастроэнтероколит (табл. 1) [3].
Установление этиопатогенетической группы диареи является важным компонентом тактики терапии: водянистая диарея в большинстве случаев вызвана вирусами и требует назначения в качестве этиотропной терапии противовирусных препаратов, инвазивная – относится к бактериальным ОКИ, что диктует необходимость рассмотрения антибактериальной терапии.
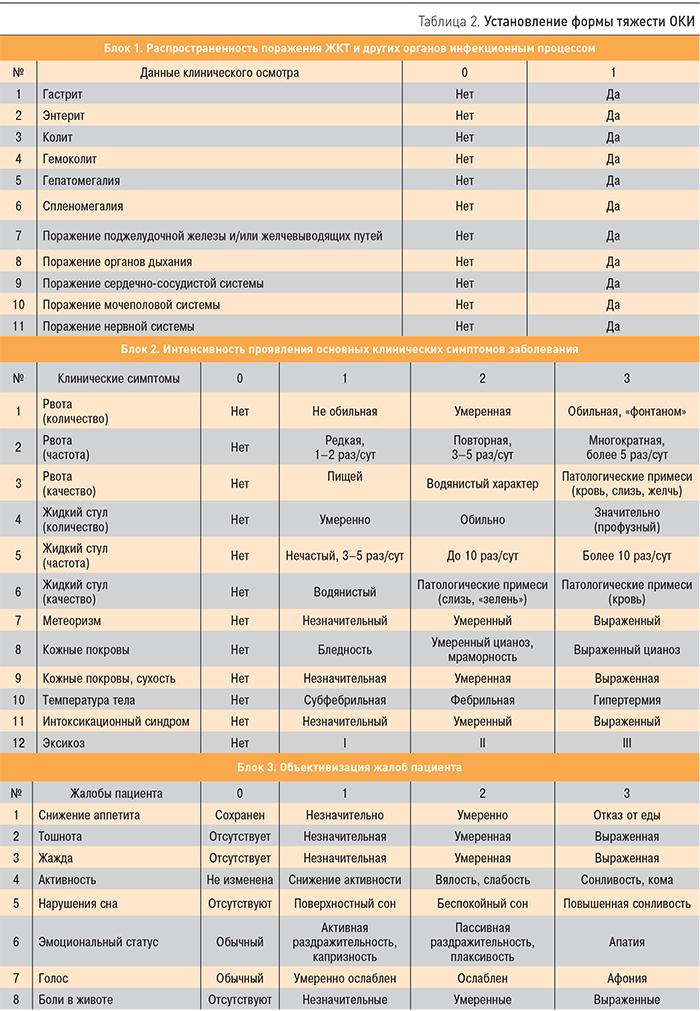
По форме тяжести ОКИ подразделяются на легкую, среднюю и тяжелую. Установление формы тяжести заболевания осуществляется путем интегрального анализа клинических данных по трем блокам:
- распространенность поражения ЖКТ и других органов инфекционным процессом;
- интенсивность проявления основных клинических симптомов заболевания;
- объективизация жалоб пациента [4].
Симптомы из представленного в блоках перечня (табл. 2) оцениваются по их наличию (есть или нет – блок 1), а также по интенсивности проявлений в соответствии с предлагаемой шкалой (блоки 2 и 3). У пациента могут отмечаться не все клинические проявления данного заболевания, представленные в блоках. В таком случае оценка проводится по имеющимся симптомам, отсутствующие проявления заболевания не учитываются. Данный метод интегральной оценки клинических данных применим как в терапевтической, так и в педиатрической практике.
Установление формы тяжести можно проводить визуально: чем больше пунктов отмечено в блоке 1 и чем больше суммарное количество баллов в блоках 2 и 3, тем более тяжелая форма заболевания отмечается у больного. Однако более предпочтительным является расчет интегрального индекса клинических симптомов, который осуществляется по формуле:
ИИКС = ((А×100/11) + (В×100/36) + (С×100/24))/3,
где показатель А – сумма положительных значений для каждого пункта блока 1, В и С– сумма положительных значений для каждого пункта блоков 2 и 3 соответственно.
Значения данного показателя в пределах от 1 до 35% относятся к легкой форме, от 36 до 70% – к среднетяжелой, а 71% и более – к тяжелой форме заболевания.
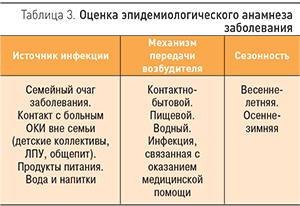
Одним из важных компонентов ведения больных ОКИ является оценка эпидемиологического анамнеза заболевания, которую наиболее удобно проводить по следующей схеме (табл. 3).
Эпидемиологический анамнез необходим врачу, чтобы сориентироваться в этиологии заболевания. Так, пищевой и водный пути передачи более характерны для бактериальных ОКИ, контактно-бытовой – для вирусных агентов. В осенне-зимний период отмечается подъем заболеваемости вирусными ОКИ, в летний – бактериальными.
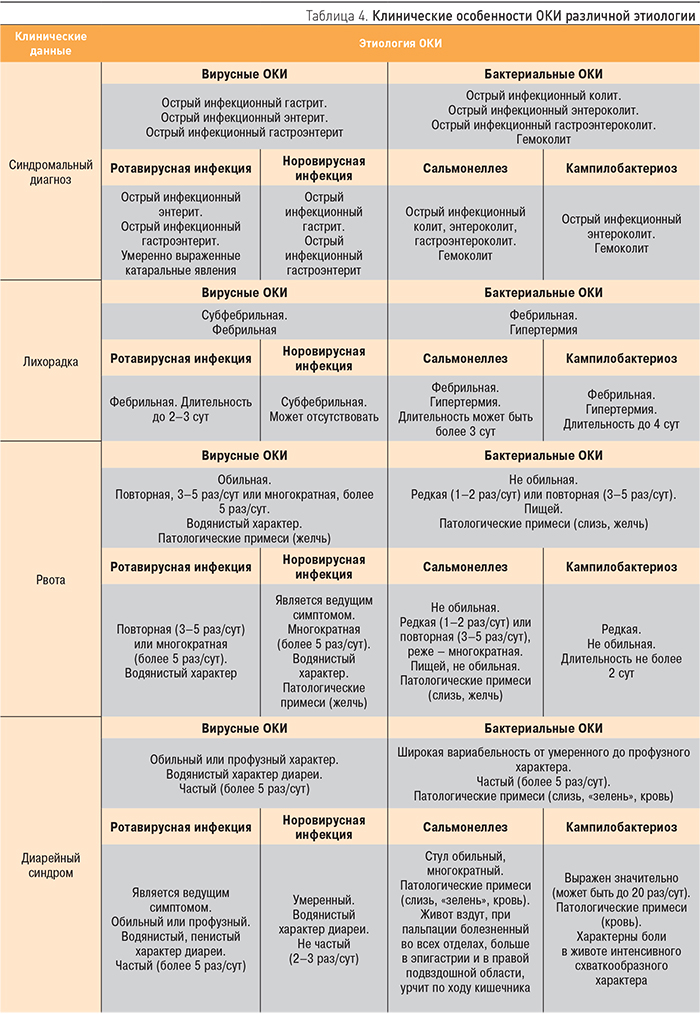
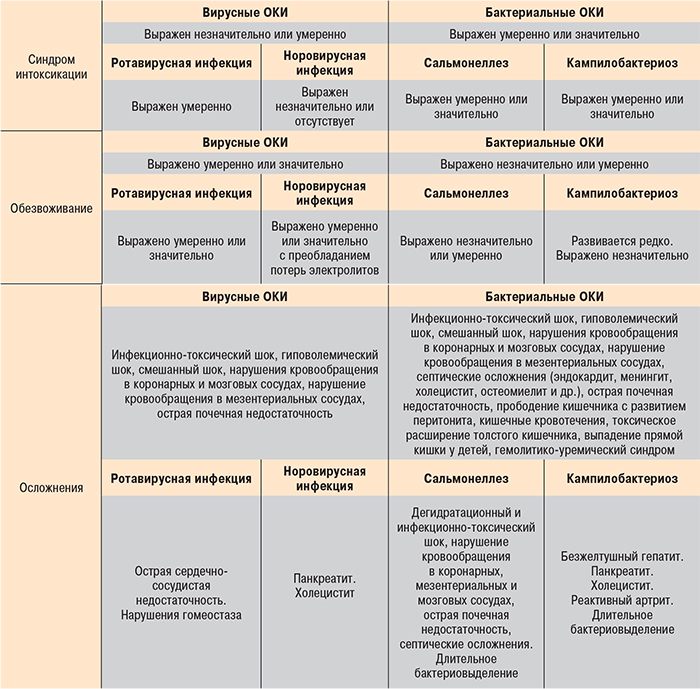
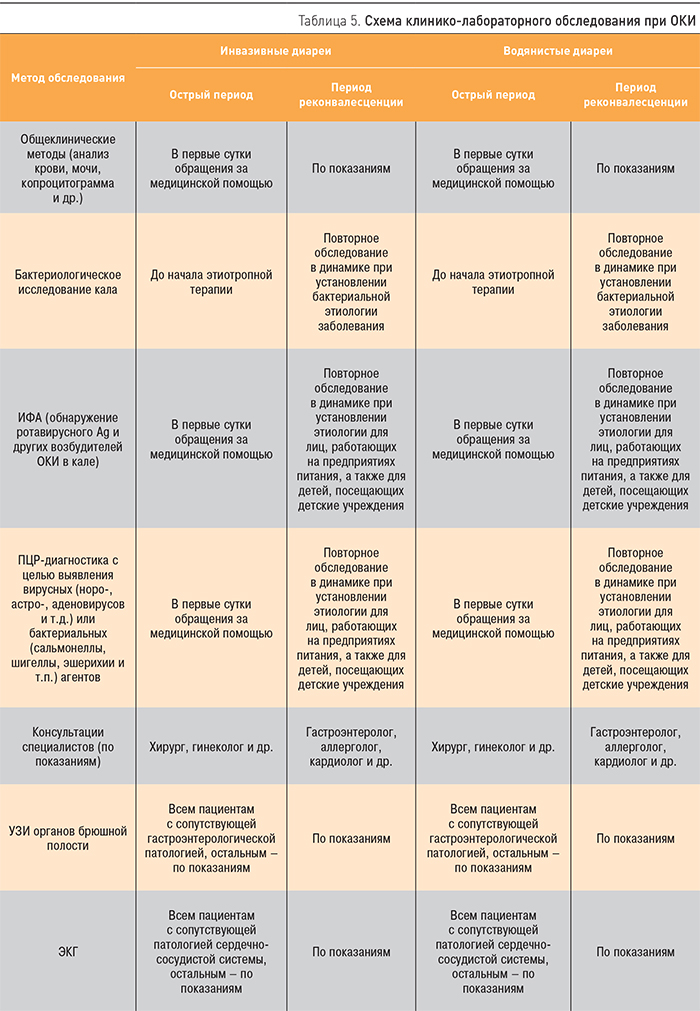
Дифференциальная диагностика ОКИ основывается на клинических особенностях ведущих синдромов – поражении ЖКТ, синдроме интоксикации и развитии дегидратации (табл. 4) и клинико-лабораторном подтверждении этиологии заболевания (табл. 5). Клинико-лабораторное обследование пациентов с ОКИ должно осуществляться поэтапно:
- 1-й этап – предварительная клиническая диагностика;
- 2-й этап – окончательная диагностика, основанная на результатах данных лабораторных и инструментальных методов диагностики, оценке дальнейшей динамики клинических проявлений болезни;
- 3-й этап – диагностика в периоде реконвалесценции (оценка санации от возбудителя, состояния органов гепатобилиарной системы, микрофлоры ЖКТ и т.п.).
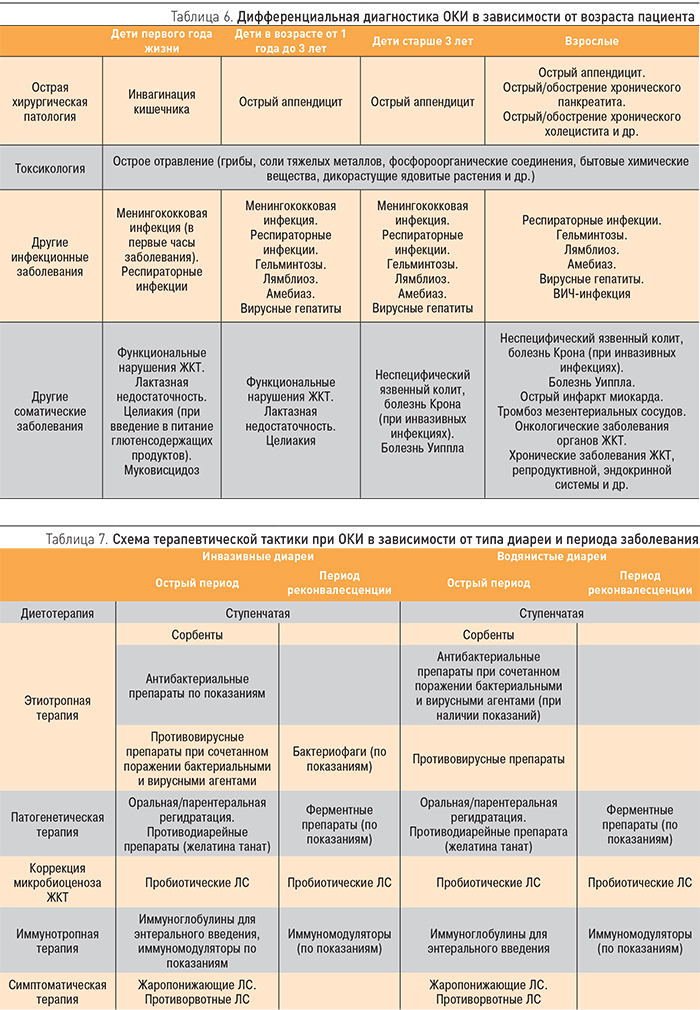
Дифференциальная диагностика ОКИ с другими заболеваниями зависит от возраста пациента (табл. 6).
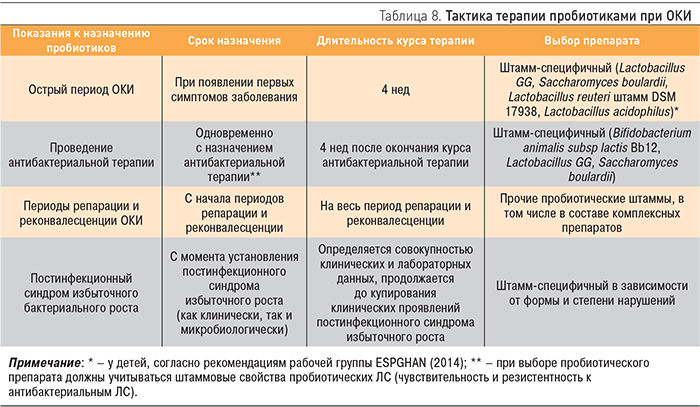
Терапевтическая тактика при ОКИ у конкретного пациента базируется на знании или предположении (на основании клинических особенностей, данных эпидемиологического анамнеза) об этиологии заболевания: бактериальная или вирусная инфекция. Кроме того, необходимо учитывать возраст пациента, особенности его преморбидного фона и период заболевания. Схема терапевтической тактики при ОКИ в зависимости от типа диареи и периода заболевания приведена в табл. 7.
Этиотропная терапия является ключевым звеном и имеет три основных направления:
- устранение возбудителя инфекции (антибактериальные, противовирусные, противопаразитарные препараты, бактериофаги);
- связывание возбудителя (специфические антитела и сыворотки, сорбенты);
- выведение (сорбенты) [3, 5].
Противовирусные препараты рекомендованы при вирусных ОКИ. Показаниями к их назначению являются:
- установленная вирусная этиология ОКИ; в связи с этим представляется целесообразным более широкое использование в рутинной клинической практике экспресс-тестов для быстрой диагностики вирусной этиологии ОКИ;
- предполагаемая вирусная этиология ОКИ (заболевание в форме острого инфекционного гастрита, энтерита, гастроэнтерита; зимний период; «вспышечная» заболеваемость);
- раннее обращение за медицинской помощью;
- профилактика инфекций, связанных с оказанием медицинской помощи, вирусной этиологии (ротавирусная, норовирусная инфекции).
Среди противовирусных препаратов эффективность в клинических исследованиях показали препараты, содержащие аффинно очищенные антитела к гамма-интерферону человека, интерферон альфа-2b в сочетании с таурином, метилфенилтиометил-диметиламинометил-гидроксиброминдол карбоновой кислоты этиловый эфир (умифеновир) [6–9].
Вопросы антибактериальной терапии ОКИ для практикующего врача остаются одними из самых насущных. К сожалению, большая часть докторов подходит к вопросу назначения антибиотиков шаблонно, без учета этиологии заболевания, рекомендуют их даже при вирусных ОКИ и без знания данных о чувствительности и резистентности основных бактериальных возбудителей. Абсолютными показаниями к назначению антибактериальных лекарственных средств (ЛС), на основании рекомендаций Всемирной организации здравоохранения, считаются установленные диагнозы дизентерии, брюшного тифа, амебиаза, холеры [2, 3]. В нашей стране предусмотрены более детальные показания для назначения антибиотиков: наличие клинических признаков инвазивной диареи, гемоколита (исключение составляет ОКИ, вызванные энтерогеморрагическими E. Coli, при которых назначение антибактериальной терапии может повысить риск развития геолитико-уремического синдрома), возраст больше 65 лет, наличие в анамнезе поражения ЖКТ воспалительного характера, иммуносупрессивные состояния (ВИЧ-инфекция, онкологические заболевания, сахарный диабет), хронические заболевания/пациенты из группы риска (гемоглобинопатии, потребность в гемодиализе и т.п.) [2].
В настоящее время существует достаточно большой выбор антибактериальных средств. При их назначении необходимо учитывать следующие факторы:
- антимикробный спектр действия ЛС;
- механизм антимикробного действия (бактерицидное, бактериостатическое);
- наличие лекарственной устойчивости возбудителей ОКИ, циркулирующих в данное время в данной местности, на данной территории или в данном стационаре – в связи с этим необходимо подчеркнуть важность регулярных бактериологических исследований с определением чувствительности в каждом регионе, лечебно-профилактическом учреждении;
- фармакодинамика и фармакокинетика препарата (всасывание, распределение, выведение, способность к внутриклеточному проникновению и накоплению в тканях организма, пути его выведения из организма) и их соответствие патогенезу данной инфекции;
- возможные побочные реакции и доказанная в клинических исследованиях безопасность при использования;
- применительно к педиатрической практике – наличие лекарственных форм, предназначенных для детей (сироп и т.п.) [10].
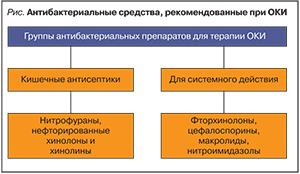
Антибактериальные средства, рекомендованные при ОКИ, подразделяются на два типа: кишечные антисептики и препараты, предназначенные для системного действия (рисунок). Первая группа может быть рекомендована для назначения в амбулаторно-поликлинической практике, где наиболее оправданной тактикой стартовой терапии ОКИ является использование нитрофуранов (нифуроксазид, нифурантел). Хинолоны (налидиксовая кислота, ципрофлоксацин) хорошо себя зарекомендовали в терапии сальмонеллезов. Цефалоспорины рекомендованы для системной антибактериальной терапии при среднетяжелых и тяжелых ОКИ в условиях стационара. Возможно назначение тетрациклинов, метронидазола, аминогликозидов, хлорамфеникола. Препаратами выбора для стартовой этиотропной терапии кампилобактериоза являются макролиды (эритромицин, макропен, азитромицин, кларитромицин).
Курс антибактериальной терапии в острой фазе локализованных ОКИ должен составлять не менее 5–7 сут. Показания к смене препарата общепринятые – клиническая неэффективность ЛС в течение 3 сут [3, 10].
Следует отметить, что в последние годы большинство возбудителей резистентны к фуразолидону. Сальмонеллы сохраняют высокую чувствительность к фторхинолонам (например, ципрофлоксацин – 96,7% штаммов чувствительны, однако к пефлоксацину 23,3% умеренно устойчивы и 17,2% устойчивы), налидиксовой кислоте (53,1%), к амикацину (61,1%), к нетилмицину (63,9%), к некоторым цефалоспоринам II (цефокситин, цефуроксим – 86,7–57,9%), III (цефтриаксон, цефотаксим, цефтазидим – 84,4, 85,0 и 81,7 соответственно) и IV поколения (цефепим – 91,3% чувствительных штаммов).
Всем пациентам вне зависимости от этиологии и формы тяжести заболевания в качестве одного из важных аспектов этиотропной терапии должны быть назначены сорбенты (угольные, синтетические, минеральные, волокнистые). В настоящее время на российском фармацевтическом рынке присутствует достаточно большое количество препаратов, обладающих сорбционными свойствами в различной степени [11]. Назначение энтеросорбентов показано в как можно более ранние сроки болезни – до идентификации возбудителя, позволяет добиваться «обрывающего» действия на течение ОКИ. Применение энтеросорбентов в поздние сроки заболевания (после 5–7-го дня), особенно при инвазивных ОКИ, меньше влияет на диарейный синдром, но оказывает выраженное дезинтоксикационное и энтеропротективное действие. К важным положительным моментам использования энтеросорбентов следует относить и отсутствие влияния этих препаратов на состав облигатной микрофлоры кишечника. Курс лечения энтеросорбентами обычно составляет 5–7 сут. Критерий ранней отмены препаратов – стойкая нормализация стула или его задержка в течение 2 сут [3].
Среди патогенетических методов терапии наиболее важными остаются средства регидратации (оральной, парентеральной), препараты, влияющие на процессы дегидратации (желатина танат), и пробиотики.
Для диагностики обезвоживания «золотым стандартом» является оценка динамики массы тела пациента. Так, эксикозу I степени соответствует потеря до 5% массы тела, что составляет до 50 мл/ кг жидкости, эксикозу II степени – потеря 6–10% массы тела (60–100 мл/кг), эксикозу III степени – потеря более 10% массы тела (110–150 мл/кг). Обезвоживание, характеризующееся потерей более 20% массы тела, несовместимо с жизнью [3].
Оральная регидратация показана всем пациентам с ОКИ. Для этих целей используют специальные, сбалансированные по электролитному составу и осмолярности растворы для оральной регидратации, содержащие 75 мэкв/л натрия и 75 мэкв/л глюкозы, с осмолярностью 245 мосм/л. Оральная регидратация проводится в два этапа:
- 1-й этап – первичная регидратация (первые 6 ч от момента обращения к врачу) – назначается суммарное количество жидкости 50–80 мл/кг за 6 ч.
- 2-й этап – поддерживающая регидратация (восполнение текущих потерь жидкости при ОКИ) – количество жидкости 80–100 мл/кг/сут.
Следует подчеркнуть, что в регидратационную терапию должны быть включены и бессолевые растворы, среди которых предпочтение следует отдать питьевой воде (не минеральной!), возможно использование пектинсодержащих отваров (яблочный компот без сахара, морковно-рисовый отвар). При этом соотношение глюкозо-солевых растворов и кипяченой воды должно быть 1:1 при водянистой диарее, 2:1 – при выраженной рвоте, 1:2 – при инвазивных диареях [2, 3].
Использование противодиарейных средств (лоперамид) при ОКИ патогенетически не оправдано, т.к. механизм действия данных препаратов подразумевает снижение моторики ЖКТ (усиление моторики является защитной реакцией организма при остром инфекционном поражении кишечника) и может способствовать усугублению интоксикационного синдрома при ОКИ.
ОКИ любых форм тяжести являются причиной значительных измененией микробиоценоза ЖКТ. Назначение пробиотиков в качестве препаратов «стартовой» терапии, особенно при вирусных диареях, позволяет сокращать сроки купирования основных симптомов заболевания, способствует восстановлению параметров микрофлоры ЖКТ. Данные препараты показаны также всем пациентам в периоде реконвалесценции с целью улучшения параметров микробиоценоза.
Современный подход к терапии пробиотиками подразумевает назначение препарата с учетом свойств штаммов, входящих в его состав. Генетическое разнообразие пробиотических штаммов определяет и их фенотипические различия, в первую очередь по клиническим эффектам, при этом не все пробиотические штаммы убедительно показали свою эффективность в клинической практике при определенных заболеваниях, что диктует необходимость анализа данных о штамм-специфичных свойствах пробиотиков в различных клинических ситуациях [13]. Тактика терапии пробиотиками при ОКИ представлена в табл. 8.
Среди штаммовых свойств пробиотиков, используемых в терапии ОКИ, наиболее существенным является способность к адгезии, играющей ключевую роль в обеспечении колонизационной резистентности и иммуннотропного влияния, что важно не только в остром периоде заболевания, но и в периоде репарации, реконвалесценции, а также в случае развития синдрома избыточного бактериального роста.
Среди пробиотических штаммов, характеризующихся высоким уровнем адгезии, можно выделить Bifidobacterium lactis Bb12. В исследованиях для данного микроорганизма in vitro была показана способность к высокоуровневой адгезии к поверхностям с муцином (использовались поликарбонатные луночные планшеты), без муцина и пленкам клеточных культур (Caco-2, HT29-MTX) [14], в том числе на фоне ротавирусной инфекции и после нее [15].
К числу важных для клинического применения свойств данного штамма следует отнести его устойчивость к действию агрессивных сред организма человека – соляной кислоты и желчи. Для Bifidobacterium lactis Bb12 было показано, что данный микроорганизм при низких рН синтезирует рН-зависимую АТФазу, регулирующую кислотно-основной баланс внутри бактерии. Данный фермент позволяет сохранить жизнедеятельность микроорганизму в условиях кислой среды желудка [16]. А наличие у Bifidobacterium lactis Bb12 гидролазы солей желчных кислот позволяет бактерии сохранять активность в присутствии желчи [17].
Штамм Bifidobacterium lactis Bb12 характеризуется выраженной антагонистической активностью в отношении целого ряда кишечных патогенов (Bacillus cereus, Clostridium difficile, Clostridium perfringens тип A, Escherichia coli, Listeria monocytogenes, Pseudomonas aeruginosa, Salmonella enterica subsp enterica serovar Typhimurium, S. enterica subsp. enterica serovar Typhi, Shigella flexneri, Shigella sonnei, Campylobacter jejuni и Candida albicans [18, 19]), что делает использование его предпочтительным при ОКИ бактериальной этиологии.
Особого внимания заслуживают пациенты, которые нуждаются в терапии антибактериальными ЛС. Вызванные течением инфекционного процесса изменения микрофлоры ЖКТ могут усугубляться действием антибиотиков. Поэтому данная категория пациентов нуждается во включении в состав комплексной терапии ОКИ пробиотических ЛС, направленных на поддержание микробиоценоза. В этом случае штамм-специфичные свойства устойчивости к антибактериальными средствам делает некоторые пробиотические штаммы препаратами выбора. Так, проведенное исследование показало, что Bifidobacterium lactis Bb12 обладает резистентностью к таким антибиотикам, как гентамицин, стрептомицин, полимиксин В, налидиксовая кислота, канамицин, неомицин, циклосерин, тетрациклин, спектиномицин. Это исследование делает препараты, в состав которых входит Bifidobacterium lactis Bb12, препаратами выбора при назначении пациентам данных антибактериальных средств, например, при ОКИ (сальмонеллез, шигеллез) [20].
Проведенные плацебо-контролируемые исследования показали, что, помимо терапевтических, штамму Bifidobacterium lactis Bb12 присущи и профилактические свойства. В частности, его применение снижает риск развития инфекций ЖКТ, в том числе ротавирусной, связанных с оказанием медицинской помощи [21, 22].
Следует отметить, что высокий профиль безопасности данного штамм был утвержден регуляторными органами в Европе (в 2008 г. European Food Safety Authority (EFSA) присвоил ему статус Qualified Presumption of Safety (безусловной безопасности)) и в США (Управлением по контролю за пищевыми продуктами и лекарственными средствами (FDA) он признан безопасным (Generally Regarded As Safe (GRAS)).
Еще одним штаммом, заслуживающим внимания, является Lactobacillus acidophilus (LA-5). Он относится к молочнокислым бактериям, основной отличительной особенностью которых является выраженная антибактериальная активность. Это реализуется путем снижения pH в кишечнике за счет синтеза молочной кислоты, выработки метаболитов, которые обладают токсическим действием в отношении патогенных бактерий, образования Н2О2, бактериоцинов, конкуренции с патогенными бактериями за питательные вещества, взаимодействия с рецепторами адгезии, предотвращая таким образом колонизацию патогенными и условно-патогенными микроорганизмами. Важным свойством Lactobacillus acidophilus, показанным в клинических исследования, является профилактика антибиотик-ассоциированной диареи (ААД) у взрослых [23].
Среди пробиотических средств терапии, содержащих Bifidobacterium lactis Bb12, можно рекомендовать препарат Линекс® Форте, содержащий молочнокислые бактерии (Lactobacillus acidophilus (LA-5) и Bifidobacterium animalis subsp. lactis (Bb12)). Каждая капсула препарата содержит 2×109 колониеобразующих единиц живых лиофилизированных молочнокислых бактерий. Данный препарат может быть назначен в остром периоде ОКИ, в периоде репарации и реконвалесценции, а также в случае развития синдрома избыточного бактериального роста после перенесенной ОКИ и в качестве профилактики развития ААД при приеме антибиотиков. Схема лечения в остром периоде ОКИ: для детей с рождения и до 2 лет – по 1 капсуле 1 раз/сут, для детей в возрасте 2–12 лет – по 1 капсуле 1–2 раза/сут, дети старше 12 лет и взрослые – по 1 капсуле 3 раза/ сут. Далее возможно снижение дозы до 1–2 капсул/сут в зависимости от клинической ситуации. В период реконвалесценции или для профилактики ААД рекомендуется назначать по 1 капсуле 1 раз/сут пациентам всех возрастных групп. Для обеспечения максимальной эффективности препарат рекомендуется принимать после еды, а для профилактики ААД – через 3 ч после приема антибиотиков.
Симптоматическая терапия включает терапию лихорадочных состояний. Жаропонижающие средства показаны не всем пациентам, т.к. повышение температуры является адаптационной реакцией организма на инфекцию, создающей оптимальные условия для иммунной перестройки организма. Назначение данной категории ЛС показано всем больным при гипертермии, а при наличии тяжелой сопутствующей патологии – при лихорадке более 38,50С.
Развитие вторичной панкреатической недостаточности, обострения хронической патологии поджелудочной железы нередко наблюдаются в периоде репарации и реконвалесценции ОКИ. Следует обратить внимание, что при норовирусной инфекции поражение поджелудочной железы отмечается чаще, чем при ОКИ другой этиологии. В таких случаях показано назначение ферментных препаратов, предпочтительно в минимикросферической форме. Следует учесть, что в остром периоде ОКИ ферментные препараты не показаны. Наиболее оптимальным сроком их назначения при наличии показаний являются 5–6-е сутки, критерий назначения – появление у пациента аппетита.
Для купирования упорной рвоты можно использовать прокинетики и противорвотные препараты: метоклопрамид, домперидон, прометазин, 0,25% новокаин – 1 ложку (чайную, десертную, столовую по возрасту) [3].
Критерии оценки эффективности лечения:
- клинические (купирование интоксикационного синдрома, нормализация температуры, купирование рвоты, диареи и других симптомов);
- клинико-лабораторные (стойкая нормализация гемограммы, копроцитограммы, отрицательные результаты при бактериологическом и ПЦР-обследовании).
В связи с тем, что санация от возбудителя, полная репарация кишечника и восстановление его нарушенных функций наступают значительно позже, чем исчезают клинические проявления болезни, целесообразно проводить динамическое наблюдение за пациентами, перенесшими ОКИ.
Таким образом, ОКИ требуют от врача особых подходов к диагностике, тактике ведения и терапии.
Плоскирева Антонина Александровна, к.м.н., доцент, старший научный сотрудник клинического отдела инфекционной патологии ФБУН «Центральный научно-исследовательский институт эпидемиологии Роспотребнадзора». Адрес: 111123, г. Москва, ул. Новогиреевская, д. 3а. Телефон: (495) 672-11-58. E-mail: antonina@ploskireva.com