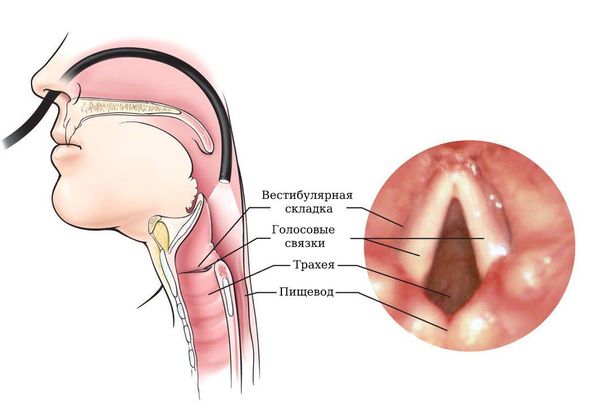
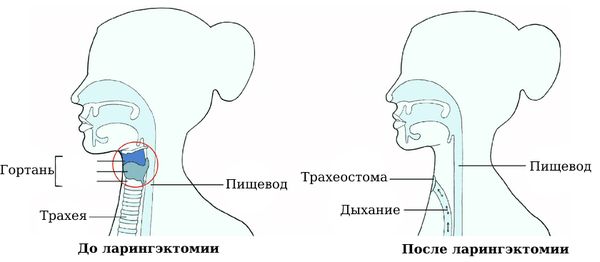
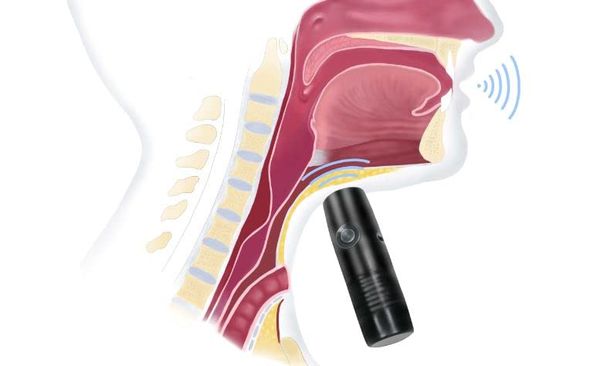
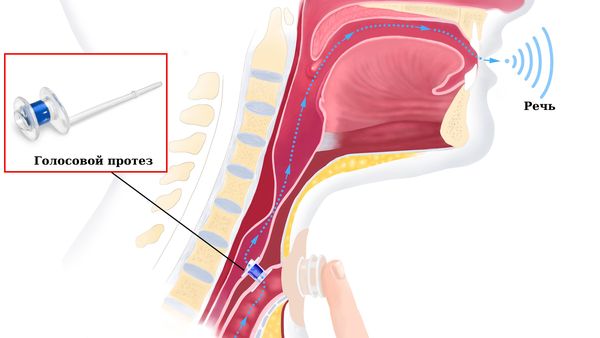
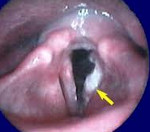
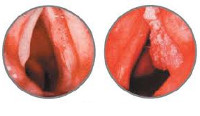
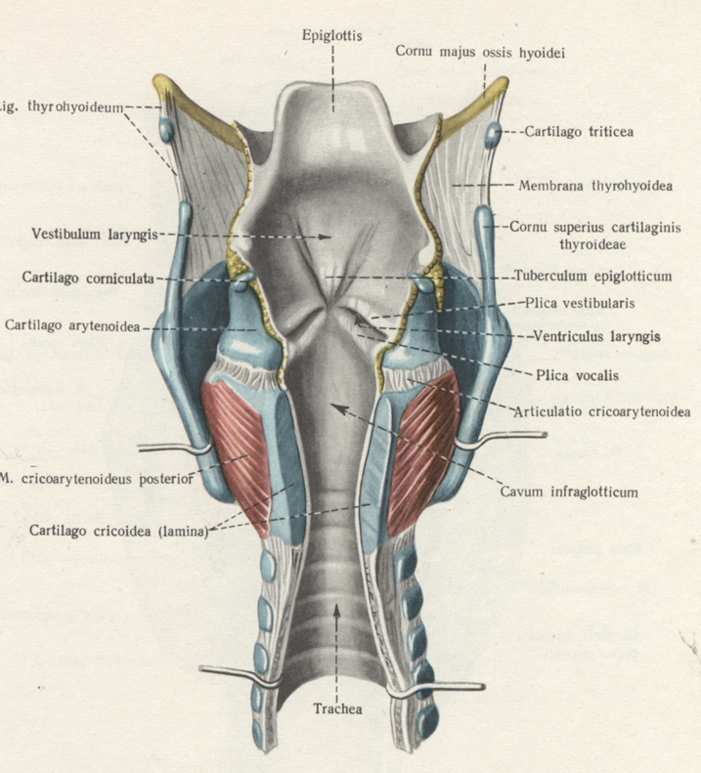
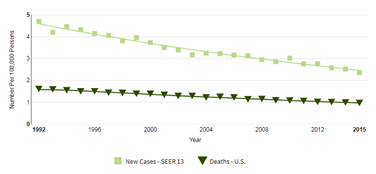
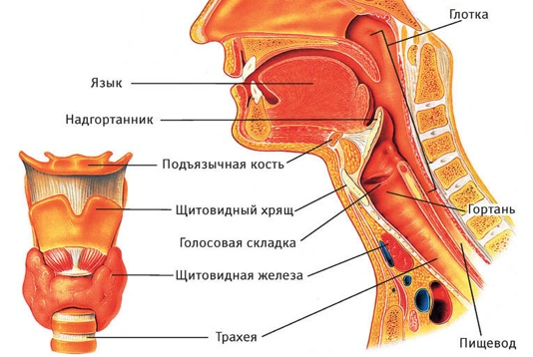
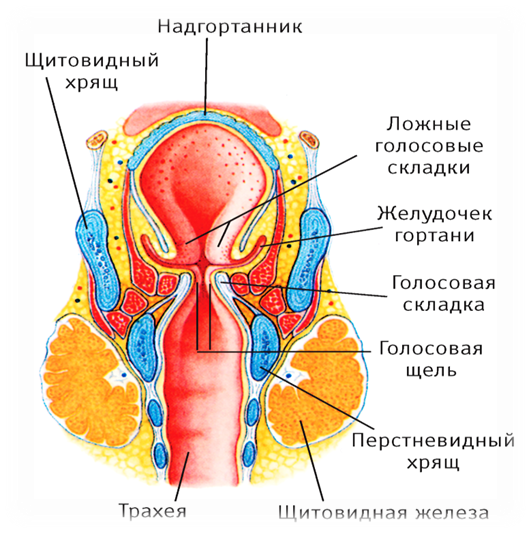
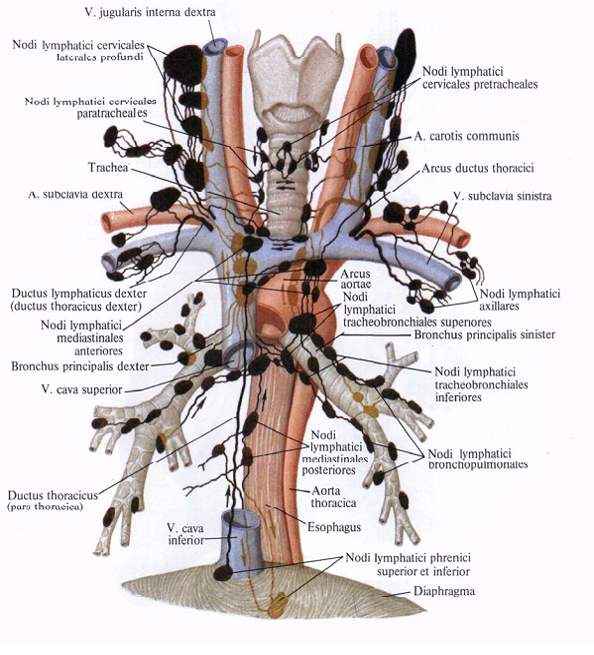
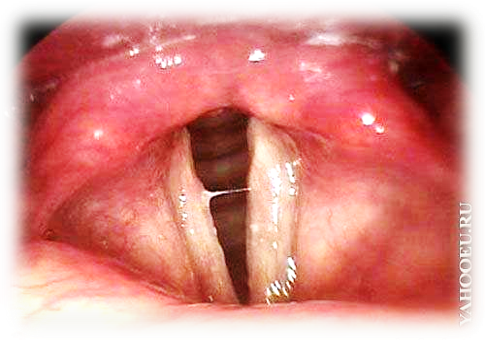
Злокачественные новообразования гортани
Версия: Клинические протоколы МЗ РК — 2018 (Казахстан)
Категории МКБ:
Злокачественное новообразование гортани (C32)
Разделы медицины:
Онкология
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «07» марта 2019 года
Протокол №57
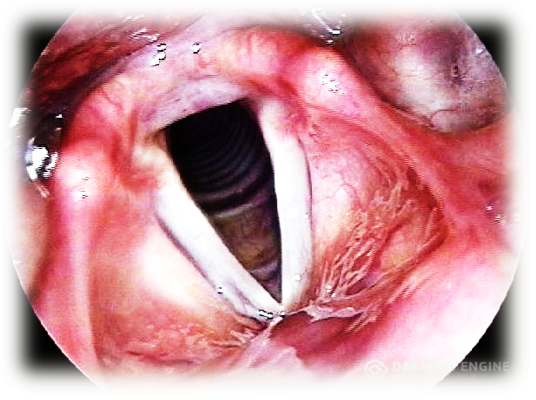
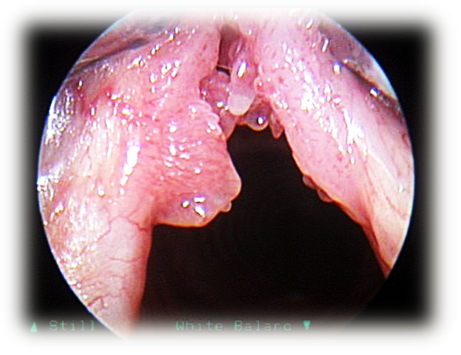
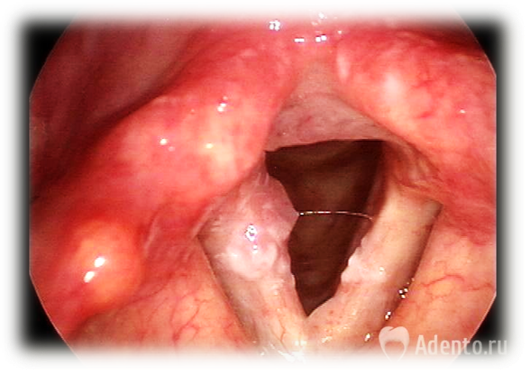
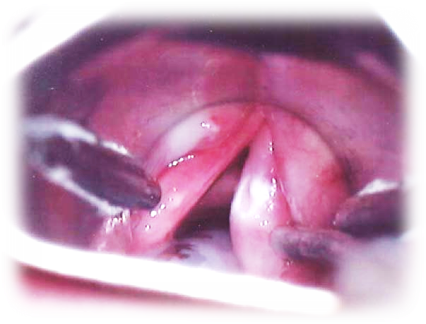
Злокачественное новообразование гортани – злокачественная опухоль, чаще всего эпителиального генеза (97–98%), поражающая верхние отделы дыхательного тракта. Мужчины болеют значительно чаще женщин, 10,0-11,0 и 0,5-1,0 соответственно, и рост заболеваемости происходит, в основном, за счет мужского населения [7] (УД – А).
Факторы риска возникновения ЗНО гортани
Этиологические факторы до настоящего времени остаются не выясненными. Основным фактором, определяющим выбор лечебной тактики, служат морфологическая структура опухоли. При злокачественных новообразованиях преимущественно используется комбинированный метод лечения [2,3,7] (УД – А).
- не леченные воспалительные и предраковые заболевания гортани (папилломы, папилломатоз, дискератоз, лейкоплакия, пахидермия, фиброма);
- возраст и пол (лица старше 55 лет мужского пола);
- вредные привычки (курение, злоупотребление алкоголем);
- генетическая предрасположенность (наличие злокачественных заболеваний у родственников) [2,3,7] (УД – А).
ВВОДНАЯ ЧАСТЬ
Название протокола: Злокачественные новообразования гортани
Код (ы) МКБ-10:
| С 32 | Злокачественное новообразование гортани |
| С32.0 | Поражение собственно голосового аппарата |
| С32.1 | Поражение надсвязочного отдела гортани |
| С32.2 | Поражение подсвязочного отдела гортани |
| С32.3 | Поражение хрящей гортани |
| С32.8 | Поражение гортани, выходящее за пределы одной и более вышеуказанных локализаций |
| С32.9 | Поражение гортани неуточненное |
Дата разработки/пересмотра протокола: 2015 г./2018 г.
Сокращения, используемые в протоколе:
| АлаТ | – | аланинаминотрансфераза |
| АсаТ | – | аспартатаминотрансфераза; |
| АЧТВ | – | активированное частичное тромбопластиновое время; |
| в/в | – | внутривенно |
| в/м | – | внутримышечно |
| ВИЧ | – | вирус иммунодефицита человека; |
| Гр | – | грей; |
| ЕД | – | единицы; |
| ЖКТ | – | желудочно – кишечный тракт; |
| ЗНО | – | злокачественное новообразование; |
| ИГС | – | истинная голосовая связка; |
| ИФА | – | иммуноферментный анализ; |
| КТ | – | компьютерная томография; |
| ЛТ | – | лучевая терапия; |
| МНО | – | международное нормализованное отношение; |
| МРТ | – | магнитно резонансная томография; |
| ОАК | – | общий анализ крови; |
| ОАМ | – | общий анализ мочи; |
| п/к | – | подкожно; |
| ПТИ | – | протромбиновый индекс; |
| ПЭТ | – | позитронно –эмиссионная томография; |
| РОД | – | разовая очаговая доза; |
| СОД | – | суммарно очаговая доза; |
| ССС | – | сердечно сосудистая система; |
| УЗИ | – | ультразвуковое исследование; |
| ЭКГ | – | электрокардиограмма; |
| ЭхоКГ | – | эхокардиография. |
| per os | –– | перорально; |
| TNM | – | Tumor Nodulus Metastasis — международная классификация стадий злокачественных новообразований |
Пользователи протокола: онкологи, отоларингологи, врачи общей практики, врачи скорой и неотложной помощи.
Категория пациентов: взрослые.
Оценка на степень доказательности приводимых рекомендаций
Таблица 1. Шкала уровней доказательности
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с не высоким (+) риском систематической ошибки. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). |
| D | Описание серии случаев или неконтролируемое исследование, или мнение экспертов. |
Облачная МИС «МедЭлемент»
Облачная МИС «МедЭлемент»

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
Классификация
Анатомическая классификация:
Гортань
- С32.0 Поражение собственно голосового аппарата
- С32.1 Поражение надсвязочного отдела гортани
- С32.2 Поражение подсвязочного отдела гортани
- С32.3 Поражение хрящей гортани
- С32.8 Поражение гортани, выходящее за пределы одной и более вышеуказанных локализаций
- С32.9 Поражение гортани неуточненное
Таблица 2. Международная классификация по системе TNM (VIII–й пересмотр, 2017г [2].
T – первичная опухоль
| Тх | недостаточно данных для оценки первичной опухоли; |
| Т0 | первичная опухоль не определяется; |
| Тis | преинвазивная карцинома (carcinoma in situ). |
| Надсвязочная область | |
| Т1 | опухоль ограничена одной анатомической частью надсвязочной области,подвижность голосовых связок сохранена; |
| Т2 | опухоль поражает слизистую оболочку более чем одного смежного участка надсвязочной области или частей голосовых связок, или область за пределами надсвязочной области (например, корня языка, валлекулы, медиальной стенки грушевидного синуса), без фиксации гортани; |
| Т3 | опухоль ограничена гортанью с фиксацией голосовых связок и/или с распространением в любую из следующих зон: заднюю перстневидную область, преднадгортанную область, пространство голосовой щели, и/или внутренней поверхности щитовидного хряща; |
| Т4а | опухоль распространяется на щитовидный хрящ и/или другие прилежащие к гортани ткани: трахею, щитовидную железу, пищевод, мягкие ткани шеи, включая глубокие мышцы языка (подбородочно-язычную, подъязычно-язычную, небно-язычную и шиловидно-язычную), подподъязычные мышцы; |
| Т4b | опухоль распространяется на превертебральное пространство, медиастинальные структуры или охватывает сонную артерию. |
| Область голосовых связок: | |
| Т1 | опухоль ограничена голосовой (ыми) связкой (ами) без нарушения подвижности (могут быть вовлечены передняя или задняя комиссуры); |
| Т1а | опухоль ограничена одной голосовой связкой; |
| Т1b | опухоль распространяется на обе голосовые связки; |
| Т2 | опухоль распространяется на надсвязочную и/или подсвязочную области, и/или нарушение подвижности голосовой связки. |
| Т3 | опухоль ограничена гортанью с фиксацией голосовой связки и/или поражает пространство голосовой щели и/или внутренней поверхности щитовидного хряща; |
| Т4а | опухоль распространяется на щитовидный хрящ и/или на другие прилежащие к гортани ткани: трахею, щитовидную железу, пищевод, мягкие ткани шеи, включая глубокие мышцы языка (подбородочно-язычную, подъязычно-язычную, небно-язычную и шило-язычную), подподъязычные мышцы; |
| Т4b | опухоль распространяется на превертебральное пространство, медиастинальные структуры или охватывает сонную артерию. |
| Подсвязочная область: | |
| Т1 | опухоль ограничена подсвязочной областью; |
| Т2 | опухоль распространяется на одну или обе голосовые связки со свободной или ограниченной подвижностью; |
| Т3 | опухоль ограничена гортанью с фиксацией голосовой связки; |
| Т4а | опухоль распространяется на перстневидный или щитовидный хрящи и/или на прилежащие к гортани ткани: трахею, щитовидную железу, пищевод, мягкие ткани шеи, включая глубокие мышцы языка (подбородочно-язычную, подъязычно-язычную, небно-язычную, шиловидно-язычную), подподъязычные мышцы; |
| Т4b | опухоль распространяется на превертебральное пространство медиастинальные структуры или охватывает сонную артерию |
N – регионарные лимфатические узлы
| Nx | Недостаточно данных для оценки состояния регионарных лимфатических узлов; |
| N0 | Нет признаков метастатического поражения регионарных лимфатических узлов; |
| N1 | Метастазы в одном ипсилатеральном лимфатическом узле, до 3 см или менее в наибольшем измерении без экстранодального расширения |
| N2 | Метастазы делятся на: |
|
N2а |
метастазы в одном ипсилатеральном лимфатическом узле, более 3 см, но не более чем 6 см в наибольшем измерении без экстранодального расширения |
| N2b | Метастазы в множественных ипсилатеральных лимфатических узлах, не более 6 см в наибольшем измерении без экстранодального расширения |
| N2с | Метастазы в двусторонних или контралатеральных лимфатических узлах, не более 6 см в наибольшем измерении без экстранодального расширения |
| N3а | Метастазы в лимфатическом узле более 6 см в наибольшем измерении без экстранодального расширения |
| N3b | Метастазы в одном или нескольких лимфатических узлах с клиническим экстранодальным расширением |
|
Примечание: Наличие вовлечения кожи или инвазии мягких тканей с глубокой фиксацией/ привязкой к лежащим в основе мышцам или смежным структурам или клинические признаки поражения нервов классифицируется как клиническое дополнительное узловое расширение. Узлы средней линии считаются ипсилатеральными узлами. |
М – отдаленные метастазы
| Мх | недостаточно данных для определения отдаленных метастазов; |
| М0 | нет признаков отдаленных метастазов; |
| М1 | имеются отдаленные метастазы. |
Категории М1 и рМ1 могут быть более уточнены в соответствии со следующими условными обозначениями:
| Пораженный орган | Обозначение | Пораженный орган | Обозначение |
| Легкие | PUL | Костный мозг | MAR |
| Кости | OSS | Плевра | PLE |
| Печень | HEP | Брюшина | PER |
| Мозг | BRA | Надпочечники | ADR |
| Лимфоузлы | LUM | Кожа | SKI |
| Другие | OTN |
Таблица 3. Группировка по стадиям:
|
Стадия |
Т |
N |
M |
|
Стадия 0 |
Tis |
N0 |
M0 |
|
Стадия I |
T1 |
N0 |
M0 |
|
Стадия II |
T2 |
N0 |
M0 |
|
Стадия III |
T2 |
N0 |
M0 |
|
T1,Т2,Т3 |
N1 |
M0 |
|
|
Стадия IV A |
T4a |
N0, N1 |
M0 |
|
T1,T2,T3,T4a |
N2 |
M0 |
|
|
T2 |
N2 |
M0 |
|
|
T3 |
N1, N2 |
M0 |
|
|
Стадия IV B |
T4b |
N любая |
M0 |
|
T любая |
N3 |
M0 |
|
|
Стадия IV C |
T любая |
N любая |
M1 |
Патогистологическая классификация – рTNM[2] (УД – А):
рТ – первичная опухоль
Для патогистологической классификации требуется исследование первичной карциномы при отсутствии макроскопической опухоли по краям резекции.
Случай можно классифицировать как рТ, если по краю имеется только микроскопическая опухоль.
Категории рТ соответствуют категориям Т.
Примечание. При классификации рТ размер опухоли есть величина инвазивного компонента. Если имеется большой компонент in situ (например, 4 см) и малый инвазивный компонент (например, 0,5 см), опухоль классифицируется как рТ1а.
рN – регионарные лимфатические узлы
Для гистопатологической классификации может быть предпринято исследование одного или более сторожевых лимфоузлов. Если классификация основывается только на биопсии сторожевого лимфоузла без последующей диссекции подмышечных лимфоузлов, то ее следует обозначать (sn) (sentinel node – сторожевой узел), например: pN1 (sn).
рTNM патогистологическая классификация
| pNх | Регионарные лимфатические узлы не могут быть оценены |
| pN0 | Метастазы регионарных лимфатических узлов отсутствуют. |
| pN1 | Метастазы в одном ипсилатеральном лимфатическом узле, 3 см или менее в наибольшем измерении без экстранодального расширения |
| pN2 | Метастазы делятся на: |
| pN2а | Метастазы в одном ипсилатеральном лимфатическом узле, менее 3 см в наибольшем размере с экстранодальным расширением или более 3 см, но не более 6 см в наибольшем измерении без экстранодального расширения |
| pN2b | Метастазы в множественных ипсилатеральных лимфатических узлах, не более 6 см в наибольшем измерении без экстранодального расширения |
| pN2с |
Метастазы в двусторонних или контралатеральных лимфатических узлах, не более 6 см в наибольшее измерение, без экстранодального расширения |
|
pN3а |
Метастазы в лимфатическом узле более 6 см в наибольшем измерении без экстранодального расширения |
|
pN3b |
Метастазы в лимфатическом узле более 3 см в наибольшем измерением с экстранодальным расширением или множественный ипсилатеральный или любой контралатеральный или двусторонний узел (ы) с экстранодальным расширением |
Гистопатологическая дифференцировка.
| Степень злокачественности (G) карцином: | |
|
GX |
степень дифференцировки не может быть установлена; |
|
G1 |
высокая степень дифференцировки; |
|
G2 |
умеренная степень дифференцировки; |
|
G3 |
низкая степень дифференцировки; |
|
G4 |
недифференцированная карцинома. |
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Диагностические критерии постановки диагноза
Жалобы и анамнез
Жалобы:
- кашель;
- осиплость голоса;
- боль в горле с иррадиацией в ухо;
- затрудненное дыхание;
- поперхивание при приеме жидкой пищи;
- увеличение шейных, надключичных, подключичных, подчелюстных, подбородочных лимфоузлов.
Анамнез:
Ранние симптомы заболевания при злокачественных опухолях гортани является наличие осиплости голоса, кашель которые появляются уже при I стадии заболевания. Но при первичном обращении пациентов осиплость голоса наблюдается в среднем в течении 6 месяцев, и отмечается присоединение других симптомов, тогда диагностируется III стадия. При более поздних стадиях (III-IV) присоединяются жалобы на боль стреляющая в ухо, затруднение дыхания, поперхивание при приеме жидкой пищи или воды, появление увеличенных узлов на шее.
Физикальные обследования:
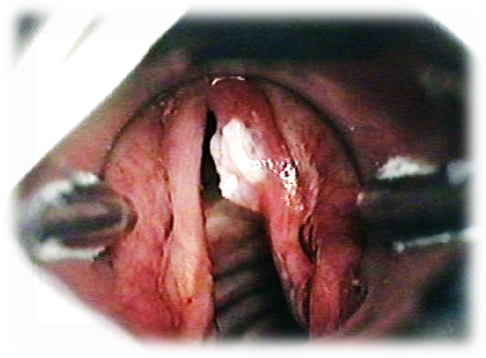
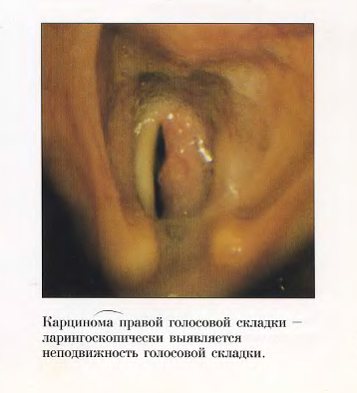
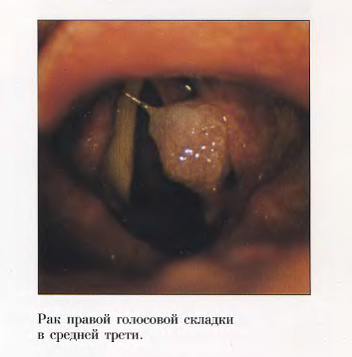
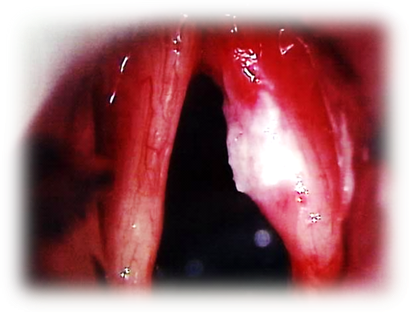
- непрямая ларингоскопия (опухолевое, образование одного из отделов гортани, ограничение подвижности ИГС или фиксация пораженной половины гортани, сужение голосовой щели);
- пальпаторное обследование лимфатических узлов шеи с обеих сторон (наличие увеличенных шейных лимфоузлов плотной консистенции, неподвижные или тугоподвижные, слабо болезненные или возможно не болезненные размером более 1,0 см).
Лабораторные исследования:
- цитологическое исследование (увеличение размеров клетки вплоть до гигантских, изменение формы и количества внутриклеточных элементов, увеличение размеров ядра, его контуров, разная степень зрелости ядра и других элементов клетки, изменение количества и формы ядрышек);
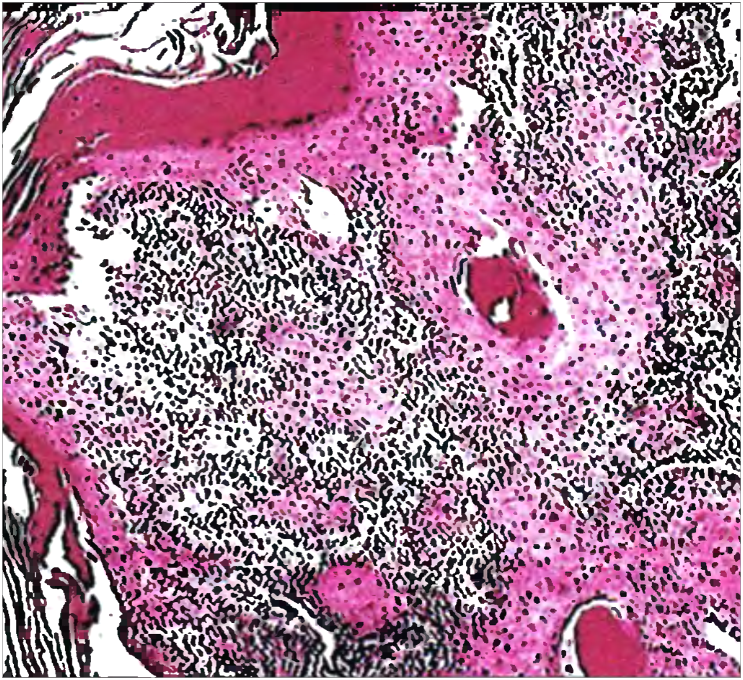
- гистологическое исследование (крупные полигональные или шиповидные клетки с хорошо выраженной цитоплазмой, округлыми ядрами с четкими ядрышками, с наличием митозов, клетки располагаются в виде ячеек и тяжей с или без образования кератина, наличие опухолевых эмболов в сосудах, выраженность лимфоцитарно-плазмоцитарной инфильтрации, митотическая активность опухолевых клеток).
Инструментальные исследования:
- УЗИ шейных, подчелюстных, надключичных, подключичных лимфоузлов (контуры четкие, неровные, эхогенность снижена, возможно наличие участков смешанной эхогенности, структура узла неоднородная, возможна повышенная васкуляризация);
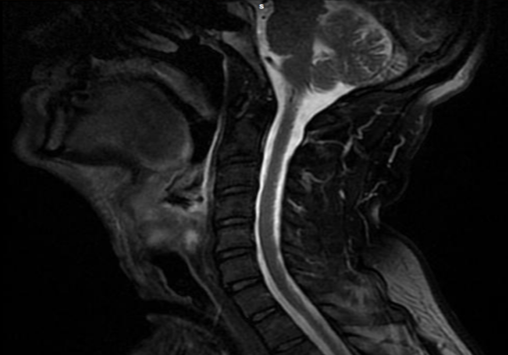
- КТ гортани (опухолевое образование гортани, занимающее правую или левую половину, распространяющееся на грушевидный синус или корень языка или мягкие ткани передней поверхности шеи, или на область трахеи, возможны конгломераты лимфоузлов различных размеров сдавливающие или оттесняющие или прорастающие сосудистонервный пучок шеи);
- биопсия из опухоли гортани (при цитологическом исследовании материала-увеличение размеров клетки вплоть до гигантских, изменение формы и количества внутриклеточных элементов, увеличение размеров ядра, его контуров, разная степень зрелости ядра и других элементов клетки, изменение количества и формы ядрышек, при гистологическом исследовании материала -крупные полигональные или шиповидные клетки с хорошо выраженной цитоплазмой, округлыми ядрами с четкими ядрышками, с наличием митозов, клетки располагаются в виде ячеек и тяжей с или без образования кератина, наличие опухолевых эмболов в сосудах, выраженность лимфоцитарно – плазмоцитарной инфильтрации, митотическая активность опухолевых клеток)
- тонкоигольная аспирационная биопсия увеличенных лимфатических узлов шеи (при цитологическом исследовании материала – увеличение размеров клетки вплоть до гигантских, изменение формы и количества внутриклеточных элементов, увеличение размеров ядра, его контуров, разная степень зрелости ядра и других элементов клетки, изменение количества и формы ядрышек).
Показания для консультации узких специалистов:
- консультация кардиолога (пациентам 50 лет и старше, так же пациенты моложе 50 лет при наличии сопутствующей патологии ССС);
- консультация невропатолога (при сосудистых мозговых нарушениях, в том числе инсультах, травмах головного и спинного мозга, эпилепсии, миастении, нейроинфекционных заболеваниях, а также во всех случаях потери сознания);
- консультация гастроэнтеролога (при наличии сопутствующей патологии органов ЖКТ в анамнезе);
- консультация нейрохирурга (при наличии метастазов в головной мозг, позвоночник);
- консультация торакального хирурга (при наличии метастазов в легких);
- консультация эндокринолога (при наличии сопутствующей патологии эндокринных органов).
Диагностический алгоритм
Дифференциальный диагноз
Дифференциальный диагноз:
Нозологическая форма |
Клинические проявления |
| Папиллома гортани |
Возникают на голосовых связках, реже на надгортаннике.Бледно-серого цвета, мелкобугристая. Осиплость голоса.Дифференциальная диагностика проводится на основании морфологического заключения. |
| Лейкоплакия |
Продолговатое белое пятно с неровной поверхностью на голосовых складках.Чаще располагается сзади черпаловидных хрящей. Нарушение фонации, кашель.Дифференциальная диагностика проводится на основании морфологического заключения. |
| Контактные фибромы |
Располагаются в задних отделах голосовых складок.На одной складке напоминает наковальню, на другой-молоточек. Изменение голоса. |
| Фибромы гортани |
Локализуются в передней трети голосовых связок.Иногда на широком основании исходящие из вестибулярной связки или гортанного желудочка.Дифференциальная диагностика проводится на основании морфологического заключения. |
Лечение
Препараты (действующие вещества), применяющиеся при лечении
| Амброксол (Ambroxol) |
| Амикацин (Amikacin) |
| Аминокапроновая кислота (Aminocaproic acid) |
| Аминофиллин (Aminophylline) |
| Апрепитант (Aprepitant) |
| Ацетилсалициловая кислота (Acetylsalicylic acid) |
| Блеомицин (Bleomycin) |
| Бромгексин (Bromhexine) |
| Винорелбин (Vinorelbine) |
| Гепарин (Heparin) |
| Гидроксиэтилкрахмал (Hydroxyethyl starch) |
| Гранисетрон (Granisetron) |
| Дарбэпоэтин альфа (Darbepoetin alfa) |
| Дексаметазон (Dexamethasone) |
| Декстран (Dextran) |
| Декстроза (Dextrose) |
| Диклофенак (Diclofenac) |
| Дифенгидрамин (Diphenhydramine) |
| Доксорубицин (Doxorubicin) |
| Доцетаксел (Docetaxel) |
| Дротаверин (Drotaverinum) |
| Железа (III) гидроксид декстран (Ferric (III) hydroxide destrane) |
| Железа (III) гидроксид декстран (Ferric (III) hydroxide destrane) |
| Железа (III) гидроксид сахарозный комплекс (Ferric (III) hydroxide sacharose complex) |
| Железа карбоксимальтозат (Ferric carboxymaltosate) |
| Имипенем (Imipenem) |
| Инсулин человеческий (Insulin human) |
| Капецитабин (Capecitabine) |
| Карбоплатин (Carboplatin) |
| Кетопрофен (Ketoprofen) |
| Комплекс аминокислот для парентерального питания (Complex of amino acids for parenteral nutrition) |
| Ленограстим (Lenograstim) |
| Липэгфилграстим (Lipegfilgrastim) |
| Метоклопрамид (Metoclopramide) |
| Метотрексат (Methotrexate) |
| Метронидазол (Metronidazole) |
| Надропарин кальция (Nadroparin calcium) |
| Натрия хлорид (Sodium chloride) |
| Неостигмина метилсульфат (Neostigmine methylsulfate) |
| Нетупитант (Netupitant) |
| Оланзапин (Olanzapine) |
| Ондансетрон (Ondansetron) |
| Офлоксацин (Ofloxacin) |
| Паклитаксел (Paclitaxel) |
| Палоносетрон (Palonosetron) |
| Парацетамол (Paracetamol) |
| Платифиллин (Platifillin) |
| Преднизолон (Prednisolone) |
| Препараты железа (III) (Formulations iron (III)) |
| Пэгфилграстим (Pegfilgrastim) |
| Ролапитант (rolapitant) |
| Спиронолактон (Spironolactone) |
| Теофиллин (Theophylline) |
| Тофизопам (Tofisopam) |
| Трамадол (Tramadol) |
| Трописетрон (Tropisetron) |
| Филграстим (Filgrastim) |
| Филграстим (Filgrastim) |
| Флуконазол (Fluconazole) |
| Фолиевая кислота (Folic acid) |
| Фосапрепитант (Fosaprepitant) |
| Фторурацил (Fluorouracil) |
| Фуросемид (Furosemide) |
| Хлоропирамин (Chloropyramine) |
| Цетуксимаб (Cetuximab) |
| Цефазолин (Cefazolin) |
| Цефепим (Cefepime) |
| Цефтазидим (Ceftazidime) |
| Цефтриаксон (Ceftriaxone) |
| Цефуроксим (Cefuroxime) |
| Цианокобаламин (Cyanocobalamin) |
| Циклофосфамид (Cyclophosphamide) |
| Циластатин (Cilastatin) |
| Ципрофлоксацин (Ciprofloxacin) |
| Цисплатин (Cisplatin) |
| Эмпэгфилграстим (Empegfilgrastimum) |
| Эноксапарин натрия (Enoxaparin sodium) |
| Эпоэтин альфа (Epoetin alfa) |
| Эпоэтин бета (Epoetin Beta) |
| Эпоэтин тета (Epoetin theta) |
| Этамзилат (Etamsylate) |
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ: нет.
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ
Общие принципы лечения
Рак среднего отдела
| Стадия | Лечение |
| I-II стадии |
(Т1–2 N0 M0). Начинать лечение больных раком среднего отдела гортани I-II стадии возможно с хирургического удаления опухоли (различные виды резекции гортани (открытая или эндоскопическая) в зависимости от локализации опухоли) [1, 7] (УД – А). При второй стадии местнораспространенного процесса возможно проведение послеоперационного курса дистанционной гамм-терапии до 40 Гр. Альтернативой при I-II стадии или при наличии противопоказаний к операции лечение начинают с лучевой терапии в дозе 63-66 Гр по 2,25 – 2,0 Гр. При резорбции опухоли менее 50% на дозе 38-45Гр, проводится оперативное вмешательство[1, 2, 3, 4, 5, 6,7] (УД – А). |
| III-IVА |
(Т1–4 N0-3 M0). Комбинированное или комплексное: Хирургическое лечение на первом этапе при местнораспространенных опухолях в объеме ларингоэктомия или расширенная ларингоэктомия с одно- или двухсторонней шейной диссекцией. Вторым этапом проводится послеоперационный курс ЛТ – на первичный очаг 60 – 66 Гр по 2,0 Гр, при клинических метастазах в лимфоузлах на шею 60 – 66Гр, при клинически не измененных лимфоузлах 44 – 64Гр на шею. При наличии в краях резекции опухолевых клеток далее проводятся курсы химиотерапии. Альтернатива — начать лечение с химиолучевой терапии с включением в схему препаратов платины, или курса лучевой терапии при клинически определяемых метастазах в дозе 70Гр (альтерирующее облучение возможно провести в режиме ускоренного гиперфракционирования 72 Гр, или гиперфракционирования 79,2 – 81,6 Гр) при клинически не измененных лимфоузлах до 44-64Гр [1] (УД – А), либо с индукционных курсов химиотерапии [1,] (УД – В). При остаточной опухоли гортани производится хирургическое лечение на гортани и шейных лимфоузлах, при полной регрессии опухоли гортани и наличии остаточных узлов на шее производится шейная диссекция[1, 2, 3, 4, 5, 6,7] (УД – А). |
| IVB стадия |
паллиативная химиотерапия или химиолучевая терапия. |
Рак надсвязочного отдела:
| Стадия | Лечение |
| I–II стадии |
Начинать лечение больных раком надсвязочного отдела гортани I-II стадии возможно с хирургического удаления опухоли (различные виды резекции гортани (открытая или эндоскопическая) учитывая большей процент метастазирования надскладочного отдела гортани необходимо одномоментное выполнение шейной диссекции. При неблагоприятных факторах (наличии в краях резекции опухолевых клеток, или выявление метастазов в лимфоузлах) проводится лучевая терапия первичный очаг 60 – 66Гр, лимфоузлы 44 – 64Гр. Альтернативой при I-II стадии или при наличии противопоказаний к операции является лучевая терапия в дозе до 66 Гр по 2,0 Гр, на клинически неизмененные лимфоузлы 44 – 64 Гр [1, 2, 3, 4, 5, 6,7] (УД – А). |
| III–IVА стадии |
Комбинированное или комплексное: Хирургическое лечение на первом этапе при местнораспространенных опухолях в объеме ларингоэктомия или расширенная ларингоэктомия с одно – или двухсторонней шейной диссекцией. Вторым этапом проводится послеоперационный курс ЛТ – на первичный очаг 60 – 66 Гр по 2,0 Гр, при клинических метастазах в лимфоузлах на шею 60-66Гр, при клинически не измененных лимфоузлах 44 – 64Гр на шею. При наличии в краях резекции опухолевых клеток далее проводятся курсы химиотерапии. Альтернатива — начать лечение с химиолучевой терапии с включением в схему препаратов платины, или курса лучевой терапии при клинически определяемых метастазах в дозе 70Гр (альтерирующее облучение возможно провести в режиме ускоренного гиперфракционирования 72 Гр, или гиперфракционирования 79,2 – 81,6 Гр) при клинически не измененных лимфоузлах до 44 – 64Гр [1] (УД – А), либо с индукционных курсов химиотерапии [1,] (УД – В). При остаточной опухоли гортани производится хирургическое лечение на гортани и шейных лимфоузлах, при полной регрессии опухоли гортани и наличии остаточных узлов на шее производится шейная диссекция [1, 2, 3, 4, 5, 6,7] (УД – А). |
| IVB стадия |
паллиативная химиотерапия или химиолучевая терапия. |
Рак подсвязочного отдела:
| Стадия | Лечение |
| I–IVА стадии | (Т1–4 N1–3 M0). Рак подсвязочного пространства нечувствителен к лучевому и химиолучевому воздействию. Поэтому при опухолях только этого отдела и при распространении рака подсвязочного пространства на соседние анатомические части, а также при распространении на подсвязочный отдел новообразований из соседних анатомических частей (голосовые складки и вестибулярный отдел) проводится только комбинированное лечение. Удаление гортани производится с долей щитовидной железы на стороне пораженного подсвязочного отдела. Послеоперационный курс ЛТ – на первичный очаг 60 – 66 Гр по 2,0 Гр, при клинических метастазах в лимфоузлах на шею 60-66Гр, при клинически не измененных лимфоузлах 44 – 64Гр на шею[1] (УД – А). |
| Примечание : |
При наличии у больного признаков перихондрита хрящей гортани, опухолевого стеноза лечение следует начинать с хирургического этапа. |
Критерии эффективности лечения
Полный эффект – исчезновение всех очагов поражения на срок не менее 4х недель.
Частичный эффект – большее или равное 50% уменьшение всех или отдельных опухолей при отсутствии прогрессирования других очагов.
Стабилизация – (без изменений) уменьшение менее чем на 50% или увеличение менее чем на 25% при отсутствии новых очагов поражения.
Прогрессирование – увеличение размеров одной или более опухолей более 25% либо появление новых очагов поражения [7] (УД – А).
Немедикаментозное лечение
Режим: при проведении консервативного лечения – общий. В ранний послеоперационный период – постельный или полупостельный (в зависимости от объема операции и сопутствующей патологии). В послеоперационном периоде – палатный.
Диета: стол – №15, после хирургического лечения – №1.
Лучевая терапия:
Показания к лучевой терапии:
- низкодифференцированные опухоли с распространенностью Т1 – Т3;
- при лечении нерезектабельных опухолей;
- отказа пациента от операции;
- наличие резидуальной опухоли;
- периневральная или перилимфатическая инвазия;
- экстракапсулярное распространение опухоли;
- метастазы в железе или регионарных лимфатических узлах;
- рецидив опухоли.
Методы лучевой терапии:
- дистанционная лучевая терапия;
- 3D-конформное облучение;
- модулированная по интенсивности лучевая терапия (IMRT).
- Томотерапия на томоаппаратах. Одним из вариантов высокотехнологичной лучевой терапии РТМ является Томотерапия – спиральное (гелическое “helical”) облучение, проводимое на специализированных линейных ускорителях – томоаппаратах. При их работе происходит одновременное ротационное движение во время сеанса облучения головки аппарата и лепестков (секторное IMRT) с одновременным поступательным продольным смещением стола. Спиральная томотерапия это сверхточная лучевая терапия управляемая по изображениям (IGRT), с помощью, которой осуществляется прецизионное подведение луча вращающего радиационного пучка к опухоли с одновременной защитой окружающих здоровых тканей, за счет визуализации и локализации анатомическихструктур на протяжении процесса лечения. Используемые в каждом направлении модулированные не только сверхточно фокусируется, но и характеризуется высокой конформностью. Существует много систем, которые позволяют создать сферическое распределение мелких доз, но томотерапия, позволяет изменить форму этой дозы при несферических и даже весьма сложных, вогнутых мишенях. Используются как стандартные методики фракционирования при подведении разовых и суммарных очаговых доз. Однако упор при томотерапии делается на гипофракционирование при РОД<2,5 Гр.
Противопоказания к лучевой терапии:
Абсолютные противопоказания:
- психическая неадекватность больного;
- лучевая болезнь;
- гипертермия >38 градусов;
- тяжелое состояние больного по шкале Карновского 50% и меньше (смотри приложение 1).
Относительные противопоказания:
- беременность;
- заболевание в стадии декомпенсации (сердечно – сосудистой системы, печени, почек);
- сепсис;
- активный туберкулез легких;
- распространение опухоли на соседние полые органы и прорастании в крупные сосуды;
- распад опухоли (угроза кровотечения);
- стойкие патологические изменения состава крови (анемия, лейкопения, тромбоцитопения);
- кахексия;
- наличие в анамнезе ранее проведенного лучевого лечения.
Медикаментозное лечение
Химиотерапия:
Существует несколько видов химиотерапии, которые отличаются по цели назначения:
- неоадъювантная химиотерапия опухолей назначается до операции, с целью уменьшения неоперабельной опухоли для проведения операции, а так же для выявления чувствительности раковых клеток к препаратам для дальнейшего назначения после операции.
- адъювантная химиотерапия назначается после хирургического лечения для предотвращения метастазирования и снижения риска рецидивов.
- лечебная химиотерапия назначается для уменьшения метастатических раковых опухолей.
В зависимости от локализации и вида опухоли химиотерапия назначается по разным схемам и имеет свои особенности.
Показания к химиотерапии:
- цитологически или гистологически верифицированные ЗНО гортани;
- при лечении нерезектабельных опухолей;
- метастазы в железе или регионарных лимфатических узлах;
- рецидив опухоли;
- удовлетворительная картина крови у пациента: нормальные показатели гемоглобина и гемокрита, абсолютное число гранулоцитов – более 200, тромбоцитов – более 100000;
- сохраненная функция печени, почек, дыхательной системы и ССС;
- возможность перевода неоперабельного опухолевого процесса в операбельный;
- отказа пациента от операции;
- улучшение отдаленных результатов лечения при неблагоприятных гистотипах опухоли (низкодифференцированный, недифференцированный).
Противопоказания к химиотерапии:
Противопоказания к химиотерапии можно разделить на две группы: абсолютные и относительные.
Абсолютные противопоказания:
- гипертермия >38 градусов;
- заболевание в стадии декомпенсации (сердечно-сосудистой системы, дыхательной системы печени, почек);
- наличие острых инфекционных заболеваний;
- психические заболевания;
- неэффективность данного вида лечения, подтвержденная одним или несколькими специалистами;
- распад опухоли (угроза кровотечения);
- тяжелое состояние больного по шкале Карновского 50% и меньше (смотри приложение 1).
Относительные противопоказания:
- беременность;
- интоксикация организма;
- активный туберкулез легких;
- стойкие патологические изменения состава крови (анемия, лейкопения, тромбоцитопения);
- кахексия.
Ниже приведены схемы наиболее часто используемых режимов полихимиотерапии при плоскоклеточном раке любой локализаций в области головы и шеи. Они могут быть использованы при проведении как неоадъювантной (индукционной) химиотерапии так и адъювантной полихимиотерапии, с последующим хирургическим вмешательством или лучевой терапией, а так же при рецидивных или метастатических опухолях.
Основными комбинациями, используемыми при проведении индукционной полихимиотерапии, на сегодняшний день признаны цисплатин с 5 – фторурацилом (ПФ) и доцетаксел с цисплатином и 5фторурацилом (ДПФ). На сегодняшний день эта комбинация химиопрепаратов стала «золотым стандартом» при сравнении эффективности применения различных химиопрепаратов в лечении плоскоклеточного рака головы и шеи для всех крупных многоцентровых исследований. Последняя схема представляется наиболее эффективной, но и наиболее токсичной, однако при этом обеспечивающей более высокие показатели выживаемости и локорегионарного контроля по сравнению с использованием традиционной схемы ПФ в качестве индукционной полихимиотерапии [9,10] (УД-А).
Из таргетных препаратов в настоящее время в клиническую практику вошел цетуксимаб.
По последним данным, единственной комбинацией химиопрепаратов, не только увеличивающей количество полных и частичных регрессий, но и продолжительность жизни больных с рецидивами и отдаленными метастазами плоскоклеточного рака головы и шеи, является схема с использованием цетуксимаба, цисплатина и 5 – фторурацила [11].
Таблица № 2. Активность препаратов в монорежиме при рецидивном/метастатическом плоскоклеточном раке головы и шеи (модифицировано по В.А. (Murphy) [9] (УД-А).
|
Препарат |
Частота ответов,% |
| Метотрексат | 10-50 |
| Цисплатин | 9-40 |
| Карбоплатин | 22 |
| Паклитаксел | 40 |
| Доцетаксел | 34 |
| 5-Фторурацил | 17 |
| Блеомицин | 21 |
| Доксорубицин | 23 |
| Цетуксимаб | 12 |
| Капецитабин | 23 |
| Винорельбин | 20 |
| Циклофосфамид | 23 |
Схемы химиотерапии:
Наиболее активными противоопухолевыми средствами при плоскоклеточном раке головы и шеи считаются как при 1 и 2 линий производные платины (цисплатин, карбоплатин) производные фторпиримидина (5 фторурацил), антрациклины, таксаны – паклитаксел, доцетаксел.
Активны при раке головы и шеи также доксорубицин, капецитабин, блеомицин, винкристин, циклофосфан как вторая линия химиотерапии.
При проведении как неоадъювантной, так и адъювантной полихимиотерапии при раке головы и шеи возможно применение следующих схем и комбинации химиопрепаратов:
PF
- Цисплатин 75 – 100мг/м2 в/в, 1-й день;
- 5 Фторурацил 1000мг/м2 24 – часовой в/в инфузией (96 часовая непрерывная инфузия)
1 – 4 –й дни;
повторение курса каждые 21 день.
PF
- Цисплатин 75-100мг/м2 в/в, 1-й день;
- 5 Фторурацил 1000мг/м2 24 – часовой в/в инфузией (120 часовая непрерывная инфузия)
1 – 5 –й дни;
повторение курса каждые 21 день.
При необходимости на фоне первичной профилактики колониестимулирующими факторами.
CpF
- Карбоплатин (AUC 5,0-6,0) в/в, 1-й день;
- 5 Фторурацил 1000мг/м2 24 – часовой в/в инфузией (96 часовая непрерывная инфузия) 1 – 4 – й дни;
повторение курса каждые 21 день.
- Цисплатин 75мг/м2 в/в 1 – й день;
- Капецитабин 1000мг/м2 перорально дважды в день, 1 – 14-й дни;
повторение курсов каждые 21 день.
- Паклитаксел 175мг/м2, в/в, 1 – й день;
- Цисплатин 75мг/м2, в/в, 2 – й день;
повторение курсов каждые 21 день.
- Паклитаксел 175мг/м2, в/в, 1 – й день;
- Карбоплатин (AUC 6,0), в/в, 1 – й день;
повторение курсов каждые 21 день.
ТР
- Доцетаксел 75мг/м2, в/в,1 – й день;
Цисплатин – 75мг/м2, в/в, 1–й день;
повторение курсов каждые 21 день.
ТPF
- Доцетаксел 75 мг/м2, в/в, 1 – й день;
Цисплатин 75 – 100мг/2,в/в,1 – й день;
5 Фторурацил 1000мг/м2 24 – часовой внутривенной инфузией (96 часовая непрерывная инфузия)1 – 4 –й дни;
повторение курсов каждые 21 день.
- Паклитаксел 175 мг/м2, в/в, 1 –й день 3 – х часовая инфузия;
- Цисплатин 75мг/2, в/в, 2 – й день;
- 5 Фторурацил 500мг/м2 24 – часовой внутривенной инфузией (120 часовая непрерывная инфузия)1 – 5 – й дни;
повторение курсов каждые 21 день.
- Цетуксимаб 400мг/м2 в/в (инфузия в течение 2 ч), 1-й день 1 – го курса, Цетуксимаб 250 мг/м2, в/в (инфузия в течение 1 ч),8,15 – й дни и 1,8 и 15 – й дни последующих курсов;
- Цисплатин 75 – 100мг/м2, в/в, 1 – й день;
- 5-фторурацил 1000 мг/м2 24 – часовой внутривенной инфузией (96 часовая непрерывная инфузия) 1 – 4 – й дни;
повторение курсов каждые 21 день в зависимости от восстановления гематологических показателей.
CAP(а)
- Цисплатин 100 мг/м2, в/в, 1 день;
- Циклофосфан 400 – 500 мг/м2, в/в 1 день;
- Доксорубицин 40 – 50 мг/м2, в/в, 1 день;
повторение курсов каждые 21 день.
PBF
- 5 – Фторурацил 1000 мг/м2, в/в 1,2,3,4 дни;
- блеомицин 15 мг 1,2,33 дни;
- цисплатин 120 мг 4 день;
повторение курса каждые 21 день.
CpP
- Карбоплатин 300 мг/м2, в/в, 1день;
- Цисплатин 100 мг/м2в/в, 3день;
повторение курса каждые 21 день.
МРF
- Метотрексат 20 мг/м2, 2и 8 день;
- Фторурацил 375 мг/м2, 2 и 3 день;
- Цисплатин 100 мг/м2, 4 день;
повторение курса каждые 21 день
*Примечание: при достижении резектабельности первичной опухоли или рецидивного, хирургическое лечение может выполнено не ранее через 3 недели после последнего введения химиопрепаратов.
* Лечение ПКР головы и шеи проблематично в основном из-за того, что на всех этапах развития болезни требуется тщательный мультидисциплинарный подход для выбора существующих опций лечения больных.
Химиотерапию в монорежиме рекомендовано проводить:
- у ослабленных больных в преклонном возрасте;
- при низких показателях кроветворения;
- при выраженном токсическом эффекте после предыдущих курсов химиотерапии;
- при проведении паллиативных курсов химиотерапии;
- при наличии сопутствующей патологии с высоким риском осложнений.
Схемы монохимиотерапии:
- Доцетаксел 75 мг/м2, вв, 1 – й день;
Повторение курса каждые 21 день.
- Паклитаксел 175 мг/м2, в/в, 1 – й день;
Повторение каждые 21 день.
- Метотрексат 40 мг/м2, в/в, или в/м 1 день;
Повторение курса каждую неделю.
- Капецитабин 1500 мг/м2, перорально ежедневно 1 – 14 дни;
Повторение курса каждые 21 день.
- Винорельбин 30 мг/м2, в/в 1 день;
Повторение курса каждую неделю.
- Цетуксимаб 400мг/м2, в/в (инфузия в течение 2 ч), 1 – е введение, затем цетуксимаб 250мг/м2, вв (инфузия в течении 1 ч) еженедельно;
Повторение курса каждую неделю.
*метотрексат, винорельбин, капецитабин в монорежиме чаще всего используют как вторую линию лечения.
Таргетная терапия:
Основными показаниями для проведения таргетной терапии является:
- местно-распространенный плоскоклеточный рак головы и шеи в комбинации с лучевой терапией;
- рецидивирующий или метастатический плоскоклеточный рак головы и шеи в случае неэффективности предшествующей химиотерапии;
- монотерапия рецидивирующего или метастатического плоскоклеточного рака головы и шеи при неэффективности предшествующей химиотерапии;
Цетуксимаб вводят 1 раз в неделю дозе 400мг/м2 (первая инфузия) в виде 120 – минутной инфузией, далее в дозе 250 мг/м2 в виде 60 – минутной инфузии.
При применении Цетуксимаба в сочетании с лучевой терапией, лечение цетуксимабом рекомендуется начинать за 7 дней до начала лучевого лечения и продолжать еженедельные введения препарата до окончания лучевой терапии.
У пациентов с рецидивирующим или метастатическим плоскоклеточным раком головы и шеи в комбинации с химиотерапией на основе препаратов платины (до 6 циклов) Цетуксимаб используется как поддерживающая терапия до появления признаков прогрессирования заболевания заболевания. Химиотерапия начинается не ранее чем через 1 час после окончания инфузии Цетуксимаба.
В случае развития кожных реакции на введение Цетуксимаба терапию можно возобновить с применением препарата в редуцированных дозах (200мг/м2 после второго реакции и 150мг/м2 – после третьего).
Перечень дополнительных лекарственных средств с указанием формы выпуска
Сопроводительная терапия для профилактики и коррекции побочных эффектов химиотерапии представлена в приложении 1.
Химиолучевая терапия:
При местно-распространенных формах рака гортани одним из способов улучшения эффективности лечения является применение методов последовательной или сочетанной химиолучевой терапии [12] (УД – А).
При последовательной химио-лучевой терапии на первом этапе проводится несколько курсов индукционной химиотерапии с последующим проведением лучевой терапии, что обеспечивает улучшение локорегионарного контроля и повышение случаев резектабельности пациентов с сохранением органа, а так же повышение качества жизни, и выживаемости пациентов [13] (УД – А).
Такой подход (химио-лучевой) можно применить не только при раке гортани, но и при других локализациях опухолей головы и шеи (носоглотки, ротоглотки, гортаноглотки) [14] (УД – А).
При стенозирующем раке гортани, при котором химиотерапия не эффективна, стандартом лечения является ларингоэктомия с последующей лучевой терапией.
При одновременном химиолучевом лечении обычно используются препараты платины обладающие способностью потенцировать эффект лучевой терапии (цисплатин или карбоплатин), а также таргетный препарат цетуксимаб [15, 16] (УД – А).
При проведении одновременного химиолучевого лечения рекомендованы следующие схемы курсы химиотерапии.
- Цисплатин 20-40мг/м2 в/в еженедельно, при проведении лучевой терапии;
Лучевая терапия в суммарной очаговой дозе 66 – 70Гр. Разовая очаговая доза – 2 Гр х 5 фракции в неделю.
- Карбоплатин (AUC1,5-2,0) в/в еженедельно, при проведении лучевой терапии;
Лучевая терапия в суммарной очаговой дозе 66 – 70Гр. Разовая очаговая доза – 2 Гр х 5 фракции в неделю.
- Цетуксимаб 400мг/м2 в/в кап(инфузия в течении 2 ч) за неделю до начало лучевой терапии, далее цетуксимаб 250мг/м2 в/в ( инфузия в течении 1 ч) еженедельно при проведении лучевой терапии.
Лечение нерезектабельных опухолей:
Одновременная химиотерапия или лучевая терапия:
- цисплатин 100 мг/м2 внутривенная инфузия со скоростью не более 1 мг/мин с пред – и постгидратацией в 1-й, 22-й и 43-й дни на фоне проведения лучевой терапии на ложе удаленной опухоли в СОД 70 Гр (РОД 2 Гр) и область регионарных лимфатических узлов на стороне поражения в СОД 50-60 Гр (при больших метастазах до 70 Гр);
- дистанционная лучевая терапия на первичный опухолевый очаг в СОД 70 Гр и регионарные лимфатические узлы в СОД 50-60 Гр (при больших метастазах до 70 Гр). При низкозлокачественных опухолях (N0) регионарные лимфатические узлы не облучают.
- если после завершения лечения опухоль стала резектабельной, возможно выполнение радикального хирургического вмешательства.
Перечень дополнительных лекарственных средств с указанием формы выпуска (менее 100% вероятности применения).
Антибактериальная терапия;
- Цефазолин 1,0 гр, по 1,0 гр в/м 3 раза в день, 7 дней;
- Цефтазидим 100мг, по 100мг в/м 3 раза в день, 7 дней;
- Цефтриаксон 1,0 гр, по 1,0 гр в/м 2 раза в день, 7 дней;
- Цефуроксим натрия 1,0гр, по 1,0гр в/м 2 раза в день, 7 дней;
- Цефепим 1,0 гр, по 1,0 гр в/м 2 раза в день, 7 дней;
- Имипенем + циластатин 500мг, по в/м 2 раза в день, 5-7 дней;
- Амикацин 500мг, из расчета 10мг/кг в/м 2 раза в день, 7 дней;
- Ципрофолоксацин 100мг, по 100мг в/в 2 раза в день, 5 – 7 дней;
- Офлоксацин 0,2гр, по 0,2 гр в/в 2 раза в день, 7 дней;
- Метронидазол 100 мл, по 100 мл в/в 2 раза в день, 5 дней.
Противогрибковая терапия;
- Флуконазол 100 мг, по 100мг в/в – однократно.
Плазмозаменящая терапия;
- Гидроксиэтилкрахмал 200мл, по 500 мл в/в 1 раз в день до 3 дней;
- Декстран 400мл, по 400 мл в/в 2 раза в день 2 – 3 дня.
Парентеральное питание;
- Комплекс аминокислот для парентерального питания 500мл, по 500мл в/в 1 раз в день, 5 – 7 дней;
- Декстроза 5% — 400мл, по 400мл в/в 2 раза в день, 5 – 7 дней.
Регидратационная терапия;
- Натрия хлорид 0,9% — 400мл, по 400 мл в/в 2 – 3 раза в день. 5 – 7 дней.
Аналгетическая терапия;
- Кетопрофен 1мл, по 1 мл, в/м 2 – 3 раза в день 5 – 7 дней;
- Диклофенак натрия в/м 2 – 3 раза в день 7 – 10 дней;
- Трамадола гидрохлорид 1 мл, по 1мл в/м 2 – 3 раза в день.
Гормональные терапия
- Преднизолон 30мг, по 30 – 60 – 90 мг в/в 1 раз в день 1 – 5 дней;
- Дексаметазон 4 мг, по 4 – 8 – 12 – 16 – 20 мг 1 раз в день 1 – 5 дней;
- Инсулин человеческий 40 ЕД, 4 – 6 ЕД 1 раз в день 2 – 10 дней.
Спазмолитическая терапия
- Дротоверин 2,0 мл, по 2,0 мл в/м, в/в 1 – 3 раза в день 1 – 7 дней;
- Платифиллина гидротартарарат 1,0 мл, по 1 мл в/м, в/в 1-3 раза в день 1-7 дней.
Бронхолитиеская терапия
- Аминофиллин 10мл, по 6 – 10мг/кг/сут в/м 3 раза в день,10 дней;
- Теофиллин 0,2гр, по 0,2 гр per os 2 – 4 раза в день, 10 – 15 дней.
Антикоагулянтная терапия
- Надропарин кальция 0,3 мл, по 0,3 мл 1 раз в день п/к;
- Эноксапарин натрия 0,2 мл, по 0,2 мл 1 раз в день п/к;
- Гепарин 10тысЕД, по 5000-10000 ЕД в/в или п/к 1 раз в день.
Муколитическая терапия
- Бромгексин 8 мг, по 8 мг per os 3 раза в день, 7 – 10 дней;
- Амброксол 2 мл, по 2 мл в/м, 3 раза в день, 7 – 10 дней.
Противорвотная терапия
- Ондансетрон 4мг, по 4 – 8 – 12 – 16 – 20 – 24 мг в/в, в/м 1 – 2 раза в день, 1 – 5 дней;
- Метоклопрамид 10 мг, по 10 – 20 мг вм, в/в 1 – 2 – 3 раз в день,1 – 5 дней.
Седативная терапия
- Тофизопам 50 мг, по 50 мг per os 1 – 2 раза в день, 1 – 5 дней;
- Неостигмина метилсульфат 1,0мл, по 1мл в/м 1 – 2 раза в день, 1 – 10 дней.
Жаропонижающая терапия
- Ацетилсалициловая кислота 0,5 гр, по 0,5 гр per os 2 раза в день;
- Парацетамол 0,5гр, по 0,5 гр per os, 3 раза в день.
Гемостатическая терапия
- Аминокапроновая кислота 5% — 100мл, по 100 мл в/в 1 раз в день, 1 – 5 дней.
- Этамзилат 12,5% — 2мл, по 2 мл в/м 2 раза в день, 1 – 5 дней.
- Дицинон 1 мл, по 1,0 мл в/м 1 – 2 раза в день.
Диуретическая терапия
- Фуросемид 1% — 2 мл, по 2 мл в/м, в/в 1-3 раза в день, 1 –5 дней;
- Спиронолактон 100мг, по 100 мг per os 1 раз в день, 5 – 14 дней.
Антианемическая терапия
- Феркайл 50мг — 2 мл, по 2 мл в/м 2-3 раза в неделю;
- Космофер 2 мл, по 2 мл в/м 2-3 раза в неделю.
Гемопоэтическая терапия
- Филграстим 1 мл – 0,3гр, 5 мг/кг п/к, 1 – 3дня.
Антигистаминная терапия
- Дифенгидрамин 1 мл – 10 мг, 10 мг в/м 1 – 2 раз в день;
- Хлоропирамин 25 мг, по 25 мг per os 3 – 4 раза в день;
Спазмолитическая терапия
- Дротоверин 2,0 мл, по 2,0 мл в/м, в/в 1 – 3 раза в день 1 – 7 дней;
- Платифиллина гидротартарарат 1,0 мл, по 1 мл в/м, в/в 1 – 3 раза в день 1 – 7 дней;
Противорвотная терапия
- Ондансетрон 4мг, по 4 – 8 – 12 – 16 – 20 – 24 мг в/в, в/м 1 – 2 раза в день, 1 – 5 дней;
- Метоклопрамид 10 мг, по 10 – 20 мг в/м, в/в 1 – 2 – 3 раз в день,1 – 5 дней;
Седативная терапия
- Тофизопам 50 мг, по 50 мг per os 1 – 2 раза в день, 1 – 5 дней;
- Неостигмина метилсульфат 1,0мл, по 1мл в/м 1 – 2 раза в день, 1 – 10 дней;
Медикаментозное лечение, оказываемые на этапе скорой неотложной помощи:
Гемостатическая терапия;
- Аминокапроновая кислота 5% -100мл, по 100 мл в/в 1 раз в день;
- Этамзилат 12,5%-2мл, по 2 мл в/м 2 раза в день;
- Дицинон 1 мл, по 1,0 мл в/м 1 – 2 раза в день.
Жаропонижающая терапия;
- Ацетилсалициловая кислота 0,5 гр, по 0,5 гр per os 2 раза в день;
- Парацетамол 0,5гр, по 0,5 гр per os, 3 раза в день.
Аналгетическая терапия;
- Кетопрофен 1мл, по 1 мл, в/м 2-3 раза в день;
- Диклофенак натрия в/м 2 – 3 раза;
- Трамадола гидрохлорид 1 мл, по 1мл в/м 2 – 3 раза в день;
Гормональные терапия
- Преднизолон 30мг, по 30 – 60 – 90 мг в/в 1 раз в день;
- Дексаметазон 4 мг, по 4 – 8 – 12 – 16 – 20 мг 1 раз в день.
Критерии эффективности лечения:
Полный эффект – исчезновение всех очагов поражения на срок не менее 4х недель.
Частичный эффект – большее или равное 50% уменьшение всех или отдельных опухолей при отсутствии прогрессирования других очагов.
Стабилизация – (без изменений) уменьшение менее чем на 50% или увеличение менее чем на 25% при отсутствии новых очагов поражения.
Прогрессирование – увеличение размеров одной или более опухолей более 25% либо появление новых очагов поражения[7] (УД – А).
Хирургическое вмешательство
Хирургическое вмешательство, оказываемые на стационарном уровне:
Виды хирургических вмешательств:
- ларингоэктомия;
- резекция гортани;
- расширенная ларингоэктомия (с резекцией гортаноглотки, щитовидной железы, мягких тканей передней поверхности шеи);
- эндоларингеальное иссечение опухоли ИГС;
- фасциально — футлярное иссечение шейных лимфатических узлов.
- При резектабельных рецидивных образованиях – удаление рецидива.
- При повторных резектабельных рецидивных метастазах — хирургическое удаление метастазов.
Показания к хирургическому лечению:
- цитологически или гистологически верифицированные ЗНО гортани;
- при отсутствии противопоказании к хирургическому лечению.
Все хирургические вмешательства по поводу злокачественных опухолей гортани выполняются под общей анестезией.
Противопоказания к хирургическому лечению при злокачественных новообразовании гортани:
- наличие у больного признаков неоперабельности и тяжелой сопутствующей патологии;
- недифференцированные опухоли гортани, которым в качестве альтернативны может быть предложено лучевое лечение;
- обширные гематогенные метастазирования, диссеминированного опухолевого процесса;
- синхронно существующий и распространенный неоперабельный опухолевый процесс другой локализации, например рак легкого и т.д.;
- хронические декомпенсированные и/или острые функциональные нарушения дыхательной, сердечно – сосудистой, мочевыделительной системы, желудочно – кишечного тракта;
- аллергия на препараты, используемые при общем наркозе;
- обширные гематогенные метастазирования, диссеминированного опухолевого процесса.
Профилактические мероприятия
Первичная профилактика:
- Борьба с табакокурением, алкоголем;
- Рационализация питания;
- Повышение физической активности и борьба с избыточным весом;
- Уменьшение воздействия канцерогенных химических и физических факторов (производство, природная среда, жилищные условия);
- Профилактика воздействия инфекционных канцерогенных факторов.
Вторичная профилактика:
- наблюдение за группами риска;
- выявление и лечение предраковых заболеваний, воспалительных процессов.
Третичная профилактика:
Применение лекарственных препаратов позволяющих восстановить иммунную систему после противоопухолевого лечения (антиоксиданты, поливитаминные комплексы), полноценные режим питания богатый витаминами, белками, отказ от вредных привычек (курение, употребление алкоголя), профилактика вирусных инфекций и сопутствующих заболеваний, регулярные профилактические осмотры у онколога, регулярные диагностические процедуры (рентгенография легких, УЗИ печени, почек, лимфоузлов шеи) [14.6].
Дальнейшее ведение
Диспансерное наблюдение за излеченными больными:
- в течение первого года после завершения лечения – 1 раз каждые 3 месяца;
- в течение второго года после завершения лечения – 1 раз каждые 6 месяцев;
- с третьего года после завершения лечения – 1 раз в год в течение 3 лет.
Методы обследования:
- локальный контроль — при каждом обследовании;
- пальпация регионарных лимфатических узлов — при каждом обследовании;
- рентгенографическое исследование органов грудной клетки — один раз в год;
- ультразвуковое исследование органов брюшной полости – один раз в 6 месяцев (при первично-распространенных и метастатических опухолях).
Индикаторы эффективности лечения
- «ответ опухоли» — регрессия опухоли после проведенного лечения;
- безрецидивная выживаемость (трех и пятилетняя);
- «качество жизни» включает кроме психологического, эмоционального и социального функционирования человека, физическое состояние организма больного.
Сопроводительная терапия при проведении химиотерапевтического лечения. (см. приложение №1)
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ
Показания для плановой госпитализации:
- наличие верифицированной опухоли гортани;
- проведение специализированного лечения в форме стационарной и стационарозамещающей медицинской помощи.
Показания для экстренной госпитализации:
- опухолевый стеноз гортани;
- кровотечение из опухоли;
- выраженный болевой синдром.
Информация
Источники и литература
-
Протоколы заседаний Объединенной комиссии по качеству медицинских услуг МЗ РК, 2018
- 1) NCCN Clinical Practice Guidelines in Oncology: head and neck. Available at Accessed March 2011;
2) Bonner JA, Harari PM, Giralt J, et al. Cetuximab prolongs survival in patients with locoregionally advanced squamous cell carcinoma of head and neck: A phase III study of high dose radiation therapy with or without cetuximab (abstract). ASCO Annual Meeting Proceedings (post-meeting edition). J Clin Oncol 2004;22:5507;
3) Greene FL, Page DL, Fleming ID, et al (eds). AJCC Cancer Staging Manual, Sixth Edition Springer-Verlag: New York 2002;
4) Colasanto JM, Prasad P, Nash MA, et al. Nutritional support of patients undergoing radiation therapy for head and neck cancer. Oncology 2005;19:371-382;
5) Медицинские клинические рекомендации Европейского общества медицинских онкологов (ЕSМО. Москва 2006г);
6) Piccirillo JF, Lacy PD, Basu A, et al. Development of a new head and neck cancerspecific comorbidity index. Arch Otolaryngol Head Neck Surg 2002;128:1172-1179;
7) А.И. Пачес. Опухоли головы и шеи. Клиническое руководство. Пятое издание. Москва, 2013г. 244- 274стр;
American Joint Committee on Cancer (AJCC). AJCC Cancer Staging Manual, 7th ed. Edge S.B., Byrd D.R., Carducci M.A. et al., eds. New York: Springer; 2009;
9) Murphy B.A Carcinoma of the head and neck. In: Handbook of cancer chemotherapy. Skeel R.Т., Khleif S.N.(eds). 8 th Edition. Lippincott Williams & Wilkins.2011: 69-63;
10) Руководство по химиотерапии опухолевых заболеваний. Под редакцией Н.И. Переводчиковой, В.А. Горбуновой. 4-е издание, расширенное и дополненное. Практическая медицина. Москва 2015г.;
11) Forastiere A.A.,Goepfert H., Maor M. et al. Concurrent chemotherapy and radiotherapy for organ prezervationin advanced laryngeal cancer. N Engl J Med.2003; 349:2091-2098;
12) Posner M.R., Hershor D.M., Blajman C.R. et al. Cisplatin and fluorouracil alone or with docetaxel in head and neck cancer. N Engl J Med. 2007; 357 (17): 1705-1715;
13) Blanchard P., Bourhis J., Lacas B. et al. Taxan-Fluorouracil as induction chemotherapy in locally advanced head and neck cancers: an individual patient data meta-analysis of the meta-analysis of chemotherapy in head and neck cancer group. J Clin Oncol. 2013; 31(23): 2854-2860;
14) Vermorken J.B., Mesia., Rivera F. et al. Platinum-based chemotherapy plus cetuximab in head and neck cancer. N Engl J Med. 2008; 359 (11): 1116-1127;
15) Forastiere A.A., Goepferi H., Maor M. et al. Concurrent chemotherapy and radiotherapy for organ preservationin advanced laryngeal cancer. N Engl J Med. 2003; 349: 2091-2098;
16) Bonner J.A., Harari P.M ., Giralt J. et al. Radiotherapy plus cetuximab for squamous-cell carcinoma of the head and neck. N. Engl. J. Med. 2006; 354(6): 567-578;Список использованной литературы для приложения №1
1) Navari RM, Reinhardt RR, Gralla RJ, et al. Reduction of cisplatin-induced emesis by a selective neurokinin-1-receptor antagonist. New Engl J Med. 1999;340(3):190-195.
2) Griffin AM, Butow PN, Coates AS, et al. On the receiving end V: patient perceptions of the side effects of cancer chemotherapy in 1993. Ann Oncol. 1996;7(2):189-195.
3) Osaba D, Zee B, Warr D, Kaizer L, Latreille J, Pater J. Quality of life studies in chemotherapy-induced emesis. Oncology. 1996;53(suppl 1):92-95.
4) Morrow GR, Roscoe JA, Kirshner JJ, Hynes HE, Rosenbluth RJ. Anticipatory nausea and vomiting in the era of 5-HT3 antiemetics. Support Care Cancer. 1998;6:244-247.
5) Bilgrami S, Fallon BG. Chemotherapy-induced nausea and vomiting. Postgrad Med. 1993;94(5):55-58, 62-64.
6) Адаптировано из 1 — Berger AM, Clark-Snow RA. In Cancer: Principles and Practice of Oncology. 7th ed. Philadelphia: Lippincott Williams & Wilkins, 2004:2515–2523; Antiemetic Subcommittee Ann Oncol 1998;9:811–819.
7) J.D. Hainsworth “Nausea and vomiting”, Abeloff’s Clinical Oncology (Fifth Edition), 2014, 626-634
https://www.sciencedirect.com/science/article/pii/B9781455728657000424
9) Roila F et al. 2016 MASCC and ESMO guideline update for the prevention of chemotherapy and radiotherapy induced nausea and vomiting and of nausea and vomiting in advanced cancer patients. Clinical practice guidelines. Annals of Oncology 27: v 119-133, 2016.
10) Antiemetic guidelines: MASCC/ESMO 2016 http://www.mascc.org/assets/Guidelines-Tools/mascc_antiemetic_guidelines_english_2016_v.1.2.pdf
11) NCCN Clinical Practice Guidelines in Oncology. Antiemesis. Version 2.2017 – March 2018, 2017
12) https://www.nccn.org/professionals/physician_gls/pdf/antiemesis.pdf
13) P. Hesketh, M. G. Kris, et al. “Antiemetics: American Society of Clinical Oncology Clinical Practice Guideline Update”. Journal of Clinical Oncology. Volume 35 (28), October 1, 2017 http://ascopubs.org/doi/pdfdirect/10.1200/JCO.2017.74.4789
- 1) NCCN Clinical Practice Guidelines in Oncology: head and neck. Available at Accessed March 2011;
Информация
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ВНЕДРЕНИЯ ПРОТОКОЛА
Список разработчиков протокола с указанием квалификационных данных:
- Кайбаров Мурат Ендалович — кандидат медицинских наук, Руководитель Центра Опухолей Головы и Шеи АО «Казахский научно – исследовательский институт онкологии и радиологии».
- Адильбаев Галым Базенович – доктор медицинских наук, профессор Центра опухолей головы и шеи. АО «Казахский научно – исследовательский институт онкологии и радиологии».
- Кыдырбаева Гульжан Жанузаковна — кандидат медицинских наук. Старший научный сотрудник Центра Опухолей Головы и Шеи АО «Казахский научно – исследовательский институт онкологии и радиологии».
- Ахметов Данияр Нуртасович — кандидат медицинских наук. врач Центра Опухолей Головы и Шеи АО «Казахский научно – исследовательский институт онкологии и радиологии».
- Ким Георгий Григорьевич — врач Центра Опухолей Головы и .еи АО «Казахский научно – исследовательский институт онкологии и радиологии».
- Савхатова Акмарал Досполовна – кандидат медицинских наук, заведующая отделением дневного стационара лучевой терапии АО «Казахский научно – исследовательский институт онкологии и радиологии».
- Медетбекова Эльмира Пердалыевна – врач-химиотерапевт. АО «Казахский научно – исследовательский институт онкологии и радиологии».
- Бабажанова Анар Бейбитовна — клинический фармаколог ООД Мангыстауской области.
Указание на отсутствие конфликта интересов: нет.
Рецензенты:
- Савхатов Д.Х — доктор медицинских наук, доцент кафедры «Онкология» КазНМУ им. Асфендиярова.
- Есентаева С.Е — доктор медицинских наук, заведующий курсом онкологии, маммологии КРМУ.
Указание условий пересмотра протокола: пересмотр протокола через 3 года после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Приложение №1
СОПРОВОДИТЕЛЬНАЯ ТЕРАПИЯ
Антиэметическая терапия
Тошнота и рвота являются одним из наиболее частых побочных эффектов химио- терапии (ХТ) и существенно ухудшают качество жизни больных.
Тошнота и рвота, сопутствующие химиотерапии, относятся к числу наиболее неприятных аспектов этого вида лечения (1,2). Не будучи самым серьезным побочным эффектом химиотерапии, рвота, тем не менее, сильно ухудшает качество жизни и снижает ощущение благополучия (1,3). В некоторых случаях пациенты откладывают или полностью прекращают химиотерапию из-за непереносимой тошноты и рвоты (1).
Кроме того, рвота, как таковая, может представлять угрозу здоровью, поскольку неконтролируемая рвота приводит к обезвоживанию, нарушению баланса метаболитов и к анорексии (4,5).
Факторы, связанные с терапией:
Высокая эметогенная способность некоторых препаратов,
Комбинированная терапия
Режим и способ введения препаратов
Высокие дозы химиотерапевтических препаратов (6).
Под уровнем эметогенности понимается риск развития рвоты у больных, получающих тот или иной цитостатик в монорежиме без противорвотной терапии. Например, высокий уровень эметогенности означает, что после введения препарата рвота будет развиваться более чем у 90 % больных. Классификация противоопухолевых препаратов в зависимости от уровня эметогенности по рекомендациям MASCC / ESMO представлена в табл. 1.
Таблица 1. Классификация противоопухолевых препаратов в зависимости от уровня эметогенности по рекомендациям MASCC / ESMO.
| Уровень эметогенности | Противоопухолевые препараты для внутривенного введения | Противоопухолевые препараты для приема per os |
| Высокий (рвота у 90 % больных и более) |
Цисплатин Мехлорэтамин Стрептозоцин Циклофосфан ≥ 1500 мг / м2 Кармустин (BCNU) Дакарбазин |
Гексаметилмеламин Прокарбазин |
|
Схема «АС»: • эпирубицин 100 мг / м2 или • доксорубицин 60 мг / м2 + – циклофосфамид 600 мг / м2 . 2) Режимы на основе карбоплатина |
||
| Умеренный (рвота у 30–90 % больных) |
Оксалиплатин Цитарабин > 1 г / м2 Карбоплатин Ифосфамид Циклофосфамид < 1500 мг / м2 Доксорубицин Даунорубицин Эпирубицин Идарубицин Иринотекан Азацитидин Бендамустиин Клофарабин Алемтузумаб Трабектидин Ромидепсин Тиотепа |
Циклофосфамид Темозоломид Винорельбин Иматиниб Кризотиниб Церитиниб Босутиниб |
| Низкий (рвота у 10–30 %) |
(Nab-) Паклитаксел Доцетаксел Митоксантрон Доксорубицин липосомальный Иксабепилон Топотекан Этопозид Пеметрексед Метотрексат Митомицин Гемцитабин Цитарабин ≤ 1000 мг / м2 5-фторурацил Винфлунин Темсиролимус Бортезомиб Цетуксимаб Трастузумаб(-эмтанзин) Панитумумаб Катумаксумаб Пертузумаб Афлиберцепт Ипилимумаб |
Капецитабин Тегафур Флюдарабин Этопозид Сунитиниб Эверолимус Лапатиниб Леналидомид Талидомид Афатиниб Дабрафениб Дазатиниб Ибрутиниб Олапариб Нилотиниб Пвзопаниб Регорафениб Вандетаниб Вариностат |
| Минимальный (< 10 % больных) |
Блеомицин Бусульфан 2-хлордеоксиаденозин Флюдарабин Винбластин Винкристин Винорельбин Бевацизумаб Офатумумаб Ниволумаб Пембролизумаб Пискантрон Пралатрексат |
Хлорамбуцил Гидроксиуреа L-фенилаланин мустард 6-тиогуанин Метотрексат Гефитиниб Эрлотиниб Сорафениб Мелфалан Вемурафениб Помалидомид Руксолитинб Висмодегиб |
ТИПЫ ТОШНОТЫ И РВОТЫ
По срокам и механизму развития выделяют 3 основных типа тошноты и рвоты, вызванной цитостатиками: острую, отсроченную и условно-рефлекторную (anticipatory – переводят также как «предшествующую», «преждевременную», «рвоту ожидания»), дополнительно выделяют неконтролируемую (breakthrough – «прорывную») и рефрактерную (7, 8).
Острая рвота развивается в первые 24 ч после химиотерапии, отличается высокой интенсивностью, редко сопровождается тошнотой.
Отсроченная рвота развивается на 2-е–5-е сутки после начала химиотерапии, менее интенсивна, чем острая, и, как правило, сопровождается постоянной тошнотой. Механизмы развития остаются неясными. Ведущая роль отводится субстанции P, серотонин имеет меньшее значение.
Условно-рефлекторная рвота представляет собой классический условный рефлекс на химиотерапию и / или сопутствующие ей манипуляции и окружающую обстановку. Формируется в тех случаях, когда противоопухолевая терапия сопровождается тошнотой и рвотой. Риск ее развития увеличивается пропорционально числу проведенных курсов и может сохраняться в течение длительного времени после окончания химиотерапии. Ведущую роль в формировании условного рефлекса играет многодневная умеренная или тяжелая тошнота. Лучшим методом профилактики условно-рефлекторной тошноты и рвоты является адекватная антиэметическая защита пациента уже с первого курса химиотерапии.
Неконтролируемая (breakthrough – «прорывная») тошнота и рвота развивается на фоне адекватной антиэметической профилактики и требует дополнительной коррекции. Рефрактерная рвота возникает на последующих циклах химиотерапии при неэффективности противорвотной профилактики и / или препаратов резерва на предыдущих курсах лечения.
ПРИНЦИПЫ СОВРЕМЕННОЙ ПРОТИВОРВОТНОЙ ТЕРАПИИ
1. Обязательность проведения, начиная с первого курса химиотерапии.
2. Введение антиэметиков до начала введения первого цитостатика.
3. Применение наиболее эффективных стандартных противорвотных комбинаций.
4. Применение каждого антиэметика, входящего в комбинацию, в адекватных дозах.
5. Соблюдение адекватной продолжительности противорвотной терапии.
6. Соблюдение необходимых для сохранения эффективной концентрации интервалов между приемами антиэметиков.
Критерием эффективности противорвотной терапии является полное отсутствие (полный контроль) рвоты и тошноты в течение 24 часов (период развития острой рвоты) с момента введения противоопухолевых препаратов.
Алгоритм профилактики и терапии тошноты и рвоты
1. Определить эметогенный потенциал назначенного режима ХТ.
2. Назначить профилактическую терапию, исходя из эметогенности режима ХТ.
3. Назначить лечение в случае развития тошноты и рвоты на фоне профилактической терапии.
4. Внести изменения в профилактическую терапию тошноты / рвоты на последующих циклах ХТ.
Антиэметики:
I. Антагонисты серотониновых рецепторов (5-HT3):
- Ондансетрон
- Гранисетрон
- Трописетрон
- Палоносетрон
II. Кортикостероиды: Дексаметазон
III. Антагонисты рецепторов NK1 :
- Апрепитант
- Фосапрепитант
- Ролапитант
- Нетупитант
IV. Антипсихотическое средство (нейролептик):
- Оланзапин (проявляет антагонизм в отношении серотониновых 5-НТ-, допаминовых и холинорецепторов).
Профилактика острой и отсроченной тошноты и рвоты при высокоэметогенной однодневной химиотерапии и при умеренно эметогенной однодневной химиотерапии.
В настоящее время наиболее эффективной антиэметической комбинацией при высокоэметогенной однодневной химиотерапии является комбинация противорвотных препаратов, включающая антагонистов NK1-рецепторов + антагонистов рецепторов серотонина (5-HT3) + дексаметазон.
Профилактика тошноты и рвоты, возникающей при проведении химиотерапии с умеренно эметогенным потенциалом, должна начинаться до начала химиотерапии и проводиться не менее 3 дней после проведения химиотерапии. Наиболее эффективной антиэметической комбинацией является комбинация противорвотных препаратов, включающая антагонистов рецепторов серотонина (5-HT3) + дексаметазон (табл 2,3) (9, 10).
Таблица 2. Обновленные рекомендации MASCC/ESMO 2016 ТРВХ.
Острая тошнота и рвота.
| Группы эметогенного риска | Антиэметики |
| Высокий (не АС) | 5-НТ3 + DEX + NK 1 |
| Высокий (АС) | 5-НТ3 + DEX + NK 1 |
| Карбоплатин | 5-НТ3 + DEX + NK 1 |
| Умеренный (кроме карбоплатина) | 5-НТ3 + DEX |
| Низкий | 5-НТ3 или DEX или DOP |
| Минимальный | Нет рутинной профилактики |
ТРВХ – тошноты и рвота, вызванная химиотерапией
MASCC — Multinational Association of Supportive Care in Cancer; ESMO – European Society for Medical Oncology
5-НТ3 — антогонисты серотиновых рецепторов
DEX — дексаметазон
NK 1 — антагонисты рецепторов нейрокинина такие как Апрепитант или
Фосапрепитант или
Ролапитант или NEPA (комбинация нетупитант и палоносетрон).
DOP — антогонист допаминовых рецепторов
ВНИМАНИЕ: Если антагонисты NK1 рецепторов недоступны при использовании схемы AC, палоносетрон является предпочтительным антагонистом 5-НТ3 рецепторов.
Таблица 3. Обновленные рекомендации MASCC/ESMO 2016 ТРВХ.
Отсроченная тошнота и рвота.
| Группы эметогенного риска | Антиэметики |
| Высокий (не АС) | DEX или (если APR 125мг для острой: (МСР+DEX) или (DEX+APR) |
| Высокий (АС) | Нет или (если APR 125мг для острой: APR+DEX) |
| Карбоплатин | Нет или (если APR 125мг для острой: APR) |
| Средний (не карбоплатин) | DEX можно использовать |
| Низкий | Профилактика не предусмотрена |
| Минимальный | Профилактика не предусмотрена |
DEX — дексаметазон
APR — апрепитант
MCP — метоклопромид
Ключевые обновления в рекомендациях по контролю ТРВХ, NCCN 2017:
Карбоплатин категоризируется как высокоэметогенный препарат при введении с площадью под кривой (ППК) ≥4, при введении с ППК <4, является умеренноэметогенным препаратом.
Инъекция подкожного гранисетрона пролонгированного действия теперь включена в рекомендации по профилактике тошноты и рвоты при высокоэмегоненной и умеренноэметогенной ХТ.
Новая схема профилактики ТРВХ из четырех препаратов теперь включена в рекомендации по профилактике ТРВХ при высокоэметогенной ХТ (11, 12).
Ключевые обновления в рекомендациях по контролю ТРВХ, ASCO 2017:
Взрослым пациентам, получающим высокоэметогенную химиотерапию цисплатином, либо комбиницией циклофосфамидов и антрациклина, к стандартному антиэметическому режиму (комбинация антагонистов рецепторов 5-НТ3 + антагонисты рецепторов NK1 + dex) следует добавить оланзапин.
Взрослым пациентам, получающим карбоплатин содержащую химиотерапию, а также детям, получающим высокоэметогенную химиотерапию, антагонисты рецепторов NK1 должны быть добавлены к стандартному антиэметическому режиму (комбинация антагонистов рецепторов 5-НТ3 + dex).
Если пациенты получают комбинацию антрациклина и циклофосфамида, прием дексаметазона можно ограничить с первым днем химиотерапии.
Экспертная комиссия рекомендует начинать антиэметическую терапию с самой эффективной схемы, подходящей к химио- и радиотерапии, вместо того чтобы оценивать эметический ответ пациента на менее эффективную антиэметическую терапию (13).
Таблица 4. Обновленные рекомендации ASCO 2017.
Взрослые пациенты.
| Группы эметогенного риска | Антиэметики |
| Высокий (не АС) | 5-НТ3 + DEX* + NK 1+Olanzapine* |
| Высокий (АС) | 5-НТ3 + DEX* + NK 1+Olanzapine* |
| Карбоплатин | 5-НТ3 + DEX + NK 1 |
| Умеренный (кроме карбоплатина) | 5-НТ3 + DEX |
| Низкий | 5-НТ3 или DEX или DOP |
| Минимальный | Нет рутинной профилактики |
* — дексаметазон и оланзапин нужно продолжать на 2-4 день
Таблица 5. Рекомендуемые дозы антогонистов серотониновых рецепторов (5-НТ) для острой тошноты и рвоты.
| Препарат | Путь введения | Доза |
| Ондансетрон | в/в | 8мг или 0,15мг/кг |
| пероральный | 16мг* | |
| Гранисетрон | в/в | 1мг или 0,01мг/кг |
| пероральный | 2мг (или 1мг**) | |
| Трописетрон | в/в | 5мг |
| пероральный | 5мг | |
| Палоносетрон | в/в | 0,25мг |
| пероральный | 0,5мг |
* В рандомизированных исследованиях был протестирован режим 8 мг два раза в день.
** Некоторыми панелистами доза 1 мг более предпочтительна
Таблица 6. Рекомендуемые дозы кортикостероидов (дексаметазон)*
| Дексаметазон | Дозы и Кратность | |
| Высокий риск | Острая рвота | 20мг однократно (12мг когда используется апрепитант или нетупитант) )** |
| Отсроченная рвота | 8мг в течение 3-4 дней (8мг один раз в день когда используется апрепитант или нетупитант ) | |
| Умеренный риск | Острая рвота | 8 мг однократно |
| Отсроченная рвота |
8 мг ежедневно в течение 2-3 дней |
|
| Низкий риск | Острая рвота | 4-8 мг один раз в день |
* Несмотря на то, что другие кортикостероиды также являются эффективными антиэметиками, режим дозирования для дексаметазона, как препарата выбора, основан на широком распространении препарата, с несколькими формами дозирования
** Только 12 мг дексаметазона было исследовано с (фос) апрепитантами/нетупитантами в рандомизированных исследованиях
Таблица 7. Рекомендуемые дозы антагонистов NK1 рецепторов.
| Антагонисты NK1 Рецепторов | Дозы и кратность |
|
Апрепитант* и фосапрепитант острая рвота |
Апрепитант 125мг внутрь однократно в день химиотерапии* -или- Фосапрепитант 150 в/в, однократно в день химиотерапии |
|
Апрепитант* и фосапрепитант отсроченная рвота |
Апрепитант 80мг внутрь однократно в течении 2-х дней после химиотерапии |
| Ролапитант | 180мг внутрь однократно в день химиотерапии |
| Нетупитант | 300 мг нетупитант / 0,5 мг палоносетрон перорально один раз в день химиотерапии |
* Апрепитант 165 мг, одна доза перед химиотерапией (не применяется на 2-3 день). Рекомендовано ЕМА и другими органами.
Рекомендации по профилактики преждевременной тошноты и рвоты
Наилучший подход для профилактики преждевременной рвоты это наилучший контроль над острой и отсроченной рвотой.
Психотерапия, особенно прогрессивное обучение мышечной релаксации, систематическая десенситизация и гипноз, могут быть использованы для лечения преждевременной тошноты и рвоты.
Только бензодиазепины уменьшают частоту преждевременной тошноты и рвоты, но их эффективность имеет тенденцию к снижению при продолжающейся химиотерапии.
Колониестимулирующая терапия:
Целесообразность назначения Г-КСФ для стимуляции кроветворения и преодоления миелосупрессии при фебрильной нейтропении (ФН) изучалась в нескольких рандомизированных исследованиях. На основании имеющихся данных сделаны следующие выводы относительно роли Г-КСФ в период ФН:
- Г-КСФ статистически значимо снижает длительность нейтропении на 1–2 дня;
- Г-КСФ не сокращает продолжительность лихорадки и длительность антибактериальной (АБ) терапии в случае развития ФН;
- Г-КСФ не снижает стоимости лечения одного эпизода ФН.
Г-КСФ могут применяться в случае высокого риска ФН при состояниях, сопровождающихся повышенной смертностью, таких как гипотония, сепсис, пневмония, инфекции тканей, системная грибковая инфекция, длительная нейтропении (>7 дней) или глубокой нейтропении.
Большинство медицинских онкологических сообществ (NCCN, ASCO, EORTC, RUSSCO) рекомендуют использовать следующие Г-КСФ: липэгфилграстим, эмпэгфилграстим, пэгфилграстим (филграстим, соединенный с полиэтиленгликолем), филграстим (негликозилированный Г-КСФ), ленограстим (гликозилированный Г-КСФ). Липэгфилграстим, эмпэгфилграстим и пэгфилграстим представляют собой препараты пролонгированного действия и вводятся однократно после курса ХТ. Пролонгированное действие обусловлено тем, что препарат не выводится с мочой и дольше циркулирует в крови.
| МНН | Группа КСФ | Режим введения |
| Филграстим | Рекомбинантный человеческий негликолизированный Г-КСФ | 5 мкг/кг массы тела 1 раз/сут. п/к или в/в ежедневно через 24–72 часа после последнего дня ХТ до необходимого стабильного АЧН |
| Пэгфилграстим | Рекомбинантный пегилированный Г-КСФ (филграстим), конъюгированный с полиэтиленгликолем, пролонгированного действия | 6 мг (без учета массы тела) однократно п/к не ранее чем через 24 часа и не позднее 14-ых сут. после курса ХТ |
| Липэгфилграстим | Гликопегилированный Г-КСФ пролонгированного действия | 100 мкг/кг или 6 мг (без учета массы тела) п/к однократно через 24 ч после окончания цикла ХТ |
| Эмпэгфилграстим | Ковалентный коньюгат филграстима с одной молекулой полиэтиленгликоля, пролонгированного действия | 7,5 мг (без учета массы тела) п/к однократно не ранее чем через 24 часа и не позднее 14-ых сут. после курса ХТ |
| Ленограстим | Рекомбинантный человеческий гликолизированный Г-КСФ | 19,2 млн. МЕ (или 150 мкг) на м² поверхности тела (0,64 млн. МЕ или 5 мкг на кг массы тела) в день п/к или в/в ежедневно через 24–72 часа после последнего дня ХТ до достижения необходимого стабильного АЧН |
Показания для назначения колониестимулирующих факторов
| Первичная профилактика | Вторичная профилактика |
|
|
|
!!! Первичная профилактика Г-КСФ не показана во время ХЛТ на область грудной клетки, так как увеличивает частоту миелосупрессии и риск осложнений и смерти. |
Коррекция анемии:
Анемия при новообразованиях (В63.0 код по МКБ 10) определяется как снижение концентрации Hb ниже нормального значения (обычно 120 г/л) и может быть обусловлена как наличием самой опухоли, так и ее лечением. Слабая степень анемии представляет собой снижение концентрации Hb в диапазоне от 100 до 119 г/л, анемия средней степени – концентрация Hb от 80 до 99 г/л, тяжелая анемия – концентрация Hb ниже 80 г/л.
Препараты рекомендованные для лечения анемии у онкологических больных
| Группа препарата | Препарат, рекомендованная доза |
| Эритропоэзстимулирующие препараты |
Эпоэтин альфа 150 МЕ/кг × 3 раза в нед. п/к 12 000 МЕ × 3 раза в нед. п/к 40 000 МЕ × 1 раз в нед. п/к |
| Эпоэтин бета 30 000 МЕ × 1 раз в нед. п/к | |
| Эпоэтин тета 20 000 МЕ × 1 раз в нед. п/к | |
|
Дарбэпоэтин альфа 2,25 мкг/кг × 1 раз в нед. п/к 500 мкг × 1 раз в 3 нед. п/к |
|
| Препараты железа |
Железа [III] гидроксид сахарозный комплекс 200 мг × 3 раза в нед. в/в струйно 7 мг железа/кг массы тела, в однократной дозе не более 500 мг железа, в/в инфузия не менее 3,5 часов |
|
Железа карбоксимальтозат 200 мг железа × 3 раза в нед. в/в струйно 20 мг максимального железа/кг массы тела в однократной дозе не более 1000 мг, в/в капельно не менее 15 мин. |
|
|
Железа [III] гидроксид декстран 100–200 мг × 2–3 раза в нед. в/в струйно 20 мг/кг железа в/в инфузия 4–6 часов |
|
| Витамины | Цианкобаламин (Витамин В12) 0,5 мг/мл – 1,0 мл, п/к через день |
| Фолиевая кислота 2 мг/сут. внутрь |
Прикреплённые файлы
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
Дата публикации 3 октября 2022Обновлено 5 октября 2022
Определение болезни. Причины заболевания
Рак гортани (laryngeal cancer) — это злокачественная опухоль, которая развивается из эпителия гортани, в частности из слизистой оболочки гортани.
Гортань относится к верхнему отделу дыхательной системы. Соединяя глотку с трахеей, она формирует голос и защищает нижележащие дыхательные пути (трахею и лёгкие) от попадания пищи и инородных тел.
Анатомически гортань делится на три отдела:
- надскладочный (выше голосовых связок);
- складочный (на уровне голосовых складок);
- подскладочный (ниже голосовых связок).
Рак чаще развивается в складочном отделе гортани.
Основной симптом рака гортани — нарушение голоса, а именно снижение звучности и осиплость. Также могут беспокоить боли в горле, попёрхивание водой и пищей, сухой беспричинный кашель, одышка. Иногда именно одышка становится первым признаком заболевания, особенно при раке подскладочного отдела гортани.
При возникновении этих симптомов нужно обратиться к ЛОРу. Если у врача появится подозрение на рак гортани, к диагностике подключится ЛОР-онколог онкологического диспансера. Лечением этого заболевания занимаются хирурги-онкологи со специализацией в области головы и шеи, радиологи и химиотерапевты.
Факторы риска развития рака гортани
Внешние факторы:
- Курение.
- Употребление спиртного.
- Вредные условия труда, например содержание в воздухе канцерогенов (фенола, асбеста, бензола и т. д.).
- Воздействие радиации.
Внутренние факторы:
- Хронические воспалительные процессы в гортани (например, ларингит).
- Предраковые заболевания гортани, их можно разделить на две группы:
- факультативные предраки с низкой частотой перерождения в рак: доброкачественные опухоли (фиброма), рубцовые процессы после ожогов и специфических инфекций (сифилиса, туберкулёза);
- облигатные предраки с высокой частотой перерождения в рак: папилломатоз гортани, пахидермия, лейкоплакия, дискератоз [2][13].
В группу повышенного риска входят курящие люди старше 50 лет, имеющие профессиональные вредности и предраковые процессы в гортани. Такие пациенты должны наблюдаться у онколога и обязательно пролечивать предраковые заболевания.
Распространённость
У мужчин рак гортани встречается чаще, чем у женщин. В России в 2021 году выявлено 29,2 случаев рака гортани на 100 тыс. населения. Среди них:
- локализованные формы опухоли гортани I и II стадии выявлены у 41 % пациентов;
- распространённые формы III стадии — у 32,9 %, IV стадии — у 25,1 %.
В этом же году летальность в течение первого года с момента установления диагноза составила 21,8 % [1].
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы рака гортани
Жалобы пациентов при раке гортани зависят от расположения опухоли.
При раке складочного отдела, т. е. непосредственно на голосовых связках, основным симптомом будет осиплость и изменение тембра голоса. Это связано с тем, что опухоль нарушает смыкание голосовых связок.
При раке надскладочного отдела, т. е. в области черпало-надгортанных складок и надгортанника, ведущим симптомом будет боль в горле и попёрхивание при приёме жидкой пищи. Боль возникает из-за того, что опухоль повреждает чувствительные верхнегортанные нервы, расположенные в этой зоне. Попёрхивание во время еды объясняется поражением надгортанника. В норме он выполняет защитную функцию — закрывает вход в гортань во время глотания и тем самым препятствует попаданию пищи в дыхательные пути. Из-за опухоли вход в гортань не будет нормально закрываться.
Рак подскладочного отдела на начальных стадиях часто протекает бессимптомно. Далее пациенты, как правило, жалуются на одышку и нехватку воздуха [3][7]. Одышка появляется при распространённом опухолевом процессе, когда опухоль увеличивается и блокирует дыхательные пути, из-за этого пациенту становится трудно дышать.
Также при раке гортани может отмечаться кашель, кровохарканье, увеличение шейных лимфоузлов из-за метастазов. В первую очередь страдают лимфоузлы глубокой ярёмной цепи, которые расположены под кивательной мышцей.
Патогенез рака гортани
Есть множество теорий развития злокачественного процесса: вирусная, молекулярно-генетическая, теория влияния факторов внешней среды, наследственная теория и др.
В 21 веке произошли революционные перемены в понимании механизмов развития рака. Расшифрован геном клеток при раке различных локализаций, выявлены гены-индукторы, которые провоцируют опухолевый рост, и гены-супрессоры, которые его подавляют.
Нашла подтверждение вирусная теория развития опухолей, выдвинутая Л. А. Зильбером в 40-х годах 20 века. В 60-х был открыт вирус лимфомы Беркита, вызывающий лимфому. Потом учёные обнаружили и другие вирусы, вызывающие онкологические заболевания:
- вирус герпеса 8-го типа — может стать причиной саркомы Капоши;
- вирус папилломы человека (ВПЧ) — может вызывать рак шейки матки и ротоглотки;
- вирус гепатита С — становится причиной опухоли печени;
- вирус Т-клеточного лейкоза взрослых — может вызвать одноимённую болезнь.
Встраиваясь в геном клетки, вирусы изменяют генетическую программу клетки-хозяина, что приводит к развитию злокачественных опухолей. Считается, что около 20–35 % всех опухолей человека ассоциировано с вирусами [16].
Генетические поломки в клетках могут также происходить под воздействием различных факторов: внешних (ионизирующего излучения, курения, химических агентов и т. п.) и внутренних (наследственной предрасположенности, имеющихся аномалий развития, заложенных во внутриутробном периоде).
Когда генетические поломки накапливаются, клетки начинают бесконтрольно делиться, потому что организм перестаёт распознавать и уничтожать изменённые клетки из-за нарушений в иммунной системе, которая и должна убивать клетки-мутанты. Из этих быстроделящихся клеток образуется опухоль. Впоследствии она проникает через базальную мембрану эпителия, т. е. происходит опухолевая инвазия (проникновение в глубжележащие слои тканей). Затем опухолевые клетки с током крови и лимфы перемещаются в другие ткани и органы, т. е. опухоль даёт метастазы.
Классификация и стадии развития рака гортани
Классификация рака гортани, как и других злокачественных опухолей, проводится по системе TNM. С 2017 года во всём мире используется 8-е издание этой классификации [4].
Символ Т (tumor — опухоль) оценивает саму первичную опухоль в гортани. Выделяют такие стадии:
- Тх — первичная опухоль не может быть оценена.
- Tis — карцинома in situ (начальноинвазивная).
Далее градации символа Т распределяются от Т1 до Т4 в зависимости от поражения определённых анатомических частей гортани. Т1 — это наименее распространённый процесс, Т4 — запущенный местно-распространённый вариант.
Символ N (nodulus — лимфоузлы) — описывает поражение метастазами регионарных лимфоузлов (регионарными для гортани являются лимфоузлы шеи). Лимфоузлы поражаются из-за распространения опухолевых клеток по лимфатической системе. В классификации выделены следующие стадии:
- Nx — недостаточно данных для оценки состояния регионарных лимфоузлов.
- N0 — нет признаков метастатического поражения регионарных лимфоузлов.
- N1–N3в — есть метастазы в лимфоузлы шеи разной степени выраженности.
Символ М (methastasis — метастазы) характеризует отдалённые метастазы. Они возникают, когда опухолевые клетки с током крови проникают в отдалённые органы и ткани. Выделяют две стадии:
- М0 — отдалённых метастазов нет.
- М1 — имеются отдалённые метастазы.
После оценки градации каждого символа определяют общую стадию распространения злокачественной опухоли. Существует четыре основных стадии рака, которые обозначают римскими цифрами от I до IV, где стадии I и II считаются местно-распространёнными и лучше поддаются лечению, а III и IV считаются широко распространёнными и имеют худший прогноз.
Осложнения рака гортани
Осложнения рака гортани можно разделить на две группы:
- местные — связаны с изменениями, происходящим непосредственно в опухолевой ткани;
- общие — связаны с влиянием злокачественной опухоли на организм в целом.
Местные осложнения
Кровотечение из сосудов, повреждённых опухолью. Проявляется примесью крови в мокроте при кашле. Кровь обычно алая, её немного. Сильные кровотечения возникают при запущенных стадиях опухолевого процесса и требуют срочной медицинской помощи.
Некроз (отмирание) опухоли с присоединением вторичной инфекции. При этом осложнении появляется зловонный запах изо рта, пациенты могут выкашливать нежизнеспособные участки, которые отрываются от опухоли, возможно повышение температуры тела. При некрозе и вторичной инфекции проводится лечение основного заболевания, иногда назначаются антибиотики.
Удушье вплоть до асфиксии. Большие опухоли в гортани могут существенно сужать просвет верхних дыхательных путей. Это вызывает чувство нехватки воздуха, одышку, которая сначала появляется при физической нагрузке, а потом и в покое. Иногда опухоль полностью перекрывает дыхательные пути, в этом случае развивается асфиксия. Это очень грозное осложнение рака гортани, которое требует срочной медицинской помощи.
Как правило, сужение просвета гортани и связанное с этим затруднение дыхания встречается при запущенных стадиях рака. В таких случаях речь идёт о спасении жизни пациента путём трахеостомии и удаления гортани [5]. Трахеостомия — это операция, при которой ниже опухоли в трахее делают отверстие, куда вводят специальную трубку (трахеостому). Через эту трубку воздух в обход гортани попадает сразу в трахею и лёгкие, и за счёт этого пациент может дышать.
Если есть вероятность восстановить проходимость дыхательных путей, то трахеостому устанавливают временно, но чаще всего трубка остаётся пожизненно, так как выше неё находится опухоль, блокирующая дыхание через естественные пути. Иногда рак гортани диагностируется только после наложения трахеостомы и пациента направляют к онкологу. Но в таких случаях, как правило, процесс в гортани уже носит распространённый характер.
Общие осложнения
К общим осложнениям рака гортани, относится анемия, кахексия (крайнее истощение организма), нарушение в работе сердца, печени, почек и других жизненно важных органов из-за токсического воздействия злокачественной опухоли. Отдалённые метастазы при раке гортани встречаются редко, чаще всего в лёгких [15]. Симптомы при этом могут быть разными: от немого поражения (отсутствие дыхания над каким-либо отделом лёгкого) до пневмонии и дыхательной недостаточности.
Диагностика рака гортани
Сбор анамнеза и осмотр
Диагностика начинается с беседы, в ходе которой нужно рассказать врачу о жалобах и имеющихся хронических заболеваниях. Документы с информацией о сопутствующих заболеваниях, проводимом обследовании и лечении можно показать врачу напрямую или открыть доступ к своей электронной медкарте.
После этого врач проводит осмотр. Сначала осматривает горло специальным гортанным зеркалом (ларингоскопия) или гибким эндоскопом с камерой (фиброларингоскопия). Затем обследует и прощупывает шею, так как именно на шее находятся пути лимфооттока от гортани, а значит, именно здесь могут возникнуть регионарные метастазы.
Биопсия опухоли и лимфозулов
Если в ходе осмотра в гортани выявляется новообразование, то проводят биопсию — берут образец ткани опухоли. Биопсию часто выполняют в ходе фиброларингоскопии под местной анестезией амбулаторно, т. е. без госпитализации. Если не удаётся сделать процедуру под местной анестезией, биопсию делают при прямой ларингоскопии под наркозом. В этом случае пациента госпитализируют.
Иногда проводят пункцию или биопсию шейных лимфоузлов, чтобы проверить, нет ли в них метастазов. Часто процедуру выполняют под контролем ультразвукового исследования (УЗИ).
Гистологическое исследование
Материал опухоли, полученный при биопсии, исследуют под микроскопом и ставят точный гистологический диагноз, что позволяет врачу рассматривать специализированное противоопухолевое лечение.
Дополнительные инструментальные методы обследования
- УЗИ шеи и брюшной полости — позволяет исключить метастазы в лимфоузлах шеи и органах брюшной полости.
- КТ или МРТ шеи — помогает оценить распространённость опухоли.
- КТ лёгких — позволяет оценить их возможное поражение.
- ПЭТ-КТ всего тела по показаниям — чаще применяют для наблюдения за рецидивами и при подозрении на метастатический процесс [2].
Дифференциальную диагностику рака гортани проводят с туберкулёзом гортани, хроническим ларингитом, папилломатозом и доброкачественными новообразованиями.
Лечение рака гортани
При лечении злокачественных новобразований используются три основных метода: хирургический, химиотерапевтический и лучевой.
Хирургический метод лечения
Объём операции подбирается строго индивидуально. В начальных стадиях заболевания (Т1 и Т2) выбор будет в пользу операций с сохранением голоса, таких как эндоларингеальная лазерная резекция гортани, эндоскопическая резекция гортани, открытая частичная резекция гортани [8][12]. Эндоларингеальные вмешательства не требуют наружных разрезов, они выполняются через рот при помощи специального оборудования.
При распространённом опухолевом процессе (стадии Т3 и Т4) выбирают ларингэктомию, т. е. полное удаление гортани [10][13].
При запущенных опухолях гортани с наличием метастазов на шее, кроме ларингэктомии или резекции гортани выполняются шейные лимфодиссекции (удаление поражённых лимфоузлов). Радикальная шейная диссекция, известная также как операция Крайля, подразумевает удаление кивательной мышцы и внутренней ярёмной вены вместе с метастазами, врастающими в эти структуры. В последнее время предпочтение отдаётся более щадящим модифицированным шейным лимфодиссекциям, при которых сохраняются важные анатомические структуры. Но такие методики применяются только в том случае, если с их помощью опухолевые ткани можно удалить полностью.
Осложнения после операции. После хирургических вмешательств возможны местные и общие осложнения. Местные встречаются в 15–25 % случаев. К ним относят: формирование глоточных свищей, кровотечение, расхождение швов и т. д. Общие осложнения, такие как острое нарушение мозгового кровообращения (ОНМК), ТЭЛА, инфаркт миокарда и другие, встречаются редко.
После удаления гортани нос и рот больше не будут соединены с трахеей, поэтому дышать через рот и нос будет невозможно. Чтобы пациент после операции мог дышать, во время ларингэктомии накладывают пожизненную трахеостому. Голос после операции утрачивается, однако голосовую функцию можно вернуть.
Как восстановить голос после удаления гортани. Для этого есть несколько методов голосовой реабилитации: пищеводный голос, электрогортань и голосовое протезирование путём трахеопищеводного шунтирования.
Пищеводный голос — это метод, при котором для произношения нужно заглатывать воздух, а не выдыхать, как при нормальных условиях. Этой технике обучает логопед. Однако выработать пищеводный голос получается далеко не у всех пациентов.
Электрогортань — это портативное устройство на батарейках, которое прикладывается к подбородку или шее и преобразует колебания мышц в голос с помощью специальной мембраны [5][9]. Минус такого голоса — его монотонность и схожесть с электронным голосом робота.
Голосовое протезирование — современная технология, которая на сегодняшний день является методом выбора в голосовой реабилитации после удаления гортани. Голосовой протез устанавливается в трахеопищеводную стенку сразу при проведении ларингэктомии или отсроченно после операции [5]. Средний срок службы протеза — 1 год, после этого его нужно заменить.
Голосовое протезирование доступно в России бесплатно в рамках квот. Протез на замену тоже выдают бесплатно, если он внесён в индивидуальный пакет реабилитации (ИПР). Замена проводится примерно за 10 минут ЛОР-онкологом, госпитализация для этого не требуется.
Лучевая терапия
Лучевая терапия включает в себя подведение гамма-излучения на область опухоли и регионарных шейных лимфоузлов. На стадиях Т1 и Т2 она может быть самостоятельным методом лечения, на поздних стадиях — этапом комплексного лечения, включающим и химиотерапию, и хирургический этап. При комплексном лечении лучевая терапия проводится либо первым этапом, либо после операции, если опухоль распространённая. Облучение проводится 5 дней в неделю до дозы 60–66 Грей в течение 5–6 недель, обычно выполняется около 30 сеансов по 2 Грея каждый [11].
Осложнения лучевого лечения: воспалительные изменения на коже и слизистых (лучевые эпителииты и мукозиты). Они развиваются почти в 60 % случаев и сохраняются иногда несколько месяцев.
Химиотерапия
Как самостоятельный метод лечения химиотерапия проводится только в запущенных стадиях заболевания или при отказе пациента от хирургического и лучевого лечения. Часто сочетается с лучевой терапией. Для химиотерапии обычно используются препараты платины с 5-фторурацилом. В последнее время в схемы лекарственного лечения также включаются таксаны (Доцетаксел, Таксотер) и таргетные препараты (Эрбитукс) [11].
Осложнения химиотерапии. Препараты токсически действуют на организм в целом. К основным осложнениям относят: ухудшение показателей крови (анемию, уменьшение количества лейкоцитов и тромбоцитов), повреждение печени, почек и сердца. Врачи-химиотерапевты должны следить за состоянием пациента и своевременно корректировать осложнения.
Варианты лечения
Какие методы лечения использовать, в каком сочетании и в какой последовательности, определяет онкологический консилиум в составе трёх специалистов: хирурга-онколога, химиотерапевта и радиолога [4].
Считается, что опухоли выше голосовых связок более чувствительны к химиолучевому лечению, поэтому их лечение чаще начинают с лучевого или химиолучевого метода. Опухоли на уровне голосовых связок и ниже на первом этапе чаще лечат хирургически.
И всё же в каждом конкретном случае решение будет индивидуальным. Его принимают совместно с пациентом, учитывая его пожелания, ведь операция на органах дыхания и голособразования часто означает установку пожизненной трахеостомы и отсутствие голоса в послеоперационном периоде. Однако, если речь идёт о спасении жизни пациента, то врач-онколог примет решение пожертвовать голосом и полностью удалить поражённый орган. Тем более что голос можно будет восстановить [6].
Прогноз. Профилактика
Прогноз рака гортани зависит от стадии и адекватности лечения. При I и II стадиях рака и своевременном правильном лечении прогноз для жизни и работы органа благоприятный. При распространённом опухолевом процессе III и IV стадий, появлении регионарных и отдалённых метастазов прогноз значительно ухудшается.
Общая 5-летняя выживаемость у пациентов с раком гортани составляет 60 %. В зависимости от стадии она будет следующей:
- если рак гортани диагностирован на ранних стадиях — 85–95 %;
- у пациентов с метастазами в регионарные лимфоузлы — 43 %;
- у пациентов с отдалёнными метастазами — 30 % [15].
Профилактика рака гортани
Для профилактики злокачественных опухолей гортани необходимо:
- отказаться от курения, как основного провоцирующего фактора;
- исключить крепкий алкоголь;
- регулярно проходить профилактические осмотры у ЛОР-врача при наличии осиплости;
- исключить факторы внешней среды, такие как радиация, вдыхание асбестовой пыли и др.;
- вести здоровый образ жизни, заниматься физкультурой;
- своевременно лечить предопухолевые заболевания слизистой гортани (папилломатоз, лейкоплакию и т. д.).
После окончания лечения рака гортани нужно приходить к онкологу один раз в 3 месяца в первый год, один раз в 4–6 месяцев во второй, с 3-го по 5-й год — один раз в 6–8 месяцев и далее 1 раз в год или при возникновении жалоб [4].
Болезнь рак горла – злокачественное новообразование в глотке или гортани, которое возникло в результате изменений тканей под действием неблагоприятных факторов. Вначале опухоль локализуется в горле. По мере развития патологического процесса опухоль из гортани и глотки проникает в соседние ткани и органы.
Все условия для лечения рака горла созданы в клинике онкологии Юсуповской больницы:
- Пациенты во время обследования и лечения пребывают в комфортных палатах;
- Они обеспечены индивидуальными средствами личной гигиены и качественным диетическим питанием;
- Обследование пациентов проводят с помощью новейшей аппаратуры ведущих фирм США, Японии, Италии;
- Врачи проводят комплексную терапию онкологии гортани и глотки.
Медицинский персонал обеспечивает профессиональный уход за пациентами.
Причины рака глотки
Различают следующие основные причины рака горла:
|
Причины |
Описание |
|
Курение |
Табачные изделия содержащие вредные вещества способствуют развитию заболевания |
|
Алкоголь |
Спиртосодержащая продукция ослабляет организм и повреждает иммунную систему при злоупотреблении. |
|
Отсутствие гигиены полости рта |
Отсутствие ухода и гигиены увеличивает рис развития онкологии горла |
|
Наследственность |
Если в роду были люди с раком горла, вероятность его появления у будущего поколения возрастает |
|
Вирус папилломы |
Инфицирование увеличивает вероятность развития онкологии. |
Сколько надо курить, чтобы был рак горла? Исследования, которые проводили учёные, обнаружили связь между числом сигарет, выкуриваемых за день, стажем курения и вероятностью возникновения рака горла. Чем выше первые 2 показателя, тем выше риск заболевания раком. На увеличение риска влияют и другие формы употребления табака. Потенциальный риск заболевания раком гортани существует и у курильщиков, и у жующих табак. У лиц, которые имеют обе эти привычки, опасность развития рака горла повышается в 3-4 раза. Излишнее употребление крепких спиртных напитков, является первой причиной, увеличивающей риск развития заболевания.
Связанный с вирусом папилломы человека рак гортани имеет характерные биологические особенности. При его лечении используют менее агрессивные органосохраняющие схемы химиотерапии. Как долго развивается рак горла? Процесс трансформации нормальный клеток в атипичные индивидуален для каждого человека. Рак горла развивается не сразу. Ему предшествуют длительно протекающие предраковые заболевания:
- Дискератозы гортани (лейкоплакия, лейкокератоз);
- Пахидермия;
- Фиброма;
- Папилломы;
- Кисты;
- Хронические воспалительные процессы в гортани, которые сопровождаются частым употреблением алкоголя и курением;
- Рубцы гортани в результате перенесенных заболеваний или травм.
Причиной развития рака гортани может быть воздействие вредных факторов на производстве, ослабленная иммунная система, ионизирующее облучение, гастроэзофагеальная рефлюксная болезнь.
Провоцирующими факторами являются краски, древесная пыль, асбест, серная кислота, никель. Как быстро развивается рак горла? От появления первых изменений в клетках слизистой оболочки глотки или гортани до клинической стадии болезни могут пройти месяцы или годы.
В последнее время в России отмечается рост количества впервые выявленного рака горла. Это связано с воздействием внешних и внутренних факторов. По всему миру статистика не менее утешительна. Ежегодно диагностируется 15000 новых случаев патологии. Соотношение заболевших мужчин по отношению к женщинам составляет 1000:8.
Какие первые признаки рака горла
Первые признаки рака горла и гортани весьма разнообразны. Они зависят от формы и места роста опухоли, степени её распространения. Начальная стадия рака горла протекает скрыто. Первые симптомы рака горла незначительно выражены. При их наличии необходимо немедленно записаться на консультацию к отоларингологу.
Как выглядит рак горла на начальной стадии? Вначале опухоль может быть в виде узелкового или папилломатозного образования, полипа, а также диффузной инфильтрации. Поверхность опухоли обычно неровная, может быть серой, красной или темной. Рак гортанного желудочка сначала имеет вид небольшого, постепенно увеличивающегося выбухания желудочковой связки кверху. Рак надгортанника появляется в виде ограниченной инфильтрации или бугристой, грибовидной массы на его гортанной поверхности его, распространяется в преднадгортанниковое пространство.
Первые признаки рака гортани зависят от локализации новообразования. На ранних стадиях рака средней части гортани, где располагаются голосовые связки, первыми симптомами рака горла являются осиплость и другие изменения голоса. Ощущение в горле комка или инородного тела усиливается во время принятия пищи, глотания воды.
Нарушение функции глотания возникает в том случае, когда опухоль локализуется в надгортаннике. Вначале появляется боль в горле, отдающая при жевании в ухо на поражённой стороне, а затем возникает постоянное чувство инородного тела в горле. Из-за боли начинает меньше есть, что приводит к потере массы тела и истощению больного.
Симптомы
Как начинается рак горла? Вначале заболевания симптомы заболевания отсутствуют. Рак горла проявляется общими симптомами, характерными для онкологии:
- Незначительным повышением температуры (до 37,5°C);
- Сонливостью и постоянной усталостью;
- Слабостью и общим недомоганием;
- Быстрой утомляемостью.
Когда опухоль горла и глотки увеличивается в размерах, появляются симптомы, характерные для злокачественного новообразования. Признаки рака гортани зависят от локализации патологического процесса.
Какие симптомы при раке горла, расположенном в вестибулярном отделе гортани? Изначально пациент не предъявляет никаких жалоб. При прогрессировании опухоли гортани симптомы становятся специфичными. Появляется боль и дискомфорт при глотании. Это происходит из-за деформации надгортанника и поражения нервных окончаний. Надгортанник деформируется и не закрывает полностью вход в гортань. По этой причине пациент постоянно попёрхивается.
Злокачественные новообразования вестибулярного отдела протекают агрессивно. Опухоль быстро распространяется на окружающие органы и метастазирует в лимфатические узлы шеи. Причиной этого является хорошо развитая лимфатическая система вестибулярного отдела и ее многочисленные соединения с лимфатическими сосудами глотки.
Какие признаки рака горла, локализованного в надсвязочном отделе гортани? На начальной стадии развития рака надсвязочного отдела гортани симптомы и проявления болезни отсутствуют. С увеличением размеров опухоли у пациента изменяется тембр голоса, ощущается дискомфорт во время глотания. Когда опухоль прорастает в окружающие ткани, появляется острая боль во время глотания, которая отдает в ухо и охриплость голоса.
Какие симптомы рака горла при локализации патологического процесса на голосовых связках? При таком расположении злокачественной опухоли боль появляется даже при небольших размерах новообразования. У пациента появляются следующие симптомы рака горла и гортани:
- Нарушается голос;
- Появляется охриплость и осиплость;
- Теряется звучность и мелодичность.
Больной начинает уставать даже после непродолжительного разговора. Если опухоль прорастает в просвет голосовой щели, у пациента нарушается дыхание.
Рак среднего отдела гортани протекает наиболее благоприятно. Бедность лимфатическими сосудами данной области объясняет редкое метастазирование злокачественных опухолей. Охриплость, которая возникает даже при небольших размерах опухоли, заставляет человека обратиться к врачу вскоре после появления этого симптома.
Как проявляется рак горла, если опухоль расположена в подсвязочном отделе гортани? Злокачественные опухоли этой области также имеют ряд особенностей:
- Эндофитная форма роста;
- Устойчивость к ионизирующему излучению;
- Метастазирование преимущественно в предгортанные и претрахеальные лимфатические узлы.
Ранние симптомы заболевания отсутствуют. Первым признаком рака гортани становится сухой приступообразный кашель. После того, как опухоль прорастает в голосовые связки, у пациента нарушается голос. При прогрессировании патологического процесса и прорастании злокачественного новообразования в просвет гортани, у больного появляются такие симптомы рака горла и гортани, как нарушение дыхания с приступами удушья. Если болезнь переходит в завершающую стадию и начинает разрушать окружающие ткани, появляется гнилостный запах изо рта и кашель с кровяными сгустками.
Как понять, что у тебя рак горла? Злокачественные новообразования глотки и гортани не имеют специфических симптомов. Врачи Юсуповской больницы устанавливают точный диагноз после осмотра и инструментального обследования пациента. Если имеет место онкология горла, симптомы заболевания, врачи во время обследование делают фото. Его можно переслать в клинику-партнер и получить консультацию других специалистов.
Стадии образования в горле опухоли
Различают 4 стадии рака гортани:
- Первая стадия – новообразование локализовано в слизистой оболочке. Опухоль ограничена и не занимает всей гортани. Новообразование не поражает расположенные рядом ткани и органы, не даёт метастазов;
- Вторая стадия – опухоль или язва занимает целиком один отдел гортани, но не выходит за его пределы. Подвижность гортани сохранена. В региональных лимфатических узлах метастазы не определяются;
- Третья стадия делится на 3А и 3В. При 3а стадии опухоль переходит на соседние отделы гортани, вызывает неподвижность соответствующей половины органа, или хотя и ограничивается одним этажом гортани, но сопровождается неподвижностью связки или черпаловидного хряща, или связки. Рак горла 3В стадии характеризуется распространением опухоли на соседние с гортанью органы, региональные лимфатические узлы;
- Четвёртая стадия – обширная опухоль занимает большую часть гортани, инфильтрирует соседние ткани, имеются неподвижные метастазы в лимфатических узлах шеи, или новообразование любого размера с отдалёнными метастазами.
При раке горла 1 стадии у пациентов появляется постоянный кашель, меняется тембр голоса. После правильно подобранного лечения рецидива опухоли в течение пяти лет не наступает у 80% пациентов. 2 стадия рака горла проявляется нарушением работы голосовых складок, проблемами с дыханием. У пациента голос становится сиплым, появляются боли при глотании. Пятилетняя выживаемость составляет 70%.
Рак горла 3 степени проявляется полным отсутствием голоса вследствие поражения голосовых связок. При раке гортани 3 степени продолжительность жизни 60% больных 5 лет.
Диагноз «рак гортани 4 степени» проявляется симптомами поражения гортани и внутренних органов, в которых локализовались метастазы (пищевода, лёгких и бронхов, органов пищеварения). Реже определяются метастазы в печень и головной мозг. Можно ли вылечить рак гортани 4 стадии? При раке горла 4 степени продолжительность жизни небольшая. Пятилетняя выживаемость менее 25%.
Диагностика рака гортаноглотки
Как диагностировать рак горла на ранних стадиях? При наличии симптомов рака горла диагностика должна быть комплексной. Диагностику рака горла и гортани врачи Юсуповской больницы проводят с помощью следующих методов:
- Прямой и непрямой ларингоскопии,
- Гипофарингоскопии;
- Компьютерной томографии;
- Гистологического исследования;
- Пробной ларингофиссуры;
- Цитологического исследования отпечатков из гортани и лимфатических узлов;
- Определения уровня онкомаркеров.
Как распознать рак горла? Отоларингологи вначале выполняют непрямую ларингоскопию. При осмотре истинных голосовых связок обращают внимание на подвижность их при фонации и присущую опухолевому процессу асимметрию поражения, уточняют размер поражения новообразования и его локализацию. Для осмотра задних отделов гортани прибегают к осмотру их гортанным зеркалом снизу-вверх, когда врач сидит перед стоящим пациентом.
Как диагностировать рак горла у пожилого человека при недостаточно ясной картине или если опухоль маскируется вторичными воспалительными явлениями с распадом, инфильтрацией и отёком? Отоларингологи в этом случае прибегают к местному обезболиванию, поднятию надгортанника, ощупыванию зондом, применяют увеличивающее зеркало, а также придают соответствующий наклон голове пациента. При подозрении на поражение подсвязочного отдела или нижних отделов глотки применяют прямую ларингоскопию и гипофарингоскопию.
Как проверить горло на онкологию с помощью компьютерной томографии. Этот метод исследования расширяет диагностические возможности при опухолях, которые локализуются в области желудочковых и истинных голосовых связок и гортанных желудочков, а также при распространении опухоли на подсвязочный отдел. В Юсуповской больнице обследование пациентов проводят с помощью компьютерных томографов последнего поколения с большими разрешающими возможностями.
Как проверить горло и гортань на рак с помощью лабораторных методов? Гистологическое исследование определяет характер опухоли, её строение, степень дифференциации клеточных элементов и степень злокачественности опухоли – все эти детали влияют на течение заболевания и учитываются при выборе метода лечения
Чтобы избежать стимуляции усиленного роста и распространения опухолевого процесса в связи с повреждением лимфатических и кровеносных сосудов при биопсии, онкологи проводят перед хирургическим вмешательством несколько сеансов лучевой терапии.
Как диагностировать рак гортани другими методами? В тех случаях, когда данные биопсии недостаточно убедительны или она невозможна, применяют пробную ларингофиссуру. Поскольку во время процедуры может произойти обсеменение атипичными клетками окружающих тканей, в подобных случаях срочно производят гистологическое исследование у операционного стола, предварительно получив согласие пациента на радикальное вмешательство. Цитологическое исследование отпечатков из гортани и лимфатических узлов проводят в тех случаях, когда пациент категорически отказывается от операции, а биопсия не показана.
Как определить рак горла на начальной стадии? Для ранней диагностики рака горла и гортани врачи Юсуповской больницы исследуют уровень онкомаркеров SCC и CYFRA 21-1. Высокая квалификация врачей, оснащение операционных современной диагностической аппаратурой и инструментарием позволяет онкологам Юсуповской больницы улучшить показатели пятилетней выживаемости при раке горла.
Как лечить рак гортани? Врачи Юсуповской больницы имеют большой опыт лечения рака гортани. Метода лечения подбирают в зависимости от стадии заболевания, вида и распространения опухоли. Используют следующие методы:
- Хирургические вмешательства (хордэктомию, резекцию гортани);
- Органосохраняющую лазерную хирургию опухолей гортани;
- Операции по удалению новообразований с использованием шейвера;
- Лучевое лечение (дистанционную гамма-терапию);
- Неоадъювантную, адъювантную и лечебную химиотерапию;
- Паллиативное лечение.
Мнение эксперта
Автор: Алексей Андреевич Моисеев
Заведующий онкологическим отделением, онколог, химиотерапевт, кандидат медицинских наук
На долю рака горла приходится 3 % всех онкологических заболеваний. В то же время опухоль является самой распространенной в числе новообразований верхних дыхательных путей. Она диагностируется в 50–70 % случаев. По мере прогрессирования рака горла формируется стойкая утрата трудоспособности. Вследствие этого опухоль остается проблемой для клинической медицины.
В последнее время в России отмечается рост количества впервые выявленного рака горла. Это связано с воздействием внешних и внутренних факторов. По всему миру статистика не менее утешительна. Ежегодно диагностируется 15000 новых случаев патологии. Соотношение заболевших мужчин по отношению к женщинам составляет 1000:8.
В Юсуповской больнице осуществляется полный курс диагностики, необходимой для выявления патологии даже на этапах формирования. Чем раньше произведено обследование, тем благоприятнее прогноз. Качество проводимого лечения соответствует мировым стандартам. Для каждого пациента разрабатывается индивидуальная программа терапии и реабилитации, направленная на повышение качества жизни и профилактику рецидива.
Основной метод лечения рака гортани – оперативное вмешательство. Радикальным хирургическим вмешательством при злокачественной опухоли является удаление гортани. Последствия могут быть разными. После операции у некоторых пациентов пропадает голос, возобновляется рост опухоли.
Ларингофиссура накладывается при локализации экзофитной опухоли на свободном крае передних двух третей истинной голосовой связки, без распространения новообразования на переднюю комиссуру и на черпаловидную область.
Если раковым процессом поражен значительный участок гортани, а подвижность в пораженной области очень ограничена или даже полностью отсутствует, процесс макроскопически является односторонним, хирурги выполняют операцию на горле при онкологии – резекцию половины гортани. Гемиларингэктомия показана не только при внутреннем раке, не прорастающем через хрящи гортани, но и при распространении опухолевого процесса на переднюю комиссуру и область черпаловидного хряща.
Если опухоль локализуется в передних двух третях одной истинной голосовой связки с переходом на переднюю комиссуру или даже на переднюю часть другой истинной голосовой связки выполняют половинную резекция гортани по Отану. При этой операции удаляют передние отделы гортани, оставляя её заднюю стенку. После вмешательства сохраняется глотание и голосовая функция. К частичным оперативным вмешательствам при раке гортани относится фронтальная резекция гортани. Её применяют при поражении передней комиссуры.
В настоящее время наиболее распространёнными органосохраняющими операциями при ограниченном раке гортани остаются хордэктомия и диагональная резекция гортани. После операции у пациентов нарушается голосовая функция, они отмечают хрипоту, быструю утомляемость во время разговора и значительное ухудшение звучания при перегрузке. Нежелательным последствием сагиттальной резекции гортани является расстройство акта глотания после операции.
Как вылечить рак горла на ранней стадии? Операцию на гортани (удаление опухоли) выполняют с применением шейвера. Во время операции не травмируются здоровые ткани. Операция выполняется эндоскопическим путём. Трахеостома при раке гортани накладывается после тотального удаления органа. В Юсуповской больнице обеспечивают питание после удаления гортани при раке горла.
Рак горла лечится противоопухолевыми препаратами. Онкологи практикуют два варианта лечения: монотерапию и полихимиотерапию. При монотерапии применяют 1 препарат, к которому особенно чувствительны раковые клетки. Препарат назначают в больших дозах. Для полихимиотерапии используют несколько цитостатических препаратов последовательно или одновременно.
Химиотерапевты Юсуповской больницы для достижения наибольшей эффективности лечения используют рекомендованные Международной Ассоциацией онкологов комбинации цитостатиков. Используют препараты, которые обладают высокой эффективностью и оказывают минимальное побочное действие. Пациенты клиники онкологии имеют возможность получать новейшие противоопухолевые препараты благодаря программе исследований, в которой участвует Юсуповская больница. Оценка эффективности лучевой терапии при раке горла проводится профессорами и врачами высшей категории.
Комбинированный подход к лечению рака гортани позволяет улучшить результаты лечения. Лучевая терапия при раке горла применяется как в качестве первичного лечения, так и входит в состав комбинированной терапии. Лечится ли рак горла? Большинство пациентов с ранними стадиями рака гортани излечиваются с помощью радиотерапии. Насколько подходит лучевая терапия при раке гортани конкретному пациенту, зависит от объёма и расположения опухоли, определяется глубиной её прорастания в ткани горла.
На ранних этапах болезни лечение в большинстве случаев сеансы облучения проводят 5 раз в неделю на протяжении 3-7 недель. Радиотерапевт подсчитывает общую дозу облучения рака гортани на весь курс, а затем делит её на фракции. Подобное разделение позволяет снизить нежелательные последствия лечения. Можно ли вылечить рак горла? Если вовремя начать комплексное лечение, прогноз для выздоровления многократно улучшается.
Прогноз выживаемости
Сколько живут с раком гортани? Когда у пациента диагностирован рак горла, прогноз напрямую зависит от локализации опухоли и распространённости ракового процесса.
Таблица №1. Прогноз выживаемости в зависимости от локализации опухоли гортани
|
Расположение новообразования |
Прогноз пятилетней выживаемости |
|
Заперстневидная область |
20% |
|
Задняя стенка гортани |
21% |
|
Грушевидный синус |
50% |
Рак горла – это смертельно? В случае если заболевание распознано своевременно, велика вероятность того, что недуг удастся победить. Пятилетняя выживаемость у больных раком горла на первой стадии составляет 85%. При выявлении рака гора 4 стадии прогноз менее оптимистичный. Если выявлен рак горла 4 степени, сколько живут? Прогноз пятилетней выживаемости больных четвёртой стадией рака гортани 20%. Многое зависит от того, согласится ли пациент на операцию по удалению гортани и голосовых связок которая может сделать человека немым.
Долговременная выживаемость больных раком горла на протяжении последних 20 лет практически не изменилась, но качество жизни вылечившихся пациентов значительно улучшилось. Если лучевая терапия не приводит к ожидаемому результату, врачи Юсуповской больницы используют методы сохранной хирургии, которые позволяют частично сохранить пациенту речь.
Профилактика
Рак горла является заболеванием, развитие которого в значительной степени связано с употреблением алкоголя, никотина и других токсичных веществ. Врачи-онкологи рекомендуют пациентам, обращающимся по данному вопросу, отказаться пагубных привычек для снижения вероятности патологии.
Другим провоцирующим фактором являются канцерогенные вещества, вдыхание которых вызывает необратимые изменения слизистых оболочек. Пациентам, относящимся к группе риска, показано ограничение манипуляций с веществами повышенной канцерогенности: бензолом, асбестом, продуктами нефтяной промышленности, фенольными смолами, угольной пылью. Если при выполнении трудовых обязанностей контакт с данными веществами невозможно исключить, следует использовать респираторы для защиты дыхательных путей.
Своевременное лечение болезней органов дыхания является важной профилактической мерой предупреждения патологического процесса. Врачи-онкологи Юсуповской больницы консультируют пациентов, относящихся к группе риска, и информируют их о факторах, негативно воздействующих на дыхательные пути, проявлениях рака горла на начальной стадии и методах профилактики.
Лечение в Москве
Лечение рака горла в Москве с помощью современных методов проводят врачи Юсуповской больницы. Клиника онкологии специализируется на лечении рака гортани. Приём ведут ведущие онкологи Москвы, которые имеют научные звания и высшую врачебную категорию. В лечебном процессе принимают участие кандидаты и доктора медицинских наук, авторы научных работ.
Пациенты находятся в комфортных палатах. Медицинский персонал проводит гигиенический уход за трахеостомой. Повара обеспечивают пациентов специальным питанием. Стоимость лечения ниже, чем в других клиниках по лечению рака горла. Цена оказываемых пациенту услуг соответствует их качеству. Сколько стоит лечение рака горла, можно узнать по телефону Юсуповской больницы.
Рак гортани — злокачественная опухоль гортани преимущественно плоскоклеточного характера. В зависимости от расположения и распространенности рак гортани может проявляться нарушением голоса, дыхательными расстройствами (одышка, хронический и острый стеноз гортани), дисфагией, болевым синдромом, кашлем, симптомами раковой кахексии. Основными методами, позволяющими диагностировать рак гортани, являются ларингоскопия, рентгенография и КТ гортани, эндоскопическая биопсия слизистой гортани и биопсия регионарных лимфоузлов. Лечение рака гортани заключается в проведении радикальной операции (резекции гортани или ларингоэктомии), лучевой терапии и восстановлении голосовой функции, иногда применяется химиотерапия.
Общие сведения
Рак гортани является довольно распространенным онкологическим заболеванием. В общей структуре злокачественных опухолей на его долю приходится 2,6% случаев. Среди злокачественных новообразований головы и шеи по частоте встречаемости рак гортани занимает первое место. Пациенты с раком гортани составляют около 70% от всех больных с раковыми заболеваниями верхних дыхательных путей. Рак гортани поражает преимущественно лиц мужского пола, на 1 заболевшую женщину приходится 9-10 мужчин. Наиболее часто рак гортани встречается у мужчин в возрасте 65-75 лет, у женщин — в 70-80 лет.
Рак гортани
Причины возникновения рака гортани
Рак гортани, как и другие злокачественные опухоли, возникает в результате злокачественного перерождения изначально нормальных клеток. Среди факторов, способных спровоцировать этот процесс, выделяют:
- табакокурение, злоупотребление алкоголем
- хронические воспалительные заболевания (хронический ларингит, ларинготрахеит, фарингит, сифилис)
- профессиональные вредности (работа на производстве асбеста, никеля, серной кислоты).
Наиболее опасным считается сочетанное воздействие на ткани гортани алкоголя и табачного дыма, которое также способно вызвать рост доброкачественных опухолей полости рта, возникновение рака языка, губы, щеки и т. п.
Рак гортани может развиться в результате злокачественной трансформации некоторых доброкачественных опухолей гортани (например, длительно существующих папиллом) и лейкоплакии гортани. В отдельных случаях рак гортани является следствием распространения опухолевого процесса при раке глотки.
Классификация рака гортани
В отоларингологии рак гортани классифицируют в зависимости от его гистологического типа, локализации, характера роста, стадии распространенности опухоли, а также по международной системе TNM. Если говорить о гистологической форме, то в 95% рак гортани является плоскоклеточным раком, 2% составляет железистый рак, еще 2% — базалиома, 1% приходится на другие, редко встречающиеся, типы рака. Рак гортани может иметь экзофитный, эндофитный (инфильтративный) и смешанный характер роста.
По топографическому признаку выделяют рак гортани верхнего (70%), среднего (28%) и нижнего (2%) отдела. Рак гортани, расположенный в ее верхнем отделе, может локализоваться на надгортаннике, желудочках гортани, черпалонадгортанных складках. Обычно он возникает с одной стороны, но быстро распространяется на другую сторону. При расположении опухоли в желудочках гортани она быстро перекрывает просвет гортани, являясь причиной расстройств дыхания и фонации. Наиболее распространен рак гортани, затрагивающий ее средний отдел. Как правило, опухоль находится только на одной голосовой связке. Еще в начальной стадии она приводит к нарушениям голосообразования, что способствует более ранней диагностике рака гортани этой локализации. Рак гортани, поражающий ее нижние отделы (подскладочное пространство), в большинстве случаев отличается интенсивным инфильтративным ростом и за короткое время захватывает противоположную сторону.
По распространенности опухолевого процесса в клинической практике рак гортани подразделяют на 4 стадии. I стадии соответствует ограниченный рак гортани, локализующийся в пределах слизистой или подслизистого слоя одной анатомической области гортани. II стадия характеризуется опухолевым процессом, который полностью поражает один отдел гортани, но не выходит за его пределы и не метастазирует. Рак гортани IIIа стадии сопровождается распространением процесса на подлежащие ткани, что приводит к ограничению подвижности гортани. В IIIб стадии в злокачественный процесс вовлекаются соседние отделы гортани и/или регионарные лимфатические узлы. Рак гортани IV стадии поражает большую часть гортани, переходит на соседние органы и/или дает регионарные и отдаленные метастазы.
Симптомы рака гортани
Клиника ракового поражения гортани зависит от локализации процесса и его распространенности. В соответствии с этим рак гортани может иметь различную симптоматику, очередность появления и степень проявленности основных симптомов.
Нарушения голоса возникают в начальном периоде рака гортани, если он локализуется в области голосовых складок. Если рак гортани расположен в других отделах, расстройство голосовой функции наблюдается в более позднем периоде и связано с распространением злокачественного процесса. Нарушения голоса при раке гортани обычно проявляются его охриплостью или осиплостью. Их отличительной чертой является постоянный характер без периодов улучшения голоса, которые наблюдаются при нейропатическом и функциональном парезе гортани. У пациентов с раком гортани отмечается постепенное прогрессирование охриплости, голос становится все более тусклым и может исчезнуть совсем.
Нарушение глотания (дисфагия) выходит на первый план при раке гортани, занимающем ее верхнюю часть. Оно сопровождаются ощущением инородного тела гортани и усиливающимся болевым синдромом.
Дыхательные нарушения наиболее рано развиваются при раке гортани в нижнем отделе. Если рак гортани ограничивается голосовой связкой, то нарушения со стороны дыхания могут возникнуть лишь через несколько месяцев или даже через год после начала опухолевого роста. При раке верхнего отдела гортани дыхательные нарушения также появляются в более поздней распространенной стадии. Они характеризуются постепенно нарастающей одышкой, возникающей сначала при физической нагрузке, а затем и в покое. Постепенное сужение просвета гортани по мере роста позволяет организму адаптироваться к возникающей гипоксии. Таким образом, при раке гортани развивается клиническая картина хронического стеноза гортани. На ее фоне при воздействии неблагоприятных факторов (ОРВИ, аллергия, вторичное инфицирование) может возникнуть острый стеноз гортани.
Болевой синдром наблюдается при раке гортани в верхнем отделе и при распространенных опухолевых процессах. Он может быть связан с распадом и изъязвлением раковой опухоли. Нередко при рак гортани сопровождается иррадиацией боли в ухо и ее усилением при глотании. Выраженный болевой синдром заставляет пациентов с раком гортани отказываться от еды.
Кашель при раке гортани имеет рефлекторное происхождение. В некоторых случаях он сопровождается приступами, типичными для ложного крупа. Кашель происходит с выделением небольшого количества слизистой мокроты. При распаде рака гортани или изъязвлении в мокроте наблюдаются прожилки крови. При распространенном характере рака гортани страдает запирательная функция гортани и происходит попадание пищи в гортань и трахею, что вызывает приступ неукротимого мучительного кашля.
Общие симптомы рака гортани обусловлены раковой интоксикацией и возникают при значительной распространенности опухолевого процесса. К ним относятся бледность, повышенная утомляемость, общая слабость, головные боли, нарушения сна, анемия, значительное похудание.
Метастазирование. Рак гортани из верхнего отдела метастазирует в верхние яремные лимфоузлы, рак гортани нижнего отдела — в перитрахеальные и нижние яремные лимфоузлы. Наиболее часто регионарными метастазами сопровождается рак гортани верхнего отдела (35-45%), при раке нижнего отдела гортани регионарные метастазы отмечаются в 15-20% случаев. По причине слабо развитой сети лимфатических сосудов среднего отдела гортани расположенный в ней рак гортани поздно и редко дает метастазы в регионарные лимфоузлы. Отдаленное метастазирование при раке гортани наблюдается достаточно редко. В 4% случаев рак гортани метастазирует в легкие с развитием рака легкого, 1,2% приходится на метастазы в печень, пищевод и кости. Метастазы рака гортани в головной мозг, желудок и кишечник наблюдаются крайне редко.
Диагностика рака гортани
Ранняя диагностика имеет определяющее значение в прогнозе и успешности лечения рака гортани. В связи с этим необходимым является осмотр отоларингологом каждого мужчины с охриплостью голоса или кашлем неясного генеза, если они сохраняются более 2-3 недель. Настораживающими в отношении рака гортани симптомами также являются чувство инородного тела в горле, не сопровождающиеся отоскопическими изменениями боли в ухе, увеличение лимфатических узлов шеи.
КТ шеи. Рак подсвязочного отдела гортани справа
Предварительно диагностировать рак гортани позволяет тщательная ларингоскопия. Выявленные эндоскопические изменения при раке гортани могут иметь самый разнообразный характер. В случае эпителиомы голосовой связки выявляется ограниченное образование, поражающее лишь одну связку и имеющее вид бугорка. В других случаях рак гортани может определяться как распространенное образование с бугристой поверхностью, имеющее красноватую окраску.
Инфильтративный рак гортани характеризуется утолщением голосовой связки и ее кровоточивостью при зондировании. В отдельных случаях рак гортани имеет полипообразный вид. Установить точный диагноз помогает произведенная в ходе ларингоскопии биопсия образования. Если гистологическое исследование не выявляет раковых клеток, а клиническая картина свидетельствует в пользу рака гортани, то возможно проведение интраоперационной диагностики.
Дополнительными методами в диагностике рака гортани являются исследования голосовой функции, позволяющие оценить подвижность голосовых связок, форму голосовой щели и пр. К ним относятся стробоскопия, электроглоттография, фонетография. Распространенность рака гортани оценивают при помощи рентгенографии и МСКТ гортани. Наличие метастазов в ткани шеи выявляют при помощи УЗИ. Для определения регионарного метастазирования производят биопсию лимфатического узла.
КТ шеи. Рак подсвязочного отдела гортани с сужением ее просвета
Лечение рака гортани
Лечебные мероприятия при раке гортани направлены на полное удаление опухоли и восстановление голосообразующей и дыхательной функции гортани. Выбор лечебной тактики в отношении рака гортани зависит от месторасположения раковой опухоли, ее границ и распространенности, наличия прорастания в соседние структуры и метастазирования, радиочувствительности опухолевых клеток.
Лучевая терапия. Рак гортани в среднем отделе отличается высокой радиочувствительностью. Поэтому рак гортани этой локализации лечат, начиная с лучевой терапии. Если в результате курса лучевого воздействия опухоль уменьшается в 2 раза, то курс предоперационного облучения можно повторить. Однако в таком случае существует опасность возникновения осложнений после операции. Лучевое воздействие, как начальный этап лечения, применяют также при раке гортани I-II стадии, расположенном в ее верхнем и нижнем отделе. Лучевую терапию рака гортани проводят в обычных условиях и в сочетании с гипербарической оксигенацией, которая усиливает повреждающее воздействие излучения на раковые клетки и уменьшает повреждение здоровых тканей.
Химиотерапия. С химиотерапии начинается лечение рака гортани III-IV стадии, расположенного в верхнем отделе. При раке гортани, локализующемся в среднем и нижнем отделах, химиотерапия малоэффективна.
Хирургическое лечение рака гортани проводят не позднее, чем через 2 недели после лучевой терапии поскольку спустя 14 дней после окончания лучевого воздействия начинается восстановление клеток опухоли. Органосохраняющие резекции гортани, гемиларингэктомия эффективны при I-II стадии рака гортани. С целью предупреждения послеоперационного стеноза гортани в ходе операции в нее вводится расширяющий эндопротез, удаление которого производят спустя 3-4 недели после операции.
Рак гортани III-IV стадии является показанием к ларингэктомии. При раке нижнего отдела гортани III-IV стадии лучевая терапия может осложниться острым стенозом. Поэтому лечение начинают сразу с ларингэктомии, удаляя во время операции 5-6 верхних колец трахеи, а лучевую терапию назначают после операции. Если рак гортани сопровождается регионарным метастазированием, то операцию дополняют иссечением шейной клетчатки и лимфатических узлов. При необходимости производят резекцию вовлеченных в опухолевый процесс анатомических образований шеи (грудино-ключично-сосцевидной мышцы, внутренней яремной вены).
Восстановление голосовой функции после проведенной ларингэктомии является важной задачей, помогающей пациенту с раком гортани сохранить свое профессиональное и социальное положение. Эта задача достигается путем установки голосового протеза и последующих занятий с врачом-фониатором.
Прогноз
Без лечения рак гортани протекает в течение 1-3 лет, в некоторых случаях и более длительно. Больные с роком гортани погибают от асфиксии, раковой кахексии, аррозивного кровотечения при распространении опухоли на крупные сосуды шеи, бронхолегочных осложнений (пневмонии инфекционного характера, аспирационной пневмонии, плеврита), отдаленных метастазов. Пятилетняя выживаемость после проведенного лечения у пациентов с раком гортани I стадии составляет 92%, с раком II стадии — 80%, III стадии — 67%.
Заболевание характеризуется появлением злокачественного эпителиального новообразования, которое поражает разные отделы гортани. Образование способно к инфильтративному или экзофитному росту. Болезнь в процессе развития дает как регионарные, так и отдаленные метастазы.
Эпидемиология
- По распространенности в мире злокачественные новообразования шеи и головы занимают 6-е место.
- Основные локализации из числа органов шеи и головы – гортань и гортаноглотка.
- В России по частоте заболеваемости рак гортани занимает 5-е место.
- Самая высокая заболеваемость – в Таиланде, Польше, штате Огайо (США), Италии, Франции, Испании.
- Более подвержены заболеванию мужчины – 1 к 10-ти.
- Чаще всего – в 95% случаев – среди злокачественных поражений гортани диагностируется плоскоклеточный рак.
- Среди всех злокачественных новообразований шеи и головы эта болезнь находится на 1-м месте.
- В общей структуре раковых патологий – 2,6%.
- На 100000 человек заболеваемость – 4-6.
- Низкая заболеваемость (то есть на 100000 человек – менее 2-х) отмечается в Японии, Норвегии, Швеции.
Предлагаем ознакомиться с визуализированной статистикой по США за 1992-2015 гг. График показывает смертность и число впервые диагностированных случаев.
Определение
Гортань – область горла, которая располагается между трахеей и корнем языка. В ее строении присутствуют голосовые связки, при вибрации которых формируется голос человека.
Чтобы дать определение распространенности процесса, нужно учитывать анатомию гортани. Она разделяется на 3 отдела по ряду особенностей: различия слизистой и подслизистого слоя, лимфо- и кровообращения и др. Рассмотрим основные отделы органа:
- Верхний, или вестибулярный. В него входят следующие структуры: черпало-надгортанные связки с гортанной стороны, морганиевы желудочки, ложные голосовые связки, надгортанник.
- Средний. Это область расположения истинных голосовых связок.
- Нижний, или подсвязочный.
Этой градацией в значительной степени определяются различия в течении заболевания. Чаще всего поражается складочный и надскладочный отделы (50-70%), при этом заболеваемость по складочному отделу составляет 30-40% случаев, а по подскладочному – 3-5%. Самое злокачественное течение – если опухоль поражает вестибулярный отдел. В этом случае с частотой 40-60% развиваются метастазы. Самый благоприятный прогноз – если поражен складочный отдел. Метастазы при этом диагностируются в 5-12% случаев. При поражении новообразованием подскладочного отдела показатели – примерно такие же.
Особенности развития метастазов, в зависимости от локализации онкологии
Надскладочный отдел
Здесь присутствует хорошо развитая лимфатическая сеть, которая способствует тому, чтобы опухоль быстро распространялась по местной и регионарной локализации. В основном метастазы поражают верхнюю и среднюю группу лимфоузлов, находящихся в глубокой яремной цепи, – 50-60% случаев. Метастазы локализуются:
- в 57% случаев на стороне опухоли;
- в 9% – с двух сторон гортани;
- в 6,3% – контрлатерально, то есть на противоположной от новообразования стороне.
Голосовые складки
Благодаря малому лимфообращению, метастазы отмечаются здесь редко. В 5-12% случаев они обнаруживаются в средних глубоких яремных лимфоузлах.
Подскладочный отдел
Регионарные метастазы встречаются в 5-12% случаев. При этом в 20% случаев они развиваются в претрахеальных и предгортанных лимфоузлах. Лимфа двигается по направлению нижних глубоких яремных лимфоузлов, где тоже диагностируется метастазирование.
Отдаленные метастазы наиболее часто диагностируются в ребрах, легких, средостении.
Предраковые заболевания
Рассмотрим патологии, которые предшествуют раку гортани:
- ларингит, которым человек болеет в хронической форме и много лет;
- особую роль в появлении этой патологии играют:
- чаще всего – папиллома, существующая длительное время, и лейкоплакия слизистой, выстилающей гортань;
- пахидермия;
- дискератозы;
- кистозные образования на гортанных желудочках;
- фиброма на широком основании;
- хронические воспаления, не поддающиеся лечению и обусловленные курением, алкоголизмом, сифилисом.
Ларингит
Ларингит
Папиллома
Папиллома
Лейкоплакия
Лейкоплакия
Факторы риска
Важно понимать, что наличие перечисленных факторов не означает, что вы обязательно столкнетесь с раком, однако и их отсутствие не гарантирует того, что у вас нет онкологии.
Основные факторы, повышающие риск заболеть раком гортани:
- Алкоголь. Те, кто регулярно выпивают крепкие спиртные напитки, болеют раком полости рта в 6 раз чаще. Очень опасно сочетание курения и алкоголя.
- Курение. Чем выше у курильщика стаж и чем больше сигарет он выкуривает, тем выше риск заболеть. Вероятность появления рака повышает в том числе пассивное курение.
- Условия работы. К факторам риска относятся: труд в условиях высокой запыленности (особенно, если пыль содержит вредные химикаты, радиоактивные вещества, металлы), при контакте с изотопами и при высокой температуре.
- Вирус папилломы человека (ВПЧ). ВПЧ-позитивными считались новообразования с подтипами вируса ВПЧ18 и ВПЧ16.
- Неправильный рацион.
Подтверждение тому, что алкоголь и курение повышают риск развития заболевания найдено в исследованиях, которые посвящены изучению того, как ведет себя опухолевый ген-супрессор р53. В соответствии с этими исследованиями среди всех больных раком гортани в 42% была выявлена мутация этого гена. У тех, кто одновременно пьет и курит, мутация отмечалась в 58% случаев. У тех, кто курит, но не пьет, – в 33%. У непьющих и некурящих мутация происходила всего в 17% случаев. Кроме того, у некурящих и непьющих людей мутация р53 отмечалась на участке ДНК, который более характерен для эндогенных мутаций.
Стадии заболевания
Рассмотрим TNM клиническую классификацию. В соответствии с ней символ N обозначает, есть ли метастазы в регионарных лимфоузлах (л/у):
- NX – не хватает данных, чтобы оценить регионарные л/у;
- N0 – признаков метастазирования в регионарных лимфоузлах нет;
- N1 – отмечаются метастазы в одном л/у, расположенном на стороне поражения, имеющие размер до 3 см в наибольшем измерении;
- N2 – на стороне поражения отмечаются метастазы в одном л/у до 6 см в наибольшем измерении, либо метастазы до 6 см в наибольшем измерении присутствуют в нескольких л/у на стороне опухоли, либо метастазы до 6 см в наибольшем измерении располагаются в л/у с обеих сторон;
- N2а – на стороне поражения в одном л/у присутствуют метастазы до 6 см в наибольшем измерении;
- N2b – на стороне поражения в нескольких л/у присутствуют метастазы до 6 см в наибольшем измерении;
- N2c – с обеих сторон либо противоположно от опухоли в л/у располагаются метастазы до 6 см в наибольшем измерении;
- N3 – в л/у обнаруживаются метастазы более 6 см в наибольшем измерении. Л/у средней линии относят к узлам на стороне поражения.
Символ М показывает, есть ли отдаленные метастазы:
- МХ – нет данных, чтобы оценить отдаленные метастазы;
- М0 – не обнаружено признаков отдаленных метастазов;
- М1 – отмечается отдаленное метастазирование.
Классификация опухолей по символу Т с учетом локализации в гортани
| Надсвязочный отдел | Т1 | Опухоль находится только в надсвязочной части, голосовые связки подвижны |
| Т2 | Поражена слизистая нескольких анатомических областей связочной или надсвязочной части либо зона вне надсвязочной части (медиальная стенка грушевидного синуса, слизистая корня языка и др.) без фиксации гортани | |
| Т3 | Новообразование ограничивается гортанью с фиксацией голосовых связок и/или распространено на заднюю часть гортанного хряща, ткань в преднадгортанной области; эрозия щитовидного хряща минимальна | |
| Т4а | Опухоль поражает щитовидный хрящ и/или распространена на мягкие ткани вокруг гортани: пищевод, шею (наружные и глубокие мышцы), щитовидную железу, лентовидные мышцы, язык | |
| Т4b | Новообразование поражает средостение либо оболочку сонной артерии, а также предпозвоночную область | |
| Связочный отдел | Т1 | Новообразование ограничивается голосовыми связками, не нарушает их подвижность, в процесс могут быть вовлечены задняя и передняя комиссуры |
| Т1а | Новообразование ограничивается одной голосовой связкой | |
| Т1b | Поражены обе голосовые связки | |
| Т2 | Патология поражает под- и/или надсвязочную зоны, нарушает подвижность голосовых связок | |
| Т3 | Поражена только гортань с фиксацией голосовых связок и/или опухоль прорастает в надсвязочную область и/или провоцирует эрозию щитовидного хряща | |
| Т4а | Опухолью поражены ткани вокруг гортани (лентовидные мышцы, трахея, глубокие/наружные мышцы языка, шея, пищевод, лентовидные мышцы) или щитовидный хрящ | |
| Т4b | Новообразование проросло в средостение, предпозвоночное пространство или оболочку сонной артерии | |
| Подсвязочный отдел | Т1 | Новообразование ограничивается подсвязочной областью |
| Т2 | Опухоль поражает одну или две голосовые связки, подвижность – свободная или ограниченная | |
| Т3 | Новообразование не выходит за пределы гортани с фиксацией голосовых связок | |
| Т4а | Новообразование прорастает в щитовидный либо перстневидный хрящ и/или поражает ткани, расположенные вокруг гортани (щитовидная железа, шея, включая наружные/глубокие мышцы языка, трахея, лентовидные мышцы) | |
| Т4b | Опухоль распространяется на предпозвоночное пространство, оболочку сонной артерии либо средостение |
Таблица общей группировки заболевания по стадиям
Симптомы и клиническая картина
Клиническая картина заболевания различна, в зависимости от пораженной опухолью зоны. Рассмотрим каждую из них.
Рак вестибулярного отдела (отмечается в 60-65% случаев)
В течение первых нескольких месяцев пациенты ощущают:
- першение в горле;
- сухость;
- ощущение присутствия инородного тела.
Позднее присоединяется следующая симптоматика:
- нарушение глотания;
- утомляемость;
- глухой голос;
- боль при глотании;
- утренняя боль при глотании, а позднее – постоянная.
Стоит отметить, что такая симптоматика также может говорить о наличии ларингита и фарингита.
При поражении голосового отдела (встречается в 30-35% случаев)
Клиническая картина при поражении этой области следующая:
- слабость и охриплость голоса;
- быстрая утомляемость при голосовой нагрузке;
- позднее – трудности при дыхании, афония.
Подголосовой отдел
Для поражения этой зоны характерны следующие симптомы:
- учащающиеся приступы кашля, сопровождающиеся трудностями при дыхании.
Для опухоли характерен эндофитный вид роста, а также склонность прорастать вниз и к хрящевым структурам трахеи.
Методы диагностики
Сначала представим таблицу дифференциальной диагностики
| Форма болезни | Клиническая картина |
| Папиллома в области гортани | Обычно возникает на голосовых связках, реже поражает надгортанник, мелкобугристая, бледно-серая, у пациента проявляется осиплость голоса |
| Лейкоплакия | На голосовых связках обнаруживается пятно белого цвета и с неровной поверхностью, чаще всего оно находится сзади черпаловидных хрящевых структур, характеризуется нарушением фонации и кашлем |
| Фибромы голосового отростка контактной формы | Находятся в задних частях голосовых складок, на одной из них напоминает молоточек, на другой – наковальню, у пациента меняется голос |
| Фибромы гортани | Располагаются в передней трети голосовых связок, иногда имеют широкое основание и исходят из гортанного желудочка или вестибулярной связки |
Диагностика этого заболевания включает физикальные и инструментальные методы обследования.
Физикальные:
- сбор анамнеза жизни и заболевания;
- осмотр и пальпация (прощупывание) лимфоузлов и гортани.
Инструментальные:
- ларингоскопия (непрямая);
- фиброларингоскопия, в ходе которой делается прицельная биопсия;
- УЗИ (выполнение пункции лимфоузлов под контролем УЗИ);
- Трепан биопсия ЛУ с последующим гистологическим исследованием биоматериала, имеющее решающее значение для постановки диагноза в онкологии.
Рассмотрим подробно методы диагностики, опишем их особенности.
Ларингоскопия
- Непрямая. С ее помощью определяют расположение и границы новообразования, формы его роста, цвет слизистой, ее целостность, размер просвета голосовой щели, уровень подвижности голосовых складок, а также наличие воспаления хрящей и надхрящницы гортани (хондроперихондрит).
- Фиброларингоскопия. Позволяет осмотреть отделы гортани, которые не видно при проведении прямой ларингоскопии (надгортанник, гортанные желудочки, переднюю комиссуру, подкладочный отдел). В ходе нее делается прицельная биопсия.
Ларингоскопия
Рентгенологические методики
Пациенту проводятся следующие обследования:
- МРТ/ КТ мягких тканей шеи с применением внутривенного контрастирования — обеспечивают данные о распространении патологического процесса по отделам гортани, а также дают информацию по регионарному лимфатическому коллектору;
- рентгенография органов грудной клетки либо КТ грудной и брюшной полостей с применением контраста.
Рентгенологические методы исследования
Рентгенологические методы исследования
Гистологическое исследование
В соответствии с гистологическим строением в 98% случаев рак гортани представлен неороговевающим или ороговевающим плоскоклеточным эпителием. Реже диагностируется аденокарцинома. В крайне редких случаях (0,4%) – саркома.
Плоскоклеточный высокодифференцированный рак
Методы лечения
Методика терапии выбирается с учетом очень многих факторов: стадия, расположение опухоли, форма ее роста, распространенность процесса, степень злокачественности. Самое важное предварительное исследование – биопсия с последующей гистологией, определяющая тип злокачественной ткани. КТ и фиброларингоскопия продемонстрировали высокую эффективность при диагностике поражения хрящей гортани и окологортанных пространств. Так, если эти структуры поражены, в комплекс терапии обязательно включается хирургическое вмешательство.
Основные методики:
- операция;
- лучевая терапия;
- химиотерапия;
- комбинация перечисленных методов.
Хирургическое вмешательство
Проводятся следующие виды операций:
- CO2- лазерные резекции;
- Ларингэктомия;
- Частичная резекция гортани
- Шейная лимфодиссекция
- Реконструктивно-пластические операции
Объем работы хирурга определяется месторасположением опухоли, ее распространенностью и радиочувствительностью.
Разновидности оперативных вмешательств:
- Хордэктомия. Представляет собой удаление одной голосовой связки. Показания к ней: поражение только одной голосовой связки без распространения процесса на голосовой отросток черпаловидного хряща и комиссуру, отсутствие иммобилизации голосовой складки.
- Гемиларингэктомия – резекция половины гортани.
- Переднебоковая (или диагональная) резекция гортани – остается 2/3 половины гортани. Показания: поражение опухолью половины гортани и переход через переднюю комиссуру.
- Передняя (или фронтальная) резекция гортани. Проводится иссечение передней комиссуры и расположенных в непосредственной близости участков голосовых связок.
- Горизонтальная резекция гортани. Иссекается пораженная часть, могут быть сохранены голосовые складки. Проводится при расположении новообразования в преддверии.
- Операция Крайля. Удаляется внутренняя яремная вена вместе с клетчаткой и лимфатическими узлами.
- Фасциально-футлярное иссечение лимфатических узлов и клетчатки шеи
- Ларингэктомия вместе с корнем языка и подъязычной костью.
Операцию Крайля и ФФИ ЛУ и клетчатки шеи (фасциально-футлярное иссечение лимфатических и клетчатки шеи) по показаниям проводят, если наблюдается недостаточная регрессия увеличенных лимфоузлов и возможность их оперирования после облучения 40 Гр, а также при первом этапе лечения
Наличие N1 и N2а подвижных л/у при отсутствии вовлечения в патологический процесс кивательной мышцы и яремной вены служит показанием к фасциально-футлярной лимфодиссекции.
Если в наличии N1, N2а, b, с вколоченные, неподвижные л/у, а в процесс также вовлечена кивательная мышца и внутренняя яремная вена, проводится операция Крайля.
Если регионарный метастаз на шее спаян с сосудами, пациенту дополнительно назначается ангиография и КТ шеи, потому что в этом случае возможно проведение операции Крайля с удалением артерии и ее пластическим замещением.
Если у пациента обнаруживаются единичные метастазы в печени и легких, нужно дообследование, чтобы решить вопрос о дальнейшей тактике ведения этого пациента
Лучевая терапия
Показаниями служат новообразования в среднем и вестибулярном отделах гортани.
Облучение может проводиться в качестве подготовки к операции (режим 40-45 Гр), а также радикально в лечебном режиме (70 Гр).
Согласно данным зарубежных и отечественных авторов, при I-II стадии рака гортани 70-80% пациентов может быть вылечено с использованием режима 70 Гр, а также 45-52% больных с III стадией.
Противопоказания к облучению на первом этапе:
- хондроперихондрит гортани;
- стеноз гортани (выраженный);
- поражение опухолью окружающих органов (трахеи, пищевода), а также ее распад;
- отдаленные метастазы;
- неподвижные конгломераты метастазов с врастанием в магистральные сосуды;
- поражение подскладочного отдела;
- общее тяжелое состояние пациента на фоне диабета, прогрессирующего туберкулеза, сердечно-сосудистых заболеваний.
Если после проведения облучения 40 Гр эффект недостаточен и при этом пациент категорически отказывается от хирургической операции, лучевую терапию продолжают до лечебной дозы (70 Гр).
Когда опухоль распространена на переднюю комиссуру, преднадгортанное пространство, боковую стенку глотки, облучение неэффективно в качестве единственного метода лечения. Его дополняют химиотерапией, СВЧ-гипертермией и/или операцией.
Часто до начала лечения, при необходимости, пациенту формируют трахеостому из-за высокого риска удушья во время лечения. Во время лучевой терапии или химиотерапии вследствие отека, может возникнуть необратимое состояние, которое может повлечь за собой смерть пациента, без предварительной трахеоостомии. Также возникает необходимость установки гастростомы, которая может быть выполнена под эндоскопическим контролем и классическим открытым способом.
Если у больного присутствует трахеостома, назогастральный зонд или гастростома — это не является препятствием к облучению или к химиотерапии. Если новообразования распространены, то трахеостома может попадать в поле облучения.
Химиотерапия
Варианты применения системной химиотерапии:
- паллиативное лечение при метастазах и рецидивировании заболевания;
- в комбинации с облучением – органосохраняющее лечение опухолей, являющихся местнораспространенными;
- неоадъювантная терапия – дает возможность провести операцию и/или снизить объем вмешательства;
- при отказе пациента от операции или невозможности хирургического вмешательства, например при непереносимости наркоза, в пожилом возрасте, при соматических болезнях.
Основные используемые препараты: 5 Фторурацил, Цисплатин, Карбоплатин, Паклитаксел
Противопоказания к химиотерапии:
- перихондрит;
- стеноз гортани 2-3-й степени;
- поражение опухолью черпаловидного и щитовидного хрящей;
- язва желудка и 12-перстной кишки;
- заболевания почек, печени, сердечно-сосудистой системы в стадии декомпенсации;
- декомпенсированный сахарный диабет;
- беременность;
- открытая форма туберкулеза легких.
Особые указания по лечению
По данным исследований, при поражении надскладочного отдела и распространенности процесса до стадии Т1N0M0 лучше отдавать предпочтение облучению (процент излечения достигает 95%, сохраняется функция гортани). При T2N0M0 и аналогичной локализации показана органосохраняющая операция, потому что до 80% рецидивов после облучения связано с поражением именно этих гортанных структур.
Если поражен складочный отдел и регистрируется стадия Т1N0M0, терапию начинают с облучения. При таком способе процент излечения составляет 75-78%, с учетом чего нужно проводить первичную оценку эффективности терапии на дозе 40 Гр. Если отмечается регресс новообразования менее 70%, то возможно проведение хирургического вмешательства – хордэктомии. Когда новообразование распространено на переднюю комиссуру и вторую голосовую складку, проводят резекцию гортани, потому что в этом случае отдаленные результаты лучше, чем при облучении.
Химиотерапия не улучшает результаты лечения при стадии Т1-2N0M0.
При терапии местнораспространенной патологии в стадии Т3N0M0-T4N0M0 наибольшую эффективность показало применение комбинированной методики с разной последовательностью облучения и хирургического вмешательства, потому что в этом случае у 70-73% пациентов добиваются пятилетней выживаемости. Однако при этом проводится ларингэктомия, инвалидизирующая пациента.
Если у пациента есть противопоказания к операции, терапию начинают с облучения. Если рак распространен Т3-Т4, то возможности лучевой терапии ограничены. При этом если операции и возможны, они носят калечащий характер. Вариантом органосохраняющего лечения местнораспространенной патологии или гортаноглотки может быть сочетание индукционной химиотерапии по схеме PF («Цисплатин» и «5-фторурацил) с дальнейшим облучением при наличии ответа на терапию. Если его не наблюдается, проводят ларингэктомию.
Лечение метастазов в лимфоузлах шеи
Регионарные метастазы при раке гортани не препятствуют консервативной терапии, потому что новообразования этой локализации (N1-N2) часто поддаются химиотерапии и облучению. Поэтому лимфоузлы с обеих сторон нужно включать в зону облучения гортани. Если нужно облучать лимфоузлы нижних отделов шеи, показано применение прямого поля с блоком. Нижний край этого поля проходит на 1 см ниже нижней границы ключицы. В случае поражения надключичных лимфоузлов, необходимо облучать лимфоузлы верхнего средостения.
Когда присутствуют несмещаемые или ограниченно смещаемые метастазы, целесообразно начинать лечение с неоадъювантной полихимиотерапии и последующим облучением 40 Гр. Дальше тактика определяется эффективностью проведенного лечения. Если наблюдается значительная или полная регрессия метастазов, а также их неоперабельность после дозы 40 Гр, то облучение доводят до 60-70 Гр.
Стоит особо отметить, что сегодня, когда показатель качества жизни так же важен, как и онконадежность лечения, специалисты направляют свои усилия на разработку и усовершенствование консервативной терапии, включающей разные виды химиотерапии и облучения, а также на проведение органосохраняющих операций, позволяющих сохранить или восстановить основные функции гортани.
Прогноз выживаемости
Прогноз зависит от стадии заболевания, однако в целом он неблагоприятен. Это в значительной степени обуславливается большой долей больных с распространенными формами рака.
Согласно клиническим наблюдениям и данным литературы, запущенные формы онкологии гортаноглотки составляют больше 85% из всех впервые установленных случаев заболеваемости.
При применении современных способов комплексной терапии у 56% пациентов удается добиться пятилетней выживаемости.
Прогноз становится хуже при наличии метастазов: при раке гортаноглотки Т3-4N0-1М0 трехлетняя выживаемость составляет до 80%, а при стадии Т3-4N2-3М0 – до 40%.
Если в результате применения химиотерапии и облучения достигнута полная регрессия заболевания, нужно регулярно наблюдаться и обследоваться, чтобы при рецидиве своевременно сделать операцию.
Таблица процентов выживаемости, в зависимости от формы патологии и ее стадии
Для больных с III-IVb стадиями пятилетняя выживаемость составляет 48,2%, при ВПЧ+ и ВПЧ- (ОР=0,73, р<0,001) – 42,1%.
Реабилитация
Широко распространена логопедическая методика реабилитации, направленная на восстановление голосовой функции и достижение хорошего качества голоса. Достигнуть поставленных целей удается в 45-60% случаев.
После ларингэктомии:
Голос – социально важная функция, что не нуждается в доказательствах, поэтому вполне обоснованно пациенты стремятся ее сохранить или восстановить. У тех, кто перенес ларингэктомию, голосовая реабилитация проводится путем обучения так называемому пищеводному голосу, использования голосовых устройств или установки трахеопищеводного шунта вида Bloom-Singer.
Один из методов при реабилитации голоса у пациентов, которые перенесли полную резекцию гортани, является применение голософормирующих аппаратов разных конструкций. Это могут быть электрогортани, звукогенераторы.
Согласно мнению многих авторов, метод обучения пищеводной речи – наиболее физиологичен и малоинвазивен. В 62-91% случаев возможно сформировать псевдоголос, которого будет достаточно для общения.
Недостатки метода:
- пациенты трудно осваивают метод заглатывания воздушных масс в пищевод и выталкивания его при фонации;
- пищевод в качестве резервуара для воздуха имеет малый объем – 180-200 мл;
- спазм и гипертонус сжимательных элементов глотки.
Хирургическая методика восстановления голоса после проведенной ларингэктомии
Метод основан на формировании шунта между пищеводом и трахеей. Через него воздух из легких попадает в глотку и пищевод, провоцируя вибрацию глоточно-пищеводного элемента, который является генератором голоса.
Помещенный в просвет шунта голосовой протез пропускает воздух из легких в пищевод и не допускает попадания пищи и жидкости в обратном направлении.
Хорошее качество голоса, благодаря этой методике, достигнуто у 93,3% пациентов. Однако авторы метода указывают, что в 7-30% случаев возможны осложнения: грибковое поражение протеза, излишний рост грануляций, смещение протеза, протекание протеза, которое может привести к аспирационной пневмонии у пациентов.
Исследования показывают, что у всех пациентов после органосохраняющих операций наблюдается нарушение функции глотания, потому что сообразно с типом вмешательства перестраивается весь механизм. Нарушения защитной функции более значительны после горизонтальной и сагиттальной резекции гортани. Чтобы предотвратить аспирацию пищи и слюны в послеоперационном периоде, используются разные способы обтурации (закупорки) гортани: начиная тампонадой по Микуличу (показана при сагиттальной операции) и заканчивая применением обтураторов и Т-образных трубок из силикона с закрытым верхним концом, вводящихся в сформированный дыхательный анастомоз. Эти меры направлены на предотвращение попадания пищи в дыхательные пути.
Аспирация слюны хронической формы часто влечет за собой пневмонию, поэтому в некоторых случаях показаны корригирующие хирургические вмешательства. Решение данной проблемы влияет на дальнейшую жизнь пациента, потому что постоянная аспирация может стать причиной необходимости проведения ларингэктомии.
Одна из самых сложных задач при проведении органосохраняющих операций – восстановление функции дыхания, потому что все разновидности резекции, за исключением экстирпации надгортанника, деформируют гортань и уменьшают ее размеры. В. О. Ольшанский приводит сравнительно более высокую цифру – у него получается деканюлировать 73,4% пациентов. Автор применял для восстановления просвета гортани эндопротез в форме трубки, состоящий из биологически совместимых полимерных материалов, пропитанных антисептическим составом.
Рак гортани: причины появления, симптомы, диагностика и способы лечения.
Определение
Рак гортани – злокачественная опухоль, развивающихся в органах дыхания и прилегающих структурах горла (миндалинах, голосовых связках, надгортаннике).
По данным мировой литературы, ежегодно в мире регистрируется порядка 238 000 случаев рака гортани и 106 000 летальных исходов в результате этого заболевания.
Рак гортани занимает восьмое место среди общего числа злокачественных заболеваний, а среди опухолей верхних дыхательных путей – первое.
По большей части рак гортани диагностируется у людей в возрасте 40-60 лет, причем у мужчин в 15-20 раз чаще, чем у женщин.
Причины появления рака гортани
Рак гортани крайне редко возникает на неизмененных (здоровых) органах. Как правило, к моменту начала злокачественного процесса эти органы испытывали воздействие тех или иных неблагоприятных факторов.
В большинстве случаев в анамнезе больных отмечается длительный период курения (среди больных раком гортани 94–97% — курящие), употребления алкоголя, работа в условиях повышенной запыленности (текстильное производство), вдыхание вредных канцерогенных веществ (нефти, продуктов ее перегонки, бензола, фенольных смол, асбеста).
Высокий риск манифестации злокачественной опухоли отмечается при папилломах (рак, ассоциированный с вирусом папилломы человека (ВПЧ)).
К факторам риска относятся хронические воспалительные процессы ротоглотки.
Классификация заболевания
В зависимости от гистологического типа и локализации различают несколько видов рака гортани. Самый распространенный (98% случаев) – плоскоклеточный рак, развивающийся из клеток плоского многослойного эпителия. Выделяют три подвида плоскоклеточного рака:
- карциному голосовой щели, местом локализации которой являются голосовые связки;
- надскладочную карциному, формирующуюся выше голосовых складок;
- субклеточную карциному, которая образуется ниже голосовых складок.
Также встречаются саркомы, меланомы, лимфомы.
Для более точного определения опухолевого процесса используется классификация по стадиям:
- 1-я стадия протекает преимущественно бессимптомно, глотательная и голосовая функции не нарушены;
- 2-я стадия – в связи с ростом опухоли поражаются соседние ткани, появляется кашель, одышка, меняется голос;
- 3-я стадия – опухоль прорастает во все слои гортани, функция голосовых связок утрачивается;
- 4-я стадия – распространение метастазов в другие органы (легкие, головной мозг, печень, лимфоузлы и т.д.).
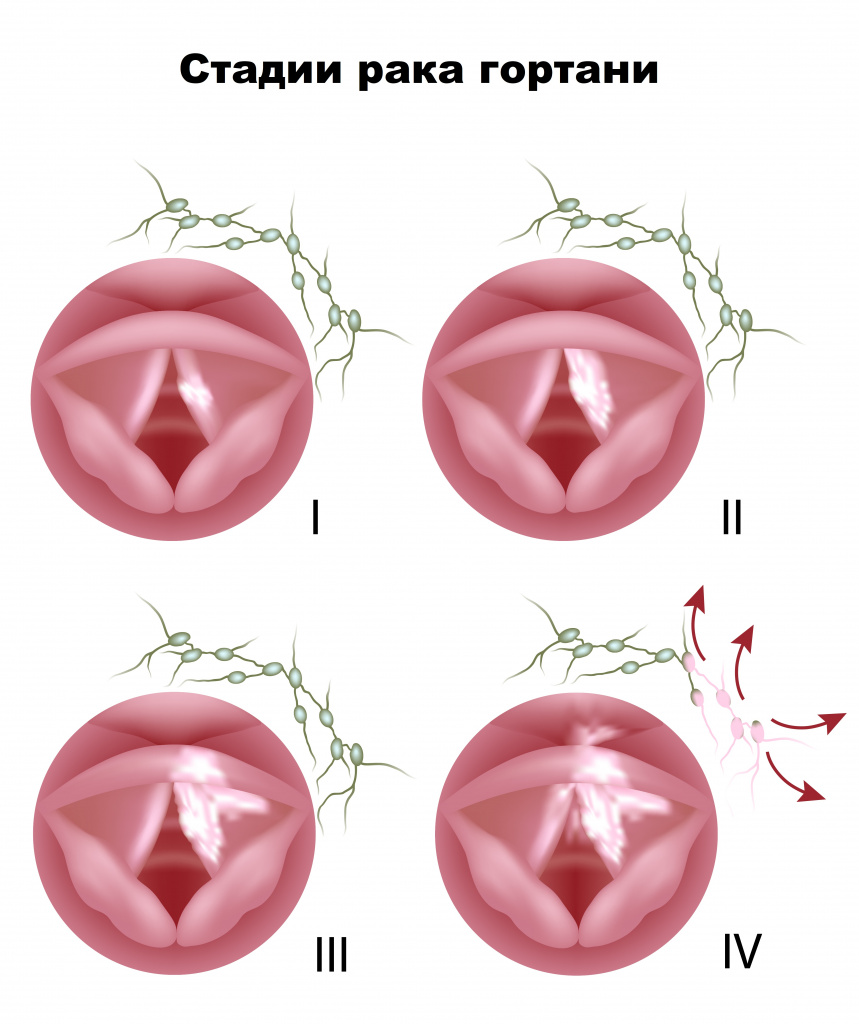
Симптомы онкологического процесса в гортани весьма разнообразны и зависят от формы и локализации опухоли, степени ее распространения. Начальный период заболевания часто бывает скрытым, поэтому его проявлениям больные могут не предавать значения. Однако даже незначительные симптомы должны насторожить:
- любые изменения голоса, включая осиплость;
- отечность шеи;
- боль или першение в горле;
- ощущение дискомфорта или инородного тела в гортани во время проглатывания пищи или жидкости;
- кашель или покашливание;
- боль в ухе.
Злокачественную опухоль вестибулярного (надскладочного) отдела диагностируют у 60-65% больных, обратившихся за медицинской помощью по поводу рака гортани. Онкологический процесс этой локализации протекает особенно агрессивно – он быстро распространяется на окружающие ткани и органы. Ранние признаки опухоли вестибулярного отдела гортани следующие: ощущение инородного тела и боль в горле с иррадиацией в ухо, увеличение лимфатических узлов шеи. Затем присоединяются более поздние симптомы: дисфагия (нарушение функции глотания), осиплость, парастезии (вид расстройства чувствительности кожи, для которого характерны спонтанно возникающие ощущения мурашек, покалывания, онемения или жжения), болевой синдром при глотании, который нарастает по мере прогрессирования заболевания, заставляя пациента ограничивать количество еды, в результате чего происходит потеря веса.
Наиболее благоприятное течение заболевания врачи отмечают при онкологическом процессе, затрагивающем средний (складочный) отдел гортани.
По всей видимости, это связано с умеренным лимфотоком в этой зоне, что снижает риск метастазирования опухоли.
Первым клиническим симптомом неоплазии гортани часто становится осиплость голоса, по поводу которой пациенты обращаются к врачу. По мере роста опухоли голосовая функция может быть полностью утеряна. На более поздних стадиях онкологического процесса появляется затрудненное дыхание, вызванное стенозом просвета гортани неподвижностью одной из ее половин.
Рак подскладочного отдела гортани диагностируют у 3-5% больных. Неоплазии этой локализации имеют, как правило, эндофитную (инфильтративную) форму роста, то есть вглубь гортани. Они сужают ее просвет, вызывая затруднения на вдохе. Распространяясь в направлении голосовой складки и инфильтрируя ее, эти опухоли приводят к осиплости. Другое направление развития опухолевого процесса – верхние кольца трахеи.
В 23,4% случаев можно обнаружить распространение опухоли на несколько отделов гортани.
Диагностика рака гортани
По характеру первых симптомов заболевания и их изменениям можно с достаточной долей вероятности судить о локализации опухолевого процесса. Однако основополагающими все же остаются инструментальные методы обследования.
Фиброларингоскопия используется для диагностики новообразований гортани и позволяет провести осмотр ее отделов, в ряде случаев недоступный для других методов исследования, и осуществить прицельную биопсию для гистологического исследования.
Диагноз злокачественной опухоли любой стадии до начала лечения должен быть подтвержден гистологическим исследованием, которое является заключительным этапом диагностики.
Компьютерная томография имеет большое значение при выявлении прорастания опухоли, позволяя увидеть состояние хрящевой ткани.
КТ гортани
Безопасное и безболезненное исследование для определения патологии гортани.
МРТ дает возможность оценить состояние мягких тканей гортани: голосовых складок, подскладочного отдела, просвета гортанных желудочков, черпалонадгортанных складок, грушевидных синусов.
Рентгенография легких проводится при подозрении на отдаленные метастазы в легких.
УЗИ печени проводят с целью определения наличия метастазов в этом органе.
УЗИ печени
Ультразвуковое сканирование печени, позволяющее оценить структуру органа, выявить изменения паренхимы (ткани органа) и другие патологические изменения.
УЗИ шейных лимфоузлов используют для раннего распознавания метастазов в регионарные лимфоузлы. При подозрении на поражение метастазами выполняют пункцию лимфатического узла. Подозрительными по метастазированию являются нарушение структуры узла, рост узла при динамическом наблюдении.
ПЭТ-сканирование (позитронно-эмиссионная томография) – эффективный и современный метод диагностики онкологических заболеваний, сочетающий позитронно-эмиссионную и компьютерную томографию. Позволяет диагностировать онкологический процесс на самых ранних стадиях, когда симптомы еще выражены слабо или отсутствуют вовсе.
Общий анализ крови. Изменения формулы крови происходят по мере прогрессирования злокачественного процесса (ускорение СОЭ, лейкоцитоз, признаки анемии), на ранних стадиях кровь может быть «спокойной».
В биохимическом анализе крови концентрация альбумина и общего белка снижается по мере прогрессирования рака гортани.
Альбумин (в крови) (Albumin)
Синонимы: Человеческий сывороточный альбумин; ЧСА; Альбумин плазмы;
Human Serum Albumin; ALB.
Краткая характеристика исследуемого вещества Альбумин
Альбумин – эт…
Общий белок (в крови) (Protein total)
Синонимы: Общий белок сыворотки крови; Общий сывороточный белок.
Total Protein; Serum Тotal Protein; Total Serum Protein; TProt; ТР.
Краткая характеристика определяемого вещества Общий бел…
При распространении метастазов в печень и желчный пузырь повышается билирубин, АСТ, АЛТ, щелочная фосфатаза. При распаде опухоли и интоксикации организма повышается уровень мочевины.
Билирубин общий (Bilirubin total)
Синонимы: Общий билирубин крови; Общий билирубин сыворотки.
Totalbilirubin; TBIL.
Краткая характеристика определяемого вещества Билирубин общий
Билирубин – это пигмен�…
Мочевина (в крови) (Urea)
Синонимы: Диамид угольной кислоты; Карбамид; Мочевина в крови; Азот мочевины.
Urea nitrogen; Urea; Blood Urea Nitrogen (BUN); Urea; Plasma Urea.
Краткая характеристика аналита Мочевина
Моче�…
Рак гортани следует дифференцировать с папилломатозом гортани (разрастанием доброкачественных, ВПЧ-ассоциированных опухолевых образований, развивающихся из эпителия).
При эндоскопическом исследовании могут обнаруживаются единичные или множественные папилломы белесого или красноватого цвета. Кроме того, выявление вируса папилломы человека и уточнение его типа проводится с помощью ПЦР-диагностики.
Определение ДНК ВПЧ (Вирус папилломы человека, Human papillomavirus, HPV) высокого онкогенного риска, скрининг 14 типов (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68) + КВМ в соскобе эпителиальных клеток слизистой прямой кишки
Синонимы: Определение ДНК папилломы в ректальном соскобе.
HPV (Human papillomavirus, HPV) DNA, high oncogenic risk, screening of 14 types (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68), epithelial cells scraping of rectal mucosa; High…
Морфологический диагноз подтверждается при гистологическом исследовании биоптата.
Дифференциальная диагностика также проводится с фибромами гортани –доброкачественными опухолями гортани соединительнотканного происхождения. При эндоскопическом обследовании они выглядят одиночными образованиями сферической формы размером 0,5-1.5 см. Для постановки окончательного диагноза проводят гистологическое исследование биоматериала.
К каким врачам обращаться
Диагностикой и лечением рака гортани занимается врач-онколог, но как правило, пациенты сначала обращаются на консультацию к
оториноларингологу
.
Лечение рака гортина
Основная задача терапии – не только добиться стойкой ремиссии, но и восстановить голосовую и дыхательную функции. На ранних стадиях рака гортани полного выздоровления можно добиться с помощью лучевой терапии, хирургического вмешательства или их сочетания.
Методы лечения зависят от стадии и локализации процесса. При 1-й стадии заболевания клиническое излечение без рецидивов и метастазов продолжительностью свыше 5 лет достигается у 83–95% больных после проведенного лучевой терапии (при хирургическом и комбинированном лечении эти показатели приближаются к 100%). На 2-й стадии – у 70–76%.
В случае недостаточного эффекта от консервативных методов проводят хирургическое лечение.
Если очаг поражения небольшой, удаляют часть гортани с захватом здоровой ткани, при этом голосовая и дыхательная функции сохраняются.
В случае значительного поражения (рак гортани на 3-4-й стадии) проводят ларингоэктомию (удаление гортани) с удалением 5-6 верхних колец трахеи. Затем пациенту назначают курс лучевой терапии.
Если рак гортани сопровождается регионарным метастазированием, то операцию дополняют иссечением шейной клетчатки и лимфатических узлов. При необходимости проводят резекцию вовлеченных в опухолевый процесс анатомических образований шеи.
После проведенного лечения важной задачей является восстановление голоса у пациента для сохранения социальной и профессиональной активности. В этом случае устанавливают голосовой протез, пользоваться которым учит врач-фониатор.
Осложнения
Осложнения, вызванные раком гортани, тяжелые и трудно купируемые:
- обструкция легких (затрудненное дыхание), которая наблюдается при прорастании опухоли в просвет дыхательных путей, и другие бронхолегочные осложнения (пневмонии, плевриты);
- истощение;
- кровотечения при распространении опухоли на крупные сосуды;
- отдаленные метастазы;
- послеоперационные осложнения: трудности при приеме пищи, нарушение голосовой функции при тотальном удалении гортани.
Профилактика рака гортани
Профилактика рака гортани сводится к тому, чтобы в первую очередь исключить факторы риска. Необходимо отказаться от курения, своевременно лечить хронические заболевания горла, соблюдать правила безопасности работы с токсичными веществами.
Важно внимательно относиться к своему здоровью и ежегодно проходить профилактические осмотры.
Источники:
- Клинические рекомендации «Рак гортани». Разраб.: Ассоциация онкологов России, Российское общество специалистов по опухолям головы и шеи. – 2020.
- Раджабова З.А-Г., Котов М.А., Эберт М.А., Митрофанов А.С., Раджабова М.А., Левченко Е.В. Распространенный рак гортани: обзор литературы // Сибирский онкологический журнал. 2019; 18(5): 97-107. doi: 10.21294/1814-4861-2019-18-5-97-107
- Гехаев А.У., Исакова Ф.С., Гаппоева Э.Т. Клиническая характеристика предраковых поражений гортани // Российская оториноларингология. 2021;20(6):35-40.
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Для корректной оценки результатов ваших анализов в динамике предпочтительно делать исследования в одной и той же лаборатории, так как в разных лабораториях для выполнения одноименных анализов могут применяться разные методы исследования и единицы измерения.
Информация проверена экспертом

Лишова Екатерина Александровна
Высшее медицинское образование, опыт работы — 19 лет
Поделитесь этой статьей сейчас
Рекомендации
-
6046
14 Мая
-
6054
14 Мая
-
6020
14 Мая
Похожие статьи
Рак пищевода
Рак пищевода: причины появления, симптомы, диагностика и способы лечения.



 American Joint Committee on Cancer (AJCC). AJCC Cancer Staging Manual, 7th ed. Edge S.B., Byrd D.R., Carducci M.A. et al., eds. New York: Springer; 2009;
American Joint Committee on Cancer (AJCC). AJCC Cancer Staging Manual, 7th ed. Edge S.B., Byrd D.R., Carducci M.A. et al., eds. New York: Springer; 2009;