Гастрит и дуоденит
Версия: Клинические рекомендации РФ 2021 (Россия)
Категории МКБ:
Гастрит и дуоденит (K29)
Разделы медицины:
Гастроэнтерология
Общая информация
Краткое описание
Разработчик клинических рекомендаций:
Российская гастроэнтерологическая ассоциация
Ассоциация «Эндоскопическое общество РЭНДО»
Гастрит и дуоденит
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем: К29
Год утверждения: 2021
Возрастная группа: взрослые
1. Краткая информация по заболеванию или состоянию (группе заболеваний или состояний)
1.1. Определение заболевания или состояния (группы заболеваний или состояний)
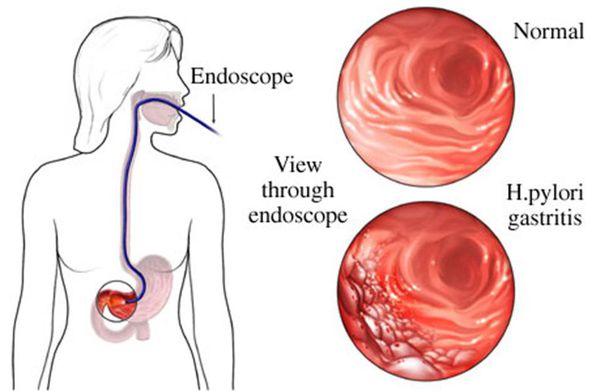
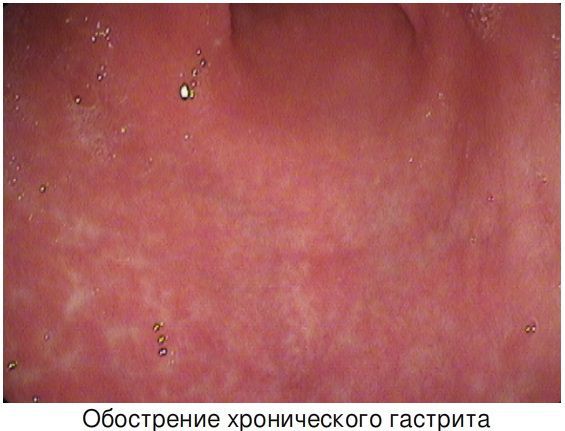
Гастрит – воспалительное заболевание слизистой оболочки желудка. Различают острый и хронический гастриты. Хронический гастрит – группа хронических заболеваний, которые морфологически характеризуются персистирующим воспалительным инфильтратом и нарушением клеточного обновления с развитием кишечной метаплазии, атрофии и эпителиальной дисплазии в слизистой оболочке желудка.
Хронический дуоденит характеризуется воспалительной инфильтрацией слизистой оболочки двенадцатиперстной кишки, желудочной метаплазией эпителия и нарушениями гистоархитектоники и в виде укорочения ворсинок и углубления крипт.
1.4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем
К29.0 — Острый геморрагический гастрит
Острый (эрозивный) гастрит с кровотечением
К29.1 — Другие острые гастриты
К29.2 — Алкогольный гастрит
К29.3 — Хронический поверхностный гастрит
К29.4 — Хронический атрофический гастрит
Атрофия слизистой оболочки
К29.5 — Хронический гастрит неуточненный
Хронический гастрит:
- антральный
- фундальный
К29.6 — Другие гастриты
Гастрит гипертрофический гигантский
К29.7 — Гастрит неуточненный
К29.8 — Дуоденит
К29.9 — Гастродуоденит неуточненный
Облачная МИС «МедЭлемент»
Облачная МИС «МедЭлемент»

Автоматизация клиники: быстро и недорого!
- Подключено 300 клиник из 4 стран
- 1 место — 800 RUB / 5500 KZT / 27 BYN в месяц
Классификация
1.5. Классификация заболевания или состояния (группы заболеваний или состояний)
В докладе Киотского консенсуса для хронического гастрита предложена классификация, в основу которой положен этиологический принцип [7]:
Аутоиммунный гастрит
Инфекционный гастрит
-
Гастрит, вызванный Helicobacte rpylori
- Бактериальный гастрит (Helicobacter heilmannii, Enterococcus, Mycobacteria, вторичный сифилитический гастрит)
- Флегмона желудка
- Вирусный гастрит (энтеровирус, цитомегаловирус, вирус Эпштейна-Барр)
- Микотический гастрит (микормикоз, кандидоз, гистоплазмоз)
- Паразитарныйгастрит (Cryptosporidium, Strongyloides stercorale)
Гастрит, вызванный внешними причинами
- Гастрит, вызванный лекарствами
- Алкогольный
- Радиационный
- Химический
- Вызванный билиарным рефлюксом
- Вызванный другими определенными внешними причинами
Гастрит, вызванный специальными причинами
- Лимфоцитарный
- Болезнь Менетрие
- Аллергический
- Эозинофильный
Гастрит, обусловленный другими классифицированными заболеваниями
- при саркоидозе
- при васкулите
- при болезни Крона.
Сиднейская классификация хронического гастрита (1990), модифицированная в 1994 году в Хьюстоне, учитывает топографию поражения (тело желудка, антральный отдел) и морфологические изменения слизистой оболочки желудка (степень активности воспаления, выраженность воспаления, выраженность атрофии и метаплазии, наличие и степень колонизации H.pylori). Данные характеристики оцениваются с помощью визуально-аналоговой шкалы, полуколичественно по степени выраженности морфологического признака – норма (отсутствие признака), слабый, умеренный, выраженный. Применение визуально-аналоговой шкалы снизило субъективность оценки при характеристике гистологической картины [19]. Топография и гистологическая характеристика гастрита важны, так как фенотип гастрита определяет риск развития таких заболеваний как язвенная болезнь двенадцатиперстной кишки, язвенная болезнь желудка и рак желудка [2, 4, 6, 7].
Стадия и степень атрофического гастрита и кишечной метаплазии (метапластической атрофии) служат индикаторами риска развития рака желудка [20-22]. Для того чтобы облегчить и по возможности стандартизировать определение прогноза хронического гастрита, в первую очередь, оценку риска развития рака желудка, применяется несколько методик. Прогностическая система OLGA (Operative Link for Gastritis Assessment) использует визуально- аналоговую шкалу Сиднейской классификации. Для определения стадии гастрита соотносят гистологическую выраженность атрофии с ее топографией: стадия 0 означает минимальный риск канцерогенеза, а стадия IV соответственно – максимальный, в 5-6 раз превышающий показатели риска рака желудка в популяции [23, 24]. Российский пересмотр системы OLGA за счет визуализации с помощью пиктограмм значительно упрощает оценку атрофии (метапластической атрофии) слизистой оболочки желудка. Российский пересмотр OLGA- system одобрен III съездом Российского общества патологоанатомов [24] и утвержден Федеральной службой в сфере здравоохранения и социального развития (ФС №2010/220 от 10.06.2010 г.) [25]. Аналогичная по базовым принципам система OLGIM анализирует вместо атрофии кишечную метаплазию [26].
Всё более широко используется эндоскопическая оценка распространённости атрофии слизистой оболочки желудка по Кимура-Такемото [27, 28] либо по модифицированной шкале EGA [29], а также эндоскопическая оценка выраженности кишечной метаплазии по шкале EGGIM [30].
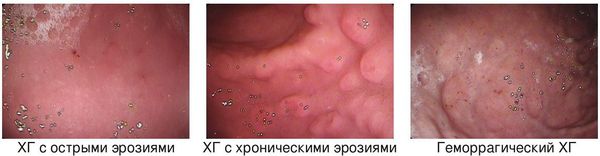
Наличие острых и/или хронических эрозий желудка и двенадцатиперстной кишки следует указывать в эндоскопическом заключении или в диагнозе как отдельную позицию. Естественное течение и клиническое значение эрозивного гастрита или эрозивного дуоденита зависит от этиологии. Частыми причинами их возникновения служат нестероидные противовоспалительные препараты (НПВП), стресс, употребление алкоголя. Среди более редких причин называют лучевое поражение, в ирусную инфекцию (например, цитомегаловирус), прямую травматизацию (например, назогастральный зонд)[7, 31].
Этиология и патогенез
1.2 Этиология и патогенез заболевания или состояния (группы заболеваний или состояний)
Гастритические изменения представляют собой реакции слизистой оболочки желудка в ответ на различные эндогенные и экзогенные патогенные факторы. К основным изменениям, из которых складывается морфологическая картина хронического гастрита, относятся воспаление, атрофия, нарушение клеточного обновления, в том числе метаплазия и дисплазия.
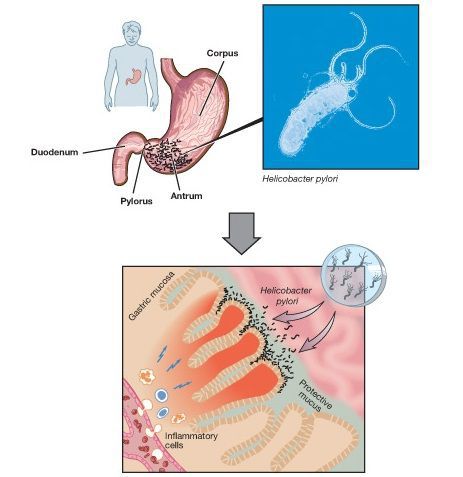
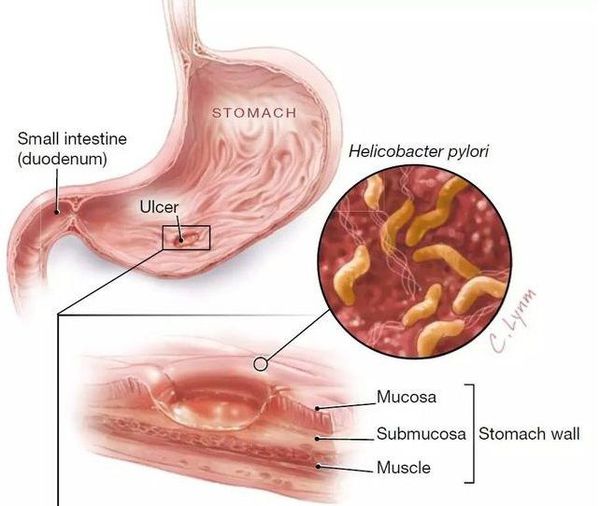
Бактерия Helicobacter pylori, колонизирующая слизистую оболочку желудка, служит этиологическим фактором гастрита. Установление этиологического значения H.pylori сделало хронический гастрит четко очерченной и клинически значимой нозологической единицей — заболеванием с известной причиной, этапами патогенетического развития, определенным прогнозом и, наконец, определило возможности этиотропного лечения. B.J.Marshall и J.R.Warren, которым впервые удалось выделить культуру ранее неизвестного грамотрицательного микроорганизма из биоптатов желудка человека, уже в первой публикации, открывшей широкомасштабное изучение H.pylori, связали наличие этой бактерии с инфильтрацией полиморфно-ядерными лейкоцитами эпителия и собственной пластинки слизистой оболочки на фоне лимфоплазмоцитарной инфильтрации [1]. СпособностьH.pylori колонизировать слизистую оболочку желудка и вызывать острый, а затем хронический гастрит, получила блестящее подтверждение в опытах по самозаражению ,независимо проведенных B.Marshall (1985) и A.Morris (1987). Большое значение для изучения патогенетического значенияH.pylori имеют эксперименты на животных: моделями, на которых удается воспроизвести геликобактерный гастрит и некоторые другиеH.pylori-ассоциированные заболевания, служат мыши, монгольские песчанки, морские свинки, гнотобионтные поросята и приматы [2]. На модели монгольской песчанки воспроизведена парадигма канцерогенеза в желудке (каскад Корреа): хроническое воспаление, вызванное H. pylori, кишечная метаплазия, атрофия, дисплазия/интраэпителиальная метаплазия и инвазивная аденокарцинома. Разным авторам удавалось воспроизвести гастрит у человека после заражения добровольцев культурой H.pylori [2, 3].
Колонизацию слизистой оболочки и выживание H. pyloriв особой среде желудка обеспечивает целый ряд факторов. Уреаза, фермент, гидролизующий мочевину с образованием аммония и углекислого газа, имеет значение для нейтрализации кислоты в окружении микроорганизма. Жгутики позволяют бактерии «целенаправленно» двигаться в слое слизи над эпителием. Другие ферменты бактерии способны вызывать деградацию муцина. Около 10% H. pylori непосредственно контактируют с эпителием. Адгезия H.pyloriс эпителиоцитами – сложный процесс, в котором участвует целый ряд поверхностных белков. Например,ВabA (blood group antigen binding adhesion) -адгезин, который связывается с Le bангигенами группы крови на эпителиоцитах; аллель гена этого адгезина — babA2 – тесно ассоциирована с развитием язвенной болезни и рака желудка в некоторых популяциях [2, 4].
В геноме бактерии выделяют «островок патогенности» cag PAI, маркером которого служит ген cagA – «цитотоксин-ассоциированный ген А». Этот ген обнаруживается у 50-70% штаммов H.pylori. Некоторые белки, которые кодируетcag PAI, служат для построения секреторной системы IV типа бактерии, благодаря которой H.pylori при прикреплении к эпителиоциту желудка вводит внутрь клетки хозяина CagA, пептидогликан, а возможно, и другие собственные молекулы. Белки H.pylori в эпителиоците «запускают» несколько сигнальных путей, результатом чего служат изменение цитоскелета клетки хозяина, нарушение межклеточных контактов, изменение пролиферации и апоптоза, а также провоспалительный эффект. Эпителиоциты желудка отвечают на присутствие H.pylori высвобождением IL-8 и хемокина, экспрессируемого и секретируемого Т-клетками при активации (RANTES), что приводит к активной воспалительной реакции в слизистой оболочке. Около 50% штаммовH.pylori секретируют высокоиммуногенныйбелок — вакуолизирующийцитотоксин А (VacA), который соответственно вызывает вакуолизацию клеток invitro, а invivoего связывают с воспалением и апоптозом[2, 4]. Таким образом, колонизацияH.pyloriподдерживает персистенцию воспалительного инфильтрата в слизистой оболочке желудка.H.pylori- индуцированное воспаление приводит к атрофии -необратимой утрате желез желудка с замещением их фиброзной тканью или метаплазированным эпителием. Атрофический гастрит, особенно с поражением тела желудка игипохлоргидрией, доказанно служит фактором риска аденокарциномы желудка [2, 5, 6, 7, 8].
Патоморфологические данные, а также исследования с применением теста проницаемости сахарозы доказывают, что при гастритах, а также при функциональной диспепсии имеет место синдром повышенной эпителиальной проницаемости, выраженность которого коррелирует с активностью воспалительного процесса в слизистой оболочке желудка. H.pylori вносит вклад в возникновение этот синдрома, оказывая негативное влияние на структурные компоненты плотных контактов эпителиоцитов [9]. Таким образом, синдром повышенной эпителиальной проницаемости участвует в патогенезе гастрита, а медикаментозная терапия, оказывающая цитопротективный эффект, патогенетически обоснована [9].
В основе аутоиммунного гастрита лежат аутоиммунные механизмы, что подтверждается наличием антител против антигенов париетальных клеток и/или против внутреннего фактора, а также сочетанием гастрита с другими аутоиммунными заболеваниями (аутоиммунный тиреоидит, сахарный диабет I типа, витилиго и др.)[10, 11, 12].
Другие особые формы гастрита встречаются реже, характеризуются специальными этиологическими факторами или могут сопровождать другие заболевания. Лимфоцитарный гастрит может быть связан с глютеновой энтеропатией, эозинофильный гастрит протекает в рамках эозинофильного гастроэнтерита, гранулематозный гастрит ассоциируют с болезнью Крона, саркоидозом, васкулитами [7].
Эпидемиология
1.3. Эпидемиология
заболевания или состояния (группы заболеваний или состояний)
Инфекция H.pylori имеет глобальное значение и широко распространена, в том числе и в нашей стране, где по данным эпидемиологических исследований в различных регионах инфицированы более 65-92% взрослого населения[13-18]. Высокая частота H.pylori определяет высокую частоту хронического гастрита.
Согласно Статистическим материалам «Заболеваемость взрослого населения России в 2019 году», зарегистрировано более 538 тысяч взрослых с установленным впервые в жизни диагнозом «гастрит и дуоденит», и заболеваемость взрослых составила 462,0:100000. Всего в 2019 году по обращаемости взрослого населения зарегистрировано более 700 тысяч случаев с диагнозом «гастрит и дуоденит». Таким образом, диагноз «гастрит» широко применяется в практике здравоохранения. Этот факт, с одной стороны, отражает высокую реальную частоту заболевания, но с другой стороны, служит свидетельством субъективных и объективных трудностей как в интерпретации симптомов диспепсии, так и в доступности необходимых методов диагностики, в первую очередь, видеоэндоскопии высокой четкости с электронной/виртуальной хромоскопией и увеличением и патологоанатомического исследования биоптатов слизистой оболочки желудка.
Клиническая картина
Cимптомы, течение
1.6 Клиническая картина заболевания или состояния (группы заболеваний или
состояний)
Под диспепсией понимают такие симптомы, как боль или жжение в эпигастральной области, переполнение в эпигастральной области, чувство раннего насыщения. Хронический гастрит, который характеризуется определенными морфологическими изменениями слизистой оболочки, часто не является причиной возникновения симптомов, в том числе диспептических. Однако у части больных с диспепсией имеющиеся клинические симптомы могут быть обусловлены хроническим Н.pylori-ассоциированным гастритом, что доказывается стойким их исчезновением после эрадикации инфекта. Диспепсию, ассоциированную с Н.pylori и хроническим гастритом, в докладе Киотского консенсуса предложено рассматривать как самостоятельную клиническую форму. Наоборот, персистенция диспептических симптомов, несмотря на успешно проведенную эрадикациюН.pylori, рассматривается как проявление функционального заболевания – функциональной диспепсии [7, 32].
Гастродуоденальные эрозии, в том числе обусловленные приемом НПВП, нередко протекают малосимптомно и могут манифестировать острым желудочно-кишечным кровотечением [7, 33].
Клиническую картину аутоиммунного гастрита обычно связывают с проявлениями дефицита витамина В12 (макроцитарная анемия, неврологическая симптоматика), железодефицитной анемией и сочетанными аутоиммунными заболеваниями [10-12]. Однако имеются исследования, которые позволяют говорить о наличии гастроэнтерологических симптомов у пациентов с аутоиммунным гастритом. Гастроэнтерологические симптомы зарегистрированы у 60% пациентов с аутоиммунным гастритом, причем представлены они в основном диспептическими симптомами, которые чаще наблюдались у пациентов моложе 55
лет, некурящих и без анемии [34]. В другом исследовании эпигастральная боль установлена в 35% случаев аутоиммунного гастрита, тошнота – в 22%, раннее насыщение – в 10%, тяжесть после еды — в 7,1%. Частыми симптомами оказались изжога (24%) и регургитация (12%) [35]. С помощью pH-импедансометрии при аутоиммунном гастрите показано, что некислые рефлюксы могут быть ассоциированы с наличием симптомов [36].
Диагностика
2. Диагностика заболевания или состояния (группы заболеваний или состояний), медицинские показания и противопоказания к применению методов диагностики
Критерии установления диагноза заболевания/состояния:
Диагноз гастрита основан на гистологическом выявлении воспаления слизистой оболочки желудка (нейтрофильные лейкоциты в собственной пластинке и интраэпителиально, плотность мононуклеарной воспалительной инфильтрации), а также атрофии и кишечной метаплазии.
Современные методы эндоскопического исследования, в частности, видеоэндоскопия высокой четкости с электронной/виртуальной хромоскопией и увеличением, предоставляют дополнительные высокоинформативные возможности для диагностики гастрита, дуоденита предраковых изменений слизистой оболочки желудка.
Важнейшим этиологическим фактором гастрита служит инфекция H.pylori, и положительные тесты на H.pylori свидетельствуют о наличии хронического гастрита.
2.1 Жалобы и анамнез
Возможные жалобы у пациентов с гастритом и интерпретация данных жалоб представлены в подразделе 1.6.
При сборе анамнеза следует уточнить, проводилась ли ранее пациенту ЭГДС с биопсией; имелись ли при этом указания на наличие предраковых состояний и изменений слизистой оболочки желудка (атрофия, кишечная метаплазия, эпителиальная дисплазия). Для оценки прогноза важно уточнить, была ли ранее проведена эрадикационная терапия инфекции H.pylori, с помощью какой схемы лечения, проведен ли контроль эффективности антигеликобактерной терапии.
Для аутоиммунного гастрита важны указания в анамнезе на дефицит витамина В12 и макроцитарную анемию, наличие таких аутоиммунных заболеваний, как аутоиммунный тиреоидит, сахарный диабет I типа, витилиго и др., выявленную при ранее проведенном эндоскопическом и патолого-анатомическом исследовании атрофию слизистой оболочки тела желудка при относительно сохранной слизистой оболочке антрального отдела.
2.2 Физикальное
обследование
При физикальном обследовании, как правило, нет данных, которые были бы характерны для гастрита.
2.3. Лабораторные диагностические исследования
- Всем пациентам с гастритом с целью исключения анемии из-за кровотечений при эрозивном поражении гастродуоденальной слизистой оболочки или из-за аутоиммунного гастрита рекомендуется выполнение общего (клинического) анализа крови с определением уровня гемоглобина, гематокрита, объема эритроцита, цветового показателя [35, 37-39].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 4)
Комментарии: Клинический анализ крови при хроническом гастрите чаще всего остается без существенных изменений, но может обнаруживаться анемия, как микроцитарная, свидетельствующая о явных, либо скрытых кровотечениях или нарушении всасывания железа, так и макроцитарная вследствие дефицита витамина В12 при аутоиммунном поражении желудка [35, 37-39].
- Всем пациентам с подозрением на аутоиммунный гастритс целью подтверждения диагноза рекомендуется проведение анализа крови на антитела к париетальным клеткам и антитела к фактору Касла [10-12, 39, 40, 41].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2)
Комментарии: Мишенью антител к париетальным клеткам служит H+/K+ ATФ-аза (альфа и бета субъединицы протонной помпы). Их выявляют у 85-90% больных с пернициозной анемией. Чувствительность для диагноза аутоиммунного гастрита составляет ~80%, специфичность низкая (обнаруживаются у лиц без аутоиммунного гастрита). Антитела к внутреннему фактору блокируют связывание кобаламина с внутренним фактором. Чувствительность для диагностики аутоиммунного гастрита ~50%, но специфичность достигает 99% [10-12, 39, 40, 41].
- Всем пациентам с подозрением на наличие при гастрите предраковых изменений желудка (атрофии, кишечной метаплазии) с целью подтверждения диагноза, оценки степени риска развития рака желудка и определения порядка эндоскопического наблюдения рекомендуется проведение анализа крови на пепсиноген I, пепсиноген II и гастрин-17 [42, 43, 7, 44-47].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
Комментарии: Диагноз атрофического гастрита стал более доступным благодаря сывороточным маркерам атрофии слизистой оболочки тела и антрального отдела желудка. Низкий уровень сывороточного пепсиногена I имеет высокую чувствительность и специфичность (84% и 95% соответственно) в диагностике выраженной атрофии слизистой оболочки тела желудка. Для атрофии слизистой оболочки антрального отдела характерны низкие уровни базального и постпрандиального гастрина-17 за счет уменьшения количества G-клеток.
При длительном наблюдении лиц с нормальным сывороточным пепсиногеном, независимо от наличия H.pylori, частота развития рака желудка была незначительной. У лиц с низким уровнем пепсиногена, свидетельствующим об атрофическом гастрите тела желудка, частота развития рака желудка было существенно выше (3,5–6 на 1000 в год). В данной группе заболеваемость раком желудка была больше при отрицательном результате антител к H.pylori, что было связно с выраженной атрофией и метаплазией, препятствующих дальнейшей колонизации H. pylori [44]. В исследовании, проведенном в Российской Федерации, рак желудка был ассоциирован с низким уровнем пепсиногена I (отношение шансов (ОШ) 2,9; 95% доверительный интервал (ДИ)1,3-6,4), низким соотношением пепсиногена I к пепсиногену II (ОШ 3,3; 95% ДИ 1,5-7,3), низким уровнем гастрина-17 (ОШ 1,8; 95% ДИ 0,7-4,8) [45]. Метаанализ 20 исследований, включавших 4241 пациента, показал, что для диагноза атрофического гастрита сочетанная оценка сывороточного пепсиногена, гастрина-17 и антител класса IgGк H.pylori продемонстрировала чувствительность 74,7% (95% ДИ 62,0- 84,3) и специфичность 95,6% (95% ДИ 92,6-97,4). Отрицательная предсказательная ценность составила 91% [42]. Метаанализ31 исследования, включавшего 1520 пациентов с аденокарциномой желудка и 2265 пациентов с атрофическим гастритом, продемонстрировал, что сывороточный пепсиноген служит надежным неинвазивным скрининговым маркером рака желудка и предракового заболевания – атрофического гастрита [43].
2.4. Инструментальные диагностические исследования
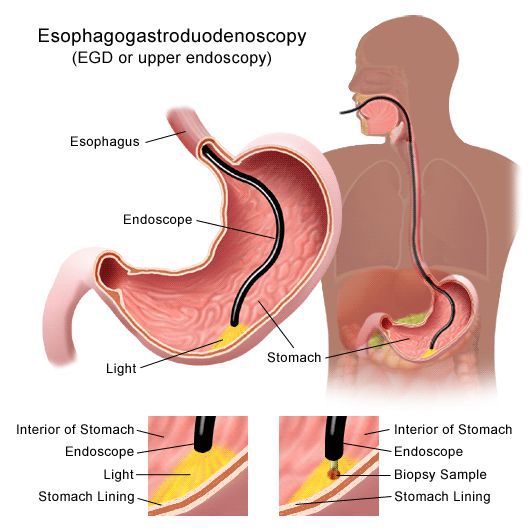
- Всем пациентам с целью подтверждения диагноза гастрита и дуоденита, выявления и ранжирования предраковых состояний и изменений слизистой оболочки желудка, в первую очередь, распространённости и степени атрофии, кишечной метаплазии и дисплазии, при отсутствии противопоказаний, рекомендуется проведение эзофагогастродуоденоскопии (ЭГДС)[48, 29, 30, 37, 38, 49; 32, 46, 47].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2)
Комментарии: Для диагностики предраковых изменений желудка при традиционной эндоскопии в белом свете корреляция между эндоскопическими и гистологическими данными неудовлетворительна [46], результаты эндоскопии высокого разрешения более надежны. В многоцентровых проспективных исследованиях специфичность эндоскопии высокого разрешения в белом свете для диагностики кишечной метаплазии составила 98%, чувствительность — 53% и 59%;для диагностики неоплазии специфичность оказалась> 95%, чувствительность — 74% и 29% [30, 49]. В метаанализе, включавшем 10 исследований и 699 пациентов, чувствительность, специфичность и площадь под кривой (AUC) хромоэндоскопии с красителями для диагностики предраковых изменений и раннего рака желудка составили 0,90 (95% ДИ 0,87 — 0,92), 0,82 (95% ДИ 0,79–0,86) и 0,95 соответственно, что превосходит результаты эндоскопии в белом свете [48].
- Всем пациентам для диагностики предраковых состояний и/или изменений слизистой оболочки желудка при возможности рекомендуется выполнение ЭГДС высокого разрешения и виртуальной хромоэндоскопии с увеличением или без него, в том числе, для выполнения прицельной биопсии с целью оценки стадии атрофии и кишечной метаплазии и выявления неоплазии [30, 47, 49, 50, 34, 35, 43, 51].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2)
Комментарии: Систематический обзор показал, что эндоскопическое исследование в режиме NBI (в большинстве исследований с увеличением) для диагностики кишечной метаплазии продемонстрировало чувствительность и специфичность 86% и 77%, а для диагностики дисплазии — 90% и 83% [49]. На основании воспроизводимых признаков эндоскопии в режиме NBI была предложена упрощенная классификация изменений слизистой оболочки, точность диагностики кишечной метаплазии составила 84%, дисплазии — 95%. Отмечено, что представленные результаты зависят от подготовки и лучше у опытных эндоскопистов [50]. В проспективном многоцентровом исследовании с применением данной классификации чувствительность и специфичность для диагностики кишечной метаплазии составили 87% и 97%, для диагностики дисплазии — и 92% и 99% [30].
- Всем пациентам, у которых впервые проводится диагностическая ЭГДС, для адекватного стадирования предраковых состояний слизистой оболочки желудка у пациентов с подозрением на наличие атрофических, метапластических и неопластических изменений рекомендуется проведение биопсии (с последующим патолого-анатомическим исследованием биопсийного материала желудка, в том числе с применением гистохимических и иммуногистохимических методов), как для диагностики инфекции H. pylori. так и для идентификации стадий атрофического гастрита [52-57, 58, 59].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
- Выполнение биопсии рекомендуется из двух отделов желудка (по два биоптата из тела и антрального отдела по малой и большой кривизне). Биоптаты из тела и антрального отдела желудка необходимо четко маркировать и помещать в отдельные контейнеры. Дополнительная биопсия должна быть взята из каждого видимого патологического участка слизистой оболочки желудка. Если для оценки тяжести атрофического гастрита планируется использование систем OLGA или OLGIM, возможно дополнительное взятие биопсии из угла желудка [52-57].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4)
Комментарии: Диагноз «гастрит» традиционно рассматривается как диагноз морфологический. В соответствии с требованиями Модифицированной Сиднейской системы для правильной интерпретации состояния слизистой оболочки желудка необходимо минимум пять биоптатов. Определены места для получения биопсийного материала: 2 из антрального отдела на расстоянии 3 см от привратника по большой и малой кривизне, 2 из тела желудка посередине большой кривизны и на 4 см проксимальнее угла по малой кривизне, 1 — из угла желудка [19]. В настоящее время хромоэндоскопия обеспечивает прецизионное взятие биопсии, что в сочетании с биопсией из фиксированных точек обеспечивает лучшую диагностику предраковых изменений. Биопсия из угла желудка позволяет более точно определять предраковые изменения, особенно в тех случаях, когда хромоэндоскопия и другие методы эндоскопии с расширенными возможностями недоступны. Биопсия из угла желудка позволяет более точно оценить стадии в соответствии с OLGA и OLGIM, которые коррелируют с риском развития рака желудка [46, 55, 56, 57].
2.5. Иные диагностические исследования
- Всем пациентам с гастритом с целью определения показаний к этиотропной эрадикационной терапии рекомендуется проведение тестирования на наличие инфекции с помощью 13С-уреазного дыхательного теста на Helicobacter pylori или определения антигена H.pylori в кале, а при проведении ЭГДС — с помощью быстрого уреазного теста [58-65, 6, 66].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарии: В соответствии с рекомендациями согласительного совещания «Маастрихт- V» (2016) [6] наиболее оптимальными тестами первичной диагностики инфекции H. pylori служат 13С-дыхательный уреазный тест и определение антигена H.pylori в кале. Так, согласно последнему Кокрейновскому обзору и мета-анализу, чувствительность 13С-дыхательного уреазного теста составляет 94% (95% ДИ: 0,89 — 0,97), а определение антигена H. pylori в кале – 83% (95% ДИ: 0,73 — 0,90) при специфичности в 90% [60].
При проведении ЭГДС методом первичной диагностики может быть быстрый уреазный тест. При использовании эндоскопических методов диагностики Н.pylori берут, как минимум, 2 биоптата из тела желудка и 1 биоптат из антрального отдела [58, 59, 63-65]. Серологический метод выявления антител класса IgG к Н.pylori также может применяться для первичной диагностики инфекции H.pylori [59]. Микробиологический (бактериологический) метод (микробиологическое (культуральное) исследование биоптатов слизистой желудка на H.pylori с определением чувствительности к антибактериальным препаратам) применяется в настоящее время для определения индивидуальной чувствительности бактерии в случаях неэффективности лечения [6, 58, 59, 66].
Для контроля эрадикации, который проводят через 4-6 недель после окончания эрадикационной терапии, лучше всего применять 13С-уреазный дыхательный тест или определение антигена Н.pylori в кале. Во избежание ложноотрицательных результатов прием ИПП необходимо прекратить за 2 недели до предполагаемого контрольного исследования. Кроме того, отрицательный результат исследования на инфекцию Н.pylori должен быть обязательно подтвержден другим методом диагностики [66].
Лечение
3. Лечение, включая медикаментозную и немедикаментозную терапии, диетотерапию, обезболивание, медицинские показания и противопоказания к применению методов лечения
3.1. Медикаментозное лечение
- Всем пациентам с хроническим гастритом с положительными результатами тестирования на инфекцию H. рylori в качестве этиологического лечения рекомендуется проведение эрадикационной терапии [3, 67-72, 7, 66].
- Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2).
- Всем пациентам с атрофическим гастритом с положительными результатами тестирования на инфекцию H.pylori для предотвращения прогрессирования атрофии рекомендуется проведение эрадикационной терапии [73-75, 6, 7, 66].
Уровень убедительности рекомендаций A (уровень достоверности доказательств – 2).
Комментарии: H.pylori служит этиологическим фактором хронического гастрита.Эрадикационная терапия инфекции позволяет излечить неатрофический гастрит, что сопровождается хорошо изученными гистологическими изменениями: в ранние сроки исчезает инфильтрация эпителия и собственной пластинки слизистой оболочки полиморфно-ядерными лейкоцитами; инфильтрация лимфоцитами и плазматическими клетками снижается в достаточно ранние сроки, но не исчезает полностью более года после эрадикации; лимфоидные фолликулы также сохраняются более года после этиологического лечения, хотя число их и сокращается [67-72]. По итогам нескольких метаанализов установлено, что в результате эрадикационной терапии H.pylori происходит регрессия или, как минимум, стабилизация атрофии слизистой оболочки в теле и антральном отделе желудка, при этом возможно добиться только стабилизации, но не обратного развития кишечной метаплазии [73-75].
В качестве схемы первой линии служит стандартная тройная схема эрадикационной терапии, включающая в себя ИПН (в стандартной дозе (#омепразол** 20 мг. пантопразол 40-20 мг, рабепразол 20 мг, #эзомепразол** 20 мг ) 2 раза в сутки ), кларитромицин** (по 500 мг 2 раза в сутки) амоксициллин** (по 1000 мг 2 раза в сутки) [6, 66, 76, 77, 78].Стандартную тройную терапию следует назначать, применяя различные меры, повышающие ее эффективность (см. ниже)[6, 66].
Как вариант эрадикационной терапии первой линии (например, при непереносимости препаратов группы пенициллина (АТХ — бета-лактамные антибактериальные препараты: пенициллины)) может быть назначена классическая четырехкомпонентная схема на основе висмута трикалия дицитрата** (120 мг 4 раза в сутки) в комбинации с ИПН (в стандартной дозе 2 раза в сутки), #тетрациклином** (500 мг 4 раза в сутки), метронидазолом** (по 500 мг 3 раза в сутки) [79, 80, 6, 66].
Квадротерапия с висмута трикалия дицитратом** применяется также как основная схема терапии второй линии при неэффективности стандартной тройной терапии [81, 6, 66]. Другой схемой терапии второй линии служит эрадикационная схема, включающая в себя ИПН (в стандартной дозе 2 раза в сутки(#омепразол** 20 мг. пантопразол 20 мг, рабепразол 20 мг, #эзомепразол** 20 мг )), #левофлоксацин** (в дозе 500 мг 2 раза в сутки) и амоксициллин** (в дозе 1000 мг 2 раза в сутки)[81, 82, 83]. Тройная терапия с #левофлоксацином** может быть назначена только врачом-гастроэнтерологом по взвешенным показаниям[6, 66].
Терапия третьей линии подбирается индивидуально в зависимости от выбора предшествующих схем лечения, при возможности по данным определения чувствительности H. pylori к антибиотикам [6, 66].
В «Рекомендациях Российской гастроэнтерологической ассоциациипо диагностике и лечению инфекции Helicobacter pylori у взрослых» были перечислены меры, повышающие эффективность эрадикационной терапии [66].Очевидно, что эти меры должны быть универсальными и применимыми в любой линии терапии, а комбинирование этих мер позволяет добиться наилучшего результата у конкретного пациента.
Меры, повышающие эффективность эрадикационной терапии:
- Продолжительность всех схем лечения H.pylori должна составлять 14 дней, минимальная продолжительность 10 дней может быть назначена в тех случаях, если исследования, проведенные в данном регионе, подтвердили ее высокую эффективность Увеличение продолжительности лечения имеет универсальный характер, так как положительный эффект наблюдается при всех изученных режимах антигеликобактерного лечения, в том числе при стандартной тройной терапии [84, 6, 66,85].
- Назначение высокой дозы ИПН (удвоенной по сравнению со стандартной) способствует повышению эффективности лечения. При проведении эрадикационной терапии предпочтение отдается #эзомепразолу** (20 мг 2 раза в сутки) и рабепразолу (20 мг 2 раза в сутки)[86-88, 6, 66].
- Добавление к стандартной тройной терапии висмута трикалия дицитрата** в дозе 240 мг2 раза в сутки или 120 мг 4 раза в сутки служит мерой повышения ее эффективности[89, 66, 80,90].
- Включение пробиотических штаммов, доказавших свою эффективность в клинических исследованиях, в состав эрадикационной терапии H.pylori приводит к повышению эффективности эрадикации и снижению числа нежелательных явлений [91-94, 6, 66].
- Включение ребамипида в дозе 100 мг 3 раза в сутки в состав эрадикационной терапии H.pylori приводит к повышению эффективности эрадикации [95, 66].
- Подробное инструктирование пациента и контроль за точным соблюдением назначенного режима приема лекарственных средств приводит к повышению эффективности эрадикаионной терапии [6, 66].
- Пациентам с эрозивным гастритом и дуоденитом, в том числе на фоне приема нестероидных противовоспалительных препарартов, с целью достижения заживления эрозий рекомендуется проведение антисекреторной терапии ингибиторами протонного насоса течение 4-6 недель [96-100] или ребамипидом в течение 4-8 недель [101, 102].
Уровень убедительности рекомендаций B (уровень достоверности доказательств – 2)
Комментарии: Базисная антисекреторная терапия с применением ИПН (назначение омепразола** в суточной дозе 20 мг, лансопразола 30 мг, пантопразола 40 мг, # #рабепразола 20 мг, #эзомепразола** 20 мг на 2-4 недели, при необходимости на более длительный срок, служит основным методом лечения гастродуоденальных эрозий, в том числе индуцированных нестероидными противовоспалительными препаратами [96-100, 103]. Эффективность ребамипида для заживления эрозивного гастрита доказана в клинических исследованиях в том числе рандомизированных[101, 102].
- Пациентам с хроническим гастритом, в том числе атрофическим, с целью потенцирования защитных свойств слизистой оболочки возможно рекомендовать терапию висмута трикалия дицитратом**[104, 105, 66] или ребамипидом в течение 4-8 недель [106-109, 6,66,110, 111].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2)
Комментарии: Цитопротективный эффект висмута трикалия дицитрата** обусловлен связыванием йонами висмута свободных радикалов и усилением эндогенного синтеза простагландинов [105], в когортном исследовании продемонстрировано снижение уровня повреждения ДНК генеративной зоны слизистой оболочки желудка пациентов после успешной эрадикации H.pylori на фоне четырехнедельной терапии висмута трикалия дицитратом**[104]. Ребамипид оказывает защитный эффект на слизистую оболочку желудочно-кишечного тракта за счет регуляции уровня простагландинов, восстановления физиологичекой продукции слизи и плотных контактов, а также и ингибирования продуктов окислительного стресса, провоспалительных цитокинов и хемокинов, что в комплексе ведет к увтранению синдрома повышеннной пронцаемости слизистых оболочек [9, 110, 111]. В рандомизированных контролируемых исследованиях ребамипид привел к уменьшению воспаления, а в одном исследовании даже к уменьшению кишечной метаплазии и дисплазии низкой степени, способствовал профилактике рака желудка у пациентов высокого риска [106- 109].
- Пациентам с хроническим гастритом и симптомами диспепсии (особенно такими, как боль и жжение в эпигастрии), в том числе в сочетании с функциональной диспепсией, в качестве симптоматического лечения рекомендуется проведение терапии ингбиторами протонного насоса [112, 113, 114, 32].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
Комментарии: Гиперчувствительность к кислоте, снижение клиренса двенадцатиперстной кишки и изменение перистальтики желудка, индуцированное кислым рефлюксом из двенадцатиперстной кишки, служат обоснованием назначения кислотосупрессивной терапии при функциональной диспепсии, особенно при синдроме эпигастральной боли [114, 115, 32]. Метаанализ 8 РКИ с участием 2216 пациентов с ФД показал, что ИПП были более эффективными, чем плацебо для улучшения симптомов, причем улучшение симптомов наблюдалось у 36,0% в группе ИПН и 30,0% в группе плацебо (относительный риск (ОР) 1,41; 95% ДИ 1,07–1,87). Число больных, которых необходимо лечить (NNT), составило 9 (95% ДИ, 6–24). ИПН ока зались эффективным с точки зрения облегчения симптомов (ОР 1,44; 95% ДИ 1,03–2,01) и полного купирования симптомом (ОР 1,26; 95% ДИ 1,07–1,49) [114].
- Пациентам с хроническим гастритом и симптомами диспепсии (особенно такими, как переполнение в эпигастрии и раннее насыщение), в том числе в сочетании с функциональной диспепсией, в качестве симптоматического лечения рекомендуется проведение терапии препаратами, обладающими прокинетическим эффектом[116, 117, 118, 32, 114, 115].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1).
Комментарии: Тримебутин — средство, действующее на энкефалинергическую систему желудочно-кишечного тракта, и таким образом, нормализующее его моторику, в РКИ продемонстрировал высокую эффективность для купирования таких симптомов диспепсии,как тяжесть после еды, быстрое насыщение, абдоминальная боль у пациентов с ФД, а также у пациентов с ФД в сочетании с синдромом раздраженного кишечника [119, 120]. Способность тримебутина купировать симптомы диспепсии подтверждена в масштабных проспективных неинтервенционных исследованиях, проведенных в РФ, общее число участников которых составило 4533 человека [121, 122]. Сцинтиграфия с коллоидной полутвердой пищей, меченной 99mTc-Tin, показала, что тримебутин нормализует
опорожнение желудка [120]. По данным сетевого метаанализа, посвященного оценке препаратов с прокинетическим действием при функциональной диспепсии, тримебутин продемонстрировал сопоставимую с метоклопрамидом** и домперидоном эффективность по показателю поверхности под кумулятивной кривой распределения (surfaceunderthecumulativerankingcurve – SUCRA) [116]. При этом безопасность тримебутина по данным метаанализов не отличалась от плацебо [123, 116].
Итоприд по механизму действия одновременно является антагонистом дофаминовых рецепторов и блокатором ацетилхолинэстеразы. Препарат активирует освобождение ацетилхолина и препятствует его деградации. Результаты крупного РКИ свидетельствовали о том, что через 8 недель лечения клинические симптомы диспепсии полностью исчезли или значительно уменьшилась их выраженность у 57, 59 и 64% больных, получавших итоприд (соответственно в дозах 50, 100 и 200 мг 3 раза в сутки), что достоверно превышало эффект плацебо (41%) [124]. Эффективность итоприда подтверждена и в других исследованиях, проведенных в том числе в России [125, 126]. Метаанализ9РКИ, включавших 2620 больных с ФД, свидетельствовал о достоверно более высокой эффективности итоприда в отношении улучшения общего состояния, уменьшения тяжести в эпигастральной области после еды и раннего насыщения. Частота возникновения побочных эффектов была одинаковой в группах итоприда и плацебо [117].
Домперидон, по механизму действия являющийся антагонистом дофаминовых рецепторов, в метаанализе продемонстрировал эффективность в уменьшении симптомов диспепсии (ОР 7,0 (95% CI 3,6-16) [118]. Однако такие нежелательные явления, как увеличение интервала Q–T и связанный с этим риск возникновения нарушений ритма сердца (особенно при одновременном приеме препаратов, метаболизирующихся, как и домперидон, с помощью системы CYP3A4), привели к ограничению показаний к назначению домперидона и продолжительности лечения [32]. В этой связи интерес представляет комбинированный препарат –Домперидон+Омепразол (фиксированная комбинация омепразола 20 мг и домперидона модифицированного высвобождения 30 мг). Клиническая эффективность обеспечивается потенцированием действия препаратов разных фармакологических групп, высоким комплаенсом (однократный прием в течение суток). Домперидон с модифицированным освобождением позволяет принимать препарат один раз в день вместо трехразового прием. При этом отсутствуют пиковые значения концентраций домперидона, возможные при использовании его обычных лекарственных форм, что снижает вероятность проявления нежелательных дозозависимых явлений. Концентрация домперидона в плазме крови на фоне применения фиксированной комбинации омепразола 20 мг с домперидоном модифицированного высвобождения 30 мг не выходит за пределы однократной дозы 10 мг, что позволяет назначать препарат для курсового лечения симптомов диспепсии [127].
- Пациентам с хроническим гастритом и симптомами диспепсии для купирования этих симптомов рекомендуется лечение #ребамипидом (100 мг 3 раза в сутки в течение 2-4 недель, при необходимости 8 недель) как в монотерапии, так и в составе комплексного лечения [128]. Уровень убедительности рекомендаций A (уровень достоверности доказательств – 1).
Комментарии: Согласно метаанализу 17 РКИ ребамипид достоверно уменьшает симптомы диспепсии не только при функциональной диспепсии, но и при гастрите, индуцированным НПВП[128].
3.3. Эндоскопическое лечение
- Пациентам с хроническим гастритом при обнаружении эндокопически видимых патологических участков дисплазии низкой или высокой степени, а также раннего рака показано определение стадии процесса и соответствующее лечение, в том числе, эндоскопическая резекция единым блоком [129, 130, 46, 47].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2)
Комментарии: Дисплазия эпителия представляет собой гистологически однозначный неопластический эпителий (клеточный атипизм, нарушение гистоархитектоники) без достоверных признаков инвазии и служит предпоследней стадией канцерогенеза желудка[131, 132]. При наблюдении за пациентами с дисплазией высокой степени в течение 4-48 месяцев доля пациентов с развитием рака или метахронным раком составила 60-85%; при наблюдении за пациентами с дисплазией низкой степени в течение 10-48 месяцев развитие рака наблюдалось в 0-23% случаев [130]. Метаанализ показывает, что при проведении биопсии при дисплазии низкой степени после патолого-анатомического исследования диагноз дисплазии высокой степени устанавливают в 25% случаев, диагноз рака – в 7% [129]. Таким образом, при выявлении патологического участка эпителиальной дисплазии взятие биоптатов малоэффективно для точного диагноза и эндоскопическое лечение служит тактикой выбора.
7. Дополнительная информация (в том числе факторы, влияющие на исход заболевания или состояния)
Нет.
Медицинская реабилитация
4. Медицинская реабилитация и санаторно-курортное лечение, медицинские показания и противопоказания к применению методов реабилитации, в том числе основанных на использовании природных лечебных факторов
- Пациентам с хроническим гастритом в стадии ремиссии рекомендуется санаторно- курортное лечение [133].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии:На санаторно-курортное лечение не направляют пациентов с противопоказаниями к курортному лечению, а также к проведению любых бальнеологических процедур (например, пациенты с болезнью Менетрие, с полипозом желудка и новообразованиями желудка). Следует обязательно учитывать возраст и наличие сопутствующих заболеваний, что определяет выбор климатического региона. Ведущими методами санаторно-курортного этапа реабилитации служат немедикаментозные: естественные природные факторы (климат, минеральная вода, лечебная грязь), искусственно моделированные природные факторы, кинезотерапия (разнообразные формы и средства ЛФК, медицинский массаж), психотерапия, диетотерапия, фитотерапия и другие. Реабилитация пациентов на санаторном этапе происходит в соответствии с режимами – щадящим, тонизирующим и тренирующим, которые выбираются в зависимости от времени пребывания в санатории, характера заболевания и адаптационных возможностей организма. Больным хроническим гастритом со сниженной секреторной функцией желудка назначают питьевые средне- и высокоминерализованные хлоридно-натриевые, гидрокарбонатные натриевые водами (курорты Бобруйск, Горячий Ключ, Ессентуки, Нальчик, Старая Русса, Усть-Качка, Юрмала и др.). С целью стимуляции секреции желудочного сока и соляной кислоты минеральную воду назначают за 15-20 минут до еды, 3 раза в день. Больным хроническим гастритом с повышенной секреторной функцией желудка назначают питьевые слабо- и среднеминерализованные углекислые гидрокарбонатные натриевые, натриево-кальциевые, сульфатные кальциево-магниево-натриевыми воды (Боржоми, Березовские минеральные воды, Дарасун, Железноводск, Ижевские минеральные воды и др.). Минеральную воду назначают за 1-1,5 часа до еды, 3 раза в день[133].
Госпитализация
6. Организация оказания медицинской помощи
Большинство пациентов с гастритом подлежат наблюдению и лечению в амбулаторных условиях.
Показаниями к плановой госпитализации пациентов с гастритом и дуоденитом служат необходимость проведения дифференциального диагноза при редких формах гастрита (эозинофильный, гранулематозный и др.), выраженная анемия при аутоиммунном гастрите, выраженная клиническая картина заболевания при эрозивном гастрите, необходимость проведения эрадикационной терапии H.pylori под непосредственным врачебным контролем, необходимость выполнения эндоскопической резекции аденомы и раннего рака желудка.
Продолжительность стационарного лечения пациентов с обострением гастрита должна составлять 16 дней.
Показанием к экстренной госпитализации является наличие признаков острого желудочно- кишечного кровотечения у пациента с подозрением на эрозивный гастрит и/или дуоденит.
Профилактика
5. Профилактика и диспансерное наблюдение, медицинские показания и противопоказания к применению методов профилактики
- Всем лицам с наличием инфекции H.pylori при отсутствии противопоказаний рекомендуется проведение эрадикационной терапии с целью профилактики рака желудка [134, 135, 136, 137, 138, 6, 7, 8, 46, 47, 66].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 2)
Комментарии: Эрадикация инфекции H.pylori признана основным методом профилактики рака желудка, эффективность которого доказана в ряде популяционных исследований и в метаанализах [134-138]. В метаанализе 7 РКИ, включавшем 8323 человека, эрадикация H.pylori снизила заболеваемость раком желудка по сравнению с лицами, которые не получали эрадикационную терапию, с показателем относительного риска 0,54 (95% ДИ 0,40 — 0,72;NNT=72), а также смертность от рака желудка с показателем относительного риска 0,61 (95% CI 0,40 – 0,92;NNT=135) [135].
- Всем пациентам, которые перенесли эндоскопическую резекцию аденомы/раннего рака желудка, рекомендуется эрадикационная терапия H.pylori для профилактики метахронного рака желудка [135, 139-141, 6, 7, 8, 46, 47, 66, 142].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 1)
Комментарии: Снижение частоты метахронного рака желудка у пациентов после эрадикации H.pylori по сравнению с группой с персистенцией инфекции доказано в РКИ и метаанализах [135, 139-141]. Так, в метаанализе 3 исследований, включавшем 1841 пациента с эндоскопической резекцией эпителиальной дисплазии/неоплазии, эрадикационная терапия снизила заболеваемость раком желудка с показателем относительного риска 0,49(95% ДИ 0,34 – 0,70, NNT=21) [135].
- Пациентам с выявленной дисплазией слизистой оболочки желудка в отсутствие видимого при эндоскопии отграниченного новообразования рекомендуется незамедлительно выполнить повторное эндоскопическое исследование высокого разрешения с хромоэндоскопией (виртуальной или с использованием красителей). В случае, если при проведении повторного исследования вновь не удается выявить отграниченное новообразование, рекомендуется выполнить биопсию для определения стадии гастрита (если это не сделано ранее) и контрольное эндоскопическое исследование не позднее, чем через 6 месяцев (при дисплазии высокой степени), и не позднее, чем через 12 месяцев (при дисплазии низкой степени)[143-150, 46, 47].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
- Пациентам со слабой и умеренной степенью атрофии слизистой оболочки, ограниченной только антральным отделом желудка, после успешной эрадикационной терапии H.pylori эндоскопическое наблюдение не рекомендуется [143-150, 46, 47].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
- Пациентам с кишечной метаплазией, ограниченной одной анатомической областью, в большинстве случаев не рекомендуется наблюдение, особенно если высококачественное эндоскопическое исследование с биопсией позволило исключить выраженные стадии атрофического гастрита. Однако при наличии у таких пациентов отягощенного по раку желудка семейного анамнеза, неполной кишечной метаплазии, персистенции инфекции H.pylori им рекомендуется эндоскопическое наблюдение с хромоэндоскопией и прицельной биопсией 1 раз в 3 года[143-152, 46, 47].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Пациентам с выраженным атрофическим гастритом (выраженная атрофия и/или кишечная метаплазия и в теле, и в антральном отделе желудка — OLGA/OLGIM III/IV) рекомендуется высококачественное эндоскопическое наблюдение каждые 3 года.Пациентам с выраженным атрофическим гастритом с отягощенным наследственным анамнезом по раку желудка рекомендуется эндоскопическое наблюдение 1 раз в 1—2 года[ 143-152, 46, 47]. Согласно приказу Министерства здравоохранения РФ от 29 марта 2019 г. № 173н “Об утверждении порядка проведения диспансерного наблюдения за взрослыми” диспансерное наблюдение при хроническом атрофическом фундальном и мультифокальном гастрите предусматривает прием (осмотр, консультация) врача-гастроэнтеролога 1 раз в год, прием (осмотр, консультация) врача-онколога по медицинским показаниям c контролируемым показателем стабилизации морфологических изменений по данным ЭГДС с биопсией.
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 3)
Комментарии: Для определения интервалов эндоскопического наблюдения предложена стратификация пациентов на основании выраженности предраковых изменений желудка и наличия дополнительных факторов риска рака желудка. Очевидно, что лица с выраженной атрофией и кишечной метаплазией слизистой оболочки желудка продолжают нуждаться в эндоскопическом наблюдении даже несмотря на ликвидацию инфекции H.pylori в результате успешной ее терапии [6, 7, 8, 46, 47, 142]. Популяционное исследование (405172 человека, за период 1979-2011) показало, что у лиц, которые проходили эндоскопическое исследование с биопсией в связи с неонкологическими показаниями, в течение 20 лет рак желудка развивается в одном случае из 256 с нормальной слизистой оболочкой желудка, в 1 из 85 с гастритом, в 1 из 50 с атрофическим гастритом, в 1 из 39 с кишечной метаплазией и в 1 случае из 19 с дисплазией [143]. В когортном исследовании при наблюдении 1755 пациентов с диспепсией в среднем в течение 55 месяцев неоплазия была выявлена исключительно у лиц с иcходными стадиями OLGAIII-IV. Риск неоплазии отсутствовал у пациентов со стадией OLGA 0, I и II (95% ДИ 0 – 0,4), составил 36,5 на 1000 человеко-лет при стадии III (95% ДИ 13,7 – 97,4) и 63,1 на 1000 человеко-лет при стадии IV (95% ДИ 20,3 – 195,6) [144].Стадии OLGAIII/IVиOLGIMI – IVоказались независимыми факторами риска рака желудка, причем даже незначительно выраженная кишечная метаплазия существенно повышала риск рака желудка [145, 146]. Данные исследования показывают, что наличие кишечной метаплазии (как маркера выраженного гастрита) может иметь даже большее значение, чем степень атрофии без кишечной метаплазии, поскольку риск рака желудка был выше с OLGIM I / II, чем с OLGA III / IV. Неполная кишечная метаплазия -прогностически неблагоприятный фактор развития рака желудка по сравнению с полной кишечной метаплазией, ее следует рассматривать как дополнительное условие определения сроков наблюдения пациентов с гастритом [148- 150]. Дополнительным фактором риска рака желудка служит наличие близких родственников, страдающих раком желудка [151, 152].
- Пациентам с аутоиммунным гастритом рекомендуется эндоскопическое наблюдение 1 раз в 1-2 года [46, 47].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5)
Комментарии: Аутоиммунный гастрит является предраковым заболеванием, что оправдывает эндоскопическое наблюдение. Так, относительный риск рака желудка при пернициозной анемии составил 6,8 (95% ДИ 2,6–18,1).Недостатком этого метаанализа служит включение любых пациентов с низким уровнем витамина B12, причиной которого служит не только аутоиммунный гастрит [153]. Через 3 года после первичного скринингового обследования у 56 пациентов были выполнены контрольные ЭГДС, в ходе которых было выявлено 2 пациента с аденокарциномой желудка, ни одного пациента с дисплазией высокой степени и 49 пациентов с кишечной метаплазией [154]. В другом исследовании в течение 6-7 лет не было выявлено случаев рака желудка [155]. Согласно приказу Министерства здравоохранения РФ от 29 марта 2019 г. № 173н “Об утверждении порядка проведения диспансерного наблюдения за взрослыми” диспансерное наблюдение при хроническом атрофическом фундальном и мультифокальном гастрите предусматривает прием (осмотр, консультация) врача- гастроэнтеролога 1 раз в год, прием (осмотр, консультация) врача-онколога по медицинским показаниям c контролируемым показателем стабилизации морфологических изменений по данным ЭГДС с биопсией. Рекомендуемый интервала наблюдения не разработан в рандомизированных контролируемых исследованиях. Учитывая кроме риска аденокарциномы желудка риск развития нейроэндокринной опухоли желудка, сочетание с другими заболеваниями, ассоциированными с повышенным риском новообразований желудочно-кишечного тракта, а также сроки диспансеризации в соответствии с приказом №173н, мы рекомендуем эндоскопический контроль 1 раз в 1-2 года.
Информация
Источники и литература
-
Клинические рекомендации Российской гастроэнтерологической ассоциации
- 1. Marshall B.J., Warren J.R. Unidentified curved bacilli in the stomach of patients with gastritis and peptic ulceration. Lancet. 1984; 1(8390):1311-1315. doi: 10.1016/s0140- 6736(84)91816-6.
2. Kusters J.G., van Vliet A.H., Kuipers E.J. Pathogenesis of Helicobacter pylori infection. ClinMicrobiolRev. 2006; 19(3):449-490. doi:10.1128/CMR.00054-05.
3. Graham D.Y., Opekun A.R., Osato M.S., El-Zimaity H.M., Lee C.K., et Y. et al. Challenge model for Helicobacter pylori infection in human volunteers. Gut. 2004; 53(9): 1235-1243. doi: 10.1136/gut.2003.037499.
4. Ansari S., Yamaoka Y. Helicobacter pylori Virulence Factors Exploiting Gastric Colonization and its Pathogenicity. Toxins (Basel). 2019; 11(11):677. doi: 10.3390/toxins11110677.
5. El-Omar E.M., Carrington M., Chow W.H., McColl K.E., Bream J.H., Young H.A., Herrera J., Lissowska J., Yuan C.C., Rothman N., Lanyon G., Martin M., Fraumeni J.F. Jr., Rabkin
C.S. Interleukin-1 polymorphisms associated with increased risk of gastric cancer.Nature. 2000; 404(6776):398-402. doi: 10.1038/35006081.
6. Malfertheiner P., Megraud F., O’Morain C.A., Gisbert J.P., Kuipers E.J., Axon A.T., et al. European Helicobacter and Microbiota Study Group and Consensus panel. Management of Helicobacter pylori infection-the Maastricht V/Florence Consensus Report. Gut. 2017;66(1):6-30. doi: 10.1136/gutjnl-2016-312288.
7. Sugano K., Tack J., Kuipers E.J., Graham D.Y., El-Omar E.M., Miura S. et al. Kyoto global consensus report on Helicobacter pylorigastritis Gut 2015;64:1353–1367. doi: 10.1136/gutjnl- 2015-309252.
8. Ивашкин В.Т., Маев И.В., Каприн А.Д., Агапов М.Ю., Андреев Д.Н., Водолеев А.С., и соавт. Раннее выявление онкологических заболеваний органов пищеварения (методическое руководство Российской гастроэнтерологической ассоциации и Ассоциации онкологов России для врачей первичного звена здравоохранения). Рос журн гастроэнтерол гепатол колопроктол. 2019;29(5):53–74. doi:10.22416/1382-4376- 2019-29-5-53-74. Ivashkin V.T., Mayev I.V., Kaprin A.D., Agapov M.Yu., Andreev D.N., Vodoleev A.S., et al. Early Detection of Oncological Diseases of the Digestive System (Guidelines of the Russian Gastroenterological Association and the Russian Association of Oncologists for Primary Care Physicians). Rus J Gastroenterol Hepatol Coloproctol. 2019;29(5):53-74. (In Russ.) https://doi.org/10.22416/1382-4376-2019- 29-5-53-749. Симаненков В.И., Маев И.В., Ткачева О.Н, Алексеенко С.А., Андреев Д.Н., Бордин Д.С. и соавт. Синдром повышенной эпителиальной проницаемости в клинической практике. Мультидисциплинарный национальный консенсус. Кардиоваскулярная терапия и профилактика. 2021;20(1):2758. doi:10.15829/1728-8800-2021-2758.
Simanenkov V.I., Maev I.V., Tkacheva O.N., Alekseenko S.A., Andreev D.N., Bordin D.S., et al. Syndrome of increased epithelial permeability in clinical practice.
Multidisciplinary national Consensus. Cardiovascular Therapy and Prevention. 2021;20(1):2758. (In Russ.) https://doi.org/10.15829/1728-8800-2021-275810. Hall S.N., Appelman H.D. Autoimmune Gastritis. Arch Pathol Lab Med. 2019; 143(11):1327-1331. doi: 10.5858/arpa.2019-0345-RA.
11. Rodriguez-Castro K.I., Franceschi M., Miraglia C., Russo M., Nouvenne A., Leandro G., et al. Autoimmune diseases in autoimmune atrophic gastritis. Acta Biomed. 2018; 89(8-S):100- 103. doi: 10.23750/abm.v89i8-S.7919.
12. Лосик Е.А., Селиванова Л.С., Антонова Т.В., Лапина Т.Л., Тертычный А.С., Ивашкин В.Т. Морфологические критерии диагноза аутоиммунного гастрита. Российскийжурнал гастроэнтерологии, гепатологии, колопроктологии. 2016;26(5):13-
20. doi:10.22416/1382-4376-2016-26-5-13-20. Losik Y.A., Selivanova L.S., Antonova T.V., Lapina T.L., Tertychny A.S., Ivashkin V.T. Morphological diagnostic criteria of autoimmune gastritis. Rus J Gastroenterol Hepatol Coloproctol. 2016;26(5):13-20. (In
Russ.) https://doi.org/10.22416/1382-4376-2016-26-5-13-20
13. Герман С.В., Зыкова И.Е., Модестова А.В., Ермаков Н.В. Распространенность инфекции H. pylori среди населения Москвы. Рос журн гастроэнтерол гепатол колопроктол. 2010;20(2):25-30. German S.V., Zykova I.Ye., Modestova A.V., Yermakov
N.V. Prevalence of H. pylori infection in the Moscow population. Rus J Gastroenterol Hepatol Coloproctol. 2010;20(2):25-30. (In Russ.)
14. Рахманин Ю.А., Зыкова И.Е., Федичкина Т.П., Соленова Л.Г., Герман С.В., Модестова А.В., Кислицин В.А. Изучение территориального раcпределения инфицированности Helicobacter pylori трудоспособного населения г. Москвы в ходе диспансеризации производственных контингентов. Гигиена и санитария 2013; 92(5):79-82. Rakhmanin Yu.A., Zykova I. Ye., Fedichkina T.P., Solenova L.G., German S.V., Modestova A.V., Kislitsin V.A. Regional distribution of Helicobacter pylori infection of able-bodied population of Moscow at medical examination of the production staff. Gigiyena i sanitariya 2013; 92(5):79-82
15. Сварваль А.В., Ферман Р.С., Жебрун А.Б. Изучение динамики превалентности инфекции, обусловленной Helicobacter pylori, среди различных возрастных групп населения Санкт-Петербурга в 2007-2011 годах. Инфекция и иммунитет. 2012. 2(4):741- 6.
16. Решетников О.В., Курилович С.А., Кротов С.А., Кротова В.А. Хеликобактерная инфекция в сибирских популяциях. Бюл. СОРАМН. 2010; 30(2):88-93.
17. Цуканов В.В., Третьякова О.В., Амельчугова О.С. и др. Распространенность атрофического гастрита тела желудка у населения г. Красноярска старше 45 лет. Рос журн гастроэнтерол гепатол колопроктол 2012; 22(4): 27-31. Tsukanov V.V., Tretyakova O.V., Amelchugova O.S. et al. Prevalence of atrophic corpus gastritis at Krasnoyarsk over 45 year-old population. Rus J Gastroenterol Hepatol Coloproctol. 2012;22(4):27-31. (In Russ.)
18. Штыгашева О.В., Цуканов В.В. Распространенность инфекции Helicobacterpyloriи частота диспептических жалоб у населения Хакасии. Рос журн гастроэнтерол гепатол колопроктол. 2004; 14(1):33-36. Shtygasheva O.V., Tsukanov V.V. Prevalence of Helicobacter pylori infection and frequency of dispeptic symptoms in Khakasia population. Rus J Gastroenterol Hepatol Coloproctol. 2004;14(1):33-36. (In Russ.)
19. Dixon M.F., Genta R.M., Yardley J.H., Correa P. Classification and grading of gastritis. The updated Sydney System. International Workshop on the Histopathology of Gastritis, Houston 1994. Am. J. Surg. Pathol. 1996; 20(10):1161-81. doi: 10.1097/00000478-199610000-00001.
20. Uemura N., Okamoto S., Yamamoto S., Matsumura N., Yamaguchi S., Yamakido M. et al. H. pylori infection and the development of gastric cancer. N Engl J Med. 2001; 345:784–9. doi: 10.1056/NEJMoa001999.
21. Meining A., Bayerdörffer E., Müller P. et al. Gastric carcinoma risk index in patients infected with Helicobacter pylori. Virchows Arch. 1998; 432(4):311–14. doi: 10.1007/s004280050171.
22. Miehlke S., Hackelsberger A., Meining A., Hatz R., Lehn N., Malfertheiner P. et al. Severe expression of corpus gastritis is characteristic in gastric cancer patients infected with Helicobacter pylori. Br J Cancer. 1998; 78(2):263–6. doi: 10.1038/bjc.1998.475.
23. Rugge M., Meggio A., Pennelli G., Piscioli F., Giacomelli L., De Pretis G. et al. Gastritis staging in clinical practice: the OLGA staging system. Gut. 2007; 56(5): 631–636. doi: 10.1136/gut.2006.106666.
24. Аруин Л.И., Кононов А.В., Мозговой С.И. Международная классификация хронического гастрита: что следует принять и что вызывает сомнения. Архив патологии. 2009; 71(4):11-18.25. Кононов А.В., Потрохова Е.А., Мозговой С.И., Поморгайло Е.Г., Новиков Д.Г. Новая медицинская технология «Молекулярно-генетическая методика прогноза и патоморфологический мониторинг риска развития рака желудка кишечного типа при Helicobacter pylori-инфекции», разрешение Федеральной службы в сфере здравоохранения и социального развития № 2010/220 от 10 июня 2010 г., серия АА 0000001.
26. Capelle L.G., de Vries A.C., Haringsma J., Borg F.T., de Vries R.A., Bruno M. et al. The staging of gastritis with the OLGA system by using intestinal metaplasia as an accurate alternative for atrophic gastritis. GastrointestEndosc. 2010; 71(7):1150-1158. doi: 10.1016/j.gie.2009.12.029.
27. Kimura K., Takemoto T. An endoscopic recognition of the atrophic border and its significance in chronic gastritis. Endoscopy. 1969;1(3):87–97. doi: 10.1055/s-0028-1098086.
28. Miwata T., Quach D.T., Hiyama T., Aoki R., Le H.M., Tran P.L. et al. Interobserver and intraobserver agreement for gastric mucosa atrophy. BMC Gastroenterol. 2015; 15:95. doi: 10.1186/s12876-015-0327-x.
29. Song J.H., Kim S.G., Jin E.H., Lim J.H., Yang S.Y. Risk Factors for Gastric Tumorigenesis in Underlying Gastric Mucosal Atrophy. Gut Liver. 2017; 11(5):612-619. doi: 10.5009/gnl16488.
30. Pimentel-Nunes P., Libânio D., Lage J., Abrantes D., Coimbra M., Esposito G. et al. A multicenter prospective study of the real-time use of narrow-band imaging in the diagnosis of premalignant gastric conditions and lesions. Endoscopy. 2016; 48(8):723-30. doi: 10.1055/s- 0042-108435.
31. Кононов А.В., Мозговой С.И., Шиманская А.Г. Прижизненная патолого-анатомическая диагностика болезней органов пищеварительной системы. Клинические рекомендации Российского общества патологоанатомов. Практическая медицина. 2019.
32. Ивашкин В.Т., Маев И.В., Шептулин А.А., Лапина Т.Л., Трухманов А.С., Картавенко И.М., Киприанис В.А., Охлобыстина О.З. Клинические рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению функциональной диспепсии. Рос журн гастроэнтерол гепатол колопроктол. 2017; 27(1):50-61. doi: 10.22416/1382-4376-2017-27-1-50-61. Ivashkin V.T., Mayev I.V., Sheptulin A.A., Lapina T.L., Trukhmanov A.S., Kartavenko I.M., Kiprianis V.A., Okhlobystina O.Z. Diagnosis and treatment of the functional dyspepsia: clinical guidelines of the Russian Gastroenterological Association. Rus J Gastroenterol Hepatol Coloproctol. 2017;27(1):50-61. (In Russ.) https://doi.org/10.22416/1382-4376-2017-27-1-50-61
33. Ивашкин В.Т., Маев И.В., Царьков П.В., Королев М.П., Андреев Д.Н., Баранская Е.К., и соавт. Диагностика и лечение язвенной болезни у взрослых (Клинические рекомендации Российской гастроэнтерологической ассоциации, Российского общества колоректальных хирургов и Российского эндоскопического общества). Рос журн гастроэнтерол гепатол колопроктол. 2020;30(1):49-70. doi:10.22416/1382-4376-2020-30- 1-49-70. Ivashkin V.T., Maev I.V., Tsar’kov P.V., Korolev M.P., Andreev D.N., Baranskaya E.K., et al. Diagnosis and Treatment of Peptic Ulcer in Adults (Clinical Guidelines of the Russian Gastroenterological Association, Russian Society of Colorectal Surgeons and the Russian Endoscopic Society). Rus J Gastroenterol Hepatol Coloproctol. 2020;30(1):49-70. (In Russ.) https://doi.org/10.22416/1382- 4376-2020-30-1-49-7034. Carabotti M., Lahner E., Esposito G., Sacchi M.C., Severi C., Annibale B. Upper gastrointestinal symptoms in autoimmune gastritis: A cross-sectional study. Medicine (Baltimore). 2017; 96(1):e5784. doi:10.1097/MD.0000000000005784.
35. Miceli E., Lenti M.V., Padula D., Luinetti O., Vattiato C., Monti C.M. et al. Common features of patients with autoimmune atrophic gastritis. Clin Gastroenterol Hepatol. 2012 Jul;10(7):812-4. doi: 10.1016/j.cgh.2012.02.018.
36. Tenca A., Massironi S., Pugliese D., Consonni D., Mauro A., Cavalcoli F. et al. Gastro- esophageal reflux and antisecretory drugs use among patients with chronic autoimmune atrophic gastritis: a study with pH-impedance monitoring. NeurogastroenterolMotil. 2016; 28(2):274-80. doi:10.1111/nmo.12723.
37. Pruthi H.S., Sharma S.K., Singh B., Anand A.C. AETIOLOGY OF UPPER GASTROINTESTINAL HAEMORRHAGEAN ENDOSCOPIC STUDY. Med J Armed Forces India. 2000; 56(3):188-191. doi:10.1016/S0377-1237(17)30162-4.
38. Biecker E. Diagnosis and therapy of non-variceal upper gastrointestinal bleeding. World J Gastrointest Pharmacol Ther. 2015; 6(4):172-82. doi: 10.4292/wjgpt.v6.i4.172.
39. Лосик Е.А., Ивашкин В.Т. Гематологические проявления аутоиммунного гастрита. Рос журн гастроэнтерол гепатол колопроктол. 2016;26(1):37-43. doi:10.22416/1382-4376-2016-26=1-37-43. Losik Y.A., Ivashkin V.T. Hematological manifestations of autoimmune gastritis. Rus J Gastroenterol Hepatol Coloproctol. 2016;26(1):37-43. (In Russ.) https://doi.org/10.22416/1382-4376-2016-26-1-37-4340. Rusak E., Chobot A., Krzywicka A., Wenzlau J. Anti-parietal cell antibodies — diagnostic significance. Adv Med Sci. 2016; 61(2):175-179. doi: 10.1016/j.advms.2015.12.004.
41. Lahner E., Norman G.L., Severi C., Encabo S., Shums Z., Vannella L. et al. Reassessment of intrinsic factor and parietal cell autoantibodies in atrophic gastritis with respect to cobalamin deficiency. Am J Gastroenterol. 2009; 104(8):2071-9. doi: 10.1038/ajg.2009.231.
42. Huang Y.K., Yu J.C., Kang W.M., Ma Z.-Q., Ye X., Tian S.-B. et al. Significance of serum pepsinogens as a biomarker for gastric cancer and atrophic gastritis screening: a systematic review and meta-analysis. PLoS One. 2015; 10(11):e0142080. doi: 10.1371/journal.pone.0142080.
43. Zagari R.M., Rabitti S., Greenwood D.C., Eusebi L.H., Vestito A., Bazzoli F. Systematic review with meta-analysis: diagnostic performance of the combination of pepsinogen, gastrin- 17 and anti-Helicobacter pylori antibodies serum as- says for the diagnosis of atrophic gastritis. Aliment PharmacolTher. 2017; 46(7):657 – 667. doi: 10.1111/apt.14248.
44. Watabe H., Mitsushima T., Yamaji Y., Okamoto M., Wada R., Kokubo T. et al. Predicting the development of gastric cancer from combining Helicobacter pylori antibodies and serum pepsinogen status: a prospective endoscopic cohort study. Gut. 2005; 54(6):764–8. doi: 10.1136/gut.2004.055400.
45. Kurilovich S., Belkovets A., Reshetnikov O., Openko T., Malyutina S., Ragino Y. et al. Stomach-specific Biomarkers (GastroPanel) Can Predict the Development of Gastric Cancer in a Caucasian Population: A Longitudinal Nested Case-Control Study in Siberia. Anticancer Res. 2016; 36(1):247-53. PMID: 26722050.
46. Pimentel-Nunes P., Libânio D., Marcos-Pinto R., Areia M., Leja M., Esposito G. et al. Management of epithelial precancerous conditions and lesions in the stomach (MAPS II): European Society of Gastrointestinal Endoscopy (ESGE), European Helicobacter and Microbiota Study Group (EHMSG), European Society of Pathology (ESP), and Sociedade Portuguesa de EndoscopiaDigestiva (SPED) guideline update 2019. Endoscopy. 2019; 51(4):365-388. doi: 10.1055/a-0859-1883.
47. Banks M., Graham D., Jansen M., Gotoda T., Coda S., di Pietro M. et al. British Society of Gastroenterology guidelines on the diagnosis and management of patients at risk of gastric adenocarcinoma. Gut. 2019; 68(9):1545-1575. doi: 10.1136/gutjnl-2018-318126.
48. Zhao Z., Yin Z., Wang S., Wang J., Bai B., Qiu Z. et al. Meta-analysis: The diagnostic efficacy of chromoendoscopy for early gastric cancer and premalignant gastric lesions. J GastroenterolHepatol. 2016; 31(9): 1539 – 1545. doi: 10.1111/jgh.13313.
- 1. Marshall B.J., Warren J.R. Unidentified curved bacilli in the stomach of patients with gastritis and peptic ulceration. Lancet. 1984; 1(8390):1311-1315. doi: 10.1016/s0140- 6736(84)91816-6.
Информация
Список сокращений
ДИ – доверительный интервал
ИПН– ингибиторы протонного насоса
Н.рylori – Helicobacter pylori
НПВП – нестероидные противовоспалительные и противоревматические препараты
ОР – относительный риск
ОШ – отношение шансов
ЭГДС –эзофагогастродуоденоскопия
ФД – функциональная диспепсия
Термины и определения
Эрадикация – лечение, направленное на уничтожение инфекции Helicobacterpylori (H.pylori)
Схема эрадикации 1-й линии — схема эрадикации инфекции H pylori, которая назначается в первую очередь.
Схема эрадикации 2-й линии — схема эрадикации, которая назначается при неэффективности схемы 1-й линии H.pylori.
Критерии оценки качества медицинской помощи
Приложение А1. Состав рабочей группы по разработке и пересмотру клинических рекомендаций
Абдулхаков Рустам Аббасович — доктор медицинских наук, профессор, член Российской гастроэнтерологической ассоциации. Конфликт интересов отсутствует.
Алексеева Ольга Поликарповна- доктор медицинских наук, профессор, член Российской гастроэнтерологической ассоциации. Конфликт интересов отсутствует.
Алексеенко Сергей Алексеевич — доктор медицинских наук, профессор, член Российской гастроэнтерологической ассоциации. Конфликт интересов отсутствует.
Андреев Дмитрий Николаевич, кандидат медицинских наук, доцент, член Российской гастроэнтерологической ассоциации. Конфликт интересов отсутствует.
Баранская Елена Константиновна – доктор медицинских наук, профессор, лауреат премии Правительства РФ в области науки и техники в 2007 г., член Российской гастроэнтерологической ассоциации. Конфликт интересов отсутствует.
Дехнич Наталья Николаевна – кандидат медицинских наук, член Межрегиональной ассоциации по клинической микробиологии и антимикробной химиотерапии.
Ивашкин Владимир Трофимович – доктор медицинских наук, профессор, академик РАН, дважды лауреат премии Правительства РФ в области науки и техники в 2007 г., в области образования – в 2013 г., заслуженный врач РФ, заслуженный деятель науки РФ, Президент Российской гастроэнтерологической ассоциации. Конфликт интересов отсутствует.
Кляритская Ирина Львовна — доктор медицинских наук, профессор, член Российской гастроэнтерологической ассоциации. Конфликт интересов отсутствует.
Козлов Роман Сергеевич – доктор медицинских наук, профессор, президент Межрегиональной ассоциации по клинической микробиологии и антимикробной химиотерапии. Конфликт интересов отсутствует.
Коган Евгения Алтаровна — доктор медицинских наук, профессор, лауреат премии Правительства РФ в области науки и техники в 2007 г., член Российского общества патологоанатомов.Конфликт интересов отсутствует.
Кононов Алексей Владимирович — доктор медицинских наук, профессор, член Российского общества патологоанатомов.Конфликт интересов отсутствует.
Королев Михаил Павлович – доктор медицинских наук, профессор, председатель Российского эндоскопического общества, член Российского общества хирургов. Конфликт интересов отсутствует
Корочанская Наталья Всеволодовна — доктор медицинских наук, профессор, член Российской гастроэнтерологической ассоциации. Конфликт интересов отсутствует.
Курилович Светлана Арсентьевна- доктор медицинских наук, профессор, член Российской гастроэнтерологической ассоциации. Конфликт интересов отсутствует.
Лапина Татьяна Львовна – кандидат медицинских наук, доцент, лауреат премии Правительства РФ в области науки и техники в 2007 г., член Российской гастроэнтерологической ассоциации. Конфликт интересов отсутствует.
Ливзан Мария Анатольевна — доктор медицинских наук, профессор, член Российской гастроэнтерологической ассоциации. Конфликт интересов отсутствует.
Маев Игорь Вениаминович, доктор медицинских наук, профессор, академик РАН, лауреат премии Правительства РФ в области науки и техники в 2006 г., заслуженный врач РФ, заслуженный деятель науки РФ, член Российской гастроэнтерологической ассоциации.
Конфликт интересов отсутствует.
Осипенко Марина Федоровна — доктор медицинских наук, профессор, член Российской гастроэнтерологической ассоциации. Конфликт интересов отсутствует.
Павлов Павел Владимирович — кандидат медицинских наук, член Российского эндоскопического общества. Конфликт интересов отсутствует.
Пирогов Сергей Сергеевич -доктор медицинских наук, член Российского эндоскопического общества. Конфликт интересов отсутствует.
СарсенбаеваАйманСилкановна — – доктор медицинских наук, профессор, член Российской гастроэнтерологической ассоциации. Конфликт интересов отсутствует.
Симаненков Владимир Ильич– доктор медицинских наук, профессор, член Российской гастроэнтерологической ассоциации. Конфликт интересов отсутствует.
Тертычный Александр Семенович — доктор медицинских наук, профессор, член Российского общества патологоанатомов. Конфликт интересов отсутствует.
Ткачев Александр Васильевич — доктор медицинских наук, профессор, член Российской гастроэнтерологической ассоциации. Конфликт интересов отсутствует.
Трухманов Александр Сергеевич – доктор медицинских наук, профессор, член Российской гастроэнтерологической ассоциации. Конфликт интересов отсутствует.
Успенский Юрий Павлович — доктор медицинских наук, профессор, член Российской гастроэнтерологической ассоциации. Конфликт интересов отсутствует.
Федоров Евгений Дмитриевич — доктор медицинских наук, профессор, заместитель председателя Российского эндоскопического общества. Конфликт интересов отсутствует.
Хлынов Игорь Борисович – доктор медицинских наук, профессор, член Российской гастроэнтерологической ассоциации. Конфликт интересов отсутствует.
Цуканов Владислав Владимирович – доктор медицинских наук, профессор, член Российской гастроэнтерологической ассоциации. Конфликт интересов отсутствует. Шептулин Аркадий Александрович — доктор медицинских наук, профессор, член Российской гастроэнтерологической ассоциации. Конфликт интересов отсутствует.
Приложение А2. Методология разработки клинических рекомендаций
Предлагаемые рекомендации имеют своей целью довести до практических врачей современные представления об этиологии и патогенезе гастрита и дуоденита, познакомить с применяющимся в настоящее время алгоритмом диагностики и лечения.
Целевая аудитория данных клинических рекомендаций
:
- Врачи-гастроэнтерологи
- Врачи общей практики (семейные врачи)
- Врачи-терапевты
- Врачи-эндоскописты
- Врачи-онкологи
Таблица 1.Шкала оценки уровней достоверности доказательств (УДД)для методов диагностики (диагностических вмешательств)
Таблица 2. Уровни достоверности доказательств с указанием использованной классификации уровней достоверности доказательств (УДД)
Таблица 3. Уровни убедительности рекомендаций (УУР) с указанием использованной классификации уровней убедительности рекомендаций
Порядок обновления клинических рекомендаций
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию – не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утверждённым КР, но не чаще 1 раза в 6 месяцев.
Приложение А3. Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата
Данные клинические рекомендации разработаны с учетом следующих нормативно-правовых документов:
- Приказ Министерства здравоохранения и социального развития Российской Федерации от 02.06.2010 № 415н “Об утверждении Порядка оказания медицинской помощи населению при заболеваниях гастроэнтерологического профиля”
- Приказ Министерства здравоохранения Российской Федерации от 10 мая 2017 г. № 203н «Об утверждении критериев оценки качества медицинской помощи».
- Приказ Министерства здравоохранения Российской Федерации от 22.11.2004 г. №248 “Об утверждении стандарта медицинской помощи больным хроническим гастритом, дуоденитом, диспепсией”.
- Приказ Министерства здравоохранения РФ от 29 марта 2019 г. № 173н “Об утверждении порядка проведения диспансерного наблюдения за взрослыми”
Приложение Б. Алгоритмы действий врача

Приложение В. Информация для пациента
Основным фактором, вызывающим гастрит, в настоящее время признан микроорганизм, называемый пилорическим геликобактером. Поэтому каждый пациент, у которого выявлен гастрит, должен быть обследован на наличие данной инфекции. При ее подтверждении необходимо проведение лечения, направленного на уничтожение данных бактерий (эрадикация) с последующим контролем через 4-6 недель. При неэффективности проведенного лечения следует провести повторный курс терапии с другой схемой назначения лекарственных средств. Важно соблюдать приверженность к лечению и строго контролировать прием лекарственных препаратов. Эрадикационная терапия, приводящая к уничтожению пилорического геликобактера, сейчас считается основной мерой, направленной на оздоровление слизистой оболочки желудка, и профилактику рака желудка. Наличие рака желудка у близких родственников (родители, бабушки и дедушки) служит дополнительным основанием для проведения лечения против пилорического геликобактера.
Приложение Г. Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях
Классификация атрофического гастрита по Кимура-Такемото [27, 28]. Рисунок воспроизведен из [156] в соответствии с Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/3.0).
Гастрит закрытого типа (closed type: C-1, C-2, C-3): граница атрофии распространяется по малой кривизне тела желудка.
Гастрит открытого типа (ореn type: О-1, О-2, О-3, Ор): граница атрофии распространяется по передней и задней стенкам желудка.
С-1 – атрофия ограничена антральным отделом
С-2 – атрофия распространяется выше угла желудка, но ограничена небольшой областью малой кривизны тела желудка
С-3 – атрофия занимает большую часть малой кривизны тела желудка, но не достигает кардии
О-1 – атрофия распространяется на тело желудка выше кардии; граница атрофии располагается между малой кривизной и передней стенкой
О-2 – граница атрофии проходит по передней стенке тела желудка
О-3 – атрофия занимает почти весь желудок; граница проходит между передней стенкой и большой кривизной
Ор — атрофический пангастрит
Эндоскопическая картина, соответствующая классификации атрофического гастрита по Кимура-Такемото [27, 28]. Граница атрофии обозначена прерывистой линией. A: C1; B: C2; C: C3; D: O1; E: O2; F: O3. Рисунок воспроизведен из [157] в соответствии с Creative Commons Attribution Non Commercial (CC BY-NC 4.0) license.
Прикреплённые файлы
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
Дата публикации 12 декабря 2018Обновлено 26 апреля 2021
Определение болезни. Причины заболевания
Хронический гастрит (ХГ) — это рецидивирующее, длительно текущее воспаление слизистой оболочки желудка, протекающее с её структурной перестройкой, приводящей к атрофии, дистрофии и дисрегенерации. В результате этих изменений происходит нарушение функции секреции соляной кислоты и пепсина (ферментов пищеварения), а также моторики и синтеза гастроинтестинальных гормонов.
Распространенность ХГ среди взрослого населения, по данным разных авторов, составляет 80-85%. Среди всех форм гастрита преобладает Helicobacter pylori ассоциированный ХГ, который составляет 85-90% всех форм ХГ. Распространенность инфекции Helicobacter pylori в РФ составляет до 80% взрослого населения.
Самой редкой формой ХГ является аутоиммунный гастрит (в три раза чаще встречается у женщин). В его основе лежит выработка антител к париетальным клеткам (продуцирующим ферменты пищеварения) и внутреннему фактору Касла (ферменту, превращающему неактивный B12 в активный).
Этиология
Все причины развития ХГ разделяются на две большие группы: предрасполагающие и причинные факторы.
К предрасполагающим факторам (создающим неблагоприятный фон и высокий риск развития ХГ) относятся:
- алиментарные погрешности (связанные с нерегулярным, неполноценным питанием);
- курение табака;
- наследственная предрасположенность;
- конституциональная отягощённость.
Причинные факторы делятся на внешние и внутренние.
Внешние причинные факторы хронического гастрита:
- инфекция Helicobacter Pylori (HP-инфекция);
- лекарственное повреждение слизистой оболочки желудка (отдельно стоит НПВС-гастрит);
- повреждение слизистой оболочки радиацией;
- другие инфекции, за исключением HP;
- алкогольный гастрит.
Внутренние причинные факторы хронического гастрита:
- рефлюкс (обратный ток) желчи;
- хроническая гипоксия (кислородное голодание);
- аутоиммунные процессы;
- нарушение обмена веществ;
- эндокринные дисфункции.
Предрасполагающие факторы под действием внешних и внутренних причинных факторов приводят к развитию и/или обострению ХГ.
Таким образом, в основе ХГ лежит не только воспалительный процесс, но и дисметаболические, дисрегенераторные, дистрофические и атрофические процессы в слизистой оболочки желудка, которые в итоге приводят к функциональной недостаточности органа.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы хронического гастрита
Неспецифические симптомы хронического гастрита можно разделить на следующие группы:
- болевой синдром;
- синдром желудочной диспепсии (нарушение пищеварения);
- общее недомогание.
Болевой синдром часто играет ведущую роль в клинической картине заболевания. Именно он чаще всего заставляет пациентов обратиться за помощью к врачу.
Где болит при гастрите
В большинстве случаев боль локализуется в эпигастрии (области, соответствующей проекции желудка на переднюю брюшную стенку), реже — в других отделах живота.
Признаком хронического гастрита с секреторной недостаточностью является боль сразу после приёма пищи, при ХГ с увеличенной секрецией боль чаще появляется спустя 1-1,5 часа после еды.
Синдром желудочной диспепсии характеризуется нарушением переваривания пищи, что сопровождается следующими симптомами:
- снижением аппетита;
- изжогой;
- тошнотой;
- отрыжкой;
- рвотой;
- дискомфортом в животе после приёма пищи.
Нарушения общего состояния организма в случае неосложнённых форм ХГ значительно не меняется. При нарастании степени воспалительных изменений слизистой желудка оно нарушается довольно часто. Могут наблюдаться:
- снижение веса;
- нарушение обмена витаминов (витаминов группы В, аскорбиновой кислоты);
- непереносимость некоторых продуктов и другое.
Очень часто в процесс вовлекаются печень, поджелудочная железа и кишечник. При длительно текущем ХГ появляются отклонения со стороны нервно-психической сферы.
В целом клиническую картину ХГ определяет характер нарушения желудочной секреции и моторно-эвакуаторной функции. Вначале заболевание длительное время протекает бессимптомно. Самым первым, как правило, возникает болевой синдром, далее по мере прогрессирования изменений в слизистой желудка присоединяются синдром диспепсии и общее недомогание. В клинической картине превалировать может любой из перечисленных выше синдромов.
Если не обращать внимания на симптомы заболевания, то ХГ будет прогрессировать, и изменения в слизистой оболочке станут необратимыми (атрофия и/или дисплазия). В финальной стадии заболевания может развиться рак желудка.
Патогенез хронического гастрита
В основе патогенеза ХГ лежит воспаление слизистой оболочки, приводящее к её структурной перестройке. При наличии предрасполагающих факторов и воздействии внешних или внутренних причин запускается процесс длительно текущего воспаления.
В основе хронического воспаления лежит круглоклеточная воспалительная инфильтрация нейтрофилами (видами лейкоцитов крови) и другими клетками иммунной системы слизистой желудка. В результате длительно текущей воспалительной реакции запускаются процессы перестройкой структуры слизистой оболочки желудка и развития в ней дисрегенераторных процессов (нарушенной регенерации) с последующим переходом в дистрофию и атрофию. Это в конечном итоге приводит к нарушению функции желудка, проявляющейся гипо- или ахлоргидрией (снижением или отсутствием соляной кислоты в желудочном соке) и желудочной ахилией.
В настоящее время ведущую роль в развитии ХГ занимает HP-инфекция (гастрит типа В). Патогенез воздействия данного возбудителя на желудок хорошо иллюстрирует каскад Correa, суть которого заключается в том, что хроническая инфекция Helicobacter Pylori вызывает изменения в тканях слизистой желудка.
Эта перестройка слизистой последовательно приводит к атрофии, кишечной метаплазии и дисплазии, с исходом в рак желудка. Развитие желудочной атрофии — это критический шаг перехода ХГ в рак желудка.
Вторым по частоте можно назвать лекарственный гастрит (тип С). При данном типе гастрита наиболее изучено влияние на желудок нестероидных противовоспалительных средств (НПВС). Прямого агрессивного действия они, как кислоты, не вызывают (соляная кислота в десятки раз агрессивнее). В основе патогенеза их действия на слизистую желудка лежит блокирование ферментов циклооксигеназы (изомеры ЦОГ-1 и ЦОГ-2). При блокировании ЦОГ-1 происходит подавление синтеза простогландинов (Е2 и I2), которые обеспечивают качество и прочность слизистого барьера (слизисто-бикарбонатного слоя), защищающего слизистую оболочку от агрессивного действия соляной кислоты и пепсина. Поэтому длительный приём НПВС приводит к истончению защитного слоя слизи и повышению агрессивного действия соляной кислоты на слизистую желудка, приводя к хроническому воспалению.
Самой редкой формой ХГ является аутоиммунный атрофический гастрит (гастрит типа А). До сих пор его этиология не известна. В основе лежит выработка иммунными клетками антител к обкладочным клеткам слизистой оболочки (синтезируют соляную кислоту) и внутреннему фактору Касла (участвует в усвоении железа в кишечнике). В результате этого развиваются воспалительные изменения, очень рано приводящие к атрофии и ахлоргидрии, часто сочетающейся с анемией Аддисона — Бирмера.
Классификация и стадии развития хронического гастрита
В настоящее время нет общепризнанной классификации заболевания. В клинической практике в РФ чаще всего используют рабочую классификацию, созданную на базе классификации С.М. Рысса и Хьюстонской модификации Сиднейской классификации ХГ. Она составлена с включением клинического и функционального разделов, с обозначением их (в духе Сиднейской системы) грамматическими терминами «флексия» (окончание). В группу ХГ типа С включены также лекарственные и профессиональные формы ХГ.[7]
Рабочая классификация ХГ
По этиологии и патогенезу (префикс):
- ХГ типа А: аутоиммунный фундальный атрофический, включая ассоциированный с мегалобластной анемией Аддисона — Бирмера;
- ХГ типа В: бактериальный антральный неатрофический, ассоциированный с НР-инфекцией;
- ХГ типа АВ: сочетанный атрофический пангастрит (с поражением всех отделов желудка).
По топографо-морфологическим особенностям (корень или ядро):
- по локализации:
- фундальный ХГ (тип А);
- антральный ХГ (тип В);
- пангастрит (тип АВ) с преимущественным поражением антрального или фундального отдела;
- по морфологическим критериям:
- поверхностный ХГ;
- интерстициальный ХГ;
- атрофический ХГ с лёгкой, средней или тяжёлой формой атрофии;
- ХГ с кишечной метаплазией (полной или неполной, тонкокишечной или толстокишечной).
По специфическим морфологическим признакам (суффикс):
- по выраженности воспалительного процесса в слизистой желудка:
- минимальный;
- незначительный;
- умеренный;
- выраженный (зависит от степени лимфоплазмоцитарной воспалительной инфильтрации слизистой желудка);
- по активности ХГ:
- активность отсутствует;
- лёгкая (I);
- средняя (II);
- ▪ высокая (III) (зависит от наличия и выраженности нейтрофильного — гранулоцитарного компонента в воспалительной инфильтрации слизистой желудка);
- по наличию и выраженности контаминации СОЖ НР-инфекцией:
- отсутствует;
- лёгкая (I);
- средняя (II);
- высокая (III);
По клиническим особенностям:
- ХГ (типа В) с преобладанием болевого синдрома (Gastritis dolorosa);
- ХГ (типа А) с преобладанием диспепсических явлений;
- ХГ с латентным (бессимптомным) течением (~50%).
По функциональным критериям (флексия) выделяют следующие формы хронического гастрита:
- ХГ с сохранённой (и повышенной) секрецией;
- ХГ с секреторной недостаточностью (умеренной, выраженной, тотальной).
Эндоскопические критерии ХГ:
- эритематозный (экссудативный) поверхностный ХГ;
- ХГ с плоскими (острыми) эрозиями;
- ХГ с возвышающимися (хроническими) эрозиями;
- геморрагический ХГ;
- гиперпластический ХГ;
- ХГ, осложнившийся ДГР (рефлюкс-гастрит).
При формулировке диагноза применяют следующий алгоритм: Префикс (этиология) — Корень (локализация) — Суффикс (морфология) — Флексия (функция) с добавлением эндоскопических критериев.
Пример постановки диагноза: Хронический хеликобактерный гастрит антрального отдела желудка с умеренно выраженным воспалением, средней степени активности, высокой контаминацией пилорическим хеликобактером с сохранённой секрецией.
В связи с большей доступностью морфологической оценки состояния слизистой желудка по результатам исследований биопсийного материала всё чаще применяется классификация ХГ по системе OLGA (Operative Link for Gastritis Assessment). Со временем морфологическая классификация ХГ станет ведущей в мире.
ХГ, как и все хронические заболевания, имеет две стадии: обострения и ремиссии, которые последовательно сменяют друг друга. С каждым обострением в слизистой происходят всё большие структурные изменения. Обострение и ремиссию ХГ можно подтверждать клинически или эндоскопически (наиболее точное подтверждение — по результатам ЭГДС и морфологии биопсийного материала).
Исходя из причины возникновения выделяют следующие виды хронического гастрита: вызванные инфекцией Helicobacter Pylori, лекарственный и аутоиммунный атрофический гастрит.
Вызванный заражением Helicobacter Pylori (HP-инфекция)
В настоящее время ведущую роль в развитии ХГ занимает HP-инфекция (гастрит типа В). Большинство взрослого населения старше 60 лет инфицировано данной бактерией. В России среди детей после 5 лет инфицировано 30 %, в возрасте 15-20 лет — 63 %, взрослые — более 85 % [10]. Патогенез воздействия данного возбудителя на желудок заключается в том, что хроническая инфекция Helicobacter Pylori вызывает изменения в тканях слизистой желудка. Длительное время инфекция протекает без симптомов. По мере распространения воспаления на тело желудка и повышении ответной реакции слизистой оболочки появляются первые симптомы гастрита. Чем длительнее протекает инфекция, тем сильнее перестройка структуры слизистой. Эта перестройка слизистой последовательно приводит к атрофии, кишечной метаплазии и дисплазии, с исходом в рак желудка. Развитие желудочной атрофии — это критический шаг перехода ХГ в рак желудка.
Лекарственный гастрит (тип С)
Это вторая по частоте форма гастрита. Наиболее изучено влияние на желудок нестероидных противовоспалительных средств (НПВС). Прямого агрессивного действия они, как кислоты, не вызывают (соляная кислота в десятки раз агрессивнее). В основе патогенеза их действия на слизистую желудка лежит блокирование ферментов циклооксигеназы (изомеры ЦОГ-1 и ЦОГ-2). При блокировании ЦОГ-1 происходит подавление синтеза простогландинов (Е2 и I2), которые обеспечивают качество и прочность слизистого барьера, защищающего слизистую оболочку от агрессивного действия соляной кислоты и пепсина. Поэтому длительный приём НПВС приводит к истончению защитного слоя слизи и повышению агрессивного действия соляной кислоты на слизистую желудка, вызывая хроническое воспаление.
Аутоиммунный атрофический гастрит (гастрит типа А)
Самой редкой формой ХГ является аутоиммунный атрофический гастрит (гастрит типа А). До сих пор его этиология не известна. В основе лежит выработка иммунными клетками антител к обкладочным клеткам слизистой оболочки (синтезируют соляную кислоту) и внутреннему фактору Касла (участвует в усвоении железа в кишечнике). В результате этого развиваются воспалительные изменения, очень рано приводящие к атрофии и ахлоргидрии (состоянию, при котором в желудочном соке отсутствует соляная кислота). Также нарушается обмен витамина В12, усугубляющий течение анемии.
Помимо перечисленных, выделяется группа специфических видов хронического гастрита.
Радиационный гастрит — причинным фактором выступает ионизирующее излучение, которое оказывает как прямое поражающее действие на слизистую оболочку, так и через каскад реакций с образованием свободных радикалов и перекисного окисления липидов клеточных мембран. В результате при длительном воздействие доз ионизирующего излучения, превышающих предельный порог, развивается хронический лучевой гастрит.
Лимфоцитарный гастрит характеризуется специфическим воспалением в слизистой облочке желудка, которое развивается на фоне протекания глютеновой энтеропатии — целиакии (патологического нарушения работы кишечника, при котором наблюдается непереносимость глютена). Происходит поражение собственными антителами слизистой оболочки с развитием хронического воспаления.
Гранулематозный гастрит развивается в результате вовлечения желудка в воспалительный процесс при болезни Крона (хроническом воспалительном заболевании кишечника) и протекает со сходными поражениями слизистой в виде эрозий и язв. В слизистой формируются специфические очаги хронического воспаления — гранулемы.
Эозинофильный хронический гастрит развивается при пищевой аллергии. При несоблюдении диеты, исключающей аллерген, развивается хроническое воспаления в слизистой оболочке желудка. Чем чаще аллергены попадают в желудок, тем ярче проявления гастрита.
Течение хронического гастрита
ХГ — длительно текущее заболевание: до развития выраженной структурной перестройки слизистой желудка в виде атрофии, дистрофии или дисплазии проходит в среднем 18-25 лет. Со временем каждое обострение приводит к распространению воспалительного процесса не только по площади (вширь), но и в глубину слизистой оболочки. При вовлечении в процесс тела и фундального отдела желудка начинает падать продукция соляной кислоты и пепсина, что приводит к нарушению пищеварения.
Осложнения хронического гастрита
Наиболее часто встречаются следующие осложнения ХГ:
- язва желудка;
- кровотечения;
- дефицит витаминов группы В;
- железодефицитная анемия (при снижении синтеза внутреннего фактора Касла);
- нарушения пищеварения (мальабсорбция и диспепсия);
- атрофия слизистой желудка;
- рак желудка.
Язва желудка
На данный момент нет чёткого представления, когда гастрит переходит в язвенную болезнь. Чаще всего язва желудка, как осложнение гастрита, возникает в результате длительно протекающей инфекции H. Pylori и/или частого употребления (НПВП) для обезболивания. В качестве первых признаков развития язвы желудка может быть усиление основных симптомов гастрита. Чаще всего симптомы остаются прежними, но не происходит отклика на стандартную терапию. При язве может развиться кровотечение, что приводит к появлению новых симптомов: усилению боли, чёрному стулу, рвоте с примесью крови. При развитии язвы прогноз становится менее благоприятным. Необходима своевременная диагностика (эзофагогастродуоденоскопия) и проведение коррекции схемы лечения при развитии этого осложнения.
Рак желудка
Самым грозным осложнением длительно протекающего ХГ является рак желудка. Его связь с ХГ до конца не изучена, но и не опровергнута. Инфекция Helicobacter Pylori признана комитетом ВОЗ канцерогеном первого класса. Также доказано, что инфицирование НР приводит к увеличению заболеваемости раком антрального отдела желудка в 4-6 раз.[2] Эрадикация (уничтожение) данного возбудителя снижает риски развития рака желудка. В этом аспекте также изучается наследственная отягощённость по раку желудка (отмечена «семейная сегрегация» рака желудка), наличие онкогенной мутации генов-супрессоров опухолевого роста (АРС,р53, k-ras) и других факторов. К предраковому состоянию относится сочетание атрофии слизистой желудка с дисплазией (II-III степени).
Также онкогенный потенциал несёт аутоиммунный атрофический гастрит тела и свода желудка. В результате агрессии иммунной системы против обкладочных клеток слизистой желудка развивается хроническое воспаление, приводящее к атрофии с последующей дисплазией и метаплазии и в финале – к трансформации в рак желудка.
Наименьший онкогенный потенциала несут химический реактивный и лимфоцитарный гастрит. При химическом гастрите воспаление в слизистой формируется при воздействии агрессивных веществ или обратном токе желчи. При лимфоцитарном ХГ воспалительные изменения слизистой сопровождаются лимфоплазоцитарной инфильтрацией собственной пластинки слизистой с повышенным содержанием зрелых Т-лимфоцитов, при этом часто формируются хронические (полные эрозии) и фовеолярная гиперплазия слизистой. Причины развития лимфоцитарного ХГ неясны. В 40-50% случаев он сочетается с целиакией (спру).[1]
Диагностика хронического гастрита
В основе диагностики ХГ лежат инструментальные и лабораторные способы исследования, сбор анамнеза заболевания и выявление факторов риска.
К какому врачу обратиться при гастрите
Для диагностики хронического гастрита необходимо обратиться к терапевту/педиатру или гастроэнтерологу. Врач выпишет направления на ЭГДС (эзофагогастродуоденоскопию) и другие виды обследований для постановки диагноза.
Что нужно обследовать
«Золотым стандартом» диагностики является проведение эндоскопического обследования желудка с измерением кислотности (эндоскопической топографической рН-метрией), биопсией для морфологического анализа и выявления инфекции Helicobacter Pylori. Совпадение диагнозов, поставленных в результате эндоскопического и морфологического исследований, не превышает 70%.[1] Это говорит об актуальности забора биопсийного материала при каждой ЭГДС с подозрением на гастрит.
Как проводится обследование при гастрите:
Повышает диагностическую ценность ЭГДС применение окраски слизистой метиленовым синим (окрашивает в сине-голубой цвет участки кишечной метаплазии и опухолевого роста).
Как вспомогательный метод применяется рентгеноскопия желудка, позволяющая оценить микрорельеф слизистой и моторную функцию. Могут выявляться язвенные дефекты и раковые изменения.
Из методов функциональной диагностики применяются рН-метрия и электрогастрография. Измерение кислотности можно проводить как при ЭГДС (топографическая рН-метрия), так и измерять её суточные колебания (суточное рН-мониторирование) при постановке специального трансназального зонда в желудок. Полученные данные отражают степень выработки соляной кислоты и косвенно могут указывать на процессы атрофии слизистой желудка. По результатам электрогастрографии судят о моторно-эвакуаторной функции желудка.
Данные УЗИ брюшной полости, биохимии крови, клинического анализа крови носят вспомогательный характер и помогают проводить дифференциальную диагностику в сложных случаях.
Лечение хронического гастрита
В основе лечения ХГ лежит полное или частичное исключение факторов «агрессии» на слизистую желудка, что позволяет ей восстановиться. Начинается терапия обострения с соблюдения щадящей диеты (вариант диеты с механическим и химическим щажением) — диета №1 и №2 по Певзнеру.
Медикаментозное лечение
Воздействие лекарственных средств направлено на снижение синтеза соляной кислоты, повышение защитных свойств слизисто-бикарбонатного слоя и регенерации слизистой. Из препаратов применяются следующие группы:
- Ингибиторы протонной помпы (ИПП): омепразол, пантопразол, рабепразол, лансопразол, эзомепразол. Механизм действия основан на снижении синтеза соляной кислоты протонной помпой. Эффективно снижают выработку соляной кислоты, привыкание не развивается.
- Блокаторы Н2-гистаминовых рецепторов: циметидин, ранитидин, фамотидин, низатидин, роксатидин. Механизм действия основан на блокировании действия гистамина на париетальные и обкладочные клетки, что приводит к снижению выработки пепсина и соляной кислоты. Увеличивают образование простагландинов, повышая защиту слизистой и стимулируя процессы регенерации. При длительном приёме развивается привыкание, что требует постоянного увеличения дозы.
- Цитопротекторы: препараты висмута (висмута субнитрат, висмута трикалия дицитрат, висмута нитрат основной), сукральфат (алюминиевая соль октасульфата сахарозы), мизопростол (синтетический простагландин).
- Антибактериальные препараты для эрадикации инфекции Helicobacter Pylori — всегда применяется в комбинациях двух или трёх препаратов (полусинтетические пенициллины, макролиды, тетрациклины, производные нитроимидазола).
- Прокинетики: метоклопрамид, домперидон, итоприда гидрохлорид, тримебутин — для снижения частоты рефлюксов желчи.
- Спазмолитики: дротаверин, гиосцина бутилбромид, мебеверин — для купирования спастического болевого синдрома.
- Заместительная терапия ферментами и препаратами желудочного сока — проводится при атрофическом гастрите и ахлоргидрии.
Другие лекарственные средства применяются в комплексе лечения сопутствующих заболеваний или осложнений ХГ.
Народные средства для лечения гастрита
Также может использоваться вспомогательное лечение: фитотерапия и желудочные сборы на основе листьев подорожника, корня девясила, душицы, полыни горькой, тысячелистника, девясила и других лекарственных растений. Применяются минеральные воды слабой газации и минерализации в подогретом виде за 60 минут до еды из расчёта 3 мл на 1 кг массы тела. Для этого используют Ессентуки № 4 или № 17, Боржоми, Нарзан или Смирновскую.
Диета при гастрите
В период обострения хронического гастрита применяется щадящая диета с протёртым вариантом готовки блюд. В её основе лежат следующие принципы:
- Механическое щажение обеспечивается за счет выбора пищевых продуктов, при котором учитывается содержание в них грубой клетчатки и продолжительность пребывания различных видов пищи в желудке. А также за счет кулинарной обработки продуктов (тушение, готовка на пару, измельчение пищи до консистенции пюре).
- Химическое щажение основано на повышении содержания жиров (растительного происхождения) и белков (животного происхождения — творог, сыр, яйца, отварные мясо и рыба) на фоне физиологической нормы углеводов, витаминов, микроэлементов, так как жиры тормозят желудочную секрецию, а белки инактивируют соляную кислоту.
- Термическое щажение достигается исключением слишком холодной и горячей пищи, которая травмирует слизистую желудка, оптимальная температура горячих блюд +30-40 °C.
- Ограничение объёма одновременно принятой пищи с целью предупреждения перерастяжения желудка: приём пищи 5-6 раз в день небольшими порциями. Приём пищи должен соответствовать ритму желудочной секреции и проводиться с интервалом 3,5-4,5 часа.
Исключаются продукты, повышающие выработку соляной кислоты желудком. Такие как: солёные приправы, крепкие мясные, рыбные или овощные бульоны, чёрный и мягкий хлеб, выпечка, газированные напитки, крепкий чай, кофе.
Рекомендуются продукты, обладающие средним уровнем стимуляции выработки соляной кислоты: отварное мясо, рыба, большинство ягод и фруктов и слабым уровнем: яйца всмятку, белые сухари или подсушенный хлеб (из муки тонкого помола), каши, сладкие фрукты и овощи.
В щадящей диете с протёртой пищей в ассортимент блюд включают:
- творог пресный, сыр неострый и нежирный, протёртый;
- супы протёртые из сборных овощей (кроме щей и борща), супы овоще-крупяные, молочные крупяные, с вермишелью или измельчёнными макаронами;
- овощи отварные протёртые — кабачки, цветная и брюссельская капуста, томаты, морковь, свекла (обязательное исключение белокочанной капусты, репы, редьки, редиса и бобовых, которые богаты растительными волокнами и эфирными маслами);
- спелые фрукты и ягоды сладких сортов (после тепловой обработки);
- компоты с протёртыми сухофруктами;
- хлеб пшеничный подсушенный.
Блюда готовят на пару, отваривают, разваривают до мягкости, пюрируют, измельчают, подают в тёплом виде.
Рекомендуемые блюда щадящей диеты с непротёртой пищей те же, что и для варианта, описанного выше. Блюда готовят на пару, отваривают, размельчают до мягкости, но не измельчают, подают в теплом виде 5-6 раз в день.
В период ремиссии рекомендуется придерживаться основных принципов здорового питания. При этом исключаются крепкие мясные и рыбные бульоны, грибной отвар, пряности, острые блюда, маринованные и копчёные продукты, обладающие раздражающим действием на слизистую оболочку и способные повышать образование соляной кислоты в желудке. Ограничивается сдобное тесто, пироги, блины, кофе, минеральные воды и напитки, содержащие углекислоту в большом количестве. Вредным является длительное (свыше 10-15 минут) использование жевательной резинки.
Лечение ХГ подбирается индивидуально в зависимости от причины, вызвавшей заболевание, выраженности симптомов и характера морфологических изменений слизистой. В настоящее время нет общепринятых клинических рекомендаций по лечению.
Хронический гастрит у детей
У детей хронический гастрит встречается редко, частота увеличивается с возрастом. Протекает чаще в стёртой форме, симптомы хронического гастрита у взрослых выражены сильнее. При этом реже возникают осложнения (язва, кровотечения и др.). Прогноз при своевременном лечении более благоприятный. Гастрит реже сочетается с инфекцией H. Pylori.
Лечение гастрита у детей аналогично лечению у взрослых, отличия составляют только ограниченный набор препаратов и их дозировки. Из базовых препаратов у детей разрешены: Омепразол с 1 года жизни, Рабепразол с 6 лет, Эзомепразол с 12 лет (данные из иностранных инструкций по применению действующих веществ). Гастропротекторы: Сукральфат с 4 лет. Антациды: Ренни с 12 лет, Гевискон с 12 лет, Маалокс с 15 лет.
Хронический гастрит у беременных
Хронический гастрит у беременных протекает без каких либо особенностей. В первую очередь требуется соблюдение правил здорового питания и исключение вредных факторов. Заболевание не приводит к высокому риску основных врождённых пороков развития, спонтанных выкидышей и преждевременных родов. Ранитидин и Эзомепразол могут применятся при грудном вскармливании, их приём безопасен для новорождённого. Из препаратов применяются: антациды (Ренни, Гевискон) и гастропротекторы (Сукральфат).
Прогноз. Профилактика
Прогноз ХГ обычно благоприятный. Представлять опасность могут лишь предраковые изменения слизистой желудка (кишечная метаплазия и дисплазия) на фоне атрофического гастрита. Своевременное лечение пернициозной анемии, которая развивается при атрофическом аутоиммунном ХГ, в большинстве случаев позволяет предотвратить нежелательное для пациента развитие событий. Следует помнить, что в случае подтверждённого аутоиммунного ХГ карциноид желудка развивается в 10 раз чаще, чем в контрольной группе.
Для того чтобы предупредить возникновение и прогрессирование ХГ необходимо:
- соблюдать правильный режим питания;
- бороться с курением и злоупотреблением алкоголя;
- проводить своевременную санацию полости рта;
- выявлять и лечить другие заболевания органов пищеварения.
Люди с ХГ, особенно с его диффузными атрофическими формами, которые сопровождаются снижением выделения соляной кислоты, должны находиться под диспансерным наблюдением с проведением эндоскопического контроля 1-2 раз в год, а весной и осенью им следует проходить курсы противорецидивной терапии.
ГБОУ ВПО «Северо-Западный государственный медицинский университет им. И.И. Мечникова» Минздрава России, Санкт-Петербург, Россия
Вялов С.С.
Европейский медицинский центр, Москва, 123104, Российская Федерация
Хронический гастрит: инструкции по применению лекарственных препаратов
Авторы:
Симаненков В.И., Вялов С.С.
Как цитировать:
Симаненков В.И., Вялов С.С. Хронический гастрит: инструкции по применению лекарственных препаратов. Терапевтический архив.
2017;89(8):129‑133.
Simanenkov VI, Vialov SS. Chronic gastritis: Instructions for use of medications. Terapevticheskii Arkhiv. 2017;89(8):129‑133. (In Russ.)
https://doi.org/10.17116/terarkh2017898129-133

ДПК — двенадцатиперстная кишка
ЖКТ — желудочно-кишечный тракт
ИПН — ингибиторы протонного насоса
ЛП — лекарственные препараты
НПВП — нестероидные противовоспалительные препараты
СОЖ — слизистая оболочка желудка
ХГ — хронический гастрит
ЯБЖ — язвенная болезнь желудка
Одной из наиболее часто диагностируемых нозологий в терапевтической амбулаторной практике является хронический гастрит (ХГ). Данный диагноз устанавливают большинству пациентов на основании клинической картины или по результатам эндоскопического исследования. Повседневная клиническая практика подсказывает врачу, что после гастроскопии у абсолютного большинства пациентов в заключении мы увидим «гастрит», «поверхностный гастрит» или нечто подобное. Таким образом, опираясь на заключение эндоскопии, мы вынуждены устанавливать пациенту диагноз К29.5. Хронический гастрит.
Диагноз «хронический гастрит» является морфологическим, что подразумевает необходимость подтверждающего эндоскопического и гистологического исследования. Но в некоторых случаях мы видим расхождение: симптомы имеются, а соответствующей морфологической картины нет. В отсутствие данных, подтверждающих наличие воспалительного процесса в слизистой оболочке желудка, на основании клинической картины и в соответствии с Римскими критериями мы констатируем диагноз функциональная диспепсия (К30. Диспепсия) (рис. 1).
Для лечения больных ХГ традиционно назначаются препараты из группы ингибиторов протонного насоса (ИПН), обеспечивающие значительное улучшение клинической картины и симптоматики у пациентов. Целью назначения ИПН у пациентов с ХГ является создание условий для заживления эрозивного или язвенного дефекта путем блокирования желудочной секреции и поддержания рН выше определенных значений. Прямого репаративного, регенерирующего и противовоспалительного действия ИПН не оказывают. Относительно рабепразола в последние годы появляются разрозненные данные о его цитопротективных эффектах [1].
В связи с широкой распространенностью ХГ встает вопрос о «реальной» заболеваемости, а также необходимости назначения препаратов, обладающих противовоспалительным и регенеративным потенциалом для уменьшения воспаления в слизистой оболочке желудка (СОЖ).
Юридический аспект назначения лекарственных препаратов (ЛП). Среди нормативных документов по лечению ХГ необходимо отметить приказ Министерства здравоохранения РФ от 28 декабря 2012 г. № 1598н «Об утверждении стандарта специализированной медицинской помощи детям при гастрите и дуодените». Данный приказ регламентирует стационарное лечение детей с гастритом и дуоденитом. Кроме того, имеется приказ Министерства здравоохранения РФ № 248 от 22 ноября 2004 г. «Об утверждении стандарта медицинской помощи больным хроническим гастритом, дуоденитом, диспепсией». Однако медико-экономические стандарты являются в большей степени экономическим документом, необходимым для расчета стоимости лечения. Они не нацелены на достижение терапевтического эффекта у конкретных пациентов, в общем описывают среднюю стоимость лечения и чаще затрагивают стационарную службу.
В связи с изложенным назначение ЛП при амбулаторном лечении осуществляется врачом в соответствии с показаниями, стандартами лечения и клиническими рекомендациями. Безусловно, на первое место при гастритах и дуоденитах выступает инструкция по медицинскому применению Л.П. Стандарты лечения и клинические рекомендации в данном случае являются вторичными по отношению к инструкции.
Назначение врачом ЛП должно осуществляться в соответствии с приказом Министерства здравоохранения РФ № 1175н от 20 декабря 2012 г. «Об утверждении порядка назначения и выписывания лекарственных препаратов, а также форм рецептурных бланков на лекарственные препараты, порядка оформления указанных бланков, их учета и хранения».
Согласно пункту 3 Порядка назначения врачам необходимо «назначать … и выписывать ЛП … в соответствии с Инструкцией о порядке выписывания ЛП». Врачам «запрещается выписывать рецепты на ЛП в отсутствие медицинских показаний» в соответствии с пунктом 6 данного Порядка назначения.
Назначение инструкции: что в ней пишут для врача? Врач получает информацию о показаниях к применению препарата из разных источников. Этими источниками могут быть фармакопейные статьи, результаты исследований, данные обзоров и метаанализов, клинические рекомендации.
Однако, с юридической точки зрения, ключевыми являются два документа: инструкция по применению и фармакопейная статья. Инструкция составляется производителем и утверждается Минздравом, с помощью инструкции производитель «показывает» врачам и пациентам, при каких заболеваниях препарат эффективен (показания), при каких запрещен (противопоказания).
Если препарат по результатам исследований оказался неэффективен при заболевании, это может быть не внесено в показания или не отражено в инструкции. В некоторых случаях препарат может быть весьма эффективен при заболевании, но производитель не проводил исследования и не имеет оснований для внесения этой нозологии в показания к препарату. В рамках данной статьи мы не будем касаться других целей производителя и других разделов инструкции.
Инструкция по медицинскому применению утверждается профильным комитетом Минздрава, т. е. является документом. Например, назначая ЛП ребенку, мы уточняем разрешенный возраст и ориентируемся на способ расчета дозы, приведенные в инструкции. Назначая препарат для парентерального введения, по инструкции мы уточняем способ введения: внутривенно или внутримышечно, капельно или струйно, скорость введения и т. д. Исходя из этой логики, мы должны внимательно изучать инструкции по медицинскому применению ЛП.
Так как инструкция является официальным документом, утвержденным Минздравом, в основание ее положены данные исследований, проведенные производителем, то она должна являться ключевым или основополагающим источником для врача при выборе препарата.
Мы можем назначать препарат не по инструкции. Например, можем назначить внутривенный препарат железа не по инструкции внутримышечно (получив нежелательные реакции) или подкожно не по инструкции препарат для внутримышечного введения (не получив никакого результата). Или мы можем назначить пероральный препарат не по инструкции, биодоступность которого ухудшает прием пищи после еды (не получив эффекта). Или дозировать препарат не по инструкции из расчета массы тела, а из расчета площади поверхности кожи (получив непредсказуемый эффект).
Назначение препарата без наличия показаний в инструкции, в зарубежной практике называемое «off-label» применение, является своего рода «клиническим исследованием», которое проводит врач индивидуально под свою юридическую ответственность.
Для проведения клинического исследования необходимо соблюдение определенной процедуры проведения, в том числе составление протокола исследования, предварительное получение информированного согласия пациента, получение разрешения на проведение исследования в контролирующем государственном органе.
Рассматривая медицинскую помощь в соответствии с нашим законодательством, в том числе как медицинскую услугу, мы понимаем, что пациент вправе требовать компенсацию затрат на лечение в случае его неэффективности. При некорректном назначении препарата, назначении не по показаниям врач не имеет никакой правовой защиты от пациента в случае возникновении претензий. Судя по нашему опыту, получение у пациента информированного согласия на терапию «off-label» не ограждает врача от последующих жалоб и в крайних случаях от судебных разбирательств.
При возникновении споров о правильности выбора того или иного препарата в лечении конкретного пациента инструкция, содержащая в показаниях к применению конкретные заболевание пациента, служит одним из доказательств правоты врача или критерием оказания квалифицированной медицинской помощи.
Инструкции к ИПН. Для оценки правомерности назначения ИПН при гастрите мы проанализировали инструкции к препаратам этой группы. Производители оригинальных препаратов (брэнды) регистрируют инструкцию, в дальнейшем производители генерических препаратов при регистрации «копируют» инструкцию оригинального препарата. Следует подчеркнуть, что при внесении в инструкцию генерического препарата новых показаний по каждому из них должны быть проведены исследования по стандартам GCP. К сожалению, в отечественной практике это правило не всегда соблюдается, и новые показания могут базироваться на пострегистрационных исследованиях низкого уровня доказательности.
При анализе указанных в инструкции показаний к применению ИПН можно обнаружить отсутствие такой нозологической формы, как «хронический гастрит» или вообще «гастрит». Единственным исключением является препарат контролок (брэндовый препарат пантопразола), в показаниях к применению которого указан «эрозивный гастрит». Таким образом, на основании инструкции по медицинскому применению только контролок может быть препаратом для лечения эрозивного гастрита.
В табл. 1 суммированы результаты изучения показаний к применению отдельных ИПН, зарегистрированных в Российской Федерации. Из шести МНН (международных непатентованных наименований) имеющихся на российском рынке ЛП, брэндами представлены пять. В табл. 1 они выделены жирным шрифтом. Необходимость этого обусловлена отсутствием в нашей стране документа, аналогичного Оранжевой книге — «Orange book» FDA, в котором представлены не только зарегистрированные в США генерики, но и указана степень их терапевтической эквивалентности по отношению к брэндам.
Как «оформить» хронический гастрит? В связи с ограниченностью арсеналаа ИПН, разрешенных к применению при ХГ, необходим практический путь решения вопроса терапии гастрита. Таким образом, при эрозивном гастрите показан к применению только контролок (пантопразол). По непонятной причине у дженериков пантопразола в показаниях гастрит не зарегистрирован. При неэрозивном гастрите нет разрешенных к применению ИПН.
Вариантом назначения ИПН может быть альтернативная интерпретация состояния пациента и постановка диагноза К30. Диспепсия. Данный диагноз подразумевает полное соответствие клинической картины и симптоматики у пациента Римским критериям IV. Однако использование диагнозов функциональных нарушений в ряде случаев вызывает сложности во взаимодействии со страховыми компаниями, требующими «более достоверной» верификации диагноза.
При наличии сочетанной патологии, а именно К29.5 ХГ и К21 ГЭРБ, возможно назначение ИПН для лечения рефлюксной болезни. При этом диагноз ГЭРБ должен быть подтвержден эндоскопическим обследованием и обоснован в амбулаторной карте или истории болезни.
Опыт показывает, что эндоскопическое исследование часто выявляет ту или иную степень гиперемии желудка, однозначно интерпретируемую эндоскопистами как Х.Г. При выявлении гастрита лечащий врач вынужден ставить диагноз на основании инструментального обследования, чтобы избежать расхождения.
Таким образом, мы вынуждены устанавливать диагноз ХГ и либо не лечить это заболевание, либо лечить не по показаниям, либо искать другие ЛП с зарегистрированными показаниями и доказанной эффективностью при гастрите.
«Гастропротекторы» для ХГ. Рациональным и логичным представляется использование в лечении ХГ препаратов, восстанавливающих СОЖ и уменьшающих ее воспаление. Поскольку назначением ИПН мы добиваемся только устойчивой кислотосупрессии у пациента, т. е. создаем условия для уменьшения воспаления или заживления эрозивно-язвенного дефекта, необходимо назначение препарата с выраженным гастропротективными свойствами.
Стимулятор синтеза простагландинов — ребамипид зарегистрирован в Российской Федерации под торговым наименованием Ребагит. Данный препарат эффективен в заживлении эрозивных и язвенных дефектов, при поражении СОЖ, а также в комплексе антихеликобактерной терапии. В показаниях к применению препарата зарегистрированы ХГ в стадии обострения, а также эрозивный гастрит и ЯБЖ (табл. 2). Самым важным является «развязывающее руки» врачу показание — в составе комбинированной терапии, которое можно интерпретировать в пользу врача.
Ребамипид разработан в Японии в 1989 г. для лечения пептических язв. Его механизм действия отличается от антисекреторных препаратов — он оказывает заживляющее действие на эрозии и язвы. За последние 10 лет в PubMed при запросе «rebamipide» определяется 183 статьи, за последние 3 года — 72. Последние работы показали влияние ребамипида на циклооксигеназу-2, стимулирование синтеза простагландина Е2 и I2, факторов роста [2].
Индукторы синтеза представляют собой вещества, стимулирующие синтез простагландинов и гликопротеинов в СОЖ. В научных работах показано действие ребамипида на синтез простагландинов Е2 и I2, факторы роста, белки теплового шока, оксид азота, молекулы адгезии, нейтрофилы. Ребамипид способствует улучшению кровоснабжения СОЖ, активизирует ее барьерную функцию, усиливает пролиферацию поврежденной СОЖ, оказывает гастропротекторное действие при воздействии на нее.
Ребамипид имеет хорошую доказательную базу (более 15 рандомизированных исследований, включавших 965 пациентов), отражающую его преимущества перед плацебо. Важно, что ребамипид дает достоверный прирост эффективности лечения в комбинации с ИПН [3].
Результаты исследования у пациентов, проходящих лечение. В японском исследовании оценивалась доля пациентов, у которых язвы зажили в рубцовой стадии после эндоскопической подслизистой резекции (хирургическое удаление участка СОЖ). Полное излечение произошло у 54,8% в группе ИПН и у 86,7% в группе комбинированной терапии ИПН + ребамипид. Среди больных с тяжелым атрофическим гастритом излечение произошло у 30% в группе ИПН, и 92,9% в группе комбинированной терапии ИПН + ребамипид [4].
Представляют значительный интерес результаты исследования монотерапии, прямого сравнения ребамипида и ИПН у 90 пациентов, перенесших эндоскопическую подслизистую резекцию. В обеих группах заживление язв было сходным: через 2 нед на фоне ИПН — 27,2%, на фоне ребамипида — 33,3%, а через 8 нед на фоне ИПН — 90,9%, на фоне ребамипида — 93,3%. Авторы отмечали, что лечение ребамипидом более экономично и предотвращает образование грануляций. Так, через 8 нед частота грануляционных поражений следующих после заживления язв оказалась значительно выше в группе ИПН (13,6%), чем в группе ребамипида (0; р=0,01) [5].
Таким образом, исходя из показаний к применению, мы должны констатировать, что в случаях гастритов, ассоциированных H. pylori, использование различных ИПН в эрадикационных схемах является вполне легитимным. В отсутствии инфицированности H. pylori единственным ИПН, который может быть назначен по показаниям, отраженным в инструкции по применению, является пантопразол (контролок) и только при эрозивном гастрите. При любых вариантах ХГ может применяться ребагит (ребамипид), поскольку он имеет данные показания и, по результатам многих исследований, проведенных в последние годы, является одним из лучших препаратов выбора в восстановлении СОЖ и других отделов пищеварительной системы. Как отмечалось ранее, его эффективность доказана при дефектах слизистой оболочки различного генеза — эрозивных и неэрозивных гастритах, язвенной болезни, патологии, вызванной приемом НПВП (рис. 2).
Другие гастропротекторы. В нашей статье мы рассматриваем аспекты применения гастропротекторов в рамках лечения ХГ (табл. 3). В связи с этим следует, что в данную группу препаратов входят и другие.
Препараты висмута используются при лечении заболеваний желудка и ДПК в фазе обострения, и они могут применяться при ХГ не более рекомендованных 4—8 нед. В течение следующих 8 нед не следует принимать препараты, содержащие висмут. Это связано с рядом побочных эффектов и накоплением висмута. В кислой среде желудка осаждаются нерастворимые вистмута оксихлорид и цитрат, образуются хелатные соединения с белковым субтратом в виде защитной пленки на поверхности язв и эрозий. Что говорит о поверхностном протективном действии, которое не имеет точки приложения в отсутствии дефектов слизистой оболочки, как, например, при ХГ.
Сукральфат не нашел широкого применения ввиду особенностей переносимости терапии. Кроме того, механизм действия сукральфата также связан с взаимодействием с белками некротизированной ткани эрозии или язвы и формированием защитного слоя. Таким образом, и здесь речь идет о поверхностном протективном действии, которое не имеет точки приложения в отсутствии дефектов слизистой оболочки, как, например, при ХГ. В показаниях к применению также отсутствует гастрит.
Заключение
Внесение в первичную документацию ХГ в качестве основного и единственного диагноза существенно ограничивает возможности применения ИПН.
При установлении диагноза гастрита, ассоциированного H. pylori, в соответствии с инструкцией могут использоваться все зарегистрированные в Российской Федерации ИПН, кроме декслансопразола.
При назначении ИПН для лечения эрозивного гастрита формальное обоснование содержится только в инструкции препарата контролок (брэнд пантопразола). При эрозивном гастрите показан препарат ребагит.
Для лечения неэрозивного ХГ нет зарегистрированных показаний у ИПН и показано назначение гастропротектора ребамипида (ребагита).
Авторы заявляют об отсутствии конфликта интересов.
Причину гастрита следует обязательно выяснять. Сделать это можно с помощью обследования у гастроэнтеролога. Если лечить болезнь неправильно, то риск осложнений повысится в значительной степени. Последствиями гастрита могут стать язвенные поражения тканей пищеварительных органов, внутренние кровотечения, предраковые состояния.
1. Правила приема
При гастрите медикаментозная терапия осуществляется комплексно. Заболевание надо лечить несколькими препаратами с разными фармакологическими свойствами.
Нельзя использовать лекарства по совету знакомых.
Воспалительный процесс сопровождается не только общими симптомами в виде изжоги, отрыжки, тошноты и болевого синдрома, но и отличается по степени прогрессирования, уровню кислотности желудочного сока.
Самолечение может стать причиной осложнений.
При составлении схемы терапии учитываются следующие факторы:
- возраст пациента;
- особые указания (например, беременность, период лактации);
- уровень кислотности желудочного сока;
- разновидность заболевания и степень развития;
- факторы, спровоцировавшие болезнь;
- индивидуальные особенности организма;
- имеющаяся симптоматика.
2. Схема лечения
Количество соляной кислоты оказывает влияние на уровень кислотности желудочного сока. Действие отдельных лекарств направлено на снижение или повышение уровня выработки данного вещества. Кроме того, гастрит может иметь острую или хроническую форму, сопровождаться осложнениями в виде язвы. При каждом из таких состояний используется определенная тактика терапии.
При пониженной кислотности
Схема терапии при гастрите с пониженной кислотностью направлена на восстановление секреторной функции желудка. Антибиотики применяются только при бактериальной природе заболевания. При подборе препаратов врач учитывает форму недуга. Атрофический тип болезни сопровождается нарушением структуры желез. При гипоацидной форме заболевания происходит блокирование секреторной функции.

- стимулирующая терапия (основным направлением курса лечения является увеличение процесса выработки соляной кислоты);
- симптоматическая терапия (используются медикаменты для устранения тошноты, изжоги, метеоризма и других сопутствующих симптомов гастрита);
- заместительная терапия (схема используется при отсутствии эффективности стимулирующих лекарств).
При повышенной кислотности
Общие принципы лечения гастрита с повышенной кислотностью не отличаются от стандартной терапии других форм заболевания.
Список медикаментов должен включать в себя препараты для устранения причины воспалительного процесса, укрепления иммунитета, улучшение функционального состояния пищеварительного тракта.
Главное отличие заключается в подборе лекарств для нормализации кислотности желудочного сока. Для снижения процесса выработки соляной кислоты используются антациды и специальные блокаторы.
Обязательным дополнением к курсу являются препараты для ускорения регенерации тканей и с обволакивающим действием.
При хронической форме
Схема лечения хронического воспалительного процесса зависит от индивидуальных особенностей организма пациента. Врач учитывает кислотность желудочного сока, сопутствующую симптоматику. Для продления ремиссии могут быть назначены витаминные комплексы, лекарственные средства для улучшения работы органов пищеварения. Антибактериальная терапия проводится только в период обострения болезни.
Лечение острого гастрита
При остром воспалительном процессе главными задачами терапии являются устранение болевого синдрома, уничтожение возбудителя болезни, предотвращение осложнений и восстановление функционального состояния пищеварительной системы. Пациенту назначаются спазмолитики, антагонисты дофаминовых рецепторов, антибиотики антациды, пробиотики, гепатопротекторы. В курс лечения обязательно включаются вяжущие и ферментные средства.
Купирование приступа обострения должно проводиться под контролем врача.
При язве
Обязательной частью терапии воспалительного процесса, осложненного язвой, является назначение ингибиторов протонной помпы.
Дополнительно могут быть использованы лекарственные средства с содержанием животных ферментов, блокаторы гистаминовых рецепторов. Для предотвращения распространения воспалительного процесса применяются вяжущие и обволакивающие медикаменты.
Такие средства не только купируют воспаление, но и избавляют от общей симптоматики гастрита (тошнота, рвота, изжога, отрыжка, метеоризм).
3. Какие лекарства можно пить при гастрите?
Лечение воспаления в тканях желудка подразумевает использование нескольких групп лекарств. Медикаменты с разными фармакологическими свойствами дополняют друг друга, ускоряя тенденцию к выздоровлению.
При составлении курса следует учитывать множество нюансов. Неправильная терапия может спровоцировать осложнения.
Например, если принимать таблетки для повышения кислотности при чрезмерной выработке соляной кислоты, то повысится риск образования эрозий на тканях желудка.
Антациды
Антацидные препараты в большинстве случаев назначаются при лечении гастрита, сочетающегося с повышенной кислотностью желудочного сока.
При приеме таблеток данной группы следует учитывать важный нюанс — если принимать лекарственные средства натощак, то период их действия сократится.
Антацидные средства устраняют проявления изжоги, отрыжки, улучшают общее состояние пищеварительного тракта. Дополнительно такие препараты повышают защитные свойства клеток и тканей желудочно-кишечного тракта.
Примеры антацидов:
- Ренни;
- Маалокс;
- Гастал;
- Алюмаг.
Антисекреторные средства
Действие антисекреторных средств направлено на блокировку гистаминовых рецепторов. Препараты данной группы снижают выработку соляной кислоты, защищают слизистые оболочки пищеварительного тракта от негативных факторов, подавляют агрессивную щелочную среду. Уровень секреции снижается независимо от причины, спровоцировавшей ее повышение.
Дополнительно антисекреторыне средства улучшают процессы микроциркуляции.
Примеры антисекреторных средств:
- Ранитидин;
- Омепразол;
- Гастроцепин;
- Омез;
- Циметидин.
Антибиотики

Антибиотики нельзя принимать без показаний врача. Неправильный прием таких медикаментов может усугубить ситуацию, спровоцировать новые приступы воспалительного процесса. Антибактериальные препараты уничтожают патогенные микроорганизмы и продукты их жизнедеятельности.
Примеры антибиотиков:
- Кларитромицин;
- Тетрациклин;
- Амоксициллин;
- Цефалексин.
Препараты висмута
При лечении воспаления в тканях желудка препараты висмута оказывают антисептическое действие. В состав таких медикаментов входят вещества, купирующие болевой синдром и останавливают воспалительные процессы в органе.
На слизистые оболочки средства на основе висмута оказывают обволакивающее действие. За счет данного эффекта повышается защита тканей пищеварительного тракта от воздействия негативных и раздражающих факторов.
Примеры средств на основе висмута:
Блокаторы дофаминовых рецепторов
Медикаменты из категории блокаторов дофаминовых рецепторов необходимы для предотвращения и устранения симптомов интоксикации организма.
Такие лекарственные средства не только устраняют приступы тошноты и рвотные позывы, но и снижают риск обезвоживания организма.
При гастрите блокаторы дофаминовых рецепторов используются в составе комплексной терапии. Отдельный прием таких таблеток не остановит развитие воспаления.
Примеры блокаторов дофаминовых рецепторов:
- Церукал;
- Реглан;
- Эглонил.
Выбор лекарств по типу кислотности
Лекарственные средства для лечения гастрита должны подбираться с учетом ряда факторов. Одним из главных моментов является кислотность желудочного сока. Если уровень выработки соляной кислоты повышен, то препараты должны его снижать.
При пониженной кислотности, наоборот, используются медикаменты для стимулирования секреторной функции.
Медикаменты для повышения кислотности желудочного сока:
- средства для регулирования процесса выделения кислоты (Ацедин-Пепсин);
- ферментные средства для улучшения процесса расщепления пищи (Панзинорм, Мезим, Фестал);
- препараты для стимулирования моторики пищеварительного тракта (Мотилиум).
Медикаменты для понижения кислотности желудочного сока:
- средства для купирования воспалительных процессов (Париет, Омез);
- препараты для купирования болевого синдрома (Но-Шпа, Атропин);
- средства для замедления процесса выработки соляной кислоты (Ренни, Алюмаг);
- медикаменты для улучшения процессов регенерации и защиты слизистых оболочек (Омез, Омепразол).
4. Какие таблетки лучше?
Таблетки от гастрита отличаются по наименованию производителя, по цене. Некоторые пациенты отдают предпочтение дорогим средствам, другие — стараются подобрать дешевые аналоги. Цена и производитель не имеют значения. Главное правило терапии заболевания — правильно составленная схема лечения. Препараты должны дополнять друг друга и взаимно усиливать фармакологические свойства.
Нюансы:
- прием любых таблеток следует согласовывать с гастроэнтерологом;
- если принимать таблетки неправильно, то может развиться медикаментозный гастрит;
- эффективность медикаментозной терапии снизится, если не соблюдать дополнительные рекомендации (сбалансированное питание, исключение стрессовых ситуаций, отказ от вредных привычек).
5. Противопоказания
Общими противопоказаниями для приема большинства таблеток от гастрита являются детский возраст, индивидуальная непереносимость отдельных компонентов из состава препаратов, период лактации или беременности. При наличии серьезных отклонений в работе печени или почек следует проконсультироваться с врачом. Специалист подберет безопасные аналоги медикаментов или скорректирует режим дозирования.
Гастрит при беременности подразумевает особые схемы терапии. В некоторых случаях врачи откладывают медикаментозное лечение до рождения ребенка.
6. Профилактика
Неправильное лечение гастрита может стать причиной перехода заболевания в хроническую форму. Для исключения такого фактора следует осуществлять специальные меры профилактики.
Организма должен получать достаточное количество витаминов. Для обеспечения такой задачи необходимо скорректировать рацион питания, принимать витаминные комплексы.
Если симптомы болезни возобновляются после проведенной терапии, то самолечение должно быть исключено.
Дополнительные меры профилактики:
- исключение переедания или длительного голодания;
- соблюдение правил сбалансированного питания;
- отказ от вредных привычек;
- ведение здорового образа жизни;
- регулярный осмотр у гастроэнтеролога.
Видео на тему: Какие препараты принимать при гастрите.
7. Итоги
- медикаментозная терапия гастрита осуществляется комплексно;
- в один курс лечения должны входить препараты с разными фармакологическими свойствами (обволакивающие, антацидные, антибактериальные, спазмолитические и другие средства);
- последствием неправильного подбора таблеток может стать медикаментозный гастрит;
- при составлении схемы лечения учитывается возраст пациента, индивидуальные особенности организма, стадия развития воспалительного процесса, разновидность болезни, уровень кислотности желудочного сока.
Принципы лечения гастрита
Как и любое заболевание органов ЖКТ, гастрит может встречаться в различных формах, протекать в остром или хроническом виде, поражать различные отделы желудка, иметь повышенную или сниженную кислотность желудка. Для назначения медикаментозной схемы лечения гастрита принимаются во внимание не только эти факторы, но и общее самочувствие пациента, его возраст и пр.
Симптоматика заболевания
Данный патологический процесс проявляется характерной симптоматикой:
- тошнота и рвота;
- чувство переполненности желудка;
- болевые ощущения;
- отрыжка, зловонный запах изо рта;
- изжога;
- метеоризм;
- присутствие на языке серого или желтого налета;
- общая слабость;
- лихорадочное состояние.
Принципы лечения
Терапия гастрита направлена на устранение причин, которые вызывают воспаление желудка. Так как симптоматика заболевания многообразна, наиболее эффективное лечение происходит при комбинации лекарственных препаратов различного воздействия.
Комплексное лечение данной патологии — это не только терапия медикаментами, но и следование специальной диете.
Терапия острого гастрита выполняется в больнице. Терапевтическая тактика назначается в зависимости от причин возникновения, клинических проявлений и стадии протекания заболевания. Когда хронический гастрит имеет выраженную симптоматику, присутствуют сильные боли, наблюдается потеря веса, стойкая желудочная диспепсия, то рекомендуется госпитализация.
Вылечить гастрит полностью можно в случае, если выполняются следующие требования:
- устраняются причины заболевания;
- происходит восстановление слизистой органа;
- стабилизируется синтез желудочного сока;
- происходит восстановление нормальной моторики ЖКТ;
- соблюдаются рекомендации по питанию.
Касательно сроков избавления от патологии можно сказать, что хроническая форма гастрита лечится дольше острой.
Эффективность лечения – от чего она зависит
Эффективность медикаментозного лечения зависит от подобранной схемы, которая должна соответствовать таким требованиям:
- Применение антибиотиков, устойчивых к кислой среде.
- Правильный подбор современных лекарственных средств, которые способны уничтожить патогенную микрофлору.
- Использование лекарств направленного воздействия.
- Назначение препаратов, выведение из организма которых происходит быстро.
Продолжительность курса медикаментозной терапии зависит от типа патологии и тяжести ее протекания. При отсутствии ярко выраженной симптоматики лечение длится около четырех недель.
Самые эффективные схемы лечения предполагают индивидуальный подход к каждому пациенту.
Как лечить гастрит у взрослых
Лечение гастрита может происходить по следующим схемам:
Первая линия:
- Схема № 1. 3-х компонентная терапия, которая рассчитана на две недели. Лечение происходит так: дважды в день принимаются «Кларитромицин», «Омепразол», «Амоксициллин». «Омепразол» можно заменить на «Зероцид», «Омез», а «Кларитромицин» — на «Нифурател».
- Схема № 2. Терапия 4-х компонентная, длится 2 недели, считается дополнением первого варианта. В этом случае к вышеописанной схеме присоединяется трикалия дицитрат висмута (240 мг), принимаемый также в день 2 раза.
- Схема №3. Комплекс из: «Амоксициллина» (1000 мг), висмута трикалия дицитрата (240 мг), «Нифуратела» (400 мг) принимают дважды в сутки на протяжении 2 недель.
- Схема № 4. Данная усеченная схема прописывается пожилым больным.
- 4А. Принимают «Амоксициллин» (1000 мг), «Омепразол», висмут трикалия дицитрат (240 мг) в течение двух недель дважды в сутки.
- 4Б. Висмут трикалия дицитрат. Прием препарата – в день 4 раза (дозировка 120 мг) в течение 4 недель.
- Схема № 5. При возникновении аллергических реакций на антибиотики, в схеме оставляется «Омепразол» или другой ИПН, добавляется 30%-й водный раствор прополиса, дозировка 100 мл, натощак — дважды в день.

- Схема № 1. 4-х компонентная: «Тетрациклин» (500 мг), висмута трикалия дицитрат (120 мг), ИПН – в сутки 4 раза, «Метронидазол» (500 мг) — в сутки 3 раза. Продолжительность терапии – 2 недели.
- Схема № 2. ИПН, «Фуразолидон» (100 мг), «Амоксициллин» (500 мг), висмута трикалия дицитрат (120 мг) – в день по четыре раза. Продолжительность лечения — две недели.
- Схема № 3. ИПН, «Амоксициллин» (500 мг), висмут трикалия дицитрат (120 мг) — в день по 4 раза, «Рифаксимин» (400 мг) – в сутки 2 приема.
3-я линия схемы
Выполняется по 2-ой линии при отсутствии эффекта от эрадикации бактерии.
Лекарства от гастрита
Для проведения лечения по любой из схем применяются определенные виды лекарственных средств:
Ингибиторы протонной помпы. Эти средства помогают снизить синтез желудочной кислоты и снижают агрессивность желудочного сока. Данные средства нужны для терапии гастрита с высокой кислотностью. К ним относят – «Нольпаза», «Эзомепразол», «Омепразол», «Омез».
Селективные холинолитики. Такие препараты предназначены для подавления синтеза соляной кислоты и оказания противоязвенного воздействия. Это препараты – «Метацин», «Платифиллин», «Атропин».
Антацидные средства. Их назначение – оказывать обволакивающее воздействие – покрывать слизистую желудка пленкой от влияния кислоты. Выпускаются в виде суспензии или таблеток – «Гастрогель», «Маалокс», «Фосфалюгель», «Алмагель».
Цитопротекторы. Они служат для повышения защитных свойств и устойчивости слизистой желудка к воздействию повреждающих факторов — «Мизопростол».
Прокинетики. Они служат для стабилизации моторики ЖКТ – «Метоклопрамид», «Мотинорм», «Бромоприд», «Мотилиум», «Моторикс».
Диета как составляющая лечения
Для эффективного лечения гастрита вместе с применением одной из схем назначается диетический стол №1. Он базируется на употреблении щадящих продуктов, которые уменьшают воспаление слизистой и способствуют заживлению язв: к ним относятся отварное или на пару мясо, рыба, разрешены каши, отдельные виды овощей и фруктов в свежем виде.
Можно ввести в меню запеченные без корочки блюда. Исключаются специи, а соль разрешена в небольшом количестве. Температура употребляемых блюд, как и напитков, должна быть комнатной. Прием пищи — 5-6 раз в день. Перед сном хорошо выпить стакан молока.
- Разрешенные супы готовятся на воде из протертых овощей, можно добавить геркулес или рис.
- Не разрешается готовить супы на мясном бульоне, к запретным блюдам относятся: окрошка, борщ и любые другие супы на жирном бульоне, со специями и поджаркой.
- Разрешается употреблять выпечку из пшеничной муки, но только вчерашнюю.
Из мясных продуктов разрешены: куриная грудка без кожи, крольчатина, говядина или баранина нежирная, индейка. Из субпродуктов — печень и язык. Запрещены: мясо утки, гуся. Разрешается рыба, но нежирная.
Из молочных продуктов можно почти все, кроме твердых и кислых продуктов. Яйца разрешаются всмятку или в виде омлета на пару.
Из круп разрешаются: гречневая, манная, овсяная. Запрещены: перловая, пшенная крупы, фасоль, горох, отдельные виды макаронных изделий.
Можно употреблять некислые овощи и фрукты в сыром виде или в протертом, приготовленные на пару.
Методы народной медицины
Лечение гастрита может происходить и с помощью народных способов. Лучшего результата можно добиться при совокупном применении методов классической медицины и народных способов лечения.
Самым популярным средством народной медицины при данном заболевании считается картофельный сок. Он очень полезен при патологии с повышенной секрецией желудка.
Для приготовления сока используют картофель с кожурой. Из натертого клубня выжимают сок через марлю. Основное условие – употребить сок сразу после отжатия. Вариантов приема — много.
Наиболее популярны такие схемы лечения:
- 150 г сока натощак за полчаса до еды выпивать ежедневно, длительность курса – индивидуальна;
- 250 мл сока за час до завтрака выпивать, после чего рекомендуется полежать 30 минут. Продолжительность лечения – 10 дней;
- ежедневно за полчаса до еды употреблять по 1 ст. ложке сока, каждый день увеличивая дозировку, дойдя до 125 мл.
Еще одним эффективным средством считается сок алоэ. Он подавляет работу болезнетворных микроорганизмов. Сок растения применяют дважды в день по 2 ст. ложки перед едой. Очень полезно употреблять его с медом. Длительность терапии – от 2 недель до полутора месяцев.
Масло облепихи обладает обволакивающим, заживляющим, противовоспалительным эффектом. Его применение имеет смысл при любых типах гастрита с высокой кислотностью, а также в случае возникновения язвы или эрозии в желудке или 12-ти перстной кишке.
Схема терапии патологии у детей
У ребенка система пищеварения окончательно сформирована лишь к 7 годам. Из-за этого выработка соляной кислоты у них в недостаточном количестве, и присутствует ослабление моторики желудка.
У детского гастрита есть свои особенности терапии. В острый период рекомендуется соблюдать постельный режим, кроме этого, не рекомендуется принимать пищу в течение 8–12 часов. Позже прием пищи происходит небольшими порциями. Лечение также комплексное и сочетает в себе употребление лекарственных препаратов, диету и физиотерапию.

При лечении гастрита у детей ставятся следующие задачи:
- Нормализация функциональности слизистой органа.
- Уменьшение агрессивного влияния кислоты.
- Восстановление всех процессов в ЖКТ.
Медикаментозная терапия, назначаемая детям, предусматривает употребление таких препаратов:
Независимо от выбранной схемы лечения, требуется соблюдение правил диетического питания, в ином случае не удастся добиться перехода патологии в состояние стойкой ремиссии:
- Из рациона убираются все продукты, которые могут способствовать активной выработке желудочного сока.
- Запрещены соления, копчености, острые, жареные блюда.
- Блюда должны иметь пюреобразное состояние.
- Продукты должны термически обрабатываться. Их разрешено запекать, тушить, отваривать, готовить на пару.
Когда патология сопровождается рвотой, назначают прием антирефлюксных средств — «Метоклопрамид» или «Домперидон». Иногда могут прибегнуть к промыванию желудка. При жалобах на боли в области живота, разрешается употребление «Дротаверина» или «Папаверина».
Когда причиной гастрита становится токсическая инфекция, лечение проводят посредством антибиотиков, ферментов и адсорбентов. При риске обезвоживания назначают инфузионную терапию. При диагностировании флегмонозного гастрита и возможной перфорации желудка требуется хирургическое лечение.
Наблюдение после проведенного лечения
После окончания медикаментозной терапии больные должны в течение трех лет числиться на диспансерном учете. По истечении срока проводят инструментальные и лабораторные исследования, по итогам которых врач делает выводы о возможности снятия с учета пациента.
Когда больной в состоянии ремиссии, ему следует выполнять такие рекомендации врача:
- Соблюдать щадящую диету.
- Пить минеральные воды (курс длится 3 недели, его можно повторить через 3 месяца).
- Употреблять целебные отвары, которые готовятся из чистотела, ромашки аптечной, зверобоя, тысячелистника.
- Употреблять витаминные комплексы.
- Принимать определенные физиотерапевтические процедуры: гидротерапия, электрофорез, грязелечение, токи (динамические).
- Проходить санаторно-курортное лечение (после рецидива через 3 месяца).
Причины неэффективности выбранной схемы лечения
Могут наблюдаться ситуации, когда пациент, закончивший курс лечения, не чувствует никаких улучшений.
К причинам неэффективности терапии следует отнести такие факторы:
- Пациенту были назначены лекарства, к составляющим которых у него наличествует непереносимость.
- Выражена резистентность болезнетворной бактерии Хеликобактер пилори.
- В схеме лечения не присутствуют антибиотики, возможно, была неправильно назначена дозировка, больной нарушил время их приема, препарат был неправильно подобран.
- Врач выбрал малоэффективную схему медикаментозной терапии.
Список литературы: med.vesti.ru/articles/zabolevaniya/hronicheskij-gastrit-lechenie-simptomy/ https://24tv.ua/health/ru/gastrit_kak_lechit_i_kak_uberechsja_ot_zabolevanija_n977317 http://webmed.irkutsk.ru/doc/pdf/aciddis.pdf https://medsi.ru/services/lechenie-gastrita/ https://www.kp.ru/guide/kak-lechit-gastrit.html https://www.lvrach.ru/2018/08/15437046/ https://fnkc-fmba.ru/zabolevaniya/gastrit/ https://www.mediasphera.ru/journals/mjmp/97/1/r1-97-18.htm https://medi.ru/info/12194/ Бордин Д. С., Машарова А. А., Хомерики С. Г. Хронический гастрит: современный взгляд на старую проблему // ЭиКГ. 2012. №5. Заметки автора статьи, основанные на личном опыте.
Данный материал носит исключительно субъективный характер и не является руководством к действию. Определить точный диагноз и назначить лечение может только квалифицированный специалист.
Последнее изменение статьи: 18.03.2020
Таблетки от гастрита: 15 эффективных препаратов — Гастро Портал
К сожалению, на сегодняшний день не существует универсальной таблетки от гастрита, и совершенно естественно возникновение вопроса о том, как лечить гастрит желудка, какие лекарства принимать при тех или иных проявлениях болезни. При лечении необходимо учитывать тип и стадию заболевания, а также уровень желудочного кислотовыделения.
По клиническому течению выделяют острые гастриты и хронические с фазами обострения. Причем первые признаки болезни наблюдаются именно в стадии воспаления. В зависимости от уровня секреции желудочного сока различают гастриты с повышенной или пониженной кислотностью.
Симптомы заболевания обусловлены, главным образом, уровнем желудочной кислотности.
| Дифференциальный признак | Симптомы гастрита | |
| Повышенная секреция желудочного сока | Секреторная недостаточность | |
| Возраст | Больные молодого возраста | Лица пожилого возраста |
| Боль: описание болевого синдрома | Интенсивные боли в области эпигастрия, возникающие утром, через 1.5 часа после еды и ночью. Могут быть спазматические или ноющие. | Чувство тяжести и дискомфорта в животе после еды |
| Диспепсические явления | Кислая отрыжка, тошнота, изжога, рвота с примесью пищи | Отрыжка пищей, иногда с неприятным запахом, тошнота, газообразование, урчание в животе |
| Нарушения стула | Запоры | Диарея |
| Аппетит | Без изменений | Снижен |
| Сопутствующие болезни | Рефлюкс-эзофагит | Дисбактериоз кишечника, гиповитаминоз |
Лечение гастрита комплексное и направлено на борьбу с причинами возникновения болезни и устранение клинических проявлений:
- боль и тяжесть в эпигастральной области;
- воспалительные изменения слизистой желудка;
- изжога и отрыжка;
- нарушение стула;
- нарушение пищеварения;
- отсутствие аппетита.
Выбор медикаментозных препаратов определяется характером функциональных нарушений желудка. Курс лечения назначается врачом после диагностики болезни, специалист расскажет все о причинах возникновения гастрита и определит, какие лекарства лучше принимать.
Лекарства при гастрите
Медикаментозная терапия гастритов включает в себя применение следующих групп препаратов:
- Антациды и антисекреторные лекарства при повышенной кислотности.
- Препараты, усиливающие выработку соляной кислоты при секреторной недостаточности.
- Ферментные лекарства для нормализации пищеварения.
- Прокинетики, нормализующие перистальтику органов ЖКТ, и направленные на устранение диспепсических явлений.
- Спазмолитики при болевом синдроме.
- Средства, возбуждающие аппетит.
- Противовоспалительные лекарства.
- Седативные препараты.
Оптимальный клинический эффект оказывает комплексное лечение гастрита: препараты должны обязательно сочетаться с диетическим питанием, предполагающим принципы механического и термического щажения пищи.
Медикаментозное лечение гастритов с повышенной и нормальной кислотностью
Цели медикаментозной терапии гастрита с повышенной кислотностью – снижение кислотной агрессии желудочного сока и подавление его секреции, а также устранение диспепсического синдрома. Для решения этих задач назначаются таблетки антацидов и антисекреторных препаратов.
Важно: для лечения гастрита с нормальным уровнем желудочного сока используются те же лекарства, что и при повышенной кислотности желудка для устранения изжоги, отрыжки и дискомфорта в эпигастральной области.
Антациды
Лекарства группы антацидов снижают активность желудочного сока, обладают обволакивающим действием, предохраняя слизистую желудка от повреждения. Средства выпускаются в виде комплексных препаратов, содержащих гидроксид алюминия, гидрокарбонат магния или карбонат кальция. Реализуются средства в виде сиропов и суспензий под торговыми названиями:
- Алмагель;
- Маалокс;
- Гастрацид;
- Фосфалюгель;
- Ренни;
- Гевискон.
Как лечить гастрит
Лечение гастрита проводится после полного обследования и выявления причин, вызвавших воспаление слизистой оболочки желудка. Проведение всех диагностических процедур является залогом эффективности лечения. В острый период заболевания необходимо снизить болезненности и успокоить воспалительную реакцию. Первостепенной задачей является снижение агрессивности желудочного сока.
В период ремиссии требуется соблюдение диеты. Вылечить воспаление желудка возможно только при соблюдении всех рекомендаций врача относительно образа жизни, питания и приема лекарственных препаратов. Невозможно точно определить, сколько лечится это заболевание, все зависит от индивидуальных факторов течения гастрита.
Принципы лечения
Лечение гастрита направлено прежде всего на устранение причин, вызвавших воспаление слизистой желудка. Поскольку симптомы гастрита многообразны, эффективное лечение достигается при комбинировании лекарственных средств различного действия. Комплексное лечение гастрита предполагает не только терапию медикаментами, но и соблюдение специальной диеты.
Ограничения касаются и объема употребляемой пищи, питание должно быть дробным и частым. По мере устранения симптомов болезни пациент возвращается к привычному режиму питания. Но необходимо соблюдать правила рациона с учетом пониженной и повышенной кислотности желудка.
Вместе с тем независимо от вида гастрита всем пациентам с таким заболеванием противопоказаны алкоголь, кофе, шоколад, газированные напитки. Больной должен отказаться от всех видов консервированной продукции и вторично переработанных продуктов. Под запретом жирная, копченая и жареная пища, а также изделия из сдобного теста.
Немаловажно отказаться от вредных привычек, а именно от злоупотребления алкоголем и курения. В период обострения гастрита больной должен соблюдать щадящую диету, которая предполагает исключение механического и химического раздражения воспаленной слизистой оболочки желудка.
Лечение острого гастрита проводится в больнице. Терапевтическая тактика подбирается в зависимости от причин развития, клинических проявлений и стадии течения болезни. Если хронический гастрит сопровождается выраженной симптоматикой, у больного стойкая желудочная диспепсия, сильные боли в желудке, потеря веса, то показана госпитализация.
Ответ на вопрос о том, можно ли вылечить гастрит, полностью заключается в выполнение следующих условий:
- устранение причины заболевания;
- восстановление слизистой оболочки органа;
- нормализация выработки желудочного сока;
- восстановление здоровой моторики ЖКТ (желудочно-кишечного тракта);
- соблюдение рекомендаций по питанию.
Относительно сроков выздоровления необходимо отметить, что хронический гастрит в отличие от острого долго лечится.
Чтобы вылечить гастрит навсегда, традиционно используют следующие типы лекарственных средств:
Народное лечение гастрита желудка
- Ингибиторы протонной помпы. Способствуют снижению выработки соляной кислоты и уменьшают агрессивность желудочного сока. Такие препараты показаны для лечения гастрита с повышенной кислотностью. Это Омепразол, Эзомепразол, Омез, Нольпаза.
- Селективные холинолитики. Подавляют выработку соляной кислоты и оказывают противоязвенное действие (Пирензепин, Платифиллин, Метацин Атропин).
- Антацидные средства. Оказывают обволакивающее действие, покрывая слизистую оболочку желудка пленкой для предотвращения воздействия кислоты. Выпускаются в виде таблеток или суспензии. Это Фосфалюгель, Гастрогель, Маалокс, Алмагель.
- Цитопротекторы. Повышают защитные свойства и устойчивость слизистой оболочки желудка к воздействию повреждающих факторов. Наиболее популярным является Мизопростол.
- Прокинетики. Улучшают моторику желудочно-кишечного тракта (Домперидон, Метоклопрамид, Диметрамед, Бромоприд, Мотилиум, Моторикс, Мотинорм).
Легче всего поддается лечению диффузный поверхностный гастрит. Это обусловлено особенностями заболевания: желудок не утратил способность к восстановлению, поражения слизистой оболочки неглубокие, и отсутствуют очаги нарушений. Но при отсутствии своевременного лечения симптомы заболевания могут прогрессировать, и патология приобретает более сложный характер.

Так, гастрит способен перейти в хронический диффузный, затем в субатрофический и далее в антральный. Последний характеризуется разрушением стенок эпигастрия. Атрофия слизистой оболочки желудка может наступить уже через 10 лет после начала заболевания и отсутствия лечения.
Первостепенной задачей лечения антрального гастрита является уничтожение бактерии хеликобактер пилори, именно она разрушает слизистую оболочку желудка. Редким видом воспаления слизистой оболочки желудка является аутоиммунный гастрит. Он характеризуется некрозом отдельных участков органа пищеварения.
Такой процесс вызван нарушением иммунной реакции организма на воспаление. Основным в лечении этого заболевания является устранение симптомов, поскольку пока медицине не совсем ясно, как восстановить нормальную реакцию иммунитета.
Антибиотики
Нередко в схему лечения гастрита врач включает антибактериальные препараты. Необходимость в приеме подобных лекарств возникает, если выясняется, что причиной заболевания стали болезнетворные микроорганизмы. В большинстве случаев эта желудочная патология вызвана воздействием бактерии под названием хеликобактер пилори.
Применение антибиотиков в лечении гастрита повышает терапевтическую эффективность и позволяет быстро устранить воспалительный процесс, а также препятствует размножению и росту болезнетворных микроорганизмов. При этом важно учесть, что подобные препараты способны вызвать дисбактериоз, поэтому их употребление желательно совмещать с лекарственными средствами для поддержки и восстановления кишечной микрофлоры.
Негативное воздействие антибиотиков на почки и печень обуславливает необходимость назначения подобных лекарств исключительно лечащим врачом. Поскольку самолечение усугубит проблему и вызовет тяжелые осложнения. Наиболее эффективными антибактериальными препаратами для устранения хеликобактер пилори сочетаются:
- Кларитромицин. Обладает широким антимикробным спектром действия и имеет минимальный перечень побочных действий. Применяется в рамках комплексного лечения, но противопоказан при наличии аллергической реакции на компоненты препарата. Аналогами являются Азиклар, Клабакс, Фромилид, Клацид, Кломед, Биноклар.
- Амоксициллин. Принадлежит в группе пенициллинов и содержится в таких препаратах, как Амоксил, Флемоксин Солютаб, Амоксил, экобол, Амосин.
- Метронидазол. Снижает активность и размножение бактерии за счет блокировки синтеза белков.
Для усиления эффективности антибактериальных препаратов их назначают в сочетании друг с другом. Так, гастроэнтерологи назначают одновременно Амоксициллин с Метронидазолом.
Подобный прием используется и при обострении заболевания.
Если же у пациента гастрит с повышенной кислотностью, то назначают, например, Кларитромицин одновременно с препаратами, подавляющими выработку соляной кислоты (Омез или Омепразол).
При гастрите с пониженной кислотностью антибиотик сочетается с одним из следующих препаратов: Пепсидил, Панзинорм, Ацидин-пепсин. Для лечения гастрита у детей и взрослых применяются различные препараты. Если не лечить хронический гастрит, вызванный бактерией хеликобактер пилори, то постепенно заболевание перейдет в язву желудка или двенадцатиперстной кишки.
Дозировку и длительность курса лечения определяет лечащий врач в зависимости от индивидуальных особенностей течения болезни. При назначении того или иного препарата учитываются сопутствующие заболевания и возраст пациента. Необходимо отметить, что быстро избавиться от хеликобактер пилори не получится.
Наиболее популярная схема лечения гастрита для полного устранения болезнетворных микроорганизмов в желудке:
- Рекомендуемый по возрасту антибиотик нового поколения.
- Препараты висмута, чаще всего это Де-нол.
- Ингибиторы протонной помпы.
- Метронидазол.

Лечение болезни у детей
У детей пищеварительная система окончательно формируется только к 7 годам. В связи с этим соляная кислота у них вырабатывается в недостаточном количестве и моторная функция желудка ослаблена. Именно поэтому гастрит у детей – явления нередкое. Повышенный уровень заболеваемости отмечается в возрасте от 5 до 6 лет и от 10 до 15.
Детский гастрит имеет свои особенности лечения. В острый период показан постельный режим. Также необходимо отказаться от приема пищи в течение 8–12 часов. В дальнейшем еда и питье принимаются маленькими порциями. Лечение также должно быть комплексным и включает в себя прием лекарственных средств, диету и физиотерапию.
Если заболевание сопровождается рвотой, то принимаются антирефлюксные средства, в качестве таковых подходят прокинетики Метоклопрамид или Домперидон. При необходимости прибегают к промыванию желудка. Если ребенок жалуется на выраженные боли в области живота, то допускается прием Папаверина или Дротаверина.
Если причиной гастрита стала токсическая инфекция, то лечение проводится с помощью антибиотиков, ферментов и адсорбентов. При опасности обезвоживания показана инфузионная терапия. Выявление флегмонозного гастрита и возможной перфорации желудка требует хирургического лечения.
Лечение хронического гастрита у детей предусматривает:
- антисекреторную терапию;
- уничтожения хеликобактер;
- прием антацидных средств;
- нормализацию моторики желудка и кишечника;
- прием спазмолитиков и ферментов.
Способы народной медицины
Лечить гастрит желудка можно не только с помощью аптечных препаратов. Значительного улучшения состояния можно добиться при сочетании традиционного лечения с применением средств народной медицины.
Использование последних направлено на устранение воспалительного процесса в слизистой оболочке желудка и понижение уровня кислотности. Заниматься таким лечением можно дома после консультации с лечащим врачом.
Одним из популярных и эффективных средств народной медицины для лечения гастрита является картофельный сок. Особенно полезен он при заболевании с повышенной секреторной функцией желудка. Такое действие обусловлено щелочной реакцией. Поскольку картофель богат крахмалом, употребление его сока способствует обволакиванию слизистой желудка, препятствуя контакту с бактериями, раздражающими ее.
Для приготовления сока использует картофель с кожурой. Достаточно тщательно промыть клубни. При отсутствии соковыжималки можно воспользоваться теркой или мясорубкой и затем выжать сок через марлю. Главное условие – выпить сок сразу после приготовления. Способы употребления картофельного сока различны.
Наиболее популярны следующие схемы лечения гастрита с помощью картофельного сока:
- 150 г сока ежедневно на голодный желудок за 30 минут до еды, длительность приема – по индивидуальному состоянию;
- 250 мл сока ежедневно натощак перед завтраком за 1 час, после 30 минут желательно полежать. Длительность курса – 10 дней;
- Каждый день за полчаса до еды принимать по одной столовой ложке сока, ежедневно увеличивая дозировку, пока она не достигнет 125 мл.
Другим, не менее действенным, средством, имеющим положительные отзывы, является сок алоэ. Он обладает выраженным антисептическим свойством и подавляет деятельность болезнетворных микроорганизмов. Сок лекарственного растения в объеме 2 ст. л. принимают 2 раза в день перед приемом пищи. Полезно сочетать сок с медом.

Для приготовления этого средства нужны листья растения, которому не меньше 3 лет. Рецепт приготовления следующий: листья срезают и на 2 недели помещают в холодильник, после чего выжимают сок и смешивают с медом.
Пропорции компонентов – 1:2, например, 100 г сока и 200 г меда. Первые 5 дней нужно принимать перед едой по 1 ч. л. средства. По истечении этого времени дозировку увеличивают до 1 ст. л.
Длительность лечения – от 2 недель до 1,5 месяцев.
Заживляющим, обволакивающим и противовоспалительным эффектом обладает масло облепихи. Его применение рекомендуется при всех видах гастрита с повышенной кислотностью, а также в случае образования язвы или эрозии в желудке или двенадцатиперстной кишке.
При грамотном сочетании традиционных и народных методов лечения гастрит вполне излечим. Но после устранения основных симптомов заболевания важно соблюдать правила питания. Без выполнения последнего пункта все другие меры окажутся неэффективными.
Отзывы
Алексей, 29 лет, г. Москва: Некоторое время назад появились неприятные ощущения в животе, которые затем перешли в болезненные.
После проведения диагностических процедур и консультации гастроэнтеролога поставили диагноз поверхностный гастрит с повышенной кислотностью. Также обнаружили в желудке хеликобактер пилори.
Врач прописал схему лечения с антибиотиками, облегчение ощутил уже на 3–4 день, а после окончания курса забыл о гастрите. Повезло с тем, что не запустил болезнь и начал сразу лечиться. Главное, своевременно принять меры.
Ирина, 35 лет, Пятигорск: Уже несколько лет страдаю от хронического воспаления слизистой желудка. При болях в желудке сразу принимаю Фосфалюгель. Помогает безотказно.
Стараюсь придерживаться рекомендаций врача по питанию, не ем жирную и жареную пищу, почти забыла об острых блюдах.
Помню предупреждение врача о том, что болезнь может перейти в язву, поэтому при малейшем дискомфорте начинаю лечение.
Марина, 25 лет, Ростов: В студенческие годы заработала гастрит и теперь пожинаю плоды своего безразличия к собственному здоровью. Диагноз – эрозивный гастрит. Лечусь при обострении симптомов лекарствами и народными средствами. Хорошо помогает облепиховое масло внутрь и картофельный сок натощак.
Гастрит — группа заболеваний разного генеза с острым или хроническим воспалением слизистой желудка. Проявляется эпигастральной болью, диспепсией, интоксикацией, астенией. Диагностируется с помощью ЭФГДС, рентгенографии желудка, уреазного теста, внутрижелудочной pH-метрии, исследования желудочного сока, других лабораторных и инструментальных методов. Для лечения применяют антибактериальные, антисекреторные, гастропротекторные препараты, компоненты желудочного сока в сочетании с лекарственными средствами, влияющими на отдельные звенья патогенеза. При некоторых формах заболевания показано хирургическое лечение.
Общие сведения
Гастрит — одно из наиболее распространенных заболеваний пищеварительных органов, составляющее до 80% болезней желудка. Частота возникновения расстройства увеличивается с возрастом. По данным наблюдений в сфере гастроэнтерологии, различными вариантами патологии страдает до 70-90% пожилых пациентов. В последние годы участились случаи диагностики гастрита у детей, возросла роль бактериального фактора в развитии воспаления — до 90% случаев связано с хеликобактерной инфекцией. Сохраняется тенденция к преимущественно хроническому течению процесса, распространенность острых вариантов болезни не превышает 20%.
Гастрит
Причины гастрита
Гастрит — полиэтиологическое заболевание, возникающее при воздействии на желудок различных повреждающих факторов. Его развитию способствуют патологические процессы, при которых нарушается локальная резистентность слизистого слоя, общая реактивность организма, регуляция секреторной и моторной функции органа. Основными причинами и предпосылками гастрита являются:
- Инфекционные агенты. У 90% пациентов с хроническим воспалением высеивается хеликобактер. Острый гастрит может быть вызван кишечной палочкой, стафилококками, стрептококками, другой условно-патогенной микрофлорой. Реже заболевание имеет вирусное происхождение или развивается на фоне сифилиса, туберкулеза, кандидоза, глистных инвазий.
- Химические воздействия. Большинство острых процессов возникают из-за попадания в желудок агрессивных веществ. При отравлении сулемой, кислотами наблюдается фибринозное воспаление, щелочами, солями тяжелых металлов — некротическое. При приеме НПВС, глюкокортикоидов, ряда антибиотиков, сердечных гликозидов, кокаина, злоупотреблении алкоголем возможен эрозивный гастрит.
- Измененная реактивность. Воспаление, обусловленное образованием антител к обкладочным клеткам и внутреннему фактору Касла, наблюдается при болезни Аддисона-Бирмера. Реже заболевание ассоциировано с аутоиммунным тиреоидитом, инсулинозависимым сахарным диабетом, аутоиммунным полигландулярным синдромом I типа. Гиперреактивность, вызванная сенсибилизацией организма, служит причиной аллергического гастрита.
- Другие заболевания пищеварительных органов. Слизистая желудка воспаляется при раздражении из-за заброса кишечного содержимого. Билиарный рефлюкс-гастрит развивается из-за функциональной несостоятельности пилорического сфинктера при хроническом дуодените, дискинезии желчевыводящих путей. Предпосылки к рефлюксу желчи отмечаются при болезнях оперированного желудка, дуоденальных опухолях.
- Хронический стресс. Нейрогуморальный дисбаланс чаще служит предрасполагающим фактором, хотя ишемия при острой стрессовой реакции может спровоцировать образование эрозий и даже геморрагического гастрита. Хронический стресс сопровождается длительным спазмом сосудов, недостаточным кровоснабжением слизистой. Ситуация усугубляется истощением резервных возможностей и дискинезиями ЖКТ.
- Пищевые погрешности. Нарушения пищевого поведения — одна из основных предпосылок к развитию хронического поверхностного гастрита. Постоянное поступление жирной, острой, горячей пищи, блюд с экстрактивными веществами, газированных напитков вызывает раздражение слизистой и усиливает эффект других факторов. Реже химическое повреждение или механическое травмирование провоцирует острый процесс.
В пожилом возрасте основным провоцирующим фактором становится инволютивное истончение слизистой, приводящее к снижению местной резистентности. При сепсисе, тяжелых соматических болезнях, онкопатологии предпосылкой к воспалению является хроническая ишемия желудочной стенки. Возможен ятрогенный генез заболевания вследствие лучевой терапии рака желудка, пищевода, других злокачественных неоплазий ЖКТ или механического повреждения органа во время гастроскопии, эзофагогастродуоденоскопии, назоинтестинальной интубации. В некоторых случаях (например, при гиперпластическом гастрите) этиология остается неустановленной. Не исключено, что ряд форм патологии имеет наследственное происхождение.
Патогенез
Механизм возникновения воспаления желудка связан с дисбалансом повреждающих и защитных факторов. Действие токсинов, химических веществ, аутоантител, аллергенов, твердой пищи, инструментов и рентгеновских лучей провоцирует местные реакции. Чем более массивным является повреждающее воздействие, тем острее воспалительный процесс. После короткой фазы альтерации нарушается микроциркуляция, отмечается отек, экссудация внутрисосудистой жидкости и компонентов крови с развитием классического катарального гастрита. В более тяжелых случаях наблюдается острая дистрофия и некроз тканей.
Хронизация острого воспаления сопровождается атрофическими, гиперпластическими, метапластическими, другими дистрофически-регенераторными изменениями железистого аппарата. При малой интенсивности повреждающих нагрузок ключевую роль играет снижение местной резистентности, вызванное как локальными, так и общими воздействиями. Постоянное раздражение эпителия продуктами питания, алкоголем, желчью, эндотоксинами, нарушение регуляции секреторно-моторной функции способствует возникновению хронического воспаления с постепенным нарастанием патоморфологических изменений.
Отдельным звеном патогенеза хронического гастрита является нарушение кислотопродуцирующей функции. Под действием аммиака, выделяемого хеликобактериями, усиливается выработка гастрина, снижается содержание соматостатина, что приводит к гиперпродукции соляной кислоты. В результате у пациента развивается гастрит с повышенной кислотностью. Атрофия слизистой фундального отдела желудка и аутоиммунное повреждение обкладочных клеток угнетают секрецию соляной кислоты при умеренно выраженном воспалении. Этот механизм лежит в основе гастрита с пониженной кислотностью.
Классификация
При систематизации клинических форм гастрита учитывают особенности течения патологического процесса, морфологические изменения слизистой, ведущий этиологический фактор, локализацию воспаления, состояние секреторной функции, стадию заболевания, наличие осложнений. Наиболее полной является Хьюстоновская классификация заболевания с учетом клинико-морфологических критериев, которые предложили Р. Стрикленд и И. МакКей (1973 г.):
- Тип воспаления. По характеру течения различают острый и хронический варианты гастрита. Отдельно рассматривают особые формы заболевания — аллергическое, гипертрофическое, лимфоцитарное, гранулематозное, другие нетипичные воспаления.
- Локализация поражения. Зачастую болезнь поражает один из отделов органа (фундальный, антральный гастрит). При вовлечении в патологический процесс всего желудка, более характерном для острых форм патологии, говорят о пангастрите.
- Этиология. С учетом наиболее значимых причин выделяют хронический аутоиммунный гастрит (тип А), хеликобактерное воспаление (тип В), химико-токсическое поражение (тип С). При сочетании нескольких факторов заболевание рассматривают как смешанный процесс.
- Характер морфологических изменений. По глубине распространения и особенностям патологического процесса воспаление бывает катаральным, фибринозным, коррозивным, флегмонозным, эрозивным. При хроническом гастрите часто преобладают атрофические процессы.
- Особенности желудочной секреции. При проведении систематизации оценивается кислотообразующая функция желудка. В зависимости от содержания в желудочном соке соляной кислоты различают гастрит с пониженной, повышенной, нормальной кислотностью.
Симптомы гастрита
Признаки острого гастрита обычно появляются внезапно на фоне погрешностей в диете, приема НПВС, отравления. Пациентов беспокоят эпигастральные боли разной интенсивности, тошнота, рвота, отрыжка, ухудшение аппетита, учащение стула. Нарушения общего состояния при остром воспалении представлены слабостью, головокружениями, снижением трудоспособности. При инфекционном генезе расстройства возможны лихорадка, озноб, насморк, кашель, миалгии, артралгии. Особенность эрозивного варианта болезни — наличие кровотечения из ЖКТ, которое проявляется в виде кровавой рвоты или мелены.
Симптомы хронического гастрита зависят от секреторной активности желудка. Для воспаления, сопровождающегося повышением кислотности, характерны интенсивные боли в надчревной зоне, возникающие через 20-30 минут после еды, хронические запоры, изжога, отрыжка кислым. При длительном течении пациента беспокоит повышенная утомляемость, эмоциональная лабильность, бессонница. У больных, страдающих хроническим гастритом со сниженной кислотностью, болевой синдром выражен незначительно или отсутствует. Отмечается утренняя тошнота, чувство быстрого насыщения, тяжесть в желудке, диарея, метеоризм, отрыжка воздухом, горький привкус во рту, серый налет на языке. Из-за нарушения переваривания и всасывания пищи наблюдается потеря массы тела, мышечная слабость, отеки на голенях.
Осложнения
Гастрит может осложняться язвенной болезнью желудка и 12-перстной кишки. В случае эрозивного поражения стенки органа возможно возникновение профузного кровотечения и геморрагического шока. При флегмонозной форме гастрита часто наблюдается перфорация желудочной стенки, рубцовая деформация органа, образуются свищи. Вследствие недостатка внутреннего фактора Касла у части больных развивается мегалобластная анемия. При атрофическом гастрите отмечается белково-энергетическое голодание с кахексией, гипопротеинемическими отеками, мышечной дистрофией, энцефалопатией. Длительное течение заболевания повышает риск образования аденокарциномы желудка.
Диагностика
Обычно при наличии типичных клинических признаков постановка диагноза гастрита не представляет затруднений. Основной задачей диагностического этапа является комплексное обследование пациента для выявления первопричины и определения клинического варианта болезни. Наиболее информативными считаются следующие инструментальные и лабораторные методы:
- Эзофагогастродуоденоскопия. Осмотр слизистой при ЭГДС выявляет патогномоничные морфологические признаки заболевания. Для гастрита характерны отечность, гиперемия, эрозии, истончение и атрофия эпителия, участки метаплазии, усиление сосудистого рисунка.
- Рентгенография желудка. Показано контрастное исследование с бариевой смесью. О наличии гастрита свидетельствует утолщение складок (более 5 мм), наличие узлов слизистой оболочки, увеличение желудочных полей, множественные эрозии.
- Внутрижелудочная рН-метрия. С помощью суточного измерения кислотности в желудке оценивается секреторная функция органа и определяется клиническая форма гастрита. Метод также может использоваться для оценки эффективности антисекреторной терапии.
- Дыхательный тест на хеликобактер. Для выявления H. pylori измеряется концентрация углерода в выдыхаемом воздухе. Результаты являются положительными при показателе более 4‰. В сомнительных случаях рекомендована ПЦР-диагностика, определение антител к хеликобактеру в крови.
- Исследование желудочного сока. Метод направлен на изучение секреторной функции желудка. В ходе анализа оценивают общую кислотность, содержание ферментов, слизи, других веществ. При микроскопии осадка выявляют эпителиоциты, мышечные волокна и др.
В общем анализе крови возможны признаки В12-дефицитной анемии: снижение эритроцитов и гемоглобина, появление мегалобластов. При подозрении на аутоиммунную природу заболевания проводят серологические реакции для поиска антипариетальных антител. Диагностически значимым является определение сывороточных уровней пепсиногенов 1 и 2, гастрина. В копрограмме обнаруживается большое количество непереваренных мышечных волокон, зерен крахмала, клетчатки, реакция Грегерсена может быть положительной. В сложных случаях рекомендована МСКТ органов брюшной полости, УЗИ желчного пузыря, печени, поджелудочной железы, антродуоденальная манометрия. Наиболее точный метод установления морфологического диагноза — гистологического исследование биоптата.
Дифференциальную диагностику осуществляют с функциональной диспепсией, другими заболеваниями ЖКТ (язвенной болезнью, хроническим панкреатитом, холециститом), патологией кишечника (целиакией, болезнью Крона), витаминной недостаточностью (пернициозной анемией, пеллагрой), кишечными инфекциями (сальмонеллезом, эшерихиозом, спру). Помимо консультации гастроэнтеролога пациенту рекомендованы осмотры инфекциониста, гематолога, гепатолога. Для исключения инфаркта миокарда назначается консультация кардиолога, при возможном раке желудка — онколога.
Лечение гастрита
Терапевтическая тактика определяется факторами, спровоцировавшими развитие гастрита, и клинической формой заболевания. Пациенту рекомендована комплексная дифференцированная терапия, дополненная коррекцией диеты, отказом от курения, употребления алкоголя. Базовая схема консервативного лечения обычно включает следующие группы препаратов:
- Антибактериальные средства. Для уничтожения хеликобактерий применяют стандартные схемы эрадикации с использованием макролидов, β-лактамных пенициллинов, нитроимидазолов, тетрациклинов, которые обязательно комбинируются с ингибиторами протонной помпы, препаратами висмута. При выявлении других возбудителей инфекционного гастрита назначают противомикробные, противогрибковые, противопаразитарные средства различных групп.
- Корректоры секреторной функции. При усилении продукции соляной кислоты используют ингибиторы протонной помпы, блокаторы Н2-гистаминорецепторов. Для коррекции секреторной недостаточности проводят заместительную терапию пепсинсодержащими средствами. Чтобы стимулировать производство желудочного сока, медикаментозную терапию дополняют фитопрепаратами на основе подорожника, пиридоксином, аскорбиновой, никотиновой, слабыми органическими кислотами.
- Гастропротекторы. Существует несколько групп средств для защиты эпителия от повреждающих воздействий. Принцип действия обволакивающих препаратов основан на осаждении тонкой пленки, механически предохраняющей слизистую от повреждения. Коллоидные суспензии также коагулируют белки хеликобактера. Антациды нейтрализуют соляную кислоту желудочного сока. Простагландины группы Е восполняют дефицит естественных защитных факторов.
При остром гастрите план лечения предусматривает промывание желудка, прием сорбентов, антидотов, инфузионную терапию. Больным с выраженными нейровегетативными расстройствами рекомендованы седативные фитопрепараты, транквилизаторы. При аутоиммунном воспалении используют кортикостероиды. Пациентам с выраженным болевым синдромом назначают миотропные спазмолитики, с осторожностью — анальгетики. Для остановки кровотечения и восполнения кровопотери при геморрагическом гастрите применяют гемостатики, переливают цельную кровь, эритроцитарную массу, плазму. При дуоденально-гастральном рефлюксе эффективны производные урсодезоксихолевой кислоты, ингибиторы дофаминовых рецепторов. Для улучшения моторики показаны прокинетики. Хирургические операции выполняют при массивной деструкции желудочной стенки у больных с флегмонозным гастритом, возникновении профузного кровотечения.
Прогноз и профилактика
Исход заболевания при остром процессе чаще благоприятный, хроническое воспаление обычно имеет рецидивирующее течение с периодами обострений и ремиссий. Наиболее неблагоприятен в прогностическом плане хронический атрофический гастрит, приводящий к необратимому снижению кислотообразования в желудке, малигнизации. Меры профилактики включают ограничение острой и жирной пищи, отказ от курения и употребления алкоголя, прием медикаментов только по назначению врача, своевременное выявление и лечение заболеваний, которые могут вызывать воспалительный процесс в желудке.
Гастрит – поражение слизистой оболочки желудка с преимущественно воспалительными изменениями при острой форме и явлениями структурной перестройки, дисрегенерации и атрофии при хроническом течении. Наиболее распространенным типом болезни является бактериальный, вызванный возбудителем Helicobacter pylori. Гастрит часто имеет психологические триггеры и также может спонтанно регрессировать (частично или полностью излечиваться) при отсутствии стрессоров.
В зависимости от формы заболевания может потребоваться прием антибиотиков. Те, кто склонен к проблемам с желудком, должны отказаться от кофе, курения, алкоголя. Цитрусовые можно есть только в небольших количествах, т. к. они содержат вещества, которые способствуют выработке кислоты в желудке и, таким образом, могут вызвать подкисление. Самолечение при гастрите недопустимо. Лекарства должен назначать врач, опираясь на тип болезни и состояние организма пациента. Предлагаем список эффективных препаратов от гастрита, который подобран на основании эффективности и соотношения цена-качество.
Особенности гастрита
Причины заболевания до сих пор точно не установлены. Триггерным фактором, безусловно, является психосоциальный стресс. По-видимому, личность также играет определенную роль в формировании болезни. Многие больные гастритом страдают от чувства вины, разочарований и постоянного конфликтного напряжения.
Наиболее распространенными причинами острого гастрита являются:
- инфекции желудочно-кишечного тракта (гастроэнтерит);
- бесконтрольный прием болеутоляющих средств и препаратов, содержащих кортизон;
- инфицирование бактерией Helicobacter pylori;
- тяжелые и сложные операции;
- ожоги щелочами или кислотами;
- воздействие ядов или пищевые отравления.
Развиться гастрит также может при злоупотреблении спиртными напитками. Алкоголь стимулирует выработку желудочной кислоты. Таким образом, в краткосрочной перспективе может возникнуть подкисление желудка. Кроме того, спиртные напитки атакуют защитный слой слизистой оболочки желудка, способствуя воспалению.
Особенно выраженным может быть воспаление слизистой оболочки желудка после тяжелых и сложных операций или при жертвах ожогов. В обеих ситуациях для организма возникает максимальный стресс, и желудок особенно восприимчив к раздражению слизистой оболочки желудка.
Симптомы гастрита
Острое воспаление слизистой, сводится к дистрофически-некробиотическому повреждению железистого аппарата и поверхностного эпителия слизистой. Данное состояние приводит к воспалительным изменениям и, как правило, не остается незамеченным. После приема пищи возникают сильные боли, иррадиирующие в спину.
Другие жалобы, вызванные гастритом, могут включать:
- выраженный дискомфорт при пальпации;
- снижение аппетита;
- вздутие живота.
Из-за большого количества желудочной кислоты также возникает изжога или отрыжка кислым содержимым.
Хронический гастрит, как правило, не вызывает сильного дискомфорта, поэтому часто остается незамеченным. Конкретные симптомы: изжога, вздутие живота или ощущение тяжести после еды.
Даже если признаки хронического гастрита не слишком выражены, к ним все же следует относиться серьезно. При повторяющемся или продолжающемся более 3-4 недель дискомфорте в верхней части живота рекомендуется обратиться к врачу. Важно своевременное лечение хронического воспаления слизистой. В противном случае может развиться язва и кровотечение.
Диагностика гастрита
Для постановки диагноза и определения формы заболевания назначаются следующие исследования:
- эзофагогастродуоденоскопия (зондирование);
- дыхательный тест для определения H.pylori;
- исследование желудочного сока на кислотность;
- анализ крови на анемию и воспаление.
Лечение гастрита
При остром гастрите часто лечение не требуется. Острая фаза длится около 24 часов. Корректируется, как правило, 24-часовой диетой. За это время слизистая оболочка желудка восстанавливается. Если причина гастрита заключается в приеме лекарств, таких как ревматические болеутоляющие средства, то лечение проводится ингибиторами протонного насоса или производными простагландина.
Особенности лечения гастрита в зависимости от его типа:
- Хронический типа А и В. Для лечения анемии вводится витамин B12 витамин. Поскольку при гастрите типа А существует повышенный риск рака желудка, следует проводить регулярное ежегодное эндоскопическое обследование со взятием образцов тканей слизистой оболочки желудка (биопсия).
- Гастрит типа B (инфекция Helicobacter pylori). Терапия направлена на подавление возбудителя лекарственными средствами. Стандартом является сочетание антибиотиков и ингибиторов протонного насоса. Только с помощью этого комбинированного лечения удается напрямую бороться с возбудителем H. pylori.
- Хронический гастрит типа С. Наиболее эффективной терапией является снижение производства желудочной кислоты, поэтому повреждение слизистой оболочки желудка может заживать или не прогрессировать дальше. Используются ингибиторы протонного насоса.
В качестве дополнительного лечения при инициировании гастрита желчными соками может быть ускорено опорожнение желудка, чтобы время контакта желчных соков со слизистой оболочкой было как можно меньше. Это может быть достигнуто путем введения определенных препаратов, называемых прокинетиками.
Рейтинг лучших препаратов для лечения гастрита взрослым
№1 – «Омез» (омепразол).
Снижает секрецию соляной кислоты. При однократном использовании оказывают обратимое угнетение. Оказывает бактерицидное действие на H.pylori. Выпускается в форме капсул с дозировкой по 10, 20 и 40 мг.
№2 – «Алмагель» (алгелдрат, магния гидроксида паста).
Выпускается в форме суспензии. Нейтрализует соляную кислоту, уменьшая переваривающую активность желудочного сока. Обладает обволакивающим действием и предохраняет слизистую от раздражения.
№3 – «Маалокс» (алгелдрат, магния гидроксид).
Нейтрализует соляную кислоту в желудке, не вызывая вторичной гиперсекреции. Повышает pH желудочного сока и обволакивает стенки, уменьшая негативное воздействие повреждающих факторов.
№4 – «Де-Нол» (висмута трикалия дицитрат).
Противоязвенное средство, которое эффективно подавляет H. pylori. Оказывает вяжущее и противовоспалительное действие. Выпускается таблетированной форме по 56 и 112 шт.
№5 – «Пиобактериофаг» (пиобактериофаг).
Назначается при атрофической форме гастрита в комплексной терапии. Антибактериальный препарат, эффективный против протеи, стафилококка, стрептококка и пр. Предварительно необходимо определить фагочувствительность возбудителя. Выпускается в форме раствора для приема внутрь во флаконах по 20 и 100 мл.
№6 – «Гастрофарм» (Lactobacillus delbrueckii spp. bulgaricus штамм 51 (LB-51)).
Назначается для лечения эрозивного гастрита. Оказывает защитное действие на слизистую желудка, стимулирует процессы регенерации. Также устраняет боль и обладает антацидным эффектом (уменьшает кислотность желудка).
№7 – «Хилак форте» (Escherichia coli, Lactobacillus acidophilus, Lactobacillus helveticus, Enterococcus faecalis DSM).
Препарат биологического происхождения для регулирования равновесия кишечной микрофлоры. Помогает справиться с гастритом и дуоденитом.
№8 – «Омепразол» (омепразол).
Ингибитор протонного насоса снижает секрецию желез желудка, независимо от природы раздражителя. Обладает выраженным бактерицидным эффектом, быстро купирует симптомы гастрита. Производители: Синтез ОАО (Россия), ПРО МЕД (Россия), Озон ООО (Россия), Teva (Испания).
№9 – «Ультоп» (омепразол).
Снижает уровень секреции соляной кислоты в желудке, оказывает бактерицидный эффект на H. pylori , купируя симптомы гастрита и заживляя слизистую желудка.
Перед началом лекарственной терапии рекомендуется проконсультироваться с врачом. Самолечение может стать причиной необратимых процессов в организме, что приведет к развитию осложнений.
Меры профилактики
Чтобы гастрит вообще не возникал, нужно придерживаться ряда рекомендаций:
- Нормализуйте психосоциальное здоровье.
- Не принимайте болеутоляющие средства на постоянной основе и без предварительной консультации с врачом.
- Не злоупотребляйте алкоголем, крепким чаем и кофе.
- Откажитесь от сигарет, и исключите из меню цитрусовые.
Лечение у взрослых рекомендуется начинать при первых симптомах гастрита. Препараты должен подбирать врач, опираясь на тип заболевания. Самую эффективную схему лечения гастрита может назначить специалист только после получения результатов комплексной диагностики.
Литература:
https://med-tutorial.ru/sprav/zabolevaniya/bolezni-organov-pishhevareniya/gastrit
https://бмэ.орг/index.php/ГАСТРИТ
https://med-info.ru/reference/disease/1515
https://www.rlsnet.ru/mkb_index_id_4545.htm
«Хронический гастрит» или «хронический гастродуоденит» – диагноз, который чрезвычайно часто реализуется в медицинской практике, причем не всегда его формулировка отражает существенную сторону заболевания у конкретного больного. Можно сказать, что это «дежурный» диагноз для больного, который обратился к врачу по поводу диспептических жалоб и у которого при эндоскопии не обнаружена язва. За последние годы медицинской наукой был сделан значительный шаг вперед, позволивший на качественно новом уровне знаний пересмотреть наши представления о гастрите.
Решающее значение имело открытие нового вида микроорганизма – бактерии Helicobacter pylori (H.pylori) – и изучение ее роли в патологии человека. Стало очевидным, что этот микроб, колонизирующий слизистую оболочку желудка, выступает возбудителем наиболее частого из вариантов гастрита. Действительно, именно установление этиологического значения H.pylori сделало хронический гастрит четко очерченной и клинически значимой нозологической единицей, превратило его из аморфного понятия в заболевание с известной причиной, прослеживаемыми этапами патогенетического развития, определенным прогнозом и, наконец, создало возможности этиотропного лечения. Классические представления о гастрите благодаря H.pylori приобрели большую устойчивость, так как это фрагмент знания позволил сбалансировать имевшуюся информацию о морфологических и функциональных изменениях (кислотная продукция, слизеобразование и др.) и связи гастрита с другими заболеваниями, в первую очередь, – язвенной болезнью и раком желудка [2,3,4].
Вторым существенным шагом стала разработка современной классификации гастритов. Так называемая Сиднейская система была предложена в 1990–м и дополнена в 1994 году. С тех пор, хотя и не лишенная недостатков (как любая классификация), Сиднейская система признана почти во всем мире. Она оказалась удобной в повседневной диагностической практике, обеспечила единый концептуальный подход и язык в описании изменений желудка. Безусловным положительным качеством классификации следует считать предложенную визуально–аналоговую шкалу для полуколичественного определения активности и выраженности гастрита, атрофии и кишечной метаплазии, степени колонизации H.pylori, что существенно снизило субъективность оценок при характеристике гистологической картины.
Хронический гастрит,
вызванный инфекцией H.pylori
Частота
Инфекция H.pylori имеет глобальное значение и широко распространена, в том числе и в нашей стране, где по эпидемиологическим данным инфицированы более 80% взрослого населения. H.pylori практически у всех инфицированных индивидуумов вызывает воспалительные изменения в гастродуоденальной слизистой оболочке, которые и представляют собой собственно субстрат гастрита. Геликобактерный гастрит – наиболее распространенный вариант гастрита. Так, около 5% всех больных гастритом страдают аутоиммунным гастритом, еще 5% – другими особыми формами гастрита, о которых речь пойдет ниже. Таким образом, воспаление слизистой оболочки желудка, вызванное H.pylori, составляет 90% среди всех форм гастритов.
H.pylori – этиологический фактор хронического гастрита
Этиологическое значение микроорганизма подтверждено вескими доказательствами, основные из которых приведены в таблице 1. После приема per os культуры H.pylori удалось воспроизвести возникновение типичных для гастрита морфологических изменений в ранее нормальной слизистой оболочке в опытах по самозаражению, один из которых провел первооткрыватель бактерии Б. Маршалл. Проводятся исследования на лабораторных животных, у которых воспроизводится формирование гастрита под воздействием бактерии–возбудителя.
Заражение H.pylori приводит к появлению воспалительного инфильтрата в слизистой оболочке желудка, а присутствие H.pylori всегда сопровождается морфологическими признаками гастрита. Инфильтрация полиморфноядерными лейкоцитами (нейтрофилами) непосредственно вызвана бактерией, которая выделяет особый белок, активирующий нейтрофилы. Ген, кодирующий его синтез (napA) выявлен у всех штаммов H.pylori. Таким образом, этому микроорганизму присуще специфическое качество вызывать нейтрофильную инфильтрацию слизистой оболочки желудка, характеризующую активность гастрита. Адгезия H.pylori к клеткам желудочного эпителия, так же как адгезия в случае любой другой бактериальной инфекции слизистой оболочки, вызывает реорганизацию цитоскелета эпителиоцитов и ряд других изменений; эпителиальные клетки отвечают на это продукцией цитокинов – интерлейкина–8 (IL–8) и некоторых других хемокинов. Эти цитокины также приводят к миграции лейкоцитов из кровеносных сосудов, развивается активная стадия воспаления. Активированные макрофаги секретируют интерферон–g и фактор некроза опухоли. Эти факторы сенситизируют рецепторы лимфоидных, эпителиальных и эндотелиальных клеток, что в свою очередь привлекает в слизистую оболочку новую волну клеток, участвующих в иммунных и воспалительных реакциях. Каталаза и супероксиддисмутаза, продуцируемые Н.pylori, нейтрализуют фагоциты, позволяют микробу избежать фагоцитоза и способствуют гибели полиморфноядерных лейкоцитов. Метаболиты активного кислорода нейтрофилов оказывают повреждающее действие на эпителиоциты желудка. Хроническая фаза инфекции отличается значительной лимфоцитарной инфильтрацией и потерей целостности эпителия.
Согласно современным представлениям, Н.pylori вызывает изменение нормальных процессов регенерации желудочного эпителия: микроорганизм обусловливает (прямо или косвенно) дисрегенераторные процессы, которые служат важной составляющей в патогенезе гастрита; Н.pylori влияет и на пролиферацию, и на апоптоз эпителиоцитов слизистой оболочки желудка. Понятно, что нарушение процессов клеточного обновления в слизистой оболочке желудка лежит в основе морфогенеза атрофии при гастрите.
Важное доказательство этиологической роли Н.pylori очень легко получить в повседневной практике, так как после успешного лечения инфекции наступает регрессия отдельных компонентов морфологической картины гастрита.
Исходы инфекции H.pylori
Заражение H.pylori происходит преимущественно в детском возрасте и без лечения персистенция микроорганизма становится пожизненной. В зависимости от вирулентных свойств H.pylori и генетических особенностей макроорганизма исходы инфекции H.pylori различны: у большинства инфицированных хронический гастрит протекает бессимптомно, у части больных (по данным некоторых авторов, у 6% инфицированных) развивается язвенная болезнь, у части больных прогрессирование гастритических изменений приводит к развитию рака желудка. Несомненна связь H.pylori с редкой формой злокачественной опухоли желудка – лимфомой, исходящей из лимфоидной ткани, ассоциированной со слизистыми оболочками (MALT–лимфомы).
Исходы инфекции H.pylori зависят от варианта хронического гастрита, который, в свою очередь, во многом определяется топографией колонизации H.pylori гастродуоденальной слизистой оболочки. Дуоденальная язва возникает на фоне гастродуоденита, т.е. преимущественно антрального гастрита, а заселение слизистой оболочки двенадцатиперстной H.pylori возможно после формирования в ней очагов желудочной метаплазии в ответ на кислотную агрессию. Высказано предположение о том, что начальными центрами ульцерации при язвенной болезни двенадцатиперстной кишки оказыввются очаги метаплазии с адгезированными H.pylori и воспалительными изменениями. Язвы желудка формируются на фоне диффузного (пан–)гастрита или гастрита преимущественно тела желудка, при котором слизистая оболочка, «ослабленная» воспалением, подвергается воздействию факторов агрессии даже при нормальных показателях кислой секреции. В таблице 2 представлены варианты хронического гастрита, определяющие возможность возникновения язвенной болезни или рака желудка [1].
Инфекция H.pylori признана Международным Агентством по исследованию рака ВОЗ канцерогенной для человека. Связь H.pylori и рака желудка в настоящее время не вызывает сомнений, и связующим звеном рассматривается хронический гастрит. Длительная персистенция H.pylori сопровождает прогрессирование гастритических изменений: с годами гастрит становится атрофическим. Еще до открытия H.pylori было известно, что атрофический гастрит может рассматриваться, как предраковое заболевание. Значимость атрофического гастрита в канцерогенезе определяется частотой – на его долю приходится 3/4 в структуре предраковых заболеваний желудка. Известно, что риск развития карциномы желудка при атрофическом гастрите в 10 раз выше, чем в популяции. Дальнейшее углубление гастритического процесса связано с формированием кишечной метаплазии: особенно опасно появление неполной (или толстокишечной) метаплазии. Именно этот эпителий при определенных условиях может стать основой дисплазии и малигнизации. Таким образом, патогенетический каскад, запускаемый H.pylori и через стадии атрофии, метаплазии и дисплазии приводящий к раку желудка, хорошо изучен и приблизился к завершенности благодаря установлению этиологической роли бактерии для хронического гастрита.
Лечение хронического
геликобактерного гастрита
Современная терапия хронического гастрита – это этиологическая терапия, направленная на эрадикацию инфекции H.pylori. Стандарты (протоколы) диагностики и лечения больных с заболеваниями органов пищеварения, утвержденные Министерством здравоохранения РФ, относят антигеликобактерные схемы к необходимым лечебным мероприятиям при гастрите с выявлением H.pylori. Однако мы знаем, что хронический гастрит, ассоциированный с H.pylori, – чрезвычайно широко распространенное заболевание. Имея основание для проведения антигеликобактерной терапии при гастрите, необходимо понять, каким конкретно больным показана эта терапия. Рекомендации по диагностике и лечению инфекции H.pylori, принятые для стран Европейского Союза в 1997 году (Маастрихтский консенсус – I) в качестве показания для эрадикационной терапии называли варианты гастрита с тяжелыми структурными изменениями – с кишечной метаплазией, атрофией, а также гастрит с эрозиями. В итоговом документе Второй согласительной конференции по диагностике и лечению инфекции H.pylori (Маастрихтский консенсус – II, 2000) в качестве безусловного показания к эрадикационной терапии установлена только одна форма гастрита – атрофический гастрит.
Анализ большого числа клинических испытаний позволяет выделить лучшие схемы для лечения инфекции H.pylori, отвечающие требованиям медицины, базирующейся на доказательствах. Эти схемы нашли отражение в итоговом документе Второй согласительной конференции по диагностике и лечению инфекции H.pylori (2000) В качестве начального курса лечения (терапия первой линии) предлагаются следующие схемы из трех препаратов как минимум на 7 дней: ингибитор протонной помпы (или ранитидин висмут цитрат) в стандартной дозе 2 раза в день + кларитромицин 500 мг 2 раза в день + амоксициллин 1000 мг 2 раза в день или метронидазол 500 мг 2 раза в день. Сочетание кларитромицина с амоксициллином предпочтительнее, чем кларитромицина с метронидзолом, так как может способствовать достижению лучшего результата при назначении лечения второй линии – квадротерапии.
В случае отсутствия успеха лечения начинается второй этап. Больному предлагается резервная схема (терапия второй линии – квадротерапия) как минимум на 7 дней: ингибитор протонной помпы в стандартной дозе 2 раза в день + висмута субсалицилат/субцитрат 120 мг 4 раза в день + метронидазол 500 мг 3 раза в день + тетрациклин 500 мг 4 раза в день.
В нашей стране в качестве терапии первой линии широко используются тройные схемы на основе препарата висмута (наиболее известен субцитрат коллоидного висмута). Следует отметить, что именно для лечения хронического гастрита такие схемы могут оказаться наиболее приемлемыми, так как при назначении эрадикации H.pylori в случае обострения язвенной болезни необходимость быстрого купирования болевого и диспептического синдрома заставляет отдать предпочтение схемам на основе ингибиторов протонной помпы. При хроническом гастрите, который не имеет симптоматики, тройные схемы на основе соли висмута могут оказаться оптимальными по соотношению «стоимость – эффективность».
Обратимость изменений,
присущих хроническому гастриту,
под влиянием эрадикации H.pylori
После эрадикации инфекции уже через месяц полностью исчезает нейтрофильная инфильтрация эпителия и собственной пластинки слизистой оболочки (отражающая активность гастрита), а в более поздние сроки исчезает мононуклеарная инфильтрация. Таким образом, хронический неатрофический гастрит полностью излечивается после уничтожения H.pylori. В отношении возможности обратного развития атрофии и кишечной метаплазии после эрадикации инфекции в литературе существуют противоречивые мнения (табл. 3). Возможно, что период наблюдения слишком ограничен для оценки таких изменений, однако были и исследования с относительно продолжительным катамнезом, которые также дали противоположные результаты. Тем не менее представляется вполне обоснованным, что успешная эрадикация H.pylori даже на этапе атрофии, приводит к прерыванию патологического каскада в слизистой оболочке желудка и может рассматриваться, как профилактика развития рака желудка. В пользу эрадикации H.pylori у больных атрофическим гастритом свидетельствует целый ряд работ (в том числе проведенных в нашей клинике), доказывающих, что уничтожение инфекции нормализует процессы клеточного обновления в слизистой оболочке желудка.
Хронический геликобактерный гастрит и функциональная диспепсия
Соотношение хронического геликобактерного гастрита и функциональной диспепсии
Диагноз гастрит – диагноз морфологический, то есть он может считаться правомочным после оценки гастробиоптатов специалистом – патологоанатомом. В соответствии с требованиями Сиднейской системы, для того чтобы правильно интерпретировать состояние слизистой оболочки желудка, необходимо минимум пять биоптатов: 2 – из антрального отдела на расстоянии 2–3 см от привратника по большой и малой кривизне, 2 – из тела желудка на расстоянии 8 см от кардии по большой и малой кривизне, 1 – из угла желудка.
«Клинический» диагноз гастрита, т.е. диагноз без морфологического исследования гастробиоптатов практически не имеет смысла. Жалобы, а это, как правило, симптомы диспепсии, которые заставляют больного обратиться к врачу, носят функциональный характер и не обусловлены теми морфологическими изменениями, которые составляют суть гастрита. Изменения, обнаруживаемые при эзофагогастродуоденоскопии (например, гиперемия слизистой оболочки), являются субъективными и лишь косвенным образом могут свидетельствовать о наличии гастрита, в особенности о степени его прогрессирования.
В случае жалоб на боли и дискомфорт в эпигастральной области и при отсутствии изъязвления при эндоскопии и для врача, и для пациента удобен синдромный диагноз функциональной диспепсии. Такой подход позволяет врачу применить весь возможный арсенал лекарственных средств и курортных факторов и установить доверительные отношения с больным, объясняя природу его недуга функциональными причинами.
Установлены критерии диагноза функциональной диспепсии (Римские критерии II). Врач вправе поставить этот диагноз при:
• наличии постоянной или повторяющейся диспепсии (боли и дискомфорт в эпигастральной области) по крайней мере в течение 12 недель (не обязятельно последовательных) в течение последних 12 месяцев;
• отсутствии органического заболевания (в том числе и по результатам эзофагогастродуоденоскопии), которое бы объясняло наличие перечисленных симптомов;
• отсутствии облегчения симптомов после дефекации и отсутствии их связи с изменением частоты и характера стула (то есть, исключен синдром раздраженной кишки).
В зависимости от преобладающего симптома выделяют варианты функциональной диспепсии: в том случае, если ведущим симптомом выступает боль в эпигастральной области, говорят о язвенноподобном варианте; если доминирующим симптомом служит дискомфорт – чувство переполнения в эпигастрии, раннее насыщение, вздутие живота, тошнота – о дискинетическом варианте; промежуточное состояние назвали неспецифическим вариантом.
Представления о патогенезе функциональной диспепсии все еще складываются. При установлении этого диагноза должны быть исключены органические заболевания – язвенная болезнь, гастроэзофагеальная рефлюксная болезнь, опухоли, заболевания панкреато–билиарной зоны и прием лекарств, например НПВП. Однако диагнозу функциональной диспепсии не противоречит наличие хронического гастрита, ассоциированного с инфекцией H.pylori. Значение присущих гастриту морфологических изменений для функциональной диспепсии практически не известно. По данным европейских авторов (для популяций с невысоким распространением H.pylori), инфекция H.pylori обнаруживается в 30–70% случаев функциональной диспепсии. Мета–анализ D. Armstrong (1996) продемонстрировал, что H.pylori чаще встречается у больных с диспепсией, чем в среднем в популяции.
Лечение функциональной диспепсии
Отсутствие полных представлений о патогенезе функциональной диспепсии, особенности больных (в том числе психологические) делают лечение этого синдрома непростой задачей.
Антацидные препараты (Алмагель) в повседневной практике применяются, как терапия первой линии при функциональной диспепсии. Антациды хорошо знакомы пациентам и врачам, известна безопасность их использования, поэтому эта группа препаратов всегда находит применение при функциональной диспепсии. Многие больные начинают прием антацидов еще до консультации врача и будут возвращаться к нему в дальнейшем, в том числе благодаря безрецептурному отпуску.
Блокаторы Н2–рецепторов гистамина – группа лекарственных препаратов, которую чаще всего применяют в лечении функциональной диспепсии. Результаты клинических исследований противоречивы. Некоторые авторы считают, что положительный результат от антагонистов Н2–рецепторов гистамина в ряде клинических испытаний получен благодаря группе больных с гастроэзофагеальной рефлюксной болезнью, которые были вовлечены в эти испытания из–за несовершенства критериев отбора больных. Однако мета–анализ G. Dobrilla и соавт. (1989) показал, что при применении блокаторов Н2–рецепторов гистамина терапевтический эффект на 20% лучше по сравнению с плацебо. Существует мнение, что при функциональной диспепсии эффективной может оказаться высокая доза антагонистов Н2–рецепторов гистамина, но для подтверждения этого мнения необходимы серьезные клинические работы.
Ингибиторы протонной помпы практически не применялись при функциональной диспепсии. Недавно завершенное серьезное клиническое исследование с высокой статистической достоверностью продемонстрировало хороший эффект омепразола при функциональной диспепсии (табл. 4), причем лучший результат был получен в группе больных с язвенноподобным вариантом синдрома по сравнению с дискинетическим. В исследовании OCAY монотерапия омепразолом оказалась так же эффективна в купировании симптомов диспепсии, как и эрадикационная терапия инфекции H.pylori.
Противоречивые результаты получены при проведении эрадикационной терапии инфекции H.pylori при функциональной диспепсии: некоторые исследования показали улучшение клинической симптоматики после уничтожения H.pylori, некоторые исследования не получили заметного положительного эффекта после эрадикации (табл. 5). Исследование J. Gillvary и соавт. (1997) выделяется из ряда таких работ, так как в качестве эрадикационной схемы использовали классическую тройную терапию с субцитратом коллоидного висмута (табл. 6). Маастрихтский консенсус–II поставил точку в этой дискуссии и назвал функциональную диспепсию в качестве показания к эрадикационной терапии на основании следующих положений: эрадикация H.pylori является приемлемым выбором в тактике лечения функциональной диспепсии; у некоторой части больных эрадикация H.pylori приводит к длительному улучшению самочувствия.
Таким образом, этиотропное для хронического геликобактерного гастрита лечение помогает не всем больным функциональной диспепсией, что свидетельствует об отсутствии тождественности этих заболеваний и о неоднородности больных функциональной диспепсией. Вероятно, воспалительные изменения слизистой оболочки желудка не являются основной причиной диспептических симптомов.
Негеликобактерные гастриты
Аутоиммунный гастрит
После широко распространенного геликобактерного гастрита наибольшее клиническое значение имеет аутоиммунный гастрит, ассоциированный с пернициозной анемией, который в Сиднейской системе помещен под рубрикой атрофического гастрита. При этом заболевании в 90% случаев обнаруживаются антитела к париетальным клеткам и к Н+,К+–АТФазе, в 60% случаев – антитела к фактору Касла, в 50% случаев– антитиреоидные антитела. Резко выраженная атрофия фундальных желез клинически проявляется ахилией, при этом характерна ответная гипергастринемия и гиперплазия G–клеток. Риск возникновения рака желудка на фоне аутоиммунного гастрита в 3–10 раз выше, чем в популяции.
Особые формы гастрита
В Сиднейской системе к особым формам гастрита отнесены химический, радиационный и инфекционный гастриты, которые мы группируем по этиологическому признаку, и эозинофильный, лимфоцитарный и гранулематозный гастриты, которые мы группируем по их морфологическим особенностям и диагностике.
Это достаточно редкие заболевания, уступающие по своему клиническому значению хроническому геликобактерному гастриту, который благодаря изучению H.pylori мы можем сегодня успешно распознавать и лечить.
Литература
1. Аруин Л.И, Капуллер Л.Л., Исаков В.А. Морфологическая диагностика болезней желудка и кишечника. Москва, Триада–Х, 1998 г.
2. Ивашкин В.Т., Успенский В.М. Некоторые функциональные и гистохимические изменения в двенадцатиперстной кишке при язвенной болезни (по данным телеметрии и дуоденобиопсии). // Советская медицина, 1970, № 3, С. 10–14.
3. Ивашкин В.Т., Дорофеев Г.И. Нарушения резистентности слизистой оболочки желудка и двенадцатиперстной кишки при хроническом гастрите и язвенной болезни. // Советская медицина, 1983, № 2, С. 10–15.
4. Ивашкин В.Т. Эрадикация инфекции Helicobacter pylori и ремиссия язвенной болезни: однозначны ли эти состояния? // Российский журнал гастроэнтерологии, гепатологии и колопроктологии, 1999, Т.8, № 3, С. 71–73.
Гидроксид алюминия + гидроксид магния–
Алмагель (торговое название)
(Balkanpharma)
Омепразол–
Гастрозол (торговое название)
(ICN Pharmaceuticals)
Коллоидный субцитрат висмута–
Де–Нол (торговое название)
(Yamanouchi Europe)
Резюме. Гастрит представляет собой реакцию слизистой оболочки (СО) желудка на повреждение и характеризуется формированием воспалительных, дистрофических и дисрегенераторных изменений в СО желудка, а также атрофией эпителиальных клеток с замещением нормальных желез фиброзной тканью. Прогрессирование хронического гастрита (ХГ) сопровождается развитием атрофии, дисплазии СО и становится значимым фактором формирования злокачественных новообразований желудка. В статье приводятся современная этиологическая классификация ХГ, подходы к диагностике ХГ, оценке стадии гастрита по шкале прогрессирующего увеличения вероятности развития рака желудка, представлены гистологические характеристики, а также обоснованы этиопатогенетические подходы к терапии различных форм ХГ, включая методы оптимизации эрадикационной терапии инфекции H. pylori, которые могут быть применены для повышения эффективности не только стандартной тройной терапии, но и других режимов антихеликобактерного лечения. Рассмотрено примение ингибиторов протонной помпы в терапии гастрита.
«Лечащий врач» осваивает новые пространства и форматы. Вся актуальная информация (и даже больше) – в нашем телеграм канале. Подписывайтесь!
Хронический гастрит (ХГ) – широко распространенное заболевание пищеварительной системы, регистрируемое у 15-30% населения в различных популяциях и составляющее 80-85% всех заболеваний желудка [1-3]. Медико-социальная значимость проблемы заключается в том, что прогрессирование ХГ сопровождается развитием атрофии, дисплазии слизистой оболочки (СО) и становится значимым фактором формирования злокачественных новообразований желудка [4, 5].
Целью данного обзора было представить гистологическую характеристику и обосновать этиопатогенетические подходы к терапии различных форм ХГ.
Дефиниции
Гастрит представляет собой реакцию СО на повреждение и характеризуется формированием воспалительных, дистрофических и дисрегенераторных изменений в СО желудка, а также атрофией эпителиальных клеток с замещением нормальных желез фиброзной тканью. Развитие этого заболевания сопровождается нарушением секреторной и моторной функций желудка.
К настоящему времени сложилось устойчивое мнение о том, что диагноз гастрита должен быть верифицирован морфологически. Основным гистологическим признаком заболевания являются инфильтрация собственной пластинки воспалительными клетками и структурные изменения железистого аппарата слизистой желудка [5]. При гистологическом исследовании гастрит подтверждается наличием нейтрофилов или мононуклеарных клеток 2-й степени по крайней мере в одном участке биопсии желудка либо нейтрофилов или мононуклеарных клеток 1-й степени по меньшей мере в двух участках [6]. Воспалительный инфильтрат представлен лимфоцитами, плазматическими клетками, гистиоцитами и гранулоцитами, расположенными диффузно или в виде скоплений в собственной пластинке СО, иногда – внутри желез. Активность воспалительного процесса определяется степенью инфильтрации полиморфноядерными лейкоцитами (нейтрофилами и ацидофильными гранулоцитами) собственной оболочки (lamina propria) слизистой желудка [7].
Международная группа патологов Оперативного звена для оценки гастрита (Operative Link for Gastritis Assessment – OLGA) предложила интегральный метод оценки выраженности морфологических изменений СО желудка и стандартизировала гистологические фенотипы по степени и стадии развития (OLGA Staging System) [8-11]. Локализация нейтрофилов определяет степень: нейтрофилы в собственной пластинке оболочки – легкая (+-) активность; нейтрофилы в эпителии – умеренная (++-) активность и нейтрофилы в просвете железы – выраженная (+++) активность.
Прогрессирование заболевания сопровождается замещением собственных железистых структур lamina propria фиброзной тканью (неметапластическая атрофия) или заменой желез метапластическими железами. Метапластическая атрофия может иметь два фенотипа: кишечная метаплазия (КМ), поражающая слизистые железы, и псевдопилорическая метаплазия, которая также известна как метаплазия псевдопилорических желез. Система позволяет оценить стадию гастрита по шкале прогрессирующего увеличения вероятности развития рака желудка – риск от самого низкого (стадия 0) до самого высокого (стадия IV). Таким образом, под степенью гастрита подразумевается выраженность суммарной воспалительной инфильтрации (нейтрофильными лейкоцитами и мононуклеарными клетками), под стадией – выраженность атрофии. Такая система дает достаточно полную характеристику гастрита и отражает его динамику.
Альтернативная система определения стадии заболевания (Operative Link on Gastric Intestinal Metaplasia Assessment – OLGIM) предлагает рассматривать только КМ для оценки атрофии [9]. Различение неатрофического и атрофического гастрита необходимо, чтобы получить информацию о том, за какими пациентами требуется клиническое/эндоскопическое наблюдение.
Этиология ХГ
Современная этиологическая классификация ХГ была предложена в 2015 г. на Международном консенсусе в Киото (Япония) [12].
С учетом этиологического фактора различают следующие формы гастрита:
I. Аутоиммунный ХГ (АИГ) (этиология неизвестна; аутоиммунный патогенез).
II. Инфекционный ХГ.
- ХГ, индуцированный Helicobacter pylori (H. pylori).
- Бактериальный нехеликобактерный ХГ (энтерококки, микобактерии, бледная трепонема).
- Вирусный ХГ (энтеровирус, цитомегаловирус).
- Грибковый ХГ (желудочный мукормикоз, кандидоз, гистоплазмоз).
- Паразитарный ХГ (при криптоспоридиозе, стронгилои-дозе, анизакидозе).
III. Экзогенный ХГ (лекарственный, алкогольный, радиационный, вызванный химическими веществами).
IV. ХГ, вызванный воздействием специфических причин (лимфоцитарный, гигантский гипертрофический (болезнь Менетрие), аллергический, эозинофильный).
V. Вторичный ХГ, вызванный другими заболеваниями (при саркоидозе, васкулитах, болезни Крона).
Аутоиммунный хронический гастрит
В общей популяции встречается нечасто – менее чем в 1% случаев, а среди больных ХГ – до 5% [13]. Заболевание вызывает поражение фундального отдела и тела желудка. АИГ является наследственно обусловленным и передается как аутосомно-доминантный признак, часто сочетаясь с другими аутоиммунными заболеваниями (сахарным диабетом 1 типа, тиреоидитом Хашимото, синдромом Шегрена) [14]. Патогенетически это аутоиммунная патология, связанная с наличием антител, направленных против париетальных клеток желудка и их компонентов (внутренний фактор и протонная помпа) с формированием атрофии СО желудка. Прогрессивное снижение количества париетальных клеток приводит к гипохлоргидрии вплоть до анацидного состояния. Снижение синтеза соляной кислоты стимулирует G-клеточную гиперплазию и таким образом способствует повышению уровня гастрина в сыворотке крови. В свою очередь гипергастринемия создает условия для гиперплазии энтерохромаффиноподобных клеток, которые иногда трансформируются в злокачественную опухоль желудка [15]. Относительный риск развития аденокарциномы желудка у этих больных возрастает в 3 раза [16]. Снижение образования внутреннего фактора приводит к мальабсорбции витамина В12 и его дефициту в организме, что может стать причиной пернициозной (мегалобластной) анемии, а также множественных неврологических расстройств (фуникулярный миелоз) [15].
Типичные гистологические паттерны аутоиммунного гастрита [16-18]
- Инфильтрация лимфоцитарными и плазматическими клетками собственной пластинки на всю толщину СО; редкие эозинофилы и нейтрофилы.
- Разрушение желудочных желез с ассоциированной псевдопилорической метаплазией и плотным лимфоплазмоцитарным инфильтратом в собственной пластинке СО.
- Прогрессирующее разрушение желез, сопровождающееся КМ.
- Полная замена желудочных желез метапластическим эпителием; не имеет выраженного воспалительного компонента.
Другие гистологические паттерны
- Линейная или узловая гиперплазия энтерохромаффино-подобных клеток вследствие гипо- и ахлоргидрии, стимулирующей повышенную секрецию гастрина антральными G-клетками.
- Изменения антрального отдела часто имитируют реактивную гастропатию и показывают гиперплазию G-клеток [16-18].
ХГ, ассоциированный с инфекцией H. pylori
Инфекция H. pylori – наиболее частая причина развития ХГ. Заболевание первоначально развивается как хронический активный гастрит, при котором H. pylori обнаруживается как в антральном отделе, так и в теле желудка (обычно в большем количестве в антральном отделе). Длительно сохраняющийся активный гастрит, ассоциированный с H. pylori, создает условия для развития вторичной атрофии СО желудка. Так, по результатам 10-летнего проспективного наблюдения больных хеликобактерным активным гастритом, атрофия выявлена у 6% пациентов через 2 года, у 22% – через 4 года, у 34% – через 6 лет и у 43% – через 10 лет наблюдения, при этом в группе контроля (Нр-негативные) атрофия не развивалась [19].
Гистология процесса представлена следующим образом: полиморфноядерные лейкоциты инфильтрируют собственную пластину, железы и фовеолярный эпителий, образуя небольшие микроабсцессы. Наблюдаются лимфоидные агрегаты и лимфоидные фолликулы, расширяющие собственную пластинку СО, иногда лимфоциты проникают в эпителий. Инфекция H. pylori – основная причина вторичной атрофии СО желудка. Атрофические изменения (как метапластические, так и неметапластические) в образце биопсии из угла и антрального отдела в первую очередь следует рассматривать как доказательства хеликобактерного гастрита. На поздних стадиях атрофии, связанной с хронической инфекцией H. pylori, как в теле, так и в антральном отделе наблюдается обширное замещение КМ, связанной с развитием гипохлоргидрии. По мере распространения КМ количество бактерий H. pylori, обнаруживаемых в желудке, уменьшается, так как H. pylori исчезает из участков метапластического эпителия. Особое значение этой проблеме придает то, что атрофический гастрит является начальной ступенью каскада изменений СО, приводящего к злокачественному новообразованию желудка (каскад Корреа) [20]. Вероятность развития рака желудка возрастает по мере нарастания тяжести атрофии слизистой, и этот риск находится в прямой зависимости от степени атрофических изменений, выявляемых в антральном отделе и в теле желудка, в особенности при наличии метаплазии [21]. Длительное течение гастрита, ассоциированного с H. pylori, повышает вероятность развития злокачественной опухоли желудка в 6 раз [21].
Типичные гистологические паттерны
- Хронический антральный гастрит: инфильтрация собственной пластинки плазматическими клетками, лимфоцитами и небольшим количеством эозинофилов.
- Активный хронический антральный гастрит: когда вышеперечисленные признаки связаны с нейтрофилами.
- Лимфоидные фолликулы в СО антрального отдела встречаются часто, но неспецифичны.
Варианты гистологических паттернов
- Может проявляться как пангастрит.
- В двенадцатиперстной кишке могут наблюдаться метаплазия и дуоденит.
- Использование ингибиторов протонной помпы (ИПП) облегчает проксимальную миграцию организмов и глубже в железы.
- Гиперпластические полипы (таким пациентам рекомендуется эрадикация H. рylori).
- Острый гастрит – начальная переходная стадия, за которой следует разрешение или начало ХГ.
- Кокковая форма H. pylori чаще всего обнаруживается у пациентов, недавно принимавших ИПП или эрадикационную терапию.
Последствия
- Атрофический антральный гастрит тела желудка.
- Язвы желудка.
- Язвы двенадцатиперстной кишки: ассоциированные с антральным гастритом обычно наблюдаются в первой части двенадцатиперстной кишки, дистальнее привратника.
- КМ, часто затрагивающая угол или антральный отдел.
- Лимфоцитарный гастрит (ЛГ).
Цитомегаловирусный (ЦМВ) гастрит
Единственная вирусная инфекция желудка с отчетливой патологической картиной. Преимущественно поражает детей и пациентов с ослабленным иммунитетом. Обычно поражаются разные участки желудочно-кишечного тракта. Эндоскопически СО желудка может выглядеть полностью нормальной или иметь эрозии и язвы. В редких случаях это может быть образование, называемое псевдоопухолью. Гистологически многочисленные включения ЦМВ в эпителиальных клетках можно увидеть реже, чем в эндотелиальных, а также в макрофагах с незначительным воспалением или его отсутствием. В этом случае иммунологический статус пациентов обычно сильно подавлен. В других случаях может наблюдаться обильная грануляционная ткань с серьезной воспалительной реакцией, в то время как включения ЦМВ трудно увидеть без методов иммуногистохимии или гибридизации in situ. Эозинофильные инфильтраты также могут быть важным компонентом воспаления при ЦМВ-гастрите [7].
Гастрит, вызванный лекарственными средствами; алкогольный гастрит; лучевой гастрит, рефлюкс-гастрит
Химические агенты увеличивают обновление эпителия желудка, что приводит к фовеолярной гиперплазии. Эти состояния часто протекают бессимптомно, но они могут привести к множественным эрозиям или язвам, даже с кровотечением. Атрофические изменения встречаются редко [7].
Диагноз основан на микроскопическом исследовании СО желудка, и, согласно существующему определению, основным его признаком является наличие не менее 25 интра-эпителиальных лимфоцитов на 100 эпителиальных клеток желудка. Большинство этих лимфоцитов имеют фенотип CD3+ и CD8+. Известно, что инфекция H. pylori связана с ЛГ, достигая от 0% до 27% случаев. Связь между ЛГ и глютеновой болезнью установлена и колеблется от 10% до 38% [7].
Эозинофильный гастрит (ЭГ)
Является частью семейства эозинофильных желудочно-кишечных расстройств, которое включает эозинофильный эзофагит, эозинофильный гастроэнтерит и эозинофильный энтерит/колит, связанные с триггерами пищевых аллергенов. У многих пациентов в анамнезе были атопические состояния, включая астму, аллергический ринит или атопический дерматит, а также аллергию на лекарственные продукты или пыльцу. Рекомендованы два основных критерия диагностики ЭГ: 1) в биоптате желудка средняя плотность эозинофилов > 127/мм2 (или > 30 эозинофилов/поле высокого увеличения (HPF) на микроскопах, оснащенных широкоугольными окулярами (FN 22), по крайней мере в пяти отдельных HPFs); 2) отсутствие известных ассоциированных причин эозинофилии (например, инфекция H. pylori, болезнь Крона, паразитарные инфекции, а также гематологические или лимфоидные нарушения) [7].
Диагностика ХГ
Диагностика ХГ включает клиническое обследование, cерологическое исследование (пепсиногены и антитела против инфекционных агентов и/или аутоантигены), эндоскопию верхних отделов желудочно-кишечного тракта (с применением стандартизированных протоколов биопсии) и последующее гистологическое исследование. Гистологическое изучение биоптата является «золотым стандартом» в диагностике заболевания. Прицельная биопсия из пяти мест: антральный отдел, большая (А1) и малая кривизна (А2), угол (А3) и тело желудка, большая (С1) и малая кривизна (С2).
Стандартизация морфологических признаков ХГ нашла отражение в полуколичественных системах гистологической классификации гастритов, которые были заложены Сиднейской системой (Sydney Systems, 1990) и получили дальнейшее развитие в Хьюстонской модифицированной классификации (1994) и системах OLGA и OLGIM (2008) [22-24].
Подходы к терапии отдельных форм ХГ
Своевременная диагностика и верное определение классификационной группы ХГ имеют основополагающее значение для успешного лечения этого заболевания.
Особенности АИГ зависят от стадии, наличия инфекции H. pylori, текущего дефицита питательных веществ, сопутствующих аутоиммунных состояний и риска злокачественной трансформации. Так как инфекция H. pylori может играть решающую роль в патогенезе АИГ, необходим скрининг на H. рylori пациентов с диагностированным АИГ, атрофией желудка, КМ/дисплазией и гипо- или ахлоргидрией. При положительном результате на H. pylori пациенты нуждаются в последующем лечении. Исследования подтверждают, что эрадикация H. pylori была связана со снижением уровней антител к париетальным клеткам и антител против внутреннего фактора на ранних стадиях AИГ.
Пероральный прием витамина B12, железа и фолиевой кислоты рекомендуется на ранних стадиях АИГ. При появлении неврологических симптомов следует назначать витамин B12 парентерально.
Поскольку различные аутоиммунные заболевания признаются сопутствующими AИГ, необходимо уделять внимание их скринингу и последующему лечению.
Тактика лечения AИГ с предотвращением осложнений требует надлежащего длительного наблюдения в соответствии с текущими симптомами, серологическими результатами и данными визуализации. Для этого необходим правильный мониторинг показателей – один раз в год (общий анализ крови, уровень гастрина, железа и витамина B12) [25, 26].
ХГ, вызванный Н. pylori, в том числе у «бессимптомных» лиц, является показанием к проведению эрадикационной терапии инфекции Н. pylori. Эрадикация способствует излечению хронического неатрофического гастрита, может привести к регрессии атрофического гастрита и снижает риск развития рака желудка у пациентов с неатрофическим и атрофическим гастритом. Эрадикация H. pylori у пациентов с КМ тяжелой степени, судя по всему, не приводит к существенному снижению риска развития рака желудка, как минимум в краткосрочной перспективе, однако обеспечивает снижение выраженности воспаления и атрофии, и у таких пациентов следует рассмотреть возможность ее проведения [27].
В России терапией первой линии эрадикации служит стандартная тройная терапия, включающая ИПП, кларитромицин и амоксициллин. Стандартную тройную терапию следует проводить, применяя различные меры, повышающие ее эффективность. Среди методов оптимизации, позволяющих повысить эффективность эрадикационной терапии инфекции H. pylori, следует отметить увеличение продолжительности лечения до 14 дней, выбор надежного ИПП или увеличение дозы ИПП, добавление висмута трикалия дицитрата или пробиотика. В качестве альтернативного варианта эрадикационной терапии первой линии может быть использована классическая четырехкомпонентная схема на основе висмута трикалия дицитрата или без препаратов висмута, которая включает ИПП, амоксициллин, кларитромицин и метронидазол. Квадротерапию с висмута трикалия дицитратом применяют также как основную схему терапии второй линии при неэффективности стандартной тройной терапии. Другая схема второй линии включает ИПП, левофлоксацин и амоксициллин. Тройная терапия с левофлоксацином может быть назначена только гастроэнтерологом по строгим показаниям. Терапию третьей линии подбирают индивидуально в зависимости от предшествующих схем лечения.
Методы оптимизации эрадикационной терапии инфекции H. pylori могут быть применены для повышения эффективности не только стандартной тройной терапии, но и других режимов антихеликобактерного лечения, а комбинирование этих методов позволяет добиться наилучшего результата у конкретного пациента [28].
Эрадикация H. pylori позволяет купировать симптомы диспепсии и активность гастрита.
Если все варианты терапии исчерпаны, обычное лечение будет направлено на снижение секреции кислоты СО желудка и защиту слизистого барьера.
В клинической практике кислая среда в желудке играет решающую роль в развитии гастрита, вызванного H. рylori, и ассоциированных с ним симптомов диспепсии, поэтому ИПП являются важной стратегией лечения пациентов с симптоматическим гастритом [29].
Однако механизм действия ИПП не ограничивается эффектами только кислотосупрессии. ИПП обладают собственной противовоспалительной активностью. ИПП необратимо ингибируют H+/K+-АТФазу в париетальных клетках желудка, вызывая подавление секреции кислоты. Примечательно, что ИПП, в частности омепразол, оказывают более сильное влияние на повышение внутрижелудочного pH у позитивных по H. pylori субъектов, чем у негативных [30].
Кислотообразующая АТФаза, известная как АТФаза вакуо-лярного типа, помимо париетальных клеток имеется также в лизосомах лейкоцитов, и на ее активность тоже влияют ИПП [31]. Противовоспалительный эффект ИПП включает торможение хемотаксиса и дегрануляции нейтрофилов, взаимодействие нейтрофилов с эндотелиоцитами, выработку нейтрофилами свободных радикалов [32]. Противовоспалительная активность ИПП подтверждена результатами клинических и экспериментальных исследований. В частности, в экспериментальном исследовании было оценено влияние омепразола на адгезивную активность нейтрофилов, стимулированную H. pylori. Адгезия нейтрофилов увеличивалась за счет присутствия H. рylori, тогда как введение ИПП (омепразола), напротив, значительно снижало адгезию дозозависимым образом [31].
Использование авторадиографии позволило выявить накопление 3H-лансопразола в цитоплазматических гранулах нейтрофилов, инфильтрирующих СО желудка. За счет повышения внутривакуолярного уровня pH в лизосомах нейтрофилов, ИПП ослабляют активацию нейтрофилов и высвобождение ими токсичных метаболитов [33].
В исследованиях in vivo было показано, что омепразол (1-100 мкМ) дозозависимо увеличивал рН в лизосомах, ингибировал подвижность активированных нейтрофилов, подавлял выработку ими токсичных продуктов и снижал работу лизосомальных ферментов. У здоровых добровольцев, которым вводили омепразол в дозе 40 мг/сут в течение 7 дней, выявлено значительное снижение хемилюминисценции (отражающей активности) периферических нейтрофилов [34].
Учитывая, что длительное воспаление в СО желудка сопряжено с повреждением ДНК и риском канцерогенеза, своевременное и эффективное лечение гастрита, особенно на ранних его стадиях, является важным аспектом канцеропревенции в гастроэнтерологии.
Таким образом, не вызывает сомнений тот факт, что класс ИПП является наиболее востребованным при лечении кислотозависимых заболеваний с позиции доказательной медицины. Согласно реестру Сomcon (2020) [35], омепразол занимал и продолжает занимать лидирующие позиции в назначениях докторов и полностью отвечает критериям эффективности и безопасности при лечении кислотозависимых заболеваний [36].
Среди препаратов омепразола, представленных на российском фармацевтическом рынке, одним из самых изученных и надежных, а также известных [37] является Омез®. Полный цикл производства лекарственного препарата Омез® соответствует международным стандартам GMP [сертификат, подтверждающий производство Омеза по стандартам GMP], что обеспечивает высокое качество препарата и достижение должного уровня рН в желудке у пациентов, необходимого для кислотосупрессии. Омез® включен в Оранжевую Книгу FDA с терапевтической эквивалентностью категории «А», что подтверждает его качество на мировом уровне и идентичность оригинальному омепразолу [38].
Сравнительное исследование по оценке эффективности генериков омепразола, назначаемых в течение 7 дней в параллельных группах (в одной из которых использовали ИПП Омез®, в других – небрендированные омепразолы разного производства), показало, что уровень кислотосупрессии желудка достоверно выше на фоне применения Омез® в дозе 20 мг 2 раза в сутки. Использование других генериков омепразола в приведенном исследовании не приводило к целевому снижению уровня кислоты в желудке, что очевидно отражает их потенциальную клиническую неэффективность. Полученные различия могут быть связаны как с качеством субстанции, так и различиями лекарственных форм. Все молекулы ИПП являются кислотонеустойчивыми, и потому для сохранения действующего вещества в нативном виде для всасывания в кровь в кишечнике абсолютно необходимо защитить молекулу от кислоты. Для этого в лекарственной форме имеется кишечнорастворимая оболочка. Из капсулы Омез®, которая растворяется в желудке, высвобождаются гранулы (пеллеты), покрытые кишечнорастворимой оболочкой (MUPS – multi-unit pellet system). Пеллеты правильной формы и одинакового размера, который позволяет им смешаться с химусом и без задержек отправиться в тонкую кишку. Здесь происходит растворение оболочки, выход омепразола в жидкую среду и абсорбция его энтероцитами. Этот процесс должен происходить дружно, и пик концентрации омепразола должен совпасть с пиком активации протонных насосов (для этого обязательно принять пищу через 30 мин после приема препарата ИПП), только в активированном состоянии они доступны для связывания и блокады. Очевидно, что оптимизация лекарственных форм отражается на клинической эффективности препаратов. Но это статья расходов, на которой дженериковые компании зачастую экономят. Поэтому при выборе медикаментозной кислотосупрессивной терапии следует учитывать потенциальные возможности лекарственных препаратов, ориентируясь на должный уровень эффективности [39].
Омез® – один из немногих препаратов омепразола, имеющих форму выпуска – капсулы 40 мг. Пациентам с низкой приверженностью к терапии можно рекомендовать Омез® 40 мг 1 раз в сутки за 30 минут до завтрака [40]. Эта доза является оптимальной и для быстрых метаболизаторов. Еще одним несомненным достоинством препарата является его доступная цена при высоком качестве субстанции и уникальной лекарственной форме, что дает возможность в сложившихся социально-экономических условиях поддерживать на высоком уровне качество жизни большого числа больных кислотозависимыми заболеваниями.
КОНФЛИКТ ИНТЕРЕСОВ. Авторы статьи подтвердили отсутствие конфликта интересов, о котором необходимо сообщить.
CONFLICT OF INTERESTS. Not declared.
Литература/References
- Аруин Л. И., Григорьев П. Я., Исаков В. А., Яковенко Э. П. Хронический гастрит. Амстердам, 1993. [Aruin L.I., Grigor’yev P.Ya., Isakov V.A., Yakovenko E.P. Khronicheskiy gastrit. [Chronic gastritis.] Amsterdam; 1993.]
- Циммерман Я. С. Хронический гастрит и язвенная болезнь. Пермь, 2000. 3. Чернин В. В. Хронический гастрит. Тверь, 2006. [Tsimmerman Ya.S. Khronicheskiy gastrit i yazvennaya bolezn’. [Chronic gastritis and peptic ulcer disease.] Perm’; 2000.]
- Циммерман Я. С. Проблема хронического гастрита // Клин. Мед. 2008; (5): 13-21. [Tsimmerman Ya.S. Problema khronicheskogo gastrita. [The problem of chronic gastritis] Klin. med. 2008; (5): 13-21.]
- Marshall B. J., Warren J. R. Unidentified curved bacilli in the stomach of patients with gastritis and peptic ulceration // Lancet. 1984; 1 (8390): 1311-1315.
- Rugge M., Pennelli G., Pilozzi E., Fassan M., Ingravallo G., Russo V. M., Di Mario F. Gruppo Italiano Patologi Apparato Digerente (GIPAD); Società Italiana di Anatomia Patologica e Citopatologia Diagnostica/International Academy of Pathology, Italian division (SIAPEC/IAP). Gastritis: the histology report // Dig Liver Dis. 2011; 43 Suppl 4: S373-84. DOI: 10.1016/S1590-8658(11)60593-8. PMID: 21459343.
- Varbanova M., Frauenschläger K., Malfertheiner P. Chronic gastritis – an update // Best Pract Res Clin Gastroenterol. 2014; 28 (6): 1031-1042. DOI: 10.1016/j.bpg.2014.10.005. Epub 2014 Oct 30. PMID: 25439069.
- Pennelli G., Grillo F. Galuppini F., et al. Gastritis: update on etiological features and histological practical approach // Pathologica. 2020; 112: 153-165. https://doi.org/10.32074/1591-951X-163.
- Capelle L. G., de Vries A. C., Haringsma J., et al. The staging of gastritis with the OLGA system by using intestinal metaplasia as an accurate alternative for atrophic gastritis // Gastrointest Endosc. 2010; 71: 1150-1158. https://doi.org/10.1016/j.gie.2009.12.02946.
- Rugge M., Fassan M., Pizzi M., et al. Operative link for gastritis assessment vs operative link on intestinal metaplasia assessment // World J Gastroenterol. 2011; 17 (41): 4596-601. https://doi.org/10.3748/wjg.v17.i41.459647.
- Rugge M., Sugano K., Scarpignato C., et al. Gastric cancer prevention targeted on risk assessment: Gastritis OLGA staging // Helicobacter. 2019; 24: e12571. https://doi.org/10.1111/hel.1257148.
- Rugge M., Genta R. M., Fassan M., et al. OLGA Gastritis Staging for the Prediction of Gastric Cancer Risk: A Long-term Follow-up Study of 7436 Patients // Am J Gastroenterol. 2018; 113: 1621-1628. https://doi.org/10.1038/s41395-018-0353-8.
- Sigano K., Tack J., Kuipers E. J. et al. Kyoto global consensus report on Helicobacter pylori gastritis // Gut. 2015; 64: 1-15. (Epub. ahead of print).
- Kulnigg-Dabsch S. Autoimmune gastritis. Autoimmungastritis // Wien Med Wochenschr. 2016; 166 (13-14): 424-430. DOI: 10.1007/s10354-016-0515-5.
- Lenti M. V., Rugge M., Lahner E., Miceli E., Toh B. H., Genta R. M., De Block C., Hershko C., Di Sabatino A. Autoimmune gastritis // Nat Rev Dis Primers. 2020; 6 (1): 56. DOI: 10.1038/s41572-020-0187-8. PMID: 32647173.
- Mayo Tsuboi, Ryota Niikura, Yoku Hayakawa, Yoshihiro Hirata, Tetsuo Ushiku, Kazuhiko Koike1 Distinct Features of Autoimmune Gastritis in Patients with Open-Type Chronic Gastritis in Japan // Biomedicines. 2020; 8 (10): 419.
- Franklin M. M., Hanson J. A. Аутоиммунный гастрит. Сайт PathologyOutlines.com. https://www.pathologyoutlines.com/topic/stomachautoimmunegastritis.html. Проверено 19 декабря 2020 г.
- El-Zimaity H., Choi W. T., Lauwers G. Y., Riddell R. The differential diagnosis of Helicobacter pylori negative gastritis // Virchows Arch. 2018; 473 (5): 533-550. DOI i: 10.1007/s00428-018-2454-6. Epub 2018 Sep 25. PMID: 30255340.
- Lauwers G. Y., Fujita H., Nagata K. et al. Патология гастрита, не связанного с Helicobacter pylori: расширение гистопатологических горизонтов // J Gastroenterol. 2010; 45: 131–145. https://doi.org/10.1007/s00535-009-0146-3.
- Correa P. Helicobacter pylori and gastric carcinogenesis // Am. J. Surg. Pathol. 1995. Vol. 19, Suppl 1. S. 37-43.
- Correa P. The biological model of gastric carcinogenesis // IARC Sci. Publ. 2004. Vol. 157. P. 301-310.
- Helicobacter and Cancer Collaborative Group. Gastric cancer and Helicobacter pylori: a combined analysis of 12 case control studies nested with prospective cohorts // Gut. 2001. Vol. 49. P. 347-353.
- Кононов А. В. Воспаление как основа Helicobacter pylori-ассоциированных болезней // Арх. Патол. 2006; 5: 3–10. [Kononov A. V. Vospaleniye kak osnova Helicobacter pylori-assotsiirovannykh bolezney [Inflammation as the basis of Helicobacter pylori-associated diseases] // Arkh. patol. 2006. № 5. S. 3-10.]
- Диксон М. Ф., Гента Р. М., Ярдли Дж. Х., Корреа П. Классификация и классификация гастрита. Обновленная Сиднейская система. Международный семинар по гистопатологии гастрита, Хьюстон 1994 // Am J Surg Pathol. 1996; 20: 1161. [Dikson M.F., Genta R.M., Yardli Dzh. Kh., Korrea P. Klassifikatsiya gastrita. [Classification of gastritis. Updated Sydney System.] Obnovlennaya Sidneyskaya sistema. Mezhdunarodnyy seminar po gistopatologii gastrita, KH’yuston 1994. Am J Surg Pathol 1996; 20: 1161.]
- Кононов А. В. Роль патологоанатомического заключения «Хронический гастрит» в системе персонифицированной канцерпревенции // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2018; 28 (4): 91-101. https://doi.org/10.22416/1382-4376-2018-28-4-91-101. [Kononov A. V. Rol’ patologoanatomicheskogo zaklyucheniya «Khronicheskiy gastrit» v sisteme personifitsirovannoy kantserpreventsii. [The role of the pathological report «Chronic gastritis» in the system of personified cancer prevention.] // Rossiyskiy zhurnal gastroenterologii, gepatologii, koloproktologii. 2018; 28 (4): 91-101. https://doi.org/10.22416/1382-4376-2018-28-4-91-101.]
- Lenti M. V., Rugge M., Lahner E., Miceli E., Toh B. H., Genta R. M., De Block C., Hershko C., Di Sabatino A. Autoimmune gastritis // Nat Rev Dis Primers. 2020; 6 (1): 56. DOI: 10.1038/s41572-020-0187-8. PMID: 32647173.
- Mayo Tsuboi, Ryota Niikura, Yoku Hayakawa, Yoshihiro Hirata, Tetsuo Ushiku, Kazuhiko Koike1 Distinct Features of Autoimmune Gastritis in Patients with Open-Type Chronic Gastritis in Japan // Biomedicines. 2020; 8 (10): 419.
- Рекомендации по лечению предраковых состояний и изменений эпителия желудка MAPSII / Pimentel-Nunes P., Libânio D., Marcos-Pinto R., Areia M., Leja M., Esposito G. Management of epithelial precancerous condi-tions and lesions in the stomach (MAPS II):European Society of Gastrointestinal Endoscopy (ESGE), European Helicobacter and Microbiota Study Group (EHMSG), European Society of Pathology (ESP), and Sociedade Portuguesa de EndoscopiaDigestiva (SPED) guideline update 2019 // Endoscopy. 2019; 51 (4): 365-388. [PedroPimentel-Nunes, DiogoLibanio, RicardoMarcos-Pintoetal. Rekomendatsii po lecheniyu predrakovykh sostoyaniy i izmeneniy epiteliya zheludka MAPSII [Recommendations for the treatment of precancerous conditions and changes in gastric epithelium MAPSII] // Endoscopy. 2019; 51].]
- Ивашкин В. Т., Маев И. В., Лапина Т. Л., Шептулин А. А., Трухманов А. С., Баранская Е. К., Абдулхаков Р. А., Алексеева О. П., Алексеенко С. А., Дехнич Н. Н., Козлов Р. С., Кляритская И. Л., Корочанская Н. В., Курилович С. А., Осипенко М. Ф., Симаненков В. И., Ткачев А. В., Хлынов И. Б., Цуканов В. В. Клинические рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению инфекции Helicobacter pylori у взрослых // Рос журн гастроэнтерол гепатол колопроктол. 2018; 28 (1): 55-70. DOI: 10.22416/1382-4376-2018-28-1-55-70. [Ivashkin V.T., Mayev I.V., Lapina T.L., Sheptulin A.A., Trukhmanov A.S., Baranskaya Ye.K., Abdulkhakov R.A., Alekseyeva O.P., Alekseyenko S.A., Dekhnich N.N., Kozlov R.S., Klyaritskaya I.L., Korochanskaya N.V., Kurilovich S.A., Osipenko M.F., Simanenkov V.I., Tkachev A.V.,Khlynov I.B., Tsukanov V.V. Klinicheskiye rekomendatsii Rossiyskoy gastroenterologicheskoy assotsiatsii po diagnostike i lecheniyu infektsii Helicobacter pylori u vzroslykh. [Clinical guidelines of the Russian Gastroenterological Association for the diagnosis and treatment of Helicobacter pylori infection in adults.] // Ros zhurn gastroenterol gepatol koloproktol 2018; 28(1):55-70 DOI: 10.22416/1382-4376-2018-28-1-55-70.]
- Bramhall S. R., Mourad M. M. // World J Meta-Anal. 2020; 8 (1): 1-3.
- Yoshida N., Yoshikawa T., Tanaka Y., Fujita N., Kassai K., Naito Y., Kondo M. A new mechanism for anti-inflammatory actions of proton pump inhibitors – inhibitory effects on neutrophil-endothelial cell interactions // Aliment. Pharmacol. Ther. 2000; 14, Suppl 1, 74-81.
- Suzuki M., Mori M., Fukumura D., Suzuki H., Miura S., Ishii H. Omeprazole attenuates neutrophil-endothelial cell adhesive interaction induced by extract of Helicobacter pylori // J. Gastroenterol. Hepatol. 1999; 14: 27-31.
- Wandall J. H. Effects of omeprazole on neutrophil chemotaxis, super oxide production, degranulation, and translocation of cytochrome b-245 // Gut. 1992; 33: 617-621.
- Suzuki M., Nakamura M., Mori M., Miura S., Tsuchiya M., Ishii H. Lansoprazole inhibites oxygen-derived free radical production from neutrophils activated by Helicobacter pylori // J. Clin. Gastroenterol. 1995; 20: S93-S96.
- Suzuki M., Mori M., Miura S., Suematsu M., Fukumura D., Kimura H., Ishii H. Omeprazole attenuates oxygen-derived free radical production from human neutrophils // Free Radical Biol. Med. 1996; 21: 727-731.
- Сomcon, выписка противоязвенных препаратов пациентам с КЗЗ, Q3, 2020. [Komkon, vypiska protivoyazvennykh preparatov patsiyentam s KZZ, [Comcon, Prescription of Antiulcer Drugs for Patients with Acid Related Diseases] Q3, 2020.]
- Гриневич В. Б., Карева Е. Н., Якоб О. В. Форум экспертов. Алгоритм лечения пациентов с кислотозависимыми заболеваниями с позиции клинициста // Эффективная фармакотерапия. 2020; 24: 14-18. [Grinevich V.B., Kareva Ye.N., Yakob O.V. Forum ekspertov. Algoritm lecheniya patsiyentov s kislotozavisimymi zabolevaniyami s pozitsii klinitsista. [Expert Forum. Algorithm for the treatment of patients with acid-dependent diseases from the standpoint of a clinician.] // Effektivnaya farmakoterapiya, 24/2020, str. 14-18.]
- IQVIA, продажи ИПП по производителям в денежном выражении на период МАТ/NOV, 2020. [IQVIA, prodazhi IPP po proizvoditelyam v denezhnom vyrazhenii na period MAT/NOV, [IQVIA, sales of PPIs by manufacturers in monetary terms for the period MAT / NOV] 2020]
- Оранжевая книга FDA http://www.accessdata.fda.gov/ по состоянию на 25.12.2020. [Oranzhevaya kniga FDA [The Orange Book (FDA)] http://www.accessdata.fda.gov/ po sostoyaniyu na 25.12.2020.]
- Пасечников В. Д., Гогуев Р. К., Пасечников Д. В. Сравнение кислотосупрессивного эффекта генериков омепразола // Клинические перспективы гастроэнтерологии, гепатологии. 2010; 5. [Pasechnikov V. D., Goguyev R. K., Pasechnikov D. V. Sravneniye kislotosupressivnogo effekta generikov omeprazola. [Comparison of the acid-suppressive effect of generics of omeprazole.] // Klinicheskiye perspektivy gastroenterologii, gepatologii 5, 2010.]
- Инструкция по медицинскому применению препарата Омез 40 мг, РУ: ЛП-000328, дата регистрации 22.02.2011, дата перерегистрации 11.05.2018. [Instruktsiya po meditsinskomu primeneniyu preparata Omez 40 mg, [Instructions forthe medical use of the drug Omez 40 mg] RU: LP-000328, data registratsii 22.02.2011, datapereregistratsii 11.05.2018.]
И. В. Долгалёв*, 1, доктор медицинских наук, профессор
Е. Н. Карева**, ***, доктор медицинских наук, профессор
Е. А. Лялюкова****, доктор медицинских наук
Н. В. Павлова*****, кандидат медицинских наук
* ФГБОУ ВО Сибирский ГМУ Минздрава России, Томск, Россия
** ФГАОУ ВО РНИМУ им. Н. И. Пирогова Минздрава России, Москва, Россия
*** ФГАОУ ВО Первый МГМУ им. И. М. Сеченова Минздрава России, Москва, Россия
**** ФГБОУ ВО ОмГМУ Минздрава России, Омск, Россия
***** ФГБОУ ВО МГМСУ им. А. И. Евдокимова Минздрава России, Москва, Россия
1Контактная информация: ivdolgalev@mail.ru
DOI: 10.26295/OS.2021.76.84.006
Хронический гастрит: от гистологического протокола до обоснования этиопатогенетической терапии/ И. В. Долгалёв, Е. Н. Карева, Е. А. Лялюкова, Н. В. Павлова
Для цитирования: Долгалёв И. В., Карева Е. Н., Лялюкова Е. А., Павлова Н. В. Хронический гастрит: от гистологического протокола до обоснования этиопатогенетической терапии // Лечащий Врач. 2021; 2 (24): 30-34.
Теги: хеликобактерная инфекция, слизистая оболочка, дисплазия, факторы риска