Содержание
-
Русское название
-
Английское название
-
Латинское название
-
Химическое название
-
Брутто формула
-
Фармакологическая группа вещества Селексипаг
-
Нозологическая классификация
-
Код CAS
-
Фармакологическое действие
-
Фармакология
-
Применение вещества Селексипаг
-
Противопоказания
-
Ограничения к применению
-
Применение при беременности и кормлении грудью
-
Побочные действия вещества Селексипаг
-
Взаимодействие
-
Передозировка
-
Способ применения и дозы
-
Меры предосторожности
-
Источники информации
-
Торговые названия с действующим веществом Селексипаг
Русское название
Селексипаг
Английское название
Selexipag
Латинское название
Selexipagum (род. Selexipagi)
Химическое название
2-[4-[(5,6-дифенилпиразин-2-ил)-пропан-2-ил-амино]бутокси]-N-метилсульфонилацетамид
Брутто формула
C26H32N4O4S
Фармакологическая группа вещества Селексипаг
Нозологическая классификация
Код CAS
475086-01-2
Фармакологическое действие
—
простациклинмиметическое, вазодилатирующее, снижающее легочное сосудистое сопротивление.
Фармакология
Механизм действия
Селексипаг является селективным агонистом простациклиновых (IP) рецепторов, отличным от простациклина и его аналогов.
Селексипаг гидролизуется карбоксилэстеразами с образованием активного метаболита, активность которого примерно в 37 раз превышает активность селексипага. Селексипаг и его активный метаболит являются высокоафинными агонистами IP-рецепторов с высокой чувствительностью к IP-рецепторам по сравнению с другими рецепторами простаноидов (ЕР1–ЕР4, DP, FP и ТР). Селективность в отношении рецепторов EP1, ЕР3, FP и ТР важна, т.к. эти рецепторы отвечают за сократительную активность в ЖКТ и кровеносных сосудах. Селективность в отношении рецепторов ЕР2, ЕР4 и DP1 важна, т.к. эти рецепторы опосредуют иммуносупрессивные эффекты.
Стимулирование селексипагом и его активным метаболитом IP-рецепторов приводит к вазодилатации, а также антипролиферативному и антифибротическому эффектам.
Селексипаг предотвращает ремоделирование сердца и легких у крыс с легочной артериальной гипертензией (ЛАГ) и вызывает пропорциональное снижение легочного и периферического давления, показывая, что периферическая вазодилатация отражает фармакодинамическую эффективность в отношении легочных сосудов. Селексипаг не вызывает десенсибилизацию IP-рецепторов in vitro и тахифилаксию у крыс.
Фармакодинамика
Электрофизиология сердца
Применение повторных доз 800 и 1600 мкг селексипага 2 раза в день не влияло на сердечную реполяризацию (интервал QTc) или проведение (интервалы PR и QRS) и вызывало умеренное повышение ЧСС.
Факторы свертывания крови
Наблюдалось незначительное снижение уровня фактора Виллебранда в плазме крови; уровень фактора Виллебранда при этом оставался выше НГН.
Легочная гемодинамика
При совместном применении селексипага в индивидуально переносимой дозе с антагонистами эндотелиновых рецепторов и/или ингибиторами ФДЭ-5 у пациентов с ЛАГ (II–III функциональные классы по классификации ВОЗ) достоверно снижалось легочное сосудистое сопротивление и повышался сердечный индекс.
Фармакокинетика
Фармакокинетика селексипага и его активного метаболита после применения однократной и повторных доз была пропорциональной в диапазоне доз до 800 мкг для однократной дозы и до 1800 мкг 2 раза в день для повторных доз. После применения повторных доз равновесные состояния селексипага и активного метаболита достигаются в течение 3 дней. Кумуляция селексипага или активного метаболита в плазме крови после применения повторных доз не наблюдалась.
У здоровых добровольцев вариабельность степени воздействия (AUC) между индивидуумами в равновесном состоянии составила 43 и 39% для селексипага и активного метаболита соответственно. Индивидуальная вариабельность AUC составила 24 и 19% для селексипага и активного метаболита соответственно.
AUC селексипага и его активного метаболита в равновесном состоянии у пациентов с ЛАГ и здоровых добровольцев была сходной. Фармакокинетика селексипага и его активного метаболита у пациентов с ЛАГ не зависела от тяжести заболевания и не изменялась с течением времени.
Абсорбция
Селексипаг быстро абсорбируется и гидролизуется карбоксилэстеразами до его активного метаболита. Tmax селексипага и его активного метаболита в плазме крови после перорального применения составляет 1–3 и 3–4 ч соответственно.
Абсолютная биодоступность селексипага у человека составляет около 49%. Наиболее вероятно, это является следствием эффекта первого прохождения селексипага через печень, т.к. концентрация его активного метаболита в плазме крови схожая после перорального и в/в введения.
AUC селексипага после приема однократной дозы 400 мкг во время еды увеличивается на 10% у представителей европеоидной расы и снижается на 15% у представителей японской нации, в то время как степень воздействия активного метаболита снижается на 27% (у представителей европеоидной расы) и 12% (у представителей японской нации). Нежелательные явления наблюдаются чаще при приеме препарата натощак по сравнению с применением во время еды.
Распределение
Селексипаг и его активный метаболит в высокой степени связываются с белками плазмы крови (примерно 99% в сумме и в равной степени с альбумином и альфа1-кислым гликопротеином). Vss селексипага составляет 11,7 л.
Биотрансформация
Селексипаг гидролизуется в активный метаболит карбоксилэстеразами в печени и в кишечнике. Окислительный метаболизм, катализируемый в основном изоферментом CYP2C8 и в меньшей степени изоферментом CYP3A4, приводит к образованию гидроксилированных и деалкилированных продуктов. Изоферменты UGT1А3 и UGT2B7 вовлечены в конъюгацию активного метаболита с глюкуроновой кислотой. За исключением активного метаболита, концентрация каждого метаболита в плазме крови не превышает 3% от общего содержания производных селексипага. У здоровых добровольцев и пациентов с ЛАГ после перорального приема AUC активного метаболита в равновесном состоянии примерно в 3–4 раза выше по сравнению с неизмененным селексипагом.
Выведение
Выведение селексипага осуществляется преимущественно через метаболизм со средним конечным T1/2 0,8–2,5 ч. T1/2 активного метаболита составляет 6,2–13,5 ч. Общий клиренс селексипага составляет 17,9 л/ч. Полное выведение наблюдается через 5 дней после приема и осуществляется преимущественно через кишечник (93% от принятой дозы) по сравнению с выведением через почки (12%).
Особые группы пациентов
Не обнаружено клинически значимого влияния пола, расы, возраста или массы тела на фармакокинетику селексипага и его активного метаболита у пациентов с ЛАГ.
Нарушение функции почек. У пациентов с тяжелыми нарушениями функции почек (расчетная СКФ <30 мл/мин/1,73 м2) наблюдается увеличение AUC селексипага и его активного метаболита в 1,4–1,7 раза.
Нарушение функции печени. У пациентов с нарушением функции печени легкой (класс А по классификации Чайлд-Пью) и средней (класс В по классификации Чайлд-Пью) степени AUC селексипага в 2 и 4 раза выше соответственно по сравнению со здоровыми добровольцами. AUC активного метаболита остается практически неизменной у пациентов с нарушением функции печени легкой степени и увеличивается в 2 раза у пациентов с нарушением функции печени средней степени. Только два пациента с нарушением функции печени тяжелой степени (класс С по классификации Чайлд-Пью) принимали селексипаг. AUC селексипага и его активного метаболита у данных пациентов была схожей с таковой у пациентов с нарушением функции печени средней степени (класс В по классификации Чайлд-Пью).
На основании данных моделирования предполагается, что AUC в равновесном состоянии у пациентов с нарушением функции печени средней степени (класс В по классификации Чайлд- Пью), получающих селексипаг 1 раз в день, будет в 2 раза выше, чем у здоровых добровольцев, получающих селексипаг 2 раза в день. AUC активного метаболита в равновесном состоянии у пациентов, получающих селексипаг 1 раз в день, должна быть сходной с AUC у здоровых добровольцев, получающих селексипаг 2 раза в день. Предполагаемая AUC в равновесном состоянии у пациентов с нарушением функции печени тяжелой степени (класс С по классификации Чайлд-Пью) является схожей с отмечаемой у пациентов с нарушением функции печени средней степени, получающих селексипаг 1 раз в день.
Применение вещества Селексипаг
Длительное лечение легочной артериальной гипертензии у взрослых пациентов (ЛАГ, группа I, II–IV функциональный класс по классификации ВОЗ) для предотвращения прогрессирования заболевания. Прогрессирование заболевания может включать смерть, госпитализацию по поводу ЛАГ, начало в/в или п/к введения простаноидов или другие случаи прогрессирования заболевания (снижение дистанции в тесте 6-минутной ходьбы, ассоциированное с ухудшением симптомов ЛАГ или необходимостью в дополнительной ЛАГ-специфической терапии).
Селексипаг эффективен в сочетании с антагонистами эндотелиальных рецепторов и/или ингибиторами ФДЭ-5, или в составе тройной терапии с антагонистами эндотелиальных рецепторов и ингибиторами ФДЭ-5, или в монотерапии.
Эффективность селексипага доказана в отношении идиопатической и наследственной ЛАГ, ЛАГ, ассоциированной с заболеваниями соединительной ткани или компенсированным простым врожденным пороком сердца.
Противопоказания
Повышенная чувствительность к селексипагу; тяжелая ИБС или нестабильная стенокардия; инфаркт миокарда, перенесенный в течение предшествующих 6 мес; декомпенсированная сердечная недостаточность при отсутствии пристального наблюдения врача; тяжелые нарушения сердечного ритма; цереброваскулярные заболевания (например, преходящее нарушение мозгового кровообращения, инсульт), перенесенные в течение предшествующих 3 мес; врожденный или приобретенный порок сердца с клинически значимыми нарушениями функции миокарда, не связанными с ЛАГ; совместное применение с сильными ингибиторами CYP2C8 (например, гемфиброзил); беременность и период грудного вскармливания; детский возраст до 18 лет (эффективность и безопасность не изучены).
Ограничения к применению
Артериальная гипотензия; веноокклюзионная болезнь легких, у пациентов старше 75 лет (ограниченный опыт применения); нарушение функции печени тяжелой степени (класс С по классификации Чайлд-Пью); нарушение функции почек тяжелой степени (расчетная СКФ <30 мл/мин/1,73 м2); гипертиреоз; женщины детородного возраста.
Применение при беременности и кормлении грудью
Данные о применении селексипага во время беременности отсутствуют. В исследованиях на животных не отмечены прямые или непрямые неблагоприятные эффекты токсического действия на репродуктивную функцию. Селексипаг и его основной метаболит показали в 20–80 раз более низкий потенциал в отношении действия на рецепторы простациклина in vitro для видов животных, используемых при исследовании репродуктивной токсичности, по сравнению с человеческой популяцией. Следовательно, резерв безопасности для потенциальных эффектов, связанных с действием на рецепторы простациклина, обусловливающие влияние на репродуктивность соответственно ниже, чем для эффектов, не связанных с действием на рецепторы простациклина.
Селексипаг не рекомендуется применять во время беременности и женщинам детородного возраста, не использующим методы контрацепции.
Неизвестно, выделяется ли селексипаг или его метаболиты с грудным молоком у женщин. Поскольку доклинические исследования на крысах показали выделение селексипага или его метаболитов с грудным молоком, нельзя исключить потенциальный риск для ребенка.
Селексипаг не должен приниматься в период грудного вскармливания.
Фертильность
Данные о влиянии на фертильность человека отсутствуют. В доклинических исследованиях на крысах селексипаг в высоких дозах вызывал кратковременное нарушение менструального цикла, которое не оказывало влияния на фертильность. Значимость этого эффекта для человека неизвестна.
Побочные действия вещества Селексипаг
Обзор профиля безопасности
Наиболее часто отмечавшимися нежелательными реакциями являлись головная боль, диарея, тошнота, рвота, боль в челюсти, боль в конечностях, артралгия, приливы крови к лицу и верхней половине тела. Данные реакции наиболее часто наблюдались во время титрования дозы. Большинство данных реакций были легкой или умеренной интенсивности.
Нежелательные реакции, отмеченные в ходе применения селексипага по частоте, представлены ниже. В пределах каждой частоты нежелательные реакции перечислены в порядке уменьшения их серьезности. Частота нежелательных реакций обозначена как очень часто (≥1/10); часто (≥1/100,<1/10); нечасто (≥1/1000, <1/100).
Со стороны крови и лимфатической системы: часто — анемия, снижение уровня Hb.
Со стороны эндокринной системы: часто — гипертиреоз, снижение концентрации ТТГ в крови.
Со стороны обмена веществ и питания: часто — снижение аппетита, снижение массы тела.
Со стороны нервной системы: очень часто — головная боль.
Со стороны сердца: нечасто — синусовая тахикардия.
Сосудистые нарушения: очень часто — приливы крови к лицу и верхней половине тела; часто — артериальная гипотензия.
Со стороны дыхательной системы, органов грудной клетки и средостения: очень часто — назофарингит (неинфекционной природы); часто — заложенность носа.
Со стороны ЖКТ: очень часто — диарея, рвота, тошнота; часто — боль в животе.
Со стороны кожи и подкожных тканей: часто — кожная сыпь, крапивница, эритема.
Со стороны скелетно-мышечной системы и соединительной ткани: очень часто — боль в челюсти, миалгия, артралгия, боль в конечностях.
Общие расстройства и нарушения в месте введения: часто — боль.
Описание отдельных нежелательных реакций
Нежелательные реакции, связанные с механизмом действия селексипага, наблюдались часто, особенно во время индивидуального титрования дозы (см таблицу).
| Нежелательные реакции, связанные с аналогами простациклина | Титрование дозы, % | Поддерживающая терапия, % | ||
| Селексипаг | Плацебо | Селексипаг | Плацебо | |
| Головная боль | 64 | 28 | 40 | 20 |
| Диарея | 36 | 12 | 30 | 13 |
| Тошнота | 29 | 13 | 20 | 10 |
| Боль в челюсти | 26 | 4 | 21 | 4 |
| Миалгия | 15 | 5 | 9 | 3 |
| Боль в конечностях | 14 | 5 | 13 | 6 |
| Рвота | 14 | 4 | 8 | 6 |
| Приливы крови к лицу и верхней половине тела | 11 | 4 | 10 | 3 |
| Артралгия | 7 | 5 | 9 | 5 |
Данные нежелательные реакции обычно являлись транзиторными или купировались симптоматическим лечением. Прекратили лечение вследствие нежелательных реакций 7,5% пациентов, получавших селексипаг. Примерная частота серьезных нежелательных реакций у пациентов, получавших селексипаг, составила 2,3% по сравнению с 0,5% у пациентов, получавших плацебо. В клинической практике нежелательные реакции со стороны ЖКТ купировались противодиарейными и противорвотными ЛС, ЛС для устранения тошноты и/или лечения функциональных нарушений со стороны ЖКТ. Нежелательные реакции, связанные с болью, наиболее часто купировались анальгетиками (такими как парацетамол).
Снижение уровня Hb
В клиническом исследовании у пациентов с ЛАГ при применении селексипага среднее абсолютное изменение уровня Hb по сравнению с исходным составило от −0,34 до −0,02 г/дл, снижение уровня Hb ниже 10 г/дл наблюдалось у 8,6% пациентов.
Гипертиреоз
В клиническом исследовании у пациентов с ЛАГ при применении селексипага гипертиреоз наблюдался у 1,6% пациентов. Снижение медианы уровня ТТГ (до −0,3 МЕ/л по сравнению с медианой исходного уровня на момент включения в исследования — 2,5 МЕ/л) наблюдалось у пациентов в группе селексипага в большинстве регулярных визитов.
Повышение ЧСС
Транзиторное повышение среднего значения ЧСС на 3–4 уд./мин наблюдается через 2–4 ч после приема селексипага.
Взаимодействие
Влияние других ЛС на селексипаг
Селексипаг гидролизуется до активного метаболита карбоксилэстеразами. Селексипаг и его активный метаболит подвергаются окислительному метаболизму в основном изоферментом CYP2C8 и в меньшей степени изоферментом CYP3A4. Конъюгация активного метаболита с глюкуроновой кислотой катализируется изоферментами UGT1A3 и UGT2B7. Селексипаг и его активный метаболит являются субстратами ОАТР1В1 и ОАТР1В3. Селексипаг является слабым субстратом эффлюксного насоса Р-gp. Активный метаболит селексипага является слабым субстратом BCRP.
Варфарин не оказывает влияния на фармакокинетику селексипага и его активного метаболита.
Ингибиторы изофермента CYP2C8
Сопутствующее применение 600 мг гемфиброзила, сильного ингибитора CYP2C8, 2 раза в день увеличивает AUC селексипага примерно в 2 раза, в то время как AUC активного метаболита, оказывающего основной фармакологический эффект, увеличивается примерно в 11 раз. Совместное применение селексипага с сильными ингибиторами CYP2C8 (например, гемфиброзил) противопоказано.
Сопутствующее применение селексипага с клопидогрелом (нагрузочная доза 300 мг или поддерживающая доза 75 мг/день), умеренным ингибитором CYP2C8, не оказывает влияния на степень воздействия селексипага, однако повышает степень воздействия его активного метаболита примерно в 2,2 и 2,7 раза после приема нагрузочной и поддерживающей дозы соответственно. Частота приема селексипага должна быть сокращена до 1 раза в день в случае совместного применения с умеренными ингибиторами изофермента CYP2C8 (например, клопидогрел, деферазирокс, терифлуномид). Частота приема селексипага должна быть восстановлена до 2 раз в день в случае отмены умеренного ингибитора изофермента CYP2C8.
Индукторы изофермента CYP2C8
Сопутствующее применение 600 мг рифампицина (индуктор CYP2C8 и УДФ-ГТ) 1 раз в день не оказывает влияния на AUC селексипага, однако приводит к снижению AUC его активного метаболита в 2 раза. Может потребоваться корректировка дозы селексипага в случае совместного применения с индукторами изофермента CYP2C8 (например, рифампицин, карбамазепин, фенитоин).
Ингибиторы UGT1A3 и UGT2B7
Влияние сильных ингибиторов UGT1A3 и UGT2B7 (вальпроевая кислота, пробенецид, флуконазол) на AUC селексипага и его активного метаболита не изучалось. Так как потенциальное ФКВ исключить нельзя, следует соблюдать осторожность при совместном применении данных ЛС с селексипагом.
Ингибиторы и индукторы изофермента CYP3A4
Сопутствующее применение в сочетании с комбинацией лопинавир/ритонавир (400/100 мг) (сильный ингибитор CYP3A4) 2 раза в день увеличивает AUC селексипага примерно в 2 раза, в то время как AUC его активного метаболита не изменяется. Принимая во внимание, что фармакологическая активность активного метаболита в 37 раз выше активности селексипага, данное влияние не является клинически значимым. Не ожидается влияния индукторов CYP3A4 на фармакокинетику активного метаболита, т.к. путь метаболизма с участием CYP3A4 не является ключевым в его выведении.
ЛАГ-специфическая терапия
Применение селексипага в сочетании с антагонистами эндотелиновых рецепторов и ингибиторами ФДЭ-5 приводит к снижению AUC активного метаболита селексипага на 30%.
Ингибиторы белков-переносчиков (лопинавир/ритонавир)
Сопутствующее применение в сочетании с комбинацией лопинавир/ритонавир (400/100 мг) (сильный ингибитор ОАТР1В1, ОАТР1В3 и Р-gp) 2 раза в день увеличивает AUC селексипага примерно в 2 раза, в то время как AUC его активного метаболита не изменяется. Принимая во внимание то, что фармакологический эффект обусловлен в основном активным метаболитом селексипага, данное влияние не является клинически значимым.
Влияние селексипага на другие ЛС
Селексипаг и его активный метаболит в клинически значимых концентрациях не ингибируют и не индуцируют ферменты CYР450 и белки-транспортеры.
Антикоагулянты и ингибиторы агрегации тромбоцитов
Селексипаг является ингибитором агрегации тромбоцитов in vitro. Повышенный риск развития кровотечений при приеме селексипага не наблюдается, в т.ч. когда он принимается совместно с ангикоагулянтами или ингибиторами агрегации тромбоцитов.
Селексипаг в дозе 400 мкг 2 раза в день не изменял AUC S-варфарина (субстрат CYP2C9) и R-варфарина (субстрат CYP3A4) после применения однократной дозы 20 мг варфарина. Фармакодинамический эффект варфарина на МНО не изменялся при совместном применении с селексипагом.
Мидазолам
В равновесном состоянии после титрования дозы до 1600 мкг 2 раза в день не наблюдается клинически значимого изменения AUC мидазолама (субстрат CYP3A4 в кишечнике и печени) или его метаболита, 1-гидроксимидазолама. Совместное применение селексипага с субстратами CYP3A4 не требует коррекции дозы.
Гормональные контрацептивы
Исследований взаимодействия селексипага с гормональными контрацептивами не проводилось. Так как селексипаг не оказывает влияния на AUC субстратов CYP3A4 (мидазолам и R-варфарин) или CYP2C9 (S-варфарин), снижения эффективности гормональных контрацептивов при совместном применении с селексипагом не ожидается.
Передозировка
Сообщалось об отдельных случаях передозировки при приеме до 3200 мкг селексипага, следствием которой являлась только легкая транзиторная тошнота.
Лечение: в случае передозировки показана соответствующая поддерживающая терапия. Маловероятно, что диализ будет эффективным по причине высокой связи селексипага и его активного метаболита с белками плазмы крови.
Способ применения и дозы
Внутрь, 2 раза в сутки (утром и вечером), одновременно с приемом пищи.
Меры предосторожности
Артериальная гипотензия
Селексипаг обладает вазодилатирующими свойствами, которые могут приводить к снижению давления крови в сосудах. До его назначения следует тщательно оценить, могут ли определенные патологические состояния у пациента ухудшаться вследствие вазодилатирующих эффектов селексипага (например, получение антигипертензивной терапии, артериальная гипотензия в состоянии покоя, гиповолемия, тяжелая обструкция выходного отдела левого желудочка или вегетативная дисфункция).
Гипертиреоз
У некоторых пациентов, получающих селексипаг, может наблюдаться гипертиреоз. В случае появления признаков и симптомов гипертиреоза рекомендованы соответствующие исследования функции щитовидной железы.
Веноокклюзионная болезнь легких
Сообщалось о случаях отека легких при применении вазодилататоров (в основном производные простациклина) у пациентов с веноокклюзионной болезнью легких. Следовательно в случае появления признаков отека легких при приеме селексипага у пациентов с ЛАГ необходимо провести обследование пациента на предмет веноокклюзионной болезни легких. В случае подтверждения диагноза лечение селексипагом должно быть прекращено.
Пожилой возраст (старше 65 лет)
Опыт применения селексипага у пациентов старше 75 лет ограничен, в связи с чем селексипаг должен применяться с осторожностью у данной группы пациентов.
Нарушение функции печени
Опыт применения селексипага у пациентов с нарушением функции печени тяжелой степени (класс С по классификации Чайлд-Пью) отсутствует, в связи с чем он не показан для лечения данной группы пациентов. AUC селексипага и его активного метаболита увеличивается у пациентов с нарушением функции печени средней степени (класс В по классификации Чайлд-Пью). У пациентов с нарушением функции печени средней степени селексипаг должен применяться 1 раз в день.
Нарушение функции почек
Титрование дозы у пациентов с нарушением функции почек тяжелой степени (расчетная СКФ <30 мл/мин/1,73 м2) должно проводиться с осторожностью. Опыт применения селексипага у пациентов, находящихся на гемодиализе, отсутствует, в связи с чем он не должен применяться у данной группы пациентов.
Женщины детородного возраста
Женщины детородного возраста должны применять надежные методы контрацепции во время применения селексипага.
Влияние на способность управлять транспортными средствами и другими механизмами. Селексипаг в небольшой степени влияет на способность управлять транспортными средствами и механизмами. Клиническое состояние пациента и профиль нежелательных реакций селексипага (такие как головная боль или гипотензия) должны быть приняты во внимание при рассмотрении способности пациента управлять транспортными средствами или механизмами.
Источники информации
Обобщенные материалы www.grls.rosminzdrav.ru, 2019–2020.
Торговые названия с действующим веществом Селексипаг
Rec.INN
зарегистрированное ВОЗ
Лекарственное взаимодействие
Входит в состав препаратов:
список
Фармакологическое действие
Является селективным агонистом простациклиновых (IP) рецепторов, отличным от простациклина и его аналогов, гидролизуется карбоксилэстеразами с образованием активного метаболита, активность которого примерно в 37 раз превышает активность самого вещества. Действующее вещество и его активный метаболит являются высокоаффинными агонистами IP рецепторов с высокой чувствительностью к IP рецепторам по сравнению с другими рецепторами простаноидов (ЕР1-ЕР4, DP, FP и ТР). Селективность в отношении EP1, ЕР3, FP и ТР рецепторов важна, так как эти рецепторы отвечают за сократительную активность в желудочно-кишечном тракте и кровеносных сосудах. Селективность в отношении ЕР2, ЕР4 и DP1 рецепторов важна, так как эти рецепторы опосредуют иммуносупрессивные эффекты.
Стимулирование действующим веществом и его активным метаболитом IP рецепторов приводит к вазодилатации, а также антипролиферативному и антифибротическому эффектам. Действующее вещество предотвращает ремоделирование сердца и легких у крыс с легочной артериальной гипертензией (ЛАГ) и вызывает пропорциональное снижение легочного и периферического давления, показывая, что периферическая вазодилатация отражает фармакодинамическую эффективность в отношении легочных сосудов.
Фармакокинетика
Селексипаг быстро абсорбируется и гидролизуется карбоксилэстеразами до его активного метаболита. Cmax в плазме крови после перорального применения достигается в течение 1-3 ч и 3-4 ч. Абсолютная биодоступность составляет около 49%. Наиболее вероятно, это является следствием эффекта первого прохождения селексипага через печень, так как концентрации активного метаболита в плазме крови являются схожими после перорального и внутривенного введения.
AUC после приема однократной дозы 400 мкг во время еды увеличивается на 10% у представителей европеоидной расы и снижается на 15% у представителей японской нации, в то время как степень воздействия активного метаболита снижается на 27% (у представителей европеоидной расы) и 12% (у представителей японской нации). Нежелательные явления наблюдаются чаще при приеме препарата натощак по сравнению с применением во время еды.
Селексипаг и его активный метаболит высоко связываются с белками плазмы крови (примерно 99% в сумме и в равной степени с альбумином и альфа-1 кислым гликопротеином). Vd селексипага в равновесном состоянии составляет 11.7 л.
Гидролизуется в активный метаболит карбоксилэстеразами в печени и в кишечнике. Окислительный метаболизм, катализируемый в основном изоферментом CYP2C8 и в меньшей степени изоферментом CYP3A4, приводит к образованию гидроксилированных и деалкилированных продуктов. Изоферменты UGT1A3 и UGT2B7 вовлечены в конъюгацию активного метаболита с глюкуроновой кислотой. За исключением активного метаболита, концентрация каждого метаболита в плазме крови не превышает 3% от общего содержания производных препарата. У здоровых добровольцев и у пациентов с ЛАГ после перорального приема AUC активного метаболита в равновесном состоянии примерно в 3-4 раза выше по сравнению с неизмененным препаратом.
Выведение осуществляется преимущественно через метаболизм со средним конечным T1/2 — 0.8-2.5 ч. T1/2 активного метаболита составляет 6.2-13.5 ч. Общий клиренс селексипага составляет 17.9 л/ч. Полное выведение наблюдается через 5 дней после приема препарата и осуществляется преимущественно через кишечник (составляет 93% от принятой дозы) по сравнению с выведением через почки (12%).
Показания активного вещества
СЕЛЕКСИПАГ
Длительное лечение легочной артериальной гипертензии у взрослых пациентов.
Режим дозирования
Внутрь. Режим дозирования индивидуальный, в зависимости от показаний, возраста пациента и клинической ситуации
Побочное действие
Со стороны системы кроветворения: часто — анемия, снижение гемоглобина.
Со стороны эндокринной системы: часто — гипертиреоз, снижение концентрации тиреотропного гормона (ТТГ) в крови.
Со стороны обмена веществ: часто — снижение аппетита, снижение веса.
Со стороны ЦНС: очень часто — головная боль.
Со стороны сердечно-сосудистой системы: очень часто — приливы крови к лицу и верхней половине тела; часто — артериальная гипотензия; нечасто — синусовая тахикардия.
Со стороны дыхательной системы, органов грудной клетки и средостения: очень часто — назофарингит (неинфекционной природы), часто — заложенность носа.
Со стороны пищеварительной системы: очень часто — диарея, рвота, тошнота; часто — боль в животе.
Со стороны кожи и подкожных тканей: часто — сыпь, крапивница, эритема.
Со стороны костно-мышечной системы: очень часто — боль в челюсти, миалгия, артралгия, боль в конечностях.
Противопоказания к применению
Повышенная чувствительность, тяжелая ишемическая болезнь сердца или нестабильная стенокардия, инфаркт миокарда, перенесенный в течение предшествующих 6 месяцев, декомпенсированная сердечная недостаточность при отсутствии пристального наблюдения врача, тяжелые нарушения сердечного ритма, цереброваскулярные заболевания (например, преходящее нарушение мозгового кровообращения, инсульт), перенесенные в течение предшествующих 3 месяцев, врожденные или приобретенные пороки сердца с клинически значимыми нарушениями функции миокарда, не связанными с легочной артериальной гипертензией, совместное применение с мощными ингибиторами CYP2C8 (например, гемфиброзилом), беременность и период грудного вскармливания, детский возраст до 18 лет.
С осторожностью
У пациентов с артериальной гипотензией, у пациентов с веноокклюзионной болезнью легких, при совместном применении с умеренными ингибиторами изофермента CYP2C8 (например, клопидогрелем, деферазироксом, терифлуномидом), у пациентов старше 75 лет, у пациентов с нарушением функции печени тяжелой степени (класс С по классификации Чайлд-Пью), у пациентов с нарушением функции почек тяжелой степени (рСКФ <30 мл/мин/1.73 м2), у пациентов с гипертиреозом и у женщин детородного возраста.
Применение при беременности и кормлении грудью
Противопоказано применение при беременности и в период лактации (грудного вскармливания).
Применение при нарушениях функции печени
Препарат противопоказан для применения при нарушении функции печени тяжелой степени (класс С по классификации Чайлд-Пью).
Применение при нарушениях функции почек
Препарат противопоказан для применения при нарушении функции тяжелой степени (рСКФ <30 мл/мин/1.73 м2).
Применение у детей
Препарат противопоказан для применения у детей и подростков в возрасте до 18 лет
Применение у пожилых пациентов
Препарат противопоказан для применения у пожилых пациентов старше 75 лет
Особые указания
Лекарственное средство обладает вазодилатирующими свойствами, которые могут приводить к снижению давления крови в сосудах. До назначения следует тщательно оценить, могут ли определенные патологические состояния у пациента ухудшаться вследствие вазодилатирующих эффектов селексипага (например, у пациентов, получающих антигипертензивную терапию, пациентов с артериальной гипотензией в состоянии покоя, гиповолемией, тяжелой обструкцией выходного отдела левого желудочка или вегетативной дисфункцией).
У некоторых пациентов может наблюдаться гипертиреоз. В случае появления признаков и симптомов гипертиреоза рекомендованы соответствующие исследования функции щитовидной железы.
Сообщалось о случаях отека легких при применении вазодилататоров (в основном производных простациклина) у пациентов с веноокклюзионной болезнью легких. Следовательно, в случае появления признаков отека легких у пациентов с ЛАГ, пациент должен быть обследован на предмет веноокклюзионной болезни легких. В случае подтверждения диагноза, лечение должно быть прекращено.
Совместное применение с умеренными ингибиторами изофермента CYP2C8 (клопидогрелем, деферазироксом, терифлуномидом) может приводить к увеличению AUC селексипага и его активного метаболита. Следует рассмотреть вопрос о коррекции дозы в случае совместного назначения умеренного ингибитора изофермента CYP2C8 или его отмены.
Опыт применения у пациентов старше 75 лет ограничен, в связи с чем должен назначаться с осторожностью у данной группы пациентов.
Опыт применения селексипага у пациентов с нарушением функции печени тяжелой степени (класс С по классификации Чайлд-Пью) отсутствует, в связи с чем препарат не показан для лечения данной группы пациентов. AUC действующего вещества и его активного метаболита увеличивается у пациентов с нарушением функции печени средней степени (класс В по классификации Чайлд-Пью). У пациентов с нарушением функции печени средней степени должен применяться один раз в день.
Титрование дозы у пациентов с нарушением функции почек тяжелой степени (рСКФ <30 мл/мин/1.73 м2) должно проводиться с осторожностью. Опыт применения у пациентов, находящихся на гемодиализе, отсутствует, в связи с чем селексипаг не рекомендуется применять у данной группы пациентов.
Влияние на способность к управлению транспортными средствами и механизмами
В период лечения пациентам следует избегать вождения автотранспорта и другой деятельности, требующей высокой концентрации внимания и скорости психомоторных реакций.
Лекарственное взаимодействие
Ингибиторы изофермента CYP2C8
Сопутствующее применение гемфиброзила, мощного ингибитора изофермента CYP2C8, два раза в день увеличивает AUC селексипага примерно в два раза, в то время как AUC активного метаболита, оказывающего основной фармакологический эффект, увеличивается примерно в 11 раз. Совместное применение с мощными ингибиторами изофермента CYP2C8 (гемфиброзилом) противопоказано.
Индукторы изофермента CYP2C8
Сопутствующее применение рифампицина, индуктора изофермента CYP2C8 (и ферментов группы УДФ-глюкуронозилтрансферазы (UGT)), один раз в день не оказывает влияния на AUC, однако приводит к снижению AUC его активного метаболита в 2 раза. Может потребоваться корректировка дозы в случае совместного применения с индукторами изофермента CYP2C8 (рифампицином, карбамазепином, фенитоином).
ЛАГ-специфическая терапия
В комбинации с антагонистами рецепторов эндотелина и ингибиторами ФДЭ5 приводит к снижению AUC активного метаболита селексипага на 30%.
Апбрави — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-005577
Торговое наименование:
Апбрави
Международное непатентованное наименование:
селексипаг
Лекарственная форма:
таблетки, покрытые плёночной оболочкой
Состав
1 таблетка 200 мкг содержит:
Ядро:
Действующее вещество: селексипаг 0,2 мг.
Вспомогательные вещества: маннитол, крахмал кукурузный, гипролоза низкозамещенная, гипролоза, магния стеарат.
Плёночная оболочка: гипромеллоза, пропиленгликоль, титана диоксид, краситель железа оксид жёлтый, воск карнаубский.
1 таблетка 800 мкг содержит:
Ядро:
Действующее вещество: селексипаг 0,8 мг.
Вспомогательные вещества: маннитол, крахмал кукурузный, гипролоза низкозамещенная, гипролоза, магния стеарат.
Плёночная оболочка: гипромеллоза, пропиленгликоль, титана диоксид, краситель железа оксид жёлтый, краситель железа оксид чёрный, воск карнаубский.
Описание
Таблетки 200 мкг: круглые двояковыпуклые таблетки, покрытые плёночной оболочкой, светло-жёлтого цвета, с тиснением “2” на одной стороне, с фаской с двух сторон, без риски.
Таблетки 800 мкг: круглые двояковыпуклые таблетки, покрытые плёночной оболочкой, тёмного серо-зелёного цвета, с тиснением “8” на одной стороне, с фаской с двух сторон, без риски.
Фармакотерапевтическая группа:
Антиагрегантное средство
Код ATX:
В01АС27
Фармакологические свойства
Механизм действия
Селексипаг является селективным агонистом простациклиновых (IP) рецепторов, отличным от простациклина и его аналогов. Селексипаг гидролизуется карбоксилэстеразами с образованием активного метаболита, активность которого примерно в 37 раз превышает активность селексипага. Селексипаг и его активный метаболит являются высокоафинными агонистами IP рецепторов с высокой чувствительностью к IP рецепторам по сравнению с другими рецепторами простаноидов (ЕР1-ЕР4, DP, FP и ТР). Селективность в отношении EP1, ЕР3, FP и ТР рецепторов важна, так как эти рецепторы отвечают за сократительную активность в желудочно-кишечном тракте и кровеносных сосудах. Селективность в отношении ЕР2, ЕР4 и DP1 рецепторов важна, так как эти рецепторы опосредуют иммуносупрессивные эффекты.
Стимулирование селексипагом и его активным метаболитом IP рецепторов приводит к вазодилятации, а также антипролиферативному и антифибротическому эффектам. Селексипаг предотвращает ремоделирование сердца и лёгких у крыс с лёгочной артериальной гипертензией (ЛАГ) и вызывает пропорциональное снижение лёгочного и периферического давления, показывая, что периферическая вазодилятация отражает фармакодинамическую эффективность в отношении лёгочных сосудов. Селексипаг не вызывает десенсибилизацию IP рецепторов in vitro и тахифилаксию у крыс.
Фармакодинамика
Электрофизиология сердца
Применение повторных доз 800 мкг и 1600 мкг селексипага дважды в день не влияло на сердечную реполяризацию (интервал QTc) или проведение (интервалы PR и QRS) и вызывало умеренное повышение частоты сердечных сокращений (ЧСС).
Факторы свёртывания крови
Наблюдалось незначительное снижение уровня фактора Виллебранда в плазме крови; уровень фактора Виллебранда при этом оставался выше нижней границы нормы.
Лёгочная гемодинамика
При совместном применении селексипага в индивидуально переносимой дозе с антагонистами эндотелиальных рецепторов (АРЭ) и/или ингибиторами фосфодиэстеразы 5-го типа (иФДЭ-5) у пациентов с ЛАГ (II-III функциональных классов (ФК) по классификации Всемирной организации здравоохранения (ВОЗ)) достоверно снижалось лёгочное сосудистое сопротивление и повышался сердечный индекс.
Фармакокинетика
Фармакокинетика селексипага и его активного метаболита, после применения однократной и повторных доз, была пропорциональной в диапазоне доз до 800 мкг для однократной дозы и до 1800 мкг два раза в день для повторных доз. После применения повторных доз равновесные состояния селексипага и активного метаболита достигаются в течение 3 дней. Кумуляция селексипага или активного метаболита в плазме крови после применения повторных доз не наблюдалась.
У здоровых добровольцев вариабельность степени воздействия (площадь под кривой «концентрация-время», AUC) между индивидуумами в равновесном состоянии составила 43% и 39% для селексипага и активного метаболита, соответственно. Индивидуальная вариабельность AUC составила 24% и 19% для селексипага и активного метаболита, соответственно.
AUC селексипага и его активного метаболита в равновесном состоянии у пациентов с ЛАГ и здоровых добровольцев была сходной. Фармакокинетика селексипага и его активного метаболита у пациентов с ЛАГ не зависела от тяжести заболевания и не изменялась с течением времени.
Абсорбция
Селексипаг быстро абсорбируется и гидролизуется карбоксилэстеразами до его активного метаболита. Максимальная концентрация селексипага и его активного метаболита в плазме крови после перорального применения достигается в течение 1-3 ч и 3-4 ч, соответственно. Абсолютная биодоступность селексипага у человека составляет около 49%. Наиболее вероятно, это является следствием эффекта первого прохождения селексипага через печень, так как концентрации активного метаболита в плазме крови являются схожими после перорального и внутривенного введения.
AUC селексипага после приёма однократной дозы 400 мкг во время еды увеличивается на 10% у представителей европеоидной расы и снижается на 15% у представителей японской нации, в то время как степень воздействия активного метаболита снижается на 27% (у представителей европеоидной расы) и 12% (у представителей японской нации). Нежелательные явления наблюдаются чаще при приёме препарата натощак по сравнению с применением во время еды.
Распределение
Селексипаг и его активный метаболит высоко связываются с белками плазмы крови (примерно 99% в сумме и в равной степени с альбумином и альфа-1 кислым гликопротеином). Объём распределения селексипага в равновесном состоянии составляет 11,7 л.
Биотрансформация
Селексипаг гидролизуется в активный метаболит карбоксилэстеразами в печени и в кишечнике. Окислительный метаболизм, катализируемый в основном изоферментом CYP2C8 и в меньшей степени изоферментом CYP3A4, приводит к образованию гидроксилированных и деалкилированных продуктов. Изоферменты UGT1A3 и UGT2B7 вовлечены в конъюгацию активного метаболита с глюкуроновой кислотой. За исключением активного метаболита, концентрация каждого метаболита в плазме крови не превышает 3% от общего содержания производных препарата. У здоровых добровольцев и у пациентов с ЛАГ после перорального приёма AUC активного метаболита в равновесном состоянии примерно в 3-4 раза выше по сравнению с неизмененным препаратом.
Выведение
Выведение селексипага осуществляется преимущественно через метаболизм со средним конечным периодом полувыведения 0,8-2,5 ч. Период полувыведения активного метаболита составляет 6,2-13,5 ч. Общий клиренс селексипага составляет 17,9 л/ч. Полное выведение наблюдается через 5 дней после приёма препарата и осуществляется преимущественно через кишечник (составляет 93% от принятой дозы) по сравнению с выведением через почки (12%).
Особые популяции пациентов
Не обнаружено клинически значимого влияния пола, расы, возраста или веса на фармакокинетику селексипага и его активного метаболита у пациентов с ЛАГ.
Пациенты с нарушением функции почек
У пациентов с тяжёлыми нарушениями функции почек (расчётная скорость клубочковой фильтрации (рСКФ) <30 мл/мин/1,73 м²) наблюдается увеличение AUC селексипага и его активного метаболита в 1,4-1,7 раза.
Пациенты с нарушением функции печени
У пациентов с нарушением функции печени лёгкой (класс А по классификации Чайлд-Пью) и средней (класс В по классификации Чайлд-Пью) степени AUC селексипага в 2 и 4 раза выше, соответственно, по сравнению со здоровыми добровольцами. AUC активного метаболита остаётся практически неизменной у пациентов с нарушением функции печени лёгкой степени и увеличивается в два раза у пациентов с нарушением функции печени средней степени. Только два пациента с нарушением функции печени тяжёлой степени (класс С по классификации Чайлд-Пью) принимали селексипаг. AUC селексипага и его активного метаболита у данных пациентов была схожей со степенью воздействия у пациентов с нарушением функции печени средней степени (класс В по классификации Чайлд-Пью).
На основании данных моделирования исследования предполагается, что AUC в равновесном состоянии у пациентов с нарушением функции печени средней степени (класс В по классификации Чайлд-Пью), принимающих препарат один раз в день, будет в два раза выше, чем у здоровых добровольцев, принимающих препарат два раза в день. AUC активного метаболита в равновесном состоянии у этих пациентов, принимающих препарат один раз в день, должна быть сходной с AUC у здоровых добровольцев, принимающих препарат два раза в день. Предполагаемая AUC в равновесном состоянии у пациентов с нарушением функции печени тяжёлой степени (класс С по классификации Чайлд-Пью) является схожей с пациентами с нарушением функции печени средней степени, принимающими препарат один раз в день.
Показания к применению
Препарат Апбрави показан для длительного лечения лёгочной артериальной гипертензии у взрослых пациентов (ЛАГ, группа I по классификации ВОЗ) II-IV ФК по классификации ВОЗ, с целью предотвращения прогрессирования заболевания. Прогрессирование заболевания может включать: смерть, госпитализацию по поводу ЛАГ, начало внутривенного или подкожного введения простаноидов, или другие случаи прогрессирования заболевания (снижение дистанции в тесте 6-минутной ходьбы, ассоциированное с ухудшением симптомов ЛАГ или необходимостью в дополнительной ЛАГ-специфической терапии).
Апбрави эффективен в комбинации с АРЭ и/или иФДЭ-5, или в составе тройной терапии с АРЭ и иФДЭ-5, или в монотерапии.
Эффективность Апбрави доказана в отношении идиопатической и наследственной ЛАГ, ЛАГ, ассоциированной с заболеваниями соединительной ткани, ЛАГ, ассоциированной с компенсированным простым врождённым пороком сердца.
Противопоказания
- Повышенная чувствительность к действующему и вспомогательным веществам
- Тяжёлая ишемическая болезнь сердца или нестабильная стенокардия
- Инфаркт миокарда, перенесённый в течение предшествующих 6 месяцев
- Декомпенсированная сердечная недостаточность при отсутствии пристального наблюдения врача
- Тяжёлые нарушения сердечного ритма
- Цереброваскулярные заболевания (например, преходящее нарушение мозгового кровообращения, инсульт), перенесённые в течение предшествующих 3 месяцев
- Врождённые или приобретённые пороки сердца с клинически значимыми нарушениями функции миокарда, не связанными с ЛАГ
- Совместное применение с мощными ингибиторами CYP2C8 (например, гемфиброзилом)
- Беременность и период грудного вскармливания
- Детский возраст до 18 лет (эффективность и безопасность не изучены)
С осторожностью
У пациентов с артериальной гипотензией, у пациентов с веноокклюзионной болезнью лёгких, при совместном применении с умеренными ингибиторами изофермента CYP2C8 (например, клопидогрелем, деферазироксом, терифлуномидом), у пациентов старше 75 лет (ограниченный опыт применения), у пациентов с нарушением функции печени тяжёлой степени (класс С по классификации Чайлд-Пью), у пациентов с нарушением функции почек тяжёлой степени (рСКФ <30 мл/мин/1,73 м²), у пациентов с гипертиреозом и у женщин детородного возраста.
Применение при беременности и в период грудного вскармливания
Беременность
Данные о применении препарата Апбрави во время беременности отсутствуют. В исследованиях на животных не отмечены прямые или непрямые неблагоприятные эффекты токсического действия на репродуктивную функцию. Селексипаг и его основной метаболит показали в 20-80 раз более низкий потенциал в отношении рецепторов простациклина in vitro для видов животных, используемых при исследовании репродуктивной токсичности, по сравнению с человеческой популяцией. Следовательно, резерв безопасности для потенциальных эффектов, связанных с рецептором простациклина, по влиянию на репродуктивность соответственно ниже, чем для эффектов, не связанных с рецептором простациклина.
Апбрави не рекомендуется применять женщинам во время беременности и женщинам детородного возраста, не использующим методы контрацепции.
Период грудного вскармливания
Неизвестно, выделяется ли селексипаг или его метаболиты с грудным молоком у женщин. Поскольку доклинические исследования на крысах показали выделение селексипага или его метаболитов с грудным молоком, нельзя исключить потенциальный риск для ребёнка.
Апбрави не должен приниматься в период грудного вскармливания.
Фертильность
Данные о влиянии на фертильность человека отсутствуют.
В доклинических исследованиях на крысах селексипаг в высоких дозах вызывал кратковременное нарушение менструального цикла, которое не оказывало влияния на фертильность. Значимость этого эффекта для человека неизвестна.
Способ применения и дозы
Апбрави применяют внутрь два раза в сутки (утром и вечером), запивая необходимым количеством воды. Для улучшения переносимости рекомендовано принимать Апбрави одновременно с приёмом пищи, а также, в начале каждой фазы титрования дозы, принимать первую повышенную дозу вечером. Не следует делить, крошить или разжёвывать таблетки. Слабовидящие пациенты должны быть проинструктированы о необходимости обратиться за помощью к другому человеку на время титрования дозы Апбрави.
Титрование дозы
Для каждого пациента с помощью титрования дозы должна быть подобрана индивидуальная максимальная переносимая доза, в диапазоне от 200 мкг два раза в день до 1600 мкг два раза в день (индивидуальная поддерживающая доза).
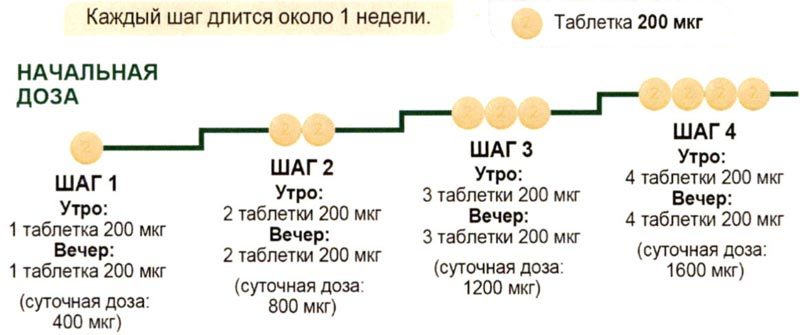
Рекомендуемая начальная доза – 200 мкг два раза в день с интервалом примерно 12 ч между приёмами. Дозу увеличивают с шагом 200 мкг два раза в день, обычно с периодичностью 1 раз в неделю. В начале терапии и в начале каждого этапа повышения дозы рекомендуется принимать первую дозу вечером.
Во время титрования дозы могут возникать некоторые нежелательные реакции, связанные с механизмом действия Апбрави (такие как, головная боль, диарея, тошнота и рвота, боль в челюсти, миалгия, боль в конечностях, артралгия, приливы крови к лицу и верхней половине тела). Данные нежелательные реакции обычно являются преходящими или купируются симптоматическим лечением. Однако, если пациенту назначена доза, которую он не может переносить, она должна быть снижена до предыдущего уровня.
У пациентов, у которых титрование дозы невозможно по причинам, отличным от возникновения нежелательных реакций, обусловленных механизмом действия Апбрави, может быть предпринята вторая попытка титрования дозы до достижения индивидуальной максимальной переносимой дозы, не превышающей 1600 мкг два раза в день.
Индивидуальная поддерживающая доза
Максимальная переносимая доза, достигнутая в процессе титрования, должна приниматься на регулярной основе. Если переносимость терапии с применением данной дозы с течением времени ухудшается, может быть назначено симптоматическое лечение и/или снижение дозы до предыдущего уровня.
Прерывание применения или отмена препарата
В случае пропуска одной дозы, она должна быть принята как можно ранее. Вместе с тем, не следует принимать пропущенную дозу менее чем за 6 ч до приёма следующей дозы. Если лечение было приостановлено на 3 дня и более, приём Апбрави должен быть возобновлен с применением более низкой дозы с последующим титрованием.
Опыт резкой отмены Апбрави у пациентов с ЛАГ ограничен. Не наблюдалось случаев резкого возобновления симптомов. Однако, если было принято решение об отмене Апбрави, отмена должна осуществляться постепенно с последующим назначением альтернативной терапии.
Пожилые пациенты (старше 65 лет)
Коррекция режима дозирования препарата у пожилых пациентов не требуется (см. раздел «Фармакокинетика»). Опыт применения Апбрави у пожилых пациентов старше 75 лет ограничен, в связи с чем препарат должен применяться с осторожностью у данной группы пациентов.
Нарушение функции печени
Апбрави не должен назначаться пациентам с нарушением функции печени тяжёлой степени (класс С по классификации Чайлд-Пью). У пациентов с нарушением функции печени средней степени (класс В по классификации Чайлд-Пью) начальная доза должна составлять 200 мкг один раз в день с шагом повышения дозы 200 мкг 1 раз в день с интервалом около 1 недели до возникновения нежелательных реакций, связанных с механизмом действия селексипага, которые не могут переноситься или купироваться соответствующим лечением. Коррекция режима дозирования препарата у пациентов с нарушением функции печени лёгкой степени (класс А по классификации Чайлд-Пью) не требуется.
Нарушение функции почек
Коррекция режима дозирования препарата у пациентов с нарушением функции почек лёгкой или средней степени не требуется. Не требуется коррекция начальной дозы у пациентов с нарушением функции почек тяжёлой степени (рСКФ <30 мл/мин/1,73 м²); титрование дозы должно выполняться с осторожностью у данной группы пациентов.
Дети (до 18 лет)
Эффективность и безопасность применения Апбрави у детей до 18 лет не установлена.
Побочное действие
Обзор профиля безопасности
Наиболее часто отмечавшимися нежелательными реакциями являются головная боль, диарея, тошнота, рвота, боль в челюсти, боль в конечностях, артралгия, приливы крови к лицу и верхней половине тела. Данные реакции наиболее часто наблюдаются во время титрования дозы. Большинство данных реакций лёгкой или умеренной интенсивности.
Список нежелательных реакций
Нежелательные реакции, отмеченные в ходе применения селексипага, представлены в таблице ниже. В пределах каждой частоты нежелательные реакции перечислены в порядке уменьшения их серьёзности.
| Системы органов |
Очень часто (≥1/10) |
Часто (≥1/100 до <1/10) |
Нечасто (≥1/1000 до <1/100) |
| Нарушения со стороны крови и лимфатической системы | Анемия Снижение гемоглобина |
||
| Нарушения со стороны эндокринной системы | Гипертиреоз Снижение концентрации тиреотропного гормона (ТТГ) в крови |
||
| Нарушения со стороны обмена веществ и питания | Снижение аппетита Снижение веса |
||
| Нарушения со стороны нервной системы | Головная боль* | ||
| Нарушения со стороны сердца | Синусовая тахикардия | ||
| Сосудистые нарушения | Приливы крови к лицу и верхней половине тела | Артериальная гипотензия | |
| Нарушения со стороны дыхательной системы, органов грудной клетки и средостения | Назофарингит (неинфекционной природы) | Заложенность носа | |
| Нарушения со стороны желудочно-кишечного тракта | Диарея* Рвота* Тошнота* |
Боль в животе | |
| Нарушения со стороны кожи и подкожных тканей | Кожная сыпь Крапивница Эритема |
||
| Нарушения со стороны скелетно-мышечной и соединительной ткани | Боль в челюсти* Миалгия* Артралгия* Боль в конечностях* |
||
| Общие расстройства и нарушения в месте введения | Боль |
*смотрите подраздел Описание отдельных нежелательных реакций
Описание отдельных нежелательных реакций
Фармакологические эффекты, связанные с режимом титрования дозы и режимом поддерживающей терапии
Нежелательные реакции, связанные с механизмом действия селексипага наблюдались часто, особенно во время индивидуального титрования дозы:
| Нежелательные реакции, связанные с аналогами простациклина |
Титрование дозы | Поддерживающая терапия | ||
| Селексипаг | Плацебо | Селексипаг | Плацебо | |
| Головная боль | 64% | 28% | 40% | 20% |
| Диарея | 36% | 12% | 30% | 13% |
| Тошнота | 29% | 13% | 20% | 10% |
| Боль в челюсти | 26% | 4% | 21% | 4% |
| Миалгия | 15% | 5% | 9% | 3% |
| Боль в конечностях | 14% | 5% | 13% | 6% |
| Рвота | 14% | 4% | 8% | 6% |
| Приливы крови к лицу и верхней половине тела | 11% | 4% | 10% | 3% |
| Артралгия | 7% | 5% | 9% | 5% |
Данные нежелательные реакции обычно являются транзиторными или купируются симптоматическим лечением. 7,5% пациентов в группе селексипага прекратили лечение вследствие нежелательных реакций. Примерная частота серьёзных нежелательных реакций в группе селексипага составила 2,3% и 0,5% в группе плацебо. В клинической практике нежелательные реакции со стороны желудочно-кишечного тракта купировались противодиарейными и противорвотными препаратами, препаратами для устранения тошноты и/или препаратами для лечения функциональных нарушений со стороны желудочно-кишечного тракта. Нежелательные реакции, связанные с болью, наиболее часто купировались анальгетиками (такими как парацетамол).
Снижение гемоглобина
В клиническом исследовании у пациентов с ЛАГ при применении селексипага среднее абсолютное изменение уровня гемоглобина по сравнению с исходным уровнем составило от -0,34 до -0,02 г/дл, снижение уровня гемоглобина ниже 10 г/дл наблюдалось у 8,6% пациентов.
Гипертиреоз
В клиническом исследовании у пациентов с ЛАГ при применении селексипага гипертиреоз наблюдался у 1,6% пациентов. Снижение медианы (до -0,3 МЕ/л по сравнению с медианой исходного уровня на момент включения в исследования 2,5 МЕ/л) ТТГ наблюдалось у пациентов в группе селексипага в большинстве регулярных визитов.
Повышение ЧСС
Транзиторное повышение среднего значения ЧСС на 3-4 уд/мин наблюдается через 2-4 ч после приёма дозы препарата.
Передозировка
Сообщалось об отдельных случаях передозировки при приёме доз до 3200 мкг, следствием которой являлась только лёгкая транзиторная тошнота. В случае передозировки, показана соответствующая поддерживающая терапия. Маловероятно, что диализ будет эффективным по причине высокой связи селексипага и его активного метаболита с белками плазмы крови.
Взаимодействие с другими лекарственными средствами
Влияние других лекарственных средств на селексипаг
Селексипаг гидролизуется до его активного метаболита карбоксилэстеразами. Селексипаг и его активный метаболит подвергаются окислительному метаболизму в основном изоферментом CYP2C8 и в меньшей степени изоферментом CYP3A4. Конъюгация активного метаболита с глюкуроновой кислотой катализируется изоферментами UGT1A3 и UGT2B7. Селексипаг и его активный метаболит являются субстратами изоферментов ОАТР1В1 и ОАТР1ВЗ. Селексипаг является слабым субстратом эффлюксного насоса Р-гликопротеина. Активный метаболит селексипага является слабым субстратом белка резистентности рака молочной железы.
Варфарин не оказывает влияния на фармакокинетику селексипага и его активного метаболита.
Ингибиторы изофермента CYP2C8
Сопутствующее применение 600 мг гемфиброзила, мощного ингибитора изофермента CYP2C8, два раза в день увеличивает AUC селексипага примерно в два раза, в то время как AUC активного метаболита, оказывающего основной фармакологический эффект, увеличивается примерно в 11 раз. Совместное применение Апбрави с мощными ингибиторами изофермента CYP2C8 (например, гемфиброзилом) противопоказано. Влияние умеренных ингибиторов изофермента CYP2C8 (например, клопидогрела, деферазирокса, терифлуномида) на степень воздействия селексипага и его активного метаболита не изучалось. Так как потенциальное фармакокинетическое взаимодействие исключить нельзя, следует рассмотреть вопрос о коррекции дозы Апбрави в случае совместного назначения с умеренным ингибитором изофермента CYP2C8 или его отмены.
Индукторы изофермента CYP2C8
Сопутствующее применение 600 мкг рифампицина, индуктора изофермента CYP2C8 (и ферментов группы УДФ-глюкуронозилтрансферазы (UGT)), один раз в день не оказывает влияния на AUC селексипага, однако приводит к снижению AUC его активного метаболита в 2 раза. Может потребоваться корректировка дозы селексипага в случае совместного применения с индукторами изофермента CYP2C8 (например, рифампицином, карбамазепином, фенитоином).
Ингибиторы изоферментов UGT1A3 и UGT2B7
Влияние мощных ингибиторов изоферментов UGT1A3 и UGT2B7 (вальпроевой кислоты, пробенецида, флуконазола) на AUC селексипага и его активного метаболита не изучалось. Так как потенциальное фармакокинетическое взаимодействие исключить нельзя, следует соблюдать осторожность при совместном применении данных лекарственных препаратов с Апбрави.
Ингибиторы и индукторы изофермента CYP3A4
Сопутствующее применение 400/100 мг лопинавира/ритонавира, мощного ингибитора CYP3A4, два раза в день увеличивает AUC селексипага примерно в два раза, в то время как AUC его активного метаболита не изменяется. Принимая во внимание то, что фармакологическая активность активного метаболита в 37 раз выше активности селексипага, данное влияние не является клинически значимым. Вследствие того, что мощный ингибитор изофермента CYP3A4 не оказывает влияния на фармакокинетику активного метаболита, показывая, что путь метаболизма с участием изофермента CYP3A4 не является ключевым в выведении активного метаболита, не ожидается влияния индукторов изофермента CYP3A4 на фармакокинетику активного метаболита.
ЛАГ-специфическая терапия
Применение селексипага в комбинации с АРЭ и иФДЭ-5 приводит к снижению AUC активного метаболита селексипага на 30%.
Ингибиторы белков-переносчиков (лопинавир/ритонавир)
Сопутствующее применение 400/100 мг лопинавира/ритонавира, мощного ингибитора транспортного полипептида органических анионов (ОАТР) (ОАТР1В1 и ОАТР1В3) и Р-гликопротеина, два раза в день увеличивает AUC селексипага примерно в два раза, в то время как AUC его активного метаболита не изменяется. Принимая во внимание то, что фармакологический эффект обусловлен в основном активным метаболитом селексипага, данное влияние не является клинически значимым.
Влияние селексипага на другие лекарственные средства
Селексипаг и его активный метаболит в клинически значимых концентрациях не ингибируют и не индуцируют ферменты цитохрома Р450 и белки-транспортёры.
Антикоагулянты и ингибиторы агрегации тромбоцитов
Селексипаг является ингибитором агрегации тромбоцитов in vitro. Повышенный риск кровотечений при приёме селексипага не наблюдается, в том числе, когда препарат принимается совместно с антикоагулянтами или ингибиторами агрегации тромбоцитов. Селексипаг в дозе 400 мкг два раза в день не изменяет AUC S-варфарина (субстрат изофермента CYP2C9) и R-варфарина (субстрат изофермента CYP3A4) после приёма однократной дозы 20 мг варфарина. Фармакодинамический эффект варфарина на международное нормализованное отношение (МНО) не изменялся при совместном применении с селексипагом.
Мидазолам
В равновесном состоянии после титрования дозы до 1600 мкг дважды в день, не наблюдается клинически значимого изменения AUC мидозалама, субстрата изофермента CYP3A4 в кишечнике и печени, или его метаболита, 1-гидроксимидазолама. Совместное применение селексипага с субстратами изофермента CYP3A4 не требует коррекции дозы.
Гормональные контрацептивы
Исследований лекарственного взаимодействия с гормональными контрацептивами не проводилось. Так как селексипаг не оказывает влияния на AUC субстратов изофермента CYP3A4 (мидазолама и R-варфарина) или субстрата изофермента CYP2C9 (S-варфарина), снижения эффективности гормональных контрацептивов при совместном применении с селексипагом не ожидается.
Особые указания
Артериальная гипотензия
Апбрави обладает вазодилатирующими свойствами, которые могут приводить к снижению давления крови в сосудах. До назначения Апбрави следует тщательно оценить, могут ли определённые патологические состояния у пациента ухудшаться вследствие вазодилатирующих эффектов селексипага (например, у пациентов, получающих антигипертензивную терапию, пациентов с артериальной гипотензией в состоянии покоя, гиповолемией, тяжёлой обструкцией выходного отдела левого желудочка или вегетативной дисфункцией).
Гипертиреоз
У некоторых пациентов, получающих Апбрави, может наблюдаться гипертиреоз. В случае появления признаков и симптомов гипертиреоза рекомендованы соответствующие исследования функции щитовидной железы.
Веноокклюзионная болезнь лёгких
Сообщалось о случаях отёка лёгких при применении вазодилятаторов (в основном производных простациклина) у пациентов с веноокклюзионной болезнью лёгких. Следовательно, в случае появления признаков отёка лёгких при приёме Апбрави у пациентов с ЛАГ, пациент должен быть обследован на предмет веноокклюзионной болезни лёгких. В случае подтверждения диагноза, лечение Апбрави должно быть прекращено.
Умеренные ингибиторы изофермента CYP2C8
Совместное применение селексипага с умеренными ингибиторами изофермента CYP2C8 (например, клопидогрелем, деферазироксом, терифлуномидом) может приводить к увеличению AUC селексипага и его активного метаболита. Следует рассмотреть вопрос о коррекции дозы селексипага в случае совместного назначения умеренного ингибитора изофермента CYP2C8 или его отмены.
Пожилые пациенты (старше 65 лет)
Опыт применения селексипага у пациентов старше 75 лет ограничен, в связи с чем Апбрави должен назначаться с осторожностью у данной группы пациентов.
Нарушение функции печени
Опыт применения селексипага у пациентов с нарушением функции печени тяжёлой степени (класс С по классификации Чайлд-Пью) отсутствует, в связи с чем Апбрави не показан для лечения данной группы пациентов. AUC селексипага и его активного метаболита увеличивается у пациентов с нарушением функции печени средней степени (класс В по классификации Чайлд-Пью). У пациентов с нарушением функции печени средней степени Апбрави должен применяться один раз в день.
Нарушение функции почек
Титрование дозы у пациентов с нарушением функции почек тяжёлой степени (рСКФ <30 мл/мин/1,73 м²) должно проводиться с осторожностью. Опыт применения Апбрави у пациентов, находящихся на гемодиализе, отсутствует, в связи с чем Апбрави не должен применяться у данной группы пациентов.
Женщины детородного возраста
Женщины детородного возраста должны применять надёжные методы контрацепции во время приёма селексипага.
Влияние на способность управлять транспортными средствами и другими механизмами
Апбрави в малой степени влияет на способность управлять транспортными средствами и механизмами. Клиническое состояние пациента и профиль нежелательных реакций селексипага (такие как головная боль или гипотензия) должны быть приняты во внимание при рассмотрении способности пациента управлять транспортными средствами или механизмами.
Форма выпуска
Таблетки, покрытые плёночной оболочкой, 200 мкг
По 10 таблеток в блистере из полиамид/алюминий/ПЭ высокой плотности/ПЭ с осушителем/ ПЭ высокой плотности, запаянном алюминиевой фольгой.
По 6 блистеров с инструкцией по медицинскому применению в картонной пачке с контролем первого вскрытия.
По 14 блистеров с инструкцией по медицинскому применению в картонной пачке с контролем первого вскрытия (упаковка для титрования дозы).
Таблетки, покрытые плёночной оболочкой, 800 мкг
По 10 таблеток в блистере из полиамид/алюминий/ПЭ высокой плотности/ПЭ с осушителем/ ПЭ высокой плотности, запаянном алюминиевой фольгой.
По 6 блистеров с инструкцией по медицинскому применению в картонной пачке с контролем первого вскрытия.
Условия хранения
При температуре не выше 30 °С.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять после истечения срока годности, указанного на упаковке.
Условия отпуска
Отпускают по рецепту.
Держатель (владелец) регистрационного удостоверения
Актелион Фармасьютикалз Лтд., Швейцария
Гевербештрассе 16, 4123 Альшвиль, Швейцария
Actelion Pharmaceuticals Ltd., Switzerland
Gewerbestrasse 16, 4123 Allschwil, Switzerland
Производитель
Экселла ГмбХ и Ко. КГ, Германия
Нюрнбергер Штрассе 12, 90537 Фойхт, Германия
Excella GmbH & Со. KG, Germany
Nuernberger Strasse 12, 90537 Feucht, Germany
Фасовщик (первичная упаковка), упаковщик (вторичная (потребительская) упаковка)
Оллпэк Груп АГ, Швейцария
Пфеффингерштрассе 45, 4153 Райнах Базель-Ланд, Швейцария
Allpack Group AG, Switzerland
Pfeffingerstrasse 45, 4153 Reinach BL, Switzerland
Выпускающий контроль качества
Актелион Фармасьютикалз Лтд., Швейцария
Гевербештрассе 12, 4123 Альшвиль, Швейцария
Actelion Pharmaceuticals Ltd., Switzerland
Gewerbestrasse 12, 4123 Allschwil, Switzerland
Организация, уполномоченная держателем (владельцем) РУ принимать сведения о рекламациях, нежелательных лекарственных реакциях и предоставлять потребителям дополнительные данные о препарате:
ООО «Актелион Фармасьютикалз РУС», Россия,
127055, г. Москва, ул. Новослободская д. 23
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
МНН: Селексипаг
Производитель: Экселла ГмбХ
Номер регистрации в РК:
РК-ЛС-5№024598
Информация о регистрации в РК:
01.07.2020 — 01.07.2025
- Скачать инструкцию медикамента
Торговое наименование
Апбрави
Международное непатентованное название
Селексипаг
Лекарственная
форма, дозировка
Таблетки,
покрытые пленочной оболочкой 200 мкг, 400 мкг, 600 мкг, 800 мкг, 1000
мкг, 1200 мкг, 1400 мкг, 1600 мкг
Фармакотерапевтическая группа
Кровь
и кроветворение. Антитромботические препараты. Ингибиторы агрегации
тромбоцитов, за исключением гепарина. Селексипаг.
Код
АТХ В01АС27
Показания к применению
Препарат
Апбрави показан для длительного лечения легочной артериальной
гипертензии (ЛАГ) у взрослых пациентов II-III функционального класса
(ФК) по классификации ВОЗ или в качестве комбинированной терапии у
пациентов, недостаточно контролируемых антагонистом рецепторов
эндотелина (АРЭ) и/или ингибитором фосфодиэстеразы 5 типа (иФДЭ-5),
или в качестве монотерапии у пациентов, не являющихся кандидатами для
лечения этими препаратами.
Эффективность
препарата была продемонстрирована у пациентов с ЛАГ, включая
идиопатическую и наследственную форму, ЛАГ, ассоциированную с
заболеваниями соединительной ткани, и ЛАГ, ассоциированную с
компенсированным простым врожденным пороком сердца.
Перечень
сведений, необходимых до начала применения
Противопоказания
—
имеется аллергия на селексипаг или любое вещество, входящее в данный
препарат (перечисленные в разделе 6).
—
имеются проблемы с сердцем, такие как:
—
плохой кровоток к сердечной мышце (тяжелая ишемическая
болезнь
сердца или нестабильная стенокардия); симптомы
могут
включать боль в груди
—
сердечный приступ за последние 6 месяцев
—
слабое сердце (декомпенсированная сердечная недостаточность)
без
тщательного медицинского наблюдения
—
нерегулярные сердцебиения тяжелой выраженности
—
дефект клапанов сердца (врожденный или приобретенный), кото-
рый
приводит к плохой работе сердца (не связан с легочной
артериальной
гипертензией)
—
был инсульт за последние 3 месяца или другие состояния, которые
снижают поступление крови в головной мозг (например, транзиторная
ишемическая атака)
—
если принимаете гемфиброзил (препарат, принимаемый для снижения
уровня жиров [липидов] в крови)
Необходимые
меры предосторожности при применении
Поговорите
с врачом, проводящего вам лечение ЛАГ или медицинской сестрой,
прежде чем принимать препарат Апбрави,
если:
—
принимаете лекарственные препараты от высокого давления
—
низкое артериальное давление, сопровождаемое такими
симптомами
как головокружение
—
недавно имели выраженную кровопотерю или потерю жидкости
вследствие
тяжелой диареи или рвоты
—
проблемы с щитовидной железой
—
тяжелые проблемы с почками или находитесь на диализе
—
имеете или имели тяжелые проблемы с печенью, которая плохо работает
Если
заметили какое-либо из перечисленных выше состояний или изменение
вашего состояния, немедленно
сообщите об этом врачу.
Взаимодействия
с другими лекарственными препаратами
Сообщите
своему врачу, если принимаете, недавно принимали или можете принимать
какие-либо другие препараты.
Прием
других препаратов может повлиять на работу препарата Апбрави.
Расскажите
своему врачу по ЛАГ или медицинской сестре, если принимаете
какой-либо из следующих препаратов:
—
Гемфиброзил (препарат, используемый для снижения уровня жиров
[липидов]
в крови)
—
Клопидогрел (препарат, используемый для угнетения образования
тромбов
при ишемической болезни сердца)
—
Деферасирокс (препарат, используемый для удаления железа из
кровотока)
—
Терифлуномид (препарат, используемый для лечения рецидивирующе-
ремиттирующего
рассеянного склероза)
—
Карбамазепин (препарат, используемый для лечения некоторых форм
эпилепсии,
невралгий или для контроля серьезных расстройств
настроения,
когда другие препараты не работают)
—
Фенитоин (препарат, используемый для лечения эпилепсии)
—
Вальпроевая кислота (препарат, используемый для лечения эпилепсии)
—
Пробенецид (препарат, используемый для лечения подагры)
—
Флуконазол, рифампицин или рифапентин (антибиотики, применяемые
для
лечения инфекций)
Специальные
предупреждения
Дети
и подростки
Не
давайте этот препарат детям до 18 лет, потому что препарат Апбрави не
изучался у детей.
Пациенты
пожилого возраста
Данные
по применению препарата Апбрави у пациентов старше 75 лет ограничены.
Препарат Апбрави следует применять с осторожностью в этой возрастной
группе.
Во
время беременности и лактации
Препарат
Апбрави
не рекомендуется во время беременности и в период кормления грудью.
Женщинам
детородного возраста следует
использовать эффективные методы контрацепции в период приема
препарата Апбрави.
Если беремен-ны или кормите грудью, думаете, что можете быть
беременны или планируете рождение ребенка, обратитесь к своему врачу
за советом перед началом применения данного препарата.
Особенности
влияния препарата на способность управлять транспортным средством или
потенциально опасными механизмами
Препарат
Апбрави
может вызвать побочные эффекты, такие как головная боль и низкое
артериальное давление, которые могут повлиять на способность
управлять транспортным средством; симптомы Вашего заболевания также
могут доставить трудности при вождении.
Рекомендации
по применению
Препарат
Апбрави
должен
назначать только врач, который имеет опыт лечения ЛАГ. Всегда
принимайте препарат Апбрави
точно, как прописал Вам врач. Проконсультируйтесь со своим врачом,
если не уверены или если остались какие-либо вопросы.
Сообщите
своему лечащему врачу, если возникнут нежелательные реакции, так как
ваш врач может порекомендовать вам изменить дозу препарата Апбрави.
Сообщите
своему врачу, если принимаете другие лекарства, так как ваш врач
может порекомендовать принимать препарат Апбрави только один раз в
день.
Если
у вас слабое зрение или есть любой тип слепоты, обратитесь за
помощью к другому человеку на время титрования дозы Апбрави.
Режим
дозирования
В
начале лечения вы будете принимать наименьшую дозу. Это 200 мкг
таблетки
утром
и 200 мкг таблетки вечером.
Лечение должно быть начато вечером. Ваш врач проинструктирует о
постепенном увеличении дозы. Это называется титрованием дозы. Это
позволит вашему организму
привыкнуть
к новому препарату. Целью титрования дозы является достижение
наиболее подходящей дозы. Это будет наивысшая доза, которую вы
сможете перенести. Она может достигнуть максимальной дозы 1600 мкг
утром и вечером.
Первая
упаковка таблеток, которую вы получите, будет содержать светло-желтые
таблетки по 200 мкг. Ваш врач расскажет, как увеличивать дозу по
шагам, обычно каждую неделю, но интервал между повышением дозы может
быть больше.
С
каждым шагом вы будете добавлять 200 мкг таблетку к утренней дозе и
еще одну 200 мкг таблетку к вечерней дозе. Первый прием увеличенной
дозы должен происходить вечером. Диаграмма ниже показывает число
таблеток для приема каждое
утро и
каждый
вечер в
период первых 4 шагов.
Если
врач проинструктировал вас о дальнейшем увеличении дозы и о движении
вверх до шага 5, это можно сделать, приняв одну зеленую 800 мкг
таблетку и одну светло-желтую 200 мкг таблетку утром и одну 800 мкг
таблетку и одну светло-желтую таблетку вечером.
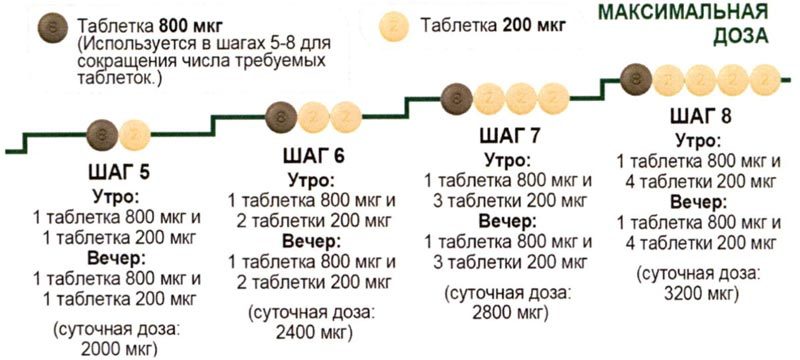
Если
врач сказал вам увеличивать дозу дальше, то
необходимо
добавить одну 200 мкг таблетку к утренней дозе и одну 200 мкг
таблетку к вечерней дозе с каждым новым шагом.
Первый
прием увеличенной дозы следует осуществлять вечером. Максимальная
доза
препарата Апбрави
– 1600 мкг утром и 1600 мкг вечером. Тем не менее, не каждый
пациент достигнет этой дозы, поскольку разным пациентам требуются
различные дозы.
Диаграмма
ниже показывает число таблеток для приема каждое
утро и
каждый
вечер на
каждом шагу, начиная с шага 5.
Упаковка
для титрования дозы также содержит руководство по титрованию дозы, в
котором содержится информация о процессе титрования и которое
позволяет записывать количество таблеток, которые принимаете каждый
день.
Не
забудьте записывать в вашем дневнике титрования дозы количество
таблеток, которые принимаете каждый день.
Шаги титрования дозы обычно длятся около 1 недели. Если врач
проинструктировал вас удлинить каждый шаг титрования дозы больше чем
на неделю, существуют дополнительные страницы дневника, которые
помогут вам отследить это. Не
забывайте регулярно говорить с
Вашим
врачом или медицинской сестрой по ЛАГ во время периода титрования
дозы.
Снижение
дозы до предыдущего уровня из-за побочных эффектов
В
период титрования дозы вы можете испытывать побочные эффекты, такие
как головная боль, диарея, недомогание (тошнота), рвота, боль в
челюсти, мышечная боль, боль в ногах, боль в суставах, или
покраснение лица. Если тяжело переносите эти побочные эффекты,
обсудите со своим врачом, как справиться с ними или как их лечить.
Существуют методы лечения, которые помогут облегчить эти побочные
эффекты. Например, анальгетики, такие как парацетамол, могут помочь в
лечении боли и головной боли.
Если
побочные эффекты не поддаются лечению или постепенно не уменьшаются в
дозе, которую вы принимаете, ваш врач может скорректировать дозу,
уменьшив количество таблеток светло-желтого цвета в 200 мкг, которые
вы принимаете, по одной утром и по одной вечером.
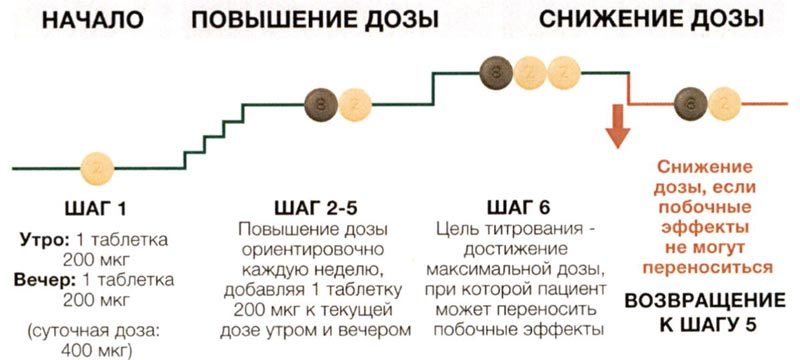
Диаграмма
ниже показывает снижение дозы к более низкой дозе препарата. Делайте
так, только если это порекомендовал ваш врач.
Если
после снижения дозы побочные эффекты поддаются лечению, врач может
решить, что вам следует остаться на этой дозе. Пожалуйста, смотри-те
ниже раздел «Поддерживающая доза» для получения
дополнительной информации.
Поддерживающая
доза
Максимальная
доза, которую
вы можете переносить в процессе титрования, станет вашей
поддерживающей дозой. Ваша поддерживающая доза – это доза,
которую вам следует принимать регулярно.
Ваш
врач назначит вам таблетку, подходящую для вашей поддерживающей дозы.
Это
позволит вам принимать одну таблетку утром и одну таблетку вечером
вместо нескольких таблеток каждый раз.
Полное описание таблеток препарата Апбрави, включая цвет и
маркировку, пожалуйста, см. в разделе Описание
внешнего вида, запаха и вкуса данного
листка-вкладыша.
Со
временем врач может cкорректировать
вашу поддерживающую дозу при необходимости.
Если
в любое время после приема одной и той же дозы в течение длительного
времени у вас возникают побочные эффекты, которые вы не можете
перенести или побочные эффекты, которые влияют на вашу повседневную
деятельность, обратитесь к врачу, поскольку может потребоваться
снижение дозы препарата. Врач может назначить вам таблетки в меньшей
дозировке. Пожалуйста, не забудьте утилизировать неиспользованные
таблетки.
Принимайте
препарат Апбрави один раз утром и один раз вечером с интервалом
примерно 12 часов между приемами.
Принимайте таблетки во время еды, так будет легче переносить
препарат. Проглатывайте таблетки целиком, запивая их стаканом воды.
Не следует делить, крошить или разжёвывать таблетки.
Меры,
которые необходимо принять в случае передозировки
Если
вы приняли больше таблеток, чем назначили, обратитесь к своему врачу.
Меры,
необходимые при пропуске одной или нескольких доз лекарственного
препарата
Если
вы забыли принять препарат Апбрави, примите дозу препарата, как
только вспомните об этом, затем продолжайте прием таблетки по обычной
схеме. Если время для следующей дозы почти наступило (в течение 6
часов до того, как вы должны принять следующую дозу), вам следует
пропустить эту дозу и продолжить принимать препарат в обычное время.
Не принимайте двойную дозу препарата, чтобы восполнить пропущенную
таблетку.
Указание
на наличие риска симптомов отмены
Резкое
прекращение лечения препаратом Апбрави
может привести к ухудшению ваших симптомов. Не прекращайте прием
препарата Апбрави,
не согласовав это со своим врачом. Ваш врач может посоветовать
постепенно снизить дозу до полной отмены препарата.
Если,
по каким-либо любым причинам, вы прекратили прием препарата Апбрави
в течение 3 дней и более (если пропустили 3 утренние и 3 вечерние
дозы, или 6 доз подряд или более), свяжитесь
со своим врачом немедленно, поскольку вам может потребоваться
коррекция дозы во избежание побочных эффектов.
Ваш врач может принять решение возобновить лечение с меньшей дозы
препарата, постепенно увеличивая ее до предшествующей поддерживающей
дозы.
Рекомендации
по обращению за консультацией к медицинскому работнику для
разъяснения способа применения лекарственного препарата
Если
у Вас остались
вопросы по применению данного препарата обратитесь к своему врачу или
медицинской сестре.
Описание
нежелательных реакций, которые
проявляются при стандартном применении ЛП и меры, которые следует
принять в этом случае
Как
и другие лекарства, этот препарат может вызвать развитие побочных
эффектов. Вы
можете испытывать побочные эффекты не только в период титрования
дозы, когда Ваша доза увеличивается, но и позже, после того, как вы в
течение длительного времени принимаете одну и ту же дозу.
Очень
часто (≥1/10)
—
головная боль
—
приливы (покраснение лица)
—
тошнота и рвота (ощущение недомогания)
—
диарея
—
боль в челюсти, мышечная боль, боль в суставах, боль в ногах
—
назофарингит (заложенность носа)
Часто
(≥1/100, <1/10)
—
анемия (низкий уровень эритроцитов)
—
гипертиреоз (гиперактивная щитовидная железа)
—
снижение аппетита
—
снижение веса
—
гипотензия (низкое артериальное давление)
—
боль в животе
—
боль
—
изменения в некоторых анализах крови, включая уровень клеток крови
или
функцию щитовидной железы
—
сыпь, включая крапивницу, могут вызвать ощущение жжения или
покалывания
и покраснение кожи
Нечасто
(≥1/1000, <1/100)
—
повышение частоты сердечных сокращений
При
возникновении нежелательных лекарственных реакций обращаться к
медицинскому работнику, фармацевтическому работнику или напрямую в
информационную базу данных по нежелательным реакциям (действиям) на
лекарственные препараты, включая сообщения о неэффективности
лекарственных препаратов
РГП
на ПХВ «Национальный Центр экспертизы лекарственных средств и
медицинских изделий» Комитета контроля качества и безопасности
товаров и услуг Министерства здравоохранения Республики Казахстан
http://www.ndda.kz
Дополнительные
сведения
Состав
лекарственного препарата
Одна
таблетка, покрытая пленочной оболочкой 200 мкг, содержит
Активное
вещество — селексипага 0.2 мг.
Вспомогательные
вещества (ядро): маннитол, крахмал кукурузный,
гидроксипропилцеллюлоза низкозамещенная, гидроксипропилцеллюлоза,
магния стеарат.
Вспомогательные
вещества (оболочка): гипромеллоза, пропиленгликоль, титана диоксид
(Е171), железа оксид желтый (Е172), карнаубский воск.
Одна
таблетка, покрытая пленочной оболочкой 400 мкг, содержит
Активное
вещество — селексипага 0.4 мг.
Вспомогательные
вещества (ядро): маннитол, крахмал кукурузный,
гидроксипропилцеллюлоза низкозамещенная, гидроксипропилцеллюлоза,
магния стеарат.
Вспомогательные
вещества (оболочка): гипромеллоза, пропиленгликоль, титана диоксид
(Е171), железа оксид красный (Е172), карнаубский воск.
Одна
таблетка, покрытая пленочной оболочкой 600 мкг, содержит
Активное
вещество — селексипага 0.6 мг.
Вспомогательные
вещества (ядро): маннитол, крахмал кукурузный,
гидроксипропилцеллюлоза
низкозамещенная, гидроксипропилцеллюлоза, магния стеарат.
Вспомогательные
вещества (оболочка): гипромеллоза, пропиленгликоль, титана диоксид
(Е171), железа оксид красный (Е172), железа оксид черный (Е172),
карнаубский воск.
Одна
таблетка, покрытая пленочной оболочкой 800 мкг, содержит
Активное
вещество — селексипага 0.8 мг.
Вспомогательные
вещества (ядро): маннитол, крахмал кукурузный,
гидроксипропилцеллюлоза низкозамещенная, гидроксипропилцеллюлоза,
магния стеарат.
Вспомогательные
вещества (оболочка): гипромеллоза, пропиленгликоль, титана диоксид
(Е171), железа оксид черный (Е172), железа оксид желтый (Е172),
карнаубский воск.
Одна
таблетка, покрытая пленочной оболочкой 1000 мкг, содержит
Активное
вещество — селексипага 1.0 мг.
Вспомогательные
вещества (ядро): маннитол, крахмал кукурузный,
гидроксипропилцеллюлоза низкозамещенная, гидроксипропилцеллюлоза,
магния стеарат.
Вспомогательные
вещества (оболочка): гипромеллоза, пропиленгликоль, титана диоксид
(Е171), железа оксид красный (Е172), железа оксид желтый (Е172),
карнаубский воск.
Одна
таблетка, покрытая пленочной оболочкой 1200 мкг, содержит
Активное
вещество — селексипага 1.2 мг.
Вспомогательные
вещества (ядро): маннитол, крахмал кукурузный,
гидроксипропилцеллюлоза низкозамещенная, гидроксипропилцеллюлоза,
магния стеарат.
Вспомогательные
вещества (оболочка): гипромеллоза, пропиленгликоль, титана диоксид
(Е171), железа оксид красный (Е172), железа оксид черный(Е172),
карнаубский воск.
Одна
таблетка, покрытая пленочной оболочкой 1400 мкг, содержит
Активное
вещество — селексипага 1.4 мг.
Вспомогательные
вещества (ядро): маннитол, крахмал кукурузный,
гидроксипропилцеллюлоза низкозамещенная, гидроксипропилцеллюлоза,
магния стеарат.
Вспомогательные
вещества (оболочка): гипромеллоза, пропиленгликоль, титана диоксид
(Е171), железа оксид желтый (Е172), карнаубский воск.
Одна
таблетка, покрытая пленочной оболочкой 1600 мкг, содержит
Активное
вещество — селексипага 1.6 мг.
Вспомогательные
вещества (ядро): маннитол, крахмал кукурузный,
гидроксипропилцеллюлоза низкозамещенная, гидроксипропилцеллюлоза,
магния стеарат.
Вспомогательные
вещества (оболочка): гипромеллоза, пропиленгликоль, титана диоксид
(Е171), железа оксид красный (Е172), железа оксид черный(Е172),
железа оксид желтый (Е172), карнаубский воск.
Описание
внешнего вида, запаха и вкуса
Таблетки,
покрытые пленочной оболочкой светло-желтого цвета, круглой формы, с
гравировкой «2»
на
одной стороне (для
дозировки 200 мкг).
Таблетки,
покрытые пленочной оболочкой красного цвета, круглой формы, с
гравировкой «4»
на
одной стороне (для
дозировки 400 мкг).
Таблетки,
покрытые пленочной оболочкой светло-фиолетового цвета, круглой формы,
с гравировкой «6»
на
одной стороне (для
дозировки 600 мкг).
Таблетки,
покрытые пленочной оболочкой зеленого цвета, круглой формы, с
гравировкой «8»
на
одной стороне (для
дозировки 800 мкг).
Таблетки,
покрытые пленочной оболочкой оранжевого цвета, круглой формы, с
гравировкой «10»
на
одной стороне (для
дозировки 1000 мкг).
Таблетки,
покрытые пленочной оболочкой темно-фиолетового цвета, круглой формы,
с гравировкой «12»
на
одной стороне (для
дозировки 1200 мкг).
Таблетки,
покрытые пленочной оболочкой темно-желтого цвета, круглой формы, с
гравировкой «14»
на
одной стороне (для
дозировки 1400 мкг).
Таблетки,
покрытые пленочной оболочкой коричневого цвета, круглой формы, с
гравировкой «16» на одной стороне (для
дозировки 1600 мкг).
Форма выпуска и упаковка
По
10 таблеток помещают в контурную ячейковую упаковку из полиамида/
алюминия/полиэтилена высокой плотности/полиэтилена со встроенным
осушителем/полиэтилена высокой плотности, запаянном алюминиевой
фольгой.
По
6 (для дозировок 200 мкг, 400 мкг, 600 мкг, 800 мкг, 1000 мкг, 1200
мкг, 1400 мкг, 1600 мкг) контурных ячейковых упаковок вместе с
инструкцией по медицинскому применению на казахском и русском языках
вкладывают в пачку из картона.
По
14 (для дозировки 200 мкг) контурных ячейковых упаковок вместе с
инструкцией по медицинскому применению, руководством по титрованию
дозы на казахском и русском языках вкладывают в пачку из картона.
Срок хранения
3
года
Не
применять по истечении срока годности!
Условия хранения
Хранить
в оригинальной упаковке в защищенном от света месте при температуре
не выше 30°C.
Хранить
в недоступном для детей месте!
Условия отпуска из аптек
По
рецепту
Сведения
о производителе
Производитель
Экселла
Гмбх и Ко. КГ,
Nürnberger
Str. 12, 90537 Фойхт, Германия
Упаковщик
Оллпэк
Груп АГ,
Pfeffingerstrasse
45, 4153, Райнах, Швейцария.
Выпускающий
контроль качества
Актелион
Фармасьютикалз Лтд.,
Gewerbestrasse
16, 4123 Allschwil, Швейцария.
Тел.:
+7 (495) 755-83-57; факс: +7 (495) 755-83-58
Электронная
почта: DrugSafetyRU@ITS.JNJ.com
Держатель
регистрационного удостоверения
ООО
«Джонсон & Джонсон»
Российская
Федерация, 121614, г. Москва, ул. Крылатская, 17/2
Тел.:
+7 (495) 755 83 57
Факс:
+7 (495) 755 83 58
Электронная
почта:
DrugSafetyRU@ITS.JNJ.com
Наименование,
адрес и контактные данные (телефон, факс, электронная почта)
организации на территории Республики Казахстан, принимающей претензии
(предложения) по качеству лекарственных средств от потребителей и
ответственной за пострегистрационное наблюдение за безопасностью
лекарственного средства
Филиал
ООО «Джонсон & Джонсон» в Республике Казахстан
Республика
Казахстан
050040,
г. Алматы,
ул.
Тимирязева, 42, павильон № 23 «А»
Тел.:
+7 (727) 356 88 11
Факс:
+7 (727) 356 88 13
Электронная
почта: DrugSafetyKZ@its.jnj.com
|
РУКОВОДСТВО |
Страница
1
|
Апбрави таблетки, Руководство по титрованию дозы Начиная лечение препаратом Апбрави Пожалуйста, прочитайте инструкцию по |
|
Страница |
Страница |
|
Содержание
Как
Как Что Когда Снижение |
Когда Если
Если Дневник |
|
Страница |
Страница |
|
Как
Начальная Следует |
Существует Титрование В Поддерживающая После Эта |
|
Страница |
Страница |
||||||||
|
Как
Вы
Первый
ностью Цель |
Каждый
Некоторые
Отдельным
Важно, |
||||||||
|
траница |
Страница |
||||||||
|
Что Каждый Начальная доза
|
таблетка таблетка 200 (Используется для таблеток, один
(Размер |
|
Страница |
Страница |
|
↓ Когда
Как
Сообщите
Наиболее
•Головная
Боль Полный |
Если
Если
Вы |
|
Страница |
Страница |
||||||
|
Снижение
Каждый
около таблетка
(Размер
(Размер |
Повышение доза
ШАГ
к
таблетка (используется сокращения необходимых препарата.) |
|
Страница |
Страница |
|
Когда Максимальная титрования, Ваша принимать
Ваш Это |
Например,
Максимальная
переносимая
Максимальная
переносимая
Со |
|
Страница |
Страница |
|
Если
Если
Не |
Если
Не
Если,
Ваш |
|
Страница |
Страница |
||||
|
Дневник Пожалуйста, медицинскому
Следующие
вечером
Используйте
Каждый
Дневник
|
Помните
Вашим
Запишите
Телефон
Телефон Заметки: |
|
Страница |
Страница |
|
неделя
сколько 1
медсестрой Дата:
Первый |
неделя
углу
сколько _____
медсестрой Дата:
Первый |
|
Страница |
Страница |
|
неделя
углу
сколько _____
медсестрой Дата: |
неделя
углу
сколько _____
медсестрой Дата:
Обратитесь |
|
Страница |
Страница |
|
неделя
углу
сколько _____
медсестрой Дата:
Обратитесь |
неделя
углу
сколько _____
медсестрой Дата:
Обратитесь |
|
Страница |
Страница |
|
неделя
углу
сколько _____
медсестрой Дата:
Обратитесь |
неделя
углу
сколько _____
медсестрой Дата:
Обратитесь |
|
Страница |
Страница |
||||
|
Используйте в к На Вы
с
|
Помните
Вашим
Запишите
Телефон
Телефон Заметки: |
|
Страница |
Страница |
|
неделя
углу
сколько _____
медсестрой Дата: |
неделя
углу
сколько _____
медсестрой Дата: |
|
Страница |
Страница |
|
неделя
углу
сколько _____
медсестрой Дата: |
неделя
углу
сколько _____
медсестрой Дата: |
|
Страница |
Страница |
|
неделя
углу
сколько _____
медсестрой Дата: |
неделя
углу
сколько _____
медсестрой Дата: |
|
Страница |
Страница |
|
неделя
углу
сколько _____
медсестрой Дата: |
неделя
углу
сколько _____
медсестрой Дата: |
|
Страница |
Страница |
|
Для |
|
Страница |
|
Actelion |
| Листок-вкладыш_Апбрави_23.062020_.docx | 1.16 кб |
| 1_Апбрави_табл._ЛВ_каз_20_.06_.2020_(wecompress_.com)_.doc | 0.82 кб |
Отправить прикрепленные файлы на почту
«Актелион», компания фармацевтического подразделения «Янссен» корпорации «Джонсон & Джонсон», объявила о регистрации на российском рынке инновационного лекарственного препарата Апбрави (селексипаг) для лечения легочной артериальной гипертензии (ЛАГ)1.
Апбрави – первый и единственный одобренный в мире пероральный селективный агонист IP-рецепторов простациклина, который показан для длительного лечения ЛАГ II-IV функционального класса по классификации Всемирной организации здравоохранения (ВОЗ) у взрослых пациентов, с целью предотвращения прогрессирования заболевания2,3,4. Апбрави эффективен как в комбинации с антагонистами рецепторов эндотелина и/или ингибиторами фосфодиэстеразы 5-го типа, так в монотерапии. Эффективность Апбрави доказана в отношении идиопатической и наследственной ЛАГ, а также ЛАГ, ассоциированной с заболеваниями соединительной ткани и ЛАГ, ассоциированной с компенсированным простым врождённым пороком сердца3.
Долгосрочная эффективность и безопасность Апбрави у пациентов с ЛАГ была продемонстрирована в клиническом исследовании GRIPHON, самом масштабном из когда-либо проводившихся у пациентов с легочной гипертензией. GRIPHON – это долгосрочное многоцентровое рандомизированное плацебо-контролируемое событийное исследование фазы 3, проводившееся в параллельных группах, в котором приняли участие 1156 пациентов с ЛАГ, проходивших лечение в 181 медицинском центре в 39 странах мира, в том числе в исследовании участвовал 91 пациент из России. Композитной первичной конечной точкой в дизайне исследования служило время от момента рандомизации до начала прогрессирования заболевания (госпитализации по поводу ЛАГ, начала внутривенного или подкожного введения простаноидов, оксигенотерапии, проведения трансплантации легких и других проявлений) или смерти. Апбрави продемонстрировал снижение риска прогрессирования заболевания/смерти у всех пациентов с ЛАГ независимо от линии терапии на 40%. Согласно результатам исследования, добавление Апбрави на раннем этапе терапии снижает риск прогрессирования ЛАГ и смерти у пациентов на 64%5,6.
Академик РАН, профессор, д.м.н. Ирина Евгеньевна Чазова, директор Института клинической кардиологии им. А.Л.Мясникова ФГБУ НМИЦ кардиологии Минздрава России комментирует: «В последнее десятилетие были достигнуты значительные успехи в понимании механизмов развития ЛАГ, разработке подходов к диагностике и лечению пациентов с этой патологией. Новые стратегии терапии с фокусом на отдаленные исходы у пациентов меняют парадигму лечения ЛАГ от краткосрочных целей (симптоматическое улучшение толерантности к физической нагрузке) до долгосрочных (замедление прогрессирования заболевания и снижение смертности). Данные последних крупных контролируемых клинических исследований диктуют необходимость ранней комбинированной терапии при ЛАГ» 8.
Легочная артериальная гипертензия (ЛАГ) – это орфанное (редкое) прогрессирующее, угрожающее жизни заболевание, характеризующееся аномально высоким давлением крови в легочных артериях. Симптомы ЛАГ неспецифичны и могут варьировать от легкой одышки и усталости при обычной повседневной активности до симптомов правожелудочковой недостаточности и серьезных ограничений в физической нагрузке7.
В развитии ЛАГ задействовано три основных биологических сигнальных пути: путь эндотелина, путь оксида азота и простациклиновый путь. Апбрави – единственный пероральный препарат, целенаправленно действующий на простациклиновый путь и улучшающий долгосрочные исходы у пациентов с ЛАГ4,8. «Мы знали, что путь простациклина может играть ключевую роль в лечении ЛАГ. До настоящего времени возможности лечения, нацеленного на путь простациклина, были в нашей стране крайне ограничены. Теперь нам доступна инновационная пероральная терапия, безопасность и эффективность которой подкрепляется результатами серьезных клинических исследований, – говорит член-корр. РАН, профессор, д.м.н. Сергей Николаевич Авдеев, главный пульмонолог Министерства здравоохранения РФ. – С появлением селексипага открываются значительные клинические возможности для проведения комбинированной терапии препаратами, воздействующими на разные механизмы развития ЛАГ. Селексипаг обеспечивает блестящие долгосрочные результаты лечения даже у тех пациентов, которые уже получают базовую терапию ЛАГ одним или двумя препаратами. Вместе с хорошей переносимостью это делает Апбрави вариантом лечения, который действительно может качественно изменить подход к терапии многих пациентов с ЛАГ».
«Наша компания была пионером в борьбе с легочной артериальной гипертензией и уже долгое время делает значимый вклад в улучшение качества жизни пациентов с этим смертельным заболеванием. Наша приверженность инновациям в этой области подтверждается регистрацией инновационного препарата Апбрави в России. Мы будем прикладывать максимальные усилия, чтобы все пациенты, которым этот препарат жизненно необходим, могли получить доступ к нему – а значит, могли жить дольше, сохраняя высокое качество жизни», – отмечает Катерина Погодина, генеральный директор ООО «Джонсон & Джонсон», управляющий директор «Янссен» в России и СНГ.
Ссылки:
- Государственный реестр лекарственных средств https://grls.rosminzdrav.ru
- Duggan ST, Keam SJ, Burness CB. Selexipag: A Review in Pulmonary Arterial Hypertension. Am J Cardiovasc Drugs. 2017 Feb;17(1):73-80. doi: 10.1007/s40256-016-0209-9.
- Инструкция по медицинскому применению лекарственного препарата Апбрави. Регистрационное удостоверение ЛП-005577
- Noel ZR et al. Selexipag for the treatment of pulmonary arterial hypertension. Am J Health-Syst Pharm. 2017; 74:1135-41
- Sitbon O, Channick R, Chin KM, et al; for the GRIPHON Investigators. Selexipag for the treatment of pulmonary arterial hypertension. N Engl J Med. 2015;373(26):2522-2533.
- Coghlan JG, Channick R, Chin K, et al. Targeting the prostacyclin pathway with selexipag in patients with pulmonary arterial hypertension receiving double combination therapy: insights from the randomized controlled GRIPHON study. Am J Cardiovasc Drugs. 2018;18(1):37-47.
- Delcroix M, Howard L. Pulmonary arterial hypertension: the burden of disease and impact on quality of life. Eur Respir Rev 2015; 24:621-9.
- Galiè N, Humbert M, Vachiery JL, et al. 2015 ESC/ERS Guidelines for the diagnosis and treatment of pulmonary hypertension). Eur Heart J 2015.
Пресс-релиз