Сиртуро (Sirturo) инструкция по применению
📜 Инструкция по применению Сиртуро
💊 Состав препарата Сиртуро
✅ Применение препарата Сиртуро
📅 Условия хранения Сиртуро
⏳ Срок годности Сиртуро
Описание лекарственного препарата
Сиртуро
(Sirturo)
Основано на официально утвержденной инструкции по применению препарата и подготовлено для электронного издания справочника Видаль 2014 года, дата обновления: 2019.07.18
Владелец регистрационного удостоверения:
Код ATX:
J04AK
(Другие противотуберкулезные препараты)
Лекарственная форма
| Сиртуро |
Таб. 100 мг: 188 шт. рег. №: ЛП-002281 |
Форма выпуска, упаковка и состав
препарата Сиртуро
Таблетки белого или почти белого цвета, круглые, двояковыпуклые, с выдавленной надписью «T» над «207» на одной стороне и «100» на другой.
Вспомогательные вещества: лактозы моногидрат 152.91 мг, крахмал кукурузный 66 мг, гипромеллоза 2910 8 мг, полисорбат 20 1 мг, целлюлоза микрокристаллическая 82.2 мг, кроскармеллоза натрия 23 мг, кремния диоксид коллоидный 1.4 мг, магния стеарат 4.6 мг.
188 шт. — флаконы из полиэтилена высокой плотности (1) — пачки картонные.
Фармакологическое действие
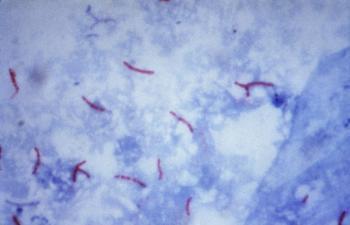
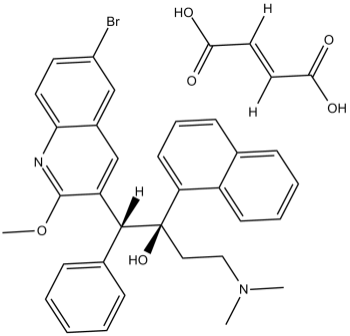
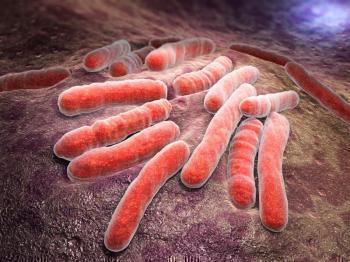
Бедаквилин относится к группе диарилхинолинов — новому классу противотуберкулезных соединений. Бактерицидное действие препарата обусловлено специфическим ингибированием протонной помпы АТФ-синтазы микобактерий (аденозин 5’трифосфат-синтазы) — фермента, играющего основную роль в процессе клеточного дыхания Mycobacterium tuberculosis. Угнетение синтеза АТФ приводит к нарушению выработки энергии и, как результат, к гибели микробной клетки.
Бедаквилин in vitro активен в отношении лекарственно чувствительных и лекарственно устойчивых (в том числе с множественной и широкой лекарственной устойчивостью) штаммов Mycobacterium tuberculosis с минимальной ингибирующей концентрацией (МИК) в диапазоне < 0,008-0,12 мкг/мл (МИК50 — 0,03 мкг/мл и МИК90 — 0,06 мкг/мл).
Механизмы развития резистентности
Механизмы, определяющие резистентность Mycobacterium tuberculosis к бедаквилину, включают в себя, по меньшей мере, 6 вариантов мутаций (замены аминокислотной последовательности) гена-мишени atpE. Не все штаммы имеют мутации гена atpE, что предполагает существование как минимум еще одного механизма развития резистентности к препарату. In vitro частота спонтанных мутаций составила 10-7-10-8 и снижалась при возрастании концентрации препарата. В низких концентрациях бедаквилин может проявлять бактериостатический эффект и потенцировать риск развития резистентности, в высоких концентрациях — оказывает бактерицидный эффект.
Фармакокинетика
Всасывание
При пероральном приеме отмечена высокая абсорбция бедаквилина. Максимальная концентрация в плазме (Cmax) достигается приблизительно через 5 ч после приема препарата. Cmax и площадь под кривой «концентрация-время» (AUC) увеличиваются пропорционально возрастанию дозы вплоть до самых высоких исследованных доз (700 мг в сутки однократно и 400 мг в несколько приемов) без изменения времени достижения максимальной концентрации (Тmax) и периода полувыведения (T1/2). Наибольшая биодоступность достигается при приеме с пищей (до 95%), которая примерно в 2 раза превышает биодоступность при приеме натощак. Таким образом, для повышения биодоступности бедаквилина препарат следует принимать во время еды.
Распределение
Бедаквилин и его активный метаболит N-монодезметил (М2) характеризуются высоким объемом распределения (примерно 164 л), соотношение концентрации в тканях к концентрации в плазме = 30. Связывание с белками плазмы составляет > 99,9%. Наивысшие концентрации создаются в легочной ткани, лимфатических узлах, селезенке, почках и печени. Проникновение через гематоэнцефалический барьер незначительно.
Метаболизм
Бедаквилин подвергается метаболизму в первую очередь путем окисления, приводящего к образованию М2. Основным изоферментом семейства Р450, участвующим в метаболизме бедаквилина и образовании М2 in vitro является CYP3A4.
В исследованиях in vitro бедаквилин не оказывает значимого воздействия на активность известных изоферментов семейства цитохрома Р450 (не ингибирует CYP1A2, CYP2A6, CYP2C8/9/10, CYP2C19, CYP2D6, CYP2E1, CYP3A4, CYP3A4/5, CYP4A и не индуцирует активность CYP1A2, CYP2C9, CYP2C19 и CYP3A4).
Метаболит М2 не оказывает существенного клинического эффекта с учетом его более слабой антибактериальной активности (в 4-6 раз ниже) по сравнению с исходным соединением.
Выведение
Бедаквилин выводится из организма главным образом кишечником. В клинических исследованиях выведение неизмененного бедаквилина почками составило ≤0,001% от введенной дозы, что свидетельствует о незначительном почечном клиренсе неизмененного препарата. После достижения Cmax концентрация бедаквилина в плазме снижается три-экспоненциальным образом. Терминальный период полувыведения (T1/2терм) бедаквилина и М2 составляет около 5,5 месяцев, что, вероятно, отражает медленное высвобождение бедаквилина и М2 из периферических тканей.
Фармакокинетика в различных группах
Возраст, пол и этническая принадлежность
По результатам популяционного фармакокинетического анализа пациентов, с диагнозом туберкулез легких, не установлено возрастных, половых и этнических клинически значимых различий в фармакокинетике бедаквилина.
Педиатрические пациенты (<18 лет)
Фармакокинетика препарата Сиртуро в педиатрической практике не оценивалась.
Пожилые пациенты (> 65 лет)
Данные о фармакокинетике препарата Сиртуро у пациентов, с диагнозом туберкулез легких, в возрасте 65 лет и старше ограничены.
Пациенты с недостаточностью функции почек
Препарат Сиртуро исследовали главным образом среди пациентов с нормальной функцией почек. Выведение неизмененного бедаквилина через почки незначительно (<0,001%). По результатам популяционного фармакокинетического анализа пациентов, получавших по 200 мг препарата Сиртуро 3 раза в неделю, клиренс креатинина не оказывал влияния на фармакокинетические параметры бедаквилина. Поэтому предполагается, что почечная недостаточность легкой или умеренной степени не будет иметь клинически значимое влияние на фармакокинетику бедаквилина. У пациентов с тяжелой почечной недостаточностью (клиренс креатинина < 30 мл/мин/1,73 м2) или терминальной стадией почечной недостаточности с необходимостью применения гемодиализа или перитонеального диализа концентрация бедаквилина может увеличиваться за счет изменения всасывания, распределения и метаболизма препарата на фоне нарушения функции почек. Так как бедаквилин в значительной степени связывается с белками плазмы, эффективность гемодиализа или перитонеального диализа для удаления препарата из плазмы будет низкой (см. раздел Способ применения и дозы, см. раздел Особые указания).
Пациенты с недостаточностью функции печени
После однократного приема препарата Сиртуро (400 мг) у 8 пациентов с умеренным нарушением функции печени (класс В по шкале Чайлд-Пью), AUC672 ч для бедаквилина и М2 была примерно на 20% ниже по сравнению со здоровыми добровольцами. Фармакокинетика бедаквилина у пациентов с тяжелой печеночной недостаточностью не изучалась (см. раздел Способ применения и дозы, см. раздел Особые указания).
ВИЧ-инфицированные пациенты
Данные о фармакокинетике препарата Сиртуро у ВИЧ-инфицированных пациентов ограничены (см. раздел Особые указания).
Показания препарата
Сиртуро
- в составе комбинированной терапии туберкулеза легких, вызванного штаммами Mycobacterium tuberculosis с множественной лекарственной устойчивостью, у взрослых (>18 лет).
Режим дозирования
Препарат Сиртуро следует принимать внутрь во время еды, так как одновременный прием с пищей увеличивает биодоступность препарата (см. раздел Фармакокинетика). Таблетку препарата Сиртуро рекомендуется проглатывать целиком, запивая водой. Препарат Сиртуро следует применять только в составе комбинированной терапии для лечения туберкулеза с множественной лекарственной устойчивостью (МЛУ ТБ) под непосредственным наблюдением специалиста (см. раздел Показания к применению, см. раздел Фармакодинамика).
Препарат Сиртуро необходимо применять только в сочетании с не менее чем 3 препаратами, к которым доказано отсутствие in vitro резистентности штамма, выделенного у пациента. Если результаты исследования in vitro отсутствуют, лечение препаратом Сиртуро может быть начато в комбинации с не менее чем 4 другими препаратами, к которым штамм, выделенный у пациента, может оказаться чувствителен. На протяжении курса лечения Сиртуро и после последнего приема препарата необходимо продолжать терапию противотуберкулезными препаратами в соответствии со стандартными режимами химиотерапии МЛУ ТБ. При выборе схемы и продолжительности приема противотуберкулезных препаратов резерва в составе комбинированной терапии лечащий врач должен руководствоваться государственными стандартами лечения туберкулеза, данными о лекарственной устойчивости микобактерий по региону с учетом лекарственной чувствительности штамма, выделенного от больного туберкулезом и данных клинико-рентгенологического обследования.
Рекомендуемый режим дозирования препарата Сиртуро:
400 мг 1 раз в сутки в течение первых 2 недель, далее (с 3 но 24 недели) по 200 мг 3 раза в неделю (с перерывом не менее 48 часов между дозами) на протяжении последующих 22 недель (в суммарной дозе 600 мг в неделю).
Общая продолжительность курса лечения препаратом Сиртуро составляет 24 недели. Пациенты должны быть предупреждены о необходимости приема препарата Сиртуро в соответствии с указаниями врача. Необходимо подчеркнуть важность приема полного курса терапии.
При пропуске приема препарата в течение первых 2 недель лечения пропущенную дозу принимать не следует. Необходимо продолжать обычный режим дозирования. При пропуске приема препарата, начиная с 3-й недели (при 3-разовом приеме в неделю по 200 мг в сутки), следует принять пропущенную дозу как можно скорее и продолжить прием препарата в соответствии с рекомендуемым режимом дозирования с перерывом после принятой пропущенной дозы не менее 24 часов, при этом, суммарная доза препарата Сиртуро за 7 дней не должна превышать 600 мг.
Особые группы пациентов
Педиатрические пациенты (<18 лет)
Безопасность и эффективность препарата Сиртуро у детей и подростков моложе 18 лет не установлены (см. раздел Особые указания).
Пожилые пациенты (> 65 лет)
Данные о применении препарата Сиртуро у пожилых пациентов ограничены (см. раздел Особые указания).
Пациенты с почечной недостаточностью
Препарат Сиртуро исследовали главным образом среди пациентов с нормальной функцией почек. Для пациентов с легкой или умеренной почечной недостаточностью коррекция дозы не требуется. Пациентам с тяжелой почечной недостаточностью или терминальной стадией почечной недостаточности, требующей гемо- или перитонеального диализа, препарат Сиртуро применять не рекомендовано (см. раздел Особые указания).
Пациенты с печеночной недостаточностью
Фармакокинетические свойства бедаквилина оценивали в исследованиях однократного приема у пациентов с умеренной печеночной недостаточностью (класса В по шкале Чайлд-Пью) (см. раздел Фармакокинетика).
У пациентов с легкой или умеренной печеночной недостаточностью изменения режима дозирования препарата Сиртуро не требуется. У пациентов с тяжелой печеночной недостаточностью эффективность и безопасность бедаквилина не изучена и применять препарат Сиртуро в данной группе пациентов не рекомендовано (см. раздел Особые указания).
ВИЧ-инфицированные пациенты
Данные о применении препарата Сиртуро у ВИЧ-инфицированных пациентов ограничены (см. раздел Особые указания).
Побочное действие
Клинические исследования проводятся в самых разных условиях, поэтому частота нежелательных побочных реакций, наблюдаемых в клинических исследованиях одного препарата, не может сравниваться напрямую с частотой нежелательных реакций в клинических исследованиях другого препарата, и может не отражать частоты, наблюдаемой в клинической практике.
Нежелательные побочные реакции (НПР) на препарат Сиртуро были определены на основании объединенных данных по пациентам, получавшим препарат Сиртуро в составе комбинированного режима противотуберкулезной терапии в проведенных контролируемых клинических исследованиях.
Нежелательные реакции па препарат Сиртуро перечислены в соответствии с системами классов органов и частотой развития (очень частые (> 1/10), частые (от > 1/100 до <1/10), нечастые (от > 1/1000 до < 1 /100), редкие (от > 1/10000 до < 1 /1000), очень редкие (<1/10000)):
Нарушения со стороны нервной системы (ЦНС): очень часто — головная боль, головокружение.
Нарушения со стороны сердечно-сосудистой системы: часто — удлинение интервала QT на ЭКГ.
Нарушения со стороны ЖКТ: очень часто — тошнота, рвота; часто — диарея.
Нарушения со стороны печени и желчевыводящих путей: часто — повышение активности трансаминаз (АЛТ, ACT).
Нарушения со стороны скелетно-мышечной и соединительной ткани: очень часто — боль в суставах, часто — боль в мышцах.
В проведенных контролируемых клинических исследованиях 2 фазы в группе пациентов получающих препарат Сиртуро в составе комбинированного режима противотуберкулезной терапии более часто, в сравнении с группой плацебо, были зарегистрированы следующие нежелательные явления: кровохарканье, анорексия, боль в грудной клетке, кожная сыпь (с частотой от > 1/100 до <1/10). Данные реакции не были идентифицированы исследователями как неблагоприятные побочные реакции.
Противопоказания к применению
- гиперчувствительность к бедаквилину и/или любому другому компоненту препарата;
- беременность;
- период лактации (грудное вскармливание);
- детский и подростковый возраст до 18 лет;
- тяжелая почечная недостаточность (КК < 30 мл/мин/1,73 м2);
- тяжелая печеночная недостаточность (в связи с отсутствием клинических данных по безопасности препарата в этой группе);
- врожденная непереносимость лактозы, дефицит лактазы, глюкозо-галактозная мальабсорбция.
С осторожностью
При удлинении интервала QT с коррекцией по формуле Фредерика (QTcF) >450 мс (с подтверждением при помощи повторного ЭКГ-исследования); при декомпенсированной сердечной недостаточности; у пациентов с личным или семейным анамнезом врожденного удлинения интервала QT, развитием аритмии по типу «torsade de points»; у пациентов с клинически значимой брадикардией, электролитными нарушениями (гипокальциемия, гипомагниемия, гипокалиемия); с указанием в анамнезе на гипотиреоз; при одновременном применении с препаратами, удлиняющими интервал QT; при совместном применении с лопинавиром/ритонавиром; у больных пожилого возраста (65 лет и старше) (см. раздел Особые указания).
Применение при беременности и кормлении грудью
Беременность
Безопасность препарата Сиртуро при беременности не установлена, поэтому препарат противопоказан к применению у беременных женщин.
Период лактации
Данные о применении бедаквилина у женщин в период лактации отсутствуют, поэтому применение препарата в период грудного вскармливания противопоказано.
Применение при нарушениях функции печени
У пациентов с легкой или умеренной печеночной недостаточностью изменения режима дозирования препарата Сиртуро не требуется. У пациентов с тяжелой печеночной недостаточностью эффективность и безопасность бедаквилина не изучена и применять препарат Сиртуро в данной группе пациентов не рекомендовано.
Применение при нарушениях функции почек
Для пациентов с легкой или умеренной почечной недостаточностью коррекция дозы не требуется. Пациентам с тяжелой почечной недостаточностью или терминальной стадией почечной недостаточности, требующей гемо- или перитонеального диализа, препарат Сиртуро применять не рекомендовано.
Применение у детей
Безопасность и эффективность препарата Сиртуро у детей и подростков моложе 18 лет не установлены, применение препарата противопоказано.
Применение у пожилых пациентов
С осторожностью следует применять препарат у больных пожилого возраста (65 лет и старше).
Особые указания
Лечение должно осуществляться под непосредственным наблюдением специалиста.
Штаммы М. tuberculosis выделенные от пациента, у которого не произошла конверсия мокроты на фоне терапии или отмечен случай рецидива после завершения лечения, должны быть исследованы на чувствительность к бедаквилину (МИК).
Влияние на летальность
В клиническом исследовании 2 фазы на протяжении 120 недель наблюдения в группе бедаквилина отмечено достоверное увеличение риска летального исхода (9/79 (11.4%)) по сравнению с группой плацебо (2/81 (2.5%)). Медиана времени развития смерти для 9 из 10 пациентов в группе исследуемого препарата составила 344 суток после приема последней дозы. Наиболее частой причиной смерти в группе бедаквилина был туберкулез (5 случаев), в 4 случаях отмечены летальные исходы от иных причин. Препарат следует использовать в случае, когда не может быть назначен другой эффективный режим терапии.
Влияние на удлинение интервала QT
В клиническом исследовании 2 фазы наблюдалось среднее увеличение QT, с коррекцией по формуле Фредерика (QTcF), начиная с 1 недели терапии (в группе Сиртуро — на 9,9 мс и на 3,5 мс в группе плацебо). Наибольшее увеличение среднего значения QTcF в течение 24 недель терапии наблюдалось на 18-й неделе и составило 15,7 мс в группе приема препарата Сиртуро в сравнении с 6,2 мс в группе плацебо. После окончания приема препарата Сиртуро (т.е. после 24-й недели) интервал QTcF не достиг нормальных величин в данной группе. В ходе клинического исследования не отмечено четкой корреляции клинически значимого удлинения интервала QT или нарушений ритма среди пациентов с летальным исходом (см. разделы Побочное действие, Взаимодействие с другими лекарственными препаратами).
Перед началом терапии препаратом Сиртуро и через 2, 12 и 24 недели лечения необходимо проведение ЭКГ-исследования для динамического контроля за интервалом QTc.
Перед началом терапии препаратом Сиртуро необходимо провести оценку концентрации калия, магния и кальция сыворотки крови и скорректировать показатели в случае отклонения от нормальных значений.
Следующие состояния могут увеличивать риск удлинения интервала QT на фоне приема препарата Сиртуро, что требует более частого ЭКГ мониторинга на фоне проводимой терапии бедаквилином:
- интервал QT с коррекцией по формуле Фредерика (QTcF) >450 мс (с подтверждением при помощи повторного ЭКГ-исследования);
- декомпенсированная сердечная недостаточность;
- личный или семейный анамнез врожденного удлинения интервала QT или развитие аритмии по типу «torsade de points»;
- клинически значимая брадикардия;
- электролитные нарушения (гипокальциемия, гипомагниемия, гипокалиемия);
- указания в анамнезе на гипотиреоз.
Отсутствуют данные по применению препарата Сиртуро у пациентов с желудочковыми аритмиями и недавно перенесенным инфарктом миокарда.
Терапию препаратом Сиртуро и любыми другими препаратами удлиняющими интервал QT следует прекратить, если у пациента развиваются клинически значимая желудочковая аритмия или интервал QT с коррекцией по формуле Фредерика (QTcF) > 500 мс (с подтверждением при помощи повторного ЭКГ-исследования). Следует проводить частый ЭКГ мониторинг до тех пор, пока значение интервала QT не вернется к норме. В случае развития приступа кратковременной потери сознания, необходимо проведение ЭКГ исследования для подтверждения удлинения интервала QT.
При совместном применении бедаквилина с препаратами, вызывающими удлинение интервала QT (в частности с антибиотиками группы фторхинолонов, макролидов, клофазимином), следует проявлять осторожность, так как нельзя исключать аддитивный или синергетический эффект, который может приводить к значительному удлинению интервала QT. В случае, если совместное применение таких лекарственных препаратов с бедаквилином необходимо, рекомендуется клиническое наблюдение пациента, в том числе регулярный мониторинг ЭКГ (см. раздел Взаимодействие с другими лекарственными препаратами).
Совместное применение с индукторами/ингибиторами CYP3A4
Следует избегать совместного применения бедаквилина и антибиотиков группы рифампицина (рифампицин, рифапентин и рифабутин) или других мощных индукторов CYP3A4, назначаемых системно, так как возможно снижение его системного действия (см. раздел Взаимодействие с другими лекарственными препаратами). Следует избегать одновременного приема бедаквилина с умеренными или мощными ингибиторами CYP3A4, назначаемыми системно, более 14 дней подряд, так как возможно увеличение времени системного действия бедаквилина и риска возникновения нежелательных реакций. В случае необходимости более длительного (>14 суток) приема ингибиторов CYP3A4 с препаратом Сиртуро следует оценивать отношение риска к пользе такой комбинации препаратов и адекватный мониторинг возможных нежелательных реакций связанных с применением Сиртуро.
Следует назначать препарат Сиртуро совместно с лопинавиром/ритонавиром с осторожностью — только после оценки отношения риска к пользе такой комбинации препаратов и при регулярном мониторинге возможных нежелательных реакций связанных с применением Сиртуро.
Влияние на функцию печени
На фоне терапии Сиртуро (в комбинации с другими противотуберкулезными препаратами) в клинических исследованиях отмечены более частые побочные реакции со стороны печени в сравнении с комбинированным режимом терапии противотуберкулезными препаратами без добавления Сиртуро (плацебо): повышение уровня трансаминаз документировано у 7/79 (8.9%) пациентов в группе Сиртуро и у 1/81 (1.2%) пациентов в группе плацебо (см. раздел Побочное действие). В связи с этим, следует проводить мониторинг клинического состояния пациента и биохимический анализ крови с определением активности «печеночных» ферментов (ACT, АЛТ) и показателей холестаза (уровень щелочной фосфатазы, билирубина) перед началом терапии препаратом Сиртуро, ежемесячно в процессе лечения и при необходимости чаще. При повышении активности аминотрансфераз (АЛТ, ACT) более чем в 3 раза следует провести повторное исследование показателей не позднее чем через 48 часов, исследовать кровь на маркеры вирусных гепатитов и прекратить прием других препаратов, обладающих гепатотоксичностью.
У пациентов, принимающих препарат Сиртуро, при появлении ранее не документированных клинически значимых изменений функциональных показателей работы печени или дальнейшее ухудшение ее функции (оцененной по уровню ACT, АЛТ и/или билирубина), а так же наличие клинических симптомов (таких как усталость, анорексия, тошнота, желтуха, потемнение мочи, гепатомегалия) необходимо особо тщательное наблюдение за больным.
Терапию препаратом Сиртуро следует прекратить, если у пациента повышение активности аминотрансфераз сочетается с увеличением общего билирубина более чем в 2 раза или отмечено увеличение показателей АЛТ и/или ACT более чем в 8 раз, или сохранение повышенной активности аминотрансфераз наблюдается более 2 недель. В период лечения Сиртуро следует избегать приема алкоголя и препаратов, обладающих гепатотоксическим эффектом.
Отсутствует опыт совместного применения антиретровирусных препаратов и препарата Сиртуро у ВИЧ-инфицированных пациентов с МЛУ ТБ, и имеются ограниченные клинические данные об использовании препарата Сиртуро у пациентов (n=22) с ВИЧ-инфекцией и МЛУ ТБ, не принимающих антиретровирусной терапии. Пациентам различных этнических групп коррекции дозы препарата не требуется.
Влияние на способность управлять автотранспортом и другими механизмами
При возникновении побочных реакций со стороны ЦНС на фоне применения препарата пациентам рекомендуется воздержаться от управления автотранспортом и занятий другими потенциально опасными видами деятельности, требующих повышенной концентрации внимания, быстроты психомоторных и двигательных реакций.
Передозировка
Информация о случаях намеренной или случайной острой передозировки бедаквилином отсутствует. В исследовании с участием 44 здоровых добровольцев, получавших однократно 800 мг препарата Сиртуро, побочные реакции соответствовали тем, которые наблюдались при приеме рекомендуемой дозы (см. раздел Побочное действие).
Лечение. Опыт лечения острой передозировки препаратом Сиртуро отсутствует. В случае преднамеренной или случайной передозировки следует принимать общие меры по поддержке основных жизненно важных функций и проводить ЭКГ-мониторинг интервала QT. Неабсорбировавшийся бедаквилин может быть удален при помощи промывания желудка и приема активированного угля. Так как бедаквилин в значительной степени связывается с белками, эффективность диализа для удаления бедаквилина из плазмы будет низкой. По возможности следует продолжать клиническое наблюдение за пациентом.
Лекарственное взаимодействие
Бедаквилин in vitro не оказывает значимого воздействия на активность известных изоферментов семейства цитохрома Р450 (см. Метаболизм).
CYP3A4 является основным изоферментом семейства цитохрома Р450, принимающим участие в метаболизме бедаквилина и образовании М2 in vitro. Поэтому содержание бедаквилина в плазме крови может уменьшиться при совместном применении с индукторами CYP3A4 и увеличиться при совместном назначении с ингибиторами CYP3A4.
Антибиотики группы рифампицина и другие индукторы CYP3A4
В исследовании лекарственного взаимодействия бедаквилина (300 мг однократно) и рифампицина (по 600 мг в сутки 21 день) у здоровых добровольцев AUC бедаквилина снизилась на 52%. В связи с возможностью уменьшения терапевтического эффекта бедаквилина по причине снижения его системного действия, следует избегать совместного применения бедаквилина и антибиотиков группы рифампицина (рифампицин, рифапентин и рифабутин) или других мощных индукторов CYP3A4, назначаемых системно (см. раздел Особые указания).
Кетоконазол и другие ингибиторы CYP3A4
При совместном применении кетоконазола (по 400 мг 4 суток) и бедаквилина (по 400 мг в сутки в течение 14 дней) у здоровых добровольцев AUC бедаквилина увеличилась на 22%, Cmax и Cmin на 9% и 33%, соответственно. В связи с потенциальным риском возникновения нежелательных реакций за счет увеличения системного действия бедаквилина, следует избегать длительного совместного применения (более 14 дней) бедаквилина с умеренными или мощными ингибиторами CYP3A4, назначаемыми системно (см. раздел Особые указания).
Другие антимикробные препараты
Совместное применение бедаквилина (400 мг в сутки) с изониазидом (300 мг в сутки 5 дней)/пиразинамидом (1000 мг в сутки 5 дней) у здоровых добровольцев в течение 14 суток не вызвало клинически значимых изменений AUC бедаквилина, изониазида или пиразинамида. При совместном применении препарата Сиртуро с изониазидом или пиразинамидом коррекции дозы не требуется. В плацебо-контролируемом клиническом исследовании у пациентов с МЛУ ТБ не наблюдалось значительного влияния препарата Сиртуро на фармакокинетику этамбутола, канамицина, пиразинамида, офлоксацина или циклосерина при их совместном применении.
Антиретровирусные препараты
В исследовании лекарственного взаимодействия между бедаквилином (400 мг однократно) и препаратом лопинавир (400 мг/ритонавир (100 мг) в режиме приема 2 раза в сутки в течение 24 дней у здоровых добровольцев AUC бедаквилина возросла на 22%. Следует назначать препарат Сиртуро совместно с препаратом лопинавир/ритонавир с осторожностью только после оценки отношения риска к пользе такой комбинации препаратов (см. раздел Особые указания).
Совместное применение невирапина (200 мг 2 раза в сутки 4 недели) с бедаквилином (400 мг однократно) не вызывало клинически значимых изменений содержания бедаквилина в плазме крови.
Клинические данные по совместному применению антиретровирусных препаратов и препарата Сиртуро у ВИЧ-инфицированных пациентов с МЛУ ТБ отсутствуют (см. раздел Особые указания).
Препараты, удлиняющие интервал QT
Информация о возможном фармакодинамическом взаимодействии между бедаквилином и препаратами, удлиняющими интервал QT, ограничена.
Наблюдался аддитивный или синергический эффект в отношении удлинения интервала QT при совместном применении бедаквилина с препаратами, которые удлиняют интервал QT. В исследовании лекарственного взаимодействия кетоконазола и бедаквилина после повторного совместного приема препаратов наблюдалось более значительное влияние на QTc данной комбинации, чем после повторного приема каждого из этих препаратов по отдельности.
Условия хранения препарата Сиртуро
При температуре не выше 25°С. Хранить в оригинальной упаковке в защищенном от света месте. Хранить в недоступном для детей месте.
Условия реализации
По рецепту.
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Сиртуро — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер
ЛП-002281
Торговое наименование препарата
Сиртуро
Международное непатентованное наименование
Бедаквилин
Лекарственная форма
Таблетки
Состав
Каждая таблетка содержит:
Активное вещество: бедаквилина фумарат — 120,89 мг, в пересчете на бедаквилин — 100.0 мг.
Вспомогательные вещества: лактозы моногидрат — 152,91 мг, крахмал кукурузный — 66.0 мг, гипромеллоза 2910, 15 мПа-с — 8,00 мг, полисорбат 20 — 1,00 мг, микрокристаллическая целлюлоза — 82,20 мг, кроскармеллоза натрия — 23,00 мг, кремния диоксид коллоидный — 1,40 мг, магния стеарат — 4,60 мг.
Описание
Круглые двояковыпуклые таблетки белого или почти белого цвета, с выдавленной надписью «Т» над «207» на одной стороне и «100» на другой стороне.
Фармакотерапевтическая группа
Противотуберкулезное средство
Код АТХ
J04AK
Фармакодинамика:
Бедаквилин относится к группе диарилхинолинов — новому классу противотуберкулезных соединений. Бактерицидное действие препарата обусловлено специфическим ингибированием протонной помпы АТФ-синтазы микобактерий (аденозин 5’трифосфат-синтазы) — фермента, играющего основную роль в процессе клеточного дыхания
Mycobacterium tuberculosis. Угнетение синтеза АТФ приводит к нарушению выработки энергии и, как результат, к гибели микробной клетки.
Бедаквилин in vitro активен в отношении лекарственно чувствительных и лекарственно устойчивых (в том числе с множественной и широкой лекарственной устойчивостью) штаммов Mycobacterium tuberculosis с минимальной ингибирующей концентрацией (МИК) в диапазоне < 0,008-0,12 мкг/мл (МИК50 — 0,03 мкг/мл и МИК90 — 0,06 мкг/мл).
Механизмы развития резистентности.
Механизмы, определяющие резистентность Mycobacterium tuberculosis к бедаквилину, включают в себя, по меньшей мере, 6 вариантов мутаций (замены аминокислотной последовательности) гена-мишени atpE. Не все штаммы имеют мутации гена atpE, что предполагает существование как минимум еще одного механизма развития резистентности к препарату. In vitro частота спонтанных мутаций составила 10-7 — 10-8 и снижалась при возрастании концентрации препарата. В низких концентрациях бедаквилин может проявлять бактериостатический эффект и потенцировать риск развития резистентности, в высоких концентрациях — оказывает бактерицидный эффект.
Фармакокинетика:
Всасывание.
При пероральном приеме отмечена высокая абсорбция бедаквилина. Максимальная концентрация в плазме (Стах) достигается приблизительно через 5 часов после приема препарата. Стах и площадь под кривой «концентрация-время» (AUC) увеличиваются пропорционально возрастанию дозы вплоть до самых высоких исследованных доз (700 мг в сутки однократно и 400 мг в несколько приемов) без изменения времени достижения максимальной концентрации (Тmах) и периода полувыведения (Т1/2). Наибольшая биодоступность достигается при приеме с пищей (до 95%), которая примерно в 2 раза превышает биодоступность при приеме натощак. Таким образом, для повышения биодоступности бедаквилина препарат следует принимать во время еды.
Распределение.
Бедаквилин и его активный метаболит N-монодезметил (М2) характеризуются высоким объемом распределения (примерно 164 л), соотношение концентрации в тканях к концентрации в плазме = 30. Связывание с белками плазмы составляет > 99,9%. Наивысшие концентрации создаются в легочной ткани, лимфатических узлах, селезенке, почках и печени. Проникновение через гематоэнцефалический барьер незначительно.
Метаболизм
Бедаквилин подвергается метаболизму в первую очередь путем окисления, приводящего к образованию М2. Основным изоферментом семейства Р450, участвующим в метаболизме бедаквилина и образовании М2 in vitro является CYP3A4.
В исследованиях in vitro бедаквилин не оказывает значимого воздействия на активность известных изоферментов семейства цитохрома Р450 (не ингибирует CYP1A2, CYP2A6, CYP2C8/9/10, CYP2C19, CYP2D6, CYP2E1, CYP3A4, CYP3A4/5, CYP4A и не индуцирует активность CYP1A2, CYP2C9, CYP2C19 и CYP3A4).
Метаболит М2 не оказывает существенного клинического эффекта с учетом его более слабой антибактериальной активности (в 4-6 раз ниже) по сравнению с исходным соединением.
Выведение.
Бедаквилин выводится из организма главным образом кишечником. В клинических исследованиях выведение неизмененного бедаквилина почками составило <0,001% от введенной дозы, что свидетельствует о незначительном почечном клиренсе неизмененного препарата. После достижения Сmах концентрация бедаквилина в плазме снижается три-экспоненциальным образом. Терминальный период полувыведения (Т 1/2 терм) бедаквилина и М2 составляет около 5,5 месяцев, что, вероятно, отражает медленное высвобождение бедаквилина и М2 из периферических тканей.
Фармакокинетика в различных группах
Возраст, пол и этническая принадлежность
По результатам популяционного фармакокинетического анализа пациентов, с диагнозом туберкулез легких, не установлено возрастных, половых и этнических клинически значимых различий в фармакокинетике бедаквилина.
Педиатрические пациенты (<18 лет)
Фармакокинетика препарата Сиртуро в педиатрической практике не оценивалась.
Пожилые пациенты (> 65 лет)
Данные о фармакокинетике препарата Сиртуро у пациентов, с диагнозом туберкулез легких, в возрасте 65 лет и старше ограничены.
Пациенты с недостаточностью функции почек
Препарат Сиртуро исследовали главным образом среди пациентов с нормальной функцией почек. Выведение неизмененного бедаквилина через почки незначительно (<0,001%). По результатам популяционного фармакокинетического анализа пациентов, получавших по 200 мг препарата Сиртуро три раза в неделю, клиренс креатинина не оказывал влияния на фармакокинетические параметры бедаквилина. Поэтому предполагается, что почечная недостаточность легкой или умеренной степени не будет иметь клинически значимое влияние на фармакокинетику бедаквилина. У пациентов с тяжелой почечной недостаточностью (клиренс креатинина < 30 мл/мин/1,73 м2) или терминальной стадией почечной недостаточности с необходимостью применения гемодиализа или перитонеального диализа концентрация бедаквилина может увеличиваться за счет изменения всасывания, распределения и метаболизма препарата на фоне нарушения функции почек. Так как бедаквилин в значительной степени связывается с белками плазмы, эффективность гемодиализа или перитонеального диализа для удаления препарата из плазмы будет низкой (см. раздел Способ применения и дозы, см. раздел Особые указания).
Пациенты с недостаточностью функции печени
После однократного приема препарата Сиртуро (400 мг) у 8 пациентов с умеренным нарушением функции печени (класс В по шкале Чайлд-Пью), AUC672ч для бедаквилина и М2 была примерно на 20% ниже по сравнению со здоровыми добровольцами. Фармакокинетика бедаквилина у пациентов с тяжелой печеночной недостаточностью не изучалась (см. раздел Способ применения и дозы, см. раздел Особые указания).
ВИЧ-инфицированные пациенты
Данные о фармакокинетике препарата Сиртуро у ВИЧ-инфицированных пациентов ограничены (см. раздел Особые указания).
Показания:
Бедаквилин показан к применению у взрослых (>18 лет) в составе комбинированной терапии туберкулеза легких, вызванного штаммами Mycobacterium tuberculosis с множественной лекарственной устойчивостью.
Противопоказания:
— гиперчувствительность к бедаквилину и/или любому другому компоненту препарата;
— беременность;
— период лактации (грудное вскармливание);
— детский и подростковый возраст до 18 лет;
— тяжелая почечная недостаточность (клиренс креатинина < 30 мл/мин/1,73 м3);
— тяжелая печеночная недостаточность (в связи с отсутствием клинических данных по безопасности препарата в этой группе);
— врожденная непереносимость лактозы, дефицит лактазы, глюкозо-галактозная мальабсорбция.
С осторожностью:
При удлинении интервала QT с коррекцией по формуле Фредерика (QTcF) >450 мс (с подтверждением при помощи повторного ЭКГ-исследования); при декомпенсированной сердечной недостаточности; у пациентов с личным или семейным анамнезом врожденного удлинения интервала QT, развитием аритмии по типу «torsade de points»; у пациентов с клинически значимой брадикардией, электролитными нарушениями (гипокальциемия, гипомагниемия, гипокалиемия); с указанием в анамнезе на гипотиреоз; при одновременном применении с препаратами, удлиняющими интервал QT; при совместном применении с лопинавиром/ритонавиром; у больных пожилого возраста (65 лет и старше) (см. раздел Особые указания).
Беременность и лактация:
Беременность
Безопасность препарата Сиртуро при беременности не установлена, поэтому препарат противопоказан к применению у беременных женщин.
Период лактации
Данные о применении бедаквилина у женщин в период лактации отсутствуют, поэтому применение препарата в период грудного вскармливания противопоказано.
Способ применения и дозы:
Препарат Сиртуро следует принимать внутрь во время еды, так как одновременный прием с пищей увеличивает биодоступность препарата (см. раздел Фармакокинетика).
Таблетку препарата Сиртуро рекомендуется проглатывать целиком, запивая водой. Препарат Сиртуро следует применять только в составе комбинированной терапии для лечения туберкулеза с множественной лекарственной устойчивостью (МЛУ ТБ) под непосредственным наблюдением специалиста (см. раздел Показания к применению, см. раздел Фармакодинамика).
Препарат Сиртуро необходимо применять только в сочетании с не менее чем 3 препаратами, к которым доказано отсутствие in vitro резистентности штамма, выделенного у пациента. Если результаты исследования in vitro отсутствуют, лечение препаратом Сиртуро может быть начато в комбинации с не менее чем 4 другими препаратами, к которым штамм, выделенный у пациента, может оказаться чувствителен. На протяжении курса лечения Сиртуро и после последнего приема препарата необходимо продолжать терапию противотуберкулезными препаратами в соответствии со стандартными режимами химиотерапии МЛУ ТБ. При выборе схемы и продолжительности приема противотуберкулезных препаратов резерва в составе комбинированной терапии лечащий врач должен руководствоваться государственными стандартами лечения туберкулеза, данными о лекарственной устойчивости микобактерий по региону с учетом лекарственной чувствительности штамма, выделенного от больного туберкулезом и данных клинико-рентгенологического обследования.
Рекомендуемый режим дозирования препарата Сиртуро:
400 мг один раз в сутки в течение первых 2 недель, далее (с 3 по 24 недели) по 200 мг 3 раза в неделю (с перерывом не менее 48 часов между дозами) на протяжении последующих 22 недель (в суммарной дозе 600 мг в неделю).
Общая продолжительность курса лечения препаратом Сиртуро составляет 24 недели. Пациенты должны быть предупреждены о необходимости приема препарата Сиртуро в соответствии с указаниями врача. Необходимо подчеркнуть важность приема полного курса терапии.
При пропуске приема препарата в течение первых 2 недель лечения пропущенную дозу принимать не следует. Необходимо продолжать обычный режим дозирования.
При пропуске приема препарата, начиная с 3-й недели (при 3-разовом приеме в неделю по 200 мг в сутки), следует принять пропущенную дозу как можно скорее и продолжить прием препарата в соответствии с рекомендуемым режимом дозирования с перерывом после принятой пропущенной дозы не менее 24 часов, при этом, суммарная доза препарата Сиртуро за 7 дней не должна превышать 600 мг.
Побочные эффекты:
Клинические исследования проводятся в самых разных условиях, поэтому частота нежелательных побочных реакций, наблюдаемых в клинических исследованиях одного препарата, не может сравниваться напрямую с частотой нежелательных реакций в клинических исследованиях другого препарата, и может не отражать частоты, наблюдаемой в клинической практике.
Нежелательные побочные реакции (НПР) на препарат Сиртуро были определены на основании объединенных данных по пациентам, получавшим препарат Сиртуро в составе комбинированного режима противотуберкулезной терапии в проведенных контролируемых клинических исследованиях.
Нежелательные реакции на препарат Сиртуро перечислены в соответствии с системами классов органов и частотой развития (очень частые (> 1/10), частые (от > 1/100 до <1/10), нечастые (от > 1/1000 до <1/100), редкие (от > 1/10000 до <1/1000), очень редкие (< 1/10000)):
Нарушения со стороны нервной системы (ЦНС): очень часто — головная боль, головокружение;
Нарушения со стороны сердечно-сосудистой системы: часто — удлинение интервала QT на ЭКГ;
Нарушения со стороны желудочно-кишечного тракта: очень часто — тошнота, рвота; часто — диарея;
Нарушения со стороны печени и желчевыводящих путей: часто — повышение активности трансаминаз (аланинаминотрансфереза (АЛТ), аспартатаминотрансфереза (ACT));
Нарушения со стороны скелетно-мышечной и соединительной ткани: очень часто — боль в суставах, часто — боль в мышцах.
В проведенных контролируемых клинических исследованиях 2 фазы в группе пациентов получающих препарат Сиртуро в составе комбинированного режима противотуберкулезной терапии более часто, в сравнении с группой плацебо, были зарегистрированы следующие нежелательные явления: кровохарканье, анорексия, боль в грудной клетке, кожная сыпь (с частотой от > 1/100 до <1/10). Данные реакции не были идентифицированы исследователями как неблагоприятные побочные реакции.
Передозировка:
Информация о случаях намеренной или случайной острой передозировки бедаквилином отсутствует. В исследовании с участием 44 здоровых добровольцев, получавших однократно 800 мг препарата Сиртуро, побочные реакции соответствовали тем, которые наблюдались при приеме рекомендуемой дозы (см. раздел Побочное действие).
Лечение. Опыт лечения острой передозировки препаратом Сиртуро отсутствует. В случае преднамеренной или случайной передозировки следует принимать общие меры по поддержке основных жизненно важных функций и проводить ЭКГ-мониторинг интервала QT. Неабсорбировавшийся бедаквилин может быть удален при помощи промывания желудка и приема активированного угля. Так как бедаквилин в значительной степени связывается с белками, эффективность диализа для удаления бедаквилина из плазмы будет низкой. По возможности следует продолжать клиническое наблюдение за пациентом.
Взаимодействие:
Бедаквилин in vitro не оказывает значимого воздействия на активность известных изоферментов семейства цитохрома Р450 (см. Метаболизм).
CYP3A4 является основным изоферментом семейства цитохрома Р-450, принимающим участие в метаболизме бедаквилина и образовании М2 in vitro. Поэтому содержание бедаквилина в плазме крови может уменьшиться при совместном применении с индукторами CYP3A4 и увеличиться при совместном назначении с ингибиторами CYP3A4.
Антибиотики группы рифампицина и другие индукторы CYP3A4
В исследовании лекарственного взаимодействия бедаквилина (300 мг однократно) и рифампицина (по 600 мг в сутки 21 день) у здоровых добровольцев AUC бедаквилина снизилась на 52%. В связи с возможностью уменьшения терапевтического эффекта бедаквилина по причине снижения его системного действия, следует избегать совместного применения бедаквилина и антибиотиков группы рифампицина (рифампицин, рифапентин и рифабутин) или других мощных индукторов CYP3A4, назначаемых системно (см. раздел Особые указания).
Кетоконазол и другие ингибиторы CYP3A4
При совместном применении кетоконазола (по 400 мг 4 суток) и бедаквилина (по 400 мг в сутки в течение 14 дней) у здоровых добровольцев AUC бедаквилина увеличилась на 22%, Сmax и Cmin на 9% и 33%, соответственно. В связи с потенциальным риском возникновения нежелательных реакций за счет увеличения системного действия бедаквилина, следует избегать длительного совместного применения (более 14 дней) бедаквилина с умеренными или мощными ингибиторами CYP3A4, назначаемыми системно (см. раздел Особые указания).
Другие антимикробные препараты
Совместное применение бедаквилина (400 мг в сутки) с изониазидом (300 мг в сутки 5 дней)/пиразинамидом (1000 мг в сутки 5 дней) у здоровых добровольцев в течение 14 суток не вызвало клинически значимых изменений AUC бедаквилина, изониазида или пиразинамида. При совместном применении препарата Сиртуро с изониазидом или пиразинамидом коррекции дозы не требуется. В плацебо-контролируемом клиническом исследовании у пациентов с МЛУ ТБ не наблюдалось значительного влияния препарата Сиртуро на фармакокинетику этамбутола, канамицина, пиразинамида, офлоксацина или циклосерина при их совместном применении.
Антиретровирусные препараты
В исследовании лекарственного взаимодействия между бедаквилином (400 мг однократно) и препаратом лопинавир (400 мг)/ритонавир (100 мг) в режиме приема 2 раза в сутки в течение 24 дней у здоровых добровольцев AUC бедаквилина возросла на 22%. Следует назначать препарат Сиртуро совместно с препаратом лопинавир/ритонавир с осторожностью только после оценки отношения риска к пользе такой комбинации препаратов (см. раздел Особые указания).
Совместное применение невирапина (200 мг 2 раза в сутки 4 недели) с бедаквилином (400 мг однократно) не вызывало клинически значимых изменений содержания бедаквилина в плазме крови.
Клинические данные по совместному применению антиретровирусных препаратов и препарата Сиртуро у ВИЧ-инфицированных пациентов с МЛУ ТБ отсутствуют (см. раздел Особые указания).
Препараты, удлиняющие интервал QT
Информация о возможном фармакодинамическом взаимодействии между бедаквилином и препаратами, удлиняющими интервал QT, ограничена.
Наблюдался аддитивный или синергический эффект в отношении удлинения интервала QT при совместном применении бедаквилина с препаратами, которые удлиняют интервал QT. В исследовании лекарственного взаимодействия кетоконазола и бедаквилина после повторного совместного приема препаратов наблюдалось более значительное влияние на QTc данной комбинации, чем после повторного приема каждого из этих препаратов по отдельности.
Особые указания:
Лечение должно осуществляться под непосредственным наблюдением специалиста. Штаммы М. tuberculosis выделенные от пациента, у которого не произошла конверсия мокроты на фоне терапии или отмечен случай рецидива после завершения лечения, должны быть исследованы на чувствительность к бедаквилину (МИК).
Влияние на летальность
В клиническом исследовании 2 фазы на протяжении 120 недель наблюдения в группе бедаквилина отмечено достоверное увеличение риска летального исхода (9/79 (11.4%)) по сравнению с группой плацебо (2/81 (2.5%)). Медиана времени развития смерти для 9 из 10 пациентов в группе исследуемого препарата составила 344 суток после приема последней дозы. Наиболее частой причиной смерти в группе бедаквилина был туберкулез (5 случаев), в 4 случаях отмечены летальные исходы от иных причин. Препарат следует использовать в случае, когда не может быть назначен другой эффективный режим терапии.
Влияние на удлинение интервала QT
В клиническом исследовании 2 фазы наблюдалось среднее увеличение QT, с коррекцией по формуле Фредерика (QTcF), начиная с 1 недели терапии (в группе Сиртуро — на 9,9 мс и на 3,5 мс в группе плацебо). Наибольшее увеличение среднего значения QTcF в течение 24 недель терапии наблюдалось на 18-й неделе и составило 15,7 мс в группе приема препарата Сиртуро в сравнении с 6,2 мс в группе плацебо. После окончания приема препарата Сиртуро (т.е. после 24-й недели) интервал QTcF не достиг нормальных величин в данной группе. В ходе клинического исследования не отмечено четкой корреляции клинически значимого удлинения интервала QT или нарушений ритма среди пациентов с летальным исходом (см. разделы Побочное действие, Взаимодействие с другими лекарственными препаратами).
Перед началом терапии препаратом Сиртуро и через 2, 12 и 24 недели лечения необходимо проведение ЭКГ-исследования для динамического контроля за интервалом QTc.
Перед началом терапии препаратом Сиртуро необходимо провести оценку концентрации калия, магния и кальция сыворотки крови и скорректировать показатели в случае отклонения от нормальных значений.
Следующие состояния могут увеличивать риск удлинения интервала QT на фоне приема препарата Сиртуро, что требует более частого ЭКГ мониторинга на фоне проводимой терапии бедаквилином:
— интервал QT с коррекцией по формуле Фредерика (QTcF) >450 мс (с подтверждением при помощи повторного ЭКГ-исследования);
— декомпенсированная сердечная недостаточность;
— личный или семейный анамнез врожденного удлинения интервала QT или развитие аритмии по типу «torsade de points»;
— клинически значимая брадикардия;
— электролитные нарушения (гипокальциемия, гипомагниемия, гипокалиемия);
— указания в анамнезе на гипотиреоз.
Отсутствуют данные по применению препарата Сиртуро у пациентов с желудочковыми аритмиями и недавно перенесенным инфарктом миокарда.
Терапию препаратом Сиртуро и любыми другими препаратами удлиняющими интервал QT следует прекратить, если у пациента развиваются клинически значимая желудочковая аритмия или интервал QT с коррекцией по формуле Фредерика (QTcF) > 500 мс (с подтверждением при помощи повторного ЭКГ-исследования). Следует проводить частый ЭКГ мониторинг до тех пор, пока значение интервала QT не вернется к норме. В случае развития приступа кратковременной потери сознания, необходимо проведение ЭКГ исследования для подтверждения удлинения интервала QT.
При совместном применении бедаквилина с препаратами, вызывающими удлинение интервала QT (в частности с антибиотиками группы фторхинолонов, макролидов, клофазимином), следует проявлять осторожность, так как нельзя исключать аддитивный или синергетический эффект, который может приводить к значительному удлинению интервала QT. В случае, если совместное применение таких лекарственных препаратов с бедаквилином необходимо, рекомендуется клиническое наблюдение пациента, в том числе регулярный мониторинг ЭКГ (см. раздел Взаимодействие с другими лекарственными препаратами).
Совместное применение с индукторами/ингибиторами CYP3A4
Следует избегать совместного применения бедаквилина и антибиотиков группы рифампицина (рифампицин, рифапентин и рифабутин) или других мощных индукторов CYP3A4, назначаемых системно, так как возможно снижение его системного действия (см. раздел Взаимодействие с другими лекарственными препаратами).
Следует избегать одновременного приема бедаквилина с умеренными или мощными ингибиторами CYP3A4, назначаемыми системно, более 14 дней подряд, так как возможно увеличение времени системного действия бедаквилина и риска возникновения нежелательных реакций. В случае необходимости более длительного (>14 суток) приема ингибиторов CYP3A4 с препаратом Сиртуро следует оценивать отношение риска к пользе такой комбинации препаратов и адекватный мониторинг возможных нежелательных реакций связанных с применением Сиртуро.
Следует назначать препарат Сиртуро совместно с лопинавиром/ритонавиром с осторожностью — только после оценки отношения риска к пользе такой комбинации препаратов и при регулярном мониторинге возможных нежелательных реакций связанных с применением Сиртуро.
Влияние на функцию печени
На фоне терапии Сиртуро (в комбинации с другими противотуберкулезными препаратами) в клинических исследованиях отмечены более частые побочные реакции со стороны печени в сравнении с комбинированным режимом терапии противотуберкулезными препаратами без добавления Сиртуро (плацебо): повышение уровня трансаминаз документировано у 7/79 (8.9%) пациентов в группе Сиртуро и у 1/81 (1.2%) пациентов в группе плацебо (см. раздел Побочное действие). В связи с этим, следует проводить мониторинг клинического состояния пациента и биохимический анализ крови с определением активности «печеночных» ферментов (ACT, АЛТ) и показателей холестаза (уровень щелочной фосфатазы, билирубина) перед началом терапии препаратом Сиртуро, ежемесячно в процессе лечения и при необходимости чаще. При повышении активности аминотрансфераз (АЛТ, ACT) более чем в 3 раза следует провести повторное исследование показателей не позднее чем через 48 часов, исследовать кровь на маркеры вирусных гепатитов и прекратить прием других препаратов, обладающих гепатотоксичностью.
У пациентов, принимающих препарат Сиртуро, при появлении ранее не документированных клинически значимых изменений функциональных показателей работы печени или дальнейшее ухудшение ее функции (оцененной по уровню ACT, АЛТ и/или билирубина), а так же наличие клинических симптомов (таких как усталость, анорексия, тошнота, желтуха, потемнение мочи, гепатомегалия) необходимо особо тщательное наблюдение за больным.
Терапию препаратом Сиртуро следует прекратить, если у пациента повышение активности аминотрансфераз сочетается с увеличением общего билирубина более чем в 2 раза или отмечено увеличение показателей АЛТ и/или ACT более чем в 8 раз, или сохранение повышенной активности аминотрансфераз наблюдается более 2 недель.
В период лечения Сиртуро следует избегать приема алкоголя и препаратов, обладающих гепатотоксическим эффектом.
Отсутствует опыт совместного применения антиретровирусных препаратов и препарата Сиртуро у ВИЧ-инфицированных пациентов с МЛУ ТБ, и имеются ограниченные клинические данные об использовании препарата Сиртуро у пациентов (n=22) с ВИЧ- инфекцией и МЛУ ТБ, не принимающих антиретровирусной терапии.
Пациентам различных этнических групп коррекции дозы препарата не требуется.
Влияние на способность управлять транспортными средствами и механизмами:
При возникновении побочных реакций со стороны ЦНС на фоне применения препарата пациентам рекомендуется воздержаться от управления автотранспортом и занятий другими потенциально опасными видами деятельности, требующих повышенной концентрации внимания, быстроты психомоторных и двигательных реакций.
Форма выпуска/дозировка:
Таблетки 100 мг.
Упаковка:
По 188 таблеток во флакон из полиэтилена высокой плотности, укупоренный полипропиленовой крышкой с системой защиты от вскрытия детьми и контролем первого вскрытия.
По 1 флакону вместе с инструкцией по применению в картонную пачку.
Условия хранения:
При температуре не выше 25 °С.
Хранить в оригинальной упаковке в защищенном от света месте.
Хранить в недоступном для детей месте.
Срок годности:
2 года. Не применять после истечения срока годности.
Условия отпуска
По рецепту
Производитель
Открытое акционерное общество «Фармстандарт-Уфимский витаминный завод» (ОАО «Фармстандарт-УфаВИТА»), 450077, Республика Башкортостан, г. Уфа, ул. Худайбердина, д. 28, Россия
Владелец регистрационного удостоверения/организация, принимающая претензии потребителей:
ОАО «Фармстандарт-УфаВИТА»
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Круглые двояковыпуклые таблетки белого или почти белого цвета, с выдавленной надписью «Т» над «207» на одной стороне и «100» на другой стороне.
Одна таблетка содержит:
Активное вещество: бедаквилин — 100,0 мг, в виде бедаквилина фумарата — 120,89 мг.
Вспомогательные вещества: лактозы моногидрат — 152,91 мг, крахмал кукурузный — 66,00 мг, гипромеллоза 2910, 15 мПа-c (Е 464) — 8,00 мг, полисорбат 20 (Е 432**) — 1,00 мг, микрокристаллическая целлюлоза (Е 460) — 82,20 мг, кроскармеллоза натрия (Е 466) — 23,00 мг, кремния диоксид коллоидный (Е 551) — 1,40 мг, магния стеарат -4,60 мг.
Прочие средства для лечения туберкулёза. Код ATX: J04AK05.
Фармакологические свойства
Фармакодинамика
Бедаквилин относится к группе диарилхинолинов — новому классу противотуберкулезных соединений. Бактерицидное действие препарата обусловлено специфическим ингибированием протонной помпы АТФ-синтазы микобактерий (аденозин 5’трифосфат-синтазы) — фермента, играющего основную роль в процессе клеточного дыхания Mycobacterium tuberculosis. Угнетение синтеза АТФ приводит к нарушению выработки энергии и, как результат, к гибели микробной клетки (делящихся и находящихся в покое микроорганизмов).
Бедаквилин in vitro активен в отношении лекарственно-чувствительных и лекарственно-устойчивых (в том числе с множественной, пре — и широкой лекарственной устойчивостью*) штаммов Mycobacterium tuberculosis с минимальной ингибирующей концентрацией (МИК) в диапазоне ≤ 0,008-0,12 мкг/мл (МИК50 — 0,03 мкг/мл и МИК90 — 0,06 мкг/мл).
*Множественная лекарственная устойчивость (МЛУ) — устойчивость возбудителя к изониазиду и рифампицину и к любому из фторхинолонов, или к любому из инъекционных препаратов второго ряда (но не в комбинации фторхинолонов с инъекционными препаратами второго ряда).
Пре — широкая лекарственная устойчивость (пре — ШЛУ) — устойчивость возбудителя к изониазиду и рифампицину и к любому из инъекционных препаратов второго ряда (но не в комбинации фторхинолонов с инъекционными препаратами второго ряда).
Широкая лекарственная устойчивость (ШЛУ) — устойчивость возбудителя к изониазиду, рифампицину и к любому фторхинолону и к любому инъекционному препарату второго ряда.
Учитывая низкий средний уровень экспозиции у человека (от 23 % до 31 %) и низкую противомикобактериальную активность (в 3-6 раз ниже) по сравнению с исходным веществом, не предполагается, что метаболит N-монодезметил (М2) оказывает значительное воздействие на клиническую эффективность.
Внутриклеточная бактерицидная активность бедаквилина в первичных перитонеальных макрофагах и макрофагоподобных клеточных линиях была выше, чем внеклеточная активность.
Бедаквилин также оказывает бактерицидное воздействие на дремлющие (находящиеся в покое) туберкулезные микобактерии. На мышиной модели, разработанной для изучения туберкулезной инфекции, бедаквилин продемонстрировал бактерицидную и стерилизующую активность.
Бедаквилин обладает бактериостатической активностью в отношении многих нетуберкулезных Бедаквилин обладает бактериостатической активностью в отношении многих нетуберкулезных микобактерий.
Mycobacterium xenopi, Mycobacterium novocastrense, Mycobacterium shimoidei и немикобактериальные виды считаются устойчивыми к действию бедаквилина.
Механизмы развития резистентности
Механизмы, определяющие резистентность Mycobacterium tuberculosis к бедаквилину, включают в себя, по меньшей мере, 6 вариантов мутаций (замены аминокислотной последовательности) гена-мишени atpE, кодирующего АТФ-синтазу-мишень. Вторым механизмом приобретенной резистентности, влияющим на МИК бедаквилина, являются мутации в гене Rv0678, регулирующим экспрессию MmpS5-MmpL5 эффлюксной помпы. Целевые мутации, созданные в ходе доклинических исследований, привели к 8-133-кратному увеличению МИК бедаквилина, в результате чего диапазон МИК составил 0,25 — 4,0 мг/л. Мутации, основанные на активации эффлюксной помпы, наблюдались у штаммов, изученных в рамках доклинических и клинических исследований. Это привело к 2-8-кратному увеличению МИК бедаквилина, в результате чего диапазон МИК составил 0,25 — 0,50 мг/л. Штаммы с эффлюксным механизмом резистентности также менее чувствительны к клофазимину.
Однако четкая взаимосвязь между повышением МИК бедаквилина относительно исходного уровня и микробиологическими результатами клинических исследований, в ходе которых пациенты получали бедаквилин в течение 24 недель с последующей фоновой терапией, выявлена не была.
Предельные значения при проверке чувствительности
Клинические микробиологические лаборатории по необходимости должны предоставлять врачам результаты проверки чувствительности in vitro для противомикробных препаратов, используемых в больницах, в качестве периодических отчетов, описывающих профиль чувствительности нозокомиальных и внебольничных патогенов. Эти отчеты должны способствовать выбору комбинации противомикробных препаратов для проведения терапии. Предельные значения
Предельные значения МИК приведены ниже:
Наивысшее значение МИК в распределении МИК микроорганизмов немутантного типа (ECOFF) — 0,25 мг/л.
Границы классификации устойчивости микроорганизмов:
Ч ≤ 0,25 мг/л;
У > 0,25 мг/л;
Ч = чувствительные;
У = устойчивые.
Фармакокинетика
Оценка фармакокинетических свойств бедаквилина проводилась у взрослых здоровых добровольцев и взрослых пациентов, инфицированных туберкулезом с множественной лекарственной устойчивостью. Экспозиция бедаквилина у пациентов, инфицированных туберкулезом с множественной лекарственной устойчивостью была ниже, чем у здоровых добровольцев.
Всасывание
При пероральном приеме отмечена высокая абсорбция бедаквилина. Максимальная концентрация в плазме (Сmах) достигается приблизительно через 5 часов после приема препарата. Сmах и площадь под кривой «концентрация-время» (AUC) увеличиваются пропорционально возрастанию дозы вплоть до самых высоких исследованных доз (700 мг в сутки однократно и 400 мг в несколько приемов) без изменения времени достижения максимальной концентрации (Тmах) и периода полувыведения (Т1/2). Наибольшая биодоступность достигается при приеме с пищей (до 95 %), которая примерно в 2 раза превышает биодоступность при приеме натощак. Таким образом, для повышения биодоступности бедаквилина препарат следует принимать во время еды.
Распределение
Бедаквилин и его активный метаболит N-монодезметил (М2) характеризуются высоким объемом распределения (примерно 164 л), соотношение концентрации в тканях к концентрации в плазме = 30. Связывание с белками плазмы составляет > 99,9 %. Наивысшие концентрации создаются в легочной ткани, лимфатических узлах, селезенке, почках и печени. Проникновение через гематоэнцефалический барьер незначительно.
Метаболизм
Бедаквилин подвергается метаболизму в первую очередь путем окисления, приводящего к образованию N-монодезметила (М2). Основным изоферментом семейства Р450, участвующим в метаболизме бедаквилина и образовании N-монодезметила (М2) in vitro является CYP3A4.
В исследованиях in vitro бедаквилин не оказывает значимого воздействия на активность известных изоферментов семейства цитохрома Р450 (не ингибирует CYP1A2, CYP2A6, CYP2C8/9/10, CYP2C19, CYP2D6, CYP2E1, CYP3A4, CYP3A4/5, CYP4A и не индуцирует активность CYP1A2, CYP2C9 или CYP2C19).
В исследованиях in vitro бедаквилин и N-монодезметил (М2) не являлись субстратами Р-гликопротеина. Бедаквилин, в отличие от N-монодезметила (М2), представлял собой слабый субстрат OCT1, ОАТР1В1 и ОАТР1ВЗ. Бедаквилин и N-монодезметил (М2) в клинически значимых концентрациях не ингибировали транспортеры P-gp, ОАТР1В1, ОАТР1ВЗ, BCRP, ОАТ1, ОАТ3, OCT1, ОСТ2, МАТЕ1 и МАТЕ2. Было показано, что бедаквилин в концентрациях, достигаемых в кишечнике после перорального применения, может ингибировать BCRP. Клиническая значимость не установлена.
Выведение
Бедаквилин выводится из организма главным образом кишечником. В клинических исследованиях выведение неизмененного бедаквилина почками составило <0,001 % от введенной дозы, что свидетельствует о незначительном почечном клиренсе неизмененного препарата. После достижения Сmах концентрация бедаквилина в плазме снижается три- экспоненциальным образом. Терминальный период полувыведения (Т 1/2 терм) бедаквилина и N-монодезметила (М2) составляет около 5 месяцев (в среднем от 2 до 8 месяцев), что, вероятно, отражает медленное высвобождение бедаквилина и N-монодезметила (М2) из периферических тканей.
Фармакокинетика в различных группах
По результатам популяционного фармакокинетического анализа пациентов, с диагнозом туберкулез легких, не установлено возрастных, половых клинически значимых различий в фармакокинетике бедаквилина.
Этническая принадлежность
По результатам популяционного фармакокинетического анализа пациентов с диагнозом туберкулез легких, получающих лечение препаратом Сиртуро, была установлена более низкая экспозиция бедаквилина у пациентов негроидной расы, по сравнению с пациентами других рас. Описанная пониженная экспозиция не рассматривалась как клинически значимая, в виду отсутствия четкой связи между экспозицией бедаквилина и ответом на терапию. Кроме того, частота положительных ответов у пациентов разных рас, прошедших курс лечения бедакви-лином, была сопоставимой.
Педиатрические пациенты (<18 лет)
Фармакокинетика препарата Сиртуро в педиатрической практике не оценивалась.
Пожилые пациенты (≥ 65 лет)
Данные о фармакокинетике препарата Сиртуро у пациентов, с диагнозом туберкулез легких, в возрасте 65 лет и старше ограничены (n=2).
Исследования фармакокинетических свойств препарата Сиртуро в группе пациентов, инфицированных туберкулезом (возрастной диапазон от 18 до 68 лет), не выявило влияние возраста на фармакокинетические свойства бедаквилина.
Пациенты с недостаточностью функции почек
Препарат Сиртуро исследовали главным образом среди пациентов с нормальной функцией почек. Выведение неизмененного бедаквилина через почки незначительно (<0,001%. По результатам популяционного фармакокинетического анализа пациентов, получавших по 200 мг препарата Сиртуро три раза в неделю, клиренс креатинина (диапазон 40-227 мл/мин) не оказывал влияния на фармакокинетические параметры бедаквилина. Поэтому предполагается, что почечная недостаточность легкой или умеренной степени не будет иметь клинически значимое влияние на фармакокинетику бедаквилина. У пациентов с тяжелой почечной недостаточностью (клиренс креатинина ≤ 30 мл/мин/1,73 м2) или терминальной стадией почечной недостаточности с необходимостью применения гемодиализа или перитонеального диализа концентрация бедаквилина может увеличиваться за счет изменения всасывания, распределения и метаболизма препарата на фоне нарушения функции почек. Так как бедаквилин в значительной степени связывается с белками плазмы, то количество бедаквилина, удаляемого при проведении процедуры гемодиализа или перитонеального диализа будет низкой (см. раздел Способ применения и дозировка, см. раздел Меры предосторожности). Пациенты с недостаточностью функции печени
После однократного приема препарата Сиртуро (400 мг) у 8 пациентов с умеренным нарушением функции печени (класс В по шкале Чайлд-Пью), А11С672 ч для бедаквилина и N- монодезметила (М2) была примерно на 20 % ниже по сравнению со здоровыми добровольцами. Коррекция дозы для пациентов с легким или умеренным нарушением функции печени не требуется. Фармакокинетика бедаквилина у пациентов с тяжелой печеночной недостаточностью не изучалась (см. раздел Способ применения и дозировка, см. раздел Меры предосторожности).
ВИЧ-инфицированные пациенты
Данные о фармакокинетике препарата Сиртуро у ВИЧ-инфицированных пациентов ограничены (см. раздел Меры предосторожности).
С осторожностью
удлинение интервала QT с коррекцией по формуле Фредерика (QTcF) >450 мс (с подтверждением при помощи повторного ЭКГ-исследования);
декомпенсированная сердечная недостаточность;
у пациентов с личным или семейным анамнезом врожденного удлинения интервала QT, или с развитием аритмии по типу «torsade de pointes»;
у пациентов с брадиаритмией, в том числе в анамнезе;
у пациентов с электролитными нарушениями (гипокальциемия, гипомагниемия, гипокалиемия);
у пациентов с гипотиреозом, в том числе в анамнезе;
одновременное применение с препаратами, удлиняющими интервал QT (в частности с антибиотиками группы фторхинолонов: с гатифлоксацином, моксифлоксацином, спарфлоксацином);
совместное применение с лопинавиром/ритонавиром;
у больных пожилого возраста (65 лет и старше) (см. раздел Особые группы пациентов).
Препарат Сиртуро показан к применению у взрослых (≥ 18 лет) в составе комбинированной терапии туберкулеза легких, вызванного штаммами Mycobacterium tuberculosis с множественной лекарственной устойчивостью.
Препарат следует использовать в случае, когда не может назначен другой эффективный режим терапии при устойчивости возбудителя или непереносимости препаратов.
Применение в период беременности и грудного вскармливания
Беременность
Безопасность препарата Сиртуро при беременности не установлена, поэтому препарат противопоказан к применению у беременных женщин.
Период лактации
Данных о выделении бедаквилина или его метаболитов с грудным молоком нет.
Данные о применении бедаквилина у женщин в период лактации отсутствуют, поэтому применение препарата в период грудного вскармливания противопоказано.
Способ применения и дозировка
Лечение должно осуществляться под непосредственным наблюдением специалиста, имеющего опыт лечения МЛУ туберкулеза.
Препарат Сиртуро необходимо применять в комбинации с не менее чем 3 препаратами, к которым in vitro доказана чувствительность штамма, выделенного у пациента.
Если результаты исследования лекарственной устойчивости отсутствуют (in vitro), препарат Сиртуро необходимо применять в комбинации с 4 другими препаратами, к которым возможно сохранена чувствительность штамма Mycobacterium tuberculosis, выделенного у пациента. Терапию следует продолжать после отмены препарата Сиртуро, соответственно стандартам лечения туберкулеза с множественной лекарственной устойчивостью. На протяжении курса лечения Сиртуро и после последнего приема препарата необходимо продолжать терапию противотуберкулезными препаратами в соответствии со стандартными режимами химиотерапии МЛУ ТБ. При выборе схемы и продолжительности приема противотуберкулезных препаратов резерва в составе комбинированной терапии лечащий врач должен руководствоваться государственными стандартами лечения туберкулеза, данными о лекарственной устойчивости микобактерий по региону с учетом лекарственной чувствительности штамма, выделенного от больного туберкулезом и данных клинико-рентгенологического обследования.
Препарат Сиртуро рекомендуется принимать внутрь во время еды, так как одновременный прием с пищей увеличивает биодоступность препарата (см. раздел Фармакокинетика). Таблетку препарата Сиртуро рекомендуется проглатывать целиком, запивая водой. Рекомендуемый режим дозирования препарата Сиртуро:
1-2 неделя: 400 мг (4 таблетки по 100 мг) 1 раз в день;
3-24 неделя: 200 мг (2 таблетки по 100 мг) 3 раза в неделю, с перерывом не менее 48 часов между приемом препарата.
Общая продолжительность курса лечения препаратом Сиртуро составляет 24 недели.
Данных по применению препарата Сиртуро с большей продолжительностью для лечения туберкулеза недостаточно.
У пациентов с широкой лекарственной устойчивостью продолжительность лечения с препаратом Сиртуро может быть увеличена только в индивидуальном порядке и при условии контроля за безопасностью терапии (побочными реакциями) (см. раздел Побочные действия). Пациенты должны быть предупреждены о необходимости приема препарата Сиртуро в соответствии с указаниями врача. Необходимо подчеркнуть важность приема полного курса терапии.
При пропуске приема препарата в течение первых 2 недель лечения пропущенную дозу принимать не следует. Необходимо продолжать прием в обычном режиме.
При пропуске суточной дозы препарата, начиная с 3-й недели (200 мг в сутки, 3 раза в неделю), следует принять пропущенную дозу как можно раньше, а затем продолжить прием в обычном режиме (3 раза в неделю). Учитывая при этом, что перерыв между дозами должен быть не менее 24 часов, а суммарная доза за 7 дней не должна превышать 600 мг.
Особые группы пациентов
Педиатрические пациенты (<18 лет)
Безопасность и эффективность препарата Сиртуро у детей и подростков моложе 18 лет не установлены (см. раздел Меры предосторожности).
Пожилые пациенты (≥ 65 лет)
Данные о применении препарата Сиртуро у пожилых пациентов (n=2) ограничены (см. раздел Меры предосторожности).
Пациенты с почечной недостаточностью
Исследования препарата Сиртуро проводили, главным образом, среди пациентов с нормальной функцией почек. Для пациентов с легкой или умеренной почечной недостаточностью коррекция дозы не требуется. Пациентам с тяжелой почечной недостаточностью (клиренс креатинина <30 мл/мин) или терминальной стадией почечной недостаточности, требующей гемо- или перитонеального диализа, препарат Сиртуро применять не рекомендовано (см. раздел Меры предосторожности).
Пациенты с печеночной недостаточностью
Фармакокинетические свойства бедаквилина оценивали в исследованиях однократного приема у пациентов с умеренной печеночной недостаточностью (класса В по шкале Чайлд-Пью) (см. раздел Фармакокинетика).
У пациентов с легкой или умеренной печеночной недостаточностью изменения в режиме дозирования препарата Сиртуро не требуется. У пациентов с тяжелой печеночной недостаточностью эффективность и безопасность бедаквилина не изучена и применять препарат Сиртуро в данной группе пациентов не рекомендовано (см. раздел Меры предосторожности). ВИЧ-инфицированные пациенты
Данные о применении препарата Сиртуро у ВИЧ-инфицированных пациентов ограничены (см. раздел Меры предосторожности).
Пациенты с внелегочным туберкулезом
У пациентов с поражением центральной нервной системы и при костно-суставной форме туберкулеза эффективность и безопасность препарата не изучена.
Пациенты с инфекцией, вызванной другими штаммами микобактерий (не Mycobacterium tuberculosis)
Клинические данные по использованию препарата Сиртуро отсутствуют.
Препараты с латентной инфекцией, вызванной Mycobacterium tuberculosis Клинические данные по использованию препарата Сиртуро отсутствуют.
Побочные действия
Нежелательные побочные реакции на препарат Сиртуро были определены на основании объединенных данных (335 пациентов), получавших препарат Сиртуро в составе комбинированного режима противотуберкулезной терапии в проведенных контролируемых и неконтролируемых клинических исследованиях. Наиболее частыми побочными реакциями (>10,0 % пациентов) во время лечения были: тошнота (35,3 % в группе Сиртуро и 25,7 % в группе плацебо), боль в суставах (29,4 % и 20,0 % соответственно), головная боль (23,5 % и 11,4 %), рвота (20,6 % и 22,9 %) и головокружение (12,7 % и 11,4 % соответственно в группе Сиртуро и группе плацебо).
В контролируемом исследовании побочные реакции в схеме лечения с Сиртуро были зафиксированы у 102 пациентов.
Нежелательные реакции на препарат Сиртуро перечислены в соответствии с системами классов органов и частотой развития (очень часто (≥ 1 /10), часто (≥ 1/100 до < 1/10), реже (≥ 1/1000 до < 1/100), редко (≥ 1/10000 до < 1/1000), очень редко (< 1/10000)):
Нарушения со стороны нервной системы (ЦНС): очень часто — головная боль, головокружение;
Нарушения со стороны сердечно-сосудистой системы: часто — удлинение интервала Q1 на ЭКГ;
Нарушения со стороны желудочно-кишечного тракта: очень часто — тошнота, рвота; часто — диарея;
Нарушения со стороны печени и желчевыводящих путей: часто — повышение активности трансаминаз (аланинаминотрансфераза (АЛТ), аспартатаминотрансфераза (ACT));
Нарушения со стороны скелетно-мышечной и соединительной ткани: очень часто – боль в суставах, часто — боль в мышцах.
гиперчувствительность к бедаквилину и/или любому другому компоненту препарата;
беременность;
период лактации (грудное вскармливание);
детский и подростковый возраст до 18 лет;
тяжелая почечная недостаточность (клиренс креатинина ≤ 30 мл/мин/1,73 м2);
тяжелая печеночная недостаточность (в связи с отсутствием клинических данных по безопасности препарата в этой группе);
врожденная непереносимость лактозы, дефицит лактазы, глюкозо-галактозная мальабсорбция.
Информация о случаях намеренной или случайной острой передозировки бедаквилином отсутствует. В исследовании с участием 44 здоровых добровольцев, получавших однократно 800 мг препарата Сиртуро, побочные реакции соответствовали тем, которые наблюдались при приеме рекомендуемой дозы (см. раздел Побочные действия).
Лечение. Опыт лечения острой передозировки препаратом Сиртуро отсутствует. В случае преднамеренной или случайной передозировки следует принимать общие меры поддержания основных жизненно важных функций и проводить ЭКГ-мониторинг интервала QT. Не абсорбировавшийся бедаквилин может быть удален при приеме активированного угля. Так как бедаквилин в значительной степени связывается с белками, эффективность диализа для удаления бедаквилина из плазмы будет низкой. По возможности следует продолжать клиническое наблюдение за пациентом.
Лечение должно осуществляться под непосредственным наблюдением специалиста.
Штаммы Micobacterium tuberculosis выделенные от пациента, у которого не произошла конверсия мокроты на фоне терапии или отмечен случай рецидива после завершения лечения, должны быть исследованы на чувствительность к бедаквилину (МИК).
Влияние на летальность
В рандомизированном клиническом исследовании 2 фазы (С208, стадия 2) было отмечено увеличение уровня летальности в группе Сиртуро (12,7 %, 10/79), по сравнению с группой плацебо (3,7%, 3/81). В группе Сиртуро во всех 5 случаях смерти от туберкулеза не достигнута конверсия мокроты при последнем обследовании. В остальных случаях, причины смерти в группе Сиртуро были алкогольное отравление, гепатит/цирроз печени, септический шок, перитонит, нарушение мозгового кровообращения, дорожно-транспортное происшествие. Один случай смерти из 10 в группе Сиртуро наступил в период первых 24 недель терапии. Остальные 9 случаев летальности у пациентов в группе Сиртуро произошли после окончания приема препарата Сиртуро (в диапазоне 86-911 дней, медиана времени развития смерти составила 344 дня после приема последней дозы). Наблюдаемый дисбаланс летальности между двумя группами необъясним. Значимой корреляции между летальностью и конверсией мокроты, рецидивом, данными чувствительности к другим противотуберкулезным препаратам, ВИЧ-статусом, или тяжестью заболевания не выявлено.
Во время клинического исследования у пациентов, которые умерли, не наблюдалось значительного удлинения интервала QTc или клинически значимых аритмий.
В открытом исследовании 2 фазы (С209) 16 из 233 (6,9 %) пациентов умерли, у 9 пациентов причина смерти туберкулез, из них 8 пациентов имелся риск развития неблагоприятной динамики или рецидив процесса. В остальных случаях смерть была от других причин.
Влияние на удлинение интервала QT
В контролируемом исследовании 2 фазы наблюдалось среднее увеличение QT, с коррекцией по формуле Фредерика (QTcF), начиная с 1 недели терапии (в группе Сиртуро — на 9,9 мс и на 3,5 мс в группе плацебо). Наибольшее увеличение среднего значения QTcF в течение 24 недель терапии наблюдалось на 18-й неделе и составило 15,7 мс в группе приема препарата Сиртуро в сравнении с 6,2 мс в группе плацебо. После окончания приема препарата Сиртуро (т.е. после 24-й недели) интервал QTcF не достиг нормальных величин в данной группе.
В открытом исследовании 2 фазы (С209) у пациентов, в схеме лечения которых были другие противотуберкулезные препараты, влияющие на удлинение интервала QTcF, включая клофазимин, наблюдается увеличение интервала пропорционально количеству препаратов в схеме лечения.
У пациентов, в схеме лечения которых был только Сиртуро, как препарат влияющий на удлинение интервала QTcF, максимально увеличение интервала составляло 23,7 мс и не превышало 480 мс. У пациентов, имеющих по крайней мере два препарата в схеме лечения с побочным действием на интервал QTcF, отмечалось максимальное увеличение интервала на 30,7 мс, удлинение интервала свыше 500 мс наблюдалось у одного пациента.
Случаи развития полиморфной желудочковой тахикардии «torsade de pointes» не зарегистрированы. Данные об изменении интервала QTcF при совместном применении бедаквилина и клофазимина см. в разделе Взаимодействие с другими лекарственными средствами.
В ходе клинических исследований не отмечено четкой корреляции клинически значимого удлинения интервала QT или нарушений сердечного ритма среди пациентов с летальным исходом (см. разделы Побочные действия, Взаимодействие с другими лекарственными средствами).
Перед началом терапии препаратом Сиртуро и затем ежемесячно необходимо проведение ЭКГ-исследования для динамического контроля за интервалом QTcF.
Перед началом терапии препаратом Сиртуро необходимо провести оценку концентрации калия, магния и кальция сыворотки крови и скорректировать показатели в случае отклонения от нормальных значений. Последующий мониторинг электролитов рекомендуется проводить ежемесячно.
Начало терапии препаратом Сиртуро не рекомендуется у пациентов со следующими состояниями, за исключением случаев, когда преимущества применения препарата превышают потенциальные риски:
интервал QT с коррекцией по формуле Фредерика (QTcF) >450 мс (с подтверждением при помощи повторного ЭКГ-исследования);
декомпенсированная сердечная недостаточность;
личный или семейный анамнез врожденного удлинения интервала QT или развитие аритмии по типу «torsade de pointes»;
брадиаритмия, в том числе в анамнезе;
электролитные нарушения (гипокальциемия, гипомагниемия, гипокалиемия);
гипотиреоз, в том числе в анамнезе;
совместное применение с антибиотиками группы фторхинолонов, вызывающими значительное удлинение интервала QT (например, гатифлоксацин, моксифлоксацин. спарфлоксацин).
Отсутствуют данные по применению препарата Сиртуро у пациентов с желудочковыми аритмиями и инфарктом миокарда в анамнезе.
Терапию препаратом Сиртуро и любыми другими препаратами удлиняющими интервал QT следует прекратить, если у пациента развиваются клинически значимая желудочковая аритмия или интервал QT с коррекцией по формуле Фредерика (QTcF) > 500 мс (с подтверждением при помощи повторного ЭКГ-исследования). Следует проводить частый ЭКГ мониторинг до тех пор, пока значение интервала QT не вернется к норме. В случае развития приступа кратковременной потери сознания, необходимо проведение ЭКГ исследования для подтверждения удлинения интервала QT.
При совместном применении бедаквилина с препаратами, вызывающими удлинение интервала QT (в частности с антибиотиками группы фторхинолонов, макролидов, клофазимином), следует проявлять осторожность, так как нельзя исключать аддитивный или синергетический эффект, который может приводить к значительному удлинению интервала QT. В случае, если совместное применение таких лекарственных препаратов с бедаквидином необходимо, рекомендуется клиническое наблюдение пациента, в том числе регулярный мониторинг ЭКГ (см. раздел Взаимодействие с другими лекарственными средствами).
Совместное применение с индукторами/ингибиторами CYP3A4
Следует избегать совместного применения бедаквилина и антибиотиков группы рифампицина (рифампицин, рифапентин и рифабутин) или других умеренных или мощных индукторов CYP3A4, назначаемых системно, так как возможно снижение его терапевтического действия (см. раздел Взаимодействие с другими лекарственными средствами).
Следует избегать одновременного приема бедаквилина с умеренными или сильными ингибиторами CYP3A4, назначаемыми системно, более 14 дней подряд, так как возможно увеличение времени терапевтического действия бедаквилина и риска возникновения нежелательных реакций. В случае необходимости более длительного (≥ 14 суток) приема ингибиторов CYP3A4 с препаратом Сиртуро следует оценивать отношение риска к пользе такой комбинации препаратов и адекватный мониторинг возможных нежелательных реакций связанных с применением Сиртуро.
Следует назначать препарат Сиртуро совместно с лопинавиром/ритонавиром с осторожностью — только после оценки отношения риска к пользе такой комбинации препаратов и при регулярном мониторинге возможных нежелательных реакций связанных с применением Сиртуро.
Влияние на функцию печени
На фоне терапии Сиртуро (в комбинации с другими противотуберкулезными препаратами) в клинических исследованиях отмечены более частые побочные реакции со стороны печени в сравнении с комбинированным режимом терапии противотуберкулезными препаратами без добавления Сиртуро (плацебо): в клиническом исследовании С208 (стадия 1 и 2) увеличение активности аминотрансфераз в крови более чем в 3 раза выше верхней границы нормы встречалось чаще в группе Сиртуро 11/102 (10,8 %), чем в группе плацебо 6/105 (5,7 %). В группе Сиртуро большинство случает было зарегистрировано в период первых 24 недель терапии и данные случаи были обратимыми.
Во 2 стадии исследования С208 повышение активности аминотрансфераз в крови наблюдалось у 7/79 (8,9 %) пациентов в группе Сиртуро, и у 1/81 (1,2 %) пациентов в группе плацебо (см. раздел Побочные действия). В связи с этим, следует проводить мониторинг клинического состояния пациента и биохимический анализ крови с определением активности «печеночных» ферментов (АЛТ, ACT) и показателей холестаза (уровень щелочной фосфатазы, билирубина) перед началом терапии препаратом Сиртуро, ежемесячно в процессе лечения и при необходимости чаще.
У пациентов, принимающих препарат Сиртуро, при появлении ранее не документированных клинически значимых изменений функциональных показателей работы печени или дальнейшее ухудшение ее функции (оцененной по уровню ACT, АЛТ и/или билирубина;, а так же наличие клинических симптомов (таких как усталость, анорексия, тошнота, желтуха, потемнение мочи, гепатомегалия) необходимо особо тщательное наблюдение за вольным и следовать алгоритму купирования побочных реакций.
Если активность аминотрансфераз (АЛТ, ACT) превышает верхний предел нормы в 5 раз, то необходимо пересмотреть режим терапии и прекратить прием Сиртуро и/или прием гепатотоксичных лекарственных препаратов.
В период применения препарата Сиртуро следует избегать приема алкоголя и препаратов, обладающих гепатотоксическим эффектом.
Отсутствует опыт совместного применения антиретровирусных препаратов и препарата Сиртуро у ВИЧ-инфицированных пациентов с МЛУ ТБ, и имеются ограниченные клинические данные об использовании препарата Сиртуро у пациентов (n=22) с ВИЧ-инфекцией и МЛУ ТБ, не принимающих антиретровирусной терапии. У пациентов, участвовавших в исследовании, количество CD4+ клеток превышало значение 250*106 клеток/л.
Пациентам различных этнических групп коррекции дозы препарата не требуется.
Непереносимость лактозы, дефицит лактазы
Препарат Сиртуро содержит лактозу. Пациенты с наследственной непереносимостью галактозы, лактазной недостаточностью или глюкозо-галактозной мальабсорбцией не должны принимать данное лекарственное средство.
Влияние на способность управлять автотранспортом и другими механизмами
При возникновении побочных реакций со стороны ЦНС на фоне применения препарата пациентам рекомендуется воздержаться от управления автотранспортом и занятий другими потенциально опасными видами деятельности, требующих повышенной концентрации внимания, быстроты психомоторных и двигательных реакций.
Бедаквилин in vitro не оказывает значимого воздействия на активность известных изоферментов семейства цитохрома Р450 (см. Метаболизм).
Бедаквилин и N-монодезметил (М2) не являются субстратами или ингибиторами Р-гликопротеина.
CYP3A4 является основным изоферментом семейства цитохрома Р450, принимающим участие в метаболизме бедаквилина и образовании N-монодезметила (М2) in vitro. Поэтому содержание бедаквилина в плазме крови может уменьшиться при совместном применении с индукторами CYP3A4 и увеличиться при совместном назначении с ингибиторами CYP3A4.
Антибиотики группы рифампицина и другие индукторы CYP3A4
Экспозиция бедаквилина может снизиться при совместном применении с индукторами CYP3A4.
В исследовании лекарственного взаимодействия бедаквилина (300 мг однократно) и рифампицина (по 600 мг в сутки 21 день) у здоровых добровольцев AUC бедаквилина снизилась на 52 %. В связи с возможностью уменьшения терапевтического эффекта бедаквилина по причине снижения его системного действия, следует избегать совместного применения бедаквилина и антибиотиков группы рифампицина (рифампицин, рифапентин и рифабутин) или других умеренных или мощных индукторов CYP3A4, назначаемых системно (эфавиренз, этравирин, карбамазепин, фенитоин, Зверобой продырявленный (Hypericum perforatum)) (см. раздел Меры предосторожности).
Кетоконазол и другие ингибиторы CYP3A4
Экспозиция бедаквилина может повыситься при совместном применении с ингибиторами CYP3A4.
При совместном применении кетоконазола (по 400 мг 4 суток) и бедаквилина (по 400 мг в сутки в течение 14 дней) у здоровых добровольцев AUC бедаквилина увеличилась на 22 %, Стах И Cmin на 9 % и 33 %, соответственно. В связи с потенциальным риском возникновения нежелательных реакций за счет увеличения терапевтического действия бедаквилина, следует избегать длительного совместного применения (более 14 дней) бедаквилина с умеренными или мощными ингибиторами CYP3A4 (ципрофлоксацин, эритромицин, флуконазол, кларитромицин, кетоконазол, ритонавир), назначаемыми системно. В случае необходимого совместного применения рекомендуется более частый мониторинг ЭКГ и активности «печеночных» трансаминаз (см. раздел Меры предосторожности).
Другие противотуберкулезные препараты
Совместное применение бедаквилина (400 мг в сутки) с изониазидом (300 мг в сутки 5 дней)/пиразинамидом (1000 мг в сутки 5 дней) у здоровых добровольцев в течение 14 суток не вызвало клинически значимых изменений AUC бедаквилина, изониазида или пиразинамида. При совместном применении препарата Сиртуро с изониазидом или пиразинамидом коррекции дозы не требуется. В плацебо-контролируемом клиническом исследовании у пациентов с МЛУ ТБ не наблюдалось значительного влияния препарата Сиртуро на фармакокинетику этамбутола, канамицина, пиразинамида, офлоксацина или циклосерина для их совместном применении.
Антиретровирусные препараты
В исследовании лекарственного взаимодействия между бедаквилином (400 мг однократно) и препаратом лопинавир (400 мг)/ритонавир (100 мг) в режиме приема 2 раза в сутки в течение 24 дней у здоровых добровольцев AUC бедаквилина возросла на 22 %. При более длительном совместном применении, влияние на AUC бедаквилина может быть более выраженным. Увеличение данного параметра, вероятно, связано с ритонавиром. Следует назначать препарат Сиртуро совместно с препаратом лопинавир/ритонавир с осторожностью только после оценки отношения риска к пользе такой комбинации препаратов (см. раздел Меры предосторожности).
Увеличение экспозиции бедаквилина в плазме следует ожидать при совместном назначении с другими ритонавирбустированными ингибиторами протеазы ВИЧ.
Совместное применение невирапина (200 мг 2 раза в сутки 4 недели) с бедаквилином (400 мг однократно) не вызывало клинически значимых изменений содержания бедаквилина в плазме крови.
Клинические данные по совместному применению антиретровирусных препаратов и препарата Сиртуро у ВИЧ-инфицированных пациентов с МЛУ ТБ отсутствуют (см. раздел Меры предосторожности).
Эфавиренз является умеренным индуктором активности СУРЗА, и его совместное применение с бедаквилином может привести к снижению AUC бедаквилина и потере активности, и, следовательно, не рекомендуется.
Препараты, удлиняющие интервал QT
Информация о возможном фармакодинамическом взаимодействии между бедаквилином и препаратами, удлиняющими интервал QT, ограничена.
Наблюдался аддитивный или синергический эффект в отношении удлинения интервала QT при совместном применении бедаквилина с препаратами, которые удлиняют интервал QT. В клиническом исследовании лекарственного взаимодействия кетоконазола и бедаквилина после повторного совместного приема препаратов наблюдалось более значительное влияние на QTc, чем после повторного приема каждого из этих препаратов по отдельности.
В открытом исследовании 2 фазы отмечается удлинение интервала QT у 17 пациентов при добавлении в схему лечения клофазимина 24 недели (на 31,9 мс), по сравнению с пациентами, в схеме которых не использовался клофазимин (на 12,3 мс).
Педиатрические пациенты
Исследования лекарственного взаимодействия проводились только для взрослых пациентов.
При температуре не выше 25 °C.
Хранить в оригинальной упаковке в защищенном от света месте:
Хранить в недоступном для детей месте.
2 года. Не применять после истечения срока годности.
По 188 таблеток во флакон из полиэтилена высокой плотности, укупоренный полипропиленовой крышкой с системой защиты от вскрытия детьми и контролем первого вскрытия.
По 1 флакону вместе с инструкцией по медицинскому применению в картонную пачку.
Производитель
ОАО «Фармстандарт-УфаВИТА»
Россия, 450077, г. Уфа, ул. Худайбердина, д. 28,
телефон/факс (347) 272 92 85, .
Владелец регистрационного удостоверения/организация, принимающая претензии потребителей:
ОАО «Фармстандарт-УфаВИТА»
Россия, 450077, г. Уфа, ул. Худайбердина, д. 28,
телефон/факс (347) 272 92 85, .

Товары из категории — Противовирусные препараты
Инструкция по применению
Цена в интернет-аптеке WER.RU: от 60 000
Фармакологические свойства
Сиртуро содержит основное вещество бедаквилина. Оно принадлежит к классу материалов, обладающих анти туберкулёзным качеством. Препарат характеризуется бактерицидным свойством. Его действие обусловлено влиянием компонентов на фермент, который непосредственно участвует в дыхании клеточной организации Mycobacterium tuberculosis. В результате нарушается воспроизводство энергии структуры, и она погибает.
При воздействии медикамента на патогены возможно возникновение 6 видов мутаций. Если вводить препарат в минимальных дозировках, то увеличивается риск развития устойчивости бактериальной формы к химвеществу. При введении большего количества продукта возникает бактерицидный эффект.
Состав и упаковка выпуска
Сиртуро выпускается в таблетированной форме. Цветовые оттенки – белые. В структуру продукта входит соединение бедаквилина фумарата. Дополнительными элементами, усиливающими действенность таблеток, считаются – крахмал кукурузный, полисорбат, магния стеарат, лактозы моногидрат и другие компоненты.
Показания к применению
Назначается продукт для лечения туберкулеза легких, который спровоцирован агентами Mycobacterium tuberculosis, резистентными к множеству оздоравливающих средств, в комбинации с другими фармакологическими изделиями.
Международная классификация болезней (МКБ-10)
J04AK Противотуберкулезные препараты другие.
Побочные эффекты
После приема таблеток могут регистрироваться акцидентные признаки в виде кружения головы, поноса, болезненного синдрома в мышечных структурах; суставах, анорексии, накожных высыпаний, тошноты; рвотных рефлексов. Замечено воздействие медикамента на ССС и функционирование печеночной организации, желчевыводящих проходов. При возникновении подобных вторичных симптомов следует немедленно обратиться к доктору. Он изменит схему терапии, или же отменит терапевтическое средство. Применение таблеток должно предваряться медицинским обследованием.
Противопоказания к применению
Сиртуро запрещено принимать при наличии повышенной сенсибилизации к некоторым химкомпонентам продукта, беременности, во время лактационного периода; при недостаточной работе печени и почек; непринятии лактозы, нехватке лактазы и некоторых других дисфункциях. Таблетки не выписывают детям до достижения ними совершеннолетнего возраста.
Ученые и врачи рекомендуют осуществлять применение препарата с внимательностью при дисфункциях сердечной деятельности, недостаточной работе сердца (декомпенсированный тип), брадикардии. С осторожностью принимают вещество при гипокальциемии, гипокалиемии, гипотиреозе. Больной должен находиться под особым контролем врача, если ему больше 65 лет, при проведении параллельной терапии лопинавиром.
Применение при беременности
Как воздействует Сиртуро на организм женщины, вынашивающей плод, неизвестно. Поэтому таблетки при беременности не выписывают. То же самое касается влияния лекарства на процесс лактации. Назначение вещества во время грудного вскармливания запрещено.
Способ и особенности применения
Средство вводят в середину. Использовать его желательно во время принятия пищи. Таким образом, увеличивается биодоступность медикамента. В инструкции указывается на необходимость проглатывать таблетку целиком, запивать жидкостью. Продукт эффективен в комбинированном составе – не менее 3 препаратов. В процессе использования изделия больной должен постоянно наблюдаться в медцентре. Курс терапевтического воздействия составляет 24 недели. При назначении средства доктор обязан руководствоваться госстандартами терапии туберкулеза.
На протяжении первых 14 дней лечения выписывают 400 мг вещества 1 раз в 24 часа. Следующие недели продукт необходимо принимать по 200 мг 3 раза в 7 дней. При этом надо сделать перерыв не менее 48 часов.
Инструкция по применению предупреждает о невозможности назначения препарата детям. Причиной запрета оказывается отсутствие данных по фармакокинетическому воздействию активного вещества на молодой организм. Лицам преклонного возраста средство назначают с осторожностью, поскольку опыт использования его в медицинской практике достаточно ограничен.
В тестировании лекарства участвовали здоровые добровольцы, у которых проблемы с почечной организацией и системой мочевыделения отсутствовала. Установлено, что при легкой и средней тяжести почечной дисфункции необходимость в проведении процедуры титрования дозировок отсутствует. Для людей с тяжелыми нарушениями деятельности почек, и которые находятся на гемодиализе, лучшим вариантом станет полный отказ от применения медикамента.
Больные, страдающие легкой или умеренной деструкцией гепатобилиарной системы, участвовали в тестировании бедаквилина и определении его влияния на состояние здоровья пациентов. По итогам эксперимента сделан вывод о том, что изменение схемы лечения не целесообразно. Пациентам же с тяжелыми поражениями печени и желчевыводящих протоков от назначения вещества лучше воздержаться. Правило запрета относится и к ВИЧ-инфицированным людям.
Взаимодействие с другими лекарствами
В опытах, проведенных на специальных стендах вне живого организма высших млекопитающих, доказано, что бедаквилин не имеет существенного воздействия на тонус ферментов группы цитохромов. С одними из них активный компонент Сиртуро увеличивает свою плотность в кровяной плазме, с другими — уменьшает. Поэтому при совместном назначении медикаментов дозировки и схемы введения устанавливать имеет право только профильный доктор.
Антибактериальные средства и другие активаторы класса рифампицина при взаимодействии с исходным средством приводили к снижению его содержания наполовину. По этой причине и, чтобы не допустить уменьшения системного влияния лечебного эффекта, нельзя допускать комбинацию этих двух групп медикаментов.
Умеренные и сильнодействующие ингибиторы цитохромов при одновременном приеме с Сиртуро увеличивали максимальную концентрацию последнего в сыворотке крови на треть, а суммарную плотность — почти на 22%. Поэтому недопустимо применять оба вида лекарств вместе на протяжении длительного времени, более 14 суток подряд.
Антиретровирусные препараты, например, в виде лопинавира, вводимые наряду с бедаквилином на протяжении 24 суток в режиме 400 мг однократно по 2 раза в день, вызывали повышение в крови уровня бедаквилина почти на четверть. Поэтому их совместное использование должно быть оценено врачом для исключения развития нежелательных реакций.
Прием препаратов, удлиняющих промежуток QT, совместно с Сиртуро, имеет ограниченный опыт.
Передозировка
Сведения о приеме овердоз лекарства в официальной статистке отсутствуют. Проводились эксперименты, в которых участвовали здоровые добровольцы. Им предлагалось к употреблению однократная доза — 800 мг химизделия. Акцидентные явления после этого соответствовали тем, которые возникают и после введения оптимальной дозировки.
При передозировке терапевтические мероприятия заключаются в проведении процедур, поддерживающих основные жизненные параметры. Обязательно необходимы показатели ЭКГ с мониторингом интервала QT. Поскольку активный компонент ввязывается с протеинами крови, гемодиализ признан малоэффективным. Основное лечение — своевременное промывание пищеварительной биосистемы и прием активированного угля.
Аналоги
Препаратами, схожими по терапевтическому воздействию с лекарством, считаются — Локсидон, Перхлозон, Пиразинамид и другие.
Условия реализации
Сиртуро отпускается в соответствии с рецептом доктора.
Условия хранения
Продукт рекомендуется содержать в месте, недоступном для несовершеннолетних лиц. Температурный режим не должен превышать 25° С.
Цены на Сиртуро в Москве
Заберите заказ в в аптеке
WER (г. Москва)
Цена: от 60 000 руб.
Сертификаты и лицензии
- Инструкция по применению Сиртуро
- Состав препарата Сиртуро
- Показания препарата Сиртуро
- Условия хранения препарата Сиртуро
- Срок годности препарата Сиртуро
Форма выпуска, состав и упаковка
таб. 100 мг: 188 шт.
Рег. №: 10672/18 от 21.11.2018 — Действующее
Таблетки белого или почти белого цвета, круглые, двояковыпуклые, с выдавленной надписью «Т» над «207» на одной стороне и «100» на другой стороне.
| 1 таб. | |
| бедаквилина фумарата | 120.89 мг, |
| что соответствует содержанию бедаквилина | 100 мг |
Вспомогательные вещества: лактозы моногидрат — 152.91 мг, крахмал кукурузный — 66 мг, гипромеллоза 2910, 15 мПа·с (Е464) — 8 мг, полисорбат 20 (Е432) — 1 мг, целлюлоза микрокристаллическая (Е460) — 82.2 мг, кроскармеллоза натрия (Е466) — 23 мг, кремния диоксид коллоидный (Е551) — 1.4 мг, магния стеарат — 4.6 мг.
188 шт. — флаконы (1) — пачки картонные.
Реклама