Состав вакцины
Состав Гам-КОВИД-Вак указан на одну дозу, которая составляет 0.5 мл.
Компонент 1 содержит:
- активное вещество: рекомбинантные аденовирусные частицы 26 серотипа, в которых содержится ген белка S вируса SARS-CoV-2, по 1 x 1011 частиц с погрешностью 0.5 x 1011 частиц;
- вспомогательные компоненты: магния хлорида гексагидрат (102 мкг), трис(гидроксиметил)аминометан (1.21 мг), сахароза (25 мг), хлорид натрия (2.19 мг), ЭДТА динатриевая соль дигидрат (19 мкг), вода для инъекции (до 0.5 мл), этанол 95% (2.5 мкл), полисорбат 80 (250 мкг).
Компонент 2 содержит:
- активное вещество: аденовирусные рекомбинантные частицы 5 серотипа, которые содержат ген белка S вируса SARS-CoV-2, по 1 x 1011 частиц в дозе с погрешностью 0.5 x 1011 частиц;
- вспомогательные вещества те же, что в первом компоненте.
В составе Гам-КОВИД-Вак-Лио содержится аналогичное количество активного компонента и вспомогательные элементы: магния хлорида гексагидрат (20.4 мкг), трис(гидроксиметил)аминометан (0.24 мг), сахароза (73.5 мг), хлорид натрия (1.4 мг), ЭДТА динатриевая соль дигидрат (3.8 мкг), полисорбат 80 (0.05 мг).
Производители
На данный момент известны следующие производители Гам-КОВИД-Вак:
- ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России;
- АО «Биннофарм»;
- АО «ГЕНЕРИУМ»;
- АО «Р-Фарм»;
- ЗАО «БИОКАД»;
- ЗАО «ЛЕККО»;
- ОАО «Фармстандарт-УфаВИТА».
Владельцем регистрационного удостоверения на производство вакцины Спутник V является ФГБУ «Национальный исследовательский центр микробиологии и эпидемиологии им. почетного академика Н.Ф. Гамалеи» Мин. здравоохранения РФ.
Когда вакцина зарегистрирована?
Вакцина от коронавируса Гам-КОВИД-Вак была зарегистрирована 11 августа 2020 года.
Форма выпуска
Препарат Гам-КОВИД-Вак (Спутник V) выпускают в форме раствора для внутримышечного введения из двух компонентов, по 0.5 мл раствора каждого компонента на 1 дозу.
Замороженный препарат
Оба компонента препарата в виде замороженного раствора — беловатая твердая плотная масса. После разморозки — однородный раствор, бесцветный или слегка желтоватый.
Производство ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи»:
- Препарат во флаконах, закрытых резиновой пробкой, обжатый алюмопластиковым колпаком. По 0.5 мл (1 доза) каждого компонента во флаконе. Флакон каждого компонента вместе с инструкцией помещен в пачку из картона.
Производство АО «Биннофарм»:
- Препарат в прозрачных ампулах с цветной точкой. По 0.5 мл (1 доза) каждого компонента в ампуле. По 5 ампул каждого компонента помещены в ячейковую контурную упаковку из поливинилхлоридной пленки, по 1 ячейковой упаковке вместе с инструкцией в картонной пачке.
Производство АО «ГЕНЕРИУМ» и ЗАО «ЛЕККО»:
- Препарат во флаконах, закрытых резиновой пробкой, обжатый алюмопластиковым колпаком с контролем первого вскрытия. По 3 мл (5 доз) каждого компонента во флаконе. Флакон каждого компонента вместе с инструкцией помещен в пачку из картона.
Производство ЗАО «БИОКАД»:
- Препарат во флаконах, закрытых резиновой пробкой, обжатый алюминиевым колпаком с пластиковой крышкой типа «flip-off». По 3 мл (5 доз) или по 0.5 мл (1 доза) каждого компонента во флаконе. Флакон 6R каждого компонента вместе с инструкцией помещен в пачку из картона. Флакон 2R каждого компонента в контурной ячейковой упаковке из ПВХ пленки вместе с инструкцией помещен в пачку из картона.
Производство ОАО «Фармстандарт-УфаВИТА»:
- Препарат в прозрачных ампулах. По 0.5 мл (1 доза) каждого компонента в ампуле. По 5 ампул каждого компонента помещены в ячейковую контурную упаковку из поливинилхлоридной пленки, по 1 ячейковой упаковке вместе с инструкцией в картонной пачке.
- Препарат во флаконах, закрытых резиновой пробкой, обжатый алюмопластиковым колпаком с контролем первого вскрытия. По 3 мл (5 доз) каждого компонента во флаконе. Флакон каждого компонента вместе с инструкцией помещен в пачку из картона.
Жидкий препарат
Оба компонента препарата в виде однородного раствора, бесцветного или слегка желтоватого оттенка.
Производство ОАО «Фармстандарт-УфаВИТА»:
- Препарат в прозрачных ампулах. По 0.5 мл (1 доза) каждого компонента в ампуле. По 5 ампул каждого компонента помещены в ячейковую контурную упаковку из поливинилхлоридной пленки, по 1 ячейковой упаковке вместе с инструкцией в картонной пачке.
Производство АО «ГЕНЕРИУМ» и ЗАО «ЛЕККО»:
- Препарат во флаконах, закрытых резиновой пробкой, обжатый алюмопластиковым колпаком с контролем первого вскрытия. По 3 мл (5 доз) каждого компонента во флаконе. Флакон каждого компонента в контурной ячейковой упаковке вместе с инструкцией помещен в пачку из картона.
Фармакологическое действие
Комбинированная векторная вакцина Гам-КОВИД-Вак применяется в качестве иммунологического средства.
Фармакодинамика и фармакокинетика
Согласно исследованиям препарата в институте Гамалеи вакцина способствует формированию клеточного и гуморального иммунитета по отношению к вирусной инфекции, ассоциированной SARS-CoV-2. Обладает иммунологической активностью. Безопасность и иммунологические свойства изучались в клинических исследованиях у взрослых пациентов обоих полов. Возраст испытываемых составлял от 18 до 60 лет. При этом 9 человек получали первый компонент и 9 — второй, 20 человек проходили вакцинацию в режиме прайм-буст.
Иммуногенность средства была оценена по уровню спец. антител к белку коронавируса и уровню нейтрализующих вирус антител. У всех пациентов, принимающих участие в исследовании в результате образовывались специфические агенты. Через 42 дня в сыворотке крови всех добровольцев были обнаружены антитела к вирусу.
В центре Гамалеи оценку уровня иммуноглобулинов проводили по сравнению с исходным уровнем до иммунизации. Степень активности клеточного иммунитета была оценена в тесте лимфопролиферации CD8+ и CD4+, по скорости прироста интерферонов гамма в ответ на стимуляцию гликопротеином S.
После проведения вакцинации Спутником V был сформирован напряженный ангитен-специфический клеточный противоинфекционный иммунитет у всех добровольцев. Формировались антиген-специфичные клетки Т-хелперов, Т-киллеров, наблюдалось повышение уровня ИФНγ.
На данный момент испытания вакцины Cпутник V продолжаются, а защитный титр антител достоверно неизвестен. Испытания должны выявить продолжительность защиты организма. Также, пока не проводились клинические исследования по изучению эпидемиологической эффективности средства.
Показания к применению
Применяют для профилактики новой коронавирусной инфекции COVID-19 у взрослых пациентов в возрасте от 18 до 60 лет.
Вакцина Спутник V, противопоказания
Были выявлены следующие противопоказания на Спутник Ви:
- сверхчувствительность к компонентам средства или к вакцинам, содержащим аналогические ингредиенты;
- наличие тяжелых аллергических реакций у пациента ранее;
- неинфекционные и инфекционные острые заболевания;
- обострение хронического заболевания (вакцинацию рекомендуется проводит не ранее, чем через 2-4 недели после полного выздоровления или достижения ремиссии);
- кормление грудью и беременность;
- возраст до 18 и более 60 лет.
Перед тем, как сделать прививку 2 компонентом нужно выяснить у пациента, не возникали ли тяжелые осложнения (аллергические реакции, анафилактический шок, судороги, повышение температуры выше 40 градусов) после инъекции 1 компонента.
Осторожность следует соблюдать:
- при хронических заболеваниях почек и печени;
- пациентам с сахарным диабетом и выраженными нарушениями работы эндокринной системы;
- при тяжелых заболеваниях системы кроветворения;
- больным эпилепсией;
- после инсульта или с другими заболеваниями центральной нервной системы;
- при патологиях сердечно-сосудистой системы, инфаркте в анамнезе, миокардите, перикардите, эндокардите, ишемической болезни;
- пациентам с первичным и вторичным иммунодефицитом;
- при аутоимунных заболеваниях;
- больным астмой, с заболеваниями легких, ХОБЛ;
- при метаболическом синдроме;
- пациентам с атопией, аллергическими реакциями, экземой.
В учреждении, где проводят вакцинацию должны быть в наличии средства противошоковой терапии. В день проведения прививки пациента необходимо осмотреть, измерить температуру. Нельзя делать укол, если у пациента температура выше 37 градусов.
Вакцина Спутник V, побочные эффекты
Побочные эффекты Гам-КОВИД-Вак были выявлены в рамках клинических испытаний и исследований прочих вакцин, разработанных по аналогичной технологии. Реакции бывают легкими или среднетяжелыми. Чаще всего возникают в 1-2 день после прививки и проходят в течение следующих 3 дней. Рекомендуют проводить симптоматические лечение, при необходимости принимать НПВС после вакцинации.
Обычно наблюдаются кратковременные общие и местные реакции:
- гриппоподобный синдром, озноб, рост температуры тела, миалгия, артралгия, общая слабость;
- астения, головные боли, недомогание;
- боли в месте инъекции, отечность и повышение температуры в месте укола.
Реже возникает:
- тошнота, несварение желудка, потеря аппетита;
- увеличение лимфоузлов, аллергические реакции;
- рост уровня ферментов печени, креатинина, трансаминаз, креатинфосфокиназы в крови.
В открытом клиническом исследовании безопасности вакцины не удалось точно определить встречаемость нежелательных реакций, так как выборка участников исследования была ограниченной.
Во время таких исследований выявили следующие побочные эффекты:
- боль, отек, зуд в месте введения вакцины;
- понос, боли в ротоглотке, заложенность носа и першение в горле, ринорея;
- рост уровня Т-лимфоцитов, CD4-лимфоцитов и процентного их содержания;
- снижение числа естественных «киллеров», СD8;
- отклонения в общем анализе мочи, наличие в ней эритроцитов.
Вакцина Гам-КОВИД-Вак (Спутник V), инструкция по применению
Прививка Спутник V от коронавируса проводится внутримышечно. Внутривенное ведение средства строго запрещено. Инъекцию производят в дельтовидную мышцу или в латеральную широкую мышцу бедра.
Лиофилизат необходимо растворить в 1,0 мл воды для инъекций. После чего флакон встряхивают, пока его содержимое полностью не растворится.
Перед введением готового препарата его достают из холодильной камеры и нагревают при комнатной температуре в течение получаса. Раствор перемешивают осторожно покачивая ампулу. Нельзя резко встряхивать средство.
Нельзя использовать препарат, если целостность флакона была нарушена, смазалась маркировка, вещество изменило свои физические свойства, изменился цвет, появились механические включения, истек срок годности.
Лекарственный препарат был зарегистрирован по особой процедуре, и при каждом применении вакцины необходимо уведомлять Федеральную службу по надзору в сфера здравоохранения. Информацию нужно вносить в соответствующий раздел инф. системы ЕГИСЗ.
Вакцинация проводится в 2 этапа. Вначале вводят компонент 1, затем через 3 недели — компонент 2.
Если дальнейшие инъекции были отложены по какой-либо причине, то можно хранить вскрытый флакон по 3 мл не более 2 часов при комнатной температуре.
Передозировка
Нет данных о передозировке Спутник Ви. Вакцина от ковида выпускается для использования в лечебно-профилактических учреждениях, процедура проводится только квалифицированными мед. персоналом и вероятность передозировки крайне мала.
Предполагается, что при случайной передозировке могут возникнуть токсические и токсико-аллергические реакции, указанные в пункте «побочные действия» в более тяжелой форме. Рекомендуется симптоматическая терапия, прием жаропонижающих препаратов и НПВС, кортикостероидов парентерально.
Взаимодействие
Неизвестно вступает ли вакцина от коронавируса Спутник V во взаимодействие с другими препаратами.
Условия продажи
Пока лекарство нельзя приобрести в аптеке самостоятельно.
Условия хранения векторной вакцины Гам-КОВИД-Вак
Раствор для внутримышечного введения хранят в защищенном от света месте при температуре не более 18 °C. Не допустимо хранение размороженного препарата для флаконов по 0,5 мл.
Для флаконов по 3,0 мл — средство можно хранить более 2 часов при комнатной температуре. Держать вакцину дальше от детей.
Срок годности
Срок хранения составляет пол года для всех лек. форм и обоих компонентов средства.
Особые указания
Пациенты, получающие иммуносупрессивную терапию или больные иммунодефицитом могут не получить достаточного иммунного ответа. Поэтому применение средств, угнетающих работу иммунной системы противопоказано за 30 дней до и 30 дней после вакцинации. Пренебрежение правилом может привести к снижению иммуногенности.
Неизвестно, влияет ли инъекция препарата на способность управлять транспортом и опасными механизмами.
Узнать подробности о лекарстве можно на официальном сайте института Гамалеи.
Аналоги
Совпадения по коду АТХ 4-го уровня:
В октябре 2020 года в РФ прошла регистрацию вторая вакцина под названием ЭпиВакКорона. Лекарство было разработано в новосибирском научном центре «Вектор» и представляет собой искусственно синтезированные короткие фрагменты вирусных пептидов, «обучающие» иммунную систему бороться с вирусом. Сейчас препарат также проходит третий этап клинических испытаний.
Также, в феврале 2021 года прошла регистрацию третья вакцина КовиВак исследовательского центра им. Чумакова, в ее состав включен цельный инактивированный вирус.
На данный момент сложно предугадать, какая из вакцин окажется наиболее эффективной.
Детям
Вакцина от ковида Спутник Ви не применяется в возрасте до 18 лет.
При беременности и лактации
Делать прививки нельзя беременным женщинам и во время грудного вскармливания.
Вакцина Спутник V, отзывы
Известно, что в Российской Федерации разработкой лекарства от новой коронавирусной инфекции занялся институт Гамалеи. Вакцина от коронавируса получила уже широко известное название «Спутник V». Перед тем, как проводить иммунизацию массово, лекарству необходимо пройти стадию клинических испытаний. И на данный момент средство проходит этот этап пострегистрационного исследования в Москве. Сделать прививку в тестовом режиме планируется 40 тысячам человек, четверть из них получат плацебо. Параллельно уже началась иммунизация мед. работников и врачей.
Сейчас среди скептически настроенного населения идут горячие споры об эффективности вакцины Спутник V, учитывая тот факт, что некоторые добровольцы, которым делали уколы Гам-КОВИД-Вак, заразились уже на следующий день после прививки. В общем известно около 20 подобных случаев. Это объясняется тем, что большинство заболевавших не успели получить второй укол и иммунитет у них выработаться тоже не успел. Ведь, как известно, устойчивость у вирусу развивается только на 42 день после проведения полного цикла вакцинации. Именно так объяснил данные инциденты директор Института трансляционной медицины и биотехнологии Сеченовского университета Минздрава РФ Вадим Тарасов, который подчеркивает высокую эффектность Спутник V.
Отзывы врачей о препарате в большинстве своем положительные. При этом медики подчеркивают, что вакцина не призвана защитить от болезни на все 100%, она также должна предотвратить развитие тяжелой формы заболевания и летальный исход. Допускается, что после применения лекарства болезнь будет просто протекать в легкой форме и без осложнений.
Интерес также вызывают отзывы привитых добровольцев, которые приняли участие в третьей фазе клинических испытаний. Рандомизированное двойное слепое плацебо-контролируемое клиническое исследование началось 26 августа 2020 года.
Некоторые интересуются, как правильно называть препарат, Спутник Ви или Спутник 5? Правильный ответ — Спутник Ви.
Отзывы добровольцев:
- «… Решила попробовать эту вакцину на себе. На второй день после первой инъекции начала болеть рука, а к вечеру третьего дня поднялась температура 37,5. На пятый день температура спала. После второго укола температура была выше, до 38 Градусов и ощущала я себя, как при гриппе. Через три дня все вроде прошло. Потом сдавала кровь на антитела, уровень IgG составил 11,3, непонятно почему так мало».
- «… Записался на вакцинацию как только узнал, что так можно. Во время прививки покалывало руку, а так не заметил каких-либо побочных реакций. Чувствую себя хорошо пока, вторая прививка тоже прошла нормально. Буду ждать теста на антитела«.
- «… После вакцинации ощущаю себя так, будто переболела гриппом, была высокая температура, головные боли и ломило суставы. Еще болел левый бок. Сбивала температуру 2 недели. К сожалению после болезни антител у меня нет, что странно«.
После прохождения последнего этапа планируется наладить массовое производство вакцины Спутник V и провести иммунизацию достаточного количества населения страны, чтобы сформировать коллективный иммунитет.
Вакцина Спутник V, цена, где купить вакцину Спутник V в Москве
На данный момент указать даже примерную стоимость Спутник Ви сложно. Есть сообщения о том, что предельная стоимость препарата составит не более 1942 рублей за оба компонента. Однако, пока Гам-КОВИД-Вак не появилась в свободной продаже, говорить о точной цене рано.
Гам-КОВИД-Вак Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
Гам-КОВИД-Вак Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2 (Gam-COVID-Vac Combined vector vaccine for the prevention of coronavirus infection caused by the SARS-CoV-2 virus) инструкция по применению
📜 Инструкция по применению Гам-КОВИД-Вак Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
💊 Состав препарата Гам-КОВИД-Вак Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
✅ Применение препарата Гам-КОВИД-Вак Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
📅 Условия хранения Гам-КОВИД-Вак Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
⏳ Срок годности Гам-КОВИД-Вак Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
Описание лекарственного препарата
Гам-КОВИД-Вак Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
(Gam-COVID-Vac Combined vector vaccine for the prevention of coronavirus infection caused by the SARS-CoV-2 virus)
Основано на официально утвержденной инструкции по применению препарата и подготовлено для электронного издания справочника Видаль 2020 года, дата обновления: 2022.04.15
Владелец регистрационного удостоверения:
Код ATX:
J07BX03
(Вакцины против COVID-19)
Лекарственные формы
| Гам-КОВИД-Вак Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2 |
Р-р д/в/м введения, компонент I — 0.5 мл/доза (замороженный препарат): фл. 1 шт. рег. №: ЛП-006395 |
|
|
Р-р д/в/м введения, компонент II — 0.5 мл/доза (замороженный препарат): амп. 5 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент II — 0.5 мл/доза (замороженный препарат): фл. 1 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент I — 0.5 мл/доза (замороженный препарат): амп. 5 или 10 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент II — 0.5 мл/доза (замороженный препарат): амп. 5 или 10 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент I — 0.5 мл/1 доза (жидкий препарат): амп. 5 или 10 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент II — 0.5 мл/1 доза (жидкий препарат): амп. 5 или 10 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент I — 0.5 мл/доза (замороженный препарат): амп. 5 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент II — 1.0 мл/2 дозы (замороженный препарат): амп. 5 или 10 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент I — 1.0 мл/2 дозы (замороженный препарат): амп. 5 или 10 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент II — 3.0 мл/5 доз (замороженный препарат): фл. 1 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент I — 3.0 мл/5 доз (замороженный препарат): фл. 1 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент I — 3.0 мл/5 доз (замороженный препарат): фл. 1 или 10 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент II — 3.0 мл/5 доз (замороженный препарат): фл. 1 или 10 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент I — 3.0 мл/5 доз (жидкий препарат): фл. 1 шт. рег. №: ЛП-006395 |
||
|
Р-р д/в/м введения, компонент II — 3.0 мл/5 доз (жидкий препарат): фл. 1 шт. рег. №: ЛП-006395 |
Раствор для в/м введения (компонент I* и компонент II).
Замороженный препарат
Компонент I*. Раствор замороженный — плотная затвердевшая беловатого цвета масса. После размораживания: однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Вспомогательные вещества: трис(гидроксиметил)аминометан — 1.21 мг, натрия хлорид — 2.19 мг, сахароза — 25.0 мг, полисорбат 80 — 250.0 мкг, магния хлорида гексагидрат — 102.0 мкг, ЭДТА динатриевая соль дигидрат — 19.0 мкг, этанол 95% — 2.5 мкл, вода д/и — до 0.5 мл.
* Идентичен составу лекарственного препарата «Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2» (номер регистрационного удостоверения ЛП-006993).
0.5 мл (1 доза компонента I) — флаконы (1) — пачки картонные.
0.5 мл (1 доза компонента I) — флаконы (5) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза компонента I) — флаконы (5) — упаковки ячейковые контурные (2) — пачки картонные.
0.5 мл (1 доза компонента I) — флаконы (типа 2R) (1, 2, 5, 10) — пачки картонные.
3.0 мл (5 доз компонента I) — флаконы (типа 10R) (1) — пачки картонные.
3.0 мл (5 доз компонента I) — флаконы (типа 10R) (10) — пачки картонные.
0.5 мл (1 доза компонента I) — флаконы (типа 2R) (1) — упаковки ячейковые контурные (1) — пачки картонные×.
3.0 мл (5 доз компонента I) — флаконы (типа 6R) (1) — пачки картонные×.
3.0 мл (5 доз компонента I) — флаконы (1) — пачки картонные с держателем.
0.5 мл (1 доза компонента I) — ампулы бесцветного стекла с цветной точкой (5) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза компонента I) — ампулы бесцветного стекла с цветной точкой (5) — упаковки ячейковые контурные (2) — пачки картонные.
0.5 мл (1 доза компонента I) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза компонента I) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (2) — пачки картонные.
1.0 мл (2 дозы компонента I) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (1) — пачки картонные.
1.0 мл (2 дозы компонента I) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (2) — пачки картонные.
Компонент II. Раствор замороженный — плотная затвердевшая беловатого цвета масса. После размораживания: однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Вспомогательные вещества: трис(гидроксиметил)аминометан — 1.21 мг, натрия хлорид — 2.19 мг, сахароза — 25.0 мг, полисорбат 80 — 250.0 мкг, магния хлорида гексагидрат — 102.0 мкг, ЭДТА динатриевая соль дигидрат — 19.0 мкг, этанол 95% — 2.5 мкл, вода д/и — до 0.5 мл.
0.5 мл (1 доза компонента II) — флаконы (1) — пачки картонные.
0.5 мл (1 доза компонента II) — флаконы (5) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза компонента II) — флаконы (5) — упаковки ячейковые контурные (2) — пачки картонные.
3.0 мл (5 доз компонента II) — флаконы (типа 10R) (1) — пачки картонные.
3.0 мл (5 доз компонента II) — флаконы (типа 10R) (10) — пачки картонные.
0.5 мл (1 доза компонента II) — флаконы (типа 2R) (1) — упаковки ячейковые контурные (1) — пачки картонные×.
3.0 мл (5 доз компонента II) — флаконы (типа 6R) (1) — пачки картонные×.
3.0 мл (5 доз компонента II) — флаконы (1) — пачки картонные с держателем.
0.5 мл (1 доза компонента II) — ампулы бесцветного стекла с цветной точкой (5) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза компонента II) — ампулы бесцветного стекла с цветной точкой (5) — упаковки ячейковые контурные (2) — пачки картонные.
0.5 мл (1 доза компонента II) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза компонента II) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (2) — пачки картонные.
1.0 мл (2 дозы компонента II) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (1) — пачки картонные.
1.0 мл (2 дозы компонента II) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (2) — пачки картонные.
Жидкий препарат
Компонент I*. Однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Вспомогательные вещества: трис(гидроксиметил)аминометан — 1.21 мг, натрия хлорид — 2.19 мг, сахароза — 25.0 мг, полисорбат 80 — 250.0 мкг, магния хлорида гексагидрат — 102.0 мкг, ЭДТА динатриевая соль дигидрат — 19.0 мкг, этанол 95% — 2.5 мкл, вода д/и — до 0.5 мл.
* Идентичен составу лекарственного препарата «Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2» (номер регистрационного удостоверения ЛП-006993).
3.0 мл (5 доз компонента I) — флаконы (1) — пачки картонные с держателем.
3.0 мл (5 доз компонента I) — флаконы (1) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза компонента I) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза компонента I) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (2) — пачки картонные.
1.0 мл (2 дозы компонента I) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (1) — пачки картонные.
1.0 мл (2 дозы компонента I) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (2) — пачки картонные.
0.5 мл (1 доза компонента I) — флаконы (типа 2R) (1) — упаковки ячейковые контурные (1) — пачки картонные×.
3.0 мл (5 доз компонента I) — флаконы (типа 6R) (1) — пачки картонные×.
Компонент II. Однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Вспомогательные вещества: трис(гидроксиметил)аминометан — 1.21 мг, натрия хлорид — 2.19 мг, сахароза — 25.0 мг, полисорбат 80 — 250.0 мкг, магния хлорида гексагидрат — 102.0 мкг, ЭДТА динатриевая соль дигидрат — 19.0 мкг, этанол 95% — 2.5 мкл, вода д/и — до 0.5 мл.
3.0 мл (5 доз компонента II) — флаконы (1) — пачки картонные с держателем.
3.0 мл (5 доз компонента II) — флаконы (1) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза компонента II) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза компонента II) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (2) — пачки картонные.
1.0 мл (2 дозы компонента II) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (1) — пачки картонные.
1.0 мл (2 дозы компонента II) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (2) — пачки картонные.
0.5 мл (1 доза компонента II) — флаконы (типа 2R) (1) — упаковки ячейковые контурные (1) — пачки картонные×.
3.0 мл (5 доз компонента II) — флаконы (типа 6R) (1) — пачки картонные×.
× На флаконы каждого компонента препарата наклеивают этикетку самоклеящуюся.
Фармакологическое действие
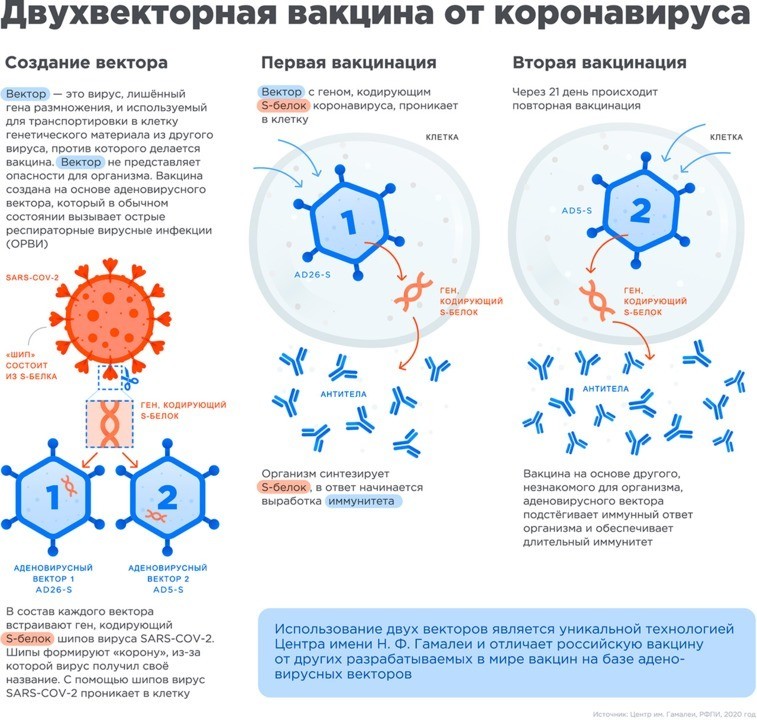
Характеристика. Вакцина получена биотехнологическим путем, при котором не используется патогенный для человека вирус SARS-CoV-2. Препарат состоит из двух компонентов: компонент I и компонент II.
В состав компонента I входит рекомбинантный аденовирусный вектор на основе аденовируса человека 26 серотипа, несущий ген белка S вируса SARS-CoV-2, что соответствует составу лекарственного препарата «Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2» (номер регистрационного удостоверения ЛП-006993).
В состав компонента II входит рекомбинантный аденовирусный вектор на основе аденовируса человека 5 серотипа, несущий ген белка S вируса SARS-CoV-2.
Вакцина индуцирует формирование гуморального и клеточного иммунитета в отношении коронавирусной инфекции, вызываемой вирусом SARS-CoV-2.
Иммунологическая эффективность
Иммунологические свойства и безопасность вакцины изучали в различных клинических исследованиях у взрослых добровольцев обоего пола в возрасте старше 18 лет.
Анализ иммуногенности показал, что вакцина формирует иммунный ответ у добровольцев: средний геометрический титр у добровольцев, иммунизированных Гам-КОВИД-Вак, на 42 день составил 9009.0, а на 180 день — 1708.0.
В группе Плацебо средний геометрический титр на 42 день составил 55.6, а на 180 день — 110.2. Сероконверсия к 42 дню наблюдается у 99.1% вакцинированных добровольцев и сохраняется к 180 дню у 93.9%.
У добровольцев на 42 сутки после вакцинации отмечается достоверное увеличение вируснейтрализующих антител в сыворотке крови, который сохраняется и на 180 день.
Иммунизация препаратом Гам-КОВИД-Вак формирует напряженный антиген-специфический клеточный противоинфекционный иммунитет практически у всех обследованных добровольцев (формирование антиген-специфичных клеток обеих популяций Т-лимфоцитов: Т-хелперных (CD4+) и Т-цитотоксических (CD8+) и достоверное повышение секреции ИФНγ).
Защитный титр антител в настоящее время неизвестен. Продолжительность защиты неизвестна.
По данным III фазы рандомизированного плацебо контролируемого клинического исследования эффективность вакцины составляет более 91% для дикого штамма (Ухань) и по результатам полученным через полгода в условиях доминирования штамма дельта — 70.5% от симптомов коронавирусной инфекции. Таким образом, иммунизация достоверно снижает вероятность заболевания. В отношении среднетяжелых, тяжелых и очень тяжелых случаев эффективность составляет более 88% в течении полугодового периода наблюдения
По результатам опубликованных данных применения вакцины за рубежом, в рамках клинической практики в Венгрии на ноябрь 2021 у 820560 вакцинированных, показана 85.7% эффективность векторной вакцины Спутник-V. Эффективность против смерти, связанной с COVID-19, варьировала от 95.4% до 100% в разных возрастных когортах, демонстрируя очень высокую и стойкую эффективность как в старшей, так и в младшей возрастных когортах.
У лиц с предсуществующим иммунитетом к коронавирусу отмечен выраженный рост титра антител на 10-й день (препаратом Спутник Лайт, соответствующего компоненту I препарата Гам-КОВИД-Вак), что может указывать на возможность применения препарата для вакцинации ранее переболевших COVID-19 после снижения титра антител с целью предотвращения повторных случаев заболевания. С учетом рекомендаций ВОЗ для достижения уровня коллективного иммунитета населения, следует проводить вакцинацию против новой коронавирусной инфекции COVID-19 по эпидемическим показаниям спустя 6 месяцев после перенесенного заболевания (в т.ч. у ранее вакцинированных лиц) или спустя 6 месяцев после предыдущей первичной вакцинации.
Показания препарата
Гам-КОВИД-Вак Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
Профилактика новой коронавирусной инфекции (COVID-19) у взрослых старше 18 лет.
Режим дозирования
Вакцина предназначена только для внутримышечного введения. Строго запрещено внутривенное введение препарата. Вакцину вводят в дельтовидную мышцу (верхнюю треть наружной поверхности плеча). При невозможности введения в дельтовидную мышцу — препарат вводят в латеральную широкую мышцу бедра.
Вакцинацию проводят в два этапа: вначале компонентом I дозе 0.5 мл, затем, через 3 недели — компонентом II в дозе 0.5 мл.
Допускается, при необходимости, однократная вакцинация компонентом I в дозе 0.5 мл.
После введения вакцины пациент должен находиться под наблюдением медицинских работников в течение 30 минут.
Применение вакцины производства ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России) (флаконов) и АО «Биннофарм» (ампул) и АО «Р-Фарм» (флаконов)
Перед вакцинированием флакон или ампулу с компонентом I или II достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон или ампулу снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона или ампулы!
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой.
Вскрывают ампулу по цветной точке.
Используя одноразовый шприц с иглой, отбирают дозу 0.5 мл для введения пациенту.
Не допускается хранение размороженного препарата!
Повторное замораживание не допускается!
Применение вакцины производства АО «ГЕНЕРИУМ» (флаконы), ОАО «Фармстандарт- УфаВИТА» (флаконы, ампулы) и ЗАО «ЛЕККО» (флаконы)
Замороженный препарат
Внимание! Повторное замораживание флакона или ампулы с раствором не допускается! Суммарное время хранения размороженного раствора при комнатной температуре не должно превышать 2 часов. Неиспользованная вакцина подлежит уничтожению.
Перед вакцинированием флакон или ампулу с компонентом I или II достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон или ампулу снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона или ампулы!
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой. Ампулу вскрывают по кольцу и/или точке излома.
Используя одноразовый шприц с иглой, отбирают дозу 0.5 мл для введения пациенту. Для каждой инъекции необходимо использовать отдельный одноразовый стерильный шприц с иглой.
Внимание! Доза, вводимая пациенту, не должна превышать 0.5 мл!
Многодозовые флаконы
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого или невскрытого флакона при комнатной температуре не более 2 часов.
Многодозовые ампулы
Содержимое ампулы рекомендуется использовать незамедлительно. Если последующие инъекции по какой-либо причине откладываются, допускается хранение вакцины при комнатной температуре: вскрытой ампулы, закрытой стерильной салфеткой, не более 1 часа; невскрытой ампулы — не более 2 часов.
ВНИМАНИЕ! Одна ампула содержит две дозы вакцины. Объем одной дозы составляет 0.5 мл. Одному пациенту вводить 1 дозу (0.5 мл).
Однодозовые ампулы
Содержимое ампулы рекомендуется использовать незамедлительно. Если последующие инъекции по какой-либо причине откладываются, допускается хранение невскрытой ампулы при комнатной температуре не более 2 часов
Жидкий препарат
Внимание! Замораживание флакона или ампулы с раствором не допускается! Неиспользованная вакцина подлежит уничтожению.
Перед вакцинированием флакон или ампулу с компонентом I или II достают из холодильника и выдерживают при комнатной температуре, допускается слегка нагреть препарат, например, подержав его в руках. Не следует нагревать препарат выше 37°С.
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой.
Ампулу вскрывают по кольцу и/или точке излома.
Используя одноразовый шприц с иглой, отбирают дозу 0.5 мл для введения пациенту. Для каждой инъекции необходимо использовать отдельный одноразовый стерильный шприц с иглой.
Внимание! Доза, вводимая пациенту, не должна превышать 0.5 мл!
Многодозовые флаконы
Если последующие инъекции по какой- либо причине откладываются, допускается хранение вскрытого или невскрытого флакона при комнатной температуре не более 2 часов.
Однодозовые ампулы
Содержимое одной ампулы рекомендуется использовать незамедлительно. Если последующие инъекции по какой-либо причине откладываются, допускается хранение невскрытой ампулы при комнатной температуре не более 2 часов
Применение вакцины производства ЗАО «БИОКАД» (флаконов)
Перед вакцинированием флакон с компонентом I или II достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона!
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой.
Используя одноразовый шприц с иглой, отбирают дозу 0.5 мл для введения пациенту.
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого флакона по 3 мл не более 2 часов при комнатной температуре.
Не допускается хранение размороженного препарата во флаконах по 0.5 мл!
Повторное замораживание не допускается!
Внимание! К использованию непригоден препарат (жидкий и/или замороженный) с дефектами укупорочной системы и/или нарушенной маркировкой флакона или ампулы, при изменении физических свойств раствора (мутность, окрашивание), неправильном хранении и/или с истекшим сроком годности.
Применение вакцины производства АО «Р- Фарм». компонент I (флаконы) и ООО СПУТНИК ТЕХНОПОЛИС», компонент II (флаконы)
Внимание! К использованию непригоден препарат с дефектами укупорочной системы и/или нарушенной маркировкой флакона, при изменении физических свойств раствора (мутность, окрашивание), неправильном хранении и/или с истекшим сроком годности.
Многодозовые флаконы. Перед вакцинированием флакон с компонентом I или II достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона!
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой. Используя одноразовый шприц с иглой, отбирают дозу 0.5 мл для введения пациенту.
Для каждой инъекции необходимо использовать отдельный одноразовый стерильный шприц с иглой.
Внимание! Доза, вводимая пациенту, не должна превышать 0. 5 мл!
Если последующие инъекции по какой- либо причине откладываются, допускается хранение вскрытого или невскрытого размороженного флакона при комнатной температуре не более 2 часов
Повторное замораживание не допускается!
Неиспользованная вакцина подлежит уничтожению.
Побочное действие
Нежелательные явления, характерные для применения вакцины, выявленные в рамках клинических исследований, бывают преимущественно легкой или средней степени выраженности, могут развиваться в первые-вторые сутки после вакцинации и разрешаются в течение 3-х последующих дней.
Частота встречаемости определяется следующим образом: часто (>1/100, <1/10), нечасто (>1/1000, <1/100), редко (>1/10000, <1/1000), очень редко (>1/10000, включая единичные случаи.
Категории частоты были сформированы на основании клинических исследований препарата. Рекомендуется назначение нестероидных противовоспалительных средств (НПВС) при повышении температуры после вакцинации и антигистаминных средств при выраженной местной реакции.
В рамках проведенных клинических исследований и в рамках фармаконадзора были зарегистрированы следующие нежелательные реакции.
Общие нарушения и реакции в месте введения: часто — гипертермия, боль, отек, зуд в месте вакцинации, озноб, астения; нечасто — пирексия, снижение аппетита.
Желудочно-кишечные нарушения: очень редко — тошнота, рвота, диспепсия.
Со стороны дыхательной системы, органов грудной клетки и средостения: очень редко — заложенность носа, першение в горле, ринорея.
Со стороны кожи и подкожной клетчатки: очень редко — ангиоотек, крапивница и сыпь (эритематозная, папулезная).
Со стороны мышечной, скелетной и соединительной ткани: часто — миалгия, артралгия, скелетно-мышечная боль; нечасто — остеоартрит.
Со стороны иммунной системы: очень редко — анафилактический шок, анафилактическая реакция и гиперчувствительность.
Со стороны крови и лимфатической системы: очень редко — увеличение регионарных лимфоузлов.
Со стороны нервной системы: очень редко — головная боль; головокружения, обмороки; сообщается о единичных случаях воспалительной полиневропатии (причинно-следственная связь с лекарственным препаратом не установлена — частота данных событий в популяции имеет сезонный характер и может быть связана с различными причинами: провоцирующими факторами могут быть инфекционные заболевания вирусной и бактериальной этиологии, хирургические вмешательства, травматическое повреждение периферических нервов, любая вакцинация, аутоиммунные и системные заболевания).
Со стороны органа зрения: нечасто — фотофобия.
Лабораторные и инструментальные данные: разнонаправленные отклонения показателей иммунологического статуса — повышение числа Т-лимфоцитов, увеличение процентного содержания лимфоцитов, снижение числа естественных клеток-киллеров, увеличение количества CD4-лимфоцитов, снижение количества CD4-лимфоцитов, повышение числа B- лимфоцитов, снижение числа B-лимфоцитов, повышение числа естественных клеток-киллеров, повышение количества CD8-лимфоцитов, повышение уровня иммуноглобулина E (IgE) в крови, увеличение соотношения CD4/CD8, уменьшение соотношения CD4/CD8, повышение уровня иммуноглобулина A(IgA) в крови, уменьшение процентного содержания лимфоцитов CD8. Отклонения в общем анализе крови — увеличение процентного содержания лимфоцитов, снижение показателя гематокрита, увеличение числа лимфоцитов, повышение СОЭ, повышение числа лейкоцитов, повышение числа моноцитов, повышение числа тромбоцитов, снижение числа нейтрофилов, снижение числа тромбоцитов. Отклонение показателей биохимического анализа крови — повышение уровня печеночных трансаминаз, креатинина и креатинфосфокиназы в сыворотке крови. Отклонения в общем анализе мочи — эритроциты в моче. Большинство нежелательных явлений (НЯ) завершились выздоровлением без последствий. Лабораторные отклонения не имели клинического значения (не нуждались в проведении дополнительных диагностических процедур и назначении терапии).
Противопоказания к применению
- гиперчувствительность к какому-либо компоненту вакцины или вакцины, содержащей аналогичные компоненты;
- тяжелые аллергические реакции в анамнезе;
- острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний — вакцинацию проводят через 2-4 недели после выздоровления или ремиссии. При нетяжелых ОРВИ, острых инфекционных заболеваниях ЖКТ- вакцинацию проводят после нормализации температуры;
- беременность;
- период грудного вскармливания;
- возраст до 18 лет (в связи с отсутствием данных об эффективности и безопасности).
Противопоказания для введения компонента II:
- тяжелые поствакцинальные осложнения (анафилактический шок, тяжелые генерализованные аллергические реакции, судорожный синдром, температура выше 40°С и т.д.) на введение компонента I вакцины.
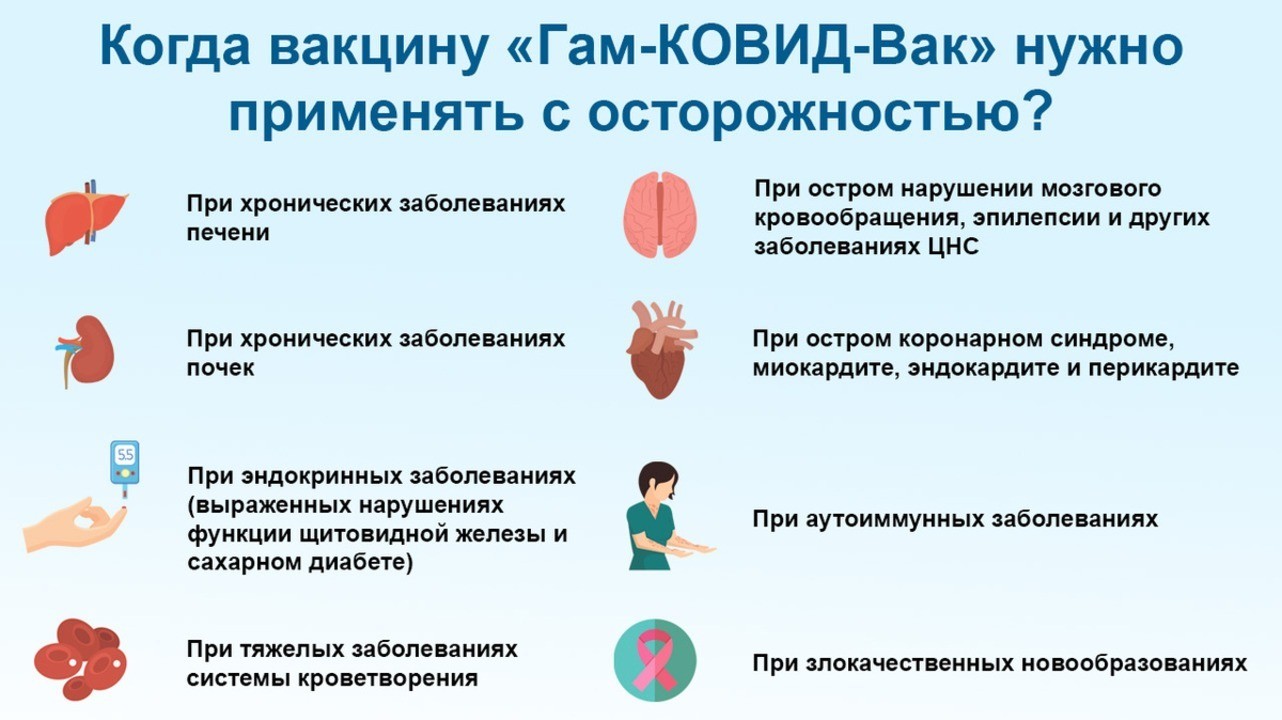
С осторожностью
Применять вакцину с осторожностью при хронических заболеваниях печени и почек, эндокринных заболеваниях (выраженных нарушениях функции щитовидной железы и
сахарном диабете в стадии декомпенсации), тяжелых заболеваниях системы кроветворения, эпилепсии и других заболеваниях ЦНС, остром коронарном синдроме и остром нарушении мозгового кровообращения, миокардитах, эндокардитах, перикардитах.
Вследствие недостатка информации вакцинация может представлять риск для следующих групп пациентов:
- с аутоиммунными заболеваниями (стимуляция иммунной системы может привести к обострению заболевания, особенно следует с осторожностью относиться к пациентам с аутоиммунной патологией, имеющей тенденцию к развитию тяжелых и жизнеугрожающих состояний);
- со злокачественными новообразованиями.
Принятие решения о вакцинации должно основываться на оценке соотношения пользы и риска в каждой конкретной ситуации.
Категориям населения старше 60 лет, ранее не прошедшим иммунизацию от COVID-19, и не болевшим COVID-19, иммунокомпрометированным лицам независимо от возраста, для формирования иммунитета не рекомендовано применение одного компонента для иммунизации в связи со снижением функции иммунной системы, для формирования иммунного ответа показана полная вакцинация двухкомпонентной вакциной Гам-КОВИД-Вак.
Применение при беременности и кормлении грудью
По результатам исследований на животных, репродуктивная токсичность и тератогенность отсутствуют. Клинические исследования Гам-КОВИД-Вак при беременности не проводились. В связи с этим применять препарат Гам-КОВИД-Вак при беременности следует в тех случаях, когда ожидаемая польза для матери превышает потенциальный риск для плода с 22 недели беременности.
Клинические данные по применению препарата Гам-КОВИД-Вак у женщин, кормящих грудью, и младенцев отсутствуют. В настоящее время неизвестно, способны ли действующие вещества, входящие в состав вакцины, проникать в грудное молоко. Перед принятием решения о вакцинации кормящей женщины необходимо оценить риски и пользу данной вакцинации.
Применение при нарушениях функции печени
С осторожностью применять у пациентов с хроническими заболеваниями печени.
Применение при нарушениях функции почек
С осторожностью применять у пациентов с хроническими заболеваниями почек.
Применение у детей
Противопоказание: возраст до 18 лет (в связи с отсутствием данных об эффективности и безопасности.
Особые указания
У пациентов, получающих иммуносупрессивную терапию и пациентов с иммунодефицитом может не развиться достаточный иммунный ответ. Поэтому прием препаратов, угнетающих функцию иммунной системы, противопоказан в течение, как минимум, 1 месяца до и после вакцинации из-за риска снижения иммуногенности.
Подобно остальным вакцинам, защитный иммунный ответ может возникать не у всех вакцинируемых лиц.
При принятии врачом (медицинским работником) решения о необходимости одновременного введения Гам-КОВИД-Вак с другой вакциной, не допускается их смешивание в одном шприце и введение в один участок тела.
Влияние на способность к управлению транспортными средствами и механизмами
Исследования по изучению влияния вакцины на способность управлять транспортными средствами и потенциально опасными механизмами не проводились.
Передозировка
О случаях передозировки не сообщалось.
Учитывая, что отпуск лекарственного препарата допускается только для лечебно-профилактических учреждений, а сама вакцинация проводится только квалифицированным медицинским персоналом, риск передозировки крайне низок.
Однако можно предположить, что при случайной передозировке возможно развитие указанных выше токсических и токсико-аллергических реакций в более тяжелой степени.
Специфических антидотов к препарату не существует.
Терапевтические мероприятия в данном случае будут включать симптоматическую терапию в соответствии с показаниями (жаропонижающие/НПВС и десенсибилизирующие средства, кортикостероиды — парентерально при выраженном токсико-аллергическом синдроме). Режим назначения препаратов должен быть выбран согласно рекомендациям по применению и дозировкам данного лекарственного средства.
Лекарственное взаимодействие
Специальных исследований лекарственного взаимодействия не проводилось.
Взаимодействие с вакциной для профилактики гриппа изучено в доклинических исследованиях, показано отсутствие снижения иммуногенности как вакцины Гам-КОВИД-Вак (Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2), так и гриппозной вакцины в эксперименте при их одновременном введении. Ожидается отсутствие снижения иммуногенности для расщепленных, субъединичных и полимерсубъединичных гриппозных вакцин.
Не допускается смешивание вакцины Гам-КОВИД-Вак с другими вакцинами или иными лекарственными средствами в одном шприце, т.к. нет данных о фармацевтическом взаимодействии.
Условия хранения препарата Гам-КОВИД-Вак Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
Замороженный препарат
Производственные площадки ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России), Россия, ЗАО «БИОКАД», Россия: Компонент I — 1 год. Компонент II — 1 год.
Производственные площадки АО «ГЕНЕРИУМ», Россия, ОАО «Фармстандарт-УфаВИТА», Россия: Компонент I — 9 месяцев. Компонент II — 9 месяцев.
Производственные площадки АО «Биннофарм», Россия, ЗАО «ЛЕККО», Россия: Компонент 1 — 6 месяцев. Компонент II — 6 месяцев.
Производственная площадка АО «Р-Фарм», Россия: Компонент 1-6 месяцев.
Производственная площадка ООО «СПУТНИК ТЕХНОПОЛИС», Россия: Компонент II — 6 месяцев.
Не применять по истечении срока годности.
Хранить в недоступном для детей месте.
Жидкий препарат
Производственные площадки АО «ГЕНЕРИУМ», Россия, ОАО «Фармстандарт-УфаВИТА», Россия: Компонент I — 6 месяцев. Компонент II — 6 месяцев.
Производственные площадки ЗАО «ЛЕККО», Россия, ЗАО «БИОКАД», Россия: Компонент I — 2 месяца. Компонент II — 2 месяца.
Не применять по истечении срока годности
Хранить в недоступном для детей месте.
Условия реализации
Для лечебно-профилактических учреждений.
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Гам-КОВИД-Вак — инструкция по применению
Синонимы, аналоги
Статьи
Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
Данный лекарственный препарат зарегистрирован по процедуре регистрации препаратов, предназначенных для применения в условиях угрозы возникновения, возникновения и ликвидации чрезвычайных ситуаций. Инструкция подготовлена на основании ограниченного объема клинических данных по применению препарата и будет дополняться по мере поступления новых данных. Применение препарата возможно только в условиях медицинских организаций, имеющих право осуществлять вакцинопрофилактику населения в установленном законодательством порядке.
Регистрационный номер:
ЛП-006395
Торговое наименование:
Гам-КОВИД-Вак, Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
Международное непатентованное или группировочное наименование:
Вакцина для профилактики новой коронавирусной инфекции (COV1D-19)
Лекарственная форма:
раствор для внутримышечного введения
Состав
Состав на 1 дозу (0,5 мл):
Компонент I содержит:
Действующее вещество: рекомбинантные аденовирусные частицы 26 серотипа, содержащие ген белка S вируса SARS-CoV-2, в количестве (1,0±0,5)×1011 частиц/доза.
Вспомогательные вещества: Трис(гидроксилметил)аминометан – 1,21 мг, натрия хлорид – 2,19 мг, сахароза – 25,0 мг, магния хлорида гексагидрат – 102,0 мкг, ЭДТАдинатриевая соль дигидрат – 19,0 мкг, полисорбат 80 – 250 мкг, этанол 95% – 2,5 мкл, вода для инъекций до 0,5 мл.
Компонент II содержит:
Действующее вещество: рекомбинантные аденовирусные частицы 5 серотипа, содержащие ген белка S вируса SARS-CoV-2, в количестве (1,0±0,5)×1011 частиц/доза.
Вспомогательные вещества: Трис(гидроксилметил)аминометан – 1,21 мг, натрия хлорид – 2,19 мг, сахароза – 25,0 мг, магния хлорида гексагидрат – 102,0 мкг, ЭДТАдинатриевая соль дигидрат – 19,0 мкг, полисорбат-80 – 250 мкг, этанол 95% – 2,5 мкл, вода для инъекций до 0,5 мл.
Описание:
Компонент I. Раствор замороженный. Представляет собой плотную затвердевшую беловатого цвета массу. После размораживания: однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Компонент II. Раствор замороженный. Представляет собой плотную затвердевшую беловатого цвета массу. После размораживания: однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Характеристика:
Вакцина получена биотехнологическим путем, при котором не используется патогенный для человека вирус SARS-CoV-2. Препарат состоит из двух компонентов: компонент I и компонент II. В состав компонента I входит рекомбинантный аденовирусный вектор на основе аденовируса человека 26 серотипа, несущий ген белка S-вируса SARS-CoV-2, в состав компонента II входит вектор на основе аденовируса человека 5 серотипа, несущий ген белка S вируса SARS-CoV-2.
Фармакотерапевтическая группа:
МИБП-вакцина.
Код ATX:
J07B
Фармакологические свойства
Вакцина индуцирует формирование гуморального и клеточного иммунитета в отношении коронавирусной инфекции, вызываемой вирусом SARS-CoV-2.
Иммунологическая эффективность
Иммунологические свойства и безопасность вакцины изучали в клиническом исследовании у взрослых здоровых добровольцев обоего пола в возрасте от 18 до 60 лет: 9 добровольцев получали компонент I, 9 – компонент II и 20 – в режиме прайм-буст. Иммуногенность оценивали по уровню специфических IgG-антител к белку S коронавируса SARS-CoV-2 и вируснейтрализущих антител, а также по образованию специфических Т-хелперных (CD4+) и цитотоксических (CD8+) лимфоцитов.
Оценку уровня специфических IgG проводили в сравнении с исходным уровнем антител (до иммунизации). У всех участников исследования, получавших препарат, образовались специфические антитела. На 42 сутки среднегеометрическое значение титра составило – 14 703, при 100% сероконверсии. Также на 42 сутки от начала вакцинации в сыворотке крови всех добровольцев детектированы вируснейтрализующие антитела к вирусу SARS-CoV-2 со средним титром 49,3.
Активность клеточного иммунитета оценивали в тесте лимфопролиферации СD4+ и CD8+, а также по приросту концентрации интерферона гамма в ответ на стимуляцию митогеном (гликопротеин S).
Иммунизация препаратом Гам-КОВИД-Вак, вызвала формирование напряженного антиген-специфического клеточного противоинфекционного иммунитета у 100% добровольцев (формирование антиген-специфичных клеток обоих популяций Т лимфоцитов: Т хелперных (CD4+) и Т киллерных (CD8+) и достоверному повышению секреции ИФНγ).
Защитный титр антител в настоящее время неизвестен. Продолжительность защиты неизвестна. Клинические исследования по изучению эпидемиологической эффективности не проводились.
Показания к применению:
Профилактика новой коронавирусной инфекции (COVID-19) у взрослых 18-60 лет
Противопоказания:
- Гиперчувствительность к какому-либо компоненту вакцины или вакцины, содержащей аналогичные компоненты;
- тяжелые аллергические реакции в анамнезе;
- острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний – вакцинацию проводят через 2-4 недели после выздоровления или ремиссии. При нетяжелых ОРВИ, острых инфекционных заболеваниях ЖКТ-вакцинацию проводят после нормализации температуры;
- беременность и период грудного вскармливания;
- возраст до 18 лет (в связи с отсутствием данных об эффективности и безопасности)
Противопоказания для введения компонента II
- тяжелые поствакцинальные осложнения (анафилактический шок, тяжелые генерализованные аллергические реакции, судорожный синдром, температура выше 40 °С и т.д.) на введение компонента I вакцины;
С осторожностью
При хронических заболеваниях печени и почек, выраженных нарушениях функции эндокринной системы (сахарный диабет), тяжелых заболеваниях системы кроветворения, эпилепсии, инсультах и других заболеваниях ЦНС, заболеваниях сердечно-сосудистой системы (инфарктах миокарда в анамнезе, миокардитах, эндокардитах, перикардитах, ишемической болезни сердца), первичных и вторичных иммунодефицитах, аутоиммунных заболеваниях, заболеваниях легких, астме и ХОБЛ, у пациентов с диабетом и метаболическим синдромом, с аллергическими реакциями, атопией, экземой.
Места, где проводится вакцинация, должны быть оснащены средствами противошоковой терапии в соответствии с Приказом Министерства здравоохранения РФ от 20 декабря 2012 г. N 1079н «Об утверждении стандарта скорой медицинской помощи при анафилактическом шоке).
В день проведения вакцинации пациент должен быть осмотрен врачом: обязательным является общий осмотр и измерение температуры тела, в случае если температура превышает 37 °С, вакцинацию не проводят.
Применение при беременности и в период грудного вскармливания
Препарат противопоказан при беременности и в период грудного вскармливания, так как его эффективность и безопасность в этот период не изучались.
Способ применения и дозы
Вакцина предназначена только для внутримышечного введения. Строго запрещено внутривенное введение препарата. Вакцину вводят в дельтовидную мышцу (верхнюю треть наружной поверхности плеча). При невозможности введения в дельтовидную мышцу – препарат вводят в латеральную широкую мышцу бедра. Вакцинацию проводят в два этапа: вначале компонентом I, затем через 3 недели компонентом II.
Препарат вводят внутримышечно: вначале компонент I в дозе 0,5 мл, затем через 3 недели компонент II в дозе 0,5 мл.
Перед введением препарат (компонент) необходимо достать из холодильной камеры и выдержать при комнатной температуре до полного размораживания не более 30 минут; перед применением перемешать, осторожно покачивая флакон (ампулу). Не допускается резко встряхивать препарат.
Хранение вскрытого флакона (ампулы) не допускается!
Повторное замораживание препарата не допускается!
Не пригоден к применению препарат во флаконах и ампулах с нарушенной целостностью и маркировкой, при изменении физических свойств (мутность, окрашивание), при истекшем сроке годности, неправильном хранении.
После введения вакцины пациент должен находиться под наблюдением медицинских работников в течение 30 минут.
Информация для медицинских работников, выполняющих вакцинацию лекарственным препаратом: данный лекарственный препарат зарегистрирован по особой процедуре регистрации, в связи, с чем необходимо уведомлять Федеральную службу по надзору в сфере здравоохранения о каждом факте применения лекарственного препарата путем внесения информации в соответствующей раздел информационной системы ЕГИСЗ
Побочное действие
Нежелательные явления, характерные для применения вакцины, выявленные в рамках клинических исследований, а также исследований других вакцин на основе аналогичной технологической платформы, бывают преимущественно легкой или средней степени выраженности, могут развиваться в первые-вторые сутки после вакцинации и разрешаются в течение 3-х последующих дней. Чаще других могут развиться кратковременные общие (непродолжительный гриппоподобный синдром, характеризующийся ознобом, повышением температуры тела, артралгией, миалгией, астенией, общим недомоганием, головной болью) и местные (болезненность в месте инъекции, гиперемия, отечность) реакции). Рекомендуется назначение нестероидных противовоспалительных средств (НПВС) при повышении температуры после вакцинации. Реже отмечаются тошнота, диспепсия, снижение аппетита, иногда – увеличение регионарных лимфоузлов. У некоторых пациентов возможно развитие аллергических реакций, кратковременное повышение уровня печеночных трансаминаз, креатинина и креатинфосфокиназы в сыворотке крови.
В открытом клиническом исследовании безопасности, переносимости и иммуногенности препарата Гам-КОВИД-Вак нежелательные явления (НЯ) по частоте встречаемости могут быть расценены как встречающиеся часто и очень часто, определить более точно встречаемость нежелательных явлений не представляется возможным из-за ограниченности выборки участников исследования. После вакцинации были зарегистрированы следующие НЯ:
«Общие нарушения и реакции в месте введения»: относились: гипертермия, боль, отек, зуд в месте вакцинации, астения, боль, недомогание, пирексия, повышение температуры кожи в месте вакцинации, снижение аппетита. «Нарушения со стороны нервной системы»: головная боль, диарея. «Нарушения со стороны дыхательной системы, органов грудной клетки и средостения»: боль в ротоглотке, заложенность носа, першение в горле, ринорея.
«Лабораторные и инструментальные данные»; разнонаправленные отклонения показателей иммунологического статуса: повышение числа Т-лимфоцитов, увеличение процентного содержания лимфоцитов, снижение числа естественных клеток-киллеров, увеличение количества СD4-лимфоцитов, снижение количества СD4-лимфоцитов, повышение числа В-лимфоцитов, снижение числа В-лимфоцитов, повышение числа естественных клеток-киллеров, повышение количества СD8-лимфоцитов, повышение уровня иммуноглобулина Е (IgE) в крови, увеличение соотношения CD4/CD8, уменьшение соотношения CD4/CD8, повышение уровня иммуноглобулина A (IgA) в крови, уменьшение процентного содержания лимфоцитов CD8. Отклонения в общем анализе крови: увеличение процентного содержания лимфоцитов, снижение показателя гематокрита, увеличение числа лимфоцитов, повышение скорости оседания эритроцитов, повышение числа лейкоцитов, повышение числа моноцитов, повышение числа тромбоцитов, снижение числа нейтрофилов, снижение числа тромбоцитов. Отклонения в общем анализе мочи: эритроциты в моче. Большинство НЯ завершились выздоровлением без последствий (144 НЯ). На 42 день исследования не завершились 31 НЯ (исход был неизвестен для – НЯ и шел процесс выздоровления – 4 НЯ) – лабораторные отклонения иммунологических показателей, что не имеет клинического значения (не нуждается в проведении дополнительных диагностических процедур и назначения терапии).
Передозировка
О случаях передозировки не сообщалось.
Учитывая, что отпуск лекарственного препарата допускается только для лечебно-профилактических учреждений, а сама вакцинация проводится только квалифицированным медицинским персоналом, риск передозировки крайне низок.
Однако можно предположить, что при случайной передозировке возможно развитие указанных выше токсических и токсико-аллергических реакций в более тяжелой степени.
Специфических антидотов к препарату не существует.
Терапевтические мероприятия в данном случае будут включать симптоматическую терапию в соответствии с показаниями (жаропонижающие/ НПВС и десенсибилизирующие средства), кортикостероиды – парентерально при выраженном токсико-аллергическом синдроме). Режим назначения препаратов должен быть выбран согласно рекомендациям по применению и дозировкам данного лекарственного средства.
Взаимодействие с другими лекарственными средствами
Не изучалось.
Особые указания
У пациентов, получающих иммуносупрессивную терапию и пациентов с иммунодефицитом может не развиться достаточный иммунный ответ. Поэтому прием препаратов, угнетающих функцию иммунной системы, противопоказан как минимум за 1 месяц до и после вакцинации из-за риска снижения иммуногенности.
Влияние на способность управлять транспортными средствами, механизмами
Исследования по изучению влияния вакцины на способность управлять транспортными средствами и потенциально опасными механизмами не проводились.
Форма выпуска
Раствор для внутримышечного введения, компонент I – 0,5 мл/доза + компонент II – 0,5 мл/доза.
При производстве ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России): по 0,5 мл (1 доза) каждого компонента препарата во флаконы нейтрального стекла первого гидролитического класса (типа 2R, 4R), герметично укупоренных пробками из резины, обжатых алюминиевыми или алюмопластиковыми колпачками.
На флаконы наклеивают этикетку из бумаги писчей по ГОСТ 18510-87 или этикеточной по ГОСТ 7625-86, или этикетку из самоклеящегося материала по ТУ 13.96.17-001-90585582-2019 или аналогичного качества.
1 флакон компонента I с инструкцией по применению помещают в пачку картонную по ОСТ 64-071-89 или в пачку из картона коробочного марки хром-эрзац или А по ГОСТ 7973-89; 1 флакон компонента II с инструкцией по применению помещают в пачку картонную по ОСТ 64-071-89 или в пачку из картона коробочного марки хром-эрзац или А по ГОСТ 7973-89
При производстве АО «Биннофарм»:
По 0,5 мл (1 доза) каждого компонента препарата в ампулы по ISO 9187 или ТУ 9462-001-53908805-2006 из бесцветного стекла 1-го гидролитического класса вместимостью 1 мл с цветной точкой. На каждую ампулу наклеивают этикетку.
По 5 ампул каждого компонента препарата помещают в контурную ячейковую упаковку из пленки поливинилхлоридной.
По 1 контурной ячейковой упаковке вместе с инструкцией по применению помещают в пачку из картона по ГОСТ 33781-2016.
Условия хранения:
Хранить в защищенном от света месте, при температуре не выше минус 18°С. Не допускается хранение размороженного препарата более 30 минут! Хранить в недоступном для детей месте.
Условия транспортирования:
Транспортирование препарата при температуре не выше минус 18 °С. Применим способ транспортировки с сухим льдом.
Срок годности:
6 месяцев. Не применять по истечении срока годности.
Условия отпуска:
для лечебно-профилактических учреждений.
Производитель
Наименования и адреса производственных площадок производителя лекарственного препарата:
1) ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России), Россия, 123098, г. Москва, улица Гамалеи, д. 18. (все стадии производства):
2) АО «Биннофарм», Россия, 124460, г. Москва, г. Зеленоград, ул. Конструктора Гуськова, д. 3, стр. 1 (очистка, розлив (первичная упаковка), упаковка (вторичная потребительская упаковка)
Владелец регистрационного удостоверения/организация, принимающая претензии потребителя:
ФГБУ «Национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика Н.Ф. Гамалеи» Министерства здравоохранения Российской Федерации (ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России).
Россия, 123098, г. Москва, улица Гамалеи, д. 18
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2 (Gam-COVID-Vac)
Регистрационный номер
Торговое наименование
Гам-КОВИД-Вак
Международное непатентованное наименование
Лекарственная форма
раствор для внутримышечного введения
Состав
Состав на 1 дозу.
Компонент Ⅰ содержит:
Действующее вещество: рекомбинантные аденовирусные частицы 26 серотипа, содержащие ген белка S вируса SARS-CoV-2, в количестве (1,0 ± 0,5) × 1011 частиц/доза.
Вспомогательные вещества: трис(гидроксиметил)аминометан — 1,21 мг, натрия хлорид — 2,19 мг, сахароза — 25,0 мг, полисорбат 80 — 250 мкг, магния хлорида гексагидрат — 102,0 мкг, ЭДТА динатриевая соль дигидрат — 19,0 мкг, этанол 95 % — 2,5 мкл, вода для инъекций — до 0,5 мл.
Компонент Ⅱ содержит:
Действующее вещество: рекомбинантные аденовирусные частицы 5 серотипа, содержащие ген белка S вируса SARS-CoV-2, в количестве (1,0 ± 0,5) × 1011 частиц/доза.
Вспомогательные вещества: трис(гидроксиметил)аминометан — 1,21 мг, натрия хлорид — 2,19 мг, сахароза — 25,0 мг, полисорбат-80 — 250 мкг, магния хлорида гексагидрат — 102,0 мкг, ЭДТА динатриевая соль дигидрат — 19,0 мкг, этанол 95 % — 2,5 мкл, вода для инъекций — до 0,5 мл.
Описание
Замороженный препарат
Компонент Ⅰ. Раствор замороженный. Представляет собой плотную затвердевшую беловатого цвета массу. После размораживания: однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Компонент Ⅱ. Раствор замороженный. Представляет собой плотную затвердевшую беловатого цвета массу. После размораживания: однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Жидкий препарат
Компонент Ⅰ. Однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Компонент Ⅱ. Однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Характеристика
Вакцина получена биотехнологическим путём, при котором не используется патогенный для человека вирус SARS-CoV-2. Препарат состоит из двух компонентов: компонент Ⅰ и компонент Ⅱ.
В состав компонента Ⅰ входит рекомбинантный аденовирусный вектор на основе аденовируса человека 26 серотипа, несущий ген белка S-вируса SARS-CoV-2, в состав компонента Ⅱ входит вектор на основе аденовируса человека 5 серотипа, несущий ген белка S вируса SARS-CoV-2.
Фармакотерапевтическая группа
Код АТХ
Фармакологические свойства
Вакцина индуцирует формирование гуморального и клеточного иммунитета в отношении коронавирусной инфекции, вызываемой вирусом SARS-CoV-2.
Иммунологическая эффективность
Иммунологические свойства и безопасность вакцины изучали в различных клинических исследованиях у взрослых добровольцев обоего пола в возрасте старше 18 лет.
Промежуточный анализ иммуногенности показал, что вакцина формирует иммунный ответ у добровольцев. При исследовании гуморального иммунного ответа сыворотки добровольцев были проанализированы на наличие антител, специфичных к рецептор-связывающему домену гликопротеина S вируса SARS-CoV-2 на 42 день от начала вакцинации: в группе вакцинированных среднее геометрическое значение титра антител составило 8996, уровень сероконверсии — 98,25. При сравнении уровня RBD-специфических антител между возрастными стратами статистически значимая разница была показана для группы 18–30 лет относительно остальных возрастных групп; среднее геометрическое значение титра антител составило 18102–22067, уровень сероконверсии — 100 %. Уровни антител достоверно не различались у мужчин и женщин. На 42-й день от начала вакцинации средний геометрический титр нейтрализующих антител у иммунизированных добровольцев составил 44,47, уровень сероконверсии — 95,83 %. Статистически значимой разницы у добровольцев различного пола и возраста не выявлено.
Иммунизация препаратом Гам-КОВИД-Вак, формирует напряженный антиген- специфический клеточный противоинфекционный иммунитет у практически у всех обследованных добровольцев (формирование антиген-специфичных клеток обоих популяций T лимфоцитов: T хелперных (CD4+) и T киллерных (CD8+) и достоверному повышению секреции ИФНγ).
Защитный титр антител в настоящее время неизвестен. Продолжительность защиты неизвестна.
Клинические исследования по изучению эпидемиологической эффективности продолжаются в настоящее время. По данным промежуточного анализа эффективность составляет более 91 %.
Показания
Профилактика новой коронавирусной инфекции (COVID-19) у взрослых старше 18 лет.
Противопоказания
- Гиперчувствительность к какому-либо компоненту вакцины или вакцины, содержащей аналогичные компоненты;
- тяжёлые аллергические реакции в анамнезе;
- острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний — вакцинацию проводят через 2–4 недели после выздоровления или ремиссии. При нетяжёлых ОРВИ, острых инфекционных заболеваниях ЖКТ — вакцинацию проводят после нормализации температуры;
- возраст до 18 лет (в связи с отсутствием данных об эффективности и безопасности).
Противопоказания для введения компонента Ⅱ
- тяжёлые поствакцинальные осложнения (анафилактический шок, тяжёлые генерализованные аллергические реакции, судорожный синдром, температура выше 40 °C и т.д.) на введение компонента Ⅰ вакцины.
С осторожностью
Применять вакцину с осторожностью при хронических заболеваниях печени и почек, эндокринных заболеваниях (выраженных нарушениях функции щитовидной железы и сахарный диабет в стадии декомпенсации), тяжёлых заболеваниях системы кроветворения, эпилепсии и других заболеваний ЦНС, остром коронарном синдроме и остром нарушении мозгового кровообращения, миокардитах, эндокардитах, перикардитах.
Вследствие недостатка информации вакцинация может представлять риск для следующих групп пациентов:
- с аутоиммунными заболеваниями (стимуляция иммунной системы может привести к обострению заболевания, особенно следует с осторожностью относиться к пациентам с аутоиммунной патологией имеющей тенденцию к развитию тяжёлых и жизнеугрожающих состояний);
- со злокачественными новообразованиями.
Принятие решения о вакцинации должно основываться на оценке соотношения пользы и риска в каждой конкретной ситуации.
Применение при беременности и в период грудного вскармливания
По результатам исследований на животных, репродуктивная токсичность и тератогенность отсутствуют. Клинические исследования Гам-КОВИД-Вак при беременности не проводились. В связи с этим применять препарат Гам-КОВИД-Вак при беременности следует в тех случаях, когда ожидаемая польза для матери превышает потенциальный риск для плода с 22 недели беременности.
Клинические данные по применению препарата Гам-КОВИД-Вак у женщин, кормящих грудью, и младенцев отсутствуют. В настоящее время неизвестно, способны ли действующие вещества, входящие в состав вакцины, проникать в грудное молоко. Перед принятием решения о вакцинации кормящей женщины необходимо оценить риски и пользу данной вакцинации.
Способ применения и дозы
Вакцина предназначена только для внутримышечного введения. Строго запрещено внутривенное введение препарата. Вакцину вводят в дельтовидную мышцу (верхнюю треть наружной поверхности плеча). При невозможности введения в дельтовидную мышцу — препарат вводят в латеральную широкую мышцу бедра.
Вакцинацию проводят в два этапа: вначале компонентом Ⅰ в дозе 0,5 мл, затем, через 3 недели — компонентом Ⅱ в дозе 0,5 мл.
После введения вакцины пациент должен находиться под наблюдением медицинских работников в течение 30 минут.
Применение вакцины производства ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России) (флаконы) и АО «Биннофарм» (ампулы)
Перед вакцинированием флакон или ампулу с компонентом Ⅰ или Ⅱ достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон или ампулу снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона или ампулы!
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой. Вскрывают ампулу по цветной точке.
Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту.
Не допускается хранение размороженного препарата!
Повторное замораживание не допускается!
Применение вакцины производства АО «ГЕНЕРИУМ» (флаконы), ОАО «Фармстандарт- УфаВИТА» (флаконы, ампулы) и ЗАО «ЛЕККО» (флаконы)
Замороженный препарат
Внимание! Повторное замораживание флакона или ампулы с раствором не допускается!
Суммарное время хранения размороженного раствора при комнатной температуре не должно превышать 2 часов. Неиспользованная вакцина подлежит уничтожению.
Перед вакцинированием флакон или ампулу с компонентом Ⅰ или Ⅱ достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон или ампулу снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона или ампулы!
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой. Вскрывают ампулу по кольцу или точке излома.
Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту.
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого флакона или ампулы — не более 2 часов при комнатной температуре.
Повторное замораживание флакона или ампулы с раствором не допускается!
Жидкий препарат
Внимание! Не использовать флакон или ампулу с препаратом с видимыми дефектами укупорочной системы и/или стекла. Замораживание флакона или ампулы с раствором не допускается!
Приготовление раствора для инъекций.
Флакон или ампулу достают из холодильника и выдерживают при комнатной температуре, допускается слегка нагреть препарат, например, подержав его в руках. Не следует нагревать препарат выше 37 °C.
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой или вскрывают ампулу по кольцу или точке излома.
Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту. Для каждой инъекции необходимо использовать отдельный одноразовый стерильный шприц с иглой.
Внимание! Доза, вводимая пациенту, не должна превышать 0,5 мл!
Многодозовые флаконы
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого или невскрытого флакона при комнатной температуре не более 2 часов.
Многодозовые ампулы
Содержимое ампулы рекомендуется использовать незамедлительно. Если последующие инъекции по какой-либо причине откладываются, допускается хранение вакцины при комнатной температуре: вскрытой ампулы, закрытой стерильной салфеткой, не более 1 часа; невскрытой ампулы — не более 2 часов.
ВНИМАНИЕ! Одна ампула содержит две дозы вакцины. Объём одной дозы составляет 0,5 мл. Одному пациенту вводить 1 дозу (0,5 мл).
Однодозовые ампулы
Содержимое ампулы рекомендуется использовать незамедлительно. Если последующие инъекции по какой-либо причине откладываются, допускается хранение невскрытой ампулы при комнатной температуре не более 2 часов.
Жидкий препарат
Внимание! Замораживание флакона или ампулы с раствором не допускается! Неиспользованная вакцина подлежит уничтожению.
Перед вакцинированием флакон или ампулу с компонентом Ⅰ или Ⅱ достают из холодильника и выдерживают при комнатной температуре, допускается слегка нагреть препарат, например, подержав его в руках. Не следует нагревать препарат выше 37 °C.
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой. Ампулу вскрывают по кольцу и/или точке излома.
Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту. Для каждой инъекции необходимо использовать отдельный одноразовый стерильный шприц с иглой.
Внимание! Доза, вводимая пациенту, не должна превышать 0,5 мл!
Многодозовые флаконы
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого или невскрытого флакона при комнатной температуре не более 2 часов.
Однодозовые ампулы
Содержимое одной ампулы рекомендуется использовать незамедлительно. Если последующие инъекции по какой-либо причине откладываются, допускается хранение невскрытой ампулы при комнатной температуре не более 2 часов.
Применение вакцины производства ЗАО «БИОКАД» (флаконы)
Перед вакцинированием флакон с компонентом Ⅰ или Ⅱ достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона!
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой.
Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту.
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого флакона по 3 мл не более 2 часов при комнатной температуре.
Не допускается хранение размороженного препарата во флаконах по 0,5 мл!
Повторное замораживание не допускается!
Жидкий препарат
Внимание! Не использовать флакон с препаратом с видимыми дефектами укупорочной системы и/или стекла. Замораживание флакона с раствором не допускается!
Флакон достают из холодильника и выдерживают при комнатной температуре, допускается слегка нагреть препарат, например, подержав его в руках. Не следует нагревать препарат выше 37 °C.
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой.
Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту.
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого флакона по 3 мл не более 2 часов при комнатной температуре.
Внимание! К использованию непригоден препарат (жидкий и/или замороженный) с дефектами укупорочной системы и/или нарушенной маркировкой флакона или ампулы, при изменении физических свойств раствора (мутность, окрашивание), неправильном хранении и/или с истекшим сроком годности.
Применение вакцины производства АО «Р-Фарм» (флаконы) и ООО «СПУТНИК ТЕХНОПОЛИС», компонент Ⅱ (флаконы)
Внимание! К использованию непригоден препарат с дефектами укупорочной системы и/или нарушенной маркировкой флакона, при изменении физических свойств раствора (мутность, окрашивание), неправильном хранении и/или с истекшим сроком годности.
Однодозовые флаконы
Перед вакцинированием флакон с компонентом Ⅰ или Ⅱ достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона!
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой.
Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту.
Для каждой инъекции необходимо использовать отдельный одноразовый стерильный шприц с иглой.
Внимание! Доза, вводимая пациенту, не должна превышать 0,5 мл!
Не допускается хранение размороженного препарата!
Повторное замораживание не допускается! Неиспользованная вакцина подлежит уничтожению.
Многодозовые флаконы
Перед вакцинированием флакон с компонентом Ⅰ или Ⅱ достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона!
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой.
Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту.
Для каждой инъекции необходимо использовать отдельный одноразовый стерильный шприц с иглой.
Внимание! Доза, вводимая пациенту, не должна превышать 0,5 мл!
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого или невскрытого размороженного флакона при комнатной температуре не более 2 часов.
Повторное замораживание не допускается! Неиспользованная вакцина подлежит уничтожению.
Внимание. К использованию непригоден препарат с дефектами укупорочной системы и/или нарушенной маркировкой флакона или ампулы, при изменении физических свойств раствора (мутность, окрашивание), неправильном хранении и/или с истекшим сроком годности.
▼ Информация для медицинских работников, выполняющих вакцинацию лекарственным препаратом: данный лекарственный препарат зарегистрирован по особой процедуре регистрации, в связи, с чем необходимо уведомлять Федеральную службу по надзору в сфере здравоохранения о каждом факте применения лекарственного препарата путём внесения информации в соответствующей раздел информационной системы ЕГИСЗ.
Побочное действие
Нежелательные явления (НЯ), характерные для применения вакцины, выявленные в рамках клинических исследований, а также исследований других вакцин на основе аналогичной технологической платформы, бывают преимущественно лёгкой или средней степени выраженности, могут развиваться в первые-вторые сутки после вакцинации и разрешаются в течение 3-х последующих дней. Чаще других могут развиться кратковременные общие (непродолжительный гриппоподобный синдром, характеризующийся ознобом, повышением температуры тела, артралгией, миалгией, астенией, общим недомоганием, головной болью) и местные (болезненность в месте инъекции, гиперемия, отёчность) реакции. Рекомендуется назначение нестероидных противовоспалительных средств (НПВС) при повышении температуры после вакцинации и антигистаминных средств при выраженной местной реакции.
Реже отмечаются тошнота, диспепсия, снижение аппетита, иногда — увеличение регионарных лимфоузлов. У некоторых пациентов возможно развитие аллергических реакций, кратковременное повышение уровня печёночных трансаминаз, креатинина и креатинфосфокиназы в сыворотке крови.
В рамках проведённых клинических исследований безопасности, переносимости и иммуногенности препарата Гам-КОВИД-Вак после вакцинации были зарегистрированы следующие нежелательные реакции:
«Общие нарушения и реакции в месте введения»: часто — гипертермия, боль, отёк, зуд в месте вакцинации, астения, боль, недомогание, пирексия, повышение температуры кожи в месте вакцинации, снижение аппетита.
«Желудочно-кишечные нарушения»: часто — тошнота, рвота, диспепсия.
«Нарушения со стороны дыхательной системы, органов грудной клетки и средостения»: часто — боль в ротоглотке, заложенность носа, першение в горле, ринорея.
«Со стороны кожи и подкожной клетчатки»: очень редко — ангиоотёк, крапивница и сыпь (эритематозная, папулёзная).
«Нарушения со стороны иммунной системы»: очень редко — анафилактический шок, анафилактическая реакция и гиперчувствительность.
«Со стороны крови и лимфатической системы»: редко — увеличение регионарных лимфоузлов.
«Нарушения со стороны нервной системы»: часто — головная боль; редко — головокружения, обмороки; очень редко — сообщается о единичных случаях воспалительной полиневропатии (причинно-следственная связь с лекарственным препаратом не установлена — частота данных событий в популяции имеет сезонный характер и может быть связана с различными причинами: провоцирующими факторами могут быть инфекционные заболевания вирусной и бактериальной этиологии, хирургические вмешательства, травматическое повреждение периферических нервов, любая вакцинация, аутоиммунные и системные заболевания).
«Лабораторные и инструментальные данные»: разнонаправленные отклонения показателей иммунологического статуса: повышение числа T-лимфоцитов, увеличение процентного содержания лимфоцитов, снижение числа естественных клеток-киллеров, увеличение количества СО4-лимфоцитов, снижение количества СО4-лимфоцитов, повышение числа B-лимфоцитов, снижение числа B-лимфоцитов, повышение числа естественных клеток-киллеров, повышение количества CDS-лимфоцитов, повышение уровня иммуноглобулина E (IgE) в крови, увеличение соотношения CD4/CD8, уменьшение соотношения CD4/CD8, повышение уровня иммуноглобулина A (IgA) в крови, уменьшение процентного содержания лимфоцитов CD8. Отклонения в общем анализе крови: увеличение процентного содержания лимфоцитов, снижение показателя гематокрита, увеличение числа лимфоцитов, повышение скорости оседания эритроцитов, повышение числа лейкоцитов, повышение числа моноцитов, повышение числа тромбоцитов, снижение числа нейтрофилов, снижение числа тромбоцитов. Отклонение показателей биохимического анализа крови: повышение уровня печёночных трансаминаз, креатинина и креатинфосфокиназы в сыворотке крови. Отклонения в общем анализе мочи: эритроциты в моче. Большинство НЯ завершились выздоровлением без последствий. Лабораторные отклонения не имели клинического значения (не нуждались в проведении дополнительных диагностических процедур и назначении терапии).
Передозировка
О случаях передозировки не сообщалось.
Учитывая, что отпуск лекарственного препарата допускается только для лечебно-профилактических учреждений, а сама вакцинация проводится только квалифицированным медицинским персоналом, риск передозировки крайне низок.
Однако можно предположить, что при случайной передозировке возможно развитие указанных выше токсических и токсико-аллергических реакций в более тяжёлой степени.
Специфических антидотов к препарату не существует.
Терапевтические мероприятия в данном случае будут включать симптоматическую терапию в соответствии с показаниями (жаропонижающие/ НПВС и десенсибилизирующие средства), кортикостероиды — парентерально при выраженном токсико-аллергическом синдроме). Режим назначения препаратов должен быть выбран согласно рекомендациям по применению и дозировкам данного лекарственного средства.
Взаимодействие с другими лекарственными средствами
Специальных исследований лекарственных взаимодействий не проводилось.
Взаимодействие с вакциной для профилактики гриппа изучено в доклинических исследованиях, показано отсутствие снижения иммуногенности как вакцины Гам-КОВИД-Вак (Комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2), так и гриппозной вакцины в эксперименте при их одновременном введении. Ожидается отсутствие снижения иммуногенности для расщепленных, субъединичных и полимерсубъединичных гриппозных вакцин.
Не допускается смешивание вакцины Гам-КОВИД-Вак с другими вакцинами или иными лекарственными средствами в одном шприце, так как нет данных о фармацевтическом взаимодействии.
Особые указания
У пациентов, получающих иммуносупрессивную терапию, и пациентов с иммунодефицитом может не развиться достаточный иммунный ответ.
Поэтому приём препаратов, угнетающих функцию иммунной системы, противопоказан в течение, как минимум, 1 месяца до и после вакцинации из-за риска снижения иммуногенности.
Подобно остальным вакцинам, защитный иммунный ответ может возникать не у всех вакцинируемых лиц.
При принятии врачом (медицинским работником) решения о необходимости одновременного введения Гам-КОВИД-Вак с другой вакциной, не допускается их смешивание в одном шприце и введение в один участок тела.
▼ Данный лекарственный препарат зарегистрирован по процедуре регистрации препаратов, предназначенных для применения в условиях угрозы возникновения, возникновения и ликвидации чрезвычайных ситуаций.
Инструкция подготовлена на основании ограниченного объёма клинических данных по применению препарата и будет дополняться по мере поступления новых данных. Применение препарата возможно только в условиях медицинских организаций, имеющих право осуществлять вакцинопрофилактику населения в установленном порядке.
Влияние на способность управлять транспортными средствами, механизмами
Исследования по изучению влияния вакцины на способность управлять транспортными средствами и потенциально опасными механизмами не проводились.
Форма выпуска
Раствор для внутримышечного введения, компонент Ⅰ — 0,5 мл/доза + компонент Ⅱ — 0,5 мл/доза.
Замороженный препарат
При производстве ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России):
по 0,5 мл (1 доза) каждого компонента препарата во флаконы нейтрального стекла, герметично укупоренные пробками из резины, обжатые алюминиевыми или алюмопластиковыми колпачками.
1 флакон компонента Ⅰ с инструкцией по применению помещают в пачку картонную или в пачку из картона коробочного; 1 флакон компонента Ⅱ с инструкцией по применению помещают в пачку картонную или в пачку из картона коробочного.
По 5 флаконов компонента Ⅰ или компонента Ⅱ помещают в контурную ячейковую упаковку из плёнки поливинилхлоридной. По 1 или 2 контурные ячейковые упаковки с компонентом Ⅰ или компонентом Ⅱ вместе с инструкцией по применению помещают в пачку картонную или в пачку из картона коробочного.
При производстве АО «Биннофарм»:
по 0,5 мл (1 доза) каждого компонента препарата в ампулы из бесцветного стекла с цветной точкой.
По 5 ампул каждого компонента препарата помещают в контурную ячейковую упаковку из плёнки поливинилхлоридной.
По 1 или 2 контурных ячейковых упаковки вместе с инструкцией по применению помещают в пачку из картона.
При производстве на АО «ГЕНЕРИУМ»:
по 3,0 мл (5 доз) каждого компонента — во флаконы, укупоренные пробками резиновыми, с обкаткой колпачками алюминиево-пластиковыми с контролем первого вскрытия.
1 флакон с компонентом Ⅰ или компонентом Ⅱ вместе с инструкцией по медицинскому применению — в пачке из картона с поролоновым держателем из пенополиуретана.
При производстве на ЗАО «ЛЕККО»:
по 3 мл (5 доз) каждого компонента препарата — во флаконы, укупоренные пробками резиновыми, с обкаткой колпачками алюминиево-пластиковыми с контролем первого вскрытия.
По 1 флакону с компонентом Ⅰ или с компонентом Ⅱ вместе с инструкцией по применению помещают в пачку из картона с поролоновым держателем из пенополиуретана.
При производстве на ОАО «Фармстандарт-УфаВИТА»:
по 0,5 мл (1 доза) или по 1,0 мл (2 дозы) каждого компонента препарата в ампулы из бесцветного стекла.
По 5 ампул каждого компонента препарата — в контурную ячейковую упаковку из плёнки поливинилхлоридной.
По 1 или 2 контурные ячейковые упаковки вместе с инструкцией по применению — в пачку из картона.
По 1 контурной ячейковой упаковке вместе с инструкцией по применению — в пачку из картона.
По 3 мл (5 доз) каждого компонента препарата — во флаконы, укупоренные пробками резиновыми, с обкаткой колпачками алюминиево-пластиковыми с контролем первого вскрытия.
По 1 флакону с компонентом Ⅰ или с компонентом Ⅱ вместе с инструкцией по применению — в пачку из картона с поролоновым держателем из пенополиуретана
При производстве на ЗАО «БИОКАД»:
по 0,5 мл (1 доза) или по 3,0 мл (5 доз) каждого компонента препарата во флаконы из нейтрального стекла Ⅰ гидролитического класса (типа 2R, 6R), герметично укупоренные резиновыми пробками, с обкаткой алюминиевыми колпачками с пластиковой крышкой типа «flip-off».
На флаконы каждого компонента препарата наклеивают этикетку самоклеящуюся.
1 флакон 6R с компонентом Ⅰ или компонентом Ⅱ с инструкцией по применению помещают в пачку картонную.
1 флакон 2R с компонентом Ⅰ или компонентом Ⅱ в контурной ячейковой упаковке из ПВХ плёнки с инструкцией по применению помещают в пачку картонную.
При производстве АО «Р-Фарм»:
по 0,5 мл (1 доза) каждого компоненте лекарственного препарата или по 3,0 мл (5 доз) компонента Ⅰ — во флаконы из нейтрального стекла Ⅰ гидролитического класса типа 2R (для однодозовых флаконов) или 10R (для пятидозовых флаконов), герметично укупоренные пробками из резины и обжатые алюмопластиковыми колпачками.
По 1, 2, 5 или 10 флаконов с компонентом Ⅰ или компонентом Ⅱ по 0,5 мл (1 доза) или по 1 или 10 флаконов с компонентом Ⅰ по 3,0 мл (5 доз) вместе с инструкцией по применению в пачку из картона.
При производстве на ООО «СПУТНИК ТЕХНОПОЛИС» (компонент Ⅱ):
по 3,0 мл (5 доз) компонента Ⅱ — во флаконы из нейтрального стекла Ⅰ гидролитического класса типа 10R герметично укупоренные пробками из резины и обжатые алюмопластиковыми колпачками.
По 1 или 10 флаконов с компонентом Ⅱ вместе с инструкцией по применению в пачку из картона.
Жидкий препарат
При производстве на АО «ГЕНЕРИУМ»:
по 3,0 мл (5 доз) каждого компонента — во флаконы, укупоренные пробками резиновыми, с обкаткой колпачками алюминиево-пластиковыми с контролем первого вскрытия.
1 флакон с компонентом Ⅰ или с компонентом Ⅱ в контурной ячейковой упаковке из плёнки поливинилхлоридной или полиэтилентерефталатной вместе с инструкцией по медицинскому применению — в пачку из картона или без контурной ячейковой упаковки вместе с инструкцией по медицинскому применению — в картонную пачку с поролоновым держателем из пенополиуретана.
При производстве на ЗАО «ЛЕККО»:
по 3 мл (5 доз) каждого компонента препарата — во флаконы, укупоренные пробками резиновыми, с обкаткой колпачками алюминиево-пластиковыми с контролем первого вскрытия.
1 флакон с компонентом Ⅰ или с компонентом Ⅱ в контурной ячейковой упаковке из плёнки поливинилхлоридной или полиэтилентерефталатной вместе с инструкцией по медицинскому применению — в пачку из картона или без контурной ячейковой упаковки вместе с инструкцией по медицинскому применению — в картонную пачку с поролоновым держателем из пенополиуретана.
При производстве на ОАО «Фармстандарт-УфаВИТА»:
по 0,5 мл (1 доза) каждого компонента препарата в ампулы из бесцветного стекла.
По 5 ампул каждого компонента препарата — в контурную ячейковую упаковку из плёнки поливинилхлоридной.
По 1 контурной ячейковой упаковке вместе с инструкцией по применению — в пачку из картона.
При производстве на ЗАО «БИОКАД»:
по 0,5 мл (1 доза) или по 3,0 мл (5 доз) каждого компонента препарата во флаконы из нейтрального стекла Ⅰ гидролитического класса (типа 2R, 6R), герметично укупоренные резиновыми пробками, с обкаткой алюминиевыми колпачками с пластиковой крышкой типа «flip-off».
На флаконы каждого компонента препарата наклеивают этикетку самоклеящуюся.
1 флакон 6R с компонентом Ⅰ или компонентом Ⅱ с инструкцией по применению помещают в пачку картонную.
1 флакон 2R с компонентом Ⅰ или компонентом Ⅱ в контурной ячейковой упаковке из ПВХ плёнки с инструкцией по применению помещают в пачку картонную.
Хранение
Замороженный препарат
Хранить в защищённом от света месте, при температуре не выше минус 18 °C. Повторное замораживание не допускается.
Хранить в недоступном для детей месте.
Жидкий препарат
Хранить в защищённом от света месте, при температуре от 2 до 8 °C. Не замораживать.
Хранить в недоступном для детей месте.
Условия транспортирования
Замороженный препарат
При температуре не выше минус 18 °C.
Для флаконов по 0,5 мл производства ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России), флаконов по 3,0 мл производства АО «ГЕНЕРИУМ», ЗАО «ЛЕККО», ОАО, «Фармстандарт-УфаВИТА» и ампул по 0,5 мл производства ОАО «Фармстандарт-УфаВИТА» допускается повышение температуры не выше минус 10 °C не более 3 суток.
Жидкий препарат
При температуре от 2 до 8 °C. Не замораживать.
Срок годности
Замороженный препарат
Производственная площадка ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России), Россия:
Компонент Ⅰ — 1 год. Компонент Ⅱ — 1 год.
Производственные площадки АО «Биннофарм», Россия, АО «ГЕНЕРИУМ», Россия, ЗАО «БИОКАД», Россия, ЗАО «ЛЕККО», Россия, ОАО «Фармстандарт-УфаВИТА», Россия, АО «Р-Фарм», Россия:
Компонент Ⅰ — 6 месяцев. Компонент Ⅱ — 6 месяцев.
Производственная площадка ООО «СПУТНИК ТЕХНОПОЛИС», Россия:
Компонент Ⅱ — 6 месяцев.
Не применять по истечении срока годности.
Жидкий препарат
Производственные площадки АО «ГЕНЕРИУМ», Россия, ОАО «Фармстандарт-УфаВИТА», Россия:
Компонент Ⅰ — 6 месяцев. Компонент Ⅱ — 6 месяцев.
Производственные площадки ЗАО «ЛЕККО», Россия, ЗАО «БИОКАД», Россия:
Компонент Ⅰ — 2 месяца. Компонент Ⅱ — 2 месяца.
Не применять по истечении срока годности.
Не применять по истечении срока годности.
Условия отпуска: для лечебно-профилактических учреждений.
Условия отпуска из аптек
Для лечебно-профилактических и санитарно-профилактических учреждений.
Производитель
Медгамал (филиал НИИ эпидемиологии и микробиологии им.Н.Ф.Гамалеи РАМН ГУ),
Российская Федерация
Биннофарм, ЗАО,
Российская Федерация
ГЕНЕРИУМ, ЗАО,
Российская Федерация
Фармацевтическая фирма ЛЕККО, ЗАО,
Российская Федерация
Фармстандарт-УфаВИТА, ОАО,
Российская Федерация
БИОКАД, ЗАО,
Российская Федерация
Р-Фарм, ЗАО,
Российская Федерация
СПУТНИК ТЕХНОПОЛИС, ООО,
Российская Федерация
Наименования и адреса производственных площадок производителя лекарственного препарата:
- ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России), Россия, 123098. г. Москва, улица Гамалеи, д. 18. (все стадии производства).
- АО «Биннофарм», Россия, 124460, г. Москва, г. Зеленоград, ул. Конструктора Гуськова, д. 3, стр. 1 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
- АО «ГЕНЕРИУМ», Россия, 601125, Владимирская обл., Петушинский район, пос. Вольгинский, ул. Заводская, стр. 263, (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
- ЗАО «Фармацевтическая фирма «ЛЕККО» (ЗАО «ЛЕККО»), Россия, 601125, Владимирская обл., Петушинский район, пос. Вольгинский, ул. Заводская, стр. 277; 601125, Владимирская обл., Петушинский район, пос. Вольгинский, ул. Заводская, стр. 279 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
- ОАО «Фармстандарт-Уфимский витаминный завод» (ОАО «Фармстандарт-УфаВИТА»), Россия, Республика Башкортостан, г. Уфа, ул. Худайбердина, д. 28 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
- ЗАО «БИОКАД», Россия, 198515, г. Санкт-Петербург, внутригородское муниципальное образование Санкт-Петербурга п. Стрельна, ул. Связи, д. 38. стр. 1 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
- АО «Р-Фарм», Россия, 150061, Ярославская обл., г.о. г. Ярославль, г. Ярославль, ул. Громова, д. 15 (производство, первичная и вторичная (потребительская) упаковка)
- ООО «СПУТНИК ТЕХНОПОЛИС» (компонент Ⅱ), 109316, Россия, г. Москва, проспект Волгоградский, д. 42, к. 5 (производство, первичная и вторичная (потребительская) упаковка
Выпускающий контроль качества
Филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России. Россия, 123098, г. Москва, улица Гамалеи, д. 18.
Владелец регистрационного удостоверения/организация, принимающая претензии потребителя:
ФГБУ «Национальный исследовательский центр эпидемиологии и микробиологии имени почётного академика Н.Ф. Гамалеи» Министерства здравоохранения Российской Федерации (ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России).
Россия. 123098. г. Москва, улица Гамалеи, д. 18.
Тел: 8 499-193-30-01, факс: 8 499-193-61-83.
Защищает ли «Спутник V» от штамма омикрон?
Штамм коронавируса омикрон быстро распространяется по планете. Он более заразен, чем другие варианты, в том числе и дельта. Поэтому многие люди интересуются, защищает ли «Спутник V» от омикрона.
Директор центра им. Гамалеи Александр Гинцбург заявил, что «Спутник V» против омикрона показывает достаточную эффективность (75%), а при ревакцинации «Спутником Лайт» эфективность увеличивается почти до 100%. Поэтому «Спутник V» не нужно модифицировать под новый штамм. Это объясняется тем, что в данном препарате структура S-белка динамичная и способна изгибаться в пространстве. Это способствует выработке в организме привитых людей широкого спектра нейтрализующих антител. Для полноценной защиты от омикрона» «Спутник V» применяют по обычной схеме — двукратная вакцинация с интервалом в 21 день, а затем введение бустерной дозы («Спутник Лайт») через 6 месяцев.
Тем временем иностранные мРНК-вакцины (Moderna, Pfizer/BioNTech) в настоящее время проходят модификацию под омикрон, так как их эффективность с приходом нового штамма значительно снизилась. В мРНК-вакцинах в молекуле S-белка пространственное расположение атомов фиксировано. И они достаточно эффективны против первоначального штамма коронавируса, который называют уханьским. Но при этом мРНК-вакцины хуже защищают от новых штаммов коронавируса.
Эффективность «Спутника V» против омикрона
Специалисты НИИЭМ им. Гамалеи совместно с сотрудниками Национального института инфекционных заболеваний им. Ладзаро Спалланцани (Италия) провели исследования эффективности «Спутника V» против штамма омикрон. Предварительные результаты опубликованы на платформе препринтов medRxiv⁸.
В ходе исследования выяснилось, что у людей, привитых «Спутником V», вырабатывается в два раза больше антител к омикрону, чем у тех, кто привился вакциной Pfizer. То есть «Спутника V» дает более сильный иммунный ответ на новый вариант коронавируса. А «Спутник Лайт» в качестве бустера (третья вакцина) значительно увеличивает вируснейтрализующую активность против штамма омикрон.
Описание вакцины Спутник V
Вакцину разработали сотрудники Национального исследовательского центра эпидемиологии и микробиологии им. Н. Ф. Гамалеи, и 11 августа 2020 года она прошла официальную регистрацию в Министерстве здравоохранения РФ.
У препарата два наименования:
- торговое — «Спутник V»;
- регистрационное — «Гам-Ковид-Вак».
Коммерческое название вакцина получила в честь первого советского космического спутника, запущенного в 1957 году — «Спутник-1». Буква V символизирует английское слово victory, которое переводится на русский язык как «победа». Таким «громким» названием создатели вакцины образно показали, что при разработке препарата использовали самые современные технологии, а его применение поможет победить коронавирусную инфекцию.
Первую и вторую фазы клинических испытаний «Гам-Ковид-Вак» завершили в августе 2020 года. В феврале 2021 года в авторитетном медицинском журнале The Lancet опубликовали итоги третьей фазы исследований препарата в России.
Производители вакцины
Сегодня производство «Спутника V» в России идет на 9 промышленных площадках — это гарантирует бесперебойные поставки препарата для населения РФ. Кроме того, российскую вакцину производят и во многих зарубежных странах:
- Казахстане;
- Республике Корея;
- Бразилии;
- Белоруссии;
- Аргентине;
- Индии;
- Сербии;
- Иране;
- Италии;
- Армении;
- Мексике;
- Вьетнаме;
- Узбекистане.
Производители вакцины в Бразилии не только покрывают потребности внутреннего рынка, но и направляют препарат в другие страны Латинской Америки.
Вне зависимости от того, где производят вакцину «Спутник V», упрепарата одинаковый состав и эффективность.
Применение
Люди старше 60 лет находятся в зоне риска, смертность среди них велика. Вакцину «Спутник V» успешно испытали на добровольцах. Поэтому Минздрав одобрил применение «Спутника V» для людей старше 60 лет.
В настоящее время проводятся исследования, направленные на изучение возможного тератогенного действия (нарушения эмбрионального развития) вакцины «Спутник V». Промежуточные результаты показывают, что препарат не оказывает на развитие плода негативного влияния. Поэтому применение вакцины «Спутник V» одобрено для беременных и кормящих женщин.
Прививаться ли беременным?
«Беременным женщинам прививаться нужно обязательно, так как для них ковид особенно опасен. Случаи гибели плода у больной матери не единичны, в то же время нет данных, говорящих о том, что «Спутник V» провоцирует выкидыши, скорее наоборот — вакцина защищает мать и дитя. Привитая кормящая мать через молоко передаст антитела младенцу и тем защитит его от коронавируса тоже».



Отличия «Спутника V» от других векторных вакцин
Векторные вакцины представляют собой отдельный класс препаратов для создания иммунной защиты. При их производстве используют относительно безопасные для человека неспособные к репликации вирусы, которые «доставляют» в организм один или несколько генов белков возбудителя инфекции.
Векторные вакцины отличаются высокой эффективностью и безопасностью, в том числе и в долгосрочной перспективе. Это подтвердили результаты свыше 250 клинических исследований, которые проводили на протяжении последних 20 лет.⁴
«Спутник V» создали на платформе аденовирусов — возбудителей обычных простудных заболеваний у людей. Свойства этих вирусов хорошо известны, поэтому реакции организма на их введение предсказуемы.
Разработка института им. Н. Ф. Гамалеи отличается от других векторных вакцин способом изготовления — в основе лежит принцип гетерогенного бустирования. На каждом из двух этапов людям вводят разные векторы. Такой вариант вакцинирования определяет более выраженный иммунный ответ и надежную защиту от инфекционного заболевания.
Суть вакцины «Спутника V»
Болезнетворные микроорганизмы, которые способны вызвать развитие заболевания, называются антигенами. При их попадании в организм иммунная система начинает образовывать защитные антитела. Она как солдаты-защитники атакует антигены и тем самым предотвращает возникновение заболевания, либо обеспечивает его легкое протекание.
Суть вакцины «Спутник V» заключается в том, что человеку вводится «программа» для выработки клетками антигена коронавируса. Она не вызовет развитие заболевания, но «обучит» иммунную систему распознавать и активно атаковать при встрече вирус SARS-CoV-2. Благодаря этому у вакцинированных людей значительно снижается риск развития тяжелых форм коронавирусной инфекции.
Эффективна ли вакцина «Спутник V»?
«Эффективность вакцины «Спутник V» высокая, хотя к ней были вопросы по поводу проведения клинических исследований. Но сейчас уже опубликованы результаты 1-2 фазы и промежуточной стадии 3-й фазы клинических испытаний, а также накопилось довольно много свидетельств из других стран, да и в России тоже. Люди, вакцинированные «Спутником V», практически не попадают в больницу с коронавирусом. Этого уже вполне достаточно для того чтобы считать эту вакцину достаточно эффективной. Среди тех, кто вакцинировался «Спутником V», госпитализированных с коронавирусом меньше 1%. Это единичные случаи среди людей, у которых нарушена иммунная система или им не повезло с формированием иммунитета. Может показаться, что таких сообщений много, но по сравнению с количеством вакцинированных, это доли процента. А антипрививочникам я бы посоветовал сходить на экскурсию в реанимацию ковидного госпиталя, где в ужасных мучениях лежат непривитые люди. Они хрипят, им не хватает воздуха. Тот, кто там побывал, испытал настоящий шок от увиденного».



Состав вакцины «Спутник V»
Действующее вещество вакцины — аденовирусный вектор. Он представляет собой аденовирус человека, неспособный к размножению, поскольку у него удалена часть генетического материала. Вместо удаленной части в него искусственно «встраивают» ген, который кодирует синтез S-белка коронавируса SARS-CoV-2.
«Спутник V» состоит из двух компонентов:
- компонент I — вектор на основе аденовируса серотипа 26 (Ad26);
- компонент II — вектор на основе аденовируса 5 серотипа (Ad5).
В качестве вспомогательных компонентов в состав вакцины входят:
- трис(гидроксиметил)аминометан — вспомогательный буферный раствор;
- натрия хлорид — соль для поддержания нужной осмолярности;
- сахароза — стабилизатор;
- ЭДТА динатриевая соль дигидрат — стабилизатор;
- полисорбат — стабилизатор;
- магния хлорид — консервант;
- этиловый спирт — консервант.²
Вакцина состоит из двух компонентов, которые необходимо ввести с разницей в 3 недели. В качестве первого препарата человек получает вектор Ad26, затем ему вводят вторую дозу с вектором Ad5. Вспомогательные вещества в обоих растворах остаются неизменными.
Принцип действия
Аденовирусный вектор в вакцине представляет собой «транспортное средство», которое доставляет генетический материал SARS-CoV-2 в клетки тела человека. В результате они начинают вырабатывать S-белок коронавируса — эта структура входит в состав оболочки вируса и образует его характерные «шипы».
Если человек, который получил прививку, в дальнейшем встретится с коронавирусом, выработанные антитела «распознают» уже знакомый S-белок и начнут «атаковать» его, а затем Т-лимфоциты будут уничтожать зараженные им клетки. Благодаря этому заболевание либо не разовьется совсем, либо будет протекать в легкой форме.
После введения первого компонента иммунная система начинает вырабатывать антитела не только к S-белку, но и к «вектору», к белкам аденовируса. Поэтому для повторного введения препарата нельзя использовать первоначальный аденовирусный компонент — иначе он может быть уничтожен антителами еще до момента внедрения в клетки. Для предотвращения такого развития событий производители вакцины «Спутник V» решили использовать два разных серологических типа аденовируса.
После введения второго компонента препарата «Спутник V» происходит формирование большего числа иммунных В-клеток памяти — они «запоминают» возбудителя заболевания и дают организму длительный иммунитет. Так, первая доза прививки помогает иммунной системе «ознакомиться» с вирусом, а вторая уже «обучает» ее активной защите.
Полноценный иммунный ответ формируется на 42-й день от момента начала вакцинации или через 21 день после введения второго компонента препарата.
Для определения поствакцинального иммунитета можно сделать тест ИФА на антитела к S-белкам коронавируса. Но следует внимательно подойти к сдаче анализа и не перепутать методы исследования. Существуют тест-системы, которые предназначены для обнаружения антител к N-белку коронавируса. Они позволяют выявить постинфекционный иммунитет — ответ, который сформировался после перенесенной болезни. У людей после вакцинации этот показатель, как правило, отрицательный, но это не означает отсутствие иммунитета к коронавирусу. Эту разницу в тест-системах необходимо учитывать при сдаче анализа.¹
Что происходит в организме после вакцинации?
«Принцип действия векторной вакцины «Спутник V» очень простой — он как бы имитирует заражение, заставляет клетку саму производить шиповидный белок коронавируса, поэтому активируются оба звена иммунитета — и гуморальное, и клеточное.
После проникновения в клетку аденовирус теряет оболочку, его ДНК идет в ядро клетки, но никуда не встраивается, а пользуется фабрикой клетки для производства в цитоплазме спайк-белка. Частично он встраивается в мембрану клетки, секретируется в межклеточную жидкость, частично разрушается и представляется на ее поверхности комплексом гистосовместимости. Место инъекции ни аденовирусный вектор, ни сам спайк-белок не покидают и в кровоток практически не попадают.
Секретируемый спайк-белок в межклеточном пространстве подбирают дендритные клетки и макрофаги. Они представляют его эпитопы В- и Т- лимфоцитам. В-клетки и сами могут связать антиген и поглотить его, а затем представить на поверхности. Т-хелперы узнают такие В-лимфоциты, связываются с ними и активируют их клональное размножение и дифференцировку. В результате образуются плазматические клетки, производящие антитела и В-клетки памяти. Отличительной особенностью векторных вакцин является активация клеточного иммунитета и образование Т-клеток памяти, причем как хелперов, так и киллеров. Этим векторные вакцины выгодно отличаются от инактивированных, где Т-клеточный ответ развивается значительно слабее.
В зависимости от степени активации иммунной системы образуется много или мало антител и клеток памяти. При встрече с антигеном клетки памяти способны быстро активироваться, размножиться и дать сильный ответ — на этом основан эффект буста, или усиления иммунного ответа при повторной встрече с антигеном. Поэтому переболевшие люди, уже имеющие клетки памяти, развивают более сильный ответ после вакцинации, чем не болевшие. Прививка выделяет и усиливает у них протективную составляющую из уже имеющегося иммунитета к ковиду».



Эффективность вакцины
Полный курс вакцинации «Гам-Ковид-Вак» дает высокий уровень защиты взрослых людей от новой коронавирусной инфекции. Результаты исследований сообщают, что эффективность этой российской вакцины достигает 97,6%⁴. По словам директора Национального исследовательского центра эпидемиологии и микробиологии им. Н.Ф. Гамалеи Александра Гинцбурга, эффективность «Спутника V» против штамма дельта составляет 83-94%, против штамма омикрон — 75%.
Сотрудниками НИЦЭМ им. Н. Ф. Гамалеи были проведены исследования, во время которых они изучали эффективность вакцины «Спутник V» против новых мутаций коронавирусной инфекции:
- английского — Alpha B. 1.1.7;
- южноафриканского — Beta B.1.351;
- бразильского — Gamma P.1;
- индийских — Delta B.1.617.2 и B.1.617.3;
- российских — B.1.1.141 и B.1.1.317;
- омикрона — B.1.1.529.
Результаты показали, что вакцинация «Спутником V» приводит к выработке достаточно высокого титра антител ко всем новым штаммам коронавируса. Эти выводы были опубликованы в международном журнале «Vaccines».6
Только «Спутник V». Альтернативы нет
«В России в качестве первой вакцины стоит выбирать только «Спутник V». Это единственная российская вакцина с опубликованными данными и доказанной эффективностью и безопасностью. Эффективность «КовиВака» не ясна. «ЭпиВакКорона» – неудачная вакцина, после нее не образуются нейтрализующие антитела. Переболевшим людям с высокими антителами вполне хватит вакцины «Спутник Лайт», с низкими лучше сделать «Спутник V».



Подготовка к вакцинации
Применение вакцины «Гам-Ковид-Вак» не требует какой-либо специальной подготовки. Желающим привиться не нужно сдавать кровь на антитела к коронавирусу или делать ПЦР-тест, чтобы исключить ковид. Самое главное условие — у человека должно быть хорошее общее самочувствие.
Влияние вакцины на организм человека — это всегда индивидуальная реакция. Поэтому непосредственно перед прививкой необходимо пройти осмотр врача — при отсутствии противопоказаний специалист даст разрешение на вакцинацию.
В инструкции к препарату указаны состояния, при которых следует отложить его введение или даже отказаться от прививки. К таким противопоказаниям относятся:
- повышенная индивидуальная чувствительность к любому из компонентов вакцины;
- тяжелые поствакцинальные осложнения во время предыдущего введения вакцины или ее компонентов (анафилактический шок, судороги, температура выше 40°С, отек или гиперемия в месте введения инъекции, тяжелая аллергическая реакция);
- указание на перенесенные ранее тяжелые аллергические реакции;
- острые неинфекционные и инфекционные заболевания (в период болезни и 2-4 недели после выздоровления);
- хронические заболевания в периоде обострения (и 2-4 недели после выздоровления);
Согласно данным производителей, вакцинация возможна спустя 2–4 недели после выздоровления при острых заболеваниях или при переходе хронических патологий в неактивную фазу. При легком течении острых респираторных и кишечных инфекций введение препарата допускается сразу после нормализации температуры тела.5
Возраст младше 18 лет также считается противопоказанием к вакцинации «Спутником V». Это связано с тем, что отсутствуют данные как об эффективности, так и о безопасности использования препарата у детей и подростков².
Вакцинация подростков
В конце ноября 2021 года НИЦЭМ им. Н. Ф. Гамалеи зарегистрировал вакцину для детей «Спутник М» — концентрация в ней снижена в 5 раз. Прививать подростков 12-17 планировали начать в конце декабря 2021 года, но вакцинация детей началась только в конце января 2022 года. Для этого нужно согласие родителей, а если подростку уже есть 15 лет, он может принять решение сделать прививку самостоятельно.
Также есть список заболеваний, при которых вакцину следует применять с большой осторожностью. Он включает в себя следующие патологии:
- эпилепсия;
- сахарный диабет в тяжелой форме;
- значительное нарушение функций щитовидной железы;
- злокачественные новообразования;
- аутоиммунные заболевания;
- тяжелые заболевания системы крови.
Перед введением второй дозы препарата необходимо также проконсультироваться с врачом — тяжелая реакция на первый раствор может стать противопоказанием для продолжения вакцинации «Спутником V».
На 17 января 2022 года Россия по доле вакцинированного населения стоит на 94 месте в мире (46,80% привитых людей).
Вакцинация у многих вызывает вопросы, и люди с недоверием относятся к новой разработке, поэтому некоторые покупают сертификаты. Выяснить точный процент поддельных сертификатов невозможно, однако директор НИЦЭМ им. Н. Ф. Гамалеи, Александр Гинцбург, заявил, что 80% тяжело перенесших болезнь людей купили документ о вакцинации.
Как проходит вакцинация
Непосредственно перед вакцинацией человеку измеряют артериальное давление и температуру тела, определяют сатурацию — насыщение крови кислородом. «Спутник V» вводят только внутримышечно. Инъекцию делают в дельтовидную мышцу — верхнюю треть наружной поверхности плеча.
При первой прививке вводят компонент I. Через 21 день необходимо снова посетить прививочный кабинет для второго этапа вакцинации — введения компонента II.
После выполнения прививки следует оставаться под наблюдением медицинских работников в течение 30 минут. Особенно важно соблюдать это условие людям, которые склонны к аллергическим реакциям.
Что нельзя делать после вакцинации
В течение 2–3 дней после вакцинации важно дать организму возможность отдохнуть — исключить высокие нагрузки и не подвергать его стрессовым ситуациям. Это создаст оптимальные условия для полноценного иммунного ответа, и эффект от прививки будет максимальным. После вакцины в течение 3 дней не рекомендуется:
- употреблять алкогольные напитки;
- принимать солнечные ванны или посещать солярий;
- мочить место инъекции;
- купаться в бассейне или открытом водоеме;
- проводить интенсивные физические тренировки.
Также после введения препарата важно полноценно питаться с достаточным количеством белковой пищи. Нельзя соблюдать строгую диету — отсутствие витаминов и полезных питательных веществ может препятствовать образованию антител.
Ревакцинация
Через некоторое время после прививки количество антител в крови начинает снижаться. Для его поддержания на достаточном для полноценной защиты уровне необходимо повторное введение вакцины — ревакцинация от коронавируса.
В соответствии с временными методическими рекомендациями Минздрава РФ, в настоящее время действует правило «экстренной ревакцинации». Поэтому повторное введение вакцины должно проводиться каждые 6 месяцев.
После того как будет достигнут коллективный иммунитет, то есть прививку получит не менее 60% взрослого населения страны и эпидемия пойдет на спад, начнут действовать правила «рутинной вакцинации». Тогда повторное введение вакцины будет проводиться один раз в год⁶.
После вакцинации «Спутником V» ревакцинацию выполняют препаратом «Спутник Лайт». Повторная иммунизация приводит к увеличению уровня антиген-специфических IgG антител более чем в 40 раз у 100% привитых людей⁴.
Побочные эффекты вакцины Спутник V
При проведении клинических испытаний выявили, что побочные эффекты после вакцинации «Спутником V» обычно отличаются легкой или среднетяжелой степенью выраженности. Они могут возникнуть в первые 48 часов после прививки, но в течение последующих 72 часов проходят самостоятельно.
Среди побочных эффектов от введения препарата чаще всего наблюдается развитие непродолжительного гриппоподобного синдрома с симптомами:
- общее недомогание;
- головная и мышечная боль;
- «ломота» в суставах;
- повышение температуры тела.
Этот синдром не требует лечения и не представляет опасности для человека. Для улучшения самочувствия при повышении температуры тела до 38,0 °С и выше следует принять жаропонижающее средство, например, парацетамол.
После прививки возможно развитие и местной реакции. Она проявляется болезненностью, отечностью и покраснением тканей в месте инъекции. Для устранения этих симптомов показан прием антигистаминных средств — препаратов с противоаллергическим действием.
К редким побочным эффектам, которые могут возникнуть после введения «Гам-Ковид-Вак», относятся:
- снижение аппетита;
- тошнота;
- увеличение лимфатических узлов;
- появление эритроцитов в моче.
Серьезных побочных эффектов после введения вакцины «Спутник V» во время клинических исследований не наблюдалось.
Риски и мифы
По данным Министерства здравоохранения РФ, при иммунизации «Спутником V» у пациентов регистрируются обычные поствакцинальные реакции — головная и мышечная боль, небольшое повышение температуры. Данные о тяжелых реакциях отсутствуют. Но несмотря на это, многие россияне относятся к препарату с опаской и отказываются от иммунизации.
Наибольшее опасение у людей вызывают следующие «мифы»:
1. Вакцинация вызывает бесплодие
Антипрививочники утверждают, что в состав шиповидного белка входит белок синцитин-1. Он необходим для нормального формирования плаценты. Однако в составе вакцины отсутствуют компоненты, которые могли бы вызвать образование антител к синцитину-1.
Что на самом деле. Чтобы утверждать, что «Спутник V» вызывает бесплодие, необходимо, чтобы женщины, прошедшие иммунизацию, на протяжении 1–2 лет безуспешно пытались забеременеть. А после этого прошли полный медицинский осмотр для выявления причины бесплодия, так как оно может быть обусловлено множеством иных причин.
2. Вакцина изменяет код ДНК
Да, в составе препарата присутствует вирусная ДНК. При помощи вектора она доставляется в клетки, которые начинают синтезировать S-белок. В ответ на его попадание в кровь иммунная система вырабатывает антитела. Через некоторое время «зараженные» клетки погибают и организм человека очищается от присутствия вирусной ДНК.
Что на самом деле. Мнение людей о высоком риске вакцины «Спутник V» во многом связано с недостаточной информированностью, верой в теорию конспиративного заговора, чипирования населения.
Где действует вакцина «Спутник V»
Применение препарата «Спутник V» для иммунизации населения одобрили в 69 странах, в которых проживает около 3,7 млрд человек. При этом вакцина доказала свою высокую эффективность и безопасность (табл. 1).
| Страна | Число вакцинированных | Эффективность после второй дозы | Эффективность против тяжелых случаев | Серьезные побочные реакции |
| Россия | 3 800 000 | 83,1% | 94,4% | нет |
| ОАЭ | 81 000 | 97,8% | 100% | нет |
| Бахрейн | 5 000 | 94,3% | 98,6% | нет |
| Аргентина | 5 000 000 | 100% | 100% | нет |
Россиян, получивших полный курс иммунизации против Covid-19, принимают без ПЦР-тестирования:
- Абхазия;
- Албания;
- Армения;
- Белоруссия;
- Босния и Герцеговина;
- Венгрия;
- Грузия;
- Египет;
- Иордания;
- Казахстан;
- Кипр;
- Ливан;
- Марокко;
- Мексика;
- Молдова;
- Монголия;
- Северная Македония;
- Словения;
- Таджикистан;
- Тунис;
- Турция;
- Узбекистан;
- Хорватия;
- Черногория.
С тестом ПЦР, сделанным не позднее чем за 72 часа до въезда в страну, россиян принимают:
- Азербайджан;
- Барбадос;
- Бахрейн;
- Венесуэла;
- Греция;
- Джибути;
- Зимбабве;
- Израиль;
- Индия;
- Иран;
- Катар;
- Кения;
- Маврикий;
- Мальдивы;
- ОАЭ;
- Сербия;
- Таиланд;
- Шри-Ланка.
Среди этих стран действует разный порядок въезда. Например, при посещении Таиланда или Индии турист предоставляет сертификат о вакцинации и результат ПЦР-теста, после чего он обязуется соблюдать временную изоляцию в течение 5–78 часов, до получения повторного отрицательного результата ПЦР-тестирования.
Вопросы и ответы о вакцине «Спутник V»
Все вакцины от коронавирусной инфекции в мире создавали в достаточно сжатые сроки. Поэтому несмотря на убедительные данные клинических исследований, которые подтверждают эффективность и безопасность российского препарата, вокруг «Спутника V» продолжаются дискуссии. Постараемся ответить на наиболее частые вопросы, которые пациенты задают врачам о вакцинации этим препаратом.
Нужно ли самоизолироваться после прививки Спутником V?
Вакцина не содержит в себе вируса, который мог бы привести к развитию заболевания COVID–19. Поэтому после прививки человек не может заразить им окружающих людей. Соответственно, самоизоляция ему не требуется.
Неоднократно слышал, что после прививки люди все равно заболевают. Зачем тогда ее делать?
В мире нет ни одной вакцины, которая смогла бы защитить от коронавирусной инфекции на 100%. Но данные исследований показывают, что заболеваемость среди людей, привитых «Спутником V», незначительная, и болезнь после вакцинации протекает в легкой форме, без развития осложнений.
На какой срок защищает «Спутник V» от коронавируса?
В настоящее время точно неизвестно, на какой именно срок препарат дает защиту от коронавируса. В крови сотрудников центра Н. Ф. Гамалеи, которых вакцинировали в марте 2020 года, антитела класса G (IgG) определялись спустя 9 месяцев после прививки. Важно отметить и тот факт, что их уровень был выше, чем у людей, которые переболели COVID-19.
Как часто необходимо делать ревакцинацию?
В соответствии с рекомендациями Министерства здравоохранения РФ, в условиях высокой заболеваемости повторное введение вакцины, то есть ревакцинацию, необходимо проводить каждые 6 месяцев. После того как иммунизацией будет охвачено 60–70% взрослых людей РФ, прививку станут выполнять в плановом порядке — один раз в год.³
Может ли второй этап вакцинации проводиться не через 21 день, а позже?
В соответствии с инструкцией к препарату, введение второго компонента «Гам-Ковид-Вак» проводят через 21 день после первой прививки. Но если человек по объективным причинам не может посетить прививочный кабинет, допускается проведение второго этапа позже. Также введение второго раствора переносят в случае развития у человека коронавируса в этот период.
Нужно ли делать ПЦР-тест перед вакцинацией?
Проведение ПЦР-теста необходимо только в случае, если в течение последних двух недель у человека был контакт с пациентом, инфицированным коронавирусом.
Нужно ли сдавать анализ на антитела перед прививкой?
Перед вакцинацией нет необходимости сдавать анализ крови на антитела к вирусу SARS-CoV-2, даже если в течение последних шести месяцев был перенесен Covid-19 или ранее была сделана прививка от этого заболевания.
Что делать, если после прививки поднялась температура?
Выработка антител после прививки может сопровождаться небольшим недомоганием и повышением температуры тела до 37,5 °C. Этот симптом — абсолютно нормальная реакция организма и не требует какого-либо лечения. Но если температура повышается до более высоких значений, следует принять жаропонижающее средство, например, парацетамол.
Есть ли разница между «Спутником V» и «Гам-Ковид-Вак»?
«Спутник V» и «Гам-Ковид-Вак» — это два названия одного и того же препарата. Первое из них — торговое, а второе — медицинское.
Оказывает ли «Спутник V» влияние на фертильную функцию?
Нет, данная вакцина не оказывает негативного влияния на репродуктивную функцию человека. Ее производство основывается на использовании аденовирусных векторов, безопасность которых подтверждена результатами многолетних научных исследований.
Защитит ли прививка от новых мутаций вируса?
«Спутник V» обеспечивает защиту от тяжелого течения от всех известных на сегодняшний день мутаций вируса. Вирус SARS-CoV-2 постоянно изменяется. Вакцинация приводит к образованию антител к S-белку, поэтому важны именно те мутации, которые затрагивают шиповидный белок и могут снижать связывание с ним антител, которые выработались на предыдущий вариант вируса. Однако нейтрализующие антитела вырабатываются именно к той части спайк-белка, которая участвует в связывании с рецептором и проникновением внутрь клетки. Поэтому, хотя ген спайка и мутирует, полное его изменение до неузнаваемости вряд ли произойдет, ведь он должен по-прежнему выполнять свою функцию и находить клеточный рецептор. Именно это мы и наблюдаем: вакцинальные антитела хуже узнают спайк-белок у новых вариантов COVID-19, но не теряют связывание полностью. Это значит, что просто повышения титра антител и увеличения количества клонов клеток памяти будет достаточно для защиты от новых мутантов, то есть поможет ревакцинация через несколько месяцев. Скорее всего, нам придется прививаться от ковида, как от гриппа — раз в год на протяжении нескольких лет».



Может ли вакцинация стать причиной положительного теста ПЦР?
ПЦР-тест направлен на выявление генетической информации самого вируса, а не на определение защитных антител. Поэтому прививка не может привести к положительному результату этого анализа.
Если прививка защищает от заражения, то зачем после нее следует носить маску?
Необходимо понимать, что вакцина защищает от тяжелого течения болезни, а не от инфицирования коронавирусом. Несоблюдения правил профилактики может стать причиной заражения даже привитого человека, также после вакцинации люди нередко становятся вирусоносителями и передают инфекцию окружающим людям.
Можно ли применять «Спутник V» для лечения коронавирусной инфекции?
Применение препарата «Спутник V» показано только с целью профилактики. В период любого острого заболевания, в том числе и Covid-19, его использование противопоказано.
Заключение
Вакцинация препаратом «Спутник V» — высокоэффективный способ защиты от заболевания ковидом. Прививка «обучает» иммунную систему бороться с ранее неизвестным для нее вирусом, дает естественную защиту организма. И даже если болезнь разовьется, она будет протекать в легкой форме — без госпитализации, проведения искусственной вентиляции легких и серьезных последствий.
Источники
- Спутник V. Википедия
- Инструкция по медицинскому применению лекарственного препарата Гам-Ковид-Вак, комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2. Министерство здравоохранения Российской Федерации.
- Официальная информация о коронавирусе в России. Часто задаваемые вопросы.
- Спутник V. Официальный сайт.
- Пандемия COVID-19. Википедия
- Временные методические рекомендации «Порядок проведения вакцинации взрослого населения против COVID-19». https://minzdrav.gov.ru/news/2021/07/02/16927-utverzhdeny-vremennye-metodicheskie-rekomendatsii-poryadok-provedeniya-vaktsinatsii-vzroslogo-naseleniya-protiv-covid-19
- Gushchin VA, Dolzhikova IV, Shchetinin AM, Odintsova AS, Gintsburg AL. Neutralizing Activity of Sera from Sputnik V-Vaccinated People against Variants of Concern (VOC: B.1.1.7, B.1.351, P.1, B.1.617.2, B.1.617.3) and Moscow Endemic SARS-CoV-2 Variants.Vaccines. 2021; 9(7):779. https://doi.org/10.3390/vaccines9070779
- Lapa D, Grousova DM, Matusali G, Meschi S, Colavita F, Bettini A, Gramigna G, Francalancia M, Garbuglia AR, Girardi E, Puro V, Antinori A, Kovyrshina AV, Dolzhikova IV, Shcheblyakov DV, Tukhvatulin AI, Zubkova OV, Logunov DY, Naroditsky BS, Vaia F, Gintsburg AL. Retention of Neutralizing response against SARS-CoV-2 Omicron variant in Sputnik V vaccinated individuals. MedRxiv. 2022 Jan 20. doi: https://doi.org/10.1101/2022.01.15.22269335
https://ria.ru/20210701/sputnikv-1739169613.html
«Спутник V». Все о первой российской вакцине от коронавируса
Гам-КОВИД-Вак (Спутник V) — что это за вакцина, противопоказания, отзывы привитых
«Спутник V». Все о первой российской вакцине от коронавируса
Гам-КОВИД-Вак», известная также как «Спутник V», — первая зарегистрированная в мире вакцина для профилактики COVID-19. По оценкам разработчиков, препарат… РИА Новости, 02.07.2021
2021-07-01T08:00
2021-07-01T08:00
2021-07-02T18:17
наука
министерство здравоохранения рф (минздрав россии)
федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека (роспотребнадзор)
здоровье
российский фонд прямых инвестиций
биология
вакцины
нии им. гамалеи (национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика н.ф.гамалеи)
/html/head/meta[@name=’og:title’]/@content
/html/head/meta[@name=’og:description’]/@content
https://cdnn21.img.ria.ru/images/07e4/0c/1c/1591207795_0:147:3072:1875_1920x0_80_0_0_b1334d2c50f7aef1b5466f0485702743.jpg
МОСКВА, 1 июл — РИА Новости. «Гам-КОВИД-Вак», известная также как «Спутник V», — первая зарегистрированная в мире вакцина для профилактики COVID-19. По оценкам разработчиков, препарат эффективен против всех выявленных штаммов коронавируса SARS-CoV-2, а ее облегченный вариант «Спутник Лайт» идеально подходит для ревакцинации.Что такое «Гам-КОВИД-Вак»»Гам-КОВИД-Вак», или «Спутник V», — первая российская вакцина против ковида, созданная в Центре эпидемиологии и микробиологии имени Н. Ф. Гамалеи. Она относится к классу векторных вакцин. Зарегистрирована 11 августа 2020 года. Состав вакцины «Спутник V»Вакцина состоит из неспособного размножаться аденовируса человека. Этот возбудитель не опасен, он вызывает лишь легкую простуду. В его ДНК встроен ген белка-шипа коронавируса SARS-CoV-2. Белок связывается с рецепторами на поверхности клеток и помогает вирусу проникнуть внутрь. Именно на белок-шип реагирует наш иммунитет. Аденовирусный вектор при этом служит средством доставки.В вакцине используют вектор на основе двух разных штаммов аденовируса человека — 26-го и пятого серотипа (Ad26, Ad5). Выпускают препарат в виде раствора со вспомогательными веществами: например, трис, хлориды натрия и магния, сахароза, полисорбат, магний хлористый гексагидрат, ЭДТА, этанол, вода.Принцип действия и отличия от других вакцинРаствор вводят в мышцу, вскоре в месте укола начинается небольшое воспаление — организм распознает чужеродные вещества и отправляет туда лимфоциты. Аденовирус проникает в них и заставляет вырабатывать коронавирусный белок-шип. В свою очередь иммунитет отвечает целым коктейлем из антител.Антитела — это сигнальные белки, которые дают команды защитной системе организма. Если произойдет встреча с реальным SARS-CoV-2, они помогут его уничтожить. В результате человек не заболеет либо коронавирусная инфекция будет перенесена в легкой форме.В мире есть несколько векторных вакцин от коронавируса. Например, американская компания Johnson & Johnson создала препарат на основе аденовируса человека Ad26, а китайская CanSino Biologics — Ad5. Обе вводят однократно. В отличие от них «Спутник V» делают в два приема. После первой дозы, или, как говорят ученые, праймирующей иммунизации, у привитых формируется первичный, а после второй, бустерной, — вторичный иммунный ответ. Уникальность российской технологии в том, что в первой и второй дозах использованы разные вирусные векторы — сначала Ad26, затем Ad5. При такой схеме общий уровень иммунизации намного выше.Еще одну векторную вакцину разработала англо-шведская компания AstraZeneca. Однако в ней в качестве вектора используют аденовирус шимпанзе.По результатам клинических исследований, которые прошли международную оценку и опубликованы в журнале The Lancet, эффективность вакцины «Спутник V» против COVID-19 составляет 91,6 процента. И в ста процентах случаев она предотвращает развитие тяжелой формы ковида. Анализ данных о заболеваемости коронавирусом среди россиян, привитых обоими компонентами препарата в период с 5 декабря 2020-го по 31 марта 2021-го, показал, что реальная эффективность «Гам-КОВИД-Вак» еще выше — 97,6 процента.Инструкция по применениюПодготовка к вакцинацииНет никаких особенных требований при подготовке в прививке. Роспотребнадзор указывает — перед вакцинацией нет необходимости делать ПЦР-тест, чтобы исключить ковид, или анализ на антитела. Главное, в день вакцинации самочувствие должно быть хорошим.Однако, по мнению ряда экспертов, реакция организма на введение любой вакцины очень индивидуальна. Поэтому людям с серьезными хроническими болезнями нужно предварительно сходить на прием к лечащему врачу и убедиться, что их заболевание в стадии ремиссии и они сейчас не принимают никаких препаратов, которые могут помешать выработке иммунитета.Как делается прививка от коронавируса»Спутник V» предназначен для внутримышечного введения. Укол делают в дельтовидную мышцу плеча. Перед процедурой флакон или ампулу с компонентом I или II достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания, чтобы не осталось включений льда. Затем протирают снаружи спиртовой салфеткой и осторожно перемешивают содержимое, не допуская встряхивания. Размороженный препарат необходимо использовать в течение двух часов, снова замораживать его нельзя.Для выявления противопоказаний пациента перед вакцинацией должен осмотреть врач. Он опрашивает о самочувствии и контактах с инфицированными, измеряет температуру тела и уровень кислорода в крови. Если температура выше 37 градусов, прививку откладывают.Что нельзя делать после прививкиРекомендуют один день до и два дня после прививки воздержаться от употребления алкоголя, не переутомляться, избегать тяжелых физических нагрузок, снизить уровень стресса, хорошо высыпаться, не злоупотреблять солнечными ваннами, а в сам день вакцинации не посещать бани и бассейны, не купаться в природных водоемах.Ученые советуют есть побольше белковых продуктов — молочных, рыбы, нежирного мяса, поскольку они дают организму необходимый строительный материал для формирования защитных антител, а также богатые пищевыми волокнами пребиотики — овощи, цельнозерновые крупы, бобовые, зелень — и пробиотики — кефир, йогурт, простоквашу, квашеную капусту. Они нужны для поддержания кишечной микрофлоры, которая вносит большой вклад в выработку иммунного ответа на вакцину.Также важно после прививки соблюдать стандартные защитные меры: носить маски в людных местах, тщательно мыть руки, использовать антисептики. Интервал между прививкамиВакцинацию проводят в два этапа с интервалом 21 день: вначале компонентом I в дозе 0,5 миллилитров, затем, через три недели, — компонентом II в дозе 0,5 миллилитров.Когда появятся антитела к коронавирусуПо оценкам ученых, полноценный иммунитет возникает в среднем через 40 дней после первого укола. До истечения этого срока важно не только избежать заражения коронавирусом, но и не подхватить другую ОРВИ, энтеровирус или прочие инфекции. Они могут помешать эффективной выработке иммунитета после вакцинации. Побочные эффекты от вакцины «Спутник V»Клинические исследования показали, что чаще всего после вакцинации возникает гриппоподобный синдром — боль, отек и зуд в месте введения, общее недомогание, озноб, повышение температуры, боль и ломота в мышцах и суставах, головная боль, снижение аппетита. Состояние может длиться от одного до трех дней.Реже проявляются нарушения со стороны дыхательной системы — боль в ротоглотке, заложенность носа, першение в горле. Возможны головокружения, обмороки, тошнота, рвота, диспепсия. В памятке Минздрава указано, что при повышении температуры можно принять нестероидные противовоспалительные препараты, а при покраснении, отечности и болезненности места укола — антигистаминные средства. Никаких серьезных последствий, в том числе тяжелых аллергических реакций, не наблюдалось.Продолжительность действияПока точно не установлено, на какой срок защищает вакцина. Согласно предварительной оценке, антитела класса G у сотрудников Центра Гамалеи, получивших вакцину в порядке эксперимента в марте 2020-го, сохранялись и через девять месяцев. При этом титр антител был выше, чем у переболевших. Противопоказания для вакцинацииПротивопоказания к применению у «Спутника V» примерно такие же, как у всех остальных вакцин: тяжелые формы аллергии, инфекционные и неинфекционные заболевания в острой форме, грудное вскармливание. Прививаться можно всем взрослым старше 18 лет, без верхнего ограничения по возрасту. Детей пока не прививают — из-за отсутствия клинических испытаний, подтверждающих эффективность и безопасность вакцины для людей младше 18. Центр Гамалеи планирует в ближайшее время начать исследование по применению «Спутника V» у детей. Соответствующую заявку ученые подали в Минздрав России.Недавно ведомство разрешило «Спутник V» для беременных женщин с высоким риском тяжелого течения COVID-19. Инструкция рекомендует с осторожностью применять вакцину при хронических заболеваниях печени и почек, тяжелых заболеваниях системы кроветворения, эпилепсии и других заболеваниях центральной нервной системы, остром коронарном синдроме и остром нарушении мозгового кровообращения, миокардитах, эндокардитах, перикардитах, а также при некоторых эндокринных заболеваниях, таких как выраженные нарушения функции щитовидной железы и сахарный диабет в стадии декомпенсации.Отмечено, что вакцинация может представлять определенный риск для пациентов со злокачественными новообразованиями и тяжелыми аутоиммунными заболеваниями, так как стимуляция иммунной системы может привести к обострению.А вот пациентам с сердечно-сосудистыми заболеваниями, диабетом, бронхиальной астмой, гепатитом С и онкозаболеваниями в стадии ремиссии, по мнению ученых, вакцинироваться необходимо.РевакцинацияОжидают, что коронавирус станет сезонным и прививаться от него нужно будет ежегодно. А во время обострения эпидемии — раз в шеть месяцев.Специалисты Центра Гамалеи и Минздрава рекомендуют проводить ревакцинацию «Спутником Лайт», которая в ближайшее время поступит в гражданский оборот. Ранее глава РФПИ Кирилл Дмитриев и владелец компании «Р-Фарм» — одного из производителей «Гам-КОВИД-Вак» — заявляли, что ревакцинироваться можно и первым компонентом «Спутника V».Отзывы привитых «Спутником V»»Сегодня привился «Спутником V». Чувствую себя хорошо. Коронавирусом я переболел, есть антитела. Но прививка необходима независимо от уровня титров. Все, кто еще не вакцинировался, — самое время это сделать», — написал врио главы Мордовии Артем Здунов в инстаграме.Врио губернатора Хабаровского края Михаил Дегтярев сделал прививку от ковида повторно. «Первый раз вакциной «Гам-Ковид-Вак» прививался в июле и августе прошлого года. По прошествии 11 месяцев количество антител в крови существенно снизилось, поэтому решил не рисковать ни своим здоровьем, ни здоровьем людей, с которыми работаю и с которыми встречаюсь каждый день», — рассказал он в Telegram-канале.Народные отчеты от вакцинации «Спутником V» публикуются в Telegram-канале @Sputnik_results. Вот несколько отзывов: «М 43, здоров. ГамКовидВакV1 — 16.03 без побочек, V2-07.04 легкая слабость на след день. Антитела на 28.06″.»Ж 22 года V1 28.06.21. В день прививки легкая слабость и сонливость, боль в месте укола».»М 65, системный васкулит (гранулематоз Вегенера) в ремиссии, V2 28.06.21, никаких симптомов, как и после первой дозы».Сертификация вакцины «Спутник V» в других странахВакцина одобрена в 67 странах с общим населением свыше 3,4 миллиарда человек. Так, имея сертификат о прививке «Спутником V», можно въезжать, например, в Грецию, Хорватию, на Кипр, в Турцию, Грузию. Пакет документов о сертификации «Спутника V» также предоставлен ВОЗ. Разработчики ожидают положительное решение в скором времени. В случае одобрения вакцинированные получат цифровые сертификаты, которые облегчат перемещение по странам ЕС.
https://ria.ru/20201225/vaktsina-1590616868.html
https://ria.ru/20210313/kovid-1600996928.html
https://ria.ru/20210413/privivka-1727931944.html
https://ria.ru/20201230/vaktsinatsiya-1591428753.html
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
2021
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
Новости
ru-RU
https://ria.ru/docs/about/copyright.html
https://xn--c1acbl2abdlkab1og.xn--p1ai/
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
https://cdnn21.img.ria.ru/images/07e4/0c/1c/1591207795_250:0:2673:1818_1920x0_80_0_0_40065ea61ff99bced84cbf06e94802b1.jpg
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
министерство здравоохранения рф (минздрав россии), федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека (роспотребнадзор), здоровье, российский фонд прямых инвестиций, биология, вакцины, нии им. гамалеи (национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика н.ф.гамалеи), коронавирус covid-19, вакцина «спутник v», вакцинация россиян от covid-19, вакцина «спутник лайт»
Наука, Министерство здравоохранения РФ (Минздрав России), Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор), Здоровье, Российский фонд прямых инвестиций, биология, Вакцины, НИИ им. Гамалеи (Национальный исследовательский центр эпидемиологии и микробиологии имени почетного академика Н.Ф.Гамалеи), Коронавирус COVID-19, Вакцина «Спутник V», Вакцинация россиян от COVID-19, Вакцина «Спутник Лайт»
МОСКВА, 1 июл — РИА Новости. «Гам-КОВИД-Вак», известная также как «Спутник V», — первая зарегистрированная в мире вакцина для профилактики COVID-19. По оценкам разработчиков, препарат эффективен против всех выявленных штаммов коронавируса SARS-CoV-2, а ее облегченный вариант «Спутник Лайт» идеально подходит для ревакцинации.
Что такое «Гам-КОВИД-Вак»
«Гам-КОВИД-Вак», или «Спутник V», — первая российская вакцина против ковида, созданная в Центре эпидемиологии и микробиологии имени Н. Ф. Гамалеи. Она относится к классу векторных вакцин. Зарегистрирована 11 августа 2020 года.
Состав вакцины «Спутник V»
Вакцина состоит из неспособного размножаться аденовируса человека. Этот возбудитель не опасен, он вызывает лишь легкую простуду. В его ДНК встроен ген белка-шипа коронавируса SARS-CoV-2. Белок связывается с рецепторами на поверхности клеток и помогает вирусу проникнуть внутрь. Именно на белок-шип реагирует наш иммунитет. Аденовирусный вектор при этом служит средством доставки.
В вакцине используют вектор на основе двух разных штаммов аденовируса человека — 26-го и пятого серотипа (Ad26, Ad5).
Выпускают препарат в виде раствора со вспомогательными веществами: например, трис, хлориды натрия и магния, сахароза, полисорбат, магний хлористый гексагидрат, ЭДТА, этанол, вода.
Принцип действия и отличия от других вакцин
Раствор вводят в мышцу, вскоре в месте укола начинается небольшое воспаление — организм распознает чужеродные вещества и отправляет туда лимфоциты. Аденовирус проникает в них и заставляет вырабатывать коронавирусный белок-шип. В свою очередь иммунитет отвечает целым коктейлем из антител.
Антитела — это сигнальные белки, которые дают команды защитной системе организма. Если произойдет встреча с реальным SARS-CoV-2, они помогут его уничтожить. В результате человек не заболеет либо коронавирусная инфекция будет перенесена в легкой форме.
В мире есть несколько векторных вакцин от коронавируса. Например, американская компания Johnson & Johnson создала препарат на основе аденовируса человека Ad26, а китайская CanSino Biologics — Ad5. Обе вводят однократно.
В отличие от них «Спутник V» делают в два приема. После первой дозы, или, как говорят ученые, праймирующей иммунизации, у привитых формируется первичный, а после второй, бустерной, — вторичный иммунный ответ. Уникальность российской технологии в том, что в первой и второй дозах использованы разные вирусные векторы — сначала Ad26, затем Ad5. При такой схеме общий уровень иммунизации намного выше.
Еще одну векторную вакцину разработала англо-шведская компания AstraZeneca. Однако в ней в качестве вектора используют аденовирус шимпанзе.
По результатам клинических исследований, которые прошли международную оценку и опубликованы в журнале The Lancet, эффективность вакцины «Спутник V» против COVID-19 составляет 91,6 процента. И в ста процентах случаев она предотвращает развитие тяжелой формы ковида.
Анализ данных о заболеваемости коронавирусом среди россиян, привитых обоими компонентами препарата в период с 5 декабря 2020-го по 31 марта 2021-го, показал, что реальная эффективность «Гам-КОВИД-Вак» еще выше — 97,6 процента.
Инструкция по применению
Подготовка к вакцинации
Нет никаких особенных требований при подготовке в прививке. Роспотребнадзор указывает — перед вакцинацией нет необходимости делать ПЦР-тест, чтобы исключить ковид, или анализ на антитела. Главное, в день вакцинации самочувствие должно быть хорошим.
Однако, по мнению ряда экспертов, реакция организма на введение любой вакцины очень индивидуальна. Поэтому людям с серьезными хроническими болезнями нужно предварительно сходить на прием к лечащему врачу и убедиться, что их заболевание в стадии ремиссии и они сейчас не принимают никаких препаратов, которые могут помешать выработке иммунитета.
Как делается прививка от коронавируса
«Спутник V» предназначен для внутримышечного введения. Укол делают в дельтовидную мышцу плеча.
Перед процедурой флакон или ампулу с компонентом I или II достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания, чтобы не осталось включений льда. Затем протирают снаружи спиртовой салфеткой и осторожно перемешивают содержимое, не допуская встряхивания. Размороженный препарат необходимо использовать в течение двух часов, снова замораживать его нельзя.
Для выявления противопоказаний пациента перед вакцинацией должен осмотреть врач. Он опрашивает о самочувствии и контактах с инфицированными, измеряет температуру тела и уровень кислорода в крови. Если температура выше 37 градусов, прививку откладывают.
Переболеть COVID-19 или привиться? Вся правда о вакцине от коронавируса
Что нельзя делать после прививки
Рекомендуют один день до и два дня после прививки воздержаться от употребления алкоголя, не переутомляться, избегать тяжелых физических нагрузок, снизить уровень стресса, хорошо высыпаться, не злоупотреблять солнечными ваннами, а в сам день вакцинации не посещать бани и бассейны, не купаться в природных водоемах.
Ученые советуют есть побольше белковых продуктов — молочных, рыбы, нежирного мяса, поскольку они дают организму необходимый строительный материал для формирования защитных антител, а также богатые пищевыми волокнами пребиотики — овощи, цельнозерновые крупы, бобовые, зелень — и пробиотики — кефир, йогурт, простоквашу, квашеную капусту. Они нужны для поддержания кишечной микрофлоры, которая вносит большой вклад в выработку иммунного ответа на вакцину.
Также важно после прививки соблюдать стандартные защитные меры: носить маски в людных местах, тщательно мыть руки, использовать антисептики.
Интервал между прививками
Вакцинацию проводят в два этапа с интервалом 21 день: вначале компонентом I в дозе 0,5 миллилитров, затем, через три недели, — компонентом II в дозе 0,5 миллилитров.
Когда появятся антитела к коронавирусу
По оценкам ученых, полноценный иммунитет возникает в среднем через 40 дней после первого укола. До истечения этого срока важно не только избежать заражения коронавирусом, но и не подхватить другую ОРВИ, энтеровирус или прочие инфекции. Они могут помешать эффективной выработке иммунитета после вакцинации.
Ждать нельзя вакцинироваться. Как долго сохраняется иммунитет к ковиду
Побочные эффекты от вакцины «Спутник V»
Клинические исследования показали, что чаще всего после вакцинации возникает гриппоподобный синдром — боль, отек и зуд в месте введения, общее недомогание, озноб, повышение температуры, боль и ломота в мышцах и суставах, головная боль, снижение аппетита. Состояние может длиться от одного до трех дней.
Реже проявляются нарушения со стороны дыхательной системы — боль в ротоглотке, заложенность носа, першение в горле. Возможны головокружения, обмороки, тошнота, рвота, диспепсия.
В памятке Минздрава указано, что при повышении температуры можно принять нестероидные противовоспалительные препараты, а при покраснении, отечности и болезненности места укола — антигистаминные средства. Никаких серьезных последствий, в том числе тяжелых аллергических реакций, не наблюдалось.
Продолжительность действия
Пока точно не установлено, на какой срок защищает вакцина. Согласно предварительной оценке, антитела класса G у сотрудников Центра Гамалеи, получивших вакцину в порядке эксперимента в марте 2020-го, сохранялись и через девять месяцев. При этом титр антител был выше, чем у переболевших.
Противопоказания для вакцинации
Противопоказания к применению у «Спутника V» примерно такие же, как у всех остальных вакцин: тяжелые формы аллергии, инфекционные и неинфекционные заболевания в острой форме, грудное вскармливание. Прививаться можно всем взрослым старше 18 лет, без верхнего ограничения по возрасту.
Без ограничений по возрасту. Доказана эффективность прививок для пожилых
Детей пока не прививают — из-за отсутствия клинических испытаний, подтверждающих эффективность и безопасность вакцины для людей младше 18. Центр Гамалеи планирует в ближайшее время начать исследование по применению «Спутника V» у детей. Соответствующую заявку ученые подали в Минздрав России.
Недавно ведомство разрешило «Спутник V» для беременных женщин с высоким риском тяжелого течения COVID-19.
Инструкция рекомендует с осторожностью применять вакцину при хронических заболеваниях печени и почек, тяжелых заболеваниях системы кроветворения, эпилепсии и других заболеваниях центральной нервной системы, остром коронарном синдроме и остром нарушении мозгового кровообращения, миокардитах, эндокардитах, перикардитах, а также при некоторых эндокринных заболеваниях, таких как выраженные нарушения функции щитовидной железы и сахарный диабет в стадии декомпенсации.
Отмечено, что вакцинация может представлять определенный риск для пациентов со злокачественными новообразованиями и тяжелыми аутоиммунными заболеваниями, так как стимуляция иммунной системы может привести к обострению.
А вот пациентам с сердечно-сосудистыми заболеваниями, диабетом, бронхиальной астмой, гепатитом С и онкозаболеваниями в стадии ремиссии, по мнению ученых, вакцинироваться необходимо.
Ревакцинация
Ожидают, что коронавирус станет сезонным и прививаться от него нужно будет ежегодно. А во время обострения эпидемии — раз в шеть месяцев.
Специалисты Центра Гамалеи и Минздрава рекомендуют проводить ревакцинацию «Спутником Лайт», которая в ближайшее время поступит в гражданский оборот. Ранее глава РФПИ Кирилл Дмитриев и владелец компании «Р-Фарм» — одного из производителей «Гам-КОВИД-Вак» — заявляли, что ревакцинироваться можно и первым компонентом «Спутника V».
Отзывы привитых «Спутником V»
«Сегодня привился «Спутником V». Чувствую себя хорошо. Коронавирусом я переболел, есть антитела. Но прививка необходима независимо от уровня титров. Все, кто еще не вакцинировался, — самое время это сделать», — написал врио главы Мордовии Артем Здунов в инстаграме.
Врио губернатора Хабаровского края Михаил Дегтярев сделал прививку от ковида повторно. «Первый раз вакциной «Гам-Ковид-Вак» прививался в июле и августе прошлого года. По прошествии 11 месяцев количество антител в крови существенно снизилось, поэтому решил не рисковать ни своим здоровьем, ни здоровьем людей, с которыми работаю и с которыми встречаюсь каждый день», — рассказал он в Telegram-канале.
Народные отчеты от вакцинации «Спутником V» публикуются в Telegram-канале @Sputnik_results. Вот несколько отзывов:
«М 43, здоров. ГамКовидВакV1 — 16.03 без побочек, V2-07.04 легкая слабость на след день. Антитела на 28.06».
«Ж 22 года V1 28.06.21. В день прививки легкая слабость и сонливость, боль в месте укола».
«М 65, системный васкулит (гранулематоз Вегенера) в ремиссии, V2 28.06.21, никаких симптомов, как и после первой дозы».
«В жар бросало». Привитые от коронавируса честно рассказали обо всем
Сертификация вакцины «Спутник V» в других странах
Вакцина одобрена в 67 странах с общим населением свыше 3,4 миллиарда человек. Так, имея сертификат о прививке «Спутником V», можно въезжать, например, в Грецию, Хорватию, на Кипр, в Турцию, Грузию.
Пакет документов о сертификации «Спутника V» также предоставлен ВОЗ. Разработчики ожидают положительное решение в скором времени. В случае одобрения вакцинированные получат цифровые сертификаты, которые облегчат перемещение по странам ЕС.
Гам-КОВИД-Вак, Спутник V – это комбинированная векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2 (Gam-COVID-Vac)
Торговое наименование: Гам-КОВИД-Вак.
Лекарственная форма: раствор для внутримышечного введения.
Состав на 1 дозу
Компонент Ⅰ содержит:
Действующее вещество: рекомбинантные аденовирусные частицы 26 серотипа, содержащие ген белка S вируса SARS-CoV-2, в количестве (1,0 ± 0,5) × 1011 частиц/доза.
Вспомогательные вещества: трис(гидроксилметил)аминометан — 1,21 мг, натрия хлорид — 2,19 мг, сахароза — 25,0 мг, магния хлорида гексагидрат — 102,0 мкг, ЭДТ Адинатриевая соль дигидрат — 19,0 мкг, полисорбат 80 — 250 мкг, этанол 95 % — 2,5 мкл, вода для инъекций до 0,5 мл.
Компонент Ⅱ содержит:
Действующее вещество: рекомбинантные аденовирусные частицы 5 серотипа, содержащие ген белка S вируса SARS-CoV-2, в количестве (1,0 ± 0,5) × 10 частиц/доза.
Вспомогательные вещества: трис(гидроксилметил)аминометан — 1,21 мг, натрия хлорид — 2,19 мг, сахароза — 25,0 мг, магния хлорида гексагидрат — 102,0 мкг, ЭДТАдинатриевая соль дигидрат — 19,0 мкг, полисорбат-80 — 250 мкг, этанол 95 % — 2,5 мкл, вода для инъекций до 0,5 мл.
Описание
Компонент Ⅰ. Раствор замороженный. Представляет собой плотную затвердевшую беловатого цвета массу. После размораживания: однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Компонент Ⅱ. Раствор замороженный. Представляет собой плотную затвердевшую беловатого цвета массу. После размораживания: однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Характеристика: Вакцина получена биотехнологическим путём, при котором не используется патогенный для человека вирус SARS-CoV-2. Препарат состоит из двух компонентов: компонент Ⅰ и компонент Ⅱ. В состав компонента Ⅰ входит рекомбинантный аденовирусный вектор на основе аденовируса человека 26 серотипа, несущий ген белка S-вируса SARS-CoV-2, в состав компонента Ⅱ входит вектор на основе аденовируса человека 5 серотипа, несущий ген белка S вируса SARS-CoV-2.
Фармакологические свойства
Вакцина индуцирует формирование гуморального и клеточного иммунитета в отношении коронавирусной инфекции, вызываемой вирусом SARS-CoV-2.
Иммунологическая эффективность
Иммунологические свойства и безопасность вакцины изучали в различных клинических исследованиях у взрослых добровольцев обоего пола в возрасте старше 18 лет.
Промежуточный анализ иммуногенности показал, что вакцина формирует иммунный ответ у добровольцев. При исследовании гуморального иммунного ответа сыворотки добровольцев были проанализированы на наличие антител, специфичных к рецептор-связывающему домену гликопротеина S вируса SARS-CoV-2 на 42 день от начала вакцинации: в группе вакцинированных среднее геометрическое значение титра антител составило 8996, уровень сероконверсии — 98,25. При сравнении уровня RBD-специфических антител между возрастными стратами статистически значимая разница была показана для группы 18–30 лет относительно остальных возрастных групп; среднее геометрическое значение титра антител составило 18102–22067, уровень сероконверсии — 100 %. Уровни антител достоверно не различались у мужчин и женщин. На 42-й день от начала вакцинации средний геометрический титр нейтрализующих антител у иммунизированных добровольцев составил 44,47, уровень сероконверсии — 95,83 %. Статистически значимой разницы у добровольцев различного пола и возраста не выявлено.
Иммунизация препаратом Гам-КОВИД-Вак, формирует напряженный антиген- специфический клеточный противоинфекционный иммунитет у практически у всех обследованных добровольцев (формирование антиген-специфичных клеток обоих популяций T лимфоцитов: T хелперных (CD4+) и T киллерных (CD8+) и достоверному повышению секреции ИФНγ).
Защитный титр антител в настоящее время неизвестен. Продолжительность защиты неизвестна.
Клинические исследования по изучению эпидемиологической эффективности продолжаются в настоящее время. По данным промежуточного анализа эффективность составляет более 91 %.
Инструкция по применению
Показания
Профилактика новой коронавирусной инфекции (COVID-19) у взрослых старше 18 лет.
Противопоказания
- Гиперчувствительность к какому-либо компоненту вакцины или вакцины, содержащей аналогичные компоненты;
- тяжёлые аллергические реакции в анамнезе;
- острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний — вакцинацию проводят через 2–4 недели после выздоровления или ремиссии. При нетяжёлых ОРВИ, острых инфекционных заболеваниях ЖКТ — вакцинацию проводят после нормализации температуры;
- беременность и период грудного вскармливания;
- возраст до 18 лет (в связи с отсутствием данных об эффективности и безопасности).
Противопоказания для введения компонента Ⅱ
- тяжёлые поствакцинальные осложнения (анафилактический шок, тяжёлые генерализованные аллергические реакции, судорожный синдром, температура выше 40 °C и т.д.) на введение компонента Ⅰ вакцины.
С осторожностью
Применять вакцину с осторожностью при хронических заболеваниях печени и почек, эндокринных заболеваниях (выраженных нарушениях функции щитовидной железы и сахарный диабет в стадии декомпенсации), тяжёлых заболеваниях системы кроветворения, эпилепсии и других заболеваний ЦНС, остром коронарном синдроме и остром нарушении мозгового кровообращения, миокардитах, эндокардитах, перикардитах.
Вследствие недостатка информации вакцинация может представлять риск для следующих групп пациентов:
- с аутоиммунными заболеваниями (стимуляция иммунной системы может привести к обострению заболевания, особенно следует с осторожностью относиться к пациентам с аутоиммунной патологией имеющей тенденцию к развитию тяжёлых и жизнеугрожающих состояний);
- со злокачественными новообразованиями.
Принятие решения о вакцинации должно основываться на оценке соотношения пользы и риска в каждой конкретной ситуации.
Места, где проводится вакцинация, должны быть оснащены средствами противошоковой терапии в соответствии с Приказом Министерства здравоохранения РФ от 20 декабря 2012 г. N 1079н «Об утверждении стандарта скорой медицинской помощи при анафилактическом шоке).
В день проведения вакцинации пациент должен быть осмотрен врачом: обязательным является общий осмотр и измерение температуры тела, в случае если температура превышает 37 °C, вакцинацию не проводят.
Применение при беременности и в период грудного вскармливания
Препарат противопоказан при беременности и в период грудного вскармливания, так как его эффективность и безопасность в этот период не изучались.
Способ применения и дозы
Вакцина предназначена только для внутримышечного введения. Строго запрещено внутривенное введение препарата. Вакцину вводят в дельтовидную мышцу (верхнюю треть наружной поверхности плеча). При невозможности введения в дельтовидную мышцу — препарат вводят в латеральную широкую мышцу бедра.
- Вакцинацию проводят в два этапа: вначале компонентом Ⅰ в дозе 0,5мл, затем, через 3 недели — компонентом Ⅱ в дозе 0,5 мл.
- Препарат вводят внутримышечно: вначале компонент Ⅰ в дозе 0,5мл, затем через 3 недели компонент Ⅱ в дозе 0,5 мл.
- После введения вакцины пациент должен находиться под наблюдением медицинских работников в течение 30 минут.
Применение вакцины (флаконов, ампул) производства ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России) и АО «Биннофарм»
Перед вакцинированием флакон или ампулу с компонентом I или II достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон или ампулу снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона или ампулы!
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой. Вскрывают ампулу по цветной точке.
Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту.
Не допускается хранение размороженного препарата!
Повторное замораживание не допускается!
Применение вакцины (флаконов, ампул) производства АО «ГЕНЕРИУМ», ОАО «Фармстандарт-УфаВИТА» и ЗАО «ЛЕККО»
Перед вакцинированием флакон или ампулу с компонентом Ⅰ или Ⅱ достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон или ампулу снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона или ампулы!
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой. Вскрывают ампулу по кольцу или точке излома.
Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту.
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого флакона или ампулы — не более 2 часов при комнатной температуре.
Повторное замораживание флакона или ампулы с раствором не допускается!
Применение вакцины производства ЗАО «БИОКАД»
Перед вакцинированием флакон с компонентом Ⅰ или Ⅱ достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания.
Остаток включений льда не допускается!
Протирают флакон снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием.
Не допускается встряхивание флакона!
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой.
Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту.
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого флакона по 3 мл не более 2 часов при комнатной температуре.
Не допускается хранение размороженного препарата во флаконах по 0,5 мл!
Повторное замораживание не допускается!
Внимание. К использованию непригоден препарат с дефектами укупорочной системы и/или нарушенной маркировкой флакона или ампулы, при изменении физических свойств раствора (мутность, окрашивание), неправильном хранении и/или с истекшим сроком годности.
Информация для медицинских работников, выполняющих вакцинацию лекарственным препаратом: данный лекарственный препарат зарегистрирован по особой процедуре регистрации, в связи, с чем необходимо уведомлять Федеральную службу по надзору в сфере здравоохранения о каждом факте применения лекарственного препарата путём внесения информации в соответствующей раздел информационной системы ЕГИСЗ.
Побочное действие
Нежелательные явления, характерные для применения вакцины, выявленные в рамках клинических исследований, а также исследований других вакцин на основе аналогичной технологической платформы, бывают преимущественно лёгкой или средней степени выраженности, могут развиваться в первые-вторые сутки после вакцинации и разрешаются в течение 3-х последующих дней.
Чаще других могут развиться кратковременные общие (непродолжительный гриппоподобный синдром, характеризующийся ознобом, повышением температуры тела, артралгией, миалгией, астенией, общим недомоганием, головной болью) и местные (болезненность в месте инъекции, гиперемия, отёчность) реакции).
Рекомендуется назначение нестероидных противовоспалительных средств (НПВС) при повышении температуры после вакцинации и антигистаминных средств при выраженной местной реакции.
Реже отмечаются тошнота, диспепсия, снижение аппетита, иногда — увеличение регионарных лимфоузлов. У некоторых пациентов возможно развитие аллергических реакций, кратковременное повышение уровня печёночных трансаминаз, креатинина и креатинфосфокиназы в сыворотке крови.
В рамках проведённых клинических исследований безопасности, переносимости и иммуногенности препарата Гам-КОВИД-Вак после вакцинации были зарегистрированы следующие НЯ:
«Общие нарушения и реакции в месте введения»: гипертермия, боль, отёк, зуд в месте вакцинации, астения, боль, недомогание, пирексия, повышение температуры кожи в месте вакцинации, снижение аппетита. Частота развития — очень часто и часто.
«Нарушения со стороны дыхательной системы, органов грудной клетки и средостения»: боль в ротоглотке, заложенность носа, першение в горле, ринорея. Частота развития — часто.
«Нарушения со стороны нервной системы»: головная боль — часто, головокружения, обмороки — редко.
«Желудочно-кишечные нарушения» тошнота, рвота, диспепсия — часто.
«Лабораторные и инструментальные данные»: разнонаправленные отклонения показателей иммунологического статуса: повышение числа Т-лимфоцитов, увеличение процентного содержания лимфоцитов, снижение числа естественных клеток-киллеров, увеличение количества С04-лимфоцитов, снижение количества СВ4-лимфоцитов, повышение числа В-лимфоцитов, снижение числа B-лимфоцитов, повышение числа естественных клеток-киллеров, повышение количества CDS- лимфоцитов, повышение уровня иммуноглобулина Е (IgE) в крови, увеличение соотношения CD4/CD8, уменьшение соотношения CD4/CD8, повышение уровня иммуноглобулина A (IgA) в крови, уменьшение процентного содержания лимфоцитов CD8. Отклонения в общем анализе крови: увеличение процентного содержания лимфоцитов, снижение показателя гематокрита, увеличение числа лимфоцитов, повышение скорости оседания эритроцитов, повышение числа лейкоцитов, повышение числа моноцитов, повышение числа тромбоцитов, снижение числа нейтрофилов, снижение числа тромбоцитов. Отклонения в общем анализе мочи: эритроциты в моче.
Большинство НЯ завершились выздоровлением без последствий.
Лабораторные отклонения не имели клинического значения (не нуждались в проведении дополнительных диагностических процедур и назначения терапии).
Передозировка
О случаях передозировки не сообщалось.
Учитывая, что отпуск лекарственного препарата допускается только для лечебно-профилактических учреждений, а сама вакцинация проводится только квалифицированным медицинским персоналом, риск передозировки крайне низок.
Однако можно предположить, что при случайной передозировке возможно развитие указанных выше токсических и токсико-аллергических реакций в более тяжёлой степени.
Специфических антидотов к препарату не существует.
Терапевтические мероприятия в данном случае будут включать симптоматическую терапию в соответствии с показаниями (жаропонижающие/ НПВС и десенсибилизирующие средства), кортикостероиды — парентерально при выраженном токсико-аллергическом синдроме). Режим назначения препаратов должен быть выбран согласно рекомендациям по применению и дозировкам данного лекарственного средства.
Взаимодействие с другими лекарственными средствами
Не изучалось.
Особые указания
У пациентов, получающих иммуносупрессивную терапию и пациентов с иммунодефицитом может не развиться достаточный иммунный ответ. Поэтому приём препаратов, угнетающих функцию иммунной системы, противопоказан как минимум за 1 месяц до и после вакцинации из-за риска снижения иммуногенности.
Данный лекарственный препарат зарегистрирован по процедуре регистрации препаратов, предназначенных для применения в условиях угрозы возникновения, возникновения и ликвидации чрезвычайных ситуаций.
Инструкция подготовлена на основании ограниченного объёма клинических данных по применению препарата и будет дополняться по мере поступления новых данных. Применение препарата возможно только в условиях медицинских организаций, имеющих право осуществлять вакцинопрофилактику населения в установленном порядке.
Влияние на способность управлять транспортными средствами, механизмами
Исследования по изучению влияния вакцины на способность управлять транспортными средствами и потенциально опасными механизмами не проводились.
Форма выпуска
Раствор для внутримышечного введения, компонент Ⅰ — 0,5 мл/доза + компонент Ⅱ — 0,5 мл/доза.
При производстве ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России):
по 0,5 мл (1 доза) каждого компонента препарата во флаконы нейтрального стекла первого гидролитического класса (типа 2R, 4R), герметично укупоренных пробками из резины, обжатых алюминиевыми или алюмопластиковыми колпачками.
1 флакон компонента Ⅰ с инструкцией по применению помещают в пачку картонную или в пачку из картона коробочного; 1 флакон компонента Ⅱ с инструкцией по применению помещают в пачку картонную или в пачку из картона коробочного.
При производстве АО «Биннофарм»:
по 0,5 мл (1 доза) каждого компонента препарата в ампулы из бесцветного стекла l-го гидролитического класса вместимостью 1 мл с цветной точкой. На каждую ампулу наклеивают этикетку.
По 5 ампул каждого компонента препарата помещают в контурную ячейковую упаковку из плёнки поливинилхлоридной.
По 1 контурной ячейковой упаковке вместе с инструкцией по применению помещают в пачку из картона.
При производстве на АО «ГЕНЕРИУМ»:
По 3,0 мл (5 доз) каждого компонента — во флаконы нейтрального стекла 1 гидролитического класса формата 2R, герметично укупоренные пробками резиновыми, с обкаткой колпачками алюминиево-пластиковыми с контролем первого вскрытия.
1 флакон с компонентом Ⅰ или компонентом Ⅱ вместе с инструкцией по медицинскому применению — в пачке из картона с поролоновым держателем из пенополиуретана.
При производстве на ЗАО «ЛЕККО»:
по 3 мл (5 доз) каждого компонента препарата во флаконы, укупоренные пробками резиновыми, обкатанные алюминиево-пластиковыми колпачками с контролем первого вскрытия.
По 1 флакону с компонентом Ⅰ или с компонентом Ⅱ вместе с инструкцией по применению помещают в пачку из картона с поролоновым держателем из пенополиуретана.
При производстве на ОАО «Фармстандарт-УфаВИТА»:
по 0,5 мл (1 доза) каждого компонента препарата в ампулы из бесцветного стекла.
По 5 ампул каждого компонента препарата — в контурную ячейковую упаковку из плёнки поливинилхлоридной.
По 1 контурной ячейковой упаковке вместе с инструкцией по применению — в пачку из картона.
По 3 мл (5 доз) каждого компонента препарата во флаконы, укупоренные пробками резиновыми, обкатанные алюминиево-пластиковыми колпачками с контролем первого вскрытия.
По 1 флакону с компонентом Ⅰ или с компонентом Ⅱ вместе с инструкцией по применению помещают в пачку из картона с поролоновым держателем из пенополиуретана.
При производстве на ЗАО «БИОКАД»:
По 0,5 мл (1 доза) или по 3,0 мл (5 доз) каждого компонента препарата во флаконы из нейтрального стекла Ⅰ гидролитического класса (типа 2R, 6R), герметично укупоренные резиновыми пробками, с обкаткой алюминиевыми колпачками с пластиковой крышкой типа «flip-off».
1 флакон 6R с компонентом Ⅰ или компонентом Ⅱ с инструкцией по применению — в пачку картонную.
1 флакон 2R с компонентом Ⅰ или компонентом Ⅱ в контурной ячейковой упаковке из ПВХ плёнки с инструкцией по применению — в пачку картонную.
Хранение
Хранить в защищённом от света месте, при температуре не выше минус 18 °C.
Для флаконов (ампул) по 0,5 мл — не допускается хранение размороженного препарата!
Для флаконов по 3,0 мл — в размороженном состоянии хранить не более 2 часов.
Повторное замораживание не допускается.
Хранить в недоступном для детей месте.
Условия транспортирования: Транспортирование препарата при температуре не выше минус 18 °C.
Срок годности
6 месяцев. Не применять по истечении срока годности.
Условия отпуска: для лечебно-профилактических учреждений.
Производитель
Медгамал (филиал НИИ эпидемиологии и микробиологии им.Н.Ф.Гамалеи РАМН ГУ), Российская Федерация
Биннофарм, ЗАО, Российская Федерация
ГЕНЕРИУМ, ЗАО, Российская Федерация
Фармацевтическая фирма ЛЕККО, ЗАО, Российская Федерация
Фармстандарт-УфаВИТА, ОАО, Российская Федерация
БИОКАД, ЗАО, Российская Федерация
Наименования и адреса производственных площадок производителя лекарственного препарата:
- ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России), Россия, 123098. г. Москва, улица Гамалеи, д. 18. (все стадии производства).
- АО «Биннофарм», Россия, 124460, г. Москва, г. Зеленоград, ул. Конструктора Гуськова, д. 3, стр. 1 (очистка, розлив (первичная упаковка), упаковка (вторичная (потребительская) упаковка).
- АО «ГЕНЕРИУМ», Россия, 601125, Владимирская обл., Петушинский район, пос. Вольгинский, ул. Заводская, стр. 263, (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
- ЗАО «Фармацевтическая фирма «ЛЕККО» (ЗАО «ЛЕККО»), Россия, 601125, Владимирская обл., Петушинский район, пос. Вольгинский, ул. Заводская, стр. 277; 601125, Владимирская обл., Петушинский район, пос. Вольгинский, ул. Заводская, стр. 279 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
- ОАО «Фармстандарт-Уфимский витаминный завод» (ОАО «Фармстандарт-УфаВИТА»), Россия, Республика Башкортостан, г. Уфа, ул. Худайбердина, д. 28 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
- ЗАО «БИОКАД», Россия, 198515, г. Санкт-Петербург, п. Стрельна, ул. Связи, д. 38. стр. 1 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
Выпускающий контроль качества
Филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России. Россия, 123098, г. Москва, улица Гамалеи, д. 18.
Владелец регистрационного удостоверения/организация, принимающая претензии потребителя:
ФГБУ «Национальный исследовательский центр эпидемиологии и микробиологии имени почётного академика Н.Ф. Гамалеи» Министерства здравоохранения Российской Федерации (ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России).
Россия. 123098. г. Москва, улица Гамалеи, д. 18.
Тел: 8 499-193-30-01, факс: 8 499-193-61-83.
Список аналогов
В списке аналогов препарата Гам-КОВИД-Вак (раствор для внутримышечного введения, Медгамал (филиал НИИ эпидемиологии и микробиологии им.Н.Ф.Гамалеи РАМН ГУ), Российская Федерация, ЛП-006395) представлены 4 названия лекарственных средств, содержащих действующее вещество вакцина для профилактики новой коронавирусной инфекции (covid-19).
Лекарственные препараты:
- Гам-КОВИД-Вак Лио – лиофилизат для приготовления раствора для внутримышечного введения. Медгамал (филиал НИИ эпидемиологии и микробиологии им.Н.Ф.Гамалеи РАМН ГУ), Российская Федерация.
- Конвидеция – раствор для внутримышечного введения. НПО ПЕТРОВАКС ФАРМ, Российская Федерация.
- Спутник Лайт – раствор для внутримышечного введения. Медгамал (филиал НИИ эпидемиологии и микробиологии им.Н.Ф.Гамалеи РАМН ГУ), Российская Федерация.
- КовиВак – суспензия для внутримышечного введения. ФНЦИРИП им. Чумакова РАН, ФГБНУ, Российская Федерация.
Официальный источник: https://medum.ru/sputnik-v