Описание препарата Спрайсел® (таблетки, покрытые пленочной оболочкой, 100 мг) основано на официальной инструкции, утверждено компанией-производителем в 2012 году
Дата согласования: 17.10.2012
Особые отметки:
Содержание
- Фотографии упаковок
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Заказ в аптеках Москвы
- Отзывы
Фотографии упаковок
17.10.2012
Действующее вещество
ATX
Фармакологическая группа
Состав
| Таблетки, покрытые пленочной оболочкой | 1 табл. |
| активное вещество: | |
| дазатиниб | 20 мг |
| 50 мг | |
| 70 мг | |
| 80 мг | |
| 100 мг | |
| 140 мг | |
| вспомогательные вещества: лактозы моногидрат — 27/67,5/94,5/108/135/189 мг; МКЦ — 27/67,5/94,5/108/135/189 мг; гипролоза — 2,4/6/8,4/9?6/12/16,8 мг; кроскармеллоза натрия — 3,2/8/11,2/12,8/16/22,4 мг; магния стеарат — 0,4/1/1,4/1,6/2/2,8 мг; Opadry белый YS-1-18177-A (титана диоксид — 31,2% — 1/2,2/2,65/3,5/3,7/5,24 мг, гипромеллоза-6 cP — 59,8% — 1,9/4,17/5/6,7/7,2/10,05 мг, макрогол 400 — 9% — 0,3/0,63/0,75/1/1,1/1,51 мг) — 3,2/7/8,4/11,2/12/16,8 мг |
Описание лекарственной формы
Таблетки 20 мг: круглые двояковыпуклые, покрытые пленочной оболочкой белого или почти белого цвета, с маркировкой «BMS» на одной стороне и «527» — на другой.
Таблетки 50 мг: овальные двояковыпуклые, покрытые пленочной оболочкой белого или почти белого цвета, с маркировкой «BMS» на одной стороне и «528» — на другой.
Таблетки 70 мг: круглые двояковыпуклые, покрытые пленочной оболочкой белого или почти белого цвета, с маркировкой «BMS» на одной стороне и «524» — на другой.
Таблетки 80 мг: треугольные двояковыпуклые, покрытые пленочной оболочкой белого или почти белого цвета, с гравировкой «BMS» и «80» (надпись BMS над цифрами 80) на одной стороне и «855» на другой.
Таблетки 100 мг: овальные двояковыпуклые, покрытые пленочной оболочкой белого или почти белого цвета, с маркировкой «BMS 100» на одной стороне и «852» — на другой.
Таблетки 140 мг: круглые двояковыпуклые, покрытые пленочной оболочкой белого или почти белого цвета, с гравировкой «BMS» и «140» (надпись BMS над цифрами 140) на одной стороне и «857» на другой.
Фармакологическое действие
Фармакологическое действие
—
противоопухолевое.
Фармакодинамика
Дазатиниб ингибирует тирозинкиназу BCR-ABL и тирозинкиназы семейства SRC, а также многие другие онкогенные киназы, включая c-KIT, киназу эфринового (EPH) рецептора и PDGFβ-рецептор. Дазатиниб связывается с активной и неактивной формами фермента BCR-ABL и в субнаномолярных концентрациях (0,6–0,8 нмоль/мл) ингибирует ее.
Механизм действия. В условиях in vitro дазатиниб проявляет активность на клеточных моделях лейкоза, как в отношении чувствительных, так и резистентных к иматинибу клеток. Дазатиниб преодолевает резистентность к иматинибу, связанную с гиперэкспрессией BCR-ABL, мутациями домена BCR-ABL киназы, активацией альтернативных механизмов, индуцирующих киназы семейства SRC (LYN, НСК), а также с гиперэкспрессией гена множественной лекарственной резистентности.
Фармакокинетика
Всасывание. Абсорбция быстрая. Cmax дазатиниба наблюдалась через 0,5–3 ч после приема внутрь. AUC и выведение являются дозозависимыми в диапазоне доз от 25 до 120 мг 2 раза в день. Средний общий терминальный T1/2 дазатиниба у пациентов составляет 5–6 ч.
При приеме однократной дозы 100 мг дазатиниба через 30 мин после приема пищи с высоким содержанием жира отмечается увеличение средней AUC на 14%; после приема пищи с низким содержанием жира — на 21%. Прием пищи не оказывает существенного влияния на всасывание.
Распределение. Кажущийся Vd дазатиниба составляет 2505 л, что свидетельствует о значительном распределении во внесосудистом пространстве. При используемых в клинической практике концентрациях связывание дазатиниба с белками плазмы составляет 96%.
Метаболизм. Изофермент CYP3A4 является основным ферментом, ответственным за метаболизм дазатиниба. После приема внутрь 100 мг 14С-дазатиниба здоровыми добровольцами 29% радиоактивности в плазме приходилось на долю неизмененного дазатиниба. Судя по концентрации в плазме и активности in vitro, можно предположить, что метаболиты не играют большой роли в фармакологическом действии дазатиниба.
Выведение. Препарат выводится главным образом кишечником, преимущественно в виде метаболитов. После однократного приема внутрь 14С-дазатиниба 4 и 85% радиоактивности выводится почками и кишечником соответственно в течение 10 сут. Неизмененный дазатиниб составляет 0,1 и 19% дозы, выводимой почками и кишечником соответственно, остальная часть дозы представлена метаболитами.
Фармакокинетику дазатиниба изучали у 8 пациентов с умеренными нарушениями функции печени после однократного приема препарата в дозе 50 мг и у 5 пациентов с тяжелыми нарушениями функции печени после однократного приема препарата в дозе 20 мг в сравнении с фармакокинетикой у здоровых добровольцев после приема препарата в дозе 70 мг. Значения Cmax и AUC для дазатиниба были ниже на 47 и 8% соответственно при умеренном повреждении печени, по сравнению со значениями Cmax и AUC у здоровых добровольцев. У пациентов с тяжелым нарушением функции печени снижение значений Cmax и AUC для дазатиниба достигало 43 и 28% соответственно.
У пациентов с нарушениями функции почек фармакокинетика дазатиниба не изменяется.
Показания
впервые выявленный хронический миелолейкоз в хронической фазе;
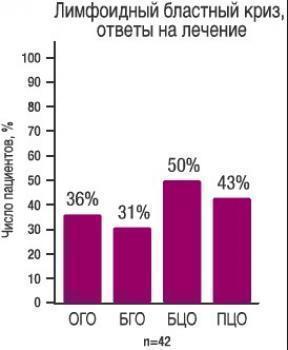
хронический миелолейкоз в хронической фазе, фазе акселерации или фазе миелоидного или лимфоидного бластного криза при резистентности или непереносимости предыдущей терапии, включая иматиниб;
острый лимфобластный лейкоз с положительной филадельфийской хромосомой при резистентности или непереносимости предыдущей терапии.
Противопоказания
повышенная чувствительность к дазатинибу или другим компонентам препарата;
беременность и период кормления грудью;
возраст до 18 лет.
С осторожностью — печеночная недостаточность; одновременный прием антикоагулянтов и препаратов, влияющих на функцию тромбоцитов; удлинение интервала QT или риск его удлинения (также при одновременном приеме препаратов, удлиняющих интервал QT); наследственная непереносимость лактозы, недостаточность лактазы или нарушение всасывания глюкозы и галактозы (препарат содержит лактозу 135 и 189 мг, соответственно суточной дозе препарата Спрайсел® в 100 или 140 мг); одновременное применение с субстратами изофермента CYP3A4 с узким терапевтическим диапазоном.
Применение при беременности и кормлении грудью
Применение препарата во время беременности и в период лактации противопоказано.
Способ применения и дозы
Внутрь, целиком, независимо от приема пищи.
Рекомендуемые начальные дозы препарата Спрайсел®:
— 100 мг 1 раз в день (утром или вечером) — в хронической фазе хронического миелолейкоза;
— 140 мг 1 раз в день (утром или вечером) — в остальных случаях.
Изменение дозы возможно с учетом клинического ответа и переносимости препарата пациентом.
Повышение дозы
В случае отсутствия гематологического или цитогенетического ответа при рекомендуемой начальной дозе возможно увеличение дозы препарата Спрайсел® до:
— 140 мг 1 раз в день — при хронической фазе хронического миелолейкоза;
— 180 мг 1 раза в день — при продвинутых фазах хронического миелолейкоза (фаза акселерации или бластного криза) или остром лимфобластном лейкозе с положительной филадельфийской хромосомой.
Прием препарата прекращают при возникновении признаков прогрессирования заболевания или непереносимости препарата пациентом.
Коррекция дозы вследствие побочных эффектов
Миелосупрессия
При миелосупрессии следует уменьшить дозу, прервать терапию или отменить ее. В случае необходимости следует провести трансфузию тромбоцитарной или эритроцитарной массы. При устойчивой миелосупрессии возможно применение гемопоэтических факторов роста.
Коррекция дозы при нейтропении и тромбоцитопении
Хроническая фаза хронического миелолейкоза (начальная доза — 100 мг 1 раз в день)
При абсолютном числе нейтрофилов <0,5·109/л или числе тромбоцитов <50·109/л:
1. Сделать перерыв в лечении препаратом Спрайсел® до достижения абсолютного числа нейтрофилов ≥1,0·109/л и числа тромбоцитов ≥50·109/л.
2. Возобновить терапию в прежней дозе.
3. При количестве тромбоцитов <25·109/л или абсолютном числе нейтрофилов <0,5·109/л, наблюдающихся более 7 дней — сделать перерыв в лечении и, после достижения исходных показателей, терапию возобновить в сниженной дозе 80 мг 1 раз в день (второй эпизод). Для пациентов с вновь выявленным хроническим миелолейкозом в хронической фазе при наступлении третьего эпизода тромбоцито/нейтропении снижают дозу до 50 мг 1 раз в день. При наступлении третьего эпизода тромбоцито/нейтропении у пациентов с другими фазами миелолейкоза и наличии устойчивости к предшествующей терапии другими препаратами (включая иматиниб), или при непереносимости ее прекращают лечение препаратом Спрайсел®.
Хронический миелолейкоз (в фазе акселерации или бластного криза) и острый лимфобластный лейкоз с положительной филадельфийской хромосомой (начальная доза — 140 мг 1 раз в день)
При абсолютном числе нейтрофилов <0,5·109/л или числе тромбоцитов <10·109/л:
1. Установить, обусловлена ли цитопения лейкозом (аспирация или биопсия костного мозга).
2. Если цитопения не связана с лейкозом, лечение следует прервать до достижения абсолютного числа нейтрофилов ≥1,0·109/л и числа тромбоцитов ≥20·109/л и возобновить терапию в прежней дозе.
3. В случае рецидива цитопении следует повторно верифицировать природу цитопении и возобновить терапию в сниженной дозе 100 мг 1 раз в день (второй эпизод) или 80 мг 1 раз в день (третий эпизод).
4. Если возникшая цитопения связана с лейкозом, следует рассмотреть вопрос об увеличении дозы до 180 мг 1 раз в день.
При развитии тяжелых негематологических побочных эффектов лечение приостанавливают до исчезновения симптоматики побочного эффекта или до улучшения состояния пациента. Лечение можно возобновить в сниженной дозе.
Применение при нарушении функции почек
Почечный клиренс дазатиниба и его метаболитов составляет <4%, поэтому коррекции дозы при нарушенной функции почек не требуется.
Применение при нарушении функции печени
Дазатиниб метаболизируется главным образом печенью, поэтому препарат следует использовать с осторожностью у пациентов с нарушением функции печени умеренной и тяжелой степени.
Применение у пациентов пожилого возраста
Клинически значимых различий в фармакокинетике у пожилых пациентов не выявлено, поэтому корректировка дозы не требуется.
Побочные действия
У большинства пациентов побочные явления были преходящими. Лечение препаратом Спрайсел® было прекращено из-за побочных реакций у 5% пациентов с впервые выявленной хронической фазой хронического миелолейкоза, 15% пациентов в хронической фазе хронического миелолейкоза с резистентностью к иматинибу или его непереносимостью, 16% — в фазе акселерации хронического миелолейкоза, 15% — в фазе миелоидного бластного криза хронического миелолейкоза; 8% — в фазе лимфоидного бластного криза хронического миелолейкоза и 8% — в фазе острого лимфобластного лейкоза с положительной филадельфийской хромосомой.
Побочные явления при применении препарата Спрайсел® представлены по частоте их регистрации: очень часто — ≥1/10; часто — ≥1/100, <1/10; нечасто — ≥1/1000, <1/100; редко — ≥1/10000, <1/1000.
Инфекции и инвазии: очень часто — инфекции (в т.ч. бактериальные, вирусные, грибковые), пнвмония (в т.ч. бактериальная, вирусная и грибковая), инфекции верхних дыхательных путей, герпетические инфекции, энтероколит; нечасто — сепсис (в т.ч. с летальным исходом).
Со стороны кроветворной системы: часто — фебрильная нейтропения, панцитопения; редко — эритробластопения.
Со стороны иммунной системы: нечасто — реакция гиперчувствительности (в т.ч. узловатая эритема).
Нарушения метаболизма: часто — анорексия, нарушение аппетита; нечасто — гиперурикемия, гипоальбуминемия.
Со стороны нервной системы: очень часто — головная боль; часто — бессонница, депрессия, нейропатия (включая периферическую нейропатию), головокружение, извращение вкуса, сонливость; нечасто — беспокойство, эмоциональная лабильность, психоз, снижение либидо, мозговое кровоизлияние, тремор, обморок, амнезия; редко — судороги, нарушение мозгового кровообращения (инсульт), транзиторная ишемическая атака, воспаление зрительного нерва.
Со стороны органа зрения: часто — нарушение зрения, сухость глаз; нечасто — конъюнктивит.
Со стороны органов слуха и равновесия: часто — шум в ушах; нечасто — вертиго.
Со стороны ССС: очень часто — кровотечения (кроме желудочно-кишечных кровотечений и кровотечений ЦНС, указанных в соответствующих разделах); часто — приливы крови к лицу; повышение АД, перикардиальный выпот, аритмия (включая тахикардию), застойная сердечная недостаточность/дисфункция миокарда, ощущение сердцебиения; нечасто — удлинение интервала QT на ЭКГ, стенокардия, кардиомегалия, снижение АД, тромбофлебит, перикардит, желудочковая аритмия (включая желудочковую тахикардию), инфаркт миокарда (в т.ч. с летальным исходом); редко — легочное сердце, миокардит, острый коронарный синдром, мраморность кожи.
Со стороны дыхательной системы: очень часто — плевральный выпот, одышка; часто — кашель, легочные инфильтраты, отек легких, пневмонит, легочная гипертензия; нечасто — бронхиальная астма, бронхоспазм; редко — острый респираторный дистресс-синдром.
Со стороны пищеварительной системы: очень часто — диарея, тошнота, рвота, боли в животе; часто — воспаление слизистых оболочек (включая мукозит/стоматит), желудочно-кишечные кровотечения, диспепсия, вздутие живота, запоры, гастрит, поражения слизистой оболочки рта; колит (включая нейтропенический колит), анорексия; нечасто — дисфагия, асцит, анальные трещины, изъязвления верхних отделов ЖКТ, панкреатит, эзофагит; редко — желудочно-кишечная энтеропатия с потерей белка.
Со стороны печени и желчевыводящих путей: нечасто — холестаз, холецистит, гепатит.
Со стороны кожи и подкожной клетчатки: очень часто — кожная сыпь; часто — зуд, угри, алопеция, сухость кожи, гипергидроз, крапивница, дерматит (включая экзему); нечасто — кожные язвы, буллезный дерматоз. нарушение пигментации, поражение ногтей, фотосенсибилизация, острый фебрильный нейтрофильный дерматоз, панникулит, синдром ладонно-подошвенной эритродизестезии.
Со стороны опорно-двигательного аппарата и соединительной ткани: очень часто — мышечно-скелетная боль, часто — артралгия, миозит, мышечная слабость, миалгия; нечасто — скелетно-мышечная скованность, увеличение активности креатинфосфокиназы в крови, рабдомиолиз; редко — тендинит.
Со стороны мочевыделительной системы: нечасто — почечная недостаточность, учащенное мочеиспускание, протеинурия.
Со стороны репродуктивной системы: нечасто — гинекомастия, нарушение менструального цикла.
Прочие: очень часто — задержка жидкости, локализованные отеки подкожной клетчатки различной локализации, отеки языка, губ, конъюнктивы, усталость, повышение температуры; часто — генерализованные отеки, астения, боль, боль в груди, распространенный отек, озноб, снижение или увеличение массы тела, спутанность сознания, кровоизлияния (в т.ч. конъюнктивальные, гематомы, кровоподтеки, кровоточивость десен, точечные, в склеру глаза); нечасто — недомогание, непереносимость высоких и низких температур, синдром лизиса опухоли.
Кроме того, при применении препарата получена информация о следующих явлениях, частота которых не установлена и связь их с применением препарата не доказана.
Со стороны ССС: фибрилляция/трепетание предсердий; тромбоэмболия (в т.ч. легочная эмболия, тромбоз глубоких вен).
Со стороны дыхательной системы: интерстициальная пневмония.
Со стороны пищеварительной системы: желудочно-кишечное кровотечение с летальным исходом.
Изменения лабораторных показателей: тромбоцитопения, анемия и нейтропения 3-й и 4-й степеней, особенно у пациентов с продвинутыми фазами хронического миелолейкоза или острым лимфобластным лейкозом с положительной филадельфийской хромосомой; гипокалиемия, гипокальциемия, гипофосфатемия; повышение активности печеночных трансаминаз (АСТ, АЛТ); повышение концентрации билирубина и/или креатинина в сыворотке крови.
Взаимодействие
Препараты, которые могут повышать концентрацию дазатиниба в плазме крови
Ингибиторы изофермента CYP3A4: дазатиниб является субстратом изофермента CYP3A4. Ингибиторы изофермента CYP3A4 (например кетоконазол, итраконазол, эритромицин, кларитромицин, ритонавир, атазанавир, индинавир, нелфинавир, саквинавир, телитромицин, грейпфрутовый сок) могут повышать концентрацию дазатиниба в плазме крови, поэтому следует избегать их совместного применения с дазатинибом. Пациенты, у которых не удается избежать системного приема мощного ингибитора изофермента CYP3A4, должны находиться под тщательным наблюдением для своевременного выявления признаков токсичности.
Препараты, которые могут снижать концентрацию дазатиниба в плазме крови
Индукторы изофермента CYP3A4: индукторы изофермента CYP3A4 могут снижать концентрацию дазатиниба в плазме. Следует избегать совместного применения мощных индукторов изофермента CYP3A4 с дазатинибом. Пациентам, принимающим индукторы изофермента CYP3A4 (например дексаметазон, фенитоин, карбамазепин, рифампицин, фенобарбитал или препараты зверобоя продырявленного (Hypericum perforatum), вместо этих препаратов следует назначать препараты, не обладающие (или обладающие в минимальной степени) способностью индуцировать этот изофермент.
Антациды (препараты, содержащие алюминия гидроксид/магния гидроксид): если антациды необходимы, рекомендуется их принимать не менее чем за 2 ч до или через 2 ч после приема дазатиниба
Блокаторы Н2-гистаминовых рецепторов и ингибиторы протонной помпы: длительное подавление секреции кислоты желудочного сока блокаторами Н2-гистаминовых рецепторов и ингибиторами протонной помпы (например фамотидином и омепразолом) может приводить к уменьшению концентрации дазатиниба. Совместное применение этих препаратов и дазатиниба не рекомендуется. В качестве их альтернативы можно использовать антациды (за 2 ч до или через 2 ч после приема препарата Спрайсел®).
Влияние дазатиниба на другие лекарственные препараты
Субстраты изофермента CYP3A4: дазатиниб является ингибитором изофермента CYP3A4, поэтому его совместное применение с субстратами изофермента CYP3A4 может усилить действие данного субстрата. Субстраты изофермента CYP3A4 с узким терапевтическим диапазоном, такие как алфентанил, астемизол, терфенадин, цизаприд, циклоспорин, фентанил, пимозид, хинидин, сиролимус, такролимус и алкалоиды спорыньи (эрготамин, дигидроэрготамин) следует использовать с осторожностью у пациентов, получающих дазатиниб.
Передозировка
Передозировка препарата Спрайсел® зарегистрирована у 2 пациентов, принимавших в течение недели по 280 мг препарата в день, что привело к значительному снижению числа тромбоцитов. В случае передозировки требуется тщательное наблюдение за пациентами с целью контроля степени миелосупрессии; при необходимости — симптоматическая терапия.
Особые указания
При лечении препаратом Спрайсел® могут возникать тяжелые (3-й и 4-й степени по общим критериям токсичности Национального института рака США (NCI СТС) тромбоцитопения, анемия и нейтропения. Полный клинический анализ крови следует проводить еженедельно первые 2 мес лечения, а затем — ежемесячно или чаще, по клиническим показаниям.
Угнетение костного мозга обычно обратимо и проходит при временной отмене или снижении дозы препарата Спрайсел®.
При тяжелых желудочно-кишечных кровотечениях обычно требуется временная отмена препарата и гемотрансфузия. Большинство случаев кровотечений связаны с тяжелой тромбоцитопенией.
При приеме препарата Спрайсел® может наблюдаться задержка жидкости, в т.ч. тяжелой степени (выраженный асцит, генерализованный отек, тяжелый отек легких). При появлении одышки или сухого кашля необходим рентгенологический контроль органов грудной клетки. Задержка жидкости обычно купируется при применении поддерживающей терапии с включением диуретиков или короткого курса ГКС. При выраженном плевральном выпоте требуется проведение оксигенотерапии и торакоцентеза. Задержка жидкости наблюдается чаще при приеме препарата 2 раза в сутки.
Следует учесть, что задержка жидкости и одышка более характерны для пациентов старше 65 лет, поэтому необходимо обеспечить тщательное наблюдение за пациентами данной возрастной группы.
Дазатиниб следует использовать с осторожностью у пациентов с удлиненным QT-интервалом или с риском его удлинения (гипокалиемия, гипомагниемия, врожденный синдром удлиненного QT-интервала, терапия антиаритмическими и другими препаратами, способными удлинять QT-интервал, предшествующая терапия высокими дозами антрациклинов). До назначения препарата Спрайсел® следует провести коррекцию гипокалиемии и гипомагниемии.
Во время терапии препаратом Спрайсел® необходимо тщательно контролировать параметры сердечной деятельности и осуществлять наблюдение за пациентами группы риска или имеющими заболевания сердца в анамнезе с целью выявления и при необходимости, коррекции возможных побочных реакций со стороны ССС.
При развитии гипокальциемии состояние корректируется приемом внутрь препаратов кальция. При повышении уровня трансаминаз или билирубина следует уменьшить дозу препарата или приостановить его прием.
В связи с тем, что в ходе лечения препаратом Спрайсел®, а также по прошествии года и более после окончания лечения отмечались случаи развития легочной артериальной гипертензии (ЛАГ), до начала лечения препаратом Спрайсел следует провести обследование пациента с целью выявления возможных признаков и симптомов заболеваний сердца и легких. Если в ходе лечения препаратом Спрайсел® у пациента отмечаются одышка или усталость, необходимо исключить наиболее типичную этиологию, включая плевральный выпот, отек легких, анемию и наличие инфильтрата в легких. При этом необходимо учитывать рекомендации, данные в разделе «Способ применения и дозы» для случаев развития негематологических побочных реакций: при развитии тяжелых негематологических побочных эффектов лечение приостанавливают до исчезновения симптоматики побочного эффекта или до улучшения состояния пациента. Если в процессе обследования пациента не был поставлен другой диагноз, следует принять к рассмотрению диагноз ЛАГ. В случае подтверждения ЛАГ у пациента, лечение препаратом Спрайсел® прекращают без последующего возобновления, обеспечив последующий контроль состояния пациента в соответствии со стандартными рекомендациями. После отмены препарата у пациентов с ЛАГ наблюдалось улучшение их гемодинамических и клинических параметров.
Пациентам (как мужчинам, так и женщинам) во время лечения и как минимум в течение 3 мес после него необходимо использовать надежные методы контрацепции. Если беременность наступила во время лечения препаратом Спрайсел®, а также если стало известно, что препарат использовался во время беременности, следует немедленно проинформировать пациентку о возможном риске для плода.
Неизвестно, проникает ли дазатиниб в грудное молоко. На время лечения препаратом Спрайсел® кормление грудью следует прекратить.
Содержание лактозы. Препарат Спрайсел® содержит лактозу: в суточной дозе 100 мг — 135 мг лактозы и в суточной дозе 140 мг — 189 мг лактозы.
Влияние на способность к вождению автотранспорта и управлению механизмами. Исследований по влиянию препарата на способность к вождению и управлению техникой не проводилось. Если больной отмечает связанные с лечением симптомы, такие как головокружение и нарушения зрения влияющие на его способность к концентрации и быстроту реакции, рекомендуется отказаться от управления автомобилем и выполнения потенциально опасных видов деятельности, требующих повышенной концентрации внимания и быстроты психомоторных реакций.
Внимание: в упаковку препарата помещен контейнер с осушителем, на который нанесены рисунок и предупредительная надпись — «Do not eat. Contents: Silica Gel.» — «Не есть. Содержимое: Силикагель». Осушитель предназначен для защиты препарата от влаги. Контейнер с осушителем не вскрывать; содержимое контейнера не принимать внутрь!
Форма выпуска
Таблетки, покрытые пленочной оболочкой, 20 мг, 50 мг, 70 мг, 80 мг, 100 мг, 140 мг. По 60 табл. (для дозировок 20/50/70 мг) и 30 табл. (для дозировок 80/100/140 мг) во флаконах из ПЭ высокого давления с крышкой, недоступной для открывания детьми.
Внутрь флакона (для дозировок 20, 50, 70 и 100 мг) помещают контейнер с осушителем (силикагель) на который нанесена предупредительная маркировка: «Do not eat. Contents: Silica Gel.» — «Не есть. Содержимое: Силикагель».
Горлышко флакона закрывают ватным тампоном (только для дозировок 20/50/70 мг) и запаивают алюминиевой фольгой. 1 флакон помещают в картонную пачку.
Производитель
Производитель, фасовщик (первичная упаковка)
Бристол-Майерс Сквибб Компани.
4601 Хайвэй, 62 Ист, Маунт Вернон, Индиана 47620, США.
Bristol-Myers Squibb Company.
4601 Highway, 62 East, Mount Vernon, Indiana, 47620 USA.
Упаковщик (вторичная упаковка), выпускающий контроль качества
Бристол-Майерс Сквибб Ср.Л., Италия.
Локалита Фонтана дель Черазо, 03012, Ананьи (ФР), Италия.
Bristol-Myers Squibb S.r.L., Italy.
Localita Fontana del Ceraso, 03012, Anagni (FR), Italy.
Юридическое лицо, на имя которого выдано регистрационное удостоверение.
Бристол-Майерс Сквибб Компани, США.
345, Парк-авеню, г. Нью-Йорк, штат Нью-Йорк, США.
Bristol-Myers Squibb Company, USA
345, Park Avenue, New York, New York, USA.
Претензии потребителей направлять по адресу.
ООО «Бристол-Майерс Сквибб», Россия.
105064, Москва, ул. Земляной вал, 9.
Тел.: +7 (495) 755-92-67, факс: +7 (495) 755-92-62.
Условия отпуска из аптек
По рецепту.
Условия хранения
При температуре 15–30 °C.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Спрайсел® (Sprycel®) инструкция по применению
📜 Инструкция по применению Спрайсел®
💊 Состав препарата Спрайсел®
✅ Применение препарата Спрайсел®
📅 Условия хранения Спрайсел®
⏳ Срок годности Спрайсел®
Описание лекарственного препарата
Спрайсел®
(Sprycel®)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для электронного издания справочника Видаль 2011
года, дата обновления: 2019.12.19
Лекарственные формы
| Спрайсел® |
Таб., покр. пленочной оболочкой, 20 мг: 60 шт. рег. №: ЛСР-000256/08 |
|
|
Таб., покр. пленочной оболочкой, 50 мг: 60 шт. рег. №: ЛСР-000256/08 |
||
|
Таб., покр. пленочной оболочкой, 70 мг: 60 шт. рег. №: ЛСР-000256/08 |
||
|
Таб., покр. пленочной оболочкой, 100 мг: 30 шт. рег. №: ЛСР-008175/10 |
Форма выпуска, упаковка и состав
препарата Спрайсел®
Таблетки, покрытые пленочной оболочкой белого или почти белого цвета, круглые, двояковыпуклые, с маркировкой «BMS» на одной стороне и «527» — на другой.
Вспомогательные вещества: лактозы моногидрат, целлюлоза микрокристаллическая, гипролоза, кроскармеллоза натрия, магния стеарат, опадрай белый (титана диоксид, гипромеллоза-6cP, макрогол 400).
60 шт. — флаконы полиэтиленовые* (1) — пачки картонные.
Таблетки, покрытые пленочной оболочкой белого или почти белого цвета, овальные, двояковыпуклые, с маркировкой «BMS» на одной стороне и «528» — на другой.
Вспомогательные вещества: лактозы моногидрат, целлюлоза микрокристаллическая, гипролоза, кроскармеллоза натрия, магния стеарат, опадрай белый (титана диоксид, гипромеллоза-6cP, макрогол 400).
60 шт. — флаконы полиэтиленовые* (1) — пачки картонные.
Таблетки, покрытые пленочной оболочкой белого или почти белого цвета, круглые, двояковыпуклые, с маркировкой «BMS» на одной стороне и «524» — на другой.
Вспомогательные вещества: лактозы моногидрат, целлюлоза микрокристаллическая, гипролоза, кроскармеллоза натрия, магния стеарат, опадрай белый (титана диоксид, гипромеллоза-6cP, макрогол 400).
60 шт. — флаконы полиэтиленовые* (1) — пачки картонные.
Таблетки, покрытые пленочной оболочкой белого или почти белого цвета, овальные, двояковыпуклые, с гравировкой «BMS 100» на одной стороне и «852» — на другой.
Вспомогательные вещества: лактозы моногидрат, целлюлоза микрокристаллическая, гипролоза, кроскармеллоза натрия, магния стеарат, опадрай белый (титана диоксид, гипромеллоза-6cP, макрогол 400).
30 шт. — флаконы полиэтиленовые* (1) — пачки картонные.
* во флаконы помещен контейнер с осушителем.
Фармакологическое действие
Противоопухолевый препарат, ингибитор протеинтирозинкиназы.
Дазатиниб ингибирует тирозинкиназу BCR-ABL и тирозинкиназы семейства SRC, а также многие другие онкогенные киназы, включая c-KIT, киназу эфринового (ЕРН) рецептора и PDGFβ-рецептор. Дазатиниб связывается с активной и неактивной формами фермента BCR-ABL и в субнаномолярных концентрациях (0.6-0.8 нмоль/мл) ингибирует ее.
В условиях in vitro дазатиниб проявляет активность на клеточных моделях лейкоза, как в отношении чувствительных, так и резистентных к иматинибу клеток. Дазатиниб преодолевает резистентность к иматинибу, связанную с гиперэкспрессией BCR-ABL, мутациями домена BCR-ABL киназы, активацией альтернативных механизмов, индуцирующих киназы семейства SRC (LYN, ИСК), а также с гиперэкспрессией гена множественной лекарственной резистентности.
Фармакокинетика
Всасывание
Абсорбция быстрая. Cmax дазатиниба наблюдается через 0.5-3 ч после приема внутрь. AUC и выведение являются дозозависимыми в диапазоне доз от 25 до 120 мг 2 раза/сут. При приеме однократной дозы 100 мг дазатиниба через 30 мин после приема пищи с высоким содержанием жира отмечается увеличение средней AUC на 14%; после приема пищи с низким содержанием жира — на 21%. Прием пищи не оказывает существенного влияния на всасывание.
Распределение
Кажущийся Vd дазатиниба составляет 2505 л, что свидетельствует о значительном распределении во внесосудистом пространстве. Связывание дазатиниба 96%.
Метаболизм
Изофермент CYP3A4 является основным ферментом, ответственным за метаболизм дазатиниба. После приема внутрь 100 мг [14С]- дазатиниба здоровыми добровольцами, 29% радиоактивности в плазме приходилось на долю неизмененного дазатиниба. Судя по концентрации в плазме и активности in vitro можно предположить, что метаболиты не играют большой роли в фармакологическом действии дазатиниба,
Выведение
Препарат выводится, главным образом, кишечником, преимущественно в виде метаболитов. После однократного приема внутрь [14С]-дазатиниба 4% и 85% радиоактивности выводится почками и кишечником, соответственно, в течение 10 сут. Неизмененный дазатиниб составляет 0.1% и 19% дозы, выводимой почками и кишечником, соответственно, остальная часть дозы представлена метаболитами.
Средний общий терминальный T1/2 дазатиниба у пациентов составляет 5-6 ч.
Фармакокинетика в особых клинических случаях
Фармакокинетику дазатиниба изучали у 8 пациентов с умеренными нарушениями функции печени после однократного приема препарата в дозе 50 мг и у 5 пациентов с тяжелым нарушением функции печени после однократного приема препарата в дозе 20 мг в сравнении с фармакокинетикой у здоровых добровольцев после приема препарата в дозе 70 мг. Значения Cmax и AUC для дазатиниба были ниже на 47% и 8%, соответственно, при умеренном повреждении печени, по сравнению со значениями у здоровых добровольцев. У пациентов с тяжелым нарушением функции печени снижение значений Cmax и AUC для дазатиниба достигало 43% и 28%, соответственно.
У пациентов с нарушениями функции почек фармакокинетика дазатиниба не изменяется.
Показания препарата
Спрайсел®
- хронический миелолейкоз в хронической фазе, фазе акселерации или фазе лимфоидного или миелоидного бластного криза при резистентности или непереносимости предыдущей терапии, включая иматиниб;
- острый лимфобластный лейкоз с положительной филадельфийской хромосомой при резистентности или непереносимости предыдущей терапии.
Режим дозирования
Препарат принимают независимо от приема пищи. Таблетки следует проглатывать целиком.
При хронической фазе хронического миелолейкоза рекомендуемая начальная доза составляет 100 мг 1 раз/сут утром или вечером.
В остальных случаях — 140 мг 1 раз/сут утром или вечером.
Изменение дозы возможно с учетом клинического ответа и переносимости препарата пациентом.
В случае отсутствия гематологического или цитогенетического ответа возможно увеличение дозы препарата при хронической фазе хронического миелолейкоза до 140 мг 1 раз/сут, при далеко зашедшем хроническом миелолейкозе (фаза акселерации или бластного криза) и остром лимфобластном лейкозе с положительной филадельфийской хромосомой — до 180 мг 1 раз/сут.
Рекомендации по коррекции дозы препарата вследствие побочных эффектов
Миелосупрессия
При миелосупрессии следует уменьшить дозу, прервать терапию или отменить ее. В случае необходимости следует провести трансфузию тромбоцитарной или эритроцитарной массы. При устойчивой миелосупрессии возможно применение гемопоэтических факторов роста.
Хроническая фаза хронического миелолейкоза (начальная доза 100 мг 1 раз/сут)
При абсолютном числе нейтрофилов < 0.5×109/л или числе тромбоцитов < 50×109/л:
- Сделать перерыв в лечении препаратом Спрайсел® до достижения абсолютного числа нейтрофилов ≥ 1×109/л и числа тромбоцитов ≥ 50×109/л.
- Возобновить терапию в прежней дозе.
- При количестве тромбоцитов < 25×109/л или абсолютном числе нейтрофилов < 0.5×109/л, наблюдающихся более 7 дней — сделать перерыв в лечении и после достижения исходных показателей, терапию возобновить в сниженной дозе 80 мг 1 раз/сут (второй эпизод) или прекратить лечение (третий эпизод).
Хронический миелолейкоз (в фазе акселерации или бластного криза) и остром лимфобластном лейкозе с положительной филадельфийской хромосомой (начальная доза 140 мг 1 раз/сут)
При абсолютном числе нейтрофилов < 0.5×109/л или числе тромбоцитов < 10×109/л:
- Установить, обусловлена ли цитопения лейкозом (аспирация или биопсия костного мозга).
- Если цитопения не связана с лейкозом, лечение следует прервать до достижения абсолютного числа нейтрофилов ≥ 1×109/л и числа тромбоцитов ≥ 20×109/л и возобновить терапию в прежней дозе.
- В случае рецидива цитопении следует снова убедиться в природе цитопении и возобновить терапию в сниженной дозе 100 мг 1 раз/сут (второй эпизод) или 80 мг 1 раз/сут (третий эпизод).
- Если возникшая цитопения связана с лейкозом, следует рассмотреть вопрос об увеличении дозы до 180 мг 1 раз/сут.
При развитии тяжелых негематологических побочных эффектов лечение приостанавливают до исчезновения симптоматики побочного эффекта или до улучшения состояния пациента. Лечение можно возобновить в сниженной дозе.
Почечный клиренс дазатиниба и его метаболитов составляет <4%, поэтому коррекции дозы при нарушенной функции почек не требуется.
Дазатиниб метаболизируется главным образом печенью, поэтому препарат следует использовать с осторожностью у пациентов с нарушением функции печени умеренной и тяжелой степени.
Клинически значимых различий в фармакокинетике у пожилых пациентов не выявлено, поэтому коррекция дозы не требуется.
Побочное действие
У большинства пациентов побочные явления были преходящими, лечение препаратом Спрайсел® было прекращено из-за побочных реакций у 9% пациентов в хронической фазе хронического миелолейкоза, у 10% — в фазе акселерации хронического миелолейкоза, у 15% — в фазе миелоидного бластного криза хронического миелолейкоза и у 8% — в фазе лимфоидного бластного криза хронического миелолейкоза или острого лимфобластного лейкоза с положительной филадельфийской хромосомой. В ходе исследований по оптимизации дозы у пациентов с хронической фазой хронического миелолейкоза прерывание терапии препаратом Спрайсел® реже было связано с побочными реакциями при приеме в дозе 100 мг 1 раз/сут, чем при приеме в дозах 70 мг 2 раза/сут (4% и 12% соответственно).
Наиболее часто наблюдались следующие побочные эффекты (у более 20% пациентов): задержка жидкости, диарея, головная боль, кожная сыпь, тошнота, кровоизлияние, усталость, одышка, миалгия, инфекционные осложнения, рвота, кашель, боль в животе, лихорадка, фебрильная нейтропения, обусловленная дазатинибом (5%).
Частота возникновения побочных эффектов приведена в соответствии со шкалой: очень часто (≥1/10), часто (≥1/100, <1/10), нечасто (≥1/1000, <1/100), редко (≥1/10 000, <1/1000).
Инфекции и инвазии: очень часто — инфекции (в т.ч. бактериальные, вирусные, грибковые), пневмония (в т.ч. бактериальная, вирусная и грибковая), инфекции верхних дыхательных путей, герпетические инфекции, энтероколит, сепсис (в т.ч. с летальным исходом).
Со стороны кроветворной системы: часто — фебрильная нейтропения, панцитопения; редко — эритробластопения.
Со стороны иммунной системы: нечасто — реакции гиперчувствительности (в т.ч. узловатая эритема).
Со стороны ЦНС и периферической нервной системы: очень часто — головная боль; часто — бессонница, депрессия, невропатия (включая периферическую невропатию), головокружение, извращение вкуса, сонливость; нечасто — беспокойство, эмоциональная лабильность, психоз, снижение либидо, мозговые кровоизлияния, тремор, обморок, амнезия; редко — судороги, нарушение мозгового кровообращения (инсульт), преходящее нарушение мозгового кровообращения.
Со стороны органа зрения: часто — нарушение зрения, сухость глаз; нечасто — конъюнктивит.
Со стороны органа слуха: часто — шум в ушах; нечасто — вертиго.
Со стороны сердечно-сосудистой системы: очень часто — кровотечения; часто — приливы, повышение АД, перикардиальный выпот, аритмия (включая тахикардию), застойная сердечная недостаточность/дисфункция миокарда, учащенное сердцебиение; нечасто — удлинение интервала QT на ЭКГ, стенокардия, кардиомегалия, снижение АД, тромбофлебит, перикардит, желудочковая аритмия (включая желудочковую тахикардию), инфаркт миокарда; редко — легочное сердце, миокардит, острый коронарный синдром, мраморность кожи.
Со стороны дыхательной системы: очень часто — плевральный выпот, одышка, кашель; часто — легочные инфильтраты, отек легких, пневмонит, легочная гипертензия; нечасто — бронхиальная астма, бронхоспазм; редко — острый респираторный дистресс-синдром.
Со стороны пищеварительной системы: очень часто — диарея, тошнота, рвота, боль в животе; часто — нарушение, аппетита, воспаление слизистых оболочек (включая мукозит/стоматит), желудочно-кишечные кровотечения, диспепсия, вздутие живота, запоры, гастрит, поражение слизистой оболочки рта, колит (включая нейтропенический колит), анорексия; нечасто — дисфагия, асцит, анальные трещины, язвы верхних отделов ЖКТ, панкреатит, эзофагит, холестаз, холецистит, гепатит.
Со стороны кожных покровов: очень часто — кожная сыпь; часто — зуд, угри, алопеция, сухость кожи, гипергидроз, крапивница, дерматит (включая экзему); нечасто — кожные язвы, буллезный дерматоз, нарушения пигментации, поражения ногтей, фотосенсибилизация, острый фебрильный нейтрофильный дерматоз, панникулит, синдром ладонно-подошвенной эритродизестезии.
Со стороны костно-мышечной системы: очень часто — мышечно-скелетная боль; часто — артралгия, миозит, мышечная слабость, скелетно-мышечная скованность; нечасто — увеличение активности креатинфосфокиназы в крови, рабдомиолиз; редко — тендинит.
Со стороны мочевыделительной системы: нечасто — почечная недостаточность, учащенное мочеиспускание, протеинурия.
Со стороны репродуктивной системы: нечасто — гинекомастия, нарушения менструального цикла.
Прочие: очень часто — задержка жидкости, локализованные отеки подкожной клетчатки различной локализации, отек языка, отек губ, отек конъюнктивы, усталость, повышение температуры; часто — астения, боль, боль в груди, распространенный отек, озноб, гиперурикемия; нечасто — недомогание, непереносимость высоких и низких температур, синдром лизиса опухоли, гипоальбуминемия.
Кроме того, при применении препарата получена информация о следующих явлениях, частота которых не установлена, и связь их с применением препарата не доказана.
Со стороны сердечно-сосудистой системы: фибрилляция предсердий/трепетание предсердий, тромбоз/эмболия (в т.ч. — легочная эмболия, тромбоз глубоких вен).
Со стороны дыхательной системы: интерстициальная пневмония.
Со стороны пищеварительной системы: желудочно-кишечное кровотечение с летальным исходом.
Изменения лабораторных показателей: тромбоцитопения, анемия и нейтропения 3 или 4 степени, особенно у пациентов с далеко зашедшей фазой хронического миелолейкоза или острым лимфобластным лейкозом с положительной филадельфийской хромосомой; гипокалиемия, гипокальциемия; повышение активности трансаминаз (АЛТ, ACT), гипербилирубинемия и/или креатинина в сыворотке крови.
Противопоказания к применению
- беременность;
- период лактации (грудного вскармливания);
- детский и подростковый возраст до 18 лет;
- повышенная чувствительность к дазатинибу или другим компонентам препарата.
С осторожностью: печеночная недостаточность; одновременный прием антикоагулянтов и препаратов, влияющих на функцию тромбоцитов; удлинение интервала QT или риск его удлинения (также при одновременном приеме препаратов, удлиняющих интервал QT); наследственная непереносимость лактозы, недостаточность лактазы или нарушение всасывания глюкозы/галактозы (препарат содержит лактозу 135 мг или 189 мг соответственно суточной дозе Спрайсела в 100 мг или 140 мг), одновременное применение с субстратами изофермента CYP3A4, одновременное применение с ингибиторами или индукторами изофермента CYP3A4 с узким терапевтическим диапазоном.
Применение при беременности и кормлении грудью
Пациентам во время лечения и как минимум в течение 3 мес после необходимо использовать надежные методы контрацепции. Если беременность наступила во время лечения препаратом Спрайсел®, а также, если стало известно, что препарат использовался при беременности, следует немедленно проинформировать пациентку о возможном риске для плода.
Неизвестно, проникаете ли дазатиниб в грудное молоко. На время лечения препаратом Спрайсел® кормление грудью следует прекратить.
Применение при нарушениях функции печени
Дазатиниб метаболизируется главным образом печенью, поэтому препарат следует использовать с осторожностью у пациентов с нарушением функции печени умеренной и тяжелой степени.
Применение при нарушениях функции почек
Почечный клиренс дазатиниба и его метаболитов составляет <4%, поэтому коррекции дозы при нарушенной функции почек не требуется.
Применение у детей
Противопоказание: детский и подростковый возраст до 18 лет.
Применение у пожилых пациентов
Клинически значимых различий в фармакокинетике у пожилых пациентов не выявлено, поэтому коррекция дозы не требуется.
Особые указания
Внимание! В упаковку препарата помещен контейнер с осушителем, на который нанесены рисунок и предупредительная надпись — Do not eat. Contents: Silica Gel — Не есть. Содержание: Силикагель. Осушитель предназначен для защиты препарата от влаги. Контейнер с осушителем не вскрывать; содержимое контейнера не принимать внутрь.
Угнетение костномозгового кроветворения
При лечении препаратом Спрайсел® возможны тяжелые (3 и 4 степени по классификации NCI CTC) тромбоцитопения, анемия и нейтропения. Чаще данные реакции регистрируются у пациентов с далеко зашедшей фазой хронического миелолейкоза или острым лимфобластным лейкозом с положительной филадельфийской хромосомой, чем у пациентов с хронической фазой хронического миелолейкоза. Полный клинический анализ крови следует проводить еженедельно первые 2 месяца лечения, а затем ежемесячно или чаще, по клиническим показаниям. Угнетение костномозгового кроветворения обычно обратимо и проходит при временной отмене или снижении дозы Спрайсела.
Кровотечения
Большинство случаев кровотечений на фоне применения препарата были связаны с тяжелой тромбоцитопенией. Тяжелые кровоизлияния в головной мозг, включая фатальные, зарегистрированы у менее 1% пациентов, получавших Спрайсел®. Тяжелые желудочно-кишечные кровотечения отмечены у 4% пациентов; обычно требовалась временная отмена препарата и гемотрансфузий. Другие тяжелые кровотечения зарегистрированы у 2% пациентов.
Задержка жидкости
При приеме Спрайсела может наблюдаться задержка жидкости. Задержка жидкости тяжелой степени была зарегистрирована у 10% пациентов, включая выраженный плевральный и перикардиальный выпот у 7% и 1% пациентов, соответственно. Выраженный асцит и генерализованный отек развились у менее 1% пациентов. У 1% пациентов зарегистрирован тяжелый отек легких. При появлении одышки или сухого кашля необходим рентгенологический контроль органов грудной клетки. Задержка жидкости обычно купируется при применении поддерживающей терапии с включением диуретиков или короткого курса ГКС. При выраженном плевральном выпоте требовались оксигенотерапия и торакоцентез.
Удлинение интервала QT
Дазатиниб следует применять с осторожностью у пациентов с удлиненным интервалом QTc или с риском его удлинения (при гипокалиемии, гипомагниемии, врожденном синдроме удлиненного интервала QT, при терапии антиаритмическими и другими препаратами, способными удлинять интервал QT, при предшествующей терапии высокими дозами антрациклинов). До назначения Спрайсела следует провести коррекцию гипокалиемии и гипомагниемии.
Содержание лактозы
Препарат Спрайсел® содержит лактозу: в суточной дозе 100 мг — 135 мг лактозы и в суточной дозе 140 мг — 189 мг лактозы.
Влияние на способность к управлению транспортными средствами и механизмами
Исследований по влиянию препарата на способность к вождению и управлению техникой не проводилось. Если больной отмечает связанные с лечением симптомы, такие как головокружение и нарушения зрения, влияющие на его способность к концентрации и быстроту реакции, рекомендуется отказаться от управления автомобилем и выполнения потенциально опасных видов деятельности, требующих повышенной концентрации внимания и быстроты психомоторных реакций.
Передозировка
Передозировка препарата Спрайсел® зарегистрирована у двух пациентов, принимавших в течение одной недели по 280 мг/сут, что привело к значительному снижению числа тромбоцитов.
В случае передозировки требуется тщательное наблюдение за пациентами с целью контроля степени миелосупрессии; при необходимости — симптоматическая терапия.
Лекарственное взаимодействие
Препараты, которые могут повышать концентрацию дазатиниба в плазме крови
Дазатиниб является субстратом изофермента CYP3A4. Ингибиторы изофермента CYP3A4 (например, кетоконазол, итраконазол, эритромицин, кларитромицин, ритонавир, атазанавир, индинавир, нелфинавир, саквинавир, телитромицин, грейпфрутовый сок) могут повышать концентрацию дазатиниба в плазме крови, поэтому следует избегать их совместного применения с дазатинибом. Пациенты, у которых не удается избежать системного приема мощного ингибитора изофермента CYP3A4, должны находиться под тщательным наблюдением для своевременного выявления признаков токсичности.
Препараты, которые могут понижать концентрацию дазатиниба в плазме крови
Индукторы изофермента CYP3A4 могут снижать концентрацию дазатиниба в плазме. Следует избегать совместного применения мощных индукторов изофермента CYP3A4 с дазатинибом. Пациентам, принимающим индукторы изофермента CYP3A4 (например, дексаметазон, фенитоин, карбамазепин; рифампицин, фенобарбитал или препараты зверобоя продырявленного), вместо этих препаратов следует назначать препараты, не обладающие (или обладающие в минимальной степени) способностью индуцировать этот изофермент.
Антациды (препараты, содержащие алюминия гидроксид/магния гидроксид) рекомендуется принимать не менее чем за 2 ч до или через 2 ч после приема дазатиниба.
Длительное подавление секреции кислоты желудочного сока блокаторами гистаминовых Н2-рецепторов и ингибиторами протонной помпы (например, фамотидином и омепразолом) может приводить к снижению концентрации дазатиниба. Совместное применение этих препаратов и дазатиниба не рекомендуется. В качестве их альтернативы можно использовать антациды.
Влияние дазатиниба на другие лекарственные препараты
Дазатиниб является ингибитором изофермента CYP3A4, поэтому его совместное применение с субстратами изофермента CYP3A4 может усилить действие данного субстрата. Субстраты изофермента CYP3A4 с узким терапевтическим диапазоном, такие как алфентанил, астемизол, терфенадин, цизаприд, циклоспорин, фентанил, пимозид, хинидин, сиролимус, такролимус и алкалоиды спорыньи (эрготамин, дигидроэрготамин) следует использовать с осторожностью у пациентов, получающих дазатиниб.
Условия хранения препарата Спрайсел®
Препарат следует хранить в недоступном для детей месте при температуре от 15° до 30°C.
Срок годности препарата Спрайсел®
Условия реализации
Препарат отпускается по рецепту.
Контакты для обращений
БРИСТОЛ-МАЙЕРС СКВИББ
(США)

|
|
BRISTOL-MYERS SQUIBB Представительство в России |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
(дазатиниб | dasatinib)
Регистрационный номер:
ЛСР-000256/08 -29/01/08
Торговое название препарата:
Спрайсел (Sprycel)
Международное непатентованное название:
дазатиниб (dasatinib)
Лекарственная форма:
таблетки, покрытые пленочной оболочкой
Состав:
Каждая таблетка, покрытая оболочкой, содержит
активное вещество: дазатиниб 20 мг, 50 мг или 70 мг.
вспомогательные вещества: лактозы моногидрат, целлюлоза микрокристаллическая, гипролоза, кроскармеллоза натрия, магния стеарат, опадрай белый (титана диоксид, гипромеллоза-6сР, макрогол-400).
Описание
Таблетки 20 мг: круглые двояковыпуклые таблетки, покрытые пленочной оболочкой белого или почти белого цвета, с маркировкой «BMS» на одной стороне и «527» на другой.
Таблетки 50 мг: овальные двояковыпуклые таблетки, покрытые пленочной оболочкой белого или почти белого цвета, с маркировкой «BMS» на одной стороне и «528» на другой.
Таблетки 70 мг: круглые двояковыпуклые таблетки, покрытые пленочной оболочкой белого или почти белого цвета, с маркировкой «BMS» на одной стороне и «524» на другой.
Фармакотерапевтическая группа:
противоопухолевое средство, протеинтирозинкиназы ингибитор
Код АТХ: L01XE06
Фармакологические свойства
Фармакодинамика
Дазатиниб в наномолярных концентрациях ингибирует следующие тирозинкиназы: BCR ABL, семейство SRC (SRC, LCK, YES, FYN), c-KIT, EPHA2 и PDGFRβ. С помощью моделирования установлено, что дазатиниб связывается со многими формами ABL киназы.
In vitro дазатиниб проявлял активность в лейкозных клеточных линиях, как чувствительных, так и резистентных к иматинибу. Дазатиниб ингибирует рост клеточных линий хронического миелолейкоза и острого лимфобластного лейкоза с гиперэкспрессией BCR-ABL. В условиях тестов дазатиниб преодолевал резистентность к иматинибу, связанную с мутациями домена BCR-ABL киназы, активацией альтернативных сигнальных путей, включающих киназы семейства SRC (LYN, HCK) и гиперэкспрессией гена лекарственной полирезистентности.
Фармакокинетика
Всасывание
Максимальная концентрация (Cmax) дазатиниба наблюдалась через 0.5–6 часов (Tmax) после приема внутрь. Площадь под кривой “концентрация-время” (AUC) и элиминация пропорциональны дозе в диапазоне доз от 15 до 240 мг/сут. Период полувыведения дазатиниба составляет 3-5 часов.
При приеме 100 мг дазатиниба через 30 минут после приема пищи с высоким содержанием жира отмечается увеличение средней AUC на 14%. Влияние пищи не было клинически значимым.
Распределение
Кажущийся объем распределения дазатиниба составляет 2505 л, что свидетельствует о значительном распределении во внесосудистом пространстве. Дазатиниб и его активный метаболит связывались in vitro с белками плазмы человека на 96% и 93%, соответственно, независимо от концентрации в диапазоне 100-500 нг/мл.
Метаболизм
Дазатиниб активно метаболизируется у людей, главным образом с помощью фермента 3A4 цитохрома P450. CYP3A4 является главным ферментом, участвующим в образовании активного метаболита. Флавин-содержащая монооксигеназа 3 и уридиндифосфат-глюкуронозилтрансфераза также участвуют в образовании метаболитов дазатиниба. В микросомах печени человека дазатиниб проявлял слабое независимое от времени ингибирующее действие в отношении CYP3A4. AUС активного метаболита дазатиниба составляет примерно 5% AUC дазатиниба. Вероятно, активный метаболит не играет большой роли в фармакологическом действии дазатиниба. Описаны и другие неактивные окисленные метаболиты дазатиниба.
Выведение
Препарат выделяется главным образом с калом. После однократного приема внутрь [14C]-дазатиниба примерно 4% и 85% радиоактивности выводится с мочой и калом, соответственно, за 10 дней. Неизмененный дазатиниб составляет 0,1% и 19% дозы, выводимой с мочой и калом, соответственно, а остальная часть дозы представлена метаболитами.
Показания к применению:
- Хронический миелолейкоз в хронической фазе или фазе акселерации, лимфоидный или миелоидный бластный криз при резистентности или непереносимости предыдущей терапии, включая иматиниб
- Острый лимфобластный лейкоз с положительной филадельфийской хромосомой при резистентности или непереносимости предыдущей терапии.
Противопоказания:
Повышенная чувствительность к дазатинибу или другим компонентам препарата.
Беременность и период кормления грудью.
Возраст до 18 лет (эффективность и безопасность не установлены).
С осторожностью: при печеночной недостаточности.
Способ применения и дозы:
Таблетки следует проглатывать целиком.
Рекомендуемая начальная доза СПРАЙСЕЛА при хронической фазе хронического миелолейкоза составляет 100 мг один раз в день утром или вечером независимо от приема пищи.
В остальных случаях рекомендуется принимать СПРАЙСЕЛ внутрь в дозе 70 мг два раза в день утром и вечером во время еды или натощак (140 мг в сутки).
В случае отсутствия гематологического или цитогенетического ответа возможно увеличение дозы СПРАЙСЕЛА до 140 мг 1 раз в день (при хронической фазе хронического миелолейкоза) или 100 мг 2 раза в день (при далеко зашедшем хроническом миелолейкозе и остром лимбофластном лейкозе с положительной филадельфийской хромосомой).
Рекомендации по корректировке дозы препарата.
В случае снижения абсолютного числа нейтрофилов менее 0,5 x 109/л и/или числа тромбоцитов менее 50 x 109/л при хроническом миелолейкозе в хронической фазе следует сделать перерыв в лечении препаратом СПРАЙСЕЛ до достижения абсолютного числа нейтрофилов 1,0 x 109/л и числа тромбоцитов ≥ 50 x 109/л. Затем терапию возобновляют в прежней дозе. Если число тромбоцитов менее 25 x 109/л и/или абсолютное число нейтрофилов становится менее 0,5 x 109/л в течение более 7 дней — делают перерыв в лечении и, после достижения исходных показателей, терапию возобновляют в сниженной дозе 80 мг 1 раз в день (второй эпизод) или прекращают лечение (третий эпизод).
В случае снижения абсолютного числа нейтрофилов менее 0,5 x 109/л и/или числа тромбоцитов менее 10 x 109/л в фазе акселерации или бластного криза при хроническом миелолейкозе и остром лимфобластном лейкозе с положительной филадельфийской хромосомой следует сначала убедиться, что цитопения не обусловлена лейкозом (аспирация или биопсия костного мозга). Если цитопения не связана с лейкозом, лечение следует прервать до достижения абсолютного числа нейтрофилов ≥ 1,0 x 109/л и числа тромбоцитов ≥ 20 x 109/л и возобновить терапию в прежней дозе. В случае рецидива следует снова убедиться в природе цитопении и возобновить терапию в сниженной дозе 50 мг 2 раза в день (второй эпизод) или 40 мг 2 раза в день (третий эпизод). Если возникшая цитопения связана с лейкозом, следует рассмотреть вопрос об увеличении дозы до 100 мг 2 раза в день.
Клинически значимых различий в фармакокинетике у пожилых пациентов не выявлено. Изменение дозы препарата при назначении пожилым пациентам не требуется.
Побочное действие:
Побочные явления при применении СПРАЙСЕЛА представлены по частоте их регистрации: часто (≥1/100 – Со стороны системы пищеварения: часто – диарея, тошнота, рвота, запоры, боли в брюшной полости, воспаление слизистых оболочек (включая мукозит/стоматит), гастрит, колит, энтероколит, трещины в области анального отверстия, дисфагия, нарушения аппетита; нечасто – эзофагит, язвы верхних отделов желудочно-кишечного тракта, непроходимость кишечника, панкреатит, холецистит, гепатит, холестаз, повышение активности трансаминаз, уровня билирубина, асцит.
Со стороны кожи и подкожной клетчатки: часто – задержка жидкости (поверхностные отеки), алопеция, сухость кожи, угри, крапивница, дерматит (включая экзему), фотосенсибилизация, изменения ногтей, нарушения пигментации; нечасто – кожные язвы, острый фебрильный нейтрофильный дерматоз, буллезный дерматоз, синдром ладонно-подошвенной эритродизестезии.
Со стороны дыхательной системы: часто – легочные инфильтраты, пневмония, астма, отек легких, плевральный выпот, кашель, одышка; нечасто – бронхоспазм, острый респираторный дистресс-синдром, ретикулярная асфиксия.
Со стороны центральной нервной системы: часто – извращение вкуса, сонливость, обморок, тремор, судороги; нечасто – амнезия, нарушение мозгового кровообращения, преходящие ишемические нарушения, синдром обратимой задней лейкоэнцефалопатии.
Со стороны системы кроветворения: часто – тромбоцитопения, анемия, нейтропения; нечасто – снижение коагуляции, эритробластопения.
Со стороны костно-мышечной системы: часто – миозит, мышечная слабость, мышечная скованность; нечастые– тендинит, рабдомиолиз.
Со стороны сердечно-сосудистой системы: часто – сердцебиение, стенокардия, кардиомегалия, инфаркт миокарда, приливы жара, снижение или повышение артериального давления; нечасто – перикардит, желудочковая тахикардия, острый коронарный синдром, миокардит, удлинение интервала QTcF на ЭКГ.
Со стороны мочевыделительной системы: часто – учащенное мочеиспускание, почечная недостаточность; нечасто – протеинурия.
Со стороны репродуктивной системы: часто – гинекомастия; нечасто – нарушения менструального цикла, снижение либидо.
Со стороны органов зрения: часто — конъюнктивит, сухость глаз.
Со стороны органов слуха: часто — шум в ушах, вертиго.
Со стороны лабораторных показателей: часто – увеличение активности креатинфосфокиназы, увеличение уровня тропонина, гиперурикемия (синдром опухолевого лизиса); нечасто – гипоальбуминемия, нарушение агрегации тромбоцитов, гипокальциемия, гипофосфатемия.
Прочие: часто – слабость, герпетическая инфекция, сепсис (включая фатальный); энтероколит; нечасто – гиперчувствительность.
Передозировка:
Описан один случай приема 280 мг препарата СПРАЙСЕЛ пациентом с хроническим миелолейкозом, не сопровождавшийся клиническими симптомами и лабораторными отклонениями. В случае передозировки требуется наблюдение и при необходимости симптоматическая терапия.
Взаимодействие с другими лекарственными средствами
Ингибиторы CYP3A4: Ингибиторы активности CYP3A4 (например, кетоконазол, итраконазол, эритромицин, кларитромицин, атазанавир, индинавир, нефазодон, нельфинавир, ритонавир, саквинавир, телитромицин) могут повышать концентрацию дазатиниба в плазме крови, поэтому следует избегать их совместного применения с дазатинибом. В случае совместного применения дозу СПРАЙСЕЛ следует уменьшить на 20-40 мг/сут.
Индукторы CYP3A4: Индукторы CYP3A4 могут снижать концентрацию дазатиниба в плазме. Пациентам, которым назначены индукторы CYP3A4 (например, дексаметазон, фенитоин, карбамазепин, рифампицин, фенобарбитал), следует назначать препараты с меньшей способностью индуцировать этот фермент.
Трава зверобоя (Hypericum perforatum) может вызывать снижение концентрации дазатиниба в плазме крови, поэтому она не должна использоваться при лечении СПРАЙСЕЛОМ.
Антациды: Одновременное применение СПРАЙСЕЛА и антацидов нежелательно. Если антациды необходимы, рекомендуется их принимать не менее чем за 2 часа или через 2 часа после приема СПРАЙСЕЛА.
Блокаторы Н2-гистаминовых рецепторов и ингибиторы протонной помпы: длительное подавление серкреции соляной кислоты блокаторами Н2-гистаминовых рецепторов и ингибиторами протонной помпы (например, фамотидином и омепразолом) может уменьшать концентрацию дазатиниба. Одновременное применение этих препаратов и СПРАЙСЕЛА не рекомендуется.
Субстраты CYP3A4: Субстраты CYP3A4 с узким терапевтическим диапазоном, такие как алфентанил, астемизол, терфенадин, цизаприд, циклоспорин, фентанил, пимозид, хинидин, сиролимус, такролимус и производные спорыньи (эрготамин, дигидроэрготамин) следует использовать с осторожностью у пациентов, получающих СПРАЙСЕЛ.
Особые указания
Угнетение костного мозга
При лечении СПРАЙСЕЛОМ могут возникать тяжелые (3 и 4 степени по классификации NCI CTC) тромбоцитопения, анемия и нейтропения. Чаще они регистрируются у пациентов с далеко зашедшей фазой хронического миелолейкоза или острым лимфобластным лейкозом с положительной филадельфийской хромосомой, чем у пациентов с хронической фазой хронического миелолейкоза. Полный клинический анализ крови следует проводить еженедельно первые 2 месяца лечения, а затем ежемесячно или чаще, по клиническим показаниям. Угнетение костного мозга обычно обратимо и проходит при временной отмене или снижении дозы СПРАЙСЕЛА.
Кровотечения
Большинство случаев кровотечений были связаны с тяжелой тромбоцитопенией. Тяжелые кровоизлияния в головной мозг, включая фатальные, зарегистрированы у менее 1% пациентов, получавших СПРАЙСЕЛ. Тяжелые желудочно-кишечные кровотечения отмечены у 4% пациентов; они обычно требовали временной отмены препарата и гемотрансфузий. Другие тяжелые кровотечения зарегистрированы у 2% пациентов.
Задержка жидкости
При приеме СПРАЙСЕЛА может наблюдаться задержка жидкости. Задержка жидкости тяжелой степени была зарегистрирована у 7% пациентов, включая выраженный плевральный и перикардиальный выпот у 4% и 1% пациентов, соответственно. Выраженный асцит и генерализованный отек развились у менее 1% пациентов. У 1% пациентов зарегистрирован тяжелый отек легких. При появлении одышки или сухого кашля необходим рентгенологический контроль органов грудной клетки. Задержка жидкости обычно купируется при применении поддерживающей терапии с включением диуретиков или короткого курса глюкокортикостероидов. При выраженном плевральном выпоте требовались оксигенотерапия и торакоцентез.
Удлинение интервала QT
Дазатиниб следует использовать с осторожностью у пациентов с удлиненным интервалом QTc или с риском удлинения этого интервала (гипокалиемия, гипомагниемия, врожденный синдром удлиненного интервала QT, при терапии антиаритмическими и другими препаратами, способными удлинять интервал QT, предшествующая терапия высокими дозами антрациклинов). До назначения СПРАЙСЕЛА следует провести коррекцию гипокалиемии и гипомагниемии.
Отклонения в лабораторных показателях
Увеличение активности трансаминаз или уровня билирубина 3 или 4 степени и гипокальциемия и гипофосфатемия 3 или 4 степени наблюдались чаще у пациентов с фазой миелоидного или лимфоидного бластного криза хронического миелолейкоза и острым лимфобластным лейкозом с положительной филадельфийской хромосомой. Нормализация активности трансаминаз и/или уровня билирубина обычно наступала после снижения дозы препарата или перерыва в лечении. Купирование гипокальциемии 3 или 4 степени наблюдалось при назначении препаратов кальция для приема внутрь.
Форма выпуска:
Таблетки, покрытые пленочной оболочкой, по 20 мг, 50 мг и 70 мг.
По 60 таблеток во флаконах из полиэтилена высокого давления с крышкой, недоступной для открывания детьми. Внутрь флакона помещают контейнер с осушителем (силикагель) на который нанесена предупредительная надпись «не есть», горлышко флакона закрывают ватным тампоном. По 1 флакону вместе с инструкцией по применению в картонной пачке.
Условия хранения:
При температуре от 15 до 30 °С.
ХРАНИТЬ В НЕДОСТУПНОМ ДЛЯ ДЕТЕЙ МЕСТЕ!
Срок годности:
2 года.
Не использовать препарат по истечении срока годности, указанного на упаковке.
Условия отпуска из аптек:
По рецепту.
Производитель:
Бристол-Майерс Сквибб Компани, США Маунт Вернон, штат Индиана, 47620, США
Bristol-Myers Squibb Company, USA
Mount Vernon, IN 47620, USA
Товары из категории — Препараты для лечения онкологических заболеваний
Инструкция по применению
Цена в интернет-аптеке WER.RU: от 72 450
Немного фактов
Спрайсел противоопухолевое лекарство, которое используется в онкологической практике. Содержит в себе дазатиниб ингибитор протеинтирозинкиназ, подавляющий биосинтез PDGFRβ, c-KIT, BCR-ABL, EPHA2 и других ферментов группы киназ. Согласно классификации МКБ-10, предназначен для лечения заболеваний класса C00-D48 /C97 / C81-C96 / C92. Используется в терапии лимфобластомного лейкоза и миелолейкоза в фазе акселерации или хронитизации патологических процессов.
Описание
Спрайсел противоопухолевый медпрепарат, который был выпущен в 2008 году американской фирмой Bristol-Myers Squibb, штаб-квартира которой находится в Нью-Йорке. Производитель разработал высокоэффективное антибластомное средство, которое обладает комбинированным действием: угнетает активность нерецепторных протеинкиназ Src-семейства и ферментов подкласса тирозинкиназ типа BCR-ABL.
В лекарстве содержится дазатиниб антибластомное вещество, которое обладает высокой активностью в отношении лейкозных линий, устойчивых к действию иматинибу. Согласно результатам лабораторных исследований, противоопухолевый медпрепарат более чем в 300 раз активнее иматиниба. Это имеет определяющее значение при подборе противоопухолевых средств для лечения лимфобластомного лейкоза и вялотекущего миелолейкоза.
Лекарственная форма и биохимический состав
Антибластомный препарат выпускается в таблетированной форме. В нем может содержаться 20 мг, 50 мг, 70 мг, 100 мг или 140 мг действующего вещества. Белые двояковыпуклые таблетки включают в свой состав такие компоненты.
- дазатиниб;
- МКЦ;
- стеарат магния;
- натрия кроскармеллоза;
- белый опадай;
- молочный сахар;
- пищевая добавка Е171;
- гипромеллоза.
Таблетки фасуются в белые непрозрачные пузырьки из пластика с закручивающейся крышкой. В картонной коробке содержится 30 или 60 таблеток вместе с детальной инструкцией по применению противоопухолевого средства.
Фармакотерапевтические свойства
В небольших концентрациях Спрайсел замедляет биосинтез тирозин-специфичных протеинкиназ PDGFRB, BCR ABL, FYN, EPHA2 , SRC и т.д. В процессе многоразового лабораторного моделирования было установлено, что действующие компоненты лекарства связываются с большинством ABL-киназ.
Дазатиниб обладает высокой антибластомной активностью в отношении лейкозных клеточных структур. В тестовых условиях противоопухолевый препарат легко преодолевает устойчивость к иматинибу, которая обусловлена мутациями гибридных белков типа BCR-ABL-киназ.
При применении лекарства активируются сигнальные линии, которые включают в себя киназы семейства SRC. Это сопровождается гиперэкспрессией гена медикаментозной полирезистентности.
Фармакокинетические свойства
Действующие компоненты препарата быстро проникают в ткани и внесосудистые пространства. Предельная концентрация достигается через 1-3 часа после употребления таблеток. Период полураспада дазатиниба колеблется в диапазоне от 3 до 5 часов. Приемы пищи не оказывают значимого воздействия на скорость всасывания активных и неактивных компонентов препарата из кишечника.
Связывание дазатиниба с белковыми компонентами крови составляет в среднем 95%. Синтетические вещества метаболизируются при помощи фермента 3A4. В образовании лекарственных метаболитов принимает участие монооксигеназа 3. Продукты распада выводятся из организма вместе с каловыми массами. Концентрация неизмененного дазатиниба не превышает 15-17%.
Условия назначения
Таблетки Спрайсел применяются в онкологической практике во время терапии пациентов с заболеваниями крови. Показаниями к назначению антибластомного средства являются.
- впервые диагностированный миелоидный лейкоз в хронической стадии;
- обострение лимфобластомной лейкемии с позитивной аномальной филадельфийской хромосомой;
- миелоидный лейкоз в период лимфоидного или миелоидного криза.
Курс терапии определяется скоростью прогрессирования онкозаболевания и сопутствующих осложнений. В случае необходимости Спрайсел применяют для проведения паллиативного лечения.
Особенности применения
Антибластомный медпрепарат принимается перорально. Нужно глотать таблетки целиком, запивая 150-200 мл питьевой воды. При вялотекущем течении миелолейкоза назначают по 100 мг лекарства в сутки. Во всех остальных случаях желательно употреблять по 70 мг препарата при приеме пищи или натощак.
При слабом цитогенетическом ответе схему лечения корректируют, а дозу Спрайсела увеличивают до 100 мг не более 2 раз в сутки. Изменение стратегии лечения требуется только при диагностировании лимфобластомной лейкемии с позитивной филадельфиской хромосомой или запущенной формы вялотекущего миелолейкоза.
Особенности корректировки дозы
При критическом уменьшении концентрации нейтрофилов в крови (не более 0.5×109 на 1 л) в лечении миелолейкоза в хронической стадии необходимо сделать небольшой перерыв. Прием Спрайсела начинают в том случае, когда уровень нейтрофилов достигает 1.0-1.1×109 на 1 л.
Если количество тромбоцитов в 1 л крови не достигает 25×109, лечение прекращают до тех пор, пока оно не увеличится вдвое. При восстановлении терапии необходимо уменьшить дозировку до 80 мг 1 раз в сутки. Принципиально значимых отличий в фармакокинетике лекарства у пожилых людей нет, поэтому коррекция дозы для людей старше 50-55 лет не требуется.
Передозировка
Спрайсел крайне редко приводит к сильному ухудшению самочувствия в случае однократного употребления высокой дозы дазатиниба. В медицинской практике зарегистрирован 1 случай передозировки, при котором больной с миелолейкозом принял 280 мг медпрепарата. Симптомов интоксикации и связанных с ними осложнений не обнаружилось.
Побочные реакции
В 87% случаев Спрайсел вызывает проходящие побочные эффекты, которые не являются весомой причиной для отмены медпрепарата. Согласно статистическим данным, терапия была прекращена только для 8% пациентов с хроническим миелолейкозом.
В первые несколько недель после начала курса терапии могут возникнуть нарушения в работе следующих органов и систем.
- со стороны костного мозга и других органов кроветворения анемия, агранулоцитоз, эритробластопения;
- со стороны нервной системы нарушение кровообращения в мозговой ткани, амнезия, частые обмороки, изменение вкуса, лейкоэнцефалопатия, сонливость;
- со стороны органов дыхания плевральный выпот, воспаление легких, бронхоспазмы, ретикулярная асфиксия, легочные инфильтрации;
- со стороны сердца и сосудистой системы перикардит, приливы жара, гипоксия миокарда, коронарный синдром, учащенное сердцебиение;
- со стороны ЖКТ боли в эпигастрии, гастрит, запоры, изжога, тошнота, рвотные позывы, энтероколит, язвы на слизистой ЖКТ, холецистит, брюшная водянка, гепатит, дисфагия;
- со стороны мочеполовой системы гинекомастия, протеинурия, болезненное и частое мочеиспускание, снижение сексуального влечения;
- со стороны клинических показателей увеличение концентрации тропонина, гипофосфатемия, нарушение свертываемости крови;
- со стороны эпидермиса крапивница, мокнущая экзема, нейтрофильный дерматоз, сухость кожи, угревая сыпь, буллезный дерматит, нарушение пигментации.
Реже всего пациенты жалуются на обострение герпетической инфекции, шум в ушах, развитие аллергического конъюнктивита и вертиго.
Противопоказания
Противоопухолевый препарат Спрайсел не назначается при высокой чувствительности к действующим и неактивным компонентам. Противопоказано употреблять таблетки детям, не достигшим 18-летнего возраста, а также женщинам во время вынашивания плода.
С осторожностью нужно принимать антибластомное средство при печеночной недостаточности и параллельном приеме медикаментов, влияющих на функции тромбоцитов. В связи с тем, что в таблетках содержится молочный сахар, их не назначают при непереносимости лактозы.
Беременность и грудное вскармливание
Контролируемые исследования у пациенток во время гестации и грудного вскармливания не проводились. В связи с этим Спрайсел не назначается женщинам во время вынашивания плода и грудного вскармливания.
Совместимость с алкоголем
Инструкция обязывает отказаться от приема спиртосодержащих напитков при прохождении противоопухолевой терапии. Этанол потенцирует седативное действие препарата и побочные реакции.
Особые указания
Курсовая терапия Спрайселом может сопровождаться развитием нейтропении и других заболеваний крови. Чаще всего они диагностируются у больных с запущенной формой миелолейкоза. Чтобы предотвратить ухудшение состояния здоровья, нужно 2 раза месяц совершать клинический анализ крови. Угнетение функций костного мозга обратимо и хорошо подается терапии на начальных стадиях развития.
Во время использования антибластомного средства часто происходит задержка межклеточной жидкости в мягких тканях. В особенности это касается пациентов пожилого возраста. Перикардиальные выпоты и асцит были зарегистрированы у 5-6% больных, прошедших противоопухолевую терапию. В случае возникновения тяжелого кашля и одышки следует пройти аппаратное обследование у врача.
Взаимодействие с медикаментами
Следует избегать параллельного использования Спрайсела с ингибиторами CYP3A4: Нефазодон, Итраконазол, Кетоконазол, Телитромицин и т.д. Это приводит к повышению концентрации активных компонентов в крови. Во время лечения желательно отказаться и от употребления индукторов CYP3A4 (Фенофарбитал, Дексаметазон), т.к. они снижают уровень дазатиниба в крови, что приводит к ослаблению терапевтического эффекта.
Блокаторы H2-гистаминовых рецепторов препятствуют выработке хлороводородной кислоты, в связи с чем уменьшается всасывание действующих веществ из кишечника. По этой причине одновременное использование антибластомного средства с медикаментами, предназначенными для лечения кислотозависимых патологий ЖКТ, нежелательно.
Аналоги
Заменителями Спрайсела считаются лекарственные средства, которые обладают выраженными антибластомными свойствами.
- Алвотиниб;
- Винат;
- Иматеро;
- Неопакс;
- Эгитинид;
- Бозулиф.
Условия продажи и хранения
Противоопухолевое средство отпускается по письменному назначению от врача. Предельный срок годности таблеток с момента выпуска составляет 24 месяца. Хранить их следует в проветриваемом и недоступном для маленьких детей месте при температуре до 30 градусов Цельсия.
Цены на Спрайсел в Москве
Заберите заказ в в аптеке
WER (г. Москва)
Цена: от 72 450 руб.
Сертификаты и лицензии
Каждая таблетка, покрытая оболочкой, содержит
активное вещество: дазатиниб 20 мг, 50 мг или 70 мг.
вспомогательные вещества: лактозы моногидрат, целлюлоза микрокристаллическая, гипролоза, кроскармеллоза натрия, магния стеарат, опадрай белый (титана диоксид, гипромеллоза-6сР, макрогол-400).
Таблетки 20 мг: круглые двояковыпуклые таблетки, покрытые пленочной оболочкой белого или почти белого цвета, с маркировкой «BMS» на одной стороне и «527» на другой.
Таблетки 50 мг: овальные двояковыпуклые таблетки, покрытые пленочной оболочкой белого или почти белого цвета, с маркировкой «BMS» на одной стороне и «528» на другой.
Таблетки 70 мг: круглые двояковыпуклые таблетки, покрытые пленочной оболочкой белого или почти белого цвета, с маркировкой «BMS» на одной стороне и «524» на другой.
противоопухолевое средство, протеинтирозинкиназы ингибитор
Код АТХ
L01XE06
Фармакодинамика
Дазатиниб в наномолярных концентрациях ингибирует следующие тирозинкиназы: BCR ABL, семейство SRC (SRC, LCK, YES, FYN), c-KIT, EPHA2 и PDGFR?. С помощью моделирования установлено, что дазатиниб связывается со многими формами ABL киназы.
In vitro дазатиниб проявлял активность в лейкозных клеточных линиях, как чувствительных, так и резистентных к иматинибу. Дазатиниб ингибирует рост клеточных линий хронического миелолейкоза и острого лимфобластного лейкоза с гиперэкспрессией BCR-ABL. В условиях тестов дазатиниб преодолевал резистентность к иматинибу, связанную с мутациями домена BCR-ABL киназы, активацией альтернативных сигнальных путей, включающих киназы семейства SRC (LYN, HCK) и гиперэкспрессией гена лекарственной полирезистентности.
Фармакокинетика
Всасывание
Максимальная концентрация (Cmax) дазатиниба наблюдалась через 0.5–6 часов (Tmax) после приема внутрь. Площадь под кривой “концентрация-время” (AUC) и элиминация пропорциональны дозе в диапазоне доз от 15 до 240 мг/сут. Период полувыведения дазатиниба составляет 3-5 часов.
При приеме 100 мг дазатиниба через 30 минут после приема пищи с высоким содержанием жира отмечается увеличение средней AUC на 14%. Влияние пищи не было клинически значимым.
Распределение
Кажущийся объем распределения дазатиниба составляет 2505 л, что свидетельствует о значительном распределении во внесосудистом пространстве. Дазатиниб и его активный метаболит связывались in vitro с белками плазмы человека на 96% и 93%, соответственно, независимо от концентрации в диапазоне 100-500 нг/мл.
Метаболизм
Дазатиниб активно метаболизируется у людей, главным образом с помощью фермента 3A4 цитохрома P450. CYP3A4 является главным ферментом, участвующим в образовании активного метаболита. Флавин-содержащая монооксигеназа 3 и уридиндифосфат-глюкуронозилтрансфераза также участвуют в образовании метаболитов дазатиниба. В микросомах печени человека дазатиниб проявлял слабое независимое от времени ингибирующее действие в отношении CYP3A4. AUС активного метаболита дазатиниба составляет примерно 5% AUC дазатиниба. Вероятно, активный метаболит не играет большой роли в фармакологическом действии дазатиниба. Описаны и другие неактивные окисленные метаболиты дазатиниба.
Выведение
Препарат выделяется главным образом с калом. После однократного приема внутрь [14C]-дазатиниба примерно 4% и 85% радиоактивности выводится с мочой и калом, соответственно, за 10 дней. Неизмененный дазатиниб составляет 0,1% и 19% дозы, выводимой с мочой и калом, соответственно, а остальная часть дозы представлена метаболитами.
- Хронический миелолейкоз в хронической фазе или фазе акселерации, лимфоидный или миелоидный бластный криз при резистентности или непереносимости предыдущей терапии, включая иматиниб
- Острый лимфобластный лейкоз с положительной филадельфийской хромосомой при резистентности или непереносимости предыдущей терапии.
Повышенная чувствительность к дазатинибу или другим компонентам препарата.
Беременность и период кормления грудью.
Возраст до 18 лет (эффективность и безопасность не установлены).
С осторожностью
при печеночной недостаточности.
Способ применения и дозировка
Таблетки следует проглатывать целиком.
Рекомендуемая начальная доза СПРАЙСЕЛА при хронической фазе хронического миелолейкоза составляет 100 мг один раз в день утром или вечером независимо от приема пищи.
В остальных случаях рекомендуется принимать СПРАЙСЕЛ внутрь в дозе 70 мг два раза в день утром и вечером во время еды или натощак (140 мг в сутки).
В случае отсутствия гематологического или цитогенетического ответа возможно увеличение дозы СПРАЙСЕЛА до 140 мг 1 раз в день (при хронической фазе хронического миелолейкоза) или 100 мг 2 раза в день (при далеко зашедшем хроническом миелолейкозе и остром лимбофластном лейкозе с положительной филадельфийской хромосомой).
Рекомендации по корректировке дозы препарата.
В случае снижения абсолютного числа нейтрофилов менее 0,5 x 109/л и/или числа тромбоцитов менее 50 x 109/л при хроническом миелолейкозе в хронической фазе следует сделать перерыв в лечении препаратом СПРАЙСЕЛ до достижения абсолютного числа нейтрофилов 1,0 x 109/л и числа тромбоцитов ? 50 x 109/л. Затем терапию возобновляют в прежней дозе. Если число тромбоцитов менее 25 x 109/л и/или абсолютное число нейтрофилов становится менее 0,5 x 109/л в течение более 7 дней — делают перерыв в лечении и, после достижения исходных показателей, терапию возобновляют в сниженной дозе 80 мг 1 раз в день (второй эпизод) или прекращают лечение (третий эпизод).
В случае снижения абсолютного числа нейтрофилов менее 0,5 x 109/л и/или числа тромбоцитов менее 10 x 109/л в фазе акселерации или бластного криза при хроническом миелолейкозе и остром лимфобластном лейкозе с положительной филадельфийской хромосомой следует сначала убедиться, что цитопения не обусловлена лейкозом (аспирация или биопсия костного мозга). Если цитопения не связана с лейкозом, лечение следует прервать до достижения абсолютного числа нейтрофилов ? 1,0 x 109/л и числа тромбоцитов ? 20 x 109/л и возобновить терапию в прежней дозе. В случае рецидива следует снова убедиться в природе цитопении и возобновить терапию в сниженной дозе 50 мг 2 раза в день (второй эпизод) или 40 мг 2 раза в день (третий эпизод). Если возникшая цитопения связана с лейкозом, следует рассмотреть вопрос об увеличении дозы до 100 мг 2 раза в день.
Клинически значимых различий в фармакокинетике у пожилых пациентов не выявлено. Изменение дозы препарата при назначении пожилым пациентам не требуется.
Побочные явления при применении СПРАЙСЕЛА представлены по частоте их регистрации: часто (?1/100 –
Со стороны системы пищеварения
часто – диарея, тошнота, рвота, запоры, боли в брюшной полости, воспаление слизистых оболочек (включая мукозит/стоматит), гастрит, колит, энтероколит, трещины в области анального отверстия, дисфагия, нарушения аппетита; нечасто – эзофагит, язвы верхних отделов желудочно-кишечного тракта, непроходимость кишечника, панкреатит, холецистит, гепатит, холестаз, повышение активности трансаминаз, уровня билирубина, асцит.
Со стороны кожи и подкожной клетчатки
часто – задержка жидкости (поверхностные отеки), алопеция, сухость кожи, угри, крапивница, дерматит (включая экзему), фотосенсибилизация, изменения ногтей, нарушения пигментации; нечасто – кожные язвы, острый фебрильный нейтрофильный дерматоз, буллезный дерматоз, синдром ладонно-подошвенной эритродизестезии.
Со стороны дыхательной системы
часто – легочные инфильтраты, пневмония, астма, отек легких, плевральный выпот, кашель, одышка; нечасто – бронхоспазм, острый респираторный дистресс-синдром, ретикулярная асфиксия.
Со стороны центральной нервной системы
часто – извращение вкуса, сонливость, обморок, тремор, судороги; нечасто – амнезия, нарушение мозгового кровообращения, преходящие ишемические нарушения, синдром обратимой задней лейкоэнцефалопатии.
Со стороны системы кроветворения
часто – тромбоцитопения, анемия, нейтропения; нечасто – снижение коагуляции, эритробластопения.
Со стороны костно-мышечной системы
часто – миозит, мышечная слабость, мышечная скованность; нечастые– тендинит, рабдомиолиз.
Со стороны сердечно-сосудистой системы
часто – сердцебиение, стенокардия, кардиомегалия, инфаркт миокарда, приливы жара, снижение или повышение артериального давления; нечасто – перикардит, желудочковая тахикардия, острый коронарный синдром, миокардит, удлинение интервала QTcF на ЭКГ.
Со стороны мочевыделительной системы
часто – учащенное мочеиспускание, почечная недостаточность; нечасто – протеинурия.
Со стороны репродуктивной системы
часто – гинекомастия; нечасто – нарушения менструального цикла, снижение либидо.
Со стороны органов зрения
часто — конъюнктивит, сухость глаз.
Со стороны органов слуха
часто — шум в ушах, вертиго.
Со стороны лабораторных показателей
часто – увеличение активности креатинфосфокиназы, увеличение уровня тропонина, гиперурикемия (синдром опухолевого лизиса); нечасто – гипоальбуминемия, нарушение агрегации тромбоцитов, гипокальциемия, гипофосфатемия.
Прочие
часто – слабость, герпетическая инфекция, сепсис (включая фатальный); энтероколит; нечасто – гиперчувствительность.
Описан один случай приема 280 мг препарата СПРАЙСЕЛ пациентом с хроническим миелолейкозом, не сопровождавшийся клиническими симптомами и лабораторными отклонениями. В случае передозировки требуется наблюдение и при необходимости симптоматическая терапия.
Взаимодействие с другими лекарственными средствами
Ингибиторы CYP3A4: Ингибиторы активности CYP3A4 (например, кетоконазол, итраконазол, эритромицин, кларитромицин, атазанавир, индинавир, нефазодон, нельфинавир, ритонавир, саквинавир, телитромицин) могут повышать концентрацию дазатиниба в плазме крови, поэтому следует избегать их совместного применения с дазатинибом. В случае совместного применения дозу СПРАЙСЕЛ следует уменьшить на 20-40 мг/сут.
Индукторы CYP3A4: Индукторы CYP3A4 могут снижать концентрацию дазатиниба в плазме. Пациентам, которым назначены индукторы CYP3A4 (например, дексаметазон, фенитоин, карбамазепин, рифампицин, фенобарбитал), следует назначать препараты с меньшей способностью индуцировать этот фермент.
Трава зверобоя (Hypericum perforatum) может вызывать снижение концентрации дазатиниба в плазме крови, поэтому она не должна использоваться при лечении СПРАЙСЕЛОМ.
Антациды: Одновременное применение СПРАЙСЕЛА и антацидов нежелательно. Если антациды необходимы, рекомендуется их принимать не менее чем за 2 часа или через 2 часа после приема СПРАЙСЕЛА.
Блокаторы Н2-гистаминовых рецепторов и ингибиторы протонной помпы: длительное подавление серкреции соляной кислоты блокаторами Н2-гистаминовых рецепторов и ингибиторами протонной помпы (например, фамотидином и омепразолом) может уменьшать концентрацию дазатиниба. Одновременное применение этих препаратов и СПРАЙСЕЛА не рекомендуется.
Субстраты CYP3A4: Субстраты CYP3A4 с узким терапевтическим диапазоном, такие как алфентанил, астемизол, терфенадин, цизаприд, циклоспорин, фентанил, пимозид, хинидин, сиролимус, такролимус и производные спорыньи (эрготамин, дигидроэрготамин) следует использовать с осторожностью у пациентов, получающих СПРАЙСЕЛ.
Угнетение костного мозга
При лечении СПРАЙСЕЛОМ могут возникать тяжелые (3 и 4 степени по классификации NCI CTC) тромбоцитопения, анемия и нейтропения. Чаще они регистрируются у пациентов с далеко зашедшей фазой хронического миелолейкоза или острым лимфобластным лейкозом с положительной филадельфийской хромосомой, чем у пациентов с хронической фазой хронического миелолейкоза. Полный клинический анализ крови следует проводить еженедельно первые 2 месяца лечения, а затем ежемесячно или чаще, по клиническим показаниям. Угнетение костного мозга обычно обратимо и проходит при временной отмене или снижении дозы СПРАЙСЕЛА.
Кровотечения
Большинство случаев кровотечений были связаны с тяжелой тромбоцитопенией. Тяжелые кровоизлияния в головной мозг, включая фатальные, зарегистрированы у менее 1% пациентов, получавших СПРАЙСЕЛ. Тяжелые желудочно-кишечные кровотечения отмечены у 4% пациентов; они обычно требовали временной отмены препарата и гемотрансфузий. Другие тяжелые кровотечения зарегистрированы у 2% пациентов.
Задержка жидкости
При приеме СПРАЙСЕЛА может наблюдаться задержка жидкости. Задержка жидкости тяжелой степени была зарегистрирована у 7% пациентов, включая выраженный плевральный и перикардиальный выпот у 4% и 1% пациентов, соответственно. Выраженный асцит и генерализованный отек развились у менее 1% пациентов. У 1% пациентов зарегистрирован тяжелый отек легких. При появлении одышки или сухого кашля необходим рентгенологический контроль органов грудной клетки. Задержка жидкости обычно купируется при применении поддерживающей терапии с включением диуретиков или короткого курса глюкокортикостероидов. При выраженном плевральном выпоте требовались оксигенотерапия и торакоцентез.
Удлинение интервала QT
Дазатиниб следует использовать с осторожностью у пациентов с удлиненным интервалом QTc или с риском удлинения этого интервала (гипокалиемия, гипомагниемия, врожденный синдром удлиненного интервала QT, при терапии антиаритмическими и другими препаратами, способными удлинять интервал QT, предшествующая терапия высокими дозами антрациклинов). До назначения СПРАЙСЕЛА следует провести коррекцию гипокалиемии и гипомагниемии.
Отклонения в лабораторных показателях
Увеличение активности трансаминаз или уровня билирубина 3 или 4 степени и гипокальциемия и гипофосфатемия 3 или 4 степени наблюдались чаще у пациентов с фазой миелоидного или лимфоидного бластного криза хронического миелолейкоза и острым лимфобластным лейкозом с положительной филадельфийской хромосомой. Нормализация активности трансаминаз и/или уровня билирубина обычно наступала после снижения дозы препарата или перерыва в лечении. Купирование гипокальциемии 3 или 4 степени наблюдалось при назначении препаратов кальция для приема внутрь.
Таблетки, покрытые пленочной оболочкой, по 20 мг, 50 мг и 70 мг.
По 60 таблеток во флаконах из полиэтилена высокого давления с крышкой, недоступной для открывания детьми. Внутрь флакона помещают контейнер с осушителем (силикагель) на который нанесена предупредительная надпись «не есть», горлышко флакона закрывают ватным тампоном. По 1 флакону вместе с инструкцией по применению в картонной пачке.
При температуре от 15 до 30 °С.
ХРАНИТЬ В НЕДОСТУПНОМ ДЛЯ ДЕТЕЙ МЕСТЕ!
2 года.
Не использовать препарат по истечении срока годности, указанного на упаковке.
Условия отпуска из аптек
По рецепту.
Производитель
Бристол-Майерс Сквибб Компани, США Маунт Вернон, штат Индиана, 47620, США
Bristol-Myers Squibb Company, USA
Mount Vernon, IN 47620, USA