Спутник Лайт — инструкция по применению
Синонимы, аналоги
Статьи
Векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-СoV-2
▼ Данный лекарственный препарат зарегистрирован по процедуре регистрации препаратов, предназначенных для применения в условиях угрозы возникновения, возникновения и ликвидации чрезвычайных ситуаций. Инструкция подготовлена на основании ограниченного объема клинических данных по применению препарата и будет дополняться по мере поступления новых данных. Применение препарата возможно только в условиях медицинских организаций, имеющих право осуществлять вакцинопрофилактику населения в установленном порядке.
Регистрационный номер:
ЛП-006993
Торговое наименование:
Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
Международное непатентованное или группировочное наименование:
Вакцина для профилактики COVID-19
Лекарственная форма:
раствор для внутримышечного введения
Состав на 1 дозу (0,5 мл):
Действующее вещество: рекомбинантные аденовирусные частицы 26 серотипа, содержащие ген белка S вируса SARS-CoV-2, в количестве (1,0±0,5)×1011 частиц/доза.
Вспомогательные вещества: трис(гидроксиметил)аминометан – 1,21 мг, натрия хлорид – 2,19 мг, сахароза – 25,0 мг, полисорбат 80 – 250 мкг, магния хлорида гексагидрат – 102,0 мкг, ЭДТА динатриевая соль дигидрат – 19,0 мкг, этанол 95 % – 2,5 мкл, вода для инъекций – до 0,5 мл.
Описание
Замороженный препарат.
Раствор замороженный – плотная затвердевшая беловатого цвета масса. После размораживания – однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Жидкий препарат.
Однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Характеристика
Вакцина получена биотехнологическим путем, при котором не используется патогенный для человека вирус SARS-CoV-2. В состав препарата входит рекомбинантный аденовирусный вектор на основе аденовируса человека 26 серотипа, несущий ген белка S вируса SARS-CoV-2.
Фармакотерапевтическая группа:
МИБП-вакцина
Код АТХ:
J07B
Фармакологические свойства
Вакцина индуцирует формирование гуморального и клеточного иммунитета в отношении коронавирусной инфекции, вызываемой вирусом SARS-CoV-2.
Иммунологическая эффективность
Иммунологические свойства и безопасность вакцины изучали в различных клинических исследованиях у взрослых добровольцев обоего пола в возрасте старше 18 лет. Промежуточный анализ иммуногенности показал, что вакцина формирует гуморальный иммунный ответ у добровольцев. На 28 день сероконверсия обнаружена у 96,88% здоровых добровольцев.
У лиц с предсуществующим иммунитетом к коронавирусу отмечен выраженный рост титра антител на 10 день после вакцинации, что может указывать на возможность применения препарата для вакцинации ранее переболевших COVID-19 после снижения титра антител с целью предотвращения повторных случаев заболевания.
В результате однократной иммунизации 100% здоровых добровольцев (все 30 человек у которых изучены показатели клеточного иммунитета) сформировали клеточный иммунный ответ против S белка SARS-Cov2.
Защитный титр антител в настоящее время неизвестен. Продолжительность защиты неизвестна.
Показания к применению
Профилактика новой коронавирусной инфекции (COVID-19) у взрослых от 18 до 60 лет.
Противопоказания
- гиперчувствительность к какому-либо компоненту вакцины или вакцине, содержащей аналогичные компоненты;
- тяжелые аллергические реакции в анамнезе;
- острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний – вакцинацию проводят через 2-4 недели после выздоровления или ремиссии. При нетяжелых ОРВИ, острых инфекционных заболеваниях ЖКТ-вакцинацию проводят после нормализации температуры;
- беременность и период грудного вскармливания;
- возраст до 18 лет (в связи с отсутствием данных об эффективности и безопасности).
С осторожностью
Применять вакцину с осторожностью при хронических заболеваниях печени и почек, эндокринных заболеваниях (выраженных нарушениях функции щитовидной железы и сахарном диабете в стадии декомпенсации), тяжелых заболеваниях системы кроветворения, эпилепсии и других заболеваниях ЦНС, остром коронарном синдроме и остром нарушении мозгового кровообращения, миокардитах, эндокардитах, перикардитах.
Вследствие недостатка информации вакцинация может представлять риск для следующих групп пациентов:
- с аутоиммунными заболеваниями (стимуляция иммунной системы может привести к обострению заболевания, особенно следует с осторожностью относиться к пациентам с аутоиммунной патологией, имеющей тенденцию к развитию тяжёлых и жизнеугрожающих состояний);
- со злокачественными новообразованиями.
Принятие решения о вакцинации должно основываться на оценке соотношения пользы и риска в каждой конкретной ситуации.
Применение при беременности и в период грудного вскармливания
Препарат противопоказан при беременности и в период грудного вскармливания, так как его эффективность и безопасность в этот период не изучались.
Способ применения и дозы
Вакцина предназначена только для внутримышечного введения. Строго запрещено внутривенное введение препарата. Вакцину вводят в дельтовидную мышцу (верхнюю треть наружной поверхности плеча). При невозможности введения в дельтовидную мышцу – препарат вводят в латеральную широкую мышцу бедра.
После введения вакцины пациент должен находиться под наблюдением медицинских работников в течение 30 минут.
Замороженный препарат
Перед вакцинированием флакон, ампулу или шприц с препаратом достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон, ампулу или шприц снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона, ампулы или шприца!
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой. Вскрывают ампулу по кольцу и/или точке излома. Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту из ампулы или флакона.
Внимание! Доза, вводимая пациенту, не должна превышать 0,5 мл!
Препарат в шприцах готов к применению без дополнительных манипуляций.
Применение вакцины производства ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России) (флаконы) и АО «Биннофарм» (ампулы, шприцы):
Не допускается хранение размороженного препарата более 30 минут!
Повторное замораживание не допускается!
Применение вакцины производства АО «ГЕНЕРИУМ» (флаконы), ОАО «Фармстандарт-УфаВИТА» (флаконы, ампулы), ЗАО «ЛЕККО» (флаконы):
Внимание! Повторное замораживание флакона или ампулы с раствором не допускается!
Суммарное время хранения размороженного раствора при комнатной температуре не должно превышать 2 часов. Неиспользованная вакцина подлежит уничтожению.
Многодозовые флаконы
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого или невскрытого флакона не более 2 часов при комнатной температуре.
Многодозовые ампулы
Содержимое ампулы рекомендуется использовать незамедлительно. Если последующие инъекции по какой-либо причине откладываются, допускается хранение вакцины при комнатной температуре: вскрытой ампулы, закрытой стерильной салфеткой, не более 1 часа, невскрытой ампулы – не более 2 часов.
ВНИМАНИЕ! Одна ампула содержит две дозы вакцины. Объем одной дозы составляет 0,5 мл. Одному пациенту вводить 1 дозу (0,5 мл).
Однодозовые ампулы
Содержимое ампулы рекомендуется использовать незамедлительно. Если последующие инъекции по какой-либо причине откладываются, допускается хранение невскрытой ампулы при комнатной температуре не более 2 часов.
Применение вакцины производства ЗАО «БИОКАД» (флаконы), АО «Р-Фарм» (флаконы):
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого флакона по 3 мл не более 2 часов при комнатной температуре.
Не допускается хранение размороженного препарата во флаконах по 0,5 мл более 30 минут!
Повторное замораживание не допускается!
Жидкий препарат
Применение вакцины производства ООО «БиоИнтегратор» (флаконы):
Внимание! Замораживание флакона с раствором не допускается!
Флакон достают из холодильника и выдерживают при комнатной температуре, допускается слегка нагреть препарат, например, подержав его в руках. Не следует нагревать препарат выше 37 °С.
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой.
Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту.
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого флакона или ампулы не более 2 часов при комнатной температуре.
Внимание! К использованию непригоден препарат (жидкий и/или замороженный) с дефектами укупорочной системы и/или нарушенной маркировкой флакона или ампулы,, при изменении физических свойств раствора (мутность, окрашивание), неправильном хранении и/или с истекшим сроком годности.
▼ Информация для медицинских работников, выполняющих вакцинацию лекарственным препаратом: данный лекарственный препарат зарегистрирован по особой процедуре регистрации, в связи с чем необходимо уведомлять Федеральную службу по надзору в сфере здравоохранения о каждом факте применения лекарственного препарата путем внесения информации в соответствующий раздел информационной системы ЕГИСЗ.
Побочное действие
Нежелательные явления, характерные для применения вакцины, выявленные в рамках клинических исследований, а также исследований других вакцин на основе аналогичной технологической платформы, бывают преимущественно легкой или средней степени выраженности, могут развиваться в первые-вторые сутки после вакцинации и разрешаются в течение 3-х последующих дней. Часто и очень часто могут развиться кратковременные общие (непродолжительный гриппоподобный синдром, характеризующийся ознобом, повышением температуры тела, артралгией, миалгией, астенией, общим недомоганием, головной болью) и местные (болезненность в месте инъекции, гиперемия, отечность) реакции. Рекомендуется назначение нестероидных противовоспалительных средств (НПВС) при повышении температуры после вакцинации и антигистаминных средств при выраженной местной реакции.
Нежелательные явления, представленные ниже, перечислены по системам организма и в соответствии с частотой встречаемости. Частота встречаемости определяется следующим образом: очень часто (≥1/10), часто (≥1/100 и < /10), нечасто (≥1/1000 и <1/100), редко (≥1/10000 и <1/1000), очень редко (<1/10000, включая отдельные случаи). Категории частоты были сформированы на основании клинических исследований препарата.
Часто отмечаются: тошнота, диспепсия, снижение аппетита, очень редко – увеличение регионарных лимфоузлов. У некоторых пациентов возможно развитие аллергических реакций, кратковременное повышение уровня печеночных трансаминаз, креатинина и креатинфосфокиназы в сыворотке крови.
В рамках проведенных клинических исследований безопасности, переносимости и иммуногенности препарата «Спутник-Лайт» после вакцинации были зарегистрированы следующие НЯ:
«Общие нарушения и реакции в месте введения»: гипертермия, боль, отек, зуд в месте вакцинации, астения, боль, недомогание, пирексия, повышение температуры кожи в месте вакцинации, снижение аппетита. Частота развития – очень часто и часто.
«Нарушения со стороны дыхательной системы, органов грудной клетки и средостения»: боль в ротоглотке, заложенность носа, першение в горле, ринорея. Частота развития – часто.
«Нарушения со стороны нервной системы»: головная боль, астения – часто; головокружения, обмороки – редко.
«Желудочно-кишечные нарушения»: тошнота, рвота, диспепсия – часто.
«Лабораторные и инструментальные данные»: разнонаправленные отклонения показателей иммунологического статуса: повышение числа Т-лимфоцитов, увеличение процентного содержания лимфоцитов, снижение числа естественных клеток-киллеров, увеличение количества CD4-лимфоцитов, снижение количества CD4-лимфоцитов, повышение числа B-лимфоцитов, снижение числа B-лимфоцитов, повышение числа естественных клеток-киллеров, повышение количества CD8-лимфоцитов, повышение уровня иммуноглобулина Е (IgE) в крови, увеличение соотношения CD4/CD8, уменьшение соотношения CD4/CD8, повышение уровня иммуноглобулина A (IgA) в крови, уменьшение процентного содержания лимфоцитов CD8. Отклонения в общем анализе крови: увеличение процентного содержания лимфоцитов, снижение показателя гематокрита, увеличение числа лимфоцитов, повышение скорости оседания эритроцитов, повышение числа лейкоцитов, повышение числа моноцитов, повышение числа тромбоцитов, снижение числа нейтрофилов, снижение числа тромбоцитов. Отклонения в общем анализе мочи: эритроциты в моче.
Большинство НЯ завершились выздоровлением без последствий. Лабораторные отклонения не имели клинического значения (не нуждались в проведении дополнительных диагностических процедур и назначении терапии).
Передозировка
О случаях передозировки не сообщалось.
Учитывая, что отпуск лекарственного препарата допускается только для лечебно-профилактических учреждений, а сама вакцинация проводится только квалифицированным медицинским персоналом, риск передозировки крайне низок.
Однако можно предположить, что при случайной передозировке возможно развитие указанных выше токсических и токсико-аллергических реакций в более тяжелой степени.
Специфических антидотов к препарату не существует.
Терапевтические мероприятия в данном случае будут включать симптоматическую терапию в соответствии с показаниями (кортикостероиды, жаропонижающие/ НПВС и десенсибилизирующие средства). Режим назначения препаратов должен быть выбран согласно рекомендациям по применению и дозировкам данного лекарственного средства.
Взаимодействие с другими лекарственными средствами
Не изучалось.
Особые указания
У пациентов, получающих иммуносупрессивную терапию, и пациентов с иммунодефицитом может не развиться достаточный иммунный ответ. Поэтому прием препаратов, угнетающих функцию иммунной системы, противопоказан в течение, как минимум, 1 месяца до и после вакцинации из-за риска снижения иммуногенности. Принять решение о возможности отмены иммуносупрессивной терапии может только лечащий врач!
Подобно остальным вакцинам, защитный иммунный ответ может возникать не у всех вакцинируемых лиц.
Влияние на способность управлять транспортными средствами, механизмами
Исследования по изучению влияния вакцины на способность управлять транспортными средствами и потенциально опасными механизмами не проводились.
Форма выпуска
Раствор для внутримышечного введения, 0,5 мл/доза.
Замороженный препарат
При производстве ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России):
по 0,5 мл (1 доза) препарата – во флаконы, укупоренные пробками из резины, обжатые алюминиевыми или алюмопластиковыми колпачками.
1 флакон препарата с инструкцией по применению в пачку картонную или в пачку из картона коробочного.
При производстве АО «Биннофарм»:
по 0,5 мл (1 доза) препарата – в ампулы из бесцветного стекла с точкой излома или в стерильном одноразовом шприце.
По 5 ампул препарата в контурную ячейковую упаковку из пленки поливинилхлоридной, или по 1 или 3 шприца с препаратом помещают в контурную ячейковую упаковку из пленки поливинилхлоридной, покрытую пленкой полиэтиленовой, или без покрытия.
По 1 контурной ячейковой упаковке вместе с инструкцией по применению в пачку из картона.
При производстве на АО «ГЕНЕРИУМ»:
по 3,0 мл (5 доз) препарата – во флаконы, укупоренные пробками резиновыми, с обкаткой колпачками алюминиево-пластиковыми с контролем первого вскрытия.
1 флакон препарата вместе с инструкцией по медицинскому применению – в пачку из картона с поролоновым держателем из пенополиуретана.
При производстве на ЗАО «ЛЕККО»:
по 3 мл (5 доз) препарата – во флаконы, укупоренные пробками резиновыми, с обкаткой колпачками алюминиево-пластиковыми с контролем первого вскрытия.
По 1 флакону вместе с инструкцией по применению – в пачку из картона с поролоновым держателем из пенополиуретана.
При производстве на ОАО «Фармстандарт-УфаВИТА»:
по 0,5 мл (1 доза) или по 1,0 мл (2 дозы) препарата в ампулы из бесцветного стекла.
По 5 ампул помещают в контурную ячейковую упаковку из пленки поливинилхлоридной.
По 1 или 2 контурные ячейковые упаковки вместе с инструкцией по применению – в пачку из картона.
По 3 мл (5 доз) препарата – во флаконы, укупоренные пробками резиновыми, с обкаткой колпачками алюминиево-пластиковыми с контролем первого вскрытия.
По 1 флакону вместе с инструкцией по применению в пачку из картона с поролоновым держателем из пенополиуретана.
При производстве на ЗАО «БИОКАД»:
по 0,5 мл (1 доза) или по 3,0 мл (5 доз) препарата во флаконы из нейтрального стекла I гидролитического класса (типа 2R, 6R), герметично укупоренные резиновыми пробками, с обкаткой алюминиевыми колпачками с пластиковой крышкой типа «flip-off».
На флаконы препарата наклеивают этикетку самоклеящуюся.
1 флакон 6R препарата с инструкцией по применению в пачку картонную.
1 флакон 2R препарата в контурной ячейковой упаковке из ПВХ пленки с инструкцией по применению в пачку картонную.
При производстве на АО «Р-Фарм»:
по 0,5 мл (1 доза) препарата во флаконы, герметично укупоренные пробками из резины и обжатые алюмопластиковыми колпачками.
По 1, 2, 5 или 10 флаконов вместе с инструкцией по применению в пачку из картона.
Жидкий препарат
При производстве на ООО «БиоИнтегратор»:
по 0,5 мл (1 доза) препарата – во флаконы, укупоренные пробками из резины, обжатые алюминиевыми или алюмопластиковыми колпачками.
1 флакон препарата с инструкцией по применению в пачку картонную или в пачку из картона коробочного.
Условия хранения
Замороженный препарат
Хранить в защищенном от света месте, при температуре не выше минус 18 °С. Повторное замораживание не допускается.
Хранить в недоступном для детей месте.
Жидкий препарат
Хранить в защищенном от света месте, при температуре от 2 до 8 °С. Не замораживать.
Хранить в недоступном для детей месте.
Условия транспортирования
Замороженный препарат
Транспортирование препарата при температуре не выше минус 18 °С.
Жидкий препарат
Транспортирование препарата при температуре от 2 до 8 °С. Не замораживать.
Срок годности
Замороженный препарат
6 месяцев. Не применять по истечении срока годности.
Жидкий препарат
1 месяц. Не применять по истечении срока годности.
Условия отпуска:
для лечебно-профилактических учреждений.
Производитель
Наименования и адреса производственных площадок производителя лекарственного препарата:
1) ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России), Россия, 123098, г. Москва, улица Гамалеи, д. 18 (все стадии производства).
2) АО «Р-Фарм», Россия, 150061, Ярославская обл., г.о. г. Ярославль, г. Ярославль, ул. Громова, д. 15 (производство готовой формы, первичная и вторичная (потребительская) упаковка).
3) АО «Биннофарм», Россия, 124460, г. Москва, г. Зеленоград, ул. Конструктора Гуськова, д. 3, стр. 1 (производство готовой формы, первичная и вторичная (потребительская) упаковка).
4) ЗАО «БИОКАД», Россия, 198515, г. Санкт-Петербург, п. Стрельна, ул. Связи, д. 38, стр. 1 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
5) АО «ГЕНЕРИУМ», Россия, 601125, Владимирская обл., Петушинский район, пос. Вольгинский, ул. Заводская, стр. 263 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
6) ЗАО «ЛЕККО», Россия, 601125, Владимирская обл., Петушинский район, пос. Вольгинский, ул. Заводская, стр. 277; 601125, Владимирская обл., Петушинский район, пос. Вольгинский, ул. Заводская, стр. 279 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
7) ОАО «Фармстандарт-УфаВИТА», Россия, Республика Башкортостан, г. Уфа, ул. Худайбердина, д. 28 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).

Выпускающий контроль качества
ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России). Россия, 123098, г. Москва, улица Гамалеи, д. 18.
Владелец регистрационного удостоверения/организация, принимающая претензии потребителя:
ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России), Россия
Россия, 123098, г. Москва, улица Гамалеи, д. 18.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
| Вакцина | Цена |
|---|---|
|
|
нет в наличии |
Вакцина «Спутник Лайт» защищает от инфекций:
Похожие вакцины (аналоги Спутник Лайт):
Торговое наименование:
Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2
Лекарственная форма:
раствор для внутримышечного введения
Состав на 1 дозу (0,5 мл):
Действующее вещество: рекомбинантные аденовирусные частицы 26 серотипа, содержащие ген белка S вируса SARS-CoV-2, в количестве (1,0±0,5)×1011 частиц/доза.
Вспомогательные вещества: трис(гидроксиметил)аминометан – 1,21 мг, натрия хлорид – 2,19 мг, сахароза – 25,0 мг, полисорбат 80 – 250 мкг, магния хлорида гексагидрат – 102,0 мкг, ЭДТА динатриевая соль дигидрат – 19,0 мкг, этанол 95 % – 2,5 мкл, вода для инъекций – до 0,5 мл.
Описание
Замороженный препарат.
Раствор замороженный – плотная затвердевшая беловатого цвета масса. После размораживания – однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Жидкий препарат.
Однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Характеристика
Вакцина получена биотехнологическим путем, при котором не используется патогенный для человека вирус SARS-CoV-2. В состав препарата входит рекомбинантный аденовирусный вектор на основе аденовируса человека 26 серотипа, несущий ген белка S вируса SARS-CoV-2.
Фармакотерапевтическая группа:
МИБП-вакцина
Код АТХ:
J07B
Фармакологические свойства
Новая редакция от 19 августа 2021 года.
Вакцина индуцирует формирование гуморального и клеточного иммунитета в отношении коронавирусной инфекции, вызываемой вирусом SARS-CoV-2.
Иммунологическая эффективность
Иммунологические свойства и безопасность вакцины изучали в различных клинических исследованиях у взрослых добровольцев обоего пола в возрасте старше 18 лет. Промежуточный анализ иммуногенности показал, что вакцина формирует гуморальный иммунный ответ у добровольцев. На 28 день сероконверсия обнаружена у 96,88% здоровых добровольцев.
У лиц с предсуществующим иммунитетом к коронавирусу отмечен выраженный рост титра антител на 10 день после вакцинации, что может указывать на возможность применения препарата для вакцинации ранее переболевших COVID-19 после снижения титра антител с целью предотвращения повторных случаев заболевания.
С учетом рекомендаций Всемирной организации здравоохранения для достижения уровня коллектннного иммунитета населения, следует проводить вакцинацию против новой коронавирусной инфекции COVID- 19 по эпидемическим показаниям спустя 6 месяцев после перенесенного заболевания (в том числе у ранее вакцинированных лиц) или спустя 6 месяцев после предыдущей первичной вакцинации.
В результате однократной иммунизации 100% здоровых добровольцев (все 30 человек у которых изучены показатели клеточного иммунитета) сформировали клеточный иммунный ответ против S белка SARS-Cov2.
Защитный титр антител в настоящее время неизвестен. Продолжительность защиты неизвестна.
Показания к применению
Новая редакция от 19 августа 2021 года.
Профилактика новой коронавирусной инфекции (COVID-19) у взрослых старше 18 лет.
Противопоказания
- гиперчувствительность к какому-либо компоненту вакцины или вакцине, содержащей аналогичные компоненты;
- тяжелые аллергические реакции в анамнезе;
- острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний – вакцинацию проводят через 2-4 недели после выздоровления или ремиссии. При нетяжелых ОРВИ, острых инфекционных заболеваниях ЖКТ-вакцинацию проводят после нормализации температуры;
- беременность и период грудного вскармливания;
- возраст до 18 лет (в связи с отсутствием данных об эффективности и безопасности).
С осторожностью
Новая редакция от 19 августа 2021 года.
Применять вакцину с осторожностью при хронических заболеваниях печени и почек, эндокринных заболеваниях (выраженных нарушениях функции щитовидной железы и сахарном диабете в стадии декомпенсации), тяжелых заболеваниях системы кроветворения, эпилепсии и других заболеваниях ЦНС, остром коронарном синдроме и остром нарушении мозгового кровообращения, миокардитах, эндокардитах, перикардитах.
Вследствие недостатка информации вакцинация может представлять риск для следующих групп пациентов:
- с аутоиммунными заболеваниями (стимуляция иммунной системы может привести к обострению заболевания, особенно следует с осторожностью относиться к пациентам с аутоиммунной патологией, имеющей тенденцию к развитию тяжёлых и жизнеугрожающих состояний);
- со злокачественными новообразованиями.
Категориям населения старше 60 лет, ранее не прошедшим иммунизацию от COVID-19, и не болевшим COVID-19, иммунокомпрометированным лицам независимо от возраста, для формирования иммунитета не рекомендовано применение препарата Спутник Лайт в связи со снижением функции иммунной системы, для формирования иммунного ответа показана вакцинация двухкомпонентной вакциной Гам-Ковид-Вак.
Принятие решения о вакцинации должно основываться на оценке соотношения пользы и риска в каждой конкретной ситуации.
Применение при беременности и в период грудного вскармливания
Препарат противопоказан при беременности и в период грудного вскармливания, так как его эффективность и безопасность в этот период не изучались.
Способ применения и дозы
Вакцина предназначена только для внутримышечного введения. Строго запрещено внутривенное введение препарата. Вакцину вводят в дельтовидную мышцу (верхнюю треть наружной поверхности плеча). При невозможности введения в дельтовидную мышцу – препарат вводят в латеральную широкую мышцу бедра.
После введения вакцины пациент должен находиться под наблюдением медицинских работников в течение 30 минут.
Замороженный препарат
Перед вакцинированием флакон, ампулу или шприц с препаратом достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон, ампулу или шприц снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона, ампулы или шприца!
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой. Вскрывают ампулу по кольцу и/или точке излома. Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту из ампулы или флакона.
Внимание! Доза, вводимая пациенту, не должна превышать 0,5 мл!
Препарат в шприцах готов к применению без дополнительных манипуляций.
Применение вакцины производства ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России) (флаконы) и АО «Биннофарм» (ампулы, шприцы):
Не допускается хранение размороженного препарата более 30 минут!
Повторное замораживание не допускается!
Применение вакцины производства АО «ГЕНЕРИУМ» (флаконы), ОАО «Фармстандарт-УфаВИТА» (флаконы, ампулы), ЗАО «ЛЕККО» (флаконы):
Внимание! Повторное замораживание флакона или ампулы с раствором не допускается!
Суммарное время хранения размороженного раствора при комнатной температуре не должно превышать 2 часов. Неиспользованная вакцина подлежит уничтожению.
Многодозовые флаконы
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого или невскрытого флакона не более 2 часов при комнатной температуре.
Многодозовые ампулы
Содержимое ампулы рекомендуется использовать незамедлительно. Если последующие инъекции по какой-либо причине откладываются, допускается хранение вакцины при комнатной температуре: вскрытой ампулы, закрытой стерильной салфеткой, не более 1 часа, невскрытой ампулы – не более 2 часов.
ВНИМАНИЕ! Одна ампула содержит две дозы вакцины. Объем одной дозы составляет 0,5 мл. Одному пациенту вводить 1 дозу (0,5 мл).
Однодозовые ампулы
Содержимое ампулы рекомендуется использовать незамедлительно. Если последующие инъекции по какой-либо причине откладываются, допускается хранение невскрытой ампулы при комнатной температуре не более 2 часов.
Применение вакцины производства ЗАО «БИОКАД» (флаконы), АО «Р-Фарм» (флаконы):
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого флакона по 3 мл не более 2 часов при комнатной температуре.
Не допускается хранение размороженного препарата во флаконах по 0,5 мл более 30 минут!
Повторное замораживание не допускается!
Жидкий препарат
Применение вакцины производства ООО «БиоИнтегратор» (флаконы):
Внимание! Замораживание флакона с раствором не допускается!
Флакон достают из холодильника и выдерживают при комнатной температуре, допускается слегка нагреть препарат, например, подержав его в руках. Не следует нагревать препарат выше 37 °С.
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой.
Используя одноразовый шприц с иглой, отбирают дозу 0,5 мл для введения пациенту.
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого флакона или ампулы не более 2 часов при комнатной температуре.
Внимание! К использованию непригоден препарат (жидкий и/или замороженный) с дефектами укупорочной системы и/или нарушенной маркировкой флакона или ампулы,, при изменении физических свойств раствора (мутность, окрашивание), неправильном хранении и/или с истекшим сроком годности.
Информация для медицинских работников, выполняющих вакцинацию лекарственным препаратом: данный лекарственный препарат зарегистрирован по особой процедуре регистрации, в связи с чем необходимо уведомлять Федеральную службу по надзору в сфере здравоохранения о каждом факте применения лекарственного препарата путем внесения информации в соответствующий раздел информационной системы ЕГИСЗ.
Побочное действие
Нежелательные явления, характерные для применения вакцины, выявленные в рамках клинических исследований, а также исследований других вакцин на основе аналогичной технологической платформы, бывают преимущественно легкой или средней степени выраженности, могут развиваться в первые-вторые сутки после вакцинации и разрешаются в течение 3-х последующих дней. Часто и очень часто могут развиться кратковременные общие (непродолжительный гриппоподобный синдром, характеризующийся ознобом, повышением температуры тела, артралгией, миалгией, астенией, общим недомоганием, головной болью) и местные (болезненность в месте инъекции, гиперемия, отечность) реакции. Рекомендуется назначение нестероидных противовоспалительных средств (НПВС) при повышении температуры после вакцинации и антигистаминных средств при выраженной местной реакции.
Нежелательные явления, представленные ниже, перечислены по системам организма и в соответствии с частотой встречаемости. Частота встречаемости определяется следующим образом: очень часто (≥1/10), часто (≥1/100 и < /10), нечасто (≥1/1000 и <1/100), редко (≥1/10000 и <1/1000), очень редко (<1/10000, включая отдельные случаи). Категории частоты были сформированы на основании клинических исследований препарата.
Часто отмечаются: тошнота, диспепсия, снижение аппетита, очень редко – увеличение регионарных лимфоузлов. У некоторых пациентов возможно развитие аллергических реакций, кратковременное повышение уровня печеночных трансаминаз, креатинина и креатинфосфокиназы в сыворотке крови.
В рамках проведенных клинических исследований безопасности, переносимости и иммуногенности препарата «Спутник-Лайт» после вакцинации были зарегистрированы следующие НЯ:
«Общие нарушения и реакции в месте введения»: гипертермия, боль, отек, зуд в месте вакцинации, астения, боль, недомогание, пирексия, повышение температуры кожи в месте вакцинации, снижение аппетита. Частота развития – очень часто и часто.
«Нарушения со стороны дыхательной системы, органов грудной клетки и средостения»: боль в ротоглотке, заложенность носа, першение в горле, ринорея. Частота развития – часто.
«Нарушения со стороны нервной системы»: головная боль, астения – часто; головокружения, обмороки – редко.
«Желудочно-кишечные нарушения»: тошнота, рвота, диспепсия – часто.
«Лабораторные и инструментальные данные»: разнонаправленные отклонения показателей иммунологического статуса: повышение числа Т-лимфоцитов, увеличение процентного содержания лимфоцитов, снижение числа естественных клеток-киллеров, увеличение количества CD4-лимфоцитов, снижение количества CD4-лимфоцитов, повышение числа B-лимфоцитов, снижение числа B-лимфоцитов, повышение числа естественных клеток-киллеров, повышение количества CD8-лимфоцитов, повышение уровня иммуноглобулина Е (IgE) в крови, увеличение соотношения CD4/CD8, уменьшение соотношения CD4/CD8, повышение уровня иммуноглобулина A (IgA) в крови, уменьшение процентного содержания лимфоцитов CD8. Отклонения в общем анализе крови: увеличение процентного содержания лимфоцитов, снижение показателя гематокрита, увеличение числа лимфоцитов, повышение скорости оседания эритроцитов, повышение числа лейкоцитов, повышение числа моноцитов, повышение числа тромбоцитов, снижение числа нейтрофилов, снижение числа тромбоцитов. Отклонения в общем анализе мочи: эритроциты в моче.
Большинство НЯ завершились выздоровлением без последствий. Лабораторные отклонения не имели клинического значения (не нуждались в проведении дополнительных диагностических процедур и назначении терапии).
Передозировка
О случаях передозировки не сообщалось.
Учитывая, что отпуск лекарственного препарата допускается только для лечебно-профилактических учреждений, а сама вакцинация проводится только квалифицированным медицинским персоналом, риск передозировки крайне низок.
Однако можно предположить, что при случайной передозировке возможно развитие указанных выше токсических и токсико-аллергических реакций в более тяжелой степени.
Специфических антидотов к препарату не существует.
Терапевтические мероприятия в данном случае будут включать симптоматическую терапию в соответствии с показаниями (кортикостероиды, жаропонижающие/ НПВС и десенсибилизирующие средства). Режим назначения препаратов должен быть выбран согласно рекомендациям по применению и дозировкам данного лекарственного средства.
Взаимодействие с другими лекарственными средствами
Не изучалось.
Особые указания
У пациентов, получающих иммуносупрессивную терапию, и пациентов с иммунодефицитом может не развиться достаточный иммунный ответ. Поэтому прием препаратов, угнетающих функцию иммунной системы, противопоказан в течение, как минимум, 1 месяца до и после вакцинации из-за риска снижения иммуногенности. Принять решение о возможности отмены иммуносупрессивной терапии может только лечащий врач!
Подобно остальным вакцинам, защитный иммунный ответ может возникать не у всех вакцинируемых лиц.
Влияние на способность управлять транспортными средствами, механизмами
Исследования по изучению влияния вакцины на способность управлять транспортными средствами и потенциально опасными механизмами не проводились.
Форма выпуска
Раствор для внутримышечного введения, 0,5 мл/доза.
Замороженный препарат
При производстве ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России):
по 0,5 мл (1 доза) препарата – во флаконы, укупоренные пробками из резины, обжатые алюминиевыми или алюмопластиковыми колпачками.
1 флакон препарата с инструкцией по применению в пачку картонную или в пачку из картона коробочного.
При производстве АО «Биннофарм»:
по 0,5 мл (1 доза) препарата – в ампулы из бесцветного стекла с точкой излома или в стерильном одноразовом шприце.
По 5 ампул препарата в контурную ячейковую упаковку из пленки поливинилхлоридной, или по 1 или 3 шприца с препаратом помещают в контурную ячейковую упаковку из пленки поливинилхлоридной, покрытую пленкой полиэтиленовой, или без покрытия.
По 1 контурной ячейковой упаковке вместе с инструкцией по применению в пачку из картона.
При производстве на АО «ГЕНЕРИУМ»:
по 3,0 мл (5 доз) препарата – во флаконы, укупоренные пробками резиновыми, с обкаткой колпачками алюминиево-пластиковыми с контролем первого вскрытия.
1 флакон препарата вместе с инструкцией по медицинскому применению – в пачку из картона с поролоновым держателем из пенополиуретана.
При производстве на ЗАО «ЛЕККО»:
по 3 мл (5 доз) препарата – во флаконы, укупоренные пробками резиновыми, с обкаткой колпачками алюминиево-пластиковыми с контролем первого вскрытия.
По 1 флакону вместе с инструкцией по применению – в пачку из картона с поролоновым держателем из пенополиуретана.
При производстве на ОАО «Фармстандарт-УфаВИТА»:
по 0,5 мл (1 доза) или по 1,0 мл (2 дозы) препарата в ампулы из бесцветного стекла.
По 5 ампул помещают в контурную ячейковую упаковку из пленки поливинилхлоридной.
По 1 или 2 контурные ячейковые упаковки вместе с инструкцией по применению – в пачку из картона.
По 3 мл (5 доз) препарата – во флаконы, укупоренные пробками резиновыми, с обкаткой колпачками алюминиево-пластиковыми с контролем первого вскрытия.
По 1 флакону вместе с инструкцией по применению в пачку из картона с поролоновым держателем из пенополиуретана.
При производстве на ЗАО «БИОКАД»:
по 0,5 мл (1 доза) или по 3,0 мл (5 доз) препарата во флаконы из нейтрального стекла I гидролитического класса (типа 2R, 6R), герметично укупоренные резиновыми пробками, с обкаткой алюминиевыми колпачками с пластиковой крышкой типа «flip-off».
На флаконы препарата наклеивают этикетку самоклеящуюся.
1 флакон 6R препарата с инструкцией по применению в пачку картонную.
1 флакон 2R препарата в контурной ячейковой упаковке из ПВХ пленки с инструкцией по применению в пачку картонную.
При производстве на АО «Р-Фарм»:
по 0,5 мл (1 доза) препарата во флаконы, герметично укупоренные пробками из резины и обжатые алюмопластиковыми колпачками.
По 1, 2, 5 или 10 флаконов вместе с инструкцией по применению в пачку из картона.
Жидкий препарат
При производстве на ООО «БиоИнтегратор»:
по 0,5 мл (1 доза) препарата – во флаконы, укупоренные пробками из резины, обжатые алюминиевыми или алюмопластиковыми колпачками.
1 флакон препарата с инструкцией по применению в пачку картонную или в пачку из картона коробочного.
Условия хранения
Замороженный препарат
Хранить в защищенном от света месте, при температуре не выше минус 18 °С. Повторное замораживание не допускается.
Хранить в недоступном для детей месте.
Жидкий препарат
Хранить в защищенном от света месте, при температуре от 2 до 8 °С. Не замораживать.
Хранить в недоступном для детей месте.
Условия транспортирования
Замороженный препарат
Транспортирование препарата при температуре не выше минус 18 °С.
Жидкий препарат
Транспортирование препарата при температуре от 2 до 8 °С. Не замораживать.
Срок годности
Замороженный препарат
6 месяцев. Не применять по истечении срока годности.
Жидкий препарат
1 месяц. Не применять по истечении срока годности.
Условия отпуска:
для лечебно-профилактических учреждений.
Производитель
Наименования и адреса производственных площадок производителя лекарственного препарата:
1) ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России), Россия, 123098, г. Москва, улица Гамалеи, д. 18 (все стадии производства).
2) АО «Р-Фарм», Россия, 150061, Ярославская обл., г.о. г. Ярославль, г. Ярославль, ул. Громова, д. 15 (производство готовой формы, первичная и вторичная (потребительская) упаковка).
3) АО «Биннофарм», Россия, 124460, г. Москва, г. Зеленоград, ул. Конструктора Гуськова, д. 3, стр. 1 (производство готовой формы, первичная и вторичная (потребительская) упаковка).
4) ЗАО «БИОКАД», Россия, 198515, г. Санкт-Петербург, п. Стрельна, ул. Связи, д. 38, стр. 1 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
5) АО «ГЕНЕРИУМ», Россия, 601125, Владимирская обл., Петушинский район, пос. Вольгинский, ул. Заводская, стр. 263 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
6) ЗАО «ЛЕККО», Россия, 601125, Владимирская обл., Петушинский район, пос. Вольгинский, ул. Заводская, стр. 277; 601125, Владимирская обл., Петушинский район, пос. Вольгинский, ул. Заводская, стр. 279 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).
7) ОАО «Фармстандарт-УфаВИТА», Россия, Республика Башкортостан, г. Уфа, ул. Худайбердина, д. 28 (производство готовой лекарственной формы, первичная и вторичная (потребительская) упаковка).

Выпускающий контроль качества
ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России). Россия, 123098, г. Москва, улица Гамалеи, д. 18.
Владелец регистрационного удостоверения/организация, принимающая претензии потребителя:
ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России), Россия
Россия, 123098, г. Москва, улица Гамалеи, д. 18.
Узнать наличие вакцины Спутник Лайт и записаться на прививку можно по телефонам центра:
«Диавакс» на Таганке
+7 (495) 988-47-76
+7 (916) 550-53-03
«Диавакс» на ВДНХ
+7 (495) 616-29-59
+7 (915) 351-92-53
Если хотите пригласить определённого специалиста, оставьте заявку и мы вам перезвоним!
Возможен выезд врача на дом и на предприятия для вакцинации сотрудников. Стоимость выезда врача – договорная. Услуги по проведению вакцинации оплачиваются отдельно в соответствии с действующим прейскурантом.
11 ноября 2021 года
Составить индивидуальный график вакцинации или получить грамотную консультацию специалиста теперь можно не выходя из дома, потому что мы заботимся о Вас, снижая количество контактов и экономя Ваше время!
Онлайн-консультация по вопросам вакцинопрофилактики
Специалистом центра «Диавакс» будет составлен Индивидуальный график вакцинации, прописаны последовательность и сроки вакцинации с перечнем всех необходимых вакцин, исходя из Вашей конкретной ситуации.
Дистанционная консультация аллерголога-иммунолога
Получить исчерпывающую консультацию аллерголога-иммунолога теперь можно в онлайне! Врач поставит предварительный диагноз, определит план обследования, ответит на любые вопросы по уже назначенному лечению, в том числе по лечебному питанию при пищевой аллергии.
А еще мы отвечаем на интересующие вас вопросы в специальном разделе! Чаще всего это вопросы индивидуального характера в отношении вакцинации, иммунитета и тому подобного.
На вопросы отвечают:
- Специалисты в области иммунопрофилактики
- Сотрудники Кафедры инфекционных болезней у детей РНИМУ им. Н.И. Пирогова
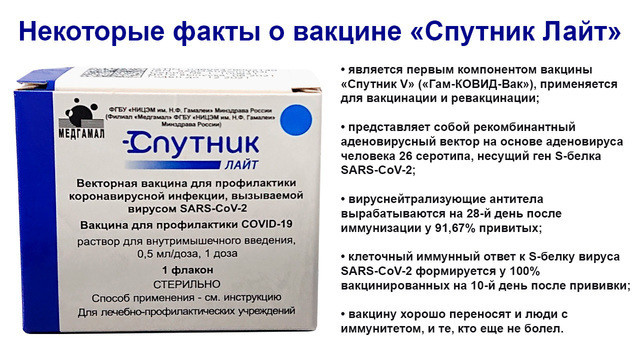
Что такое «Спутник Лайт»?
Вакцина «Спутник Лайт» является векторной и применяется для профилактики заражения и тяжелого течения COVID-19. Она зарегистрирована 6 мая 2021 года и используется для иммунизации людей старше 18 лет¹.
Будет ли эффективен «Спутник Лайт» для тех, кто еще не болел коронавирусом?
«Безусловно будет, потому что в инструкции для «Спутника Лайт» сказано, что он рекомендуется в качестве одной из признанных в нашей стране вакцин. Основными документами для вакцинации являются методические руководства, который присылает Минздрав (и они периодически обновляются), а также собственно инструкция для вакцины. В этой инструкции сказано, что «Спутник Лайт» разрешен для вакцинирования лицам с 18 до 60 лет. И в рекомендациях для него указаны те же самые положения, что и для других вакцин».



Защищает ли «Спутник Лайт» от омикрона?
Начиная с декабря 2021 года, в России распространяется омикрон-штамм вируса SARS-CoV-2. Его считают более опасным по сравнению с предыдущими вариантами коронавируса потому что он лучше преодолевает иммунитет, сформированный как после болезни, так и после вакцинации. Из-за этого количество заболевших среди людей, уже привитых от новой коронавирусной инфекции, может быстро увеличиться.
Точной информации о том, насколько вакцина «Спутник Лайт» защищает от омикрона, пока нет. Клинические данные, позволяющие судить об этом, должны быть представлены в конце января-начале февраля 2022 года. Пока есть следующая информация:
- Уже проведенные исследования показывают, что нейтрализующая способность антител против нового штамма снижается в десятки раз.
- Также снижается защита иммунитета, сформированного после вакцинации. Для разных вакцин называют разные цифры, однако точных и подтвержденных данных пока нет ни для одной из них.
- Известно, что уровень защиты резко возрастает в результате ревакцинации, то есть после введения третьей дозы вакцины.
Директор Центра им. Гамалеи заявил, что эффективность «Спутника V» против омикрона составляет почти 100%, если сделана ревакцинация «Спутником Лайт». С учетом этого первый компонент «Спутника V» не планируют адаптировать под новый штамм.
Эффективность вакцины «Спутник Лайт» при омикроне
В Российском фонде прямых инвестиций утверждают, что даже в случае заражения омикроном, «Спутник V» лучше, чем другие вакцины помогает снизить риск тяжелого течения болезни. Насколько эффективен «Спутник Лайт», отдельно не оценивают, однако разработчики вакцины отмечают, что при ревакцинации он сможет обеспечить необходимую защиту. Это подтверждает исследование, проведенное Центром им. Гамалеи и Национальным институтом инфекционных заболеваний им. Ладзаро Спалланцани (Италия). Предварительные результаты эффективности «Спутника» против штамма омикрон опубликованы на платформе препринтов medRxiv⁷. Ученые выяснили, что «Спутник Лайт» в качестве бустера (третья вакцина) значительно увеличивает вируснейтрализующую активность против штамма омикрон.
Омикрон-штамм появился недавно и пока плохо исследован. Он быстро распространяется, может вызывать тяжелую форму коронавирусной инфекции. Судить о том, насколько эффективен «Спутника Лайт» против омикрона, пока рано. Но уже есть данные, позволяющие предположить, что уровень защиты снизится (но все равно останется более высоким, чем у тех, кто вообще не имеет иммунитета против коронавируса). Это значит, что даже после вакцинации важно продолжать соблюдать меры предосторожности.
Эффективность «Спутник Лайт»
Судить об эффективности будет можно, когда завершится III фаза клинических испытаний и будут опубликованы ее результаты. Планируется, что это случится 31 января 2022 года, еще некоторое время понадобится на оценку результатов. Пока есть только предварительные оценки эффективности.
На декабрь 2021 года центр им. Н. Ф. Гамалеи оценивает эффективность вакцины «Спутник Лайт» следующим образом:
- около 80% против заражения коронавирусом;
- около 70% против штамма дельта при использовании для первичной вакцинации;
- более 83% против штамма дельта при использовании для ревакцинации в качестве бустера¹.
Эффективность защиты против тяжелого течения болезни в случае заражения является еще более высокой.
«Спутник Лайт» и QR-код
«Спутник Лайт» может применяться в качестве самостоятельной вакцины, и после прививки им человек получает сертификат о вакцинации вместе с QR-кодом. Вот главные факты об этом:
- Срок действия сертификата о вакцинации и QR-кода после прививки «Спутник Лайт» составляет 1 год. Его могут сократить до 6 месяцев, если эпидемическая ситуация будет неблагоприятной.
- Сертификат с QR-кодом должен формироваться автоматически после внесения данных о вакцинации в информационную систему портала Госуслуг.
- Согласно приказу №1053 Минздрава РФ от 12 ноября 2021 года, на формирование сертификата о вакцинации отводится не более трех дней.
На практике, если вакцинация в регионе идет высокими темпами и сразу прививается много людей, сертификат может формироваться с задержкой. В этом случае нужно проверить, правильно ли указаны данные СНИЛС, паспорта и полиса на портале Госуслуг. Если ошибок нет, обратитесь в пункт вакцинации. Его сотрудники проверят, были ли переданы ваши данные в информационную систему. Если да, нужно обращаться в поддержку портала Госуслуг.
Безопасность «Спутник Лайт»
Авторитетное медицинское издание The Lancet уже опубликовало результаты первых двух фаз клинических исследований вакцины. В ходе них, в том числе проверялась безопасность препарата. Согласно этой публикации, здоровые взрослые хорошо переносят вакцинацию — и те, у кого до иммунизации не было антител к коронавирусу, и те, у кого они есть⁶.
Результаты исследования, опубликованные в The Lancet
Это — результаты первой и второй фазы исследования вакцины «Спутник Лайт». Их задача — оценка безопасности, реактогенности (способности вызывать побочные эффекты) и иммуногенности (способности вызывать иммунный ответ).
Для исследования было отобрано 110 здоровых добровольцев в возрасте от 18 до 59 лет. У 14 из них уже были антитела к коронавирусу, и их поместили в отдельную группу.
У 100% добровольцев к 42-му дню после вакцинации в сыворотке крови появились специфические антитела. При этом у тех, кто ранее имел антитела к коронавирусу, формирование иммунного ответа происходило быстрее, а средние титры антител после вакцинации были выше на 10-й, 28-й и 42-й день. Это дает основания расценивать «Спутник Лайт» как хороший бустер при ревакцинации после применения других вакцин.
Легкие побочные реакции возникали в 67% случаев, умеренные в 5,5% случаев. Самая частая реакция — гриппоподобный синдром, при котором у человека появлялась лихорадка и озноб, боли в мышцах, головная боль.
В публикации в The Lancet авторы также ссылаются на проведенное в Аргентине исследование, результаты которого показывают, что «Спутник Лайт» эффективен и безопасен для вакцинации людей старше 65 лет. В этой возрастной группе его эффективность против заражения коронавирусом составила 78%, против тяжелого течения болезни, госпитализации и смерти — 87%.
С августа 2021 года Минздрав РФ разрешает применение вакцины для иммунизации людей старше 60 лет³.
Не ориентируйтесь на уровень антител, принимая решение о вакцинации
«Уровень антител не рекомендуется контролировать в плане определения показаний и противопоказаний для вакцинации и ревакцинации. Дело в том, что этот показатель оценивает только гуморальный, но не клеточный иммунитет. А только взаимоотношение этих двух составляющих иммунитета формирует иммунный ответ человека. Хотя произносятся фразы о том, что есть некий базовый, минимальный уровень антител, после которого рассчитывать на собственный иммунный ответ нельзя, но это личное мнение тех или иных специалистов.
Есть инструкции, которые вложены в наборы для определения количества антител и там тоже указаны определенные уровни, но это лишь вкладыши к диагностическим наборам, но никак не официальные рекомендации. Так что ключевым моментом для вакцинации на сегодняшний день является временной фактор. Для ревакцинации сейчас больше рекомендуется именно «Спутник Лайт». Верхний разрешенный возраст для этой вакциной — 60 лет, и он определяется тем, что это однокомпонентная вакцина и она вводится один раз. Поэтому пожилым пациентам, у которых иммунный ответ происходит несколько медленнее, лучше проводить вакцинацию двумя инъекциями. При этом достигается более высокий уровень защиты. По сути, «Спутник Лайт» — это первый компонент вакцины «Спутник V».



Отличие от вакцины «Спутник V»
Между «Спутником Лайт» и «Спутником V» много общего. У вакцин один и тот же принцип действия. По составу «Спутник Лайт» идентичен первому компоненту «Гам-Ковид-Вак». Однако есть и различия, и нужно учитывать их, принимая решение о вакцинации:
- При использовании «Спутник Лайт» прививку делают только один раз, а не два.
- Сертификат о вакцинации с QR-кодом человек получает сразу после прививки (ждать второй укол не нужно).
- При прививке «Спутник Лайт» вводится только один компонент вакцины, и поэтому уровень защиты ниже. Предварительно его оценивают в 79,4% против более 90% эффективности у «Спутника V».
Есть разница и в сроках регистрации. На декабрь 2021 года «Спутник V» прошел регистрацию почти в 70 странах. По нему есть больше официальной информации. Его клинические исследования завершатся раньше. «Спутник Лайт» — другой препарат, который другие государства и регуляторы будут признавать отдельно. Это может повлиять на возможность въезда в зарубежные страны.
«Спутник Лайт» в мире
На конец 2021 года некоторые страны уже применяют «Спутник Лайт», включая ОАЭ, Аргентину, Мексику, Сербию, Венгрию, Филиппины, Сан-Марино и другие. Тем не менее, многие государства не признают препарат в качестве самостоятельной вакцины и устанавливают ограничения для людей, которые привиты только им¹.
Когда появятся антитела?
При вакцинации «Спутник Лайт» уже после одного укола человек считается полностью вакцинированным. Однако чтобы выработались антитела, нужно некоторое время. Точно оценить эти сроки можно будет, когда завершатся клинические исследования препарата. Результаты первой и второй фазы клинических исследований показали, что сроки формирования антител различаются для тех, кто ранее вакцинировался против коронавируса или болел им, и для тех, кто не прививался и не болел. В первой группе выработка антител шла быстрее, и уже к 10 дню регистрировали более выраженный иммунный ответ по сравнению со второй группой⁶. Несмотря на то, что антитела могут появиться уже спустя 10 суток, человек считается защищенным только через 21 день после прививки. Даже после этого важно продолжать соблюдать меры предосторожности. Пока нет точных данных о продолжительности защиты.
Противопоказания
Прививка «Спутник Лайт» противопоказана в следующих случаях:
- Если есть непереносимость или гиперчувствительность к любому из компонентов в составе вакцины.
- При наличии в анамнезе тяжелой аллергической реакции.
- Тяжелые поствакцинальные осложнения во время предыдущего введения вакцины или ее компонентов (анафилактический шок, судороги, температура выше 40°С, отек или гиперемия в месте введения вакцины, тяжелая аллергическая реакция).
- В период беременности и лактации.
- При возрасте меньше 18 лет.
Вакцинацию нужно отложить при любом остром заболевании, а также при обострении хронических болезней. Сделать прививку можно будет только после выздоровления или снятия обострения (спустя 2-4 недели).
При острой инфекции ЖКТ или ОРВИ в легкой форме привиться можно, когда нормализуется температура².
Наличие антител — не противопоказание
Если человек переболел новой коронавирусной инфекцией бессимптомно или не обращаясь за медицинской помощью, и у него появились антитела к SARS-CoV-19, ему все равно нужно привиться. Сделать это можно вакциной «Спутник Лайт». По рекомендациям Всемирной организации здравоохранения, наличие антител класса IgG против коронавируса не считается противопоказанием для вакцинации.
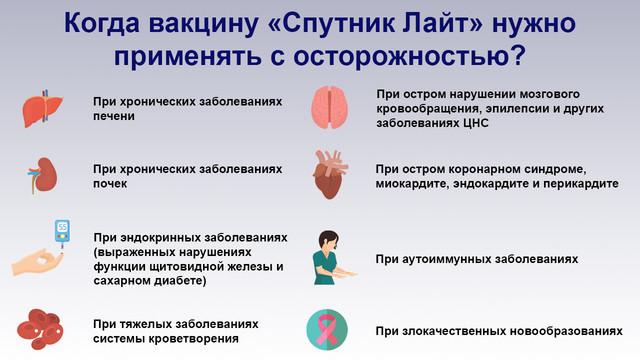
В некоторых случаях препарат применяется с осторожностью. Лучше проконсультироваться с лечащим врачом, если есть эндокринные нарушения, болезни почек, печени, системы кроветворения, центральной нервной системы, а также аутоиммунные или онкологические заболевания, воспалительные заболевания сердца, а также при остром коронарном синдроме, при нарушении мозгового кровообращения.
Прививка может не вызвать иммунный ответ при наличии иммунодефицита и при получении иммуносупрессивной терапии. Планируя вакцинацию, минимум за месяц до нее нужно прекратить принимать угнетающие функцию иммунной системы лекарства. Делать это можно только по согласованию с лечащим врачом².
С какими рисками и заболеваниями рекомендуется использовать «Спутник Лайт»?
«Я бы не проводил различия в рекомендациях по вакцинации, исходя из особенностей того или иного человека, его заболеваний и факторов риска. Главное, чтобы он вакцинировался. Удобство «Спутника Лайт» в том, что это однократное введение вакцины. Но для тех, кто по-настоящему беспокоится о своем здоровье и хочет получить потенциально более надежный ответ, я бы, конечно, рекомендовал двухкомпонентную вакцину во всех случаях».



Побочные действия
На первый или второй день после прививки «Спутник Лайт» самочувствие может немного ухудшаться. Обычно симптомы легкие или средние по тяжести и проходят в срок до трех дней. Среди них (в порядке убывания распространенности):
- в месте укола боль, небольшое покраснение, отек;
- озноб, боль в мышцах и суставах, недомогание, головная боль как при простуде или гриппе;
- першение, боль в горле, насморк;
- расстройство желудка, тошнота и снижение аппетита.
При плохом самочувствии, если повышается температура тела, можно принять жаропонижающее или нестероидное противовоспалительное средство. Но даже без лечения побочные эффекты от вакцинации проходят быстро и без последствий².
Принцип действия
Вакцина «Спутник Лайт» называется векторной, так как ее основой является вектор аденовируса. Векторами называют вирусы, лишенные способности размножаться и не представляющие угрозу. Их используют для «доставки» генетического материала других вирусов (в случае со «Спутник Лайт»
— коронавируса SARS-CoV-2). Генетическим материалом является код S-белка, формирующего шипы оболочки коронавируса. Вектор со встроенным в него генетическим материалом коронавируса безопасен для организма человека. При этом он «учит» иммунную систему реагировать на настоящий вирус и защищаться от инфекции¹.
В качестве основы, «платформы» используются векторы человеческих аденовирусов, так как их легче модифицировать. Существуют разные серотипы таких аденовирусов, для «Спутник V» применяют два — 26-й и 5-й серотип в составе первого и второго компонентов соответственно. «Спутник Лайт» предполагает использование только 26-го серотипа. Поэтому уровень защиты после вакцинации им ниже, если сравнивать со «Спутником V».
Комбинации с другими вакцинами
При ревакцинации «Спутник Лайт» можно использовать как бустер в комбинации с другими вакцинами. Среди них все зарегистрированные в России вакцины, а также зарубежные препараты. На декабрь 2021 года есть данные о безопасности сочетания «Спутник Лайт» с иностранными вакцинами AstraZeneca, SinoPharm, Moderna. Возможность комбинированного применения пока продолжает изучаться⁴.
Также «Спутник Лайт» допускается использовать одновременно с назальной вакциной «Спутник» (препарат на стадии клинических исследований. По предварительным данным, эта комбинация не вызывает серьезных побочных эффектов).
Состав «Спутника Лайт»
Препарат не содержит живой вирус или его частицы. Вместо них используется только генетический материал коронавируса. Это защищает от заражения, а если оно все-таки происходит, болезнь протекает в легкой форме.
В качестве основного действующего вещества используется вектор (обезвреженный аденовирус 26-го серотипа), в который «встроен» ген S-белка коронавируса¹.
В качестве вспомогательных компонентов используются:
- ТРИС (нетоксичный буферный раствор);
- вода;
- хлорид натрия;
- динатриевая соль, дигидрат;
- сахароза;
- этанол;
- хлорид магния.
Уточните наличие вакцины
При предварительной записи нельзя выбрать препарат, которым будет проводиться вакцинация. Такой выбор можно сделать только в прививочном пункте. Если важно привиться именно «Спутник Лайт», нужно учесть, что этой вакцины часто нет в наличии. Она пользуется повышенным спросом. Бывают и обратные ситуации, когда в прививочном пункте нет достаточного количества желающих привиться, из-за чего медперсонал не может разморозить флакон на несколько доз.
Жидкая или замороженная? Зависит от места производства
«Спутник Лайт» изготавливается несколькими предприятиями, и от места производства зависит, как будет поставляться препарат: в жидком или замороженном виде, в ампулах или во флаконах на несколько доз².
В замороженном виде «Спутник Лайт» поставляют:
- ФГБУ «НИЦЭМ им. Н. Ф. Гамалеи», АО «Биннофарм», АО «Р-Фарм» — ампулы или флаконы по 1 дозе;
- ЗАО ЛЕККО, АО Генериум — флаконы по 5 доз;
- ЗАО «БИОКАД» — флаконы по 1 или 5 доз;
- ОАО «Фармстандарт-УфаВИТА» — ампулы по 1 или 2 дозы, флаконы по 5 доз.
На декабрь 2021 года в жидком виде вакцину производит только компания «Биоинтегратор». Фасовка во флаконах по 1 дозе.
После размораживания препарат может храниться ограниченное время. Повторно замораживать его нельзя. По этой причине флаконы на 2 или 5 доз размораживаются и вскрываются только при условии, что в прививочном кабинете есть достаточное количество желающих вакцинироваться. Иногда приходится ждать, пока наберется нужное количество людей, что замедляет процедуру вакцинации.
Инструкция по применению
Вакцинацию против коронавирусной инфекции проводят в прививочных кабинетах или пунктах. Прививку делает медицинский персонал, который обязан соблюдать не только инструкцию к препарату, но и методические рекомендации Минздрава. Это исключает риск передозировки, неправильного введения или других ошибок, однако даже с учетом этого тем, кто прививается, важно знать, как должен применяться препарат.
Чаще всего «Спутник Лайт» поставляется замороженным. Перед инъекцией ампула или флакон должны быть выдержаны при комнатной температуре, пока жидкость полностью не разморозится. Не вскрывая ампулу или флакон, нужно осторожно перемешать содержимое (покачивая, но не встряхивая).
Инъекцию делают одноразовым шприцем, объем одной дозы — 0,5 мл. Вакцину вводят внутримышечно в область плеча.
Срок хранения после размораживания ограничен:
- если флакон не вскрыт, он составляет 2 часа;
- после вскрытия — 30 минут.
Замораживать вакцину после разморозки или вводить ее после того, как истек срок хранения, нельзя².
Как делают прививку?
Прививку можно сделать в прививочном кабинете или в мобильном пункте вакцинации — по записи (например, через портал Госуслуг) или в порядке живой очереди.
Вся процедура занимает около 45 минут и проводится в несколько этапов:
- Рядом с прививочным кабинетом нужно взять и заполнить анкету и добровольное информированное согласие. Понадобятся паспорт, СНИЛС и полис ОМС.
- До вакцинации нужно пройти осмотр у терапевта. Он измерит температуру, артериальное давление и сатурацию (уровень насыщения крови кислородом), а также задаст вопросы о самочувствии и состоянии здоровья. Врачу нужно рассказать обо всех имеющихся заболеваниях и принимаемых препаратах.
- Если терапевт разрешает вакцинацию, нужно пройти в прививочный кабинет. Укол делают внутримышечно в предплечье.
- После укола или во время осмотра до него врач даст памятку с подробной информацией о том, как может изменяться самочувствие, что можно и что нельзя делать после вакцинации.
- После прививки нужно оставаться рядом с прививочным кабинетом в течение получаса. Это важно на случай появления побочных эффектов, развития тяжелой реакции. В каждом прививочном кабинете есть противошоковая укладка, а персонал готов оказать необходимую первую помощь. Если спустя 30 минут самочувствие остается нормальным, можно уходить из прививочного пункта⁵.
Ревакцинация
«Спутник Лайт» можно использовать как самостоятельную вакцину или при ревакцинации. Точных данных о том, какой вакциной лучше прививаться после его применения, пока нет. Известно только, что при неблагоприятной эпидемической ситуации ревакцинироваться после любой прививки лучше каждые полгода, даже несмотря на то, что сертификат о вакцинации действует в течение года.
Кто выпускает «Спутник Лайт»?
Вакцину разработали в ФГБУ «НИЦЭМ им. Н. Ф. Гамалеи». Это крупный научно-исследовательский центр, работающий в области микробиологии, иммунологии, эпидемиологии. Ранее центр уже создавал векторные вакцины. В частности, «ГамЭвак-Комби» — для профилактики лихорадки Эбола¹.
Заключение
«Спутник Лайт» часто называют «облегченной» версией вакцины «Гам-Ковид-Вак» и рекомендуют использовать для ревакцинации, а также после перенесенной болезни. Тем не менее, Минздрав разрешает применять «Спутник Лайт» и при первичной вакцинации. Выбирая его в качестве первой вакцины, важно учитывать, что уровень защиты от заражения коронавирусной инфекцией будет ниже, если сравнивать с двухкомпонентным «Спутником V».
Источники
- О «Спутник Лайт». НИЦЭМ им. Н. Ф. Гамалеи.
- Министерство здравоохранения Российской Федерации. Инструкция по медицинскому применению лекарственного препарата «Спутник Лайт». Векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS CoV-2.
- Министерство здравоохранения Российской Федерации. Михаил Мурашко: вакцина «Спутник Лайт» разрешена экспертами для применения у лиц старше 60 лет. 21.08.2021
- Комбинация «Спутник Лайт» с зарубежными вакцинами показала высокий профиль безопасности. Интерфакс. 04.08.2021
- Министерство здравоохранения Российской Федерации. Временные методические рекомендации. Порядок вакцинации взрослого населения против COVID-19.
- Amir I. Tukhvatulin, Inna V. Dolzhikova, Dmitry V. Shcheblyakov, Olga V. Zubkova, Alina S. Dzharullaeva, Anna V. Kovyrshina. An open, non-randomised, phase 1/2 trial on the safety, tolerability, and immunogenicity of single-dose vaccine «Sputnik Light» for prevention of coronavirus infection in healthy adults. The Lancet. 02.11.2021.
- Lapa D, Grousova DM, Matusali G, Meschi S, Colavita F, Bettini A, Gramigna G, Francalancia M, Garbuglia AR, Girardi E, Puro V, Antinori A, Kovyrshina AV, Dolzhikova IV, Shcheblyakov DV, Tukhvatulin AI, Zubkova OV, Logunov DY, Naroditsky BS, Vaia F, Gintsburg AL. Retention of Neutralizing response against SARS-CoV-2 Omicron variant in Sputnik V vaccinated individuals. MedRxiv. 2022 Jan 20. doi: https://doi.org/10.1101/2022.01.15.22269335
Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой SARS-CoV-2
Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой SARS-CoV-2 (Sputnik Light Vector vaccine for the prevention of coronavirus infection caused by the SARS-CoV-2 virus) инструкция по применению
📜 Инструкция по применению Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой SARS-CoV-2
💊 Состав препарата Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой SARS-CoV-2
✅ Применение препарата Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой SARS-CoV-2
📅 Условия хранения Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой SARS-CoV-2
⏳ Срок годности Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой SARS-CoV-2
Описание лекарственного препарата
Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой SARS-CoV-2
(Sputnik Light Vector vaccine for the prevention of coronavirus infection caused by the SARS-CoV-2 virus)
Основано на официально утвержденной инструкции по применению препарата и подготовлено для электронного издания справочника Видаль 2021 года, дата обновления: 2022.04.06
Владелец регистрационного удостоверения:
Код ATX:
J07BX03
(Вакцины против COVID-19)
Лекарственные формы
| Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2 |
Р-р д/в/м введения — 0.5 мл/1 доза (жидкий препарат): фл. 0.5 мл 1 шт. рег. №: ЛП-006993 |
|
|
Р-р д/в/м введения — 0.5 мл/1 доза (замороженный препарат): фл. 0.5 мл 1 шт. рег. №: ЛП-006993 |
||
|
Р-р д/в/м введения — 0.5 мл/1 доза (замороженный препарат): амп. 0.5 мл 5 шт. рег. №: ЛП-006993 |
||
|
Р-р д/в/м введения — 0.5 мл/1 доза (замороженный препарат): шприцы 0.5 мл 1 или 3 шт. рег. №: ЛП-006993 |
||
|
Р-р д/в/м введения — 0.5 мл/1 доза (замороженный препарат): фл. 3.0 мл 1 шт. рег. №: ЛП-006993 |
||
|
Р-р д/в/м введения — 0.5 мл/1 доза (замороженный препарат): амп. 0.5 мл 5 или 10 шт. рег. №: ЛП-006993 |
||
|
Р-р д/в/м введения — 0.5 мл/1 доза (замороженный препарат): амп. 1.0 мл 5 или 10 шт. рег. №: ЛП-006993 |
||
|
Р-р д/в/м введения — 0.5 мл/1 доза (замороженный препарат): фл. 3.0 мг 1 шт. рег. №: ЛП-006993 |
||
|
Р-р д/в/м введения — 0.5 мл/1 доза (замороженный препарат): фл. 0.5 мл 1, 2, 5 или 10 шт. рег. №: ЛП-006993 |
Раствор для в/м введения.
Замороженный препарат.
Раствор замороженный — плотная затвердевшая беловатого цвета масса. После размораживания — однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Вспомогательные вещества: трис(гидроксиметил)аминометан — 1.21 мг, натрия хлорид — 2.19 мг, сахароза — 25.0 мг, полисорбат 80 — 250.0 мкг, магния хлорида гексагидрат — 102.0 мкг, ЭДТА динатриевая соль дигидрат — 19.0 мкг, этанол 95% — 2.5 мкл, вода д/и — до 0.5 мл.
0.5 мл (1 доза) — флаконы (1) — пачки картонные.
0.5 мл (1 доза) — флаконы (1, 2, 5, 10) — пачки картонные.
0.5 мл (1 доза) — флаконы 6R (1) — пачки картонные с этикеткой самоклеящейся.
0.5 мл (1 доза) — флаконы 2R (1) — упаковки ячейковые контурные (1) — пачки картонные с этикеткой самоклеящейся.
3.0 мл (5 доз) — флаконы 6R (1) — пачки картонные с этикеткой самоклеящейся.
3.0 мл (5 доз) — флаконы 2R (1) — упаковки ячейковые контурные (1) — пачки картонные с этикеткой самоклеящейся.
3.0 мл (5 доз) — флаконы (1) — пачки картонные с держателем.
0.5 мл (1 доза) — шприцы одноразовые (1) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза) — шприцы одноразовые (3) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза) — ампулы бесцветного стекла с точкой излома (5) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (1) — пачки картонные.
0.5 мл (1 доза) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (2) — пачки картонные.
1.0 мл (2 дозы) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (1) — пачки картонные.
1.0 мл (2 дозы) — ампулы бесцветного стекла (5) — упаковки ячейковые контурные (2) — пачки картонные.
Раствор для в/м введения.
Жидкий препарат.
Однородный бесцветный или с желтоватым оттенком слегка опалесцирующий раствор.
Вспомогательные вещества: трис(гидроксиметил)аминометан — 1.21 мг, натрия хлорид — 2.19 мг, сахароза — 25.0 мг, полисорбат 80 — 250.0 мкг, магния хлорида гексагидрат — 102.0 мкг, ЭДТА динатриевая соль дигидрат — 19.0 мкг, этанол 95% — 2.5 мкл, вода д/и — до 0.5 мл.
0.5 мл (1 доза) — флаконы (1) — пачки картонные.
Фармакологическое действие
Характеристика. Вакцина получена биотехнологическим путем, при котором не используется патогенный для человека вирус SARS-CoV-2. В состав препарата входит рекомбинантный аденовирусный вектор на основе аденовируса человека 26 серотипа, несущий ген белка S — вируса SARS-CoV-2.
Вакцина индуцирует формирование гуморального и клеточного иммунитета в отношении коронавирусной инфекции, вызываемой вирусом SARS-CoV-2.
Иммунологическая эффективность
Иммунологические свойства и безопасность вакцины изучали в различных клинических исследованиях у взрослых добровольцев обоего пола в возрасте старше 18 лет.
Промежуточный анализ иммуногенности показал, что вакцина формирует иммунный ответ у добровольцев. На 28 день сероконверсия обнаружена у 96.88% здоровых добровольцев.
У лиц с предсуществующим иммунитетом к коронавирусу отмечен выраженный рост титра антител на 10 день после вакцинации, что может указывать на возможность применения препарата для вакцинации ранее переболевших COVID-19 после снижения титра антител с целью предотвращения повторных случаев заболевания. С учетом рекомендаций ВОЗ для достижения уровня коллективного иммунитета населения, следует проводить вакцинацию против новой коронавирусной инфекции COVID-19 но эпидемическим показаниям спустя 6 месяцев после перенесенного заболевания (в том числе у ранее вакцинированных лиц) или спустя 6 месяцев после предыдущей первичной вакцинации.
В результате однократной иммунизации 100% здоровых добровольцев (все 30 человек, у которых изучены показатели клеточного иммунитета) сформировали клеточный иммунный ответ против S белка SARS-CoV-2.
Защитный титр антител в настоящее время неизвестен. Продолжительность защиты неизвестна.
Показания препарата
Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой SARS-CoV-2
Профилактика новой коронавирусной инфекции (COVID-19) у взрослых старше 18 лет.
Режим дозирования
Вакцина предназначена только для внутримышечного введения. Строго запрещено внутривенное введение препарата. Вакцину вводят в дельтовидную мышцу (верхнюю треть наружной поверхности плеча). При невозможности введения в дельтовидную мышцу — препарат вводят в латеральную широкую мышцу бедра.
После введения вакцины пациент должен находиться под наблюдением медицинских работников в течение 30 минут.
Замороженный препарат
Перед вакцинированием флакон, ампулу или шприц с препаратом достают из морозильной камеры и выдерживают при комнатной температуре до полного размораживания. Остаток включений льда не допускается! Протирают флакон, ампулу или шприц снаружи салфеткой спиртовой для удаления влаги. Осторожно перемешивают содержимое покачиванием. Не допускается встряхивание флакона, ампулы или шприца! Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой. Вскрывают ампулу по кольцу и/или точке излома. Используя одноразовый шприц с иглой, отбирают дозу 0.5 мл для введения пациенту из ампулы или флакона.
Внимание! Доза, вводимая пациенту, не должна превышать 0.5 мл!
Препарат в шприцах готов к применению без дополнительных манипуляций.
Применение вакцины производства ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России (филиал «Медгамал» ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России) (флаконы) и АО «Биннофарм» (ампулы, шприцы)
Не допускается хранение размороженного препарата более 30 минут!
Повторное замораживание не допускается!
Применение вакцины производства АО «ГЕНЕРИУМ» (флаконы), ОАО «Фармстандарт — УфаВИТА» (флаконы, ампулы), ЗАО «ЛЕККО» (флаконы)
Внимание! Повторное замораживание флакона или ампулы с раствором не допускается! Суммарное время хранения размороженного раствора при комнатной температуре не должно превышать 2 часов. Неиспользованная вакцина подлежит уничтожению.
Многодозовые флаконы
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого или невскрытого флакона не более 2 часов при комнатной температуре.
Многодозовые ампулы
Содержимое ампулы рекомендуется использовать незамедлительно. Если последующие инъекции по какой-либо причине откладываются, допускается хранение вакцины при комнатной температуре: вскрытой ампулы, закрытой стерильной салфеткой, не более 1 часа, невскрытой ампулы — не более 2 часов.
ВНИМАНИЕ! Одна ампула содержит две дозы вакцины. Объем одной дозы составляет 0.5 мл. Одному пациенту вводить 1 дозу (0.5 мл).
Однодозовые ампулы
Содержимое ампулы рекомендуется использовать незамедлительно. Если последующие инъекции по какой-либо причине откладываются, допускается хранение невскрытой ампулы при комнатной температуре не более 2 часов.
Применение вакцины производства ЗАО «БИОКАД» (флаконы), АО «Р-Фарм» (флаконы), АО «Фармасинтез-Норд» (флаконы)
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого флакона по 3 мл не более 2 часов при комнатной температуре.
Не допускается хранение размороженного препарата во флаконах по 0.5 мл более 30 минут!
Повторное замораживание не допускается!
Жидкий препарат
Применение вакцины производства ООО «БиоИнтегратор» (флаконы)
Внимание! Замораживание флакона с раствором не допускается!
Флакон достают из холодильника и выдерживают при комнатной температуре, допускается слегка нагреть препарат, например, подержав его в руках. Не следует нагревать препарат выше 37°С.
Снимают защитную пластиковую накладку с флакона и обрабатывают резиновую пробку салфеткой спиртовой.
Используя одноразовый шприц с иглой, отбирают дозу 0.5 мл для введения пациенту.
Если последующие инъекции по какой-либо причине откладываются, допускается хранение вскрытого флакона или ампулы не более 2 часов при комнатной температуре.
Внимание! К использованию непригоден препарат (жидкий и/или замороженный) с дефектами укупорочной системы и/или нарушенной маркировкой флакона или ампулы, при изменении физических свойств раствора (мутность, окрашивание), неправильном хранении и/или с истекшим сроком годности.
Побочное действие
Нежелательные явления (НЯ), характерные для применения вакцины, выявленные в рамках клинических исследований, а также исследований других вакцин на основе аналогичной технологической платформы, бывают преимущественно легкой или средней степени выраженности, могут развиваться в первые-вторые сутки после вакцинации и разрешаются в течение 3-х последующих дней. Часто и очень часто могут развиться кратковременные общие (непродолжительный гриппоподобный синдром, характеризующийся ознобом, повышением температуры тела, артралгией, миалгией, астенией, общим недомоганием, головной болью) и местные (болезненность в месте инъекции, гиперемия, отечность) реакции. Рекомендуется назначение нестероидных противовоспалительных средств (НПВС) при повышении температуры после вакцинации и антигистаминных средств при выраженности местной реакции.
Нежелательные явления, представленные ниже, перечислены по системам организма и в соответствии с частотой встречаемости. Частота встречаемости определяется следующим образом: очень часто (≥1/10), часто (≥1/100 и < /10), нечасто (≥1/1000 и <1/100), редко (≥1/10000 и <1/1000), очень редко (<1/10000, включая отдельные случаи). Категории частоты были сформированы на основании клинических исследований препарата.
Часто отмечаются: тошнота, диспепсия, снижение аппетита; очень редко — увеличение регионарных лимфоузлов. У некоторых пациентов возможно развитие аллергических реакций, кратковременное повышение уровня печеночных трансаминаз, креатинина и креатинфосфокиназы в сыворотке крови
В рамках проведенных клинических исследований безопасности, переносимости и иммуногенности препарата Спутник Лайт после вакцинации были зарегистрированы следующие НЯ.
Общие нарушения и реакции в месте введения: очень часто и часто — гипертермия, боль, отек, зуд в месте вакцинации, астения, боль, недомогание, пирексия, повышение температуры кожи в месте вакцинации, снижение аппетита.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения: часто — боль в ротоглотке, заложенность носа, першение в горле, ринорея.
Нарушения со стороны нервной системы: часто — головная боль; редко — головокружение, обморок.
Желудочно-кишечные нарушения: часто — тошнота, рвота, диспепсия.
Лабораторные и инструментальные данные: разнонаправленные отклонения показателей иммунологического статуса — повышение числа Т-лимфоцитов, увеличение процентного содержания лимфоцитов, снижение числа естественных клеток-киллеров, увеличение количества CD4-лимфоцитов, снижение количества CD4-лимфоцитов, повышение числа В-лимфоцитов, снижение числа В-лимфоцитов, повышение числа естественных клеток-киллеров, повышение количества CD8-лимфоцитов, повышение уровня иммуноглобулина Е (IgE) в крови, увеличение соотношения CD4/CD8, уменьшение соотношения CD4/CD8, повышение уровня иммуноглобулина А (IgA) в крови, уменьшение процентного содержания лимфоцитов CD8. Отклонения в общем анализе крови — увеличение процентного содержания лимфоцитов, снижение показателя гематокрита, увеличение числа лимфоцитов, повышение скорости оседания эритроцитов, повышение числа лейкоцитов, повышение числа моноцитов, повышение числа тромбоцитов, снижение числа нейтрофилов, снижение числа тромбоцитов. Отклонения в общем анализе мочи — эритроциты в моче.
Большинство НЯ завершились выздоровлением без последствий. Лабораторные отклонения не имели клинического значения (вакцинированные не нуждались в проведении дополнительных диагностических процедур и назначения терапии).
Противопоказания к применению
- гиперчувствительность к какому-либо компоненту вакцины или вакцине, содержащей аналогичные компоненты;
- тяжелые аллергические реакции в анамнезе;
- острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний — вакцинацию проводят через 2-4 недели после выздоровления или ремиссии. При нетяжелых ОРВИ, острых инфекционных заболеваниях ЖКТ — вакцинацию проводят после нормализации температуры;
- беременность;
- период грудного вскармливания;
- возраст до 18 лет (в связи с отсутствием данных об эффективности и безопасности).
С осторожностью
Применять вакцину с осторожностью при хронических заболеваниях печени и почек, эндокринных заболеваниях (выраженных нарушениях функции щитовидной железы и
сахарном диабете в стадии декомпенсации), тяжелых заболеваниях системы кроветворения, эпилепсии и других заболеваниях ЦНС, остром коронарном синдроме и остром нарушении мозгового кровообращения, миокардитах, эндокардитах, перикардитах.
Вследствие недостатка информации вакцинация может представлять риск для следующих групп пациентов:
- с аутоиммунными заболеваниями (стимуляция иммунной системы может привести к обострению заболевания, особенно следует с осторожностью относиться к пациентам с аутоиммунной патологией, имеющей тенденцию к развитию тяжелых и жизнеугрожающих состояний);
- со злокачественными новообразованиями.
Категориям населения старше 60 лет, ранее не прошедшим иммунизацию от COVID-19, и не болевшим COVID-19, иммунокомпрометированным лицам независимо от возраста, для формирования иммунитета не рекомендовано применение препарата Спутник Лайт в связи со снижением функции иммунной системы, для формирования иммунного ответа показана вакцинация двухкомпонентной вакциной Гам-Ковид-Вак.
Принятие решения о вакцинации должно основываться на оценке соотношения пользы и риска в каждой конкретной ситуации.
Применение при беременности и кормлении грудью
Препарат противопоказан при беременности и в период грудного вскармливания, т.к. его эффективность и безопасность в этот период не изучались.
Применение при нарушениях функции печени
С осторожностью применять у пациентов с хроническими заболеваниями печени.
Применение при нарушениях функции почек
С осторожностью применять у пациентов с хроническими заболеваниями почек.
Применение у детей
Противопоказание: возраст до 18 лет (в связи с отсутствием данных об эффективности и безопасности.
Применение у пожилых пациентов
Категориям населения старше 60 лет, ранее не прошедшим иммунизацию от COVID-19, и не болевшим COVID-19, для формирования иммунитета не рекомендовано применение препарата Спутник Лайт в связи со снижением функции иммунной системы, для формирования иммунного ответа показана вакцинация двухкомпонентной вакциной Гам-Ковид-Вак.
Особые указания
У пациентов, получающих иммуносупрессивную терапию, и пациентов с иммунодефицитом может не развиться достаточный иммунный ответ. Поэтому прием препаратов, угнетающих функцию иммунной системы, противопоказан в течение, как минимум, 1 месяца до и после вакцинации из-за риска снижения иммуногенности.
Подобно остальным вакцинам, защитный иммунный ответ может возникать не у всех вакцинируемых лиц.
При принятии врачом (медицинским работником) решения о необходимости одновременного введения Спутник Лайт с другой вакциной, не допускается их смешивание в одном шприце и введение в один участок тела.
Влияние на способность к управлению транспортными средствами и механизмами
Исследования по изучению влияния вакцины на способность управлять транспортными средствами и потенциально опасными механизмами не проводились.
Передозировка
О случаях передозировки не сообщалось.
Учитывая, что отпуск лекарственного препарата допускается только для лечебно-профилактических учреждений, а сама вакцинация проводится только квалифицированным медицинским персоналом, риск передозировки крайне низок.
Однако можно предположить, что при случайной передозировке возможно развитие указанных выше токсических и токсико-аллергических реакций в более тяжелой степени.
Специфических антидотов к препарату не существует.
Терапевтические мероприятия в данном случае будут включать симптоматическую терапию в соответствии с показаниями (кортикостероиды, жаропонижающие/НПВС и десенсибилизирующие средства). Режим назначения препаратов должен быть выбран согласно рекомендациям по применению и дозировкам данного лекарственного средства.
Лекарственное взаимодействие
Специальных исследований лекарственного взаимодействия не проводилось.
Взаимодействие с вакциной для профилактики гриппа изучено в доклинических исследованиях, показано отсутствие снижения иммуногенности как вакцины Спутник Лайт (Векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2), так и гриппозной вакцины в эксперименте при их одновременном введении. Ожидается отсутствие снижения иммуногенности для расщепленных, субъединичных и полимерсубъединичных гриппозных вакцин.
Не допускается смешивание вакцины Спутник Лайт с другими вакцинами или иными лекарственными средствами в одном шприце, т.к. нет данных о фармацевтическом взаимодействии.
Условия хранения препарата Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой SARS-CoV-2
Условия хранения
Замороженный препарат
Хранить в защищенном от света месте, при температуре не выше минус 18°С. Повторное замораживание не допускается.
Хранить в недоступном для детей месте.
Жидкий препарат
Хранить в защищенном от света месте, при температуре от 2° до 8°С. Не замораживать.
Хранить в недоступном для детей месте.
Условия транспортирования
Замороженный препарат
Транспортирование препарата при температуре не выше минус 18°С.
Жидкий препарат
Транспортирование препарата при температуре от 2° до 8°С. Не замораживать.
Срок годности препарата Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой SARS-CoV-2
Срок годности
Замороженный препарат
6 месяцев. Не применять по истечении срока годности.
Жидкий препарат
1 месяц. Не применять по истечении срока годности.
Условия реализации
Для лечебно-профилактических учреждений.
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Обобщенные научные материалы по действующему веществу препарата Спутник Лайт Векторная вакцина для профилактики коронавирусной инфекции, вызываемой вирусом SARS-CoV-2 (раствор для внутримышечного введения, 0.5 мл/доза)
Дата последней актуализации: 30.03.2022
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Владелец РУ
- Условия хранения
- Срок годности
- Источники информации
- Фармакологическая группа
- Предупреждения
- Характеристика
- Фармакология
- Показания к применению
- Нозологическая классификация (МКБ-10)
- Противопоказания
- Ограничения к применению
- Применение при беременности и кормлении грудью
- Побочные действия
- Взаимодействие
- Передозировка
- Способ применения и дозы
- Меры предосторожности
- Отзывы
Действующее вещество
ATX
Владелец РУ
ГУ НИИЭМ им. Н.Ф. Гамалеи РАМН (филиал «Медгамал»)
Условия хранения
раствор для внутримышечного введения 0.5 мл/доза шприц —
В защищенном от света месте, при температуре не выше минус 18 °C (повторное замораживание не допускается) .
раствор для внутримышечного введения 0.5 мл/доза флакон —
В защищенном от света месте, при температуре 2–8 °C (не замораживать).
Условия транспортирования — В защищенном от света месте, при температуре 2–8 °C (не замораживать)
Хранить в недоступном для детей месте.
Срок годности
раствор для внутримышечного введения 0.5 мл/доза шприц — 6 мес.
раствор для внутримышечного введения 0.5 мл/доза ампула — 1 год — замороженный препарат; 6 мес — жидкий препарат .
раствор для внутримышечного введения 0.5 мл/доза флакон — 1 год.
раствор для внутримышечного введения 0.5 мл/доза флакон — 9 мес.
Не применять по истечении срока годности, указанного на упаковке.
Источники информации
www.grls.rosminzdrav.ru, 2021.
Фармакологическая группа
Предупреждения
Данная вакцина зарегистрирована по процедуре регистрации препаратов, предназначенных для применения в условиях угрозы возникновения, возникновения и ликвидации чрезвычайных ситуаций. Описание подготовлено на основании ограниченного объема клинических данных по применению вакцины и будет дополняться по мере поступления новых данных. Применение вакцины возможно только в условиях медицинских организаций, имеющих право осуществлять вакцинопрофилактику у населения в установленном законодательством порядке.
Характеристика
Вакцина получена биотехнологическим путем, при котором не используется патогенный для человека вирус SARS-CoV-2. Состоит из двух компонентов. В состав входит рекомбинантный аденовирусный вектор на основе аденовируса человека серотипа 26, несущий ген белка S вируса SARS-CoV-2.
Фармакология
Вакцина индуцирует формирование гуморального и клеточного иммунитета в отношении коронавирусной инфекции, вызываемой вирусом SARS-CoV-2.
Иммунологическая эффективность
Иммунологические свойства и безопасность вакцины изучали в различных клинических исследованиях у взрослых добровольцев обоего пола в возрасте старше 18 лет.
Промежуточный анализ иммуногенности показал, что вакцина формирует гуморальный иммунный ответ у добровольцев. На 28-й день сероконверсия обнаружена у 96,88% здоровых добровольцев.
У лиц с предсуществующим иммунитетом к коронавирусу отмечен выраженный рост титра антител на 10-й день после вакцинации, что может указывать на возможность применения для вакцинации ранее переболевших COVID-19 после снижения титра антител с целью предотвращения повторных случаев заболевания.
В результате однократной иммунизации 100% здоровых добровольцев (все 30 человек у которых изучены показатели клеточного иммунитета) сформировали клеточный иммунный ответ против S белка SARS-Co-2.
Защитный титр антител в настоящее время неизвестен. Продолжительность защиты неизвестна.
Показания к применению
Профилактика новой коронавирусной инфекции (COVID-19) у взрослых старше 18 лет.
Противопоказания
Гиперчувствительность к какому-либо компоненту вакцины или вакцине, содержащей аналогичные компоненты; тяжелые аллергические реакции в анамнезе; острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний (вакцинацию проводят через 2–4 нед после выздоровления или ремиссии. При нетяжелых ОРВИ, острых инфекционных заболеваниях ЖКТ вакцинацию проводят после нормализации температуры); возраст до 18 лет (в связи с отсутствием данных об эффективности и безопасности).
Ограничения к применению
Хронические заболевания печени и почек, эндокринные заболевания (выраженные нарушения функции щитовидной железы и сахарном диабете в стадии декомпенсации), тяжелые заболевания системы кроветворения, эпилепсия и другие заболевания ЦНС, острый коронарный синдром и острое нарушение мозгового кровообращения, миокардит, эндокардит, перикардит.
Вследствие недостатка информации вакцинация может представлять риск для следующих групп пациентов:
— с аутоиммунными заболеваниями (стимуляция иммунной системы может привести к обострению заболевания, особенно следует с осторожностью относиться к пациентам с аутоиммунной патологией, имеющей тенденцию к развитию тяжелых и жизнеугрожающих состояний);
— со злокачественными новообразованиями.
Принятие решения о вакцинации должно основываться на оценке соотношения польза/риск в каждой конкретной ситуации.
Применение при беременности и кормлении грудью
По результатам исследований а животных, репродуктивная токсичность и тератогенность отсутствуют. Клинические исследования вакцины при беременности не проводились. В связи с этим применять вакцину при беременности следует в тех случаях, когда ожидаемая польза для матери превышает потенциальный риск для плода с 22-й нед беременности.
Клинические данные по применению вакцины у женщин, кормящих грудью, и у младенцев отсутствуют. В настоящее время неизвестно, способны ли ДВ, входящие в состав вакцины, проникать в грудное молоко. Перед принятием решения о вакцинации кормящей женщины необходимо оценить риски и пользу данной вакцинации.
Побочные действия
Нежелательные явления, характерные для применения вакцины, выявленные в рамках клинических исследований, а также исследований других вакцин на основе аналогичной технологической платформы, бывают преимущественно легкой или средней степени выраженности, могут развиваться в первые-вторые сутки после вакцинации и разрешаются в течение 3-х последующих дней. Часто и очень часто могут развиться кратковременные общие (непродолжительный гриппоподобный синдром, характеризующийся ознобом, повышением температуры тела, артралгией, миалгией, астенией, общим недомоганием, головной болью) и местные (болезненность в месте инъекции, гиперемия, отечность) реакции. Рекомендуется назначение НПВС при повышении температуры после вакцинации и антигистаминных ЛС при выраженной местной реакции.
Нежелательные явления, представленные ниже, перечислены по системам организма и в соответствии с частотой встречаемости. Частота встречаемости определяется следующим образом: очень часто (≥1/10); часто (≥1/100, <1/10); нечасто (≥1/1000, <1/100); редко (≥1/10000, <1/1000); очень редко (<1/10000, включая отдельные случаи). Категории частоты были сформированы на основании клинических исследований вакцины.
Часто отмечаются тошнота, диспепсия, снижение аппетита, очень редко — увеличение регионарных лимфоузлов. У некоторых пациентов возможно развитие аллергических реакций, кратковременное повышение уровня печеночных трансаминаз, креатинина и КФК в сыворотке крови. В рамках проведенных клинических исследований безопасности, переносимости и иммуногенности после вакцинации были зарегистрированы следующие нежелательные явления.
Общие нарушения и реакции в месте введения: очень часто и часто — гипертермия, боль, отек, зуд в месте вакцинации, астения, боль, недомогание, пирексия, повышение температуры кожи в месте вакцинации, снижение аппетита.
Со стороны дыхательной системы, органов грудной клетки и средостения: часто — боль в ротоглотке, заложенность носа, першение в горле, ринорея.
Со стороны нервной системы: часто — головная боль, астения; редко — головокружение, обморок.
Со стороны ЖКТ: часто — тошнота, рвота, диспепсия.
Отклонения данных лабораторных и инструментальных исследований:
— разнонаправленные отклонения показателей иммунологического статуса такие как повышение числа Т-лимфоцитов, увеличение процентного содержания лимфоцитов, снижение числа естественных клеток-киллеров, увеличение количества СD4-лимфоцитов, снижение количества СD4-лимфоцитов, повышение числа B-лимфоцитов, снижение числа B-лимфоцитов, повышение числа естественных клеток-киллеров, повышение количества CD8-лимфоцитов, повышение уровня IgE в крови, увеличение соотношения CD4/CD8, уменьшение соотношения CD4/CD8, повышение уровня IgA в крови, уменьшение процентного содержания лимфоцитов CD8;
— отклонения в общем анализе крови — увеличение процентного содержания лимфоцитов, снижение показателя гематокрита, увеличение числа лимфоцитов, повышение СОЭ, повышение числа лейкоцитов, повышение числа моноцитов, повышение числа тромбоцитов, снижение числа нейтрофилов, снижение числа тромбоцитов;
— отклонения в общем анализе мочи — эритроциты в моче.
Большинство нежелательных явлений разрешалось без последствий. Лабораторные отклонения не имели клинического значения (не нуждались в проведении дополнительных диагностических процедур и назначении терапии).
Взаимодействие
Не изучалось.
Передозировка
О случаях передозировки не сообщалось. Учитывая, что вакцинация проводится только квалифицированным медицинским персоналом, риск передозировки крайне низок.
Симптомы: можно предположить, что при случайной передозировке возможно развитие указанных выше токсических и токсико-аллергических реакций в более тяжелой степени. Специфических антидотов к вакцине не существует.
Лечение: терапевтические мероприятия в данном случае будут включать симптоматическую терапию в соответствии с показаниями (ГКС, жаропонижающие/НПВС и десенсибилизирующие средства). Режим назначения ЛС должен быть выбран согласно рекомендациям по их применению и дозировкам.
Способ применения и дозы
В/м, в дельтовидную мышцу (верхняя треть наружной поверхности плеча). При невозможности введения в дельтовидную мышцу — в латеральную широкую мышцу бедра. После введения вакцины пациент должен находиться под наблюдением медицинских работников в течение 30 мин.
Строго запрещено в/в введение.
Меры предосторожности
У пациентов, получающих иммуносупрессивную терапию, и пациентов с иммунодефицитом может не развиться достаточный иммунный ответ. Поэтому прием ЛС, угнетающих функцию иммунной системы, противопоказан в течение, как минимум, 1 мес до и после вакцинации из-за риска снижения иммуногенности. Принять решение о возможности отмены иммуносупрессивной терапии может только лечащий врач.
Подобно остальным вакцинам, защитный иммунный ответ может возникать не у всех вакцинируемых лиц.
Влияние на способность управлять транспортными средствами, механизмами. Исследования по изучению влияния вакцины на способность управлять транспортными средствами и потенциально опасными механизмами не проводились.
«Спутник Лайт» — четвёртая российская вакцина от коронавируса SARS-CoV-2, зарегистрированная Минздравом РФ 6 мая 2021 года. Препарат разработан Национальным исследовательским центром эпидемиологии и микробиологии имени Гамалеи и рекомендован в качестве универсального бустера.
- Для людей, переболевших COVID-19;
- Для ревакцинации после прививки «Спутник V», AstraZeneca, Sinopharm, Moderna.
Что нужно знать о составе вакцины?
По составу «Спутник Лайт» — полная копия первого компонента векторной вакцины «Спутник V». Препарат содержит ген белка-шипа вируса SARS-CoV-2, который встроен в аденовирусный вектор, отвечающий за его доставку в клетки организма. Это рекомбинантный аденовирус человека 26 серотипа (rАd26).
Вакцина получена биотехнологическим путём. Потенциально опасный для человека коронавирус не используется в производстве и не может попасть в вакцину. Задействован только ген Spike-белка SARS-CoV-2, на который реагирует наш иммунитет.
Аденовирусный вектор — это безопасно?
Аденовирус 26 серотипа, который выполняет функцию вектора (то есть средства доставки) в составе вакцины «Спутник Лайт», не способен размножаться в организме и не может стать причиной инфекционного процесса.
Технология, когда для доставки генетического материала одного вируса используется оболочка другого (в данном случае, аденовируса), хорошо изучена. Например, она применялась при разработке вакцины от вируса Эбола.
Как проходит вакцинация?
В отличие от вакцины «Спутник V», «Спутник Лайт» вводится в один этап.
Инъекция вакцины может выполняться в дельтовидную мышцу плеча или в латеральную широкую мышцу бедра.
Что будет после вакцинации?
Задача вакцины — познакомить иммунную систему с антигеном SARS-CoV-2, чтобы сформировать механизмы защиты при контакте с реальным возбудителем COVID-19. Когда иммунитет реагирует на белок-шип вируса SARS-CoV-2, активируются все звенья иммунитета, в том числе выработка антител.
В первые-вторые сутки после вакцинации, когда S-белок презентуется клеткам иммунной системы, возможны кратковременные местные реакции и общее ощущение дискомфорта:
- повышение температуры тела (но не выше 38,5°) и озноб;
- болевые ощущения в мышцах и суставах;
- покраснение и болезненность в месте укола.
В норме эти явления проходят за 2-3 дня. По отзывам, большинство пациентов переносят вакцинацию препаратом «Спутник Лайт» легко, без серьёзного дискомфорта.
Эффективность вакцины «Спутник Лайт»
По данным, которые приводит НИЦЭМ им. Н. Ф. Гамалеи, «Спутник Лайт» продемонстрировал высокие результаты при прохождении I/II фазы исследования.
- Антиген-специфические антитела IgG вырабатываются у 96,9% привитых (спустя 28 дней после вакцинации).
- Вируснейтрализующие антитела вырабатываются у 91,67% привитых (спустя 28 дней после вакцинации).
- Клеточный иммунитет к спайковому белку коронавируса SARS-CoV-2 формируется у 100% привитых на 10 день после вакцинации.
- При иммунизации после перенесённого COVID-19 «Спутник Лайт» позволяет повысить уровень антиген-специфических антител IgG до 40 раз.
Есть ли противопоказания?
Желательно отложить вакцинацию в период обострения хронических заболеваний (оптимальный вариант — ремиссия в течение 1 месяца), при респираторных заболеваниях и повышении температуры до 37°.
Абсолютных противопоказаний немного — это тяжёлая аллергическая реакция (отёк Квинке, анафилактический шок) и гиперчувствительность к компонентам препарата.
Серьёзных побочных эффектов после вакцинации препаратом «Спутник Лайт» не выявлено.
Вакцина
«Спутник Лайт»
Разработчик
Национальный исследовательский центр эпидемиологии и микробиологии имени Гамалеи
Производители
- «Биннофарм»
- «Генериум»
- «Р-Фарм»
- «Биокад»
- Предприятия «Лекко»
- «Фармстандарт-Уфимский витаминный завод»
- «Центр им. Гамалеи»
Стадия
Регистрационное удостоверение №ЛП-006993.
Вакцина прошла 3 из 4 этапов испытаний, включая доклинические (на животных) и клинические. На данный момент «Спутник Лайт» находится на III фазе. НИЦЭМ им. Н.Ф. Гамалеи и РФПИ 21 февраля 2021 года запустили глобальное исследование эффективности «Спутник Лайт». Фаза III клинического исследования с участием 7 тыс. человек проходит в РФ, ОАЭ, Гане и других странах.
Основная информация
Из чего состоит вакцина?
Препарат является полной копией первого компонента «Спутник V», производится биотехнологическим путем, при котором не используется патогенный для человека вирус SARS-CoV-2.