Стелара® (Stelara®) инструкция по применению
📜 Инструкция по применению Стелара®
💊 Состав препарата Стелара®
✅ Применение препарата Стелара®
📅 Условия хранения Стелара®
⏳ Срок годности Стелара®
Описание лекарственного препарата
Стелара®
(Stelara®)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для электронного издания справочника Видаль 2022
года, дата обновления: 2021.12.16
Владелец регистрационного удостоверения:
Код ATX:
L04AC05
(Устекинумаб)
Лекарственные формы
| Стелара® |
Р-р д/п/к введения 45 мг/0.5 мл: шприцы 1 шт. рег. №: ЛП-001104 |
|
|
Р-р д/п/к введения 90 мг/1.0 мл: шприцы 1 шт. рег. №: ЛП-001104 |
Форма выпуска, упаковка и состав
препарата Стелара®
Раствор для п/к введения прозрачный или слегка опалесцирующий, от бесцветного до светло-желтого цвета; раствор может содержать единичные прозрачные частицы белка.
Вспомогательные вещества: сахароза — 38 мг, L-гистидин (в том числе L-гистидина гидрохлорида моногидрат) — 0.5 мг, полисорбат 80 — 0.02 мг, вода д/и — до 0.5 мл.
0.5 мл — шприцы из боросиликатного стекла (тип I) (1) с устройством UltraSafe Passive® — пачки картонные.
0.5 мл — шприцы из боросиликатного стекла (тип I) (1) с устройством UltraSafe Passive® — лотки пластиковые — пачки картонные.
Раствор для п/к введения прозрачный или слегка опалесцирующий, от бесцветного до светло-желтого цвета; раствор может содержать единичные прозрачные частицы белка.
Вспомогательные вещества: сахароза — 76 мг, L-гистидин (в том числе L-гистидина гидрохлорида моногидрат) — 1.0 мг, полисорбат 80 — 0.04 мг, вода д/и — до 1.0 мл.
1.0 мл — шприцы из боросиликатного стекла (тип I) (1) с устройством UltraSafe Passive® — пачки картонные.
1.0 мл — шприцы из боросиликатного стекла (тип I) (1) с устройством UltraSafe Passive® — лотки пластиковые — пачки картонные.
Фармакологическое действие
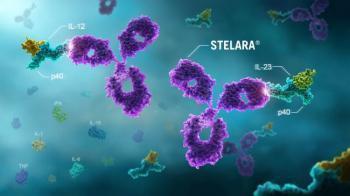
Устекинумаб представляет собой полностью человеческое моноклональное антитело IgG1?, которое специфично связывается с общей единицей белка p40 интерлейкинов (ИЛ) ИЛ-12 и ИЛ-23 человека. Препарат Стелара® ингибирует биоактивность ИЛ-12 и ИЛ-23 человека, предотвращая связывание p40 с рецептором ИЛ-12Rβ1, экспрессируемым на поверхности иммунных клеток. Препарат Стелара® не связывается с ИЛ-12 или ИЛ-23, которые уже связаны с рецепторами ИЛ-12Rβ1 на поверхности клеток. Таким образом, маловероятно, что препарат Стелара® будет способствовать опосредованной комплементом или антителами цитотоксичности в отношении клеток, экспрессирующих рецепторы к ИЛ-12 и/или ИЛ-23.
ИЛ-12 и ИЛ-23 представляют собой гетеродимерные цитокины, секретируемые активированными антигенпредставляющими клетками, например, макрофагами и дендритными клетками. ИЛ-12 стимулирует клетки-естественные киллеры (NK) и дифференцировку CD4+ T-клеток до фенотипа Т-хелпера-1 (Th1), а также стимулирует выработку интерферона гамма (ИФНγ). ИЛ-23 индуцирует путь Т-хелперов-17 (Th17) и способствует выработке ИЛ-17A, ИЛ-21, и ИЛ-22. У пациентов с псориазом определятся повышенные уровни ИЛ-12 и ИЛ-23 в коже и крови. Концентрация ИЛ12/23p40 в сыворотке крови является фактом дифференциации пациентов с псориатическим артритом, что подтверждает участие ИЛ-12 и ИЛ-23 в патогенезе псориатических воспалительных заболеваний. Полиморфизм генов, кодирующих ИЛ-23А, ИЛ-23R и ИЛ-12B, определяет предрасположенность к таким заболеваниям. Кроме того, высокий уровень экспрессии ИЛ-12 и ИЛ-23 обнаруживается в пораженной псориазом коже, а опосредованная ИЛ-12 индукция интерферона гамма коррелирует с активностью псориатического процесса. Чувствительные к ИЛ-23 Т-клетки были обнаружены в энтезах у мышей со смоделированным воспалительным артритом, где ИЛ-23 вызывал воспаление энтезов. Кроме того, имеются доклинические данные, свидетельствующие об участии ИЛ-23 и нисходящих путей в процессах эрозии и разрушения костной ткани посредством повышения экспрессии рецепторного активатора лиганда ядерного фактора κB (RANKL), который активирует остеокласты.
У пациентов с болезнью Крона отмечено повышение уровней ИЛ-12 и ИЛ-23 в кишечнике и лимфатических узлах. Это сопровождается увеличением уровней интерферона и ИЛ-17A в сыворотке, указывая, что ИЛ-12 и ИЛ-23 способствуют активации Th1 и Th17 при болезни Крона. Кроме того, как ИЛ-12, так и ИЛ-23 могут стимулировать выработку Т-клетками ФНО-α, что приводит к хроническому воспалению кишечника и повреждению эпителиальных клеток. Была обнаружена достоверная взаимосвязь между болезнью Крона и генетическим полиморфизмом генов ИЛ23R и ИЛ12B, что указывает на потенциальную причинную роль сигнальной системы ИЛ-12/23 в развитии заболевания. Это подтверждается доклиническими данными, свидетельствующими, что активация сигнального пути ИЛ-12/23 необходима для развития повреждения кишечника у мышей со смоделированным воспалительным поражением кишечника.
Связывая общую субъединицу p40 ИЛ-12 и ИЛ-23, препарат Стелара® может влиять на клиническое течение псориаза, псориатического артрита, болезни Крона и язвенного колита посредством прерывания пути выработки цитокинов Th1 и Th17, которые играют центральную роль в патогенезе этих заболеваний.
У пациентов с псориазом и/или псориатическим артритом при терапии препаратом Стелара® не отмечалось очевидного влияния на относительное количество популяций циркулирующих иммунных клеток, в том числе субпопуляции Т-клеток памяти и неактивированных Т-клеток, или уровни циркулирующих цитокинов.
В исследованиях, проведенных у пациентов с псориазом и псориатическим артритом, клинический ответ (улучшение оценок по PASI и ACR соответственно), по-видимому, был взаимосвязан с концентрацией устекинумаба в сыворотке. У пациентов с псориазом с лучшим клиническим ответом по шкале PASI средняя концентрация устекинумаба в сыворотке крови была выше, чем у пациентов с менее выраженным клиническим ответом. Доля пациентов, у которых на 28-ой неделе терапии был достигнут ответ PASI 75, увеличивалась по мере увеличения концентрации устекинумаба в сыворотке. Доля пациентов, у которых были достигнуты оценки ACR 20 и ACR 50, увеличивалась по мере увеличения концентрации устекинумаба в сыворотке крови.
У пациентов с болезнью Крона и язвенным колитом в результате терапии препаратом Стелара® отмечалось значимое снижение уровней маркеров воспаления, в том числе С-реактивного белка (CRP) и фекального кальпротектина. У пациентов, получавших препарат Стелара® в течение 44 недель, по сравнению с группой плацебо достигалось и сохранялось снижение в сыворотке крови концентраций ИФНγ и ИЛ-17А, являющихся провоспалительными цитокинами, регулируемыми ИЛ-12 и ИЛ-23.
Иммунизация
Во время долгосрочного клинического исследования III фазы (PHOENIX 2), у пациентов с псориазом, получавших препарат Стелара® в течение, по крайней мере, 3,5 лет, наблюдался иммунный ответ на полисахаридную пневмококковую и противостолбнячную вакцину, схожий с таковым в контрольной группе пациентов, получавших несистемную терапию псориаза. У примерно одинакового относительного числа (%) пациентов, получающих лечение препаратом Стелара®, и пациентов из контрольной группы достигалась защитная концентрация противопневмококковых и противостолбнячных антител.
Фармакокинетика
Всасывание
Медиана времени до достижения Cmax устекинумаба в сыворотке крови у здоровых лиц составила 8.5 дней после его однократного п/к введения в дозе 90 мг. Медианы показателя tmax устекинумаба после его однократного подкожного введения в дозе 45 мг или 90 мг у пациентов с псориазом были сравнимы с таковыми, отмечаемыми у здоровых добровольцев.
Абсолютная биодоступность устекинумаба после его однократного подкожного введения пациентам с псориазом составляет оценивается равной 57.2%.
Распределение
Среднее значение Vd устекинумаба у пациентов с псориазом в терминальной фазе выведения после однократного в/в введения составляла от 57 до 83 мл/кг.
По результатам популяционного фармакокинетического анализа Vd устекинумаба в равновесном состоянии составил 4.62 л у пациентов с болезнью Крона и 4,44 л у пациентов с язвенным колитом.
Метаболизм
Метаболический путь устекинумаба не известен.
Выведение
Медиана системного клиренса устекинумаба у пациентов с псориазом после однократного в/в введения составляла от 1.99 до 2.34 мл/сут/кг.
В ходе клинических исследований T1/2 устекинумаба у пациентов с болезнью Крона, псориазом и/или псориатическим артритом находился в диапазоне от 15 до 32 дней, а его медиана составила около 3 недель.
По результатам популяционного фармакокинетического анализа клиренс устекинумаба составил 0.19 л/сут, а T1/2 – около 19 дней у пациентов с болезнью Крона и язвенным колитом.
Линейность дозы
Системная экспозиция устекинумаба (Cmax и AUC) после однократного внутривенного введения в дозе от 0.09 мг/кг до 4.5 мг/кг или после однократного п/к введения в дозе от приблизительно 24 мг и до 240 мг у пациентов с псориазом возрастала примерно пропорционально введенной дозе.
Фармакокинетика после однократного и многократного введения
Профили изменения концентрации устекинумаба в плазме крови с течением времени после однократного или многократного п/к введения в целом были предсказуемы. Css устекинумаба в плазме крови у пациентов с псориазом достигалась к 28-ой неделе после первого п/к введения и на 0-й и 4-й неделях при последующих введениях каждые 12 недель. Медиана наименьших значений Css находилась в диапазоне от 0.21 мкг/мл до 0.26 мкг/мл (при введении в дозе 45 мг) и от 0.47 мкг/мл до 0.49 мкг/мл (при введении в дозе 90 мг).
После в/в введения рекомендованной инициирующей дозы медиана Cmax устекинумаба составила 126.1 мкг/мл у пациентов с болезнью Крона и 127.0 мкг/мл у пациентов с язвенным колитом Начиная с 8-ой недели, п/к введение поддерживающей дозы устекинумаба, составляющей 90 мг, проводилось каждые 8 или 12 недель. Css устекинумаба достигалась к моменту введения второй поддерживающей дозы. При п/к введении устекинумаба 1 раз каждые 8 или 12 недель не наблюдалось признаков кумуляции дозы с течением времени.
При п/к введении поддерживающей дозы 90 мг устекинумаба 1 раз каждые 8 недель медиана наименьших значений Css находилась в диапазоне от 1.97 мкг/мл до 2.24 мкг/мл у пациентов с болезнью Крона и в диапазоне от 2.69 мкг/мл до 3.09 мкг/мл у пациентов с язвенным колитом. При п/к введении поддерживающей дозы 90 мг устекинумаба 1 раз каждые 12 недель медиана наименьших значений Css находилась в диапазоне от 0.61 мкг/мл до 0.76 мкг/мл у пациентов с болезнью Крона и в диапазоне от 0.92 мкг/мл до 1.19 мкг/мл у пациентов с язвенным колитом. На фоне наименьших значений Css устекинумаба, достигавшихся при его введении в дозе 90 мг с частотой 1 раз каждые 8 недель, отмечались более высокие показатели клинической ремиссии, чем при наименьших значениях Css, достигавшихся после введения устекинумаба в дозе 90 мг с частотой 1 раз каждые 12 недель.
Определение частоты п/к введения
На основании полученных данных и популяционного фармакокинетического анализа отмечено, что у пациентов с болезнью Крона и язвенным колитом с потерей ответа на терапию наблюдается понижение концентрации устекинумаба в крови с течением времени по сравнению с пациентами с сохраненным ответом на терапию. При терапии болезни Крона изменение кратности подкожного введения дозы 90 мг с 1-го раза в 12 недель до 1-го раза в 8 недель вызывало повышение наименьших значений Css устекинумаба и сопровождалось повышением эффективности. При терапии язвенного колита симуляции на основании популяционной фармакокинетической модели показали, что при изменении кратности п/к введения дозы 90 мг с 1-го раза в 12 недель до 1-го раза в 8 недель ожидается троекратное увеличение наименьших значений Css устекинумаба. Кроме того на основании данных клинических исследований у пациентов с язвенным колитом отмечается прямая зависимость между наименьшими значениями Css устекинумаба в плазме крови и клиническим ответом на терапию, клинической ремиссией и заживлением слизистой оболочки кишечника.
Влияние массы тела на фармакокинетику
У пациентов с псориазом или псориатическим артритом концентрация устекинумаба в плазме крови изменялась в зависимости от массы тела. При применении в любой из доз (45 мг или 90 мг) у пациентов с более высокой массой тела (>100 кг) отмечалась более низкая медиана концентрации устекинумаба по сравнению с пациентами с более низкой массой тела (≤100 кг). Однако при сравнении разных доз медиана наименьших концентраций устекинумаба в плазме крови у пациентов с более высокой массой тела (>100 кг) при дозе 90 мг была сравнима с таковой у пациентов с более низкой массой тела (≤100 кг) при дозе 45 мг.
Популяционный фармакокинетический анализ
В ходе популяционного фармакокинетического анализа с использованием данных, полученных у пациентов с псориазом, кажущийся клиренс и кажущийся Vd составили 0.465 л/сут и 15.7 л соответственно, а T1/2 у пациентов с псориазом составил около 3-х недель. Кажущийся клиренс устекинумаба не зависел от пола, возраста или расы. Он зависел от массы тела, при этом отмечалась тенденция к более высоким показателям кажущегося клиренса у пациентов с более высокой массой тела. Медиана кажущегося клиренса у пациентов с массой тела >100 кг была приблизительно на 55% выше, чем у пациентов с массой тела ≤100 кг. Медиана кажущегося Vd у пациентов с массой тела >100 кг была приблизительно на 37% выше, чем у пациентов с массой тела ≤100 кг. Аналогичные результаты были получены и в результате подтверждающего популяционного фармакокинетического анализа, проводившегося по данным, полученным для пациентов с псориатическим артритом.
В ходе популяционного фармакокинетического анализа у пациентов с псориазом была проведена оценка влияния сопутствующих заболеваний (сахарный диабет, артериальная гипертензия и гиперлипидемия) на фармакокинетику устекинумаба. На нее оказывало влияние наличие сахарного диабета, при этом у пациентов с сахарным диабетом отмечалась тенденция к более высоким показателям кажущегося клиренса. Средние показатели кажущегося клиренса у пациентов с сахарным диабетом были приблизительно на 29% выше, чем у пациентов без сахарного диабета.
Популяционный фармакокинетический анализ установил наличие тенденции к более высоким показателям клиренса устекинумаба у пациентов с положительным иммунным ответом.
Специальных исследований лекарственных взаимодействий у здоровых лиц или у пациентов с псориазом, псориатическим артритом, болезнью Крона или язвенным колитом не проводилось.
В ходе популяционного фармакокинетического анализа было изучено влияние лекарственных препаратов, наиболее часто применяемых у пациентов с псориазом (в т.ч. парацетамола/ацетаминофена, ибупрофена, ацетилсалициловой кислоты, метформина, аторвастатина, напроксена, левотироксина, гидрохлортиазида и противогриппозной вакцины), на фармакокинетику устекинумаба. Было установлено, что ни один из этих препаратов не оказывает значимого влияния. Фармакокинетика устекинумаба не изменялась при одновременном применении с НПВС и в случае предшествующей терапии ингибиторами ФНО-α у пациентов с псориатическим артритом. Фармакокинетика устекинумаба не изменялась при одновременном применении с метотрексатом, пероральными ГКС, 6-меркаптопурином или азатиоприном у пациентов с болезнью Крона, а также в случае предшествующей терапии биологическими препаратами (например, ингибиторами ФНО-α и/или ведолизумабом) у пациентов с язвенным колитом.
Эффекты ИЛ-12 или ИЛ-23 в отношении регуляции активности изоферментов CYP450 были изучены в ходе исследования in vitro с применением гепатоцитов человека. В результате было установлено, что ИЛ-12 и/или ИЛ-23 при концентрации 10 нг/мл не влияют на активность изоферментов CYP450 (CYP1A2, 2B6, 2C9, 2C19, 2D6 или 3A4).
Особые группы пациентов
Дети (в возрасте от 6 до 18 лет). Фармакокинетика устекинумаба у детей в возрасте от 6 до 18 лет, с псориазом, получавших рекомендованную дозу, в целом была сравнима с фармакокинетикой у взрослых пациентов с псориазом.
Фармакокинетика устекинумаба у детей в возрасте до 18 лет с болезнью Крона или язвенным колитом не изучалась.
Пожилые пациенты (в возрасте от 65 лет и старше). Исследования фармакокинетики у пациентов пожилого возраста не проводилось. Популяционный фармакокинетический анализ среди пациентов старше 65 лет не выявил влияния возраста на величины кажущегося клиренса и Vd.
Пациенты с нарушением функции почек. Данные о фармакокинетике препарата у пациентов с нарушением функции почек отсутствуют.
Пациенты с нарушением функции печени. Данные о фармакокинетике препарата у пациентов с нарушением функции печени отсутствуют.
Другие группы пациентов. Фармакокинетика устекинумаба сравнима у пациентов азиатского происхождения и пациентов неазиатского происхождения с псориазом, болезнью Крона или язвенным колитом.
Употребление алкоголя или табака не влияло на фармакокинетику устекинумаба.
Показания препарата
Стелара®
- Бляшечный псориаз
Препарат Стелара® показан для лечения бляшечного псориаза средней или тяжелой степени у взрослых пациентов при отсутствии ответа или при наличии противопоказаний, или при непереносимости других методов системной терапии, в т.ч. циклоспорина, метотрексата или ПУВА-терапии (псорален и ультрафиолет А).
- Бляшечный псориаз у детей
Препарат Стелара® показан для лечения бляшечного псориаза средней или тяжелой степени у детей и подростков в возрасте от 6 лет и старше при отсутствии адекватного ответа или непереносимости других методов системной терапии или фототерапии.
- Псориатический артрит
Лечение взрослых пациентов с активным псориатическим артритом (ПсА) в качестве монотерапии или в комбинации с метотрексатом при отсутствии адекватного ответа на предыдущую стандартную терапию при отсутствии адекватного ответа на предыдущую стандартную терапию.
- Болезнь Крона
Лечение взрослых пациентов с активной болезнью Крона средней или тяжелой степени с неадекватным ответом, утратой ответа или непереносимостью стандартной терапии или терапии ингибиторами ФНО, или имеющих медицинские противопоказания к проведению такой терапии.
- Язвенный колит
Лечение взрослых пациентов с активным язвенным колитом умеренной и тяжелой степени с неадекватным ответом, утратой ответа или непереносимостью стандартной или биологической терапии, или имеющих медицинские противопоказания к проведению такой терапии.
Режим дозирования
Препарат Стелара® в лекарственной форме раствор для п/к введения предназначен для п/к инъекций.
Взрослые пациенты
Бляшечный псориаз
Рекомендованная доза составляет 45 мг. Вторую инъекцию делают 4 недели спустя после первого применения, затем каждые 12 недель.
У пациентов с массой тела более 100 кг препарат рекомендуется использовать в дозе 90 мг.
При неэффективности терапии в течение 28 недель рекомендуется рассмотреть целесообразность применения препарата.
Коррекция дозы
Пациентам, у которых клиническая эффективность препарата при применении каждые 12 недель выражена недостаточно, следует увеличить дозу препарата до 90 мг каждые 12 недель. В случае если такой режим дозирования не эффективен, дозу препарата 90 мг следует вводить каждые 8 недель.
Возобновление лечения
Было показано, что возобновление терапии по схеме: вторая инъекция через 4 недели спустя после первого применения, а затем каждые 12 недель, является эффективным и безопасным.
Псориатический артрит
Рекомендованная доза составляет 45 мг. Вторую инъекцию делают 4 недели спустя после первого применения, затем каждые 12 недель.
У пациентов с массой тела более 100 кг препарат рекомендуется использовать в дозе 90 мг.
Болезнь Крона и язвенный колит
Пациентам с болезнью Крона или язвенным колитом рекомендовано однократное, инициирующее терапию внутривенное введение препарата Стелара® в лекарственной форме концентрат для приготовления раствора для инфузий в дозе, рассчитанной на основании массы тела, с последующим п/к введением дозы 90 мг через 8 недель (первое п/к введение) и 1 раз каждые 12 недель в дальнейшем.
Подробная информация о в/в введении препарата Стелара® указана в инструкции по медицинскому применению препарата Стелара®, концентрат для приготовления раствора для инфузий.
Пациенты, у которых через 8 недель после первого п/к введения не удалось получить достаточный ответ, в это время могут получить вторую п/к инъекцию.
У пациентов с потерей ответа при введении 1 раз в 12 недель положительный результат может получен при увеличении частоты введений до 1-го раза в 8 недель.
В дальнейшем препарат пациентам можно вводить 1 раз в 8 недель или 1 раз в 12 недель, в зависимости от клинической ситуации.
Во время терапии препаратом Стелара®можно продолжать терапию иммуномодуляторами и/или ГКС. Пациентам, у которых удалось добиться ответа на терапию препаратом Стелара®, терапию ГКС можно сократить или отменить, в соответствии со стандартами терапии.
При прерывании терапии болезни Крона возобновление ее посредством подкожных инъекций каждые 8 недель является безопасным и эффективным.
Дети (6 лет и старше)
Бляшечный псориаз
Рекомендованная доза зависит от массы тела пациента, как показано в таблице 1. Вторую инъекцию делают 4 недели спустя после первого применения, затем каждые 12 недель.
Таблица 1. Рекомендованная доза препарата Стелара® у детей с бляшечным псориазом
* для расчета необходимого объема препарата (мл) для пациентов с массой тела менее 60 кг используется следующая формула: масса тела (кг) × 0,0083 (мл/кг).Рассчитанный объем препарата округляется до сотой доли мл (0,01 мл). Инъекция осуществляется градуированным шприцем вместимостью 1 мл. Для пациентов, которым необходима доза менее 45 мг, препарат Стелара® выпускается во флаконах с дозировкой 45 мг.
Таблица 2. Объем введения препарата Стелара® у детей с бляшечным псориазом с массой тела менее 60 кг
Детям препарат применяется в условиях стационара.
При неэффективности терапии в течение 28 недель рекомендуется рассмотреть целесообразность применения препарата.
Особые группы пациентов
Дети. Исследования препарата Стелара® у детей младше 6 лет не проводились.
Пожилые пациенты. В клинических исследованиях не наблюдалось существенных возрастных различий клиренса или объема распределения препарата. Количество пациентов в возрасте от 65 лет и старше было недостаточным для окончательного вывода о влиянии возраста на клиническую эффективность препарата.
Пациенты с нарушением функции почек. У пациентов с почечной недостаточностью не проводилось отдельных исследований препарата.
Пациенты с нарушением функции печени. У пациентов с печеночной недостаточностью не проводилось отдельных исследований препарата.
Указания по введению препарата
Препарат предназначен для п/к введения.
Перед введением препарата внимательно осмотрите содержимое шприца. Раствор может быть прозрачным или слегка опалесцирующим от бесцветного до светло-желтого цвета, может содержать единичные прозрачные частицы белка. Такой внешний вид является нормальным для белковых растворов. При изменении цвета, помутнении или наличии твердых частиц раствор использовать нельзя. Устекинумаб не содержит консервантов, поэтому любой неиспользованный остаток препарата в шприце использовать нельзя.
Препарат не следует смешивать с другими жидкостями для инъекции. Если для введения дозы 90 мг используют 2 шприца по 45 мг препарата, следует сделать 2 последовательные инъекции. При этом вторая инъекция должна быть сделана сразу же после первой. Инъекции следует делать в разные области. Не встряхивайте препарат. Длительное энергичное встряхивание может повредить препарат. Не используйте препарат, если его встряхивали. В начале лечения инъекции препарата Стелара® должен делать только медицинский персонал, однако, в последующем, если врач сочтет это возможным, пациенты или лица, осуществляющие уход за ними, или лица, осуществляющие уход за ними, могут делать инъекции препарата Стелара® самостоятельно, соблюдая все необходимые предосторожности и пройдя предварительно обязательное обучение технике подкожных инъекций, с последующим контролем врача. У детей в возрасте от 6 до 18 лет все инъекции должны проводиться медицинским персоналом.
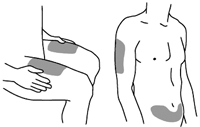
Рекомендованными местами для инъекции являются верхняя часть бедра или область живота примерно 5 см ниже пупка. Также можно использовать область плеча (см. 
Рис.1. Рекомендованные места для инъекции
Рис. 2. Шприц с препаратом Стелара®
Достаньте шприц с препаратом из картонной пачки, держа его в направлении иголкой от себя. Убедитесь, что шприц не поврежден. Тщательно вымойте руки и обработайте место инъекции ватным тампоном, смоченным антисептиком. Снимите защитный колпачок с иглы. Вы можете увидеть пузырек воздуха в шприце. Это допустимо, не пытайтесь удалить его. Вы также можете увидеть капельку жидкости на конце иглы. Это также допустимо.
Никогда не снимайте защитный колпачок, пока не определились с местом инъекции. Не допускайте контакта иголки с посторонними предметами.
Аккуратно зажмите кожу в области инъекции между большим и указательным пальцами, воткните иголку в кожу и медленно опустите поршень шприца до предела (Рис. 3).
Рис. 3.
После этого отпустите кожу и осторожно выньте иглу. Как только вы уберете палец с поршня, иголка автоматически скроется в корпусе шприца (Рис.4).
Рис. 4.
Приложите ватный тампон, смоченный антисептиком, к месту инъекции и подержите несколько секунд. Не трите место инъекции. При необходимости заклейте пластырем.
Использованный шприц необходимо утилизировать в соответствии с местными требованиями по уничтожению такого рода отходов. Повторное использование шприца и иглы запрещено.
Побочное действие
Побочные реакции — это нежелательные явления, которые были расценены как обоснованно связанные с использованием устекинумаба на основании всесторонней оценки имеющихся данных о нежелательных явлениях. В отдельных случаях не представляется возможным достоверно установить наличие причинной связи между нежелательным явлением и применением устекинумаба. Кроме того, поскольку клинические исследования проводятся в разных условиях, невозможно провести непосредственное сравнение частоты нежелательных реакций, наблюдаемых в клиническом исследовании препарата, с частотой, наблюдаемой в клинических исследованиях другого препарата, и частота нежелательного явления, наблюдаемая в клиническом исследовании, может не соответствовать частоте, наблюдаемой в клинической практике.
Опыт применения в клинических исследованиях у взрослых пациентов с псориазом, псориатическим артритом, болезнью Крона и язвенным колитом
Данные по безопасности, представленные далее, отражают применение препарата Стелара® в 14 исследованиях II фазы и III фазы, проведенных у 6709 пациентов (4135 пациентов с псориазом и/или псориатическим артритом, 1749 пациентов с болезнью Крона и 825 пациентов с язвенным колитом). Наиболее частыми (>5%) побочными действиями, наблюдавшимися в контролируемых периодах клинических исследований препаратом Стелара®, проведенных у пациентов по всем показаниям к применению, были назофарингит и головная боль. Большинство случаев были расценены как легкие и не требующие прекращения терапии. Общий профиль безопасности препарата Стелара® был схожим у пациентов по всем показаниям к применению.
В Таблице 3 представлен обзор побочных реакций, зарегистрированных в клинических исследованиях. Расчет частоты этих побочных реакций проводился на основании случаев, зарегистрированных во время начальных контролируемых периодов клинических исследований. Побочные реакции расположены в порядке уменьшения частоты, в соответствии со следующими категориями: очень часто (≥1/10), часто (≥1/100, <1/10), нечасто (≥1/1000, <1/100), редко (≥1/10000, <1/1000).
Таблица 3. Обзор побочных реакций, зарегистрированных в клинических исследованиях
Инфекции
В плацебо-контролируемых исследованиях частота инфекций или серьезных инфекций была сравнима у пациентов, получавших препарат Стелара®, и у пациентов, получавших плацебо. В плацебо-контролируемых периодах клинических исследований частота инфекций составляла 1.36 и 1.34 на пациенто-год наблюдения в группах, получавших препарат Стелара®, и плацебо соответственно.
В ходе контролируемых и неконтролируемых периодов клинических исследований, что составляет 11581 пациенто-лет терапии у 6709 пациентов, получавших препарат Стелара®, частота инфекций составляла 0.91 на пациенто-год наблюдения. Частота серьезных инфекций у пациентов, получавших препарат Стелара®, составляла 0.02 на пациенто-год наблюдения.
В клинических исследованиях у пациентов с латентным туберкулезом, одновременно получавших изониазид, не отмечалось случаев развития туберкулеза.
Злокачественные новообразования
В ходе плацебо-контролируемых периодов клинических исследований, проведенных у пациентов с псориазом, псориатическим артритом, болезнью Крона и язвенным колитом, частота возникновения злокачественных новообразований, без учета случаев немеланомного рака кожи, у пациентов, получавших препарат Стелара®, составляла 0.11 на 100 пациенто-лет наблюдения и 0.23 на 100 пациенто-лет наблюдения у пациентов, получавших плацебо.
Частота возникновения немеланомного рака кожи у пациентов, получавших препарат Стелара®, составляла 0.43 на 100 пациенто-лет наблюдения по сравнению с 0.46 на 100 пациенто-лет наблюдения у пациентов, получавших плацебо, в ходе контролируемых и неконтролируемых периодов клинических исследований, что составляет 11561 пациенто-лет терапии у 6709 пациентов.
Злокачественные новообразования, кроме случаев немеланомного рака кожи, были зарегистрированы с частотой 0.54 на 100 пациенто-лет наблюдения у пациентов, получавших препарат Стелара®. Частота случаев возникновения немеланомного рака кожи у пациентов, получавших препарат Стелара®, составила 0.49 на 100 пациенто-лет наблюдения (56 пациентов на 11545 пациенто-лет наблюдения).
Частота возникновения злокачественных новообразований у пациентов, получавших препарат Стелара®, была аналогична частоте, ожидаемой в общей популяции (стандартизованное отношение частоты = 0.93 [95% доверительный интервал: 0.71, 1.20], с учетом поправок на возраст, пол и расовую принадлежность)1.
Соотношение пациентов с базальноклеточным и плоскоклеточным типами рака (3:1) соответствовало соотношению, ожидаемому в общей популяции.
1 — База данных программы наблюдения, эпидемиологии и отслеживания исходов (SEER) (www.seer.cancer.gov) SEER*Srart Database: Incidence — SEER 6.6.2 Regs Research Data, подача — ноябрь 2009 (1973-2007) — в связи с характеристиками страны — США в целом, 1969-2007 Округи, Национальный институт онкологии, DCCPS, исследовательская программа наблюдения, группа наблюдательных систем, выпущено в апреле 2010, на основании подачи в ноябре 2009 года.
Реакции гиперчувствительности и инфузионные реакции
Подкожное введение. Во время контролируемых периодов клинических исследований препарата Стелара®, проведенных у пациентов с псориазом и псориатическим артритом, сыпь и крапивница наблюдались менее чем у 1% пациентов каждая
Внутривенное введение. В исследованиях индуцирующей терапии при болезни Крона и язвенном колите не было зарегистрировано случаев развития анафилактических или других серьезных инфузионных реакций. В исследованиях по показанию болезнь Крона побочные действия, развивавшиеся во время инфузии или в течение часа после инфузии, были зарегистрированы у 2.4% из 466 пациентов, получавших плацебо, и у 2.6% из 470 пациентов, получавших препарат Стелара в рекомендованной дозе. В исследованиях по показанию язвенный колиту 1.9% из 319 пациентов, получавших плацебо, и у 0.9% из 320 пациентов, получавших рекомендуемую дозу препарата Стелара, побочные реакции отмечались во время инфузии или в течение часа после инфузии.
Иммуногенность
В клинических исследованиях при псориазе и псориатическом артрите образование антител к устекинумабу было выявлено у 12,4% пациентов, получавших препарат Стелара®. У пациентов с положительными результатами тестов на антитела к устекинумабу отмечалась тенденция к более низкой эффективности, тем не менее, наличие антител не препятствовало развитию клинического ответа. У большинства пациентов с положительными результатами тестов на антитела присутствовали также и нейтрализующие их антитела.
В клинических исследованиях у пациентов с болезнью Крона и язвенным колитом образование антител к устекинумабу было выявлено соответственно у 2.9% и у 4.6% пациентов, получавших препарат Стелара® в течение около одного года. Не наблюдалось очевидной взаимосвязи между образованием антител к устекинумабу и развитием реакций в месте введения препарата.
Опыт применения в клинических исследованиях у детей с псориазом
Безопасность препарата Стелара® изучалась в двух исследованиях фазы 3 у детей с бляшечным псориазом от средней до тяжелой степени. Первое исследование включало 110 пациентов в возрасте от 12 до 18 лет, которые получали лечение в течение 60 недель (CADMUS), а второе – 44 пациента в возрасте от 6 до 12 лет, которые получали лечение в течение 56 недель (CADMUS Jr). В целом, зарегистрированные побочные действия были аналогичны наблюдавшимся в предшествующих исследованиях у взрослых пациентов с бляшечным псориазом
Опыт пострегистрационного применения
Побочные реакции в Таблице 4 расположены в порядке уменьшения частоты* с использованием следующих категорий:
очень часто (≥1/10), часто (≥1/100, <1/10), нечасто (≥1/1000, <1/100), редко (≥1/10000, <1/1000), в т.ч. отдельные сообщения.
Таблица 3. Пострегистрационные сообщения
* Расчет частоты побочных реакций, зарегистрированных при пострегистрационном периоде наблюдения, проводился на основании 11 плацебо-контролируемых клинических исследований, в случае, если такое побочное действие наблюдалось в этих исследованиях. В противном случае, считалось, что частота ниже определенного значения, учитывая объем применения в 11 клинических исследованиях, в которых это побочное действие не наблюдалось.
Противопоказания к применению
- повышенная чувствительность к устекинумабу или любому вспомогательному веществу препарата;
- детский возраст до 6 лет (по показанию «бляшечный псориаз»), до 18 лет (по показаниям «псориатический артрит», «болезнь Крона» и «язвенный колит»);
- беременность;
- период грудного вскармливания;
- серьезные инфекционные заболевания в острой фазе, в т.ч. туберкулез;
- злокачественные новообразования.
С осторожностью
- хронические или рецидивирующие паразитарные и инфекционные заболевания вирусной, грибковой или бактериальной природы;
- злокачественные опухоли в анамнезе;
- пожилой возраст (≥ 65 лет).
Применение при беременности и кормлении грудью
Способные к деторождению женщины
Женщины, способные к деторождению, должны использовать эффективные методы контрацепции во время терапии и в течение как минимум 15 недель после ее окончания.
Беременность
Данные о применении устекинумаба у беременных женщин являются недостаточными. В исследованиях у животных не обнаружено прямого или косвенного негативного влияния в отношении беременности, развития эмбриона/плода, родоразрешения и постнатального развития. В качестве меры предосторожности предпочтительно избегать применения препарата Стелара®во время беременности.
Период грудного вскармливания
Неизвестно выделяется ли устекинумаб с человеческим грудным молоком. В исследованиях у животных устекинумаб в небольшом количестве выделялся с грудным молоком. Неизвестно абсорбируется ли устекинумаб системно после введения. В связи с потенциальным риском возникновения нежелательных реакций устекинумаба у младенцев, находящихся на грудном вскармливании, решение о прекращении грудного вскармливания во время применения препарата и в течение 15 недель после завершения терапии или о прекращении применения препарата Стелара® должно быть принято на основании оценки пользы грудного вскармливания для ребенка и пользы терапии препаратом Стелара® для матери.
Фертильность
Оценка влияния препарата Стелара® на фертильность человека не проводилась
Применение при нарушениях функции печени
Данных о фармакокинетике препарата у пациентов с печеночной недостаточностью нет.
Изучение препарата у пациентов с печеночной недостаточностью не проводилось.
Применение при нарушениях функции почек
Данных о фармакокинетике препарата у пациентов с почечной недостаточностью нет.
Изучение препарата у пациентов с почечной недостаточностью не проводилось.
Применение у детей
Противопоказания: детский возраст до 6 лет — по показанию «бляшечный псориаз»; до 18 лет — по показаниям «псориатический артрит», «болезнь Крона» и «язвенный колит».
Применение у пожилых пациентов
С осторожностью следует применять у пациентов пожилого возраста.
Особые указания
Прослеживаемость
Для улучшения прослеживаемости биологических лекарственных препаратов необходимо записывать торговое наименование и номер серии введенного препарата.
Инфекции
Препарат Стелара® является селективным иммунодепрессантом, и потенциально может увеличивать риск возникновения инфекций и реактивации латентных инфекций.
В ходе клинических исследований у пациентов, получавших препарат Стелара®, наблюдались случаи возникновения серьезных бактериальных и вирусных инфекций.
Препарат Стелара® не следует применять у пациентов с клинически значимой активной инфекцией. Следует с осторожностью применять препарат Стелара® у пациентов с хронической инфекцией или рецидивирующей инфекцией в анамнезе.
Перед началом терапии препаратом Стелара® следует обследовать пациентов на наличие туберкулеза. Препарат Стелара® не следует применять у пациентов с активным туберкулезом. Перед применением препарата Стелара® следует провести терапию латентного туберкулеза. Кроме того, противотуберкулезную терапию перед началом применения препарата Стелара® следует провести пациентам с латентным или активным туберкулезом в анамнезе, для которых отсутствует подтверждение проведения эффективного курса лечения. У пациентов, получающих препарат Стелара®, во время и после терапии следует внимательно контролировать признаки или симптомы активного туберкулеза.
Пациентов следует проинструктировать о необходимости обращения за медицинской помощью в случае появления признаков или симптомов, указывающих на развитие инфекции. В случае, если у пациента развивается серьезная инфекция, необходимо проводить тщательное наблюдение пациента и не применять препарат Стелара® до разрешения инфекционного процесса.
Злокачественные новообразования
Препарат Стелара® является селективным иммунодепрессантом. Препараты-иммунодепрессанты могут способствовать увеличению риска развития злокачественных новообразований. У некоторых пациентов, получавших препарат Стелара® в рамках клинических исследований, наблюдалось развитие кожных и некожных злокачественных новообразований.
Применение препарата Стелара® не изучалось у пациентов со злокачественными новообразованиями в анамнезе. Следует проявлять осторожность при назначении препарата Стелара® пациентам со злокачественными новообразованиями в анамнезе, а также при рассмотрении возможности продолжения терапии препаратом Стелара® у пациентов с диагностированными злокачественными новообразованиями.
У всех пациентов, особенно у пациентов в возрасте старше 60 лет и у пациентов, ранее получавших длительную терапию иммунодепрессантами или ПУВА-терапию, необходимо проводить обследование на наличие немеланомного рака кожи.
Реакции гиперчувствительности
Системные реакции гиперчувствительности. В ходе пострегистрационного наблюдения были зарегистрированы серьезные реакции гиперчувствительности, в некоторых случаях через несколько дней после применения. Отмечалась анафилаксия и ангионевротический отек. В случае развития анафилактических или других серьезных реакций гиперчувствительности следует начать соответствующую терапию и прекратить применение препарата Стелара®.
Реакции гиперчувствительности со стороны органов дыхания. Случаи аллергического альвеолита, эозинофильной пневмонии и неинфекционной организующейся пневмонии отмечались в пострегистрационный период применения устекинумаба. Клинические проявления включали кашель, одышку и интерстициальные инфильтраты после применения от одной до трех доз препарата. Серьезные исходы включали дыхательную недостаточность и длительную госпитализацию. Улучшение состояния отмечалось после прекращения терапии устекинумабом, а также, в некоторых случаях, после применения глюкокортикостероидов. Если инфекция исключена и диагноз гиперчувствительности подтвержден, то необходимо прекратить применение устекинумаба и назначить соответствующую терапию.
Гиперчувствительность к латексу. Защитный колпачок для иглы содержит в своем составе натуральную резину (производное латекса) и при наличии гиперчувствительности к латексу может вызвать аллергические реакции.
Вакцинация
Не рекомендуется применять живые вирусные или живые бактериальные вакцины одновременно с препаратом Стелара®.
Данные о вторичном инфицировании при применении живых вакцин у пациентов, получающих препарат Стелара®, отсутствуют.
Следует соблюдать осторожность при применении живых вакцин для иммунизации членов семьи пациента, получающего лечение препаратом Стелара®, поскольку имеется риск вирусо- или бактериовыделения и передачи инфекции от этих лиц пациентам.
Пациентам, получающим препарат Стелара®, можно одновременно вводить инактивированные или неживые вакцины.
Длительное лечение препаратом Стелара® не подавляет гуморальный иммунный ответ на вакцины, содержащие пневмококковый полисахарид и противостолбнячную вакцину.
Сопутствующая иммуносупрессивная терапия
Безопасность и эффективность препарата Стелара® при применении в комбинации с иммунодепрессантами или фототерапией не изучалась в исследованиях у пациентов с псориазом.
В исследованиях у пациентов с псориатическим артритом одновременное применение метотрексата не влияло на безопасность и эффективность препарата Стелара®. В исследованиях у пациентов с болезнью Крона и язвенным колитом совместное применение препарата Стелара® с иммуномодуляторами (6-меркаптопурином, азатиоприном, метотрексатом) или с глюкокортикостероидами не влияло на безопасность и эффективность препарата Стелара®. Следует проявлять осторожность при рассмотрении возможности одновременного применения иммунодепрессантов и устекинумаба, а также при переходе с терапии другими биологическими препаратами на терапию устекинумабом.
Иммунотерапия
Безопасность и эффективность применения препарата Стелара® у пациентов, прошедших иммунотерапию аллергических заболеваний, не установлена. Препарат Стелара® может оказывать влияние на иммунотерапию аллергических заболеваний. Следует соблюдать осторожность при применении устекинумаба у пациентов, получающих или ранее получавших иммунотерапию аллергических заболеваний, особенно если такая терапия связана с анафилаксией.
Серьезные кожные реакции
У пациентов с псориазом отмечались случаи эксфолиативного дерматита после применения устекинумаба. У пациентов с бляшечным псориазом может развиваться эритродермический псориаз, являющий частью естественного течения заболевания, с симптомами, которые могут быть клинически неотличимы от эксфолиативного дерматита. При наблюдении пациентов с псориазом врачу необходимо проявлять настороженность в отношении симптомов эритродермического псориаза и эксфолиативного дерматита. При появлении таких симптомов необходимо назначить соответствующую терапию. Применение препарата Стелара®должно быть прекращено при подозрении на проявление данного побочного действия.
Особые группы пациентов
Пожилые пациенты (≥ 65 лет). В целом не наблюдалось различий между эффективностью и безопасностью препарата Стелара®при его применении у пациентов в возрасте от 65 и старше по сравнению с более молодыми пациентами в клинических исследованиях по одобренным показаниям. Однако количество пациентов в возрасте от 65 лет и старше было недостаточным для определения различий их ответа на терапию от более молодых пациентов. Так как в целом в популяции пожилых пациентов наблюдается более частое возникновение инфекций, то необходимо соблюдать осторожность при терапии таких пациентов.
Хранение
В случае необходимости шприцы можно однократно хранить при комнатной температуре не выше 30 °С, в оригинальной упаковке, в защищенном от света месте в течение не более 30 дней.
После хранения шприцев при комнатной температуре не выше 30 °С запрещается их хранение в холодильнике (при температуре от 2 °С до 8 °С).
Влияние на способность к управлению транспортными средствами и механизмами
Исследований не проводилось.
Передозировка
При однократных в/в введениях доз до 6 мг/кг в рамках клинических исследований не отмечалось токсичности, ограничивающей дозу.
Лечение: в случае передозировки рекомендуется наблюдать пациента на предмет любых признаков и проявлений нежелательных реакций с целью немедленного начала соответствующей симптоматической терапии.
Лекарственное взаимодействие
Исследования лекарственного взаимодействия с препаратом Стелара® у человека не проводились.
Эффекты ИЛ-12 или ИЛ-23 на регуляцию изоферментов CYP450 оценивались in vitro с использованием гепатоцитов человека. В исследовании было показано, что ИЛ-12 и/или ИЛ-23 в концентрации 10 нг/мл не влияют на активность изоферментов CYP450 человека (CYP1A2, 2В6, 2С9, 2С19, 2D6 или 3А4). Полученные результаты не предполагают необходимости коррекции дозы у пациентов, принимающих одновременно с препаратом Стелара® препараты, метаболизируемые изоферментами CYP450.
Живые вакцины не следует вводить одновременно с применением препарата Стелара®.
При совместном применении препарата Стелара® и таких препаратов, как парацетамол (ацетаминофен), ибупрофен, ацетилсалициловая кислота, метформин, аторвастатин, напроксен, левотироксин и гидрохлоротиазид взаимодействия не было выявлено.
Безопасность и эффективность совместного применения препарата Стелара® с другими иммунодепрессантами (метотрексат, циклоспорин) или биологическими препаратами для лечения псориаза не была оценена.
Условия хранения препарата Стелара®
Препарат следует хранить в недоступном для детей, защищенном от света месте, в оригинальной упаковке при температуре от 2° до 8°С. Не замораживать. Не встряхивать.
Срок годности препарата Стелара®
Срок годности — 3 года. Не использовать после истечения срока годности.
Условия реализации
Препарат отпускают по рецепту.
Контакты для обращений
ЯНССЕН, ФАРМАЦЕВТИЧЕСКОЕ ПОДРАЗДЕЛЕНИЕ ООО «ДЖОНСОН & ДЖОНСОН»

|
|
ЯНССЕН, 121614 Москва, ул. Крылатская, д. 17, корп. 2 |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Стелара — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер
ЛП-005728
Торговое наименование препарата
Стелара
Международное непатентованное наименование
Устекинумаб
Лекарственная форма
концентрат для приготовления раствора для инфузий
Состав
1 мл концентрата содержит:
действующее вещество: устекинумаб — 5,0 мг;
вспомогательные вещества: L-гистидин — 0,8 мг, L-гистидина гидрохлорида моногидрат — 1,1 мг, сахароза — 85 мг, полисорбат 80 — 0,40 мг, L-метионин — 0,40 мг, динатрия эдетата дигидрат — 0,02 мг, вода для инъекций — до 1,0 мл.
Описание
Прозрачная или почти прозрачная, бесцветная жидкость или жидкость с коричневатым или коричневато-желтоватым или желтоватым оттенком, которая может содержать незначительное количество небольших прозрачных или белых частиц белка.
Фармакотерапевтическая группа
Иммуносупрессоры, ингибиторы интерлейкина
Код АТХ
L04A
Фармакодинамика:
Механизм действия
Устекинумаб представляет собой полностью человеческое моноклональное антитело IgG1к, которое специфично связывается с общей единицей белка р40 интерлейкинов (ИЛ) ИЛ-12 и ИЛ-23 человека. Препарат Стелара ингибирует биоактивность ИЛ-12 и ИЛ-23 человека, предотвращая связывание р40 с рецептором ИЛ-12Rβ1, экспрессируемым на поверхности иммунных клеток. Препарат Стелара не связывается с ИЛ-12 или ИЛ-23, которые уже связаны с рецепторами ИЛ-12Rβ1 на поверхности клеток. Таким образом, маловероятно, что препарат Стелара будет способствовать опосредованной комплементом или антителами цитотоксичности в отношении клеток, экспрессирующих рецепторы к ИЛ-12 и/или ИЛ-23.
ИЛ-12 и ИЛ-23 представляют собой гетеродимерные цитокины, секретируемые активированными антигенпредставляющими клетками, например, макрофагами и дендритными клетками. ИЛ-12 стимулирует клетки-естественные киллеры (NK) и дифференцировку CD4+ Т-клеток до фенотипа Т-хелпера-1 (Тh1), а также стимулирует выработку интерферона гамма (ИФНγ). ИЛ-23 индуцирует путь Т-хелперов-17 (Тh17) и способствует выработке ИЛ-17А, ИЛ-21 и ИЛ-22.
У пациентов с болезнью Крона отмечено повышение уровней ИЛ-12 и ИЛ-23 в кишечнике и лимфатических узлах. Это сопровождается увеличением уровней интерферона и ИЛ-17А в сыворотке, указывая, что ИЛ-12 и ИЛ-23 способствуют активации Th1 и Тh17 при болезни Крона. Кроме того, как ИЛ-12, так и ИЛ-23 могут стимулировать выработку Т-клетками ФНО-α, что приводит к хроническому воспалению кишечника и повреждению эпителиальных клеток. Была обнаружена достоверная взаимосвязь между болезнью Крона и генетическим полиморфизмом генов ИЛ23R и ИЛ 2В, что указывает на потенциальную причинную роль сигнальной системы ИЛ-12/23 в развитии заболевания. Это подтверждается доклиническими данными, свидетельствующими, что активация сигнального пути ИЛ-12/23 необходима для развития повреждения кишечника у мышей со смоделированным воспалительным поражением кишечника. Связывая общую субъединицу р40 ИЛ-12 и ИЛ-23, препарат Стелара может влиять на клиническое течение болезни Крона посредством прерывания пути выработки цитокинов Тh1 и Тh17, которые играют центральную роль в патогенезе этих заболеваний.
У пациентов с болезнью Крона в результате терапии препаратом Стелара отмечалось значимое снижение уровней маркеров воспаления, в том числе С-реактивного белка (CRP) и фекального кальпротектина. У пациентов, получавших препарат Стелара в течение 44 недель, по сравнению с группой плацебо достигалось и сохранялось снижение в сыворотке крови концентраций ИФНγ и ИЛ-17А, являющихся провоспалительными цитокинами, регулируемыми ИЛ-12 и ИЛ-23.
Иммунизация
Во время долгосрочного клинического исследования у пациентов, получавших препарат Стелара в течение, по крайней мере, 3.5 лет, наблюдался иммунный ответ на полисахаридную пневмококковую и противостолбнячную вакцину, схожий с таковым в контрольной группе пациентов, получавших несистемную терапию. У примерно одинакового относительного числа (%) пациентов, получающих лечение препаратом Стелара, и пациентов из контрольной группы достигалась защитная концентрация противопневмококковых и противостолбнячных антител.
Фармакокинетика:
Всасывание
Медиана времени до достижения максимальной концентрации устекинумаба в сыворотке крови (tmax) у здоровых лиц составила 8,5 дней после его однократного подкожного введения в дозе 90 мг. Медианы показателя tmax устекинумаба после его однократного подкожного введения в дозе 45 мг или 90 мг у пациентов были сравнимы с таковыми, отмечаемыми у здоровых добровольцев. Абсолютная биодоступность устекинумаба после его однократного подкожного введения пациентам оценивается равной 57,2%.
Распределение
Среднее значение объема распределения устекинумаба у пациентов в терминальной фазе выведения (Vz) после однократного внутривенного введения составляла от 57 до 83 мл/кг.
Метаболизм
Метаболический путь устекинумаба не известен.
Выведение
Медиана системного клиренса (CL) устекинумаба у пациентов после однократного внутривенного введения составляла от 1,99 до 2,34 мл/сут/кг.
В ходе клинических исследований период полувыведения (Т1/2) устекинумаба у пациентов с болезнью Крона в диапазоне от 15 до 32 дней, а его медиана составила около 3-х недель.
Линейность дозы
Системная экспозиция устекинумаба (Сmах и AUC) после однократного внутривенного введения в дозе от 0,09 мг/кг до 4,5 мг/кг или после однократного подкожного введения в дозе от приблизительно 24 мг и до 240 мг у пациентов возрастала примерно пропорционально введенной дозе.
Фармакокинетика после однократного и многократного введения
У пациентов с болезнью Крона после внутривенного ведения в рекомендованной инициирующей дозе медиана максимальной концентрации устекинумаба составила 126,1 мкг/мл. Начиная с 8-ой недели, подкожное введение поддерживающей дозы устекинумаба. составляющей 90 мг, проводилось каждые 8 или 12 недель.
Равновесная концентрация устекинумаба достигалась к моменту введения второй поддерживающей дозы. Медиана наименьших равновесных концентраций устекинумаба при введении в дозе 90 мг каждые 8 или 12 недель находилась в диапазоне от 1,97 мкг/мл до 2,24 мкг/мл и от 0,61 мкг/мл до 0,76 мкг/мл соответственно. На фоне наименьших равновесных концентраций устекинумаба. достигавшихся при его введении в дозе 90 мг с частотой 1 раз каждые 8 недель, отмечались более высокие показатели клинической ремиссии, чем при наименьших равновесных концентрациях, достигавшихся после введения устекинумаба в дозе 90 мг с частотой 1 раз каждые 12 недель.
Влияние массы тела на фармакокинетику
Концентрация устекинумаба в плазме крови при подкожном введении изменялась в зависимости от массы тела. При применении в дозе 45 мг или 90 мг у пациентов с более высокой массой тела (>100 кг) отмечалась более низкая медиана концентрации устекинумаба по сравнению с пациентами с более низкой массой тела (<100 кг). Однако при сравнении разных доз медиана наименьших концентраций устекинумаба в плазме крови у пациентов с более высокой массой тела (>100 кг) при дозе 90 мг была сравнима с таковой у пациентов с более низкой массой тела (≤100 кг) при дозе 45 мг.
Популяционный фармакокинетический анализ
В ходе популяционного фармакокинетического анализа при подкожном введении кажущийся клиренс (CL/F) и кажущийся объем распределения (V/F) составили 0,465 л/сут и 15,7 л соответственно, а Т1/2 составил около 3-х недель. Кажущийся клиренс при подкожном введении устекинумаба не зависел от пола, возраста или расы. Он зависел от массы тела, при этом отмечалась тенденция к более высоким показателям кажущегося клиренса у пациентов с более высокой массой тела. Медиана кажущегося клиренса у пациентов с массой тела >100 кг была приблизительно на 55% выше, чем у пациентов с массой тела ≤100 кг. Медиана кажущегося объема распределения у пациентов с массой тела >100 кг была приблизительно на 37% выше, чем у пациентов с массой тела ≤100 кг.
В ходе популяционного фармакокинетического анализа была проведена оценка влияния сопутствующих заболеваний (сахарный диабет, артериальная гипертензия и гиперлипидемия) на фармакокинетику устекинумаба при подкожном введении. На нее оказывало влияние наличие сахарного диабета, при этом у пациентов с сахарным диабетом отмечалась тенденция к более высоким показателям кажущегося клиренса. Средние показатели кажущегося клиренса у пациентов с сахарным диабетом были приблизительно на 29% выше, чем у пациентов без сахарного диабета.
Популяционный фармакокинетический анализ установил наличие тенденции к более высоким показателям клиренса устекинумаба у пациентов с положительным иммунным ответом.
Специальных исследований лекарственных взаимодействий не проводилось.
В ходе популяционного фармакокинетического анализа было изучено влияние некоторых лекарственных препаратов (в том числе парацетамола/ ацетаминофена ибупрофена, ацетилсалициловой кислоты, метформина, аторвастатина, напроксена, левотироксина. гидрохлортиазида и противогриппозной вакцины) на фармакокинетику устекинумаба. Было установлено, что ни один их этих препаратов не оказывает значимого влияния. У пациентов с болезнью Крона фармакокинетика устекинумаба не изменялась при одновременном применении с метотрексатом, нестероидными противовоспалительными лекарственными средствами, пероральными кортикостероидами, 6-меркаптопурином, азатиоприном, или в результате предшествующего применения препаратов, блокирующих ФНО-α.
Эффекты ИЛ-12 или ИЛ-23 в отношении регуляции активности изоферментов CYP450 были изучены в ходе исследования in vitro с применением гепатоцитов человека. В результате было установлено, что ИЛ-12 и/или ИЛ-23 при концентрации 10 нг/мл не влияют на активность изоферментов CYP450 (CYP1А2, 2В6, 2С9, 2С19, 2D6 или 3А4).
Особые группы пациентов
Дети (в возрасте до 18 лет)
Фармакокинетика устекинумаба в лекарственной форме концентрат для приготовления раствора для инфузий у детей в возрасте до 18 лет не изучалась.
Пожилые пациенты (в возрасте от 65 лет и старше)
Исследования фармакокинетики у пациентов пожилого возраста не проводилось. Популяционный фармакокинетический анализ среди пациентов старше 65 лет не выявил влияния возраста на величины кажущегося клиренса (CL/F) и объема распределения (V/F).
Пациенты с нарушением функции почек
Данные о фармакокинетике препарата у пациентов с нарушением функции почек отсутствуют. Пациенты с нарушением функции печени
Данные о фармакокинетике препарата у пациентов с нарушением функции печени отсутствуют.
Другие группы пациентов
Фармакокинетика устекинумаба сравнима у пациентов азиатского происхождения и у пациентов неазиатского происхождения.
Употребление алкоголя или табака не влияло на фармакокинетику устекинумаба.
Показания:
Препарат Стелара в лекарственной форме концентрат для приготовления раствора для инфузий предназначен для терапии взрослых пациентов с болезнью Крона умеренной и тяжелой степени.
Препарат Стелара в лекарственной форме концентрат для приготовления раствора для инфузий предназначен для:
- индукции и поддержания клинического ответа
- индукции и поддержания клинической ремиссии
- достижения бесстероидной ремиссии
- индукции эндоскопической ремиссии
- улучшения связанного со здоровьем качества жизни
у взрослых пациентов с активной болезнью Крона умеренной и тяжелой степени, у которых:
- прогрессирование заболевания продолжалось на фоне терапии иммуномодуляторами или кортикостероидами, или была выявлена непереносимость этих препаратов, или
- наблюдалась зависимость от кортикостероидов, или
- прогрессирование заболевания продолжаюсь на фоне терапии одним или несколькими ингибиторами ФНO), или была выявлена непереносимость одного или нескольких ингибиторов ФHО.
Противопоказания:
— Клинически значимая повышенная чувствительность к устекинумабу или любому вспомогательному веществу препарата;
— клинически значимая активная инфекция (например, активный туберкулез);
— детский возраст до 18 лет.
Беременность и лактация:
Беременность
В исследованиях на животных не было получено доказательств тератогенности, врожденных дефектов или задержек развития при применении доз, примерно в 45 раз превышающих самую высокую эквивалентную дозу, предназначенную для применения у людей. Тем не менее, исследования влияния устекинумаба на репродуктивную функцию и на развитие потомства у животных не всегда прогнозируют реакции, развивающиеся у человека.
Неизвестно, может ли применение препарата Стелара нанести вред плоду при применении у беременных женщин или повлиять на репродуктивную функцию. Препарат Стелара следует применять у беременных женщин только в случае, если ожидаемая польза от применения у матери перевешивает потенциальный риск для плода.
Период грудного вскармливания
Выделение препарата Стелара с грудным молоком наблюдалось у обезьян. Неизвестно, абсорбируется ли препарат Стелара системно после приема внутрь. Поскольку многие препараты и иммуноглобулины выделяются с грудным молоком у человека и в связи с возможностью возникновения нежелательных явлений у детей, получающих грудное молоко, следует принять решение о прекращении грудного вскармливания в период приема препарата или об отмене терапии устекинумабом.
Фертильность
Оценка влияния препарата Стелара на фертильность человека не проводилась. В исследовании фертильности, проведенном у мышей, не было выявлено неблагоприятных эффектов в отношении фертильности самок.
Способ применения и дозы:
Болезнь Крона
Дозы
Пациентам с болезнью Крона рекомендовано однократное, инициирующее терапию внутривенное введение препарата Стелара в дозе, рассчитанной на основании массы тела (Таблица 1).
|
Таблица 1: Инициирующая доза препарата Стелара (внутривенное введение)а |
||
|
Масса тела пациента на момент введения препарата |
Доза |
Количество флаконов препарата Стелара, концентрат для приготовления раствора для инфузий, 130 мг |
|
< 55 кг |
260 мг |
2 |
|
> 55 кг-≤ 85 кг |
390 мг |
3 |
|
> 85 кг |
520 мг |
4 |
а Рекомендованная доза (около 6 мг/кг)
Через 8 недель после введения инициирующей дозы препарат Стелара вводится подкожно в дозе 90 мг (первое подкожное введение). Для подкожного введения используется препарат Стелара в лекарственной форме раствор для подкожного введения.
Информация о последующих подкожных введениях препарата указана в инструкции по медицинскому применению препарата Стелара, раствор для подкожного введения.
Особые группы пациентов
Дети
Исследования препарата Стелара в лекарственной форме концентрат для приготовления раствора для инфузий у детей младше 18 лет не проводились.
Пожилые пациенты
В клинических исследованиях не наблюдалось существенных возрастных различий клиренса или объема распределения препарата. Количество пациентов в возрасте от 65 лет и старше было недостаточным для окончательного вывода о влиянии возраста на клиническую эффективность препарата.
Пациенты с нарушением функции почек
У пациентов с почечной недостаточностью не проводилось отдельных исследований препарата.
Пациенты с нарушением функции печени
У пациентов с печеночной недостаточностью не проводилось отдельных исследований препарата.
Способ применения
Препарат Стелара, концентрат для приготовления раствора для инфузий, 130 мг, предназначен только для внутривенного инфузионного введения.
Внутривенное инфузионное введение препарата Стелара должно проводиться только квалифицированными медицинскими работниками.
Инструкции по приготовлению раствора, обращению с ним и его утилизации
Приготовление раствора препарата Стелара, концентрат для приготовления раствора для инфузий, 130 мг, должно производиться квалифицированными специалистами с соблюдением требований асептики, следующим образом:
1. Рассчитайте необходимую дозу и требуемое количество флаконов препарата Стелара на основании массы тела пациента (см. Таблицу 1). Каждый флакон препарата Стелара объемом 26 мл содержит 130 мг устекинумаба.
2. Из инфузионной емкости, содержащей 250 мл 0,9% раствора хлорида натрия, извлеките объем раствора, равный объему препарата Стелара, который необходимо ввести пациенту (на каждый флакон препарата Стелара необходимо извлечь из инфузионной емкости 26 мл раствора хлорида натрия, т.е. при необходимости введения двух флаконов требуется извлечь 52 мл, при введении трех флаконов — 78 мл, при введении четырех флаконов — 104 мл; извлеченный раствор утилизируется). При необходимости допускается использование инфузионных емкостей объемом 250 мл, содержащих 0,45% раствор хлорида натрия.
3. Из каждого флакона препарата Стелара извлеките 26 мл концентрата и введите его емкость с инфузионным раствором. Итоговый объем получившегося раствора препарата должен быть равен 250 мл. Осторожно перемешайте.
4. Перед введением внимательно осмотрите полученный раствор. При выявлении в растворе видимых непрозрачных частиц, изменении цвета или наличии инородных частиц использовать такой раствор запрещается.
5. Введите полученный раствор препарата пациенту путем внутривенной инфузии длительностью не менее одного часа. Раствор необходимо использовать в течение 8 часов после приготовления.
6. Используйте только инфузионные наборы со встроенным стерильным, апирогенным фильтром с низким связыванием белков (размер пор 0,2 микрометра).
7. Запрещается вводить препарат Стелара одновременно с другими препаратами через одну и ту же инфузионную систему.
8. Каждый флакон препарата Стелара предназначен только для одноразового использования и весь неиспользованный концентрат должен быть утилизирован в соответствии с действующими правилами.
Побочные эффекты:
В этом разделе представлены данные о побочных действиях. Побочные действия — это нежелательные явления, которые были расценены как обоснованно связанные с использованием устекинумаба на основании всесторонней оценки имеющихся данных о нежелательных явлениях.
В отдельных случаях не представляется возможным достоверно установить наличие причинной связи между нежелательным явлением и применением устекинумаба. Кроме того, поскольку клинические исследования проводятся в разных условиях, невозможно провести непосредственное сравнение частоты нежелательных реакций, наблюдаемых в клиническом исследовании препарата, с частотой, наблюдаемой в клинических исследованиях другого препарата, и частота нежелательного явления, наблюдаемая в клиническом исследовании, может не соответствовать частоте, наблюдаемой в клинической практике.
Опыт применения в клинических исследованиях у взрослых пациентов
Данные по безопасности, представленные далее, отражают применение препарата Стелара в 12 исследованиях 11 фазы и III фазы.
Наиболее частыми (>5%) побочными действиями, наблюдавшимися в контролируемых периодах клинических исследований препарата Стелара, были назофарингит и головная боль. Большинство случаев были расценены как легкие и не требующие прекращения терапии.
В Таблице 2 представлен обзор побочных действий, зарегистрированных в клинических исследованиях. Расчет частоты этих побочных действий проводился на основании случаев, зарегистрированных во время начальных контролируемых периодов клинических исследований.
Побочные действия расположены в порядке уменьшения частоты, в соответствии со следующими категориями:
Очень часто (≥1/10)
Часто (≥1/100, <1/10)
Нечасто (≥1/1000, <1/100)
Редко (≥1/10000, <1/1000)
|
Таблица 2: Обзор побочных действий, зарегистрированных в клинических исследованиях |
|
|
Инфекции и инвазии |
Часто: инфекции верхних дыхательных путей, назофарингит, синусит |
|
Нечасто: воспаление подкожной жировой клетчатки, одонтогенные инфекции, опоясывающий лишай, вирусные инфекции верхних дыхательных путей, вульвовагинальные грибковые инфекции |
|
|
Нарушения со стороны психики |
Нечасто: депрессия |
|
Нарушения со стороны нервной системы |
Часто: головокружение, головная боль |
|
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения |
Часто: орофарингеальная боль |
|
Нечасто: заложенность носа |
|
|
Нарушения со стороны желудочно-кишечного тракта |
Часто: диарея, тошнота, рвота |
|
Нарушения со стороны кожи и подкожной клетчатки |
Часто: зуд |
|
Нечасто: акне |
|
|
Нарушения со стороны опорно-двигательного аппарата и соединительной ткани |
Часто: боль в спине, миалгия, артралгия |
|
Общие нарушения и реакции в месте введения препарата |
Часто: усталость, эритема в месте введения, боль в месте введения |
|
Нечасто: реакции в месте введения (в том числе, кровотечение, гематома, уплотнение, припухлость и зуд), астения |
Инфекции
В плацебо-контролируемых исследованиях частота инфекций или серьезных инфекций была сравнима у пациентов, получавших препарат Стелара, и у пациентов, получавших плацебо. В плацебо-контролируемых периодах клинических исследований частота инфекций составляла 1,38 и 1,35 на пациенто-год наблюдения в группах, получавших препарат Стелара, и плацебо соответственно.
В ходе контролируемых и неконтролируемых периодов клинических исследований, что составляет 10953 пациенто-лет терапии у 5884 пациентов, получавших препарат Стелара, частота инфекций составляла 0,91 на пациенто-год наблюдения. Частота серьезных инфекций у пациентов, получавших препарат Стелара, составляла 0,02 на пациенто-год наблюдения.
В клинических исследованиях у пациентов с латентным туберкулезом, одновременно получавших изониазид, не отмечалось случаев развития туберкулеза.
Злокачественные новообразования
В ходе плацебо-контролируемых периодов клинических исследований частота возникновения злокачественных новообразований, без учета случаев немеланомного рака кожи, у пациентов, получавших препарат Стелара, составляла 0,12 на 100 пациенто-лет наблюдения и 0,26 на 100 пациенто-лет наблюдения у пациентов, получавших плацебо.
Частота возникновения немеланомного рака кожи у пациентов, получавших препарат Стелара. составляла 0,48 на 100 пациенто-лет наблюдения и 0,52 на 100 пациенто-лет наблюдения у пациентов, получавших плацебо, в ходе контролируемых и неконтролируемых периодов клинических исследований, что составляет 10935 пациенто-лет терапии у 5884 пациентов. Злокачественные новообразования, кроме случаев немеланомного рака кожи, были зарегистрированы с частотой 0,53 на 100 пациенто-лет наблюдения у пациентов, получавших препарат Стелара. Частота случаев возникновения немеланомного рака кожи у пациентов, получавших препарат Стелара, составила 0,49 на 100 пациенто-лет наблюдения (53 пациента на 10919 пациенто-лет наблюдения).
Частота возникновения злокачественных новообразований у пациентов, получавших препарат Стелара®, была аналогична частоте, ожидаемой в общей популяции (стандартизованное отношение частоты = 0,87 [95% доверительный интервал: 0,66, 1,14], с учетом поправок на возраст, пол и расовую принадлежность)1.
Соотношение пациентов с базальноклеточным и плоскоклеточным типами рака (4:1) соответствовало соотношению, ожидаемому в общей популяции.
1 — Ваза данных программы наблюдения, эпидемиологии и отслеживания исходов (SEER) (wwvv.seer.cancer.gov) SEER*Stat Database: Incidence — SEER 6.6.2 Regs Research Data подача — ноябрь 2009 (1973-2007) — в связи с характеристиками страны — США в целом, 1969-2007 Округи, Национальный институт онкологии, DCCPS, исследовательская программа наблюдения, группа наблюдательных систем, выпущено в апреле 2010, на основании подачи в ноябре 2009 года.
Реакции гиперчувствительности и инфузионные реакции
Подкожное введение
Во время контролируемых периодов клинических исследований препарата Стелара сыпь и крапивница наблюдались менее чем у 1% пациентов каждая.
Внутривенное введение
В исследованиях индуцирующей терапии при болезни Крона не было зарегистрировано случаев развития анафилактических или других серьезных инфузионных реакций. В этих исследованиях побочные действия, развивавшиеся во время инфузии или в течение часа после инфузии, были зарегистрированы у 2,4% из 466 пациентов, получавших плацебо, и у 2,6% из 470 пациентов, получавших препарат Стелара в рекомендованной дозе.
Иммуногенность
В клинических исследованиях у пациентов с болезнью Крона образование антител к устекинумабу было выявлено менее чем у 3% пациентов, получавших препарат Стелара. Не наблюдалось очевидной взаимосвязи между образованием антител к устекинумабу и развитием реакций в месте введения препарата. У пациентов с положительными результатами тестов на антитела к устекинумабу отмечалась тенденция к более низкой эффективности, тем не менее, наличие антител не препятствовало развитию клинического ответа. У большинства пациентов с положительными результатами тестов на антитела присутствовали также и нейтрализующие их антитела.
Опыт пострегистрационного применения
Побочные действия в Таблице 3 расположены в порядке уменьшения частоты* с использованием следующих категорий:
Очень часто: ≥1/10
Часто: ≥1/100 и <1/10
Нечасто: ≥1/1000 и <1/100
Редко: ≥1/10000 и <1/1000
Очень редко: <1/10000, в том числе отдельные
|
Таблица 3: Пострегистрационные сообщения |
|
|
Нарушения со стороны иммунной системы |
Нечасто: реакции гиперчувствительности (в том числе сыпь, крапивница) |
|
Редко: серьезные реакции гиперчувствительности (в том числе анафилаксия и ангионевротический отек) |
|
|
Инфекции и инвазии |
Нечасто: инфекции нижних отделовдыхательных путей |
|
Нарушения со стороны кожи и подкожной клетчатки |
Нечасто: пустулёзный псориаз |
|
Редко: эритродермический псориаз |
* Расчет частоты побочных действий, зарегистрированных при пострегистрационном периоде наблюдения, проводился на основании 11-ти плацебо-контролируемых клинических исследований, в случае, если такое побочное действие наблюдалось в этих исследованиях. В противном случае, считалось, что частота ниже определенного значения, учитывая объем применения в 11-ти клинических исследованиях, в которых это побочное действие не наблюдалось.
Передозировка:
При однократных внутривенных введениях доз до 6 мг/кг в рамках клинических исследований не отмечалось токсичности, ограничивающей дозу. В случае передозировки рекомендуется наблюдать пациента на предмет любых признаков и проявлений нежелательных реакций с целью немедленного начала соответствующей симптоматической терапии.
Взаимодействие:
Исследования лекарственных взаимодействий с препаратом Стеларау человека не проводились. Эффекты ИЛ-12 или ИЛ-23 на регуляцию изоферментов CYP450 оценивались in vitro с использованием гепатоцитов человека. В исследовании было показано, что ИЛ-12 и/или ИЛ-23 в концентрации 10 нг/мл не влияют на активность изоферментов CYP450 человека (CYP1А2, 2В6, 2С9, 2С19, 2D6 или 3А4). Полученные результаты не предполагают необходимости коррекции дозы у пациентов, принимающих одновременно с препаратом Стелара препараты, метаболизируемые изоферментами CYP450.
Живые вакцины не следует вводить одновременно с применением препарата Стелара.
Особые указания:
Инфекции
Препарат Стелара является селективным иммунодепрессантом, и потенциально может увеличивать риск возникновения инфекций и реактивации латентных инфекций.
В ходе клинических исследований у пациентов, получавших препарат Стелара, наблюдались случаи возникновения серьезных бактериальных и вирусных инфекций.
Препарат Стелара не следует применять у пациентов с клинически значимой активной инфекцией. Следует с осторожностью применять препарат Стелара у пациентов с хронической инфекцией или рецидивирующей инфекцией в анамнезе.
Перед началом терапии препаратом Стелара следует обследовать пациентов на наличие туберкулеза. Препарат Стелара не следует применять у пациентов с активным туберкулезом. Перед применением препарата Стелара следует провести терапию латентного туберкулеза. Кроме того, противотуберкулезную терапию перед началом применения препарата Стелара следует провести пациентам с латентным или активным туберкулезом в анамнезе, для которых отсутствует подтверждение проведения эффективного курса лечения. У пациентов, получающих препарат Стелара, во время и после терапии следует внимательно контролировать признаки или симптомы активного туберкулеза.
Пациентов следует проинструктировать о необходимости обращения за медицинской помощью в случае появления признаков или симптомов, указывающих на развитие инфекции. В случае, если у пациента развивается серьезная инфекция, необходимо проводить тщательное наблюдение пациента и не применять препарат Стелара до разрешения инфекционного процесса.
Злокачественные новообразования
Препарат Стелара является селективным иммунодепрессантом. Препараты-иммунодепрессанты могут способствовать увеличению риска развития злокачественных новообразований. У некоторых пациентов, получавших препарат Стелара в рамках клинических исследований, наблюдалось развитие кожных и некожных злокачественных новообразований.
Применение препарата Стелара не изучалось у пациентов со злокачественными новообразованиями в анамнезе. Следует проявлять осторожность при назначении препарата Стелара пациентам со злокачественными новообразованиями в анамнезе, а также при рассмотрении возможности продолжения терапии препаратом Стелара у пациентов с диагностированными злокачественными новообразованиями.
У всех пациентов, особенно у пациентов в возрасте старше 60 лет и у пациентов, ранее получавших длительную терапию иммунодепрессантами или ПУВА-терапию, необходимо проводить обследование на наличие немеланомного рака кожи.
Реакции гиперчувствительности
В ходе пострегистрационного наблюдения были зарегистрированы серьезные реакции гиперчувствительности, включая анафилаксию и ангионевротический отек. В случае развития анафилактических или других серьезных реакций гиперчувствительности следует начать соответствующую терапию и прекратить применение препарата Стелара.
Вакцинация
Не рекомендуется применять живые вирусные или живые бактериальные вакцины одновременно с препаратом Стелара.
Данные о вторичном инфицировании при применении живых вакцин у пациентов, получающих препарат Стелара, отсутствуют.
Следует соблюдать осторожность при применении живых вакцин для иммунизации членов семьи пациента, получающего лечение препаратом Стелара. поскольку имеется риск вирусо- или бактериовыделения и передачи инфекции от этих лиц пациентам.
Пациентам, получающим препарат Стелара, можно одновременно вводить инактивированные или неживые вакцины.
Длительное лечение препаратом Стелара не подавляет гуморальный иммунный ответ на вакцины, содержащие пневмококковый полисахарид и противостолбнячную вакцину.
Иммуносупрессия
В исследованиях у пациентов с болезнью Крона совместное применение препарата Стелара с иммуномодуляторами (6-меркаптопурином, азатиоприном, метотрексатом) или с кортикостероидами не влияло на безопасность и эффективность препарата Стелара. Следует проявлять осторожность при рассмотрении возможности одновременного применения иммунодепрессантов и устекинумаба, а также при переходе с терапии другими биологическими препаратами на терапию устекинумабом.
Иммунотерапия
Безопасность и эффективность применения препарата Стелара у пациентов, прошедших иммунотерапию аллергических заболеваний, не установлена. Препарат Стелара может оказывать влияние на иммунотерапию аллергических заболеваний. Следует соблюдать осторожностью при применении устекинумаба у пациентов, получающих или ранее получавших иммунотерапию аллергических заболеваний, особенно если такая терапия связана с анафилаксией.
Влияние на способность управлять транспортными средствами и механизмами:
Исследований не проводилось.
Форма выпуска/дозировка:
Концентрат для приготовления раствора для инфузий, 5 мг/мл.
Упаковка:
По 26 мл концентрата во флаконе из стекла I типа, укупоренном пробкой из бутилового каучука и алюминиевым колпачком с защитным диском из пластмассы.
По 1 флакону вместе с инструкцией по применению в пачке картонной.
Условия хранения:
При температуре от 2 до 8 °С, в защищенном от света месте.
Не замораживать. Не встряхивать. После приготовления раствор можно хранить при комнатной температуре не более 4 ч.
Хранить в недоступном для детей месте.
Срок годности:
3 года.
Не применять по истечении срока годности.
Условия отпуска
По рецепту
Производитель
Силаг АГ, Hochstrasse 201, 8200 Schaffhausen, Switzerland, Швейцария
Владелец регистрационного удостоверения/организация, принимающая претензии потребителей:
ООО «Джонсон & Джонсон»
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
П/к, пациентам старше 18 лет.
Рекомендованная доза — 45 мг. Вторую инъекцию делают 4 нед спустя после первого применения, затем каждые 12 нед.
У пациентов с массой тела более 100 кг препарат рекомендуется использовать в дозе 90 мг.
При неэффективности терапии в течение 28 нед рекомендуется рассмотреть целесообразность применения препарата.
Коррекция дозы. Пациентам, у которых клиническая эффективность препарата при применении каждые 12 нед выражена недостаточно, следует увеличивать дозу препарата до 90 мг каждые 12 нед. В случае, если такой режим дозирования не эффективен, дозу препарата 90 мг следует вводить каждые 8 нед.
Возобновление лечения. Возобновление лечения по предложенной схеме — вторая инъекция через 4 нед спустя после первого применения, а затем каждые 12 нед — было так же эффективно, как и впервые проводимая терапия.
Применение у пожилых больных (старше 65 лет). В ходе клинических исследований не было выявлено влияния возраста на клиренс или Vd препарата. В ходе исследований препарата не было выявлено различий в безопасности и эффективности препарата для пожилых пациентов старше 65 лет по сравнению с более молодыми пациентами.
Применение у детей. Безопасность и эффективность устекинумаба у детей не изучалась.
Применение при почечной и печеночной недостаточности. Изучение препарата у пациентов с почечной или печеночной недостаточностью не проводилось.
Указания по введению препарата
Перед введением препарата внимательно осмотреть содержимое шприца или флакона. Раствор может быть прозрачным или слегка опалесцирующим от бесцветного до светло-желтого цвета, может содержать единичные прозрачные частицы белка. При изменении цвета, помутнении или наличии твердых частиц раствор использовать нельзя. Устекинумаб не содержит консервантов, поэтому любой неиспользованный остаток препарата в шприце или флаконе использовать нельзя.
Препарат не смешивать с другими жидкостями для инъекции. Если для введения дозы 90 мг используют 2 шприца или флакона по 45 мг препарата, следует сделать 2 последовательные инъекции. При этом вторая инъекция должна быть сделана сразу же после первой. Инъекции делать в разные области.
Не встряхивать препарат. Длительное энергичное встряхивание может повредить препарат. Не использовать препарат, если его встряхивали.
В начале лечения инъекции препарата Стелара® должен делать только медицинский персонал, однако в последующем, если врач сочтет это возможным, пациент может делать себе инъекции препарата Стелара® самостоятельно, соблюдая все необходимые предосторожности и пройдя предварительно обязательное обучение технике п/к инъекций, с последующим контролем врача.
Рекомендованными местами для инъекции являются верхняя часть бедра или область живота (примерно 5 см ниже пупка). Также можно использовать область плеча. Следует избегать инъекций в область, пораженную псориазом.

— Для раствора для п/к введения во флаконах
Тщательно вымыть руки и обработать место инъекции ватным тампоном, смоченным антисептиком.

Снять защитный колпачок с флакона с препаратом. Не снимать резиновый колпачок. Протереть резиновый колпачок ватным тампоном, смоченным антисептиком. Снять защитный колпачок с иголки шприца (шприц не входит в комплект упаковки препарата). Не допускать контакта иголки с посторонними предметами и не трогать иголку.

Поставить флакон с препаратом на ровную поверхность и воткнуть иглу шприца в резиновый колпачок флакона. Перевернуть флакон с препаратом и воткнутым в него шприцом.
Набрать содержимое флакона в шприц. Во избежание попадания пузырьков воздуха в шприц, кончик иглы, при наборе препарата в шприц, всегда должен находиться в жидкости.

Вынуть шприц из флакона. Держать шприц иголкой в направлении от себя и проверить наличие в нем пузырьков воздуха. При наличии пузырьков воздуха в шприце осторожно постучать по стенке шприца, пока пузырьки воздуха не переместятся вверх.
Надавить на поршень шприца, чтобы выпустить пузырьки воздуха. Не класть шприц и не допускать контакта иглы с посторонними предметами.

Аккуратно зажать кожу в области инъекции между большим и указательным пальцами, воткнуть иголку в кожу и медленно опустить поршень шприца до предела.
После этого отпустить кожу и осторожно вынуть иглу. Из места инъекции может выделиться небольшое количество крови, что нормально. Приложить ватный тампон, смоченный антисептиком, к месту инъекции и подержать несколько секунд. Не тереть место инъекции. При необходимости заклеить пластырем.
Использованный шприц необходимо утилизировать в соответствии с местными требованиями по уничтожению такого рода отходов. Никогда не использовать иглы повторно.
— Для раствора для п/к введения в шприцах

Достать шприц с препаратом из картонной пачки, держа его в направлении иголкой от себя. Убедиться, что шприц не поврежден. Тщательно вымыть руки и обработать место инъекции ватным тампоном, смоченным антисептиком. Снять защитный колпачок с иглы. В шприце может быть пузырек воздуха, что допустимо, не следует удалять его. На конце иглы может быть капелька жидкости, что также допустимо.
Никогда не снимать защитный колпачок, пока не будет определено место инъекции. Не допускать контакта иголки с посторонними предметами.

Аккуратно зажать кожу в области инъекции между большим и указательным пальцами, воткнуть иголку в кожу и медленно опустить поршень шприца до предела.

После этого отпустить кожу и осторожно вынуть иглу. Как только палец будет убран с поршня, иголка автоматически скроется в корпусе шприца.
Приложить ватный тампон, смоченный антисептиком, к месту инъекции и подержать несколько секунд. Не тереть место инъекции. При необходимости заклеить пластырем.
Использованный шприц необходимо утилизировать в соответствии с местными требованиями по уничтожению такого рода отходов.
Немного фактов
Стелара ингибитор интерлейкина, обладающий иммунодепрессивным действием. Содержит в себе антитела, которые специфически воздействуют на субъединицы р40 интерлейкинов типа ИЛ-12 и ИЛ-23. Препарат используется в дерматологической практике для лечения вульгарного псориаза. Его действующие компоненты уменьшают влияние цитокинов, продуцируемых лейкоцитами, на активность иммунокомпетентных клеток. За счет этого прерывается цепь патологических реакций, имеющих ключевое значение в прогрессировании псориаза.
Нозологическая классификация (МКБ-10)
Противопсориатический препарат предназначен для лечения болезней класса XII группы L00-L99.
Лекарственная форма и состав
Стелара раствор для парентерального введения с единичными вкраплениями частиц белкового происхождения. В его состав входят:
- устекинумаб;
- вода для инъекций;
- L-histidine;
- эмульгатор;
- олигосахариды.
Бесцветный раствор выпускается в специальных одноразовых шприцах объемом по 0.5 мл, 1.0 мл или 2.0 мл. В каждом из них содержится по 45 мл или 90 мг действующего вещества.
Фармакотерапевтические свойства
В медпрепарате содержатся человеческие антитела IgGlk, которые обладают специфической активностью по отношению субъединицам р40 цитокинов ИЛ-12 и Ил-23. Лекарство угнетает активность информационных молекул и препятствует их присоединению к рецепторам типа ИЛ-12Rb1. За счет этого нарушается экспрессия рецепторов на поверхности иммунокомпетентных клеток.
Действующие вещества препарата не способны объединяться с ИЛ-12 и ИЛ-23, которые уже имеют связь с белковыми рецепторами. В связи с этим Стелара не принимает участие в формировании антителозависимой цитотоксичности.
Антигенпрезентирующие клетки секретируют гетеродимерные цитокины, к которым относятся ИЛ-12 и ИЛ-23. Они принимают участие в иммунных процессах, которые стимулируют активацию CD4 +Т-клеток и NK-клето. Но при развитии дерматологических патологий регуляция скорости биосинтеза ИЛ-12 и ИЛ-23 нарушается. Иммунодепрессант ликвидирует влияние гетеродимерных цитокинов на передачу сигналов внутри клеток и выработку гормоноподобных белков.
Стелара обрывает цепь патологических реакций и продукцию цитокинов, которые провоцируют развитие псориатического артрита и вульгарного псориаза. Устекинумаб нарушает процесс образования цитокинов типа TH1 и TH17, которые относятся к основным звеньям патогенеза дерматологической болезни.
Фармакокинетические свойства
Предельная концентрация активных компонентов в крови после введения противопсориатического раствора наблюдается через 8.5 суток. При этом биодоступность после парентерального введения не превышает 58%. Пути метаболизма Стелары не были определены.
При подкожном введении растворного иммунодепрессанта в течение 3 месяцев накопление устекинумаба в крови не наблюдается. Согласно результатам фармакокинетического анализа, употребление спиртосодержащих напитков и табакокурение никак не влияет на период полураспада активных компонентов и их терапевтическую активность.
Показания к применению
Препарат Стелара используется в терапии дерматологических патологий у больных, достигших 12-летнего возраста. Показаниями к назначению иммунодепрессанта являются:
- бляшечный (вульгарный) псориаз средней и тяжелой степени развития;
- псориатический артрит средней и тяжелой степени развития.
Лекарственный раствор может использоваться в качестве монопрепарата или в составе комбинированной терапии вульгарного псориаза у пациентов в возрасте от 12 лет. Стелара комбинируется с Метотрексатом при прохождении курсовой терапии псориатического артрита.
Режим дозирования
Оптимальная доза препарата 45.0 мг в сутки. Спустя 28 дней делают вторую подкожную инъекцию. После стабилизации состояния раствор вводят 1 раз в 12 недель. В тех случаях, когда масса пациента превышает 100 кг, дозировку повышают до 90.0 мг. В случае неэффективности лечения в течение 25-30 недель необходимо заменить Стелару другим противопсориатическим средством.
Больным, у которых фармакологическая эффективность препарата выражается слабо, повышают дозировку до 90.0 мг через каждые 3 месяца. При отсутствии нужного эффекта раствор вводят через каждые 2 месяца.
Во время медицинских испытаний влияние возраста пациента на клиренс и объем перераспределения иммунодепрессанта не было установлено. Поэтому при лечении больных старше 55 лет схему терапии и дозировку не корректируют.
Указания по использованию раствора
Перед использованием медпрепарата нужно внимательно рассмотреть стеклянный флакончик или содержимое шприца. В жидкости могут содержаться единичные вкрапления белковых соединений. При потемнении раствора и наличии осадка использовать иммунодепрессант нельзя.
В процессе терапии смешивать препарат Стелару с другими лекарственными растворами нельзя. Если пациенту назначили 90.0 мг иммунодепрессанта, необходимо сделать две инъекции шприцами объемом по 45.0 мг. Раствор вводится в нижнюю часть живота или в бедро. При наличии псориатических высыпаний на указанных участках можно ввести инъекцию в область плеча.
Беременность и грудное вскармливание
При изучении свойств Стелары животным вводили раствор в концентрации, которая в 45 раз превышала оптимальную терапевтическую дозу для людей. Токсическое и тератогенное действие медпрепарата на внутриутробное развитие эмбриона не было установлено. Но результаты медицинских исследований применимы к человеку не всегда.
Достоверно неизвестно, могут ли действующие компоненты иммунодепрессанта воздействовать на репродуктивную активность женщины и особенности развития плода. Кроме того, устекинумаб экскретируется в грудное молоко. В связи с этим нежелательно использовать лекарственный раствор во время гестации и кормления грудью.
Совместимость с алкоголем
Согласно инструкции по применению иммунодепрессанта, употребление спиртосодержащих напитков никак не влияет на фармакокинетические свойства устекинумаба.
Взаимодействие с медикаментами
Полноценных исследований медикаментозного взаимодействия устекинумаба с участием людей не проводилось. Параллельное применение противопсориатического средства с медикаментами, которые используются в терапии псориаза (Левотироксин, Ибупрофен, Метформин), не приводит к ухудшению самочувствия.
На фармакокинетику активных веществ не влияет прием пероральных кортикостероидов и анти-TNFα медпрепаратов. При параллельном применении субстратов CYP450 дозировку не уменьшают.
Передозировка
Разовое введение дозы до 6.0 мг на 1 кг веса не сопровождается обострением симптомов дозолимитирующей токсичности. При превышении назначенной врачом дозировки нужно контролировать состояние пациента. В случае обнаружения токсических реакций необходимо начать паллиативную терапию.
Побочные реакции
Согласно инструкции, иммунодепрессант нечасто вызывает побочные эффекты. При прохождении противопсориатической терапии больные чаще всего жаловались на:
- головные боли;
- ринофарингит;
- стоматологические инфекции;
- воспаление дыхательных путей;
- крапивницу;
- ангионевротический отек;
- депрессию;
- парез лицевого нерва;
- диспепсические явления;
- эксфолиативный дерматит;
- воспаление подкожной клетчатки.
Не исключено развитие местных реакций после введения раствора кожный зуд, покраснение, отек кожи, гематомы и т.д. Чтобы предотвратить побочные эффекты, рекомендуется чаще менять места для уколов.
Противопоказания
Препарат Стелара не назначается детям, которые не достигли 12-летнего возраста. Абсолютными противопоказаниями к применению противопсориатического средства являются:
- туберкулез в анамнезе;
- рецидивы инфекционных болезней;
- беременность и лактация;
- повышенная чувствительность к устекинумабу;
- злокачественные опухоли.
Лечение иммунодепрессантом проводится под наблюдением врача при рецидивирующих паразитарных патологиях, а также септических воспалениях бактериального и микотического генеза.
Особые указания
Стелара селективный иммунодепрессант, который влияет на реактивность организма. Длительный прием медпрепарата может сопровождаться реактивацией инфекций, которые до начала терапии находились в латентной фазе.
В ходе медицинских исследований было выявлено, что у большинства пациентов с серьезными инфекционными патологиями в анамнезе наблюдались рецидивы инфекций. По этой причине лекарственный раствор нежелательно использовать лицам с вялотекущими инфекциями, в особенности с туберкулезом.
Информация о фармакокинетике противопсориатического средства у пожилых людей, а также больных с нарушением функций органов детоксикации отсутствует. Анализ среди лиц старше 60 лет не обнаружил негативного воздействия возраста на объем распределения действующих веществ и величину клиренса.
Безопасность противопсориатического раствора у детей дошкольного возраста не изучалась. Стелара используется в педиатрии при лечении пациентов от 12 лет, но только в условиях стационара. Дозировка зависит от массы тела ребенка. Если она не превышает 60 кг, назначают не более 0.75 мг на 1 кг веса, если больше 45 мг на 1 кг веса.
При исследованиях медпрепарата на животных выяснилось, что его действующие компоненты могут влиять на биологическую способность приматов к зачатию. В связи с этим женщинам репродуктивного возраста следует использовать пероральные контрацептивы на протяжении курса терапии, а также в течение 15-16 недель после его окончания. Компоненты медпрепарата способствуют повышению фертильности и, как следствие, вероятности нежелательной беременности.
Аналоги
В случае необходимости средство заменяется антидепрессантами, которые обладают выраженной противопсориатической активностью:
- Локоид;
- Имунофан;
- Эльтеанс;
- Псориатен;
- Кортомицетин.
Некоторые из вышеперечисленных средств отпускаются в аптечных сетях без предписания врача. Однако перед их использованием рекомендуется проконсультироваться с дерматологом. Нерациональное использование медикаментов чревато обострением псориаза или псориатического артрита.
Условия продажи и хранения
Растворный иммунодепрессант отпускается только при наличии письменного назначения от дерматолога. Хранить раствор нужно в защищенном от света месте при соблюдении температурного режима 2-8 градусов Цельсия. После замораживания использовать медпрепарат не рекомендуется. Предельный срок годности составляет 24 месяца с момента выпуска.
Цены на Стелара в Москве
Заберите заказ в в аптеке
WER (г. Москва)
Цена: от 94 000 руб.
Сертификаты и лицензии
Стелара® (45 мг/0.5 мл)
МНН: Устекинумаб
Производитель: Силаг АГ
Анатомо-терапевтическо-химическая классификация: Ustekinumab
Номер регистрации в РК:
№ РК-ЛС-5№019548
Информация о регистрации в РК:
11.01.2013 — 11.01.2018
Информация о реестрах и регистрах
Информация по ценам и ограничения
Предельная цена закупа в РК:
1 043 469.75 KZT
- Скачать инструкцию медикамента
Торговое название
Стелара®
Международное непатентованное название
Устекинумаб
Лекарственная форма
Раствор для инъекций 45 мг/0.5 мл и 90 мг/1 мл в предварительно заполненных шприцах
Состав
Один шприц содержит
активное вещество — устекинумаба 45 мг или 90 мг,
вспомогательные вещества: сахароза, L-гистидин (в том числе L-гисти-дина монохлорида моногидрат), полисорбат 80, вода для инъекций.
Описание
Опалесцирующий раствор от бесцветного до светло-желтого цвета. Раствор может содержать единичные прозрачные частицы белка.
Фармакотерапевтическая группа
Иммунодепрессанты. Ингибиторы интерлейкина. Устекинумаб.
Код АТХ L04AC05
Фармакологические свойства
Фармакокинетика
Всасывание. Медианное время до достижения максимальной сывороточной концентрации устекинумаба (tmax) составило 8,5 дней после однократного подкожного введения дозы 90 мг здоровым добровольцам. Медианные значения tmax для устекинумаба после однократного подкожного введения в дозе 45 мг или 90 мг пациентам с псориазом были сопоставимы со значениями, полученными для здоровых добровольцев. Абсолютная биодоступность устекинумаба после однократного подкожного введения составила 57,2% у пациентов с псориазом.
Распределение. Медианный объем распределения в терминальной фазе (Vz) после однократного внутривенного введения устекинумаба пациентам с псориазом колебался от 57 до 83 мл/кг.
Метаболизм
Метаболический путь устекинумаба не известен.
Элиминация. Медианный системный клиренс (CL) после однократного внутривенного введения пациентам с псориазом находился в диапазоне 1,99-2,34 мл/сутки/кг. Медианный период полувыведения (t1/2) устекинумаба составлял примерно 3 недели у пациентов с псориазом и/или псориатическим артритом и колебался от 15 до 32 дней во всех исследованиях псориаза и/или псориатического артрита. В популяционном фармакокинетическом анализе кажущийся клиренс (CL/F) и кажущийся объем распределения (V/F) у пациентов с псориазом составили 0,465 л/день и 15,7 л соответственно. CL/F устекинумаба не зависел от пола. В популяционном фармакокинетическом анализе наблюдалась тенденция в сторону повышения клиренса устекинумаба у пациентов с положительным тестом на антитела к устекинумабу.
Линейность дозы. У пациентов с псориазом системная экспозиция устекинумаба (Cmax и AUC) увеличивалась практически дозозависимым образом после однократного внутривенного введения в дозах от 0,09 мг/кг до 4,5 мг/кг или однократного подкожного введения в дозах от 24 до 240 мг.
Однократное применение препарата в сравнении с многократным применением препарата. Сывороточные профили зависимости концентрации устекинумаба от времени были в целом предсказуемыми в случае однократного и многократного подкожного введения препарата. Сывороточные концентрации устекинумаба в равновесном состоянии достигались к 28-й неделе после исходного введения на 0-й и 4-й неделе, а затем каждые 12 недель. У пациентов с псориазом медианное значение минимальной концентрации в равновесном состоянии колебалось от 0,21 до 0,26 мкг/мл (для дозы 45 мг) и от 0,47 до 0,49 мкг/мл (для дозы 90 мг). При подкожном введении каждые 12 недель не наблюдалось явной акумуляции сывороточного устекинумаба во времени.
Влияние массы тела на фармакокинетику препарата. В популяционном фармакокинетическом анализе масса тела пациента с псориазом была признана наиболее существенной ковариатой, влияющей на клиренс устекинумаба.
Медианное значение CL/F у пациентов с массой тела > 100 кг оказалось примерно на 55% выше в сравнении со значением у пациентов с массой тела < 100 кг. Медианное значение V/F у пациентов с массой тела > 100 кг было примерно на 37% выше в сравнении с таковым у пациентов с массой тела < 100 кг. Медианное значение минимальной концентрации устекинумаба у пациентов с более высокой массой тела (> 100 кг) в группе 90 мг была сопоставима со значением этого показателя у пациентов с меньшей массой тела (< 100 кг) в группе 45 мг. Аналогичные результаты получены при подтверждающем анализе популяционных фармакокинетических данных среди пациентов с псориатическим артритом.
Особые группы пациентов. Отсутствуют фармакокинетические данные по пациентам с нарушением функции почек или печени. Не проводились специальных исследовании с участием пожилых пациентов. Фармакокинетика устекинумаба в целом была сопоставима у пациентов с псориазом, являющихся представителями азиатской и неазиатской расы. В популяционном фармакокинетическом анализе не было выявлено влияние курения или употребления алкоголя на фармакокинетику устекинумаба.
Регуляция системы ферментов CYP450. Влияние ИЛ-12 или ИЛ-23 на регуляцию системы ферментов CYP450 изучалось в исследовании in vitro с использованием человеческих гепатоцитов. Было установлено, что ИЛ-12 и/или ИЛ-23 при уровнях 10 нг/мл не изменяли активности ферментов человеческого CYP450 (CYP1A2, 2B6, 2C9, 2С19, 2D6 или 3А4; см. раздел «Лекарственные взаимодействия»).
Фармакодинамика
Устекинумаб представляет собой полностью человеческие моноклональные антитела IgG1к, которые с высокой аффинностью и специфичностью связываются с белковыми субъединицами р40 человеческих цитокинов ИЛ-12 (интерлейкина-12) и ИЛ-23. Устекинумаб ингибирует биологическую активность человеческих ИЛ-12 и ИЛ-23, препятствуя связыванию этих цитокинов с их ИЛ-12R1-рецепторным белком, экспрессируемым на поверхности иммунных клеток. Устекинумаб не может связываться с ИЛ-12 или ИЛ-23, которые уже связаны с рецепторами ИЛ-12R1 на поверхности клеток. Таким образом, устекинумаб не склонен усиливать комплементарную или антителозависимую цитотоксичность в клетках, несущих рецепторы. ИЛ-12 и ИЛ-23 являются гетеродимерными цитокинами, которые секретируются клетками, содержащими активированный антиген, например, макрофагами и дендритными клетками. ИЛ-12 и ИЛ-23 включаются в иммунную функцию, участвуя в активации натуральных киллеров (NK-клетки) и дифференциации/активации CD4+ Т-клеток по фенотипу Т-хелперов 1 (Th1), а также стимулирует образование интерферона гамма (ИФγ). ИЛ-23 индуцирует развитие по пути Т-хелперов 17 и способствует секреции ИЛ-17А, ИЛ-21 и ИЛ-22. В крови и коже у пациентов с псориазом наблюдаются повышенные уровни ИЛ-12 и ИЛ-23, а у пациентов с псориазом и псориатическим артритом, в отличие от здоровых лиц, в сыворотке определяется ИЛ12/23p40, что позволяет предположить участие ИЛ-12 и ИЛ-23 в патофизиологии псориатических воспалительных заболеваний.
Генетический полиморфизм генов ИЛ23А (IL23A), ИЛ23 R (IL23R) и ИЛ-12В (IL-12B) определяет восприимчивость к этим заболеваниям. В участках кожи с псориатическим поражением наблюдается значительная экспрессия ИЛ-12 и ИЛ-23, а ИЛ-12-опосредованная индукция ИФγ коррелирует с активностью псориаза. Т-клетки, чувствительные к ИЛ-23, определялись в энтезисах (места соединения сухожилии и связок с костью) на мышиной модели воспалительного артрита, в которых ИЛ-23 определял воспаление энтезисов.
Связывание общей субъединицы р40 ИЛ-12 и ИЛ-23 обуславливает клиническое действие устекинумаба при псориазе и при псориатическом артрите, которое происходит в результате нарушения цитокиновых путей Th1 и Th17, лежащих в основе патологических изменений при данных заболеваниях.
Однако аномальная регуляция ИЛ-12 и ИЛ-23 связана с такими иммунно-опосредованными заболеваниями как псориаз. Устекинумаб препятствует участию ИЛ-12 и ИЛ-23 в активации иммунных клеток, например, во внутриклеточной передаче сигнала и секреции цитокинов. Таким образом, считается, что устекинумаб прерывает передачу сигнала и каскад экспрессии цитокинов, которые характерны для патологии псориаза.
Лечение препаратом устекинумаб сопровождалось значительным уменьшением гистологических признаков псориаза, в том числе гиперплазии эпидермиса и пролиферации клеток. Полученные результаты соответствуют наблюдаемой клинической эффективности препарата.
У пациентов с псориазом и/или псориатическим артритом устекинумаб не оказывал значимого воздействия на процентное соотношение популяции циркулирующих клеток иммунной системы, в том числе клеток памяти и неактивированных Т-лейкоцитов, а также на уровни циркулирующих цитокинов. Системные маркеры воспаления определялись в сыворотке при исходном обследовании, а для 4 маркеров (MDC, VEGF, MCSF-1 и YKL-40) были установлены небольшие различия концентрации после лечения у пациентов, применявших устекинумаб по сравнению с пациентами из группы плацебо.
Согласно результатам анализа мРНК биоптатов пораженной кожи у пациентов с псориазом при исходном обследовании и в течение периода до 2 недель после применения препарата, лечение устекинумабом приводило к снижению экспрессии генов и молекул-мишеней ИЛ-12 и ИЛ-23. Кроме того, препарат Стелара® подавлял экспрессию генов воспалительных цитокинов и хемокинов, таких как MCP-1, ФНО-альфа, IP-10 и ИЛ-8 в биоптатах пораженных участков кожи. Эти данные показывают значительное клиническое преимущество, которое наблюдалось при лечении устекинкмабом при псориазе.
При проведении исследований у пациентов с псориазом и псориатическим артритом были получены данные, свидетельствующие о том, что клинический ответ (улучшение индекса распространенности и тяжести псориаза (PASI — Psoriasis Area and Severity Index) или оценки по критериям Американской коллегии ревматологии (ACR — American College of Rheumatology), соответственно) коррелировал с концентрацией устекинумаба в сыворотке. У пациентов с псориазом, у которых наблюдался лучший ответ по индексу PASI, медиана концентрации устекинумаба была выше, чем у пациентов с низким клиническим ответом. При проведении исследований по применению препарата при псориазе соотношение пациентов, у которых на 28 неделе был получен индекс PASI 75, увеличилось, и это сопровождалось увеличением концентрации устекинумаба перед следующим введением препарата на 28 неделе. При проведении исследований у пациентов с псориатическим артритом у пациентов, у которых был достигнут уровень ответа ACR 20, медиана концентраций устекинумаба в сыворотке была выше, чем у лиц, у которых не был достигнут уровень ACR 20. Соотношение пациентов, у которых был достигнут уровень ACR 20 и ACR 50 увеличивалось по мере увеличения концентраций устекинумаба в сыворотке.
Показания к применению
— для лечения взрослых пациентов с умеренной и тяжелой степенью бляшечного псориаза, у которых не было ответа, или были противопоказания или непереносимость других системных методов лечения, включая циклоспорин, метотрексат или PUVA
— для лечения взрослых пациентов с псориатическим артритом в качестве монотерапии или в комбинации с метотрексатом при недостаточном ответе на предыдущую терапию небиологическими болезнь-модифицирующими антиревматическими препаратами
Способ применения и дозы
Препарат Стелара® необходимо использовать по показанию и требует наблюдения врача, имеющего опыт в диагностике и лечении псориаза или псориатического артрита. Препарат Стелара® предназначен для подкожного введения.
Бляшечный псориаз
Для взрослых пациентов рекомендованная доза составляет 45 мг подкожно. Вторую инъекцию делают 4 недели спустя после первого применения, затем каждые 12 недель.
Для пациентов с массой тела > 100 кг рекомендованная доза составляет 90 мг подкожно. Вторую инъекцию делают 4 недели спустя после первого применения, затем каждые 12 недель.
У пациентов с массой тела более 100 кг дозировка 45 мг также эффективна, однако наилучший результат достигается при введении 90 мг.
Следует рассмотреть возможность отмены лечения у пациентов, с неудовлетворительным ответом на терапию в течение 28 недель.
Псориатический артрит
Для взрослых пациентов рекомендованная доза составляет 45 мг. Вторую инъекцию делают 4 недели спустя после первого применения, затем каждые 12 недель.
Для пациентов с массой тела > 100 кг рекомендованная доза составляет 90 мг.
Следует рассмотреть возможность отмены лечения у пациентов, с неудовлетворительным ответом на терапию в течение 28 недель.
Пожилые пациенты (> 65 лет)
Для пожилых пациентов не требуется корректировка дозы (см. раздел «Особые указания).
Почечная и печеночная недостаточность
Действие препарата Стелара® не изучалось среди данной группы пациентов. Отсутствуют рекомендации по дозе.
Пациенты педиатрического возраста
Безопасность и эффективность препарата Стелара® у детей младше 12 лет не установлена. Данных нет.
Способ применения
Препарат Стелара® предназначен для применения в виде подкожных инъекций. Если возможно, при выборе места для инъекции нужно избегать участков кожи, пораженных псориазом.
После освоения метода подкожных инъекций пациенты могут самостоятельно делать инъекции препарата, если врач сочтёт это возможным. Однако врач должен вести за пациентами соответствующее наблюдение. Пациенты должны быть проинструктированы относительно введения всего объема препарата в соответствии с указаниями, представленными в инструкции по медицинскому применению, где содержится исчерпывающая информация по применению препарата. Следует обратиться к разделу «Особые указания» относительно дополнительных сведений по препарату и особых предосторожностей по его применению.
Указания по введению препарата
В начале лечения инъекции препарата Стелара® должен делать только медицинский персонал, однако, в последующем, если врач сочтет это возможным, пациент может делать себе инъекции препарата Стелара® самостоятельно, соблюдая все необходимые предосторожности и пройдя предварительно обязательное обучение технике подкожных инъекций.
-
Препарат Cтелара® не следует смешивать с другими жидкостями для инъекции
-
Не встряхивайте препарат. Длительное энергичное встряхивание может повредить препарат. Не используйте препарат, если его встряхивали.
Рис. 1 Шприц с препаратом Стелара®
| 454107401477976950_ru.doc | 680 кб |
| 429643531477978107_kz.doc | 693 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники