Тривентин
МНН: Тикагрелор
Производитель: Абди Ибрахим Глобал Фарм ТОО
Анатомо-терапевтическо-химическая классификация: Ticagrelor
Номер регистрации в РК:
№ РК-ЛС-5№024592
Информация о регистрации в РК:
24.06.2020 — 24.06.2025
- Скачать инструкцию медикамента
Торговое наименование
Тривентин
Международное непатентованное название
Тикагрелор
Лекарственная
форма, дозировка
Таблетки,
покрытые пленочной оболочкой, 90
мг
Фармакотерапевтическая группа
и органы кроветворения. Антитромботические препараты.
Ингибиторы
агрегации тромбоцитов, исключая гепарин. Тикагрелор
Код АТХ B01AC24
Показания к применению
Тривентин при совместном приеме с
ацетилсалициловой кислотой (АСК), показан для профилактики
атеротромботических осложнений у взрослых пациентов:
— с острым коронарным синдромом (ОКС)
-инфарктом миокарда (ИМ) и высоким
риском возникновения атеротромботических осложнений.
Перечень сведений необходимых до
начала применения
Противопоказания
— гиперчувствительность к
действующему веществу или к любому из вспомогательных веществ
препарата
— наличие патологического
кровотечения
— внутричерепное кровоизлияние в
анамнезе
— печеночная недостаточность средней
или тяжелой степени
— совместное применение тикагрелора с
мощными ингибиторами CYP3A4
(например, кетоконазол, кларитромицин, нефазодон, ритонавир и
атазанавир), так как совместное применение может привести к
значительному увеличению воздействия тикагрелора
—
беременность и период лактации
—
детский и подростковый возраст до 18 лет
Необходимые меры
предосторожности при применении
Риск
развития кровотечения
Как и при применении других
антитромботических препаратов, при назначении тикагрелора следует
оценить соотношение пользы от профилактики тромботических событий и
риска у пациентов с повышенным риском развития кровотечений.
Необходимо принять во внимание
следующее:
— предрасположенность пациентов к
развитию кровотечения (например, в связи с недавно полученной
травмой, недавно проведенной операцией, нарушениями свертываемости
крови, активным или недавним желудочно-кишечным кровотечением). Прием
тикагрелора противопоказан пациентам с активным патологическим
кровотечением, с внутричерепным кровоизлиянием в анамнезе и тяжелой
печеночной недостаточностью;
— сопутствующее применение
препаратов, которые могут повысить риск развития кровотечения
(например, нестероидные противовоспалительные препараты, пероральные
антикоагулянты и/или фибринолитики, принимаемые в течение 24 часов до
приема тикагрелора);
Отсутствуют данные о применении
тикагрелора и гемостатической эффективности трансфузий тромбоцитами;
тикагрелор может ингибировать трансфузированные тромбоциты в крови.
Так как при сопутствующем применении тикагрелора и десмопрессина не
уменьшалось стандартизированное время кровотечения, то маловероятно,
что десмопрессин будет эффективно купировать кровотечение.
Антифибринолитическая терапия
(аминокапроновая кислота или транексамовая кислота) и/или
рекомбинантный фактор VIIa
могут усиливать гемостаз. После установления причины кровотечения и
его купирования можно возобновить терапию тикагрелором.
Хирургические операции
Пациенты должны сообщить терапевту и
стоматологам, что они принимают тикагрелор, до того, как будет
спланирована любая хирургическая операция, и до начала приема нового
лекарственного препарата.
Если пациенту предстоит плановая
операция, в связи с чем антитромботический эффект нежелателен, прием
тикагрелора следует прекратить за 7 дней до хирургического
вмешательства.
Пациенты, перенесшие ишемический
инсульт
Пациенты с ОКС, ранее перенесшие
ишемический инсульт, могут проходить терапию тикагрелором в течение
не более 12 месяцев.
Печеночная недостаточность
Пациентам с острой печеночной
недостаточностью противопоказано применение тикагрелора. Опыт
применения тикагрелора у пациентов с умеренной печеночной
недостаточностью является небольшим, в связи с чем, рекомендуется
проявлять осторожность при лечении этих больных.
Пациенты с риском развития
брадикардии
В связи с раннее выявленными данными
по бессимптомным желудочковым асистолиям, пациенты с повышенным
риском развития брадикардии (например, больные без кардиостимулятора,
у которых диагностирован синдром слабости синусового узла,
атриовентрикулярная блокада 2-ой или 3-ей степени; обморок, связанный
с брадикардией) не были включены в основное исследование для оценки
безопасности и эффективности тикагрелора. Поэтому, в связи с
ограниченным клиническим опытом применения препарата у этих больных,
рекомендуется с осторожностью назначать тикагрелор таким пациентам.
Кроме того, следует соблюдать осторожность при приеме тикагрелора
одновременно с лекарственными препаратами, которые могут вызвать
брадикардию.
Одышка
Одышка, отмеченная при применении
тикагрелора, обычно слабая или умеренная по своей интенсивности,
часто проходит по мере продолжения терапии препаратом. Пациенты с
бронихиальной астмой, хронической обструктивной болезнью легких
(ХОБЛ) могут иметь увеличенный абсолютный риск возникновения одышки
при приеме тикагрелора. Тикагрелор следует использовать с
осторожностью пациентами с бронхиальной астмой, ХОБЛ в анамнезе.
Механизм до настоящего времени не установлен. Если у пациента
развился новый эпизод, одышка сохранилась или усилилась, необходимо
провести полное обследование. Если установлено, что одышка вызвана
терапией тикагрелором, прием препарата следует прекратить.
Повышение креатинина
Во время лечения тикарелором уровни
креатинина могут повыситься. Механизм не выяснялся. Почечную функцию
следует проверять согласно рутинной клинической практике. У пациентов
с АКШ рекомендуется проверять уровень креатинина через месяц с начала
терапии тикагрелором, обращая особое внимание на пациентов ≥ 75
лет, пациентов со средней/тяжелой почечной недостаточностью и на тех,
кто получал сопутствующее лечение блокаторами
рецепторов ангиотензина-II
(ARB).
Повышение мочевой кислоты
Следует соблюдать меры
предосторожности при приеме тикагрелора
пациентами, у которых в анамнезе есть гиперурикемия или подагрический
артрит. В качестве меры предосторожности, использование
тикагрелора
у
пациентов с мочекислой нефропатией не рекомендуется.
Тромботическая
тромбоцитопеническая пурпура (ТТП)
О случаях тромботической
тромбоцитопенической пурпуры (ТТП) сообщается очень редко при
применении тикагрелора. ТТП характеризуется тромбоцитопенией и
микроангиопатической гемолитической анемией, связанной с
неврологическими признаками, почечной дисфункцией или лихорадкой. ТТП
является потенциально смертельным состоянием, требующим немедленного
лечения, включая плазмаферез.
Другие
Совместный прием тикагрелора и
высокой поддерживающей дозы АСК (более 300 мг) не рекомендуется.
Прекращение терапии
Досрочное прекращение любой
антиагрегантной терапии, в том числе тикагрелором, может привести к
повышению риска смерти от сердечно-сосудистых заболеваний или риска
инфаркта миокарда, как следствие основного заболевания. Поэтому,
следует избегать преждевременного прекращения терапии.
Дети
Безопасность и эффективность
тикагрелора у детей младше 18 лет не установлена.
Взаимодействия с другими
лекарственными препаратами
Тикагрелор
является, прежде всего, субстратом CYP3A4
и слабым ингибитором CYP3A4.
Тикагрелор
также является субстратом Р-гликопротеина и слабым ингибитором
Р-гликопротеина и может увеличить воздействие субстратов
Р-гликопротеина.
Влияние других лекарственных
препаратов на препарат Тикагрелор
Лекарственные препараты,
метаболизируемые CYP3A4
Ингибиторы CYP3A4
— Мощные ингибиторы CYP3A4
– совместное применение кетоконазола с тикагрелором
приводит к увеличению Cmax
и площади под
кривой (AUC)
тикагрелора
соответственно в 2,4
раза и 7,3 раза. Cmax
и площадь под кривой (AUC)
активного метаболита уменьшились на 89%
и 56%, соответственно. Можно предположить, что другие мощные
ингибиторы CYP3A4
(кларитромицин, нефазодон, ритонавир и атазанавир) имеют аналогичные
эффекты и их совместное применение с тикагрелором противопоказано.
— Умеренные ингибиторы CYP3A4
– совместное применение дилтиазема с тикагрелором приводит к
увеличению Cmax
тикагрелора на
69%, а площади под кривой (AUC)
– в 2,7 раза, и уменьшению Cmax
активного метаболита на 38% без изменения площади
под кривой (AUC).
Тикагрелор
не влияет на уровни дилтиазема в плазме крови. Можно
предположить, что другие умеренные ингибиторы CYP3A4
(например, ампренавир, апрепитант, эритромицин и флуконазол) имеют
аналогичные эффекты и могут в той же степени совместно применяться с
тикагрелором.
Индукторы CYP3A
Совместное применение рифампицина с
тикагрелором
приводит к снижению Cmax
и площади под кривой
(AUC)
тикагрелора
на 73% и 86%, соответственно.
Cmax
активного метаболита
оставалась без изменения, а площади под кривой (AUC)
снизилась на 46%, соответственно. Можно
предположить, что другие индукторы CYP3A
(например, дексаметазон, фенитоин, карбамазепин и фенобарбитал) также
будут уменьшать воздействие тикагрелора Совместное применение
тикагрелора с мощными индукторами CYP3A
может уменьшить воздействие и эффективность тикагрелора. В связи с
чем их совместное применение не рекомендовано.
Циклоспорин (ингибитор
Р-гликопротеина и CYP3A4)
Одновременный прием циклоспорина (600
мг) с тикагрелором увеличивает Cmax
и AUC
тикагрелора в 2,3 и 2,8 раза, соответственно. AUC
активного метаболита повышается на 32%, а Cmax
снижается на 15%
в присутствии циклоспорина.
Нет данных об одновременном
использовании тикагрелора с другими действующими веществами, также
являющимися мощными ингибиторами Р-гликопротеина и умеренными
ингибиторами CYP3A
(например, верапамилом, хинидином), которые также могут увеличить
воздействие тикагрелора. Если этого сочетания нельзя избежать, их
одновременное использование следует осуществлять с осторожностью.
Другие
Данные фармакологических
взаимодействий показывают, что совместное применение тикагрелора
с гепарином, эноксапарином и ацетилсалициловой кислотой или
десмопрессином не оказывает какого-либо влияния на фармакокинетику
препарата или его активного метаболита, или на АДФ-индуцированную
агрегацию тромбоцитов по сравнению с приемом только тикагрелора.
При наличии клинических показаний, лекарственные препараты, которые
изменяют гемостаз, следует применять с осторожностью совместно с
тикагрелором.
Влияние тикагрелора на другие
лекарственные препараты
Лекарственные препараты,
метаболизируемые CYP3A4
Симвастатин –
совместное применение тикагрелора с симвастатином приводит к
увеличению Cmax
симвастатина на 81%, а
площади под кривой (AUC)
— на 56%, и к увеличению Cmax
симвастатиновой кислоты на 64%, а
площади под кривой (AUC)
– на 52%, в некоторых отдельных случаях с увеличением в 2 –
3 раза. Совместное применение тикагрелора
и симвастатина в дозе более 40 мг в день может привести к побочным
эффектам симвастатина, и, поэтому, перед применением следует
сопоставить это с потенциальной пользой. Симвастатин не влияет на
уровень тикагрелора в плазме крови. Тикагрелор может оказывать
аналогичное влияние на ловастатин. Не рекомендуется совместное
применение тикагрелора с симвастатином или ловастатином в дозе более
40 мг.
Аторвастатин –
совместное применение аторвастатина и тикагрелора
приводит к увеличению
Cmax
аторвастатиновой кислоты на 23%, а
площади под кривой (AUC)
– на 36%. Аналогичное увеличение площади под кривой (AUC)
и Cmax
наблюдается для всех метаболитов аторвастатиновой кислоты. Эти
увеличения не рассматриваются как клинически значимые.
Подобное воздействие на другие
статины, которые метаболизируются CYP3A4,
не может быть исключено.
Тикагрелор
является умеренным ингибитором CYP3A4.
Не рекомендуется совместное применение тикагрелора
и субстратов CYP3A4
с узким терапевтическим диапазоном (например, цизаприд или алкалоиды
спорыньи), так как тикагрелор
может увеличить воздействие этих лекарственных препаратов.
Субстраты P-гликопротеина
(P—gp)
(включая, дигоксин, циклоспорин)
Совместное применение с тикагрелором
приводит к увеличению Cmax
дигоксина на 75%, а площади
под кривой (AUC)
– на 28%. Средние минимальные уровни дигоксина увеличились
примерно на 30% при совместном применении с тикагрелором,
в некоторых отдельных случаях максимум увеличивался до 2 раз. В
присутствии дигоксина, не оказывалось влияния на Cmax
и площадь под кривой
(AUC)
тикагрелора
и его активного метаболита. Следовательно, при совместном применении
тикагрелора с Р-гликопротеин зависимыми лекарственными препаратами с
узким терапевтическим диапазоном, такими как дигоксин или
циклоспорин, рекомендуется соответствующий клинический и/или
лабораторный мониторинг.
Воздействие тикагрелора на уровни
циклоспорина в крови не выявлено. Воздействие тикагрелора на другие
субстраты Р-гликопротеина не изучено.
Лекарственные препараты,
метаболизируемые CYP2C9
Совместное применение тикагрелора
с толбутамидом не
изменяет уровней любого из двух лекарственных препаратов в плазме
крови, это позволяет предположить, что тикагрелор
не является ингибитором CYP2C9,
и вряд ли будет влиять на CYP2C9
опосредованный метаболизм лекарственных препаратов, таких как
варфарин и толбутамид.
Оральные контрацептивные средства
Совместное применение тикагрелора
с левоноргестрелом и
этинилэстрадиолом приводит к увеличению воздействия этинилэстрадиола
примерно на 20%, но не влияет на фармакокинетику левоноргестрела. При
одновременном приеме левоноргестрела и этинилэстрадиола с
тикагрелором не
предполагается клинически значимого влияния на эффективность оральных
контрацептивных средств.
Другие варианты сопутствующего
лечения
Лекарственные препараты, известные
как вызывающие брадикардию
Из-за наблюдений главным образом
асимптоматических эпизодов асистолии желудочков и брадикардии,
следует соблюдать осторожность при совместном применении тикагрелора
с лекарственными препаратами, которые вызывают брадикардию.
Совместное применение тикагрелора с
гепарином, эноксапарином или десмопрессином не влияло на показатели
активированного частичного тромбопластинового времени (aPTT),
активированного времени свертывания (ACT)
или фактора Xa.
Однако, из-за потенциальных фармакодинамических взаимодействий,
следует соблюдать осторожность при совместном применении тикагрелора
с лекарственными препаратами, которые, как известно, изменяют
гемостаз.
В связи с сообщениями о
патологических кровоизлияниях кожных покровов при приеме селективных
ингибиторов обратного захвата серотонина
(SSRIs)
(например, пароксетин, сертралин и циталопрам), следует соблюдать
осторожность при приеме селективных
ингибиторов обратного захвата серотонина
(SSRIs)
с тикагрелором, так как это может привести к увеличению риска
кровотечений.
Специальные
предупреждения
Пожилые пациенты
Коррекция дозы не требуется.
Пациенты с почечной
недостаточностью
Пациентам с почечной недостаточностью
коррекция дозы не требуется. Информация о лечении пациентов на
гемодиализе отсутствует, и, следовательно, прием тикагрелора не
рекомендуется для этих пациентов.
Пациенты с печеночной
недостаточностью
Данные воздействия тикагрелора на
пациентов с тяжелой степенью печеночной недостаточности не
проводились. Следовательно, его использование для таких пациентов
противопоказано. Имеется лишь ограниченная информация о пациентах с
умеренной печеночной недостаточностью. Коррекция дозы не
рекомендована, однако применение тикагрелора должно осуществляться с
осторожностью. Пациентам с легкой степенью печеночной недостаточности
коррекция дозы не требуется.
Применение в педиатрии
Безопасность и эффективность
тикагрелора у детей младше 18 лет не установлена.
Во время беременности или лактации
Беременность
Женщины
детородного возраста должны применять соответствующие
противозачаточные средства, чтобы избежать беременности во время
лечения тикагрелором. Нет никаких данных об использовании тикагрелора
беременными женщинами. Прием тикагрелора во время беременности не
рекомендуется.
Лактация
При кормлении грудью риск для
новорожденных/младенцев не может быть исключен. Следовательно,
требуется тщательная оценка соотношения польза/риск для
новорожденных/младенцев и кормящей женщины, чтобы определить,
прекратить ли кормление грудью или лечение тикагрелором.
Особенности
влияния препарата на способность управлять транспортным средством или
потенциально опасными механизмами
Тикагрелор
может незначительно влиять на способность управлять автотранспортом и
механизмами. При лечении тикагрелором наблюдалось головокружение.
Поэтому пациентам с такими симптомами следует с осторожностью водить
автотранспорт или работать с механизмами.
Рекомендации по применению
Режим
дозирования
Пациенты, принимающие препарат
Тривентин, должны
ежедневно принимать поддерживающую дозу ацетилсалициловой кислоты
(АСК) в объеме 75-150 мг, если отсутствуют специфические
противопоказания.
Острый коронарный синдром
Применение препарата Тривентин
следует начинать с
однократной нагрузочной дозы 180 мг (две таблетки по 90 мг) и затем
продолжать прием по 90 мг два раза в сутки. Пациентам с острым
коронарным синдромом рекомендуется проводить лечение препаратом
Тривентин по 90 мг два
раза в сутки в течение 12 месяцев, кроме случаев клинической
необходимости в досрочной отмене препарата Тривентин.
Инфаркт миокарда в анамнезе
Тривентин объемом 60 мг дважды в день
является рекомендуемой дозой в случае возникновения необходимости в
расширенном лечении пациентов, у которых в анамнезе по крайней мере
одного года есть инфаркт миокарда, а также пациентов, которые
находятся в группе риска возникновения атеротромботических
осложнений. Лечение можно начать без перерыва, в качестве продолжения
терапии после первоначального годичного лечения препаратом Тривентин
по 90 мг или
лечения другим ингибитором рецепторов аденозиндифосфата (АДФ) у
пациентов с ОКС, подверженных риску возникновения атеротромботических
осложнений. Лечение также можно начать в течение 2 лет после ИМ или в
течение одного года после окончания предыдущего лечения ингибитором
рецептора АДФ. Данные об эффективности препарата Тривентин после 3
лет расширенного лечения являются ограниченными.
Если необходимо провести изменение,
первую дозу препарата Тривентин нужно ввести в течение 24 часов после
приема последней дозы антитромбозитарного препарата.
Метод и путь введения
Для перорального применения.
Препарат Тривентин можно применять
независимо от приема пищи. Для пациентов, которые не могут проглотить
таблетку целиком, таблетки могут быть измельчены в мелкий порошок и
смешаны с половиной стакана воды, при условии немедленного приема.
Стакан следует промыть еще одной половиной стакана воды и выпить
содержимое. Смесь также можно принять через назогастральный зонд (СН8
или больше). Важно промыть назогастральный зонд водой после приема
смеси.
Меры, необходимые при пропуске
одной или нескольких доз лекарственного препарата
Необходимо избегать отклонений в
лечении. Пациент, пропустивший прием дозы препарата Тривентин, должен
принять только одну таблетку (следующую дозу) по расписанию.
Меры,
которые необходимо принять в случае передозировки
Симптомы:
Кровотечение является предполагаемым фармакологическим действием
передозировки препаратом Тривентин,
поэтому при развитии кровотечения необходимо проводить
соответствующие поддерживающие мероприятия. Другие клинически
значимые побочные реакции, которые могут встречаться при
передозировке, включают диспноэ и эпизоды желудочковой асистолии.
Лечение:
специфического антидота не существует. В случае передозировки лечение
следует проводить в соответствии с местными стандартами медицинской
практики. При развитии кровотечения необходимо проводить
соответствующие поддерживающие мероприятия. Тикагрелор не выводится
при гемодиализе. Рекомендуется общая поддерживающая терапия,
наблюдение за больным и контроль функции жизненно важных органов и
систем (ЭКГ-мониторинг).
Рекомендации
по обращению за консультацией к медицинскому работнику для
разъяснения способа применения лекарственного препарата
Если у Вас возникли дополнительные
вопросы по применению этого препарата, проконсультируйтесь с врачом
или фармацевтом.
Описание нежелательных реакций,
которые
проявляются при стандартном применении ЛП и меры, которые следует
принять в этом случае
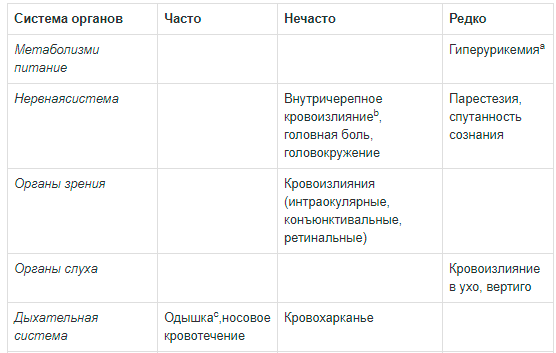
Категории частоты определяются в
соответствии со следующими условными обозначениями: очень часто (≥
1/10), часто (≥ 1/100 до <1/10), не часто (≥1/1000 до
<1/100), редко (≥1/10000 до <1/1000), очень редко
(<1/10000), неизвестно (исходя из известных данных, не может быть
оценена)
Очень часто
— Кровотечения при заболеваниях крови
(повышенная склонность к синякам, спонтанные гематомы,
геморрагический диатез);
— гиперурикемия;
— одышка
Часто
— подагра;
— головокружение, обморок;
— гипотензия;
— кровотечения из органов дыхательной
системы (носовое кровотечение, кровохарканье);
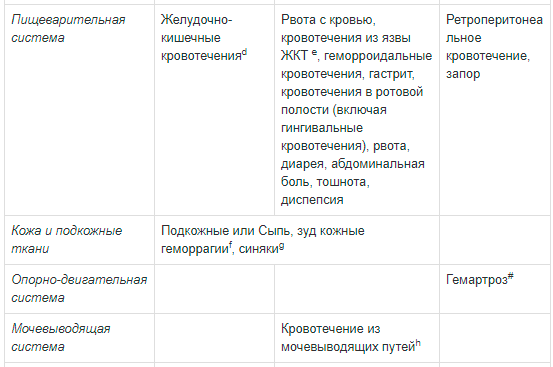
— желудочно-кишечные кровотечения
(кровоточивость десен, ректальное кровотечение, кровотечение из язвы
желудка), диарея, тошнота;
— подкожное или кожное кровотечение
(экхимоз, кожное кровотечение, петехии), зуд;
— кровотечение мочевыводящих путей
(гематурия, геморрагический цистит);
— повышение уровня креатинина в
крови;
— послеоперационное кровотечение,
травматическое кровотечение (ушиб, травматическая гематома,
травматическое геморрагическое кровотечение)
Не часто
— опухолевые кровотечения
(кровотечения из опухолевых очагов мочевого пузыря, желудка, толстой
кишки);
— спутанность сознания;
— внутричерепное кровоизлияние;
— кровоизлияния глаза (внутриглазное,
конъюнктивальное, в сетчатку);
— ушное кровотечения;
— забрюшинное кровотечение;
— мышечное кровоизлияние (гемартроз,
мышечное кровотечение);
— кровотечения из органов
репродуктивной системы (вагинальное кровотечение, гематоспермия,
кровотечение в постменопаузе)
При
возникновении нежелательных лекарственных реакций обращаться к
медицинскому работнику, фармацевтическому работнику или напрямую в
информационную базу данных по нежелательным реакциям (действиям) на
лекарственные препараты, включая сообщения о неэффективности
лекарственных препаратов РГП
на ПХВ «Национальный Центр экспертизы лекарственных средств и
медицинских изделий» Комитет контроля качества и безопасности
товаров и услуг Министерства здравоохранения Республики Казахстан
http://www.ndda.kz
Дополнительные
сведения
Состав
лекарственного препарата
Одна
таблетка содержит
активное вещество —
тикагрелор 90 мг,
вспомогательные вещества —
маннитол, маннитол
(гранулы), кальция гидрофосфата дигидрат, натрия кроскармеллоза,
гидроксипропилцеллюлоза, кремния диоксид коллоидный безводный, магния
стеарат
состав оболочки:
Опадрай® 03B220055 желтый (Opadry® 03B220055 Yellow),
гипромеллоза, титана диоксид (Е171), тальк,
полиэтиленгликоль/макрогол, железа оксид желтый (Е172))
Описание внешнего вида, запаха,
вкуса
Круглые,
двояковыпуклые таблетки, покрытые пленочной оболочкой светло-желтого
цвета, с фаской
Форма выпуска и упаковка
По 14 таблеток помещают в контурную
ячейковую упаковку из фольги алюминиевой и пленки
поливинилхлорид/полиэтилен/поливинили-денхлоридной (PVC/PE/PVDC).
По 4 контурные ячейковые упаковки
вместе с инструкцией по медицинскому применению на казахском и
русском языках помещают в пачку из картона.
Срок хранения
2 года.
Не
применять по истечении срока годности!
Условия хранения
Хранить в оригинальной упаковке при
температуре не выше 25 °С.
Хранить в недоступном для детей
месте!
Условия отпуска из аптек
По
рецепту
Сведения о производителе
ТОО
«Абди Ибрахим Глобал Фарм»,
Республика
Казахстан, Алматинская обл., Илийский р-он, Промзона 282, тел.:
+7 (727) 356-11-00,
8-800-070-11-00,
адрес
электронной почты: info@aigp.kz
Держатель
регистрационного удостоверения
ТОО
«Абди Ибрахим Глобал Фарм»,
Республика
Казахстан, Алматинская обл., Илийский р-он, Промзона 282, тел.:
+7 (727) 356-11-00,
8-800-070-11-00,
адрес
электронной почты: info@aigp.kz
Наименование,
адрес и контактные данные организации на территории Республики
Казахстан, принимающей претензии (предложения) по качеству
лекарственных средств от потребителей и ответственной
за пострегистрационное наблюдение за безопасностью лекарственного
средства
ТОО
«Абди Ибрахим Глобал Фарм»,
Республика
Казахстан, Алматинская обл., Илийский р-он, Промзона 282, тел.:
+7 (727) 356-11-00,
8-800-070-11-00,
адрес
электронной почты: info@aigp.kz
| ИМП_(ЛВ)_тривентин_90_мг_итог.docx | 0.05 кб |
| ИМП_(ЛВ)_Тривентин_90_мг_каз_10.20_Дурыс_.docx | 0.06 кб |
Отправить прикрепленные файлы на почту
МНН: Тикагрелор
Производитель: Абди Ибрахим Глобал Фарм ТОО
Анатомо-терапевтическо-химическая классификация: Ticagrelor
Номер регистрации в РК:
РК-ЛС-5№024593
Информация о регистрации в РК:
24.06.2020 — 24.06.2025
- Скачать инструкцию медикамента
Торговое наименование
Тривентин
Международное непатентованное название
Тикагрелор
Лекарственная
форма, дозировка
Таблетки,
покрытые пленочной оболочкой, 60 мг
Фармакотерапевтическая группа
и органы кроветворения. Антитромботические препараты. Ингибиторы
агрегации тромбоцитов, исключая гепарин. Тикагрелор
Код
АТХ B01AC24
Показания к применению
Тривентин при совместном приеме с
ацетилсалициловой кислотой (АСК), показан для профилактики
атеротромботических осложнений у взрослых пациентов:
— с острым коронарным синдромом (ОКС)
-инфарктом миокарда (ИМ) и высоким
риском возникновения атеротромботических осложнений.
Перечень сведений необходимых до
начала применения
Противопоказания
— гиперчувствительность к
действующему веществу или к любому из вспомогательных веществ
препарата
— наличие патологического
кровотечения
— внутричерепное кровоизлияние в
анамнезе
— печеночная недостаточность средней
или тяжелой степени
— совместное применение тикагрелора с
мощными ингибиторами CYP3A4
(например, кетоконазол, кларитромицин, нефазодон, ритонавир и
атазанавир), так как совместное применение может привести к
значительному увеличению воздействия тикагрелора
—
беременность и период лактации
—
детский и подростковый возраст до 18 лет
Необходимые меры
предосторожности при применении
Риск развития кровотечения
Как и при применении других
антитромботических препаратов, при назначении тикагрелора следует
оценить соотношение пользы от профилактики тромботических событий и
риска у пациентов с повышенным риском развития кровотечений.
Необходимо принять во внимание
следующее:
— предрасположенность пациентов к
развитию кровотечения (например, в связи с недавно полученной
травмой, недавно проведенной операцией, нарушениями свертываемости
крови, активным или недавним желудочно-кишечным кровотечением). Прием
тикагрелора противопоказан пациентам с активным патологическим
кровотечением, с внутричерепным кровоизлиянием в анамнезе и тяжелой
печеночной недостаточностью;
— сопутствующее применение
препаратов, которые могут повысить риск развития кровотечения
(например, нестероидные противовоспалительные препараты, пероральные
антикоагулянты и/или фибринолитики, принимаемые в течение 24 часов до
приема тикагрелора);
Отсутствуют данные о применении
тикагрелора и гемостатической эффективности трансфузий тромбоцитами;
тикагрелор может ингибировать трансфузированные тромбоциты в крови.
Так как при сопутствующем применении тикагрелора и десмопрессина не
уменьшалось стандартизированное время кровотечения, то маловероятно,
что десмопрессин будет эффективно купировать кровотечение.
Антифибринолитическая терапия
(аминокапроновая кислота или транексамовая кислота) и/или
рекомбинантный фактор VIIa
могут усиливать гемостаз. После установления причины кровотечения и
его купирования можно возобновить терапию тикагрелором.
Хирургические операции
Пациенты должны сообщить терапевту и
стоматологам, что они принимают тикагрелор, до того, как будет
спланирована любая хирургическая операция, и до начала приема нового
лекарственного препарата.
Если пациенту предстоит плановая
операция, в связи с чем антитромботический эффект нежелателен, прием
тикагрелора следует прекратить за 7 дней до хирургического
вмешательства.
Пациенты, перенесшие ишемический
инсульт
Пациенты с ОКС, ранее перенесшие
ишемический инсульт, могут проходить терапию тикагрелором в течение
не более 12 месяцев.
Печеночная недостаточность
Пациентам с острой печеночной
недостаточностью противопоказано применение тикагрелора. Опыт
применения тикагрелора у пациентов с умеренной печеночной
недостаточностью является небольшим, в связи с чем, рекомендуется
проявлять осторожность при лечении этих больных.
Пациенты с риском развития
брадикардии
В связи с раннее выявленными данными
по бессимптомным желудочковым асистолиям, пациенты с повышенным
риском развития брадикардии (например, больные без кардиостимулятора,
у которых диагностирован синдром слабости синусового узла,
атриовентрикулярная блокада 2-ой или 3-ей степени; обморок, связанный
с брадикардией) не были включены в основное исследование для оценки
безопасности и эффективности тикагрелора. Поэтому, в связи с
ограниченным клиническим опытом применения препарата у этих больных,
рекомендуется с осторожностью назначать тикагрелор таким пациентам.
Кроме того, следует соблюдать осторожность при приеме тикагрелора
одновременно с лекарственными препаратами, которые могут вызвать
брадикардию.
Одышка
Одышка, отмеченная при применении
тикагрелора, обычно слабая или умеренная по своей интенсивности,
часто проходит по мере продолжения терапии препаратом. Пациенты с
бронихиальной астмой, хронической обструктивной болезнью легких
(ХОБЛ) могут иметь увеличенный абсолютный риск возникновения одышки
при приеме тикагрелора. Тикагрелор следует использовать с
осторожностью пациентами с бронхиальной астмой, ХОБЛ в анамнезе.
Механизм до настоящего времени не установлен. Если у пациента
развился новый эпизод, одышка сохранилась или усилилась, необходимо
провести полное обследование. Если установлено, что одышка вызвана
терапией тикагрелором, прием препарата следует прекратить.
Повышение креатинина
Во время лечения тикарелором уровни
креатинина могут повыситься. Механизм не выяснялся. Почечную функцию
следует проверять согласно рутинной клинической практике. У пациентов
с АКШ рекомендуется проверять уровень креатинина через месяц с начала
терапии тикагрелором, обращая особое внимание на пациентов ≥ 75
лет, пациентов со средней/тяжелой почечной недостаточностью и на тех,
кто получал сопутствующее лечение блокаторами
рецепторов ангиотензина-II
(ARB).
Повышение мочевой кислоты
Следует соблюдать меры
предосторожности при приеме тикагрелора
пациентами, у которых в анамнезе есть гиперурикемия или подагрический
артрит. В качестве меры предосторожности, использование
тикагрелора
у
пациентов с мочекислой нефропатией не рекомендуется.
Тромботическая
тромбоцитопеническая пурпура (ТТП)
О случаях тромботической
тромбоцитопенической пурпуры (ТТП) сообщается очень редко при
применении тикагрелора. ТТП характеризуется тромбоцитопенией и
микроангиопатической гемолитической анемией, связанной с
неврологическими признаками, почечной дисфункцией или лихорадкой. ТТП
является потенциально смертельным состоянием, требующим немедленного
лечения, включая плазмаферез.
Другие
Совместный прием тикагрелора и
высокой поддерживающей дозы АСК (более 300 мг) не рекомендуется.
Прекращение терапии
Досрочное прекращение любой
антиагрегантной терапии, в том числе тикагрелором, может привести к
повышению риска смерти от сердечно-сосудистых заболеваний или риска
инфаркта миокарда, как следствие основного заболевания. Поэтому,
следует избегать преждевременного прекращения терапии.
Дети
Безопасность и эффективность
тикагрелора у детей младше 18 лет не установлена.
Взаимодействия с другими
лекарственными препаратами
Тикагрелор
является, прежде всего, субстратом CYP3A4
и слабым ингибитором CYP3A4.
Тикагрелор
также является субстратом Р-гликопротеина и слабым ингибитором
Р-гликопротеина и может увеличить воздействие субстратов
Р-гликопротеина.
Влияние других лекарственных
препаратов на препарат Тикагрелор
Лекарственные препараты,
метаболизируемые CYP3A4
Ингибиторы CYP3A4
— Мощные ингибиторы CYP3A4
– совместное применение кетоконазола с тикагрелором
приводит к увеличению Cmax
и площади под
кривой (AUC)
тикагрелора
соответственно в 2,4
раза и 7,3 раза. Cmax
и площадь под кривой (AUC)
активного метаболита уменьшились на 89%
и 56%, соответственно. Можно предположить, что другие мощные
ингибиторы CYP3A4
(кларитромицин, нефазодон, ритонавир и атазанавир) имеют аналогичные
эффекты и их совместное применение с тикагрелором противопоказано.
— Умеренные ингибиторы CYP3A4
– совместное применение дилтиазема с тикагрелором приводит к
увеличению Cmax
тикагрелора на
69%, а площади под кривой (AUC)
– в 2,7 раза, и уменьшению Cmax
активного метаболита на 38% без изменения площади
под кривой (AUC).
Тикагрелор
не влияет на уровни дилтиазема в плазме крови. Можно
предположить, что другие умеренные ингибиторы CYP3A4
(например, ампренавир, апрепитант, эритромицин и флуконазол) имеют
аналогичные эффекты и могут в той же степени совместно применяться с
тикагрелором.
Индукторы CYP3A
Совместное применение рифампицина с
тикагрелором
приводит к снижению Cmax
и площади под кривой
(AUC)
тикагрелора
на 73% и 86%, соответственно.
Cmax
активного метаболита
оставалась без изменения, а площади под кривой (AUC)
снизилась на 46%, соответственно. Можно
предположить, что другие индукторы CYP3A
(например, дексаметазон, фенитоин, карбамазепин и фенобарбитал) также
будут уменьшать воздействие тикагрелора Совместное применение
тикагрелора с мощными индукторами CYP3A
может уменьшить воздействие и эффективность тикагрелора. В связи с
чем их совместное применение не рекомендовано.
Циклоспорин (ингибитор
Р-гликопротеина и CYP3A4)
Одновременный прием циклоспорина (600
мг) с тикагрелором увеличивает Cmax
и AUC
тикагрелора в 2,3 и 2,8 раза, соответственно. AUC
активного метаболита повышается на 32%, а Cmax
снижается на 15%
в присутствии циклоспорина.
Нет данных об одновременном
использовании тикагрелора с другими действующими веществами, также
являющимися мощными ингибиторами Р-гликопротеина и умеренными
ингибиторами CYP3A
(например, верапамилом, хинидином), которые также могут увеличить
воздействие тикагрелора. Если этого сочетания нельзя избежать, их
одновременное использование следует осуществлять с осторожностью.
Другие
Данные фармакологических
взаимодействий показывают, что совместное применение тикагрелора
с гепарином, эноксапарином и ацетилсалициловой кислотой или
десмопрессином не оказывает какого-либо влияния на фармакокинетику
препарата или его активного метаболита, или на АДФ-индуцированную
агрегацию тромбоцитов по сравнению с приемом только тикагрелора.
При наличии клинических показаний, лекарственные препараты, которые
изменяют гемостаз, следует применять с осторожностью совместно с
тикагрелором.
Влияние тикагрелора на другие
лекарственные препараты
Лекарственные препараты,
метаболизируемые CYP3A4
Симвастатин –
совместное применение тикагрелора с симвастатином приводит к
увеличению Cmax
симвастатина на 81%, а
площади под кривой (AUC)
— на 56%, и к увеличению Cmax
симвастатиновой кислоты на 64%, а
площади под кривой (AUC)
– на 52%, в некоторых отдельных случаях с увеличением в 2 –
3 раза. Совместное применение тикагрелора
и симвастатина в дозе более 40 мг в день может привести к побочным
эффектам симвастатина, и, поэтому, перед применением следует
сопоставить это с потенциальной пользой. Симвастатин не влияет на
уровень тикагрелора в плазме крови. Тикагрелор может оказывать
аналогичное влияние на ловастатин. Не рекомендуется совместное
применение тикагрелора с симвастатином или ловастатином в дозе более
40 мг.
Аторвастатин –
совместное применение аторвастатина и тикагрелора
приводит к увеличению
Cmax
аторвастатиновой кислоты на 23%, а
площади под кривой (AUC)
– на 36%. Аналогичное увеличение площади под кривой (AUC)
и Cmax
наблюдается для всех метаболитов аторвастатиновой кислоты. Эти
увеличения не рассматриваются как клинически значимые.
Подобное воздействие на другие
статины, которые метаболизируются CYP3A4,
не может быть исключено.
Тикагрелор
является умеренным ингибитором CYP3A4.
Не рекомендуется совместное применение тикагрелора
и субстратов CYP3A4
с узким терапевтическим диапазоном (например, цизаприд или алкалоиды
спорыньи), так как тикагрелор
может увеличить воздействие этих лекарственных препаратов.
Субстраты P-гликопротеина
(P—gp)
(включая, дигоксин, циклоспорин)
Совместное применение с тикагрелором
приводит к увеличению Cmax
дигоксина на 75%, а площади
под кривой (AUC)
– на 28%. Средние минимальные уровни дигоксина увеличились
примерно на 30% при совместном применении с тикагрелором,
в некоторых отдельных случаях максимум увеличивался до 2 раз. В
присутствии дигоксина, не оказывалось влияния на Cmax
и площадь под кривой
(AUC)
тикагрелора
и его активного метаболита. Следовательно, при совместном применении
тикагрелора с Р-гликопротеин зависимыми лекарственными препаратами с
узким терапевтическим диапазоном, такими как дигоксин или
циклоспорин, рекомендуется соответствующий клинический и/или
лабораторный мониторинг.
Воздействие тикагрелора на уровни
циклоспорина в крови не выявлено. Воздействие тикагрелора на другие
субстраты Р-гликопротеина не изучено.
Лекарственные препараты,
метаболизируемые CYP2C9
Совместное применение тикагрелора
с толбутамидом не
изменяет уровней любого из двух лекарственных препаратов в плазме
крови, это позволяет предположить, что тикагрелор
не является ингибитором CYP2C9,
и вряд ли будет влиять на CYP2C9
опосредованный метаболизм лекарственных препаратов, таких как
варфарин и толбутамид.
Оральные контрацептивные средства
Совместное применение тикагрелора
с левоноргестрелом и
этинилэстрадиолом приводит к увеличению воздействия этинилэстрадиола
примерно на 20%, но не влияет на фармакокинетику левоноргестрела. При
одновременном приеме левоноргестрела и этинилэстрадиола с
тикагрелором не
предполагается клинически значимого влияния на эффективность оральных
контрацептивных средств.
Другие варианты сопутствующего
лечения
Лекарственные препараты, известные
как вызывающие брадикардию
Из-за наблюдений главным образом
асимптоматических эпизодов асистолии желудочков и брадикардии,
следует соблюдать осторожность при совместном применении тикагрелора
с лекарственными препаратами, которые вызывают брадикардию.
Совместное применение тикагрелора с
гепарином, эноксапарином или десмопрессином не влияло на показатели
активированного частичного тромбопластинового времени (aPTT),
активированного времени свертывания (ACT)
или фактора Xa.
Однако, из-за потенциальных фармакодинамических взаимодействий,
следует соблюдать осторожность при совместном применении тикагрелора
с лекарственными препаратами, которые, как известно, изменяют
гемостаз.
В связи с сообщениями о
патологических кровоизлияниях кожных покровов при приеме селективных
ингибиторов обратного захвата серотонина
(SSRIs)
(например, пароксетин, сертралин и циталопрам), следует соблюдать
осторожность при приеме селективных
ингибиторов обратного захвата серотонина
(SSRIs)
с тикагрелором, так как это может привести к увеличению риска
кровотечений.
Специальные
предупреждения
Пожилые пациенты
Коррекция дозы не требуется.
Пациенты с почечной
недостаточностью
Пациентам с почечной недостаточностью
коррекция дозы не требуется. Информация о лечении пациентов на
гемодиализе отсутствует, и, следовательно, прием тикагрелора не
рекомендуется для этих пациентов.
Пациенты с печеночной
недостаточностью
Данные воздействия тикагрелора на
пациентов с тяжелой степенью печеночной недостаточности не
проводились. Следовательно, его использование для таких пациентов
противопоказано. Имеется лишь ограниченная информация о пациентах с
умеренной печеночной недостаточностью. Коррекция дозы не
рекомендована, однако применение тикагрелора должно осуществляться с
осторожностью. Пациентам с легкой степенью печеночной недостаточности
коррекция дозы не требуется.
Применение в педиатрии
Безопасность и эффективность
тикагрелора у детей младше 18 лет не установлена.
Во время беременности или лактации
Беременность
Женщины
детородного возраста должны применять соответствующие
противозачаточные средства, чтобы избежать беременности во время
лечения тикагрелором. Нет никаких данных об использовании тикагрелора
беременными женщинами. Прием тикагрелора во время беременности не
рекомендуется.
Лактация
При кормлении грудью риск для
новорожденных/младенцев не может быть исключен. Следовательно,
требуется тщательная оценка соотношения польза/риск для
новорожденных/младенцев и кормящей женщины, чтобы определить,
прекратить ли кормление грудью или лечение тикагрелором.
Особенности
влияния препарата на способность управлять транспортным средством или
потенциально опасными механизмами
Тикагрелор
может незначительно влиять на способность управлять автотранспортом и
механизмами. При лечении тикагрелором наблюдалось головокружение.
Поэтому пациентам с такими симптомами следует с осторожностью водить
автотранспорт или работать с механизмами.
Рекомендации по применению
Режим
дозирования
Пациенты, принимающие препарат
Тривентин, должны
ежедневно принимать поддерживающую дозу ацетилсалициловой кислоты
(АСК) в объеме 75-150 мг, если отсутствуют специфические
противопоказания.
Острый коронарный синдром
Применение препарата Тривентин
следует начинать с
однократной нагрузочной дозы 180 мг (две таблетки по 90 мг) и затем
продолжать прием по 90 мг два раза в сутки. Пациентам с острым
коронарным синдромом рекомендуется проводить лечение препаратом
Тривентин по 90 мг два
раза в сутки в течение 12 месяцев, кроме случаев клинической
необходимости в досрочной отмене препарата Тривентин.
Инфаркт миокарда в анамнезе
Тривентин объемом 60 мг дважды в день
является рекомендуемой дозой в случае возникновения необходимости в
расширенном лечении пациентов, у которых в анамнезе по крайней мере
одного года есть инфаркт миокарда, а также пациентов, которые
находятся в группе риска возникновения атеротромботических
осложнений. Лечение можно начать без перерыва, в качестве продолжения
терапии после первоначального годичного лечения препаратом Тривентин
по 90 мг или
лечения другим ингибитором рецепторов аденозиндифосфата (АДФ) у
пациентов с ОКС, подверженных риску возникновения атеротромботических
осложнений. Лечение также можно начать в течение 2 лет после ИМ или в
течение одного года после окончания предыдущего лечения ингибитором
рецептора АДФ. Данные об эффективности препарата Тривентин после 3
лет расширенного лечения являются ограниченными.
Если необходимо провести изменение,
первую дозу препарата Тривентин нужно ввести в течение 24 часов после
приема последней дозы антитромбозитарного препарата.
Метод и путь введения
Для перорального применения.
Препарат Тривентин можно применять
независимо от приема пищи. Для пациентов, которые не могут проглотить
таблетку целиком, таблетки могут быть измельчены в мелкий порошок и
смешаны с половиной стакана воды, при условии немедленного приема.
Стакан следует промыть еще одной половиной стакана воды и выпить
содержимое. Смесь также можно принять через назогастральный зонд (СН8
или больше). Важно промыть назогастральный зонд водой после приема
смеси.
Меры, необходимые при пропуске
одной или нескольких доз лекарственного препарата
Необходимо избегать отклонений в
лечении. Пациент, пропустивший прием дозы препарата Тривентин, должен
принять только одну таблетку (следующую дозу) по расписанию.
Меры,
которые необходимо принять в случае передозировки
Симптомы:
Кровотечение является предполагаемым фармакологическим действием
передозировки препаратом Тривентин,
поэтому при развитии кровотечения необходимо проводить
соответствующие поддерживающие мероприятия. Другие клинически
значимые побочные реакции, которые могут встречаться при
передозировке, включают диспноэ и эпизоды желудочковой асистолии.
Лечение:
специфического антидота не существует. В случае передозировки лечение
следует проводить в соответствии с местными стандартами медицинской
практики. При развитии кровотечения необходимо проводить
соответствующие поддерживающие мероприятия. Тикагрелор не выводится
при гемодиализе. Рекомендуется общая поддерживающая терапия,
наблюдение за больным и контроль функции жизненно важных органов и
систем (ЭКГ-мониторинг).
Рекомендации
по обращению за консультацией к медицинскому работнику для
разъяснения способа применения лекарственного препарата
Если у Вас возникли дополнительные
вопросы по применению этого препарата, проконсультируйтесь с врачом
или фармацевтом.
Описание нежелательных реакций,
которые
проявляются при стандартном применении ЛП и меры, которые следует
принять в этом случае
Категории частоты определяются в
соответствии со следующими условными обозначениями: очень часто (≥
1/10), часто (≥ 1/100 до <1/10), не часто (≥1/1000 до
<1/100), редко (≥1/10000 до <1/1000), очень редко
(<1/10000), неизвестно (исходя из известных данных, не может быть
оценена)
Очень часто
— Кровотечения при заболеваниях крови
(повышенная склонность к синякам, спонтанные гематомы,
геморрагический диатез);
— гиперурикемия;
— одышка
Часто
— подагра;
— головокружение, обморок;
— гипотензия;
— кровотечения из органов дыхательной
системы (носовое кровотечение, кровохарканье);
— желудочно-кишечные кровотечения
(кровоточивость десен, ректальное кровотечение, кровотечение из язвы
желудка), диарея, тошнота;
— подкожное или кожное кровотечение
(экхимоз, кожное кровотечение, петехии), зуд;
— кровотечение мочевыводящих путей
(гематурия, геморрагический цистит);
— повышение уровня креатинина в
крови;
— послеоперационное кровотечение,
травматическое кровотечение (ушиб, травматическая гематома,
травматическое геморрагическое кровотечение)
Не часто
— опухолевые кровотечения
(кровотечения из опухолевых очагов мочевого пузыря, желудка, толстой
кишки);
— спутанность сознания;
— внутричерепное кровоизлияние;
— кровоизлияния глаза (внутриглазное,
конъюнктивальное, в сетчатку);
— ушное кровотечения;
— забрюшинное кровотечение;
— мышечное кровоизлияние (гемартроз,
мышечное кровотечение);
— кровотечения из органов
репродуктивной системы (вагинальное кровотечение, гематоспермия,
кровотечение в постменопаузе)
При
возникновении нежелательных лекарственных реакций обращаться к
медицинскому работнику, фармацевтическому работнику или напрямую в
информационную базу данных по нежелательным реакциям (действиям) на
лекарственные препараты, включая сообщения о неэффективности
лекарственных препаратов РГП
на ПХВ «Национальный Центр экспертизы лекарственных средств и
медицинских изделий» Комитет контроля качества и безопасности
товаров и услуг Министерства здравоохранения Республики Казахстан
http://www.ndda.kz
Дополнительные
сведения
Состав
лекарственного препарата
Одна
таблетка содержит
активное вещество —
тикагрелор 60 мг,
вспомогательные вещества-маннитол,
маннитол (гранулы), кальция гидрофосфата дигидрат, натрия
кроскармеллоза, гидроксипропилцеллюлоза, кремния диоксид коллоидный
безводный, магния стеарат
состав оболочки:
опадрай® 03B240022 розовый (Opadry® 03B240022 Pink),
гипромеллоза, титана диоксид (Е171), полиэтиленгликоль/макрогол,
железа оксид красный (Е172), железа оксид желтый (Е172), железа оксид
черный (Е172))
Описание внешнего вида, запаха,
вкуса
Круглые, двояковыпуклые таблетки,
покрытые пленочной оболочкой светло-розового цвета, с фаской
Форма выпуска и упаковка
По 14 таблеток помещают в контурную
ячейковую упаковку из фольги алюминиевой и пленки
поливинилхлорид/полиэтилен/поливинили-денхлоридной (PVC/PE/PVDC).
По 4 контурные ячейковые упаковки
вместе с инструкцией по медицинскому применению на казахском и
русском языках помещают в пачку из картона.
Срок хранения
2 года.
Не
применять по истечении срока годности!
Условия хранения
Хранить в
оригинальной упаковке при температуре не выше 25 °С.
Хранить в недоступном для детей
месте!
Условия отпуска из аптек
По
рецепту
Сведения о производителе
ТОО
«Абди Ибрахим Глобал Фарм»,
Республика
Казахстан, Алматинская обл., Илийский р-он, Промзона 282, тел.: +7
(727) 356-11-00, 8-800-070-1100,
адрес
электронной почты: info@aigp.kz
Держатель
регистрационного удостоверения
ТОО
«Абди Ибрахим Глобал Фарм»,
Республика
Казахстан, Алматинская обл., Илийский р-он, Промзона 282, тел.: +7
(727) 356-11-00, 8-800-070-1100,
адрес
электронной почты: info@aigp.kz
Наименование,
адрес и контактные данные организации на территории Республики
Казахстан, принимающей претензии (предложения) по качеству
лекарственных средств от потребителей и ответственной
за пострегистрационное наблюдение за безопасностью лекарственного
средства
ТОО
«Абди Ибрахим Глобал Фарм»,
Республика
Казахстан, Алматинская обл., Илийский р-он, Промзона 282, тел.:
+7 (727) 356-11-00,
8-800-070-11-00,
адрес
электронной почты: info@aigp.kz
| ИМП_(ЛВ)_Тривентин_60_мг_итог.docx | 0.05 кб |
| ИМП_(ЛВ)_Тривентин_60_мг_каз_10.20_Дурыс_.docx | 0.06 кб |
Отправить прикрепленные файлы на почту
активное вещество — тикагрелор 90 мг,
вспомогательные вещества: маннитол, кальция гидрофосфат, натрия крахмалгликолят, гидроксипропилцеллюлоза, магния стеарат,
состав оболочки: гипромеллоза 2910, титана диоксид (E171), тальк, полиэтиленгликоль 400, железа оксид жёлтый (E172).
Круглые двояковыпуклые таблетки, покрытые пленочной оболочкой желтого цвета, с гравировкой «» на одной стороне и гладкие на другой стороне.
Кровь и органы кроветворения. Антитромботические препараты. Ингибиторы агрегации тромбоцитов, за исключением гепарина. Тикагрелор.
Код АТХ B01AC24
Брилинта™ применяется совместно с ацетилсалициловой кислотой для профилактики атеротромботических событий у взрослых пациентов с
— острым коронарным синдромом
— инфарктом миокарда в анамнезе, а также высоким риском развития атеротромботического осложнения
— гиперчувствительность к действующему веществу или к любому вспомогательному веществу
— наличие патологического кровотечения
— внутричерепное кровоизлияние в анамнезе
— печеночная недостаточность тяжелой степени
— совместное применение тикагрелора с мощными ингибиторами CYP3A4 (например, кетоконазол, кларитромицин, нефазодон, ритонавир и атазанавир), так как совместное применение может привести к значительному увеличению воздействия тикагрелора
— беременность и период лактации
Препарат применяют по назначению врача. В следующих случаях также следует проконсультироваться с врачом перед применением препарата:
— повышенный риск развития кровотечения в связи с недавно полученной травмой, недавно проведенной или планируемой операцией, нарушениями свертываемости крови, активным или недавним желудочно-кишечным кровотечением
— повышенный риск развития брадикардии в отсутствие кардиостимулятора, одновременное применение с лекарственными средствами, которые, вызывают брадикардию
— астма или ХОБЛ в анамнезе
— печеночная недостаточность средней степени тяжести
— гиперурикемия или подагрический артрит в анамнезе
— увеличение содержания мочевой кислоты
— применение гепарина (одновременное применение может повлиять на результат диагностики тромбоцитопении)
Брилинта™ является, прежде всего, субстратом CYP3A4 и слабым ингибитором CYP3A4. Брилинта™ также является субстратом Р-гликопротеина и слабым ингибитором Р-гликопротеина и может увеличить воздействие субстратов Р-гликопротеина.
Влияние других лекарственных средств и веществ на тикагрелор
Ингибиторы CYP3A4
Мощные ингибиторы CYP3A4: совместное применение кетоконазола с тикагрелором увеличивает Сmах и AUC тикагрелора в 2.4 и 7.3 раза соответственно. Сmах и AUC активного метаболита уменьшаются на 89% и 56% соответственно. Другие мощные ингибиторы CYP3A4 (кларитромицин, нефазодон, ритонавир и атазанавир) будут оказывать такие же эффекты, поэтому их совместное применение с препаратом Брилинта™ противопоказано.
Умеренные ингибиторы CYP3A4: совместное применение дилтиазема с тикагрелором увеличивает Сmах тикагрелора на 69%, a AUC в 2.7 раз, при этом снижает Сmах активного метаболита на 38%, a AUC не меняется. Тикагрелор не влияет на плазменные концентрации дилтиазема. Другие умеренные ингибиторы CYP3A4 (например, ампренавир, апрепитант, эритромицин, флуконазол) можно назначать одновременно с препаратом Брилинта™.
Грейпфрутовый сок: усиление воздействия тикагрелора в 2 раза наблюдалось после ежедневного употребления большого количества грейпфрутового сока (3 раза в день по 200 мл). Ожидается, что данная величина повышенного воздействия не является клинически значимой для большинства пациентов.
Циклоспорин (ингибитор P-gp и CYP3A4)
Совместное применение циклоспорина (в дозе 600 мг) с тикагрелором увеличивает Cmax и AUC тикагрелора в 2.3 и 2.8 раз соответственно. При этом отмечается увеличение AUC активного метаболита на 32% и снижение Cmax на 15%. Нет данных о совместном применении тикагрелора с мощными ингибиторами Р-гликопротеина (например, верапамил и хинидин). Если совместного применения избежать невозможно, то комбинированную терапию следует проводить с осторожностью.
Индукторы CYP3A
Совместное применение рифампицина с тикагрелором снижает Сmах и AUC тикагрелора на 73% и 86% соответственно. Сmах активного метаболита не меняется, a AUC понижается на 46%. Другие индукторы CYP3A4 (например, фенитоин, карбамазепин и фенобарбитал), по-видимому, будут снижать экспозицию препарата Брилинта™. Мощные индукторы CYP3A4 могут уменьшать экспозицию и эффективность препарата Брилинта™, поэтому их одновременное применение не рекомендуется.
Другие препараты
По результатам фармакологических исследований взаимодействия сопутствующее применение тикагрелора с гепарином, эноксапарином и ацетилсалициловой кислотой или десмопрессином не влияет на фармакокинетику тикагрелора, его активного метаболита и АДФ-зависимую агрегацию тромбоцитов. В случае наличия клинических показаний к назначению препаратов, влияющих на гемостаз, их следует применять с осторожностью в комбинации с препаратом Брилинта™.
Задержка и снижение воздействия пероральных ингибиторов P2Y12, включая тикагрелор и его активный метаболит, наблюдалось у пациентов с ОКС, получавших морфин (снижение воздействия тикагрелора на 35%). Это взаимодействие может быть связано со снижением моторики желудочно-кишечного тракта и может распространяться на другие опиоиды. Клиническая значимость данного эффекта неизвестна, но данные указывают на возможность снижения эффективности тикагрелора у пациентов, принимающих одновременно тикагрелор и морфин. Пациентам с ОКС, у которых прекращение приема морфина невозможно и у которых быстрое ингибирование P2Y12 считается решающим, необходимо рассмотреть возможность применения парентерального ингибитора P2Y12.
Влияние тикагрелора на другие лекарственные средства
Лекарственные препараты, метаболизирующиеся изоферментом CYP3A4
Симвастатин: сопутствующее применение тикагрелора и симвастатина повышает Сmах и AUC симвастатина на 81% и 56% соответственно; Сmах и AUC симвастатиновой кислоты увеличиваются на 64% и 52% соответственно, при этом, в некоторых случаях эти показатели повышаются в 2-3 раза. Совместное применение симвастатина в дозе выше 40 мг/сут с тикагрелором может приводить к развитию побочных эффектов симвастатина. Поэтому при необходимости данной комбинации следует оценить соотношение потенциального риска и пользы терапии. Не рекомендуется совместное применение препарата Брилинта™ с симвастатином и ловастатином в дозе свыше 40 мг.
Аторвастатин: сопутствующее применение аторвастатина и тикагрелора повышает Сmах и AUC метаболитов аторвастатиновой кислоты на 23% и 36% соответственно. Подобное увеличение значений Cmax и AUC наблюдается для всех метаболитов аторвастатиновой кислоты. Эти изменения признаны клинически не значимыми.
Сходные эффекты со статинами, метаболизирующимися CYP3A4, не могут быть исключены. В исследовании PLATO у 93% пациентов в группе, получавшей тикагрелор и различные статины, не наблюдалось каких-либо нежелательных признаков, касающихся безопасности статинов.
Тикагрелор — умеренный ингибитор CYP3A4. Совместное применение препарата Брилинта™ и субстратов CYP3A4 с узким терапевтическим индексом (например, цизаприд или алкалоиды спорыньи) не рекомендуется, т.к. тикагрелор может увеличивать экспозицию этих препаратов.
Лекарственные препараты, метаболизирующиеся изоферментом CYP2C9
При одновременном применении тикагрелора и толбутамида не изменялись плазменные концентрации ни одного из этих препаратов. Это свидетельствует о том, что тикагрелор не является ингибитором изофермента CYP2C9, и, маловероятно, что он влияет на CYP2C9-опосредованный метаболизм препаратов, подобных варфарину и толбутамиду.
Пероральные контрацептивы
Совместное применение тикагрелора, левоноргестрела и этинилэстрадиола увеличивает экспозицию этинилэстрадиола примерно на 20%, но не влияет на фармакокинетику левоноргестрела. Не ожидается клинически значимого воздействия на эффективность контрацепции при одновременном применении левоноргестрела, этинилэстрадиола и препарата Брилинта™.
Субстрат P-gp (включая дигоксин и циклоспорин)
Сопутствующее применение дигоксина с тикагрелором повышает Сmах и AUC дигоксина на 75% и 28% соответственно. При совместном приеме с тикагрелором в среднем Сmin дигоксина увеличивалась на 30%, в отдельных случаях — в 2 раза. Сmах и AUC тикагрелора при применении дигоксина не менялись. Поэтому рекомендуется проводить соответствующий клинический и/или лабораторный мониторинг при одновременном применении препарата Брилинта™ и P-gp-зависимых препаратов с узким терапевтическим индексом, наподобие дигоксина и циклоспорина.
Лекарственные средства, вызывающие брадикардию
Признаков клинически значимых побочных реакций после сопутствующего введения одного или нескольких лекарственных препаратов, о которых известно, что они вызывают брадикардию (например, бета-блокаторов, блокаторов кальциевых каналов, дилтиазем и верапамил, и дигоксин) не наблюдалось. Следует соблюдать осторожность при одновременном назначении тикагрелора с лекарственными средствами, которые, вызывают брадикардию.
Другая сопутствующая терапия
В клинических исследованиях препарат Брилинта™ преимущественно назначался совместно с ацетилсалициловой кислотой, ингибиторами протоновой помпы, статинами, бета-адреноблокаторами, ингибиторами АПФ и антагонистами рецепторов ангиотензина в рамках длительного приема, а также с гепарином, низкомолекулярными гепаринами, ингибиторами гликопротеиновых IIb/IIIа рецепторов для в/в введения в рамках краткосрочной терапии. По результатам этих исследований не выявлено клинически значимого нежелательного взаимодействия.
Совместное применение препарата Брилинта™ с гепарином, эноксапарином или десмопрессином не оказывало влияния на АЧТВ, активированное время свертывания (ABC) и исследование фактора Ха, однако вследствие потенциального фармакодинамического взаимодействия, требуется соблюдать осторожность при совместном применении с препаратами, влияющими на гемостаз.
В связи с сообщениями о подкожных кровоизлияниях на фоне применения селективных ингибиторов обратного захвата серотонина (например, пароксетин, сертралин и циталопрам), рекомендуется соблюдать осторожность при их совместном приеме с препаратом Брилинта™.
Риск развития кровотечения
Как и при применении других антитромботических препаратов, при назначении препарата Брилинта™ следует оценить соотношение пользы от профилактики тромботических событий и риска у пациентов с повышенным риском развития кровотечений. При наличии клинических показаний тикагрелор следует применять с осторожностью следующим группам пациентов:
— Пациенты с предрасположенностью к развитию кровотечения (например, в связи с недавно полученной травмой, недавно проведенной операцией, нарушениями свертываемости крови, активным или недавним желудочно-кишечным кровотечением). Прием тикагрелора противопоказан пациентам с активным патологическим кровотечением, с внутричерепным кровоизлиянием в анамнезе и тяжелой печеночной недостаточностью.
— Пациенты с сопутствующим применение препаратов, которые могут повысить риск развития кровотечения (например, нестероидные противовоспалительные препараты, пероральные антикоагулянты и/или фибринолитики), принимаемые в течение 24 часов до приема препарата Брилинта™.
Трансфузия тромбоцитами не обратила антиагрегационный эффект тикагрелора у здоровых пациентов, и ее клиническая польза у пациентов с кровотечением маловероятна; Так как при сопутствующем применении препарата Брилинта™ и десмопрессина не уменьшалось стандартизированное время кровотечения, то маловероятно, что десмопрессин будет эффективно купировать кровотечение.
Антифибринолитическая терапия (аминокапроновая кислота или транексамовая кислота) и/или рекомбинантный фактор VIIa могут усиливать гемостаз. После установления причины кровотечения и его купирования можно возобновить терапию препаратом Брилинта™.
Хирургические операции
Пациенты должны сообщить терапевту и стоматологам, что они принимают тикагрелор, до того, как будет спланирована любая хирургическая операция, и до начала приема нового лекарственного препарата.
Если пациенту предстоит плановая операция, в связи с чем антитромботический эффект нежелателен, прием тикагрелора следует прекратить за 5 дней до хирургического вмешательства.
Пациенты, перенесшие ишемический инсульт
Пациенты с ОКС, ранее перенесшие ишемический инсульт, могут получать терапию тикагрелором не более 12 месяцев.
Печеночная недостаточность
Пациентам с острой печеночной недостаточностью противопоказано применение тикагрелора. Опыт применения тикагрелора у пациентов с умеренной печеночной недостаточностью является небольшим, в связи с чем рекомендуется проявлять осторожность при лечении этих больных.
Пациенты с риском развития брадикардии
Холтеровское суточное мониторирование ЭКГ показало повышенную частоту в основном бессимптомных желудочковых пауз во время лечения тикагрелором по сравнению с клопидогрелом.
Пациенты с повышенным риском развития брадикардии (например, больные без кардиостимулятора, у которых диагностирован синдром слабости синусового узла, атриовентрикулярная блокада 2-ой или 3-ей степени; обморок, связанный с брадикардией) не были включены в основное исследование для оценки безопасности и эффективности препарата Брилинта™. Поэтому, в связи с ограниченным клиническим опытом применения препарата, рекомендуется с осторожностью назначать препарат Брилинта™ таким пациентам. Кроме того, следует соблюдать осторожность при приеме тикагрелора одновременно с лекарственными препаратами, которые могут вызвать брадикардию.
Одышка
Одышка, отмеченная при применении препарата Брилинта™, обычно слабая или умеренная по своей интенсивности, часто проходит по мере продолжения терапии препаратом. Пациенты с астмой/хронической обструктивной болезнью легких (ХОБЛ) могут иметь увеличенный абсолютный риск возникновения одышки при приеме тикагрелора. Тикагрелор следует использовать с осторожностью пациентами с астмой/ХОБЛ в анамнезе. Механизм до настоящего времени не установлен. Если у пациента развился новый эпизод, одышка сохранилась или усилилась, необходимо провести полное обследование. Если установлено, что одышка вызвана терапией препаратом Брилинта™, прием препарата Брилинта™ следует прекратить.
Повышение креатинина
Во время лечения препаратом Брилинта™ уровни креатинина могут повыситься. Механизм не выяснялся. Почечную функцию следует проверять согласно рутинной медицинской практике. У пациентов с ОКС, почечную функцию рекомендуется проверять через 1 месяц после начала лечения тикагрелором, обращая особое внимание на пациентов старше 75 лет, пациентов со средней/тяжелой почечной недостаточностью и на тех, кто получает сопутствующее лечение блокаторами рецепторов ангиотензина-II (ARB).
Повышение мочевой кислоты
Гиперурикемия может возникнуть при лечении тикагрелором. Следует соблюдать меры предосторожности при приеме Брилинты пациентами, у которых в анамнезе есть гиперурикемия или подагрический артрит. В качестве меры предосторожности, использование Брилинты у пациентов с мочекислой нефропатией не рекомендуется.
Тромботическая тромбоцитопеническая пурпура (ТТП)
О возникновении тромботической тромбоцитопенической пурпуры (ТТП) при использовании тикагрелора сообщалось очень редко.
Она характеризуется тромбоцитопенией и микроангиопатической гемолитической анемией, связанной с неврологическими явлениями, почечной дисфункцией или лихорадкой. ТТП является потенциально смертельным состоянием, требующим немедленного лечения, включая плазмаферез.
Влияние на лабораторные показатели тромбоцитов при диагностике гепарин-индуцированной тромбоцитопении (ГИТ)
При проведении теста гепарин-индуцированной агрегации тромбоцитов (HIPA), который применяется для диагностики ГИТ происходит агрегация тромбоцитов в сыворотке крови пациента в присутствии гепарина.
У пациентов, которые принимают тикагрелор, могут наблюдаться ложноотрицательные результаты теста функции тромбоцитов (включая, но не ограничиваясь HIPA) при диагностике ГИТ. Это связано с ингибированием P2Y12-рецептора. Информация о сопутствующем лечении тикагрелором необходима для интерпретации ГИТ при тестировании функции тромбоцитов.
У пациентов, у которых наблюдается развитие ГИТ, продолжение лечения тикагрелором возможно только после оценки соотношения риска и пользы, принимая во внимание как протромботическое состояние ГИТ, так и повышенный риск кровотечения с сопутствующим лечением антикоагулянтами и тикагрелором.
Другие
Совместный прием тикагрелора и высокой поддерживающей дозы АСК (более 300 мг) не рекомендуется.
Преждевременное прекращение терапии
Преждевременное прекращение любой антиагрегантной терапии, включая лечение Брилинтой, может привести к повышенному риску смерти от сердечно-сосудистого заболевания, инфаркта миокарда или инсульта из-за основного заболевания пациента. Поэтому следует избегать преждевременного прекращения лечения.
Безопасность и эффективность препарата Брилинта™ у детей младше 18 лет не установлена.
Женщины детородного возраста должны применять соответствующие противозачаточные средства, чтобы избежать беременности во время лечения тикагрелором. Практически нет никаких данных об использовании тикагрелора беременными женщинами. Прием тикагрелора во время беременности не рекомендуется. При кормлении грудью риск для новорожденных/младенцев не может быть исключен. Следует принять решение относительно того, прекратить ли кормление грудью или лечение тикагрелором, с учетом пользы кормления грудью для ребенка и пользы лечения для женщины.
Брилинта™ не влияет или незначительно влияет на способность управлять автотранспортом и механизмами. При лечении тикагрелором наблюдалось головокружение. Поэтому пациентам с такими симптомами следует с осторожностью водить автотранспорт или работать с механизмами.
Пациенты, принимающие препарат Брилинта™, должны ежедневно принимать поддерживающую дозу ацетилсалициловой кислоты (АСК) в объеме 75-150 мг, если отсутствуют специфические противопоказания.
Способ применения и дозы
Для перорального применения.
Препарат Брилинта™ можно применять независимо от приема пищи. Для пациентов, которые не могут проглотить таблетку целиком, таблетки могут быть измельчены в мелкий порошок и смешаны с половиной стакана воды, при условии немедленного приема. Стакан следует промыть еще одной половиной стакана воды и выпить содержимое. Смесь также можно принять через назогастральный зонд (СН8 или больше). Важно промыть назогастральный зонд водой после приема смеси.
Острый коронарный синдром
Применение препарата Брилинта™ следует начинать с однократной нагрузочной дозы 180 мг (две таблетки по 90 мг) и затем продолжать прием по 90 мг два раза в сутки. Пациентам с острым коронарным синдромом рекомендуется проводить лечение препаратом Брилинта™ 90 мг в течение 12 месяцев, кроме случаев клинической необходимости в досрочной отмене препарата.
Инфаркт миокарда в анамнезе
Брилинта™ 60 мг дважды в день является рекомендуемой дозой в случае возникновения необходимости в длительном лечении пациентов, у которых в анамнезе по крайней мере одного года есть инфаркт миокарда, а также пациентов, которые находятся в группе риска возникновения атеротромботических осложнений. Лечение можно начать без перерыва, в качестве продолжения терапии после первоначального годичного лечения препаратом Брилинта™ по 90 мг или лечения другим ингибитором рецепторов аденозиндифосфата (АДФ) у пациентов с ОКС, подверженных риску возникновения атеротромботических осложнений. Лечение также можно начать в течение 2 лет после ИМ или в течение одного года после окончания предыдущего лечения ингибитором рецептора АДФ. Данные об эффективности препарата Брилинта™ после 3 лет длительного лечения являются ограниченными.
Если необходимо провести изменение, первую дозу препарата Брилинта™ нужно ввести в течение 24 часов после приема последней дозы антитромбозитарного препарата.
Тикагрелор хорошо переносится при однократной дозе препарата до 900 мг.
Симптомы:
Кровотечение является предполагаемым фармакологическим действием передозировки препаратом Брилинта™, поэтому при развитии кровотечения необходимо проводить соответствующие поддерживающие мероприятия. Другие клинически значимые побочные реакции, которые могут встречаться при передозировке, включают диспноэ и эпизоды желудочковой асистолии.
Лечение:
специфического антидота не существует. В случае передозировки лечение следует проводить в соответствии с местными стандартами медицинской практики. При развитии кровотечения необходимо проводить соответствующие поддерживающие мероприятия. Тикагрелор не выводится при гемодиализе. Рекомендуется общая поддерживающая терапия, наблюдение за больным и контроль функции жизненно важных органов и систем (ЭКГ-мониторинг).
Меры, необходимые при пропуске одной или нескольких доз
Необходимо избегать отклонений в лечении. Пациент, пропустивший прием дозы препарата Брилинта™, должен принять только одну таблетку (следующую дозу) по расписанию.
Особые группы пациентов
Пожилые пациенты
Коррекция дозы не требуется.
Пациенты с почечной недостаточностью
Пациентам с почечной недостаточностью коррекция дозы не требуется.
Пациенты с печеночной недостаточностью
У пациентов с тяжелой степенью печеночной недостаточности использование препарата Брилинта™ противопоказано. Пациентам с умеренной печеночной недостаточностью коррекция дозы не требуется, однако применение тикагрелора должно осуществляться с осторожностью. Пациентам с легкой степенью печеночной недостаточности коррекция дозы не требуется.
Нежелательные реакции классифицированы по частоте развития. Категории частоты определяются в соответствии со следующими условными обозначениями: очень часто (≥ 1/10), часто (≥ 1/100 до <1/10), не часто (≥1/1000 до <1/100), редко (≥1/10000 до <1/1000), очень редко (<1/10000), неизвестно (исходя из известных данных, не может быть оценена).
Очень часто
— кровотечения при заболевании крови
— гиперурикемия
— одышка
Часто (≥1/100 до <1/10)
— подагра, подагрический артрит
— головокружение, синкопе, головная боль
— вертиго
— гипотензия
— кровотечения дыхательной системы
— кровотечение из желудочно-кишечного тракта, рвота, диарея, боль в животе, тошнота, диспепсия, констипация
— подкожное или кожное кровотечение, сыпь, зуд
— кровотечение из мочевыводящих путей
— повышение уровня креатинина в крови
— послеоперационное кровотечение, травматическое кровотечение
Не часто (≥1/1000 до <1/100)
— опухолевое кровотечение
— повышенная чувствительность, в том числе ангионевротический отек
— спутанность сознания
— внутричерепное кровоизлияние
— кровоизлияния глаза (внутриглазное, конъюнктивальное, в сетчатку)
— ушные кровотечения
— забрюшинное кровотечение
— мышечные кровотечения
— кровотечения органов репродуктивной системы
Неизвестно (исходя из известных данных, не может быть оценена)
— тромботическая тромбоцитопеническая пурпура
При возникновении нежелательных лекарственных реакций обращаться к медицинскому работнику, фармацевтическому работнику или напрямую в информационную базу данных по нежелательным реакциям (действиям) на лекарственные препараты, включая сообщения о неэффективности лекарственных препаратов
РГП на ПХВ «Национальный Центр экспертизы лекарственных средств и медицинских изделий» Комитет контроля качества и безопасности товаров и услуг Министерства здравоохранения Республики Казахстан http://www.ndda.kz
По 14 таблеток помещают в контурную ячейковую упаковку из пленки поливинилхлорид/поливинилиденхлорид и фольги алюминиевой печатной лакированной.
По 4 или 12 контурных ячейковых упаковок вместе с инструкцией по медицинскому применению на казахском и русском языках помещают в пачку из картона.
Хранить при температуре не выше 30°С.
Хранить в недоступном для детей месте!
По рецепту
Производитель
АстраЗенека АБ, 18 СЕ- 151 85, Содерталье, Швеция
Тел.: +46 8 553 260 00
Факс: +46 8 553 290 00
Адрес электронной почты: adverse.events.kz@astrazeneca.com
Упаковщик
АстраЗенека АБ, 18 СЕ- 151 85, Содерталье, Швеция
Владелец регистрационного удостоверения
АстраЗенека АБ, 18 СЕ- 151 85, Содерталье, Швеция
Тел.: +46 8 553 260 00
Факс: +46 8 553 290 00
Наименование, адрес и контактные данные (телефон, факс, электронная почта) организации на территории Республики Казахстан, принимающей претензии (предложения) по качеству лекарственных средств от потребителей и ответственной за пострегистрационное наблюдение за безопасностью лекарственного средства
Представительство ЗАК “АстраЗенека Ю-Кей Лимитед”,
Республика Казахстан, г. Алматы, 050022
Ул. Шевченко, 144
Телефон: +7 727 232 14 15; +7 701 0326745
e-mail:
adverse.events.kz@astrazeneca.com
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-001059
Торговое название:
Брилинта®
Международное непатентованное название:
тикагрелор
Лекарственная форма:
таблетки, покрытые плёночной оболочкой
Состав на 1 таблетку:
Активное вещество: тикагрелор 90 мг
Вспомогательныевещества: маннитол 126 мг, кальция гидрофосфат 63 мг, карбоксиметилкрахмал натрия 9 мг, гипролоза 9 мг, магния стеарат 3 мг;
всоставеплёночнойоболочкитаблетки: гипромеллоза 2910 5,6 мг, титана диоксид E 171 1,7 мг, тальк 1,0 мг, макрогол 400 0,6 мг, краситель железа оксид жёлтый E 172 0,1 мг.
Описание
Круглые, двояковыпуклые таблетки, покрытые плёночной оболочкой жёлтого цвета, с гравировкой 90 на одной стороне.
ФАРМАКОТЕРАПЕВТИЧЕСКАЯ ГРУППА:
антиагрегантное средство
Код АТХ: В01АС24
ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА
Механизм действия
Препарат Брилинта® содержит в своем составе тикагрелор, представитель химического класс циклопентилтриазолопиримидинов, который является пероральным, селективным и обратимым антагонистом P2Y12 рецепторов прямого действия и предотвращает аденозиндифосфат-опосредованную P2Y12-зависимую активацию и агрегацию тромбоцитов. Тикагрелор не предотвращает связывание аденозиндифосфата (АДФ), но его взаимодействие с Р2Y12 рецептором тромбоцитов предотвращает АДФ-индуцированную трансдукцию сигналов. Так как тромбоциты участвуют в инициировании и/или развитии тромботических осложнений атеросклероза, было показано, что ингибирование функции тромбоцитов уменьшает риск развития сердечно-сосудистых явлений, таких как летальный исход, инфаркт миокарда или инсульт.
Тикагрелор имеет дополнительный механизм действия, повышая локальные концентрации эндогенного аденозина путем ингибирования эндогенного равновесного нуклеозидного транспортера (ENT-1).
Аденозин образуется локально в местах гипоксии и повреждения тканей путем высвобождения из аденозинтрифосфата и АДФ. Тикагрелор ингибирует ENT-1 и продлевает период полувыведения аденозина, тем самым увеличивая его локальную внеклеточную концентрацию, усиливая локальный аденозиновый
ответ. Тикагрелор не имеет клинически значимого прямого влияния на аденозиновые рецепторы (A1, A2a, A2b, A3) и не метаболизируется до аденозина.
Аденозин обладает следующими эффектами, которые включают в себя: вазодилатацию, кардиопротекцию, ингибирование агрегации тромбоцитов, модуляцию воспаления и возникновение одышки, которые могут влиять на клинический профиль тикагрелора. Было показано, что у здоровых добровольцев и у пациентов с острым коронарным синдромом (ОКС) тикагрелор усиливал следующие эффекты аденозина: вазодилатацию (оцениваемую как увеличение коронарного кровотока у здоровых добровольцев; головную боль), ингибирование функции тромбоцитов ( in vitro в цельной человеческой крови) и одышку. Тем не менее, связь повышенных локальных концентраций аденозина с клиническими исходами (показатели заболеваемости и смертности) не доказана.
Фармакодинамика
Начало действия
У пациентов со стабильным течением ишемической болезни сердца (ИБС) на фоне применения ацетилсалициловой кислоты тикагрелор начинает быстро действовать, что подтверждается результатами определения среднего значения ингибирования агрегации тромбоцитов (ИАТ): через 0,5 часа после приема нагрузочной дозы 180 мг тикагрелора среднее значение ИАТ составляет примерно 41%, максимальное значение ИАТ 89% достигается через 2-4 часа после приема препарата и поддерживается в течение 2-8 часов. У 90% пациентов окончательное значение ИАТ более 70% достигается через 2 часа после приема препарата.
Конец действия
При планировании АКШ, риск кровотечений возрастает, если тикагрелор прекращают менее, чем за 96 часов до процедуры.
Данные о переходе с одного препарата на другой
Переход с клопидогрела на тикагрелор приводит к увеличению абсолютного значения ИАТ на 26,4%, а изменение терапии с тикагрелора на клопидогрел приводит к снижению абсолютного значения ИАТ на 24,5%. Можно менять терапию с клопидогрела на тикагрелор без прерывания антитромботического эффекта.
Клиническая эффективность
В исследовании PLATO (PLATelet Inhibition and Patient Outcomes – Ингибирование тромбоцитов и исходы у пациентов) участвовало 18 624 пациента, у которых за последние 24 часа развились симптомы нестабильной стенокардии, инфаркта миокарда без подъема сегмента ST или инфаркта миокарда с подъемом сегмента ST и которые лечились консервативно, или посредством чрескожного коронарного вмешательства (ЧКВ), или аортокоронарного шунтирования (АКШ) (см. раздел «Показания к применению»). В этом исследовании на фоне ежедневной терапии ацетилсалициловой кислотой тикагрелор 90 мг дважды в сутки сравнивался с клопидогрелом 75 мг в сутки в отношении эффективности в предупреждении развития комбинированной конечной точки сердечно-сосудистой смерти, инфаркта миокарда или инсульта за счет влияния на частоту сердечнососудистых смертей и инфарктов миокарда. Нагрузочная доза составляла 300 мг клопидогрела (доза 600 мг также допускалась при проведении ЧКВ) или 180 мг тикагрелора.
Эффект тикагрелора проявлялся рано (на 30 день снижение абсолютного риска (САР) на 0,6% и снижение относительного риска (СОР) на 12%), с поддержанием постоянного эффекта терапии в течение 12 месяцев, что приводило к снижению абсолютного риска (САР) на 1,9% и снижению относительного риска (СОР) на 16% в течение года.
Брилинта® снижает относительный риск комбинированной конечной точки (совокупность сердечно-сосудистых смертей, инфаркта и инсульта) у пациентов с нестабильной стенокардией, инфарктом миокарда без подъема сегмента ST и инфарктом миокарда с подъемом сегмента ST на 16% (отношение рисков (ОР) 0,84; 95% доверительный интервал (ДИ) 0,77-0,92; p = 0,0003), сердечно-сосудистой смерти на 21% (ОР 0,79; 95% ДИ 0,69-0,91; р=0,0013), инфаркта миокарда на 16% (ОР 0,84; 95% ДИ 0,75-0,95; р=0,0045).
Эффективность препарата Брилинта® показана у различных подгрупп пациентов, независимо от массы тела, пола, наличия в анамнезе сахарного диабета, транзиторной ишемической атаки или негеморрагического инсульта, реваскуляризации, сопутствующей терапии (включая гепарин, ингибиторы гликопротеиновых llb/llla рецепторов (см. раздел «Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия»), окончательного диагноза (инфаркт миокарда без подъема сегмента ST, инфаркт миокарда с подъемом сегмента ST и нестабильная стенокардия) и лечения, запланированного при рандомизации (инвазивное или консервативное). Дополнительный анализ позволил предположить наличие возможной связи с дозой ацетилсалициловой кислоты, которая выражалась в том, что пониженная эффективность наблюдалась при приеме препарата Брилинта® в комбинации с повышенными дозами ацетилсалициловой кислоты. Рекомендуемая доза ацетилсалициловой кислоты для постоянного приема в сочетании с препаратом Брилинта® — 75-150 мг (см. разделы «Способ применения и дозы» и «Особые указания»).
Брилинта® продемонстрировала статистически значимое СОР по совокупному критерию: смерть от сердечно-сосудистых причин, инфаркт миокарда и инсульт — у пациентов с острым коронарным синдромом, которым запланировано инвазивное вмешательство (СОР 16%, САР 1,7%, р=0,0025). В поисковом анализе Брилинта® также продемонстрировала СОР по первичной конечной точке у пациентов с острым коронарным синдромом, которым назначалась консервативная терапия (СОР 15%, САР 2,3%, номинальное р=0,0444). У пациентов после стентирования при применении тикагрелора отмечалось снижение частоты тромбоза стентов (СОР 32%, САР 0,6%, номинальное р=0,0123).
Брилинта® вызывала статистически значимое СОР на 16% (САР 2,1%) по такому совокупному критерию как смерть от всех причин, инфаркт миокарда и инсульт. СОР смерти от всех причин на приеме препарата Брилинта® составляло 22% при номинальном уровне значимости р=0,0003 и САР — 1,4%.
Совокупный критерий объединенной эффективности и безопасности
Совокупный критерий объединенной эффективности и безопасности (смерть от сердечно-сосудистых причин, инфаркт миокарда, инсульт или большое кровотечение по определению исследования PLATO) подтверждает, что в течение 12 месяцев после острого коронарного синдрома положительный эффект тикагрелора не нейтрализуется случаями больших кровотечений (СОР 8%, САР 1,4%, OP 0,92; p=0,0257).
Фармакокинетика
Тикагрелор демонстрирует линейную фармакокинетику, и экспозиция тикагрелора и активного метаболита (AR-C124910XX) примерно пропорциональна дозе вплоть до 1260 мг.
Абсорбция
Тикагрелор быстро абсорбируется со средней tmax примерно 1,5 часа. Формирование основного циркулирующего в крови метаболита AR-C124910XX (также активного) из тикагрелора происходит быстро со средней tmax примерно 2,5 часа. После приема натощак тикагрелора в дозе 90 мг Cmax составляет 529 нг/мл и AUC – 3451 нг*ч/мл.
Средняя абсолютная биодоступность тикагрелора составляет 36%. Прием жирной пищи не влияет на Cmax тикагрелора или AUC активного метаболита, но приводит к повышению на 21% AUC тикагрелора и снижению на 22% Cmax активного метаболита. Эти небольшие изменения имеют минимальную клиническую значимость; поэтому тикагрелор можно назначать вне зависимости от приема пищи.
Тикагрелор в виде суспензии измельченных таблеток в питьевой воде, принятой внутрь или введенной в желудок через назогастральный зонд, биоэквивалентен тикагрелору, принятому внутрь в виде таблеток препарата Брилинта ® (AUC и Cmax тикагрелора и активного метаболита в диапазоне 80-125%).
В случае приема суспензии первоначальная экспозиция (через 0,5 ч и 1 ч после приема) была выше, чем при приеме тикагрелора в виде таблеток препарата Брилинта ®, но в дальнейшем (от 2 до 48 часов) профиль концентраций был практически одинаковым.
Распределение
Объем распределения тикагрелора в равновесном состоянии составляет 87,5 л. Тикагрелор и активный метаболит активно связываются с белками плазмы крови (> 99%).
Метаболизм
CYP3A4 является основным изоферментом, отвечающим за метаболизм тикагрелора и формирование активного метаболита, и их взаимодействия с другими субстратами CYP3A варьируют от активации до ингибирования.
Тикагрелор и активный метаболит являются слабыми ингибиторами гликопротеина Р (P-gp).
Основным метаболитом тикагрелора является AR-C124910XX, который также активен, что подтверждается результатами оценки связывания с P2Y12 рецептором АДФ тромбоцитов in vitro. Системная экспозиция активного метаболита составляет примерно 30-40% от экспозиции тикагрелора.
Экскреция
Основной путь выведения тикагрелора – через печеночный метаболизм. При введении меченного изотопом тикагрелора в среднем примерно 57,8% радиоактивности выделяется с фекалиями, 26,5% с мочой. Выведение тикагрелора и активного метаболита с мочой составляет менее 1% дозы. В основном активный метаболит выводится с желчью. Средний период полувыведения тикагрелора и активного метаболита составлял 7 и 8,5 часов, соответственно.
Особые популяции больных
Пожилые пациенты
У пожилых пациентов (в возрасте от 75 лет и старше) отмечена более высокая экспозиция тикагрелора (Cmax и AUC примерно на 25% выше) и активного метаболита по сравнению с молодыми пациентами. Эти различия не считаются клинически значимыми (см. раздел «Способ применения и дозы»).
Дети
Нет данных по применению тикагрелора у детей.
Пол
У женщин отмечена более высокая экспозиция тикагрелора и активного метаболита по сравнению с мужчинами. Эти различия не считаются клинически значимыми.
Этнические группы
Средняя биодоступность препарата у пациентов-азиатов на 39% выше, чем у европеоидов. Биодоступность препарата Брилинта ® на 18% ниже у пациентов негроидной расы по сравнению с больными европеоидной расы.
Почечная недостаточность
Экспозиция тикагрелора примерно на 20% ниже, а его активного метаболита примерно на 17% выше у пациентов с тяжелой почечной недостаточностью (клиренс креатинина < 30 мл/мин) по сравнению с пациентами с нормальной функцией почек (см. раздел «Способ применения и дозы»).
Печеночная недостаточность
Сmах и AUC тикагрелора были на 12% и 23% выше у пациентов с печеночной недостаточностью легкой степени по сравнению со здоровыми добровольцами. Не проводились исследования тикагрелора у пациентов с умеренной или тяжелой печеночной недостаточностью, и его использование у этих пациентов противопоказано (см. разделы «Способ применения и дозы» и «Противопоказания»).
ПОКАЗАНИЯ К ПРИМЕНЕНИЮ
Брилинта®, применяемая одновременно с ацетилсалициловой кислотой, показана для профилактики атеротромботических событий у пациентов с острым коронарным синдромом (нестабильной стенокардией, инфарктом миокарда без подъема сегмента ST или инфарктом миокарда с подъемом сегмента ST [STEMI]), включая больных, получавших лекарственную терапию, и пациентов, подвергнутых чрескожному коронарному вмешательству (ЧКВ) или аортокоронарному шунтированию (АКШ)).
ПРОТИВОПОКАЗАНИЯ
- Повышенная чувствительность к тикагрелору или любому из компонентов препарата
- Активное патологическое кровотечение
- Внутричерепное кровоизлияние в анамнезе
- Умеренная или тяжелая печеночная недостаточность
- Совместное применение тикагрелора с мощными ингибиторами CYP3A4 (например, кетоконазолом, кларитромицином, нефазодоном, ритонавиром и атазанавиром)
- Детский возраст до 18 лет (в связи с отсутствием данных об эффективности и безопасности применения у данной группы пациентов)
С ОСТОРОЖНОСТЬЮ
Предрасположенность пациентов к развитию кровотечения (например, в связи с недавно полученной травмой, недавно проведенной операцией, нарушениями свертываемости крови, активным или недавним желудочно-кишечным кровотечением) (см. раздел «Особые указания»).
Пациенты с сопутствующей терапией препаратами, повышающими риск кровотечений (т.е. нестероидные противовоспалительные препараты, пероральные антикоагулянты и/или фибринолитики) в течение 24 часов до приема препарата Брилинта ®.
Пациенты с повышенным риском развития брадикардии (например, больные с синдромом слабости синусового узла без кардиостимулятора, с атриовентрикулярной блокадой 2-ой или 3-ей степени; обмороком, связанным с брадикардией) в связи с недостаточным опытом клинического применения препарата Брилинта ® (см. раздел «Особые указания»). При совместном применении с препаратами, вызывающими брадикардию.
Тикагрелор должен использоваться с осторожностью у пациентов с бронхиальной астмой и хронической обструктивной болезнью легких (ХОБЛ). Если пациент сообщает о возникновении нового эпизода одышки, о длительной одышке или ухудшении одышки, необходимо провести обследование, и в случаенепереносимости, лечение тикагрелором должно быть прекращено.
На фоне приема препарата Брилинта® уровень креатинина может повыситься (см. разделы «Побочное действие», «Особые указания»), в связи с чем необходимо производить оценку почечной функции в соответствии с рутинной клинической практикой, обращая особое внимание на пациентов от 75 лет и старше, пациентов с умеренной или тяжелой почечной недостаточностью, пациентов, получающих терапию антагонистами рецепторов к ангиотензину.
Необходимо соблюдать осторожность у пациентов с гиперурикемией или подагрическим артритом в анамнезе. В качестве превентивной меры следует избегать применения тикагрелора у пациентов с гиперурикемической нефропатией.
Не рекомендуется совместное применение тикагрелора и высокой поддерживающей дозы ацетилсалициловой кислоты (более 300 мг).
При совместном применении дигоксина и препарата Брилинта® рекомендован тщательный клинический и лабораторный мониторинг (частоты сердечных сокращений, и при наличии клинических показаний также ЭКГ и концентрации дигоксина в крови).
Нет данных о совместном применении тикагрелора с мощными ингибиторами гликопротеина P (например, верапамил и хинидин), в связи с чем их совместное применение должно осуществляться с осторожностью (см. раздел «Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия»).
БЕРЕМЕННОСТЬ И ПЕРИОД ЛАКТАЦИИ
Данные о применении препарата Брилинта ® у беременных женщин отсутствуют или ограничены.
В исследованиях на животных тикагрелор вызывал незначительное снижение прибавки массы тела у матери, снижение жизнеспособности новорожденного и его массы тела, замедление роста. Брилинта ® не рекомендована во время беременности.
Доступные фармакодинамические, токсикологические данные у животных показали, что тикагрелор и его активные метаболиты выделяются с молоком. Не может быть исключен риск для новорожденного/младенца. Не рекомендуется применять препарат Брилинта ® в период кормления ребенка грудью.
СПОСОБ ПРИМЕНЕНИЯ И ДОЗЫ
Для приёма внутрь. Препарат Брилинта ® можно принимать вне зависимости от приёма пищи.
Применение препарата Брилинта® следует начинать с однократной нагрузочной дозы 180 мг (две таблетки по 90 мг) и затем продолжать прием по 90 мг два раза в сутки.
Для пациентов с затруднением глотания таблетку (или 2 таблетки – в случае приема нагрузочной дозы) следует измельчить до состояния мелкого порошка, размешать в половине стакана питьевой воды и сразу же выпить полученную суспензию. Остатки смешать с дополнительной половиной стакана питьевой воды и выпить полученную суспензию. Суспензию можно также вводить через назогастральный зонд (CH8 или большего размера). После введения суспензии необходимо промыть назогастральный зонд водой для того, чтобы доза препарата полностью попала в желудок пациента.
Пациенты, принимающие препарат Брилинта®, должны ежедневно принимать ацетилсалициловую кислоту (от 75 мг до 150 мг при постоянном приеме) (см.раздел «Фармакологические свойства»), если отсутствуют специфические противопоказания.
Следует избегать перерывов в терапии. Пациент, пропустивший прием препарата Брилинта®, должен принять только одну таблетку 90 мг (следующая доза) в намеченное время.
При необходимости пациенты, принимающие клопидогрел, могут быть переведены на прием препарата Брилинта ® (см. раздел «Фармакологические свойства»).
Рекомендуется проводить терапию препаратом Брилинта ® в течение 12 месяцев, кроме случаев клинической необходимости в досрочной отмене препарата (см. раздел «Фармакологические свойства»). Данные о применении тикагрелора более 12 месяцев ограничены. У пациентов с острым коронарным синдромом досрочная отмена любой антиагрегантной терапии, включая препарат Брилинта ®, может повысить риск сердечно-сосудистой смерти или инфаркта миокарда в результате основного заболевания (см. раздел «Особые указания»). Необходимо избегать преждевременного прекращения приема препарата.
Пожилые пациенты
Не требуется коррекции дозы (см. раздел «Фармакологические свойства»).
Пациенты с почечной недостаточностью
Не требуется корректировать дозу препарата у пациентов с почечной недостаточностью (см. раздел «Фармакологические свойства»). Отсутствует информация о применении препарата Брилинта ® у пациентов на гемодиализе, поэтому его применение у этих пациентов не показано.
Пациенты с печеночной недостаточностью
Не требуется корректировать дозу препарата у пациентов с легкой печеночной недостаточностью. Не проводились исследования препарата Брилинта ® у пациентов с умеренной или тяжелой печеночной недостаточностью, поэтому его у этих пациентов противопоказано (см. разделы «Фармакологические свойства» и «Противопоказания»).
Дети
Безопасность и эффективность препарата Брилинта ® у детей младше 18 лет по одобренному у взрослых показанию не установлена.
ПОБОЧНОЕ ДЕЙСТВИЕ
По данным исследования PLATO самыми частыми отмечавшимися нежелательными явлениями у пациентов, принимавших тикагрелор, были одышка, ушибы и носовые кровотечения.
Нежелательные реакции классифицированы по частоте развития и классу системы органов. Частота развития нежелательных реакций определяется с использованием следующих условных обозначений: очень часто (≥1/10), часто (≥1/100, <1/10), нечасто (≥1/1000, <1/100), редко (≥1/10000, <1/1000).
Нежелательные лекарственные реакции по частоте развития и классу системы органов
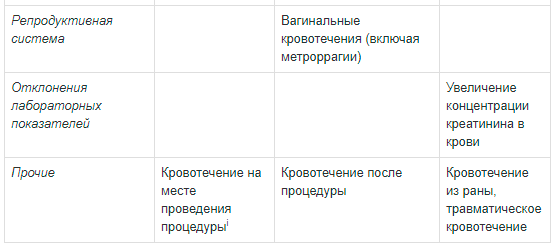
a гиперурикемия, повышение концентрации мочевой кислоты в крови; смотрите раздел «Отклонения в значениях лабораторных показателей» ниже.
b кровоизлияние в мозг, внутричерепное кровоизлияние, геморрагический инсульт.
c одышка, одышка при нагрузке, одышка в покое, ночная одышка
d желудочно-кишечное кровотечение, ректальное кровотечение, кишечное
кровотечение, мелена, положительный анализ на скрытую кровь
е кровотечение из язвы ЖКТ, кровотечение из язвы желудка, кровотечение из язвы двенадцатиперстной кишки, кровотечение из пептической язвы
f подкожная гематома, кожные и подкожные геморрагии, петехии
g ушиб, гематома, экхимоз, повышенная тенденция к синякам, травматическая гематома
h гематурия, кровотечение из мочевыводящих путей
i кровотечение из места пункции сосуда, гематома в месте пункции сосуда, кровотечение из места инъекции, кровотечение из места пункции, кровотечение из места катетеризации
# у пациентов, принимавших тикагрелор в исследовании PLATO (п=9235), случаев гемартроза отмечено не было. Частота гемартроза была рассчитана с использованием верхнего предела 95% ДИ для ожидаемой частоты (по формуле 3/Х, где Х — количество пациентов, получавших тикагрелор, т.е. 9235).
Предполагаемая частота гемартроза составляет 3/9235, что соответствует частоте «редко».
Описание некоторых нежелательных реакций
Кровотечение
В исследовании PLATO использовались следующие определения кровотечения:
• Большое летальное/угрожающее жизни кровотечение: летальное, или внутричерепное кровоизлияние, или кровотечение в полость перикарда с тампонадой сердца; или гиповолемический шок или тяжелая гипотония, вызванные кровотечением и требующие применения вазоконстрикторов или проведения оперативного вмешательства, или клинически явное кровотечение, сопровождающееся снижением уровня гемоглобина более, чем на 50 г/л, или требующее трансфузии 4 или более единиц цельной крови или эритроцитов.
• Большое иное кровотечение: вызывающее существенную недееспособность больного (например, внутриглазное кровоизлияние с необратимой потерей зрения), или клинически явное кровотечение, сопровождающееся снижением уровня гемоглобина на 30-50 г/л, или требующее трансфузии 2-3 единиц цельной крови или эритроцитов.
• Малое кровотечение: требует медицинского вмешательства для остановки или лечения кровотечения (например, носовое кровотечение, требующее посещения больницы для тампонады носа).
Брилинта® и клопидогрел не различались по частоте больших кровотечений в целом по критериям PLATO (11,6%/год и 11,2%/год, соответственно), летальных/угрожающих жизни кровотечений по критериям PLATO (5,8%/год в обеих группах). Однако частота совокупности больших и малых кровотечений по критериям PLATO была выше в группе тикагрелора (16,1%) по сравнению с клопидогрелом (14,6%, р=0,0084).
Возраст, пол, масса тела, раса, географический регион, сопутствующие заболевания, сопутствующая терапия, анамнез, включая предшествующий инсульт и транзиторную ишемическую атаку, не влияли на частоту больших кровотечений в целом и несвязанных с процедурами по критериям PLATO. Не было выявлено групп с повышенным риском кровотечений.
Кровотечение, связанное с АКШ: В исследовании PLATO у 42% больных из 1584 (12% из когорты), подвергнутых АКШ, развивались большие летальные/ угрожающие жизни больного кровотечения без значимых различий в обеих группах лечения. Летальное кровотечение, связанное с АКШ, отмечалось у 6 пациентов в каждой группе лечения.
Кровотечение, не связанное с АКШ, и кровотечение, не связанное с процедурами:
Брилинта® и клопидогрел не отличались по частоте случаев большого летального/ угрожающего жизни кровотечения, не связанного с АКШ по критериям PLATO, но при применении препарата Брилинта® чаще развивались большие кровотечения в целом по определению исследования PLATO (4,5%/год по сравнению с 3,8%/год; р=0,0264). Если удалить случаи развития кровотечений, связанных с АКШ, в группе тикагрелора отмечалось больше кровотечений (3,1%/год), чем в группе клопидогрела (2,3%/год; р=0,0058). Прекращение лечения вследствие кровотечений, не связанных с процедурой, было более частым на фоне тикагрелора (2,9%) по сравнению с клопидогрелом (1,2%, p<0,001).
Внутричерепное кровоизлияние: В группе тикагрелора развивалось больше внутричерепных кровотечений, не связанных с процедурами (n=27 кровотечений у 26 пациентов, 0,3%), чем в группе клопидогрела (n=14 кровотечений, 0,2%), из которых 11 кровотечений на тикагрелоре и 1 на клопидогреле были фатальными. Однако не было значимых различий по общему числу фатальных кровотечений.
Одышка
Нежелательные явления в виде одышки (одышка, одышка в покое, одышка при физической нагрузке, пароксизмальная ночная одышка и ночная одышка) в комбинации развивались у 13,8% больных, получавших препарат Брилинта ®, и у 7,8% пациентов, принимавших клопидогрел. Исследователи посчитали, что у 2,2% пациентов из группы тикагрелора одышка была связана с терапией. Большинство случаев одышки были слабыми или умеренными по своей интенсивности и представляли собой однократные эпизоды сразу после начала терапии. Примерно 30% от всех случаев одышки разрешились в течение 7 дней. Чаще одышка развивалась у пожилых больных, у пациентов с застойной сердечной недостаточностью, ХОБЛ или бронхиальной астмой в начале исследования. 0,9% пациентов прекращали прием препарата Брилинта ® из-за одышки. Одышка не была связана с развитием нового или ухудшением имеющегося заболевания сердца или легких (см. раздел «Особые указания»). Препарат Брилинта® не влияет на показатели функции внешнего дыхания.
Отклонения в значениях лабораторных показателей
Сывороточная концентрация креатинина повышалась более, чем на 30% у 25,5% пациентов и больше, чем на 50% у 8,3% пациентов, получающих препарат Брилинта®. Повышение креатинина более, чем на 50%, чаще встречалось у пациентов старше 75 лет, у пациентов с тяжелой почечной недостаточностью при включении в исследование и у пациентов, получающих терапию антагонистами рецепторов к ангиотензину. Общее число почечных нежелательных явлений составляло 4,9% у пациентов на тикагрелоре, однако исследователи связывали их с приемом препарата в 0,6% случаев.
Сывороточная концентрация мочевой кислоты увеличивалась выше верхней границы нормы у 22% пациентов, получающих препарат Брилинта®.
Нежелательные явления, связанные с гиперурикемией, отмечались в 0,5% случаев на тикагрелоре, из них исследователи связывали с приемом тикагрелора 0,05% случаев. Подагрический артрит наблюдался у 0,2% пациентов на тикагрелоре, ни один из этих случаев не был расценен исследователем, как связанный с приемом препарата.
Постмаркетинговое применение
Ниже представлены нежелательные реакции, которые были отмечены при постмаркетинговом применении препарата Брилинта ®. Поскольку сообщения получены спонтанно от популяции неустановленного размера, не всегда возможно достоверно оценить частоту развития.
Нарушениясостороныиммуннойсистемы:реакции повышенной чувствительности, включая ангионевротический отек (см. раздел «Противопоказания»).
ПЕРЕДОЗИРОВКА
Тикагрелор хорошо переносится в однократной дозе препарата до 900 мг. В единственном исследовании с увеличением дозы неблагоприятное воздействие на желудочно-кишечный тракт было дозолимитирующим. Другими клинически значимыми нежелательными явлениями, которые могли наблюдаться при передозировке, были одышка и желудочковые паузы. В случае передозировки рекомендуется осуществлять наблюдение на предмет этих нежелательных явлений и проводить мониторирование ЭКГ.
Брилинта® не выводится при гемодиализе (см. раздел «Особые указания»), антидот не известен. При передозировке следует проводить симптоматическую терапию в соответствии с локальными стандартами. В связи с ингибированием тромбоцитов увеличение продолжительности кровотечения является предполагаемым фармакологическим действием передозировки препаратом Брилинта®, поэтому при развитии кровотечения необходимо проводить соответствующие поддерживающие мероприятия.
ВЗАИМОДЕЙСТВИЕ С ДРУГИМИ ЛЕКАРСТВЕННЫМИ СРЕДСТВАМИ И ДРУГИЕ ВИДЫ ЛЕКАРСТВЕННОГО ВЗАИМОДЕЙСТВИЯ
Воздействие других лекарственных препаратов на препарат Брилинта®
Лекарственные препараты, метаболизируемые изоферментом CYP3A4 Ингибиторы CYP3A4
• Мощные ингибиторы CYP3A4: совместное применение кетоконазола с тикагрелором увеличивает Cmax и AUC тикагрелора в 2,4 и 7,3 раза, соответственно. Cmax и AUC активного метаболита понижается на 89% и 56%, соответственно. Другие мощные ингибиторы CYP3A4 (кларитромицин, нефазодон, ритонавир и атазанавир) будут оказывать такие же эффекты, поэтому их совместное применение с препаратом Брилинта® противопоказано (см. разделы «Противопоказания», «Особые указания»).
• Умеренные ингибиторы CYP3A4: совместное применение дилтиазема с тикагрелором увеличивает Сmax тикагрелора на 69%, а AUC в 2,7 раз, и снижает Сmax активного метаболита на 38%, а AUC не меняется. Тикагрелор не влияет на плазменные концентрации дилтиазема. Другие умеренные ингибиторы CYP3A4 (например, ампренавир, апрепитант, эритромицин, флуконазол) можно назначать одновременно с препаратом Брилинта®.
Циклоспорин (ингибитор P-gp и CYP3A4)
Совместное применение циклоспорина (600 мг) с тикагрелором увеличивает C max и AUC тикагрелора в 2,3 и 2,8 раз, соответственно. При этом отмечается увеличение AUC активного метаболита на 32% и снижение Cmax на 15%. Тикагрелор не влияет на плазменную концентрацию циклоспорина.
Индукторы CYP3A4
Совместное применение рифампицина с тикагрелором снижает C max и AUC тикагрелора на 73% и 86%, соответственно. Cmax активного метаболита не меняется, а AUC понижается на 46%. Другие индукторы CYP3A4 (например, фенитоин, карбамазепин и фенобарбитал), по-видимому, будут снижать экспозицию препарата Брилинта®. Мощные индукторы CYP3A4 могут уменьшать экспозицию и эффективность препарата Брилинта®.
Другие
По результатам фармакологических исследований взаимодействия сопутствующее применение тикагрелора с гепарином, эноксапарином и ацетилсалициловой кислотой или десмопрессином не влияет на фармакокинетику тикагрелора, его активного метаболита и АДФ-зависимую агрегацию тромбоцитов. В случае наличия клинических показаний к назначению препаратов, влияющих на гемостаз, они должны использоваться с осторожностью в комбинации с препаратом Брилинта® (см. раздел «С осторожностью»).
Нет данных о совместном применении препарата Брилинта® с мощными ингибиторами гликопротеина P (например, верапамил и хинидин), которые могут повысить экспозицию тикагрелора. Если нельзя избежать их совместного применения, оно должно осуществляться с осторожностью (см. разделы «С осторожностью», «Особые указания»).
Влияние препарата Брилинта® на другие лекарственные средства
Лекарственные препараты, метаболизируемые изоферментом CYP3A4
• Симвастатин: сопутствующее применение тикагрелора и симвастатина повышает C max и AUC симвастатина на 81% и 56%, соответственно, и увеличивает C max и AUC симвастатиновой кислоты на 64% и 52%, соответственно, при этом, в некоторых случаях эти показатели повышаются в 2-3 раза. Совместное применение симвастатина в дозе выше 40 мг/сут. с тикагрелором может приводить к развитию побочных эффектов симвастатина, и необходимо оценить соотношение потенциального риска и пользы. Не рекомендуется совместное применение препарата Брилинта® с симвастатином и ловастатином в дозе свыше 40 мг. Аторвастатин: сопутствующее применение аторвастатина и тикагрелора повышает Сmax и AUC метаболитов аторвастатиновой кислоты на 23% и 36%, соответственно. Подобное увеличение значений Cmax и AUC наблюдается для всех метаболитов аторвастатиновой кислоты. Эти изменения признаны клинически не значимыми.
• Сходные эффекты со статинами, метаболизирующимися CYP3A4, не могут быть исключены. В исследовании PLATO пациенты, получавшие тикагрелор, принимали различные статины при отсутствии каких-либо опасений относительно безопасности у 93% пациентов, принимавших эту группу препаратов.
Тикагрелор — умеренный ингибитор CYP3A4. Совместное применение препарата Брилинта® и субстратов CYP3A4 с узким терапевтическим индексом (например, цизаприд или алкалоиды спорыньи) не рекомендуется, так как тикагрелор может увеличивать экспозицию этих препаратов.
Лекарственные препараты, метаболизируемые изоферментом CYP2C9
Сопутствующее применение тикагрелора и толбутамида не меняло плазменные концентрации ни одного из этих препаратов, что говорит о том, что тикагрелор не является ингибитором изофермента CYP2C9, и, маловероятно, что он влияет на СУР2С9-опосредованный метаболизм препаратов, подобных варфарину и толбутамиду.
Оральные контрацептивы
Совместное применение тикагрелора, левоноргестрела и этинилэстрадиола увеличивает экспозицию этинилэстрадиола примерно на 20%, но не влияет на фармакокинетику левоноргестрела. Не ожидается клинически значимого воздействия на эффективность контрацепции при одновременном применении левоноргестрела, этинилэстрадиола и препарата Брилинта®.
Субстрат Р—др (включая дигоксин и циклоспорин)
Сопутствующее применение дигоксина с тикагрелором повышает Cmax и AUC дигоксина на 75% и 28%, соответственно. При совместном приеме с тикагрелором среднее значение самой низкой концентрации дигоксина увеличивалось на 30%, в некоторых индивидуальных случаях в два раза. Cmax и AUC тикагрелора при применении дигоксина не менялись. Поэтому рекомендуется проводить соответствующий клинический и/или лабораторный мониторинг при одновременном применении препарата Брилинта® и P-gp-зависимых препаратов с узким терапевтическим индексом, наподобие дигоксина и циклоспорина.
Другая сопутствующая терапия
При совместном применении препарата Брилинта® с препаратами, способными
вызвать брадикардию, должна соблюдаться осторожность. Однако в исследовании PLATO не наблюдалось клинически значимых нежелательных явлений при совместном применении с одним или более препаратами, способными вызвать брадикардию (например, 96% бета-адреноблокаторы, 33% антагонисты кальция, включая дилтиазем и верапамил, и 4% – дигоксин). В исследовании PLATO Брилинта® преимущественно назначалась совместно с ацетилсалициловой кислотой, ингибиторами протонной помпы, статинами, бета-адреноблокаторами, ингибиторами ангиотензинпревращающего фермента и антагонистами рецепторов ангиотензина в рамках длительного приема, а также с гепарином, низкомолекулярными гепаринами, ингибиторами гликопротеиновых IIb/IIIa рецепторов для внутривенного введения в рамках краткосрочной терапии. По результатам этих исследований не выявлено клинически значимых нежелательных взаимодействий.
Совместное применение препарата Брилинта® с гепарином, эноксапарином или десмопрессином не оказывало влияние на активированное частичное тромбопластиновое время (АЧТВ), активированное время свертывания (АВС) и исследование фактора Xa, однако вследствие потенциального фармакодинамического взаимодействия, требуется соблюдать осторожность при совместном применении с препаратами, влияющими на гемостаз.
В связи с сообщениями о подкожных кровоизлияниях на фоне селективных ингибиторов обратного захвата cеротонина, (например, пароксетин, сертралин и циталопрам), рекомендуется соблюдать осторожность при их совместном приеме с препаратом Брилинта ®.
При ежедневном употреблении больших объемов грейпфрутового сока (по 200 мл 3 раза в день) было отмечено 2-кратное увеличение экспозиции тикагрелора. Ожидается, что такое увеличение экспозиции тикагрелора не имеет клинического значения для большинства пациентов.
ОСОБЫЕ УКАЗАНИЯ
Риск развития кровотечения
У пациентов с острым коронарным синдромом, получавших терапию препаратом Брилинта® и ацетилсалициловой кислотой, отмечался повышенный риск несвязанных с АКШ больших кровотечений и кровотечений, требующих повышенного медицинского внимания, таких как большие + малые кровотечения по определению PLATO, но не увеличился риск летальных/угрожающих жизни кровотечений (см. раздел «Побочное действие»). При назначении препарата Брилинта® следует оценить соотношение пользы от профилактики атеротромботических событий и риска у пациентов с повышенным риском развития кровотечений.
При наличии клинических показаний Брилинта® должна использоваться с осторожностью в следующих группах пациентов:
• Предрасположенность пациентов к развитию кровотечения (например, в связи с недавно полученной травмой, недавно проведенной операцией, нарушениями свертываемости крови, активным или недавним желудочно-кишечным кровотечением). Использование препарата Брилинта® противопоказано у пациентов с активным патологическим кровотечением, внутричерепным кровоизлиянием в анамнезе, умеренной или тяжелой печеночной недостаточностью.
• Сопутствующее применение препаратов, которые могут повысить риск развития кровотечения (например, нестероидные противовоспалительные препараты, пероральные антикоагулянты и/или фибринолитики, принимаемые в течение 24 часов до приема препарата Брилинта®).
Отсутствуют данные о гемостатической эффективности трансфузий тромбоцитов при применении препарата Брилинта®; Брилинта® может ингибировать трансфузированные тромбоциты в крови. Так как при сопутствующем применении препарата Брилинта® и десмопрессина не уменьшалось стандартизированное время кровотечения, то маловероятно, что десмопрессин будет эффективно купировать кровотечение.
Антифибринолитическая терапия (аминокапроновая кислота или транексамовая кислота) и/или рекомбинантный фактор Vila могут усиливать гемостаз. После установления причины кровотечения и его купирования можно возобновить терапию препаратом Брилинта®.
Хирургические операции
Перед запланированной операцией или началом приема новых препаратов пациенту следует проинформировать врача о том, что он принимает препарат Брилинта®.
У пациентов, подвергающихся аортокоронарному шунтированию (АКШ), частота развития больших кровотечений при применении препарата Брилинта® была такой же, как при применении клопидогрела во все дни после отмены терапии, кроме дня 1, когда частота развития больших кровотечений была выше при приеме препарата Брилинта ® (см. раздел «Побочное действие»).
Если пациент подвергается плановой операции и не желателен
антитромботический эффект, то терапию препаратом Брилинта ® следует прекратить за 7 дней до операции.
Пациенты с риском развития брадикардии
В связи с выявлением в ранее проведенном клиническом исследовании, в основном, бессимптомных пауз, пациенты с повышенным риском развития брадикардии (например, больные без кардиостимулятора, у которых диагностирован синдром слабости синусового узла, атриовентрикулярная блокада сердца 2-ой или 3-ей степени; обморок, связанный с брадикардией) не были включены в основное исследование для оценки безопасности и эффективности препарата Брилинта®. Поэтому в связи с ограниченным клиническим опытом применения препарата у этих больных, рекомендуется с осторожностью назначать препарат Брилинта® таким пациентам (см. раздел «Фармакологические свойства»).
Дополнительная предосторожность должна соблюдаться при совместном применении препарата Брилинта® с препаратами, способными вызвать брадикардию. Однако не отмечалось клинически значимых побочных эффектов при совместном применении с одним или более препаратами, которые могут вызвать брадикардию (например, 96% бета-адреноблокаторы, 33% блокаторы кальциевых каналов, включая дилтиазем и верапамил, и 4% дигоксин) (см. раздел «Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия»).
В ходе под-исследования с использованием суточного мониторирования ЭКГ по Холтеру в группе тикагрелора по сравнению с клопидогрелом больше пациентов в острой фазе ОКС имели желудочковые паузы > 3 секунд. Повышение числа желудочковых пауз, зарегистрированных с помощью суточного мониторирования по Холтеру, на фоне приема тикагрелора отмечалось чаще у пациентов с хронической сердечной недостаточностью по сравнению с общей популяцией в острой фазе ОКС, но не на первом месяце. Паузы у этих пациентов не сопровождались последующими нежелательными клиническими последствиями (обмороки и установка кардиостимулятора).
Одышка
Одышка при применении препарата Брилинта® обычно слабая или умеренная по своей интенсивности, часто проходит по мере продолжения терапии препаратом. Пациенты с бронхиальной астмой/ХОБЛ могут иметь повышенный абсолютный риск одышки на приеме препарата Брилинта® (см. раздел «Побочное действие»). У пациентов с бронхиальной астмой/ХОБЛ тикагрелор должен использоваться с осторожностью. Механизм одышки на приеме тикагрелора не выяснен. Если у пациента развился новый эпизод одышки, сохраняется или усилилась одышка во время применения препарата Брилинта®, то необходимо провести полноценное обследование, и в случае непереносимости, прием препарата следует прекратить.
Повышение уровня
креатинина
На приеме препарата Брилинта® уровень креатинина может увеличиться (см. раздел «Побочное действие»). Механизм этого эффекта не известен. Оценку почечной функции необходимо производить через месяц от начала приема препарата, а в последующем в соответствии с рутинной клинической практикой, обращая особое внимание на пациентов от 75 лет и старше, пациентов с умеренной или тяжелой почечной недостаточностью и получающих терапию антагонистами рецепторов ангиотензина.
Повышение уровня мочевой кислоты
Пациенты на тикагрелоре имели более высокий риск гиперурикемии, чем
принимавшие клопидогрел (см. раздел «Побочное действие»). Необходимо соблюдать осторожность у пациентов с гиперурикемией или подагрическим артритом в анамнезе. В качестве превентивной меры следует избегать применения тикагрелора у пациентов с гиперурикемической нефропатией.
Другие
На основании наблюдаемого взаимодействия между поддерживающей дозой ацетилсалициловой кислоты и эффективностью тикагрелора по сравнению с клопидогрелом, совместное применение высокой поддерживающей дозы ацетилсалициловой кислоты (более 300 мг) и препарата Брилинта® не рекомендуется (см. разделы «Фармакологические свойства», «С осторожностью»).
Совместное применение препарата Брилинта® с мощными ингибиторами CYP3A4 (например, кетоконазол, кларитромицин, нефазодон, ритонавир и атазанавир) противопоказано (см. раздел «Противопоказания»), так как оно может привести к значительному повышению экспозиции препарата Брилинта® (см. раздел «Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия»).
Совместное применение препарата Брилинта® с мощными индукторами CYP3A4 (например, рифампицин, фенитоин, карбамазепин и фенобарбитал) не рекомендуется, так как их совместный прием может снижать экспозицию и эффективность тикагрелора (см. раздел «Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия»). Совместное применение препарата Брилинта® и субстратов CYP3A4 с узким терапевтическим индексом (например, цизаприд и алкалоиды спорыньи) не рекомендовано, так как тикагрелор может увеличить экспозицию этих препаратов.
Совместное применение препарата Брилинта® с симвастатином или ловастатином в дозе более 40 мг не рекомендуется (см. раздел «Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия»).
При совместном применении дигоксина и препарата Брилинта® рекомендован тщательный клинический и лабораторный мониторинг (частоты сердечных сокращений, и при наличии клинических показаний также ЭКГ и концентрации дигоксина в крови).
Нет данных о совместном применении тикагрелора с мощными ингибиторами гликопротеина P (например, верапамил и хинидин), которые могут повысить экспозицию тикагрелора. Если нельзя избежать их совместного применения, оно должно осуществляться с осторожностью (см. разделы «С осторожностью», «Взаимодействие с другими лекарственными средствами и другие виды лекарственного взаимодействия»).
ВЛИЯНИЕ НА СПОСОБНОСТЬ УПРАВЛЯТЬ АВТОМОБИЛЕМ И ДРУГИМИ МЕХАНИЗМАМИ
Не проводилось исследований влияния препарата Брилинта® на способность к вождению автотранспорта и управлению механизмами. Брилинта® не влияет или в незначительной степени влияет на способность управлять транспортом и механизмами. Во время терапии острого коронарного синдрома сообщалось о головокружении и спутанности сознания. В случае развития данных явлений пациентам следует соблюдать осторожность при управлении автомобилем и другими механизмами.
ФОРМА ВЫПУСКА
Таблетки, покрытые плёночной оболочкой, 90 мг. По 14 таблеток в блистере из Ал/ПВХ/ПВДХ. 1, 4 или 12 блистеров с инструкцией по медицинскому применению в картонной пачке с контролем первого вскрытия.
УСЛОВИЯ ХРАНЕНИЯ
При температуре не выше 30°С, в недоступном для детей месте.
СРОК ГОДНОСТИ
3 года. Не применять по истечении срока годности, указанного на упаковке.
УСЛОВИЯ ОТПУСКА ИЗ АПТЕК
По рецепту.
Наименование и адрес юридического лица, на имя которого выдано регистрационное удостоверение
АстраЗенека АБ, SE-151 85 Содерталье, Швеция AstraZeneca AB, SE-151 85 Sodertalje, Sweden
Производитель и фасовщик (первичная упаковка)
АстраЗенека АБ, SE-151 85 Содерталье, Швеция AstraZeneca AB, SE-151 85 Sodertalje, Sweden
Упаковщик (вторичная (потребительская) упаковка) и выпускающий контроль качества
ООО «АстраЗенека Индастриз»
249006, Россия, Калужская область, Боровский район, деревня Добрино, 1-ый Восточный проезд, владение 8
Дополнительная информация предоставляется по требованию: ООО Астра Зенека Фармасьютикалз
125284 Москва, ул. Беговая д.3, стр. 1.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Трентал® (Trental®) инструкция по применению
📜 Инструкция по применению Трентал®
💊 Состав препарата Трентал®
✅ Применение препарата Трентал®
📅 Условия хранения Трентал®
⏳ Срок годности Трентал®
Описание лекарственного препарата
Трентал®
(Trental®)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для печатного издания справочника Видаль 2019 года.
Дата обновления: 2018.11.28
Владелец регистрационного удостоверения:
Контакты для обращений:
САНОФИ
Код ATX:
C04AD03
(Пентоксифиллин)
Лекарственная форма
| Трентал® |
Таб., покр. кишечнорастворимой пленочной оболочкой, 100 мг: 60 шт. рег. №: П N014229/01 |
Форма выпуска, упаковка и состав
препарата Трентал®
Таблетки, покрытые кишечнорастворимой пленочной оболочкой белого цвета, круглые, двояковыпуклые.
Вспомогательные вещества: лактоза — 20 мг, крахмал — 30 мг, тальк — 8.5 мг, кремния диоксид коллоидный — 0.5 мг, магния стеарат — 1 мг.
Состав оболочки: метакриловой кислоты сополимер — 11.45 мг, натрия гидроксид — 0.168 мг, макрогол (полиэтиленгликоль) 8000 — 1.4 мг, тальк — 0.388 мг, титана диоксид (E171) — 1.272 мг.
10 шт. — блистеры (6) — пачки картонные.
15 шт. — блистеры (4) — пачки картонные.
Фармакологическое действие
Трентал® уменьшает вязкость крови и улучшает реологические свойства крови (текучесть) за счет улучшения нарушенной деформируемости эритроцитов, уменьшения агрегации тромбоцитов и эритроцитов, снижения концентрации фибриногена, снижения активности лейкоцитов и уменьшения адгезии лейкоцитов к эндотелию сосудов.
Активное вещество препарата Трентал® — пентоксифиллин — представляет собой производное ксантина. Механизм его действия связан с ингибированием фосфодиэстеразы и накоплением цАМФ в клетках гладкой мускулатуры сосудов и форменных элементах крови.
Оказывая слабое миотропное сосудорасширяющее действие, пентоксифиллин несколько уменьшает общее периферическое сосудистое сопротивление и незначительно расширяет коронарные сосуды.
Пентоксифиллин обладает слабым положительным инотропным эффектом на сердце.
Улучшает микроциркуляцию в зонах нарушенного кровообращения.
Лечение препаратом Трентал® приводит к улучшению симптоматики нарушений мозгового кровообращения.
При окклюзионных заболеваниях периферических артерий применение препарата Трентал® приводит к удлинению дистанции ходьбы, устранению ночных судорог в икроножных мышцах и исчезновению болей в покое.
Фармакокинетика
Всасывание
После приема внутрь пентоксифиллин быстро и почти полностью всасывается. Абсолютная биодоступность исходной субстанции составляет 19±13%.
Метаболизм
Пентоксифиллин подвергается эффекту «первого прохождения» через печень. Концентрация основного активного метаболита 1-(5-гидроксигексил)-3,7-диметилксантина (метаболит I) в плазме крови в 2 раза превышает концентрацию исходного пентоксифиллина. Метаболит I находится с пентоксифиллином в обратимом биохимическом редокс-равновесии. Поэтому пентоксифиллин и метаболит I рассматриваются вместе как активная единица. Вследствие этого доступность активной субстанции значительно больше.
Пентоксифиллин полностью метаболизируется в организме.
Выведение
T1/2 пентоксифиллина после приема внутрь составляет 1.6 ч. Более 90% выводится почками в виде неконъюгированных водорастворимых метаболитов.
Фармакокинетика в особых клинических случаях
У пациентов с нарушениями функции почек выведение метаболитов замедляется.
У пациентов с нарушением функции печени T1/2 пентоксифиллина удлиняется и повышается его абсолютная биодоступность.
Показания препарата
Трентал®
- окклюзионная болезнь периферических артерий атеросклеротического или диабетического генеза (например, перемежающаяся хромота, диабетическая ангиопатия);
- трофические нарушения (например, трофические язвы голеней, гангрена);
- нарушения мозгового кровообращения (последствия церебрального атеросклероза, такие как снижение концентрации внимания, головокружение, ухудшение памяти), ишемические и постинсультные состояния;
- нарушения кровообращения в сетчатой и сосудистой оболочке глаза;
- отосклероз, дегенеративные изменения на фоне патологии сосудов внутреннего уха и снижения слуха.
Режим дозирования
Препарат принимают внутрь. Таблетки следует проглатывать целиком, запивая достаточным количеством воды, во время или сразу после еды.
Доза устанавливается врачом в соответствии с индивидуальными особенностями пациента.
Рекомендуемая доза препарата составляет 100 мг (1 таб.) 3 раза/сут с последующим медленным повышением дозы до 200 мг (2 таб.) 2-3 раза/сут. Максимальная разовая доза — 400 мг. Максимальная суточная доза — 1200 мг.
У пациентов с нарушениями функции почек (КК менее 30 мл/мин) доза может быть снижена до 100-200 мг (1-2 таб.)/сут.
Уменьшение дозы с учетом индивидуальной переносимости необходимо у пациентов с тяжелым нарушением функции печени.
Лечение может быть начато малыми дозами у пациентов с низким АД, а также у пациентов, находящихся в группе риска ввиду возможного снижения АД (пациенты с тяжелой формой ИБС или с гемодинамически значимыми стенозами сосудов головного мозга). В этих случаях доза может быть увеличена только постепенно.
Побочное действие
Ниже представлены побочные реакции, которые отмечались в клинических исследованиях и при постмаркетинговом применении препарата (частота неизвестна).
Со стороны нервной системы: головная боль, головокружение, асептический менингит, судороги.
Нарушения психики: ажитация, нарушения сна, тревога.
Со стороны сердечно-сосудистой системы: тахикардия, аритмия, снижение АД, стенокардия, «приливы» крови к кожным покровам, кровотечения (в т.ч. кровотечения из сосудов кожи, слизистых оболочек, желудка, кишечника).
Со стороны пищеварительной системы: ксеростомия (сухость полости рта), анорексия, атония кишечника, чувство давления и переполнения в области желудка, тошнота, рвота, диарея, запор, гиперсаливация (повышенное слюноотделение).
Со стороны печени и желчевыводящих путей: внутрипеченочный холестаз, повышение активности печеночных трансаминаз, повышение активности ЩФ.
Со стороны системы кроветворения: лейкопения/нейтропения, тромбоцитопения, панцитопения, гипофибриногенемия.
Со стороны органа зрения: нарушение зрения, скотома.
Со стороны кожи и подкожных тканей: кожный зуд, кожная сыпь, эритема (покраснение кожи), крапивница, повышенная ломкость ногтей, отеки.
Со стороны иммунной системы: анафилактические/анафилактоидные реакции, ангионевротический отек, анафилактический шок, бронхоспазм.
Противопоказания к применению
- массивное кровотечение (риск усиления кровотечения);
- обширное кровоизлияние в сетчатую оболочку глаза (риск усиления кровотечения);
- кровоизлияние в головной мозг;
- острый инфаркт миокарда;
- беременность (недостаточно данных);
- период грудного вскармливания (недостаточно данных);
- возраст до 18 лет;
- непереносимость галактозы, дефицит лактазы и синдром глюкозо-галактозной мальабсорбции (в связи с наличием в составе препарата лактозы;
- повышенная чувствительность к пентоксифиллину, другим метилксантинам или к любому вспомогательному веществу препарата.
С осторожностью следует применять препарат у пациентов с тяжелыми нарушениями ритма сердца (риск ухудшения аритмии); артериальной гипотензией (риск дальнейшего снижения АД); хронической сердечной недостаточностью; язвенной болезнью желудка и двенадцатиперстной кишки; нарушением функции почек (КК менее 30 мл/мин) (риск кумуляции и повышенный риск развития побочных эффектов); тяжелыми нарушениями функции печени (риск кумуляции и повышенный риск побочных эффектов); после недавно перенесенных оперативных вмешательств; при повышенном риске развития кровотечений (например, при нарушениях со стороны свертывающей системы крови (риск развития более тяжелых кровотечений)); при одновременном применении с антикоагулянтами (в т.ч. с непрямыми антикоагулянтами [антагонистами витамина К]); одновременном применении с ингибиторами агрегации тромбоцитов (клопидогрел, эптифибатид, тирофибан, эпопростенол, илопрост, абциксимаб, анагрелид, НПВП [кроме селективных ингибиторов ЦОГ-2], ацетилсалициловая кислота, тиклопидин, дипиридамол); одновременном применении с гипогликемическими средствами для приема внутрь и инсулином; одновременном применении с ципрофлоксацином; одновременном применении с теофиллином.
Применение при беременности и кормлении грудью
Препарат не рекомендуется к применению при беременности, т.к. недостаточно данных.
Пентоксифиллин проникает в грудное молоко в незначительных количествах. При необходимости применения препарата в период лактации следует прекратить грудное вскармливание (учитывая отсутствие опыта применения).
Применение при нарушениях функции печени
С осторожностью следует применять препарат у пациентов с тяжелыми нарушениями функции печени (риск кумуляции и повышенный риск побочных эффектов).
Применение при нарушениях функции почек
С осторожностью следует применять препарат у пациентов нарушением функции почек (КК менее 30 мл/мин) (риск кумуляции и повышенный риск развития побочных эффектов).
Применение у детей
Противопоказан в возрасте до 18 лет.
Применение у пожилых пациентов
У пациентов пожилого возраста может потребоваться уменьшение дозы препарата (повышение биодоступности и снижение скорости выведения пентоксифиллина).
Особые указания
Лечение следует проводить под контролем АД.
У пациентов с сахарным диабетом, принимающих гипогликемические средства, назначение препарата в высоких дозах может вызвать выраженную гипогликемию (может потребоваться коррекция доз гипогликемических средств и проведение гликемического контроля).
При назначении препарата Трентал® одновременно с антикоагулянтами необходим контроль показателей свертывающей системы крови.
У пациентов, недавно перенесших оперативное вмешательство, необходим регулярный контроль гемоглобина и гематокрита.
У пациентов с низким и нестабильным АД дозу пентоксифиллина необходимо уменьшить.
У пациентов пожилого возраста может потребоваться уменьшение дозы препарата (повышение биодоступности и снижение скорости выведения пентоксифиллина).
Курение может снижать терапевтическую эффективность препарата.
Использование в педиатрии
Безопасность и эффективность пентоксифиллина у детей изучены недостаточно.
Влияние на способность к управлению транспортными средствами и механизмами
Учитывая возможные побочные эффекты (например, головокружение), следует соблюдать осторожность при вождении автотранспорта и занятиях потенциально опасными видами деятельности.
Передозировка
Симптомы: головокружение, тошнота, рвота типа «кофейной гущи», падение АД, тахикардия, аритмия, покраснение кожных покровов, потеря сознания, озноб, арефлексия, тонико-клонические судороги. В случае возникновения описанных выше нарушений пациенту необходимо срочно обратиться к врачу.
Лечение: проведение симптоматической терапии. При появлении первых признаков передозировки (потливость, тошнота, цианоз) немедленно прекращают прием препарата. Если препарат принят недавно, следует обеспечить меры, направленные на предотвращение дальнейшего всасывания препарата путем его выведения (промывание желудка) или замедления всасывания (например, прием активированного угля). Особое внимание должно быть направлено на поддержание АД и функции дыхания. При судорожных припадках вводят диазепам. Специфический антидот неизвестен.
Лекарственное взаимодействие
Пентоксифиллин повышает риск развития артериальной гипотензии при одновременном применении с гипотензивными средствами (например, ингибиторы АПФ) или другими лекарственными средствами, обладающими потенциальным антигипертензивным эффектом (например, нитраты).
Пентоксифиллин может усиливать действие лекарственных средств, влияющих на свертывающую систему крови (прямые и непрямые антикоагулянты, тромболитики, антибиотики, такие как цефалоспорины). При совместном применении пентоксифиллина и непрямых антикоагулянтов (антагонистов витамина К) в постмаркетинговых исследованиях отмечались случаи усиления антикоагулянтного действия (риск развития кровотечений). Поэтому в начале приема пентоксифиллина или при изменении его дозы рекомендуется контролировать степень выраженности антикоагулянтного действия у пациентов, принимающих данную комбинацию препаратов, например, проводить регулярный контроль MHO.
Циметидин повышает концентрацию пентоксифиллина и активного метаболита I в плазме крови (риск возникновения побочных эффектов).
Совместное назначение с другими ксантинами может приводить к чрезмерному нервному возбуждению.
Гипогликемическое действие инсулина или гипогликемических средств для приема внутрь может усиливаться при одновременном применении пентоксифиллина (повышенный риск развития гипогликемии). Необходим строгий контроль состояния таких пациентов, включая регулярный гликемический контроль.
У некоторых пациентов при одновременном применении пентоксифиллина и теофиллина отмечается увеличение концентрации теофиллина. В дальнейшем это может приводить к увеличению или усилению побочных действий, связанных с теофиллином.
У некоторых пациентов при одновременном применении пентоксифиллина и ципрофлоксацина отмечается увеличение концентрации пентоксифиллина в плазме крови. В дальнейшем это может приводить к увеличению или усилению побочных действий, связанных с применением данной комбинации.
При одновременном применении пентоксифиллина с ингибиторами агрегации тромбоцитов (клопидогрел, эптифибатид, тирофибан, эпопростенол, илопрост, абциксимаб, анагрелид, НПВП [кроме селективных ингибиторов ЦОГ-2], ацетилсалициловая кислота, тиклопидин, дипиридамол) возможно развитие потенциального аддитивного действия, увеличивающего риск развития кровотечения. Поэтому следует с осторожностью применять пентоксифиллин одновременно с вышеперечисленными ингибиторами агрегации тромбоцитов.
Условия хранения препарата Трентал®
Препарат следует хранить в недоступном для детей, сухом месте при температуре не выше 25°С.
Срок годности препарата Трентал®
Срок годности — 4 года. Не применять по истечении срока годности, указанного на упаковке.
Условия реализации
Препарат отпускается по рецепту.
Контакты для обращений
САНОФИ

|
|
Представительство |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Аналоги препарата
Вазонит®
(БАУШ ХЕЛС, Россия)
Пентоксифиллин
(МОСХИМФАРМПРЕПАРАТЫ им. Н.А.Семашко, Россия)
Пентоксифиллин
(ВАЛЕНТА ФАРМАЦЕВТИКА, Россия)
Пентоксифиллин
(ФАРМПРОЕКТ, Россия)
Пентоксифиллин
(ОРГАНИКА, Россия)
Пентоксифиллин
(ВЕЛФАРМ, Россия)
Пентоксифиллин
(ЛЕКХИМ, Украина)
Пентоксифиллин
(SHREYA LIFE SCIENCES, Индия)
Пентоксифиллин
(АТОЛЛ, Россия)
Пентоксифиллин
(БИОСИНТЕЗ, Россия)
Все аналоги