Описание препарата Вайдаза (лиофилизат для приготовления суспензии для подкожного введения, 100 мг) основано на официальной инструкции, утверждено компанией-производителем в 2013 году
Дата согласования: 09.09.2013
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Отзывы
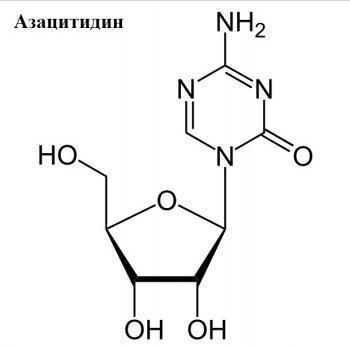
Действующее вещество
ATX
Фармакологическая группа
Состав
| Лиофилизат для приготовления суспензии для подкожного введения | 1 фл. |
| активное вещество: | |
| азацитидин | 100 мг |
| вспомогательные вещества: маннитол — 100 мг |
Описание лекарственной формы
Лиофилизат: белый лиофилизированный порошок или пористая масса.
Готовая суспензия: белого цвета.
Фармакологическое действие
Фармакологическое действие
—
противоопухолевое.
Фармакодинамика
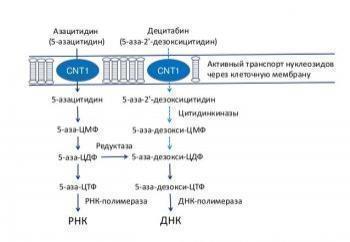
Противоопухолевое действие азацитидина обусловлено разнообразными механизмами, включая цитотоксичность в отношении патологически измененных гематопоэтических клеток костного мозга и гипометилирование ДНК. Механизмы, участвующие в реализации цитотоксического действия азацитидина, включают ингибирование синтеза ДНК, РНК и белка, инкорпорацию препарата в ДНК и РНК, а также активацию путей повреждения ДНК. Непролиферирующие клетки практически не чувствительны к азацитидину. Инкорпорация азацитидина в ДНК приводит к инактивации метилтрансферазы ДНК, в результате чего происходит гипометилирование ДНК. Гипометилирование ДНК в аберрантно метилированных генах, присутствующее и в регуляторном цикле нормальных клеток, их дифференциации и клеточной смерти, может вызывать реэкспрессию гена и восстановление свойств подавления опухолевого роста у самих раковых клеток. Клиническая значимость механизма гипометилирования ДНК в сравнении с цитотоксическим и другими эффектами азацитидина еще не установлена.
Клиническая эффективность и безопасность Вайдазы была подтверждена результатами многоцентрового рандомизированного исследования III фазы. У больных с миелодиспластическим синдромом, хроническим миеломоноцитарным лейкозом и острым миелолейкозом терапия Вайдазой превосходила современную традиционную терапию по всем критериям эффективности, включая продолжительность жизни и общую частоту ответа на лечение.
Фармакокинетика
Абсорбция. После п/к введения азацитидин быстро абсорбируется, достигая Cmax (750±403) нг/мл через 0,5 ч после введения. Абсолютная биодоступность азацитидина при п/к введении составляет 89% по отношению к данному показателю при в/в введении, на основании результатов определения AUC.
Метаболизм. Результаты исследования in vitro показали, что в метаболизме азацитидина не участвуют изоферменты системы цитохрома P450, UDP-глюкуронилтрансфераза, сульфотрансфераза и глютатионтрансфераза.
Азацитидин метаболизируется путем спонтанного гидролиза и дезаминирования, которое индуцируется цитидиндезаминазой.
Выведение. Азацитидин быстро выводится из организма, его T1/2 после п/к введения составляет (41±8) мин. Бóльшая часть азацитидина (50–85%) и/или его метаболитов выводится почками. Через кишечник выводится менее 1% препарата.
Данных о поступлении азацитидина в грудное молоко нет.
Влияние нарушения функции печени или почек, а также возраста, пола или расы на фармакокинетические параметры азацитидина не изучалось.
Показания
Лечение взрослых больных, у которых не может быть выполнена трансплантация гемопоэтических стволовых клеток, имеющих:
— миелодиспластический синдром (МДС) с высокой или промежуточной-2 степенью риска в соответствии со шкалой IPSS (Международная прогностическая система баллов);
— острый миелоидный лейкоз;
— хронический миеломоноцитарный лейкоз без признаков МДС.
Противопоказания
повышенная чувствительность к азацитидину или другим компонентам препарата;
распространенные метастазы в печени;
беременность и период кормления грудью;
детский возраст (отсутствие данных по эффективности и безопасности).
С осторожностью: больные с сердечно-сосудистыми заболеваниями, заболеваниями легких, нарушениями функции почек и печени, включая обширные метастатические поражения печени.
Способ применения и дозы
П/к, в область плеча, бедра или живота. Места инъекции должны чередоваться.
Место для очередной инъекции должно находиться на удалении более чем 2,5 см от предыдущего. Вайдаза не должна вводиться в поврежденные, гиперемированные, уплотненные или болезненные участки кожи (в т.ч. в участки кожи с кровоизлияниями).
Перед введением Вайдазы рекомендуется назначить противорвотные препараты.
Рекомендуемая начальная доза препарата Вайдаза при проведении первого цикла терапии для всех больных, независимо от значений исходных гематологических показателей, составляет 75 мг/м2 и вводится ежедневно в течение 7 дней с последующим перерывом в 21 день (28-дневный терапевтический цикл).
Должно быть проведено не менее 6 терапевтических циклов. Лечение продолжают до тех пор, пока сохраняется его эффективность, или до появления симптомов прогрессирования заболевания.
В ходе наблюдения за больными оценивают ответ со стороны показателей крови и возможные проявления токсичности, в частности со стороны крови и почек, которые могут требовать отсрочки следующего курса лечения или коррекции дозы препарата.
Ниже представлены возможности модификации дозы препарата Вайдаза при развитии различных видов токсичности.
Модификация дозы при выявлении симптомов гематологической токсичности
Гематологической токсичностью считается максимальное снижение количества клеток в течение данного цикла лечения (надир), если уровень тромбоцитов опускается ниже 50·109/л и/или абсолютное число нейтрофилов опускается ниже 1·109/л.
Восстановлением считается повышение количества клеток в клеточной(ых) линии(ях) на по крайней мере половину разницы между исходным количеством клеток и надиром (т.е. количество клеток при восстановлении ?надир + (0,5 ?(исходное(ые) количество(а) ? надир).
1. Больные с исходными (до начала терапии Вайдазой) показателями количества лейкоцитов >3·109/л, абсолютного количества нейтрофилов >1,5·109/л, количества тромбоцитов >75·109/л.
Если на фоне лечения препаратом Вайдаза у этих пациентов появляются симптомы гематологической токсичности, следующий цикл лечения препаратом откладывается до восстановления количества тромбоцитов и абсолютного количества нейтрофилов до исходных значений. Если продолжительность восстановительного периода не превышает 14 дней, модификация дозы препарата не требуется. Если количество клеток крови не увеличилось до необходимого уровня в течении 14 дней, доза препарата должна быть снижена согласно рекомендациям, изложенным ниже (табл. 1). При использовании модифицированной дозы продолжительность цикла терапии должна восстановиться до 28 дней.
Таблица 1
|
Количество клеток крови |
% от начальной дозы для следующего цикла, если восстановление* количества клеток крови потребовало больше 14 дней |
|
|
Абсолютное количество нейтрофилов, клеток/л |
Количество тромбоцитов, клеток/л |
|
| ?1·109 | ?50·109 | 50% |
| >1·109 | >50·109 | 100% |
*Восстановление = количество (к-во) ?минимальное к-во + (0,5 ? (исходное к-во?минимальное к-во)).
2. Больные с исходными (до начала терапии Вайдазой) показателями количества лейкоцитов <3·109/л, абсолютного количества нейтрофилов <1,5·109/л, количества тромбоцитов <75·109/л
Если перед очередным курсом лечения препаратом Вайдаза наблюдается снижение количества лейкоцитов или абсолютного количества нейтрофилов или тромбоцитов не более 50% от их исходных значений или более 50%, но при наличии признаков улучшения дифференциации любого клеточного ростка, схема введения препарата Вайдаза и его доза не должны меняться.
Больным, у которых количество клеток крови не превысило 50% порога от исходного уровня при отсутствии признаков улучшения дифференциации клеточных ростков, очередной курс лечения препаратом Вайдаза должен быть отсрочен до восстановления абсолютного количества нейтрофилов и тромбоцитов. Если восстановительный процесс занял не более 14 дней, корректировка дозы препарата Вайдаза не требуется. Если количество клеток крови не достигло желаемого уровня в течение 14 дней, необходимо определение клеточного насыщения костного мозга. При показателе клеточного насыщения >50% не требуется изменения дозы препарата. Если клеточное насыщение костного мозга ?50%, введение препарата Вайдаза должно быть отложено, а доза уменьшена согласно приведенным в таблице 2 рекомендациям:
Таблица 2
| Клеточное насыщение костного мозга | % от начальной дозы для следующего цикла, если восстановление* количества клеток крови потребовало больше 14 дней | |
| Восстановление* ?21 день | Восстановление* >21 день | |
| 15–50% | 100% | 50% |
| <15% | 100% | 33% |
*Восстановление = количество (к-во) ?минимальное к-во + (0,5 ? (исходное к-во?минимальное к-во)).
После модификации дозы продолжительность цикла должна быть восстановлена до 28 дней.
Пример расчета индивидуальной дозы азацитидина представлен в таблице 3.
Таблица 3
| Площадь поверхности тела, м2 | 100% рекомендованной начальной дозы (75 мг/м2) |
50% рекомендованной начальной дозы (37,5 мг/м2) | 33% рекомендованной начальной дозы (25 мг/м2) | |||
| Суточная доза, мг | Объем раствора, мл | Суточная доза, мг | Объем раствора, мл | Суточная доза, мг | Объем раствора, мл | |
| 1,4 | 105 | 4,2 ** | 52,5 | 2,1 | 35 | 1,4* |
| 1,5 | 112,5 | 4,5** | 56,25 | 2,25* | 37,5 | 1,5* |
| 1,6 | 120 | 4,8** | 60 | 2,4* | 40 | 1,6* |
| 1,7 | 127,5 | 5,1** | 63,75 | 2,55* | 42,5 | 1,7* |
| 1,8 | 135 | 5,4** | 67,5 | 2,7* | 45 | 1,8* |
| 1,9 | 142,5 | 5,7** | 71,25 | 2,85* | 47,5 | 1,9* |
* 1 флакон, содержащий 100 мг азацитидина.
** 2 флакона, содержащих 100 мг азацитидина.
Особенности использования препарата Вайдаза у отдельных групп пациентов
Применение препарата у пациентов с нарушениями функций почек
Специальных исследований у больных с нарушением функции почек не проводилось. Больные с тяжелой почечной недостаточностью должны тщательно мониторироваться для контроля нежелательных явлений. Не требуется изменять начальную дозу препарата у больных с нарушениями функции почек (например исходный уровень креатинина сыворотки крови или концентрация мочевины в крови в 2 раза больше ВГН или концентрация бикарбоната менее 20 ммоль/л). Последующая модификация дозы базируется на результатах исследования гематологических параметров и показателей функции почек. При необъяснимом снижении уровня бикарбонатов в сыворотке менее 20 ммоль/л доза препарата для следующего цикла терапии должна быть уменьшена на 50%. При необъяснимом повышении уровня креатинина сыворотки крови или концентрации азота мочевины в крови в 2 раза или более от исходных значений или выше ВГН очередной цикл терапии должен быть отложен до восстановления этих параметров до нормальных или исходных значений, а доза препарата в следующем цикле должна быть уменьшена на 50%.
Применение у пациентов с нарушениями функций печени
Специальных исследований у больных с нарушениями функций печени не проводилось. Больные с тяжелой печеночной недостаточностью должны тщательно мониторироваться для своевременного выявления нежелательных явлений. Данной категории больных не требуется изменять начальную дозу препарата. Последующая модификация дозы будет зависеть от результатов исследования крови.
Пожилые пациенты. Пожилым больным не требуется специального режима дозирования.
Поскольку у пожилых больных вероятность нарушения функции почек выше, во время лечения рекомендуется мониторировать функцию почек.
Дети и подростки. Вайдазу не рекомендуется назначать детям младше 18 лет ввиду недостаточного клинического опыта.
Рекомендации по приготовлению раствора и проведению инъекций
Содержимое флакона с препаратом растворяется в 4 мл воды для инъекций до концентрации 25 мг/1 мл. После добавления во флакон воды для инъекций его необходимо энергично потрясти до получения однородной суспензии белого цвета. При необходимой дозе, превышающей 100 мг, используются 2 флакона с препаратом.
Непосредственно перед введением необходимо повторно перевести содержимое шприца в состояние суспензии. Для этого следует энергично покатать шприц между ладонями до получения однородной суспензии белого цвета. Температура суспензии во время инъекции должна составлять 20–25 °C. Не следует использовать препарат, если он содержит крупные частицы.
Для проведения п/к инъекции рекомендуется использовать иглу 25-го калибра, при этом игла вводится под кожу плеча, бедра или живота под углом 45–90°. В одну область вводится не более 4 мл растворенного препарата. Дозы более 4 мл следует вводить в 2 разные области.
Суспензию Вайдаза следует готовить непосредственно перед использованием. Готовую суспензию хранить при температуре 25 °C не более 45 мин или при температуре от 2–8 °C не более 8 ч. Перед введением необходимо дать шприцу достичь температуры 20–25 °C (но не более чем в течение 30 мин). Если данные временные ограничения превышены, приготовленная суспензия должны быть утилизирована соответствующим образом, и должна быть приготовлена новая суспензия.
Побочные действия
Наиболее частыми нежелательными явлениями при лечении азацитидином являлись гематологические реакции (71,4%), включая тромбоцитопению, нейтропению и лейкопению (обычно 3–4-й степени тяжести); желудочно-кишечные осложнения (60,6%) включая тошноту и рвоту (обычно 1–2-й степени тяжести) или локальные реакции в месте введения (77,1%; степень тяжести — 1–2).
К наиболее частым (>2%) серьезным нежелательным реакциям также относятся фебрильная нейтропения (8%) и анемия (2,3%). Среди других серьезных нежелательных реакций отмечались сепсис на фоне нейтропении, пневмония, тромбоцитопения и кровотечения (например внутричерепные).
Частота побочных реакций, приведенных ниже, определялась соответственно следующей градации: очень часто: (≥1/10); часто (≥1/100, <1/10); нечасто (≥1/1000, <1/100); редко (≥1/10000, <1/1000) и очень редко (<1/10000); неизвестно (оценить по имеющимся данным невозможно).
Со стороны системы кроветворения: очень часто — нейтропения, фебрильная нейтропения, лейкопения, тромбоцитопения, анемия; часто — панцитопения.
Со стороны органов пищеварения: очень часто — диарея, запор, тошнота, рвота, боль в животе, анорексия; часто — желудочно-кишечное кровотечение, геморроидальное кровотечение, стоматит, кровоточивость десен, диспепсия.
Со стороны печени и желчевыводящих путей: нечасто — печеночная недостаточность*, прогрессирующая печеночная кома.
Со стороны ЦНС: очень часто — головокружение, головная боль; часто — внутричерепное кровотечение, сонливость.
Со стороны ССС: часто — повышение или снижение АД, гематомы.
Со стороны органов дыхания: очень часто — одышка; часто — одышка при физической нагрузке, боль в гортани и глотке; редко — интерстициальные заболевания легких.
Со стороны мочевыделительной системы: часто — гематурия, почечная недостаточность*, повышение концентрации креатинина; нечасто — почечно-канальцевый ацидоз.
Со стороны кожи и подкожно-жировой клетчатки: очень часто — петехии, зуд, сыпь, экхимозы; часто — пурпура, алопеция, эритема, пятнистая сыпь.
Со стороны костно-мышечной системы: очень часто — артралгия; часто — боли в костях, миалгия.
Со стороны органа зрения: часто — внутриглазные кровотечения, кровоизлияния в конъюнктиву.
Инфекции: очень часто — пневмония, назофарингит; часто — сепсис на фоне нейтропении, инфекции верхних дыхательных путей и мочевыводящих путей, воспаление подкожной клетчатки, синусит, фарингит, ринит, простой герпес.
Со стороны иммунной системы: нечасто — реакции гиперчувствительности.
Метаболические расстройства и нарушения питания: очень часто — анорексия; часто — гипокалиемия; редко — синдром лизиса опухоли.
Нарушения психики: часто — спутанность сознания, тревожность, бессонница.
Местные реакции: очень часто — боль, покраснение, неспецифические реакции в месте инъекции; часто — кровоточивость, кровоизлияние, гематома, уплотнение, воспаление, сыпь, зуд, изменение цвета кожных покровов, образование узелков и болезненность в месте введения; редко — некроз тканей в месте введения.
Прочие: очень часто — слабость, лихорадка, боли в области грудной клетки; часто — уменьшение массы тела.
Взаимодействие
Не проводилось целенаправленных клинических исследований взаимодействия азацитидина с другими лекарственными препаратами. Данные исследований in vitro свидетельствуют о том, что участие изоферментов системы цитохрома Р450, UDP-глюкуронилтрансферазы, сульфотрансферазы и глютатионтрансферазы в метаболизме азацитидина маловероятно. В связи с этим, взаимодействие in vivo с данными ферментами, участвующими в метаболизме, не представляется клинически значимым.
Передозировка
Симптомы: сообщалось об одном случае передозировки азацитидина в ходе клинического исследования. У больного отмечалась диарея, тошнота и рвота после однократного в/в введения препарата в дозе 290 мг/м2, которая превышает рекомендованную начальную дозу почти в 4 раза.
Лечение: при передозировке рекомендуется мониторировать уровень соответствующих клеток крови и назначать, при необходимости, поддерживающее лечение.
Не существует специфического антидота при передозировке азацитидина.
Особые указания
Лечение препаратом Вайдаза должно проводиться под наблюдением врача, имеющего опыт применения противоопухолевых препаратов.
Лабораторные тесты
До начала терапии и перед началом каждого цикла должны быть получены результаты исследования функциональной активности печени, концентрации креатинина и бикарбонатов сыворотки крови, а также данные развернутого анализа крови. Регулярные анализы крови показаны для мониторирования эффективности и безопасности лечения.
Сердечно-сосудистые и легочные заболевания
Безопасность и эффективность Вайдазы у пациентов, страдающих тяжелой застойной сердечной недостаточностью, другими выраженными сердечно-сосудистыми или легочными заболеваниями не установлена.
Гематологическая токсичность
Наиболее частыми побочными эффектами при лечении азацитидином являлись гематологические реакции, включая тромбоцитопению, нейтропению и лейкопению (обычно 3–4-й степени тяжести). Наибольший риск развития этих реакций отмечается во время первых двух циклов терапии, после чего они с меньшей частотой возникают у пациентов с восстановившимися гематологическими показателями. Большинство гематологических реакций разрешается при отсрочке очередного цикла лечения, профилактическом назначении антибиотиков и/или колониестимулирующего фактора при нейтропении и гемотрансфузий при анемии или тромбоцитопении.
Развернутый анализ крови должен проводиться для контроля эффективности лечения и возможных побочных реакций как минимум перед каждым циклом лечения. После проведения первого лечебного цикла дозировка для последующего лечения рассчитывается на основе исходных показателей и их динамики в процессе лечения. Медицинский персонал и пациент должны получить указания о необходимости контроля температуры тела (лихорадки) и симптомов, позволяющих диагностировать кровотечение.
Инфекции
Миелосупрессия может привести к нейтропении и увеличению риска инфекции. У пациентов на фоне лечения азацитидином отмечались серьезные побочные реакции, такие как сепсис на фоне нейтропении (0,8%) и пневмония (2,5%). В случае инфекционных осложнений возможно назначение этиотропного лечения и колониестимулирующего фактора при нейтропении.
Кровотечение
У пациентов, получающих лечение азацитидином, могут развиваться кровотечения, в т.ч. относящиеся к категории серьезных побочных реакций, такие как желудочно-кишечные (0,8%) и внутричерепные кровотечения (0,5%). Необходимо осуществлять контроль симптомов, позволяющих диагностировать кровотечения, в особенности у пациентов с исходной тромбоцитопенией или тромбоцитопенией, возникшей на фоне лечения.
Гиперчувствительность
У пациентов, получавших лечение азацитидином, отмечались реакции гиперчувствительности, относящиеся к категории серьезных (0,25%). В случае развития анафилактических реакций лечение азацитидином должно быть немедленно остановлено и назначено симптоматическое лечение.
Побочные реакции со стороны кожи и подкожно-жировой клетчатки
Большинство побочных реакций со стороны кожи и подкожно-жировой клетчатки отмечалось в месте инъекции. Большинство подобных реакций возникало во время двух первых циклов лечения, при этом отмечалась тенденция к их уменьшению при продолжении лечения. Такие местные побочные реакции, как сыпь, воспаление, зуд в месте инъекции, эритема, могут потребовать назначения антигистаминных препаратов, кортикостероидов и НПВС.
Нарушение функций печени
На фоне лечения азацитидином у пациентов с распространенными метастатическими поражениями печени, особенно при уровне альбумина в сыворотке крови менее 30 г/л, отмечены случаи развития печеночной комы с летальным исходом.
Нарушение функций почек
У пациентов, получавших лечение азацитидином, в редких случаях отмечались нарушения функции почек, включавшие различные состояния от повышения концентрации креатинина и почечного канальцевого ацидоза до развития почечной недостаточности, в том числе с летальным исходом.
При необъяснимом снижении концентрации бикарбонатов в сыворотке, необъяснимом повышении концентрации креатинина сыворотки крови или концентрации мочевины в крови очередной цикл терапии должен быть отложен до восстановления этих параметров до нормальных или исходных значений, а доза препарата в следующем цикле должна быть уменьшена.
Так как азацитидин и его метаболиты выводятся преимущественно почками, больные с почечной недостаточностью должны тщательно мониторироваться для контроля нежелательных явлений.
Нарушения со стороны ЖКТ
На фоне лечения азацитидином наиболее часто отмечались запор, диарея, тошнота и рвота. Эти побочные реакции купировались с помощью симптоматических средств: противорвотных — при тошноте и рвоте, антидиарейных — при диарее, и слабительных — при запоре.
Контрацепция
Мужчины и женщины, способные к деторождению, должны использовать эффективные методы контрацепции во время лечения и в течение 3 мес после его окончания. Мужчинам следует рекомендовать рассмотреть возможность консервации образцов собственной спермы перед началом лечения.
Вайдаза — это цитотоксическое ЛС, с которым, как и с другими токсическими веществами, следует обращаться с осторожностью. Любой неиспользованный или расходный материал должен быть утилизирован согласно местным требованиям.
При контакте восстановленного раствора азацитидина с кожей, немедленно тщательно промыть ее с мылом и водой. При контакте со слизистой оболочкой, тщательно промыть ее водой.
Влияние на способность управлять автомобилем или выполнять работы, требующие повышенной скорости физических и психических реакций. Исследования по изучению влияния на способность к управлению транспортными средствами и использованию механизмов не проводились. Учитывая возможность развития слабости на фоне лечения препаратом Вайдаза, нужно проявлять особую осторожность при управлении автомобилем и работе с механизмами.
Форма выпуска
Лиофилизат для приготовления суспензии для п/к введения, 100 мг. 200 мг лиофилизата во флаконе из бесцветного стекла тип I (USP) вместимостью 30 мл, укупоренном резиновой пробкой, уплотненной сверху алюминиевым колпачком с отрывающейся пластмассовой крышечкой. 1 флакон в картонной пачке.
Производитель
Бен Венью Лабораторис Инк., 300 Носфилд Роуд, Бедфорд, Огайо 44146, США.
Бакстер Онкология ГмбХ, Кантштрассе 2,33790 Халле/ Вестфалия, Германия.
Владелец РУ и выпускающий контроль качества: Селджен Интернешнл Сарл; Рут де Перро, 1, 2017 Бодри, Швейцария.
Адрес представительства в России: Селджен Интернэшнл Холдингз Корпорэйшн (США). 125047, Москва, ул. 1-я Тверская-Ямская, 21, Бизнес-центр Four Winds Plaza, 2-й этаж.
Тел.: (495) 777-65-55; факс: (495) 213-09-39.
Условия отпуска из аптек
По рецепту.
Условия хранения
При температуре не выше 30 °C.
Хранить в недоступном для детей месте.
Срок годности
4 года.
Не применять по истечении срока годности, указанного на упаковке.
Вайдаза — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер
ЛСР-003474/10
Торговое наименование препарата
Вайдаза
Международное непатентованное наименование
Азацитидин
Лекарственная форма
лиофилизат для приготовления суспензии для подкожного введения
Состав
1 флакон содержит:
действующее вещество: азацитидин 100,0 мг;
вспомогательное вещество: маннитол 100,0 мг
Описание
Белый лиофилизированный порошок или пористая масса.
Фармакотерапевтическая группа
Противоопухолевое средство — антиметаболит
Код АТХ
L01BC
Фармакодинамика:
Механизм действия
Противоопухолевое действие азацитидина обусловлено разнообразными механизмами, включая цитотоксичность в отношении патологически измененных гематопоэтических клеток костного мозга и гипометилирование ДНК.
Механизмы, участвующие в реализации цитотоксического действия азацитидина, включают ингибирование синтеза ДПК, РПК и белка, инкорпорацию препарата в ДНК и РНК, а также активацию путей повреждения ДНК. Непролиферирующие клетки практически нечувствительны к азацитидину. Инкорпорация азацитидина в ДНК приводит к инактивации метилтрансферазы ДНК, в результате чего происходит гипометилирование ДНК. Гипометилирование ДНК в аберрантно метилированных генах, присутствующее и в регуляторном цикле нормальных клеток, их дифференциации и клеточной смерти, может вызывать ре-экспрессию гена и восстановление свойств подавления опухолевого роста у самих раковых клеток.
Клиническая значимость механизма гипометилирования ДНК в сравнении с цитотоксическим и другими эффектами азацитидина еще не установлена.
Доклинические данные о безопасности
Азацитидин индуцирует как генные мутации, так и хромосомные аберрации в бактериальных клетках и клетках млекопитающих in vitro. Потенциальная канцерогенность азацитидина оценивалась на мышах и крысах. Азацитидин стимулировал рост опухолей гематопоэтической системы у самок мышей при внутрибрюшинном введении 3 раза в неделю в течение 52 недель. Повышение частоты опухолей лимфоретикулярной системы, легких, молочной железы и кожи отмечалось у мышей, получавших азацитидин при внутрибрюшинном введении в течение 50 недель.
Результаты исследований на крысах выявили увеличенный риск развития опухолей яичек. В исследованиях раннего эмбриогенеза у мышей с частотой возникновения 44% наблюдалась внутриутробная смерть эмбрионов (повышение резорбции) при однократном внутрибрюшинном введении азацитидина в период органогенеза.
Кроме того, обнаруживались и пороки развития головного мозга у мышей, получавших азацитидин во время или до закрытия твердого неба. У крыс азацитидин, вводимый до имплантации, не вызывал развития нежелательных реакций, но оказывал выраженное эмбриотоксическое действие при введении во время органогенеза. Пороки эмбрионального развития в период органогенеза у крыс включали: аномалии развития ЦНС (экзенцефалия/цефалоцеле), пороки развития конечностей (микромелия, врожденная косолапость, синдактилия, олигодактилия) и другие (микрофтальмия, микрогнатия, гастрошизис, отек и дефекты ребер).
Введение азацитидина самцам мышей до спаривания с самками, не получавшими азацитидин, приводило к снижению фертильности и последующей потере потомства в период эмбриогенеза и постнатального развития.
Введение препарата самцам крыс приводило к снижению веса яичек и придатков яичек, уменьшению числа сперматозоидов, частоты наступления беременности, увеличению количества аномальных эмбрионов и гибели эмбрионов у спариваемых самок (см. «Особые указания»).
Фармакокинетика:
Абсорбция
После однократного подкожного введения в дозе 75 мг/м2 азацитидин быстро абсорбируется, достигая максимальной концентрации (Сmах) 750±403 нг/мл через 0,5 часа после введения (первая точка забора образца).
Абсолютная биодоступность азацитидина при подкожном введении составляет 89% по отношению к данному показателю при внутривенном введении (однократная доза 75 мг/м2) на основании результатов определения площади под кривой «концентрация-время» (AUC).
При подкожном введении азацитидина в дозах от 25 до 100 мг/м2 AUC и Сmах изменялись практически пропорционально.
Распределение
После внутривенного введения среднее значение объема распределения составило 76±26 л, а системный клиренс 147±47 л/час.
Метаболизм
Результаты исследования in vitro показали, что в метаболизме азацитидина не участвуют изоферменты системы цитохрома Р450, UDP-глюкуронилтрансфераза, сульфотрансфераза и глютатионтрансфераза.
Азацитидин метаболизируется путем спонтанного гидролиза и дезаминирования, которое индуцируется цитидиндезаминазой. При проведении исследования на S9 фракциях печени метаболиты азацитидина формировались независимо от НАДФН, следовательно, метаболизм азацитидина не опосредуется изоферментами цитохрома Р450.
Результаты исследования азацитидина in vitro на культивированных гепатоцитах человека показали, что в концентрациях от 1,0 до 100 мкМ (т.е. примерно в 30 раз выше концентраций, достигаемых в клинических условиях) азацитидин не индуцировал CYP 1А2, 2С19 или 3А4 или 3А5. В исследованиях, определяющих ингибирующее действие азацитидина на ряд изоферментов цитохрома Р450 (CYP 1А2, 2В6, 2С8, 2С9, 2С19, 2D6, 2Е1 и 3А4), препарат в концентрациях до 100 мкМ не ингибировал активность этих ферментов. Таким образом, маловероятно, что азацитидин в концентрациях, достигаемых в клинических условиях, оказывал индуцирующее или ингибирующее действие на ферменты цитохрома CYP.
Выведение
Азацитидин быстро выводится из организма, после подкожного введения его период полувыведения составляет 41 ±8 мин. После подкожного введения азацитидина в дозе 75 мг/м2 1 раз в день в течение 7 дней не наблюдалось его аккумуляции. Большая часть азацитидина (50-85%) и/или его метаболитов выводится почками.
После внутривенного и подкожного введения 14С-азацитидина в моче определялось 85 и 50% введенных радиоизотопов, соответственно. Через кишечник выводится < 1% препарата.
Особые группы пациентов
Влияние нарушения функции печени (см. «Способ применения и дозы»), а также возраста, пола или расы на фармакокинетические параметры азацитидина не изучалось.
Почечная недостаточность
Почечная недостаточность не оказывает существенного влияния на фармакокинетические показатели экспозиции азацитидина после однократного и многократного подкожного введения.
После подкожного введения однократной дозы 75 мг/м2 значения показателей экспозиции /AUC и Сmах) у пациентов с почечной недостаточностью легкой, средней и тяжелой степени тяжести увеличились, соответственно, на 11-21%, 15-27% и 41-66% по сравнению со значениями этих показателей у пациентов с нормальной функцией почек. Тем не менее абсолютные значения экспозиции находились в пределах нормы. Для пациентов с почечной недостаточностью изменение стартовой дозы азацитидина не требуется.
Так как азацитидин и/или его метаболиты выводятся преимущественно почками, состояние пациентов с почечной недостаточностью следует тщательно мониторировать для контроля нежелательных явлений.
Показания:
Вайдаза применяется для лечения взрослых пациентов, которым не может быть выполнена трансплантация гемопоэтических стволовых клеток (ТГСК), имеющих:
— миелодиспластический синдром (МДС) с высокой или промежуточной-2 степенью риска в соответствии со шкалой IPSS (Международная прогностическая система баллов);
— острый миелоидный лейкоз;
— хронический миеломоноцитарный лейкоз без признаков МДС.
Противопоказания:
— Повышенная чувствительность к азацитидину или другим компонентам препарата.
— распространенные злокачественные опухоли печени;
— беременность и период грудного вскармливания;
— детский возраст (отсутствие данных по эффективности и безопасности).
С осторожностью:
У пациентов с сердечно-сосудистыми заболеваниями, заболеваниями легких, с нарушениями функции почек и печени.
Беременность и лактация:
Женщины репродуктивного возраста/ контрацепция у мужчин и женщин
Женщины репродуктивного возраста и мужчины должны использовать эффективные методы контрацепции во время лечения и в течение 3 месяцев после его окончания.
Беременность
Недостаточно данных о применении азацитидина у беременных. В исследованиях на животных выявлена репродуктивная токсичность (см. «Фармакодинамика»). Потенциальный риск для человека не известен.
Период грудного вскармливания
Неизвестно, проникает ли азацитидин/его метаболиты в грудное молоко. Учитывая возможные серьезные нежелательные лекарственные реакции (НЛР) у детей, находящихся на грудном вскармливании, женщины, которым показано лечение азацитидином, должны прекратить кормление грудью.
Фертильность
Не получено данных о влиянии азацитидина на фертильность человека. В исследованиях на животных показана способность азацитидина снижать репродуктивную функцию у самцов (см. «Фармакодинамика»).
Мужчинам следует рекомендовать избегать зачатия детей на фоне терапии азацитидином и применять надежные методы контрацепции как в период лечения, так и в течение 3 месяцев после его завершения.
Перед началом лечения мужчинам следует проконсультироваться относительно возможности консервации спермы.
Способ применения и дозы:
Лечение препаратом Вайдаза должно проводиться под наблюдением врача, имеющего опыт применения противоопухолевых препаратов. Перед введением препарата рекомендуется назначить противорвотные препараты.
Способ применения
Восстановленная суспензия препарата Вайдаза вводится подкожно в область плеча, бедра или живота. Места инъекции должны чередоваться. Место для очередной инъекции должно находиться более чем на 2,5 см от предыдущего. Препарат не должен вводиться в поврежденные, гиперемированные, уплотненные или болезненные участки кожи (в том числе в участки кожи с кровоизлияниями).
После восстановления суспензию не следует фильтровать. Подробные инструкции по восстановлению и введению препарата Вайдаза даны ниже (см. «Рекомендации по приготовлению раствора и проведению инъекции»).
Рекомендуемая начальная доза препарата Вайдаза при проведении первого цикла терапии для всех пациентов, независимо от значений исходных гематологических показателей, составляет 75 мг/м2 поверхности тела. Препарат вводится ежедневно в течение 7 дней с последующим перерывом в 21 день (28-дневный терапевтический цикл).
Должно быть проведено не менее 6 терапевтических циклов. Лечение продолжают до тех пор, пока сохраняется его эффективность или до появления симптомов прогрессирования заболевания.
В ходе наблюдения за пациентами оценивают ответ со стороны показателей крови и возможные проявления токсичности, в частности, со стороны крови и почек (см. «Особые указания»), которые могут потребовать отсрочки следующего курса лечения или снижения дозы препарата.
Лабораторные тесты
До начала лечения и перед каждым циклом лечения необходимо оценивать активность печеночных ферментов, концентрацию креатинина и натрия бикарбоната в плазме крови. Развернутый клинический анализ крови следует проводить до начала лечения и по мере необходимости для оценки ответа и степени токсических эффектов, но как минимум перед началом каждого цикла лечения.
Изменение дозы при выявлении симптомов гематологической токсичности
Гематологической токсичностью считается максимальное снижение количества клеток в течение данного цикла лечения (надир), если количество тромбоцитов снижается до 50,0х109/л и ниже и/или абсолютное число нейтрофилов (АЧН) снижается до 1х109/л и ниже.
Восстановлением считается повышение количества клеток в клеточной(ых) линии(ях) на, по меньшей мере, половину разницы между исходным количеством клеток и надиром, плюс надир (т.е. количество клеток при восстановлении > надир + (0,5х[исходное количество — надир]).
Пациенты, с исходными (до начала терапии препаратом Вайдаза) показателями количества лейкоцитов ≥3,0×109/л, абсолютного числа нейтрофилов ≥1,5×109/л, количества тромбоцитов ≥75,0х109/л
Если на фоне лечения препаратом Вайдаза у этих пациентов появляются симптомы гематологической токсичности, следующий цикл лечения препаратом откладывается до восстановления количества тромбоцитов и абсолютного количества нейтрофилов до исходных значений.
Если продолжительность восстановительного периода не превышает 14 дней, изменение дозы препарата не требуется. Если количество клеток крови не увеличилось до необходимого значения в течении 14 дней, доза препарата должна быть снижена согласно рекомендациям, изложенным ниже. При использовании измененной дозы продолжительность цикла терапии должна восстановиться до 28 дней.
|
Количество клеток крови |
% от начальной дозы для следующего цикла, если восстановление* количества клеток крови потребовало больше 14 дней |
|
|
Абсолютное число нейтрофилов |
Количество тромбоцитов |
|
|
≤1,0 х 109/л |
≤50,0 х 109/л |
50% |
|
>1,0 х 109/л |
>50,0 х 109/л |
100% |
* Восстановление = количество (к-во) ≥ надир + (0,5 х [Исходное к-во — надир])
Пациенты с исходными (до начала терапии препаратом Вайдаза) показателями количества лейкоцитов <3,0×109/л, абсолютного числа нейтрофилов <1,5×109/л, количества тромбоцитов <75,0х109/л
Если перед очередным курсом лечения препаратом Вайдаза наблюдается снижение количества лейкоцитов или абсолютного числа нейтрофилов или тромбоцитов ≤ 50% от их исходных значений, или более 50%, но при наличии признаков улучшения дифференциации любого клеточного ростка, схема введения препарата Вайдаза и его доза не должны меняться.
Пациентам, у которых количество клеток крови не превысило 50% порога от исходного уровня при отсутствии признаков улучшения дифференцировки клеточных ростков, очередной курс лечения препаратом Вайдаза должен быть отсрочен до восстановления абсолютного количества нейтрофилов и тромбоцитов.
Если восстановительный процесс занял не более 14 дней, изменение дозы препарата Вайдаза не требуется. Если количество клеток крови не достигло желаемого уровня в течение 14 дней, необходимо определение клеточного насыщения костного мозга. При показателе клеточного насыщения >50% не требуется изменение дозы препарата. Если клеточная насыщенность костного мозга ≤50%, введение препарата Вайдаза должно быть отложено, а доза уменьшена согласно приведенным в таблице рекомендациям:
|
Клеточное насыщение костного мозга |
% от начальной дозы для следующего цикла, если восстановление * количества клеток крови потребовало больше 14 дней |
|
|
Восстановление* ≤21 день |
Восстановление* >21день |
|
|
15-50% |
100% |
50% |
|
<15% |
100% |
33% |
* Восстановление = количество (к-во) ≥ надир ч- (0,5 х [Исходное к-во — надир])
После изменения дозы продолжительность цикла должна быть восстановлена до 28 дней.
Расчет индивидуальной дозы:
Общую дозу с учетом площади поверхности тела (ППТ) можно рассчитать следующим образом:
общая доза (мг) = доза (мг/м2) х ППТ (м2)
Пример расчета индивидуальной дозы азацитидина представлен в таблице ниже:
|
Поверхность тела (м2) |
100% рекомендованной начальной дозы (75 мг/м2) |
50% рекомендованной начальной дозы (37,5 мг/м2) |
33% рекомендованной начальной дозы (25 мг/м2) |
|||
|
Суточная доза |
Объем раствора |
Суточная доза |
Объем раствора |
Суточная доза |
Объем раствора |
|
|
1,4 |
105 мг |
4,2 мл ** |
52,5 мг |
2,1 мл |
35 мг |
1,4 мл * |
|
1,5 |
112,5 мг |
4,5 мл ** |
56,25 мг |
2,25 мл * |
37,5 мг |
1,5 мл * |
|
1,6 |
120 мг |
4,8 мл ** |
60 мг |
2,4 мл * |
40 мг |
1,6 мл * |
|
1,7 |
127,5 мг |
5,1 мл ** |
63,75 мг |
2,55 мл * |
42,5 мг |
1,7 мл * |
|
1,8 |
135 мг |
5,4 мл ** |
67,5 мг |
2,7 мл * |
45 мг |
1,8 мл * |
|
1,9 |
142,5 мг |
5,7 мл ** |
71,25 мг |
2,85 мл * |
47,5 мг |
1,9 мл * |
|
* 1 флакон, содержащий 100 мг азацитидина ** 2 флакона, содержащих 100 мг азацитидина |
Особенности применения у отдельных групп пациентов
Применение у пациентов с нарушениями функций почек
Не требуется изменять стартовую дозу азацитидина у пациентов с нарушениями функции почек (см. «Фармакокинетика»). При необъяснимом снижении концентрации бикарбонатов в сыворотке менее 20 ммоль/л доза препарата для следующего цикла терапии должна быть уменьшена на 50%.
При необъяснимом повышении концентрации креатинина сыворотки крови или концентрации азота мочевины в крови в 2 раза или более от исходных значений или выше верхней границы нормы очередной цикл терапии должен быть отложен до восстановления этих параметров до нормальных или исходных значений, а доза препарата в следующем цикле должна быть уменьшена на 50% (см. «Особые указания»).
Применение у пациентов с нарушениями функций печени
Специальных исследований у пациентов с нарушениями функций печени не проводилось (см. «Особые указания»). Состояние пациентов с тяжелой печеночной недостаточностью следует тщательно мониторировать для своевременного выявления нежелательных явлений. Данной категории пациентов не требуется изменять начальную дозу препарата. Последующее изменение дозы будет зависеть от результатов исследования крови.
Противопоказано применение препарата Вайдаза у пациентов с распространенными злокачественными опухолями печени (см. «Противопоказания» и «Особые указания»).
Пожилые пациенты
Пожилым пациентам не требуется специального режима дозирования.
Поскольку у пожилых пациентов вероятность нарушения функции почек выше, во время лечения рекомендуется мониторировать функцию почек.
Дети и подростки
Эффективность и безопасность применения препарата Вайдаза у детей в возрасте 0-17 лет в настоящее время не установлены. Данные по эффективности и безопасности отсутствуют.
Рекомендации по приготовлению раствора и проведению инъекции
Препарат Вайдаза — это цитотоксический лекарственный препарат, с которым, как и с другими токсическими веществами, следует обращаться с осторожностью. Любой неиспользованный или расходный материал должен быть утилизирован согласно локальным требованиям.
При контакте восстановленной суспензии азацитидина с кожей следует немедленно тщательно промыть ее водой с мылом. При попадании на слизистую оболочку — тщательно промыть ее водой.
Приготовление восстановленной суспензии
Препарат Вайдаза необходимо восстанавливать водой для инъекций. Срок хранения восстановленной суспензии препарата можно увеличить путем восстановления охлажденной (от 2 до 8 °С) водой для инъекций. Подробная информация о хранении восстановленного препарата представлена ниже (см. «После восстановления»).
1. Готовят следующие материалы:
флакон(ы) азацитидина; флакон(ы) воды для инъекций; нестерильные хирургические перчатки; салфетки, смоченные спиртом; шприц(ы) объемом 5 мл и иглу(ы).
2. Набирают шприцом 4 мл воды для инъекции, убедившись в отсутствии пузырьков воздуха в шприце.
3. Протыкают иглой шприца, содержащего 4 мл воды для инъекций, резиновую пробку флакона азацитидина и вводят воду для инъекций во флакон.
4. После добавления во флакон воды для инъекций и удаления иглы флакон энергично встряхивают до получения однородной суспензии белого цвета. После восстановления 1 мл суспензии содержит 25 мг азацитидина (100 мг/4 мл). Восстановленный препарат — это однородная суспензия белого цвета без агломератов. Не следует использовать препарат, содержащий крупные частицы или агломераты. После восстановления не следует фильтровать суспензию, так как это может удалить действующее вещество. Необходимо учесть, что некоторые адаптеры, иглы и закрытые системы снабжены фильтрами, поэтому, такие системы не должны быть использованы для введения лекарственного препарата после восстановления.
5. Протирают резиновую пробку флакона и вставляют в нее новый шприц с иглой. Затем переворачивают флакон вверх дном, убедившись, что кончик иглы находится ниже уровня жидкости. Оттягивают поршень шприца назад и набирают в шприц количество препарата, необходимое для получения точной дозы, убедившись в отсутствии пузырьков воздуха в шприце. Затем вынимают из флакона шприц с иглой и утилизируют иглу.
6. Плотно закрепляют на шприце новую иглу для подкожных введений (25 калибра). Не следует чистить иглу перед проведением инъекции для снижения частоты развития реакций в месте введения.
7. Если пациенту требуется более одного флакона с препаратом, следует повторно выполнить все вышеописанные этапы подготовки суспензии. В тех случаях, когда для получения необходимой дозы нужно более одного флакона с препаратом, эту необходимую дозу следует затем разделить поровну, например, доза 150 мг = 6 мл, 2 шприца по 3 мл в каждом. В связи с тем, что на стенках флакона и в игле остается часть препарата, не представляется возможным извлечь полностью весь объем суспензии из флакона.
8. Непосредственно перед введением необходимо повторно перевести содержимое шприца в состояние суспензии. Температура суспензии во время введения должна составлять 20-25 °С. Если время введения откладывается на 30 минут и более, суспензия подлежит уничтожению и готовится новая доза. Чтобы восстановить пригодность суспензии, энергично покатайте шприц между ладонями до появления однородной суспензии белого цвета. Запрещается использовать препарат, если он содержит крупные частицы и агломераты.
После восстановления
Если для восстановления препарата используют воду для инъекций, которая не была охлаждена в холодильнике, восстановленный препарат демонстрирует химическую и физическую стабильность при температуре 25 °С в течение 45 минут и при температуре 2-8 °С в течение 8 часов.
Срок хранения восстановленной суспензии может быть увеличен путем восстановления охлажденной (от 2 до 8 °С) водой для инъекций.
Если для восстановления препарата используют охлажденную (от 2 до 8 °С) воду для инъекций, восстановленный препарат демонстрирует химическую и физическую стабильность при температуре 2-8 °С в течение 22 часов.
С микробиологической точки зрения восстановленный препарат следует использовать немедленно. Если препарат не используется сразу, ответственность за сроки и условия хранения возлагается на пользователя, но в любом случае срок хранения не более 8 часов при температуре от 2 до 8 °С при восстановлении с использованием воды для инъекций, которая не была охлаждена в холодильнике, или не более 22 часов при восстановлении с использованием охлажденной (от 2 до 8 °С) воды для инъекций.
Побочные эффекты:
В Таблице 1 представлены НЛР, зарегистрированные на фоне лечения азацитидином в ходе основных клинических исследований у пациентов с МДС и острым миелоидным лейкозом, а также в пострегистрационном периоде.
Частота НЛР определялась соответственно следующей градации: очень часто: (>1/10); часто (≥1/100, <1/10); нечасто (≥1/1000, <1/100), редко (≥1/10000, <1/1000) и очень редко (< 1/10000); частота не установлена (оценить по имеющимся данным невозможно). Частота НЛР указана в Таблице 1 согласно максимальному значению, полученному в одном из основных клинических исследований.
Таблица 1: НЛР, зарегистрированные у пациентов с МДС и острым миелоидным лейкозом на фоне лечения азацитидином (в ходе клинических исследований и в пострегистрационном периоде).
|
Поражение органов и систем органов |
Очень часто |
Часто |
Нечасто |
Редко |
Частота не установлена |
|
Инфекционные и паразитарные заболевания |
пневмония* (включая бактериальную, вирусную и грибковую), назофарингит |
сепсис* (включая бактериальный, вирусный и грибковый), сепсис на фоне нейтропении*, инфекции дыхательных путей (верхних отделов и бронхит), инфекции мочевыводящих путей, воспаление подкожной клетчатки, дивертикулит, грибковое поражение слизистой оболочки полости рта, синусит. фарингит, ринит, простой герпес, кожные инфекции |
некротизирующий фасциит* |
||
|
Нарушения со стороны крови и лимфатической системы |
фебрильная нейтропения*, нейтропения, лейкопения, тромбоцитопения, анемия |
панцитопения*, недостаточность костного мозга |
|||
|
Нарушения со стороны иммунной системы |
реакции гиперчувствительности |
||||
|
Нарушения со стороны обмена веществ и питания |
анорексия, снижение аппетита, гипокалиемия |
дегидратация |
синдром лизиса опухоли |
||
|
Нарушения психики |
бессонница |
спутанность сознания, тревожность |
|||
|
Нарушения со стороны нервной системы |
головокружение, головная боль |
внутричерепное кровотечение*, обморок, сонливость, летаргия |
|||
|
Нарушения со стороны органа зрения |
внутриглазное кровотечение, кровоизлияние в конъюнктиву |
||||
|
Нарушения со стороны сердца |
выпот в полость перикарда |
перикардит |
|||
|
Нарушения со стороны сосудов |
снижение артериального давления* (АД), повышение АД, ортостатическая гипотензия. гематома |
||||
|
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения |
одышка, носовое кровотечение |
плевральный выпот, одышка при физической нагрузке, боль в гортани и глотке |
интерстициальное заболевание легких |
||
|
Нарушения со стороны желудочно-кишечного тракта |
диарея, рвота, запор, тошнота, боль в животе, включая чувство дискомфорта в эпигастральной области и в животе |
желудочно-кишечное кровотечение* (включая кровотечения в полости рта), геморроидальное кровотечение, стоматит, кровоточивость десен, диспепсия |
|||
|
Нарушения со стороны печени и желчевыводящих путей |
печеночная недостаточность*, прогрессирующая печеночная кома |
||||
|
Нарушения со стороны кожи и подкожных тканей |
петехии,зуд (включая генерализованный), сыпь, экхимозы |
пурпура, алопеция, крапивница, эритема, пятнистая сыпь |
острый фебрильный нейтрофильный дерматоз, гангренозная пиодермия |
||
|
Нарушения со стороны скелетно-мышечной и соединительной ткани |
артралгия, костно-мышечная боль (включая боль в спине, костях и конечностях) |
мышечные спазмы, миалгия |
|||
|
Нарушения со стороны почек и мочевыводящих путей |
почечная недостаточность *, гематурия, повышение концентрации креатинина |
почечный канальцевый ацидоз |
|||
|
Общие расстройства и нарушения в месте введения |
пирексия*, повышенная утомляемость, астения, боль в области грудной клетки; покраснение, боль и реакции в месте введения (не уточнены) |
кровоизлияние, гематома уплотнение, сыпь, зуд, воспаление, изменение цвета кожных покровов, образование узелков и кровоточивость (в месте инъекции), недомогание, озноб, кровоточивость в месте установки катетера |
некроз в месте инъекции |
||
|
Лабораторные и инструментальные данные |
уменьшение массы тела |
* — редко сопровождались летальным исходом.
Описание отдельных НЛР
Гематологические НЛР
Наиболее частыми (наблюдавшимися у ≥10% пациентов) гематологическими НЛР, связанными с применением азацитидина, являлись анемия, тромбоцитопения, нейтропения, фебрильная нейтропения и лейкопения (обычно 3-4 степени тяжести). Наибольший риск развития этих реакций отмечается во время первых двух циклов терапии, после чего они с меньшей частотой возникают у пациентов с восстановившейся гематопоэтической функцией.
С большинством гематологических реакций удавалось справляться путем регулярного развернутого исследования крови, отсрочки очередного цикла лечения, профилактического назначения антибиотиков и/или фактора роста (например, колонисстимулирующего фактора) при нейтропении и гемотрансфузий при анемии или тромбоцитопении в случае необходимости.
Инфекции
Миелосупрессия может привести к развитию нейтропении и повышению риска инфекции. У пациентов на фоне лечения азацитидином были отмечены серьезные НЛР, такие как сепсис, в том числе на фоне нейтропении, и пневмония, некоторые — с летальным исходом. При развитии инфекций может быть назначена антибактериальная терапия, а также фактор роста (например, колониестимулирующий фактор) при нейтропении.
Кровотечения
У пациентов, получающих лечение азацитидином, могут развиваться кровотечения, в том числе, относящиеся к категории серьезных НЛР, такие как желудочно-кишечные и внутричерепные кровотечения. Необходимо осуществлять контроль признаков и симптомов, позволяющих диагностировать кровотечения, в особенности, у пациентов с исходной тромбоцитопенией или тромбоцитопенией, связанной с лечением.
Гиперчувствительность
У пациентов, получавших лечение азацитидином, отмечались реакции гиперчувствительности, относящиеся к категории серьезных. В случае развития анафилактических реакций лечение азацитидином должно быть немедленно прекращено и назначена симптоматическая терапия.
Нежелательные реакции со стороны кожи и подкожных тканей
Большинство НЛР со стороны кожи и подкожных тканей развивались в месте инъекции. Ни одна из этих НЛР не привела к отмене терапии азацитидином или уменьшению дозы азацитидина в ходе клинических исследований. Большинство НЛР развивалось во время двух первых циклов лечения, при этом отмечалась тенденция к их уменьшению при продолжении лечения.
Такие локальные НЛР как сыпь, воспаление, зуд в месте инъекции, эритема и поражение кожи могут потребовать назначения сопутствующей терапии антигистаминными препаратами, глюкокортикостероидами и нестероидными противовоспалительными препаратами (НПВП). Эти реакции со стороны кожи следует дифференцировать с инфекциями мягких тканей, иногда развивающимися в месте инъекции.
Инфекции мягких тканей, включая флегмону и некротизирующий фасциит, с редкими летальными исходами, были отмечены на фоне применения азацитидина в пострегистрационном периоде. Рекомендации по лечению инфекционных осложнений указаны выше (см. «Инфекции»).
Желудочно-кишечные НЛР
Наиболее частыми желудочно-кишечными НЛР, связанными с терапией азацитидином, были запор, диарея, тошнота и рвота. При развитии вышеуказанных НЛР назначали симптоматическую терапию противорвотными препаратами для купирования тошноты и рвоты, антидиарейными препаратами для лечения диареи, и слабительными препаратами для лечения запора.
НЛР со стороны почек
У пациентов, получавших лечение азацитидином, были отмечены нарушения функции почек, включавшие различные состояния от повышения уровня креатинина и гематурии до развития почечного канальцевого ацидоза, почечной недостаточности, в том числе с летальным исходом (см. «Особые указания»).
НЛР со стороны печени
На фоне лечения азацитидином у пациентов с распространенным метастатическим поражением печени отмечены случаи развития печеночной недостаточности, прогрессирующей печеночной комы с летальным исходом (см. «Особые указания»).
Сердечно-сосудистые НЛР
Согласно данным клинического исследования у пациентов, получавших азацитидин по поводу впервые выявленного ОМЛ, в ходе которого было разрешено включать пациентов, имевших указание в анамнезе на сердечно-сосудистое или легочное заболевание, было отмечено статистически значимое увеличение частоты НЛР со стороны сердца (см. «Особые указания»).
Пожилые пациенты
Имеются ограниченные данные о безопасности применения азацитидина у пациентов в возрасте ≥85 лет (в том числе у 14 [5,9%] пациентов в возрасте ≥85 лет, принимавших участие в исследовании AZA-AML-001).
Информирование о подозрении на НЛР
Важно сообщать обо всех подозреваемых НЛР в пострегистрационном периоде. Своевременное информирование позволяет контролировать соотношение пользы и риска при применении лекарственного препарата. Специалистов здравоохранения просят сообщать обо всех подозреваемых НЛР в национальную службу по мониторингу эффективности и безопасности лекарственных препаратов.
Передозировка:
Сообщалось об одном случае передозировки азацитидина в ходе клинического исследования.
У пациента отмечалась диарея, тошнота и рвота после однократного внутривенного введения препарата в дозе 290 мг/м2, которая превышала рекомендованную начальную дозу почти в 4 раза.
При передозировке рекомендуется мониторировать концентрацию соответствующих клеток крови и назначать, при необходимости, поддерживающее лечение.
Не существует специфического антидота при передозировке азацитидином.
Взаимодействие:
Данные исследований in vitro свидетельствуют о том, что участие изоферментов системы цитохрома Р450, UDP-глюкуронилтрансферазы, сульфотрансферазы и глютатионтрансферазы в метаболизме азацитидина маловероятно. В связи с этим взаимодействие in vivo с данными ферментами, участвующими в метаболизме, не представляется клинически значимым.
Клинически значимое ингибирующее или индуцирующее действие азацитидина на ферменты цитохрома Р450 маловероятно (см. «Фармакокинетика»).
Не проводилось целенаправленных клинических исследований взаимодействия азацитидина с другими лекарственными препаратами.
Особые указания:
Лабораторные тесты
До начала лечения и перед каждым циклом лечения необходимо оценивать активность печеночных ферментов, концентрацию креатинина и натрия бикарбоната в плазме крови. Развернутый клинический анализ крови следует проводить до начала лечения и по мере необходимости для оценки ответа и степени токсических эффектов, но как минимум перед началом каждого цикла лечения (см. «Побочное действие»).
Сердечно-сосудистые и легочные заболевания
Пациенты, страдающие тяжелой застойной сердечной недостаточностью, другими выраженными сердечно-сосудистыми или легочными заболеваниями, не были включены в регистрационные исследования (AZA PH GL 2003 CL 001 и AZA-AML-001), поэтому безопасность и эффективность препарата Вайдаза у них не установлена.
Данные, полученные в ходе недавних клинических исследований препарата Вайдаза, показали, что частота нежелательных сердечно-сосудистых явлений существенно выше у пациентов, имеющих в анамнезе сердечно-сосудистые заболевания или заболевания легких (см. «Побочное действие»). Поэтому данной категории пациентов препарат Вайдаза следует назначать с осторожностью. До начала лечения и во время терапии препаратом Вайдаза рекомендуется проводить исследование сердечно-сосудистой и легочной системы.
Некротизирующий фасциит
Некротизирующий фасциит, включая случаи с летальным исходом, был зарегистрирован у пациентов на фоне применения препарата Вайдаза. У пациентов, у которых диагностирован некротизирующий фасциит, терапия препаратом Вайдаза должна быть прекращена, и незамедлительно назначено соответствующее лечение.
Синдром лизиса опухоли
Высокий риск развития синдрома лизиса опухоли отмечается у тех пациентов, у которых выявляется высокая опухолевая нагрузка перед началом лечения. За этими пациентами необходимо установить постоянное наблюдение и принимать соответствующие меры предосторожности.
Гематологическая токсичность
Лечение азацитидином сопровождается развитием анемии, нейтропении и тромбоцитопении, особенно в течение первых двух циклов (см. «Побочное действие»). Для контроля эффективности лечения и возможных НЛР должен проводиться развернутый анализ крови, как минимум, перед каждым циклом лечения. После проведения первого лечебного цикла доза для последующего лечения рассчитывается на основе исходных показателей и их динамики в процессе лечения. Медицинский персонал и пациент должны получить указания о необходимости контроля температуры тела (лихорадки) и симптомов, позволяющих диагностировать кровотечение.
Нарушения функций печени
Специальные исследования у пациентов с нарушениями функций печени не проводились. На фоне лечения азацитидином у пациентов с распространенными метастатическими поражениями печени отмечены случаи развития печеночной комы с летальным исходом, особенно при уровне альбумина в сыворотке крови < 30 г/л.
Противопоказано применение азацитидина у пациентов с распространенными злокачественными опухолями печени (см. «Противопоказания»).
Нарушения функций почек
У пациентов, получавших лечение азацитидином внутривенно в сочетании с другими химиотерапевтическими препаратами, отмечались нарушения функции почек, включавшие различные состояния: от повышения концентрации креатинина в плазме крови до развития почечной недостаточности, в том числе с летальным исходом. Кроме того почечный канальцевый ацидоз, диагностированный на основании снижения концентрации бикарбонатов в плазме крови <20 ммоль/л в сочетании с защелачиванием мочи и гипокалиемией (концентрация калия в плазме крови <3 ммоль/л) развился у 5 пациентов с хроническим миелолейкозом, получавших лечение азацитидином и этопозидом.
В случае необъяснимого снижения концентрации бикарбонатов в плазме крови (<20 ммоль/л) или необъяснимого повышения концентрации креатинина или концентрации мочевины в плазме крови доза препарата должна быть снижена или очередной цикл терапии должен быть отложен (см. «Способ применения и дозы»). Пациентов следует проинструктировать немедленно сообщать врачу о развитии олигурии и анурии.
Хотя не отмечено клинически значимой разницы в частоте нежелательных явлений у пациентов с нормальной и нарушенной функцией почек, состояние пациентов с почечной недостаточностью следует тщательно мониторировать для контроля нежелательных явлений, так как азацитидин/его метаболиты выводятся преимущественно почками.
Влияние на способность управлять транспортными средствами и механизмами:
Азацитидин оказывает незначительное или умеренно выраженное влияние на способность пациента к управлению транспортными средствами и использованию механизмов. Учитывая возможность развития слабости на фоне лечения препаратом Вайдаза, следует соблюдать особую осторожность при выполнении этих видов деятельности при появлении данного нежелательного явления.
Форма выпуска/дозировка:
Лиофилизат для приготовления суспензии для подкожного введения, 100 мг.
Упаковка:
200 мг лиофилизата во флаконе из бесцветного стекла типа I вместимостью 30 мл, укупоренном резиновой пробкой, уплотненной сверху алюминиевым колпачком с отрывающейся пластмассовой крышечкой, на боковую поверхность колпачка наносят номер серии препарата «ин балк». На флакон наносят этикетку.
Один флакон вместе с инструкцией по применению помещают в пачку картонную с контролем первого вскрытия (специальный стикер).
Условия хранения:
Хранить при температуре не выше 30 °С.
Хранить в недоступном для детей месте.
Срок годности:
4 года
Не применять после даты истечения срока годности.
Условия отпуска
По рецепту
Производитель
Открытое акционерное общество «Фармстандарт-Уфимский витаминный завод» (ОАО «Фармстандарт-УфаВИТА»), 450077, Республика Башкортостан, г. Уфа, ул. Худайбердина, д. 28, Россия
Владелец регистрационного удостоверения/организация, принимающая претензии потребителей:
Селджен Интернешнл Сарл.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Вайдаза (Vidaza) инструкция по применению
📜 Инструкция по применению Вайдаза
💊 Состав препарата Вайдаза
✅ Применение препарата Вайдаза
📅 Условия хранения Вайдаза
⏳ Срок годности Вайдаза
Описание лекарственного препарата
Вайдаза
(Vidaza)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для электронного издания справочника Видаль 2014
года, дата обновления: 2013.05.30
Владелец регистрационного удостоверения:
Код ATX:
L01BC07
(Азацитидин)
Лекарственная форма
| Вайдаза |
Лиофилизат д/пригот. сусп. д/п/к введения 100 мг: фл. 1 шт. рег. №: ЛСР-003474/10 |
Форма выпуска, упаковка и состав
препарата Вайдаза
Лиофилизат для приготовления суспензии для п/к введения в виде порошка или пористой массы белого цвета; приготовленная суспензия белого цвета.
Вспомогательные вещества: маннитол — 100 мг.
Флаконы бесцветного стекла вместимостью 30 мл (1) — пачки картонные.
Фармакологическое действие
Противоопухолевый препарат. Антиметаболит. Противоопухолевое действие азацитидина обусловлено разнообразными механизмами, включая цитотоксичность в отношении патологически измененных гемопоэтических клеток костного мозга и гипометилирование ДНК. Механизмы, участвующие в реализации цитотоксического действия азацитидина, включают ингибирование синтеза ДНК, РНК и белка, инкорпорацию препарата в ДНК и РНК, а также активацию путей повреждения ДНК. Непролиферирующие клетки практически не чувствительны к азацитидину. Инкорпорация азацитидина в ДНК приводит к инактивации метилтрансферазы ДНК, в результате чего происходит гипометилирование ДНК. Гипометилирование ДНК в аберрантно метилированных генах, присутствующее и в регуляторном цикле нормальных клеток, их дифференциации и клеточной смерти, может вызывать ре-экспрессию гена и восстановление свойств подавления опухолевого роста у самих раковых клеток. Клиническая значимость механизма гипометилирования ДНК в сравнении с цитотоксическим и другими эффектами азацитидина еще не установлена.
Клиническая эффективность и безопасность Вайдазы была подтверждена результатами многоцентрового рандомизированного исследования III фазы. У больных с миелодиспластическим синдромом, хроническим миеломоноцитарным лейкозом и острым миелолейкозом терапия Вайдазой превосходила современную традиционную терапию по всем критериям эффективности, включая продолжительность жизни и общую частоту ответа на лечение.
Фармакокинетика
Всасывание
После п/к введения азацитидин быстро абсорбируется, достигая Cmax 750±403 нг/мл через 0.5 ч после введения. Абсолютная биодоступность азацитидина при п/к введении составляет 89% по отношению к данному показателю при в/в введении на основании результатов определения AUC.
Метаболизм
Результаты исследования in vitro показали, что в метаболизме азацитидина не участвуют изоферменты системы цитохрома Р450, UDP-глюкуронилтрансфераза, сульфотрансфераза и глютатионтрансфераза. Азацитидин метаболизируется путем спонтанного гидролиза и дезаминирования, которое индуцируется цитидиндезаминазой.
Выведение
Азацитидин быстро выводится из организма, его T1/2 после п/к введения составляет 41±8 мин. Большая часть азацитидина (50-85%) и/или его метаболитов выводится почками. Через кишечник выводится менее 1% препарата. Данных о поступлении азацитидина в грудное молоко нет.
Фармакокинетика в особых клинических случаях
Влияние нарушения функции печени или почек, а также возраста, пола или расы на фармакокинетические параметры азацитидина не изучалось.
Показания препарата
Вайдаза
Лечение взрослых больных, у которых не может быть выполнена трансплантация гемопоэтических стволовых клеток:
- миелодиспластический синдром (МДС) с высокой или промежуточной-2 степенью риска в соответствии со шкалой IPSS (Международная прогностическая система баллов);
- острый миелоидный лейкоз;
- хронический миеломоноцитарный лейкоз без признаков МДС.
Режим дозирования
Препарат Вайдаза вводят п/к в область плеча, бедра или живота. Места инъекции следует чередовать. Место для очередной инъекции должно находиться более чем на 2.5 см от предыдущего. Вайдаза не должна вводиться в поврежденные, гиперемированные, уплотненные или болезненные участки кожи (в т.ч. в участки кожи с кровоизлияниями).
Перед введением Вайдазы рекомендуется назначить противорвотные препараты.
Рекомендуемая начальная доза препарата Вайдаза при проведении первого цикла терапии для всех пациентов, независимо от значений исходных гематологических показателей, составляет 75 мг/м2 поверхности тела и вводится ежедневно в течение 7 дней с последующим перерывом в 21 день (28-дневный терапевтический цикл).
Должно быть проведено не менее 6 терапевтических циклов. Лечение продолжают до тех пор, пока сохраняется его эффективность или до появления симптомов прогрессирования заболевания.
В ходе наблюдения за больными оценивают ответ со стороны показателей крови и возможные проявления токсичности, в частности со стороны крови и почек, которые могут требовать отсрочки следующего курса лечения или коррекции дозы препарата. Ниже представлены возможности модификации дозы препарата Вайдаза при развитии различных видов токсичности.
Модификация дозы при выявлении симптомов гематологической токсичности
Гематологической токсичностью считается максимальное снижение количества клеток в течение данного цикла лечения (надир), если количество тромбоцитов снижается до 50×109/л и ниже и/или абсолютное число нейтрофилов (АЧН) снижается до 1×109/л и ниже.
Восстановлением считается повышение количества клеток в клеточной(ых) линии(ях) на, по крайней мере, половину разницы между исходным количеством клеток и надиром (т.е. количество клеток при восстановлении > надир + (0.5×([исходное количество — надир]).
Пациенты с исходными (до начала терапии Вайдазой) показателями количества лейкоцитов >3×10 9/л, абсолютного количества нейтрофилов >1.5×10 9/л, количества тромбоцитов >75×10 9/л
Если на фоне лечения препаратом Вайдаза у этих пациентов появляются симптомы гематологической токсичности, следующий цикл лечения препаратом откладывается до восстановления количества тромбоцитов и абсолютного количества нейтрофилов до исходных значений. Если продолжительность восстановительного периода не превышает 14 дней, модификации дозы препарата не требуется. Если количество клеток крови не увеличилось до необходимого уровня в течении 14 дней, доза препарата должна быть снижена согласно рекомендациям изложенным ниже. При использовании модифицированной дозы, продолжительность цикла терапии должна восстановиться до 28 дней.
* Восстановление = количество (к-во) ≥ минимальное к-во + (0.5 × [Исходное к-во — минимальное к-во])
Пациенты с исходными (до начала терапии Вайдазой) показателями количества лейкоцитов <3×10 9/л, абсолютного количества нейтрофилов<1.5×10 9/л, количества тромбоцитов <75×10 9/л.
Если перед очередным курсом лечения препаратом Вайдаза наблюдается снижение количества лейкоцитов или абсолютного количества нейтрофилов или тромбоцитов менее или равное 50% от их исходных значений, или более 50%, но при наличии признаков улучшения дифференциации любого клеточного ростка, схема введения препарата Вайдаза и его доза не должны меняться.
Пациентам, у которых количество клеток крови не превысило 50% порога от исходного уровня при отсутствии признаков улучшения дифференцировки клеточных ростков, очередной курс лечения препаратом Вайдаза должен быть отсрочен до восстановления абсолютного количества нейтрофилов и тромбоцитов. Если восстановительный процесс занял не более 14 дней, коррекция дозы препарата Вайдаза не требуется. Если количество клеток крови не достигло желаемого уровня в течение 14 дней, необходимо определение клеточного насыщения костного мозга. При показателе клеточного насыщения > 50% не требуется изменения дозы препарата. Если клеточная насыщенность костного мозга ≤ 50%, введение препарата Вайдаза должно быть отложено, а доза уменьшена согласно приведенным в таблице рекомендациям:
* Восстановление = количество (к-во) ≥ минимальное к-во + (0.5 × [Исходное к-во — минимальное к-во])
После модификации дозы, продолжительность цикла должна быть восстановлена до 28 дней.
Пример расчета индивидуальной дозы азацитидина представлен в таблице ниже:
Особенности применения у отдельных групп пациентов
У пациентов с нарушением функции почек специальных исследований не проводилось. Пациентам с почечной недостаточностью тяжелой степени требуется тщательное мониторирование для контроля нежелательных явлений. Не требуется изменять начальную дозу препарата у пациентов с нарушениями функции почек (например, исходный уровень креатинина сыворотки крови или концентрация мочевины в крови в 2 раза больше ВГН или концентрация бикарбоната менее 20 ммоль/л). Последующая модификация дозы базируется на результатах исследования гематологических параметров и показателей функции почек. При необъяснимом снижении концентрации бикарбонатов в сыворотке менее 20 ммоль/л доза препарата для следующего цикла терапии должна быть уменьшена на 50%. При необъяснимом повышении концентрации креатинина сыворотки крови или концентрации азота мочевины в крови в 2 или более раза от исходных значений или выше ВГН, очередной цикл терапии должен быть отложен до восстановления этих параметров до нормальных или исходных значений, а доза препарата в следующем цикле должна быть уменьшена на 50%.
У пациентов с нарушениями функции печени специальных исследований не проводилось. Пациентам с тяжелой печеночной недостаточностью требуется тщательное мониторирование для своевременного выявления нежелательных явлений. Данной категории пациентов не требуется изменять начальную дозу препарата. Последующая модификация дозы будет зависеть от результатов исследования крови.
Пациентам пожилого возраста не требуется специального режима дозирования. Поскольку у данной категории пациентов вероятность нарушения функции почек выше, во время лечения рекомендуется мониторировать функцию почек.
Не рекомендуется назначать Вайдазу детям и подросткам младше 18 лет ввиду недостаточного клинического опыта.
Правила приготовления раствора и проведения инъекций
Содержимое флакона с препаратом следует растворить в 4 мл воды для инъекций до концентрации 25 мг/1 мл. После добавления во флакон воды для инъекций его необходимо энергично потрясти до получения однородной суспензии белого цвета. При необходимой дозе, превышающей 100 мг, используются 2 флакона с препаратом.
Непосредственно перед введением необходимо повторно перевести содержимое шприца в состояние суспензии. Для этого следует энергично покатать шприц между ладонями до получения однородной суспензии белого цвета. Температура суспензии во время инъекции должна составлять 20-25°С. Не использовать препарат, если он содержит крупные частицы.
Для проведения п/к инъекции рекомендуется использовать иглу 25 калибра, при этом иглу следует ввести под кожу плеча, бедра или живота под углом 45-90°. В одну область следует вводить не более 4 мл растворенного препарата. Дозы более 4 мл следует вводить в 2 разные области.
Суспензию Вайдаза следует готовить немедленно перед использованием. Готовую суспензию хранить при температуре 25°С не более 45 мин или при температуре от 2° до 8°С не более 8 ч. Необходимо, чтобы перед введением температура суспензии в шприце достигла 20-25°С (но не более чем в течение 30 мин). Если данные временные ограничения превышены, приготовленная суспензия должны быть утилизирована соответствующим образом, и новая суспензия должна быть приготовлена.
Побочное действие
Наиболее часто: гематологические реакции (71.4%), включая тромбоцитопению, нейтропению и лейкопению (обычно 3-4 степени тяжести); желудочно-кишечные осложнения (60.6%), включая тошноту и рвоту (обычно 1-2 степени тяжести) или локальные реакции в месте введения (77.1%; степень тяжести 1-2); серьезные нежелательные реакции — фебрильная нейтропения (8%), анемия (2.3%), а также — сепсис на фоне нейтропении, пневмония, тромбоцитопения и кровотечения (например, внутричерепные).
Определение частоты побочных реакций: очень часто (≥1/10), часто (≥1/100, <1/10), нечасто (≥1/1000, <1/100), редко (≥1/10 000, <1/1000), очень редко (<1/10 000); неизвестно (оценить по имеющимся данным невозможно).
Со стороны системы кроветворения: очень часто — нейтропения, фебрильная нейтропения, лейкопения, тромбоцитопения, анемия; часто – панцитопения.
Со стороны пищеварительной системы: очень часто — диарея, запор, тошнота, рвота, боль в животе, анорексия; часто — желудочно-кишечное кровотечение, геморроидальное кровотечение, стоматит, кровоточивость десен, диспепсия.
Со стороны печени и желчевыводящих путей: нечасто — печеночная недостаточность, прогрессирующая печеночная кома.
Со стороны нервной системы: очень часто — головокружение, головная боль; часто — внутричерепное кровотечение, сонливость,
Со стороны психики: спутанность сознания, тревожность, бессонница.
Со стороны сердечно-сосудистой системы: часто — повышение или снижение АД, гематомы.
Со стороны дыхательной системы: очень часто — одышка; часто — одышка при физической нагрузке, боль в гортани и глотке; редко — интерстициальные заболевания легких.
Со стороны мочевыделительной системы: часто — гематурия, почечная недостаточность, повышение концентрации креатинина; нечасто — почечноканальцевый ацидоз.
Со стороны кожи и подкожно-жировой клетчатки: очень часто — петехии, зуд, сыпь, экхимозы; часто — пурпура, алопеция, эритема, пятнистая сыпь.
Со стороны костно-мышечной системы: очень часто — артралгия; часто — боли в костях, миалгия.
Со стороны органа зрения: часто — внутриглазные кровотечения, кровоизлияния в конъюнктиву.
Инфекции: очень часто — пневмония, назофарингит; часто — сепсис на фоне нейтропении, инфекции верхних дыхательных путей и мочевыводящих путей, воспаление подкожной клетчатки, синусит, фарингит, ринит, простой герпес.
Со стороны иммунной системы: нечасто — реакции гиперчувствительности.
Со стороны обмена веществ: очень часто — анорексия, часто — гипокалиемия; редко — синдром лизиса опухоли.
Местные реакции: очень часто — боль и покраснение, неспецифические реакции в месте инъекции; часто — кровоточивость, кровоизлияние, гематома, уплотнение, воспаление, сыпь, зуд, изменение цвета кожных покровов, образование узелков и болезненность в месте введения; редко — некроз тканей в месте введения.
Прочие: очень часто — слабость, лихорадка, боли в области грудной клетки; часто — уменьшение массы тела.
Противопоказания к применению
- распространенные метастазы в печени;
- беременность;
- лактация (период грудного вскармливания);
- детский возраст (отсутствие данных по эффективности и безопасности);
- повышенная чувствительность к азацитидину или другим компонентам препарата.
С осторожностью следует применять препарат у пациентов с сердечно-сосудистыми заболеваниями, заболеваниями легких, с нарушениями функции почек и печени, включая обширные метастатические поражения печени.
Применение при беременности и кормлении грудью
Препарат противопоказан при беременности и в период грудного вскармливания.
Мужчины и женщины детородного возраста должны использовать эффективные методы контрацепции во время лечения и в течение 3 месяцев после его окончания. Мужчинам следует рекомендовать рассмотреть возможность консервации образцов собственной спермы перед началом лечения.
Применение при нарушениях функции печени
С осторожностью при нарушении функции печени.
Специальных исследований у больных с нарушениями функций печени не проводилось. Больные с тяжелой печеночной недостаточностью должны тщательно мониторироваться для своевременного выявления нежелательных явлений. Данной категории больных не требуется изменять начальную дозу препарата. Последующая модификация дозы будет зависеть от результатов исследования крови.
На фоне лечения азацитидином у пациентов с распространенными метастатическими поражениями печени, особенно при уровне альбумина в сыворотке крови менее 30 г/л, отмечены случаи развития печеночной комы с летальным исходом.
Применение при нарушениях функции почек
С осторожностью при нарушении функции почек.
Специальных исследований у больных с нарушением функции почек не проводилось. Больные с тяжелой почечной недостаточностью должны тщательно мониторироваться для контроля нежелательных явлений. Не требуется изменять начальную дозу препарата у больных с нарушениями функции почек (например, исходный уровень креатинина сыворотки крови или концентрация мочевины в крови в 2 раза больше верхней границы нормы (ВГН) или концентрация бикарбоната менее 20 ммоль/л). Последующая модификация дозы базируется на результатах исследования гематологических параметров и показателей функции почек. При необъяснимом снижении уровня бикарбонатов в сыворотке менее 20 ммоль/л доза препарата для следующего цикла терапии должна быть уменьшена на 50%. При необъяснимом повышении уровня креатинина сыворотки крови или концентрации азота мочевины в крови в 2 или более раза от исходных значений или выше ВГН, очередной цикл терапии должен быть отложен до восстановления этих параметров до нормальных или исходных значений, а доза препарата в следующем цикле должна быть уменьшена на 50%.
Применение у детей
Противопоказано в детском возрасте (отсутствие данных по эффективности и безопасности).
Применение у пожилых пациентов
Пожилым больным не требуется специального режима дозирования. Поскольку у пожилых больных вероятность нарушения функции почек выше, во время лечения рекомендуется мониторировать функцию почек.
Особые указания
Лечение препаратом Вайдаза должно проводиться под наблюдением врача, имеющего опыт применения противоопухолевых препаратов.
Безопасность и эффективность Вайдазы у пациентов, страдающих тяжелой застойной сердечной недостаточностью, другими выраженными сердечно-сосудистыми или легочными заболеваниями не установлена.
До начала терапии и перед началом каждого цикла должны быть получены результаты исследования функциональной активности печени и креатинина сыворотки крови, а также данные развернутого анализа крови. Регулярные анализы крови показаны для мониторирования эффективности и безопасности лечения.
Наиболее частыми побочными эффектами при лечении азацитидином являлись гематологические реакции, включая тромбоцитопению, нейтропению и лейкопению (обычно 3-4 степени тяжести). Наибольший риск развития этих реакций отмечается во время первых двух циклов терапии, после чего они с меньшей частотой возникают у пациентов с восстановившимися гематологическими показателями. Большинство гематологических реакций разрешается при отсрочке очередного цикла лечения, профилактическом назначении антибиотиков и/или колониестимулирующего фактора при нейтропении и гемотрансфузий при анемии или тромбоцитопении.
Развернутый анализ крови должен проводиться для контроля эффективности лечения и возможных побочных реакций как минимум перед каждым циклом лечения. После проведения первого лечебного цикла дозировка для последующего лечения рассчитывается на основе исходных показателей и их динамики в процессе лечения.
Медицинский персонал и пациент должны получить указания о необходимости контроля температуры тела (лихорадки) и симптомов позволяющих диагностировать кровотечение.
Миелосупрессия может привести к нейтропении и увеличению риска инфекции. У пациентов на фоне лечения азацитидином отмечались серьезные побочные реакции, такие как сепсис на фоне нейтропении (0.8%) и пневмония (2.5%). В случае инфекционных осложнений возможно назначение этиотропного лечения и колониестимулирующего фактора при нейтропении.
У пациентов, получающих лечение азацитидином, могут развиваться кровотечения, в т.ч. относящиеся к категории серьезных побочных реакций, такие как желудочно-кишечные (0.8%) и внутричерепные кровотечения (0.5%). Необходимо осуществлять контроль симптомов, позволяющих диагностировать кровотечения, особенно у пациентов с исходной тромбоцитопенией или тромбоцитопенией, возникшей на фоне лечения.
У пациентов, получавших лечение азацитидином, отмечались реакции гиперчувствительности, относящиеся к категории серьезных (0.25%). В случае развития анафилактических реакций лечение азацитидином должно быть немедленно остановлено и назначено симптоматическое лечение.
Большинство побочных реакций со стороны кожи и подкожно-жировой клетчатки отмечались в месте инъекции. Большинство подобных реакций возникало во время двух первых циклов лечения, при этом отмечалась тенденция к их уменьшению при продолжении лечения. Такие местные побочные реакции как сыпь, воспаление, зуд в месте инъекции, эритема могут потребовать назначения антигистаминных препаратов, кортикостероидов и НПВС.
На фоне лечения азацитидином у пациентов с распространенными метастатическими поражениями печени отмечены случаи развития печеночной комы с летальным исходом.
У пациентов, получавших лечение азацитидином, в редких случаях отмечались нарушения функции почек, включавшие различные состояния от повышения уровня креатинина и почечноканальцевого ацидоза до развития почечной недостаточности, в т.ч. с летальным исходом.
При необъяснимом снижении уровня бикарбонатов в сыворотке, необъяснимом повышении уровня креатинина сыворотки крови или концентрации мочевины в крови очередной цикл терапии должен быть отложен до восстановления этих параметров до нормальных или исходных значений, а доза препарата в следующем цикле должна быть уменьшена. Т.к. азацитидин и его метаболиты выводятся преимущественно почками, пациенты с почечной недостаточностью должны тщательно мониторироваться для контроля нежелательных явлений.
На фоне лечения азацитидином наиболее часто отмечались запор, диарея, тошнота и рвота. Эти побочные реакции купировались с помощью симптоматических средств: противорвотных — при тошноте и рвоте, противодиарейных — при диарее, и слабительных — при запоре.
Вайдаза — это цитотоксическое лекарственное средство, с которым, как и с другими токсическими веществами, следует обращаться с осторожностью. Любой неиспользованный или расходный материал должен быть утилизирован согласно местным требованиям.
При контакте восстановленного раствора азацитидина с кожей, немедленно тщательно промыть ее с мылом и водой. При контакте со слизистой оболочкой — тщательно промыть ее водой.
Влияние на способность к управлению транспортными средствами и механизмами
Исследования по изучению влияния на способность к управлению транспортными средствами и использованию механизмов не проводились. Учитывая возможность развития слабости на фоне лечения препаратом Вайдаза, пациенты должны проявлять особую осторожность при управлении автомобилем и работе с механизмами.
Передозировка
Симптомы: сообщалось об одном случае передозировки азацитидина в ходе клинического исследования. У больного отмечалась диарея, тошнота и рвота после однократного внутривенного введения препарата в дозе 290 мг/м2, которая превышает рекомендованную начальную дозу почти в 4 раза.
Лечение: рекомендуется мониторировать уровень соответствующих клеток крови и назначать, при необходимости, поддерживающее лечение. Не существует специфического антидота при передозировке азацитидина.
Лекарственное взаимодействие
Не проводилось целенаправленных клинических исследований взаимодействия азацитидина с другими лекарственными препаратами. Данные исследований in vitro свидетельствуют о том, что участие изоферментов системы цитохрома Р450, UDP-глюкуронилтрансферазы, сульфотрансферазы и глютатионтрансферазы в метаболизме азацитидина маловероятно. В связи с этим, взаимодействие in vivo с данными ферментами, участвующими в метаболизме, не представляется клинически значимым.
Условия хранения препарата Вайдаза
Препарат следует хранить в недоступном для детей месте при температуре не выше 30°С.
Срок годности препарата Вайдаза
Условия реализации
Препарат отпускается по рецепту.
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Нозологическая классификация болезней (МКБ-10)
Вайдаза — аналог пиримидинового нуклеозида цитидина, обладающий выраженными цитостатическими свойствами. Применяется в противоопухолевой терапии следующих категорий заболеваний:
- C92.0 — острый миелогенный (нелимфобластный) лейкоз;
- C92.1 — вялотекущий миелолейкоз;
- D46 — группы гетерогенных клональных патологий.
Лекарственный состав и форма производства
Противоопухолевое средство выпускается в виде пористой массы (лиофилизата) белого цвета, в состав которого входят:
- 5-азацитидин (азацитидин) — 100.0 мг;
- шестиатомный спирт (маннитол).
Рассыпчатый порошок расфасовывается в стеклянные пузырьки емкостью по 25 мл. В бело-зеленой упаковке содержится 1 пузырек вместе с инструкцией по применению лиофилизата.
Фармакотерапевтические свойства
Противоопухолевая активность лекарственного средства обусловлена сразу несколькими принципами действия азацитидина, в частности цитотоксичностью по отношению к мутированным гематопоэтическим клеткам. Компоненты лиофилизата ингибируют продукцию РНК и ДНК, а также инкорпорацию лекарства в упомянутые структуры.
Непролиферирующие (здоровые) клетки не чувствительны к воздействию производных цитидина. Их инкорпорация в ДНК раковых клеток сопровождается инактивацией катехол-О-метилтрансферазы, в связи с чем наблюдается гипометилирование ДНК. За счет этого создаются оптимальные условия для реэкспрессии генов и нормализации свойств угнетения опухолевого развития патологических клеток.
Фармакологическая результативность цитостатического препарата была неоднократно подтверждена результатами рандомизированного обследования. У пациентов с гетерогенными клональными заболеваниями эффективность лечения была выше, чем в случае использования традиционным методов противоопухолевой терапии.
Фармакокинетические свойства
При подкожном введении лекарство быстро проникает в общий кровоток и достигает максимальной сывороточной концентрации через 30-40 минут. Биодоступность действующих веществ варьируется в пределах от 85 до 89%. Согласно результатам исследований in vitro, Вайдаза расщепляется без участия изоэнзимов цитохрома P450.
Азацитидин метаболизируется в результате дезаминирования и спонтанного гидролиза. Большая часть продуктов распада лекарства выводятся вместе с мочой, а меньшая — вместе с желчью. Период их полувыведения равен 40-45 минутам при условии нормального функционирования органов детоксикации.
Показания к применению
Противоопухолевый медпрепарат применяется в терапии раковых заболеваний системы кроветворения. Показаниями к применению цитостатика считаются:
- миеломоноцитарный лейкоз;
- гетерогенные клональные заболевания;
- нелимфобластная лейкемия;
- хроническая лейкемия.
Часто Вайдаза назначается пациентам с миелодиспластическим синдромом. Лиофилизат используется только совершеннолетними пациентами при отсутствии возможности трансплантации в костный мозг гемопоэтических стволовых клеток.
Особенности применения
Перед использованием лиофилизат разбавляют с водой для инъекций. Для этого в пузырек с порошком добавляют 4 мл жидкости, после чего встряхивают до получения однородного раствора. Если в препарате присутствуют крупные частицы лиофилизата, использовать его нельзя. Суспензию необходимо готовить перед использованием, вводится она подкожно с использованием иглы 25-го калибра.
Правила введения раствора:
- противоопухолевое средство вводится под углом 90 градусов;
- в одну область нежелательно вводить более 4 мл раствора;
- Вайдаза используется после предварительного приема противорвотного средства;
- температура вводимой жидкости должна находиться в пределах 20-25 градусов Цельсия;
- области для последующих инъекций должны располагаться на расстоянии минимум 2.5-3 см друг от друга;
- препарат не вводится в участки тела с нарушенной целостностью кожи.
Суспензия пригодна к применению только в течение 40-45 минут после приготовления. При температуре до 8 градусов Цельсия препарат сохраняет свои фармакологические свойства на протяжении 450-480 минут.
Дозировочный режим
Вне зависимости от гематологических показателей, противоопухолевая терапия начинается с невысоких дозировок — не более 75 мг азацитидина на м2 поверхности кожи. Лечение проводят в течение недели, после чего делают перерыв на 21 день. Один курс терапии состоит минимум из 6-7 таких циклов. Лечение продолжают до тех пор, пока очевидна положительная динамика в выздоровлении пациента.
В процессе противораковой терапии необходимо контролировать работоспособность жизненно важных органов и систем. Лекарство может вызывать побочные эффекты со стороны системы кроветворения, поэтому на протяжении всего курса необходимо проверять концентрацию тромбоцитов, нейтрофилов, лейкоцитов и других клеток крови.
Если уровень нейтрофилов и тромбоцитов резко уменьшается, это приводит к появлению у больных гематологической токсичности. В случае возникновения патологической симптоматики дозу противоопухолевого средства уменьшают.
Особые указания
Применение цитостатического средства проводится исключительно в стационарных условиях под наблюдением онколога. Каждый последующий цикл противораковой терапии начинают после оценки результатов анализа на содержание в сыворотке крови креатинина. Регулярный мониторинг показателей крови позволяет контролировать самочувствие пациентов и следить за динамикой развития болезни.
Осложнения со стороны кроветворной системы чаще возникают в первые два цикла терапии. При нарушении гематологических показателей у больных диагностируют нейтропению, тромбоцитопению, гипокалиемию и т.д. В случае изменения состава крови рекомендована отсрочка начала следующего цикла противоопухолевой терапии.
Препарат Вайдаза не используется в педиатрической практике из-за отсутствия сведений о безопасности парентерального введения азацитидина детям до 18 лет. В связи с повышенной сенсибилизацией детского организма, использование цитостатика может привести к анафилактоидным реакциям и механической асфиксии, возникающей на фоне отека слизистых респираторного тракта.
Патологии почек и печени являются основанием для снижения дозы противоопухолевого средства. Нерациональное использование цитостатика чревато повышением активности печеночных ферментов, некрозом паренхимы и снижением скорости клубочковой фильтрации. Нежелательно назначать лекарство пациентам с метастатическим поражением печеночной ткани, что связано с высокой вероятностью развития комы.
Пациентам после 65 лет дозировочный режим не корректируют при условии отсутствия нарушений в работе органов детоксикации. В связи с тем, что вероятность понижения функции почек у пожилых больных высокая, рекомендуется контролировать их функциональную активность в течение всего курса.
Гестация и лактация
В исследованиях на приматах азацитидин проявлял выраженную репродуктивную токсичность. В связи с риском развития внутриутробных патологий лиофилизат не назначается пациенткам в гестационный период.
Неизвестно, экскретируются ли компоненты цитостатика в грудное молоко, поэтому специалисты рекомендуют отказаться от грудного вскармливания во время проведения противораковой терапии.
Совместимость с алкоголем
Этанолсодержащие напитки усиливают токсичность противоракового средства, поэтому на время прохождения курса лечения необходимо отказаться от употребления алкоголя.
Взаимодействие с медикаментами
Целенаправленных лабораторных исследований взаимодействия цитостатика с другими медикаментами не проводилось. Сведения, полученные в испытания in vitro, указывают на то, что лекарство не метаболизируется под воздействием изоэнзимов цитохрома P450. Поэтому азацитидин можно сочетать с приемом индукторов или ингибиторов изоферментов.
Передозировка
Введение цитостатического препарата в дозировке от 290.0 мг на м2 поверхности тела чревато развитием передозировки. Ее проявлениями могут стать:
- тошнота;
- нарушение сознания;
- жидкий стул;
- отсутствие аппетита;
- рвотные позывы;
- головные боли;
- сонливость.
Следует учитывать, что многократное превышение рекомендованной дозы азацитидина увеличивает риск возникновения внутренних кровотечений. Основными проявлениями геморрагического синдрома являются быстрая утомляемость, снижение температуры тела, побледнение кожных покровов.
Лечение заключается в приеме адсорбирующих средств и внутривенном введении препаратов, уменьшающих концентрацию азацитидина в общем кровотоке. Во время терапии необходимо контролировать работу печени и почек.
Побочные эффекты
В 75% случаев во время прохождения противораковой фармакотерапии у пациентов возникают нежелательные гематологические реакции. Значительно реже диагностируются патологии со стороны сердечно-сосудистой, пищеварительной и нервной систем. К наиболее вероятным нежелательным эффектам от использования азацитидина относят:
- диарею;
- геморроидальные кровотечения;
- головокружение;
- недостаточность почек;
- боль в животе;
- лейкопению;
- тромбоцитопению;
- боль в мышцах и суставах;
- назофарингит;
- спутанность сознания;
- кожные высыпания;
- кровоточивость десен;
- лихорадочное состояние;
- гипокалиемию.
Цитостатическое средство действует угнетающе на иммунную систему, в связи с чем возникают иммунодефицитные состояния. Впоследствии это приводит к обострению хронических заболеваний и развитию септического воспаления в респираторном тракте.
Противопоказания
Вайдаза не используется для лечения детей и больных с гиперчувствительностью к производным цитидина. Противопоказаниями к использованию цитостатика являются:
- метастазы в печени;
- гестация и лактация;
- гипокалиемия;
- нарушенная свертываемость крови.
С осторожностью следует проходить противораковую терапию при кардиологических патологиях, воспалении легких, дисфункции почек и некротическом поражении паренхиматозной ткани.
Аналоги
Заменителями противоракового лекарства могут стать медикаменты из той же фармакологической группы, обладающие цитостатическими свойствами:
- Цитозар;
- Визфлур;
- Гемцитабин;
- Онкогем;
- Гематикс;
- Гемцитовер;
- Алимта;
- Флудара.
Некоторые вышеперечисленные средства обладают более обширным перечнем противопоказаний к назначению. Поэтому перед их использованием необходимо проконсультироваться с лечащим врачом-онкологом.
Условия продажи и хранения
Противоопухолевый препарат отпускается в аптеках только по письменному рецепту от врача. Лиофилизат хранится в сухом и недоступном для прямых лучей солнца месте при температуре 2-25 градусов Цельсия. Срок его годности в неразбавленном виде составляет 4 года. После его истечения использовать цитостатик не рекомендуется, что связано с высоким риском развития аллергических эффектов.
Цены на Вайдаза в Москве
Заберите заказ в в аптеке
WER (г. Москва)
Цена: от 12 200 руб.