Варилрикс — инструкция по применению
Синонимы, аналоги
Статьи
(Вакцина против ветряной оспы живая аттенуированная)
Регистрационный номер:
ЛСР-001354/08.
Торговое наименование:
Варилрикс® (Вакцина против ветряной оспы живая аттенуированная) / Varilrix®.
Группировочное наименование:
вакцина для профилактики ветряной оспы.
Лекарственная форма:
лиофилизат для приготовления раствора для подкожного введения.
Состав
1 прививочная доза (0,5 мл) содержит1,2:
|
Наименование компонентов |
Количество |
|
Действующее вещество |
|
|
Живой аттенуированный вирус Varicella Zoster (штамм Oka) |
≥ 103,3 БОЕ3,4 |
|
Вспомогательные вещества |
|
|
Лактоза |
32 мг |
|
Сорбитол |
6 мг |
|
Маннитол |
8 мг |
|
Аминокислоты |
8 мг |
|
Растворитель |
|
|
Вода для инъекций |
0,5 мл |
Примечания
1. Вакцина не содержит консервантов.
2. Вакцина содержит следовые количества неомицина сульфата (не более 25 мкг/дозу).
3. БОЕ — бляшкообразующие единицы.
4. Номинальный титр вируса соответствует минимальному титру, гарантируемому производителем на дату окончания срока годности. Содержание вируса в одной прививочной дозе на момент выпуска препарата должно отличаться и превышать минимальный титр, указанный в составе.
Описание
Aморфная масса или порошок от кремового до светло-желтого или светло-розового цвета; восстановленный препарат — жидкость от чистого желто-розового до розового цвета.
Растворитель: прозрачная бесцветная жидкость без видимых механических включений.
Характеристика
Варилрикс® (Вакцина против ветряной оспы живая аттенуированная) (далее — Варилрикс®) — живая аттенуированная вакцина для профилактики ветряной оспы, представляет собой живой аттенуированный вирус Varicella Zoster (штамм Oka), культивированный в культуре диплоидных клеток человека MRC-5. Варилрикс® отвечает всем требованиям Всемирной организации здравоохранения к производству медицинских иммунобиологических препаратов.
Фармако-терапевтичекая группа:
МИБП-вакцина.
Код АТХ:
J07BK01.
Иммунологические свойства
Иммунологическая и эпидемиологическая эффективность
Иммунологическую эффективность вакцины Варилрикс® в отношении профилактики ветряной оспы (случаи заболевания, подтвержденные результатами ПЦР или контактом с клинически подтвержденным случаем ветряной оспы) оценивали в масштабном международном клиническом исследовании с группой активного контроля, в котором дети в возрасте 12-22 месяцев получали одну дозу вакцины Варилрикс® или две дозы комбинированной вакцины для профилактики кори, паротита, краснухи и ветряной оспы.
Иммунологическая эффективность вакцинации вакциной Варилрикс® составила:
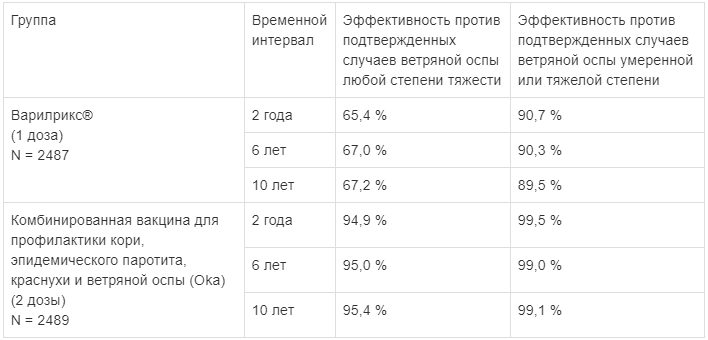
Данные по эпидемиологической эффективности свидетельствуют о повышении уровня защиты и снижении частоты эпизодов «прорыва» ветряной оспы после введения 2 доз вакцины по сравнению с введением 1 дозы.
Иммунный ответ
Здоровые лица
У детей в возрасте от 11 до 21 месяца включительно сероконверсия, измеренная методом иммуноферментного анализа (50 мМЕ/мл) через 6 недель после вакцинации, составила 89,6 % после введения 1 дозы и 100 % после введения 2 доз вакцины.
У всех детей в возрасте от 9 месяцев до 12 лет включительно сероконверсия, измеренная в реакции иммунофлуоресценции через 6 недель после введения 1 дозы, достигала 98 %.
У детей в возрасте от 9 месяцев до 6 лет сероконверсия, измеренная в реакции иммунофлуоресценции через 6 недель после введения второй дозы вакцины, составила 100 % (увеличение средней геометрической величины титра антител в 5-26 раз).
У детей в возрасте от 13 лет и старше сероконверсия, измеренная в реакции иммунофлуоресценции через 6 недель после введения второй дозы вакцины, составила 100 %. При контроле через 1 год после курса вакцинации все лица были серопозитивными.
В клинических исследованиях было показано, что большинство вакцинированных, находившихся впоследствии в контакте с заболевшими, либо не подвержены инфекции, либо переносят заболевание в значительно более легкой форме (меньшее количество высыпаний, отсутствие лихорадки).
Для оценки уровня защиты от развития осложнений ветряной оспы, таких как энцефалит, гепатит или пневмония, данных недостаточно.
Данные клинических исследований по применению вакцины Варилрикс® у пациентов из групп высокого риска развития ветряной оспы являются ограниченными. Установлено, что общая частота сероконверсии у пациентов данной категории составляет ≥ 80 %.
У пациентов из групп высокого риска после вакцинации следует периодически осуществлять определение титра антител к вирусу ветряной оспы для принятия решения о необходимости дополнительной прививки.
Показания к применению
— Плановая профилактика ветряной оспы с 12 месяцев, в первую очередь у лиц, отнесенных к группам высокого риска (см. раздел «Особые указания»), не болевших ветряной оспой и не привитых ранее.
— Экстренная профилактика ветряной оспы у лиц, не болевших ветряной оспой и не привитых ранее, находившихся в тесном контакте с больными ветряной оспой (члены семей, врачи, средний и младший медицинский персонал, а также другие лица).
Противопоказания
— Гиперчувствительность к какому-либо компоненту вакцины, в том числе к неомицину; симптомы гиперчувствительности на предыдущее введение вакцины для профилактики ветряной оспы.
— Тяжелый гуморальный или клеточный иммунодефициты, такие как: первичный или приобретенный иммунодефицит (развившийся вследствие лейкоза, лимфомы, дискразии крови, клинических проявлений ВИЧ-инфекции, применения иммунодепрессантов, включая высокодозную терапию кортикостероидами), определяемый по количеству лимфоцитов — менее 1200/мм3, а также при наличии других признаков клеточного иммунодефицита.
— Острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний являются временными противопоказаниями для проведения прививок; при нетяжелых ОРВИ, острых кишечных заболеваниях вакцинацию проводят сразу после нормализации температуры.
— Беременность или планируемая беременность в течение 1 месяца после вакцинации. Период кормления грудью.
Применение при беременности и в период грудного вскармливания
Фертильность
Данные отсутствуют.
Беременность
Беременных женщин нельзя вакцинировать препаратом Варилрикс®. Не следует допускать наступления беременности в течение 1 месяца после вакцинации. Женщинам, планирующим беременность, следует рекомендовать отложить наступление беременности.
Соответствующие данные о применении препарата Варилрикс® у человека во время беременности отсутствуют, а исследования репродуктивной токсичности на животных не проводились.
Период грудного вскармливания
Данные о применении у женщин в период грудного вскармливания отсутствуют.
Способ применения и дозы
Способ введения
Вакцина Варилрикс® предназначена для подкожного введения. Вакцину следует вводить в область дельтовидной мышцы или в переднебоковую область бедра.
Вакцину Варилрикс® нельзя вводить внутрисосудисто или внутрикожно.
Растворитель и восстановленную вакцину перед использованием необходимо визуально проверить на отсутствие механических включений и/или изменение внешнего вида (см. раздел «Описание»). В случае их обнаружения следует отказаться от применения растворителя или восстановленной вакцины.
Вакцину Варилрикс® нельзя смешивать в одном шприце с другими вакцинами.
Приготовление вакцины перед введением с использованием растворителя в шприце
Вакцину Варилрикс® необходимо восстановить путем добавления полного объема растворителя из предварительно наполненного шприца во флакон, содержащий лиофилизат.
Внимание! Упаковка вакцины Варилрикс® может быть представлена двумя типами шприцев, различающихся по способу соединения иглы с носиком шприца.
Для правильного выбора способа соединения иглы и шприца следуйте представленным ниже инструкциям. Шприц, вкладываемый в упаковку вакцины Варилрикс®, может незначительно отличаться от изображения шприца на рисунке 1.
Шприц 1 типа
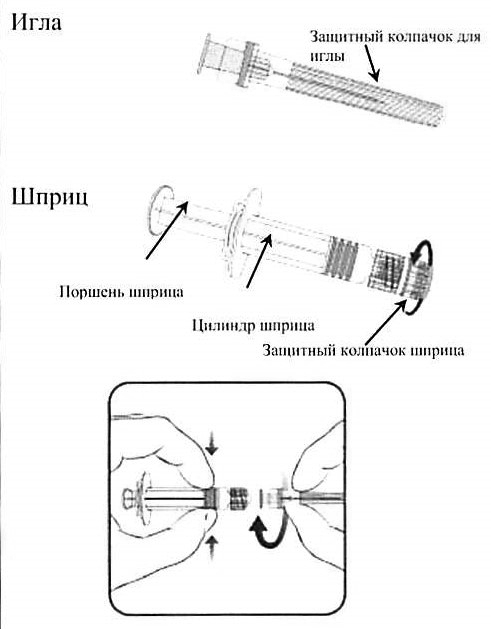
Рисунок 1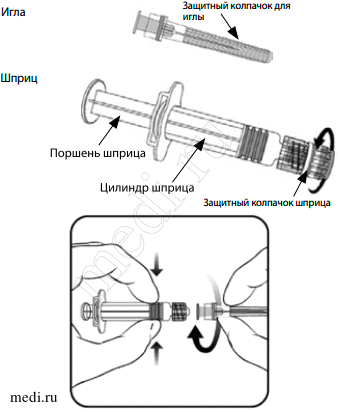
Инструкция по подготовке шприца 1 типа (рисунок 1) к использованию:
1. Открутите защитный колпачок шприца, поворачивая его против часовой стрелки (при этом следует удерживать шприц за цилиндр, избегая контакта с поршнем шприца).
2. Крутящим движением по часовой стрелке соедините иглу со шприцем до момента, когда вы ощутите их защелкивание друг на друге.
3. Удалите защитный колпачок с иглы (в отдельных случаях он может быть туго закреплен на игле).
Шприц 2 типа
В случае, если упаковка содержит шприц, отличный от представленного на рисунке 1, то после удаления защитного колпачка с носика шприца игла надевается на шприц до упора без дополнительного накручивания.
Перенести растворитель из шприца во флакон с лиофилизатом. После добавления растворителя к лиофилизату хорошо встряхнуть образовавшуюся суспензию до полного растворения лиофилизата в растворителе (приблизительно 3 минуты). После восстановления вакцину необходимо незамедлительно ввести. Для введения вакцины следует использовать новую иглу. Для введения извлекают из флакона с восстановленной вакциной все его содержимое.
Приготовление вакцины перед введением с использованием растворителя в ампуле
Варилрикс® необходимо восстановить путем добавления полного объема растворителя из ампулы во флакон, содержащий лиофилизат.
После добавления растворителя к лиофилизату хорошо встряхнуть образовавшуюся суспензию до полного растворения лиофилизата в растворителе (приблизительно 3 минуты). После восстановления вакцину необходимо незамедлительно ввести. Для введения вакцины следует использовать новую иглу. Для введения извлекают из флакона с восстановленной вакциной все его содержимое.
После обработки места проведения инъекции спиртом или другим веществом, применяющимся для дезинфекции, следует подождать, пока это вещество испарится, поскольку при контакте с подобными соединениями может произойти инактивация вакцинного вируса.
Вакцину следует вводить сразу после ее разведения растворителем.
Неиспользованный препарат и отходы от его использования должны быть уничтожены в соответствии с требованиями, принятыми в Российской Федерации.
Схемы вакцинации
Плановая профилактика
По 1 дозе вакцины (0,5 мл) двукратно.
Рекомендованный минимальный интервал между прививками должен составлять 6 недель.
Экстренная профилактика
Вакцинацию проводят однократно 1 дозой вакцины (0,5 мл) в течение первых 96 часов после контакта (предпочтительно в течение первых 72 часов).
Вакцинация групп высокого риска
Пациенты с острым лейкозом, пациенты с тяжелыми хроническими заболеваниями и пациенты, получающие терапию иммунодепрессантами и лучевую терапию
Иммунизация проводится в состоянии полной гематологической ремиссии. При этом необходимо удостовериться, что общее количество лимфоцитов составляет не менее 1200/мм3, а также отсутствуют симптомы, указывающие на недостаточность клеточного иммунитета.
Если вакцинацию планируется провести в острой фазе лейкоза, необходимо прервать химиотерапию на срок, равный одной неделе до и одной неделе после вакцинации. Не следует проводить вакцинацию в периоды лучевой терапии.
Пациенты, которым планируется произвести трансплантацию органа
Если пациентам предстоит трансплантация органа, то курс вакцинации должен быть завершен за несколько недель до начала проведения терапии иммунодепрессантами.
Пациентам групп высокого риска могут потребоваться дополнительные дозы вакцины. Решение о необходимости введения дополнительных доз вакцины Варилрикс® принимает лечащий врач (иммуногематолог, онколог, трансплантолог).
Взаимозаменяемость вакцин
Вакцина Варилрикс® может быть введена тем, кто уже был вакцинирован другой вакциной, содержащей компонент для профилактики ветряной оспы. Курс вакцинации против ветряной оспы, начатый вакциной Варилрикс®, может быть продолжен другой вакциной, содержащей компонент для профилактики ветряной оспы.
Побочное действие
Данные клинических исследований
Здоровые лица
Профиль безопасности вакцины, приведенный ниже, основан на данных, полученных для 5 369 доз вакцины, вводившейся детям, подросткам и взрослым.
Нежелательные реакции, представленные ниже, перечислены в соответствии с поражением органов и систем органов и частотой встречаемости. Частота встречаемости определяется следующим образом: очень часто (≥ 1/10), часто (≥ 1/100 и < 1/10), нечасто (≥ 1/1 000 и < 1/100), редко (≥ 1/10 000 и < 1/1 000), очень редко (< 1/10 000, включая отдельные случаи).
Частота встречаемости нежелательных реакций
Инфекционные и паразитарные заболевания
Нечасто: инфекции верхних дыхательных путей, фарингит.
Нарушения со стороны крови и лимфатической системы
Нечасто: лимфаденопатия.
Нарушения психики
Нечасто: раздражительность.
Нарушения со стороны нервной системы
Нечасто: головная боль, сонливость.
Нарушения со стороны органа зрения
Редко: конъюнктивит.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения
Нечасто: кашель, ринит.
Нарушения со стороны желудочно-кишечного тракта
Нечасто: тошнота, рвота.
Редко: боли в абдоминальной области, диарея.
Нарушения со стороны кожи и подкожных тканей
Часто: сыпь.
Нечасто: сыпь, сходная с высыпаниями при ветряной оспе, прурит.
Редко: крапивница.
Нарушения со стороны скелетно-мышечной системы и соединительной ткани
Нечасто: артралгия, миалгия.
Общие расстройства и нарушения в месте введения
Очень часто: боль и покраснение в месте инъекции.
Часто: отек в месте инъекции, повышение температуры тела (ректальной ≥ 38 °C, в подмышечной впадине или ротовой полости ≥ 37,5 °C).
Отек в месте инъекции и повышение температуры тела встречались очень часто в исследованиях, проводимых у подростков и взрослых. Отек также очень часто встречается после введения второй дозы детям до 13 лет. Тенденция увеличения количества случаев боли, покраснения и отека в месте инъекции после введения второй дозы была сопоставима с количеством этих нежелательных реакций, наблюдавшихся после введения первой дозы.
Нечасто: повышение температуры тела (ректальной ≥ 39,5°C; в подмышечной впадине или ротовой полости > 39°C), слабость, недомогание.
Не выявлены различия между профилем реактогенности у изначально серопозитивных и серонегативных лиц.
Пациенты из групп высокого риска
Существуют только ограниченные данные клинических исследований среди пациентов повышенного риска осложненного течения ветряной оспы. Вакциноассоциированные реакции (в основном папуло-везикулезная сыпь и повышение температуры тела) имеют, как правило, легкое течение. Как и у здоровых лиц, покраснение, отек и боль в месте инъекции имеют легкую степень и являются преходящими.
Данные пострегистрационного наблюдения
В ходе пострегистрационного наблюдения дополнительно зарегистрированы следующие нежелательные реакции после вакцинации.
Инфекционные и паразитарные заболевания
Редко: инфекция, вызванная Herpes Zoster.
Нарушения со стороны крови и лимфатической системы
Редко: тромбоцитопения.
Нарушения со стороны иммунной системы
Редко: реакции гиперчувствительности, анафилактические реакции.
Нарушения со стороны нервной системы
Редко: энцефалит, острое нарушение мозгового кровообращения, церебеллит, симптомы, напоминающие церебеллит (включая преходящее нарушение походки и преходящую атаксию), судороги.
Нарушения со стороны сосудов
Редко: васкулит (включая пурпуру Шенлейна-Геноха и синдром Кавасаки).
Нарушения со стороны кожи и подкожных тканей
Редко: многоформная эритема.
При наблюдении за массовым применением вакцины зарегистрированы случаи анафилактоидных реакций.
Передозировка
Зарегистрированы отдельные сообщения о случайной передозировке вакцины. В некоторых из них сообщалось о развитии таких симптомов, как летаргия, судороги. В других случаях передозировка не привела к развитию нежелательных явлений.
Взаимодействие с другими лекарственными препаратами
При необходимости постановки туберкулиновой пробы она должна быть проведена до вакцинации, поскольку по имеющимся данным живые вирусные вакцины могут вызывать временное снижение чувствительности кожи к туберкулину. В связи с тем, что подобное снижение чувствительности может сохраняться до 6 недель, не следует осуществлять туберкулинодиагностику в течение указанного периода времени после вакцинации во избежание получения ложноотрицательных результатов.
Вакцинация препаратом Варилрикс® возможна не ранее чем через 3 месяца после введения иммуноглобулинов или после гемотрансфузии.
Следует избегать назначения салицилатов в течение 6 недель после вакцинации препаратом Варилрикс®, поскольку имелись сообщения о развитии синдрома Рея на фоне инфекции, вызванной естественным вирусом ветряной оспы.
Одновременное назначение с другими вакцинами
Вакцину Варилрикс® можно вводить одновременно с инактивированными вакцинами национального календаря профилактических прививок и календаря прививок по эпидемическим показаниям, за исключением антирабической вакцины.
Вакцину Варилрикс® можно назначать в один день с вакцинами для профилактики кори, краснухи и паротита.
При этом различные вакцины вводят в разные участки тела.
Здоровые лица
Варилрикс® может применяться одновременно с любыми другими вакцинами.
При применении с коревой вакциной, в случае если прививки не были сделаны в один день, рекомендуется соблюдать интервал 30 дней.
Пациенты из групп высокого риска
Вакцину Варилрикс® не следует назначать одновременно с другими живыми аттенуированными вакцинами, за исключением комбинированной вакцины против кори, краснухи и паротита. Однако если эти вакцины не были назначены одновременно, то интервал между их назначением для достижения максимального уровня антител должен составлять не менее 30 дней.
Особые указания
Как и при любой другой вакцинации, иммунный ответ может развиться не у всех вакцинированных.
Как и при применении других вакцин для профилактики ветряной оспы, отмечены случаи заболевания ветряной оспой у лиц, привитых вакциной Варилрикс®. Однако такие случаи ветряной оспы обычно протекают в легкой форме, с небольшим количеством элементов сыпи и менее выраженным повышением температуры тела, по сравнению со случаями ветряной оспы у невакцинированных лиц. Отмечены редкие случаи передачи вакцинного штамма вируса от вакцинированных лиц с сыпью к контактным серонегативным лицам. Нельзя исключать передачу вакцинного штамма вируса контактным серонегативным лицам от вакцинированных лиц при отсутствии у последних элементов сыпи.
При вакцинации в течение первых 72 часов после контакта с инфекцией, вызванной естественным вирусом ветряной оспы, защита от ветряной оспы может быть достигнута не полностью.
Вакцинированные лица, у которых выявляются высыпания в течение 3 недель после вакцинации, должны исключить любые контакты с беременными женщинами (особенно в течение первого триместра беременности) и с лицами с иммунодефицитными состояниями в течение 14 дней с момента появления последнего высыпания.
Как и при парентеральном введении любых других вакцин, наготове должно быть все необходимое для купирования возможной анафилактической реакции на вакцину Варилрикс®. Вакцинированный должен находиться под медицинским наблюдением в течение 30 минут после иммунизации.
После вакцинации или иногда перед ней возможен обморок (потеря сознания) как психологическая реакция на инъекцию. Перед вакцинацией важно удостовериться, что пациент не получит повреждений в случае обморока.
Следует принимать адекватные меры контрацепции в течение 1 месяца после введения вакцины Варилрикс®.
Данные о применении вакцины Варилрикс® у лиц с иммунодефицитными состояниями ограничены, поэтому вакцинацию следует проводить с осторожностью и только в том случае, когда, по мнению врача, польза превышает риск.
У лиц с иммунодефицитными состояниями, не имеющих противопоказаний к вакцинации (раздел «Противопоказания»), как и у иммунокомпетентных пациентов, может не выявиться иммунная защитная реакция, соответственно часть вакцинированных может заразиться ветряной оспой, несмотря на правильно проведенную вакцинацию. Лица с иммунодефицитными состояниями должны находиться под тщательным наблюдением для выявления признаков ветряной оспы.
Сообщается о единичных случаях диссеминации вируса ветряной оспы с вовлечением в процесс внутренних органов после вакцинации препаратом, содержащим штамм Oka, преимущественно у пациентов с иммунодефицитом.
При наличии первичного или приобретенного иммунодефицита вакцинацию проводят после определения количества лимфоцитов. У пациентов, которые получают массивную терапию иммунодепрессантами, после вакцинации могут развиться клинические признаки ветряной оспы.
Пациенты из групп высокого риска
Следующие группы лиц предрасположены к развитию тяжелой формы ветряной оспы:
— пациенты с острым лейкозом;
— пациенты, получающие терапию иммуносупрессантами, включая применение кортикостероидов по поводу злокачественных солидных опухолей или по поводу тяжелых хронических заболеваний (почечная недостаточность, аутоиммунные заболевания, коллагенозы, тяжелая бронхиальная астма);
— пациенты, которым планируется произвести операцию трансплантации;
— пациенты с тяжелыми хроническими заболеваниями, такими как метаболические и эндокринные расстройства, хронические заболевания легких и сердечно-сосудистой системы, муковисцидоз и нервно-мышечные нарушения.
Иммунизация лиц из групп высокого риска против ветряной оспы вакциной Варилрикс® позволяет снизить риск развития осложнений, вызываемых ветряной оспой.
С целью дополнительного снижения риска инфицирования пациентов из группы высокого риска рекомендуется также проводить вакцинацию лиц, находящихся в тесном контакте с заболевшими ветряной оспой или с пациентами из групп высокого риска. К данной категории относятся родители, братья и сестры пациентов из групп высокого риска, старший и средний медицинский персонал и другие лица, находившиеся в тесном контакте с лицами, заболевшими ветряной оспой.
Влияние на способность управлять транспортными средствами, механизмами
Не установлено.
Форма выпуска
Лиофилизат для приготовления раствора для подкожного введения.
Лиофилизат
По 1 дозе вакцины во флаконе из прозрачного стекла типа I (Евр.Ф.) вместимостью 3 мл, укупоренном пробкой из резины и алюминиевым колпачком под обкатку, снабженным защитной пластиковой крышечкой.
Растворитель
По 0,5 мл в ампуле прозрачного стекла типа I (Евр.Ф.) вместимостью 1 мл.
По 0,5 мл в шприце из прозрачного стекла типа I (Евр.Ф.) вместимостью 1,25 мл. Носик шприца герметично укупорен защитным резиновым колпачком или герметичной резиновой пробкой с защитным завинчивающимся пластиковым колпачком.
Комплектность
По 1 флакону с лиофилизатом, 1 ампуле с растворителем в блистере из поливинилхлорида, закрытом пленкой из полиэтилентерефталата. По 1 блистеру с инструкцией по применению в картонной пачке.
По 1 флакону с лиофилизатом, 1 шприцу с растворителем в блистере из поливинилхлорида, закрытом пленкой из полиэтилентерефталата. По 1 блистеру с инструкцией по применению в картонной пачке.
По 1 флакону с лиофилизатом, 1 шприцу с растворителем в комплекте с 1 иглой в отдельном пластиковом контейнере с канюлей, закрытой пластиковым колпачком, в блистере из поливинилхлорида, закрытом пленкой из полиэтилентерефталата. По 1 блистеру с инструкцией по применению в картонной пачке.
По 1 флакону с лиофилизатом, 1 шприцу с растворителем в комплекте с 2 иглами в отдельных пластиковых контейнерах с канюлями, закрытыми пластиковыми колпачками, в блистере из поливинилхлорида, закрытом пленкой из полиэтилентерефталата. По 1 блистеру с инструкцией по применению в картонной пачке.
По 100 флаконов с лиофилизатом с 1 или 10 инструкциями по применению в картонной коробке. По 25 ампул с растворителем в блистере из поливинилхлорида или полиэтилена, закрытом пленкой, или без пленки. По 4 блистера в картонной коробке.
Срок годности
Лиофилизат: 2 года.
Растворитель: 5 лет.
Срок годности комплекта указывается по наименьшему сроку годности одного из компонентов.
Не применять после истечения срока годности, указанного на упаковке.
Датой окончания срока годности является последний день месяца, указанного на упаковке.
Условия хранения
Лиофилизат
Хранить при температуре от 2 до 8°С. Хранить в защищенном от света месте.
Растворитель
Хранить при температуре от 2 до 25°С. Не замораживать.
Комплект (лиофилизат, растворитель, с иглами или без игл)
Хранить при температуре от 2 до 8°С. Не замораживать.
Хранить в защищенном от света месте.
Хранить в недоступном для детей месте.
Условия транспортирования
Лиофилизат
Транспортировать при температуре от 2 до 8°С.
Растворитель
Транспортировать при температуре от 2 до 25°С. Не замораживать.
Комплект (лиофилизат, растворитель, с иглами или без игл)
Транспортировать при температуре от 2 до 8°С. Не замораживать.
Условия отпуска
Упаковка, содержащая 1 флакон с лиофилизатом и 1 ампулу или шприц с растворителем, — отпускают по рецепту.
Упаковка, содержащая 100 флаконов с вакциной, упаковка, содержащая 100 ампул с растворителем, — для лечебнопрофилактических учреждений.
Производитель
Производитель готовой лекарственной формы
Лиофилизат
«ГлаксоСмитКляйн Байолоджикалз с.а.», Бельгия
«Корикса Корпорейшен», США
Растворитель
«Аспен Нотр Дам де Бондевиль», Франция
«Дельфарм Тур», Франция
«Каталент Бельгия с.а.», Бельгия
Фасовщик (первичная упаковка)
Лиофилизат
«ГлаксоСмитКляйн Байолоджикалз с.а.», Бельгия
«Корикса Корпорейшен», США
Растворитель
«Аспен Нотр Дам де Бондевиль», Франция
«Дельфарм Тур», Франция
«Каталент Бельгия с.а.», Бельгия
Упаковщик (вторичная (потребительская) упаковка)
«ГлаксоСмитКляйн Байолоджикалз с.а.», Бельгия
«Дельфарм Тур», Франция (для формы выпуска растворителя по 100 ампул)
ООО «СмитКляйн Бичем-Биомед», Россия
Выпускающий контроль качества
«ГлаксоСмитКляйн Байолоджикалз с.а.» / GlaxoSmithKline Biologicals s.a. Рю де л’Энститю, 89, 1330 Риксенсарт, Бельгия / Rue de l’Institut, 89, 1330 Rixensart, Belgium
ООО «СмитКляйн Бичем-Биомед»
Россия, Московская обл., Красногорский р-н, с. Петрово-Дальнее
Наименование и адрес держателя или владельца регистрационного удостоверения лекарственного препарата
АО «ГлаксоСмитКляйн Трейдинг», Россия
125167, г. Москва, Ленинградский проспект, д. 37А, корпус 4, этаж 3, помещение XV, комната 1
Рекламации на качество препарата и развитие поствакцинальных осложнений направлять в адрес:
Федеральной службы по надзору в сфере здравоохранения (Росздравнадзор)
109074, Россия, г. Москва, Славянская пл., 4, стр. 1
и
АО «ГлаксоСмитКляйн Трейдинг», Россия
125167, г. Москва, Ленинградский проспект, д. 37А, корпус 4,
этаж 3, помещение XV, комната 1
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
| Вакцина | Цена |
|---|---|
|
|
нет в наличии |
Вакцина «Варилрикс» защищает от инфекций:
Похожие вакцины (аналоги Варилрикс):
Варилрикс (GlaxoSmithKline Biologicals S.A., Бельгия) – это живая аттенуированная (ослабленная) вакцина, предназначенная для профилактики ветряной оспы.
В своем составе вакцина Варилрикс содержит живой аттенуированный вирус Varicella zoster (штамм Oka), полученный размножением в культуре диплоидных клеток человека MRC-5, со специфической активностью.
Показания к применению
- Плановая профилактика ветряной оспы с 9 месяцев у лиц, не болевших ветряной оспой и не привитых ранее, а также у лиц, отнесенных к группам высокого риска
- Плановая профилактика ветряной оспы у здорового окружения лиц, отнесенных к группам риска, не болевших ветряной оспой и не привитых ранее
- Экстренная профилактика ветряной оспы у лиц, не болевших ветряной оспой и не привитых ранее, находившихся в тесном контакте с больными ветряной оспой (члены семей, врачи, средний и младший медицинский персонал, а также другие лица) в первые 96 часов контакта
Режим дозирования
Разовая доза составляет 0.5 мл. Вакцина поставляется в двух компонентах: флакон с лиофилизированной вакциной (специально высушенной) и шприцем с растворителем. Данный шприц снабжен специальной иглой, минимизирующей болевые ощущения от инъекции. Применение подобного шприца исключает передозировку и его повторное использование.
Вакцина соответствует требованиям ВОЗ по производству биологических препаратов, требованиям к вакцинам против ветряной оспы.
Способ применения
В асептически упакованном блистере находится шприц с жидким растворителем и флакон с лиофилизатом ветряночной вакцины. Непосредственно перед введением сухая вакцина во флаконе растворяется жидким растворителем из шприца и вводится из того же шприца.
Вакцина Варилрикс предназначена для подкожного или внутримышечного введения. Вакцину следует вводить в область дельтовидной мышцы или в переднебоковую область бедра. Вакцину Варилрикс следует вводить подкожно пациентам с нарушениями свертываемости крови (например, тромбоцитопения или любое другое нарушение коагуляции). Вакцину нельзя вводить внутрисосудисто или внутрикожно!
Схема вакцинации
Плановая профилактика
По 1 дозе вакцины (0,5 мл) двукратно.
Для детей в возрасте от 9 до 12 месяцев вторая доза должна быть введена с минимальным интервалом 3 месяца после первой дозы.
Для детей в возрасте от 12 месяцев и старше, подростков и взрослых рекомендованный минимальный интервал между прививками должен составлять 6 недель.
Экстренная профилактика
Вакцинацию проводят однократно 1 дозой вакцины (0,5 мл) в течение первых 96 часов после контакта (предпочтительно в течение первых 72 часов).
Вакцинация групп высокого риска
Пациенты с острым лейкозом, пациенты с тяжелыми хроническими заболеваниями и пациенты, получающие терапию иммунодепрессантами и лучевую терапию
Иммунизация проводится в состоянии полной гематологической ремиссии. При этом необходимо удостовериться, что общее количество лимфоцитов составляет не менее 1200/мм³, а также отсутствуют симптомы, указывающие на недостаточность клеточного иммунитета.
Если вакцинацию планируется провести в острой фазе лейкоза, необходимо прервать химиотерапию на срок, равный одной неделе до и одной неделе после вакцинации. Не следует проводить вакцинацию в периоды лучевой терапии.
Пациенты, которым планируется произвести трансплантацию органа
Если пациентам предстоит трансплантация органа, то курс вакцинации должен быть завершен за несколько недель до начала проведения терапии иммунодепрессантами.
Пациентам групп высокого риска могут потребоваться дополнительные дозы вакцины. Решение о необходимости введения дополнительных доз вакцины Варилрикс принимает лечащий врач (иммуногематолог, онколог, трансплантолог).
Взаимозаменяемость вакцин
Вакцина Варилрикс может быть введена тем, кто уже был вакцинирован другой вакциной, содержащей компонент для профилактики ветряной оспы.
Курс вакцинации против ветряной оспы, начатый вакциной Варилрикс, может быть продолжен другой вакциной, содержащей компонент для профилактики ветряной оспы.
Иммунологические свойства
Клинические исследования показали высокую эффективность вакцины Варилрикс. Уровень сероконверсии (выработка иммунитета) у здоровых детей в возрасте от 9 месяцев до 12 лет включительно, определенный через 6 недель после вакцинации, превышал 98% и сохранялся, по крайней мере, в течение 7 лет после вакцинации.
Уровень сероконверсии, определяемый у детей в возрасте 13 лет, после двукратной вакцинации, составлял 100% и сохранялся в течение как минимум 1 года.
В клинических исследованиях было показано, что большинство вакцинированных, находившихся впоследствии в контакте с заболевшими, либо не подвержены инфекции, либо переносят заболевание в значительно более легкой форме (меньшее количество высыпаний, отсутствие лихорадки).
Для того чтобы уровень сероконверсии был как можно выше с конца 2012 года вакцина Варилрикс применяется с ревакцинацией у всех возрастов, что предотвращает возникновение так называемых «ветрянок прорыва» (вспышки ветряной оспы у привитых детей).
Вакцина против ветряной оспы не входит в Национальный календарь прививок, но входит в некоторые региональные календари, например Москвы.
Применение препарата Варилрикс совместно с другими вакцинами
Вакцину Варилрикс можно вводить одновременно со всеми препаратами из национального календаря профилактических прививок в один день, в разные участки тела, за исключением вакцины БЦЖ и антирабической вакцины (вакцинация против бешенства).
Применение вакцины Варилрикс совместно с другими прививками не влияет на их иммуногенность (способность выработки иммунитета). Переносимость вакцин не ухудшается, количество побочных реакций не возрастает.
Введение нескольких вакцин в один день не является избыточной нагрузкой на иммунитет.
Введение вакцины Варилрикс возможно не ранее, чем через 3 месяца после введения иммуноглобулинов или после гемотрансфузии.
Побочные реакции
Реакции на вакцину Варилрикс редки и чаше всего переносятся легко. Делятся на местные и общие.
Местные реакции: боль и покраснение в месте инъекции.
Общие реакции: повышение температуры тела до субфебрильных цифр, лимфоаденопатия, слабость, недомогание. Возможно появление сыпи сходной с ветряночной. Сыпь необильная, редко развивается до пузырьков.
Чаще всего подобные реакции специального лечения не требуют, проводится симптоматическая терапия.
В среднем реактогенность вакцины при введении второй дозы (ревакцинации) не превышает реактогенность первой дозы. Также не отмечалось различий в профиле безопасности вакцины у людей, имеющих иммунитет к ветряной оспе и у людей не имеющих такового.
Противопоказания к применению
- Первичный или приобретенный иммунодефицит (развившийся вследствие лейкоза, лимфомы, дискразии крови, клинических проявлений ВИЧ-инфекции, применения иммунодепрессантов, включая высокодозную терапию кортикостероидами), а также при наличии других признаков клеточного иммунодефицита
- Острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний являются временными противопоказаниями для проведения прививок, при нетяжелых ОРВИ, острых кишечных заболеваниях прививки проводят сразу после нормализации температуры
- Беременность или планируемая беременность в течение 3 месяцев
- Период лактации (грудного вскармливания)
- Повышенная чувствительность к какому-либо компоненту вакцины (в т.ч. к неомицину)
- Симптомы повышенной чувствительности на предыдущее введение вакцины Варилрикс
Применение препарата Варилрикс при беременности и кормлении грудью
Вакцина противопоказана к применению при беременности или планируемой беременности (в течение 3 месяцев) и в период грудного вскармливания.
Дополнительные сведения
Применение вакцины Варилрикс возможно только у здоровых детей, сдавших общий анализ крови и мочи перед вакцинацией, и не имеющих отклонений в них. Перед вакцинацией ребенка осматривает педиатр на предмет инфекционных заболеваний. Проведение иммунизации вакциной Варилрикс возможно у тех детей, которые не имеют противопоказаний со стороны нервной системы, это устанавливает невролог.
Вакцинация взрослых возможна только после осмотра врача на предмет наличия острых воспалительных заболеваний и обострения хронических.
Для экстренной профилактики вакцина может применяться только в первые 96 часов. Время отсчитывается не от момента установления диагноза больному, а от момента последнего контакта с больным ветряной оспой. Важно помнить, что больной ветряной оспой становится заразным в среднем за сутки до появления высыпаний.
Вакцина Варилрикс защищает только от ветряной оспы и не защищает от других заболеваний, сопровождающихся поражением кожи и от других заболеваний, вызванных вирусами семейства герпес.
Женщинам детородного возраста рекомендуется предохраняться от беременности в течение 1 месяца перед вакцинацией и 2 месяцев после вакцинации.
Узнать наличие вакцины Варилрикс и записаться на прививку можно по телефонам центра:
«Диавакс» на Таганке
+7 (495) 988-47-76
+7 (916) 550-53-03
«Диавакс» на ВДНХ
+7 (495) 616-29-59
+7 (915) 351-92-53
Если хотите пригласить определённого специалиста, оставьте заявку и мы вам перезвоним!
Возможен выезд врача на дом и на предприятия для вакцинации сотрудников. Стоимость выезда врача – договорная. Услуги по проведению вакцинации оплачиваются отдельно в соответствии с действующим прейскурантом.
25 апреля 2021 года
Составить индивидуальный график вакцинации или получить грамотную консультацию специалиста теперь можно не выходя из дома, потому что мы заботимся о Вас, снижая количество контактов и экономя Ваше время!
Онлайн-консультация по вопросам вакцинопрофилактики
Специалистом центра «Диавакс» будет составлен Индивидуальный график вакцинации, прописаны последовательность и сроки вакцинации с перечнем всех необходимых вакцин, исходя из Вашей конкретной ситуации.
Дистанционная консультация аллерголога-иммунолога
Получить исчерпывающую консультацию аллерголога-иммунолога теперь можно в онлайне! Врач поставит предварительный диагноз, определит план обследования, ответит на любые вопросы по уже назначенному лечению, в том числе по лечебному питанию при пищевой аллергии.
А еще мы отвечаем на интересующие вас вопросы в специальном разделе! Чаще всего это вопросы индивидуального характера в отношении вакцинации, иммунитета и тому подобного.
На вопросы отвечают:
- Специалисты в области иммунопрофилактики
- Сотрудники Кафедры инфекционных болезней у детей РНИМУ им. Н.И. Пирогова
Педиатр, Инфекционист
Стаж работы с 2005 года
Кандидат медицинских наук, Доцент кафедры инфекционных болезней у детей ПФ РНИМУ им. Н.И. Пирогова
м. ВДНХ
Педиатр, Инфекционист
Стаж работы с 2009 года
Кандидат медицинских наук, Доцент кафедры инфекционных болезней у детей ПФ РНИМУ им. Н.И. Пирогова
м. Таганская
Педиатр, Инфекционист
Стаж работы с 2013 года
Кандидат медицинских наук, Ассистент кафедры инфекционных болезней у детей ПФ РНИМУ им. Н.И. Пирогова
м. Таганская
Педиатр, Инфекционист, Неонатолог
Стаж работы с 2012 года
Кандидат медицинских наук
м. Таганская
Педиатр
Стаж работы с 2014 года
м. Таганская
Педиатр, Аллерголог-иммунолог, Врач функциональной диагностики
Стаж работы с 2013 года
м. ВДНХ
Педиатр
Стаж работы с 2020 года
м. ВДНХ
Педиатр
Стаж работы с 2008 года
м. ВДНХ
Педиатр, Неонатолог
Стаж работы с 1986 года
м. ВДНХ
Педиатр
Стаж работы с 2020 года
м. ВДНХ
Педиатр, Неонатолог
Стаж работы с 1987 года
м. ВДНХ
Педиатр
Стаж работы с 2021 года
м. Таганская
Форма выпуска, упаковка и состав
препарата Варилрикс®
Лиофилизат для приготовления раствора для п/к и в/м введения в виде аморфной массы или порошка от кремового до светло-желтого или светло-розового цвета; восстановленный препарат — жидкость от чистого желто-розового до розового цвета; растворитель — прозрачная бесцветная жидкость без видимых механических включений.
1 вакцина не содержит консервантов.
2 вакцина содержит следовые количества неомицина сульфата (не более 25 мкг/дозу).
3 БОЕ — бляшкообразующие единицы.
Вспомогательные вещества: лактоза — 32 мг, сорбитол — 6 мг, маннитол — 8 мг, аминокислоты — 8 мг.
Растворитель: вода д/и — 0.5 мл.
1 доза (0.5 мл) — флаконы из прозрачного стекла вместимостью 3 мл (1) в комплекте с растворителем (шприц 0.5 мл 1 шт.) — блистеры из поливинилхлорида (1) — пачки картонные.
1 доза (0.5 мл) — флаконы из прозрачного стекла вместимостью 3 мл (1) в комплекте с растворителем (шприц 0.5 мл 1 шт.) и 1 иглой× (1) — блистеры из поливинилхлорида (1) — пачки картонные.
1 доза (0.5 мл) — флаконы из прозрачного стекла вместимостью 3 мл (1) в комплекте с растворителем (шприц 0.5 мл 1 шт.) и 2 иглами×× (1) — блистеры из поливинилхлорида (1) — пачки картонные.
× в отдельном пластиковом контейнере с канюлей, закрытой пластиковым колпачком.
×× в отдельных пластиковых контейнерах с канюлями, закрытыми пластиковыми колпачками.
Фармакологическое действие
Вакцина против вируса Varicella zoster живая аттенуированная.
Если после проведения вакцинации у пациента обнаруживаются антитела, это расценивается как признак развившейся защиты против заболевания.
Показания активных веществ препарата
Варилрикс®
Профилактика ветряной оспы у перечисленных ниже категорий людей, при условии, что они не переболели ветряной оспой: здоровые дети, начиная с возраста 9 месяцев; пациенты группы высокого риска (в т.ч. при остром лейкозе, на фоне терапии иммунодепрессантами, пациенты, которым планируется произвести трансплантацию органа, при хронических заболеваниях); здоровые люди, проживающие в тесном контакте с заболевшими.
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Доза зависит от возраста.
Вводят п/к или в/м.
Вакцину вводят в область дельтовидной мышцы или в переднебоковую область бедра.
П/к вводят пациентам с нарушениями свертываемости крови (например, тромбоцитопения или любое другое нарушение коагуляции).
Не вводят внутрикожно.
Внутрисосудистое введение вакцины недопустимо.
Побочное действие
Возможно: незначительное повышение температуры тела (чаще наблюдалось в течение первых 6 недель после вакцинации; проходило быстро, применения жаропонижающих средств не требовалось), везикуло-папулезная сыпь (чаще возникала в течение первых 3 недель после вакцинации, наблюдалось не более 10 элементов; как правило возникает у пациентов с лейкозами и иммунодефицитом), головная боль, лихорадка, парестезии, утомляемость; возможны аллергические реакции (в т.ч. анафилактический шок, бронхоспазм).
Противопоказания к применению
Острое заболевание, сопровождающееся повышением температуры тела, лимфопения (менее 1200/мкл), а также наличие других симптомов клеточного иммунодефицита, беременность, повышенная чувствительность к неомицину при его системном применении, повышенная чувствительность к вакцине.
Применение при беременности и кормлении грудью
При беременности введение вакцины противопоказано.
Вакцинацию следует проводить за 3 месяца до предполагаемого срока наступления беременности.
Данные о безопасности применения вакцины в период лактации отсутствуют.
Женщинам детородного возраста следует избегать беременности в течение 3 месяцев после вакцинации.
Вакцинированные пациенты, у которых выявляются высыпания в течение 3 недель после вакцинации, должны исключить любые контакты с беременными женщинами (особенно в течение I триместра беременности).
Особые указания
В случае острого заболевания, сопровождающегося повышением температуры тела, вакцинацию следует отложить. Инфекция в легкой форме не является противопоказанием для вакцинации.
Вакцину следует вводить в условиях, позволяющих провести неотложную терапию в редких случаях развития анафилактических реакций на введение вакцины. По этой причине вакцинируемый должен быть под медицинским наблюдением в течение 30 минут после вакцинации.
После применения данной вакцины (как и других вакцин против инфекций, вызванных вирусом Varicella zoster) наблюдались случаи развития инфекции, течение которой было более легким и сопровождалось менее выраженной лихорадкой, меньшим количеством высыпаний, по сравнению с невакцинированными пациентами.
В исключительно редких случаях была зарегистрирована передача вируса вакцины. Поэтому вакцинированные лица должны избегать контактов с пациентами группы высокого риска (например, с пациентами с лейкозами или с пациентами, получающими лечение иммунодепрессантами), особенно если через 2-3 недели после иммунизации появилась кожная сыпь.
Вакцинацию следует проводить не менее чем через 3 месяца после терапии иммуноглобулинами или после переливания крови, поскольку вследствие пассивного приобретения антител к вирусу Varicella zoster применение вакцины может быть неэффективным.
Если вакцинация проводится в острой фазе лейкоза, необходимо прервать химиотерапию на срок, равный одной неделе до и одной неделе после вакцинации. Кроме того, как правило, не вакцинируются пациенты в период проведения им рентгенотерапии.
Иммунизация таких пациентов обычно проводится тогда, когда они находятся в состоянии полной гематологической ремиссии основного заболевания. При этом необходимо удостовериться, что общее количество лимфоцитов составляет не менее 1200/мкл, и что не выявляются симптомы, указывающие на недостаточность клеточного иммунитета.
Пациенты, получающие терапию иммунодепрессантами (включая применение кортикостероидов) по поводу злокачественных солидных опухолей или по поводу тяжелых хронических заболеваний (почечная недостаточность, аутоиммунные заболевания, коллагенозы, тяжелая бронхиальная астма), предрасположены к заболеванию ветряной оспой в тяжелой форме. Иммунизация таких пациентов обычно проводится в период полной гематологической ремиссии заболевания. При этом необходимо удостовериться, что общее количество лимфоцитов составляет не менее 1200/мкл, и что не выявляются симптомы, указывающие на недостаточность клеточного иммунитета.
Пациентам, которым планируется произвести трансплантацию органа, вакцинацию следует проводить за несколько недель до начала проведения терапии иммунодепрессантами.
Пациенты с хроническими заболеваниями, такими как метаболические и эндокринные расстройства, хронические заболевания легких и сердечно-сосудистой системы, муковисцидоз и нервно-мышечные нарушения, предрасположены к заболеванию ветряной оспой в тяжелой форме.
Пациентам группы высокого риска после вакцинации можно рекомендовать периодически определять уровни антител против ветряной оспы, для выявления случаев необходимости повторной вакцинации.
Чтобы заранее предупредить возможность развития инфекционного заболевания у лиц из группы высокого риска, рекомендуется вакцинировать также неиммунизированных лиц, которые проживают в тесном контакте с заболевшими ветряной оспой, или с пациентами группы высокого риска. В эту категорию входят родители, а также братья и сестры пациентов группы высокого риска, врачи, средний и младший медицинский персонал, а также другие лица, проживающие в тесном контакте с заболевшими.
Лекарственное взаимодействие
Следует избегать назначения салицилатов в течение 6 недель после вакцинации, т.к. сообщается о развитии синдрома Рейе после их применения при инфекции, вызванной вирусом Varicella zoster.
Не допускать смешивания вакцины с другими вакцинами в одном шприце.
Пациентам группы риска данную вакцину не следует вводить в одно и то же время с другими живыми аттенуированными вакцинами.
Между введением данной вакцины и противокоревой вакцины (или вакцинных препаратов, содержащих противокоревую вакцину) следует соблюдать интервал, по крайней мере, 1 месяц, т.к. считается, что противокоревая вакцина может вызывать кратковременное подавление клеточного иммунитета.
Varilrix®
Регистрационный номер
Торговое наименование
Варилрикс®
Международное непатентованное наименование
Лекарственная форма
лиофилизат для приготовления раствора для подкожного введения
Состав
1 прививочная доза (0,5 мл) содержит4:
|
Наименование компонентов |
Количество |
|
Действующее вещество |
|
|
Живой аттенуированный вирус Varicella Zoster (штамм Oka) |
≥ 103,3 БОЕ1,2 |
|
Вспомогательные вещества |
|
|
Сывороточный альбумин человека3 Лактоза Сорбитол Маннитол Аминокислоты Неомицина сульфат Растворитель Вода для инъекций |
1 мг 32 мг 6 мг 8 мг 8 мг менее 25 мкг 0,5 мл |
Примечание:
1. БОЕ — бляшкообразующие единицы.
2. Номинальный титр вируса. Соответствует минимальному титру, гарантируемому производителем на дату окончания срока годности. С целью компенсации снижения титра вируса в течение срока годности препарата в состав введен избыток: на момент выпуска препарата 1 прививочная доза содержит ≥ 103,7 БОЕ.
3. Выполняет функцию стабилизатора.
4. Вакцина не содержит консервантов.
Описание
Аморфная масса или порошок от кремово-жёлтого до светло-жёлтого цвета; восстановленный препарат — прозрачная жидкость от желто-розового до розового цвета.
Растворитель: прозрачная бесцветная жидкость без видимых механических включений.
Фармакотерапевтическая группа
Фармакологические свойства
Фармакодинамика
Варилрикс® — живая аттенуированная вакцина для профилактики ветряной оспы, представляет собой живой аттенуированный вирус Varicella Zoster (штамм Oka), культивированный в культуре диплоидных
клеток человека MRC-5. Варилрикс® отвечает всем требованиям Всемирной организации здравоохранения к производству медицинских иммунобиологических препаратов.
Механизм действия
Введение вакцины Варилрикс® вызывает выработку антител к вирусу ветряной оспы, обеспечивая специфическую защиту от этой инфекции. Определённая степень защиты может быть достигнута при иммунизации в течение до 72 часов после контакта с вирусом Varicella Zoster. Титр антител ≥1/4, установленный методом непрямой реакции иммунофлюоресценции (НРИФ), считается протективным.
Иммунологическая эффективность
Здоровые лица
Практически у всех здоровых детей в возрасте от 9 месяцев до 12 лет включительно через шесть недель после вакцинации определялся уровень защиты, который сохранялся, по крайней мере, в течение 7 лет после вакцинации. Введение даже 1 дозы вакцины эффективно предотвращает 81 % всех госпитализаций у детей, связанных с заболеванием, и 87 % амбулаторных визитов. Тем не менее, у детей, получивших 1 дозу вакцины Варилрикс®, в сроки, превышающие 42 дня после прививки, регистрировались отдельные случаи заболевания, вызванного диким штаммом Varicella Zoster. Введение 2-ой дозы эффективно предотвращает случаи заражения ветряной оспой.
Все дети в возрасте от 13 лет после двукратной вакцинации имели выраженный уровень защиты, который сохранялся как минимум один год (во время наблюдения в рамках клинического исследования). В клинических исследованиях было показано, что большинство вакцинированных, находившихся впоследствии в контакте с заболевшими, либо не подвержены инфекции, либо переносят заболевание в значительно более лёгкой форме (меньшее количество высыпаний, отсутствие лихорадки).
Пациенты из групп высокого риска
Ветряная оспа представляет собой важный фактор риска, ухудшающий течение и прогноз имеющегося тяжёлого заболевания в следующих группах пациентов:
- пациенты с острым лейкозом;
- пациенты, получающие терапию иммунодепрессантами, включая применение кортикостероидов;
- пациенты, которым планируется произвести операцию трансплантации;
- пациенты, страдающие тяжёлыми хроническими заболеваниями, такими как метаболические и эндокринные расстройства, хронические заболевания лёгких и сердечно-сосудистой системы, муковисцидоз и нервно-мышечные нарушения;
- здоровые люди, находящиеся в тесном контакте с заболевшими или группами высокого риска, не болевшие ветряной оспой и не привитые ранее.
Пациенты из вышеуказанных групп, получающие терапию иммунодепрессантами (включая применение кортикостероидов) по поводу злокачественных солидных опухолей или по поводу тяжёлых хронических заболеваний (почечная недостаточность, аутоиммунные заболевания, системные заболевания соединительной ткани, тяжёлая бронхиальная астма), предрасположены к заболеванию ветряной оспой в тяжёлой форме.
У пациентов из групп высокого риска следует периодически осуществлять определение титров антител к вирусу ветряной оспы для принятия решения о необходимости дополнительной прививки.
Показания
— Плановая профилактика ветряной оспы с 12 месяцев, в первую очередь у лиц, отнесенных к группам высокого риска, не болевших ветряной оспой и не привитых ранее.
— Экстренная профилактика ветряной оспы у лиц, не болевших ветряной оспой и не привитых ранее, находившихся в тесном контакте с больными ветряной оспой (члены семей, врачи, средний и младший медицинский персонал, а также другие лица).
Противопоказания
— Гиперчувствительность к какому-либо компоненту вакцины, в том числе к неомицину; симптомы гиперчувствительности на предыдущее введение вакцины для профилактики ветряной оспы.
— Тяжёлый гуморальный или клеточный иммунодефициты, такие как: первичный или приобретённый иммунодефицит (развившийся вследствие лейкоза, лимфомы, дискразии крови, клинических проявлений ВИЧ-инфекции, применения иммунодепрессантов, включая высокодозную терапию кортикостероидами), определяемый по количеству лимфоцитов — менее 1200/мм, а также при наличии других признаков клеточного иммунодефицита.
— Острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний являются временными противопоказаниями для проведения прививок; при нетяжёлых ОРВИ, острых кишечных заболеваниях вакцинацию проводят сразу после нормализации температуры.
Беременность или планируемая беременность в течение 1 месяца после вакцинации. Период кормления грудью.
Применение при беременности и в период грудного вскармливания
Фертильность
Данные отсутствуют.
Беременность
Беременных женщин нельзя вакцинировать препаратом Варилрикс®. Не следует допускать наступления беременности в течение 1 месяца после вакцинации. Женщинам, планирующим беременность, следует рекомендовать отложить наступление беременности.
Соответствующие данные о применении препарата Варилрикс® у человека во время беременности отсутствуют, а исследования репродуктивной токсичности на животных не проводились.
Способ применения и дозы
Способ введения
Препарат Варилрикс® предназначен для подкожного введения.
Варилрикс® нельзя вводить внутрисосудисто или внутрнкожно.
Предпочтительное место введения препарата Варилрикс® — дельтовидная область плеча. Растворитель и восстановленную вакцину перед использованием необходимо визуально проверить на отсутствие механических включений и/или изменение внешнего вида. В случае их обнаружения следует отказаться от применения растворителя или восстановленной вакцины. Восстановленный препарат представляет собой прозрачную жидкость от желто- розового до розового цвета, Восстановленный препарат не должен содержать осадок и видимые посторонние включения.
Варилрикс® нельзя смешивать в одном шприце с другими вакцинами.
Приготовление вакцины перед введением с использованием растворителя в шприце
Варилрикс® необходимо восстановить путём добавления полного объёма растворителя из предварительно наполненного шприца во флакон, содержащий лиофилизат.
Внимание! Упаковка препарата Варилрикс® может быть представлена двумя типами шприцев, различающихся по способу соединения иглы с носиком шприца.
Для правильного выбора способа соединения иглы и шприца, следуйте представленным ниже инструкциям.
Шприц 1 типа
Рисунок 1.
Инструкция по подготовке шприца 1 типа (рисунок 1) к использованию:
1. Открутите защитный колпачок шприца, поворачивая его против часовой стрелки (при этом следует удерживать шприц за цилиндр, избегая контакта с поршнем шприца).
2. Крутящим движением по часовой стрелке соедините иглу со шприцем до момента, когда вы ощутите их защелкивание друг на друге.
Удалите защитный колпачок с иглы (в отдельных случаях он может быть туго закреплен на игле).
Шприц 2 типа
В случае, если упаковка содержит шприц, отличный от представленного на рисунке 1, то после удаления защитного колпачка с носика шприца игла надевается на шприц до упора без дополнительного накручивания. Перенести растворитель из шприца во флакон с лиофилизатом. После добавления растворителя к лиофилизату хорошо встряхнуть образовавшуюся суспензию до полного растворения лиофилизата в растворителе (приблизительно 3 минуты). После восстановления вакцину необходимо незамедлительно ввести. Для введения вакцины следует использовать новую иглу. Для введения извлекают из флакона с восстановленной вакциной все его содержимое.
Приготовление вакцины перед введением с использованием растворителя в ампуле
Варилрикс® необходимо восстановить путём добавления полного объёма растворителя из ампулы во флакон, содержащий лиофилизат. После добавления растворителя к лиофилизату хорошо встряхнуть образовавшуюся суспензию до полного растворения лиофилизата в растворителе (приблизительно 3 минуты). После восстановления вакцину необходимо незамедлительно ввести. Для введения вакцины следует использовать новую иглу. Для введения извлекают из флакона с восстановленной вакциной все его содержимое.
После обработки места проведения инъекции спиртом или другим веществом, применяющимся для дезинфекции, следует подождать, пока это вещество испарится, поскольку мри контакте с подобными соединениями может произойти инактивация вакцинного вируса. Вакцину следует вводить сразу после её разведения растворителем. Неиспользованный препарат и отходы от его использования должны быть уничтожены в соответствии с требованиями, принятыми в РФ.
Схемы вакцинации
Плановая профилактика
По 1 дозе вакцины (0,5 мл) двукратно.
Рекомендованный минимальный интервал между прививками должен составлять 6 недель.
Экстренная профилактика
Вакцинацию проводят однократно 1 дозой вакцины (0,5 мл) в течение первых 96 часов после контакта (предпочтительно в течение первых 72 часов).
Вакцинация групп высокого риска
Пациенты с острым лейкозом, пациенты с тяжёлыми хроническими заболеваниями и пациенты, получающие терапию иммунодепрессантами и лучевую терапию
Иммунизация проводится в состоянии полной гематологической ремиссии. При этом необходимо удостовериться, что общее количество лимфоцитов составляет не менее 1200/мм3, а также отсутствуют симптомы, указывающие на недостаточность клеточного иммунитета.
Если вакцинацию планируется провести в острой фазе лейкоза, необходимо прервать химиотерапию на срок, равный одной неделе до и одной неделе после вакцинации. Не следует проводить вакцинацию в периоды лучевой терапии.
Пациенты, которым планируется произвести трансплантацию органа
Если пациентам предстоит трансплантация органа, то курс вакцинации должен быть завершен за несколько недель до начала проведения терапии иммунодепрессантами.
Пациентам групп высокого риска могут потребоваться дополнительные дозы вакцины. Решение о необходимости введения дополнительных доз препарата Варилрикс® принимает лечащим врач (иммуногематолог, онколог, трансплантолог).
Взаимозаменяемость вакцин
Варилрикс® может быть введен тем. кто уже был вакцинирован другой вакциной для профилактики ветряной оспы.
Курс вакцинации против ветряной оспы, начатый препаратом Варилрикс®, может быть продолжен другой вакциной для профилактики ветряной оспы.
Побочное действие
Данные клинических исследований
Здоровые лица
Профиль безопасности вакцины, приведенный ниже, основан на данных, полученных для 5 369 доз вакцины, вводившейся детям, подросткам и взрослым.
Нежелательные реакции, представленные ниже, перечислены в соответствии с поражением органов и систем органов и частотой встречаемости. Частота встречаемости определяется следующим образом: очень часто (≥ 1/10), часто (≥ 1/100 и < 1/10), нечасто (≥1/1 000 и < 1/100), редко (≥1/10 000 и <1/1000), очень редко (< 1/10 000, включая отдельные случаи).
Частота встречаемости нежелательных реакций
Инфекционные и паразитарные заболевания
Нечасто: инфекции верхних дыхательных путей, фарингит.
Нарушения со стороны крови и лимфатической системы
Нечасто: лимфаденопатия.
Нарушения психики
Нечасто: раздражительность.
Нарушения со стороны нервной системы
Нечасто: головная боль, сонливость.
Нарушения со стороны органа зрения
Редко: конъюнктивит.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения
Нечасто: кашель, ринит.
Нарушения со стороны желудочно-кишечного тракта
Нечасто: тошнота, рвота.
Редко: боли в абдоминальной области, диарея.
Нарушения со стороны кожи и подкожных тканей
Часто: любая экзантема, визуально не сходная с везикулезом, вызванным Varicella Zoster.
Нечасто: сыпь, сходная с высыпаниями при ветряной оспе, прурит.
Редко: крапивница.
Нарушения со стороны скелетно-мышечной системы и соединительной ткани
Нечасто: артралгия, миалгия.
Общие расстройства и нарушения в месте введения
Очень часто: боль и покраснение в месте инъекции.
Часто: отёк в месте инъекции, повышение температуры тела (ректальной ≥ 38 °C, в подмышечной впадине или ротовой полости: ≥ 37,5 °C).
Отек в месте инъекции и повышение температуры тела встречались очень часто в исследованиях, проводимых у подростков и взрослых. Отек также очень часто встречается после введения второй дозы детям до 13 лет. Тенденция увеличения случаев боли и отёка в месте инъекции после введения второй дозы была сопоставима с количеством этих нежелательных реакций, наблюдавшихся после введения первой дозы.
Нечасто: повышение температуры тела (ректальной ≥ 39,5 °C; в подмышечной впадине или ротовой полости: ≥ 39 °C), слабость, недомогание. Не было различий между профилем реактогенности у изначально серопозитивных и серонегативных лиц.
Пациенты из групп высокого риска
Существуют только ограниченные данные клинических исследований среди пациентов повышенного риска осложнённого течения ветряной оспы. Вакциноассоциированные реакции (в основном папуло-везикулезная сыпь и повышение температуры тела) имеют, как правило, лёгкое течение. Как н у здоровых лиц, покраснение, отёк и боль в месте инъекции имеют лёгкую степень и являются преходящими.
Данные пострегистрационного наблюдения
В ходе пострегистрационного наблюдения дополнительно зарегистрированы следующие нежелательные реакции после вакцинации.
Инфекционные и паразитарные заболевания
Редко: инфекция, вызванная Herpes Zoster.
Нарушения со стороны крови и лимфатической системы
Редко: тромбоцитопения.
Нарушения со стороны иммунной системы
Редко: реакции гиперчувствительности, анафилактические реакции.
Нарушения со стороны нервной системы
Редко: энцефалит, острое нарушение мозгового кровообращения, церебеллит, симптомы, напоминающие церебеллит (включая преходящее нарушение походки и преходящую атаксию), судороги.
Нарушения со стороны сосудов
Редко: васкулит (включая пурпуру Шонлейна-Геноха и синдром Кавасаки).
Нарушения со стороны кожи и подкожных тканей
Редко: многоформная эритема. При наблюдении за массовым применением вакцины зарегистрированы случаи анафилактоидных реакций.
Передозировка
Зарегистрированы отдельные сообщения о случайной передозировке вакцины. В некоторых из них сообщалось о развитии таких симптомов, как летаргия, судороги. В других случаях передозировка не привела к развитию нежелательных явлений.
Взаимодействие с другими лекарственными средствами
При необходимости постановки туберкулиновой пробы она должна быть проведена до вакцинации, поскольку по имеющимся данным живые вирусные вакцины могут вызывать временное снижение чувствительности кожи к туберкулину. В связи с тем, что подобное снижение чувствительности может сохраняться до 6 недель, не следует осуществлять туберкулинодиагностику в течение указанного периода времени после вакцинации во избежание получения ложноотрицательных результатов. Вакцинация препаратом Варилрикс® возможна не ранее чем через 3 месяца после введения иммуноглобулинов или после гемотрансфузии.
Следует избегать назначения салицилатов в течение 6 недель после вакцинации препаратом Варилрнкс®, поскольку имелись сообщения о развитии синдрома Рейя на фоне инфекции, вызванной естественным вирусом ветряной оспы.
Одновременное назначение с другими вакцинами
Варилрикс® может вводиться одновременно с инактивированными вакцинами национального календаря профилактических прививок РФ и календаря прививок по эпидемическим показаниям РФ. за исключением антирабической вакцины. Препарат Варилрикс® может быть назначен в один день с вакцинами для профилактики кори, краснухи и паротита. При этом различные вакцины вводятся в разные участки тела.
Здоровые лица
Варилрикс® может применяться одновременно с любыми другими вакцинами.
При применении с коревой вакциной, в случае если прививки не были сделаны в один день, рекомендуется интервал 30 дней.
Пациенты из групп высокого риска
Варилрикс® не следует назначать одновременно с другими живыми аттенуированными вакцинами, за исключением комбинированной вакцины против кори, краснухи и паротита. Однако если эти вакцины не были назначены одновременно, то интервал между их назначением для достижения максимального уровня антител должен составлять не менее 30 дней.
Особые указания
Как и при любой другой вакцинации, иммунный ответ может развиться не у всех вакцинированных.
Было показано, что, как и при введении других вакцин для профилактики ветряной оспы, у лип, привитых препаратом Варилрикс®, могут в дальнейшем наблюдаться случаи заболевания ветряной оспой. Однако такие случаи ветряной оспы обычно протекают в лёгкой форме, с небольшим количеством элементов сыпи и менее выраженным повышением температуры тела, но сравнению со случаями ветряной оспы у невакцинированных лиц. Было показано, что в ряде случаев может встречаться передача вакцинного штамма вируса от вакцинированных лиц с сыпью к контактным серонегативным лицам. Нельзя исключать передачу вакцинного штамма вируса контактным серонегативным лицам от вакцинированных лиц при отсутствии у последних элементов сыпи. При вакцинации в течение первых 72 часов после контакта с инфекцией, вызванной естественным вирусом ветряной оспы, защита от ветряной оспы может быть достигнута не полностью. Вакцинированные пациенты, у которых выявляются высыпания в течение 3 недель после вакцинации, должны исключить любые контакты с беременными женщинами (особенно в течение первого триместра беременности) и лицами с иммунодефицитными состояниями на период 14 дней с момента появления последнего высыпания. Как и при парентеральном введении любых других вакцин, наготове должно быть все необходимое для купирования возможной анафилактической реакции на Варилрикс®. Вакцинированный должен находиться под медицинским наблюдением в течение 30 минут после иммунизации. После вакцинации или иногда перед ней возможны обмороки или выраженная слабость как психологическая реакция на инъекцию. Перед вакцинацией важно удостовериться, что пациент не получит повреждений в случае обморока. Следует принимать адекватные меры контрацепции в течение трёх месяцев после вакцинации препаратом Варилрикс®. Данные о применении препарата Варилрикс® у лиц с иммунодефицитными состояниями ограничены, поэтому вакцинацию следует проводить с осторожностью и только в том случае, когда, по мнению врача, польза превышает риск.
У лиц с иммунодефицитными состояниями, не имеющих противопоказаний к вакцинации (раздел «Противопоказания»), как и у иммунокомпетентных пациентов, может не выявиться иммунная защитная реакция, соответственно часть вакцинированных может заразиться ветряной оспой несмотря на правильно проведенную вакцинацию. Лица с иммунодефицитными состояниями должны находиться под тщательным наблюдением для выявления признаков ветряной оспы. Сообщается о единичных случаях диссеминации вируса ветряной оспы с вовлечением в процесс внутренних органов после вакцинации препаратом, содержащим штамм Ока. преимущественно у пациентов с иммунодефицитом.
При наличии первичного или при обретенного иммунодефицита вакцинацию проводят после определения количества лимфоцитов. У пациентов, которые получают массивную терапию иммунодепрессантами, после вакцинации могут развиться клинические признаки ветряной оспы.
Влияние на способность управлять транспортными средствами, механизмами
Не установлено.
Форма выпуска
Лиофилизат для приготовления раствора для подкожного введения, 1 доза (0,5 мл).
Лиофилизат
По 1 дозе вакцины во флаконе из прозрачного стекла типа I (Евр. Ф.) вместимостью 3 мл, укупоренном пробкой из резины и алюминиевым колпачком под обкатку, снабжённым защитной пластиковой крышечкой.
Растворитель
По 0,5 мл в ампуле прозрачного стекла типа I (Евр. Ф.) вместимостью 1 мл. По 0,5 мл в шприце из прозрачного стекла типа I (Евр. Ф.) вместимостью 1,25 мл. Носик шприца герметично укупорен защитным резиновым колпачком или герметичной резиновой пробкой с защитным завинчивающимся пластиковым колпачком.
Комплектность
По 1 флакону с лиофилизатом, 1 ампуле с растворителем в блистере из поливинилхлорида, закрытом плёнкой из полиэтилентерефталата. По 1 блистеру с инструкцией по применению в картонной пачке.
По 1 флакону с лиофилизатом, 1 шприцу с растворителем в блистере из поливинилхлорида, закрытом плёнкой из полиэтилентерефталата. По 1 блистеру с инструкцией по применению в картонной пачке.
По 1 флакону с лиофилизатом, 1 шприцу с растворителем в комплекте с 1 иглой в отдельном пластиковом контейнере с канюлей, закрытой пластиковым колпачком, в блистере из поливинилхлорида, закрытом плёнкой из полиэтилентерефталата. По 1 блистеру с инструкцией по применению в картонной пачке.
По 1 флакону с лиофилизатом, 1 шприцу с растворителем в комплекте с 2 иглами в отдельных пластиковых контейнерах с канюлями, закрытыми пластиковыми колпачками, в блистере из поливинилхлорида, закрытом плёнкой из полиэтилентерефталата. По 1 блистеру с инструкцией по применению в картонной пачке.
По 100 флаконов с лиофилизатом с 1 или 10 инструкциями по применению в картонной коробке. По 25 ампул с растворителем в блистере из поливинилхлорида или полиэтилена, закрытом плёнкой или без плёнки. По 4 блистера в картонной коробке.
Хранение
Лиофилизат
Хранить при температуре от 2 до 8 °C. Хранить в защищённом от света месте.
Растворитель
Хранить при температуре от 2 до 25 °C. Не замораживать.
Комплект (лиофилизат, растворитель, с иглами или без игл)
Хранить при температуре от 2 до 8 °C. Не замораживать.
Хранить в защищённом от света месте. Хранить в недоступном для детей месте.
УСЛОВИЯ ТРАНСПОРТИРОВАНИЯ
Лиофилизат
Транспортировать при температуре от 2 до 8 °C.
Растворитель
Транспортировать при температуре от 2 до 25 °C. Не замораживать.
Комплект (лиофилизат, растворитель, с иглами или без игл)
Транспортировать при температуре от 2 до 8 °C. Не замораживать.
Срок годности
Лиофилизат: 2 года.
Растворитель: 5 лет.
Срок годности комплекта указывается по наименьшему сроку годности одного из компонентов.
Не применять после истечения срока годности, указанного на упаковке. Датой окончания срока годности является последний день месяца, указанного на упаковке.
Условия отпуска из аптек
Отпускают по рецепту.
Производитель

Товары из категории — Вакцины
Инструкция по применению
Цена в интернет-аптеке WER.RU: от 2 210
Форма выпуска, состав и упаковка
Варилрикс выпускается в форме лиофилизата против ветрянки. Согласно инструкции основным веществом является бактериальный varicella virus vaccine live. Согласно инструкции состав препарата дополнен:
• углевод группы дисахаридов, содержится в молоке и молочных продуктах;
• глюцит;
• альдит;
• простые растворимые в воде белки, умеренно растворимые в концентрированных растворах соли и свёртывающиеся при нагревании;
• органические соединения, в молекуле которых одновременно содержатся карбоксильные и аминные группы.
Таблетки имеют форму плоского цилиндра и специфический запах. Упаковка стандартная. Купить препарат Варилрикс можно в нашей интернет-аптеке. Наличие препарата уточняйте при заказе, а также компанию производителя и способ доставки. Отзывы Варилрикс характеризуются позитивными откликами на форумах. Не уступают по степени влияния препарату и аналоги Варилрикс. Средняя цена Варилрикс доступна большинству семей. Варилрикс в Москве отпускается без рецепта. Заказать Варилрикс можно в любой интернет-аптеке. Варилрикс выпускается в ампулах.
Фармакологическое действие
Живая вакцина против ветряной оспы, выявляет детектируемый гуморальный иммунный ответ антител IgG у высокой части людей и хорошо переносится. Вакцинированные пациенты также имеют клеточно-опосредованный иммунный ответ, состоящий из экспрессии специфической активации ветряной оспы как CD4 + T-хелпер, так и CD8 + T-лимфоцитов.
Значение гуморального иммунитета и клеточного иммунитета в обеспечении защиты от ветряной оспы неизвестно, но пациенты, которые не сероконвертируют после вакцинации, все же получают некоторую защиту от инфекции через клеточный иммунитет. Вакцинация, по-видимому, предотвращает тяжелые заболевания даже у пациентов, которые не сероконвертируют. Тяжесть прорывной ветряной оспы, по-видимому, не зависит от продолжительности времени после иммунизации, случаи, наблюдаемые через 8 лет после вакцинации против вируса ветряной оспы, все еще остаются умеренными. Послепродажный надзор за вакцинами позволяет предположить, что после вакцинации против вируса ветряной оспы может наблюдаться более низкая частота возникновения опоясывающего лишая, чем при естественной инфекции ветряной оспы, но для подтверждения этих результатов необходим более длительный эпидемиологический надзор.
Риск развития опоясывающего герпеса, по-видимому, связан со снижением специфического иммунитета против вируса ветряной оспы (VZV). Предполагается, что повышение VZV-специфического клеточного иммунитета является механизмом, с помощью которого вакцина против вируса ветряной оспы защищает организм от опоясывающего герпеса и его осложнений. В целом, у получателей вакцины было меньше случаев опоясывающего герпеса (5,4 случая на 1000 человеко-лет), чем у получателей плацебо (11,1 случая на 1000 человеко-лет). Число случаев на 1000 человеко-лет в возрастных группах 60–69, 70–79 и более 80 лет было довольно схожим (10,8–12,2). Напротив, вакцина обеспечивала большую защиту от развития опоясывающего герпеса у молодых и пожилых людей. Например, было 3,9 случая на 1000 человеко-лет в возрасте от 60 до 69 лет, 6,7 случая на 1000 человеко-лет среди людей в возрасте 70–79 лет и 9,9 случая на 1000 человеко-лет среди пациентов в возрасте не менее 80 лет. Хотя вакцина предотвращала большее число случаев опоясывающего герпеса у молодых людей, вероятность развития постгерпетической невралгии (PHN), определяемой как, по меньшей мере, 3 из 10 выраженности боли, возникающей или сохраняющейся, по меньшей мере, через 90 дней после появления сыпи, была ниже среди пожилых людей, у которых развился опоясывающий герпес. Например, 6,6% реципиентов вакцины с опоясывающим герпесом имели PHN, а 6,9% реципиентов плацебо имели случай от 60 до 69 лет. Соответствующие показатели для детей в возрасте 70–79 лет составляют 7,7% и 17,2%, а среди пациентов в возрасте не менее 80 лет 18,9% получателей вакцины и 25,5% получателей плацебо имели PHN. Средняя продолжительность клинически значимой боли составляла 20 дней у получателей вакцины и 22 дня у получателей плацебо с подтвержденными случаями опоясывающего герпеса. Кроме того, общий процент случаев опоясывающего герпеса с ПГН был ниже среди получателей вакцины (8,6%) по сравнению с получателями плацебо (12,5%).
Введение вакцины против вируса ветряной оспы: подкожно.
Варилрикс: разовая доза лекарства, назначаемая пациентам> = 13 лет, вызывала сероконверсию у 75% получателей вакцины через 4 недели. Вторая доза, введенная через 4 недели после первой, увеличила частоту сероконверсии до 99%. В другом исследовании взрослым и подросткам вводили 2 прививки с интервалом в 8 недель. Частота сероконверсии составила 94% через 6 недель после первой дозы и 99% через 6 недель после второй. Продолжительность защиты неизвестна, однако антитела IgG к ветряной оспе после вакцинации сохраняются на высоком уровне в течение по крайней мере 10 лет и усиливаются при воздействии естественной инфекции ветряной оспы.
По сравнению с плацебо, средние геометрические титры концентраций антител к вирусу ветряной оспы (измеренные через 6 недель после вакцинации) были в 1,7 раза (95% ДИ, 1,6-1,8) выше у получателей вакцины, возраст> = 60 лет и 2,3- кратность (95% ДИ, 2,2—2,4) выше у получателей вакцины в возрасте 50—59 лет. Конкретная концентрация антител, которая коррелирует с защитой от опоясывающего герпеса, не установлена. В клиническом исследовании защита от опоясывающего герпеса была продемонстрирована через 4 года наблюдения. Необходимость ревакцинации прививкой не была определена.
Показания
Варилрикс имеет применение для обеспечения иммунитета против вируса ветряной оспы. Противопоказан беременным и пациентам с иммуносупрессией.
Противопоказания
Варилрикс имеет ряд противопоказаний:
• индивидуальная непереносимость препарата;
• наследственные или приобретенные во внутриутробном периоде иммунодефицитные состояния;
• Т-клеточный дефицит;
• X-сцепленная инфантильная, врожденная агаммаглобулинемия;
• синдром приобретенного иммунного дефицита;
• вирус иммунодефицита человека;
• высокая дозировка подкласса стероидных гормонов, производимых исключительно корой надпочечников.
Способ применения и дозы
Первоначально 0,5 мл Варилрикс подкожно, затем через 4-8 недель вводят вторую дозу 0,5 мл подкожно. Консультативный комитет по практике иммунизации (ACIP) рекомендует вводить 2 дозы вакцины против ветряной оспы пациентам без признаков иммунитета к ветряной оспе. Для пациентов, которые ранее получали только 1 дозу, рекомендуется повторная вакцинация против ветряной оспы. Доказательства иммунитета к ветряной оспе включают в себя любое из следующего: документирование 2 доз Варилрикса против ветряной оспы с интервалом не менее 4 недель; США, родившиеся до 1980 года, но роды до 1980 года не должны рассматриваться как свидетельство иммунитета для работников здравоохранения, пациентов с ослабленным иммунитетом и беременных женщин. История ветряной оспы, основанная на диагнозе или проверке ветряной оспы медицинским работником (для пациента, сообщающего историю болезни или имеющего атипичный случай, легкий случай или оба, поставщики медицинских услуг должны искать либо эпидемиологическую связь с типичный случай ветряной оспы или лабораторное подтверждение, если оно было выполнено во время острого заболевания), история опоясывающего герпеса на основе диагноза поставщика медицинских услуг или лабораторные доказательства иммунитета или лабораторное подтверждение.
Побочные действия
Варилрикс имеет ряд побочных эффектов:
• судороги;
• асептический менингит;
• миелит;
• синдром Гийена-Барре;
• инсульт;
• анафилактоидные реакции;
• анафилактический шок;
• мультиформная эритема;
• ангионевротический отек;
• синдром Стивенса-Джонсона;
• апластическая анемия;
• пневмонит;
• лимфаденопатия;
• запор;
• отек;
• эритема;
• гематома;
• менингит;
• атаксия;
• тромбоцитопения;
• реакция в месте введения;
• лихорадка;
• головная боль;
• везикулярная сыпь;
• грипп;
• ринит;
• астения;
• инфекция;
• боль в животе;
• миалгия;
• артралгия;
• рвота;
• диарея;
• раздражительность;
• анорексия;
• кашель;
• тошнота;
• озноб;
• усталость;
• недомогание;
• бессонница;
• зуд;
• крапивница;
• фарингит;
• парестезии;
• сыпь;
• пурпура.
Передозировка
Варилрикс вводится специалистами, поэтому нет зарегистрированных случаев передозировки.
Лекарственное взаимодействие
Не вводите живые вакцины получателям винорелбина. Нет данных относительно риска вторичной передачи инфекции живыми вакцинами у пациентов, получающих винорелбин. Перед началом лечения винорелбином следует рассмотреть возможность завершения всех прививок, соответствующих возрасту, согласно действующим руководствам по иммунизации. Получатели винорелбина могут получать инактивированные вакцины, но иммунный ответ на вакцины или токсоиды может быть уменьшен.
Особые указания
Производитель рекомендует соблюдать осторожность при введении вакцины против вируса ветряной оспы, живите с кормящими женщинами.
Вакцина против вируса ветряной оспы противопоказана к применению во время беременности. Никаких адекватных и контролируемых исследований не проводилось, и неизвестно, может ли вакцина нанести вред плоду или повлиять на репродуктивную способность.
Сроки и условия хранения
Не замораживать Варилрикс.
Цены на Варилрикс в Москве
Заберите заказ в в аптеке
WER (г. Москва)
Цена: от 2 210 руб.