Вориконазол Сандоз лиофилизат — инструкция по применению
Синонимы, аналоги
Статьи
В настоящее время препарат не числится в Государственном реестре лекарственных средств или указанный регистрационный номер исключен из реестра.
Регистрационный номер:
ЛП-004708 — 150218
Торговое наименование:
Вориконазол Сандоз
Международное непатентованное наименование:
вориконазол
Лекарственная форма:
лиофилизат для приготовления концентрата для приготовления раствора для инфузий.
Состав
В 1 флаконе содержится:
Действующее вещество: вориконазол — 211,3 мг*;
Вспомогательное вещество: бетадекса сульфобутилат натрия — 3380,8 мг*.
* с учетом заложенного избытка 5,65 % в целях компенсации неизвлекаемого объема для гарантии заявленного количества вориконазола (200 мг) и бетадекса сульфобутилата натрия (3200 мг).
Описание
Лиофилизат: порошок от белого до почти белого цвета;
Восстановленный раствор: прозрачная бесцветная жидкость.
Фармакотерапевтическая группа:
противогрибковое средство.
Код ATX: J02AC03.
Фармакологические свойства
Фармакодинамика
Механизм действия
Вориконазол — противогрибковое средство широкого спектра действия из группы триазолов.
Механизм действия препарата связан с ингибированием грибкового цитохрома Р450, что является ключевым этапом биосинтеза эргостерола. Накопление 14?-метилстерола коррелирует с последующей потерей эргостерола в грибковых клеточных мембранах, что обуславливает противогрибковую активность вориконазола. Было установлено, что вориконазол более селективен в отношении изоферментов цитохрома Р450 грибков, чем в отношении различных ферментных систем цитохрома Р450 млекопитающих. Положительной связи между средними, максимальными и минимальными значениями концентрации вориконазола в плазме крови и эффективностью препарата в терапевтических исследованиях не выявлено, в профилактических исследованиях эта взаимосвязь не изучалась. Фармакодинамический и фармакокинетический анализ данных клинических исследований выявил положительную связь между концентрацией вориконазола в плазме крови и отклонением от нормы биохимических показателей функции печени, а также зрительными нарушениями.
In vitro вориконазол обладает широким спектром противогрибкового действия: активен в отношении Candida spp. (включая штаммы С. krusei, устойчивые к флуконазолу, и резистентные штаммы С. glabrata и С. albicans), а также проявляет фунгицидный эффект в отношении всех изученных штаммов Aspergillus spp. и патогенных грибов, ставших актуальными в последнее время, включая Scedosporium spp. или Fusarium spp., которые ограниченно чувствительны к другим существующим противогрибковым средствам. Клиническая эффективность (с частичным или полным ответом) вориконазола была продемонстрирована при инфекциях, вызванных Aspergillus spp., включая A. flavus, A. fumigatus, A. terreus, A. niger, A. nidulans, Candida spp., включая С. albicans, С. glabrata, С. krusei, С. parapsilosis и С. tropicalis, а также в отношении некоторых штаммов С. dubliniensis, С. inconspicua и С. guilliermondii, Scedosporium spp., включая S. apiospermum и S. prolificans, и Fusarium spp.
Другие грибковые инфекции, при которых применялся вориконазол (иногда с частичным или полным ответом), включали в себя отдельные случаи инфекций, вызванных Alternaria spp., Blastomyces dermatitidis, Blastoschizomyces capitatus, Cladosporium spp., Coccidioides immitis, Conidiobolus coronatus, Cryptococcus neoformans, Exserohilum rostratum, Exophiala spinifera, Fonsecaea pedrosoi, Madureila mycetomatis, Paecilomyces lilacinus, Penicillium spp., включая P. marneffei, Phialophora richardsiae, Scopulariopsis brevicaulis и Trichosporon spp., включая Т. beigelii.
Продемонстрирована активность вориконазола in vitro в отношении клинических штаммов Acremonium spp., Alternaria spp., Bipolaris spp., Cladophialophora spp., Histoplasma capsulatum. Рост большинства штаммов подавлялся при концентрациях вориконазола от 0,05 мкг/мл до 2 мкг/мл.
Выявлена также активность вориконазола in vitro в отношении Curvularia spp. и Sporothrix spp., однако клиническое значение данного эффекта неизвестно.
Фармакокинетика
Общая характеристика
Фармакокинетические параметры вориконазола характеризуются значительной межиндивидуальной вариабельностью, его фармакокинетика является нелинейной за счет насыщаемого метаболизма. При повышении дозы вориконазола наблюдается непропорциональное (более выраженное) увеличение площади под кривой «концентрация-время» (AUCt). Увеличение пероральной дозы с 200 мг 2 раза в сутки до 300 мг 2 раза в сутки приводит к увеличению AUCt в среднем в 2,5 раза. Действие вориконазола при приеме внутрь поддерживающей дозы 200 мг (или 100 мг для пациентов с массой тела менее 40 кг) соответствует действию вориконазола при применении внутривенно в дозе 3 мг/кг. При приеме внутрь поддерживающей дозы 300 мг (или 150 мг для пациентов с массой тела менее 40 кг) действие сопоставимо с внутривенным введением вориконазола в дозе 4 мг/кг. При внутривенном введении или приеме внутрь насыщающих доз вориконазола равновесная концентрация достигается в течение первых 24 ч. Если препарат назначается 2 раза в сутки в средних (но не в насыщающих) дозах, происходит кумуляция вориконазола, а равновесные концентрации достигаются к 6-му дню у большинства пациентов.
Всасывание
Вориконазол быстро и практически полностью всасывается после приема внутрь: максимальная концентрация в плазме крови (Сmах) достигается через 1-2 ч после приема. Биодоступность вориконазола при приеме внутрь составляет 96 %. При повторном приеме с пищей с большим содержанием жиров Сmах и AUCt снижаются на 34 % и 24 % соответственно. Всасывание вориконазола не зависит от рН желудочного сока.
Распределение
Средний объем распределения вориконазола в равновесном состоянии составляет около 4,6 л/кг, что указывает на активное распределение вориконазола в тканях. Связь с белками плазмы крови составляет 58 %. Вориконазол проникает через гематоэнцефалический барьер и определяется в спинномозговой жидкости.
Метаболизм
Согласно данным исследований in vitro вориконазол метаболизируется под действием изоферментов CYP2C19, CYP2C9, CYP3A4. Важную роль в метаболизме вориконазола играет изофермент CYP2C19, имеющий выраженный генетический полиморфизм, в связи с чем замедленный метаболизм вориконазола возможен у 15-20 % представителей азиатского происхождения и у 3-5 % представителей европеоидной и негроидной рас. Установлено, что у пациентов с замедленным метаболизмом вориконазола его AUCT в среднем в 4 раза больше. чем у гомозиготных пациентов с быстрым метаболизмом. У гетерозиготных пациентов с быстрым метаболизмом вориконазола его AUCT в среднем в 2 раза больше, чем у гомозиготных.
Основным метаболитом вориконазола является N-оксид, доля которого составляет около 72 % от общего количества циркулирующих в плазме крови метаболитов с радиоактивной меткой.
Этот метаболит обладает минимальной противогрибковой активностью и не влияет на клинический эффект вориконазола.
Выведение
Вориконазол выводится в виде метаболитов после биотрансформации в печени; в неизмененном виде почками выводится менее 2 % от введенной дозы препарата.
После внутривенного введения вориконазола в моче обнаруживается около 80 % введенной дозы препарата. Большая часть (>94 %) общей дозы вориконазола выводится в течение первых 96 ч после приема внутрь или внутривенного введения. Период полувыведения (T1/2) вориконазола зависит от дозы и составляет примерно 6 ч при приеме препарата внутрь в дозе 200 мг. В связи с нелинейностью фармакокинетики величина Т1/2 не позволяет предсказать кумуляцию или выведение вориконазола.
Особые группы пациентов
Пожилые пациенты
При многократном приеме вориконазола внутрь Сmах и AUCT у здоровых пожилых мужчин (>65 лет) на 61 % и 86 % соответственно выше, чем у здоровых молодых мужчин (18-45 лет).
Значимых различий Сmах и AUCt у здоровых пожилых женщин (>65 лет) и здоровых молодых женщин (18-45 лет) не выявлено.
Профиль безопасности вориконазола у молодых и пожилых пациентов не отличается. Коррекция дозы вориконазола в зависимости от возраста не требуется.
Дети
У детей отмечается большая межиндивидуальная вариабельность, чем у взрослых. Сравнение детской и взрослой популяций показало, что предполагаемая AUCT у детей после введения насыщающей дозы вориконазола 9 мг/кг была сопоставима с таковой у взрослых после введения насыщающей дозы 6 мг/кг. Предполагаемая общая концентрация у детей после введения поддерживающей дозы 4 мг/кг и 8 мг/кг два раза в сутки была также сопоставима с таковой у взрослых после введения поддерживающей дозы 3 мг/кг и 4 мг/кг два раза в сутки.
Концентрация вориконазола при внутривенном введении в дозе 8 мг/кг в два раза выше, чем при приеме внутрь в дозе 9 мг/кг. Биодоступность вориконазола при приеме внутрь у детей может ограничиваться нарушением всасывания и достаточно низкой массой тела, в этом случае может быть показано внутривенное введение.
Полученные данные свидетельствуют о более быстрой элиминации вориконазола у детей по сравнению с взрослыми в связи с большим соотношением массы печени и массы тела.
У большинства подростков концентрация вориконазола в плазме крови соответствует этому показателю у взрослых пациентов. Тем не менее, отмечались меньшие значения концентрации вориконазола в плазме крови у некоторых подростков с низкой массой тела по сравнению с взрослыми и были ближе к значениям того же показателя у детей. Основываясь на популяционном фармакокинетическом анализе, подростки в возрасте от 12 до 14 лет с массой тела менее 50 кг должны получать дозу вориконазола, рекомендованную для приема у детей.
Нарушение функции почек
Выраженность почечной недостаточности не влияет на связь препарата с белками плазмы крови. У пациентов с нарушением функции почек средней или тяжелой степени тяжести (концентрация креатинина в сыворотке крови >220 мкмоль/л или 2,5 мг/дл) наблюдается кумуляция вспомогательного вещества — бетадекса сульфобутилата натрия, входящего в состав препарата.
Нарушение функции печени
Нарушение функции печени не влияет на связь вориконазола с белками плазмы крови. Сведения о фармакокинетике вориконазола у пациентов с тяжелым циррозом печени (класс С по классификации Чайлд-Пью) отсутствуют.
Пол
При многократном приеме вориконазола внутрь Сmax и AUCT у здоровых молодых женщин были на 83 % и 113 % соответственно выше, чем у здоровых молодых мужчин (18-45 лет).
Значимых различий Сmax и AUCT у здоровых пожилых мужчин и здоровых пожилых женщин (>65 лет) выявлено не было. Равновесная концентрация вориконазола в плазме крови у женщин была на 100 % и 91 % выше, чем у мужчин после приема препарата в виде таблеток или суспензии соответственно. Коррекция дозы вориконазола в зависимости от пола не требуется. Концентрации в плазме крови у мужчин и женщин сопоставимы.
Показания к применению
Вориконазол показан для применения у взрослых и детей старше 2 лет по следующим показаниям:
- инвазивный аспергиллез;
- кандидемия у пациентов без нейтропении;
- лечение тяжелых инвазивных кандидозных инфекций (включая С. krusei);
- кандидоз пищевода;
- тяжелые грибковые инфекции, вызванные Scedosporium spp. и Fusarium spp.;
- другие тяжелые инвазивные грибковые инфекции при непереносимости или рефрактерности к другим лекарственным препаратам;
- профилактика «прорывных» грибковых инфекций у пациентов со сниженной функцией иммунной системы, лихорадкой и неитропениеи, из групп высокого риска (реципиенты трансплантации гемопоэтических стволовых клеток, пациенты с рецидивом лейкоза);
- профилактика инвазивных грибковых инфекций у пациентов (взрослые и дети старше 12 лет) из группы высокого риска, таких как реципиенты трансплантации гемопоэтических стволовых клеток.
Противопоказания
- гиперчувствительность к вориконазолу или вспомогательному веществу препарата;
- одновременное применение следующих препаратов (см. раздел «Взаимодействие с другими лекарственными средствами»):
- субстраты изофермента CYP3A4, которые могут приводить к удлинению интервала QT: терфенадин, астемизол, цизаприд, пимозид или хинидин;
- сиролимус;
- рифампицин;
- карбамазепин и длительно действующие барбитураты (фенобарбитал);
- эфавиренз в дозах 400 мг и выше один раз в сутки (с вориконазолом в стандартных дозах);
- ритонавир в высоких дозах (400 мг и выше два раза в сутки);
- алкалоиды спорыньи (эрготамин, дигидроэрготамин), являющиеся субстратами изофермента CYP3A4;
- зверобой продырявленный (индуктор изоферментов цитохрома Р450 и Р- гликопротеина);
- детский возраст до 2 лет.
С осторожностью
- повышенная чувствительность к другим препаратам — производным азолов;
- печеночная и/или почечная недостаточность тяжелой степени;
- проаритмические состояния: врожденное или приобретенное удлинение интервала QT, кардиомиопатия, в особенности с сердечной недостаточностью, синусовая брадикардия, наличие аритмии с клиническими проявлениями, одновременный прием препаратов, вызывающих удлинение интервала QT (см. раздел «Особые указания»);
- применение у пациентов с электролитными нарушениями, такими как гипокалиемия, гипомагниемия и гипокальциемия.
Применение при беременности и в период грудного вскармливания
Достаточной информации о применении вориконазола у беременных женщин нет. В исследованиях на животных установлено, что препарат оказывает токсическое действие на репродуктивную функцию. Возможный риск для человека неизвестен. Вориконазол не следует применять у беременных женщин за исключением тех случаев, когда ожидаемая польза для матери превышает возможный риск для плода.
Выведение вориконазола с грудным молоком не изучалось. Следует прекратить грудное вскармливание в случае необходимости применения препарата.
Женщины репродуктивного возраста при применении вориконазола должны использовать надежные методы контрацепции.
Способ применения и дозы
Препарат Вориконазол Сандоз® следует вводить внутривенно капельно. Препарат не предназначен для болюсного введения. Рекомендуемая скорость инфузии вориконазола составляет 3 мг/кг в час в течение 1-3 часов.
Нарушения электролитного баланса, например, гипокалиемию, гипомагниемию и гипокальциемию, следует контролировать и корректировать, при необходимости, до начала и во время лечения вориконазолом.
Взрослые пациенты
Терапию вориконазолом следует начинать с внутривенного введения рекомендуемой насыщающей дозы, чтобы уже в первый день добиться адекватной концентрации препарата в плазме крови. Внутривенное введение следует продолжать в течение как минимум 7 дней, после чего возможен переход на пероральный прием препарата, при условии, что пациент способен принимать лекарственные препараты внутрь. Учитывая, что биодоступность препарата при приеме внутрь достигает 96 % (см. раздел «Фармакокинетика»), при наличии клинических показаний возможен переход с внутривенного на пероральное применение препарата без коррекции дозы.
В таблице приведена подробная информация по режиму дозирования вориконазола.
|
Внутривенно |
Внутрь |
||
|
Пациенты с массой тела 40 кг и более |
Пациенты с массой тела менее 40 кг* |
||
|
Насыщающая доза — все показания (первые 24 ч) |
6 мг/кг каждые 12 ч |
400 мг каждые 12ч |
200 мг каждые 12 ч |
|
Поддерживающая доза (после первых 24 ч) |
|||
|
Профилактика инвазивных грибковых инфекций у пациентов (взрослых и детей старше 12 лет) группы высокого риска, таких как реципиенты трансплантации гемопоэтических стволовых клеток; Профилактика «прорывных» грибковых инфекций у пациентов с лихорадкой |
3-4 мг/кг каждые 12 ч |
200 мг каждые 12 ч |
100 м г каждые 12 ч |
|
Инвазивный аспергиллез; Инфекции, вызванные Scedosporium spp. и Fusahum spp.; Другие тяжелые инвазивные грибковые инфекции |
4 мг/кг каждые 12 ч |
200 мг каждые 12 ч |
100 мг каждые 12 ч |
|
Кандидемия у пациентов без проявлений нейтропении |
3-4 мг/кг каждые 12 ч |
200 мг каждые 12 ч |
100 мг каждые 12ч |
|
Кандидоз пищевода |
Не установлено |
200 мг каждые 12ч |
100 мг каждые 12 ч |
* относится к пациентам от 15 лет и старше
Подбор дозы для внутривенного введения
При недостаточной эффективности лечения поддерживающая доза вориконазола для внутривенного введения может быть увеличена до 4 мг/кг каждые 12 ч. Если пациент не переносит препарат в дозе 4 мг/кг, ее следует снизить до 3 мг/кг каждые 12 ч.
Длительность лечения
Длительность лечения должна быть как можно короче в зависимости от клинического эффекта и результатов микологического исследования. Длительность лечения не должна превышать 180 дней.
Профилактика грибковых инфекции у взрослых и детей
Профилактическое применение препарата следует начинать в день трансплантации и можно продолжать до 100 дней. Продлить профилактику до 180 дней после трансплантации можно только в случае продолжения иммуносупрессивной терапии или развития реакции «трансплантат против хозяина» (РТПХ). Безопасность и эффективность вориконазола при применении более 180 дней в клинических исследованиях надлежащим образом не изучались.
Режим дозирования с целью профилактики такой же, как и в случае лечения в соответствующих возрастных группах.
Нарушение функции почек
У пациентов с нарушением функции почек средней или тяжелой степени тяжести (клиренс креатинина <50 мл/мин) наблюдается кумуляция вспомогательного компонента препарата бетадекса сульфобутилата натрия. Таким пациентам вориконазол следует назначать только внутрь, за исключением тех случаев, когда предполагаемая польза внутривенного введения превышает потенциальный риск. В подобных ситуациях необходимо регулярно контролировать концентрацию креатинина в плазме крови и, в случае её повышения, следует обсудить возможность перехода на прием вориконазола внутрь.
Вориконазол выводится при проведении гемодиализа с клиренсом 121 мл/мин. 4-часовой сеанс гемодиализа не приводит к удалению значительной части дозы вориконазола и не требует ее коррекции. Бетадекса сульфобутилат натрия выводится в ходе гемодиализа с клиренсом 55 мл/мин.
Нарушение функции печени
При остром повреждении печени, проявляющемся повышением активности «печеночных» трансаминаз (аланинаминотрансферазы (АЛТ) и аспартатаминотрансферазы (ACT)), коррекция дозы не требуется, но рекомендуется продолжать контроль показателей функции печени. Пациентам с печеночной недостаточностью легкой или средней степени тяжести (классы А и В по классификации Чайлд-Пью) следует назначать стандартную насыщающую дозу препарата, а поддерживающую дозу снижать в 2 раза.
Отсутствуют достаточные клинические данные по безопасности применения вориконазола у пациентов с повышенными биохимическими показателями функции печени (АЛТ, ACT, щелочная фосфатаза, общий билирубин >5 верхних границ нормы).
Применение препарата у пациентов с тяжелой степенью нарушения функции печени (класс С по классификации Чайлд-Пью) не изучалось, таким пациентам вориконазол следует назначать только в тех случаях, когда ожидаемая польза превышает возможный риск, и под постоянным контролем с целью выявления признаков токсического действия препарата.
Пожшые пациенты
Коррекция дозы вориконазола у пожилых людей не требуется.
Применение у детей
Безопасность и эффективность вориконазола у детей младше 2 лет не установлены (см. раздел «.Противопоказания»). Дети в возрасте от 12 до 14 лет при массе тела >50 кг, а также дети старше 15 лет должны получать вориконазол в дозах, аналогичных применяемым у взрослых. Режим дозирования вориконазола у детей (в возрасте от 2 до 12 лет) и подростков в возрасте от 12 до 14 лет и массой тела менее 50 кг:
|
Внутривенно |
Внутрь |
|
|
Насыщающая доза (первые 24 ч) |
9 мг/кг каждые 12 ч |
Не рекомендуется |
|
Поддерживающая доза (после первых 24 ч) |
8 мг/кг 2 раза в сутки |
9 мг/кг 2 раза в сутки (максимальная доза 350 мг 2 раза в сутки) |
Терапию рекомендуется начинать с внутривенного введения препарата, а возможность перорального приема вориконазола следует рассматривать только после клинического улучшения с учетом возможности пациента принимать пероральные лекарственные препараты.
Необходимо учитывать, что воздействие препарата при внутривенном введении в дозе 8 мг/кг приблизительно в два раза выше, чем при применении внутрь в дозе 9 мг/кг.
Применение вориконазола у детей в возрасте от 2 до 12 лет с нарушениями функции печени или почек не изучалось.
Коррекция дозы у детей
При неадекватном клиническом ответе пациента доза препарата может быть увеличена с шагом 1 мг/кг (или 50 мг в случае, если изначально применялась пероральная доза 350 мг).
Если ребенок не переносит лечение, возможно снижение дозы вориконазола с шагом 1 мг/кг (или 50 мг в случае, если изначально применялась пероральная доза 350 мг).
Правила приготовления раствора
Вориконазол в лекарственной форме лиофилизат для приготовления концентрата для приготовления раствора для инфузий представляет собой стерильный порошок без консерванта, предназначенный для однократного применения. Лиофилизат восстанавливается при помощи введения во флакон 19 мл стерильной воды для инъекций или 19 мл 0,9% раствора натрия хлорида. В результате восстановления получается раствор объемом 20 мл с концентрацией вориконазола 10 мг/мл. Для восстановления рекомендуется использовать стандартный неавтоматический 20 мл шприц, чтобы удостовериться в объеме извлеченного раствора. Не следует использовать раствор, если растворитель не попадает во флакон под действием вакуума.
Флакон следует встряхнуть до полного растворения препарата. Допустимо использование только прозрачного раствора, в случае образования крупных частиц раствор следует утилизировать.
|
Масса тела (кг) |
Объем концентрата вориконазола (10 мг/мл), требуемый для: |
||||
|
Дозы 3 мг/кг (количество флаконов) |
Дозы 4 мг/кг (количество флаконов) |
Дозы 6 мг/кг (количество флаконов) |
Дозы 8 мг/кг (количество флаконов) |
Дозы 9 мг/кг (количество (флаконов) |
|
|
10 |
— |
4,0 мл (1) |
— |
8,0 мл (1) |
9,0 мл (1) |
|
15 |
— |
6,0 мл (1) |
— |
12,0 мл (1) |
13,5 мл (1) |
|
20 |
— |
8,0 мл (1) |
— |
16,0 мл (1) |
18,0 мл (1) |
|
25 |
— |
10,0 мл (1) |
— |
20,0 мл (1) |
22,5 мл (2) |
|
30 |
9,0 мл (1) |
12,0 мл (1) |
18,0 мл (1) |
24,0 мл (2) |
27.0 мл (2) |
|
35 |
10,5 мл (1) |
14,0 мл (1) |
21,0 мл (2) |
28,0 мл (2) |
31,5 мл (2) |
|
40 |
12,0 мл (1) |
16,0 мл (1) |
24,0 мл (2) |
32,0 мл (2) |
36,0 мл (2) |
|
45 |
13,5 мл (1) |
18,0 мл (1) |
27,0 мл (2) |
36.0 мл (2) |
40,5 мл (3) |
|
50 |
15,0 мл (1) |
20,0 мл (1) |
30,0 мл (2) |
40,0 мл (2) |
45,0 мл (3) |
|
55 |
16,5 мл (1) |
22,0 мл (2) |
33,0 мл (2) |
44,0 мл (3) |
49.5 мл (3) |
|
60 |
18,0 мл (1) |
24,0 мл (2) |
36,0 мл (2) |
48,0 мл (3) |
54.0 мл (3) |
|
65 |
19,5 мл (1) |
26,0 мл (2) |
39,0 мл (2) |
52,0 мл (3) |
58,5 мл (3) |
|
70 |
21,0 мл (2) |
28,0 мл (2) |
42,0 мл (3) |
— |
— |
|
75 |
22,5 мл (2) |
30,0 мл (2) |
45,0 мл (3) |
— |
— |
|
80 |
24,0 мл (2) |
32,0 мл (2) |
48,0 мл (3) |
— |
— |
|
85 |
25,5 мл (2) |
34,0 мл (2) |
51,0 мл (3) |
— |
— |
|
90 |
27,0 мл (2) |
36,0 мл (2) |
54.0 мл (3) |
— |
— |
|
95 |
28,5 мл (2) |
38,0 мл (2) |
57,0 мл (3) |
— |
— |
|
100 |
30,0 мл (2) |
40,0 мл (2) |
60,0 мл (3) |
— |
— |
Восстановленный раствор (концентрат) можно хранить в холодильнике не более 24 ч при температуре от 2 до 8 °С в том случае, если он был приготовлен в контролируемых асептических условиях. С микробиологической точки зрения препарат следует вводить немедленно.
Получившийся восстановленный раствор следует разбавить путем добавления к нему одного из нижеперечисленных растворов до конечной концентрации 0,5-5 мг/мл:
- 0.9 % раствор натрия хлорида для внутривенного введения;
- раствор Рингера лактата для внутривенного введения;
- 5 % раствор декстрозы и раствор Рингера лактата для внутривенного введения;
- 5 % раствор декстрозы и 0,45 % раствор натрия хлорида для внутривенного введения:
- 5 % раствор декстрозы для внутривенного введения;
- 5 % раствор декстрозы и 0,15 % раствор калия хлорида для внутривенного введения;
- 0,45 % раствор натрия хлорида для внутривенного введения;
- 5 % раствор декстрозы и 0,9 % раствор натрия хлорида для внутривенного введения.
Готовый к применению раствор (0,5-5 мг/мл) можно хранить не более 3 ч при температуре 20-30 °С. Совместимость вориконазола с растворами, помимо указанных выше, неизвестна.
Побочное действие
Данные о безопасности вориконазола у взрослых основаны на результатах лечения более 2000 человек (1655 принимали участие в клинических исследованиях) и применении для профилактики грибковых инфекций у 279 пациентов. Данная популяция была гетерогенной (пациенты со злокачественными новообразованиями крови, ВИЧ-инфицированные пациенты с кандидозом пищевода и рефрактерными грибковыми инфекциями, пациенты без нейтропении с кандидемией или аспергиллезом, а также здоровые добровольцы).
Ниже перечислены нежелательные реакции, которые наблюдались при применении препарата и, возможно, были связаны с лечением. Наиболее распространенными нежелательными реакциями являлись зрительные нарушения, лихорадка, сыпь, рвота, тошнота, диарея, головная боль, периферические отеки, изменение лабораторных показателей функции печени, дыхательные расстройства и боль в животе. Нежелательные реакции обычно были легко или умеренно выражены. Клинически значимой зависимости безопасности препарата от возраста, расы или пола не выявлено.
По данным Всемирной организации здравоохранения (ВОЗ) нежелательные эффекты классифицированы в соответствии с их частотой развития следующим образом: очень часто (>1/10), часто (от >1/100 до <1/10), нечасто (от >1/1000 до <1/100), редко (от >1/10000 до <1/1000), очень редко (<1/10000); частота неизвестна — по имеющимся данным установить частоту возникновения не представлялось возможным.
Инфекционные и паразитарные заболевания
часто: синусит; редко: псевдомембранозный колит.
Нарушения со стороны крови и лимфатической системы
часто: агранулоцитоз (в том числе нейтропения и фебрильная нейтропения), панцитопения, лейкопения, тромбоцитопения (включая иммунную тромбоцитопеническую пурпуру), анемия (в том числе макроцитарная, микроцитарная, нормоцитарная, мегалобластная, апластическая); нечасто: угнетение костномозгового кроветворения, лимфаденопатия, эозинофилия; редко: синдром диссеминированного внутрисосудистого свертывания.
Нарушения со стороны иммунной системы
часто: реакции гиперчувствительности; нечасто: анафилактоидные реакции.
Нарушения со стороны эндокринной системы
нечасто: недостаточность коры надпочечников, гипотиреоз; редко: гипертиреоз.
Нарушения со стороны обмена веществ и питания
очень часто: периферические отеки; часто: гипокалиемия, гипогликемия, гипонатриемия; нечасто: гиперхолестеринемия.
Психические нарушения
часто: депрессия, галлюцинации, тревожность, бессонница, ажитация.
Нарушения со стороны нервной системы
очень часто: головная боль; часто: головокружение, судороги, тремор, гипертонус (включая ригидность затылочных мышц, тетанию), парестезия, спутанность сознания, обморок, сонливость; нечасто: отек головного мозга, атаксия, дисгевзия, гипестезия, периферическая нейропатия, энцефалопатия (по гипоксически-ишемическому типу или метаболическая), экстрапирамидные симптомы (включая акатизию и паркинсонизм); редко: синдром Гийена-Барре, нистагм.
Нарушения со стороны органа зрения
очень часто: зрительные нарушения (см. подраздел «Описание отдельных нежелательных реакций»); часто: кровоизлияние в сетчатую оболочку глаза; нечасто: отек диска зрительного нерва, нарушения со стороны зрительного нерва (включая неврит зрительного нерва*), окулогирный криз, диплопия, склерит, блефарит; редко: атрофия зрительного нерва, помутнение роговицы.
Нарушения со стороны органа слуха и лабиринтные нарушения
редко: снижение остроты слуха (гипоакузия), шум в ушах.
Нарушения со стороны сердиа
часто: наджелудочковая аритмия, брадикардия, тахикардия; нечасто: фибрилляция желудочков, желудочковая экстрасистолия, наджелудочковая тахикардия, удлинение интервала QT, желудочковая тахикардия (включая желудочковую тахикардию по типу «пируэт»), полная атриовентрикулярная блокада, блокада ножки пучка Гиса, узловые аритмии.
Нарушения со стороны сосудов
часто: снижение артериального давления, флебит; редко: лимфангит, тромбофлебит.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения
очень часто: нарушения дыхания (включая одышку и одышку при физической нагрузке); часто: острый респираторный дистресс-синдром, отек легких, боль в грудной клетке.
Нарушения со стороны желудочно-кишечного тракта
очень часто: тошнота, рвота, диарея, боль в животе; часто: диспепсия, запор, гингивит; нечасто: гастроэнтерит, панкреатит, перитонит, дуоденит, глоссит, отек языка.
Нарушения со стороны печени и желчевыводящих путей
очень часто: изменение лабораторных показателей функции печени (ACT, АЛТ, щелочная фосфатаза);
часто: желтуха (в т.ч. холестатическая), гепатит (включая лекарственно индуцированные поражения печени, токсический гепатит, печеночно-клеточную недостаточность и гепатотоксические реакции); нечасто: печеночная недостаточность, гепатомегалия, холецистит, холелитиаз; редко: печеночная энцефалопатия.
Нарушения со стороны колеи и подкожных тканей
очень часто: сыпь; часто: эксфолиативный дерматит, макулопапулезная сыпь, хейлит, кожный зуд, алопеция, эритема;
нечасто: макулезная сыпь, папулезная сыпь, фототоксические реакции, пурпура, синдром Стивенса-Джонсона (злокачественная экссудативная эритема), лекарственная фиксированная эритема, экзема, крапивница, аллергический дерматит;
редко: псориаз, ангионевротический отек, токсический эпидермальныи некролиз (синдром Лайелла), мультиформная эритема, псевдопорфирия, солнечный кератоз*;
частота неизвестна: веснушки*, лентиго*, кожная форма красной волчанки*, плоскоклеточный рак кожи*.
Нарушения со стороны скелетно-мышечной и соединительной ткани
часто: боль в спине; нечасто: артрит; частота неизвестна: периостит*.
Нарушения со стороны почек и мочевыводящих путей
часто: острая почечная недостаточность, гематурия, повышение концентрации креатинина в плазме крови;
нечасто: протеинурия, нефрит, некроз почечных канальцев, повышение концентрации мочевины в плазме крови.
Общие расстройства и нарушения в месте введения
очень часто: лихорадка;
часто: астения, озноб, отек лица (в том числе периорбитальный отек, отек губ);
нечасто: гриппоподобный синдром, реакция/воспаление в месте введения.
* Нежелательные реакции, отмеченные в постмаркетинговом периоде.
Описание отдельных нежелательных реакций
Нарушения зрения
В клинических исследованиях на фоне применения вориконазола очень часто отмечалось развитие нарушений зрения. На фоне долговременной или кратковременной терапии препаратом пациенты отмечали появление усиленного/измененного зрительного восприятия (гемералопия, радужные круги вокруг источника света, осциллопсия, мерцательная скотома, зрительная яркость, фотопсия), «пелену» перед глазами (помутнение стекловидного тела), изменения цветовосприятия (хлоропсия, цианопсия, ксантопсия, ахроматопсия), снижение остроты зрения, изменение полей зрения или светобоязнь. Эти нарушения были преходящими и полностью обратимыми, в большинстве случаев они разрешались самостоятельно в течение 60 минут; случаев развития клинически значимых длительных нарушений зрения зафиксировано не было. Было отмечено ослабление данного побочного эффекта на фоне повторяющихся введений вориконазола. В большинстве случаев нарушения зрения, возникавшие на фоне терапии препаратом, имели минимальную выраженность, необходимость в отмене препарата возникала редко, они не приводили к развитию стойких нарушений зрения. Развитие зрительных нарушений на фоне лечения может быть связано с повышением концентрации препарата в плазме крови или с использованием высоких доз вориконазола.
Механизм развития данного нежелательного явления неизвестен, наиболее вероятно, что источником его возникновения является сетчатка. В исследовании с участием здоровых добровольцев изучалось воздействие вориконазола на функцию сетчатки, в ходе его проведения было отмечено уменьшение амплитуды волн на электроретинограмме (ЭРГ). Изменения на ЭРГ не прогрессировали после 29 дня терапии и полностью исчезали после отмены вориконазола.
В постмаркетинговом периоде сообщалось о случаях пролонгированных нежелательных реакций со стороны органа зрения.
Кожные реакции
Среди пациентов, получавших вориконазол в рамках клинических исследований, очень часто отмечалось развитие нежелательных реакций со стороны кожи. Как правило, у таких пациентов имелись серьезные сопутствующие заболевания, по поводу которых им проводилось лечение несколькими другими препаратами. В большинстве случаев сыпь была легкой или средней степени тяжести. Развитие серьезных кожных реакций, включая синдром Стивенса-Джонсона, токсический эпидермальный некролиз и полиморфную эритему, отмечалось редко.
Если у пациентов появляется сыпь, их состояние следует тщательно контролировать, необходимо отменить вориконазол в случае, если отмечается усугубление тяжести симптомов со стороны кожных покровов. Были отмечены реакции фоточувствительности, такие как веснушки, лентиго, солнечный кератоз, особенно во время долгосрочного лечения. Были отмечены случаи плоскоклеточного рака кожи у пациентов, получавших вориконазол в течение длительного периода времени. Механизм развития неизвестен (см. раздел «Особые указания»).
Показатели функции печени
Общая частота развития повышения активности «печеночных» трансаминаз (более трех верхних границ нормы) в клинической программе изучения вориконазола составила 18,0% (319/1768) взрослых пациентов и 25,8 % (73/283) детей, проходивших лечение вориконазолом. Нарушение показателей функции печени может быть связано с более высокими концентрациями препарата в плазме крови и/или с применением более высоких доз. В большинстве случаев данные отклонения разрешались самостоятельно без необходимости в коррекции дозы во время лечения либо после корректировки дозы или отмены препарата. В некоторых случаях у пациентов с другими тяжелыми основными заболеваниями применение вориконазола было ассоциировано с развитием серьезной печеночной токсичности, включая случаи желтухи, редкие случаи гепатита и печеночной недостаточности, приводящей к летальному исходу (см. раздел «Особые указания»).
Инфузионные реакции
Во время внутривенной инфузии вориконазола здоровым пациентам возникали реакции анафилактоидного типа, включая приливы крови к коже лица, лихорадку, усиление потоотделения, тахикардию, чувство стеснения в груди, одышку, потерю сознания, тошноту, кожный зуд и сыпь. Указанные симптомы развивались непосредственно после начала инфузии (см. раздел «Особыеуказания»).
Профилактика грибковых инфекций
В открытом многоцентровом сравнительном исследовании, где вориконазол или итраконазол применяли для первичной профилактики грибковых инфекций у взрослых и подростков -реципиентов аллогенной трансплантации костного мозга без или с вероятной грибковой инфекцией, продолжительная отмена вориконазола на фоне развития нежелательных реакций отмечалась в 39,3 % по сравнению с 39,6 % пациентов, принимавших итраконазол. Связанные с лечением нежелательные реакции со стороны печени приводили к отмене препарата у 50 пациентов (21,4%), получавших лечение вориконазолом, и у 18 пациентов (7,1%), принимавших итраконазол.
Применение у детей
Безопасность вориконазола была изучена у 288 пациентов (169 в возрасте от 2 до <12 лет и 119 в возрасте от 12 до <18 лет), получавших вориконазол для лечения (105) или профилактики (183) инфекций в рамках клинических исследований и у 158 пациентов в возрасте от 2 до <12 лет в рамках программ расширенного доступа. Профиль нежелательных реакций при применении препарата у детей был схож с профилемем безопасности у взрослых. Данные пострегистрационных исследований позволяют предположить, что частота развития кожных реакций (особенно эритемы) среди пациентов детского возраста, может быть выше, чем среди взрослых. У 22 пациентов в возрасте младше 2 лет, получавших вориконазол в рамках программ расширенного доступа, было отмечено развитие следующих нежелательных реакций, для которых нельзя исключить связь с применением вориконазола: реакции фотосенсибилизации (1), аритмия (1), панкреатит (1), повышение концентрации билирубина в плазме крови (1), повышение активности «печеночных» трансаминаз (1), сыпь (1) и отек диска зрительного нерва (1). Были получены пострегистрационные данные о случаях развития панкреатита среди пациентов детского возраста.
Передозировка
В клинических исследованиях вориконазола было отмечено 3 случая развития случайной передозировки. Все случаи произошли у пациентов детского возраста, которые получили внутривенную дозу вориконазола, превышающую стандартную до 5 раз. Была отмечена единичная побочная реакция, проявившаяся в виде светобоязни, длившаяся 10 минут. Антидот для вориконазола неизвестен. В случае передозировки показана симптоматическая и поддерживающая терапия.
Вориконазол выводится при гемодиализе с клиренсом 121 мл/мин, бетадекса сульфобутилат натрия — с клиренсом 55 мл/мин. В случае передозировки гемодиализ может способствовать удалению вориконазола и бетадекса сульфобутилата натрия.
Взаимодействие с другими лекарственными препаратами
Вориконазол метаболизируется и ингибирует активность изоферментов Р450, включая CYP2C19, CYP2C9 и CYP3A4. Ингибиторы или индукторы этих изоферментов могут соответственно повышать или снижать концентрацию вориконазола в плазме крови. Также существует вероятность, что вориконазол может повышать плазменную концентрацию препаратов, метаболизирующихся при участии этих изоферментов.
Исследования по межлекарственному взаимодействию были проведены среди здоровых взрослых пациентов мужского пола, которым перорально назначался вориконазол в дозе 200 мг 2 раза в сутки до достижения равновесной концентрации препарата в плазме крови. Данные результаты подходят и для оценки вероятности взаимодействия при использовании в других популяциях и других способов введения препарата.
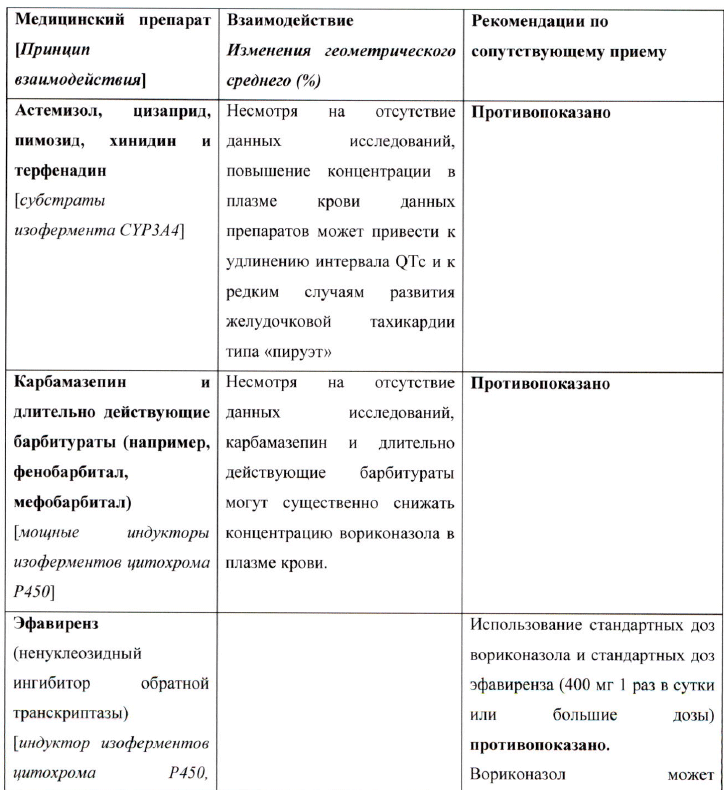
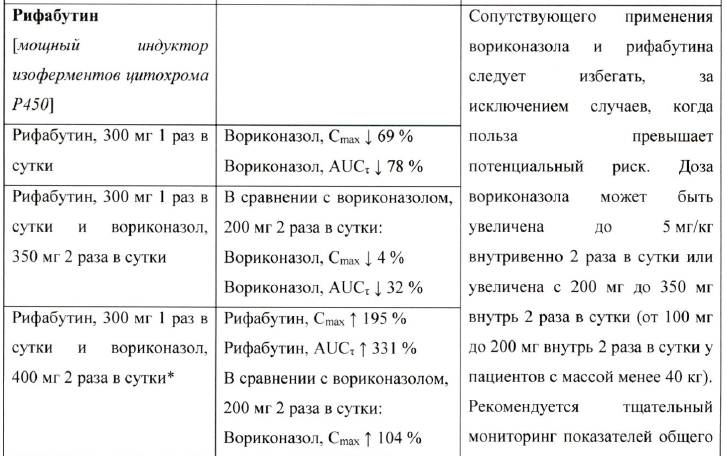
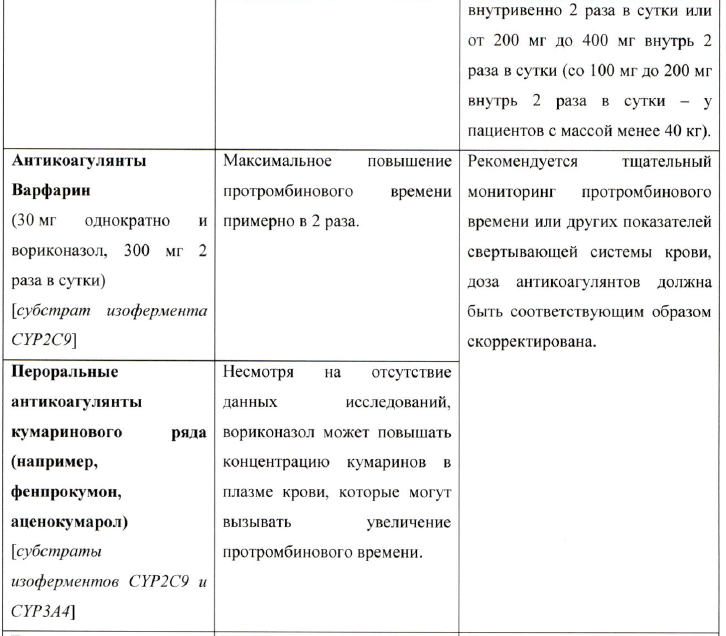
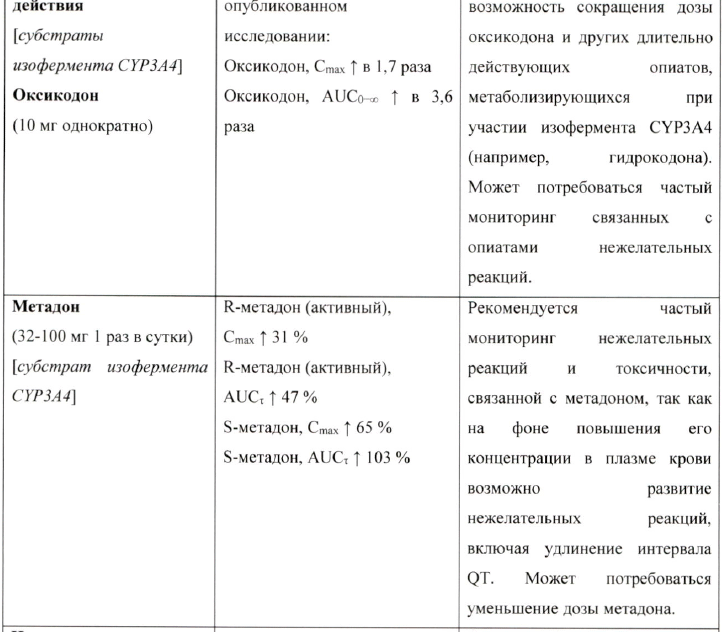
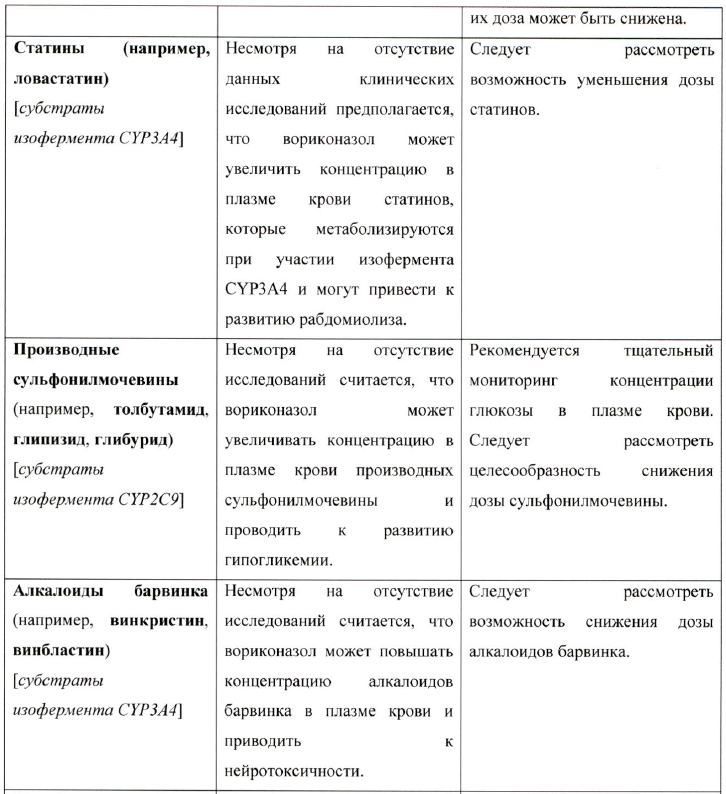
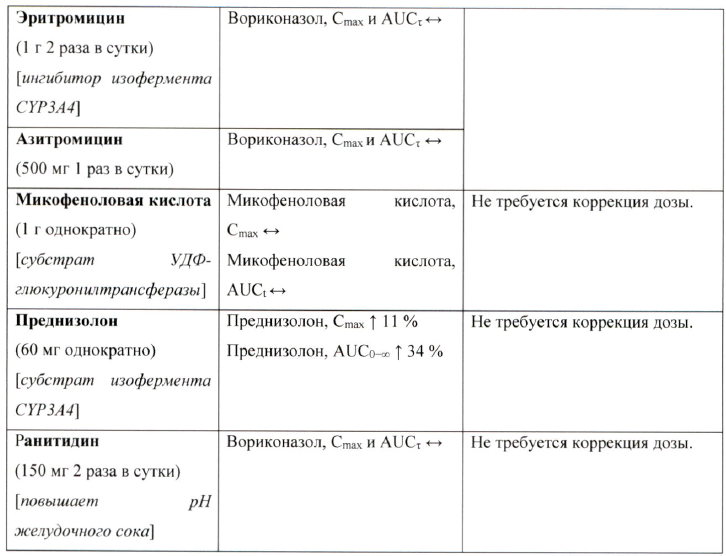
Таблица взаимодействия
Взаимодействие между вориконазолом и другими медицинскими препаратами представлены в таблице ниже. Направление стрелки для каждого фармакокинетического параметра основано на 90 % доверительном интервале соотношения геометрических средних, которые могут быть: в диапазоне (↔), ниже (↓) или выше (↑) диапазона, составляющего 80-125%. Звездочка (*) означает двустороннее взаимодействие. AUCT, AUC и AUC0-∞ представляют собой площадь под кривой интервала дозирования, от времени 0 до времени с определяемым показателем, а также от времени 0 до бесконечности соответственно.
Взаимодействия в таблице представлены согласно следующему порядку: противопоказания, требуется корректировка дозы и тщательный клинический и/или биологический мониторинг, а также препараты, с которыми не отмечено существенного фармакокинетического взаимодействия, но которые могут быть клинически интересны в данной терапевтической сфере.
Фармацевтическая несовместимость
Вориконазол несовместим с 4,2 % раствором натрия гидрокарбоната, поэтому его не рекомендуется использовать в качестве растворителя. Совместимость с другими концентрациями раствора натрия гидрокарбоната неизвестна.
Вориконазол нельзя вводить одновременно с препаратами крови или растворами электролитов высокой концентрации, даже если для инфузий используются разные катетеры.
Инфузию вориконазола не следует проводить через один катетер или канюлю с другими лекарственными средствами, включая препараты для парентерального питания (Аминофузин 10 % Плюс). Однако препарат может вводиться одновременно с парентеральным питанием, а также с растворами электролитов невысокой концентрации через отдельные катетеры или отдельный вход многоканального катетера.
Вориконазол не следует смешивать с другими лекарственными средствами за исключением перечисленных в разделе «Правила приготовления раствора» (см. раздел «Способ применения и дозы»).
Особые указания
Взятие материала для посева и других лабораторных исследований (серология, гистология) с целью выделения и идентификации возбудителей следует производить до начала лечения.
Лечение можно начать до получения результатов лабораторных исследований. Однако после получения этих результатов необходимо скорректировать противогрибковую терапию соответствующим образом.
К видам, наиболее часто вызывающим грибковые инфекции у человека, относятся С. Albicans, С. paraphlosis, С. tropicalis, С. glabrata и С. krusei. Для всех указанных видов минимальная подавляющая концентрация (МПК) вориконазола обычно составляет менее 1 мг/мл. Тем не менее, in vitro активность вориконазола против разных видов Candida не одинакова. В частности, МПК вориконазола для устойчивых к флуконазолу изолятов С. glabrata пропорционально выше, чем для изолятов, чувствительных к флуконазолу. В связи с этим, грибки рода Candida следует во всех возможных случаях идентифицировать до уровня вида. При возможности определения чувствительности грибов к противогрибковым препаратам полученные значения МПК следует интерпретировать с использованием пороговых критериев.
Выделены клинические штаммы микроорганизмов, обладающие пониженной чувствительностью к вориконазолу. Однако повышенные МПК не всегда позволяют предсказать клиническую неэффективность: известны случаи, когда вориконазол был эффективен у пациентов, инфицированных микроорганизмами, устойчивыми к другим азолам. Оценить корреляцию между активностью вориконазола в условиях in vitro и клиническими результатами лечения трудно, учитывая тяжелое состояние пациентов, которых включали в клинические исследования. Пограничные концентрации вориконазола, позволяющие оценивать чувствительность к этому препарату, не установлены.
Нежелательные явления со стороны сердечно-сосудистой системы
Применение вориконазола может приводить к удлинению интервала QT на электрокардиограмме, что сопровождается редкими случаями мерцания/трепетания желудочков у тяжелобольных пациентов с множественными факторами риска, такими как кардиотоксическая химиотерапия, кардиомиопатия, гипокалиемия, сопутствующая терапия, которые могли способствовать развитию данного осложнения. Следует с осторожностью вводить вориконазол пациентам с потенциально проартимогенными состояниями, такими как:
- врожденное или приобретенное удлинение интервала QT;
- кардиомиопатия, особенно в сочетании с сердечной недостаточностью;
- синусовая брадикардия:
- существующие аритмии с клиническими проявлениями;
- сопутствующая терапия препаратами, которые могут привести к удлинению интервала QT (см. раздел «Взаимодействие с другими лекарственными препаратами»).
Нарушения электролитного баланса, например, гипокалиемию, гипомагниемию и гипокальциемию, следует контролировать и корректировать при необходимости, до начала лечения и во время лечения вориконазолом.
Было проведено исследование с участием здоровых добровольцев, в рамках которого изучалось влияние на интервал QT однократных доз вориконазола, превышавших ежедневную стандартную дозу не более, чем в 4 раза. Ни у одного из пациентов не было отмечено удлинение интервала QT на 60 мсек или более от нормы или выше клинически значимого порога в 500 мсек.
Гепатотоксичность
Частота клинически значимого повышения активности «печеночных» трансаминаз у пациентов, получающих вориконазол, составляет 13,4 %. В большинстве случаев показатели функции печени нормализуются как при продолжении лечения без изменения дозы или после ее коррекции, так и после прекращения терапии. При применении вориконазола нечасто наблюдались случаи тяжелой гепатотоксичности (желтуха, гепатит и печеночно-клеточная недостаточность, в т.ч. с летальным исходом) у пациентов с серьезными основными заболеваниями.
Нежелательные явления со стороны печени наблюдаются, в основном, у пациентов с серьезными заболеваниями, главным образом, злокачественными новообразованиями кроветворной системы. У пациентов без каких-либо факторов риска наблюдаются преходящие реакции со стороны печени, включая гепатит и желтуху. Нарушения функции печени обычно обратимы и проходят после прекращения лечения.
Мониторинг функции печени
Во время лечения вориконазолом рекомендуется постоянно контролировать функцию печени у детей и взрослых. Клиническое ведение таких пациентов должно включать лабораторную оценку функции печени (в частности, определение активности ACT и АЛТ) в начале лечения вориконазолом и не реже 1 раза в неделю в течение первого месяца терапии. В случае продолжения лечения при отсутствии изменений со стороны биохимических показателей функции печени частота мониторинга может быть уменьшена до одного раза в месяц. При выраженном повышении биохимических показателей функции печени вориконазол следует отменить, если только соотношение пользы и риска терапии согласно медицинской оценке не оправдает его дальнейшее применение.
Зрительные нарушения
При лечении вориконазолом примерно у 21 % пациентов наблюдается нарушение зрительного восприятия: затуманивание зрения, изменение цветового зрения или фотофобия. Нарушения зрения являются преходящими и полностью обратимыми; в большинстве случаев они самопроизвольно исчезают в течение 60 мин. При повторном применении вориконазола отмечается ослабление их выраженности. Зрительные нарушения обычно легко выражены, редко требуют прекращения лечения и не приводят к каким-либо отдаленным последствиям.
Механизм развития зрительных нарушений неизвестен. Установлено, что вориконазол снижает амплитуду волн на электроретинограмме (ЭРГ) у здоровых добровольцев. Данные изменения на ЭРГ не нарастали при продолжении лечения в течение 29 дней и полностью исчезали после отмены вориконазола.
Длительная терапия вориконазолом (в среднем в течение 169 дней) у пациентов с паракокцидиоидозом не оказывала клинически значимого эффекта на зрительную функцию, что подтвердили результаты тестов на остроту зрения, зрительных полей, цветовосприятия и контрастной чувствительности.
По данным постмаркетинговых исследований сообщается о развитии случаев зрительных нарушений, сохраняющихся продолжительное время, в частности, возникновение «пелены» перед глазами, неврит зрительного нерва и отек диска зрительного нерва. Следует отметить, что данными нарушения развиваются чаще всего у тяжелобольных пациентов и/или получающих сопутствующую терапию, которая может вызывать подобные нежелательные явления.
Нежелательные явления со стороны почек
У тяжелобольных пациентов, получающих лечение вориконазолом, отмечались случаи развития острой почечной недостаточности, что, вероятно, было связано с терапией нефротоксическими лекарственными препаратами основного или сопутствующих заболеваний.
Мониторинг функции почек
Состояние пациентов следует регулярно контролировать с целью выявления признаков нарушения функции почек. Для этого необходимо проводить лабораторные исследования, в частности, определять концентрацию креатинина в плазме крови (см. раздел «Способ применения и дозы»).
Мониторинг функции поджелудочной железы
Взрослые и дети, имеющие факторы риска развития острого панкреатита (например, недавно проведенная химиотерапия, трансплантация гематопоэтических стволовых клеток), должны пройти обследование (определение активности амилазы и липазы в сыворотке крови) для решения вопроса о терапии вориконазолом.
Нежелательные явления со стороны кожи
При терапии вориконазолом часто развиваются кожные реакции, в основном, у пациентов с серьезными основными заболеваниями, одновременно принимающих другие лекарственные препараты. В большинстве случаев отмечалась легко или умеренно выраженная кожная сыпь. Во время лечения вориконазолом редко отмечались случаи развития эксфолиативных кожных реакций, например, синдрома Стивенса-Джонсона. Если у пациента развиваются эксфолиативные кожные реакции, вориконазол следует отменить.
Кроме того, на фоне применения вориконазола возможно развитие фотосенсибилизации (включая веснушки, лентиго и солнечный кератоз) и псевдопорфирии. Рекомендуется всем пациентам, включая детей, избегать сильного или длительного воздействия прямых солнечных лучей во время лечения вориконазолом, а также принимать защитные меры, например, носить защищающую одежду и пользоваться солнцезащитными средствами с высоким коэффициентом защиты от ультрафиолетового излучения (SPF).
Длительное лечение
У пациентов с кожными реакциями фоточувствительности и дополнительными факторами риска сообщается о развитии плоскоклеточного рака кожи и меланомы на фоне продолжительной терапии. В случае возникновения у пациента фототоксических реакций он должен быть проконсультирован соответствующими специалистами и направлен к дерматологу. Следует рассмотреть возможность отмены вориконазола и назначения других противогрибковых препаратов. При продолжении терапии вориконазолом, несмотря на возникновение фототоксических поражений кожи, пациент должен регулярно проходить дерматологическое обследование с целью раннего выявления и лечения предраковых заболеваний кожи. Если у пациента развиваются поражения кожи, связанные с предраковыми заболеваниями кожи, плоскоклеточным раком кожи или меланомой, то следует рассмотреть вопрос о прекращении терапии вориконазолом.
Неинфекционный периостит
Имеются сообщения о случаях развития периостита у перенесших трансплантацию пациентов на фоне длительной терапии вориконазолом. Если у пациента боль в костях и имеются рентгенологические данные, указывающие на наличие периостита, следует рассмотреть возможность прекращения терапии вориконазолом после мультидисциплинарной оценки состояния пациента.
Применение у детей
Безопасность и эффективность применения препарата у детей младше 2 лет не изучалась. Вориконазол показан пациентам детского возраста от 2 лет и старше при постоянное контроле функции печени (у детей выше, чем у взрослых, частота повышения «печеночных» ферментов на фоне применения вориконазола). Биодоступность вориконазола при приеме внутрь у детей в возрасте от 2 до 12 лет может быть снижена вследствие нарушения всасываемости или низкой массы тела. В таких случаях рекомендуется внутривенное введение вориконазола. Частота развития фототоксических реакций у детей выше. В связи с тем, что фототоксические поражения могут перерождаться в плоскоклеточную карциному, у детей необходимо применять строгие меры по защите кожи от ультрафиолетового излучения. Детям с признаками фотостарения кожи, например, лентиго или веснушки, рекомендуется избегать солнца и обследоваться у дерматолога даже после прекращения лечения.
Наркотические анальгетики короткого действия (субстраты изофермента CYP3A4) Период полураспада алфентанила удлиняется в 4 раза при одновременном введении с вориконазолом, поэтому необходим тщательный мониторинг связанных с применением наркотических анальгетиков нежелательных реакций (включая более продолжительный мониторинг функции дыхания).
Наркотические аначъгетики длительного действия (субстраты изофермента CYP3A4) Следует рассмотреть возможность снижения дозы оксикодона и других наркотических анальгетиков длительного действия, метаболизирующихся при участии изофермента CYP3A4 (например, гидрокодон), при одновременном применении с вориконазолом. Необходимо проводить тщательный мониторинг связанных с применением наркотических анальгетиков нежелательных реакций (см. раздел «Взаимодействие с другими лекарственными препаратами»).
Фенитоин (субстрат изофермента CYP2C9 и мощный индуктор изоферментов цитохрома Р450)
При одновременном применении фенитоина и вориконазола рекомендуется осуществлять постоянный контроль концентрации фенитоина. Следует избегать одновременной терапии вориконазолом и фенитоином, за исключением тех случаев, когда предполагаемая польза превышает потенциальный риск (см. раздел «Взаимодействие с другими лекарственными препаратами»).
Эфавиренз (индуктор изоферментов цитохрома Р450; ингбитор и субстрат изофермента CYP3A4)
В случае одновременного применения вориконазола и эфавиренза следует увеличить дозу вориконазола до 400 мг каждые 12 часов, а дозу эфавиренза следует снизить до 300 мг каждые 24 часа (см. раздел «Взаимодействие с другими лекарственными препаратами»). Рифабутин (индуктор изоферментов цитохрома Р450)
Одновременное применение вориконазола и рифабутина противопоказано, так как рифабутин значительно снижает концентрацию вориконазола в плазме крови.
Ритонавир (мощный индуктор изоферментов цитохрома Р450, ингибитор и субстрат изофермента CYP3A4J
Применять одновременно вориконазол и ритонавир в низких дозах (100 мг 2 раза в сутки) следует лишь в том случае, если ожидаемая польза от приема вориконазола значительно превышает риск от их совместного применения (см. разделы «Противопоказания» и «Взаимодействие с другими лекарственными препаратами»). Эверолимус (субстрат изофермента CYP3A4 и Р-гликопротеина)
Одновременное применение вориконазола и эверолимуса не рекомендуется, так как ожидается, что вориконазол существенно увеличит концентрацию эверолимуса в плазме крови. В настоящее время нет достаточного количества данных, которые позволили бы дать рекомендации по коррекции режима дозирования в такой ситуации.
Методом (субстрат изофермента CYP3A4J
Рекомендуется постоянный мониторинг нежелательных и токсических реакций, связанных с метадоном, включая удлинение интервала QTc, при совместном применении с вориконазолом, так как возможно увеличение плазменной концентрации метадона. Может потребоваться снижение дозы метадона (см. раздел «Взаимодействие с другими лекарственными препаратами»).
Флуконазол (ингибитор изоферментов CYP2C9, CYP2C19 и CYP3A4)
Одновременное применение вориконазола и флуконазола внутрь у здоровых добровольцев приводит к существенному увеличению Сmax и AUCt вориконазола. Подходящий режим дозирования и частоты приема вориконазола и флуконазола не установлен. Рекомендуется мониторинг связанных с вориконазолом нежелательных реакций, если вориконазол применяется сразу после флуконазола.
Содержание натрия
Извлекаемое из одного флакона препарата количество бетадекса сульфобутилата натрия(3200 мг) соответствует 222,82 мг натрия. Это необходимо принимать во внимание при назначении препарата пациентам, которым следует придерживаться диеты с ограничением содержания поваренной соли.
Инфузионные реакции
При внутривенном введении вориконазола могут наблюдаться связанные с инфузией реакции, в частности, «приливы» крови к коже лица и тошнота. Если эти симптомы выражены, то следует рассмотреть целесообразность прекращения лечения (см. раздел «Побочное действие»).
Специальные меры предосторожности при уничтожении неиспользованного лекарственного препарата
Весь неиспользованный препарат и расходные материалы должны быть утилизированы в соответствии с локальными нормативными требованиями.
Влияние на способность управлять транспортными средствами, механизмами
Вориконазол оказывает умеренное влияние на способность управлять автомобилем и работать с механизмами. Он может вызвать преходящие и обратимые изменения зрения, включая нечеткость зрения, измененное/усиленное визуальное восприятие и/или фотофобию. При наличии таких симптомов пациентам следует избегать потенциально опасных действий. например, управление автомобилем или работа с механизмами. Пациенты, получающие терапию вориконазолом, не должны управлять автомобилем в темное время суток.
Форма выпуска
Лиофилизат для приготовления концентрата для приготовления раствора для инфузий. 200 мг
Первичная упаковка
По 3592,1 мг порошка во флаконы из прозрачного стекла (тип I. Евр. Ф.) вместимостью 25 мл, укупоренные красными резиновыми хлорбутиловыми пробками (Евр. Ф.), обжатыми алюминиевыми колпачками (flip-off) с защитной пластиковой крышкой бордового цвета.
Вторичная упаковка
По 1, 5 или 10 флаконов помещают в пачку картонную вместе с инструкцией по применению.
Условия хранения
Лиофилизат — при температуре не выше 25 °С.
Восстановленный раствор (10 мг/мл) — при температуре от 2 до 8 °С в холодильнике.
Готовый к применению раствор (0,5-5 мг/мл) — при температуре от 20 до 30 °С.
Хранить в недоступном для детей месте.
Срок годности
Лиофилизат — 2 года.
Восстановленный раствор (10 мг/мл) — не более 24 ч.
Готовый к применению раствор (0.5-5 мг/мл) — не более 3 ч.
Не применять препарат после истечения срока годности, указанного на упаковке.
Условия отпуска
Отпускают по рецепту.
Производитель
Держатель РУ: Сандоз д.д.. Веровшкова 57. 1000 Любляна, Словения;
Произведено: Лек д.д., Веровшкова 57, 1526 Любляна, Словения.
Претензии потребителей направлять в ЗАО «Сандоз»:
125315, г. Москва, Ленинградский проспект, д. 72, корп. 3.
Купить Вориконазол Сандоз лиофилизат в planetazdorovo.ru
*Цена в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Вориконазол ПСК (Voriconazole PSK)
💊 Состав препарата Вориконазол ПСК
✅ Применение препарата Вориконазол ПСК
Описание активных компонентов препарата
Вориконазол ПСК
(Voriconazole PSK)
Приведенная научная информация является обобщающей и не может быть использована для принятия
решения о возможности применения конкретного лекарственного препарата.
Дата обновления: 2020.11.16
Владелец регистрационного удостоверения:
Код ATX:
J02AC03
(Вориконазол)
Лекарственная форма
| Вориконазол ПСК |
Лиофилизат д/пригот. концентрата д/пригот. р-ра д/инф. 200 мг: фл. рег. №: ЛП-007372 |
Форма выпуска, упаковка и состав
препарата Вориконазол ПСК
Лиофилизат для приготовления концентрата для приготовления раствора для инфузий в виде плотной массы или смеси плотной и раскрошенной лиофилизированной массы белого цвета.
Вспомогательное вещество: бетадекса сульфобутилат натрия — 3200 мг
3400 мг — флаконы — пачки картонные.
Фармакологическое действие
Противогрибковое средство, производное триазола. Механизм действия связан с ингибированием деметилирования 14α-стерола, опосредованного грибковым цитохромом P450, эта реакция является ключевым этапом биосинтеза эргостерола.
In vitro вориконазол обладает широким спектром противогрибкового действия, активен в отношении Candida spp. (включая штаммы Candida krusei, устойчивые к флуконазолу, и резистентные штаммы Candida glabrata и Candida albicans) и обладает фунгицидным эффектом в отношении всех изученных штаммов Aspergillus spp., а также патогенных грибов, ставших актуальными в последнее время, включая Scedosporium или Fusarium, которые в ограниченной степени чувствительны к противогрибковым средствам.
Клиническая эффективность вориконазола была продемонстрирована при инфекциях, вызванных Aspergillus spp. (включая Aspergillus flavus, Aspergillus fumigatus, Aspergillus terreus, Aspergillus niger, Aspergillus nidulans), Candida spp. (включая штаммы Candida albicans, Candida dubliniensis, Candida glabrata, Candida inconspicua, Candida krusei, Candida parapsilosis, Candida tropicalis и Candida guillermondii), Scedosporium spp. (включая Scedosporium apiospermum /Pseudoallescheria boydii/, Scedosporium prolifecans) и Fusarium spp.
Другие грибковые инфекции, при которых наблюдался частичный или полный противогрибковый эффект, включали отдельные случаи инфекций, вызванных Alternaria spp., Blastomyces dermatitidis, Blastoschizomyces capitatus, Cladosporium spp., Coccidoides immitis, Conidiobolus coronatus, Cryptococcus neoformans, Exserohilum rostratum, Exophiala spinifera, Fonsecaea pedrosoi, Madurella mycetomatis, Paecilomyces lilacinus, Penicillium spp. (включая Penicillium marneffei), Philaphora richardsiae, Scopulariopsis brevicaulis и Trychosporon spp. (включая Trychosporon beigelii).
In vitro продемонстрирована активность вориконазола в отношении клинических штаммов Acremonium spp., Alternaria spp., Bipolaris spp., Cladophialophora spp., Histoplasma capsulatum. Рост большинства штаммов подавлялся при концентрациях вориконазола от 0.05 до 2 мкг/мл.
In vitro выявлена активность вориконазола в отношении Curvularia spp. и Sporothrix spp., однако клиническое значение ее неизвестно.
Фармакокинетика
Фармакокинетические параметры вориконазола характеризуются значительной межиндивидуальной вариабельностью.
Фармакокинетика вориконазола является нелинейной за счет насыщения его метаболизма. При повышении дозы наблюдается непропорциональное (более выраженное) увеличение AUC. Увеличение дозы с 200 мг 2 раза/сут до 300 мг 2 раза/сут приводит к увеличению AUC в среднем в 2.5 раза. При в/в введении или приеме внутрь ударных доз концентрации в плазме приближаются к равновесным в течение первых 24 ч. При кратности применения 2 раза/сут в средних (не в ударных) дозах происходит кумуляция активного вещества, а Css достигаются в большинстве случаев к 6 дню.
Вориконазол быстро и практически полностью всасывается после приема внутрь; Cmax в плазме крови достигается через 1-2 ч после приема. Биодоступность вориконазола при приеме внутрь составляет 96%, при повторном приеме с пищей с большим содержанием жиров Cmax и AUC снижаются на 34% и 24% соответственно. Всасывание вориконазола не зависит от рН желудочного сока.
Расчетный Vd вориконазола в равновесном состоянии составляет 4.6 л/кг, что указывает на активное распределение вориконазола в ткани. Связывание с белками плазмы составляет 58%.
Вориконазол проникает через ГЭБ и определяется в спинномозговой жидкости.
По данным исследований in vitro установлено, что вориконазол метаболизируется при участии печеночных изоферментов CYP2C19, CYP2C9, CYP3A4, при этом CYP2C19 играет важную роль в метаболизме вориконазола. Этот фермент проявляет выраженный генетический полиморфизм, в связи с чем сниженный метаболизм вориконазола возможен у 15-20% пациентов азиатского происхождения и у 3-5% европейцев и чернокожих. Исследования у представителей европеоидной расы и японцев показали, что у пациентов с пониженным метаболизмом AUC вориконазола в среднем в 4 раза выше, чем у гомозиготных пациентов с высоким метаболизмом. У гетерозиготных пациентов с активным метаболизмом AUC вориконазола в среднем в 2 раза выше, чем у гомозиготных.
Основным метаболитом вориконазола является N-оксид (72% среди циркулирующих в плазме метаболитов, меченных радиоактивной меткой). Этот метаболит обладает минимальной противогрибковой активностью.
В неизмененном виде с мочой выводится менее 2%.
После повторного приема внутрь или в/в введения в моче обнаруживается примерно 83% и 80% дозы (меченной радиоактивной меткой) соответственно. Большая часть (>94%) общей дозы выводится в течение первых 96 ч после приема внутрь и в/в введения.
T1/2 вориконазола в терминальной фазе зависит от дозы и составляет примерно 6 ч при приеме препарата внутрь в дозе 200 мг. В связи с нелинейностью фармакокинетики величина T1/2 не позволяет предсказать кумуляцию или выведение вориконазола.
Фармакокинетика в особых клинических случаях
При повторном приеме внутрь Cmax и AUC у здоровых молодых женщин были на 83% и 113% соответственно выше, чем у здоровых молодых мужчин (18-45 лет). Значимых различий Cmax и AUC у здоровых пожилых мужчин и здоровых пожилых женщин (≥ 65 лет) нет.
При повторном приеме вориконазола внутрь Cmax и AUC у здоровых пожилых мужчин (≥ 65 лет) на 61% и 86% соответственно выше, чем у здоровых молодых мужчин (18-45 лет).
Средние Css в плазме у детей, получающих вориконазол в дозе 4 мг/кг каждые 12 ч, сопоставимы с таковыми у взрослых, получающих вориконазол в дозе 3 мг/кг каждые 12 ч. Средняя концентрация была 1186 нг/мл у детей и 1155 нг/мл у взрослых. В связи с этим рекомендуемая поддерживающая доза у детей в возрасте от 2 до 12 лет составляет 4 мг/кг каждые 12 ч.
При однократном приеме вориконазола внутрь в дозе 200 мг у пациентов с нормальной функцией почек и пациентов от легких (КК 41-60 мл/мин) до тяжелых (КК менее 20 мл/мин) нарушений функции почек фармакокинетика вориконазола существенно не зависит от степени нарушений. Связывание с белками плазмы сходно у больных с различной степенью почечной недостаточности.
После однократного приема внутрь в дозе 200 мг AUC вориконазола у пациентов с легкой или умеренно выраженной степенью тяжести цирроза печени (классы А и В по шкале Чайлд-Пью) на 233% выше, чем у пациентов с нормальной функцией печени. Нарушение функции печени не влияет на связывание вориконазола с белками плазмы.
При повторном приеме внутрь AUC вориконазола сопоставима у больных с умеренно выраженным циррозом печени (класс В по шкале Чайлд-Пью), получавших поддерживающую дозу 100 мг 2 раза/сут, и у пациентов с нормальной функцией печени, получавших вориконазол в дозе 200 мг 2 раза/сут.
Показания активных веществ препарата
Вориконазол ПСК
Инвазивный аспергиллез; тяжелые инвазивные формы кандидозных инфекций (включая Candida krusei); кандидоз пищевода; тяжелые грибковые инфекции, вызванные Scedosporium spp. и Fusarium spp.; тяжелые грибковые инфекции при непереносимости или рефрактерности к другим лекарственным средствам; профилактика прорывных грибковых инфекций у пациентов с лихорадкой из групп высокого риска (реципиенты аллогенного костного мозга, больные с рецидивом лейкоза).
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Применяют внутрь или парентерально в виде инфузии.
Дозу устанавливают индивидуально, в зависимости от показаний, возраста и массы тела пациента, схемы лечения.
Побочное действие
Со стороны организма в целом: очень часто – лихорадка, периферические отеки; часто – ознобы, астения, боль в груди, реакции и воспаление в месте инъекции, гриппоподобный синдром.
Со стороны сердечно-сосудистой системы: часто – снижение АД, тромбофлебит, флебит; редко – предсердные аритмии, брадикардия, тахикардия, желудочковые аритмии; очень редко – наджелудочковая тахикардия, полная AV-блокада, блокада ножки пучка Гиса, узловые аритмии, желудочковая тахикардия (включая трепетание желудочков), удлинение интервала QT, фибрилляция желудочков.
Со стороны пищеварительной системы: очень часто – тошнота, рвота, диарея, боли в животе; часто – повышение активности АЛТ, АСТ, ЩФ, ЛДГ, ГГТ и уровня билирубина в плазме крови, желтуха, хейлит, холестаз; редко – холецистит, холелитиаз, запор, дуоденит, диспепсия, увеличение печени, гингивит, глоссит, гепатит, печеночная недостаточность, панкреатит, отек языка, перитонит; очень редко – псевдомембранозный колит, печеночная кома. У пациентов с серьезными основными заболеваниями (злокачественные гематологические заболевания) на фоне применения вориконазола редко отмечались случаи тяжелой гепатотоксичности (случаи желтухи, гепатита, гепатоцеллюлярной недостаточности, приводящей к смерти).
Со стороны эндокринной системы: редко – недостаточность коры надпочечников; очень редко – гипертиреоз, гипотиреоз.
Аллергические реакции: редко – токсический эпидермальный некролиз, синдром Стивенса-Джонсона, крапивница; очень редко – ангионевротический отек, многоформная эритема. При в/в инфузии описаны анафилактоидные реакции, включающие приливы, лихорадку, потливость, тахикардию, чувство стеснения в груди, одышку, обморочные состояния, зуд, сыпь.
Со стороны системы кроветворения: часто – тромбоцитопения, анемия (в т.ч. макроцитарная, микроцитарная, нормоцитарная, мегалобластная, апластическая), лейкопения, панцитопения; редко – лимфаденопатия, агранулоцитоз, эозинофилия, синдром диссеминированного внутрисосудистого свертывания, угнетение костномозгового кроветворения; очень редко – лимфангит.
Со стороны обмена веществ: часто – гипокалиемия, гипогликемия; редко – гипохолестеринемия.
Со стороны костно-мышечной системы: часто — боль в спине; редко – артрит.
Со стороны ЦНС и периферической нервной системы: очень часто – головная боль; часто – головокружение, галлюцинации, спутанность сознания, депрессия, тревога, тремор, ажитация, парестезии; редко – атаксия, отек головного мозга, внутричерепная гипертензия, гипестезия, нистагм, головокружение, обморок; очень редко – синдром Гийена-Барре, окуломоторный криз, эсктрапирамидный синдром.
Со стороны дыхательной системы: часто – респираторный дистресс-синдром, отек легких, синусит.
Дерматологические реакции: очень часто – сыпь; часто – зуд, макуло-папулезная сыпь, фотосенсибилизация, алопеция, эксфолиативный дерматит, отек лица, пурпура; редко – псориаз; очень редко – дискоидная красная волчанка.
Со стороны органов чувств: часто — зрительные нарушения (включая нарушение/усиление зрительного восприятия, туман перед глазами, изменение цветового восприятия, фотофобия); редко – блефарит, неврит зрительного нерва, отек соска зрительного нерва, склерит, нарушение вкусового восприятия, диплопия; очень редко – кровоизлияние в сетчатку, помутнение роговицы, атрофия зрительного нерва.
Со стороны мочевыделительной системы: часто – повышение уровня креатинина в сыворотке крови, острая почечная недостаточность, гематурия; редко – повышение остаточного азота мочевины, альбуминурия, нефрит; очень редко – некроз почечных канальцев.
Противопоказания к применению
Одновременный прием лекарственных средств – субстратов CYP3A4 – терфенадина, астемизола, цизаприда, пимозида и хинидина; одновременный прием сиролимуса; одновременный прием рифампицина, карбамазепина и длительно действующих барбитуратов; одновременный прием ритонавира; одновременный прием эфавиренза; одновременный прием алкалоидов спорыньи (эрготамина, дигидроэрготамина); повышенная чувствительность к вориконазолу.
Применение при беременности и кормлении грудью
Адекватных и строго контролируемых исследований по безопасности применения вориконазола при беременности не проводилось. В экспериментальных исследованиях на животных установлено, что вориконазол в высоких дозах оказывает токсическое действие на репродуктивную функцию. Возможный риск для человека не известен.
Выведение вориконазола с грудным молоком не изучалось.
Вориконазол не следует применять при беременности и в период лактации, за исключением тех случаев, когда ожидаемая польза для матери превышает потенциальный риск для плода или грудного ребенка.
В период лечения женщины репродуктивного возраста должны пользоваться надежными методами контрацепции.
Применение при нарушениях функции печени
С осторожностью применять у пациентов с тяжелой печеночной недостаточностью. В период лечения следует регулярно контролировать функцию печени (при появлении клинических признаков заболевания печени следует обсудить целесообразность прекращения терапии).
Применение при нарушениях функции почек
С осторожностью применять у пациентов с тяжелой почечной недостаточностью (при парентеральном введении). В период лечения следует регулярно контролировать функцию почек (в т.ч. уровень креатинина в сыворотке крови).
Применение у детей
Безопасность и эффективность применения вориконазола у детей младше 2 лет не установлены.
Особые указания
С осторожностью применять у пациентов с тяжелой печеночной недостаточностью, с тяжелой почечной недостаточностью (при парентеральном введении), а также при повышенной чувствительности к другим лекарственным средствам – производным азолов.
Перед началом лечения требуется коррекция электролитных нарушений (гипокалиемии, гипомагниемии и гипокальциемии).
Забор проб для культурального и других лабораторных исследований (серологических, гистопатологических) с целью выделения и идентификации возбудителей следует производить до начала лечения. Терапию можно начать до получения результатов лабораторных исследований, а затем, при необходимости, скорректировать.
Применение вориконазола может приводить к удлинению интервала QT на ЭКГ, что сопровождается редкими случаями мерцания-трепетания желудочков у пациентов со множественными факторами риска (кардиотоксическая химиотерапия, кардиомиопатия, гипокалиемия и сопутствующая терапия, которая могла способствовать развитию нежелательных явлений со стороны сердечно-сосудистой системы). У пациентов с данными потенциально проаритмическими состояниями вориконазол следует применять с осторожностью.
В период лечения следует регулярно контролировать функцию печени (при появлении клинических признаков заболевания печени следует обсудить целесообразность прекращения терапии), функцию почек (в т.ч. уровень креатинина в сыворотке крови).
При прогрессировании дерматологических реакций препарат следует отменить.
В период лечения пациенты, получающие вориконазол, должны избегать пребывания на солнце и УФ-облучения.
При одновременном применении вориконазола у пациентов, получающих циклоспорин и такролимус, следует провести коррекцию дозы последних и контролировать их концентрацию в плазме. После отмены вориконазола следует оценить концентрацию циклоспорина и такролимуса в плазме и при необходимости повысить их дозу.
При необходимости совместного применения вориконазола и фенитоина следует тщательно оценить предполагаемую пользу и потенциальный риск комбинированной терапии и постоянно мониторировать уровень фенитоина.
При необходимости совместного применения вориконазола и рифабутина следует тщательно оценить предполагаемую пользу и потенциальный риск от комбинированной терапии и проводить ее под контролем картины периферической крови, а также других возможных нежелательных эффектов рифабутина.
Безопасность и эффективность применения вориконазола у детей младше 2 лет не установлены.
Влияние на способность к управлению транспортными средствами и механизмами
Поскольку вориконазол может вызвать преходящие нарушения зрения, включая затуманивание зрения, нарушение/усиление зрительного восприятия и/или фотофобию, то при появлении таких реакций пациенты не должны заниматься потенциально опасными видами деятельности, такими как, например, управление автомобилем или использование сложной техники. На фоне применения вориконазола пациенты не должны водить автомобиль в темное время суток.
Лекарственное взаимодействие
Вориконазол метаболизируется при участии изоферментов CYP2C19, CYP2C9 и CYP3A4. Ингибиторы или индукторы этих изоферментов могут вызвать, соответственно, повышение или снижение концентраций вориконазола в плазме.
При одновременном применении с рифампицином (индуктор изоферментов CYP) в дозе 600 мг/сут Cmax и AUC вориконазола снижаются на 93% и 96% соответственно (комбинация противопоказана).
При одновременном применении с вориконазолом, ритонавир (индуктор изоферментов CYP, ингибитор и субстрат CYP3A4) в дозе 400 мг каждые 12 ч снижал Cmax в равновесном состоянии и AUC вориконазола, принимаемого внутрь, в среднем на 66% и 82% соответственно. Эффект более низких доз ритонавира на концентрации вориконазола пока не известен. Установлено, что повторное применение вориконазола внутрь не оказывает выраженного эффекта на Cmax в равновесном состоянии и AUC ритонавира, также принимаемого повторно (одновременное применение вориконазола и ритонавира в дозе 400 мг каждые 12 ч противопоказано).
При совместном применении с мощными индукторами изоферментов CYP карбамазепином или длительно действующими барбитуратами (фенобарбиталом) возможно значительное снижение Cmax вориконазола в плазме, хотя их взаимодействие не изучалось. Такая комбинация противопоказана.
При совместном применении с циметидином (неспецифический ингибитор изоферментов изоферментов CYP) в дозе 400 мг 2 раза/сут Cmax и AUC вориконазола повышаются на 18% и 23% соответственно (коррекции дозы вориконазола не требуется).
Вориконазол ингибирует активность CYP2C19, CYP2C9, CYP3A4, поэтому возможно повышение концентраций в плазме лекарственных средств, которые метаболизируются этими изоферментами.
При одновременном применении вориконазола с терфенадином, астемизолом, цизапридом, пимозидом и хинидином возможно значительное повышение их концентрации в плазме, что может привести к удлинению интервала QT и в редких случаях к развитию мерцания/трепетания желудочков (комбинация противопоказана).
При совместном применении вориконазол повышает Cmax и AUC сиролимуса (2 мг однократно) на 556% и 1014% соответственно (комбинация противопоказана).
При одновременном применении вориконазол может вызывать повышение концентрации алкалоидов спорыньи (эрготамина и дигидроэрготамина) в плазме и развитие эрготизма (такая комбинация противопоказана).
При совместном применении у пациентов, перенесших трансплантацию почки и находящихся в стабильном состоянии, вориконазол повышает Cmax и AUC циклоспорина, по крайней мере, на 13% и 70% соответственно, что сопровождается повышением риска развития нефротоксических реакций. При применении вориконазола у пациентов, получающих циклоспорин, рекомендуется уменьшить дозу циклоспорина в 2 раза и контролировать его уровни в плазме. После отмены вориконазола необходимо контролировать уровни циклоспорина и при необходимости увеличить его дозу.
При совместном применении вориконазол повышает Cmax и AUC такролимуса (применяемого в дозе 0.1 мг/кг однократно) на 117% и 221% соответственно, что может сопровождаться нефротоксическими реакциями. При применении вориконазола у пациентов, получающих такролимус, рекомендуется уменьшить дозу последнего до 1/3 и контролировать его уровни в плазме. После отмены вориконазола необходимо контролировать концентрацию такролимуса и при необходимости увеличить его дозу.
Одновременное применение вориконазола (в дозе 300 мг 2 раза/сут) и варфарина (30 мг 1 раз/сут) сопровождалось увеличением максимального протромбинового времени до 93%. При одновременном назначении варфарина и вориконазола рекомендуется контролировать протромбиновое время.
Вориконазол при совместном применении может вызывать повышение концентрации в плазме фенпрокумона, аценокумарола (субстраты CYP2C9, CYP3A4) и протромбинового времени. При применении вориконазола у пациентов, получающих препараты кумарина, необходимо контролировать протромбиновое время с короткими интервалами и соответствующим образом подбирать дозы антикоагулянтов.
При совместном применении вориконазол может вызывать повышение концентрации производных сульфонилмочевины (субстраты CYP2C9) — толбутамида, глипизида и глибенкламида в плазме и вызвать гипогликемию. При одновременном их применении необходимо тщательно контролировать уровни глюкозы в крови.
In vitro вориконазол ингибирует метаболизм ловастатина (субстрат CYP3A4). При совместном применении возможно повышение концентрации в плазме статинов, метаболизирующихся под действием CYP3A4, что может увеличить риск развития рабдомиолиза. При одновременном их применении рекомендуется оценить целесообразность коррекции дозы статина.
In vitro вориконазол ингибирует метаболизм мидазолама (субстрат CYP3A4). При совместном применении возможно повышение концентрации в плазме метаболизирующихся под действием CYP3A4 бензодиазепинов (мидазолама, триазолама, алпразолама) и развитие пролонгированного седативного эффекта. При одновременном применении этих препаратов рекомендуется обсудить целесообразность коррекции дозы бензодиазепина.
При совместном применении вориконазол может повысить содержание алкалоидов барвинка (субстраты CYP3A4) — винкристина, винбластина в плазме и привести к развитию нейротоксических реакций. Рекомендуется обсудить целесообразность коррекции дозы алкалоидов барвинка.
Вориконазол повышает Cmax и AUC преднизолона (субстрат CYP3A4), применяемого в дозе 60 мг однократно на 11% и 34% соответственно. Коррекция дозы не рекомендуется.
При одновременном применении с вориконазолом, эфавиренз (субстрат CYP3A4, по данным ряда исследований в зависимости от дозы — ингибитор или индуктор CYP3A4), применяемый в дозе 400 мг 1 раз/сут в равновесном состоянии снижает Cmax и AUC вориконазола в среднем на 61% и 77% соответственно. Вориконазол в равновесном состоянии (400 мг внутрь каждые 12 ч в первый день, затем 200 мг внутрь каждые 12 ч в течение 8 дней) повышает равновесную Cmax и AUC эфавиренза в среднем на 38% и 44% соответственно (такая комбинация противопоказана).
При совместном применении фенитоин (субстрат CYP2C9 и мощный индуктор изоферментов цитохрома P450), применяемый в дозе 300 мг 1 раз/сут, снижает Cmax и AUC вориконазола на 49% и 69% соответственно; а вориконазол (400 мг 2 раза/сут) повышает Cmax и AUC фенитоина на 67% и 81% соответственно (при необходимости совместного применения следует тщательно оценить соотношение предполагаемой пользы и потенциального риска комбинированной терапии, а также тщательно мониторировать уровни фенитоина в плазме).
При совместном применении рифабутин (индуктор цитохрома P450), применяемый в дозе 300 мг 1 раз/сут снижает Cmax и AUC вориконазола (200 мг 1 раз/сут) на 69% и 78% соответственно. При совместном применении с рифабутином Cmax и AUC вориконазола (350 мг 2 раза/сут) составляет соответственно 96% и 68% от показателей при монотерапии вориконазолом (200 мг 2 раза/сут). При применении вориконазола в дозе 400 мг 2 раза/сут Сmax и AUC соответственно на 104% и 87% выше, чем при монотерапии вориконазолом в дозе 200 мг 2 раза/сут. Вориконазол в дозе 400 мг 2 раза/сут повышает Cmax и AUC рифабутина на 195% и 331% соответственно. При одновременном лечении рифабутином и вориконазолом рекомендуется регулярно проводить развернутый анализ картины периферической крови и контролировать нежелательные эффекты рифабутина (например, увеит).
При совместном применении в дозе 40 мг 1 раз/сут омепразол (ингибитор CYP2C19; субстрат CYP2C19 и CYP3A4) повышает Cmax и AUC вориконазола на 15% и 41% соответственно, а вориконазол повышает Cmax и AUC омепразола на 116% и 280% соответственно (следовательно, коррекции дозы вориконазола не требуется, а дозу омепразола следует уменьшить в 2 раза). Следует учесть возможность лекарственного взаимодействия вориконазола с другими ингибиторами Н+-К+-АТФ-азы, которые являются субстратами CYP2C19.
При одновременном применении с другими ингибиторами протеазы ВИЧ (субстраты и ингибиторы CYP3A4) следует тщательно контролировать состояние пациента с целью возможных токсических эффектов, т.к. исследования in vitro показали, что вориконазол и ингибиторы протеазы ВИЧ (саквинавир, ампренавир, нелфинавир) могут взаимно ингибировать метаболизм друг друга.
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Подобно всем лекарственным препаратам ВОРИКОНАЗОЛ может вызывать нежелательные реакции, однако они возникают не у всех.
Немедленно обратитесь к врачу при появлении приведенных ниже нежелательных реакций – Вам может понадобиться неотложная медицинская помощь:
• сыпь;
• желтуха (пожелтение кожи); изменения результатов анализов крови, которые характеризуют функциональное состояние печени;
• панкреатит.
Также могут возникать следующие нежелательные реакции:
Очень часто (могут проявляться не менее чем у 1 из 10 человек)
• нарушение зрения (включая помутнение зрения, изменения цветового зрения, светобоязнь, дальтонизм (снижение способности видеть или различать цвета), ночная слепота, снижение остроты и яркости зрения, потеря части поля зрения, пятна перед глазами);
• лихорадка;
• сыпь;
• тошнота, рвота, диарея, боль в животе;
• головная боль;
• периферические отеки;
• затрудненное дыхание;
• изменения в анализах крови, в том числе связанные с нарушениями функции печени.
Часто (могут проявляться менее чем у 1 из 10 человек):
• воспаление пазух носа, воспаление десен, озноб, слабость;
• изменение клеточных элементов крови, такие как пониженное количество эритроцитов (анемия) и/или лейкоцитов (уменьшение количества лейкоцитов может вызвать необъяснимое повышение температуры), уменьшение количества тромбоцитов (что может вызвать легкое появление синяков и кровотечение);
• пониженный уровень сахара, калия, натрия в крови;
• тревога, депрессия, растерянность, возбуждение, бессонница, галлюцинации;
• судороги, тремор или неконтролируемые движения мышц, покалывание на коже, повышение мышечного тонуса, сонливость, головокружение;
• кровоизлияние в сетчатку глаза;
• нерегулярное сердцебиение, обморок;
• пониженное артериальное давление, воспаление вен (что может быть связано с образованием тромба);
• серьезное затруднение дыхания, сопровождающееся болью в груди, отек лица (рот, губы и вокруг глаз), скопление жидкости в легких;
• запор, нарушение пищеварения, воспаление губ и кожи вокруг них;
• желтуха, воспаление печени и повреждение печени;
• кожная сыпь, которая может привести к покраснению кожи всего тела, образованию пузырей, шелушению и отеку кожи;
• зуд;
• синдром хронической усталости;
• выпадение волос;
• боль в спине;
• почечная недостаточность, гематурия (кровь в моче), изменения некоторых результатов анализов крови, включая те, которые характеризуют функцию Ваших почек.
Нечасто (могут проявляться менее чем у 1 из 100 человек):
• псевдомембранозный колит (нарушение нормального состояния кишечной микрофлоры, чаще возникает на фоне приема антибиотиков и сопровождается диареей);
• аллергические реакции;
• увеличение лимфатических узлов (иногда болезненных на ощупь), снижение количества всех форменных элементов крови, повышенный уровень эозинофилов;
• нарушение функции надпочечников и щитовидной железы;
• отек мозга;
• нарушение функции мозга, симптомы паркинсонизма, повреждение нервов, приводящее к онемению, боли, покалыванию или жжению в руках или ногах;
• дисгевзия (расстройство вкуса);
• диплопия (двоение в глазах); боль и воспаление глаз и век; нехарактерные движения глаз; повреждение зрительного нерва, приводящее к ухудшению зрения; отек диска зрительного нерва;
• нарушение сердцебиения, нарушения сердечного ритма;
• изменения на электрокардиограмме (ЭКГ);
• воспаление поджелудочной железы, воспаление двенадцатиперстной кишки, отек и воспаление языка;
• увеличение печени, печеночная недостаточность, заболевание желчного пузыря, образование камней в желчном пузыре;
• воспаление почек (нефрит), протеинурия (белок в моче), повреждение почек;
• повышенный уровень холестерина в крови, повышенный уровень мочевины в крови;
• аллергические кожные реакции (иногда тяжелые), включая обильную кожную сыпь, крапивницу, покраснение кожи всего тела, сильный зуд, образование пузырей, шелушение и отек кожи, воспаление слизистых оболочек, особенно во рту, воспаление на коже, солнечный ожог, красные пятна на коже, которые могут быть вызваны изменениями количества определенных клеток крови (тромбоцитов), экзема;
• воспаление суставов;
• гриппоподобные симптомы (усталость, озноб, боль в суставах и мышцах); раздражение и воспаление слизистой желудочно-кишечного тракта, что может вызвать диарею, связанную с приемом антибиотиков; воспаление стенок лимфатических сосудов;
• воспаление тонкой оболочки, которая выстилает внутреннюю стенку брюшной полости и покрывает поверхность внутренних органов (перитонит);
• реакции в месте введения;
• нарушения слуха, звон в ушах, головокружение.
Редко (могут проявляться менее чем у 1 из 1000 человек):
• анафилактоидная реакция (тяжелая гиперчувствительность/аллергическая реакция);
• кровотечение или кровоподтеки из-за широко распространенных тромбов в мелких кровеносных сосудах тела (диссеминированное внутрисосудистое свертывание);
• повышенная функция щитовидной железы;
• токсическое поражение центральной нервной системы, проявляющееся как осложнение печеночной недостаточности, непроизвольные колебательные движения глаз;
• атрофия зрительного нерва, помутнение роговицы;
• нарушение координации и равновесия;
• нерегулярное сердцебиение (пируэтная тахикардия), что может привести к летальному исходу; удлинение интервала QT на ЭКГ;
• воспалительные заболевания лимфатической системы; воспаление внутренней стенки вены с последующим образованием тромба;
• поражение мозга, вызванное заболеванием печени (печеночная энцефалопатия);
• токсический эпидермальный некролиз (синдром Лайелла) (отслоение верхнего слоя кожного покрова), лекарственная реакция с эозинофилией и системными симптомами (DRESS-синдром), ангионевротический отек (отек лица, губ, рук или пальцев); образование грубых, чешуйчатых пятен на коже под воздействием солнца, сыпь, псориаз, дерматит, вызванный действием лекарственного средства.
Частота неизвестна (исходя из имеющихся данных, частоту возникновения определить невозможно):
• веснушки и пигментные пятна;
• рак кожи;
• периостит (воспалительный процесс, который протекает в надкостнице (пленке, покрывающей кость по всей поверхности));
• красные, чешуйчатые пятна или кольцевидные кожные образования, которые могут быть симптомом аутоиммунного заболевания (кожной красной волчанки)
Если у Вас усиливается любая из перечисленных нежелательных реакций или у Вас появилась нежелательная реакция, не указанная в данном листке-вкладыше, пожалуйста, сообщите об этом лечащему врачу.
Сообщение о нежелательных реакциях
Если у Вас возникают какие-либо нежелательные реакции, проконсультируйтесь с врачом. Данная рекомендация распространяется на любые возможные нежелательные реакции, в том числе на не перечисленные в листке-вкладыше.
Вы также можете сообщить о нежелательных реакциях в информационную базу данных по нежелательным реакциям (действиям) на лекарственные препараты, включая сообщения о неэффективности лекарственных препаратов, выявленным на территории государства (УП «Центр экспертиз и испытаний в здравоохранении МЗ РБ», rceth.by). Сообщая о нежелательных реакциях, Вы помогаете получить больше сведений о безопасности препарата.
 |
Международное непатентованное название? Вориконазол |
 |
В одном флаконе содержится: действующее вещество: вориконазол 200мг (что эквивалентно концентрации раствора после разведения 10мг/мл); вспомогательные вещества: натриевая соль сульфобутилового эфира бета-циклодекстрина. |
 |
Противогрибковые средства — производные имидазола и триазола |
 |
ПроизводителиКурская биофабрика(Россия), Фармстандарт-УфаВИТА(Россия), Белмедпрепараты(Беларусь) |
 |
Показания к применению Вориконазол лиофилизат для инъекций 200мгИнвазивный аспергиллез.Кандидемия у пациентов без нейтропении.Тяжелые инвазивные кандидозные инфекции (включая С. krusei).Кандидоз пищевода.Тяжелые грибковые инфекции, вызванные Scedosporium spp. и Fusarium spp.Другие тяжелые инвазивные грибковые инфекции при непереносимости или рефрактерности к другим лекарственным средствам.Профилактика «прорывных» грибковых инфекций у пациентов со сниженной функцией иммунной системы, лихорадкой и нейтропенией, из групп высокого риска (реципиенты трансплантации гемопоэтических стволовых клеток, больные с рецидивом лейкоза). Профилактика инвазивных грибковых инфекций у пациентов (взрослых и детей старше 12 лет) группы высокого риска, таких как реципиенты трансплантации гемопоэтических стволовых клеток. |
 |
Способ применения и дозировка Вориконазол лиофилизат для инъекций 200мгПрепарат Вориконазол не рекомендуется вводить в виде болюсных инъекций (струйно). Скорость инфузии не должна превышать 3мг/кг/ч в течение 1-3ч.Перед началом терапии необходимо откорректировать такие электролитные нарушения, как гипокалиемия. гипомагниемия и гипокальциемия. Взрослые пациенты: назначение препарата следует начинать с внутривенного введения в рекомендуемой насыщающей дозе, чтобы уже в первый день добиться адекватной концентрации в плазме крови. Внутривенное введение следует продолжать как минимум 7 дней, после чего возможен переход на пероральный прием препарата, при условии, что пациент способен принимать лекарственные средства для приема внутрь. Учитывая высокую биодоступность препарата при приеме внутрь, достигающую 96%, при наличии клинических показаний можно переходить с внутривенного на пероральное применение препарата без коррекции дозы.Далее приведена подробная информация по дозированию препарата:Насыщающая доза — все показания (первые 24ч) Внутривенные инфузии — 6мг/кг каждые 12ч; внутрь — не рекомендуется.Поддерживающая доза (после первых 24ч): Профилактика инвазивных грибковых инфекций у пациентов (взрослых и детей старше 12 лет) группы высокого риска, таких как реципиенты трансплантации гемопоэтических стволовых клеток, профилактика «прорывных» грибковых инфекций у лихорадящих пациентов. Внутривенные инфузии 3-4мг/кг каждые 12ч; внутрь — пациенты с массой тела 40кг и более — 200мг каждые 12ч, пациенты с массой тела менее 40кг — 100мг каждые 12ч.Инвазивный аспергиллез/инфекции, вызванные Scedosporium spp. и Fusarium spp./другие тяжелые инвазивные грибковые инфекции. Внутривенные инфузии 4мг/кг каждые 12ч; внутрь — пациенты с массой тела 40кг и более — 200мг каждые 12ч, пациенты с массой тела менее 40кг — 100мг каждые 12ч.Кандидемия у пациентов без проявлений нейтропении. Внутривенные инфузии 3-4 мг/кг каждые 12ч; внутрь — пациенты с массой тела 40кг и более — 200мг каждые 12ч, пациенты с массой тела менее 40кг — 100мг каждые 12ч.Кандидоз пищевода. Внутривенные инфузии не установлено; внутрь — пациенты с массой тела 40кг и более — 200мг каждые 12ч, пациенты с массой тела менее 40кг — 100мг каждые 12ч.Подбор дозы для внутривенного введения: при недостаточной эффективности лечения поддерживающая доза препарата для внутривенного введения может быть увеличена до 4мг/кг каждые 12ч. Если пациент не переносит препарат в высокой дозе, ее снижают до 3мг/кг каждые 12ч. Длительность лечения должна быть как можно короче в зависимости от клинического эффекта и результатов микологического исследования. Длительность лечения не должна превышать 180 дней.Профилактика у взрослых и детей: профилактическое применение препарата следует начинать в день трансплантации и можно продолжать до 100 дней. Продлить профилактику до 180 дней после трансплантации можно только в случае продолжения иммуносупрессивной терапии или развития реакции «трансплантат против хозяина» (ТПХ). Безопасность и эффективность вориконазола при применении более 180 дней в клинических исследованиях надлежащим образом не изучались.Режим дозирования с целью профилактики такой же, как и с целью лечения в соответствующих возрастных группах. Нарушение функции почек: у больных со средней или тяжелой степенью почечной недостаточностью (клиренс креатинина менее 50мл/мин) наблюдается кумуляция вспомогательного компонента препарата натриевой соли сульфобутилового эфира бета-циклодекстрина. Таким больным препарат Вориконазол следует назначать внутрь за исключением тех случаев, когда предполагаемая польза внутривенного введения превышает потенциальный риск. В подобных ситуациях необходимо регулярно контролировать концентрацию креатинина и в случае его повышения следует обсудить возможность перехода на прием вориконазола внутрь. Вориконазол выводится в ходе гемодиализа с клиренсом 121мл/мин 4-часовой сеанс гемодиализа не приводит к удалению значительной части дозы вориконазола и не требует ее коррекции. Натриевая соль сульфобутилового эфира бета-циклодекстрина выводится в ходе гемодиализа с клиренсом 55мл/мин.Нарушение функции печени: при остром повреждении печени, проявляющемся повышением активности «печеночных» трансаминаз: аланинаминотрансферазы (АЛТ) и аспартатаминотрансферазы (ACT), коррекция дозы не требуется, но рекомендуется продолжать контроль показателей функции печени.Больным с легкими или среднетяжелыми нарушениями функции печени (классы А и В по классификации Чайлд-Пью) следует назначать стандартную насыщающую дозу препарата, а поддерживающую дозу снижать в 2 раза. Больным с тяжелой степенью нарушения функции печени (класс С по классификации Чайлд-Пью) препарат следует назначать только в тех случаях, когда ожидаемая польза превышает возможный риск, и под постоянным контролем с целью выявления признаков токсического действия препарата.Пожилые пациенты: коррекции дозы у пожилых людей не требуется.Применение у детей: безопасность и эффективность вориконазола у детей младше 2 лет не установлены.Режим дозирования вориконазола у детей (в возрасте от 2 до 12 лет) и подростков в возрасте от 12 до 14 лет и массой тела менее 50кг:Насыщающая доза (первые 24ч): внутривенные инфузии — 9мг/кг каждые 12ч; внутрь — не рекомендуется.Поддерживающая доза (после первых 24ч): внутривенные инфузии — 8мг/кг 2 раза в сутки; внутрь — 9мг/кг 2 раза в сутки (максимальная доза 350мг 2 раза в сутки).Терапию рекомендуется начинать с внутривенного введения препарата, возможность перорального приема препарата следует рассматривать только после клинического улучшения и возможности пациента принимать пероральные лекарственные средства.Следует принимать во внимание, что воздействие препарата при внутривенном введении в дозе 8мг/кг приблизительно в два раза выше, чем при применении внутрь в дозе 9мг/кг. Применение вориконазола у детей в возрасте от 2 до 12 лет с нарушениями функции печени или почек не изучалось.У подростков (в возрасте от 12 до 14 лет с массой тела 50кг или более; от 15 до 18 лет вне зависимости от массы тела) вориконазол дозируется так же, как для взрослых. Коррекция дозы: при неадекватном клиническом ответе пациента, доза может быть увеличена с шагом 1мг/кг (или 50мг в случае, если изначально применяли максимальную пероральную дозу 350мг). В случае, если ребенок не переносит лечение, можно снизить дозу вориконазола с шагом 1мг/мл (или 50мг в случае, если изначально применяли максимальную пероральную дозу 350мг).Инструкция по приготовлению раствора для инфузий: препарат выпускается во флаконах для однократного применения. Содержимое флакона восстанавливают, растворяя в 19мл воды для инъекции или 19мл 0,9% раствора натрия хлорида, и получают 20мл прозрачного концентрата, содержащего вориконазол в концентрации 10мг/мл. Если растворитель не поступает во флакон под действием вакуума, то флакон использовать нельзя. Перед применением необходимый объем концентрата прибавляют к рекомендуемому совместимому раствору для инфузии и получают раствор, содержащий вориконазол в концентрациях от 0,5мг/мл до 5мг/мл.Необходимые объемы раствора препарата вориконазола, содержащего 10мг/мл.Масса тела 10кг — для дозы 4мг/кг необходимо 4,0мл восстановленного раствора, для дозы 8мг/кг — 8мл раствора, для дозы 9мг/кг — 9мл раствора.Масса тела 15кг — для дозы 4мг/кг необходимо 6,0мл восстановленного раствора, для дозы 8мг/кг — 12мл раствора, для дозы 9мг/кг — 13,5мл раствора.Масса тела 20кг — для дозы 4мг/кг необходимо 8,0мл восстановленного раствора, для дозы 8мг/кг — 16мл раствора, для дозы 9мг/кг — 18,0мл раствора.Масса тела 25кг — для дозы 4мг/кг необходимо 10,0мл восстановленного раствора, для дозы 8мг/кг — 20мл раствора, для дозы 9мг/кг — 22,5мл раствора.Масса тела 30кг — для дозы 3мг/кг необходимо 9,0мл восстановленного раствора, для дозы 4мг/кг — 12мл раствора, для дозы 6мг/кг — 18мл раствора, для дозы 8мг/кг — 24мл раствора, для дозы 9мг/кг — 27мл раствора.Масса тела 35кг — для дозы 3мг/кг необходимо 10,5мл восстановленного раствора, для дозы 4мг/кг — 14мл раствора, для дозы 6мг/кг — 21мл раствора, для дозы 8мг/кг — 28мл раствора, для дозы 9мг/кг — 31,5мл раствора.Масса тела 40кг — для дозы 3мг/кг необходимо 12,0мл восстановленного раствора, для дозы 4мг/кг — 16мл раствора, для дозы 6мг/кг — 24мл раствора, для дозы 8мг/кг — 32мл раствора, для дозы 9мг/кг — 36мл раствора.Масса тела 45кг — для дозы 3мг/кг необходимо 13,5мл восстановленного раствора, для дозы 4мг/кг — 18мл раствора, для дозы 6мг/кг — 27мл раствора, для дозы 8мг/кг — 36мл раствора, для дозы 9мг/кг — 40,5мл раствора.Масса тела 50кг — для дозы 3мг/кг необходимо 15,0мл восстановленного раствора, для дозы 4мг/кг — 20мл раствора, для дозы 6мг/кг — 30мл раствора, для дозы 8мг/кг — 40мл раствора, для дозы 9мг/кг — 45мл раствора.Масса тела 55кг — для дозы 3мг/кг необходимо 16,5мл восстановленного раствора, для дозы 4мг/кг — 22мл раствора, для дозы 6мг/кг — 33мл раствора, для дозы 8мг/кг — 44мл раствора, для дозы 9мг/кг — 49,5мл раствора.Масса тела 60кг — для дозы 3мг/кг необходимо 18,0мл восстановленного раствора, для дозы 4мг/кг — 24мл раствора, для дозы 6мг/кг — 36мл раствора, для дозы 8мг/кг — 48мл раствора, для дозы 9мг/кг — 54мл раствора.Масса тела 65кг — для дозы 3мг/кг необходимо 19,5мл восстановленного раствора, для дозы 4мг/кг — 26мл раствора, для дозы 6мг/кг — 39мл раствора, для дозы 8мг/кг — 52мл раствора, для дозы 9мг/кг — 58,5мл раствора.Масса тела 70кг — для дозы 3мг/кг необходимо 21мл восстановленного раствора, для дозы 4мг/кг — 28мл раствора, для дозы 6мг/кг — 42мл раствора.Масса тела 75кг — для дозы 3мг/кг необходимо 22,5мл восстановленного раствора, для дозы 4мг/кг — 30мл раствора, для дозы 6мг/кг — 45мл раствора.Масса тела 80кг — для дозы 3мг/кг необходимо 24мл восстановленного раствора, для дозы 4мг/кг — 32мл раствора, для дозы 6мг/кг — 48мл раствора.Масса тела 85кг — для дозы 3мг/кг необходимо 25,5мл восстановленного раствора, для дозы 4мг/кг — 34мл раствора, для дозы 6мг/кг — 51мл раствора.Масса тела 90кг — для дозы 3мг/кг необходимо 27,0мл восстановленного раствора, для дозы 4мг/кг — 36мл раствора, для дозы 6мг/кг — 54мл раствора.Масса тела 95кг — для дозы 3мг/кг необходимо 28,5мл восстановленного раствора, для дозы 4мг/кг — 38мл раствора, для дозы 6мг/кг — 57мл раствора.Масса тела 100кг — для дозы 3мг/кг необходимо 30,0мл восстановленного раствора, для дозы 4мг/кг — 40мл раствора, для дозы 6мг/кг — 60мл раствора.Препарат Вориконазол, лиофилизат для приготовления концентрата для приготовления раствора для инфузий представляет собой стерильный лиофилизат без консерванта, предназначенный для однократного применения. С микробиологической точки зрения препарат следует вводить немедленно. Восстановленный раствор (концентрат) можно хранить не более 24ч при температуре от 2 до 8°C в том случае, если он был приготовлен в контролируемых асептических условиях.Концентрат можно далее разводить следующими растворами: 0,9% раствор натрия хлорида для внутривенного введения;раствор Рингера лактата для внутривенного введения;5% раствор декстрозы и раствор Рингера лактата для внутривенного введения;5% раствор декстрозы и 0,45% раствор натрия хлорида для внутривенного введения;5% раствор декстрозы для внутривенного введения;5% раствор декстрозы и 0,15% раствор калия хлорида для внутривенного введения;0,45% раствор натрия хлорида для внутривенного введения;5% раствор декстрозы и 0,9% раствор натрия хлорида для внутривенного введения. Совместимость вориконазола с другими растворами, помимо указанных выше неизвестна. |
 |
Противопоказания Вориконазол лиофилизат для инъекций 200мгПрепарат Вориконазол противопоказан больным с гиперчувствительностью к вориконазолу или любому другому компоненту препарата.Противопоказано одновременное применение Вориконазола и следующих препаратов: субстраты изофермента CYP3A4 — терфенадин, астемизол, цизаприд, пимозид или хинидин; сиролимус; рифампицин, карбамазепин и длительно действующие барбитураты (фенобарбитал); рифабутин; эфавиренз в дозах 400мг и выше один раз в сутки (с вориконазолом в стандартных дозах); ритонавир в высоких дозах (400мг и выше два раза в сутки); алкалоиды спорыньи (эрготамин, дигидроэрготамин), являющиеся субстратами изофермента CYP3A4: зверобой продырявленный (индуктор цитохрома Р450 и Р-гликопротеина).Препарат противопоказан детям в возрасте младше 2 лет.С осторожностью: повышенная чувствительность к другим препаратам — производным азолов.Тяжелая степень недостаточности функции печени, тяжелая степень недостаточности функции почек.Вориконазол следует применять с осторожностью у пациентов с проаритмическими состояниями: врожденное или приобретенное увеличение интервала QT, кардиомиопатия, в особенности с сердечной недостаточностью, синусовая брадикардия, наличие симптоматической аритмии, одновременный прием препаратов, вызывающих удлинение интервала QT.Также следует соблюдать осторожность при применении препарата у пациентов с электролитными нарушениями, такими как: гипокалиемия, гипомагниемия и гипокальциемия.Применение при беременности и в период грудного вскармливания: достаточной информации о применении вориконазола у беременных женщин нет. В исследованиях на животных установлено, что препарат оказывает токсическое действие на репродуктивную функцию. Возможный риск для человека неизвестен. Вориконазол не следует применять у беременных женщин за исключением тех случаев, когда ожидаемая польза для матери явно превышает возможный риск для плода. Выведение вориконазола с грудным молоком не изучалось. На время применения препарата грудное вскармливание следует прекратить.Женщины репродуктивного возраста при применении препарата должны использовать надежные методы контрацепции. |
 |
Фармакологическое действиеФармакодинамика: вориконазол — противогрибковый препарат широкого спектра действия из группы триазолов. Механизм действия вориконазола связан с ингибированием грибкового цитохрома Р450, что является ключевым этапом биосинтеза эргостерола. Накопление 14альфа — метилстирола коррелирует с последующей потерей эргостерола в грибковых клеточных мембранах, что обуславливает противогрибковую активность вориконазола. Было установлено, что вориконазол более селективен в отношении изоферментов цитохрома Р450 грибков, чем в отношении различных ферментных систем цитохрома Р450 млекопитающих.Положительной связи между средними, максимальными и минимальными значениями концентрации вориконазола в плазме крови и терапевтических исследованиях не выявлено и эта взаимосвязь в профилактических исследованиях не изучалась.Фармакодинамический и фармакокинетический анализ данных клинических исследований выявил положительную связь между концентрацией вориконазола в плазме крови и отклонением от нормы биохимических показателей функции печени, а также зрительными нарушениями.In vitro вориконазол обладает широким спектром противогрибкового действия: активен в отношении Candida spp. (включая штаммы С. krusei, устойчивые к флуконазолу, и резистентные штаммы С. glabrata и С. albicans), а также проявляет фунгицидный эффект в отношении всех изученных штаммов Aspergillus spp. и патогенных грибов, ставших актуальными в последнее время, включая Scedosporium spp. или Fusarium spp., которые ограниченно чувствительны к существующим противогрибковым средствам.Клиническая эффективность (с частичным или полным ответом) вориконазола была продемонстрирована при инфекциях, вызванных Aspergillus spp., включая A. flavus, А. fumigatus, A. terreus. A. niger, A. nidulans, Candida spp., включая С. albicans, С. glabrata, С. krusei, С. parapsilosis и С. tropicalis, а также в отношении ограниченного числа штаммов С. dubliniensis, С. inconspicua, и С. guilliermondii, Scedosporium spp., включая S. apiospermum, S. prolificans и Fusarium spp.Другие грибковые инфекции, при которых применялся вориконазол (иногда с частичным или полным ответом), включали в себя отдельные случаи инфекций, вызванных Alternaria spp., Blastomyces dermatitidis, Blastoschizomyces capitatus, Cladosporium spp., Coccidioides immitis, Conidiobolus coronatus, Cryptococcus neoformans, Exserohilum rostratum, Exophiala spinifera, Fonsecaea pedrosoi, Madurella mycetomatis, Paecilomyces lilacinus, Penicillium spp., включая P. marneffei, Phialophora richardsiae, Scopulariopsis brevicaulis и Trichosporon spp., включая T. beigelii.Продемонстрирована активность вориконазола in vitro в отношении клинических штаммов Acremonium spp., Alternaria spp., Bipolaris spp., Cladophialophora spp., Histoplasma capsulatum. Рост большинства штаммов подавлялся при концентрациях вориконазола от 0,05мкг/мл до 2мкг/мл.Выявлена также активность вориконазола in vitro в отношении Curvularia spp. Sporothrix spp., однако клиническое значение данного эффекта неизвестно.Фармакокинетика: фармакокинетические параметры вориконазола характеризуются значительной межиндивидуальной вариабельностью.Фармакокинетика вориконазола является нелинейной за счет насыщения его метаболизма. При повышении дозы наблюдается непропорциональное (более выраженное) увеличение площади под кривой «концентрация-время» (AUC). Увеличение пероральной дозы с 200мг 2 раза в сутки до 300мг 2 раза в сутки приводит к увеличению AUC в среднем в раза. Воздействие вориконазола при приеме внутрь поддерживающей дозы 200мг (или 100мг для пациентов с массой тела менее 40кг) соответствует воздействию вориконазола при применении внутривенно в дозе 3мг/кг. При приеме внутрь поддерживающей дозы 300мг (или 150мг для пациентов с массой тела менее 40кг) воздействие соответствует воздействию вориконазола при внутривенном применении в дозе 4мг/кг.При внутривенном введении или приеме внутрь насыщающих доз вориконазола равновесная концентрация достигается в течение первых 24ч. Если препарат назначают 2 раза в сутки в средних (но не в насыщающих) дозах, то происходит кумуляция вориконазола, а равновесные концентрации достигаются к 6-му дню у большинства пациентов.Вориконазол быстро и практически полностью всасывается после приема внутрь: максимальная концентрация в плазме крови (Cmax) достигается через 1-2ч после приема. Биодоступность вориконазола при приеме внутрь составляет 96%. При повторном приеме с пищей с большим содержанием жиров Cmax и AUC снижаются на 34% и 24%, соответственно. Всасывание вориконазола не зависит от pH желудочного сока.Средний объем распределения вориконазола в равновесном состоянии составляет около 4,6л/кг, что указывает на активное распределение вориконазола в ткани. Связывание с белками плазмы крови составляет 58%.Вориконазол проникает через гематоэнцефалический барьер (ГЭБ) и определяется в спинномозговой жидкости.Согласно данным исследований in vitro вориконазол метаболизируется под действием изоферментов CYP2C19, CYP2C9, CYP3A4. Важную роль в метаболизме вориконазола играет изофермент CYP2C19, проявляющий выраженный генетический полиморфизм, в связи, с чем пониженный метаболизм вориконазола возможен у 15-20% представителей азиатского происхождения и у 3-5% представителей европеоидной и негроидной рас.Установлено, что у пациентов с пониженным метаболизмом AUC вориконазола в среднем в 4 раза выше, чем у гомозиготных пациентов с высоким метаболизмом. У гетерозиготных пациентов с высоким метаболизмом; AUC вориконазола в среднем в 2 раза выше, чем у гомозиготных.Основным метаболитом вориконазола является N-оксид, доля которого составляет около 72% от общего количества циркулирующих в плазме крови метаболитов с радиоактивной меткой. Этот метаболит обладает минимальной противогрибковой активностью и не вносит вклад в клинический эффект вориконазола.Вориконазол выводится в виде метаболитов после биотрансформации в печени; в неизмененном виде почками выводится менее 2% от введенной дозы препарата.После многократного приема вориконазола внутрь или внутривенного введения в моче обнаруживается около 83% и 80% дозы препарата, соответственно. Большая часть (более 94%) общей дозы выводится в течение первых 96ч после приема внутрь и внутривенного введения. Период полувыведения (Т1/2) вориконазола зависит от дозы и составляет примерно 6ч при приеме препарата внутрь в дозе 200мг. В связи с нелинейностью фармакокинетики величина Т1/2 не позволяет предсказать кумуляцию или выведение вориконазола.Пол: при многократном приеме вориконазола внутрь Cmax и AUC у здоровых молодых женщин были на 83% и 113% соответственно выше, чем у здоровых молодых мужчин (18-45 лет). Значимых различий Cmax и AUC у здоровых пожилых мужчин и здоровых пожилых женщин (старше 65 лет) нет. Равновесная концентрация вориконазола в плазме крови у женщин была на 100% и 91% выше, чем у мужчин после приема препарата в виде таблеток или суспензии, соответственно. Необходимости коррекции дозы вориконазола в зависимости от пола нет. Концентрации в плазме крови у мужчин и женщин сходны. Возраст: при многократном приеме вориконазола в виде таблеток внутрь Cmax и AUC у здоровых пожилых мужчин (старше 65 лет) на 61% и 86% соответственно выше, чем у здоровых молодых мужчин (18-45 лет). Значимых различий Cmax и AUC у здоровых пожилых женщин (старше 65 лет) и здоровых молодых женщин (18-45 лет) нет.Профиль безопасности вориконазола у молодых и пожилых пациентов не отличается. Необходимости коррекции дозы вориконазола в зависимости от возраста нет.Дети: у детей отмечается большая внутрииндивидуальная вариабельность, чем у взрослых.Сравнение детской и взрослой популяций показало, что предполагаемая AUC у детей после введения насыщающей дозы 9мг/кг была сравнима с таковой у взрослых после введения насыщающей дозы 6мг/кг. Предполагаемая общая концентрация у детей после введения поддерживающей дозы 4мг/кг и 8мг/кг два раза в сутки была также сравнима с таковой у взрослых после введения поддерживающей дозы 3мг/кг и 4мг/кг два раза в сутки. Концентрация вориконазола при внутривенном введении в дозе 8мг/кг в два раза выше, чем при приеме внутрь в дозе 9мг/кг. Биодоступность вориконазола при приеме внутрь у детей может ограничиваться нарушением всасывания и достаточно низкой массой тела в этом возрасте и в этом случае может быть показано внутривенное введение. Полученные данные свидетельствуют о более высокой элиминации вориконазола у детей по сравнению с взрослыми в связи с большим соотношением массы печени и массы тела. У большинства подростков концентрация вориконазола в плазме крови соответствует этому показателю у взрослых пациентов. Тем не менее, отмечались меньшие значения концентрации вориконазола в плазме крови у некоторых подростков с низкой массой тела по сравнению с взрослыми и были ближе к значениям того же показателя у детей. Основываясь на популяционном фармакокинетическом анализе, подростки в возрасте от 12 до 14 лет с массой тела менее 50кг должны получать дозу вориконазола. рекомендованную для приема у детей.Нарушение функции почек: связывание с белками плазмы сходно у больных с различной степенью почечной недостаточности. У пациентов со средней или тяжелой степенью нарушения функции почек (концентрация креатинина в сыворотке более 220мкмоль/л или 2,5мг/дл) наблюдается кумуляция вспомогательного вещества — натриевой соли сульфобутилового эфира р-циклодекстрина, входящего в состав лиофилизата для приготовления концентрата для приготовления раствора для инфузий.Нарушение функции печени: нарушение функции печени не влияет на связывание вориконазола с белками плазмы крови. Сведений о фармакокинетике вориконазола у пациентов с тяжелым циррозом печени (класс С по классификации Чайлд-Пью) нет. |
 |
Побочное действие Вориконазол лиофилизат для инъекций 200мгДанные о безопасности вориконазола основаны на результатах исследования более чем 2000 человек (1655 пациентов, применяющих вориконазол в лечебных целях и 279 с профилактической целью), представленных гетерогенной популяцией (пациенты со злокачественными новообразованиями крови, ВИЧ-инфицированные больные с кандидозом пищевода и рефрактерными грибковыми инфекциями, пациенты без нейтропении с кандидемией или аспергиллезом, а также здоровые добровольцы).Наиболее распространенными нежелательными реакциями являются нарушения со стороны органа зрения, отклонение от нормы результатов функциональных проб печени, лихорадка, сыпь, рвота, тошнота, диарея, головная боль, периферические отеки, боль в животе и угнетение дыхания. Нежелательные реакции обычно было легко или умеренно выражены. Клинически значимой зависимости безопасности препарата от возраста, расы или пола не выявлено.Критерии оценки частоты: очень часто — более 10%; часто — более 1%, но менее 10%; нечасто — более 0,1%, но менее 1%; редко — более 0,01%, но менее 0,1%; очень редко — менее 0,01%; частота неизвестна — невозможно определить частоту на основании имеющихся данных.Со стороны сердца: часто — наджелудочковая аритмия, тахикардия, брадикардия; нечасто — фибрилляция желудочков, желудочковая экстрасистолия, наджелудочковая тахикардия, желудочковая тахикардия; редко — аритмия по типу «пируэт», полная атриовентрикулярная блокада, блокада ножки пучка Гиса, узловые аритмии.Со стороны сосудов: часто — артериальная гипотензия, флебит; нечасто — тромбофлебит. Со стороны системы кроветворения и лимфатической системы: часто — агранулоцитоз (включая фебрильную нейтропению и нейтропению), панцитопения, тромбоцитопения (включая иммунную тромбоцитопеническую пурпуру), анемия; нечасто — депрессия костного мозга, лейкопения, лимфаденопатия, эозинофилия, синдром диссеминированного внутрисосудистого свертывания.Со стороны нервной системы: очень часто — головная боль; часто — синкопа, тремор, парестезия, сонливость, головокружение, судороги, нистагм; нечасто — отек головного мозга, энцефалопатия, экстрапирамидное расстройство, периферическая нейропатия, атаксия, гипестезия, дисгевзия (нарушение вкусового восприятия); редко — печеночная энцефалопатия, синдром Гийена-Барре.Со стороны органа зрения: очень часто — нарушение со стороны органа зрения (в том числе нечеткость зрения, затуманенное зрение, фотофобия, хлоропсия, хроматопсия, светобоязнь, цветовая слепота, цианопсия, наличие в поле зрения радужных кругов вокруг источников света, ночная слепота, осциллопсия, фотопсия, мерцательная скотома, снижение остроты зрения, зрительная яркость, дефект полей зрения, плавающие помутнения стекловидного тела и ксантопсия); часто — кровоизлияние в сетчатую оболочку глаза; нечасто — неврит зрительного нерва, отек соска зрительного нерва, окулогирный криз, диплопия, склерит, блефарит; редко — атрофия зрительного нерва, помутнение роговицы.Со стороны органа слуха и вестибулярного аппарата: нечасто — вертиго, гипоакузия, шум в ушах.Со стороны дыхательной системы, грудной клетки и средостения: очень часто — угнетение дыхания; часто — отек легких, острый респираторный дистресс-синдром.Со стороны желудочно-кишечного тракта: очень часто — тошнота, рвота, диарея, боль в животе; часто — хейлит, диспепсия, запор; нечасто — дуоденит, глоссит, панкреатит, отек языка.Со стороны почек и мочевыделительной системы: часто — острая почечная недостаточность, гематурия; нечасто — некроз почечных канальцев, протеинурия, нефрит.Со стороны кожи и подкожных тканей: очень часто — сыпь; часто — эксфолиативный дерматит, алопеция, кожный зуд, макулопапулезная сыпь, эритема; нечасто — синдром Стивенса-Джонсона, фотосенсибилизация, крапивница, экзема, токсический эпидермальный некролиз, ангионевротический отек, мультиформная эритема, псориаз, аллергический дерматит, пурпура, папулезная сыпь, макулярная сыпь; редко — псевдопорфирия, стойкая лекарственная эритема; частота неизвестна — кожная форма системной красной волчанки.Со стороны опорно-двигательного аппарата и соединительной ткани: часто — боль в спине; нечасто — артрит; частота неизвестна — периостит.Со стороны эндокринной системы: нечасто — недостаточность коры надпочечников, гипотиреоз; редко — гипертиреоз.Нарушения метаболизма и питания: очень часто — периферические отеки; часто — гипокалиемия, гипогликемия, гипонатриемия (выявлено в пострегистрационных исследованиях).Инфекции и инвазии: часто — синусит, гастроэнтерит, гингивит; нечасто — псевдомембранозный колит, лимфангит, перитонит.Общие расстройства и нарушения в месте введения: очень часто — лихорадка; часто — озноб, астения, боль в грудной клетке, гриппоподобное заболевание, отек лица (включая периорбитальный отек, отек губ и отек рта); нечасто — реакция/воспаление на месте инъекции.Со стороны иммунной системы: нечасто — аллергические реакции; редко — анафилактоидные реакции.Со стороны гепатобилиарной системы: очень часто — отклонения от нормы результатов функциональных печеночных тестов (повышение активности аспартатаминотрансферазы, аланинаминотрансферазы, щелочной фосфатазы, гамма-глутамилтрансферазы, лактатдегидрогеназы, гипербилирубинемия); часто — желтуха, холестатическая желтуха, гепатит; нечасто — печеночная недостаточность, холецистит, холелитиаз, увеличение печени.Психические расстройства: часто — галлюцинации, спутанность сознания, депрессия, тревога, бессонница, ажитация.Новообразования доброкачественные, злокачественные и неуточненные (включая кисты и полипы): частота неизвестна — плоскоклеточный рак кожи. Исследования: часто — повышение концентрации креатинина в крови, нечасто — удлинение интервала QT на электрокардиограмме, повышение концентрации мочевины в крови, повышение концентрации холестерина в крови.Побочное действие при применении у детей: было установлено, что нежелательные эффекты препарата у детей в возрасте от 2 до 12 лет аналогичны таковым у взрослых. У детей наблюдалась более высокая частота повышения активности печеночных ферментов. В ходе пострегистрационных исследований выявлено развитие панкреатита у детей на фоне терапии вориконазолом, а также более частое возникновение кожных реакций |
 |
ПередозировкаИзвестно о трех случаях случайной передозировки. Все упомянутые случаи произошли у детей, которым внутривенно была введена доза вориконазола, в пять раз превышающая рекомендованную.Имеется сообщение о единичном случае фотофобии, продолжительностью 10 минут. Антидот вориконазола неизвестен. В случае передозировки показана симптоматическая и поддерживающая терапия.Вориконазол выводится в ходе гемодиализа с клиренсом 121мл/мин, натриевая соль сульфобутилового эфира Р-циклодекстрина — с клиренсом 55мл/мин. В случае передозировки гемодиализ может способствовать выведению вориконазола и натриевой соли сульфобутилового эфира Р-циклодекстрина из организма. |
 |
Взаимодействие Вориконазол лиофилизат для инъекций 200мгИнгибиторы или индукторы изоферментов цитохрома Р450 (CYP2C19, CYP2C9 и CYP3A4) могут вызвать соответственно повышение или снижение концентрации вориконазола в плазме крови.Вориконазол ингибирует активность изоферментов цитохрома Р450 — CYP2C19, CYP2C9 и CYP3A4, и может повышать плазменные концентрации веществ, которые метаболизируются с участием изоферментов цитохрома Р450.Взаимодействие вориконазола с другими лекарственными средствами и рекомендации при одновременном применении представлены ниже.Астемизол, терфенадин, цизаприд, пимозид и хинидин (субстраты изофермента CYP3A4) + вориконазол. Одновременное применение противопоказано.Карбамазепин и длительно действующие барбитураты (например, фенобарбитал, мефобарбитал) (мощные индукторы цитохрома Р450) + вориконазол. Одновременное применение противопоказано.Эфавиренз (ненуклеозидный ингибитор обратной транскриптазы) (индуктор цитохрома Р450; ингибитор и субстрат изофермента CYP3A4) Одновременное применение эфавиренза в дозе 400мг 1 раз в сутки и вориконазола в дозе 200мг 2 раза в сутки + вориконазол. Применение стандартных доз вориконазола и эфавиренза в дозе 400мг 1 раз в сутки противопоказано.Одновременное применение 300мг эфавиренза 1 раз в сутки и вориконазола 400мг 2 раза в сутки + вориконазол. Одновременное применение возможно, если поддерживающая доза вориконазола будет повышена до 400мг 2раза в сутки, а доза эфавиренза снижена до 300мг вориконазолом, 1 раз в сутки. При отмене терапии начальная доза эфавиренза должна быть восстановлена.Алкалоиды спорыньи (например, эрготамин, дигидроэрготамин) (субстраты изофермента CYP3A4) + вориконазол. Одновременное применение противопоказано.Рифабутин 300мг 1 раз в сутки (мощный индуктор цитохрома Р450) 300мг 1 раз в сутки + вориконазол (400мг 2 раза в сутки). Одновременное применение противопоказано.Рифампицин 600мг 1 раз в сутки (мощный индуктор цитохрома Р450) + вориконазол. Одновременное применение противопоказано.Ритонавир (ингибитор протеаз) (мощный индуктор цитохрома Р450, ингибитор и субстрат изофермента CYP3A4). Высокие дозы (400мг 2 раза в сутки) + вориконазол. Одновременное применение вориконазола и высоких доз ритонавира (400мг и выше 2 раза в сутки) противопоказано.Ритонавир (ингибитор протеаз) (мощный индуктор цитохрома Р450, ингибитор и субстрат изофермента CYP3A4). Низкие дозы (100мг 2 раза в сутки) + вориконазол. Одновременное применение вориконазола и ритонавира в низких дозах (100мг 2 раза сутки) допустимо лишь в том случае, если ожидаемая польза от приема вориконазола значительно превышает риск от их совместного применения.Зверобой продырявленный (индуктор цитохрома Р450 и Р-гликопротеина) 300мг 3 раза в сутки + вориконазол 400мг однократно. Одновременное применение противопоказано.Эверолимус (субстрат изофермента CYP3A4 и Р-гликопротеина) + вориконазол. Одновременное применение не рекомендуется, так как ожидается, что вориконазол значительно повышает концентрацию эверолимуса в плазме крови. На данный момент не имеется достаточной информации для рекомендации по коррекции режима дозирования.Флуконазол (ингибитор изоферментов CYP2C9 CYP2C19 и CYP3A4) 200мг 1 раз в сутки + вориконазол. Подходящий режим коррекции дозы и/или частоты приема вориконазола и флуконазола не установлен. В том случае, если вориконазол применяется после флуконазола, рекомендуется проводить тщательный контроль нежелательных реакций, связанных с приемом вориконазола.Фенитоин (субстрат изофермента CYP2C9 и мощный индуктор системы цитохрома Р450) 300мг 1 раз в сутки + вориконазол. Следует избегать одновременного приема вориконазола и фенитоина, за исключением случаев, когда польза для пациента превышает риск. Рекомендуется контролировать концентрацию фенитоина в плазме крови.Фенитоин (субстрат изофермента CYP2C9 и мощный индуктор системы цитохрома Р450) 300мг 1 раз в сутки (одновременное применение с вориконазолом в дозе 400мг 2 раза в сутки) + вориконазол. Одновременное применение возможно только в случае, если поддерживающая доза вориконазола будет увеличена до 5мг/кг внутривенно или с 200мг до 400мг внутрь 2 раза в сутки (у пациентов с массой тела менее 40кг со 100мг до 200мг внутрь 2 раза в сутки).Антикоагулянты Варфарин (30мг однократно) (субстрат изофермента CYP2C9) или другие пероральные антикоагулянты, например, фенпрокумон, аценокумарол (субстраты изоферментов CYP2C9, CYP3A4) + вориконазол 300мг 2 раза в сутки. Если пациентам получающим препараты кумарина назначают вориконазол, необходимо контролировать протромбиновое время с короткими интервалами и соответствующим образом подбирать дозы антикоагулянтов.Бензодиазепины (например, мидазолам, триазолам, алпразолам) (субстраты изофермента CYP3A4) + вориконазол. Рекомендуется оценить целесообразность коррекции дозы бензодиазепинов.Иммунодепрессанты (субстраты изофермента CYP3A4). Сиролимус (2мг однократно) + вориконазол. Одновременное применение вориконазола и сиролимуса противопоказано.Циклоспорин (у пациентов, перенесших трансплантацию почки и находящихся в стабильном состоянии) + вориконазол. При применении вориконазола у пациентов, получающих циклоспорин, рекомендуется уменьшить дозу циклоспорина вдвое и контролировать его концентрацию в плазме крови. Повышение концентрации циклоспорина сопровождается нефротоксичностью. После отмены вориконазола необходимо контролировать концентрацию циклоспорина и при необходимости увеличить его дозу.Такролимус (0,1мг/кг однократно) + вориконазол. При применении вориконазола у пациентов, получающих такролимус, рекомендуется уменьшить дозу последнего до одной трети и контролировать его концентрацию в плазме крови. Повышение концентрации такролимуса сопровождается нефротоксичностью. После отмены вориконазола необходимо контролировать концентрацию такролимуса и при необходимости увеличить его дозу.Длительно действующие опиаты (субстраты изофермента CYP3A4) Оксикодон (10мг однократно) + вориконазол. Следует оценить возможность снижения дозы оксикодона и других длительно действующих опиатов, метаболизируемых изоферментом CYP3A4 (например, гидрокодона). Может понадобиться контроль состояния пациента с короткими интервалами на предмет развития нежелательных реакций связанных с опиатами.Метадон (32-100мг 1 раз в сутки) + вориконазол. Повышение концентрации метадона в плазме крови приводит к проявлению токсических эффектов, включая удлинение интервала QT. Рекомендуется частый контроль состояния пациента на предмет развития нежелательных реакций и токсичности (в том числе, удлинение интервала QT), связанных с метадоном. Возможно, понадобится снижение дозы метадона.Нестероидные противовоспалительные препараты (НПВП) (субстраты изофермента CYP2C9): ибупрофен (400мг однократно), диклофенак (50мг однократно) + вориконазол. Пациентов следует наблюдать с целью выявления возможных токсических эффектов и при необходимости корректировать дозу НПВП. Омепразол (40мг 1 раз в сутки) (ингибитор изофермента СYP2C19; субстрат изоферментов CYP2C19 и CYP3A4) + вориконазол. Коррекции дозы вориконазола не требуется. При начале приема вориконазола у пациентов, уже получающих терапию омепразолом в дозах 40мг или выше, рекомендуется дозу омепразола уменьшить вдвое. Пероральные контрацептивы (субстраты изофермента CYP3A4; ингибиторы изофермента CYP2C19) Норэтистерон/этинилэстрадиола (1мг/0,35мг 1 раз в сутки) + вориконазол. Рекомендуется контроль состояния пациента на предмет развития нежелательных реакций, связанных с применением пероральных контрацептивов и вориконазола.Наркотические анальгетики короткого действия (субстраты изофермента CYP3A4): алфентанил (однократная доза 20мкг/кг с одновременным применением налоксона) или фентанил (однократная доза 5мкг/кг) + вориконазол. Следует оценить возможность снижения дозы алфентанила, фентанила и других наркотических анальгетиков короткого действия, имеющих схожую с алфентанилом химическую структуру и метаболизируемых изоферментом CYP3A4 (например, суфентанила).Пациенты должны находиться под постоянным наблюдением для предотвращения угнетения функции дыхания или других побочных эффектов, связанных с приемом наркотических анальгетиков короткого действия, и при необходимости их доза должна быть снижена.Статины (например, ловастатин) (субстраты изофермента CYP3A4) + вориконазол. Следует оценить возможность снижения дозы статинов.Производных сульфонилмочевины (например, толбутамид, глипизид, глибенкламид) (субстраты изофермента CYP2C9) + вориконазол. Необходимо тщательно контролировать концентрацию глюкозы в крови.Алкалоиды барвинка (например, винкристин, винбластин) (субстраты изофермента CYP3A4) + вориконазол. Рекомендуется оценить целесообразность коррекции дозы алкалоидов барвинка.Другие ингибиторы протеазы (ИП) ВИЧ (например, саквинавир, ампренавир, нелфинавир) (ингибиторы и субстраты изофермента CYP3A4) + вориконазол. Рекомендуется тщательный контроль состояния пациента на предмет развития любых проявлений лекарственной токсичности и/или недостаточности действия. Возможно, потребуется коррекция дозы препаратов.Другие ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ) (например, делавирдин, невирапин) (субстраты изофермента CYP3A4, ингибиторы или индукторы цитохрома Р450) + вориконазол. Рекомендуется тщательный контроль состояния пациента на предмет развития любых проявлений лекарственной токсичности и/или недостаточности действия. Возможно, потребуется коррекция дозы препаратов.Циметидин (400мг два раза в сутки) (неспецифически ингибирует цитохром Р450 и повышает уровень pH желудочного сока) + вориконазол. Коррекции дозы не требуется.Дигоксин (0,25мг 1 раз в сутки) (субстрат Р-гликопротеина) + вориконазол. Коррекции дозы не требуется.Индинавир (800мг 3 раза в сутки) (ингибитор и субстрат изофермента CYP3A4) + вориконазол. Коррекции дозы не требуется.Антибиотики группы макролидов Эритромицин (1г 2 раза в сутки) (ингибитор изофермента CYP3A4) или Азитромицин (500мг 1 раз в сутки) + вориконазол. Коррекции дозы не требуется.Микофеноловая кислота (1г однократно) (субстрат уридин-5-дифосфат-глюкуронилтрансферазы) + вориконазол. Коррекции дозы не требуется.Преднизолон (60мг однократно) (субстрат изофермента CYP3A4) + вориконазол. Коррекции дозы не требуется.Ранитидин (150мг 2 раза в сутки) (повышает pH желудочного сока) + вориконазол. Коррекции дозы не требуется. |
 |
Особые указанияВзятие материала для посева и других лабораторных исследований (серология, гистопатология) с целью выделения и идентификации возбудителей следует производить до начала лечения. Лечение можно начать до получения результатов лабораторных исследований. Однако после получения этих результатов необходимо скорректировать противогрибковую терапию.К видам, наиболее часто вызывающим инфекции у человека, относятся С. albicans, С. parapsilosis, С. tropicalis, С. glabrata и С. krusei, при этом для всех них минимальная подавляющая концентрация (МПК) вориконазола обычно составляет менее 1мг/мл. Однако, активностью вориконазола в условиях in vitro против грибков разных видов Candida не одинакова. В частности, МПК вориконазола для устойчивых к флуконазолу изолятов С. glabrata пропорционально выше, чем МПК для изолятов, чувствительных к флуконазолу. В связи с этим, грибки рода Candida следует во всех возможных случаях идентифицировать до уровня вида. При возможности определения чувствительности грибов к противогрибковым препаратам полученные значения МПК следует интерпретировать с использованием пороговых критериев.Выделены клинические штаммы микроорганизмов, обладающие пониженной чувствительностью к вориконазолу. Однако повышенные минимальные подавляющие концентрации (МПК) не всегда позволяют предсказать клиническую неэффективность: известны случаи, когда вориконазол был эффективен у больных, инфицированных микроорганизмами, устойчивыми к другим азолам. Оценить корреляцию между активностью вориконазола в условиях in vitro и клиническими результатами лечения трудно, учитывая сложность больных, которых включали в клинические исследования. Пограничные концентрации вориконазола, позволяющие оценивать чувствительность к этому препарату, не установлены.Нежелательные явления со стороны сердечно-сосудистой системы Применение вориконазола связано с удлинением интервала QT на электрокардиограмме, что сопровождается редкими случаями мерцания/трепетания желудочков у тяжелобольных пациентов с множественными факторами риска, такими как кардиотоксическая химиотерапия, кардиомиопатия, гипокалиемия и сопутствующая терапия, которые могли способствовать развитию данного осложнения. Вориконазол следует с осторожностью применять у пациентов со следующими потенциально проаритмическими состояниями:врожденное и приобретенное удлинение интервала QT;кардиомиопатия, особенно в сочетании с сердечной недостаточностью;синусовая брадикардия;существующие аритмии с клиническими проявлениями;одновременное применение лекарственных препаратов, удлиняющих интервал QT.Электролитные нарушения, например, гипокалиемию, гипомагниемию и гипокальциемию, при необходимости, следует контролировать и устранять до начала и во время терапии вориконазолом.При исследовании на здоровых добровольцах влияния вориконазола на интервал QT на ЭКГ при применении однократных доз, превышающих обычную дневную дозу не более чем в 4 раза, было установлено, что ни у одного из испытуемых не наблюдалось удлинения интервала QT на 60 или более мсек от нормы. Также ни у одного из испытуемых не наблюдалось удлинения интервала выше клинически значимого порога в 500 мсек.Гепатотоксичность: частота клинически значимого повышения активности «печеночных» трансаминаз у пациентов, получающих вориконазол, составляет 13,4%. В большинстве случаев показатели функции печени нормализуются как при продолжении лечения без изменения дозы или после ее коррекции, так и после прекращения терапии. При применении вориконазола нечасто наблюдались случаи тяжелой гепатотоксичности (желтуха, гепатит и печеночноклеточная недостаточность, приводящая к смерти) у пациентов с серьезными основными заболеваниями.Нежелательные явления со стороны печени наблюдаются, в основном, у пациентов с серьезными заболеваниями, главным образом, злокачественными опухолями крови. У пациентов без каких-либо факторов риска наблюдаются преходящие реакции со стороны печени, включая гепатит и желтуху. Нарушения функции печени обычно обратимы и проходят после прекращения лечения.Мониторинг функции печени: во время лечения вориконазолом рекомендуется постоянно контролировать функцию печени, как у детей, так и у взрослых. Клиническое ведение таких пациентов должно включать лабораторную оценку функции печени (в частности определение активности ACT и АЛТ) в начале лечения вориконазолом и не реже одного раза в неделю в течение первого месяца терапии. В случае продолжения лечения при отсутствии изменений со стороны биохимических показателей функции печени частота лабораторного обследования может быть уменьшена до одного раза в месяц. При выраженном повышении биохимических показателей функции печени вориконазол следует отменить, если только соотношение пользы и риска терапии согласно медицинской оценке не оправдывает его дальнейшее применение.Нарушения зрения: при лечении вориконазолом примерно у 21% пациентов наблюдается нарушение зрительного восприятия: затуманивание зрения, изменение цветового зрения или фотофобия. Нарушения зрения являются преходящими и полностью обратимыми; в большинстве случаев они самопроизвольно исчезают в течение 60 мин. При повторном применении вориконазола отмечается ослабление их выраженности. Зрительные нарушения обычно легко выражены, редко требуют прекращения лечения и не приводят к каким-либо отдаленным последствиям.Механизм развития зрительных нарушений неизвестен. Установлено, что вориконазол снижает амплитуду волн на электроретинограмме (ЭРГ) у здоровых добровольцев. Данные изменения ЭРГ не нарастали при продолжении лечения в течение 29 дней и полностью исчезали после отмены вориконазола.Длительная терапия вориконазолом (в среднем в течение 169 дней) у пациентов с паракокцидиоидозом не оказывала клинически значимого эффекта на зрительную функцию, что подтверждено результатами тестов на остроту зрения, зрительных полей, цветовосприятия и контрастной чувствительности.По данным пострегистрационных исследований сообщается о развитии случаев зрительных нарушений, сохраняющихся продолжительное время, в частности, возникновение «пелены» перед глазами, неврит зрительного нерва и отек диска зрительного нерва. Следует отметить, что данные нарушения развиваются чаще всего у тяжелобольных пациентов и/или получающих сопутствующую терапию, которая может вызывать подобные нежелательные явления.Нежелательные явления со стороны почек: у тяжелобольных пациентов, получающих вориконазол, отмечались случаи развития острой почечной недостаточности, что, вероятно, было связано с терапией, основного или сопутствующих заболеваний нефротоксичными лекарственными средствами. Мониторинг функции почек: пациентов следует наблюдать с целью выявления признаков нарушения функции почек. Для этого необходимо проводить лабораторные исследования, в частности, определять концентрацию креатинина в сыворотке крови. Мониторинг функции поджелудочной железы: взрослые и дети, имеющие факторы риска развития острого панкреатита (недавняя химиотерапия, трансплантация гемопоэтических стволовых клеток) должны пройти обследование (определение активности амилазы и липазы в сыворотке крови) для решения вопроса о терапии вориконазолом.Нежелательные явления со стороны кожи: при терапии вориконазолом часто развиваются кожные реакции, в основном, у пациентов с серьезными основными заболеваниями, одновременно принимающих другие лекарственные средства. В большинстве случаев отмечалась легко или умеренно выраженная кожная сыпь.Во время лечения вориконазолом у пациентов наблюдались случаи эксфолиативных кожных реакций, таких как синдром Стивенса-Джонсона. Если у пациента развиваются эксфолиативные кожные реакции, то вориконазол следует отменить.Так как во время терапии вориконазолом возможно развитие фотосенсибилизации, то во время лечения пациентам рекомендуется избегать воздействия прямых солнечных лучей и принимать защитные меры, такие как ношение одежды и применение солнцезащитных средств с высоким коэффициентом защиты от ультрафиолетового излучения (SPF). Длительное лечение: у пациентов с кожными реакциями фоточувствительности и дополнительными факторами риска сообщается о развитии плоскоклеточного рака кожи и меланомы на фоне продолжительной терапии. При возникновении у пациента фототоксических реакций он должен быть проконсультирован соответствующими специалистами и направлен к дерматологу. Следует рассмотреть возможность отмены вориконазола. При продолжении терапии вориконазолом, несмотря на возникновение фототоксических поражений кожи, пациент должен регулярно проходить дерматологическое обследование с целью раннего выявления и лечения предраковых заболеваний кожи. Если у пациента развиваются поражения кожи, связанные с предраковыми заболеваниями кожи, плоскоклеточным раком кожи или меланомой, то следует рассмотреть вопрос о прекращении терапии вориконазолом. Неинфекционный периостит: имеются сообщения о случаях развития периостита у пациентов после трансплантации, получающих длительную терапию вориконазолом. Терапию вориконазолом следует отменить в случае, если у пациента имеется боль в костях и на рентгенограмме отмечаются изменения, характерные для периостита.Применение у детей: вориконазол показан для применения у детей в возрасте от 3 лет (для данной лекарственной формы) и старше при постоянном контроле функции печени. У детей чаще отмечается повышение активности ферментов печени. Биодоступность вориконазола при приеме внутрь у детей в возрасте от 3 до 12 лет может быть снижена за счет нарушения всасывания или за счет пониженной массы тела. В таких случаях показано внутривенное введение вориконазола.Частота фототоксических реакций у детей выше. В связи с тем, что фототоксические поражения могут перерождаться в плоскоклеточную карциному (ПКК), у детей необходимо применять строгие меры по защите кожи от ультрафиолетового излучения. Детям с признаками фотостарения кожи, например, лентиго или веснушки, рекомендуется избегать солнца и обследоваться у дерматолога даже после прекращения лечения. Наркотические анальгетики короткого действия (субстраты изофермента CYP3A4) Поскольку период полувыведения алфентанила при его одновременном применении с вориконазолом увеличивается в 4 раза, необходим тщательный мониторинг нежелательных явлений, связанных с применением наркотических анальгетиков, включая более продолжительный мониторинг функции дыхания.Наркотические анальгетики длительного действия (субстраты изофермента CYP3A4) Следует предусмотреть возможность снижения дозы оксикодона и других наркотических анальгетиков продолжительного действия, которые метаболизируются изоферментом CYP3A4 (гидрокодон) при одновременном применении с вориконазолом. Необходимо проводить тщательный мониторинг нежелательных явлений, связанных с применением наркотических анальгетиков.Фенитоин (мощный индуктор цитохрома Р450 и субстрат изофермента CYP2C9): при одновременном применении фенитоина и вориконазола рекомендуется осуществлять постоянный контроль концентрации фенитоина. По возможности следует избегать одновременного применения вориконазола и фенитоина за исключением тех случаев, когда ожидаемая польза превышает возможный риск.Эфавиренз (ненуклеозидный ингибитор обратной транскриптазы индуктор цитохрома Р450, ингибитор и субстрат изофермента CYP3A4): в случае одновременного применения вориконазола и эфавиренза дозу вориконазоласледует увеличить до 400мг 2 раза в сутки, а доза эфавиренза должна быть снижена до 300мг каждые 24ч.Рифабутин: одновременное применение вориконазола и рифабутина противопоказано, так как рифабутин значительно снижает концентрацию вориконазола в плазме крови.Ритонавир (мощный индуктор цитохрома Р450, ингибитор и субстрат изофермента CYP3A4): применять одновременно вориконазол и ритонавир в низких дозах (100мг 2 раза в сутки) следует лишь в том случае, если ожидаемая польза от приема вориконазола значительно превышает риск от их совместного применения.Эверолимус (субстрат изофермента CYP3A4 и Р-гликопротеина): одновременное применение вориконазола и эверолимуса не рекомендуется, так как ожидается, что вориконазол значительно повышает концентрацию эверолимуса в плазме крови. На данный момент не имеется достаточной информации для рекомендации по коррекции режима дозирования.Метадон (субстрат изофермента CYP3A4): повышение концентрации метадона в плазме крови приводит к проявлению токсических эффектов, включая удлинение интервала QT. При одновременном применении вориконазола и метадона необходимо внимательно следить за проявлением нежелательных и токсических эффектов. При необходимости доза метадона может быть снижена. Флуконазол (ингибитор изоферментов CYP2C9, CYP2C19, CYP3A4): одновременное применение вориконазола и флуконазола внутрь у здоровых добровольцев приводит к значительному повышению Cmax и AUC вориконазола. Подходящий режим коррекции дозы и/или частоты приема вориконазола и флуконазола не установлен. В том случае, если вориконазол применяется после флуконазола, рекомендуется проводить тщательный контроль нежелательных реакций, связанных с приемом вориконазола.Влияние на способность управлять транспортными средствами, механизмами: вориконазол может вызвать преходящие и обратимые нарушения зрения включая возникновение «пелены» перед глазами, нарушение/усиление зрительного восприятия и/или фотофобию. При наличии таких симптомов пациенты должны избегать выполнения потенциально опасных действий, в частности, управления автомобилем или использования сложной техники. При приеме вориконазола пациенты не должны управлять автомобилем по ночам. |
 |
Условия храненияЛиофилизат: в защищенном от света недоступном для детей месте при температуре не выше 25°С.Восстановленный раствор: в течение не более 24 часов при температуре от 2°С до 8°С. |