Самый частый вопрос, который покупатели задают в чат поддержки нашего интернет-магазина — как правильно приготовить рабочий раствор дезинфицирующего средства. С этим вопросом обычно обращаются рядовые потребители, поэтому будет уместным собрать всю информацию по данному вопросу в один обзор.
Для начала хотелось бы обратить Ваше внимание на следующее: Всегда строго следуйте инструкции к дезинфицирующему средству!
В инструкции указываются те требования к приготовлению рабочих растворов дезинфицирующих средств, которые производитель посчитал важными для конкретного дезсредства.
Производители дезсредств придерживаются некоторых общих правил, которые справедливы для приготовления рабочих растворов практических всех дезинфицирующих средств. Например:
- Посуда для должна быть химически нейтральна, чистой, без следов ржавчины. Обычно это эмалированная посуда (без повреждения эмали), стеклянные или пластмассовые ёмкости
- Для приготовления обычно используют чистую холодную питьевую воду. Если производитель требует дистиллированную воду, то это будет обязательно указано в инструкции к раствору для дезинфекций.
- Некоторые препараты, могут быть использованы не только в виде водного раствора, но в виде водно-спиртового. Для приготовления таких дезсредств используют не 2 компонента, а 3.
- К работе не допускаются лица моложе 18 лет и не страдающие аллергическими заболеваниями и повышенной чувствительностью к химическим веществам.
- При работе со средством кожу рук необходимо защищать резиновыми перчатками.
- Мерная посуда должна быть чистой, сухой и химически нейтральной. Весьма желательно пользоваться раздельной посудой для каждого компонента рабочего раствора.
- При всех работах следует избегать попадания средства в глаза и на кожу.
Ключевое понятие для приготовления рабочего раствора дезинфицирующего средства — концентрация, которая подразумевает долю дезсредства в общем объеме рабочего раствора. Обратите внимание, что обычно концентрация дезсредства для разных режимов обработки и разных обрабатываемых поверхностей отличаются, порой — существенно. Концентрация — понятие относительное и поэтому справедливо для любого дезинфицирующего средства, то есть 1%-ный рабочий раствор препарата Альфадез, Миродез или любого иного означает, что в составе присутствует 1/100 часть дезинфицирующего средства и 99/100 частей воды.
Ниже приведена универсальная таблица для приготовления рабочих растворов для дезинфекции в диапазоне 0,1% — 4%. Иные концентрации можно высчитать из данных таблица по правилам обычной пропорции.
Концентрация рабочих растворов дезинфицирующих средств
|
Концентрация рабочего раствора (%) по препарату |
Количество концентрата средства и воды (мл), необходимые для приготовления: |
|||
|
1 л раствора |
10 л раствора |
|||
|
средство |
вода |
средство |
вода |
|
|
0,1 |
1,0 |
999,0 |
10 |
9990 |
|
0,2 |
2,0 |
998,0 |
20 |
9980 |
|
0,3 |
3,0 |
997,0 |
30 |
9970 |
|
0,4 |
4,0 |
996,0 |
40 |
9960 |
|
0,5 |
5,0 |
995,0 |
50 |
9950 |
|
0,8 |
8,0 |
992,0 |
80 |
9920 |
|
1,0 |
10,0 |
990,0 |
100 |
9900 |
|
1,2 |
12,0 |
988,0 |
120 |
9880 |
|
1,5 |
15,0 |
985,0 |
150 |
9850 |
|
2,0 |
20,0 |
980,0 |
200 |
9800 |
|
2,5 |
25,0 |
975,0 |
250 |
9750 |
|
3,0 |
30,0 |
970,0 |
300 |
9700 |
|
3,5 |
35,0 |
965,0 |
350 |
9650 |
|
4,0 |
40,0 |
960,0 |
400 |
9600 |
После приготовления рабочего раствора дезинфицирующего средства рекомендуется проверить концентрацию дезсредства с помощью соответствующих индикаторных полосок. Сами индикаторные полоски не входят в комплект поставки дезинфицирующего средства, их можно купить отдельно в нашем интернет-магазине.
Внимательно читайте и следуйте инструкции при приготовлении рабочего раствора дезинфицирующего средства!
Задать интересующие Вас вопросы, а также купить дезинфицирующие средства в Москве с доставкой, Вы можете в нашем интернет-магазине по телефону или через онлайн-чат.
Если вы уже знаете, как приготовить рабочий раствор дезсредства, то вам будет интересно узнать, как провести дезинфекцию парикмахерских или маникюрных инструментов.
Д. А. Меркулов, к.х.н., зав. кафедрой фундаментальной и прикладной химии, ФГБОУ ВПО «Удмуртский государственный университет», г. Ижевск
Введение
Гипохлоритами называют соли хлорноватистой кислоты HClO. Наиболее распространенными из них являются гипохлорит натрия, гипохлорит кальция и гипохлорит калия. Гипохлориты широко применяются для обеззараживания питьевой воды, отбеливания, дегазации и дезинфекции. Гипохлориты являются одними из самых важных химических соединений.
Таблица 1. Наиболее распространенные гипохлориты.
| Систематическое наименование | Традиционное название | Хим. формула | CAS № | М, г/моль |
|---|---|---|---|---|
| Гипохлорит натрия | Хлорноватистокислый натрий, лабарракова вода (гипохлорит натрия в смеси с хлоридом натрия и гидроксидом натрия) | NaClO | 7681–52–9 | 74,44 |
| Гипохлорит калия | Хлорноватистокислый калий,
жавелевая вода (гипохлорит калия в смеси с гидрокарбонатом калия и хлоридом калия) |
KClO | 7778–66–7 | 90,55 |
| Гипохлорит кальция | Хлорноватистокислый кальций, хлорная известь (гипохлорит кальция в смеси с хлоридом кальция, оксихлоридом кальция и гидроксидом кальция) | Ca(ClO)2 | 7778–54–3 | 142,98 |
История открытия
В 1774 г. шведский химик Карл Вильгельм Шееле получил хлор (Cl2) в результате взаимодействия оксида марганца(IV) MnO2 и соляной кислоты (HCl). Позже, в 1785 г. французский химик Клод Луи Бертолле обнаружил, что водный раствор газообразного хлора («хлорная вода»), содержащий хлорноватистую и хлороводородную кислоты, может отбелить белье, и сообщил о своих выводах Французской академии наук.
Cl2 + H2O = HClO + HCl
Знания об отбеливающих свойствах хлора были незамедлительно использованы Джеймсом Уаттом на текстильной фабрике в Глазго. Несмотря на то, что отбеливание с использованием хлора был значительно эффективнее традиционных способов отбеливания солнечным светом, слабыми растворами кислот и щелочей, применение хлора ограничивалось его токсичностью и разрушающим действием на ткани. Для стабилизации раствора газообразного хлора в воде и безопасности его применения, в 1787 г. на Парижском предприятии Societe Javel хлор стали пропускать через водный раствор карбоната калия (поташа)
Cl2 + K2СO3 = 2KHCO3 + KClO + KCl.
Глава предприятия Леонард Альбан назвал новый продукт «Eau de Javel» («жавелевая вода»), и вскоре белильная жидкость стала популярной во Франции и Англии.
В 1820 г. француз Антуан Лабаррак усовершенствовал способ получения отбеливателя, заменив поташ на более дешевый гидроксид натрия (каустическую соду). Полученный раствор гипохлорита и хлорида натрия получил название «Eau de Labarraque» («лабарракова вода»).
Cl2 + 2NaOH = NaClO + NaCl + H2O.
Широкое применение гипохлоритов для обеззараживания питьевой воды и дезинфекции стало возможным гораздо позже, в начале XX века, благодаря развитию промышленного производства хлора электролизом поваренной соли.
Физические свойства
Гипохлориты встречаются нам преимущественно в виде водных растворов, хотя некоторые из них можно выделить в твердом виде. Так, известен безводный гипохлорит натрия, который представляет собой неустойчивое бесцветное кристаллическое вещество. Из кристаллогидратов наиболее устойчивой формой является NaClO×5H2O. Это соединение представляет собой белые или бледно-зеленые ромбические кристаллы, расплывающиеся на воздухе. При нагревании пентагидрата гипохлорита натрия до температуры 24,4°С, он плавится. Кристаллогидрат NaClO×2,5H2O плавится при температуре 57,5°С. Моногидрат крайне неустойчив и разлагается выше 60°С, при более высоких температурах разложение протекает со взрывом.
Таблица 2. Плотности и температуры замерзания водных растворов гипохлорита натрия.
| Концентрация, % | 1 | 2 | 4 | 6 | 8 | 10 | 14 |
| Плотность, г/мл (18 °С) | 1,0053 | 1,0121 | 1025,8 | 1,0397 | 1,0538 | 1,0681 | 1,0977 |
| Концентрация, % | 18 | 22 | 26 | 30 | 34 | 38 | 40 |
| Плотность, г/мл (18 °С) | 1,1288 | 1,1614 | 1,1953 | 1,2307 | 1,2680 | 1,3085 | 1,3285 |
| Концентрация, % | 2 | 4 | 6 | 8 | 10 | 12 | 15,6 |
| tзам, °С | – 2,2 | – 4,4 | – 7,5 | – 10,0 | – 13,9 | – 19,4 | –29,7 |
В отличие от гипохлорита калия, известного только в растворах, гипохлорит кальция можно выделить в форме бесцветных кристаллов, устойчивых в сухой атмосфере без углекислого газа. Из водных растворов гипохлорит кальция можно выделить в виде кристаллогидратов Ca(ClO)2×2H2O, Ca(ClO)2×3H2O, Ca(ClO)2×4H2O.
Кислотно-основное равновесие между хлорноватистой кислотой и гипохлорит-ионом описывается обратимой реакцией с константой равновесия Ka = 2,63×10–8 при 20°С.
HClO = H+ + ClO–.
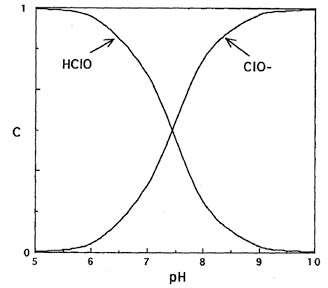
Используя константу равновесия Ka, можно рассчитать мольное долевое распределение хлорноватистой кислоты и гипохлорит-ионов в зависимости от рН (рис.1).
Данные свидетельствуют, что при подкислении растворов гипохлоритов увеличивается доля неустойчивой хлорноватистой кислоты. При рН < 7,58 в растворе присутствует преимущественно хлорноватистая кислота, а при рН > 7,58 существуют преимущественно гипохлорит-ионы.
Рис. 1. Мольное долевое распределение хлорноватистой кислоты и гипохлорит-ионов в зависимости от кислотности среды.
Химические свойства
Гипохлориты являются неустойчивыми соединениями, легко разлагающимися с выделением кислорода. Разложение твердых гипохлоритов натрия и кальция можно представить уравнениями
2NaClO = 2NaCl + O2↑ и 2Сa(ClO)2 = СaCl2 + O2↑.
Процессы при комнатной температуре происходят медленно, а при нагревании могут протекать со взрывом. Параллельно реакциям, сопровождающимся образованием хлоридов и свободного кислорода, могут протекать реакции диспропорционирования
3NaClO = NaClO3 + 2NaCl и 3Сa(ClO)2 = Ca(ClO3)2 + 2СaCl2.
Разложение гипохлоритов в водных растворах зависит от кислотности раствора и его температуры. В сильнокислых средах при рН ≤ 3 хлорноватистая кислота при комнатной температуре разлагается до хлора и кислорода
4HClO = 2Cl2↑ + O2↑ + 2H2O.
Если при подкислении используется соляная кислота или в растворе присутствуют хлориды, образование кислорода не происходит
HClO + HCl = Cl2↑ + H2O.
Хлорноватистая кислота очень слабая, поэтому она может быть вытеснена из раствора ее солей действием углекислого газа
ClO– + CO2 + H2O = HCO3– + HClO.
В слабокислых и нейтральных средах при 3 < рН < 7,5 протекает следующая окислительно-восстановительная реакция
2HClO = 2HCl + O2↑.
В нейтральных и щелочных растворах имеет место конкурирующая реакция образования хлоридов и хлоратов
3ClO– = ClO3– + 2Cl–.
При комнатной температуре реакция диспропорционирования протекает медленно, но при температурах выше 70°С эта реакция становится преобладающей.
В щелочных средах при рН > 7,5 в растворах преобладают гипохлорит-ионы, разлагающиеся следующим образом:
2ClO– = 2Cl– + O2↑.
Стабилизация гипохлоритов в водных растворах. Соли хлорноватистой кислоты значительно устойчивее самой кислоты. С ростом рН уменьшается мольная доля хлорноватистой кислоты в растворе и тем самым повышается стабильность гипохлоритов (рис. 1). В области рН > 11 содержание хлорноватистой кислоты крайне низкое, однако, и при этой кислотности наблюдается медленное разложение соединений хлора(I). Протекающие реакции можно записать в виде:
2ClO– = ClO2– + Cl–, (1)
ClO2– + ClO– = ClO3– + Cl–, (2)
2ClO– = O2 + 2Cl–. (3)
Около 95% от общего количества гипохлорит-ионов разлагается в результате последовательных реакций (1) и (2), причем реакция (1) является самой медленной (лимитирующей) и определяет общую скорость процесса. Реакция (3) не является основной, но отвечает за выделение кислорода, количество которого может быть значительным.
В присутствии некоторых ионов металлов, например, меди, никеля, кобальта наблюдается каталитическое разложение гипохлорит-ионов. Ионы железа обладают слабым каталитическим действием и являются сокатализаторами в сочетании с другими ионами металлов. В простейшем случае, при содержании ионов меди(II) в растворе в концентрации 1мг/кг порядки гомогенной реакции по гипохлориту и по меди(II) равны единице.
Гетерогенный катализ металлами и их нерастворимыми соединениями, является сложным и плохо воспроизводимым. Из нерастворимых катализаторов наибольшее мешающее влияние оказывает никель и его оксиды, которые попадают в растворы гипохлоритов при их контакте с легированными никелевыми сталями, используемыми для изготовления трубопроводов и резервуаров.
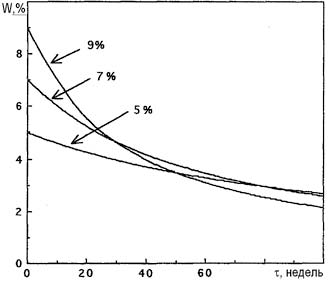
На константы скорости реакций (1)-(3) большое влияние оказывает ионная сила растворов. Высокие концентрации электролитов уменьшают константы скорости реакций и обеспечивают разумную стабильность при хранении растворов электролитов. Увеличение концентрации гипохлорит-ионов, напротив, уменьшает их стабильность в водных растворах. На рис. 2 показан феномен «кривой пересечения». Растворы гипохлорита натрия с концентрацией 9% и 5% при хранении разлагаются настолько, что через 50 недель показывают одинаковую концентрацию вещества, а через 100 недель первоначально более концентрированный раствор содержит гипохлорит-ионов меньше, чем разбавленный.
Рис. 2. Разложение гипохлорита натрия различных концентраций при 30°С.
Повышение температуры способствует ускорению процессов разложения гипохлоритов, поэтому целесообразно хранить растворы гипохлоритов в прохладном месте для обеспечения срока годности (рис. 3).
Рис. 3. Влияние температуры на разложение 5%-ного раствора NaClO.
Для стабилизации водных растворов гипохлоритов, а так же продуктов на их основе, каждый производитель применяет собственные методы, которые редко публикуются в виде статей. Однако известны некоторые запатентованные методы, которые, не претендуя на полноту, можно представить следующим списком:
- удаление хлорид-ионов, сопутствующих гипохлорит-ионам, методом кристаллизации;
- приготовление хлорноватистой кислоты, свободной от хлорид-ионов, методами электродиализа, дистилляции и жидкостной экстракции с последующей нейтрализацией щелочью;
- добавление многоатомных спиртов (например галактита, маннита, сорбита, инозита и пентаэритрита);
- добавление амидов;
- осаждение и фильтрация после добавления соединений щелочноземельных металлов;
- добавление перйодатов или перйодат-образующих соединений, способных образовывать комплексы с ионами металлов – катализаторов разложения гипохлоритов;
- добавление силикатов совместно с добавками или без добавок;
- добавление бромидов;
- добавление арилсульфаниламидов или их производных;
- увеличение светостойкости гипохлоритов путем добавления солей имидодисульфатов; солей церия и ЭДТА; феррицианидов; изоциануровой кислоты и цитрата натрия;
- добавление избытка хлорида железа с последующей фильтрацией;
- добавление гептоната натрия или боргептоната натрия;
- добавление 2-оксазолидинонов;
- добавление фосфата натрия;
- добавление бихромата калия;
- добавление солей кальция;
- добавление полидентатных гетероароматических соединений.
Направление окислительно-восстановительных процессов с участием гипохлорит-ионов и хлорноватистой кислоты обусловлены значениями стандартных электродных потенциалов полуреакций в водной среде:
в кислой среде
2HClO + 2H+ + 2e– = Cl2↑ + 2H2O, E° = 1,630 В,
HClO + H+ + 2e– = Cl– + H2O, E° = 1,500 В.
в нейтральной и щелочной среде
ClO– + H2O + 2e– = Cl– + 2OH–, E° = 0,890 В,
2ClO– + 2H2O + 2e– = Cl2↑ + OH–, E° = 0,421 В.
Таким образом, гипохлорит-ионы и хлорноватистая кислота обладают выраженными окислительными свойствами, причем их окисляющая способность в кислой среде значительно выше, чем в нейтральной и щелочной средах.
Дезинфицирующее действие
Гипохлориты являются одними из лучших антибактериальных средств. Они убивают микроорганизмы очень быстро даже при очень низких концентрациях.
Наивысшее бактерицидное действие гипохлоритов проявляется в нейтральной среде, когда концентрации хлорноватистой кислоты и гипохлорит-ионов приблизительно равны (рис. 1). Образующиеся при разложении гипохлоритов активные частицы (атомарный кислород и хлор) обладают высоким биоцидным действием. Они уничтожают микроорганизмы, взаимодействуя с биополимерами в их структуре, способными к окислению. Аналогичным образом, например, действуют клетки человека нейтрофилы, гепатоциты и др., которые синтезируют хлорноватистую кислоту и сопутствующие высокоактивные радикалы для борьбы с микроорганизмами и чужеродными субстанциями.
Бактерицидная активность гипохлоритов настолько велика, что они способны привести к гибели дрожжеподобных грибов, вызывающих кандидоз, Candida albicans, в течение 30 секунд при действии 5,0 – 0,5%-го гипохлоритного раствора. Патогенный Enterococcus faecalis погибает через 30 секунд после обработки 5,25%-ым раствором и через 30 минут после обработки 0,5%-ым раствором. Грамотрицательные анаэробные бактерии, такие как Porphyromonas gingivalis, Porphyromonas endodontalis и Prevotella intermedia, погибают в течение 15 секунд после обработки 5,0 – 0,5%-м раствором гипохлорит-ионов.
Несмотря на высокую биоцидную активность гипохлоритов, некоторые потенциально опасные простейшие организмы, например, возбудители лямблиоза или криптоспоридиоза, к сожалению, устойчивы к его действию.
При помощи гипохлорит-ионов можно успешно обезвреживать различные токсины (табл. 3).
Таблица 3. Результаты инактивации токсинов при 30-минутной экспозиции различных концентраций гипохлорита натрия («+» – токсин инактивирован; «–» – токсин остался активен).
| Токсин | 2,5% NaClO + 0,25 н. NaOH | 2,5% NaClO | 1,0% NaClO | 0,1% NaClO |
|---|---|---|---|---|
| Т-2 токсин | + | – | – | – |
| Бреветоксин | + | + | – | – |
| Микроцистин | + | + | + | – |
| Тетродотоксин | + | + | + | – |
| Сакситоксин | + | + | + | + |
| Палитоксин | + | + | + | + |
| Рицин | + | + | + | + |
| Ботулотоксин | + | + | + | + |
Методы анализа
Качественными реакциями на гипохлорит-ион могут служить:
- окисление йодид-иона до йода в сильнокислой среде;
- выпадение коричневого осадка метагидроксида таллия(III) (TlO(OH)) при действии щелочного раствора соли таллия (I);
- цветная реакция с 4,4´-тетраметилдиаминодефенилметаном или N,N´-диокситрифенил метаном в присутствии бромата калия.
Наиболее распространенным методом количественного анализа гипохлорит-иона является титриметрический метод с использованием йодида калия. Для проведения испытания водный раствор или водную суспензию, содержащие гипохлорит-ион, смешивают с избытком раствора йодида калия в сернокислой среде. Выдерживают герметично закрытую смесь в течение 5 минут в темном месте. Выделившийся йод титруют стандартизированным раствором тиосульфата натрия. В качестве индикатора вблизи точки эквивалентности используют крахмальный раствор.
При количественном определении гипохлорит-иона косвенным йодометрическим методом результаты анализа пересчитывают на концентрацию «активного хлора» в ыделившегося при реакции
2H+ + ClO– + Cl– = Cl2↑ + H2O.
Альтернативным методом количественного определения гипохлорит-иона является потенциометрический анализ с использованием бром-ионселективного электрода. Концентрацию гипохлорит-иона находят методом добавок анализируемого раствора к стандартному раствору или методом уменьшения концентрации анализируемого раствора при его добавлении к стандартному раствору.
Способы получения наиболее важных товарных продуктов
Крупнотоннажными гипохлоритсодержащими продуктами являются гипохлорит натрия и гипохлорит кальция. Их глобальный объем производства превышает 1 млн тонн/год. При этом почти половина этого объема используется в быту, а другая половина в промышленности. Гипохлорит калия, являющийся исторически первым гипохлоритом, нашедшим промышленное применение, производится в ограниченном количестве.
Для промышленного производства гипохлорита натрия используются химический и электрохимический методы. При химическом методе производится хлорирование водных растворов гидроксида натрия. Суть химического превращения не изменилась со времен его открытия и применения Лабарраком
Cl2 + 2NaOH = NaClO + NaCl + H2O.
Существуют две производственные схемы данного метода:
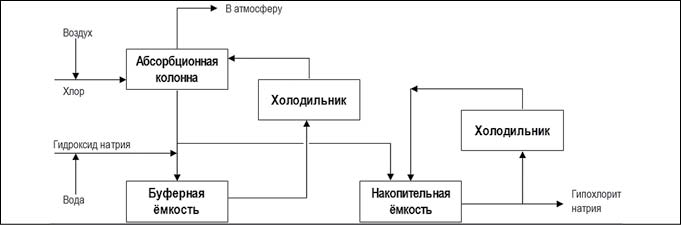
- основной процесс, в результате которого производится 16%-ный раствор гипохлорита натрия в смеси с хлоридом натрия и гидроксидом натрия (рис. 4).
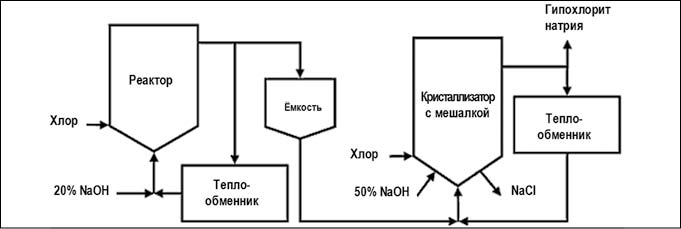
- низко-солевой или концентрированный процесс позволяет получить концентрированные растворы (25–40%) гипохлорита натрия с меньшим содержанием примесей. Его отличие от основного способа заключается в добавлении второй стадии хлорирования. Во второй реактор подается не гидроксид натрия, а раствор гипохлорита натрия из первого реактора, в результате происходит концентрирование готового продукта (рис. 5).
Рис. 4. Химический метод получения гипохлорита натрия основным процессом (рис. с сайта https://ru.wikipedia.org)
Рис. 5. Химический метод получения гипохлорита натрия концентрированным процессом (рис. с сайта https://ru.wikipedia.org)
При электрохимическом методе получения гипохлорита натрия водный раствор хлорида натрия подвергается электролизу в электролизере с открытыми электродными зонами (бездиафрагменный способ). Гидроксид натрия, образующийся на катоде, и хлор, выделяющийся на аноде, беспрепятственно смешиваются в ходе электрохимического процесса
NaCl + H2O = NaClO + H2↑(суммарная реакция).
Гипохлорит кальция производится в виде хлорной извести, представляющей собой смесь целевого продукта с хлоридом кальция и гидроксидом кальция. В качества сырья для получения хлорной извести используется порошкообразный гидроксид кальция (пушенка), содержащий менее 1% свободной влаги и разбавленный влажным воздухом хлор. Небольшая влажность исходных веществ обеспечивает начало реакции гидролиза хлора, сопровождающейся нейтрализацией образующихся кислот известью. Затем реакция продолжается за счет воды, выделяющейся из гидроксида кальция при хлорировании
2Сa(OH)2 + 2Cl2 = Сa(ClO)2 + СaCl2 + 2H2O (суммарно).
Хлорирование пушенки осуществляется в аппаратах непрерывного действия – механических полочных камерах Бакмана.
Таблица 4. Производители гипохлорита натрия в России.
| Название предприятия | Сайт предприятия |
|---|---|
| «Каустик» ЗАО, г. Стерлитамак | www.kaus.ru/ |
| «Каустик» ОАО, г. Волгоград | www.kaustik.ru/ |
| «Новомосковский хлор» ООО, г. Новомосковск | www.hlor.biz/ |
| «Сода-хлорат» ООО, г. Березняки | www.soda.perm.ru/ |
Характеристика товарных гипохлоритов, обращение, хранение и транспортировка
В Российской Федерации гипохлориты производятся в соответствии с ГОСТ 11086–76 «Гипохлорит натрия. Технические условия» и ГОСТ 1692–85 «Известь хлорная. Технические условия». Гипохлорит натрия по назначению и показателям выпускается двух марок «А» и «Б» (табл. 5).
Таблица 5. Физико-химические показатели и назначение гипохлорита натрия по ГОСТ 11086–76
| Наименование показателя |
Марка А |
Марка Б |
|---|---|---|
| Внешний вид |
Жидкость зеленовато-желтого цвета |
|
| Коэффициент светопропускания, % не менее |
20 |
20 |
| Массовая концентрация активного хлора, г/дм3, не менее |
190 |
170 |
| Массовая концентрация щелочи в пересчете на NaOH, г/дм3 |
10–20 |
40–60 |
| Массовая концентрация железа, г/дм3, не более |
0,02 |
0,06 |
| Область применения |
В химической промышленности для обеззараживания питьевой воды и воды плавательных бассейнов, для дезинфекции и отбелки |
В витаминной промышленности как окислитель и для отбеливания ткани |
Гипохлорит натрия должен храниться в специальных полиэтиленовых, стальных гуммированных или других, покрытых коррозионно-стойкими материалами ёмкостях, наполненных на 90% объёма и оборудованных воздушником для сброса образующегося при распаде кислорода. Емкости с гипохлоритом натрия хранят в защищённых от света закрытых складских неотапливаемых помещениях. Перевозка продукции осуществляется в соответствии с правилами транспортировки опасных грузов.
Хлорная известь в зависимости от способа получения выпускается двух марок «А» и «Б» и трех сортов для каждой марки (табл. 6).
Таблица 6. Физико-химические показатели и способ получения хлорной извести по ГОСТ 1692–85
|
Наименование показателя |
Марка А | Марка Б | ||||
| 1-й сорт | 2-й сорт | 3-й сорт | 1-й сорт | 2-й сорт | 3-й сорт | |
|
Внешний вид |
Порошок белого цвета или слабоокрашенный, с наличием комков |
|||||
|
Массовая концентрация активного хлора, %, не менее |
28 | 25 | 20 | 35 | 32 | 27 |
|
Коэффициент термостабильности, не менее |
0,90 | 0,90 | 0,80 | 0,75 | 0,70 | 0,60 |
|
Способ получения |
Хлорирование пушенки в кипящем слое | Хлорирование пушенки в аппаратах Бакмана |
Хлорную известь упаковывают в полиэтиленовые мешки и стальные барабаны, окрашенные со всех сторон химически стойкой краской. Хлорную известь хранят в закрытых складских неотапливаемых, затемненных и хорошо проветриваемых помещениях. Не допускается хранение с хлорной известью взрывчатых веществ, огнеопасных грузов и баллонов со сжатыми газами. Гарантийный срок хранения хлорной извести марки А 1-го и 2-го сортов – 3 года со дня изготовления, марки А 3-го сорта и марки Б – 1 год со дня изготовления. Перевозка продукции осуществляется в соответствии с правилами транспортировки опасных грузов.
Требования безопасности
Гипохлориты являются окислителями, вызывающими раздражение кожных покровов и слизистых оболочек. Гипохлориты при попадании на кожу могут вызвать ожоги, а при попадании в глаза – слепоту. При попадании гипохлоритов на кожные покровы необходимо обмывать их обильной струей воды в течение 10–15 мин. При попадании гипохлоритов в глаза следует немедленно промыть их обильным количеством воды и направить пострадавшего к врачу. Приём внутрь разбавленных растворов (3 – 6%) гипохлоритов приводит обычно только к раздражению пищевода и иногда ацидозу, в то время как концентрированные растворы способны вызвать довольно серьёзные повреждения, вплоть до перфорации желудочно-кишечного тракта. При работе с гипохлоритами следует иметь специальные средства защиты: защитные очки, резиновые сапоги, резиновые перчатки, фартук из прорезиненной ткани и противогаз, а также использовать специальную одежду.
Несмотря на свою высокую химическую активность, безопасность гипохлоритов для человека документально подтверждена исследованиями токсикологических центров Северной Америки и Европы. Результаты показывают, что гипохлориты не являются мутагенными, канцерогенными и тератогенными соединениями, а также кожными аллергенами. Международное агентство по изучению рака пришло к выводу, что питьевая вода, прошедшая обработку гипохлоритом натрия, не содержит человеческих канцеро- генов.
При нагревании выше 35°С растворы гипохлоритов разлагаются с образованием хлоратов и выделением кислорода. Слабощелочной раствор достаточно устойчив. Растворы гипохлоритов негорючи и невзрывоопасны. Однако в процессе высыхания гипохлориты могут вызвать загорание органических продуктов и горючих веществ. При взаимодействии гипохлоритов с кислотами выделяется токсичный хлор (раздражающий и удушающий эффект), поэтому не допускается смешение и совместное хранение данных веществ.
При работе с гипохлоритами производственные помещения должны быть оборудованы приточно-вытяжной вентиляцией. Оборудование должно быть герметичным. Негерметичные узлы должны быть снабжены местными вентиляционными отсосами.
Применение в средствах бытовой химии
Применение гипохлоритов в средствах бытовой химии обусловлено их окислительными и дезинфицирующими свойствами. Гипохлориты являются основными действующими веществами в химических отбеливателях, пятновыводителях, средствах для обеззараживания воды в бассейнах, в чистящих и моющих средствах с дезинфицирующим эффектом.
Отбеливатели
Мировое производство гипохлорита натрия оценивается в 5 миллионов тонн. Более половины всего производимого гипохлорита натрия используется в качестве отбеливателя и пятновыводителя для тканей. Гипохлорит натрия может быть использован для многих видов тканей, включая хлопок, полиэстер, нейлон, ацетат, лен, вискозу и другие. Он эффективен для удаления следов почвы и широкого спектра пятен, в том числе, от кофе, крови, травы, горчицы, ягодных и фруктовых соков и т.д.
Содержание гипохлорита натрия в отбеливателях и пятновыводителях для тканей обычно находится в диапазоне от 2,5 до 10%. В большинстве случаев эти средства выпускаются в жидкой форме в пластиковых бутылках или канистрах. Дополнительными компонентами отбеливателей являются поверхностно-активные вещества, модификаторы реологии, оптические отбеливатели, стабилизаторы разложения и др.
Преимуществами отбеливателей на основе гипохлоритов являются:
- быстрое и качественное отбеливание;
- использование отбеливателя без нагревания и даже в холодной воде;
- доступная цена;
- более удобная форма выпуска: не «пылят», в отличие от порошков и легко дозируются;
- многофункциональность, так как помимо отбеливания и удаления пятен подходят для дезинфекции различных поверхностей.
Недостатками отбеливателей на основе гипохлоритов являются:
- активное использование хлорсодержащих отбеливателей приводит к тому, что ткани быстрее изнашиваются и, как следствие, легко рвутся;
- невозможность отбеливания шёлковых, шерстяных и некоторых синтетических волокон из-за интенсивного разрушения;
- относительно короткий срок хранения;
- невозможность использования в автоматической стиральной машине, особенно в сочетании с современными порошками;
- сильный специфичный запах хлора.
Моющие и чистящие средства с дезинфицирующими свойствами
Гипохлориты используются во многих жидких и порошкообразных средствах:
- для автоматических посудомоечных машин;
- для ухода за ванными комнатами, душевыми и туалетами;
- для очистки кухонных плит;
- для мытья каменных и бетонных полов;
- для очистки коптилен и грилей;
- очистки канализационных сливов;
- для уборки поверхностей в кухнях и столовых и др.
Эффективность очистки средствами, содержащими гипохлорит-ионы, обусловлена их сильным окисляющим действием. При деструкции крупных молекул загрязнителей образуются низкомолекулярные продукты разложения, характеризующиеся высокой растворимостью, отсутствием окраски и запаха. Одновременно с очищающим действием, гипохлориты проявляют высокую дезинфицирующую способность. В целом эффективность гипохлоритов возрастает с увеличением концентрации и температуры раствора, а так же при понижении кислотности раствора.
Гипохлоритсодержащие средства с дезинфицирующими свойствами обладают следующими достоинствами:
- эффективны в отношении различных бактерий, грибов и вирусов;
- дезинфицирующая активность мало зависит от жесткости воды;
- при использовании не образуют побочных токсичных продуктов;
- выпускаются в жидкой, порошкообразной и гранулированной формах.
К недостаткам можно отнести:
- нестабильность и потерю активности с увеличением температуры и при взаимодействии с органическими веществами;
- снижение биологической активности с увеличением кислотности среды;
- коррозия нержавеющей стали и других металлов, что допускает лишь кратковременный контакт с поверхностями и оборудованием из металлов;
- потеря активности при хранении на свету;
- ограниченный перечень поверхностно-активных веществ, комплексообразователей, красителей, отдушек, способных быть устойчивыми в композиции моющего или чистящего средства, содержащего гипохлориты.
В заключение следует отметить, что рост производства и потребления гипохлоритов составляет более 2,5% ежегодно. Причем более половины всех произведенных гипохлоритов используется для бытовых целей, а менее половины для промышленных. Широкое использование гипохлоритов в средствах бытовой химии стало возможным благодаря их коммерческой доступности и высокой эффективности. Гипохлорит натрия является безусловным лидером среди других солей хлорноватистой кислоты, занимая 91% мирового рынка. Почти 9% остается за гипохлоритом кальция. Использование гипохлорита калия имеет историческое значение, однако, объемы его современного применения незна- чительные.
Источники
- Handbook of detergents. Part A: Properties/ Edited by Guy Broze. New York: Marsell Dekker, 1999. 809 p.
- Фурман Л. А. Хлорсодержащие окислительно-отбеливающие и дезинфицирующие вещества. М.: Химия, 1976. 88 с.
- Ушакова В.Н. Мойка и дезинфекция. Пищевая промышленность, торговля, общественное питание. – СПб.: Профессия, 2009. 288 с.
- ГОСТ 1692–85. Известь хлорная. Технические условия.
- ГОСТ 11086–76. Гипохлорит натрия. Технические условия.
- Лидин Р.А. и др. Константы неорганических веществ: справочник / Под ред. проф. Р.А. Лидина. М.: Дрофа, 2000. 480 с.
- Химическая энциклопедия/ Гл. ред. И.Л. Кнунянц. М.: Советская энциклопедия, 1992. Т. 3. 555 с.
- Вредные вещества в промышленности. Справочник для химиков, инженеров и врачей/ Под ред. проф. Н.В. Лазарева и проф. И.Д. Гадаскиной. Л.: Химия, 1977. Т. 3. 608 с.
- https://ru.wikipedia.org/wiki/Гипохлорит_натрия
Дезинфекции всегда должна предшествовать стадия очистки поверхности. Пищевые загрязнения, оставшиеся на плохо очищенной поверхности, являются источниками питания и очагами роста микроорганизмов. Хорошее санитарно-гигиеническое состояние на пищевом предприятии достигается комбинированной программой тщательной очистки всех поверхностей и оборудования с последующей дезинфекцией. Известно, что при тщательной очистке с поверхности удаляется до 90% микроорганизмов. На недомытой поверхности остатки загрязнений не только защищают микроорганизмы от санитарной обработки, но и снижают эффективность дезинфицирующего средства за счет эффекта разбавления или химической реакции органического вещества с дезинфектантом.
Химические соединения, предназначенные для использования в пищевой промышленности в качестве дезинфектантов, отличаются химической структурой, активностью против различного вида микроорганизмов и условиями, при которых они проявляют максимальную активность. В общем, случае справедлива закономерность – чем выше концентрация дезинфицирующего средства, тем быстрее и эффективнее его действие. Чтобы выбрать эффективное дезинфицирующее средство, нужно экспериментальным или теоретическим путем определить потенциальные патогенные микроорганизмы и убедиться в том, что, выбранный дезинфектант активен в отношении этих микроорганизмов. Поскольку химические дезинфектанты не обладают высокой проникающей способностью, микроорганизмы в трещинах, царапинах и других неровностях поверхности, внутри минеральных загрязнений могут быть не полностью уничтожены после обработки. Чтобы действие химических дезинфектантов было эффективно, поверхность перед обработкой должна быть тщательно очищена.
Эффективность обработки зависит от ряда физико-химических факторов:
- время экспозиции. Исследования показали, что гибель популяции микроорганизмов носит логарифмический характер: 90% микроорганизмов гибнет в определенный интервал времени, 90% оставшихся организмов гибнет в следующий интервал времени, при этом остается лишь 1% от первоначального количества микроорганизмов. Время экспозиции зависит от эффективности воздействия дезинфицирующего средства на данный вид микроорганизмов, способности к образованию спор и других физико-химических факторов.
- температура. С увеличением температуры возрастают скорости роста микроорганизмов и их гибели вследствие действия химических дезинфицирующих средств. Увеличение температуры приводит к снижению поверхностного натяжения, вязкости и изменению ряда других параметров, которые способствуют гибели микроорганизмов.
- концентрация. С увеличением концентрации дезинфицирующего средства возрастает скорость гибели микроорганизмов.
- показатель pH . Активность антимикробных соединений, как правило, зависит от показателя pH среды. Например, хлор и йод содержащие дезинфицирующие средства теряют свою активность с увеличением показателя pH среды.
- жесткость воды. С увеличением концентрации солей жесткости воды снижается биологическая активность дезинфицирующих средств, в результате их взаимодействия с солями жесткости воды. Например, четвертичные аммониевые соединения не совместимы с солями кальция и магния. При жесткости воды выше 200 ppm дезинфицировать поверхность четвертичными аммониевыми соединениями без добавления комплексообразователей, смягчающих воду, бесполезно.
- чистота поверхности и оборудования. Многие дезинфицирующие вещества – гипохлорит, йодофоры и многие другие химические дезинфектанты взаимодействуют с органическими соединениями, оставшимися на плохо очищенной поверхности, и теряют свою биологическую активность. Характеристики идеального дезинфектанта.
Идеальный дезинфектант должен обладать следующими свойствами
- высокой биологической активностью против вегетативных бактерий, грибов, дрожжей, обеспечивающей быструю гибель микроорганизмов;
- устойчивостью к окружающей среде (быть эффективным в жесткой воде, в присутствии остатков органических соединений, остатков моющих средств);
- отсутствием токсичности и кожно-раздражающего действия;
- отсутствием запаха;
- стабильностью в концентрированном виде и виде рабочего раствора;
- легкостью в использовании;
- доступностью;
- доступной ценой;
- легкостью идентификации во время использования.
К сожалению, идеальное дезинфицирующее средство, удовлетворяющее одновременно всем выше перечисленным параметрам пока не создано. На практике следует выбирать дезинфектант с высокой биологической активностью против микроорганизмов, которые есть или теоретически могут появиться на предприятии. От правильного выбора дезинфицирующего средства и соблюдения санитарно-гигиенических правил обработки поверхностей и оборудования будет зависеть безопасность произведенных продуктов питания.
Классификация химических дезинфицирующих веществ.
Дезинфицирующие средства классифицируют по их действию на различные формы микроорганизмов: бактерициды уничтожают вегетативные микроорганизмы, спороциды уничтожают споры, фунгициды уничтожают грибы, вируциды уничтожают вирусы. Химические антисептики используются для дезинфекции кожи. Бактериостатические вещества препятствуют размножению бактерий, фактически их не уничтожая.
Химические соединения воздействуют на клетку несколькими способами. Один из них — коагуляция протеина. В обычном состоянии протеин диспергирован внутри клетки. Дезинфицирующее соединение взаимодействует с протеином, вызывая его коагуляцию и выпадение в осадок. Клетка перестает функционировать в нормальном режиме и погибает. Еще один способ воздействия дезинфицирующего вещества на микроорганизмы – разрушение мембраны клетки. Мембрана клетки работает как избирательный барьер, одни растворы она пропускает внутрь клетки, другие растворы не могут преодолеть этот барьер. Вещества, которые сорбируются на клеточной мембране, могут заметно изменить ее физико-химические характеристики, препятствуя нормальному функционированию. Это может привести к ингибированию активности или к гибели клетки.
Химический антагонизм. Ферменты выполняют свою каталитическую функцию благодаря их сродству с некоторыми химическими соединениями, которые называют природными субстратами. Природные субстраты в стандартном режиме находятся внутри клетки. Если природные субстраты в заметном количестве заменяются дезинфектантом, фермент будет связан с химическим веществом, а не субстратом. В случае образования достаточно устойчивой связи фермент — химический дезинфектант клетка теряет способность к размножению.
Обычно химические дезинфицирующие вещества классифицируют по типу биологически-активного вещества, входящего в его состав.
Хлор-содержащие дезинфицирующие средства.
Жидкий хлор, гипохлорит, хлорамин, диоксид хлора являются дезинфицирующими агентами. Они различаются по своей антимикробной активности. Хлор в газообразном состоянии (Cl2) вводят в воду и получают антимикробный агент — хлорноватистую кислоту (НОСl). НОСl диссоциирует в воде с образованием иона водорода Н+ и иона гипохлорита (OCl— ).
Жидким хлором называют раствор гипохлорита натрия в воде (NaOCl), это наиболее распространенная форма дезинфицирующего средства на основе хлора. Следует отметить, что хлорноватистая кислота в 80 раз активнее в качестве дезинфицирующего агента, чем гипохлорит ион. Считается, что механизм антимикробного действия хлорсодержащих соединений заключается в окислении аминокислот мембраны клетки, разрушении мембраны, прерывании синтеза протеина, ингибировании поглощения кислорода клетки и т.д. Некоторые соединения хлорамина более активны против ряда микроорганизмов, чем гипохлориты. Например, дихлороизоцианурат натрия более активен, чем гипохлорит натрия против таких бактерий, как E.coli, S.aureus и некоторых других.
В последние годы возрос интерес к дезинфицирующим средствам на основе диоксида хлора (ClO2). Диоксид хлора в 2.5 раза активнее, чем гипохлорит натрия в качестве окислителя. Диоксид хлора наиболее активен при рН=8.5.
Один из способов получения диоксида хлора можно представить следующим образом:
5NaClO2 + 4HCl → 4ClO2 + 5NaCl + 2H2O
NaOCl + HCl → NaCl + HOCl
HOCl + 2NaClO2 → ClO2 + 2NaCl + H2O
Используя эти химические реакции, можно непосредственно в пенной пушке или пеногенераторе получать пену, содержащую 5 ppm диоксида хлора. Диоксид хлора активен против широкого спектра микроорганизмов, в том числе спорообразующие бактерии и вирусы. Его действие на микроорганизмы заключается в ингибировании воспроизведения микроорганизмов, поскольку диоксид хлора является сильным окислителем.
Когда хлорсодержащие соединения используют для обработки поверхностей, уничтожаются клетки вегетативных и спорообразующих бактерий. Вегетативные клетки уничтожить легче, чем споры Clostridium, которые в свою очередь легче уничтожить, чем споры Bacillius. Хлорсодержащие соединения в концентрации 50 ppm обладают слабой активностью в отношении Listeria monocytogenes, концентрации выше 50 ppm хлорсодержащие соединения эффективны в отношении этого патогенного микроорганизма. В целом эффективность хлорсодержащих соединений возрастает с увеличением концентрации и температуры раствора и понижением значения pH. Следует отметить, что с увеличением температуры увеличивается и скорость коррозии металлов, если обрабатывается металлическая поверхность.
К достоинствам хлорсодержащих соединений следует отнести:
- эффективность в отношении различных бактерий, грибков и вирусов;
- доступность в жидкой и гранулированной форме;
- соли жесткости воды оказывают слабое влияние на активность;
- при использовании хлорсодержащих соединений не происходит образования токсичных побочных продуктов;
Хлорсодержащие соединения обладают меньшей коррозионной способностью, чем жидкий хлор.
К недостаткам хлорсодержащих соединений следует отнести:
- нестабильность и потеря активности с увеличением температуры и при взаимодействии с органическими веществами;
- снижение биологической активности с увеличением показателя pH среды.
- коррозия нержавеющей стали и других металлов, что допускает лишь кратковременный контакт с поверхностями и оборудованием из металлов;
- теряют активность при хранении на свету и использовании при температурах выше 60ºС
- в области низких значений pH (pH <4.0) может происходить образование токсичного газа Cl2, обладающего сильным коррозионным действием;
- при высоких концентрациях в жидких формах могут быть взрывоопасными.
Йод содержащие соединения.
Соединения йода используются для дезинфекции поверхностей и оборудования, а также в качестве кожных антисептиков. Йодофоры используют также как соединения хлора в водоподготовке. Оказалось, что двухатомный йод J2 является самым активным антимикробным агентом из йодсодержащих соединений. Его активность проявляется в том, что он разрушает связи, удерживающие протеины в клетке вместе и ингибирует синтез протеинов. Свободный элементарный йод и йодноватистая кислота проявляют высокую активность в уничтожении микроорганизмов. В качестве дезинфицирующих агентов используют спиртосодержащие соединения йода и соединения на водной основе, эти растворы также используют в качестве кожных антисептиков. Активными в отношении микроорганизмов формами являются J2 и иодноватистая кислота НОJ.
Йодофорами называют комплексы элементарного йода J с неионогенными ПАВ, например нонилфенолэтиленоксидом, или комплекс йода с полимером – поливинилпирролидоном в водном растворе. Йодофоры чаще других йод содержащих соединений используются в качестве дезинфицирующих агентов. Поскольку активность в отношении микроорганизмов увеличивается с понижением значения pH, йодофоры комбинируют с фосфорной кислотой. Сочетание йодофоров с поверхностно-активными веществами и кислотами придает им моющие свойства. Такие средства обладают одновременно моющими и дезинфицирующими свойствами, они обладают лучшей растворимостью в водных растворах, чем суспензии или водные растворы йода. Они не обладают запахом и кожно-раздражающим действием.
Поведение комплекса ПАВ-йод можно объяснить химическим равновесием:
R + J2 ↔ RJ + HJ, R — неионогенное ПАВ
Количество доступного свободного йода определяет биологическую активность йодофора. Спорообразующие бактерии более устойчивы к действию йодофоров, чем вегетативные, и времена экспозиции, приведенные в таблице 4.1, в 10 -1000 раз больше, чем времена экспозиции, необходимые для аналогичного воздействия на вегетативные клетки. Активность йод содержащих веществ по своему действию на вегетативные клетки сравнима с хлор содержащими дезинфектантами, однако действие йодофоров на спорообазующие бактерии слабее. Йод содержащие дезинфицирующие агенты более устойчивы к воздействию органических веществ, чем хлор содержащие. Йодофоры обычно используют в концентрациях 12.5 – 25 ppm. Йодофоры более активны против Tubercule bacillus и других вирусов, чем остальные дезинфицирующие агенты. Йод содержащие соединения проявляют максимальную активность в области значений pH 2.5 – 3.5. Йодофоры в виде концентрированных и стабилизированных растворов имеют длительные сроки хранения. В разбавленных растворах йод имеет тенденцию к испарению, особенно активно этот процесс протекает при температуре выше 50ºС.
Таблица 1 Инактивация спорообразующих бактерий. Тесты проведены в дистиллированной воде при Т=15-20ºС.
|
Микроорганизм |
Показатель рН |
Концентрация, ppm |
Время снижения числа микроорганизмов на 90%, мин. |
|
Bacillus cereus |
6.5 |
50 |
10 |
|
6.5 |
25 |
30 |
|
|
2.3 |
25 |
30 |
|
|
Bacillus subtilis |
— |
25 |
5 |
|
Clostridium botulinum A |
2.8 |
100 |
6 |
Материалы из пластмасс и резины способны адсорбировать соединения йода, что может привести к появлению пятен. В желтый цвет соединения йода окрашивают и органические загрязнения, этот эффект можно использовать для контроля остатков пищевых загрязнений на поверхностях.
Растворы йодофоров имеют кислый характер, поэтому они эффективны в жесткой воде, не способствуя при этом удалению минеральных отложений. Многие органические вещества, особенно молоко и молочные продукты инактивируют дезинфектанты на основе соединений йода.
К недостаткам дезинфицирующих агентов на основе соединений йода следует отнести невысокую активность против спорообразующих бактерий и бактериофагов, а также слабую биологическую активность при низких температурах. При температурах выше 50ºС.
Четвертичные аммониевые соединения.
Четвертичные аммониевые соединения часто используют для обработки полов, стен, мебели и оборудования. Эти соединения являются поверхностно-активными веществами и обладают хорошей смачивающей способностью. Невысокая моющая способность четвертичных аммониевых соединений при великолепной антимикробной активности предопределило их использование в качестве дезинфицирующих средств. Например, четвертичные аммониевые соединения обладают высокой активностью против L.monocytogenes и плесневых грибов.
В четвертичных аммониевых соединениях азот, соединенный с четырьмя органическими радикалами имеет положительный заряд:
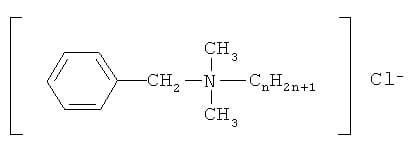
Механизм воздействия четвертичных аммониевых соединений на микроорганизмы отличается от соединений хлора и йода. Дезинфицирующие агенты на основе четвертичных аммониевых соединений образуют бактериостатическую пленку на поверхности. Эти соединения селективно убивают патогенные микроорганизмы. Они не убивают спорообразующие бактерии, однако ингибируют их рост. Четвертичные аммониевые соединения обладают большей стабильностью в присутствии органических соединений по сравнению с хлор и йод содержащими дезинфектантами, однако присутствие органических веществ может привести к снижению их активности. Как правило, в состав дезинфицирующих веществ на основе четвертичных аммониевых солей входят диметилбезиламмонийхлорид, диметилэтилбензиламмонийхлорид, оба соединения не теряют активности в воде с содержанием солей жесткости от 500 до 1000 ppm, даже без добавления комплексообразующих агентов. В концентрациях, в которых четвертичные аммониевые соли используются для дезинфекции оборудования и поверхностей они не являются токсичными, не обладают кожно-раздражающим действием, не вызывают коррозию металлов, что является большим преимуществом по сравнению с хлор — содержащими соединениями. Следует иметь в виду, что четвертичные аммониевые соединения инактивируются анионными ПАВ, поэтому их можно комбинировать или использовать совместно только с определенными классами ПАВ – катионными и амфотерными.
К преимуществам дезинфектантов на основе четвертичных аммониевых солей следует отнести – бесцветность и отсутствие запаха, стабильность в присутствии органических веществ, отсутствие коррозии металлов, стабильность в широком интервале температур, отсутствие кожно-раздражающего действия, эффективность при высоких значениях pH, высокая активность в отношении плесневых грибов, отсутствие токсичности.
К недостаткам четвертичных аммониевых оснований следует отнести потерю активности в присутствии анионных ПАВ, пленкообразование на пищевом оборудовании и поверхностях, а также слабую активность в отношении грам-отрицательных бактерий за исключением Salmonella и E.coli. Активность в отношении грам-отрицательных бактерий усиливают, комбинируя четвертичные аммониевые соли с другими дезинфицирующими агентами.
Учитывая выше приведенные сведения, компания НПФ Химитек разработала и выпускает дезинфицирующее средство ХИМИТЕК УНИВЕРСАЛ-ДЕЗ. В качестве действующего вещества продукт содержит в составе четвертичное аммонийное соединение (ЧАС) нового поколения – дидецилдиметиламмоний хлорида, который внесён в Реестр Биоцидной продукции по Регламенту №(EU) 528/2012.
Рабочие растворы средства обладают стабильностью в жёсткой воде, а также не теряет активности при наличии на поверхности органических загрязнений и остаточных количеств ПАВ. На практике это означает: если предварительная очистка поверхности проведена не очень тщательно, эффективность дезинфектанта не снижается. Рабочие растворы средство обладают активностью против грамположительных и грамотрицательных бактерий, дрожжеподобных грибов и дрожжей — специфической микрофлоры предприятий пищевой промышленности и общественного питания. Средство не проявляет коррозионную активность, т.е. не повреждает объекты и поверхности из любых материалов. Обладают широкой областью применения: можно обеззараживать всё — от яичной скорлупы до мусоровозов. Обладает моющей способностью и высокой стабильность растворов при хранении.
Дезинфектанты на основе кислот
Дезинфицирующие вещества на основе кислот считаются токсикологически безопасными и биологически активными. Их используют в ополаскивающих и дезинфицирующих составах. Чаще всего используют органические кислоты, такие как уксусная, надуксусная, молочная, пропионовая и муравьиная. Присутствие кислот в ополаскивающих составах позволяет нейтрализовать и удалить остатки щелочных моющих и дезинфицирующих веществ. Действие кислотосодержащих дезинфицирующих веществ основано на взаимодействии и разрушении мембраны клетки. Появление технологий автоматической мойки, в которых последнюю стадию ополаскивания желательно комбинировать с дезинфекцией, вызвало появление большого количества дезинфицирующих продуктов на основе кислот. Эти продукты, как правило, используют в заключительной стадии обработки оборудования – ополаскивания и дезинфекции, после чего оборудование оставляют на ночь с минимальным риском микробного обсеменения. Требования к таким продуктам – отсутствие коррозионной способности по отношению к металлам.
На активность дезинфицирующих веществ на основе кислот может повлиять изменение pH среды, pH <3 — наиболее благоприятная среда для таких продуктов. В отличие от йодофоров соли жесткости воды не оказывают заметного влияния активность кислотосодержащих дезинфицирующих веществ. Кислотосодержащие вещества относятся к быстро действующим, они проявляют активность не только в отношении бактерий, но и дрожжей и вирусов. Дезинфектанты на основе кислот обладают хорошими смачивающими свойствами, не оставляют пятен, не вызывают коррозию оборудования. Жесткая вода и присутствие органических веществ практически не оказывают влияния на эффективность продуктов. Дезинфицирующие вещества наносят на поверхность различными способами – распылением, с помощью пеногенератора, с помощью уборочного инвентаря – салфеток и губок, а также используют в CIP- мойках. Поскольку кислотосодержащие дезинфицирующие вещества теряют активность в щелочной области pH, следует тщательно смывать щелочные моющие и дезинфицирующие средства перед обработкой кислотосодержащими дезинфицирующими веществами. В состав кислотосодержащих средств входят анионные ПАВ, кислоты – фосфорная кислота или органические кислоты, перекись водорода. Дезинфицирующий продукт выбирают в зависимости от способа применения (ручная уборка, уборка с использованием пеногенератора, CIP- мойка и т.д.), вида поверхности и устойчивости поверхности к действию продукта.
В последние годы очень сильно вырос интерес к дезинфицирующим веществам на основе надуксусной кислоты. Дезинфицирующие средства на надуксусной (перуксусной) кислоте, обладают высокой эффективностью, широким спектром действия. В зависимости от задачи надуксусную кислоту используют в интервале концентрации от 30 до 250 ppm. Надуксусная кислота практически безопасна для человека: в концентрациях до 80 ppm может присутствовать на овощах и фруктах, а в концентрациях до 250 ppm – на обработанных поверхностях. Дезинфицирующие средства на основе надуксусной кислоты не требуют смывания (если не содержат моющих компонентов или других веществ, которые сами по себе должны смываться с поверхностей или пищевого оборудования). Использование таких средств позволяет сэкономить время, снизить расход воды, и таким образом, сократить финансовые затраты на дезинфекцию.
Надуксусная кислота нашла широкое применение в различных областях. Ее используют для дезинфекции оборудования и предварительно очищенных твёрдых поверхностей в производстве молочных продуктов, вина, напитков, оборудования птицеферм и животноводческих хозяйств. Поскольку надуксусная кислота активна против дрожжей Candida, Saccharomyces, Hansenula и плесневых грибов – Penicillium, Aspergillus, Mucor Geotrichum, она нашла широкое применение в производстве пива и безалкогольных напитков. Именно надуксусная кислота используется для дезинфекции алюминиевой тары – банок для пива и безалкогольных напитков и для консервированных продуктов.. Увеличившийся интерес к использованию надуксусной кислоты в пищевой промышленности связан с ее высокой активностью в отношении таких патогенных микроорганизмов, как Listeria, Salmonella,
а также способностью уничтожать биопленки. Надуксуная кислота нашла широкое применение для ограничения роста бактерий, грибов и слизи в системах охлаждения воды, парообразования, системах обратного осмоса и фильтрации. Кроме того, ее используют для удаления минеральных отложений, запахов, биопленок с оборудования и поверхностей. К положительным свойствам надуксусной кислоты следует также отнести свойства отбеливателя.
Действие надуксусной кислоты основано на окислении внешней клеточной мембраны вегетативных бактериальных клеток, эндоспор, дрожжей и плесневых грибов. Чем сильнее окислитель, тем быстрее погибает патогенный микроорганизм. Надуксусная кислота является очень эффективным окислителем. По своей окислительной способности надуксусная кислота уступает только озону и намного превосходит хлорсодержащие соединения (Таблица 2).
Таблица 2. Окислительная способность некоторых дезинфектантов.
|
Дезинфицирующее вещество |
Окислительная .способность, эВ |
|
Озон |
2.07 |
|
Надуксуная кислота |
1.81 |
|
Диоксид хлора |
1.51 |
|
Гипохлорит натрия |
1.36 |
Дезинфицирующие средства на основе надуксусной кислоты не оказывают значительного воздействия на окружающую среду. Средства имеют короткий период полураспада на уксусную кислоту и кислород и обычно не требуют нейтрализации перед выбросом в сточные воды. Результаты токсикологических исследований показали, что надуксусная кислота обладает гораздо меньшей токсичностью для живых организмов морской и пресной воды, чем другие средства дезинфекции. При попадании на почву надуксусная кислота разлагается в течение нескольких минут, не оказывая влияния на качество почвы.
Хранение продуктов на основе надуксусной кислоты осуществляют с соблюдением несложных правил – в отсутствии прямого попадания солнечных лучей и при температуре, не превышающей 20°С.
Одним из немногих ограничений для использования этого дезинфектанта является характерный запах уксуса. Но поскольку надуксусная кислота эффективно воздействует на патогенные микроорганизмы даже в очень низких концентрациях, рабочие растворы обладают очень слабым запахом.
Надуксусную кислоту (НУК) в качестве действующего вещества содержат дезинфицирующие средства ХИМИТЕКПОЛИДЕЗ®-СУПЕР и ХИМИТЕК ПОЛИДЕЗ®-DRY. Оба высокоэффективны при низких концентрациях, работают в воде любой степени жёсткости, обладают отбеливающими свойствами, применяются в различных областях. ХИМИТЕК ПОЛИДЕЗ®-СУПЕР жидкий концентрированный продукт, широко используется на предприятиях пищевой и перерабатывающей промышленности после мойки для дезинфекции всех кислотостойких поверхностей. Средство эффективно в малых концентрациях – от 0,2%, не требует ротации. Средство разрешено для дезинфекции не только поверхностей, но и продуктов питания: овощного сырьё, зелени, скорлупы яиц и тушек птиц.
ХИМИТЕК ПОЛИДЕЗ®-DRY отличается от средства ХИМИТЕК ПОЛИДЕЗ®-СУПЕР тем, что выпускается в форме порошка, при растворении которого в воде происходит реакция образования НУК, при этом раствор обладает нейтральным рН (7,0-8,5) и не имеет резкого химического запаха. Он не оказывает коррозионного воздействия на металлические поверхности. Средство не имеет побочных эффектов в форме фиксации белковых загрязнений и развития резистентности у микроорганизмов. Безопасно и экологично. Дополнительным свойством этого дезинфектанта является хорошая моющая способность за счет содержащихся в составе ПАВ, что позволяет добиться высокой степени чистоты обрабатываемых поверхностей.
Перекись водорода.
Перекись водорода используется в пищевой промышленности в различных концентрациях от 3% и до 90% применяется в пищевой промышленности. Перекисью водорода обрабатывают поверхность упаковки для фруктов. В концентрации 6% перекись водорода проявляет бактерицидные свойства. В общем можно сказать, что перекись водорода более активна в отношении грам — положительных бактерий, чем грам — отрицательных. Уничтожение спор спорообразующих бактерий происходит при обработке поверхности перекись водорода в концентрации от 10 до 30%. Этот антимикробный агент может использоваться на любом оборудовании и поверхностях. В случае использования концентрированных растворов пероксида и опасения возможности коррозии оборудования следует использовать антикоррозионные добавки. Было показано, что перекись водорода убивает Listeria monocytogenes на латексных перчатках. Перекись водорода используют для обработки различных поверхностей из полимерных материалов, смол и каучуков.
Перекись водорода часто используют в комбинации с другими дезинфицирующими веществами, например, надуксусной кислотой или четвертичными аммониевыми соединениями.
Средство ПОЛИДЕЗ® производства НПФ Химитек в качестве действующего вещества содержит перекись водорода и четвертичные аммонийные соединения. Средство активно в отношении грамотрицательных и грамположительных бактерий (включая бактерии туберкулёза), вирусов, грибов рода Кандида и Трихофитон. Продукт имеет нейтральный pH (5,8–7,0), не вызывает коррозию металлов, не имеет резкого запаха. Рабочие растворы стабильны в широком температурном диапазоне, режим разведения и применения – от 20 до 50°C, работает в воде любой степени жёсткости.
Дезинфектанты на основе спиртов.
В целя дезинфекции наиболее часто используют три спирта- этиловый, изопропиловый и n-пропиловый, последний, в основном, используется в Европе. Дезинфицирующие агенты на основе спиртов проявляют максимальную эффективность в интервале концентраций 60-70%. Концентрации дезинфицирующего агента, необходимые для инактивации патогенных микроорганизмов выше, чем концентрации хлор- содержащих, четвертичных аммониевых солей и кислотосодержащих дезинфицирующих агентов. Спорообразующие микроорганизмы в достаточной степени устойчивы к действию спиртов, однако обработка спиртосодержащими растворами при концентрации спирта 70% и 65ºС инактивирует споры, например споры Bacillus subtilis. Обработка спиртосодержащими дезинфектантами дороже, чем продуктами других химических классов, поэтому их не используют для полной обработки поверхностей или оборудования. В основном, такими составами обрабатывают небольшие малодоступные участки оборудования и поверхностей. Кроме того, составы на основе спиртов используют для дезинфекции рук персонала.
Для проведения экспресс-дезинфекции небольших по площади, а также труднодоступных поверхностей компания НПФ Химитек разработала и выпускает дезинфицирующее средство ХИМИТЕК ПОЛИДЕЗ-ЭКСПРЕСС. В качестве действующего вещества продукт содержит изопропиловый и пропиловый спирты, обладает антимикробной активностью в отношении грамотрицательных и грамположительных бактерий, дрожжеподобных грибов и дрожжей. Помимо всего продукт готов к использованию, имеет удобную упаковку и не требует смывания. Обладает стабильностью микробиологической активности при хранении, низкой токсичностью.
Дезинфектанты на основе альдегидов.
Наиболее известными дезинфицирующими агентами этого класса являются глютаровый альдегид и формальдегид. Альдегиды активны в отношении бактерий, вирусов, плесневых грибов и спор. Однако этот класс соединений очень быстро инактивируется протеинами, поэтому для достижения необходимого эффекта дезинфекции поверхность должна быть предварительно тщательно очищена. Известно, что глютаровый альдегид вызывает сильную денатурацию белка и потому, в случае некачественной очистки, фиксирует загрязнения на обрабатываемой поверхности.
Действие альдегидов основано на их взаимодействии с внешними слоями клетки, в результате чего клетка метаболизирует, и происходит ингибирование ее активности. Щелочная среда наиболее благоприятна для взаимодействия альдегидов с внешними слоями клетки. Для обработки используют растворы различных концентраций — 0.8-1.6% для ингибирования E.coli. Для ингибирования спорообразующих бактерий концентрацию альдегидов в растворе увеличивают до 2%.
При работе с дезинфицирующими агентами на основе альдегидов персонал должен быть хорошо обучен, нарушение правил работы с такими продуктами может нанести ущерб здоровью работников, поскольку обладает альдегиды обладают ярко выраженным раздражающим, наркологическим, сенсибилизирующим и токсическим эффектом.
Бисфенолы.
Бисфенолы – это соединения дифенил метана, дифенил эфира, дифенил сульфида, содержащие галогены и гидроксильные группы. Они проявляют активность в отношении бактерий, грибов и водорослей. Триклозан и гексахлоропрен – представители этого класса соединений, которые наиболее часто используются в качестве дезинфектантов и антисептиков. Триклозан — 5-хлоро-2-(2,4-дихлорфеноси)фенол входит в состав антибактериального мыла, очищающих гелей для рук и зубных паст, поскольку проявляет высокую активность в отношении стафилокков. Триклозан может содержать высоко токсичные для человека соединения диоксин и дибензофуран, поэтому перед использованием этого дезинфицирующего агента на пищевом средстве следует внимательно ознакомиться со способом производства этого соединения и содержанием примесей, которые должны присутствовать в паспорте безопасности.
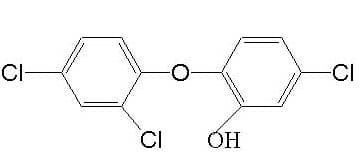
Механизм действия триклозана на бактериальную клетку считается до конца не установленным. Предполагается, что триклозан блокирует биосинтез липидов путем специфического ингибирования фермента еноил-ацил-преносящий белок-редуктазы.
Действие триклозана, как и диоксинов и фенолов — подавление развития микроорганизмов. Но в свою очередь они могут вызывать у них мутации. Помимо этого, у них у всех сильно выражено раздражающее действие на кожу.
Бигуанидины.
Группа бигуанидинов представлена хлоргексидином, алексидином и полимерными бигуанидинами. Хлоргексидин один из наиболее используемых антисептиков для обработки рук, в концентрации 0.0001 мг/л он является бактериостатиком. В концентрации 0.002 мг/л – бактерицидом с широким спектром действия. Активность хлоргексидина зависит от pH среды, в щелочной среде она выше, чем в кислой среде. Его активность заметно снижается в присутствии органических веществ. При концентрации выше 0.005 мг/л и температуре 70º С хлоргексидин проявляет активность в отношении спорообразующих бактерий, хотя действует, в основном, как бактериостатик. Полимерные бигуанидины нашли применение в пищевой промышленности, в медицине, в санитарной обработке бассейнов.
Таблица 3.Основные дезинфицирующие вещества.
|
Дезинфицирующие агенства |
Применение |
Активность в отношении бактерий |
Активность в отношении спор |
Комментарии |
|
Галоген-содержащие |
50-250 мг/л |
> 10 мг/л |
> 50 мг/л |
Хлор содержащие соединение дешевле, чем йодофоры, но обладают коррозионным действием |
|
Четвертичные аммониевые соединения |
150-250 мг/л |
>100 мг/л |
— |
Обладают пролонгированным действием (~ 1 день), нейтральны, не агрессивны |
|
Перекись водорода |
3-90% |
>6% |
10-30% |
Более эффективна в сочетании с надуксусной кислотой |
|
Надуксусная кислота |
30-250 ppm |
30 ppm |
> 100 ppm |
Широкий спектр активности, присутствие органических веществ практически не снижает активности |
|
Спирты (этанол) |
20-70% |
>22% |
60-70% |
Имеют промышленное применение |
|
Альдегиды |
0.8-16 мг/л |
< 10 мг/л |
20 мг/л |
Имеют ограниченное промышленное применение в пищевой промышленности |
|
Бисфенолы |
2-20 мг/л |
> 10 мг/л |
— |
|
|
Бигуанидины |
> 150 мг/л |
1-60 мг/л |
— |
Используют в рецептурах кожного антисептика |
Стратегия оптимизации процессов очистки и дезинфекции.
Устойчивость патогенных микроорганизмов к действию моющих и дезинфицирующих веществ пока еще не стала глобальной проблемой пищевой промышленности. Однако работники пищевой промышленности должны осознавать возможность появления устойчивых штаммов патогенных микроорганизмов в случае неправомерного использования моющих и дезинфицирующих средств. Исследования показали, что даже кратковременное воздействие дезинфицирующими веществами на Listeria Monocytogenes в концентрациях, недостаточных для гибели патогенных микроорганизмов вызывают их мутацию, при этом могут сформироваться патогенные микроорганизмы, устойчивые к действию дезинфицирующих веществ. При использовании моющих и дезинфицирующих веществ следует принимать во внимание следующие факторы:
- выбор дезинфектанта, активного против данного вида патогенных микроорганизмов,
- соблюдение условий применения, рекомендованных производителем (температура, pH среды),
- присутствие веществ, способных к инактивации моющих или дезинфицирующих веществ,
- мониторинг чистоты поверхности и микробного фона до и после применения моющих и дезинфицирующих средств.
Как уже отмечалось, важным обстоятельством является правильный выбор дезинфицирующего агента, обладающего необходимым спектром активности против конкретного вида микроорганизмов. Например, не имеет смысла использовать дезинфицирующий агент на основе спиртов против спорообразующих бактерий вследствие низкой эффективности и возможности мутации некоторых микроорганизмов. Использование дезинфицирующих агентов, выделяющих активный хлор, будет ограничено их способностью к коррозии металлов и их способностью разрушать материалы на полимерной основе.
Соблюдение условий применения, обеспечивающих максимальный эффект снижения числа микроорганизмов, является важным обстоятельством как с точки зрения безопасности пищевого производства, так и с точки зрения сохранения сокращения финансовых затрат на уборку и дезинфекцию. К основным факторам, влияющим на процессы мойки и дезинфекции, относят концентрацию моющих или дезинфицирующих веществ, механическую работу, время и температуру. При применении дезинфицирующих средств следует руководствоваться рекомендациями производителя. Использование более концентрированных растворов, чем это необходимо, может привести к образованию нерастворимых соединений и активизации коррозионных процессов. Обработка поверхностей и оборудования при температурах более высоких, чем рекомендовано в инструкции производителя может привести к химическому разложению активного вещества, выпадению солей жесткости воды, полимеризации протеинов и жиров, что негативно скажется на качестве дезинфекции. Еще одним важным фактором в процессе дезинфекции является время контакта дезинфицирующего вещества, чем выше время контакта, тем выше число инактивированных микроорганизмов.
Существует много математических моделей, описывающих процесс инактивации микроорганизмов. При использовании этих моделей возникают трудности, поскольку они включают в себя параметры, которые сложно определить экспериментальным путем. Одна из моделей, которая используется чаще других, является линейно-логарифмическая модель Чика-Ватсона:
Log(N1/N0) = — ĸCnt ,
N1 — выжившее число микроорганизмов,
N0 –первоначальное число микроорганизмов,
ĸ — константа скорости дезинфекции,
C –концентрация дезинфектанта,
n – коэффициент разбавления,
t – время контакта.
Коэффициент разбавления n зависит от вида дезинфицирующего агента. Например, для четвертичных аммониевых солей n=1. Это означает, что при снижении концентрации n в два раза следует в два раза увеличить время экспозиции. Для этанола n=10, это означает, что при снижении концентрации этанола в два раза эффективность обработки снижается в 2¹º, т.е. в 1024 раза.
Очевидно, что механическая работа вносит важный вклад в качество дезинфекционной обработки. Чем больше затрачено механических усилий, тем меньше количество микроорганизмов остается на поверхности после очистки. Конечный результат зависит от правильности выбора дезинфектанта и технологий мойки и дезинфекции. При выборе моющих и дезинфицирующих средств и определении порядка выполнения технологических операций следует выбирать такое сочетание моющих и дезинфицирующих средств, чтобы не происходило инактивации дезинфицирующего вещества.
Таблица 5. Характеристики стандартных дезинфицирующих веществ
|
Характеристики |
Йодофоры |
Хлорсодержа- щие соединения |
Кислотосодер- жащие соединения |
Четвертичные аммониевые соли |
|
Антимикробная активность |
Вегетативные клетки |
Хорошая |
Хорошая |
Хорошая, имеется некоторая селективность |
|
Воздействие на дрожжи |
Хорошая |
Хорошая |
Хорошая |
Хорошая |
|
Воздействие на плесневые грибы |
Хорошая |
Хорошая |
Хорошая |
Хорошая |
|
Стабильность |
||||
|
при хранении |
Зависит от температуры |
Низкая |
Великолепная |
Великолепная |
|
при использовании |
Зависит от температуры |
Зависит от температуры |
Великолепная |
Великолепная |
|
Быстрота воздействия |
Быстрое |
Быстрое |
Быстрое |
Быстрое |
|
Проницаемость |
Хорошая |
Слабая |
Хорошая |
Великолепная |
|
Пленкообразование |
Нет или слабое |
— |
— |
+ |
|
Влияние органических веществ |
Среднее |
Сильное |
Незначительное |
Незначительное |
|
Легкость измерения |
Великолепная |
Великолепная |
Великолепная |
Великолепная |
Если после прочтения статьи у вас позникли вопросы — звоните по телефону вверху страницы! Или пишите на service@chemitech.ru Ответим на ваши вопросы по применению!
Group
Группировочное наименование
Оглавление
- Фармакологическое действие
- Фармакокинетика
- Показания препарата
- Режим дозирования
- Побочное действие
- Противопоказания к применению
- Особые указания
- Лекарственное взаимодействие
Входит в состав препаратов:
список
Фармакологическое действие
Неорганическое соединение, соль хлорноватистой кислоты. Оказывает выраженное бактерицидное, фунгицидное, вирулицидное действие. Эффективность снижается в присутствии белка, сыворотки и цельной крови.
Фармакокинетика
Натрия гипохлорит разрушается почти мгновенно при контакте с кровью и компонентами крови, поэтому не ожидается, что он будет обнаруживаться в крови.
Показания активного вещества
НАТРИЯ ГИПОХЛОРИТ
В качестве антисептического и дезинфицирующего средства: обработка ран, язв, ожогов; дезинфекция кожи и слизистых оболочек (в т.ч. полости рта и глотки), включая дезинфекцию наружных половых органов.
Режим дозирования
Применяют наружно в виде орошений, наложения влажных повязок, компрессов, тампонов, турунд для антисептической обработки кожи, слизистых оболочек, ран.
Частота смены повязок — 1 раз/сут. При гнойных ранах с обильным отделяемым повязки меняют каждые 2-3 часа.
Продолжительность наложения компрессов не должна превышать 2 часов.
Побочное действие
Возможно: аллергические реакции, чувство жжения в месте аппликации.
Противопоказания к применению
Повышенная чувствительность к натрия гипохлориту, к хлорсодержащим соединениям, детский возраст до 12 лет.
Применение при беременности и кормлении грудью
При необходимости применения при беременности и в период грудного вскармливания следует тщательно оценить ожидаемую пользу терапии для матери и возможный риск для плода и грудного ребенка.
Применение у детей
Противопоказано применению у детей в возрасте до 12 лет.
Особые указания
С осторожностью применять на больших поверхностях кожи, под окклюзионными повязками.
Следует избегать попадания данного средства в глаза.
Данное средство не используется для обработки медико-хирургических инструментов.
Лекарственное взаимодействие
Следует избегать одновременного или последовательного применения других антисептических средств или мыла без предварительного тщательного промывания обрабатываемого участка (возможно снижение эффективности данного средства).
- Производитель: Юнитор
- Модель: 1111
- Артикул: 00030454
- Наличие: Есть в наличии
- Обзор товара
- Отзывов (0)
Концентрированное средство.
Прозрачная жидкость от светло-желтого до зеленовато-желтого цвета с запахом хлора и отдушки.
Действующее вещество: гипохлорит натрия (6,25% по «активному хлору»).
В составе функциональные добавки: стабилизаторы, инертные антикоррозионная и моющие щелочные добавки, ароматизатор, вода.
рН средства: 11.5±1.5.
Срок годности: концентрат — 2 года; рабочие растворы-14 суток.
Биологическая активность
Рабочие растворы обладают бактерицидными (в том числе в отношении внутрибольничных инфекций), туберкулоцидными (тестировано на Mycobacterium Terrae), вирулицидными, фунгицидными, овоцидными свойствами. Средство активно в отношении плесени, анаэробных инфекций, а так же в отношении возбудителей особо опасных инфекций (ООИ) — холеры, туляримии, бруцеллеза, сибирской язвы.
Сфера применения
Лечебно-профилактические учреждения; клинические, микробиологические и др. лаборатории; коммунально-бытовые объекты; спортивные и административные учреждения; предприятия общественного питания; потребительские промышленные рынки; учреждения: социального обеспечения, пенитенциарные, детские; санитарный транспорт; населением в быту.
Способ применения
Протирание, погружение, орошение.
Назначение
- Для профилактической, текущей, заключительной дезинфекции поверхностей в помещениях, предметов ухода за больными, игрушек, посуды, санитарно-технического оборудования, резиновых ковриков, уборочного инвентаря и т.п.;
- для дезинфекции, стирки, отбеливания белья ручным способом и в автоматических стиральных машинах;
- для обеззараживания поверхности скорлупы пищевых яиц;
- для обеззараживания вакцин;
- для дезинфекции изделий медицинского назначения, за исключением эндоскопического оборудования;
- для дезинфекции контуров диализных аппаратов и систем подачи воды;
- для дезинфекции (обезвреживания) медицинских отходов перед их утилизацией;
- для использования в дезбарьерах, дезковриках, дезматах.
Каждая партия средства ЯНИЛИС (гипохлорит натрия, 6,25%) сопровождается
УДОСТОВЕРЕНИЕМ О КАЧЕСТВЕ, содержащем значения показателей качества согласно требований ТУ 20.20.14-001-315619600001672-2017
Преимущества
- Дезинфекция в отношении широкого спектра патогенных микроорганизмов, в том числе спор сибирской язвы.
- Высокоэкономичное средство.
- Антикоррозионные добавки в составе для защиты изделий и поверхностей из металлов, включая изделия из аллюминия.
- Эффективно работает в жесткой воде.
- Высокая стабильность концентрата и рабочих растворов. При соблюдении условий хранения, средство стабильно в течение 2 лет.
- Высокая отбеливающая способность при стирке, отсутствие инкрустации тканей при ручной и машинной стирке.
- Низкая ингаляционная токсичность.
- Возможно использование для проведения дезинфекции в детских учреждениях..
- Разрешено для использования населением в быту.
- Эффективное и выгодное использование для дезинфекции медицинских отходов.
Нет отзывов о данном товаре.