Зинфоро® (Zinforo®) инструкция по применению
📜 Инструкция по применению Зинфоро®
💊 Состав препарата Зинфоро®
✅ Применение препарата Зинфоро®
📅 Условия хранения Зинфоро®
⏳ Срок годности Зинфоро®
Описание лекарственного препарата
Зинфоро®
(Zinforo®)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для электронного издания справочника Видаль 2015
года, дата обновления: 2021.07.23
Владелец регистрационного удостоверения:
Код ATX:
J01DI02
(Цефтаролина фосамил)
Лекарственная форма
| Зинфоро® |
Порошок д/пригот. концентрата д/пригот. р-ра д/инфузий 600 мг: фл. 1 или 10 шт. рег. №: ЛП-001912 |
Форма выпуска, упаковка и состав
препарата Зинфоро®
Порошок для приготовления концентрата для приготовления раствора для инфузий от желтовато-белого до светло-желтого цвета.
Вспомогательные вещества: L-аргинин — 395 мг.
Флаконы стеклянные вместимостью 20 мл (1) — пачки картонные с контролем первого вскрытия.
Флаконы стеклянные вместимостью 20 мл (10) — пачки картонные с контролем первого вскрытия.
Фармакологическое действие
Антибиотик группы цефалоспоринов V поколения. После в/в введения про-лекарство цефтаролина фосамил быстро превращается в активный цефтаролин.
Цефтаролин — антибиотик класса цефалоспоринов с активностью в отношении грамположительных и грамотрицательных микроорганизмов. В исследованиях in vitro показано бактерицидное действие цефтаролина, обусловленное ингибированием биосинтеза клеточной стенки бактерий за счет связывания с пенициллинсвязывающими белками (ПСБ). Цефтаролин проявляет бактерицидную активность в отношении Staphylococcus aureus (MRSA) и в отношении пенициллин-нечувствительного Streptococcus pneumoniae (PNSP) в связи с его высоким сродством к измененным ПСБ этих микроорганизмов.
Антимикробная активность цефтаролина, также как и других бета-лактамных антибиотиков, лучше всего коррелирует с интервалом времени, в течение которого концентрации препарата остаются выше минимальной подавляющей концентрации (МПК) инфицирующего микроорганизма (%Т>МПК).
Цефтаролин не активен в отношении штаммов Enterobacteriaceae, продуцирующих β-лактамазы расширенного спектра действия (БЛРС) семейств ТЕМ, SHV или СТХ-М, сериновые карбапенемазы (такие как КРС), металло-β-лактамазы класса В или класса С (цефалоспориназы AmpC). Резистентность также может быть связана с нарушением проницаемости клеточной стенки бактерий или с активным выведением антибиотика (эффлюкс). Микроорганизм может обладать одним или несколькими механизмами резистентности.
Несмотря на возможное развитие перекрестной резистентности, некоторые штаммы, резистентные к другим цефалоспоринам, могут быть чувствительны к цефатролину. Микроорганизмы, обладающие природной резистентностью: Chlamydophila spp., Legionella spp., Mycoplasma spp., Proteus spp., Pseudomonas aeruginosa.
Исследования in vitro не выявили антагонизма при применении цефтаролина в комбинации с другими часто назначаемыми антимикробными препаратами (такими как амикацин, азитромицин, азтреонам, даптомицин, левофлоксацин, линезолид, меропенем, тигециклин и ванкомицин).
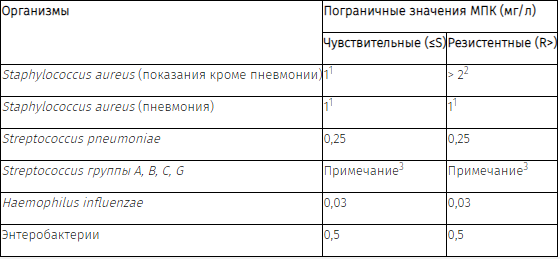
Чувствительность антибиотиков in vitro меняется в зависимости от географического региона и с течением времени, поэтому при выборе антибактериальной терапии необходимо учитывать местную информацию о резистентности. Если локальная резистентность такова, что эффективность препарата в отношении некоторых инфекций становится сомнительной, необходимо обратиться за консультацией к эксперту.
Чувствительность к цефатролину следует определять с помощью стандартных методов. Интерпретацию результатов следует проводить в соответствии с локальными руководствами.
Клиническая эффективность в отношении отдельных патогенных микроорганизмов
Ниже перечислены патогенные микроорганизмы (по показаниям к применению), чувствительные к цефатролину in vitro, в отношении которых в клинических исследованиях была показана эффективность цефтаролина.
Осложненные инфекции кожи и мягких тканей: грамположительные микроорганизмы — Staphylococcus aureus (включая метициллинрезистентные штаммы), Streptococcus pyogenes, Streptococcus agalactiae, группа Streptococcus anginosus (включает S. anginosus, S. intermedius и S. constellatus), Streptococcus dysgalactiae; грамотрицательные микроорганизмы — Escherichia coli, Klebsiella pneumoniae, Klebsiella oxytoca, Morganella morganii.
Внебольничная пневмония: грамположительные микроорганизмы — Streptococcus pneumoniae (включая случаи, сопровождающиеся бактериемией), Staphylococcus aureus (включая метициллин-чувствительные штаммы); грамотрицательные микроорганизмы — Escherichia coli, Haemophilus influenzae, Haemophilus parainfluenzae, Klebsiella pneumoniae.
Клиническая эффективность цефтаролина в отношении перечисленных ниже патогенных микроорганизмов не была установлена, однако результаты исследований in vitro позволяют предполагать, что они чувствительны к цефатролину в отсутствие приобретенных механизмов резистентности: грамположительные анаэробы (Peptostreptococcus spp.), грамотрицательные анаэробы (Fusobacterium spp.).
Фармакокинетика
Всасывание
Cmax и AUC цефтаролина увеличиваются почти пропорционально дозе при однократном введении препарата в диапазоне доз от 50 до 1000 мг. Не наблюдалось заметной кумуляции цефтаролина после многократного в/в введения препарата в дозе 600 мг в течение 60 мин каждые 12 ч в течение 14 дней здоровым добровольцам с нормальной функцией почек.
Распределение
Степень связывания цефтаролина с белками плазмы низкая (примерно 20%), препарат не проникает в эритроциты. Медиана Vd в равновесном состоянии у здоровых взрослых мужчин после однократного в/в введения 600 мг цефтаролина фосамила, меченного изотопом, составила 20.3 л, почти как и объем внеклеточной жидкости.
Метаболизм
В плазме крови под действием фосфатаз про-лекарство цефтаролина фосамил быстро преобразуется в активный цефтаролин; концентрации пролекарства поддаются измерению в плазме, преимущественно, во время в/в инфузии. При гидролизе бета-лактамного кольца цефтаролина образуется микробиологически неактивный метаболит, цефтаролин М-1. Соотношение средних значений AUC цефтаролина М-1 к цефатролину в плазме крови после однократного в/в введения 600 мг цефтаролина фосамила здоровым добровольцам составляет примерно 20-30%.
Метаболизм цефтаролина протекает без участия ферментов системы цитохрома Р450.
Выведение
Цефтаролин выводится, преимущественно, почками. Почечный клиренс цефтаролина примерно равен или немного ниже скорости клубочковой фильтрации в почках, исследования транспортеров in vitro показывают, что активная секреция не способствует почечной элиминации цефтаролина. Средний T1/2 цефтаролина у здоровых взрослых людей составляет примерно 2.5 ч. После однократного в/в введения 600 мг меченного изотопом цефтаролина фосамила здоровым взрослым мужчинам примерно 88% радиоактивности обнаруживалось в моче и 6% — в фекалиях.
Фармакокинетика у особых групп пациентов
После однократной в/в инфузии 600 мг цефтаролина фосамила в течение 60 мин Cmax цефтаролина в плазме составила 28.4±6.9 мкг/мл, 28.2±5.4 мкг/мл и 30.8±4.9 мкг/мл у пациентов с нормальной функцией почек, почечной недостаточностью легкой и средней степени тяжести, соответственно. Cmax цефтаролина достигалась приблизительно через 60 мин после начала инфузии. AUC цефтаролина увеличивалась пропорционально степени почечной недостаточности и составила 75.6±9.7 мкг×ч/мл, 92.3±25.3 мкг×ч/мл и 114.8±14.1 мкг×ч/мл у пациентов с нормальной функцией почек, почечной недостаточностью легкой и средней степени тяжести, соответственно. Коррекция дозы требуется только у пациентов с почечной недостаточностью средней степени тяжести (КК 30-50 мл/мин). Недостаточно данных для рекомендаций по коррекции дозы у пациентов с почечной недостаточностью тяжелой степени (КК ≤30 мл/мин) и терминальной стадией почечной недостаточности, включая пациентов, находящихся на гемодиализе.
Исследования фармакокинетики цефтаролина у пациентов с печеночной недостаточностью не проводили. Т.к. цефтаролин не подвергается печеночному метаболизму в значительной степени, не ожидается, что печеночная недостаточность будет существенно влиять на системный клиренс цефтаролина. Поэтому не рекомендуется корректировать дозу препарата у пациентов с печеночной недостаточностью.
После однократного в/в введения 600 мг цефтаролина фосамила параметры фармакокинетики препарата были схожими у здоровых пожилых людей (≥65 лет) и здоровых молодых пациентов (18-45 лет). У добровольцев пожилого возраста отмечено небольшое увеличение AUC0-∞ (на 33%), что обусловлено, главным образом, возрастными изменениями функции почек. Не требуется коррекции дозы препарата у пациентов пожилого возраста с КК >50 мл/мин.
Безопасность и эффективность препарата Зинфоро® у детей и подростков в возрасте до 18 лет не установлены.
Параметры фармакокинетики цефтаролина были схожими у мужчин и женщин. Не требуется коррекции дозы в зависимости от пола пациента.
Не наблюдалось существенных различий параметров фармакокинетики цефтаролина у пациентов, принадлежащих разным этническим группам. Не требуется корректировать дозу препарата в зависимости от расы пациента.
Показания препарата
Зинфоро®
Лечение у взрослых следующих инфекций:
- осложненные инфекции кожи и мягких тканей, вызванные чувствительными штаммами следующих грамположительных и грамотрицательных микроорганизмов: Staphylococcus aureus (включая метициллинрезистентные штаммы), Streptococcus pyogenes, Streptococcus agalactiae, Streptococcus anginosus, Streptococcus dysgalactiae, Escherichia coli, Klebsiella pneumoniae, Klebsiella oxytoca и Morganella morganii;
- внебольничная пневмония, вызванная чувствительными штаммами следующих грамположительных и грамотрицательных микроорганизмов: Streptococcus pneumoniae (включая случаи, сопровождающиеся бактериемией), Staphylococcus aureus (только метициллин-чувствительные штаммы), Haemophilus influenzae, Haemophilus parainfluenzae, Klebsiella pneumoniae и Escherichia coli.
Режим дозирования
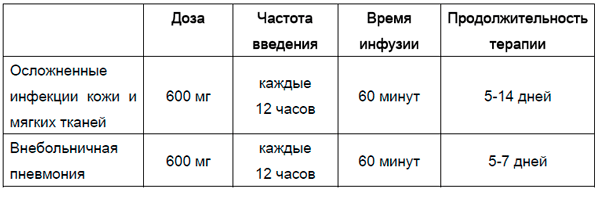
Препарат Зинфоро® вводится в/в в виде инфузии в течение 60 мин.
Продолжительность терапии следует устанавливать в зависимости от типа и тяжести инфекции, ответа пациента на терапию. Рекомендуется следующий режим дозирования:
Особые группы пациентов
У пациентов с почечной недостаточностью тяжелой степени (КК ≤30 мл/мин), терминальной стадией почечной недостаточности и пациентов, находящихся на гемодиализе, применение препарата противопоказано.
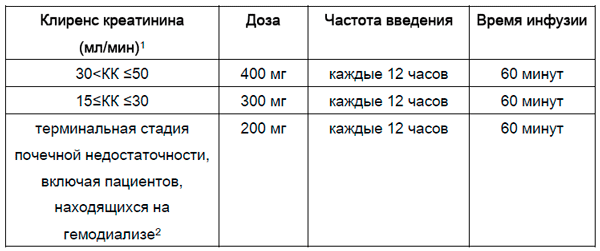
При КК 30-50 мл/мин, дозу следует скорректировать следующим образом:
Нет необходимости корректировать дозу препарата у пациентов с печеночной недостаточностью.
Нет необходимости корректировать дозу препарата у пациентов пожилого возраста (≥65 лет) с КК >50 мл/мин.
Безопасность и эффективность препарата Зинфоро® у детей и подростков в возрасте до 18 лет не установлены.
Правила приготовления раствора для инфузии
При приготовлении и введении препарата необходимо соблюдать стандартные правила асептики. Каждый флакон предназначен только для однократного применения.
Зинфоро® порошок для приготовления концентрата для приготовления раствора для инфузии следует растворить в 20 мл стерильной воды для инъекций. 1 мл концентрата содержит 30 мг цефтаролина фосамила. Полученный концентрат представляет собой раствор бледно-желтого цвета, свободный от видимых частиц. Концентрат необходимо немедленно использовать, не хранить (время от начала растворения порошка до полного приготовления раствора для в/в инфузии не должно превышать 30 мин).
Для приготовления раствора для инфузии полученный концентрат встряхивают и переносят в инфузионный флакон, содержащий одну из перечисленных ниже совместимых инфузионных жидкостей: 0.9% раствор натрия хлорида, 5% раствор декстрозы, 0.45% раствор натрия хлорида и 2.5% раствор декстрозы, раствор Рингера лактат.
При применении препарата в дозе 600 мг во флакон с совместимой инфузионной жидкостью переносят весь полученный концентрат (20 мл), при применении в дозе 400 мг — 14 мл концентрата.
Раствор для инфузии можно приготовить путем добавления концентрата во флакон с инфузионной жидкостью объемом 50 мл, 100 мл или 250 мл.
Раствор для инфузии следует использовать в течение 6 ч с момента приготовления. Приготовленный раствор для инфузии сохраняет стабильность в течение 24 ч при хранении в холодильнике (2-8°С). После извлечения из холодильника раствор для инфузии необходимо использовать в течение 6 ч при комнатной температуре.
Неиспользованный препарат или отходы необходимо утилизировать в соответствии с местными требованиями.
Побочное действие
Наиболее частыми нежелательными реакциями, развившимися у ≥3% пациентов, получавших цефтаролин, были диарея, головная боль, тошнота и зуд, и были обычно слабо или умеренно выраженными.
Ниже представлены нежелательные реакции, отмечавшиеся в объединенных клинических исследованиях фазы 3 по показаниям осложненные инфекции кожи и мягких тканей и внебольничная пневмония (1305 взрослых пациентов в группе терапии Зинфоро®). Частота нежелательных реакций представлена в виде следующей градации: очень часто (≥1/10), часто (≥1/100,<1/10), нечасто (≥1/1000, <1/100), редко (≥1/10 000,<1/1000).
Частота развития нежелательных реакций по классу системы органов
1 см. раздел «Особые указания»
2 см. раздел «Противопоказания»
Противопоказания к применению
- почечная недостаточность тяжелой степени (КК ≤30 мл/мин), терминальная стадия почечной недостаточности и пациенты, находящиеся на гемодиализе;
- детский и подростковый возраст до 18 лет;
- повышенная чувствительность к цефтаролина фосамилу или L-аргинину;
- повышенная чувствительность к цефалоспоринам;
- тяжелые реакции повышенной чувствительности немедленного типа (например, анафилактическая реакция) на любое другое антибактериальное средство, имеющее бета-лактамную структуру (например, пенициллины или карбапенемы).
С осторожностью следует назначать препарат пациентам с судорожным синдромом в анамнезе.
Применение при беременности и кормлении грудью
Клинические данные о применении цефтаролина фосамила у беременных женщин отсутствуют. Экспериментальные исследования на животных не выявили неблагоприятного воздействия цефтаролина фосамила на фертильность, беременность, роды или послеродовое развитие.
Препарат Зинфоро® не следует применять при беременности, за исключением случаев, когда потенциальная польза для матери превышает возможный риск для плода.
Данные о проникновении цефтаролина в грудное молоко отсутствуют. Однако, в связи с тем, что многие бета-лактамные антибиотики выделяются с грудным молоком, в случае необходимости терапии препаратом Зинфоро®, рекомендуется прекращение грудного вскармливания.
Применение при нарушениях функции печени
Нет необходимости корректировать дозу препарата у пациентов с печеночной недостаточностью.
Применение при нарушениях функции почек
У пациентов с почечной недостаточностью тяжелой степени (КК ≤30 мл/мин), терминальной стадией почечной недостаточности и пациентов, находящихся на гемодиализе, применение препарата противопоказано.
При КК 30-50 мл/мин, дозу следует скорректировать следующим образом:
Применение у детей
Противопоказано применение препарата Зинфоро® у детей и подростков в возрасте до 18 лет, т.к. безопасность и эффективность не установлены.
Применение у пожилых пациентов
Нет необходимости корректировать дозу препарата у пациентов пожилого возраста (≥65 лет) с КК >50 мл/мин.
Особые указания
При применении препарата необходимо руководствоваться официальными рекомендациями по надлежащему использованию антибактериальных препаратов.
Реакции гиперчувствительности
Как и при применении всех бета-лактамных антибиотиков возможно развитие серьезных реакций гиперчувствительности (иногда с летальным исходом).
У пациентов с гиперчувствительностью к цефалоспоринам, пенициллинам или другим бета-лактамным антибиотикам в анамнезе, может также развиться аллергическая реакция к цефтаролина фосамилу. Перед началом терапии препаратом Зинфоро® следует тщательно изучить данные пациента на предмет выявления реакций гиперчувствительности к бета-лактамным антибиотикам. Препарат противопоказан пациентам с повышенной чувствительностью к цефалоспоринам в анамнезе. Также препарат противопоказан пациентам, у которых ранее отмечались тяжелые реакции повышенной чувствительности немедленного типа (например, анафилактическая реакция) на любое другое антибактериальное средство, имеющее бета-лактамную структуру (например, пенициллины или карбапенемы).
При развитии тяжелой аллергической реакции необходимо прекратить введение лекарственного препарата и принять соответствующие меры.
Диарея, ассоциированная с Clostridium difficile
При применении почти всех антибактериальных препаратов, в т.ч. препарата Зинфоро®, сообщалось о развитии антибиотикоассоциированного колита и псевдомембранозного колита, которые могут варьировать по тяжести от легких до угрожающих жизни форм. Следует принимать во внимание возможность развития колита при возникновении диареи на фоне применения цефтаролина фосамила. В этом случае необходимо прекратить терапию препаратом Зинфоро®, проводить поддерживающие мероприятия и назначить специфическое лечение Clostridium difficile.
Пациенты с судорожным синдромом в анамнезе
Как и при применении других цефалоспоринов, в исследованиях токсичности цефтаролина наблюдалось развитие судорог при приеме препарата в дозах, превышающих Cmax в 7-25 раз. Опыт применения цефтаролина у пациентов с судорожным синдромом в анамнезе ограничен, в связи с чем следует соблюдать осторожность при применении препарата Зинфоро® у этой группы пациентов.
Почечная недостаточность
Опыт применения цефтаролина у пациентов с почечной недостаточностью тяжелой степени и терминальной стадией почечной недостаточности и у пациентов, находящихся на гемодиализе, ограничен. Поэтому применение препарата Зинфоро® у этой популяции больных противопоказано.
Прямой антиглобулиновый тест (проба Кумбса)
Положительный прямой антиглобулиновый тест (ПАТ) может быть получен на фоне применения цефалоспоринов. Частота положительного ПАТ у пациентов, получавших цефтаролина фосамил, составила 10.7% в объединенных исследованиях фазы 3. Ни у одного пациента с положительным ПАТ на фоне применения цефтаролина не выявлены признаки гемолиза.
Нечувствительные микроорганизмы
При применении цефтаролина фосамила, как и других антибиотиков, может развиться суперинфекция.
Влияние на способность к управлению транспортными средствами и механизмами
Не проводилось исследований по изучению влияния препарата Зинфоро® на способность к вождению автотранспорта и управлению иными механизмами. Во время терапии может возникать головокружение, поэтому следует соблюдать осторожность при управлении транспортными средствами и при занятиях другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций. При появлении головокружения следует воздержаться от выполнения указанных видов деятельности.
Передозировка
Данные о передозировке ограничены. Вероятность передозировки выше у пациентов с нарушением функции почек. При применении препарата в дозах выше рекомендованных наблюдались такие же нежелательные реакции, как и при применении препарата в рекомендованных дозах.
Лечение: симптоматическое. Цефтаролин частично выводится с помощью гемодиализа.
Лекарственное взаимодействие
Клинические исследования по изучению лекарственного взаимодействия с цефтаролином не проводились.
В исследованиях in vitro цефтаролин не ингибировал изоферменты цитохрома Р450 CYP1A1, CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1 и CYP3A4 и не индуцировал изоферменты CYP1A2, CYP2B6, CYP2C8, CYP2C9, CYP2C19, или CYP3A4/5. В связи с этим вероятность взаимодействия цефтаролина с препаратами, которые метаболизируются под действием изоферментов системы цитохрома Р450, низка. Цефтаролин не метаболизируется под действием изоферментов цитохрома Р450 in vitro, поэтому, маловероятно влияние на параметры фармакокинетики цефтаролина при совместном применении с индукторами или ингибиторами изоферментов цитохрома Р450.
In vitro цефтаролин не переносится эффлюксными транспортерами P-gp или BCRP. Цефтаролин не ингибирует P-gp, следовательно, взаимодействие с субстратами, такими как дигоксин, не ожидается. Цефтаролин является слабым ингибитором BCRP, но данный эффект не имеет клинической значимости.
Исследования in vitro показали, что цефтаролин не является субстратом, и не ингибировал транспортеры органических катионов (ОСТ2) и анионов (OAT1, ОАТ3) в почках; поэтому, маловероятно взаимодействие с препаратами, которые ингибируют активную почечную секрецию (например, пробенецид) или с препаратами, которые являются субстратами этих транспортеров.
Взаимодействие с другими антибактериальными препаратами
Тесты in vitro не выявили антагонизма при совместном применении цефтаролина и других часто используемых антибактериальных препаратов (например, амикацина, азитромицина, азтреонама, даптомицина, левофлоксацина, линезолида, меропенема, тигециклина и ванкомицина).
Условия хранения препарата Зинфоро®
Препарат следует хранить в недоступном для детей месте при температуре не выше 25°С.
Срок годности препарата Зинфоро®
Условия реализации
Препарат отпускается по рецепту.
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Обобщенные научные материалы по действующему веществу препарата Зинфоро® (порошок для приготовления концентрата для приготовления раствора для инфузий, 600 мг)
Дата последней актуализации: 23.08.2016
Особые отметки:
Содержание
- Действующее вещество
- ATX
- Владелец РУ
- Условия хранения
- Срок годности
- Источники информации
- Фармакологическая группа
- Характеристика
- Фармакология
- Показания к применению
- Противопоказания
- Ограничения к применению
- Применение при беременности и кормлении грудью
- Побочные действия
- Взаимодействие
- Передозировка
- Способ применения и дозы
- Меры предосторожности
- Заказ в аптеках Москвы
- Отзывы
Действующее вещество
ATX
Владелец РУ
Пфайзер Инк.
Условия хранения
При температуре не выше 30 °C.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Источники информации
Обобщенные материалы www.grls.rosminzdrav.ru, 2012–2015.
Фармакологическая группа
Характеристика
Антибиотик класса цефалоспоринов.
Фармакология
Фармакодинамика
После в/в введения пролекарство цефтаролина фосамил быстро превращается в активный цефтаролин.
Механизм действия
Цефтаролина фосамил обладает активностью в отношении грамположительных и грамотрицательных микроорганизмов.
В исследованиях in vitro показано бактерицидное действие цефтаролина, обусловленное ингибированием биосинтеза клеточной стенки бактерий за счет связывания с пенициллинсвязывающими белками (ПСБ). Цефтаролина фосамил проявляет бактерицидную активность в отношении метициллинрезистентного Staphylococcus aureus (MRSA) и пенициллиннечувствительного Streptococcus pneumoniae (PNSP) в связи с его высоким сродством к измененным ПСБ этих микроорганизмов.
Связь фармакокинетики и фармакодинамики
Антимикробная активность цефтаролина фосамила, также как и других бета-лактамных антибиотиков, лучше всего коррелирует с интервалом времени, в течение которого концентрация остается выше МПК инфицирующего микроорганизма (%Т >МПК).
Механизм резистентности
Цефтаролина фосамил неактивен в отношении штаммов Enterobacteriaceae, продуцирующих бета-лактамазы расширенного спектра (БЛРС) семейств ТЕМ, SHV или СТХ-М, сериновые карбапенемазы (такие как КРС), металло-бета-лактамазы класса В или С (цефалоспориназы AmpC). Резистентность также может быть связана с нарушением проницаемости клеточной стенки бактерий или с активным выведением антибиотика (эффлюкс). Микроорганизм может обладать одним или несколькими механизмами резистентности.
Перекрестная резистентность
Несмотря на возможное развитие перекрестной резистентности, некоторые штаммы, резистентные к другим цефалоспоринам, могут быть чувствительны к цефтаролина фосамилу.
Микроорганизмы, обладающие природной резистентностью: Chlamydophila spp., Legionella spp., Mycoplasma spp., Proteus spp., Pseudomonas aeruginosa.
Взаимодействие с другими антимикробными ЛС
Исследования in vitro не выявили антагонизма при применении цефтаролина фосамила в комбинации с другими часто назначаемыми антимикробными ЛС (такими как амикацин, азитромицин, азтреонам, даптомицин, левофлоксацин, линезолид, меропенем, тигециклин и ванкомицин).
Чувствительность
Чувствительность антибиотиков in vitro меняется в зависимости от географического региона и с течением времени, поэтому при выборе антибактериальной терапии необходимо учитывать местную информацию о резистентности.
Если локальная резистентность такова, что эффективность антибиотика в отношении некоторых инфекций становится сомнительной, необходимо обратиться за консультацией к эксперту. Чувствительность к цефтаролина фосамилу должна определяться с помощью стандартных методов. Интерпретацию результатов следует проводить в соответствии с локальными руководствами.
Клиническая эффективность в отношении отдельных патогенных микроорганизмов
Ниже перечислены патогенные микроорганизмы (по показаниям к применению), чувствительные к цефтаролина фосамилу in vitro, в отношении которых в клинических исследованиях была показана эффективность цефтаролина фосамила.
Осложненные инфекции кожи и мягких тканей
Грамположительные микроорганизмы: Staphylococcus aureus (включая метициллинрезистентные штаммы), Streptococcus pyogenes, Streptococcus agalactiae, группа Streptococcus anginosus (включает S. anginosus, S. intermedius и S. constellatus), Streptococcus dysgalactiae.
Грамотрицательные микроорганизмы: Escherichia coli, Klebsiella pneumoniae, Klebsiella oxytoca, Morganella morganii.
Внебольничная пневмония
Грамположительные микроорганизмы: Streptococcus pneumoniae (включая случаи, сопровождающиеся бактериемией), Staphylococcus aureus (только метициллинчувствительные штаммы).
Грамотрицательные микроорганизмы: Escherichia coli, Haemophilus influenzae, Haemophilus parainfluenzae, Klebsiella pneumoniae.
Эффективность в отношении других значимых патогенных микроорганизмов
Клиническая эффективность цефтаролина фосамила в отношении перечисленных ниже патогенных микроорганизмов не была установлена, однако результаты исследований in vitro позволяют предполагать, что они чувствительны к цефтаролину в отсутствие приобретенных механизмов резистентности.
Грамположительные анаэробы: Peptostreptococcus spp.
Грамотрицательные анаэробы: Fusobacterium spp.
Фармакокинетика
Сmax и AUC цефтаролина фосамила увеличиваются почти пропорционально дозе при однократном введении в диапазоне доз от 50 до 1000 мг. Не наблюдалось заметной кумуляции цефтаролина фосамила после многократного в/в введения в дозе 600 мг в течение 60 мин каждые 12 ч в течение 14 дней здоровым добровольцам с нормальной функцией почек.
Распределение. Степень связывания цефтаролина фосамила с белками плазмы низкая (примерно 20%), он не проникает в эритроциты. Медиана Vss у здоровых взрослых мужчин после однократного в/в введения 600 мг цефтаролина фосамила, меченного изотопом, составляет 20,3 л и практически соответствует объему внеклеточной жидкости.
Метаболизм. В плазме крови под действием фосфатаз пролекарство цефтаролина фосамил быстро преобразуется в активный цефтаролин; концентрации пролекарства поддаются измерению в плазме преимущественно во время в/в инфузии. При гидролизе бета-лактамного кольца цефтаролина фосамила образуется микробиологически неактивный метаболит, цефтаролин М-1. Соотношение средних значений AUC цефтаролина М-1 к цефтаролина фосамилу в плазме крови после однократного в/в введения 600 мг цефтаролина фосамила здоровым добровольцам составляет примерно 20–30%.
Метаболизм цефтаролина фосамила протекает без участия изоферментов системы цитохрома Р450.
Экскреция. Цефтаролина фосамил выводится преимущественно почками. Почечный клиренс цефтаролина фосамила примерно равен или немного ниже СКФ в почках. Исследования транспортеров in vitro показывают, что активная секреция не способствует почечной элиминации цефтаролина фосамила. Средний T1/2 цефтаролина фосамила у здоровых взрослых людей составляет примерно 2,5 ч. После однократного в/в введения 600 мг меченного изотопом цефтаролина фосамила здоровым взрослым мужчинам примерно 88% радиоактивности обнаруживалось в моче и 6% — в фекалиях.
Особые группы пациентов
Почечная недостаточность. После однократной в/в инфузии 600 мг цефтаролина фосамила в течение 60 мин Сmax в плазме составила (28,4 ±6,9), (28,2 ±5,4) и (30,8 ±4,9) мкг/мл у пациентов с нормальной функцией почек, легкой почечной недостаточностью и почечной недостаточностью средней степени тяжести соответственно. Сmax цефтаролина фосамила достигалась приблизительно через 60 мин после начала инфузии. AUC цефтаролина увеличивалась пропорционально степени почечной недостаточности и составила (75,6 ±9,7), (92,3 ±25,3) и (114,8 ±14,1) мкг·ч/мл у пациентов с нормальной функцией почек, легкой почечной недостаточностью и почечной недостаточностью средней степени тяжести соответственно.
Пациентам с почечной недостаточностью средней и тяжелой степени, терминальной стадией почечной недостаточности, включая пациентов, находящихся на гемодиализе, требуется коррекция дозы.
Печеночная недостаточность. Исследования фармакокинетики цефтаролина фосамила у пациентов с печеночной недостаточностью не проводили. Так как цефтаролина фосамил не подвергается печеночному метаболизму в значительной степени, не ожидается, что печеночная недостаточность будет существенно влиять на системный клиренс цефтаролина. Поэтому не рекомендуется корректировать дозу у пациентов с печеночной недостаточностью.
Пожилые пациенты (≥65 лет). После однократного в/в введения 600 мг цефтаролина фосамила параметры фармакокинетики были схожими у здоровых пожилых людей (≥65 лет) и молодых пациентов (18–45 лет). У пожилых добровольцев отмечено небольшое увеличение AUC0–∞ (на 33%), что обусловлено главным образом возрастными изменениями функции почек. Не требуется коррекция дозы у пожилых пациентов с Cl креатинина >50 мл/мин.
Дети. Безопасность и эффективность цефтаролина фосамила у детей в возрасте до 18 лет не установлены.
Пол. Параметры фармакокинетики цефтаролина фосамила были схожими у мужчин и женщин. Не требуется коррекция дозы в зависимости от пола пациента.
Раса. Не наблюдались существенные различия параметров фармакокинетики цефтаролина фосамила у пациентов, принадлежащих к разным этническим группам. Не требуется корректировать дозу в зависимости от расы пациента.
Показания к применению
Осложненные инфекции кожи и мягких тканей, вызванные чувствительными штаммами следующих грамположительных и грамотрицательных микроорганизмов: Staphylococcus aureus (включая метициллинрезистентные), Streptococcus pyogenes, Streptococcus agalactiae, Streptococcus anginosus, Streptococcus dysgalactiae, Escherichia coli, Klebsiella pneumoniae, Klebsiella oxytoca и Morganella morganii; внебольничная пневмония, вызванная чувствительными штаммами следующих грамположительных и грамотрицательных микроорганизмов: Streptococcus pneumoniae (включая случаи, сопровождающиеся бактериемией), Staphylococcus aureus (только метициллинчувствительные), Haemophilus influenzae, Haemophilus parainfluenzae, Klebsiella pneumoniae и Escherichia coli.
Противопоказания
Повышенная чувствительность к цефтаролина фосамилу или L-аргинину; повышенная чувствительность к цефалоспоринам; тяжелые реакции повышенной чувствительности немедленного типа (например анафилактическая реакция) на любое другое антибактериальное средство, имеющее бета-лактамную структуру (например пенициллины или карбапенемы); детский возраст до 18 лет.
Ограничения к применению
Судорожный синдром в анамнезе.
Применение при беременности и кормлении грудью
Категория действия на плод по FDA — B.
Клинические данные о применении цефтаролина фосамила у беременных женщин отсутствуют. Исследования на животных не выявили неблагоприятное воздействие цефтаролина фосамила на фертильность, беременность, роды или послеродовое развитие. Цефтаролина фосамил не следует применять во время беременности, за исключением случаев, когда потенциальная польза для матери превышает возможный риск для плода.
Данные о проникновении цефтаролина фосамила в грудное молоко отсутствуют. Однако в связи с тем, что многие бета-лактамные антибиотики выделяются с грудным молоком, в случае необходимости терапии цефтаролина фосамилом рекомендуется прекращение грудного вскармливания.
Побочные действия
Объединенные исследования фазы 3
В четырех клинических исследованиях по показаниям осложненные инфекции кожи и мягких тканей и внебольничная пневмония с участием 1305 взрослых пациентов, цефторалина фосамил назначался в дозе 600 мг в виде в/в инфузии продолжительностью 60 мин каждые 12 ч.
Наиболее частыми нежелательными реакциями, развившимися у ≥3% больных, получавших цефтаролина фосамил, были диарея, головная боль, тошнота и зуд, которые были обычно слабо или умеренно выраженными.
Дополнительные исследования фазы 3
В исследовании по показанию внебольничная пневмония, которое проводилось в азиатских странах с участием 381 взрослого пациента, профиль безопасности цефтаролина фосамила (600 мг в виде в/в инфузии продолжительностью 60 мин каждые 12 ч) соответствовал профилю безопасности в объединенных клинических исследованиях фазы 3 по показаниям осложненные инфекции кожи и мягких тканей и внебольничная пневмония.
В исследовании по показанию осложненные инфекции кожи и мягких тканей с участием 506 взрослых пациентов цефтаролина фосамил назначался в дозе 600 мг в виде в/в инфузии продолжительностью 120 мин каждые 8 ч (см. «Меры предосторожности»).
Ниже представлены нежелательные реакции, отмечавшиеся в объединенных клинических исследованиях фазы 3 по показаниям осложненные инфекции кожи и мягких тканей и внебольничная пневмония (1305 взрослых пациентов в группе терапии цефтаролина фосамилом). Частота нежелательных реакций по органам и системам представлена в виде следующей градации: очень часто (≥1/10); часто (≥1/100, <1/10); нечасто (≥1/1000, <1/100); редко (≥1/10000, <1/1000).
Отклонения лабораторных показателей: очень часто — положительная прямая проба Кумбса (см. «Меры предосторожности»); нечасто — удлинение ПВ, АЧТВ, МНО.
Со стороны ЖКТ: часто — диарея, тошнота, рвота, боль в животе, запор.
Со стороны нервной системы: часто — головная боль, головокружение; нечасто — судороги.
Со стороны кожи и подкожных тканей: часто — сыпь, зуд; нечасто — крапивница.
Со стороны печени и желчевыводящих путей: часто — повышение активности трансаминаз; нечасто — гепатит.
Со стороны ССС: часто — флебит, брадикардия; нечасто — ощущение сердецбиения.
Со стороны обмена веществ и нарушения питания: часто — гипергликемия, гипокалиемия; нечасто — гиперкалиемия.
Общие расстройства и реакции в месте введения: часто — лихорадка, реакции в месте введения (эритема, флебит, боль).
Со стороны крови и лимфатической системы: нечасто — анемия, лейкопения, нейтропения, тромбоцитопения; редко — эозинофилия.
Со стороны иммунной системы: нечасто — гиперчувствительность/анафилаксия (см. «Меры предосторожности», «Противопоказания»), отек губ и лица.
Инфекции и инвазии: нечасто — колит, вызванный Clostridium difficile (см. «Меры предосторожности»).
Со стороны почек и мочевыводящих путей: нечасто — нарушение функции почек (повышение концентрации креатинина в крови).
Описание отдельных нежелательных реакций
Сыпь. Сыпь часто отмечалась у пациентов с осложненными инфекциями кожи и мягких тканей, получавших цефтаролина фосамил в дозе 600 мг как в виде в/в инфузии продолжительностью 60 мин каждые 12 ч (в объединенных исследованиях фазы 3), так и в виде в/в инфузии продолжительностью 120 мин каждые 8 ч. Однако в подгруппе пациентов монголоидной расы, получавших цефтаролина фосамил каждые 8 ч, сыпь отмечалась очень часто (18,5%).
Взаимодействие
Клинические исследования по изучению лекарственного взаимодействия с цефтаролина фосамилом не проводились.
В исследованиях in vitro цефтаролина фосамил не ингибировал изоферменты цитохрома Р450 CYP1A1, CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1 и CYP3A4 и не индуцировал изоферменты CYP1A2, CYP2B6, CYP2C8, CYP2C9, CYP2C19 или CYP3A4/5. В связи с этим вероятность взаимодействия цефтаролина фосамил с ЛС, которые метаболизируются под действием изоферментов системы цитохрома Р450, низка. Цефтаролина фосамил не метаболизируется под действием изоферментов цитохрома Р450 in vitro, поэтому маловероятно влияние на параметры фармакокинетики цефтаролина фосамила при совместном применении с индукторами или ингибиторами изоферментов цитохрома Р450.
In vitro цефтаролина фосамил не переносится эффлюксными транспортерами P-gp или BCRP. Цефтаролина фосамил не ингибирует P-gp, следовательно взаимодействие с его субстратами, такими как дигоксин, не ожидается. Цефтаролина фосамил является слабым ингибитором BCRP, но данный эффект не имеет клинической значимости.
Исследования in vitro показали, что цефтаролина фосамил не является субстратом и не ингибирует транспортеры органических катионов (ОСТ2) и анионов (ОАТ1, ОАТ3) в почках, поэтому маловероятно взаимодействие с ЛС, которые ингибируют активную почечную секрецию (например пробенецид) или являются субстратами этих транспортеров.
Взаимодействие с другими антибактериальными ЛС. Тесты in vitro не выявили антагонизма при совместном применении цефтаролина фосамила и амикацина, азитромицина, азтреонама, даптомицина, левофлоксацина, линезолида, меропенема, тигециклина и ванкомицина.
Передозировка
Данные о передозировке ограничены. Вероятность передозировки выше у пациентов с нарушением функции почек. При применении цефтаролина фосамила в дозах выше рекомендованных наблюдались схожие нежелательные реакции, как и применении в рекомендованных дозах.
Лечение: симптоматическое.
Цефтаролина фосамил частично выводится с помощью гемодиализа.
Способ применения и дозы
В/в, в виде инфузии в течение 60 мин. Доза и продолжительность терапии устанавливаются в зависимости от типа и тяжести инфекции и ответа пациента на терапию.
Меры предосторожности
При применении цефтаролина фосамила необходимо руководствоваться официальными рекомендациями по надлежащему использованию антибактериальных ЛС.
Реакции гиперчувствительности
Как и при применении других бета-лактамных антибиотиков, возможно развитие серьезных реакций гиперчувствительности (иногда с летальным исходом).
У пациентов с гиперчувствительностью к цефалоспоринам, пенициллинам или другим бета-лактамным антибиотикам в анамнезе может также развиться аллергическая реакция на цефтаролина фосамил. Перед началом терапии следует тщательно изучить данные пациента на предмет выявления реакций гиперчувствительности к бета-лактамным антибиотикам. Цефтаролина фосамил противопоказан пациентам с повышенной чувствительностью к цефалоспоринам в анамнезе. Также он противопоказан пациентам, у которых ранее отмечались тяжелые реакции повышенной чувствительности немедленного типа (например анафилактическая реакция) на любое другое антибактериальное средство, имеющее бета-лактамную структуру (например пенициллины или карбапенемы).
При развитии тяжелой аллергической реакции необходимо прекратить введение цефтаролина фосамила и принять соответствующие меры.
Диарея, ассоциированная с Clostridium difficile
При применении почти всех антибактериальных ЛС, в т.ч. цефтаролина фосамила, сообщалось о развитии антнбиотикассоциированного колита и псевдомембранозного колита, которые могут варьировать по тяжести от легких до угрожающих жизни форм. Следует принимать во внимание возможность развития колита при возникновении диареи на фоне применения цефтаролина фосамила. В этом случае необходимо прекратить терапию, проводить поддерживающие мероприятия и назначить специфическое лечение Clostridium difficile.
Пациенты с судорожным синдромом в анамнезе
Как и при применении других цефалоспоринов, в исследованиях токсичности цефтаролина фосамила наблюдалось развитие судорог при приеме в дозах, превышающих Сmax в 7–25 раз. Опыт применения цефтаролина фосамила у пациентов с судорожным синдромом в анамнезе ограничен, в связи с чем следует соблюдать осторожность при его применении у этой группы пациентов.
Прямой антиглобулиновый тест (проба Кумбса)
Положительный прямой антиглобулиновый тест (ПАТ) может быть получен на фоне применения цефалоспоринов. Частота положительного ПАТ у пациентов, получавших цефтаролина фосамил в дозе 600 мг в виде в/в инфузии продолжительностью 60 мин каждые 12 ч, составила 10,7% в объединенных исследованиях фазы 3 и 32,3% в исследовании, где цефтаролина фосамил назначали в дозе 600 мг в виде в/в инфузии продолжительностью 120 мин каждые 8 ч. Ни у одного пациента с положительным ПАТ на фоне применения цефтаролина фосамила не выявлены признаки гемолиза.
Нечувствительные микроорганизмы
При применении цефтаролина фосамила, как и других антибиотиков, может развиться суперинфекция.
Влияние на способность управлять транспортными средствами и работать с механизмами. Не проводились исследования по изучению влияния цефтаролина фосамила на способность к вождению автотранспорта и управлению иными механизмами. Во время терапии может возникать головокружение, поэтому следует соблюдать осторожность при управлении транспортными средствами и занятиях другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций. При появлении описанного выше нежелательного явления следует воздержаться от выполнения указанных видов деятельности.
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Зинфоро — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-001912
Торговое название:
Зинфоро® (Zinforo®)
Международное непатентованное название:
цефтаролина фосамил
Лекарственная форма:
порошок для приготовления концентрата для приготовления раствора для инфузий
СОСТАВ
В 1 флаконе содержится:
Активное вещество: цефтаролина фосамила ацетат моногидрат 668,4 мг,эквивалентный цефтаролину фосамилу 600,0 мг.
Вспомогательное вещество: L-аргинин 395,0 мг
ОПИСАНИЕ
Порошок от желтовато-белого до светло-желтого цвета
Фармакотерапевтическая группа:
Антибиотик, цефалоспорин
ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА
Фармакодинамика
После внутривенного введения пролекарство цефтаролина фосамил быстро превращается в активный цефтаролин.
Механизм действия
Цефтаролин – антибиотик класса цефалоспоринов с активностью в отношении грамположительных и грамотрицательных микроорганизмов. В исследованиях in vitro показано бактерицидное действие цефтаролина, обусловленное ингибированием биосинтеза клеточной стенки бактерий за счет связывания с пенициллинсвязывающими белками (ПСБ). Цефтаролин проявляет бактерицидную активность в отношении метициллин-резистентного Staphylococcus aureus (MRSA) и в отношении пенициллин-нечувствительного Streptococcus pneumoniae (PNSP) в связи с его высоким сродством к измененным ПСБ этих микроорганизмов.
Связь фармакокинетики и фармакодинамики
Антимикробная активность цефтаролина, также как и других бета-лактамных антибиотиков, лучше всего коррелирует с интервалом времени, в течение которого концентрация препарата остается выше минимальной подавляющей концентрации (МПК) инфицирующего микроорганизма (%T > МПК).
Механизм резистентности
Цефтаролин не активен в отношении штаммов Enterobacteriaceae, продуцирующих бета-лактамазы расширенного спектра (БЛРС) семейств TEM, SHV или CTX-M, сериновые карбапенемазы (такие как KPC), металло-бета-лактамазы класса В или класса С (цефалоспориназы AmpC). Резистентность также может быть связана с нарушением проницаемости клеточной стенки бактерий или с активным выведением антибиотика (эффлюкс). Микроорганизм может обладать одним или несколькими механизмами резистентности.
Перекрестная резистентность
Несмотря на возможное развитие перекрестной резистентности, некоторые штаммы, резистентные к другим цефалоспоринам, могут быть чувствительны к цефтаролину.
Микроорганизмы, обладающие природной резистентностью: Chlamydophila spp. Legionella spp. Mycoplasma spp. Proteus spp. Pseudomonas aeruginosa
Взаимодействие с другими антимикробными препаратами
Исследования in vitro не выявили антагонизма при применении цефтаролина в комбинации с другими часто назначаемыми антимикробными препаратами (такими как амикацин, азитромицин, азтреонам, даптомицин, левофлоксацин, линезолид, меропенем, тигециклин и ванкомицин).
Чувствительность
Чувствительность антибиотиков in vitro меняется в зависимости от географического региона и с течением времени, поэтому при выборе антибактериальной терапии необходимо учитывать местную информацию о резистентности. Если локальная резистентность такова, что эффективность препарата в отношении некоторых инфекций становится сомнительной, необходимо обратиться за консультацией к эксперту. Чувствительность к цефтаролину должна определяться с помощью стандартных методов. Интерпретацию результатов следует проводить в соответствии с локальными руководствами. Клиническая эффективность в отношении отдельных патогенных микроорганизмов Ниже перечислены патогенные микроорганизмы (по показаниям к применению), чувствительные к цефтаролину in vitro, в отношении которых в клинических исследованиях была показана эффективность цефтаролина.
Осложненные инфекции кожи и мягких тканей
Грамположительные микроорганизмы
Staphylococcus aureus (включая метициллин-резистентные штаммы)
Streptococcus pyogenes
Streptococcus agalactiae
Группа Streptococcus anginosus (включает S. anginosus, S. intermedius и S. constellatus) Streptococcus dysgalactiae
Грамотрицательные микроорганизмы
Escherichia coli
Klebsiella pneumoniae
Klebsiella oxytoca
Morganella morganii
Внебольничная пневмония
Грамположительные микроорганизмы
Streptococcus pneumoniaе (включая случаи, сопровождающиеся бактериемией) Staphylococcus aureus (только метициллин-чувствительные штаммы)
Грамотрицательные микроорганизмы
Escherichia coli
Haemophilus influenzae
Haemophilus parainfluenzae
Klebsiella pneumoniae
Эффективность в отношении других значимых патогенных микроорганизмов Клиническая эффективность цефтаролина в отношении перечисленных ниже патогенных микроорганизмов не была установлена, однако результаты исследований in vitro позволяют предполагать, что они чувствительны к цефтаролину в отсутствие приобретенных механизмов резистентности.
Грамположительные анаэробы Peptostreptococcus spp.
Грамотрицательные анаэробы Fusobacterium spp.
Фармакокинетика
Максимальная концентрация (Cmax) и площадь под кривой «концентрация-время» (AUC) цефтаролина увеличиваются почти пропорционально дозе при однократном введении препарата в диапазоне доз от 50 до 1000 мг. Не наблюдалось заметной кумуляции цефтаролина после многократного внутривенного введения препарата в дозе 600 мг в течение 60 минут каждые 12 часов в течение 14 дней здоровым добровольцам с нормальной функцией почек.
Распределение
Степень связывания цефтаролина с белками плазмы низкая (примерно 20%), препарат не проникает в эритроциты. Медиана объема распределения в равновесном состоянии у здоровых взрослых мужчин после однократного внутривенного введения 600 мг цефтаролина фосамила, меченного изотопом, составила 20,3 л, почти как и объем внеклеточной жидкости.
Метаболизм
В плазме крови под действием фосфатаз пролекарство цефтаролина фосамил быстро преобразуется в активный цефтаролин; концентрации пролекарства поддаются измерению в плазме, преимущественно, во время внутривенной инфузии. При гидролизе бета-лактамного кольца цефтаролина образуется микробиологически неактивный метаболит, цефтаролин М-1. Соотношение средних значений AUC цефтаролина М-1 к цефтаролину в плазме крови после однократного внутривенного введения 600 мг цефтаролина фосамила здоровым добровольцам составляет примерно 20-30%. Метаболизм цефтаролина протекает без участия изоферментов системы цитохрома P450.
Экскреция
Цефтаролин выводится, преимущественно, почками. Почечный клиренс цефтаролина примерно равен или немного ниже скорости клубочковой фильтрации в почках. Исследования транспортеров in vitro показывают, что активная секреция не способствует почечной элиминации цефтаролина. Средний период полувыведения цефтаролина у здоровых взрослых людей составляет примерно 2,5 часа. После однократного внутривенного введения 600 мг меченного изотопом цефтаролина фосамила здоровым взрослым мужчинам примерно 88% радиоактивности обнаруживалось в моче и 6% – в фекалиях.
Особые группы пациентов
Почечная недостаточность
После однократной внутривенной инфузии 600 мг цефтаролина фосамила в течение 60 минут Cmax цефтаролина в плазме составила 28,4 ± 6,9 мкг/мл, 28,2 ± 5,4 мкг/мл и 30,8 ± 4,9 мкг/мл у пациентов с нормальной функцией почек, легкой почечной недостаточностью и почечной недостаточностью средней степени тяжести, соответственно. Cmax цефтаролина достигалась приблизительно через 60 минут после начала инфузии. AUC цефтаролина увеличивалась пропорционально степени почечной недостаточности и составила 75,6 ± 9,7 мкг×ч/мл, 92,3 ± 25,3 мкг×ч/мл и 114,8 ± 14,1 мкг×ч/мл у пациентов с нормальной функцией почек, легкой почечной недостаточностью и почечной недостаточностью средней степени тяжести, соответственно. Пациентам с почечной недостаточностью средней и тяжелой степени, терминальной стадией почечной недостаточности, включая пациентов, находящихся на гемодиализе, требуется коррекция дозы (см. раздел «Способ применения и дозы»).
Печеночная недостаточность
Исследования фармакокинетики цефтаролина у пациентов с печеночной недостаточностью не проводили. Так как цефтаролин не подвергается печеночному метаболизму в значительной степени, не ожидается, что печеночная недостаточность будет существенно влиять на системный клиренс цефтаролина. Поэтому не рекомендуется корректировать дозу препарата у пациентов с печеночной недостаточностью.
Пожилые пациенты (≥ 65 лет)
После однократного внутривенного введения 600 мг цефтаролина фосамила параметры фармакокинетики препарата были схожими у здоровых пожилых людей (≥ 65 лет) и здоровых молодых пациентов (18-45 лет). У пожилых добровольцев отмечено небольшое увеличение AUC0-∞ (на 33%), что обусловлено, главным образом, возрастными изменениями функции почек. Не требуется коррекции дозы препарата у пожилых пациентов с клиренсом креатинина выше 50 мл/мин.
Дети
Безопасность и эффективность препарата Зинфоро® у детей в возрасте до 18 лет не установлены.
Пол
Параметры фармакокинетики цефтаролина были схожими у мужчин и женщин. Не требуется коррекции дозы в зависимости от пола пациента.
Раса
Не наблюдалось существенных различий параметров фармакокинетики цефтаролина у пациентов, принадлежащих к разным этническим группам. Не требуется корректировать дозу препарата в зависимости от расы пациента.
ПОКАЗАНИЯ
Препарат Зинфоро® показан для лечения у взрослых следующих инфекций:
• осложненные инфекции кожи и мягких тканей, вызванные чувствительными штаммами следующих грамположительных и грамотрицательных микроорганизмов: Staphylococcus aureus (включая метициллин-резистентные штаммы), Streptococcus pyogenes, Streptococcus agalactiae, Streptococcus anginosus, Streptococcus dysgalactiae, Escherichia coli, Klebsiella pneumoniae, Klebsiella oxytoca и Morganella morganii;
• внебольничная пневмония, вызванная чувствительными штаммами следующих грамположительных и грамотрицательных микроорганизмов: Streptococcus pneumoniae (включая случаи, сопровождающиеся бактериемией), Staphylococcus aureus (только метициллин-чувствительные штаммы), Haemophilus influenzae, Haemophilus parainfluenzae, Klebsiella pneumoniae и Escherichia coli
ПРОТИВОПОКАЗАНИЯ
- Повышенная чувствительность к цефтаролина фосамилу или L-аргинину.
- Повышенная чувствительность к цефалоспоринам.
- Тяжелые реакции повышенной чувствительности немедленного типа (например, анафилактическая реакция) на любое другое антибактериальное средство, имеющее бета-лактамную структуру (например, пенициллины или карбапенемы).
- Детский возраст до 18 лет.
С ОСТОРОЖНОСТЬЮ: судорожный синдром в анамнезе.
ПРИМЕНЕНИЕ ПРИ БЕРЕМЕННОСТИ И В ПЕРИОД ГРУДНОГО ВСКАРМЛИВАНИЯ
Беременность
Клинические данные о применении цефтаролина фосамила у беременных женщин отсутствуют. Исследования на животных не выявили неблагоприятного воздействия цефтаролина фосамила на фертильность, беременность, роды или послеродовое развитие. Препарат Зинфоро® не следует применять во время беременности, за исключением случаев, когда потенциальная польза для матери превышает возможный риск для плода.
Период грудного вскармливания
Данные о проникновении цефтаролина в грудное молоко отсутствуют. Однако, в связи с тем, что многие бета-лактамные антибиотики выделяются с грудным молоком, в случае необходимости терапии препаратом Зинфоро® рекомендуется прекращение грудного вскармливания.
СПОСОБ ПРИМЕНЕНИЯ И ДОЗЫ
Зинфоро® вводится внутривенно в виде инфузии в течение 60 минут (см. «Приготовление раствора для инфузий»).
Продолжительность терапии должна устанавливаться в зависимости от типа и тяжести инфекции, ответа пациента на терапию.
Рекомендуется следующий режим дозирования:
Применение у особых групп пациентов
Почечная недостаточность
Если клиренс креатинина (КК) ≤ 50 мл/мин, дозу препарата следует корректировать следующим образом:
1. Рассчитывается по формуле Кокрофта-Голта.
2. Цефтаролин удаляется при гемодиализе. Препарат следует вводить по окончании процедуры гемодиализа в дни её проведения.
Печеночная недостаточность
Нет необходимости корректировать дозу препарата у пациентов с печеночной недостаточностью.
Пожилые пациенты (≥ 65 лет)
Нет необходимости корректировать дозу препарата у пожилых пациентов с КК > 50 мл/мин.
Дети
Безопасность и эффективность препарата Зинфоро® у детей в возрасте до 18 лет не установлены.
Приготовление раствора для инфузий
При приготовлении и введении препарата необходимо соблюдать стандартные правила асептики. Каждый флакон предназначен только для однократного применения.
Зинфоро® порошок для приготовления концентрата для приготовления раствора для инфузий следует растворить в 20 мл стерильной воды для инъекций. Один мл концентрата содержит 30 мг цефтаролина фосамила. Полученный концентрат представляет собой раствор бледно-желтого цвета, свободный от видимых частиц. Концентрат необходимо немедленно использовать, не хранить (время от начала растворения порошка до полного приготовления раствора для внутривенных инфузий не должно превышать 30 минут).
Для приготовления раствора для инфузий полученный концентрат встряхивают и переносят в инфузионный флакон, содержащий одну из перечисленных ниже совместимых инфузионных жидкостей:
- 0,9% раствор натрия хлорида,
- 5% раствор декстрозы,
- 0,45% раствор натрия хлорида и 2,5% раствор декстрозы,
- раствор Рингер лактат.
При применении дозы препарата 600 мг во флакон с совместимой инфузионной жидкостью переносят весь полученный концентрат (20 мл), при применении дозы 400 мг — 14 мл концентрата. Для применения дозы 300 мг следует перенести 10 мл концентрата, а для дозы 200 мг — 7 мл концентрата. Раствор для инфузий можно приготовить путем добавления концентрата во флакон с инфузионной жидкостью объемом 50 мл, 100 мл или 250 мл. После приготовления раствора для инфузий его следует использовать в течение 6 часов с момента приготовления. Приготовленный раствор для инфузий сохраняет стабильность в течение 24 часов при хранении в холодильнике (2-8°С).
После извлечения из холодильника раствор для инфузий необходимо использовать в течение 6 часов при комнатной температуре.
Неиспользованный препарат или отходы необходимо утилизировать в соответствии с местными требованиями.
ПОБОЧНОЕ ДЕЙСТВИЕ
Объединенные исследования фазы 3
В четырех клинических исследованиях по показаниям осложненные инфекции кожи и мягких тканей и внебольничная пневмония с участием 1305 взрослых пациентов, препарат Зинфоро® назначался в дозе 600 мг в виде внутривенной инфузии продолжительностью 60 минут каждые 12 часов.
Наиболее частыми нежелательными реакциями, развившимися у ≥ 3% больных, получавших цефтаролин, были диарея, головная боль, тошнота и зуд, которые были обычно слабо или умеренно выраженными.
Дополнительные исследования фазы 3
В исследовании по показанию внебольничная пневмония, которое проводилось в азиатских странах с участием 381 взрослого пациента, профиль безопасности препарата Зинфоро® (600 мг в виде внутривенной инфузии продолжительностью 60 минут каждые 12 часов) соответствовал профилю безопасности в объединенных клинических исследованиях фазы 3 по показаниям осложненные инфекции кожи и мягких тканей и внебольничная пневмония.
В исследовании по показанию осложненные инфекции кожи и мягких тканей с участием 506 взрослых пациентов препарат Зинфоро® назначался в дозе 600 мг в виде внутривенной инфузии продолжительностью 120 минут каждые 8 часов (см. далее по тексту раздела и раздел «Особые указания»).
Ниже представлены нежелательные реакции, отмечавшиеся в объединенных клинических исследованиях фазы 3 по показаниям осложненные инфекции кожи и мягких тканей и внебольничная пневмония (1305 взрослых пациентов в группе терапии Зинфоро®). Частота нежелательных реакций представлена в виде следующей градации: очень часто (≥ 1/10), часто (≥ 1/100, < 1/10), нечасто (≥ 1/1000, < 1/100), редко (≥ 1/10000, < 1/1000).
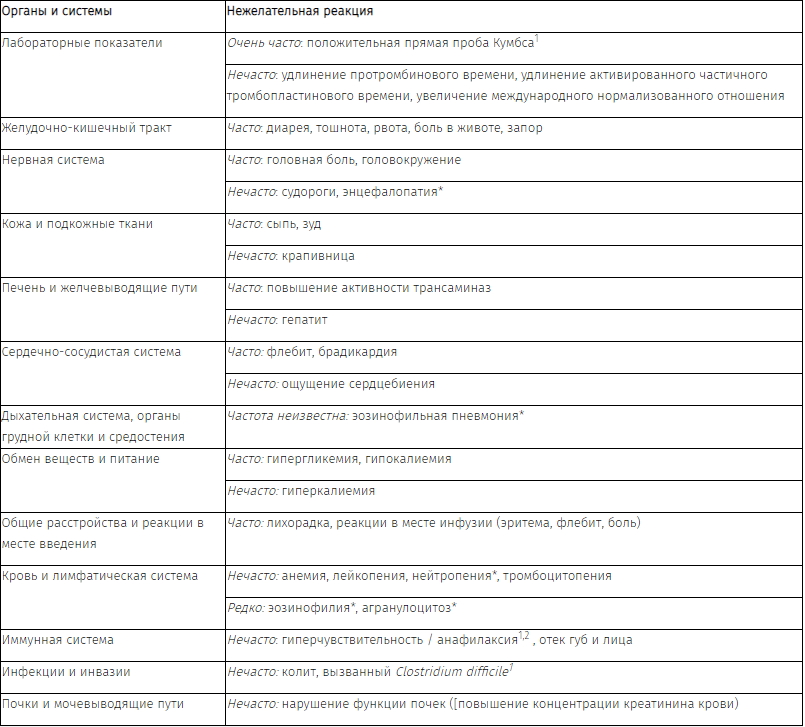
Частота развития нежелательных реакций по классу системы органов
|
Органы и системы |
Нежелательная реакция |
|
Лабораторные показатели |
Очень часто: положительная прямая проба Кумбса1 |
|
Нечасто: удлинение протромбинового времени, |
|
|
удлинение активированного частичного тромбопластинового времени, увеличение международного нормализованного отношения |
|
|
Желудочно-кишечный тракт |
Часто: диарея, тошнота, рвота, боль в животе, запор |
|
Нервная система |
Часто: головная боль, головокружение |
|
Нечасто: судороги |
|
|
Кожа и подкожные ткани |
Часто: сыпь, зуд |
|
Нечасто: крапивница |
|
|
Печень и желчевыводящие пути |
Часто: повышение активности трансаминаз |
|
Нечасто: гепатит |
|
|
Сердечно-сосудистая система |
Часто: флебит, брадикардия |
|
Нечасто: ощущение сердцебиения |
|
|
Обмен веществ и питание |
Часто: гипергликемия, гипокалиемия |
|
Нечасто: гиперкалиемия |
|
|
Общие расстройства и реакции в месте введения |
Часто: лихорадка, реакции в месте инфузии (эритема, флебит, боль) |
|
Кровь и лимфатическая система |
Нечасто: анемия, лейкопения, нейтропения, тромбоцитопения |
|
Редко: эозинофилия |
|
|
Иммунная система |
Нечасто: гиперчувствительность / анафилаксия1,2, отек губ и лица |
|
Инфекции и инвазии |
Нечасто: колит, вызванный Clostridium difficile1 |
|
Почки и мочевыводящие пути |
Нечасто: нарушение функции почек (повышение концентрации креатинина крови) |
1. См. раздел «Особые указания».
2. См. раздел «Противопоказания».
Описание отдельных нежелательных реакций
Сыпь
Сыпь часто отмечалась у пациентов с осложненными инфекциями кожи и мягких тканей, получавших цефтаролина фосамил в дозе 600 мг как в виде внутривенной инфузии продолжительностью 60 минут каждые 12 часов (в объединенных исследованиях фазы 3), так и в виде внутривенной инфузии продолжительностью 120 минут каждые 8 часов. Однако в подгруппе пациентов монголоидной расы, получавших цефтаролина фосамил каждые 8 часов, сыпь отмечалась очень часто (18,5%).
ПЕРЕДОЗИРОВКА
Данные о передозировке ограничены. Вероятность передозировки выше у пациентов с нарушением функции почек. При применении препарата в дозах выше рекомендованных наблюдались схожие нежелательные реакции, как и при применении препарата в рекомендованных дозах.
Лечение: симптоматическое. Цефтаролин частично выводится с помощью гемодиализа.
ВЗАИМОДЕЙСТВИЕ С ДРУГИМИ ЛЕКАРСТВЕННЫМИ СРЕДСТВАМИ И ДРУГИЕ ВИДЫ ЛЕКАРСТВЕННОГО ВЗАИМОДЕЙСТВИЯ
Клинические исследования по изучению лекарственного взаимодействия с цефтаролином не проводились.
В исследованиях in vitro цефтаролин не ингибировал изоферменты цитохрома P450 CYP1A1, CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1 и CYP3A4 и не индуцировал изоферменты CYP1A2, CYP2B6, CYP2C8, CYP2C9, CYP2C19, или CYP3A4/5. В связи с этим вероятность взаимодействия цефтаролина с препаратами, которые метаболизируются под действием изоферментов системы цитохрома Р450, низка.
Цефтаролин не метаболизируется под действием изоферментов цитохрома P450 in vitro, поэтому, маловероятно влияние на параметры фармакокинетики цефтаролина при совместном применении с индукторами или ингибиторами изоферментов цитохрома P450. In vitro цефтаролин не переносится эффлюксными транспортерами P-gp или BCRP. Цефтаролин не ингибирует P-gp, следовательно, взаимодействие с субстратами, такими как дигоксин, не ожидается. Цефтаролин является слабым ингибитором BCRP, но данный эффект не имеет клинической значимости. Исследования in vitro показали, что цефтаролин не является субстратом, и не ингибировал транспортеры органических катионов (OCT2) и анионов (OAT1, OAT3) в почках; поэтому, маловероятно взаимодействие с препаратами, которые ингибируют активную почечную секрецию (например, пробенецид) или с препаратами, которые являются субстратами этих транспортеров.
Взаимодействие с другими антибактериальными препаратами
Тесты in vitro не выявили антагонизма при совместном применении цефтаролина и других часто используемых антибактериальных препаратов (например, амикацина, азитромицина, азтреонама, даптомицина, левофлоксацина, линезолида, меропенема, тигециклина и ванкомицина).
ОСОБЫЕ УКАЗАНИЯ
При применении препарата необходимо руководствоваться официальными рекомендациями по надлежащему использованию антибактериальных препаратов.
Реакции гиперчувствительности
Как и при применении всех бета-лактамных антибиотиков, возможно развитие серьёзных реакций гиперчувствительности (иногда с летальным исходом).
У пациентов с гиперчувствительностью к цефалоспоринам, пенициллинам или другим бета-лактамным антибиотикам в анамнезе может также развиться аллергическая реакция на цефтаролина фосамил. Перед началом терапии препаратом Зинфоро® следует тщательно изучить данные пациента на предмет выявления реакций гиперчувствительности к бета-лактамным антибиотикам.
Препарат противопоказан пациентам с повышенной чувствительностью к цефалоспоринам в анамнезе. Также препарат противопоказан пациентам, у которых ранее отмечались тяжелые реакции повышенной чувствительности немедленного типа (например, анафилактическая реакция) на любое другое антибактериальное средство, имеющее бета-лактамную структуру (например, пенициллины или карбапенемы). При развитии тяжелой аллергической реакции необходимо прекратить введение лекарственного препарата и принять соответствующие меры.
Диарея, ассоциированная с Clostridium difficile
При применении почти всех антибактериальных препаратов, в том числе препарата Зинфоро®, сообщалось о развитии антибиотикоассоциированного колита и псевдомембранозного колита, которые могут варьировать по тяжести от легких до угрожающих жизни форм. Следует принимать во внимание возможность развития колита при возникновении диареи на фоне применения цефтаролина фосамила. В этом случае необходимо прекратить терапию препаратом Зинфоро®, проводить поддерживающие мероприятия и назначить специфическое лечение Clostridium difficile.
Пациенты с судорожным синдромом в анамнезе
Как и при применении других цефалоспоринов, в исследованиях токсичности цефтаролина наблюдалось развитие судорог при приеме препарата в дозах, превышающих Сmax в 7-25 раз. Опыт применения цефтаролина у пациентов с судорожным синдромом в анамнезе ограничен, в связи с чем следует соблюдать осторожность при применении препарата Зинфоро® у этой группы пациентов.
Прямой антиглобулиновый тест (проба Кумбса) Положительный прямой антиглобулиновый тест (ПАТ) может быть получен на фоне применения цефалоспоринов. Частота положительного ПАТ у пациентов, получавших цефтаролина фосамил в дозе 600 мг в виде внутривенной инфузии продолжительностью 60 минут каждые 12 часов, составила 10,7% в объединенных исследованиях фазы 3 и 32,3% в исследовании, где цефтаролина фосамил назначался в дозе 600 мг в виде внутривенной инфузии продолжительностью 120 минут каждые 8 часов. Ни у одного пациента с положительным ПАТ на фоне применения цефтаролина фосамила не выявлены признаки гемолиза.
Нечувствительные микроорганизмы
При применении цефтаролина фосамила, как и других антибиотиков, может развиться суперинфекция.
ВЛИЯНИЕ НА СПОСОБНОСТЬ УПРАВЛЯТЬ ТРАНСПОРТНЫМИ СРЕДСТВАМИ, МЕХАНИЗМАМИ
Не проводилось исследований по изучению влияния препарата Зинфоро® на способность к вождению автотранспорта и управлению иными механизмами. Во время терапии может возникать головокружение, поэтому следует соблюдать осторожность при управлении транспортными средствами и при занятиях другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций. При появлении описанного выше нежелательного явления следует воздержаться от выполнения указанных видов деятельности.
ФОРМА ВЫПУСКА
Порошок для приготовления концентрата для приготовления раствора для инфузий, 600 мг.
По 600 мг активного вещества в прозрачные стеклянные флаконы вместимостью 20 мл (тип I Евр.Фарм.) закрытые бромбутиловой резиновой пробкой с покрытием из фторированного полимера, закрытой сверху алюминиевым колпачком c полипропиленовой крышкой (“флип-офф”). По 1 или 10 флаконов с инструкцией по применению в картонную пачку с контролем первого вскрытия.
УСЛОВИЯ ХРАНЕНИЯ
При температуре не выше 30 °С. Хранить в местах, недоступных для детей.
СРОК ГОДНОСТИ
3 года. Не применять по истечении срока годности, указанного на упаковке.
УСЛОВИЯ ОТПУСКА
По рецепту.
НАИМЕНОВАНИЕ И АДРЕС ЮРИДИЧЕСКОГО ЛИЦА, НА ИМЯ КОТОРОГО ВЫДАНО РЕГИСТРАЦИОННОЕ УДОСТОВЕРЕНИЕ
АстраЗенека ЮК Лимитед, Великобритания 2 Кингдом Стрит, Лондон W2 6BD, Великобритания AstraZeneca UK Limited, United Kingdom 2 Kingdom Street, London W2 6BD, United Kingdom
ПРОИЗВОДИТЕЛЬ
ЭйСиЭс Добфар С.п.А. Виале Аддетта 4/12, 20067 Трибиано, Милан, Италия ACS Dobfar S.p.A. Viale Addetta, 4/12, 20067 Tribiano, Milano, Italy
ФАСОВЩИК (ПЕРВИЧНАЯ УПАКОВКА), УПАКОВЩИК (ВТОРИЧНАЯ (ПОТРЕБИТЕЛЬСКАЯ) УПАКОВКА), ВЫПУСКАЮЩИЙ КОНТРОЛЬ КАЧЕСТВА
Факта Фармачеутичи С.п.А.
Нуклео Индастриале С. Атто, 64100 Терамо, Италия
Facta Farmaceutici S.p.A
Nucleo Industriale S. Atto, 64100 Teramo, Italy
Дальнейшая информация предоставляется по требованию:
Представительство АстраЗенека ЮК Лимитед Великобритания в г. Москве и ООО АстраЗенека Фармасьютикалз:
125284 Москва, ул. Беговая д. 3, стр. 1
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Инструкция по применению
Описание препарата
Зинфоро порошок относится к группе бактерицидных медпрепаратов цефалоспорина с интенсивным уровнем in vitro против грамположительного и грамотрицательного вида бактерий. Антимикробное воздействие, обуславливается замедлением синтеза клеточных стенок, опосредуется связыванием с основными пенициллинсвязывающим белком (PBP).
Инструкция по применению Зинфоро информирует об активности против S. aureus обусловлена его сродством к PBP2a, а активность против S. pneumoniae обусловлена его сродством к PBP2x. Цефтаролин также проявляет активность против ванкомицин-резистентного S. aureus (VRSA), ванкомицин-нечувствительного S. aureus (VISA) и гетеростабильной ванкомицин-чувствительной S. aureus (hVISA). Ceftaroline не активен против грамотрицательных бактерий, которые продуцируют бета-лактамазы расширенного спектра (ESBL) из семейств TEM, SHV или CTX-M; сериновые карбапенемазы (то есть KPC); металл-бета-лактамазы класса B; или класса C (AmpC) цефалоспориназы.
Бета-лактамы, включая цефтаролин, проявляют не зависящее от концентрации или зависящее от времени убийство. Исследования на животных in vitro и in vivo продемонстрировали, что основным фармакодинамическим параметром, определяющим эффективность бета-лактамов, является количественное наличие свободных от времени (небелковых) концентраций препарата, превышающих минимальную ингибирующую концентрацию (MIC) организма (свободный T> MIC). Эта микробиологическая картина отзыва обусловлена механизмом действия, который является ацилированием PBP. Существует максимальная доля PBP, которые могут быть ацилированы; поэтому, как только максимальное ацилирование произошло, скорость убийства не может увеличиться. Свободные концентрации бета-лактама не должны оставаться выше MIC для всего интервала дозирования. Процент времени, необходимого для бактериостатической и максимальной бактерицидной активности, различен для различных классов бета-лактамов. Карбапенемы требуют концентрации свободных лекарств, чтобы превышать MIC 20% интервала дозирования для бактериостатической активности и 40% интервала дозирования для максимальной бактерицидной активности. Цефалоспорины требуют, чтобы концентрация свободных лекарств превышала ВПК на 35-40% интервала дозирования для бактериостатической активности и 60-70% интервала дозирования для бактерицидной активности. Пенициллины требуют концентрации свободных лекарств, чтобы превышать MIC в течение 30% интервала дозирования для достижения бактериостатической активности и 50% интервала дозирования для достижения бактерицидной активности. Пост-антибиотический эффект (PAE) представляется минимальным для S. pneumoniae и E. coli, но дольше для S. aureus (0,8-7,2 часа).
Цена препарата Зинфоро варьируется от 25 800 рублей.
Форма выпуска, состав и упаковка
Порошкообразное вещество для внутривенных инфузий. Компоненты: аргигин типа Л, цефтаролина фосамила ацетат моногидрат.
Показания
Согласно инструкции по применению Зинфоро, порошок имеет широкий спектр цефалоспоринового антибиотика. Используется для острой бактериальной инфекции кожи и структуры кожи и внебольничной пневмонии. Показания Зинфоро информируют о первом бета-лактам, одобренными для лечения устойчивых к метициллину S. aureus (MRSA), резистентных к ванкомицину S. aureus (VRSA), ванкомицин-нечувствительный S. aureus (VISA) и гетеростабильной ванкомицин-чувствительной S. aureus (hVISA)
Противопоказания
Противопоказания препарата включают в себя:
• тяжелые формы почечной недостаточности;
• дети до 18 лет;
• индивидуальная непереносимость цефтаролина;
• терминальная фаза поражения почек (с использованием гемодиализа);
• судорожный синдром;
• сильные реакции на цефтаролин фосамил.
Дозировка
Применение препарата обуславливается инструкцией по применению Зинфоро и рекомендациями врача. Для лечения острых бактериальных инфекций кожи и кожи (ABSSSI) из-за восприимчивых организмов.
Показания Зинфоро для приготовления внутривенной дозы
Взрослые
600 мг каждые 12 часов в течение 5-14 дней. Рекомендации по клинической практике предлагают zinforo как вариант для пациентов с зарегистрированными или подозреваемыми инфекциями MRSA.
Дети и подростки старше 2 лет весом более 33 кг
400 мг каждые 8 часов или 600 мг каждые 12 часов в течение 5-14 дней. Рекомендации по клинической практике предлагают цефтаролин как вариант для пациентов с зарегистрированными или подозреваемыми инфекциями MRSA.
Дети и подростки старше 2 лет весом не более 33 кг
12 мг/кг/доза каждые 8 часов в течение 5-14 дней. Рекомендации по клинической практике предлагают цефтаролин, как вариант для пациентов с зарегистрированными или подозреваемыми инфекциями MRSA.
Младенцы и дети от 2 месяцев до 2 лет
8 мг/кг/доза каждые 8 часов в течение 5-14 дней. Рекомендации по клинической практике предлагают Зинфоро, как вариант для пациентов с зарегистрированными или подозреваемыми инфекциями MRSA.
Для лечения бактериальной внебольничной пневмонии из-за восприимчивых организмов.
Внутривенная доза
Взрослые
600 мг каждые 12 часов в течение 5-7 дней.
Дети и подростки старше 2 лет весом более 33 кг
400 мг каждые 8 часов или 600 мг каждые 12 часов в течение 5-14 дней.
Дети и подростки старше 2 лет весом не более 33 кг
12 мг/кг/доза каждые 8 часов в течение 5-14 дней.
Младенцы и дети от 2 месяцев до 2 лет
8 мг/кг/доза каждые 8 часов в течение 5-14 дней.
Для лечения сепсиса.
Внутривенная доза
Взрослые
600 мг каждые 12 часов использовалось для других показаний. Начните в течение 1 часа после признания в рамках эмпирической мульти-лекарственной терапии. Продолжительность терапии обычно составляет от 7 до 10 дней, но может быть короче или длиннее в зависимости от реакции пациента, места заражения и выделенного патогена (ов). Лечение может быть сужено с идентификацией патогена и/или адекватным клиническим ответом. Цена препарата Зинфоро приемлема, поэтому необходимо приобрести его с запасом, чтобы исключить пропуск дозы.
Побочные действия
• гиперкалиемия;
• эозинофилия;
• анафилактический шок;
• брадикардия;
• флебит;
• почечная недостаточность;
• агранулоцитоз;
• повышенные печеночные ферменты;
• псевдомембранозный колит;
• запор;
• гепатит;
• гипергликемия;
• гипокалиемия;
• анемия;
• усиленное сердцебиение;
• лейкопения;
• диарея;
• сыпь;
• рвота;
• тошнота;
• зуд;
• лихорадка;
• тромбоцитопения;
• мигрени;
• боли в животе;
• крапивница;
• нейтропения;
• головокружение.
Лекарственное взаимодействие
Петлевые диуретики: нефротоксичность, связанная с цефалоспоринами, может быть усилена сопутствующей терапией фуросемидом. Клиницисты должны знать, что это может произойти даже у пациентов с незначительной или временной почечной недостаточностью.
Оральные контрацептивы: рекомендовано альтернативные или дополнительные контрацепции, когда оральные контрацептивы (ОК) используются в сочетании с антибиотиками. Ранее считалось, что антибиотики могут снижать эффективность OC, содержащих эстрогены, из-за стимуляции обмена веществ или снижения энтерогепатического кровообращения с помощью изменений флоры GI.
Антитуберкулезные препараты (например, рифампин или аналог) были единственными агентами, связанными с отказом OC и беременностью. Основываясь на результатах исследования, эти авторы рекомендовали, чтобы резервная контрацепция не требовалась, если OCs надежно используются во время использования антибиотиков. Другой обзор согласуется с этими данными, но отметил, что были идентифицированы отдельные пациенты, у которых наблюдалось значительное снижение концентрации в плазме комбинированных компонентов OC и которые, как оказалось, овулировали. Агенты, чаще всего связанные с этими изменениями, были: рифампицин, тетрациклины и производные пенициллина. Медики пришли к выводу, что, поскольку женщины, наиболее подвержены риску отказа или несоблюдения OC, не могут быть легко идентифицированы, и истинная частота таких событий может быть недооценена и с учетом серьезных последствий нежелательной беременности рекомендует рекомендовать дополнительный метод контрацепции во время коротких использование антибиотика может быть оправдано. При длительном применении антибиотиков риск взаимодействия с ОКС менее ясен, но альтернативные или дополнительные контрацептивы могут быть целесообразными в отдельных обстоятельствах. Данные о прогестиновых противозачаточных средствах или о новых комбинированных контрацептивных поставках (например, патчи, кольца) недоступны.
Пикосульфат натрия; Оксид магния; Безводная лимонная кислота: предварительное или одновременное применение антибиотиков с пикосульфатом натрия; оксид магния; безводная лимонная кислота может снизить эффективность подготовки кишечника, так как превращение пикосульфата натрия в его активный метаболит бис- (п-гидроксифенил) -пиридил-2-метан (BHPM) опосредуется кишечными бактериями. Если возможно, избегайте совместного администрирования. Некоторые антибиотики (то есть тетрациклины и хинолоны) могут хелатироваться с магнием в пикосульфате натрия; оксид магния; безводный раствор лимонной кислоты. Следовательно, эти антибиотики следует принимать не менее чем за 2 часа до и не менее чем через спустя 6 часов использования пикосульфата натрия; оксид магния; безводный раствор лимонной кислоты.
Период беременности и грудного вскармливания
Не существует достоверных клинических доказательств использования во время беременности. Данные о животных не обнаруживают тератогенных воздействий. За счет того, что организм животных, отличается от человеческого, и не дает возможности точно определить последствия препарата, зинфиро не стоит использовать беременным женщинам. Применение обуславливается только потенциальной пользой для матери, если это оправдывает риски для ребенка.
Неизвестно, выделяется ли zinforo в материнском молоке. Производитель рекомендует придерживаться особой осторожности при введении его женщинам, которые кормят грудью. Несмотря на отсутствие исследований с цефтаролином, Американская академия педиатрии (AAP) предполагает, что ряд других цефалоспоринов совместим с грудным вскармливанием. Зинфоро в Москве можно приобрести в аптеках, при этом проверяйте целостность упаковки и логотип производителя.
При нарушениях функциональности почек
Регулировка дозировки почечной массы для взрослых:
CrCl более 50 мл/мин: корректировка дозировки не требуется.
CrCl 31 до 50 мл/мин: 400 мг IV каждые 12 часов.
CrCl от 15 до 30 мл/мин: 300 мг IV каждые 12 часов.
CrCl менее 15 мл/мин: 200 мг IV каждые 12 часов.
Педиатрическая коррекция дозы почек (уравнение Шварца):
CrCl более 50 мл/мин/1,73 м2: не требуется корректировка дозировки.
CrCl 50 мл/мин/1,73 м2 или менее: недостаточно информации, чтобы рекомендовать режим дозировки.
При нарушениях функциональности печени
Zinforo, практически не выводится с помощью печени. Следовательно, не оказывается негативных воздействий на функциональность печени. Конкретные рекомендации по корректировке дозировки пациентов с поражениями печени отсутствуют; кажется, что никаких корректировок дозировки не требуется.
Передозировка
Не было зарегистрированных случаев чрезмерной дозы, но при почечной недостаточности возможен повышенный уровень в крови. При передозировке проводится гемодиализ.
Особые указания
С осторожностью применять при индивидуальной непереносимости состава препарата.
Применение в детском возрасте
Лечение после достижения 2-х месячного возраста.
Применение в пожилом возрасте
Не проводится корректировка дозы.
Условия и сроки хранения
Хранить при температурном режиме от +5 до +30 градусов. Готовый раствор при температурном режиме 2-8 градусов, не более суток. Купить препарат Зинфоро можно в аптеках России.
Цены на Зинфоро™ в Москве
Заберите заказ в в аптеке
WER (г. Москва)
Выгодные цены
Сертификаты и лицензии
Инструкция по применению
Состав
В 1 флаконе содержится:
Действующее вещество: цефтаролина фосамила ацетат моногидрат 668,4 мг, эквивалентный цефтаролину фосамилу 600,0 мг;
Вспомогательное вещество: L-аргинин 395,0 мг.
Фармакокинетика
Максимальная концентрация (Сmах) и площадь под кривой «концентрация-время» (AUC) цефтаролина увеличиваются почти пропорционально дозе при однократном введении препарата в диапазоне доз от 50 до 1000 мг.
Не наблюдалось заметной кумуляции цефтаролина после многократного внутривенного введения препарата в дозе 600 мг в течение 60 минут каждые 12 часов в течение 14 дней здоровым добровольцам с нормальной функцией почек.
Наблюдались аналогичные показатели системного воздействия (AUC), периода полувыведения цефтаролина (Т1/2) и клиренса цефтаролина после введения 600 мг цефтаролина фбсамила здоровым добровольцам в объеме 50 мл каждые 8 часов в течение 5дней в виде 5 минутной или 60 минутной инфузии, и время достижения максимальной концентрации (Тmах) цефтаролина составило 5 минут после окончания инфузии цефтаролина фосамила для обеих продолжительностей инфузии.
Среднее значение (SD) Сmах цефтаролина составило 32,5 (4,82) мг/л при продолжительности инфузии 5 минут (n=11) и 17,4 (3,87) мг/л при продолжительности инфузии 60 минут (n=12).
Распределение
Степень связывания цефтаролина с белками плазмы низкая (примерно 20%), препарат не проникает в эритроциты. Медиана объема распределения в равновесном состоянии у здоровых взрослых мужчин после однократного внутривенного введения 600 мг цефтаролина фосамила, меченного изотопом, составила 20,3 л, почти как и объем внеклеточной жидкости.
Метаболизм
В плазме крови под действием фосфатаз пролекарство цефтаролина фосамил быстро преобразуется в активный цефтаролин; концентрации пролекарства поддаются измерению в плазме, преимущественно, во время внутривенной инфузии.
При гидролизе бета-лактамного кольца цефтаролина образуется микробиологически неактивный метаболит, цефтаролин М-1. Соотношение средних значений AUC цефтаролина М-1 к цефтаролину в плазме крови после однократного внутривенного введения 600 мг цефтаролина фосамила здоровым добровольцам составляет примерно 20-30%.
Метаболизм цефтаролина протекает без участия изоферментов системы цитохрома Р450.
Экскреция
Цефтаролин выводится преимущественно почками. Почечный клиренс цефтаролина примерно равен или немного ниже скорости клубочковой фильтрации в почках. Исследования транспортеров in vitro показывают, что активная секреция не способствует почечной элиминации цефтаролина.
Средний период полувыведения цефтаролина у здоровых взрослых людей составляет примерно 2,5 часа. После однократного внутривенного введения 600 мг меченного изотопом цефтаролина фосамила здоровым взрослым мужчинам примерно 88% радиоактивности обнаруживалось в моче и 6% — в фекалиях.
Особые группы пациентов
Нарушение функции почек
После однократной внутривенной инфузии 600 мг цефтаролина фосамила в течение 60 минут Сmах цефтаролина в плазме составила 28,4 ± 6,9 мкг/мл, 28,2 ± 5,4 мкг/мл и 30,8 ± 4,9 мкг/мл у пациентов с нормальной функцией почек, нарушением функции почек легкой степени и нарушением функции почек средней степени тяжести, соответственно. Сmах цефтаролина достигалась приблизительно через 60 минут после начала инфузии.
AUC цефтаролина увеличивалась пропорционально степени нарушения функции почек и составила 75,6 ± 9,7 мкг.ч/мл, 92,3 ± 25,3 мкг.ч/мл и 114,8 ± 14,1 мкг.ч/мл у пациентов с нормальной функцией почек, нарушением функции почек легкой степени и нарушением функции почек средней степени тяжести, соответственно.
Коррекция дозы препарата требуется детям, подросткам и взрослым пациентам, если клиренс креатинина (КК) ≤ 50 мл/мин (см. раздел «Способ применения и дозы»).
Недостаточно данных, позволяющих рекомендовать коррекцию дозы при терминальной стадии почечной недостаточности у подростков в возрасте от 12 до 18 лет с массой тела менее 33 кг и детей в возрасте от 2 до 12 лет.
Недостаточно данных, позволяющих рекомендовать коррекцию дозы у детей в возрасте до 2 лет с нарушением функции почек средней и тяжелой степени тяжести, а также с терминальной стадией почечной недостаточности.
Нарушение функции печени
Исследования фармакокинетики цефтаролина у пациентов с нарушением функции печени не проводили. Так как цефтаролин не подвергается печеночному метаболизму в значительной степени, не ожидается, что нарушение функции печени будет существенно влиять на системный Клиренс цефтаролина. Поэтому не рекомендуется корректировать дозу препарата у пациентов с нарушением функции печени.
Пожилые пациенты (≥ 65 лет)
После однократного внутривенного введения 600 мг цефтаролина фосамила параметры фармакокинетики препарата были схожими у здоровых пожилых людей (≥ 65 лет) и здоровых молодых пациентов (18-45 лет).
У пожилых добровольцев отмечено небольшое увеличение AUC0-∞ (на 33%), что обусловлено, главным образом, возрастными изменениями функции почек. Не требуется коррекции дозы препарата у пожилых пациентов с клиренсом креатинина выше 50 мл/мин.
Дети
Детям в возрасте от 2 месяцев до 12 лет и подросткам в возрасте от 12 до 18 лет с массой тела менее 33 кг требуется коррекция дозы (см. раздел «Способ применения и дозы»). Безопасность и эффективность препарата Зинфоро® у детей в возрасте до 2 месяцев не установлены.
Пол
Параметры фармакокинетики цефтаролина были схожими у мужчин и женщин. Не требуется коррекции дозы в зависимости от пола пациента.
Раса
Не наблюдалось существенных различий параметров фармакокинетики цефтаролина у пациентов, принадлежащих к разным этническим группам. Не требуется корректировать дозу препарата в зависимости от расы пациента.
Показания к применению
Препарат Зинфоро® показан к применению у новорожденных, младенцев, детей, подростков и взрослых для лечения следующих инфекций:
- осложненные инфекции кожи и мягких тканей;
- внебольничная пневмония.
Препарат Зинфоро® может применяться при лечении взрослых пациентов с вторичной бактериемией, ассоциированной с осложненной инфекцией кожи и мягких тканей и внебольничной пневмонией. Недостаточно данных, позволяющих рекомендовать применение препарата Зинфоро® при лечении пациентов детского возраста с вторичной бактериемией, ассоциированной с осложненной инфекцией кожи и мягких тканей и внебольничной пневмонией.
Чувствительность антибиотиков in vitro меняется в зависимости от географического региона и с течением времени, поэтому при выборе антибактериальной терапии необходимо учитывать местную информацию о резистентности.
Противопоказания
- Повышенная чувствительность к цефтаролина фосамилу или L-аргинину.
- Повышенная чувствительность к цефалоспоринам.
- Тяжелые реакции повышенной чувствительности немедленного типа (например, анафилактическая реакция) на любое другое антибактериальное средство, имеющее бета-лактамную структуру (например, пенициллины или карбапенемы).
С осторожностью:
Способ применения и дозы
Зинфоро® вводится внутривенно в виде инфузии в течение 5-60 или 120 минут (см. «Приготовление раствора для инфузий»).
Продолжительность терапии должна устанавливаться в зависимости от типа и тяжести инфекции, ответа пациента на терапию.
Режим дозирования у взрослых и пациентов детского возраста
Рекомендованная дозировка препарата Зинфоро® составляет 600 мг каждые 12 часов в виде внутривенной инфузии продолжительностью 5-60 минут (стандартная доза), с соответствующим снижением дозы для пациентов детского возраста (Таблица 2).
Для лечения осложненных инфекций кожи и мягких тканей, доказано или предположительно вызванных Staphylococcus aureus (S. aureus) c MПK цефтаролина < 2 мг/л, дозировка препарата Зинфоро® составляет 600 мг каждые 12 часов в виде внутривенной инфузии продолжительностью 5-60 минут (стандартная доза), с соответствующим снижением дозы для пациентов детского возраста (Таблица 2).
Для лечения пациентов с осложненными инфекциями кожи и мягких тканей, доказано или предположительно вызванными S. aureus с MПK цефтаролина от 2 мг/л до 4 мг/л, дозировка препарата Зинфоро® составляет 600 мг каждые 8 часов в виде внутривенной инфузии продолжительностью 120 минут (высокая доза), с соответствующим снижением дозы для пациентов детского возраста.
Рекомендуемая длительность лечения составляет 5-14 дней для осложненных инфекций кожи и мягких тканей и 5-7 дней для внебольничной пневмонии.
Таблица 2. Дозировка у взрослых с нормальной функцией почек, клиренс креатинина (КК) > 50 мл/мин*
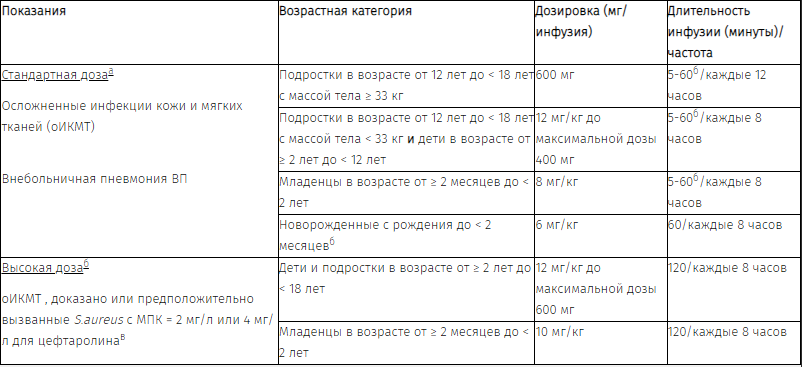
а Для пациентов с клиренсом креатинина, превышающим нормальные значения, получающих стандартную дозу препарата, может быть предпочтительнее длительность инфузии 60 минут.
б Рекомендации по длительности инфузии менее 60 минут и применению высоких доз основаны только на результатах фармакокинетических и фармакодинамических анализов. См разделы Особые указания, Фармакологические свойства.
в Для лечения инфекций, вызванных S.aureus, для которого МПК цефтаролина составляет ≤1 мг/л, рекомендуется стандартная доза препарата.
* Рассчитано по формуле Шварца (в мл/мин/1,73 м2) для пациентов детского возраста.
Применение у особых групп пациентов
Нарушение функции почек
Если КК ≤ 50 мл/мин, дозу препарата следует корректировать в соответствии с информацией, приведенной в Таблицах 4 и 5 (см. раздел «Фармакокинетика»).
Рекомендуемая длительность лечения составляет 5-14 дней для осложненных инфекций кожи и мягких тканей и 5-7 дней для внебольничной пневмонии.
Таблица 4. Дозировка у взрослых с нарушением функции почек, клиренс креатинина (КК) ≤ 50 мл/мин
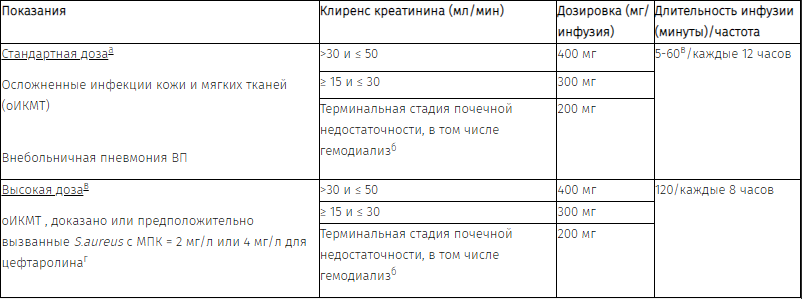
а Рассчитано по формуле Кокрофта — Голта для взрослых. Доза основана на КК. КК следует тщательно контролировать, а дозу препарата следует корректировать в соответствии с функцией почек.
б Цефтаролин выводится при гемодиализе, поэтому препарат Зинфоро® необходимо вводить после выполнения гемодиализа в дни гемодиализа.
в Рекомендации по длительности инфузии менее 60 минут и применению высоких доз основаны только на результатах фармакокинетических и фармакодинамических анализов. См. разделы Особые указания, Фармакологические свойства
г Для лечения инфекций, вызванных S aureus, для которого МПК цефтаролина составляет ≤ 1 мг/л, рекомендуется стандартная доза препарата.
Рекомендации по дозированию у детей и подростков основаны на данных фармакокинетического моделирования. Недостаточно данных, позволяющих рекомендовать коррекцию дозы при терминальной стадии почечной недостаточности у подростков в возрасте от 12 до 18 лет с массой тела менее 33 кг и детей в возрасте от 2 до 12 лет. Недостаточно данных, позволяющих рекомендовать коррекцию дозы у детей в возрасте до 2 лет с нарушением функции почек средней и тяжелой степени, а также с терминальной стадией почечной недостаточности.
Таблица 5. Дозировка у пациентов детского возраста с нарушением функции почек, клиренс креатинина (КК) ≤ 50 мл/мин
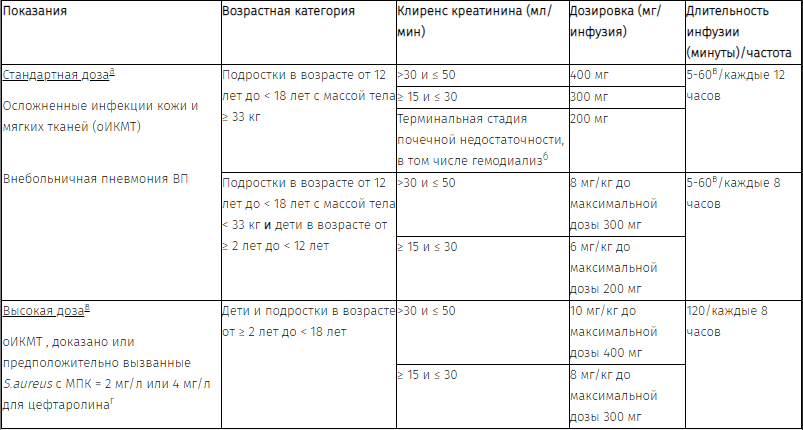
а Рассчитано по формуле Шварца для пациентов детского возраста (в мл/мин/1,73 м2). Доза основана на КК. КК следует тщательно контролировать, а дозу препарата следует корректировать в соответствии с функцией почек.
б Цефтаролин выводится при гемодиализе, поэтому препарат Зинфоро® необходимо вводить после выполнения гемодиализа в дни гемодиализа.
в Рекомендации по длительности инфузии менее 60 минут и применению высоких доз основаны только на результатах фармакокинетических и фармакодинамических анализов. См. разделы Особые указания, Фармакологические свойства.
г Для лечения инфекций, вызванных S.aureus, для которого МПК цефтаролина составляет ≤ 1 мг/л, рекомендуется стандартная доза препарата.
Нарушение функции печени
Нет необходимости корректировать дозу препарата у пациентов с нарушением функции печени.
Пожилые пациенты (≥65 лет)
Нет необходимости корректировать дозу препарата у пожилых пациентов с КК > 50 мл/мин.
Приготовление раствора для инфузий
При приготовлении и введении препарата необходимо соблюдать стандартные правила асептики. Каждый флакон предназначен только для однократного применения.
Препарат Зинфоро® порошок для приготовления концентрата для приготовления раствора для инфузий следует растворить в 20 мл стерильной воды для инъекций. Один мл концентрата содержит 30 мг цефтаролина фосамила. Полученный концентрат представляет собой раствор бледно-желтого цвета, свободный от видимых частиц. Концентрат необходимо немедленно использовать, не хранить (время от начала растворения порошка до полного приготовления раствора для внутривенных инфузий не должно превышать 30 минут).
Для приготовления раствора для инфузий полученный концентрат встряхивают и переносят в инфузионный флакон, содержащий одну из перечисленных ниже совместимых инфузионных жидкостей: 0,9% раствор натрия хлорида, 5% раствор декстрозы, 0,45% раствор натрия хлорида и 2,5% раствор декстрозы, раствор Рингер лактат.
При применении дозы препарата 600 мг во флакон с совместимой инфузионной жидкостью переносят весь полученный концентрат (20 мл), при применении дозы 400 мг 14 мл концентрата. Для применения дозы 300 мг следует перенести 10 мл концентрата, а для дозы 200 мг — 7 мл концентрата.
Раствор для инфузий можно приготовить путем добавления концентрата во флакон с инфузионной жидкостью объемом 50 мл, 100 мл или 250 мл.
Объем инфузионной жидкости у пациентов детского возраста зависит от массы тела. Концентрация раствора для инфузий в процессе его приготовления и введения не должна превышать 12 мг/мл цефтаролина фосамила.
После приготовления раствора для инфузий его следует использовать в течение 6 часов с момента приготовления. Приготовленный раствор для инфузий сохраняет стабильность в течение 24 часов при хранении в холодильнике (2-8оС). После извлечения из холодильника раствор для инфузий необходимо использовать в течение 6 часов при комнатной температуре.
Неиспользованный препарат или отходы необходимо утилизировать в соответствии с местными требованиями.
Условия хранения
При температуре не выше 30 °С. Хранить в местах, недоступных для детей.
Особые указания
При применении препарата необходимо руководствоваться официальными рекомендациями по надлежащему использованию антибактериальных препаратов.
Реакции гиперчувствительности
Как и при применении всех бета-лактамных антибиотиков, возможно развитие серьёзных реакций гиперчувствительности (иногда с летальным исходом).
У пациентов, принимающих бета-лактамные антибиотики, были зарегистрированы такие тяжелые кожные нежелательные реакции (SCARs), как синдром Стивенса-Джонсона, токсический эпидермальный некролиз, лекарственная реакция с эозинофилией и системными симптомами (DRESS), острый генерализованный экзантематозный пустулез (AGEP).
У пациентов с гиперчувствительностью к цефалоспоринам, пенициллинам или другим бета-лактамным антибиотикам в анамнезе может также развиться аллергическая реакция на цефтаролина фосамил. Перед началом терапии препаратом Зинфоро® следует тщательно изучить данные пациента на предмет выявления реакций гиперчувствительности к бета-лактамным антибиотикам. Препарат противопоказан пациентам с повышенной чувствительностью к цефалоспоринам в анамнезе. Также препарат противопоказан пациентам, у которых ранее отмечались тяжелые реакции повышенной чувствительности немедленного типа (например, анафилактическая реакция) на любое другое антибактериальное средство, имеющее бета-лактамную структуру (например, пенициллины или карбапенемы).
При развитии тяжелой аллергической реакции или тяжелых кожных нежелательных реакций (SCAR) необходимо прекратить введение лекарственного препарата и принять соответствующие меры.
Диарея, ассоциированная с Clostridium difficile
При применении почти всех антибактериальных препаратов, в том числе препарата Зинфоро®, сообщалось о развитии антибиотикоассоциированного колита и псевдомембранозного колита, которые могут варьировать по тяжести от легких до угрожающих жизни форм. Следует принимать во внимание возможность развития колита при возникновении диареи на фоне применения цефтаролина фосамила. В этом случае необходимо прекратить терапию препаратом Зинфоро®, проводить поддерживающие мероприятия и назначить специфическое лечение Clostridium difficile.
Пациенты с судорожным синдромом в анамнезе
Как и при применении других цефалосноринов, в исследованиях токсичности цефтаролина наблюдалось развитие судорог при приеме препарата в дозах, превышающих Сmах в 7-25 раз. Опыт применения цефтаролина у пациентов с судорожным синдромом в анамнезе ограничен, в связи с чем следует соблюдать осторожность при применении препарата Зинфоро® у этой группы пациентов.
Прямой антиглобулиновый тест (проба Кумбса)
Положительный прямой антиглобулиновый тест (ПАТ) может быть получен на фоне применения цефалоспоринов. Частота положительного ПАТ у пациентов, получавших цефтаролина фосамил в дозе 600 мг в виде внутривенной инфузии продолжительностью 60 минут каждые 12 часов, составила 11,2% в пяти объединенных исследованиях фазы 3 и 32,3% в исследовании, где цефтаролина фосамил назначался в дозе 600 мг в виде внутривенной инфузии продолжительностью 120 минут каждые 8 часов. Ни у одного пациента с положительным ПАТ на фоне применения цефтаролина фосамила не выявлены признаки гемолиза. Однако, возможность развития гемолитической анемии на фоне применения цефалоспоринов, включая препарат Зинфоро®, нельзя исключить. Такую возможность необходимо учитывать у пациентов с анемией, наблюдающейся во время или после применения препарата Зинфоро®.
Нечувствительные микроорганизмы
При применении цефтаролина фосамила, как и других антибиотиков, может развиться суперинфекция.
Ограниченность клинических данных
Эффективность терапии цефтаролином фосамилом взрослых пациентов с вторичной бактериемией была продемонстрирована на ограниченных клинических данных, включая отдельные сообщения об опыте пострегистрационного применения и данные ретроспективных исследований. Отсутствует опыт применения цефтаролина для лечения внебольничной пневмонии в следующих группах пациентов: пациенты с иммунодефицитом с тяжелым сепсисом/септическим шоком, тяжелой фоновой болезнью легких, пациенты с V классом риска но шкале PORT и (или) с внебольничной пневмонией, требующей искусственной вентиляции легких на момент постановки диагноза, с внебольничной пневмонией, вызванной метициллин-резистентными S. aureus, или пациенты, требующие интенсивной терапии. Таким пациентам лечение рекомендуется назначать с осторожностью.
Нет опыта лечения цефтаролином осложненных инфекций кожи и мягких тканей в следующих группах пациентов: пациенты с иммунодефицитом, пациенты с тяжелым сепсисом/септическим шоком, некротическим фасциитом, периректальным абсцессом и пациенты с ожогами третьей степени и обширными ожогами. Ограничен опыт лечения пациентов с инфекциями диабетической стопы. Таким пациентам лечение рекомендуется назначать с осторожностью.
Осложненные инфекции кожи и мягких тканей, вызванные S. aureus с МПК > 1 мг/л к цефтаролину
Существуют ограниченные клинические данные о лечении цефтаролином у взрослых осложненных инфекций кожи и мягких тканей, вызванных S. aureus с МПК > 1 мг/л к цефтаролину, и отсутствуют клинические данные о лечении осложненных инфекций кожи и мягких тканей при МПК к цефтаролину, равной 2 мг/л — 4 мг/л. Тем не менее рекомендации по дозировке препарата Зинфоро® для лечения осложненных инфекций кожи и мягких тканей, вызванных S. aureus с МПК > 1 мг/л к цефтаролину, основываются на фармакокинетическом/фармакодинамическом моделировании и симуляции (см. раздел «Способ применения и дозы»). Препарат Зинфоро® не следует использовать для лечения осложненных инфекций кожи и мягких тканей, вызванных S.Aureus с МПК > 4 мг/л к цефтаролину.
Пациенты детского возраста < 2 месяцев
Рекомендуемый режим дозирования препарата Зинфоро приведенный в таблице 3 для детей в возрасте < 2 месяцев, основан на фармакокинетическом и фармакодинамическом моделировании и симуляции.
Рекомендации по длительности инфузии менее 60 минут основаны только на результатах фармакокинетических и фармакодинамических анализов.
Описание
Антибиотик, цефалоспорин.
Фармакодинамика
После внутривенного введения прлекарство цефтаролина фосамил быстро превращаемся в активный цефтаролин.
Механизм действия
Цефтаролин — антибиотик класса цефалоспоринов с активностью в отношении грамположительных и грамотрицательных микроорганизмов.
В исследованиях in vitro показано бактерицидное действие цефтаролина, обусловленное ингибированием биосинтеза клеточной стенки бактерий за счет связывания с пенициллинсвязывающими белками (ПСБ). Цефтаролин проявляет бактерицидную активность в отношении метициллин-резистентного Staphylococcus aureus (MRSA) и в отношении пенициллин-нечувствительного Streptococcus pneumoniae (PNSP) в связи с его высоким сродством к измененным ПСБ этих микроорганизмов.
Связь фармакокинетики и фармакодинамики
Антимикробная активность цефтаролина, также как и других бета-лактамных антибиотиков, лучше всего коррелирует с интервалом времени, в течение которого концентрация препарата остается выше минимальной подавляющей концентрации (МПК) инфицирующего микроорганизма (%Т > МПК).
Механизм резистентности
Цефтаролин не активен в отношении штаммов Enterobacteriaceae, продуцирующих бета-лактамазы расширенного спектра (БЛРС) семейств ТЕМ, SHV или СТХ-М, сериновые карбапенемазы (такие как КРС), металло-бета-лактамазы класса В или класса С (цефалоспориназы АтрС). Резистентность также может быть связана с нарушением проницаемости клеточной стенки бактерий или с активным выведением антибиотика (эффлюкс). Микроорганизм может обладать одним или несколькими механизмами резистентности.
Перекрестная резистентность
Несмотря на возможное развитие перекрестной резистентности, некоторые штаммы, резистентные к другим цефалоспоринам, могут быть чувствительны к цефтаролину.
Микроорганизмы, обладающие природной резистентностью:
Chlamydophila spp.
Legionella spp.
Mycoplasma spp.
Proteus spp.
Pseudomonas aeruginosa
Взаимодействие с другими антимикробными препаратами
Исследования in vitrо не выявили антагонизма при применении цефтаролина в комбинации с другими часто назначаемыми антимикробными препаратами (такими как амикацин, азитромицин, азтреонам, даптомицин, левофлоксацин, линезолид, меропенем, тигециклин и ванкомицин).
Чувствительность
Чувствительность антибиотиков in vitro меняется в зависимости от географического региона и с течением времени, поэтому при выборе антибактериальной терапии необходимо учитывать местную информацию о резистентности.
Если локальная резистентность такова, что эффективность препарата в отношении некоторых инфекций становится сомнительной, необходимо обратиться за консультацией к эксперту.
Чувствительность к цефтаролину должна определяться с помощью стандартных методов. Интерпретацию результатов следует проводить в соответствии с локальными руководствами.
Таблица 1. Пограничные значения для определения чувствительности Европейского комитета по тестированию антимикробной чувствительности (EUCAST) представлены ниже
1. Относится к введению цефтаролина взрослым или подросткам (с 12 лет и от 33 кг) каждые 12 часов в виде 1-часовых инфузий (см. раздел «Способ применения и дозы»). Обратите внимание, что нет данных по клиническим исследованиям применения цефтаролина для лечения внебольничной пневмонии, вызванной S. aureus, для которых МПК цефтаролина составляет > 1 мг/л.
2. Относится к введению цефтаролина для лечения осложненных инфекций кожи и мягких тканей взрослым или подросткам (с 12 лет и от 33 кг) каждые 8 часов в виде 2-часовых инфузий (см. раздел «Способ применения и дозы»). Согласно данным фармакокинетического и фармакодинамическ|)го анализов есть основание полагать, что изоляты с МПК 4 мг/л можно лечить высокими дозами. S. aureus, для которых МПК цефтаролина составляет ≥ 4 мг/л, выделяются редко.
3. Чувствительность определяется по чувствительности к бензилпенициллину.
Клиническая эффективность в отношении отдельных патогенных микроорганизмов
Ниже перечислены патогенные микроорганизмы (по показаниям к применению), чувствительные к цефтаролину in vitro, в отношении которых в клинических исследованиях была показана эффективность цефтаролина.
Осложненные инфекции кожи и мягких тканей
Грамположительные микроорганизмы
Staphylococcus aureus (включая метициллин-резистентные штаммы)
Streptococcus pyogenes
Streptococcus agalactiae
Группа Streptococcus anginosus (включает S. anginosus, S. intermedius и S. constellatus)
Streptococcus dysgalactiae
Грамотрицательные микроорганизмы
Escherichia coli
Klebsiella pneumoniae
Klebsiella oxytoca
Morganella morganii
Внебольничная пневмонияГрамположительные микроорганизмы
Streptococcus pneumoniae (включая случаи, сопровождающиеся бактериемией)
Staphylococcus aureus (только метициллин-чувствительные штаммы)
Грамотрицательные микроорганизмы
Escherichia coli
Haemophilus influenzae
Haemophilus parainfluenzae
Klebsiella pneumoniae
Эффективность в отношении других значимых патогенных микроорганизмов
Клиническая эффективность цефтаролина в отношении перечисленных ниже патогенных микроорганизмов не была установлена, однако результаты исследований in vitro позволяют предполагать, что они чувствительны к цефтаролину в отсутствие приобретенных механизмов резистентности.
Грамположительные анаэробы
Peptostreptococcus spp.
Грамотрицательные анаэробы
Fusobacterium spp.
Клиническая эффективность при вторичной бактериемии
Ограниченное количество пациентов с вторичной бактериемией было включено в клинические исследования, проводившиеся по показаниям осложненной инфекции кожи и мягких тканей и внебольничной пневмонии. Среди 6 исследований среди взрослых 85/1446 (5,9%) пациентов с осложненной инфекцией кожи и мягких тканей и 53/530 (10,0%) пациентов с внебольничной пневмонией имели бактериемию на исходном уровне, из которых 72 пациента получали цефтаролин фосамил. Частота клинического излечения у пациентов с вторичной бактериемией составили 76,4% в группе цефтаролина фосамила и 77,3% в группе сравнения (азтреонам / ванкомицин для осложненной инфекции кожи и мягких тканей и цефтриаксон для внебольничной пневмонии). Частота клинического излечения у пациентов, не страдающих бактериемией, составили 85,1% и 82,2% в группе цефтаролина фосамила и в группе сравнения, (азтреонам / ванкомицин для осложненной инфекции кожи и мягких тканей и цефтриаксон для внебольничной пневмонии) соответственно.
Побочные действия
Наиболее распространенными побочными реакциями, возникающими у ≥ 3% из приблизительно 3242 пациентов, получавших препарат Зинфоро® в клинических исследованиях, были диарея, головная боль, тошнота и зуд, которые обычно были легкой или средней степени тяжести. Также могут возникнуть побочные реакции, связанные с Clostridium difficile, и реакции гиперчувствительности.
Более высокая частота появления кожной сыпи у азиатских пациентов (см. ниже) и более высокая частота положительной прямой пробы Кумбса (см. раздел «Особые указания») наблюдались в исследовании у взрослых пациентов с осложненными инфекциями кожи и мягких тканей, получавшие препарат Зинфоро® в дозе 600 мг в виде внутривенной инфузии продолжительностью 120 минут каждые 8 часов.
Оценка безопасности у пациентов детского возраста основана на данных по безопасности 2 клинических исследований, в ходе которых 227 пациентов в возрасте от 2 месяцев до 17 лет с осложненными инфекциями кожи и мягких тканей или внебольничной пневмонией принимали препарат Зинфоро®. В целом, профиль безопасности препарата Зинфоро® у этих 227 пациентов был схожим с наблюдаемым у взрослых пациентов.
Кроме того, оценка безопасности у новорожденных и младенцев основана на данных по безопасности 2 исследований, в которых 34 пациента (возраст от рождения до 60 дней) получали препарат Зинфоро®; 23 из этих пациентов получили только одну дозу препарата Зинфоро®. В целом, побочные эффекты, о которых сообщалось в этих исследованиях, соответствовали известному профилю безопасности препарата Зинфоро®.
Ниже представлены нежелательные реакции, отмечавшиеся в клинических исследованиях и при пострегистрационном применении препарата Зинфоро®.
Частота нежелательных реакций представлена в виде следующей градации: очень часто (≥ 1/10), часто (≥ 1/100, < 1/10), нечасто (≥ 1/1000, < 1/100), редко (≥ 1/10000, < 1/1000), частота неизвестна (невозможно оценить на основании имеющихся данных).
Таблица 4. Частота развития нежелательных реакций но классу системы органов
1 См. раздел «Особые указания».
2 См. раздел «Противопоказания».
* Нежелательные реакции выявленные при пострегистрационном применении.
Описание отдельных нежелательных реакций
Тяжелые кожные нежелательные реакции
При применении бета-лактамных антибиотиков, в том числе цефалоспоринов, были с зарегистрированы тяжелые кожные нежелательные реакции (SCARs) (синдром Стивенса — Джонсона, токсический эпидермальный некролиз, лекарственная реакция с эозинофилией и системными симптомами, острый генерализованный экзантематозный пустулез) (см. раздел Особые указания).
Сыпь
Сыпь часто отмечалась у пациентов с осложненными инфекциями кожи и мягких тканей, получавших цефтаролина фосамил в дозе 600 мг как в виде внутривенной инфузии продолжительностью 60 минут каждые 12 часов (в объединенных исследованиях фазы 3), так и в виде внутривенной инфузии продолжительностью 120 минут каждые 8 часов. Однако в подгруппе пациентов монголоидной расы, получавших цефтаролина фосамил каждые 8 часов, сыпь отмечалась очень часто (18,5%).
Применение при беременности и кормлении грудью
Беременность
Клинические данные о применении цефтаролина фосамила у беременных женщин отсутствуют. Исследования на животных не выявили неблагоприятного воздействия цефтаролина фосамила на фертильность, беременность, роды или послеродовое развитие. Препарат Зинфоро® не следует применять во время беременности, за исключением случаев, когда потенциальная польза для матери превышает возможный риск для плода.
Период грудного вскармливания
Данные о проникновении цефтаролина в грудное молоко отсутствуют. Однако, в связи с тем, что многие бета-лактамные антибиотики выделяются с грудным молоком, в случае необходимости терапии препаратом Зинфоро® рекомендуется прекращение грудного вскармливания.
Взаимодействие
Клинические исследования по изучению лекарственного взаимодействия с цефтаролином не проводились.
В исследованиях in vitro цефтаролин не ингибировал изоферменты цитохрома Р450 CYP1A1, CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1 и CYP3A4 и не индуцировал изоферменты CYP1A2, CYP2B6, CYP2C8, CYP2C9, CYP2C19, или CYP3A4/5. В связи с этим вероятность взаимодействия цефтаролина с препаратами, которые метаболизируются под действием изоферментов системы цитохрома Р450, низка.
Цефтаролин не метаболизируется под действием изоферментов цитохрома Р450 in vitro, поэтому маловероятно влияние на параметры фармакокинетики цефтаролина при совместном применении с индукторами или ингибиторами изоферментов цитохрома Р450.
In vitro цефтаролин не переносится эффлюксными транспортерами P-gp или BCRP. Цефтаролин не ингибирует P-gp, следовательно, взаимодействие с субстратами, такими как дигоксин, не ожидается. Цефтаролин является слабым ингибитором BCRP, но данный эффект не имеет клинической значимости. Исследования in vitro показали, что цефтаролин не является субстратом, и не ингибировал транспортеры органических катионов (ОСТ2) и анионов (ОАТ1, ОАТ3) в почках; поэтому маловероятно взаимодействие с препаратами, которые ингибируют активную почечную секрецию (например, пробенецид) или с препаратами, которые являются субстратами этих транспортеров.
Взаимодействие с другими антибактериальными препаратами
Тесты in vitro не выявили антагонизма при совместном применении цефтаролина и других часто используемых антибактериальных препаратов (например, амикацина, азитромицина, азтреонама, даптомицина, левофлоксацина, линезолида, меропенема, тигециклина и ванкомицина).
Передозировка
Ограниченные данные по пациентам, получавшим препарат Зинфоро® в дозах, превышавших рекомендуемые, показывают нежелательные реакции, аналогичные наблюдавшимся у пациентов, получавших препарат в рекомендуемых дозах. Относительные передозировки могли возникать у пациентов с умеренным нарушением функции почек. При лечении передозировки необходимость следовать стандартной медицинской практике.
Цефтаролин можно удалить с помощью гемодиализа; в течение 4-часового периода диализа приблизительно 74 % полученной дозы выводилось с диализатом.
Форма выпуска
Порошок для приготовления концентрата для приготовления раствора для инфузий.
Влияние на способность к вождению автотранспорта и управлению механизмами
Не проводилось исследований по изучению влияния препарата Зинфоро® на способность к вождению автотранспорта и управлению иными механизмами. Во время терапии могут возникать нежелательные явления (например, головокружение), поэтому следует соблюдать осторожность при управлении транспортными средствами и при занятиях другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций. При появлении описанного выше нежелательного явления следует воздержаться от выполнения указанных видов деятельности.